Грибовидный микоз
 Версия: Клинические рекомендации РФ 2023 (Россия)
Версия: Клинические рекомендации РФ 2023 (Россия)
Общая информация
Краткое описание
Разработчик клинической рекомендации:
- Общероссийская общественная организация "Российское общество дерматовенерологов и косметологов"
- Региональная общественная организация «Общество онкогематологов»
- Национальное гематологическое общество
Одобрено Научно-практическим Советом Минздрава РФ (протокол № 23 от 27.12.2022 г)
В соответствии с Правилами поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 –9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», утвержденных постановлением Правительства Российской Федерации от 19.11.2021 № 1968, клинические рекомендации применяются следующим образом:
– размещенные в Рубрикаторе после 1 июня 2022 года – с 1 января 2024 года.
Клинические рекомендации
Грибовидный микоз
Год утверждения: 2023
Пересмотр не позднее: 2025
Дата размещения: 10.02.2023
Статус: Действует
ID:223
Применение отложено
Определение заболевания или состояния (группы заболеваний или состояний)
Грибовидный микоз (ГМ) – первичная эпидермотропная Т-клеточная лимфома кожи (ЛК), характеризующаяся пролиферацией малых и средних Т-лимфоцитов с церебриформными ядрами.
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статической класификации болезней и проблем, связанных со здоровьем
C84.0 – Грибовидный микоз
Классификация
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
2. Другие формы грибовидного микоза:
b. редко встречающиеся варианты:
Этиология и патогенез
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Эпидемиология
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Клиническая картина
Cимптомы, течение
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
При классическом варианте грибовидного микоза заболевание протекает стадийно с нарастанием распространенности процесса и делится на 3 клинических стадии: пятнистая (эритематозная), бляшечная и опухолевая.
Сиринготропный грибовидный микоз представляет собой редкий вариант заболевания, имеющим много общего с фолликулотропным грибовидным микозом. Он характеризуется выраженным поражением эккринных желез, часто ассоциируясь с пилотропизмом. Поражения кожи могут быть солитарными или, чаще, генерализованными [4].
Педжетоидный ретикулез представляет собой редкий вариант грибовидного микоза, характеризующийся локализованными пятнами или бляшками с интраэпидермальной пролиферацией неопластических Т-лимфоцитов. Термин педжетоидный ретикулез следует использовать только для локализованного типа болезни (тип Ворингера-Колоппа), но не для диссеминированного типа (тип Кетрона-Гудмана), так как в настоящее время у большинства пациентов с генерализованными высыпаниями заболевание рассматривают как первичную кожную CD8+ агрессивную эпидермотропную цитотоксическую лимфому, первичную кожную γ/δ Т-клеточную лимфому или опухолевую стадию грибовидного микоза [5]. Поражение кожи у пациентов обычно представлено солитарными, медленно прогрессирующими псориазиформными или гиперкератотическими бляшками, которые обычно локализуются на конечностях, чаще всего на кистях и стопах [5].
Синдром гранулематозной вялой кожи – это крайне редкий вариант грибовидного микоза, характеризующийся медленным формированием складок вялой кожи и гранулематозным инфильтратом с клональными Т-лимфоцитами. Первоначальным проявлением поражения кожи при синдроме гранулематозной вялой кожи, как и при классическом грибовидном микозе, являются пятна и бляшки, которые трансформируются в крупные, висящие складки атрофичной кожи в области сгибов (подмышки и пах), напоминающие синдром вялой кожи — cutislaxa. Внекожная диссеминация патологического процесса развивается крайне редко, и у большинства пациентов заболевание имеет индолентное течение [5].
Гипопигментный грибовидный микоз часто обнаруживается у людей с темной кожей и часто встречается у детей и подростков. У пациентов с белой кожей гипопигментированные очаги поражения обычно сосуществуют вместе с эритематозными высыпаниями, типичными для классического грибовидного микоза. Заболевание проявляется гипопигментированными пятнами, которые локализуются преимущественно на туловище и конечностях и не сопровождаются субъективными ощущениями [5].
Диагностика
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Морфологические особенности, характерные для разных стадий и форм грибовидного микоза, подробно приведены в комментариях, в том числе с применением иммуногистохимического метода с использованием антител к CD2, CD3, CD4, CD5, CD7, CD8, CD20, CD30, CD56, TIA1, granzyme B, TCR (ßF1), TCR-γ, CD45RO [3–5].
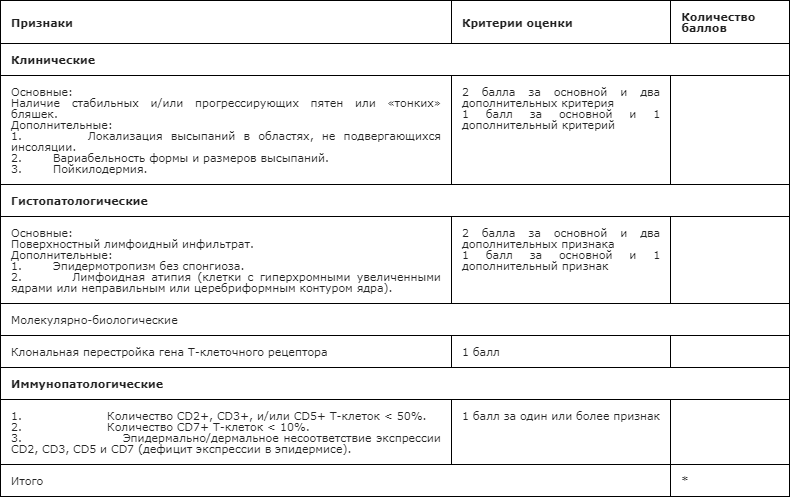
Иммуногистохимические критерии диагностики грибовидного микоза:
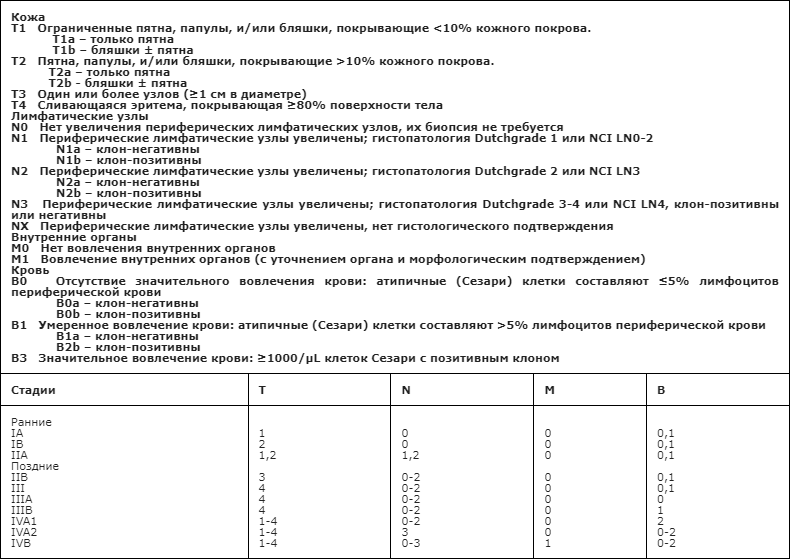
Согласно рекомендациям Международного общества по лимфомам кожи и Европейской организации по изучению и лечению рака выделяют 4 стадии грибовидного микоза – I стадию, выделяя стадии IA и IB, а также II, III и IV стадии.
План обследования варьирует в зависимости от стадии грибовидного микоза:
Для грибовидного микоза характерно постепенное начало заболевания и медленное развитие. Высыпания часто спонтанно бесследно разрешаются. Пациенты предъявляют жалобы на высыпания на коже, которые часто сопровождаются чувством зуда [3–5].
Для установления стадии заболевания согласно рекомендациям ISLE-EORTC при наличии пятен/бляшек необходимо определение площади поражения кожного покрова, при наличии узлов – определение их общего количества, размеров наибольшего узла и вовлеченных областей кожи. Необходима также пальпация лимфатических узлов и оценка их размеров, консистенции, подвижности, спаянности с окружающими тканями, болезненности [6].
-
Рекомендуется общий (клинический) анализ крови развернутый для выявления возможных отклонений [6] и состояний, являющихся противопоказаниями к назначению системной терапии грибовидного микоза и для контроля безопасности проводимой системной терапии или фототерапии [15–17].
-
Рекомендуется проведение анализа крови биохимического общетерапевтического с включением показателей лактатдегидрогеназы и мочевой кислоты [3,22], а также для выявления возможных отклонений [6] и состояний, являющихся противопоказаниями к назначению системной терапии грибовидного микоза и для контроля безопасности проводимой системной терапии или фототерапии кожи [15–17].
-
Рекомендуется всем пациентам с грибовидным микозом проведение ультразвукового исследования лимфатических узлов (периферических) для определения степени их вовлеченности в патологический процесс и стадии заболевания [3,6,7].
-
Рекомендуется всем пациентам с грибовидным микозом проведение прицельной рентгенографии органов грудной клетки [3,6,7].
-
Рекомендуется проведение магнитно-резонансной томографии или позитронно-эмиссионной томографии, совмещенной с компьютерной томографией (ПЭТ/КТ), органов грудной полости, брюшной полости и малого таза для выявления потенциальной вовлеченности в патологический процесс лимфатических узлов и внутренних органов у пациентов с грибовидным микозом на поздних стадиях и/или обнаружении измененных периферических лимфатических узлов при обследовании [3,6,7].
2.5 Иные диагностические исследования
-
Рекомендуется всем пациентам с подозрением на грибовидный микоз проведение патолого-анатомического исследования биопсийного (операционного) материала кожи из очага поражения для верификации диагноза [6,24–27].
При проведении патолого-анатомического исследования необходимо учитывать клеточный состав дермального инфильтрата и его расположение. Основными диагностическими критериями являются [6,24–27]:
Морфологические особенности, характерные для разных стадий и форм грибовидного микоза, подробно приведены в комментариях
Фолликулотропный грибовидный микоз морфологически характеризуется перифолликулярным или диффузным лимфоцитарным инфильтратом дермы с различной степени выраженности инфильтрацией фолликулярного эпителия мелкими, среднего размера и иногда крупными Т-клетками с церебриформными гиперхромными ядрами. Во многих случаях обнаруживается муцинозная дегенерация фолликулярного эпителия (фолликулярный муциноз), которая может быть визуализирована окраской альциановым синим или коллоидным железом, однако были также описаны случаи без фолликулярного муциноза. Инфильтрация фолликулярного эпителия может сопровождаться инфильтрацией эккринных потовых желез (сиринготропизм), комбинацию которых часто называют аднексотропным грибовидным микозом [32]. Тем не менее, одновременная инфильтрация интерфолликулярного эпидермиса (эпидермотропизм), характеризующая ранние стадии классического грибовидного микоза, встречается редко. В ранних поражениях, клинически характеризующихся приуроченными к фолликулам пятнами или акнеформными высыпаниями или высыпаниями, подобными волосяному кератозу, перифолликулярный инфильтрат обычно скудный и содержит помимо атипичных Т-клеток различное количество мелких реактивных Т-клеток], гистиоцитов и иногда – эозинофилов. При прогрессировании поражения кожи до более инфильтрированных бляшек или опухолей дермальные инфильтраты становятся более диффузными и могут содержать большее количество крупных клеток или среднего размера клеток с тонкодисперсным хроматином. Часто наблюдается значительная примесь эозинофилов и особенно в случаях вторичной бактериальной инфекции – плазматических клеток. В некоторых случаях могут присутствовать кластеры мелких В-лимфоцитов. В случаях разрушения эпителия волосяных фолликулов может наблюдаться гранулематозная реакция. В случаях с диффузными дермальными инфильтратами с частичным или даже полным разрушением эпителиальных структур дифференциальная диагностика между фолликулярным грибовидным микозом и другими типами ТКЛК может быть сложной.
Крупноклеточная трансформация, которую определяют по присутствию более 25% бластных клеток или присутствию кластеров бластных клеток, была описана более, чем в 20% случаев фолликулотропного грибовидного микоза, и наблюдается чаще, чем при классическом грибовидном микозе [5].
Типичная гистологическая картина представлена гиперплазией эпидермиса с выраженной инфильтрацией мелкими и среднего размера атипичными клетками, расположенными по отдельности или гнездами или кластерами. Атипичные клетки имеют среднего размера или крупные церебриформные ядра и обильную вакуолизированную цитоплазму. В поверхностной дерме может присутствовать инфильтрат, состоящий преимущественно из мелких лимфоцитов, но изредка он содержит неопластические Т-лимфоциты [5].
Гистологически синдром гранулематозной вялой кожи характеризуется плотным инфильтратом по всей толщине дермы из мелких и среднего размера Т-лимфоцитов с примесью многочисленных макрофагов и множества рассеянных многоядерных гигантских клеток. Присутствие многоядерных гигантских клеток, содержащих более 10 ядер на клетку, считается характерной особенностью заболевания, но наблюдалось также и в случаях гранулематозного грибовидного микоза. Обычно наблюдаются потеря эластических волокон, эластофагоцитоз и эмпериполез (поглощение лимфоцитов) многоядерными клетками. Эпидермис может быть инфильтрирован мелкими атипичными Т-лимфоцитами с церебриформными ядрами, как и при классическом грибовидном микозе [5].
При гипопигментном грибовидном микозе обнаруживаются типичная гистологическом картина ранней пятнистой стадии грибовидного микоза. Такие варианты грибовидного микоза как гиперпигментный, буллезный/везикулезный, пойкилодермический, пигментный пурпуроподобный, пустулезный, ихтиозиформный, ладонно-подошвенный характеризуются теми же гистологическими признаками, что и классический грибовидный микоз [5].
-
Рекомендуется при наличии гистологических признаков грибовидного микоза (лимфопролиферативного заболевания) в морфологической картине применение иммуногистохимического метода исследования с использованием антител к CD2, CD3, CD4, CD5, CD7, CD8, CD20, CD30, CD56, TIA1, granzyme B, TCR (ßF1), TCR-γ, CD45RO [3–5].
Иммуногистохимические критерии диагностики грибовидного микоза:
При педжетоидном ретикулезе фенотип непластических Т-лимфоцитов может характеризоваться либо как CD3+/CD4−/CD8+, либо реже как CD3+/CD4+/CD8− или CD3+/CD4−/CD8−. В случаях с фенотипами CD8+ или CD4−/CD8− экспрессируются цитотоксические белки (например, Т-клеточный внутриклеточный антиген (TIA)-1, гранзим A/B и перфорин). Часто экспрессируется CD30 [34].
В большинстве случае синдрома гранулематозной вялой кожи отмечается фенотип Т-лимфоцитов CD3+/CD4+/CD8– [5].
В описании иммуногистохимического исследования и в патоморфологическом заключении необходимо указывать наличие CD30-позитивных клеток лимфоидного инфильтрата, включая клетки реактивного микроокружения, при полуколичественной оценке с учетом градации: <10%, 10-30%. >30%. >50%. При наличии в инфильтрате CD30-позитивных клеток (независимо от их количества) при формулировке диагноза должно быть указано: грибовидный микоз (CD30-позитивный).
-
Рекомендуется проведение патолого-анатомического исследования биопсийного (операционного) материала лимфоузла в случае выявления признаков поражения лимфатических узлов (увеличение размеров > 1,5 см в диаметре и/или с плотной, неравномерной структурой) в результате ультразвукового исследования и/или прицельной рентгенографии грудной клетки и/или МРТ и/или позитронно-эмиссионной томографии совмещенной с компьютерной томографией (ПЭТ/КТ) [6].
-
Рекомендуется проведение молекулярно-биологического исследования пунктата органов кроветворения (лимфатический узел) в случае обнаружения опухолевого субстрата при патолого-анатомическом исследовании биопсийного (операционного) материала лимфоузла с применением иммуногистохимических методов [6,35].
-
Рекомендуется применение патолого-анатомического исследования биопсийного (операционного) материала с применением иммуногистохимических методов в случае обнаружения опухолевого субстрата лимфатического узла [6,35].
-
Рекомендуется проведение патолого-анатомическое исследование биопсийного (операционного) материала костного мозга у пациента с поздними стадиями грибовидного микоза и/или подозрением на поражение костного мозга [36]. При обнаружении патологических изменений в субстрате костного мозга рекомендуется проведение ПЦР-исследования, иммуногистохимического исследования и/или исследование биологического материала методом проточной цитофлуориметрии [36].
-
Рекомендуется молекулярно-генетическое исследование перестройки гена Т-клеточного рецептора [3,4,8–14].
-
Рекомендуется проведение проточной цитофлуориметрии периферической крови для оценки наличия и числа T-лимфоцитов с аберрантным фенотипом (CD4+/CD26- или CD4+/CD7-) в следующих случаях:
Лечение
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1 Лечение пациентов с ранними стадиями грибовидного микоза
-
Рекомендуются для лечения пациентов с ранними стадиями (IA–IIA) грибовидного микоза наружно глюкокортикоиды, применяемые в дерматологии [7,38,39]:
#бетаметазон**, крем, мазь 2 раза в сутки наносить на очаги поражения до полного разрешения высыпаний [7,38,39, 67, 68].
Для взрослых: Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2)
Для детей: Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
или
#мометазон** крем, мазь 2 раза в сутки наносить на очаги поражения до полного разрешения высыпаний [7,38,39, 69, 70].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: для ранних стадий грибовидного микоза консервативный подход с применением наружной терапии является предпочитаемым лечением первой линии. Для пациентов в IA стадии с небольшими очагами поражения кожи допускается тактика «наблюдай и жди» под строгим наблюдением врача.
-
Рекомендуется ультрафиолетовое облучение кожи пациентам с грибовидным микозом на стадиях IA-IIB [40–43]:
общая или локальная узкополосная средневолновая ультрафиолетовая терапия [40–44].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: облучение проводится 2–3 раза в неделю, первая экспозиция должна быть не более 70% от ранее определенной минимальной эритемной дозы. Последующие экспозиции проводятся следующим образом: при отсутствии эритемы – время экспозиции увеличивается на 40%, при слабой эритеме – на 20%, при выраженной эритеме – остается тем же. Рекомендовано для пятен и тонких бляшек, отсутствуют выраженные побочные эффекты.
или
фотохимиотерапия с внутренним применением псораленов для системного применения (ПУВА) [40, 42,44].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: за 2 часа до облучения пациент принимает перорально -#метоксален в дозе 0,6 мг на кг массы тела, начальная доза облучения зависит от типа кожи (0.25–1.0 Дж/см2), затем с каждым сеансом доза повышается на 0,25–0,5 Дж/см2 или более в зависимости от выраженности эритемы. Лечение проводится 3–4 раза в неделю до разрешения высыпаний (30–35 сеансов). Общая доза варьирует от 50 до 80 Дж/см2, что бывает достаточным для достижения клинической ремиссии. Применяется при распространенных и более инфильтрированных элементах, фолликулярной форме грибовидного микоза. Побочные эффекты включают эритему, тошноту, фоточувствительность и фотокарциногенез.
-
Рекомендуется применение дистанционной лучевой терапии при поражении мягких тканей на медицинском ускорителе электронов у пациентов с грибовидным микозом при локализованных поражениях кожи без вовлечения в патологический процесс лимфатических узлов и костного мозга [3,45–47].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: при локализованных стадиях ГМ оптимально использование дистанционной лучевой терапии на медицинских ускорителях электронов мощностью 4-8 МЭВ, в зависимости от глубины поражения кожи. При наличии единственного очага поражения рекомендуемая суммарная очаговая доза облучения (СОД) составляет 24-30 Гр. При наличии нескольких отдельных очагов СОД не должна превышать 8-12 Гр, при этом СОД 8 Гр может быть подведена за 2 фракции.
Тотальное облучение кожи (дистанционная лучевая терапия на медицинских ускорителях электронов) используется при генерализованном поражении кожи при отсутствии вовлечения лимфатических узлов и органного поражения. Суммарные очаговые дозы варьируются от 12 до 36 Гр, не более 4-6 Гр за неделю. Преимуществами использования низких суммарных доз облучения являются уменьшение степени лучевых реакций и возможность в дальнейшем использования повторных курсов лучевого лечения.
При вовлечении лимфатических узлов и висцеральных органов возможно дополнительное использование дистанционной гама - терапии в суммарной дозе 20-30 Гр.
3.2 Лечение пациентов с распространенными стадиями грибовидного микоза и рецидивных и рефрактерных форм грибовидного микоза
-
Рекомендуются как препараты первой линии для лечения пациентов с IIB, III стадиями грибовидного микоза, а также в качестве второй линии ранних стадий грибовидного микоза при отсутствии или недостаточном эффекте от проводимой терапии #интерферон альфа-2b ** в умеренно высоких дозах: 3–10 млн МЕ ежедневно или 3 раза в неделю [18].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: лечение проводят до достижения полного контроля (отсутствия признаков дальнейшего прогрессирования). Можно комбинировать с ПУВА-терапией, ретиноидами и химиотерапией. На фоне длительного приема препарата возможны изменения со стороны щитовидной железы. У пациентов с заболеваниями щитовидной железы перед началом лечения необходимо определить концентрацию тиреотропного гормона, рекомендуется контролировать его уровень не реже 1 раза в 6 месяцев. Очень редко – сахарный диабет. При длительном применении, обычно после нескольких месяцев лечения, возможны нарушения со стороны органа зрения. До начала терапии рекомендуется провести офтальмологическое обследование. При жалобах на любые офтальмологические нарушения необходима немедленная консультация врача-офтальмолога. Пациентам с заболеваниями, при которых могут происходить изменения в сетчатке, например, с сахарным диабетом или артериальной гипертензией, необходимо проходить офтальмологический осмотр не реже 1 раза в 6 месяцев. Пациентам с заболеваниями сердечно-сосудистой системы и/или прогрессирующими онкологическими заболеваниями требуется тщательное наблюдение и мониторинг ЭКГ. В случае появления изменений со стороны психической сферы и/или ЦНС, включая развитие депрессии, рекомендуется наблюдение психиатра в период лечения, а также в течение 6 месяцев после его окончания.
-
Рекомендуется пациентам с грибовидным микозом на поздних стадиях, а также в случае неэффективности или недостаточном ответа на ранее проведенную наружную терапию и/или фототерапию и/или терапию интерфероном альфа-2b вне зависимости от стадии #метотрексат** в дозе не более 50 мг в неделю (стандартная доза – 25 мг 1 раз в неделю перорально) [48,76].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: лечение проводят до достижения полного контроля (отсутствия признаков дальнейшего прогрессирования) или до появления признаков неприемлемой токсичности можно комбинировать с интерфероном альфа-2b (IFN-α).
Перед началом лечения #метотрексатом** или при возобновлении терапии после перерыва необходимо проводить общий (клинический анализ) крови с подсчетом лейкоцитарной формулы и количества тромбоцитов, оценивать активность «печеночных» ферментов (исследование уровня альбумина в крови, общего билирубина в крови, определение активности аспартатаминотрансферазы и аланинаминотрансферазы в крови), а также прицельное рентгенографическое исследование органов грудной клетки и функциональные почечные тесты. При наличии клинических показаний назначают исследования с целью исключения гепатита и других соматических заболеваний.
В процессе лечения #метотрексатом** (ежемесячно в первые 6 месяцев и не реже, чем каждые 3 месяца в дальнейшем, при повышении доз целесообразно повышать частоту обследований) проводят следующие исследования:
1. Обследование ротовой полости и горла для выявления изменений слизистых оболочек.
2. Анализ крови с определением лейкоцитарной формулы и количества тромбоцитов. Даже при применении в обычных терапевтических дозах #метотрексат** может вызвать угнетение системы кроветворения. В случае значительного снижения количества лейкоцитов или тромбоцитов лечение #метотрексатом** немедленно прекращают и назначают симптоматическую поддерживающую терапию.
3. Функциональные печеночные пробы. Особое внимание необходимо уделять выявлению признаков повреждения печени. Лечение #метотрексатом** не следует начинать или необходимо приостанавливать в случае любых отклонений результатов функциональных печеночных тестов или биопсии печени. Обычно показатели нормализуются в течение 2 недель, после чего лечение по решению может быть возобновлено.
4. Функциональные почечные пробы и исследование мочи. Поскольку #метотрексат** экскретируется преимущественно почками, у пациентов с нарушениями функции почек может наблюдаться повышение концентрации #метотрексата** в крови, следствием чего могут быть тяжелые побочные реакции. Необходимо тщательно контролировать состояние пациентов, у которых возможны нарушения функции почек (например, пожилых пациентов).
5. Поскольку #метотрексат** оказывает воздействие на иммунную систему, он может изменять реакцию на вакцинацию и влиять на результаты иммунологических тестов. Особая осторожность необходима при лечении пациентов с неактивными, хроническими инфекциями (такими как опоясывающий лишай, туберкулез, вирусный гепатит В или С) ввиду их возможной активации. В период лечения #метотрексатом** не следует проводить вакцинацию живыми вакцинами.
В связи с возможностью активации хронической инфекции пациентам, которым планируется или проводится терапия #метотрексатом**, может потребоваться определение антител к поверхностному антигену (HBsAg) вируса гепатита B (Hepatitis B virus), определение антител к вирусу гепатита C (Hepatitis C virus) в крови, определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови, определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови.
-
Рекомендуются при поздних стадиях (IIB–IVB) грибовидного микоза, а также в качестве второй линии ранних стадий грибовидного микоза при отсутствии или недостаточном эффекте от проводимой терапии #вориностат 200–400 мг перорально ежедневно [49–52].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: из побочных эффектов ингибитора гистондеацетилаз #вориностата встречаются тромбоцитопения, анемия, анорексия, тошнота, мышечные спазмы. Лечение проводят до достижения отсутствия признаков дальнейшего прогрессирования или до появления признаков неприемлемой токсичности. Противопоказанием является детский возраст до 18 лет. При приеме #вориностата возможно развитие тромбоцитопении и анемии, которые могут потребовать прекращения приема препарата или прекращения лечения. Возможно развитие лейкопении и нейтропении, требующих уменьшения дозы препарата. Отмечалось увеличение плазменной концентрации креатинина. Возможно также развитие гипокалиемии и увеличения плазменной концентрации креатинина, что может потребовать снижения дозы препарата. На фоне приема #вориностата отмечались гипергликемия, в связи с чем может потребоваться назначение диеты и/или гипогликемической терапии. Возможно развитие протеинурии.
Применение комбинированной химиорадиотерапии не только не улучшает среднюю выживаемость пациентов по сравнению с «консервативной» терапией, а даже увеличивает частоту рецидивов, поэтому предпочтительно использовать наружную терапию, биологические препараты или их комбинацию [49].
-
Рекомендуется у пациентов с грибовидным микозом на поздних стадиях с агрессивным течением и/или неэффективностью других методов лечения применение в качестве системной химиотерапии монотерапия #гемцитабином** по схеме 1200 мг/м2 в 1, 8 и 15-й дни 28-дневного цикла, всего 6 циклов [53]
Уровень убедительности рекомендаций С (уровень достоверности доказательств –4)
или
#гемцитабин** в малых дозах с продолжительной инфузией в дозе 250 мг/м2 в течение 6 часов 1 раз в неделю [77]
Уровень убедительности рекомендаций С (уровень достоверности доказательств –4)
-
Рекомендуется брентуксимаб ведотин** для лечения взрослых пациентов при отсутствии или недостаточном эффекте после минимум одной линии предшествующей системной терапии при наличии экспрессии CD30 + антигена [21,54].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Комментарии: назначается в дозе 1,8 мг/кг внутривенно каждый 21 день. Лечение проводят в течение 8 циклов, при достижении частичного ответа допускается проведение еще 8 циклов. При появлении побочных эффектов (наиболее часто – периферическая полинейропатия) допустимо снижение дозы до 1,2 мг/кг и увеличение интервала между циклами. При лечении брентуксимабом ведотином** может развиться анемия, тромбоцитопения и тяжелая пролонгированная (≥1 недели) нейтропения, и это может увеличить риск тяжелых инфекций. Были зарегистрированы случаи повышения уровней аланинаминотрансферазы и аспартатаминотрансферазы. Гипергликемия была зарегистрирована в клинических исследованиях у пациентов с увеличенным индексом массы тела, как с наличием, так и с отсутствием сахарного диабета в анамнезе.
-
Рекомендуется пациентам с прогрессирующими формами грибовидного микоза, рефрактерными как минимум к 5 линиям системной терапии (в том числе, интерферону альфа-2b**, #метотрексату**, брентуксимабу ведотину**, #гемцитабину**, #вориностату) возможно применение непрограммных схем лечения с паллиативной целью, таких как (в убывающем порядке):
- #циклофосфамид** (50-100 мг внутрь ежедневно, не более 1 года терапии, учитывая риск развития миелодиспластического синдрома) [55],
- #этопозид** (50 мг внутрь 2 раза в день) [56],
- #бендамустин** (120мг/м2 в 1,2 дни каждого 3 недельного цикла, всего 6 циклов) [57],
- #бортезомиб** (1,3мг/м2 1,4,8,11 дни, всего 6 циклов терапии) [58].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендуется у пациентов с трансформацией грибовидного микоза в крупноклеточную лимфому и/или внекожном распространении грибовидного микоза в качестве системной химиотерапии режима CHOP – Доксорубицин** 50 мг/м2 в/в кап., день 1, Циклофосфамид** 750 мг/м2 в/в кап., день 1, #Винкристин** 1,4 мг/м2 (суммарно не более 2 мг) в/в, день 1, #Преднизолон** 100 мг внутрь, дни 1-5 , цикл 21 день, всего 6 циклов [59–62, 71-75].
Для взрослых: Уровень убедительности рекомендаций В (уровень достоверности доказательств –2)
Для детей: Уровень убедительности рекомендаций С (уровень достоверности доказательств –4)
-
Рекомендуется аллогенная трансплантация костного мозга (гемопоэтических стволовых клеток) пациентам моложе 60 лет при отсутствии эффекта от других видов терапии, при раннем прогрессировании в поздние стадии заболевания, крупноклеточной трансформацией грибовидного микоза, и поздних стадий ГМ при условии достиждения частичной или полной ремиссии на предтрансплантационном этапе [62,63].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
- Рекомендуется пациентам с жалобами на зуд назначение антигистаминных средств системного действия в соответствии с инструкциями к их применению [64, 65]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Повторное взятие биопсии кожи и повторное проведение патолого-анатомического исследований биопсийного материала кожи, в том числе с применением иммуногистохимического метода, особенно при изменениях клинических проявлений болезни позволяет своевременно выявить прогрессирование заболевания и при необходимости скорректировать терапию.
Медицинская реабилитация
4. Медицинская реабилитация, медицинские показания и противопоказания к применению методов реабилитации
Специальных методов реабилитации при грибовидном микозе не существует.
Госпитализация
6. Организация оказания медицинской помощи
В рамках оказания первичной врачебной медико-санитарной помощи врачи-терапевты участковые, врачи-педиатры участковые, врачи общей практики (семейные врачи) при выявлении у пациентов высыпаний на коже, кожного зуда, выявление симптомов или признаков грибовидного микоза направляют пациента в медицинскую организацию дерматовенерологического профиля или кабинет врача онколога/ гематолога для оказания ему первичной специализированной медико-санитарной помощи, а также осуществляют оказание медицинской помощи в соответствии с рекомендациями медицинской организации дерматовенерологического профиля и/или врача онколога/ гематолога, при отсутствии медицинских показаний для направления в нее.
При невозможности оказания медицинской помощи в рамках первичной специализированной медико-санитарной помощи и наличии медицинских показаний пациент направляется в медицинскую организацию, оказывающую специализированную медицинскую помощь.
Специализированная, в том числе высокотехнологичная, медицинская помощь оказывается врачами-дерматовенерологами и/или врачом-гематологом в стационарных условиях.
Специализированная, медицинская помощь оказывается пациентам на ранних стадиях (IA–IIA) врачами-дерматовенерологами
Специализированная, в том числе высокотехнологичная медицинская помощь оказывается пациентам на стадиях (IIB–IVB) врачами гематологами/онкологами
Показания для плановой госпитализации в медицинскую организацию:
1) Показания для оказания медицинской помощи в дневном стационаре:
2) Показания для оказания медицинской помощи в стационарных условиях:
3) Показания к экстренной госпитализации в стационар медицинской организации, оказывающей специализированную, в том числе высокотехнологичную, медицинскую помощь по профилю «гематология» и «онкология»:
Показания к выписке пациента из медицинской организации:
Профилактика
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Методов профилактики грибовидного микоза в настоящее время не существует, поскольку неизвестен этиологический фактор(ы), ведущие к развитию заболевания. Диспансерное наблюдение врачом-гематологом или врачом-онкологом осуществляется в период лечения и после достижения ремиссии лимфомы.
При рецидиве или прогрессировании грибовидного микоза необходимо выполнять повторную биопсию кожи и повторное патолого-анатомическое исследование (операционного) биопсийного материала кожи, а также повторное патолого-анатомическое исследование (операционного) биопсийного материала кожи с применением иммуногистохимического метода для исключения крупноклеточной трансформации, при необходимости – повторную процедуру стадирования. Тактика лечения рецидивов также базируется на определении стадии заболевания, учитывается развитие резистентности к предыдущим видам терапии.
-
Рекомендуется пациентам с ранними стадиями ежегодно проходить: физикальный осмотр с картированием кожи, прицельную рентгенографию органов грудной клетки и УЗИ лимфатических узлов (одна анатомическая зона) периферических[3, 6, 7, 65]
-
Рекомендуется пациентам с поздними стадиями каждые 6 месяцев проходить: физикальный осмотр с картированием кожи, УЗИ лимфатических узлов (периферических), КТ органов грудной полости, брюшной полости и малого таза) [3, 6, 7, 65]
Информация
Источники и литература
-
Клинические рекомендации Национального гематологического общества
-
Клинические рекомендации Российского общества дерматовенерологов и косметологов
- Korgavkar K., Xiong M., Weinstock M. Changing incidence trends of cutaneous T-cell lymphoma. JAMA Dermatology. 2013; 149 (11): 1295–1299. DOI:10.1001/jamadermatol.2013.5526 Zwierzina H., Suciu S., Loeffler-Ragg J. et al. Low-dose cytosine arabinoside (LD-AraC) vs LD-AraC plus granulocyte/macrophage colony stimulating factor vs LD-AraC plus Interleukin-3 for myelodysplastic syndrome patients with a high risk of developing acute leukemia: final results of a randomized phase III study (06903) of the EORTC Leukemia Cooperative Group. Leukemia. 2005;19 (11):1929–1933. DOI:10.1038/sj.leu.2403934. Keehn C.A., Belongie I.P., Shistik G. et al. The diagnosis, staging, and treatment options for mycosis fungoides. Cancer Control. 2007; 14 (2): 102–111. DOI:10.1177/107327480701400203. Cerroni L. Mycosis fungoides-clinical and histopathologic features, differential diagnosis, and treatment. Semin Cutan Med Surg. 2018; 37 (1): 2–10. DOI:10.12788/j.sder.2018.002. Willemze R. Mycosis fungoides variants-clinicopathologic features, differential diagnosis, and treatment. Semin Cutan Med Surg. 2018; 37 (1):11–17. DOI:10.12788/j.sder.2018.004. Olsen E., Vonderheid E., Pimpinelli N. et al. Revisions to the staging and classification of mycosis fungoides and Sézary syndrome: A proposal of the International Society for Cutaneous Lymphomas (ISCL) and the cutaneous lymphoma task force of the European Organization of Research and Treatment of Cancer (EORTC). Blood. 2007 15; 110 (6): 1713–1722. DOI:10.1182/blood-2007-03-055749. Horwitz S.M., Olsen E.A., Duvic M. et al. Review of the treatment of mycosis fungoides and sézary syndrome: a stage-based approach. J Natl Compr Canc Netw. 2008; 6 (4): 436–442. doi: 10.6004/jnccn.2008.0033 Delfau-Larue M.H., Laroche L., Wechsler J. et al. Diagnostic value of dominant T-cell clones in peripheral blood in 363 patients presenting consecutively with a clinical suspicion of cutaneous lymphoma. Blood. 2000; 96 (9): 2987–2992. DOI:10.1182/blood.v96.9.2987 Ponti R., Quaglino P., Novelli M. et al. T-cell receptor γ gene rearrangement by multiplex polymerase chain reaction/heteroduplex analysis in patients with cutaneous T-cell lymphoma (mycosis fungoides/Sézary syndrome) and benign inflammatory disease: Correlation with clinical, histological and immunophenotypical findings. Br J Dermatol. 2005; 153 (3): 565–573. DOI:10.1111/j.1365-2133.2005.06649.x Kirsch I.R., Watanabe R., O’Malley J.T. et al. TCR sequencing facilitates diagnosis and identifies mature T cells as the cell of origin in CTCL. Sci Transl Med. 2015 Oct 7;7 (308): 308ra158. DOI:10.1126/scitranslmed.aaa9122 Matos T.R., de Rie M.A., Teunissen M.B. Research techniques made simple: High-throughput sequencing of the T-cell receptor. J Invest Dermatol. 2017; 137 (6): e131–e138. DOI:10.1016/j.jid.2017.04.001 Scherer F., Kurtz D.M., Diehn M., Alizadeh A.A. High-throughput sequencing for noninvasive disease detection in hematologic malignancies. Blood. 2017; 130 (4): 440–452. DOI:10.1182/blood-2017-03-735639 Jawed S.I., Myskowski P.L., Horwitz S. et al. Primary cutaneous T-cell lymphoma (mycosis fungoides and Sézary syndrome): part I. Diagnosis: clinical and histopathologic features and new molecular and biologic markers. J Am Acad Dermatol. 2014; 70 (2): 205.e1–16 DOI:10.1016/j.jaad.2013.07.049 Rea B., Haun P., Emerson R. et al. Role of high-throughput sequencing in the diagnosis of cutaneous T-cell lymphoma. J Clin Pathol. 2018; 71 (9): 814–820. DOI:10.1136/jclinpath-2018-205004 Ferner R.E. Adverse drug reactions in dermatology. Clin Exp Dermatol. 2015; 40 (2): 105–109. DOI:10.1111/ced.12572 Federico M., Bellei M., Marcheselli L. et al. Peripheral T cell lymphoma, not otherwise specified (PTCL-NOS). A new prognostic model developed by the International T cell Project Network. Br J Haematol. 2018; 181 (6): 760–769. DOI:10.1111/bjh.15258 Huang D.Y., Hu Y.F., Wei N., et al. Innovative analysis of predictors for overall survival from systemic non-Hodgkin T cell lymphoma using quantile regression analysis. Chin Med J (Engl). 2019; 132 (3): 294–301. DOI:10.1097/CM9.0000000000000088 Olsen E.A. Interferon in the treatment of cutaneous T-cell lymphoma. Dermatol Ther. 2003; 16 (4): 311–321. DOI:10.1111/j.1396-0296.2003.01643.x Campbell J.M., Bateman E., Stephenson M.D. et al. Methotrexate-induced toxicity pharmacogenetics: an umbrella review of systematic reviews and meta-analyses. Cancer Chemother Pharmacol. 2016; 78 (1): 27–39. DOI:10.1007/s00280-016-3043-5 Mann B.S., Johnson J.R., Cohen M.H. et al. FDA approval summary: Vorinostat for treatment of advanced primary cutaneous T‐cell lymphoma. Oncologist. 2007; 12 (10): 1247–1252. DOI:10.1634/theoncologist.12-10-1247 Prince H.M., Kim Y.H., Horwitz S. et al. Brentuximab vedotin or physician’s choice in CD30-positive cutaneous T-cell lymphoma (ALCANZA): an international, open-label, randomised, phase 3, multicentre trial. Lancet. 2017; 390 (10094): 555–566. DOI:10.1016/S0140-6736(17)31266-7 Gerami P., Guitart J. The spectrum of histopathologic and immunohistochemical findings in folliculotropic mycosis fungoides. Am J Surg Pathol. 2007; 31 (9): 1430–1438. DOI:10.1097/PAS.0b013e3180439bdc Alpdogan O., Kartan S., Johnson W. et al. Systemic therapy of cutaneous T-cell lymphoma (CTCL). Chin Clin Oncol. 2019; 8 (1): 10. DOI:10.21037/cco.2019.01.02 Swerdlow S.H., Campo E., Pileri S.A. et al. The 2016 revision of the World Health Organization classification of lymphoid neoplasms. Blood. 2016; 127 (20): 2375–2390. DOI:10.1182/blood-2016-01-643569 Guitart J., Kennedy J., Ronan S. et al. Histologic criteria for the diagnosis of mycosis fungoides: Proposal for a grading system to standardize pathology reporting. J Cutan Pathol. 2001; 28 (4): 174–183. DOI:10.1034/j.1600-0560.2001.028004174.x Raghavan S.S., Kim J. Histopathologic approach to epidermotropic lymphocytic infiltrates. Semin Cutan Med Surg. 2018; 37 (1): 56–60. DOI:10.12788/j.sder.2018.003 Charli-Joseph Y., Toussaint-Caire S., Lome-Maldonado C. et al. Approach to dermal-based lymphoid infiltrates and proliferations. Semin Cutan Med Surg. 2018; 37 (1): 61–74. DOI:10.12788/j.sder.2018.015 Kempf W., Mitteldorf C. Pathologic diagnosis of cutaneous lymphomas. Dermatol Clin. 2015; 33 (4): 655–681. DOI: 10.1016/j.det.2015.05.002 Vandergriff T., Nezafati K.A., Susa J. et al. Defining early mycosis fungoides: Validation of a diagnostic algorithm proposed by the International Society for Cutaneous Lymphomas. J Cutan Pathol. 2015; 42 (5): 318–328. DOI:10.1111/cup.12470 Pimpinelli N., Olsen E.A., Santucci M. et al. Defining early mycosis fungoides. J Am Acad Dermatol. 2005; 53 (6): 1053–1063. DOI:10.1016/j.jaad.2005.08.057 Kash N., Massone C., Fink-Puches R. et al. Phenotypic variation in different lesions of mycosis fungoides biopsied within a short period of time from the same patient. Am J Dermatopathol. 2016; 38 (7): 541–545. DOI:10.1097/DAD.0000000000000493 De Masson A., Battistella M., Vignon-Pennamen M.D. et al. Syringotropic mycosis fungoides: Clinical and histologic features, response to treatment, and outcome in 19 patients. J Am Acad Dermatol. 2014; 71 (5): 926–934. DOI:10.1016/j.jaad.2014.06.033 Zhang Y., Wang Y., Yu R. et al. Molecular markers of early-stage mycosis fungoides. J Invest Dermatol. 2012; 132 (6): 1698–1706. DOI:10.1038/jid.2012.13 Haghighi B., Smoller B.R., LeBoit P.E. et al. Pagetoid reticulosis (Woringer-Kolopp disease): An immunophenotypic, molecular, and clinicopathologic study. Mod Pathol. 2000; 13 (5): 502–510. DOI:10.1038/modpathol.3880088 Haththotuwa R., Zilinskiene L., Oliff J. et al. Biopsy correlation of surface area vs. single‐axis measurements on computed tomography scan of lymph nodes in patients with erythrodermic mycosis fungoides and Sézary syndrome. Br J Dermatol. 2017; 177 (3): 877–878. DOI:10.1111/bjd.15266 Salhany K.E., Greer J.P., Cousar J.B. et al. Marrow involvement in cutaneous T-cell lymphoma. A clinicopathologic study of 60 cases. Am J Clin Pathol. 1989; 92 (6): 747–754. DOI:10.1093/ajcp/92.6.747 Horna P., Wang S.A., Wolniak K.L. et al. Flow cytometric evaluation of peripheral blood for suspected Sézary syndrome or mycosis fungoides: International guidelines for assay characteristics. Cytometry B Clin Cytom. 2021; 100 (2): 142–155. DOI:10.1002/cyto.b.21878 Kim E.J., Hess S., Richardson S.K. et al. Immunopathogenesis and therapy of cutaneous T cell lymphoma. J Clin Invest. 2005; 115 (4): 798–812. DOI:10.1172/jci24826 Zackheim H.S. Treatment of patch-stage mycosis fungoides with topical corticosteroids. Dermatol Ther. 2003; 16 (4): 283–287. DOI:10.1111/j.1396-0296.2003.01639.x Diederen P.V., Van Weelden H., Sanders C.J. et al. Narrowband UVB and psoralen-UVA in the treatment of early-stage mycosis fungoides: A retrospective study. J Am Acad Dermatol. 2003; 48 (2): 215–219. DOI:10.1067/mjd.2003.80
-
Клинические рекомендации Российского общества онкогематологов
Информация
Список сокращений
Термины и определения
Критерии оценки качества медицинской помощи

Критерии оценки качества медицинской помощи Грибовидный микоз (стационарный этап)

-
Кубанов Алексей Алексеевич –академик РАН, доктор медицинских наук, профессор, Президент Российского общества дерматовенерологов и косметологов.
-
Поддубная Ирина Владимировна – академик РАН, заслуженный деятель образования РФ, доктор медицинских наук, профессор, председатель Российского общества онкогематологов.
-
Белоусова Ирена Эдуардовна – доктор медицинских наук, член Российского общества дерматовенерологов и косметологов.
-
Самцов Алексей Викторович – доктор медицинских наук, профессор, Заслуженный деятель науки РФ, Заслуженный врач РФ, член Российского общества дерматовенерологов и косметологов.
-
Знаменская Людмила Федоровна – доктор медицинских наук, член Российского общества дерматовенерологов и косметологов.
-
Чикин Вадим Викторович – доктор медицинских наук, член Российского общества дерматовенерологов и косметологов
-
Карамова Арфеня Эдуардовна – кандидат медицинских наук, член Российского общества дерматовенерологов и косметологов.
-
Кузьмин Алексей Александрович, главный врач КОГКБУЗ «Центр онкологии и медицинской радиологии», г. Киров.
-
Горенкова Лилия Гамилевна – кандидат медицинских наук, член Ассоциации содействия развитию гематологии и трансплантологии костного мозга "Национальное гематологическое общество".
-
Кравченко Сергей Кириллович – кандидат медицинских наук, член Ассоциации содействия развитию гематологии и трансплантологии костного мозга "Национальное гематологическое общество"
-
Чернова Наталья Геннадиевна – к.м.н., заведующая отделением гематологии и химиотерапии ГБУЗ «ГКБ40 ДЗМ40»
-
Стефанов Дмитрий Николаевич – научный сотрудник, зав. научно-организационным отделом, ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России, член Российского общества онкогематологов.
-
Воронцова Анастасия Александровна – научный сотрудник отдела дерматологии ФГБУ «Государственный научный центр дерматовенерологии и косметологии» Минздрава России, член Российского общества дерматовенерологов и косметологов.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
1. Врачи-специалисты: дерматовенерологи, гематологи, онкологи.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД)для методов диагностики (диагностических вмешательств)
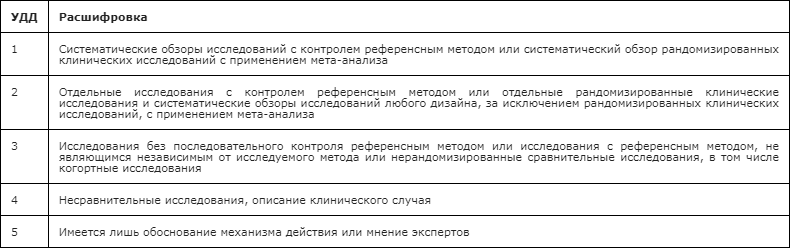
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД)для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)

Таблица 3. Шкала оценки уровней убедительности рекомендаций(УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)

Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Алгоритм диагностики ранних форм грибовидного микоза
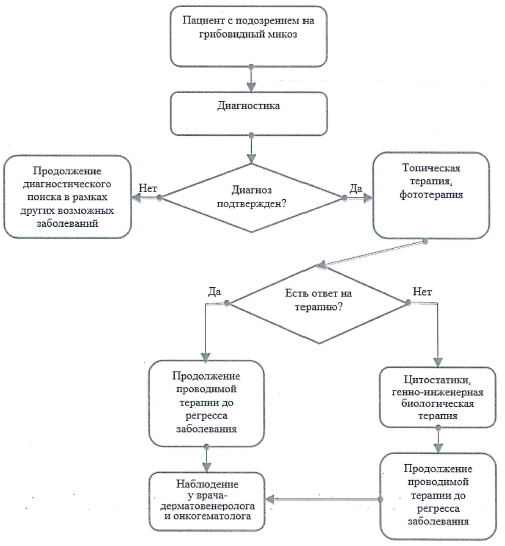
1. Грибовидный микоз относят к злокачественным заболеваниям кожи, с относительно благоприятным течением и медленной прогрессией. У большинства пациентов с ранними стадиями грибовидного микоза не происходит прогрессирования в более поздние стадии. Причина развития грибовидного микоза не установлена.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Нет
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.