Хронический гепатит С у взрослых
 Версия: Клинические протоколы МЗ РК - 2025 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2025 (Казахстан)
Хронический вирусный гепатит c (B18.2)
Гастроэнтерология
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «13» февраля 2026 года
Протокол №245
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
ХРОНИЧЕСКИЙ ГЕПАТИТ С У ВЗРОСЛЫХ
Хронический гепатит С – заболевание печени, вызванное вирусом гепатита С, длительностью 6 и более месяцев.
Хронический гепатит С – заболевание печени, вызванное вирусом гепатита С, длительностью 6 и более месяцев.
Вводная часть
Код (ы) МКБ:
Дата разработки и пересмотра протокола: 2014 г. (пересмотр: 2015 г., 2017 г., 2020 г., 2025 г.)
Категория пациентов: взрослые.
Шкала уровня доказательности
|
МКБ-10
|
МКБ-11 | ||
|
В18.2
|
Хронический вирусный гепатит С |
1E51.1
|
Хронический вирусный гепатит С |
Дата разработки и пересмотра протокола: 2014 г. (пересмотр: 2015 г., 2017 г., 2020 г., 2025 г.)
Пользователи протокола: гастроэнтерологи, гепатологи, врачи общей практики, терапевты, инфекционисты, онкологи, хирурги.
Категория пациентов: взрослые.
Шкала уровня доказательности
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты, которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
Классификация
Клиническая классификация включает [2, 40, 46]:
• вирусологический статус;
• активность (биохимическая и/или гистологическая);
• стадия фиброза;
• осложнения;
• внепеченочные проявления.
Диагностика
Методы, подходы и процедуры диагностики [2-10, 25-38, 41, 44]
Диагностические критерии постановки диагноза хронический гепатит С: наличие в крови HCV РНК на протяжении 6 и более месяцев.
Жалобы [2-6]
Хронический гепатит С протекает бессимптомно, может проявляться:
• повышенной утомляемостью;
• артралгией;
• тошнотой и снижением аппетита;
• нарушениями сна;
• другими неспецифическими симптомами.
Внепеченочные проявления гепатита С:
• депрессия (оценивается у всех пациентов с использованием шкалы Бека);
• криоглобулинемия;
• В-клеточные лимфопролиферативные заболевания;
• поздняя кожная порфирия;
• васкулиты;
• красный плоский лишай;
• синдром Шегрена;
• гломерулонефрит;
• сахарный диабет 2 типа.
Физикальное обследование [3,4]
При физикальном обследовании изменения могут не определяться. В продвинутой стадии вирусного гепатита С возможна желтуха, гепатомегалия, телеангиоэктазии, пальмарная эритема, спленомегалия.
Таблица 1. Интерпретация результатов ИХА/ИФА и ПЦР
Таблица 2. Биохимическая активность [11]
Таблица 3. Интерпретация результатов VCTE [31, 48]
Критериями успешного результата исследования являются:
Таблица 4. Морфологическая диагностика степени некровоспалительной активности гепатита [34, 35]
Диагностический алгоритм
Последовательность тестирования (CDC) для гепатита С, адаптированная разработчиками на схеме 1 [46].
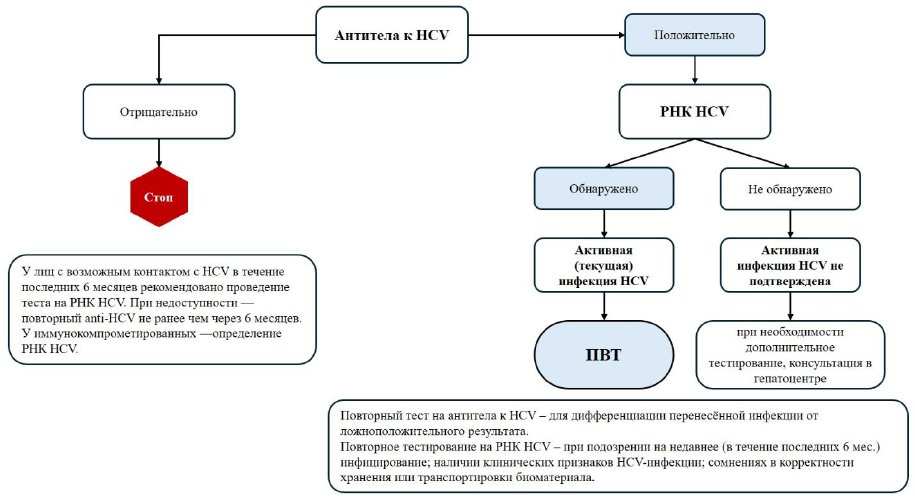 Схема 1. Алгоритм диагностики вирусного гепатита С
Схема 1. Алгоритм диагностики вирусного гепатита С
Анамнез [25-29]
При сборе анамнеза следует учитывать принадлежность к группам риска:
• дети, рожденные от матерей, инфицированных вирусами гепатита B, C, D;
• доноры и реципиенты крови, её компонентов, других тканей и органов;
• беременные;
• медицинские работники;
• контактные в очагах инфекции по гепатитам B, C, D;
• пациенты перед плановыми и экстренными оперативными вмешательствами;
• инвазивные медицинские манипуляции с использованием многоразовых инструментов (оперативные вмешательства, иглорефлексотерапия, косметологические процедуры и др.) и оборудования (эндоскопов), стоматологические манипуляции;
• инвазивные немедицинские манипуляции с использованием многоразовых инструментов (народные/традиционные методы лечения, пирсинг, татуаж и др.);
• экстракорпоральные методы детоксикации (диализ, плазмаферез и др.);
• пациенты с онкологическими и онкогематологическими заболеваниями;
• пациенты, получающие иммуносупрессивную терапию (в т.ч. химиотерапия; иммуносупрессия после трансплантации печени; кортикостероиды, иммуносупрессоры и биологическая терапия при аутоиммунных заболеваниях);
• пациенты с туберкулезом;
• лица, живущие с ВИЧ (включая планирующих или получающих доконтактную профилактику ВИЧ);
• уязвимые группы (лица, употребляющие инъекционные наркотики, мужчины, имеющие половые контакты с мужчинами, работники коммерческого секса).
• лица, находящиеся в местах заключения;
• иностранные граждане, постоянно проживающие на территории Республики Казахстан.
Физикальное обследование [3,4]
Лабораторные исследования:
Основные (обязательные) лабораторные обследования:
Основные (обязательные) лабораторные обследования:
• общий анализ крови – оценка общего состояния; исключение лейкоцитоза, анемии, тромбоцитопении или других цитопений;
• биохимический анализ крови (АЛТ, АСТ, общий билирубин, прямой билирубин, креатинин) – определение тяжести гепатита, активности воспаления печени;
• экспресс тест капиллярной крови для выявления anti-HCV с целью первичной диагностики гепатита С (УД-А1) / anti-HCV в сыворотке и плазме (УД-А1) [2,7,8,10, 30,41];
• HCV РНК (качественный анализ) – маркёр репликации гепатита С.
Дополнительные лабораторные обследования:
• коагулограмма – состояние гемостаза и возможных нарушений коагуляции;
• альфа-фетопротеин в крови – скрининг гепатоцеллюлярной карциномы;
• биохимический анализ крови (ГГТП, ЩФ, альбумин, глюкоза, мочевая кислота, протеинограмма, липидограмма, натрий) – исследование функций печени, почек, углеводного и жирового обмена;
• тест на беременность – исключение беременности перед назначением ПВТ;
• HCV РНК (количественный) – мониторинг вирусной нагрузки (УД-А);
• генотип HCV – при неудачах ПВТ;
• маркеры других парентеральных инфекций, таких как HBV (HBsAg, anti-HBs, anti-HBc total), HDV (anti-HDV у носителей HBsAg), ВИЧ (anti-HIV), а также (при подозрении на острый гепатит) HAV (anti-HAV IgM) и HEV (anti-HEV IgM);
• ANA, AMA-М2, IgG или гамма-глобулин – исключение аутоиммунных заболеваний печени;
• церулоплазмин, суточная экскреция меди с мочой – исключение болезни Вильсона-Коновалова;
• сывороточное железо, ферритин, фолиевая кислота, витамин В12 в крови –диагностика анемии, синдрома вторичной перегрузки железом, гемохроматоза;
• общий анализ мочи – для исключения мочевой инфекции.
Таблица 1. Интерпретация результатов ИХА/ИФА и ПЦР
|
Показатели
|
Интерпретация | Дальнейшая тактика |
|
anti-HCV (+)
HCV РНК (+)
|
• ВГС.
|
Установление активности и стадии заболевания, генотипа, показаний к ПВТ |
|
anti-HCV (–)
HCV РНК (+)
|
• Лабораторная ошибка.
• ОГС в первые недели (anti-HCV определяется в 50% в момент острых проявлений).
• ВГС у лиц с иммуносупрессией (пациенты, получающие иммуносупрессивные препараты (ГКС, химио- и/или лучевую терапию), находящиеся на гемодиализе, после трансплантации, с ВИЧ-инфекцией*).
|
ИХА/ИФА и ПЦР в динамике |
|
anti-HCV (+)
HCV РНК (–)
|
• Лабораторная ошибка.
• Паст-инфекция.
• Ложноположительный результат ИФА.
• Пассивно приобретенные антитела во время гемотрансфузии.
• Пассивно приобретенные ребенком антитела матери.
• Интермиттирующая виремия.
• Низкая ВН < лимита определения.
|
ПЦР через 12 и 24 недели для подтверждения элиминации вируса |
Таблица 2. Биохимическая активность [11]
|
АЛТ (АСТ)
|
Активность |
|
<1 ВГН
|
Минимальная |
|
1-2 ВГН
|
Пограничная |
|
2-5 ВГН
|
Слабовыраженная |
|
5-15 ВГН
|
Умеренно выраженная |
|
>15 ВГН
|
Выраженная |
|
> 10000 Ед/л
|
Массивная |
Биомаркеры фиброза печени:
• APRI (AST / Platelets Ratio Index) включает два параметра: АСТ и количество тромбоцитов.
− Формула расчета: APRI = (AСT/ВГН) x 100)/Количество тромбоцитов (109/л).
− Электронный калькулятор: www.hepatitisc.uw.edu/page/clinical-calculators/apri
− Интервал 0,3-0,5 исключают значимый фиброз и цирроз, более 1,5 - указывают на клинически значимый фиброз.
• FIB-4 (Fibrosis 4 Score) включает показатели: возраст, АСТ, АЛТ, тромбоциты.
− Формула расчета: FIB-4 = возраст (лет) х АСТ / (тромбоциты (109/л) х √(АЛТ)).
− Электронный калькулятор: https://www.hepatitisc.uw.edu/page/clinical-calculators/fib-4.
− Интерпретация результатов: <1.30 = F0-F1; >2.67 = F3-F4.
− При сочетании с HCV и / или с HIV: <1.45 = F0-F1; >3.25 = F3-F4.
Инструментальные исследования
Основные (обязательные) инструментальные обследования:
Основные (обязательные) инструментальные обследования:
• УЗИ органов брюшной полости: позволяет оценить структуру, признаки фиброза, цирроза печени и его осложнений; наличие объемных образований (ГЦК и др.) (УД – А).
• VCTE (вибрационно-контролируемая транзиентная эластография) для определения эластических свойств печени на основании отраженных вибрационных импульсов и их последующего компьютерного анализа. (УД – А).
Таблица 3. Интерпретация результатов VCTE [31, 48]
|
Стадия фиброза по METAVIR
|
Размах значений, кПа | Диагностическая точность |
| F2 | 7,0 – 9,9 | чувствительность 75% и специфичность 84% |
| F3 | 10 – 12,9 | чувствительность 87% и специфичность 88% |
| F4 | более 13 | чувствительность 88% и специфичность 94% |
Получение корректных результатов эластометрии затруднено в случаях:
• ожирения (ИМТ>35кг/м2) и выраженного стеатоза печени (целесообразно выполнение эластометрии с применением XL-датчика);
• цитолиза (АЛТ или АСТ >3 ВГН);
• выраженного холестаза;
• застойной сердечной недостаточности.
Критериями успешного результата исследования являются:
• интерквартильный коэффициент (IQR) не более 30% показателя эластичности;
• не менее 10 достоверных измерений в одной точке исследования;
• не менее 60% успешных измерений.
Дополнительные инструментальные обследования [36, 41, 44]
• Пункционная биопсия печени для морфологической оценки степени повреждения печени. Оценка полуколичественных шкал степени некро-воспалительных изменений и стадии фиброза печени в таблицах 4 и 5;
• МРТ или КТ органов брюшной полости с контрастным усилением с целью выявления признаков цирроза печени и его осложнений, а также для обнаружения и дифференциального диагноза объемных образований печени;
• ВГДС для исключения варикозно расширенных вен пищевода и желудка, портальной гипертензивной гастропатии, согласно критериям Baveno VII, ВГДС рекомендована пациентам с показателями VCTE>20 кПа и количеством тромбоцитов <150 000/мм3, особенно с показателями VCTE селезенки ≥40 кПа);
• ЭКГ для пациентов с прогрессирующим заболеванием печени.
Таблица 4. Морфологическая диагностика степени некровоспалительной активности гепатита [34, 35]
|
Диагноз гистологический
|
METAVIR | Knodell (IV) | Ishak |
| ХГ минимальной активности | А1 | 0-3 | 0-3 |
| ХГ слабовыраженной активности | А1 |
4-5
|
4-6 |
| ХГ умеренной активности | А2 |
6-9
|
7-9 |
| ХГ выраженной активности | А3 | 10-12 | 10-15 |
| ХГ выраженной активности с мостовидными некрозами | А3 |
13-18
|
16-18 |
Таблица 5. Морфологическая диагностика стадии заболевания печени (выраженности фиброза) [34, 35]
|
Стадия фиброза
|
METAVIR* | Knodell (IV) | Ishak |
|
Нет фиброза
|
F0 | 0 | 0 |
|
Портальный фиброз нескольких портальных трактов
|
F1 | 1 | 1 |
| Портальный фиброз большинства портальных трактов | F1 | 1 | 2 |
|
Несколько мостовидных фиброзных септ
|
F2 | 3 | 3 |
|
Много мостовидных фиброзных септ
|
F3 | 3 | 4 |
|
Неполный цирроз
|
F4 | 4 | 5 |
|
Полностью сформировавшийся цирроз
|
F4 | 4 | 6 |
* Для определения стадии заболевания печени чаще применяется шкала METAVIR
Показания для консультации узких специалистов:
• Эндокринолог – нарушения углеводного обмена, метаболический синдром, патология щитовидной железы;
• Психиатр – подозрение на депрессию;
• Дерматолог/аллерголог/ревматолог – кожные/аллергические и аутоиммунные реакции;
• Трансплантолог – показания к ТП;
• Нефролог – внепеченочные проявления ХГС;
• Онколог – опухоли печени;
• Консультация других специалистов – по показаниям.
Диагностический алгоритм
Последовательность тестирования (CDC) для гепатита С, адаптированная разработчиками на схеме 1 [46].

Дифференциальный диагноз
Дифференциальный диагноз [1-7]
Таблица 6. Дифференциальный диагноз хронического гепатита С
|
Диагноз
|
Обоснование для диф. диагностики | Обследование | Критерии исключения диагноза |
| ОВГ | Общие клинико-лабораторные симптомы гепатита | anti-HAV IgM; HBsAg, HBeAg, anti-HBs, anti-HBe, anti-HBc /IgM, anti-НВс /IgG, anti-HDV IgM, anti-HDV total, anti-HЕV IgM, anti-HCV; ПЦР: HCV РНК, HBV ДНК, РНК HDV, ДНК HEV в крови и стуле | Отсутствие маркеров вирусных гепатитов, отрицательные результаты ПЦР, либо положительные результаты серологических и/или молекулярных тестов при длительности инфекции менее 6 месяцев |
| ХГВ, ХГD | Общие клинико-лабораторные симптомы гепатита | HBsAg, anti-HDV, ПЦР (HBV ДНК, HDV РНК) | Отсутствие маркеров вирусных гепатитов B и D, отрицательные результаты молекулярных тестов |
|
ПБХ
|
Общие клинико-лабораторные симптомы гепатита | ЩФ, ГГТП, AMA, АМА2, IgM, липидограмма, в сложных случаях – биопсия печени | Отсутствие синдрома холестаза, дислипидемии, гистологических признаков ПБХ, отрицательные результаты AMA, АМА2, нормальный уровень IgM |
|
ПСХ
|
Общие клинико-лабораторные симптомы гепатита | ЩФ, ГГТП, рANCA, ЭРХПГ, МР-холангиография, в сложных случаях – биопсия печени | Отсутствие синдрома холестаза, отсутствие изменений желчных протоков на холангиограммах |
|
МАСГ
|
Общие клинико-лабораторные симптомы гепатита | Физикальный осмотр, ФПП, липидограмма, глюкоза крови, инсулин, HbA1c, УЗИ органов брюшной полости, в сложных случаях – биопсия печени | Отсутствие признаков метаболического синдрома (в т.ч. ожирения, АГ, инсулинорезистентности, сахарного диабета 2 типа, дислипидемии), признаков стеатоза печени при УЗИ и биопсия печени |
| Гемохроматоз и симптомы перегрузки железом | Общие клинико-лабораторные симптомы гепатита | Железо, ферритин в сыворотке крови, генетические исследования, в сложных случаях – биопсия печени | Отсутствие клинико-лабораторных признаков перегрузки железом, отрицательные результаты генетических исследований, отсутствие сидероза печени |
| Лекарственно-индуцированное повреждение печени | Общие клинико-лабораторные симптомы гепатита | Анамнез, ФПП, IgE, тест ППН, генетические исследования, в сложных случаях – биопсия печени | Отсутствие связи с приемом причинного препарата, отрицательные результаты аллерготестов и генетических исследований |
|
АИГ
|
Общие клинико-лабораторные симптомы гепатита | ANA, ASMA, AAA, LKM-1, SLA/LP, anti-LC, IgG, гамма-глобулины | Отсутствие аутоантител, гипергаммаглобулинемии, характерной гистологической картины, сопутствующих аутоиммунных заболеваний |
Лечение (амбулатория)
Тактика лечения на амбулаторном уровне [2, 7-8, 37-38, 41]
Цели лечения ХГС:
• эрадикация ВГС;
• улучшение качества жизни и снижение стигматизации;
• профилактика дальнейшей передачи ВГС (УД-А1).
Компоненты лечения:
• режимные (немедикаментозные) мероприятия;
• этиотропная терапия.
Общие мероприятия [41]:
• Вакцинация против вирусных гепатитов А и В у пациентов, не имеющих иммунитет к данным инфекциям (УД-А1);
• Барьерная контрацепция.
Рекомендации по физической активности [40]:
Немедикаментозное лечение [7, 8, 40-43]
Минимизация факторов риска прогрессирования: исключение алкоголя, табака, наркотических веществ (включая марихуану), гепатотоксичных лекарственных средств, включая биологически активные добавки, нормализация веса тела и т.д. (УД – А).
Рекомендации по физической активности [40]:
У пациентов с ХГС с сопутствующим метаболическим синдромом рекомендуется умеренная аэробная активность ≥150 мин/неделю или ≥75 мин/нед. интенсивной активности.
Таблица 8. Противовирусные препараты ХГС [10-11]
Упрощенные режимы ПВТ [40].
Таблица 7. Противопоказания к ПВТ [10-11]
Общие рекомендации по проведению ПВТ [1, 6, 8, 41]
Схема 2. Рекомендованная тактика ведения пациентов при перерывах в терапии ПППД, у ранее не лечившихся пациентов без цирроза или с компенсированным циррозом, получающих глекапревир/пибрентасвир или софосбувир/велпатасвир [46]
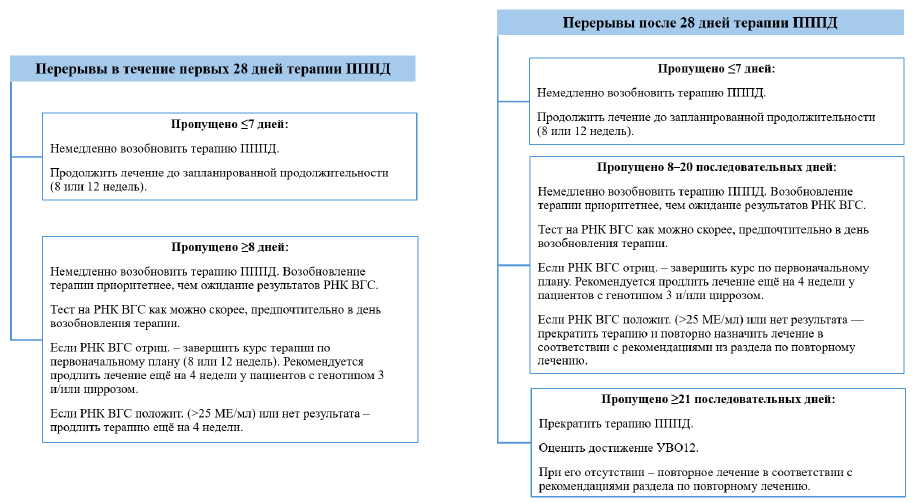
Таблица 9. Режимы противовирусной терапии хронического гепатита С [2, 7-8, 19-20, 40-41]
Рекомендации по питанию [43]:
• Сбалансированное питание с акцентом на:
− нормальный белковый рацион (1–1,2 г/кг/сут).
− умеренное потребление жиров (30–35% суточной калорийности).
− ограничение простых углеводов и насыщенных жиров.
• Рекомендуется средиземноморская диета:
− овощи, фрукты, бобовые, цельнозерновые.
− рыба, орехи, оливковое масло.
− ограничение красного и переработанного мяса, сахара и фруктозы.
• Отказ от алкоголя строго рекомендован, особенно у пациентов с активным фиброзом.
− Кофе разрешён и полезен: умеренное потребление (2–3 чашки в день) связано со снижением риска фиброза и ГЦК [7, 37, 38, 41].
Медикаментозное лечение на амбулаторном уровне [1-2, 5-8, 10-24, 40]
Таблица 8. Противовирусные препараты ХГС [10-11]
|
№
|
Международное непатентованное наименование ЛС | Способ применения | Кратность применения | Длительность применения | УД |
| 1 |
Софосбувир
|
400 мг внутрь | 1 раз в сутки | 12/24 недель | А |
| 2 | Софосбувир/ велпатасвир | 400 мг/100 мг внутрь | 1 раз в сутки | 12/24 недель | А |
| 3 |
Глекапревир/ пибрентасвир
|
300 мг/120 мг внутрь | 1 раз в сутки | 8/16/12 недель | А |
| 4 | Элбасвир/ гразопревир* | 50 мг/100 мг внутрь | 1 раз в сутки | 12 недель | А |
| 5 | Софосбувир/велпатасвир/ воксилапревир* |
400мг/100мг
/100 мг внутрь
|
1 раз в сутки | 12 недель | А |
| 6 |
Рибавирин
|
600-1200мг внутрь | 1/2 раза в сутки | 12/16/24 недель | А |
* После регистрации и разрешения к применению в РК по соответствующим показаниям
Упрощенные режимы ПВТ [40].
Упрощенные режимы ПВТ предполагают пангенотипические комбинации ПППД у пациентов с компенсированным заболеванием печени (УД-В1).
Схема 3. Алгоритм упрощенного лечения ХГС [2, 30, 40, 46]
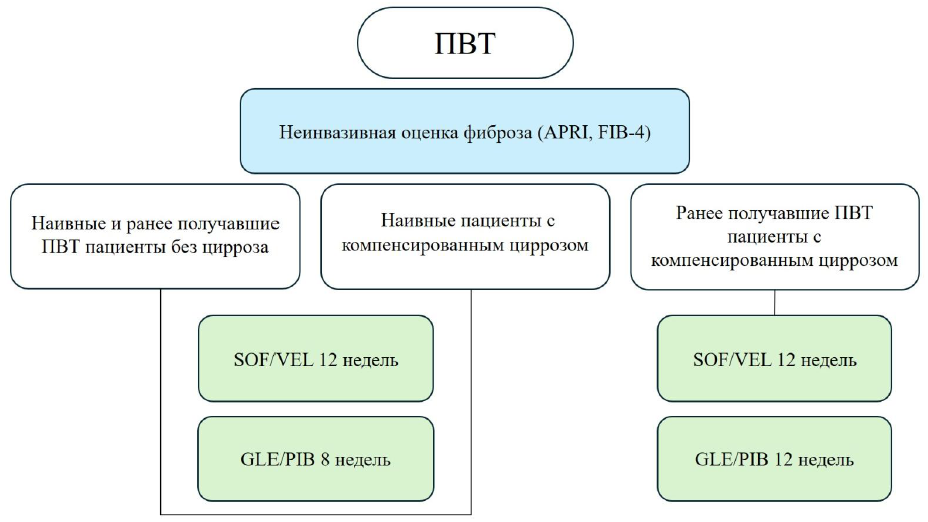
Схема 3. Алгоритм упрощенного лечения ХГС [2, 30, 40, 46]

Таблица 7. Противопоказания к ПВТ [10-11]
|
ПВТ
|
Противопоказания |
| Все режимы |
• Использование некоторых индукторов цитохрома P450/P-gp (карбамазепин, фенитоин и фенобарбитал), если их нельзя заменить другими препаратами, из-за риска значительного снижения концентрации ПППД (УД-А1)
• Беременность (УД-А1)
|
|
GLE/PIB
EBR/GZR*
SOF/VEL/VOX*
|
• Пациенты с декомпенсированным ЦП (классы В и С по CTP) и пациенты с эпизодами декомпенсации ЦП в анамнезе (УД-А1)
|
| RBV |
• Анемия при уровне Hb <85 г/л
• СКФ <50 мл/мин/1,73 м2
• Гемоглобинопатии
|
* После регистрации и разрешения к применению в РК по соответствующим показаниям
Общие рекомендации по проведению ПВТ [1, 6, 8, 41]
• Полная приверженность к ПВТ – важный фактор достижения УВО (УД-А1).
• В случае, если с момента пропуска приема препарата прошло менее 18 часов, то пропущенную дозу можно принять в течение 18 часов после предполагаемого времени приема; в случае, если с момента пропуска приема препарата прошло более 18 часов, то пропущенную дозу не следует принимать; следующая доза должна быть принята в соответствии с обычным графиком, и пациента необходимо проинструктировать о недопустимости приема двойной дозы.
Схема 2. Рекомендованная тактика ведения пациентов при перерывах в терапии ПППД, у ранее не лечившихся пациентов без цирроза или с компенсированным циррозом, получающих глекапревир/пибрентасвир или софосбувир/велпатасвир [46]

* Продлить продолжительность терапии таким образом, чтобы пациент получил полный запланированный курс лечения (то есть общее количество таблеток, предусмотренное схемой). Например, если пациент пропустил 10 дней из запланированного 8-недельного курса терапии, лечение следует продлить до 8 недель + 10 дней [47].
Таблица 9. Режимы противовирусной терапии хронического гепатита С [2, 7-8, 19-20, 40-41]
|
Противовирусные препараты
|
Генотип |
Без ЦП
(F0-F3)
|
Компенсированный ЦП /F4 (Child-Pugh А) |
Декомпенсированный ЦП /F4 (Child-Pugh B, C) или компенсированный ЦП с эпизодами декомпенсации в анамнезе
|
| Софосбувир/ велпатасвир | 1, 2, 4-6 | 12 нед. | 12 нед. |
24 нед. или
+ рибавирин 12 нед.
|
| 3 | 12 нед. |
24 нед.
или
+ рибавирин 12 нед.
|
24 нед. или
+ рибавирин 12 нед.
|
|
| Глекапревир/ пибрентасвир | 1, 2, 4-6 | 8 нед. |
8 нед.
12 нед. – при ПВТ в анамнезе
|
не одобрен |
| 3 |
8 нед.
12 нед. – при ПВТ в анамнезе
|
12 нед.
16 нед. – при ПВТ в анамнезе
|
не одобрен | |
| Элбасвир/ гразопревир* |
1b
|
12 нед. | 12 нед. | не одобрен |
| Софосбувир/ велпатасвир/ воксилапревир* | 3 |
Не одобрен
|
12 нед. | не одобрен |
| Софосбувир/ даклатасвир | 1, 2, 4-6 | 12 нед. | 24 нед. | не одобрен |
| 3 | 12 нед. | 24 нед. |
* После регистрации и разрешения к применению в РК по соответствующим показаниям.
NB! Рибавирин в зависимости от массы тела: у пациентов <75 кг 1000 мг (400 мг утром + 600 мг вечером) или при весе ≥75 кг 1200 мг (600 мг два раза в день); при декомпенсированном циррозе печени можно начинать с 600 мг в сутки с последующей коррекцией дозы в зависимости от переносимости (УД-В).
NB! При ПВТ в анамнезе – это лица, ранее получавшие противовирусную терапию ХГС на основе схем Peg-IFNα + RBV, Peg-IFNα + RBV ± SOF или SOF + RBV. NB! Режим софосбувир/даклатасвир упоминается только как альтернатива при ограниченном доступе к фиксированным пангенотипным схемам терапии.
Таблица 10. Побочные явления ПВТ ХГС
Лечение пациентов с ХГС с неудачей ПВТ, проводившейся с использованием ПППД [41, 49]:
Таблица 11. Повторное лечение пациентов с ХГС с неудачей предшествующей ПВТ на основе ПППД [12]
Таблица 12. Тактика лечения ХГС в особых группах [7, 21-24, 41]
Хирургическое вмешательство на амбулаторном этапе: не проводится.
| Общие сведения |
• ПППД обычно хорошо переносятся
• Наиболее частыми побочными явлениями являются головная боль,
утомляемость, диарея, анемия, бессонница, тошнота
• Пациентам рекомендуется использовать эффективные средства контрацепции на период лечения, а получающим рибавирин – во время лечения и в течение не менее 6 мес. после его завершения (УД-А1)
|
| RBV |
• Может вызвать гемолиз/анемию
• При развитии анемии требуется пошаговое снижение дозы
• У пациентов (в т.ч. с ЦП), не имеющих сердечно-сосудистых заболеваний, с Hb 85 - 100 г/л рекомендуется пошаговое (на 200 мг) снижение дозы до 600 мг/сутки, при уровне Hb <85 г/л – отмена препарата (УД-А1)
• У пациентов со стабильным сердечно-сосудистым заболеванием при снижении Hb на ≥20 г/л в течение любых 4 недель терапии рекомендуется снижение дозы до 600 мг/сутки, при уровне Hb <120 г/л даже через 4 недели терапии в сниженной дозе – отмена препарата
• Другие нежелательные явления (усталость, головная боль, миалгия, тошнота, озноб, лихорадка, бессонница, депрессия, гипербилирубинемия, артралгия, алопеция, раздражительность, костно-мышечная боль, сыпь и др.)
• Обязательна контрацепция на период лечения и в течение не менее 6 мес. после его завершения (УД-А1)
|
Лечение пациентов с ХГС с неудачей ПВТ, проводившейся с использованием ПППД [41, 49]:
• Целесообразно участие междисциплинарной команды, включающей опытного гастроэнтеролога, гепатолога и/ или инфекциониста (УД-В1);
• При планировании повторной ПВТ у пациентов с неудачей предшествующей ПВТ на основе ПППД, при возможности, целесообразно определение резистентных вариантов HCV (УД-В1).
Таблица 11. Повторное лечение пациентов с ХГС с неудачей предшествующей ПВТ на основе ПППД [12]
|
Режим терапии
|
Генотип | Длительность | Уровень доказательности | Особые замечания и ограничения |
| Неудача терапии на основе софосбувира, без цирроза или с компенсированным циррозом | ||||
| Софосбувир / велпатасвир / воксилапревир* |
1–6
|
12 нед. | I, A | При инфицировании генотипом 3 и компенсированном циррозе добавить рибавирин по массе тела при отсутствии противопоказаний. |
| Глекапревир / пибрентасвир |
1, 2, 4, 5, 6
|
16 нед. | I, A | Не рекомендуется пациентам, ранее получавшим комбинацию ингибитора NS5A и ингибитора протеазы NS3/4A (например, элбасвир / гразопревир). |
| Неудача терапии глекапревиром / пибрентасвиром, без цирроза или с компенсированным циррозом | ||||
| Глекапревир / пибрентасвир + софосбувир + рибавирин по массе тела |
1–6
|
16 нед. | IIa, B | |
| Софосбувир / велпатасвир / воксилапревир* |
1–6
|
12 нед. | IIa, B | У пациентов с компенсированным циррозом рекомендуется добавление рибавирина по массе тела. |
| Неудача терапии софосбувиром / велпатасвиром / воксилапревиром или софосбувиром + глекапревир / пибрентасвиром, без цирроза или с компенсированным циррозом | ||||
| Глекапревир / пибрентасвир + софосбувир + рибавирин по массе тела |
1–6
|
16 нед. | IIa, B | Удлинение терапии до 24 недель следует рассмотреть в особо сложных случаях (например, генотип 3 при компенсированном циррозе) или после неудачи схемой ПВТ софосбувир + глекапревир / пибрентасвир. |
| Софосбувир / велпатасвир / воксилапревир + рибавирин по массе тела |
1–6
|
24 нед. | IIa, B | |
| Неудача терапии на основе софосбувира или ингибитора NS5A при декомпенсированном циррозе | ||||
| Софосбувир / велпатасвир + рибавирин по массе тела |
1–6
|
24 нед. | II, C | Рекомендованная начальная доза рибавирина 600 мг при циррозе класса C по шкале CTP; далее увеличение дозы по переносимости. |
* После регистрации и разрешения к применению в РК по соответствующим показаниям
Наблюдение за нелеченными и пациентами при неэффекивности неоднократных курсов ПВТ (инкурабельные пациенты) [20, 41]
• Пациенты должны регулярно наблюдаться (УД-A1).
• Неинвазивная оценка фиброза проводится ежегодно (УД-A1).
• Скрининг ГЦК у пациентов с тяжелым фиброзом (F3) и ЦП (F4) должен проводиться каждые 6 месяцев.
Таблица 12. Тактика лечения ХГС в особых группах [7, 21-24, 41]
|
Категории пациентов
|
Тактика |
| Компенсированный ЦП |
• Режимы ПВТ приведены в таблице 10.
• Мониторинг и менеджмент побочных явлений должен быть особенно тщательным.
|
| Декомпенсированный ЦП (CTP B или C) |
• Пациенты должны проходить противовирусную терапию в экспертных центрах с доступом к ТП (УД-А1).
• Требуется тщательный мониторинг, с возможной остановкой ПВТ, при появлении признаков ухудшения во время лечения (УД-А1).
• Режимы ПВТ приведены в таблице 10; ингибиторы протеаз противопоказаны; в комбинированных режимах RBV можно начинать с дозы 600 мг/сутки c последующей коррекцией, в зависимости от переносимости (УД-А1).
• Пациенты, не находящиеся в листе ожидания ТП и не имеющие угрожающих сопутствующих заболеваний, должны лечиться в срочном порядке (УД-А1).
• Пациентам без ГЦК, ожидающим ТП, с показателями MELD <18–20, проведение ПВТ целесообразно до ТП (УД-А1), с показателями MELD ≥18–20 – после ТП (УД-В1), либо до ТП, если время ожидания превышает 6 месяцев, в индивидуальном порядке (УД-В).
|
| ГЦК без ЦП или с компенсированным ЦП (CTP А) с показаниями к радикальной терапии, включая ТП |
• ПВТ откладывается до завершения лечения ГЦК (УД-А1).
• У пациентов, ожидающих ТП, сроки ПВТ (до или после ТП) определяются индивидуально (УД-В1); при длительном времени ожидания – до ТП (УД-В2).
• Режимы ПВТ соответствуют общим рекомендациям (таблица 10) (УД-А1).
|
| Пролеченная ГЦК без показаний к ТП |
• Режимы ПВТ соответствуют общим рекомендациям (таблица 10) (УД-А1).
• У пациентов, достигших УВО, сохраняется риск рецидива ГЦК, и они нуждаются в постоянном скрининге ГЦК посредством УЗИ каждые 6 месяцев (УД-А1).
• Пациенты, получающие паллиативную терапию по поводу ГЦК, могут получать ПВТ зависимости от общего прогноза и потенциальной пользы (УД-В2).
|
| Рецидивы после ТП |
• Лечение следует начинать в возможно короткие сроки после стабилизации состояния пациента (как правило, через 3 месяца) после ТП (УД-А1).
• Срочными показаниями к ПВТ являются острый холестатический гепатит, умеренный-распространенный фиброз или портальная гипертензия (УД-А1).
• У пациентов без ЦП или с компенсированным ЦП (СТР А) рекомендованы фиксированные комбинации SOF/VEL в течение 12 нед. (при этом коррекции доз иммуносупрессантов не требуется) или GLE/PIB (при этом необходим контроль уровней и коррекция доз иммунодепрессантов) (УД-В1).
• У пациентов с декомпенсированным ЦП (СТР В, С) рекомендована фиксированная комбинация SOF/VEL+RBV (УД-В1) (таблица 10).
• Назначение ПВТ требует учета лекарственных взаимодействий, а уровень иммуносупрессантов в крови подлежит тщательному мониторингу (УД-А1).
|
| HCV-позитивные реципиенты солидных органов (кроме печени) |
• Реципиентам солидных органов, включая почки, сердце, легкие, поджелудочную железу или тонкую кишку, ПВТ рекомендована до или после трансплантации (УД-А1).
• Режимы ПВТ до трансплантации соответствуют общим рекомендациям (таблица 10) (УД-А1).
• После трансплантации при лечении фиксированной комбинацией SOF/VEL коррекции доз иммуносупрессантов не требуется;
• При противовирусной терапии фиксированной комбинации GLE/PIB контроль уровней и коррекция доз иммунодепрессантов (УД-В1).
|
| Острый гепатит С (ОГС) |
• Пациентам с ОГС назначаются комбинации ПППД, соответствующие общим рекомендациям (таблица 10), с продолжительностью ПВТ в течение 8 недель (УД-В1).
• УВО оценивается через 12 и 24 недели после ПВТ ввиду риска поздних рецидивов (УД-В2).
• ПВТ не проводится в целях постконтактной профилактики, при отсутствии документально подтвержденной трансмиссии ВГС (УД-В1).
|
| Беременные |
• Лечение HCV во время беременности не рекомендуется, при отсутствии данных о безопасности и эффективности (УД-C2).
• В случае случайного зачатия на фоне противовирусной терапии лечение может быть продолжено в индивидуальном порядке после обсуждения рисков и пользы с пациенткой и совместного решения акушера и гепатолога (УД-C2).
• Грудное вскармливание не противопоказано при HCV, за исключением случаев кровоточивости или трещин сосков, при которых требуется консультация специалиста (УД-B1).
|
| ЛУИН и лица, получающие ОЗТ |
• ЛУИН должны тестироваться на anti-HCV и HCV РНК; HCV РНК-негативные ЛУИН продолжают тестирование ежегодно, и после каждого употребления наркотиков с высоким риском инфицирования (УД-А1).
• Режимы ПВТ соответствуют общим рекомендациям (таблица 10).
• Лицам, находящимся на ОЗТ, коррекции дозы метадона или бупренорфина во время ПВТ не требуется (УД-А1).
• После успешного лечения ЛУИН следует обучать и информировать о путях предотвращения реинфекции ВГС с учетом рекомендаций программ по снижению вреда окружающим (УД-В1).
• После достижения УВО у ЛУИН должен проводиться скрининг на реинфицирование (наличие HCV РНК) с помощью ПЦР с периодичностью 1 раз в год (УД-А1).
• В случае реинфекции рекомендуется повторное лечение (УД-А1).
|
| Иммуно-опосредованные проявления ХГС |
• Для лечения смешанной криоглобулинемии и заболеваний почек, связанного с ВГС, используются стандартные режимы ПВТ (таблица 10) с тщательным мониторингом побочных явлений (УД-В1).
• Для лечения ВГС-ассоциированной лимфомы рекомендуются стандартные режимы ПВТ в комбинации с химиотерапией с учетом лекарственных взаимодействий; показания к назначению ритуксимаба обсуждаются мультидисциплинарной группой (УД-В1).
• Учитывают противопоказания к назначению RBV (УД-В1).
|
| Ко-инфекция ВИЧ |
• Показания и режимы ПВТ аналогичны таковым для пациентов с моноинфекцией ВГС (таблица 1) (УД-А1).
• При проведении ПВТ необходимо учитывать потенциальные лекарственные взаимодействия с препаратами АРВТ (УД-А1).
|
| Ко-инфекция ВГВ |
• Пациенты с коинфекцией ВГС/ ВГВ должны пройти тестирование на ВИЧ, если их ВИЧ-статус неизвестен (УД-А1).
• Режимы ПВТ ХГС соответствуют моноинфекции (таблица 11) (УД-А1).
• При стандартных показаниях к ПВТ ХГВ показаны аналоги нуклеот(з)идов, согласно соответствующим рекомендациям с учетом потенциальных лекарственных взаимодействий (УД-А1).
• HBsAg-позитивным пациентам показана профилактика аналогами нуклеот(з)идов во время, и спустя не менее 12 недель после окончания ПВТ ХГС с последующим мониторингом в первые месяцы, если лечение ВГВ прекращается (УД-В1).
• У HBsAg-негативных anti-HBc-позитивных пациентов требуется ежемесячный контроль АЛТ; при отсутствии нормализации или повышении АЛТ во время или после ПВТ по поводу ХГС необходимо определение HBsAg и HBV ДНК, и при позитивных результатах – показаны аналоги нуклеот(з)идов (УД-В1).
|
| Почечная недостаточность |
• При почечной недостаточности легкой и средней степени тяжести (СКФ ≥30 мл/мин/1,73 м2) ПВТ ПППД проводится без коррекции доз в соответствии с общими рекомендациями (таблица 10), с тщательным мониторингом побочных явлений (УД-А1).
• Пациенты с тяжелой почечной недостаточностью (СКФ <30 мл/мин/1,73 м2), при терминальной стадии ХБП и на гемодиализе, должны получать лечение в специализированных центрах (УД-В1).
• Пациентам с компенсированным заболеванием печени и тяжелой (СКФ <30 мл/мин/мин/1,73 м2) или терминальной болезнью почек, требующих гемодиализа, с любым генотипом HCV, предпочтительна фиксированная комбинация GLE/PIB, а инфицированным генотипом 1b HCV – также фиксированная комбинации EBR/GZR согласно стандартным режимам (таблицы 33-34); также возможно использование комбинации SOF/VEL (УД-В1).
• Пациентам с декомпенсированным ЦП (классы B или C по CTP) и легкой и средней почечной недостаточностью (СКФ ≥30 мл/мин/1,73м2) рекомендована фиксированная комбинация SOF/VEL совместно с RBV в течение 24 недель с 3 генотипом и 12 недель при остальных генотипах: RBV можно инициировать с дозы 600 мг/сутки, а затем доза корректируется в зависимости от переносимости и уровня Hb; при непереносимости и противопоказаниях к RBV длительность терапии составляет 24 недели (B1).
• При декомпенсированном ЦП (классы В или С CTP) и тяжелой почечной недостаточности (СКФ <30 мл/мин/1,73м2) рекомендована фиксированная комбинация SOF/VEL без RBV в течение 24 недель (УД-В1).
• Использование режимов на основе SOF у пациентов с тяжелой почечной недостаточностью (СКФ <30 мл/мин/1,73 м2) осуществляется согласно инструкциям по применению противовирусных препаратов; лечение проводится под тщательным наблюдением и прерывается при ухудшении функции почек (УД-В2).
• Польза и риски лечения пациентов с конечной стадией заболеваний почек до и после трансплантации почек требует индивидуальной оценки и учета лекарственных взаимодействий (УД-В1).
|
| Гемоглобинопатии и нарушения свертываемости крови |
• Показания и режимы ПВТ соответствуют стандартным (таблица 10, УД-А1).
• Учитывают противопоказания к назначению RBV (УД-В1).
|
Таблица 13. Перечень основных лекарственных средств (имеющих 100% вероятность применения)
|
Лекарственная группа
|
МНН ЛС | Способ применения | Уровень доказательности |
|
Противовирусные препараты прямого действия.
Ингибитор NS5B/Ингибитор NS5A.
|
Софосбувир/ велпатасвир | 400 мг/100 мг однократно внутрь | А |
Таблица 14. Перечень дополнительных лекарственных средств (имеющих менее 100% вероятность применения)
|
Лекарственная группа
|
МНН ЛС | Способ применения | Уровень доказательности |
| Противовирусные препараты прямого действия. Нуклеозиды. | Рибавирин | в зависимости от массы тела: 1000 мг (400 мг утром + 600 мг вечером) или 1200 мг (600 мг два раза в день) у пациентов <75 кг или ≥75 кг соответственно; при декомпенсированном циррозе печени можно начинать с 600 мг в сутки с последующей коррекцией дозы в зависимости от переносимости | А |
|
Противовирусные препараты прямого действия.
Ингибитор протеазы NS3/4A/ Ингибитор NS5A
|
Глекапревир/ пибрентасвир | 300 мг/120 мг однократно внутрь | А |
|
Противовирусные препараты прямого действия.
Ингибитор NS5A / Ингибитор протеазы NS3/4A
|
Элбасвир/ гразопревир*
|
50 мг/100 мг однократно внутрь | А |
| Противовирусные препараты прямого действия. Ингибитор NS5B/Ингибитор NS5A / Ингибитор протеазы NS3/4A |
Софосбувир/ велпатасвир/ воксилапревир*
|
400 мг/100 мг/100 мг однократно внутрь | А |
|
Противовирусные препараты прямого действия.
Нуклеозидный ингибитор полимеразы NS5B
|
Софосбувир | SOF 400 мг + DCV 60 мг, однократно внутрь | А |
|
Противовирусные препараты прямого действия.
Ингибитор NS5A
|
Даклатасвир | А |
* После регистрации и разрешения к применению в РК по соответствующим показаниям
Хирургическое вмешательство на амбулаторном этапе: не проводится.
Лечение (стационар)
Тактика лечения на стационарном уровне
Немедикаментозное лечение: соответствует лечению на амбулаторном уровне.
Медикаментозное лечение, оказываемое на стационарном уровне: соответствует лечению на амбулаторном уровне.
Хирургическое вмешательство:
• трансплантация печени пациентам с ЦП и ГЦК (в соответствии с критериями отбора) [45];
• проведение эндоскопических и иных инвазивных вмешательств.
Профилактические мероприятия: снижения рисков инфицирования, у лиц употребляющих инъекционные наркотики, обеспечение инфекционной безопасности медицинских и немедицинских процедур, универсальный и риск-ориентированный скрининг населения с последующим лечением всех выявленных пациентов, профилактика реинфекции после достижения УВО.
Мониторинг эффективности ПВТ [2, 7, 8, 19, 20, 41].
Дальнейшее ведение:
Профилактические мероприятия: снижения рисков инфицирования, у лиц употребляющих инъекционные наркотики, обеспечение инфекционной безопасности медицинских и немедицинских процедур, универсальный и риск-ориентированный скрининг населения с последующим лечением всех выявленных пациентов, профилактика реинфекции после достижения УВО.
Мониторинг ПВТ включает динамическую оценку ее эффективности, безопасности и оценку лекарственных взаимодействий [1, 2, 5, 6].
Мониторинг эффективности ПВТ [2, 7, 8, 19, 20, 41].
• Конечной точкой терапии является элиминация ВГС, подтверждаемая отрицательным результатом HCV РНК с помощью ПЦР крови с нижним лимитом менее 15 МЕ/мл через 12 недель (УВО12) или 24 недели (УВО24) после окончания ПВТ (УД-А1).
• Для оценки УВО в качестве альтернативны может использоваться определение HCV core Ag (УД-А1).
• При недоступности высокочувствительной ПЦР для оценки УВО в качестве альтернативны может использоваться доступный качественный ПЦР тест (УД-В1).
• У пациентов, получающих ПППД, уровни HCV РНК или HCV core Ag должны определятся исходно, по окончании (опционально), а также спустя 12 или 24 недели после завершения терапии (УД-А1).
• У пациентов с тяжелым фиброзом (METAVIR F3) и ЦП (METAVIR F4) необходимо продолжать скрининг ГЦК, поскольку УВО снижает, но не устраняет ее риск (УД-А1).
Схема 4. Упрощённый алгоритм ведения HCV-инфекции у ранее не леченных взрослых пациентов без цирроза печени [47]
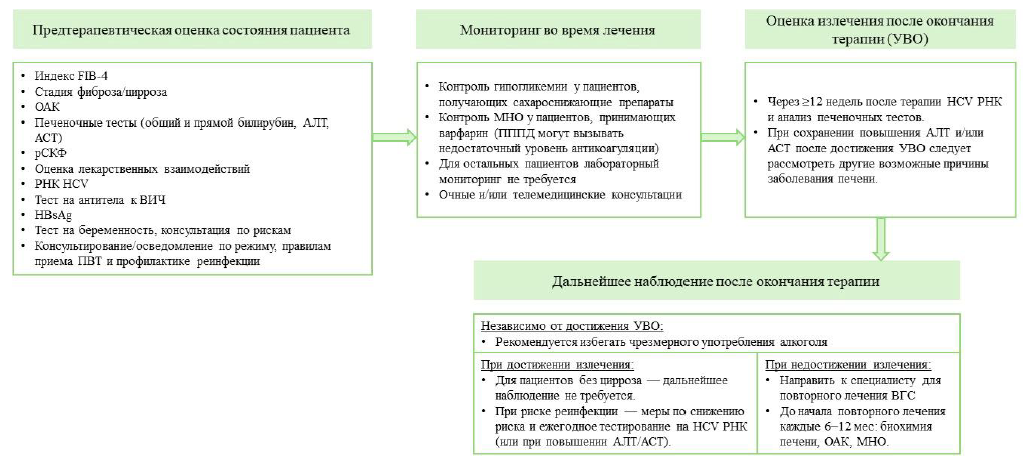
Схема 5. Упрощённый алгоритм лечения HCV у взрослых пациентов, ранее не получавших терапию, с компенсированным циррозом [47].
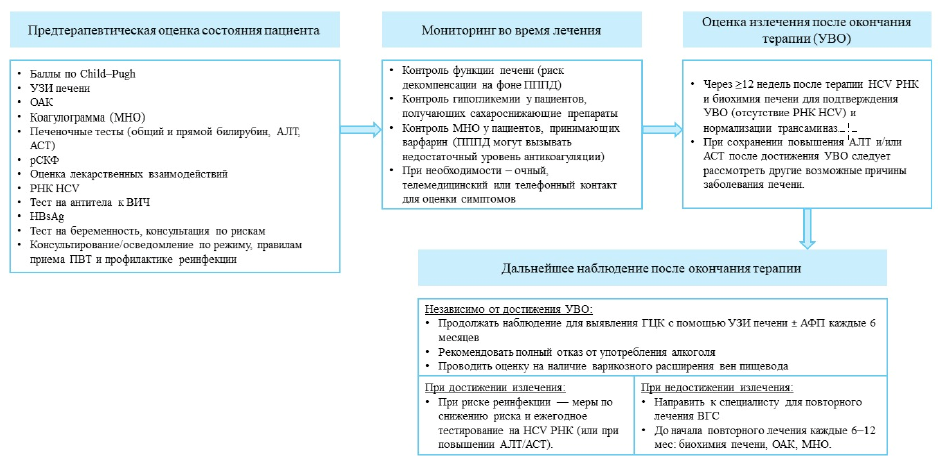
Схема 4. Упрощённый алгоритм ведения HCV-инфекции у ранее не леченных взрослых пациентов без цирроза печени [47]

Схема 5. Упрощённый алгоритм лечения HCV у взрослых пациентов, ранее не получавших терапию, с компенсированным циррозом [47].

Мониторинг безопасности ПВТ [2,7,8,41,47]:
• Рекомендуется мониторинг на наличие побочных явлений ПВТ во время каждого визита (УД-А1).
• Контроль за соблюдением эффективной контрацепции женщинами репродуктивного возраста и/или их партнерами-мужчинами, получающими ПВТ, а, в случае использования RBV – еще не менее 6 месяцев после окончания лечения (УД-А1).
• У пациентов, получающих комбинацию элбасвир/гразопревир, следует проводить исследование функциональных проб печени на 8-й неделе терапии и повторно — на 12-й неделе при длительности лечения 16 недель (УД-B1).
• Повышение уровня АЛТ ≥ в 10 раз и более от исходного на любом этапе лечения или увеличение уровня прямого билирубина, щелочной фосфатазы, МНО требует прекращения терапии ПППД (УД-B1).
• Повышение АЛТ < в 10 раз от исходного, сопровождающееся слабостью, тошнотой, рвотой, желтухой либо значительным повышением билирубина, ЩФ или МНО, также требует прекращения терапии (УД-B1).
• Бессимптомное повышение АЛТ < в 10 раз от исходного уровня требует повторного контроля через 2 недели; при сохранении повышенных значений следует рассмотреть вопрос о прекращении терапии (УД-B1).
Дальнейший мониторинг после УВО [2,7, 8,19-20,41]:
• Информирование о риске повторного инфицирования (УД-В1).
• Пациентам из групп риска повторного инфицирования, достигших УВО, рекомендуется скрининг на наличие РНК HCV методом ПЦР один раз в год (УД-В2).
• Пациентам c отсутствием фиброза исходно – умеренным фиброзом (METAVIR F0-F2), не относящимся к группам риска повторного инфицирования, последующее наблюдение не требуется (УД-А1).
• Пациенты с исходным тяжелым фиброзом (F3) и ЦП (F4), достигшие УВО, должны проходить скрининг на ГЦК (УЗИ ± АФП) каждые 6 месяцев (УД-А1).
• У пациентов с ЦП при наличии ВРВП/ВРВЖ до ПВТ, или с показателями VCTE >20 кПа и количеством тромбоцитов <150 000/мм3, особенно с показателями VCTE селезенки ≥40 кПа (УД-А1), обязателен контроль за варикозно расширенными венами пищевода и желудка (ВГДС).
Индикаторы эффективности лечения:
• УВО – отрицательный результат HCV РНК в сыворотке или плазме с помощью ПЦР с нижним лимитом менее 15 МЕ/мл через 12 недель (УВО12) или 24 недели (УВО24) после завершения ПВТ (УД-А1). При недоступности высокочувствительной ПЦР для оценки УВО, в качестве альтернативы, может использоваться доступный качественный ПЦР тест РНК HCV (УД-В1), или определение HCV core Ag (УД-А1);
• Биохимический ответ – нормализации АЛТ и АСТ;
• Морфологический ответ – улучшение гистологической картины, регрессия фиброза.
Госпитализация
Показания для госпитализации с указанием типа госпитализации
Показания для плановой госпитализации:
• проведение биопсии;
• осложненные формы прогрессирующего заболевания печени.
Показания для экстренной госпитализации:
• прогрессирующее заболевание печени с осложнением
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2025
- 1) Roudot-Thoraval, F. (2021). Epidemiology of hepatitis C virus infection. In Clinics and Research in Hepatology and Gastroenterology (Vol. 45, Issue 3). Elsevier Masson s.r.l. https://doi.org/10.1016/j.clinre.2020.101596. 2) World Health Organization. Updated recommendations on treatment of adolescents and children with chronic HCV infection, and HCV simplified service delivery and diagnostics. Geneva: WHO; 2022 Oct 17. https://www.who.int/publications/i/item/9789240069428. 3) Hepatology: A clinical textbook. The Editors Stefan Mauss, Thomas Berg, Jürgen Rockstroh, Christoph Sarrazin, Heiner Wedemeyer, 2020 – 728 p. https://www.hepatologytextbook.com/download/hepatology2020.pdf. 4) Vinod K Dhawan. Hepatitis C. Medscape (Updated: Oct 07, 2019). https://emedicine.medscape.com/article/177792-overview. 5) Mazzaro, C., Quartuccio, L., Adinolfi, L. E., Roccatello, D., Pozzato, G., Nevola, R., Tonizzo, M., Gitto, S., Andreone, P., & Gattei, V. (2021). A review on extrahepatic manifestations of chronic hepatitis c virus infection and the impact of direct-acting antiviral therapy. In Viruses (Vol. 13, Issue 11). MDPI. https://doi.org/10.3390/v13112249. 6) Cacoub P, Saadoun D. Extrahepatic Manifestations of Chronic HCV Infection. N Engl J Med. 2021 Mar 18;384(11):1038-1052. doi: 10.1056/NEJMra2033539. PMID: 33730456. 7) Ghany, M. G., & Morgan, T. R. (2020). Hepatitis C Guidance 2019 Update: American Association for the Study of Liver Diseases–Infectious Diseases Society of America Recommendations for Testing, Managing, and Treating Hepatitis C Virus Infection. Hepatology, 71(2), 686–721. https://doi.org/10.1002/hep.31060. 8) Warkad, S. D., Nimse, S. B., Song, K. S., & Kim, T. (2018). HCV detection, discrimination, and genotyping technologies. In Sensors (Switzerland) (Vol. 18, Issue 10). MDPI AG. https://doi.org/10.3390/s18103423. 9) Havens, P. L., & Anderson, J. R. (2020). Updated CDC Recommendations for Universal Hepatitis C Virus Screening among Adults and Pregnant Women: Implications for Clinical Practice. In JAMA - Journal of the American Medical Association (Vol. 323, Issue 22, pp. 2258–2259). American Medical Association. https://doi.org/10.1001/jama.2020.3693. 10) Lazarus J.V., Picchio C.A., Guy D., Aleman S., James C., Nava F.A., Øvrehus A., Turnes J., Ward J.W., Ustianowski A. Hepatitis C standards of care: A review of good practices since the advent of direct-acting antiviral therapy // Clinical Research in Hepatology and Gastroenterology. – 2021. – Vol. 45, № 2. – P. 101564. – DOI: 10.1016/j.clinre.2020.11.001. – PMID: 33740477. 11) Kwo, Paul Y MD, FACG, FAASLD1; Cohen, Stanley M MD, FACG, FAASLD2; Lim, Joseph K MD, FACG, FAASLD3. ACG Clinical Guideline: Evaluation of Abnormal Liver Chemistries. American Journal of Gastroenterology 112(1):p 18-35, January 2017. | DOI: 10.1038/ajg.2016.517. 12) American Association for the Study of Liver Diseases & Infectious Diseases Society of America. Clinical Practice Guidance for Testing, Managing, and Treating Hepatitis C Virus Infection: 2023 Update. Published 25 May 2023. DOI: 10.1093/cid/ciad319. 13) European Association for the Study of the Liver (EASL). Clinical Practice Guidelines on Autoimmune Hepatitis. May 2025. DOI: 10.1016/j.jhep.2025.03.017. 14) Dore GJ, Feld JJ, Thompson AJ, et al. HCC incidence after hepatitis C cure among patients with advanced fibrosis or cirrhosis: a meta-analysis. Hepatology. 2022;76(1):139–154. DOI: 10.1002/hep.32341. 15) Drug Safety. “Consensus Guidelines: Best Practices for the Prevention, Detection and Management of Hepatitis B Virus Reactivation in Clinical Trials with Immunosuppressive/Immunomodulatory Therapy”. Drug Saf. 2024;47:321-332. 16) Alghamdi A, Alghamdi H, Alserehi HA, Babatin MA, Alswat KA, Alghamdi M, et al. SASLT guidelines: Update in treatment of hepatitis C virus infection, 2024. Saudi J Gastroenterol. 2024;30(Suppl 1):S1–S42. DOI:10.4103/sjg.sjg_333_23. 17) World Gastroenterology Organisation. Hepatitis C: WGO Practice Guideline. 2023/24. Available from: https://www.worldgastroenterology.org/guidelines/hepatitis-c 18) Doğrugörün A, Doyuk Kartal E, Nayman Alpat S, et al. Clinical Efficacy and Safety of Direct-Acting Antivirals in Chronic Hepatitis C Treatment: Real-World Data. Viral Hepat J. 2023;29(3):95–100. doi:10.4274/vhd.galenos.2023.2023-6-1. 19) Alshuwaykh, O., & Kwo, P. Y. (2021). Current and future strategies for the treatment of chronic hepatitis c. In Clinical and Molecular Hepatology (Vol. 27, Issue 2, pp. 246–256). Korean Association for the Study of the Liver. https://doi.org/10.3350/cmh.2020.0230. 20) Ioannou, G. N. (2021). HCC surveillance after SVR in patients with F3/F4 fibrosis. In Journal of Hepatology (Vol. 74, Issue 2, pp. 458–465). Elsevier B.V. https://doi.org/10.1016/j.jhep.2020.10.016. 21) Alqahtani, S. A., & Colombo, M. G. (2021). Treating paediatric hepatitis C in the era of direct-acting antiviral agents. In Liver International (Vol. 41, Issue 6, pp. 1189–1200). John Wiley and Sons Inc. https://doi.org/10.1111/liv.14810. 22) European Association for the Study of the Liver (EASL). (2025). EASL Clinical Practice Guidelines on the management of hepatitis B virus infection. Journal of Hepatology. https://doi.org/10.1016/j.jhep.2025.03.018. 23) Kulkarni, A. v., & Duvvuru, N. R. (2021). Management of hepatitis B and C in special population. In World Journal of Gastroenterology (Vol. 27, Issue 40, pp. 6861–6873). Baishideng Publishing Group Co. https://doi.org/10.3748/wjg.v27.i40.6861. 24) Kidney Disease: Improving Global Outcomes (KDIGO) Hepatitis C Work Group. KDIGO 2022 Clinical Practice Guideline FOR the Prevention, Diagnosis, Evaluation, and Treatment of Hepatitis C in Chronic Kidney Disease. Kidney Int. 2022 Dec;102(6S):S129-S205. doi: 10.1016/j.kint.2022.07.013. PMID: 36410841. 25) Hsu YC, Huang DQ, Nguyen MH. Global burden of hepatitis B virus: current status, missed opportunities and a call for action. Nat Rev Gastroenterol Hepatol. 2023 Aug;20(8):524-537. doi: 10.1038/s41575-023-00760-9. 26) WHO Guidelines for the prevention, diagnosis, care and treatment for people with chronic hepatitis B infection. March 2024: https://www.who.int/publications/i/item/9789240090903. 27) Terrault, N. A., Lok, A. S. F., McMahon, B. J., Chang, K. M., Hwang, J. P., Jonas, M. M., Brown, R. S., Bzowej, N. H., & Wong, J. B. (2018). Update on prevention, diagnosis, and treatment of chronic hepatitis B: AASLD 2018 hepatitis B guidance. Hepatology, 67(4), 1560–1599. https://doi.org/10.1002/hep.29800. 28) Sarin, S. K., Kumar, M., Lau, G. K., Abbas, Z., Chan, H. L. Y., Chen, C. J., Chen, D. S., Chen, H. L., Chen, P. J., Chien, R. N., Dokmeci, A. K., Gane, E., Hou, J. L., Jafri, W., Jia, J., Kim, J. H., Lai, C. L., Lee, H. C., Lim, S. G., … Kao, J. H. (2016). Asian-Pacific clinical practice guidelines on the management of hepatitis B: a 2015 update. In Hepatology International (Vol. 10, Issue 1, pp. 1–98). Springer. https://doi.org/10.1007/s12072-015-9675-4. 29) You, H., Wang, F., Li, T., Xu, X., Sun, Y., Nan, Y., Wang, G., Hou, J., Duan, Z., Wei, L., Jia, J., & Zhuang, H. (2023). Guidelines for the Prevention and Treatment of Chronic Hepatitis B (version 2022). Journal of Clinical and Translational Hepatology, 11(6), 1425–1442. https://doi.org/10.14218/JCTH.2023.00320. 30) World Health Organization. Priorities in planning person‑centred hepatitis B and C testing services: operational guide. Geneva: WHO; 2024 Dec 4. ISBN: 978‑92‑4‑010408‑2. Available from: https://www.who.int/publications/i/item/9789240104082 . 31) Berzigotti, A., Tsochatzis, E., Boursier, J., Castera, L., Cazzagon, N., Friedrich-Rust, M., Petta, S., & Thiele, M. (2021a). EASL Clinical Practice Guidelines on non-invasive tests for evaluation of liver disease severity and prognosis – 2021 update. Journal of Hepatology, 75(3), 659–689. https://doi.org/10.1016/j.jhep.2021.05.025. 32) Hamran S, Al-Rajhi AA, Jasim K, Al-Theyab MA, Elahtam M, Al-Hail M K, et al. Efficacy and Safety of Adding Ribavirin to Sofosbuvir-Based Direct-Acting Antivirals (DAAs) in Re-Treating Non-Genotype 1 Hepatitis C—A Systematic Review and Meta-Analysis. Diseases. 2025;13(5):138. doi:10.3390/diseases13050138. 33) Lim, J. K., Flamm, S. L., Singh, S., Falck-Ytter, Y. T., Gerson, L., Hirano, I., Nguyen, G. C., Rubenstein, J. H., Smalley, W. E., Stollman, N., Sultan, S., Vege, S. S., Wani, S. B., Weinberg, D., & Yang, Y. X. (2017b). American Gastroenterological Association Institute Guideline on the Role of Elastography in the Evaluation of Liver Fibrosis. Gastroenterology, 152(6), 1536–1543. https://doi.org/10.1053/j.gastro.2017.03.017. 34) Jeong D, Wong S, Karim ME, Manges AR, Makuza JD, Velásquez García HA, et al. Direct-Acting Antivirals and Risk of Hepatitis C Extrahepatic Manifestations. JAMA Netw Open. 2025;8(6):e2514631. doi:10.1001/jamanetworkopen.2025.14631. 35) Neuberger, J., Patel, J., Caldwell, H., Davies, S., Hebditch, V., Hollywood, C., Hubscher, S., Karkhanis, S., Lester, W., Roslund, N., West, R., Wyatt, J. I., & Heydtmann, M. (2020a). Guidelines on the use of liver biopsy in clinical practice from the British Society of Gastroenterology, the Royal College of Radiologists and the Royal College of Pathology. Gut, 69(8), 1382–1403. https://doi.org/10.1136/gutjnl-2020-321299. 36) Horowitz, J. M., Venkatesh, S. K., Ehman, R. L., Jhaveri, K., Kamath, P., Ohliger, M. A., Samir, A. E., Silva, A. C., Taouli, B., Torbenson, M. S., Wells, M. L., Yeh, B., & Miller, F. H. (2017a). Evaluation of hepatic fibrosis: a review from the society of abdominal radiology disease focus panel. In Abdominal Radiology (Vol. 42, Issue 8, pp. 2037–2053). Springer New York LLC. https://doi.org/10.1007/s00261-017-1211-7. 37) Kennedy, O. J., Roderick, P., Buchanan, R., Fallowfield, J. A., Hayes, P. C., & Parkes, J. (2017b). Coffee, including caffeinated and decaffeinated coffee, and the risk of hepatocellular carcinoma: A systematic review and dose-response meta-Analysis. In BMJ Open (Vol. 7, Issue 5). BMJ Publishing Group. https://doi.org/10.1136/bmjopen-2016-013739. 38) Yu, C., Cao, Q., Chen, P., Yang, S., Deng, M., Wang, Y., & Li, L. (2016b). An updated dose-response meta-analysis of coffee consumption and liver cancer risk. Scientific Reports, 6. https://doi.org/10.1038/srep37488. 39) Sallam M, Khalil R. Contemporary Insights into Hepatitis C Virus: A Comprehensive Review. Microorganisms. 2024;12(6):1035. doi:10.3390/microorganisms12061035. 40) Pawlotsky, J. M., Negro, F., Aghemo, A., Berenguer, M., Dalgard, O., Dusheiko, G., Marra, F., Puoti, M., & Wedemeyer, H. (2020b). EASL recommendations on treatment of hepatitis C: Final update of the series. Journal of Hepatology, 73(5), 1170–1218. https://doi.org/10.1016/j.jhep.2020.08.018. 41) Jiang, X. W., Ye, J. Z., Li, Y. T., & Li, L. J. (2018). Hepatitis B reactivation in patients receiving direct-acting antiviral therapy or interferon-based therapy for hepatitis C: A systematic review and meta-analysis. World Journal of Gastroenterology, 24(28), 3181–3191. https://doi.org/10.3748/wjg.v24.i28.3181. 42) European Centre for Disease Prevention and Control (ECDC). Hepatitis C – Annual epidemiological report for 2023. Stockholm: ECDC; 2024. Available from: https://www.ecdc.europa.eu/en/publications-data/hepatitis-c-annual-epidemiological-report-2023. 43) European Association for the Study of the Liver. EASL Clinical Practice Guidelines on nutrition in chronic liver disease. J Hepatol. 2019 Jan;70(1):172-193. doi: 10.1016/j.jhep.2018.06.024. Epub 2018 Aug 23. PMID: 30144956; PMCID: PMC6657019. 44) de Franchis R., Bosch J., Garcia-Tsao G., Reiberger T., Ripoll C.; Baveno VII Faculty. Baveno VII – Renewing consensus in portal hypertension // Journal of Hepatology. – 2022. – Vol. 76, № 4. – P. 959–974. – DOI: 10.1016/j.jhep.2021.12.022. – PMID: 35120736. 45) Клинический протокол МЗ РК медицинского вмешательства «Трансплантация печени», 2021 г. 46) Centers for Disease Control and Prevention (CDC). Testing for HCV infection: an update of guidance for clinicians and laboratorians // MMWR. Morbidity and Mortality Weekly Report. – 2013. – Vol. 62, No. 18. – P. 362–365. – PMID: 23657112. 47) American Association for the Study of Liver Diseases (AASLD); Infectious Diseases Society of America (IDSA). In: HCV Guidance: Recommendations for Testing, Managing, and Treating Hepatitis C. Updated March 2025. Available at: https://www.hcvguidelines.org/. 48) Sterling R.K., Duarte-Rojo A., et al. AASLD Practice Guideline on Imaging-Based Noninvasive Liver Disease Assessment of Hepatic Fibrosis and Steatosis. Hepatology. 2025;81(2):672–724. 49) Maikenova A, Nersesov A, Kuantay E, Kulimbet M, Colombo M, Pavlov C, Yerlanova Y. Evaluation of predictors of ineffectiveness of antiviral therapy for chronic hepatitis C in the Republic of Kazakhstan: a matched case-control study. Georg Med News. 2024 Jul–Aug;(352–353):147–154. PMID: 39441286.
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1) Нерсесов Александр Витальевич – доктор медицинских наук, профессор, заведующий кафедрой гастроэнтерологии НАО «Казахский национальный медицинский университет имени С. Д. Асфендиярова», консультант Медицинского центра управления делами Президента РК, приглашенный профессор Северо-Западного государственного медицинского университета имени И.И. Мечникова (Санкт-Петербург), эксперт Европейского регионального бюро ВОЗ, Председатель ОО «Казахская ассоциация по изучению печени».
2) Калиаскарова Кульпаш Сагындыковна – доктор медицинских наук, профессор Национального научного онкологического центра, Президент Ассоциации гепатологов/гастроэнтерологов «Gastro Hepato Transplant Group.Kz», главный внештатный гастроэнтеролог/гепатолог Министерства здравоохранения Республики Казахстан.
3) Есмембетов Кахарман Избасарович – кандидат медицинских наук, вице-президент ассоциации гепатологов Казахстана «Gastro Hepato Transplant Group.Kz», профессор Национального научного онкологического центра, заведующий отделения гастроэнтерологии клиники внутренних болезней, гастроэнтерологии и интервенционной эндоскопии, Marienhospital Aachen, Аахен, Германия.
4) Жанасбаева Маржан Сиязбековна – руководитель отделения онкогепатологии, гастроэнтерологии и трансплантации печени Национального научного онкологического центра.
5) Дуйсенова Амангуль Куандыковна – доктор медицинских наук, профессор, заведующая кафедрой инфекционных и тропических болезней НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова», заместитель председателя ОО «Казахская ассоциация по изучению печени».
6) Раисова Айгуль Муратовна – кандидат медицинских наук, доцент кафедры гастроэнтерологии НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова».
7) Рсалиева Жанар Махсутовна – кандидат медицинских наук, заведующая отделением гастроэнтерологии, нефрологии и гематологии, руководитель городского гепатологического центра города Шымкент, главный внештатный гепатолог Управления здравоохранения города Шымкент.
8) Кыздарбеков Аскар Мырзахметович – руководитель гепатологического центра Управления здравоохранения Жамбылской области, Жамбылская областная инфекционная больница.
9) Лозинская Ирина Анатольевна – руководитель гепатологического центра Управления здравоохранения Карагандинской области.
10) Майкенова Арайлым Мураткызы – ассистент кафедры гастроэнтерологии НАО «Казахский национальный медицинский университет имени С. Д. Асфендиярова».
11) Қуантай Эльмира Қырғызбайқызы – ассистент кафедры гастроэнтерологии НАО «Казахский национальный медицинский университет имени С. Д. Асфендиярова».
12) Биджиев Алан Салихович – гастроэнтеролог/гепатолог отделения онкогепатологии, гастроэнтерологии и трансплантации печени Национального научного онкологического центра.
13) Баромыко Наталья Александровна – гастроэнтеролог/гепатолог отделения онкогепатологии и гастроэнтерологии Национального научного онкологического центра.
14) Аубакирова Алма Серкпаевна – магистр медицины, главный специалист отдела мониторинга, оценки и координации онкологической и онкогепатологической помощи в регионах и эпидемиологических исследований в области онкологии Центра по координации и стратегическому развитию онкологической службы ТОО «Национальный научный онкологический центр».
15) Ахмадьяр Нуржамал Садыровна – доктор медицинских наук, профессор, заведующая кафедрой клинической фармакологии НАО «Медицинский университет Астана», врач-клинический фармаколог высшей категории, независимый эксперт Министерства здравоохранения Республики Казахстан.
Конфликт интересов: нет.
Рецензенты:
1) Чуланов Владимир Петрович – доктор медицинских наук, профессор кафедры инфекционных болезней Сеченовского университета, заместитель директора по научной работе и инновационному развитию НМИЦ фтизиопульмонологии и инфекционных заболеваний МЗ РФ, главный внештатный специалист по инфекционным болезням МЗ РФ, г. Москва, Россия.
2) Кошерова Бахыт Нургалиевна – доктор медицинских наук, профессор, Председатель Правления – Ректор НАО «Карагандинский медицинский университет», главный внештатный взрослый инфекционист Министерства здравоохранения Республики Казахстан.
Указание условий пересмотра протокола: пересмотр не реже 1 раза в 5 лет и не чаще 1 раза в 3 года при наличии новых методов диагностики и лечения с уровнем доказательности.
Сокращения, используемые в протоколе:
Сокращения, используемые в протоколе:
|
ANA
|
антинуклеарные антитела |
|
AMA
|
антимитохондриальные антитела |
|
anti-HAV IgM
|
антитела класса IgM к вирусу гепатита А |
|
anti-HBc
|
антитела к HBcAg |
|
anti-HBe
|
антитела к HBeAg |
|
anti-HBs
|
антитела к HBsAg |
|
anti-HCV
|
антитела к вирусу гепатита C |
|
anti-HDV
|
антитела к вирусу гепатита D |
|
anti-HEV IgM
|
антитела класса IgM к вирусу гепатита Е |
|
anti-HIV
|
антитела к ВИЧ |
|
CAP
|
контролируемый параметр ослабления сигнала |
|
CDC
|
Centers for Disease Control and Prevention |
|
CTP
|
класс тяжести цирроза печени по Child-Turcotte-Pugh |
|
DCV
|
даклатасвир |
|
EBR/GZR
|
фиксированная комбинация элбасвира и гразопревира |
|
EASL
|
Европейская ассоциация по изучению печени |
|
GLE/PIB
|
фиксированная комбинация глекапревира и пибрентасвира |
|
HBeAg
|
внутренний антиген вируса гепатита В |
|
HBsAg
|
поверхностный антиген вируса гепатита В |
|
HCV РНК
|
РНК ВГС |
|
HCV
|
вирус гепатита С |
|
HCV Ag
|
ядерный антиген вируса гепатита С |
|
IgG
|
иммуноглобулины класса G |
|
LBx
|
биопсия печени |
|
METAVIR
|
морфологическая система оценки заболевания печени |
|
NS5A
|
ингибитор(ы) NS5A комплекса вируса гепатита С |
|
Peg-IFNα
|
пегилированный интерферон альфа |
|
RBV
|
рибавирин |
|
SOF
|
софосбувир |
|
SOF/VEL
|
софосбувир/велпатасвир |
|
SOF/VEL/VOX
|
софосбувир/велпатасвир/воксилопревир |
|
VCTE
|
вибрационно-контролируемая транзиентная эластография |
|
АИГ
|
аутоиммунный гепатит |
|
АНФ
|
антинуклеарный фактор |
|
АРВТ
|
антиретровирусная терапия |
|
АФП
|
альфа-фетопротеин |
|
ВГА
|
вирусный гепатит А |
|
ВГВ
|
вирусный гепатит B |
|
ВГЕ
|
вирусный гепатит Е |
|
ВГН
|
верхняя граница нормы |
|
ВГС
|
вирусный гепатит С |
|
ВИЧ
|
вирус иммунодефицита человека |
|
ВРВ
|
варикозно расширенные вены |
|
ГЦК
|
гепатоцеллюлярная карцинома |
|
ИМТ
|
индекс массы тела |
|
ИП
|
ингибитор(ы) протеаз NS3/4A вируса гепатита С |
|
ИФА
|
иммуноферментный анализ |
|
ИХА
|
иммунохимический анализ |
|
ЛУИН
|
лица, употребляющие инъекционные наркотики |
|
МАСГ
|
метаболически-ассоциированный стеатогепатит |
|
МНН
|
международное непатентованное название |
|
МНО
|
международное нормализованное отношение |
|
ОВГ
|
острый вирусный гепатит |
|
ОГС
|
острый гепатит С |
|
ОЗТ
|
опиоидная заместительная терапия |
|
ПВТ
|
противовирусная терапия |
|
ППН
|
показатели повреждения нейтрофилов |
|
ПППД
|
противовирусные препараты прямого действия |
|
ПСХ
|
первичный склерозирующий холангит |
|
ПЦР
|
полимеразная цепная реакция |
|
ТП
|
трансплантация печени |
|
УВО
|
устойчивый вирусологический ответ |
|
УЗИ
|
ультразвуковое исследование |
|
ФПП
|
функциональные печеночные пробы |
| ХБП | хроническая болезнь почек |
|
ЦП
|
цирроз печени |
|
ВГДС
|
видеогастродуоденоскопия |
| ЭРХПГ | эндоскопическая ретроградная холангиопанкреатография |
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.