Тромбоэмболия легочной артерии
 Версия: Клинические протоколы КР 2024 (Кыргызстан)
Версия: Клинические протоколы КР 2024 (Кыргызстан)
Общая информация
Краткое описание
Министерство здравоохранения Кыргызской Республики
Национальный центр кардиологии и терапии имени академика М.М. Миррахимова
КЛИНИЧЕСКОЕ РУКОВОДСТВО ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ
ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ
Клиническая проблема
Тромбоэмболия легочной артерии
Клиническое руководство применимо к пациентам с тромбоэмболией легочной артерии
Дата создания: Создано в 2024 г.
Дата утверждения:
Утверждено
приказом
Министерством здравоохранения КР
№785 от 18.07.2024 год.
Обоснование приоритетности проблемы
В структуре причин внезапной смерти ТЭЛА занимает третье место после инфаркта миокарда и инсультов, а среди пациентов с сердечно-сосудистыми заболеваниями оно оказывает второе по значимости воздействие, достигая до 50%. Годовая смертность от ТЭЛА составляет 0,1% населения Земли, причём у пациентов, не получавших антитромботическую терапию, летальность может достигать 30%. ТЭЛА становится причиной смерти у 60% больных с патологией сердечно-сосудистой системы.
Тромбоэмболия лёгочной артерии также часто вызывает острое лёгочное сердце. В США каждый год госпитализируют около 600 000 пациентов с ТЭЛА, и треть из них умирают от массивной формы этого осложнения, причём около 60 000 человек умирают в первые часы после его возникновения.
Проблема ТЭЛА также актуальна во Франции, Англии, Уэльсе, Италии и других странах, где ежегодно регистрируется значительное количество новых случаев. Летальность среди нелеченных пациентов может достигать 40%, но при своевременном лечении она не превышает 10%.
Важно отметить, что диагностика и лечение ТЭЛА остаются сложными задачами, и их эффективность зависит от использования современных методов диагностики, таких как компьютерная томография и магнитно-резонансная томография. Кроме того, эндоваскулярные технологии играют существенную роль в профилактике и лечении ТЭЛА.
Кодирование по МКБ 10
I 74.8 Эмболия и тромбоз других артерий
I 26.0 Легочная эмболия с упоминанием об остром легочном сердце
I 26.9 Легочная эмболия без упоминания об остром легочном сердце
Классификация
Клиническая классификация ТЭЛА
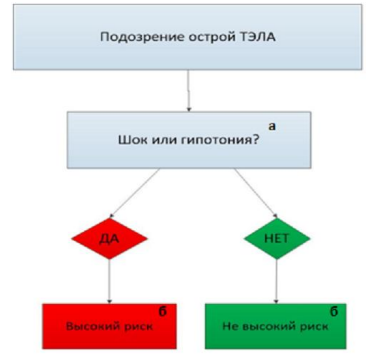 Рис. 2. Клиническая классификация тяжести ТЭЛА (начальная стратификация риска)
Рис. 2. Клиническая классификация тяжести ТЭЛА (начальная стратификация риска)а- шок определяется при систолическом давлении <90 мм. рт. ст., или падение систолического давления ≥ 40 мм рт.ст. в течение >15 мин. не вызванных началом новых экстрасистол, гиповолемией или сепсисом.
б- оценка ТЭЛА основывается на оценке риска ранней смертности от ТЭЛА (определяемой в стационаре) или по шкале 30-дневной смертности (Таблица 10).
Эпидемиология
Эпидемиология
Изучение временных рядов в популяциях Европы, Азии и Северной Америки показывает, что существует потенциал для снижения смертности от острой тромбоэмболии легочной артерии (ТЭЛА) [3-6, 9, 10]. Внедрение и широкое использование более эффективных методов лечения, а также инвазивных вмешательств, возможно, с более тщательным соблюдением рекомендаций, вероятнее всего, оказали значительное положительное влияние на прогноз ТЭЛА в последние годы [11, 12]. На данный момент наблюдается тенденция к гипердиагностике ТЭЛА, включая субсегментарную или даже несуществующую форму [13]. Это может привести к ложному снижению показателей летальности за счет увеличения числа случаев ТЭЛА, что является знаменателем в данной статистике.
Исследования показали, что у детей ежегодная частота ВТЭ варьирует от 53 до 57 случаев на 100 тысяч среди госпитализированных пациентов [14, 15] и от 1,4 до 4,9 случаев на 100 тысяч в общей популяции [16, 17].
Патофизиология
Внезапное увеличение ЛСС ведёт к дилатации ПЖ, что влияет на сократимость его миокарда по механизму Франка-Старлинга. Перегрузка давлением и объёмом ПЖ приводят к усилению напряжения его стенки и растяжению миоцитов. Время сокращения ПЖ увеличивается, тогда как нейрогуморальная активация ведёт к инотропной и хронотропной стимуляции. В сочетании с системной вазоконстрикцией эти компенсаторные механизмы повышают ДЛА, улучшая кровоток сквозь частично перекрытый лёгочный бассейн, и таким образом временно стабилизируют системное артериальное давление (АД). Однако способность ПЖ к такой быстрой адаптации ограничена: неадаптированный к нагрузке и имеющий тонкую стенку ПЖ не может создавать среднее ДЛА >40 мм рт.ст.
Удлинение времени сокращения ПЖ до периода ранней диастолы левого желудочка (ЛЖ) ведёт к выбуханию межжелудочковой перегородки в полость ЛЖ [21]. Асинхронная работа желудочков может усиливаться развитием блокады правой ножки пучка Гиса. В результате наполнение ЛЖ в раннюю диастолу нарушается, что приводит к снижению сердечного выброса, приводя к системной гипотензии и гемодинамической нестабильности [22].
Как было описано выше, чрезмерная нейрогуморальная активация при ТЭЛА может быть результатом как аномального напряжения стенки ПЖ, так и циркуляторного шока. Обнаружение массивных инфильтратов воспалительных клеток в миокарде ПЖ у пациентов умерших в течение 48 ч после острой ТЭЛА может быть объяснено высоким уровнем эпинефрина, высвобождаемого в результате ТЭЛА-индуцированного “миокардита” [23]. Эта воспалительная реакция могла бы объяснить вторичную гемодинамическую дестабилизацию, которая иногда наступает через 24- 48 ч после острой ТЭЛА, хотя ранний рецидив ТЭЛА может быть альтернативным объяснением в некоторых из этих случаев.
Наконец, взаимосвязь между повышением циркулирующих уровней биомаркеров повреждения миокарда и нежелательных ранних исходов указывает на то, что ишемия ПЖ имеет значимое патофизиологическое значение в острую фазу ТЭЛА [24, 25]. Несмотря на то, что инфаркт ПЖ редко встречается при ТЭЛА, складывается впечатление, что дисбаланс между доставкой кислорода и потреблением может вести к повреждению кардиомиоцитов и ещё большему снижению сократительной способности миокарда ПЖ. При этом системная гипотензия является ключевым элементом в патогенезе правожелудочковой недостаточности, приводя к ухудшению коронарного кровотока в условиях перегрузки ПЖ.
Негативные эффекты острой ТЭЛА на миокард ПЖ и кровообращение обобщены на рисунке 1.
Дыхательная недостаточность при ТЭЛА — наиболее частое последствие гемодинамических нарушений [26]. Низкий сердечный выброс ведёт к десатурации смешанной венозной крови. В дополнение к этому появление зон со сниженным кровотоком в пораженных сосудах в сочетании с зонами перегрузки потоком в интактных капиллярах ведет к появлению вентиляционно-перфузионного (V/Q) несоответствия, усугубляющего гипоксемию. У примерно одной третьей пациентов по данным эхокардиографии (ЭхоКГ) также обнаруживается шунтирование крови справа налево через незакрытое овальное окно: это вызвано инверсией градиента давления в предсердиях и может вести к тяжёлой гипоксемии и повышать риск парадоксальной эмболии и инсульта [27]. И наконец, мелкие дистальные эмболы, не влияющие на гемодинамику, могут создавать зоны альвеолярных кровоизлияний, проявляющихся кровохарканьем, плевритом, плевральным выпотом, которые по своей интенсивности обычно носят умеренный характер. Такая клиническая картина известна под названием “инфаркт лёгкого”, наличие которого незначительно влияет на газообмен в целом, за исключением пациентов с сопутствующей сердечно-лёгочной патологией.
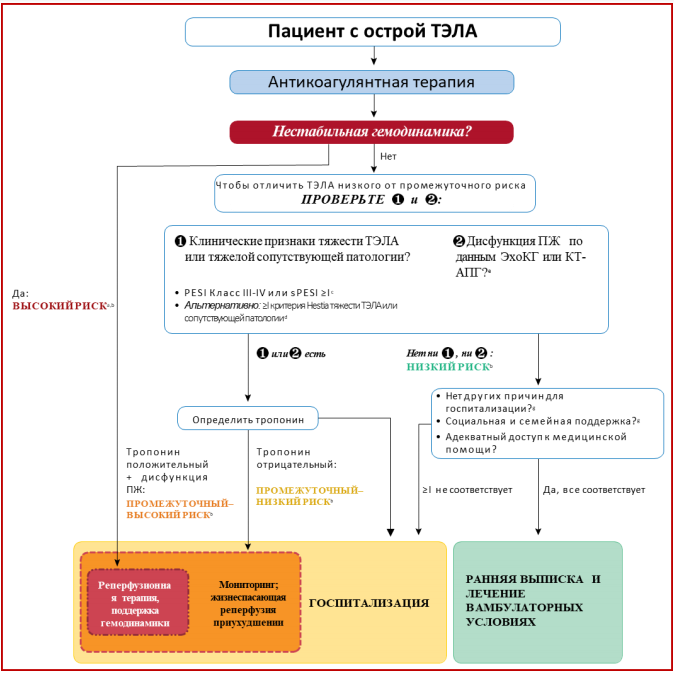
Согласно вышеизложенным патофизиологическим аспектам, острая правожелудочковая СН, определяемая как быстро прогрессирующий синдром с системным застоем в результате нарушения наполнения ПЖ и/или снижения ударного объёма ПЖ [11], является критическим фактором, определяющим клиническую тяжесть и исход при острой ТЭЛА. Соответственно, клинические симптомы и признаки недостаточности ПЖ и гемодинамической нестабильности указывают на высокий риск ранней (внутрибольничной или 30-дневной) смертности. ТЭЛА высокого риска определяется гемодинамической нестабильностью и включает в себя клинические варианты, представленные в таблице 1.
ТЭЛА высокого риска является состоянием, непосредственно угрожающим жизни пациента, в связи с чем требует экстренной диагностики (при подо- зрении) и незамедлительной выработки терапевтической стратегии (при подтверждении ТЭЛА или ее высокой вероятности) тактики, как описано в разделе 2.4. Однако отсутствие гемодинамической нестабильности не исключает начала (и, возможно, прогрессирования) дисфункции ПЖ и, следовательно, повышенного раннего риска, связанного с ТЭЛА. В этой большой популяции пациентов необходима дополнительная оценка уровня риска и соответствующая коррекция тактики ведения больного.
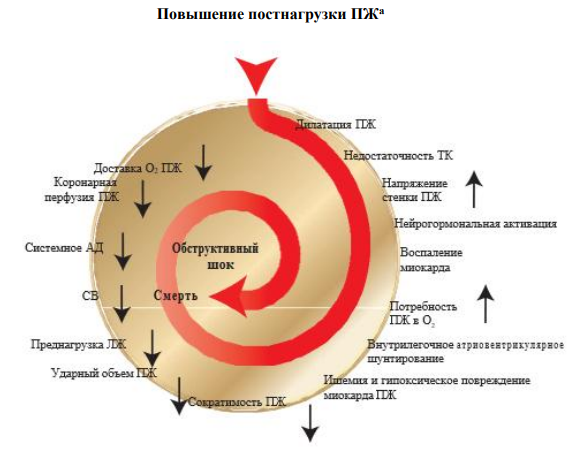
Рис. 1. Ключевые факторы развития гемодинамического коллапса и смерти при острой ТЭЛА (Konstantinides et al.).
Примечание: а — точная последовательность событий, приводящая к повышению постнагрузки ПЖ, до конца неизвестна.
Сокращения: АД — артериальное давление, ЛЖ — левый желудочек, ПЖ — правый желудочек, СВ — сердечный выброс, ТК — трикуспидальный клапан, О2 — кислород.
Таблица 1.
Определение гемодинамической нестабильности (проявляется одним из представленных ниже клинических вариантов)
|
(1) Остановка кровообращения
|
(2) Обструктивный шок
|
(3) Персистирующая гипотензия
|
|
Необходима сердечно- легочная реанимация
|
Систолическое АД <90 мм рт.ст. или необходимость использования вазопрессоров для поддержания АД ≥90 мм рт.ст. несмотря на адекватную коррекцию объема циркулирующей крови И Гипоперфузия органов и тканей (измененный психический статус; холодная, липкая кожа; олигурия/ анурия; повышенное содержание лактата в сыворотке)
|
Систолическое АД <90 мм рт.ст. или падение систолического АД ≥40 мм рт.ст., длительностью >15 мин и не связанное с такими состояниями как аритмия, гиповолемия или сепсис
|
Факторы и группы риска
Предрасполагающие факторы
Обширная травма, перелом нижних конечностей, повреждение спинного мозга, а также хирургические вмешательства, включая протезирование суставов, являются серьезными провоцирующими факторами для ВТЭ [29, 30]. Рак относится к общепризнанным предрасполагающим фактором для ВТЭ, при этом риск ВТЭ варьируется в зависимости от различных типов рака [31, 32]. Рак поджелудочной железы, онкогематологические заболевания, рак легких, рак желудка и рак головного мозга относятся к наиболее значимым провоцирующим факторам в отношении ВТЭ [33, 34]. Более того, наличие онкологического заболевания является важным предиктором смерти от всех причин в рамках эпизода ВТЭ события [35]. Использование пероральных контрацептивов, содержащих эстроген, ассоциировано с повышенным риском ВТЭ, а применение контрацептивов является наиболее частым ФР ВТЭ у женщин репродуктивного возраста [36-38]. Использование комбинированных оральных контрацептивов (содержащих как эстроген, так и прогестаген) приводит к увеличению риска ВТЭ примерно в 2-6 раз по сравнению с исходным уровнем [38, 39]. В целом, абсолютный риск ВТЭ остается низким у большинства среди более чем 100 млн пользователей комбинированных оральных контрацептивов во всем мире [40]; однако ФР ВТЭ, включая тяжелую наследственную тромбофилию (обсуждается в разделе 8) [41], увеличивают этот риск. Комбинированные оральные контрацептивы третьего поколения, содержащие прогестагены, такие как дезогестрел или гестоден, связаны с более высоким риском ВТЭ, чем комбинированные оральные контрацептивы второго поколения, которые содержат такие прогестагены, как левоноргестрел или норгестрел [42, 43]. С другой стороны, применение внутриматочных устройств, высвобождающих гормоны, и некоторых таблетированных форм, содержащих только прогестерон (используются в противозачаточных дозах), не ассоциировано со значительным увеличением риска ВТЭ [39, 44]; следовательно, после консультирования и полной оценки риска эти вари- анты часто предлагаются женщинам с семейным анамнезом ВТЭ событий.
У женщин в постменопаузе, которые получают заместительную гормональную терапию, риск ВТЭ, широко варьируется в зависимости от используемого препарата [45].
Инфекция является распространенным триггером для ВТЭ [29, 46, 47]. Переливание крови и препараты, стимулирующие эритропоэз, также связаны с повышенным риском ВТЭ [29, 48].
У детей ТЭЛА обычно ассоциирована с ТГВ и редко бывает неспровоцированной.
Серьезные хронические заболевания и наличие центральных венозных катетеров считаются вероятными триггерами ТЭЛА [49]. ВТЭ можно рассматривать как часть континуума сердечно-сосудистых заболеваний, и такие общие ФР, как курение сигарет, ожирение, гиперхолестеринемия, гипертония и сахарный диабет [50-53], являются общими для сосудистых заболеваний, в частности, атеросклероза [54-57]. Однако это может быть косвенной ассоциацией опосредованной, по крайней мере частично, осложнениями ишемической болезни сердца, а, в случае курения — раком [58, 59]. Инфаркт миокарда и сердечная недостаточность (СН) увеличивают риск ТЭЛА [60, 61]. И наоборот, у пациентов с ВТЭ повышен риск перенесения инфаркта миокарда, инсульта и эмболизации периферических артерий [62].
Факторы риска развития ВТЭ
|
Факторы риска при венозной тромбоэмболии
|
|
Большие факторы риска (отношение шансов ˃ 10)
|
|
Перелом нижней конечности
|
|
Госпитализация по поводу сердечной недостаточности или мерцания/трепетания предсердий (в предыдущие 3 месяца)
|
|
Замена тазобедренного или коленного сустава
|
|
Крупная (большая) травма
|
|
Инфаркт миокарда (в предыдущие 3 месяца)
|
|
Предыдущая венозная тромбоэмболия
|
|
Повреждение спинного мозга
|
|
Средние факторы риска (отношение шансов 2-9)
|
|
Артроскопическая операция на коленом суставе
|
|
Аутоиммунные заболевания
|
|
Переливание крови
|
|
Центральный венозный застой
|
|
Химиотерапия
|
|
Застойная сердечная или дыхательная недостаточность
|
|
Эритропоэз-стимулирующие агенты
|
|
Заместительная гормональная терапия (зависит от препарата)
|
|
Экстракорпоральное оплодотворение
|
|
Инфекции (специфическая пневмония, инфекции мочевыводящих путей, ВИЧ)
|
|
Воспалительное заболевание кишечника
|
|
Онкопатология (высокий риск метастазов)
|
|
Оральная контрацептивная терапия
|
|
Паралитический инсульт
|
|
Послеродовой период
|
|
Поверхностный тромбоз вен
|
|
Тромбофилия
|
|
Малые факторы риска (отношение шансов ˂ 2)
|
|
Постельный режим › 3 дней
|
|
Сахарный диабет
|
|
Гипертензия
|
|
Неподвижность в сидячем положении (например, длительная поездка на автомобиле или воздушном транспорте)
|
|
Пожилой возраст
|
|
Лапароскопическая операция (например, холецистоэктомия)
|
|
Ожирение
|
|
Беременность
|
|
Варикозное расширение вен
|
Клиническая картина
Cимптомы, течение
Клиническая картина
Клинические предикторы для прогнозирования тромбоэмболии легочной артерий (Женевская шкала) год?
|
|
Баллы для определения тактики ведения
|
|
|
Пересмотренная Женевская шкала
|
Полная версия
|
Упрощенная версия
|
|
Предшествовавшая ТЭЛА и тромбоз глубоких вен
|
3
|
1
|
|
ЧСС 75-94 в мин.
≥95 в мин. |
3
5 |
1
2 |
|
Хирургическое вмешательство/иммобилизация в течении предшествовавшего месяца
|
2
|
1
|
|
Кровохарканье
|
2
|
1
|
|
Активно растущая раковая опухоль
|
2
|
1
|
|
Одностороння боль в нижней конечности
|
3
|
1
|
|
Боль при пальпации вен нижних конечностей, сопровождающаяся ее отеком
|
4
|
1
|
Таблица. 4.
Клиническая оценка Женевской шкалы
|
События
|
Баллы для определения тактики ведения
|
|
|
Клиническая вероятность
|
Полная версия
|
Упрощенная версия
|
|
Трехуровневая шкала
|
|
|
|
Низкая
|
0-3
|
0-1
|
|
Умеренная
|
4-10
|
2-4
|
|
Высокая
|
≥11
|
≥5
|
|
Двухуровневая шкала
|
|
|
|
Тромбоэмболия легочной артерий маловероятна
|
0-5
|
0-2
|
|
Тромбоэмболия легочной артерий вероятна
|
≥6
|
≥3
|
Диагностика
Диагностика
-
Одышка в покое или при нагрузке (73 %)
-
Плевритная боль (66 %)
-
Кашель (37 %)
-
Ортопноэ (28 %)
-
Боль и/или отек в икрах или бедрах (44 %)
-
Хрипы (21 %)
-
Кровохарканье (13 %)
Менее распространенные проявления включают преходящие или постоянные аритмии (например, мерцание предсердий), предобморочные состояния, обмороки и гемодинамический коллапс (<10 %каждая) [68, 69]. Охриплость голоса из-за расширенной легочной артерии является редким проявлением (синдром Ортнера) [70].
Одышка часто (но не всегда) возникает быстро, обычно в течение нескольких секунд (46 %) или минут (26 %) [66]. Одышка может возникать реже у пожилых пациентов без предшествующих сердечно-легочных заболеваний. Одышка чаще возникает у пациентов с ТЭЛА в магистральных или долевых сосудах.
Примерно у 10 % пациентов наблюдаются симптомы инфаркта легкого, обычно из-за более мелких периферических эмболов. Плевральная боль типична для данной категории пациентов из-за воспаления плевры. Кровотечение из инфарктного легкого также считается причиной кровохарканья.
Данные ретроспективных исследований кто??? свидетельствуют о том, что обморок является основным симптомом в ≤10 % случаев. И наоборот, среди пациентов с обмороками частота ТЭЛА составляет от 1 до 17 % [71-79]. Частота может быть выше у госпитализированных с обмороком [76, 79]. Подчеркивая обморок, как проявление ТЭЛА, 560 пациентов, поступивших в отделение неотложной помощи с первым эпизодом обморока и поступивших в больницу, прошли тщательное обследование на предмет ТЭЛА, включающее D-димер, компьютерную томографию (КТ) и легочную ангиографию (КТ-АПГ). ) [76]. В этой популяции распространенность ТЭЛА составила 17 %, причем она была выше у тех, у кого не было другой идентифицируемой этиологии обмороков (25%). Хотя выписанные из отделения неотложной помощи не проходили обследование на предмет ТЭЛА, когда они были включены в анализ, частота ТЭЛА была ниже и ближе к показателям, наблюдавшимся в других ретроспективных исследованиях (4%). Обмороки могут указывать на большое количество тромбов, поскольку до 2/3 пациентов с ТЭЛА с обмороками имеют крупные тромбы, расположенные в магистральных или долевых артериях [68,69]. Причины обмороков у пациентов с ТЭЛА плохо изучены, но могут быть частично объяснены преходящими аритмиями при прохождении тромба через сердце или преходящей обструкцией при прохождении эмбола через клапан легочной артерии.
У некоторых пациентов проявление болезни возникает с задержкой в несколько недель или дней. В одном проспективном исследовании сообщалось, что у пациентов с отсроченным проявлением более чем на неделю, как правило, наблюдалась более крупная и более центрально расположенная ТЭЛА по сравнению с пациентами, обратившимися в течение семи дней (41 против 26 %) [80]. Симптомы и признаки ПЭ также могут развиваться с течением времени, и пациенты, у которых вначале наблюдались слабые симптомы, могут становиться все более симптоматичными или гемодинамически нестабильными, иногда очень быстро (от нескольких минут до нескольких часов). Это может быть следствием рецидивирующей эмболизации или прогрессирующей легочной гипертензии, вызванной сужением сосудов. Аналогично, по мере развития инфаркта легкого у пациентов могут развиваться прогрессирующая одышка, гипоксемия, плевральная боль и кровохарканье.
Общие признаки при осмотре включают [66]:
-
Тахипноэ (54 %)
-
Отек голени или бедра, эритема, отек, болезненность при пальпации (47 %)
-
Тахикардия (24 %)
-
Хрипы (18 %)
-
Снижение звуков дыхания (17 %)
-
Усиленный легочный компонент второго тона сердца (15 %)
-
Набухание яремных вен (14 %)
-
Лихорадка, имитирующая пневмонию (3 %)
Хотя ТГВ верхних конечностей (ТГВВ) эмболизируется реже, чем ТГВ нижних конечностей, симптомы ТГВ (например, боль или стеснение в руке) также должны вызывать подозрение на ТЭЛА.
ТЭЛА является частой причиной внезапной остановки сердца или циркуляторного коллапса (8 %), особенно среди пациентов моложе 65 лет [66,82,83]. Среди таких пациентов одышка или тахипноэ наблюдаются у 91%. Массивная ТЭЛА может сопровождаться острой правожелудочковой недостаточностью, проявляющейся повышением давления в яремных венах, акцентом II тона над легочной артерией, цианозом и обструктивным шоком. Однако шок может также развиться у пациентов с небольшой ТЭЛА и тяжелой легочной гипертензией. Переход от тахикардии к брадикардии или от узкокомплексной тахикардии к широкой (т. е. блокада правой ножки пучка Гиса) является зловещим признаком перенапряжения правого желудочка и надвигающегося шока. ТЭЛА следует заподозрить в любой момент, когда имеется гипотония, сопровождающаяся повышенным центральным венозным давлением, которое не объясняется острым инфарктом миокарда, напряженным пневмотораксом, тампонадой перикарда или новой аритмией [84,85].
2. Лабораторная диагностика
-
Общий анализ и биохимический анализ крови. Обычные лабораторные данные включают лейкоцитоз, повышенную скорость оседания эритроцитов (СОЭ), повышенный уровень лактата в сыворотке, повышенный уровень лактатдегидрогеназы в сыворотке (ЛДГ) и аспартатаминотрансферазы (АСТ). Креатинин сыворотки и расчетная скорость клубочковой фильтрации (СКФ) помогают определить безопасность введения контраста при ангиографии.
-
Газы артериальной крови и пульсоксиметрия. Необъяснимая гипоксемия на фоне нормальной рентгенограммы грудной клетки должна вызвать клиническое подозрение на ТЭЛА и потребовать дальнейшего обследования. У пациентов с подозрением на ТЭЛА показатели крови часто бывают аномальными; однако они могут быть нормальными у 18 процентов пациентов с ТЭЛА [86]. Нарушение газообмена может быть связано с основным сердечно-легочным заболеванием или усугубляться им [87]. Общие отклонения, наблюдаемые при анализе газов крови, включают одно или несколько из следующих [64,86,88]:
-
Гипоксемия (74 %)
-
Расширенный альвеолярно-артериальный градиент кислорода (от 62 до 86 %)
-
Респираторный алкалоз и гипокапния (41 %)
-
-
Мозговой натрийуретический пептид (BNP). Повышенный уровень BNP имеет ограниченную диагностическую ценность у пациентов с подозрением на ТЭЛА [90,91]. Однако повышенный уровень BNP или N-концевой (NT)-proBNP, может быть полезен с прогностической точки зрения для стратификации риска пациентов с диагнозом острой ТЭЛА.
-
Тропонин. Точно так же уровни тропонина I и Т в сыворотке полезны с прогностической точки зрения, но не с диагностической точки зрения [91-95]. В качестве маркеров дисфункции правого желудочка уровни тропонина повышены у 30–50 процентов пациентов с умеренной и массивной ТЭЛА [91,96] и связаны с клиническим ухудшением и смертью после ТЭЛА. Повышение тропонина обычно проходит в течение 40 часов после ТЭЛА, в отличие от более длительного повышения после острого повреждения миокарда [97].
-
D-димер. Специфичность D-димера при подозрении на ТЭЛА постоянно снижается с возрастом до ∼10% у пациентов старше 80 лет. Использование скорректированных по возрасту (вместо «стандартного» 500 мкг / л) пороговых значений D-димера увеличивает число пациентов, у которых можно исключить ТЭЛА с 6,4 до 30% без дополнительных ложноотрицательных результатов. Скорректированные по возрасту пороговые значения для D-димера определяются следующим подходом – (возраст × 10 мкг / л для пациентов в возрасте> 50 лет)
Оценка D-димера
-
Уровни D-димера повышены в плазме крови при остром тромбозе из-за одновременной активации коагуляции и фибринолиза
-
Отрицательная прогностическая ценность D-димер теста высокая и аномальный уровень D-димера с малой вероятностью показывает острую ТЭЛА или ТГВ
-
Положительная прогностическая ценность повышенного D-димера низкая и тестирование D-димера бесполезно для подтверждения ТЭЛА
-
часто повышен у онкологических больных, госпитализированных больных, при тяжелых инфекциях, воспалительных заболеваниях, при беременности
-
Зависит от возраста (чем старше – тем выше)
отрицательный результат ИФА D-димера может в сочетании с низкой/средней клинической вероятностью исключить заболевание без дальнейшего тестирования примерно у 30% пациентов с подозрением на ТЭЛА
|
Запомните:
|
|
Пороги D-димера с поправкой на возраст
|
Аномалии, которые исторически считались наводящими на мысль о ТЭЛА (паттерн S1Q3T3, перенапряжение правого желудочка, новая неполная блокада правой ножки пучка Гиса), встречаются редко (≤10 %) [47,48]. Нарушения ЭКГ, которые связаны с плохим прогнозом у пациентов с диагнозом ТЭЛА, включают [98,99,101]:
-
Предсердные аритмии (например, мерцательная аритмия)
-
Брадикардия (<50 ударов в минуту) или тахикардия (>100 ударов в минуту)
-
Новая блокада правой ножки пучка Гиса
-
Нижние зубцы Q (отведения II, III и aVF)
-
Изменения переднего сегмента ST и инверсия зубца Т
-
Паттерн S1Q3T3
Рентгенограмма органов грудной клетки. При ТЭЛА часто встречаются неспецифические отклонения на рентгенограмме грудной клетки (например, ателектаз, выпот), но нормальную рентгенограмму грудной клетки можно увидеть у 12–22 % пациентов [64,65,103]. Рентгенограмма грудной клетки обычно проводится большинству пациентов с подозрением на ТЭЛА, чтобы найти альтернативную причину симптомов пациента.
Эхокардиография. Острая ТЭЛА может привести к перегрузке давлением ПЖ и его дисфункции, что можно обнаружить с помощью ЭхоКГ. Учитывая специфическую геометрию ПЖ, не существует отдельного ЭхоКГ параметра, быстро и надежно оценивающего размер или функции ПЖ. Именно поэтому ЭхоКГ критерии диагностики ТЭЛА различались в разных исследованиях. В силу низкой отрицательной прогностической ценности — ~40-50%, отрицательный результат при выполнении ЭхоКГ не может исключать ТЭЛА [104, 105, 106]. С другой стороны, признаки перегрузки или дисфункции ПЖ могут выявляться и при отсутствии острой ТЭЛА, и могут быть связаны в таком случае с сопутствующей патологией [107].
ЭхоКГ признаки перегрузки и/или дисфункции ПЖ графически представлены на рисунке 3. Дилатация ПЖ обнаруживается у более чем 25% пациентов с ТЭЛА при выполнении трансторакальной ЭхоКГ (ТТЭхоКГ) и полезна для стратификации риска заболевания [108]. Было показано, что более специфические ЭхоКГ данные сохраняют высокую положительную прогностическую ценность для ТЭЛА даже при наличии у больного предсуществующих кардиореспираторных заболеваний. Так, сочетание времени ускорения кровотока в выносящем тракте ПЖ <60 мсек с максимальным систолическим градиентом на ТК <60 мм рт.ст. (признак “60/60”) или со снижением сократимости свободной стенки ПЖ в сравнении с верхушкой (симптом Макконела) предполагает наличие ТЭЛА [109]. Однако эти признаки присутствуют примерно у 12% и 20% пациентов, соответственно, в общей группе больных с ТЭЛА [108]. Обнаружение ЭхоКГ признаков перегрузки ПЖ помогает дифференцировать острую ТЭЛА от гипокинезии/акинезии свободной стенки ПЖ при инфаркте ПЖ, который может имитировать симптом Макконела [110]. Следует отметить, что примерно у 10% пациентов с ТЭЛА при выполнении ЭхоКГ могут выявляться такие находки, как значительная систолическая дисфункция ЛЖ или клапанная патология, которые вводят врача в заблуждение [110]. Снижение систолической экскурсии фиброзного кольца ТК (TAPSE) также может присутствовать у пациентов с ТЭЛА [111, 112]. Показатели тканевой допплерографии и деформации (strain) свободной стенки ПЖ, свидетельствующие о функции ПЖ, также могут изменяться у больного с ТЭЛА (рис. 3). Однако эти показатели, имеют низкую чувствительность в качестве самостоятельных критериев, т.к. в ряде работ было показано, что они могут оставаться нормальными у гемодинамически стабильных пациентов, несмотря на наличие ТЭЛА [113, 114].
Подвижные тромбы в правых камерах сердца выявляются с помощью чреспищеводной ЭхоКГ (ЧПЭхоКГ) или КТ-АПГ у <4% пациентов с ТЭЛА [116-118]. Их распространенность может достигать 18% среди пациентов с ТЭЛА в условиях отделения интенсивной терапии [119]. Наличие подвижных правосторонних тромбов в сердце подтверждает диагноз ТЭЛА и ассоциировано с высокой ранней смертностью, особенно у пациентов с дисфункцией ПЖ [118, 121-122].
У некоторых пациентов с подозрением на острую ТЭЛА при ЭхоКГ может выявиться утолщение стенки ПЖ или высокая скорость трикуспидальной регургитации, превышающая значения, совместимые с острой перегрузкой давления ПЖ (>3,8 м/с или пиковый систолический градиент на ТК >60 мм рт.ст.) [123]. В этих случаях необходимо проводить дифференциальный диагноз с ХТЭЛГ или другой легочной гипертензией (ЛГ).
Подвижные тромбы в правых камерах сердца выявляются с помощью чреспищеводной ЭхоКГ (ЧПЭхоКГ) или КТ-АПГ у <4% пациентов с ТЭЛА [116-118]. Их распространенность может достигать 18% среди пациентов с ТЭЛА в условиях отделения интенсивной терапии [119]. Наличие подвижных правосторонних тромбов в сердце подтверждает диагноз ТЭЛА и ассоциировано с высокой ранней смертностью, особенно у пациентов с дисфункцией ПЖ [118, 120-122].
У некоторых пациентов с подозрением на острую ТЭЛА при ЭхоКГ может выявиться утолщение стенки ПЖ или высокая скорость трикуспидальной регургитации, превышающая значения, совместимые с острой перегрузкой давления ПЖ (>3,8 м/с или пиковый систолический градиент на ТК >60 мм рт.ст.) [123]. В этих случаях необходимо проводить дифференциальный диагноз с ХТЭЛГ или другой легочной гипертензией (ЛГ).
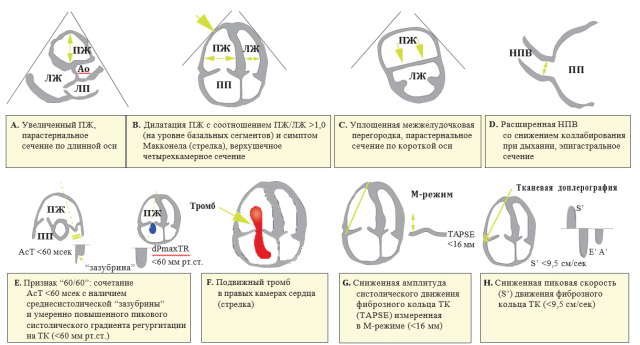
Рис. 3. Показатели ЭхоКГ, оценивающие перегрузку давлением ПЖ.
Сокращения: A’ — пиковая поздняя диастолическая (при сокращении предсердий) скорость движения трикуспидального кольца ТК при тканевой допплеро- графии, AcT — время ускорения кровотока в выносящем тракте ПЖ, Ao — аорта, E’ — пиковая ранняя диастолическая скорость движения трикуспидального кольца ТК при тканевой допплерографии, НПВ — нижняя полая вена, ЛП — левое предсердие, ЛЖ — левый желудочек, ПП — правое предсердие, ПЖ — правый желудочек, S’ — пиковая систолическая скорость движения трикуспидального кольца ТК при тканевой допплерографии, ТК — трикуспидальный клапан, ЭхоКГ — эхокардиография, TAPSE — cистолическая экскурсия фиброзного кольца ТК, dPmaxTR — максимальный градиент трикуспидальной регургитации.
ЭхоКГ параметры, используемые для стратификации раннего риска у пациентов с ТЭЛА, представлены на рисунке 3, а их прогностические значения суммированы в Дополнительной таблице 5. Для таких показателей как, соотношение диаметров ПЖ/ЛЖ ≥1,0 и TAPSE <16 мм в исследованиях наиболее часто демонстрировалась ассоциация с неблагоприятным прогнозом [111].
В целом, признаки дисфункции ПЖ при ЭхоКГ обнаруживаются у более чем 25% пациентов с острой ТЭЛА [108]. Результаты систематических обзоров и метаанализов позволяют предположить, что дисфункция ПЖ ассоциирована с повышенным риском краткосрочной смертности у пациентов, гемодинамически стабильных на момент обследования [124, 125]. При этом общая положительная прогностическая ценность дисфункции ПЖ в отношении смерти, связанной с ТЭЛА, была низкой (<10%) по данным метаанализа [124]. Это отчасти связано с трудностями стандартизации показателе ЭхоКГ [111, 180]. Тем не менее, ЭхоКГ оценка морфологии и функции ПЖ является ценным инструментом для оценки прогноза гемодинамически стабильных пациентов с ТЭЛА. В дополнение к оценке функции ПЖ, ЭхоКГ может идентифицировать шунт справа налево через открытое овальное окно и наличие тромбов в правых отделах сердца, наличие которых ассоциировано с повышенной смертностью у пациентов с острой ТЭЛА [27, 121]. Существование открытого овального окна также увеличивает риск ишемического инсульта из-за парадоксальной эмболии у пациентов с острой ТЭЛА и дисфункцией ПЖ [126, 127].
Компьютерная томография легочной артерии с контрастным усилением (КТ- АПГ). Мультидетекторная компьютерная томография (КТ) с контрастным усилением является методом выбора для визуализации легочной артерии у пациентов с подозрением на ТЭЛА, позволяя адекватно визуализировать ветви легочной артерии вплоть до субсегментарного уровня [128-130]. В проспективном исследовании PIOPED II (Prospective Investigation On Pulmonary Embolism Diagnosis) для КТ-АПГ (преимущественно четырехдетекторной КТ) была показана чувствительность 83% и специфичность 96% [131]. В данном исследовании также было выявлено влияние предтестовой клинической вероятности ТЭЛА на прогностическую ценность КТ- АПГ. У пациентов с низкой и промежуточной клинической вероятностью ТЭЛА отрицательный результат КТ-АПГ имел высокую отрицательную прогностическую ценность для диагностики ТЭЛА (96% и 89%, соответственно), но она снижалась до 60% у больных с высокой предтестовой вероятностью ТЭЛА. И наоборот, положительная прогностическая ценность положительного результата КТ-АПГ была высокой (92-96%) у пациентов с промежуточной или высокой клинической предтестовой вероятностью ТЭЛА, но в группе с низкой вероятностью ТЭЛА составляла всего 58% [131]. Поэтому, врачи должны рассмотреть возможность дальнейшего обследования пациента в случае наличия расхождений между результатом КТ-АПГ и клиническим представлением о больном.
Параметры КТ-АПГ, используемые для стратификации раннего риска смерти у пациентов с ТЭЛА суммированы в Дополнительной таблице 5. В качестве индикатора дисфункции ПЖ при выполнении КТ-АПГ при анализе четырехкамерного сечения сердца может визуализироваться увеличенный ПЖ (конечно-диастолический размер ПЖ и соотношение ПЖ/ЛЖ, измеренное в поперечном или четырехкамерном сечении). Прогностическая значимость увеличенного ПЖ подтверждается результатами проспективного многоцентрового когортного исследования, включавшего 457 пациентов [132]. Так увеличение ПЖ (определяемое как отношение ПЖ/ЛЖ ≥0,9) было независимым предиктором неблагоприятного исхода в ходе госпитализации как в общей популяции с пациентов с ТЭЛА (отношение рисков (ОР) 3,5, 95% ДИ 1,6-7,7), так и у гемодинамически стабильных больных с ТЭЛА (ОР 3,8, 95% ДИ 1,3-10,9) [132]. Мета-анализ 49 исследований с включением более чем 13 тыс. пациентов с ТЭЛА, подтвердил то, что увеличение соотношения ПЖ/ЛЖ ≥1,0 по данным КТ-АПГ, было связано с повышением риска смертности от всех при- чин в 2,5 раза (отношение шансов (ОШ) 2,5, 95% ДИ 1,8-3,5) и с пятикратным повышением риска смерти по причине ТЭЛА (ОШ 5,0, 95% ДИ 2,7-9,2) [133].
Умеренное расширение ПЖ (ПЖ/ЛЖ незначительно выше 0,9) является частой находкой при выполнении КТ (обнаруживается у >50% гемодинамически стабильных пациентов с ТЭЛА [134]), но, вероятно, имеет низкое прогностическое значение. Тем не менее, увеличение соотношения диаметра ПЖ/ЛЖ ассоциировано с повышением специфичности прогноза [135, 136], даже у пациентов, которые относятся к категории “низкого” риска на основании клинических критериев [134]. Таким образом, соотношения ПЖ/ЛЖ ≥1,0 (вместо 0,9) по данным КТ-АПГ, вероятно, с большей точностью определяет плохой прогноз больных.
Помимо оценки размера ПЖ и отношения ПЖ/ ЛЖ, КТ может давать дополнительную информацию для оценки прогноза, основанную измерении объёмов камер сердца [138-139] и оценке заброса контрастного вещества в нижнюю полую вену (НПВ) [133, 140, 141].
Компрессионное ультразвуковое исследование вен (КВУЗИ). В большинстве случаев источником ТЭЛА служат тромбированные глубокие вены нижних конечностей и очень редко — глубокие вены верхних конечностей (в основном после катетеризации этих вен). В исследовании с использованием венографии ТГВ был обнаружен у 70% пациентов с верифицированной ТЭЛА [142]. В настоящее время КВУЗИ в значительной степени заменило венографию для диагностики ТГВ. КВУЗИ имеет чувствительность >90% и специфичность ~95% для проксимального симптомного ТГВ [143, 144]. КВУЗИ выявляет ТГВ у 30-50% пациентов с ТЭЛА [143-145], при этом выявление проксимального ТГВ у пациентов с подозрением на ТЭЛА достаточно для инициации терапии анти- коагулянтами без дальнейшего дообследования [146]. При этом таким пациентам (косвенное подтверждение ТЭЛА) в обязательном порядке должна быть выполнена оценка тяжести ТЭЛА и стратификация риска ранней смерти.
У гемодинамически нестабильных пациентов, поступивших в отделение неотложной помощи с подозрением на ТЭЛА, сочетание КВУЗИ с ЭхоКГ может еще больше повысить специфичность. И наоборот, по данным одного исследования, отсутствие дисфункции ПЖ при выполнении ЭхоКГ в сочетании с нормальным вариантом КВУЗИ исключало ТЭЛА с высокой (96%) отрицательной прогностической ценностью [148].
Таблица 5.
Прогностические значения для стратификации раннего риска смерти
|
Рекомендации
|
Класса
|
Уровеньb
|
|
Вероятная ТЭЛА с нестабильной гемодинамикой
|
||
|
При подозрении на ТЭЛА высокого риска с нестабильной гемодинамикой рекомендовано выполнение ЭхоКГ “у постели” или неотложной КТ-АПГ (в
зависимости от доступности и конкретной клинической ситуации). |
I
|
C
|
|
Рекомендовано безотлагательное в/в введение НФГ, включая скорректированное по возрасту болюсное введение у пациентов с вероятной ТЭЛА высокого риска.
|
I
|
C
|
|
Вероятная ТЭЛА без нестабильной гемодинамики
|
||
|
Рекомендовано использование валидированных критериев для диагностики
ТЭЛА. |
I
|
B
|
|
Рекомендована безотлагательная инициация антикоагулянтной терапии у пациентов с высокой и промежуточной вероятностью ТЭЛА в процессе
реализации диагностического алгоритма. |
I
|
C
|
|
Клиническая оценка
|
||
|
Диагностическая стратегия должна основываться на оценке клинической вероятности по клиническим данным или валидированным прогностическим
шкалам. |
I
|
A
|
|
D-димер
|
||
|
Рекомендовано измерять уровень D-димера в плазме крови у амбулаторных/экстренно госпитализированных пациентов с низким или промежуточным риском ТЭЛА, либо если ТЭЛА маловероятна, чтобы избежать лишних методов визуализации и облучения пациента.
|
I |
A |
|
Отрицательное значение теста на D-димер с использованием порогового значения, скорректированного по возрасту пациента (возраст*10 мг/л, у пациентов >50 лет), должно использоваться для исключения ТЭЛА в качестве альтернативы фиксированным значениям нормального уровня D-димера у пациентов с низким и промежуточным предтестовым риском ТЭЛА или в случае, когда ТЭЛА маловероятна.
|
IIa |
B |
|
Отрицательное значение теста на D-димер с использованием порогового значения, скорректированного по уровню клинической вероятностис ТЭЛА, должно использоваться для исключения ТЭЛА в качестве альтернативы фиксированным значениям нормального уровня D-димера.
|
IIa |
B |
|
Измерение уровня D-димера не рекомендовано у пациентов с высокой предтестовой вероятностью ТЭЛА, т. к. нормальный уровень D-димера достоверно не исключает ТЭЛА, даже при использовании высоко чувствительных тест-систем.
|
III |
A |
|
КТ-АПГ
|
||
|
У пациентов с низкой и промежуточной предтестовой вероятностью ТЭЛА, а также в случае, когда ТЭЛА маловероятна, отрицательный результат КТ-АПГ исключает диагноз ТЭЛА без необходимости дальнейшего обследования.
|
I
|
A
|
|
У пациентов с промежуточной и высокой предтестовой вероятностью ТЭЛА визуализация при КТ-АПГ сегментарных и более проксимальных дефектов контрастирования подтверждает диагноз ТЭЛА без необходимости дальнейшего дообследования
|
I |
B |
|
У пациентов с высокой предтестовой вероятностью ТЭЛА, а также в случае,
когда ТЭЛА вероятна нормальный вариант КТ-АПГ может исключать диагноз ТЭЛА может без необходимости дальнейшего обследования. |
IIa
|
B
|
|
Дальнейшее применение визуализирующих методов может потребоваться для
подтверждения ТЭЛА при обнаружении изолированных субсегментарных дефектов контрастирования. |
IIb
|
C
|
|
КТ-венография не рекомендована в качестве дополнения к КТ-АПГ
|
III
|
B
|
|
КВУЗИ
|
||
|
КВУЗИ нижних конечностей, верифицирующее проксимальный ТГВ у пациента с клиническим подозрением на ТЭЛА, подтверждает ВТЭ (или ТЭЛА).
|
I
|
A
|
|
Если КВУЗИ нижних конечностей визуализирует только дистальный ТГВ,
дальнейшее обследование следует рассмотреть для подтверждения ТЭЛА . |
IIa
|
B
|
|
Если наличие ТГВ по данным КВУЗИ используется для подтверждения ТЭЛА,
необходимо провести оценку тяжести ТЭЛА для выбора стратегии лечения . |
IIa
|
C
|
|
МРТ
|
||
|
МРТ не используется для исключения ТЭЛА.
|
III
|
A
|
Сокращения: в/в — внутривенное введение, ВТЭ — венозные тромбоэмболии, КВУЗИ — компрессионное ультразвуковое исследование вен, КТ — компьютер- ная томография, КТ-АПГ — компьютерная томография с контрастным усилением легочной артерии, МРТ — магнитно-резонансная томография, ТЭЛА — легочная эмболия, НФГ — нефракционированный гепарин, ОФЭКТ — однофотонная эмиссионная компьютерная томография, ТГВ — тромбоз глубоких вен, ЭхоКГ — эхо- кардиография, V/Q — вентиляционно-перфузионная (сцинтиграфия легких).
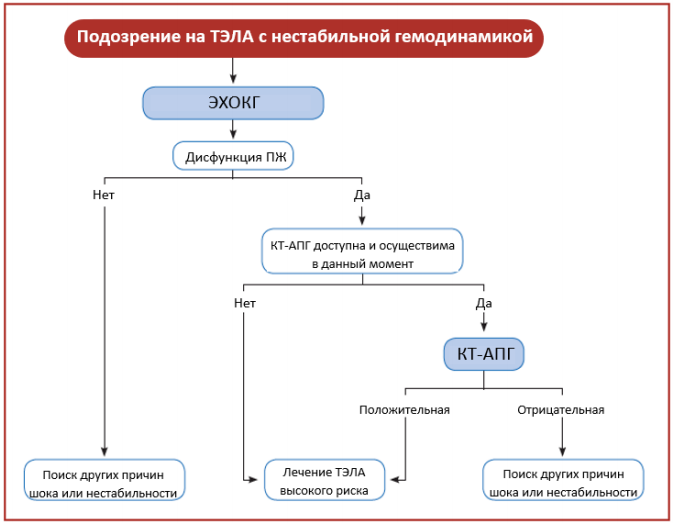
Сокращения: КТ — компьютерная томография, КТ-АПГ — компьютерная томография-ангиопульмонография, ТЭЛА — тромбоэмболия в легочную артерию, ЭхоКГ — эхокардиография.
КТ (ангиография) второстепенное обследование у больных с повышенным уровнем D- димера, но первостепенное у лиц с высокой клинической вероятностью. ТЭЛА на КТ (ангиографии) считается достоверным, когда оно показывает сгусток, по крайней мере в одной сегментарной ветви легочной артерии. Ниже представлен алгоритм действий при отсутствии шока или гипотонии (Рис. 5.)
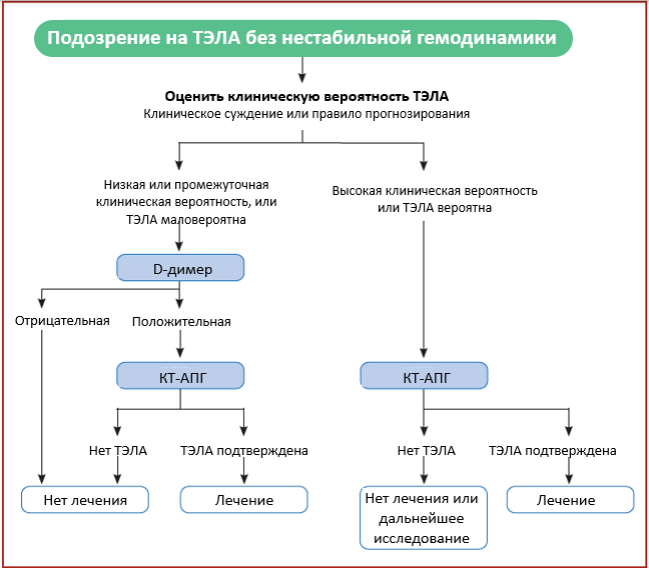
Рис. 5. Алгоритм диагностики для пациентов с подозрением на ТЭЛА без признаков нестабильной гемодинамики.
Сокращения: КТ-АПГ — компьютерная томография-ангиопульмонография, ТЭЛА – тромбоэмболия легочной артерии.
Оценка прогноза.
Таблица. 6.
Индекс тяжести ТЭЛА
| Исходный и упрощенный индекс тяжести ТЭЛА (PESI) | ||
| параметры | исходная версия | Упрощ. версия |
| возраст | возраст в годах | 1 балл (если возраст > 80 лет) |
| Мужской пол | +10 баллов | - |
| Онкопроцесс | +30 баллов | 1 балл |
| Хроническая сердечная недостаточность | +10 баллов | 1 балл |
| Хронические легочные заболевания | +10 баллов | |
| ЧСС ≥ 110 | +20 баллов | 1 балл |
| САД ˂ 100 мм.рт.ст. | +30 баллов | 1 балл |
| ЧД ˃ 30 в мин | +20 баллов | - |
| Температура ˂ 36 С | +20 баллов | - |
| Изменения психического состояния | +60 баллов | - |
| Сатурация ˂ 90 % | +20 баллов | 1 балл |
| Градация риска а | ||
|
Класс 1: ≤ 65 баллов очень низкий риск 30 дневной летальности (0-1,6%) Класс 2:66-85 баллов низкий риск смертности (1,7-3,5%) Класс 3: 86-105 баллов Умеренный риск смертности (3,2-7,31%) Класс 3: 106-125 баллов Высокий риск смертности (4,0-11,4%) Класс 3: более 126 баллов Очень высокий риск смертности (10,0- 24,5%) |
0 баллов = риск 30 дневной летальности 1,0% (95 % Cl 0,0%-2,1%) ≥ 1 балл (ов) = 30 дневная летальность 10,9% (95 % Cl 8,5%-13,2%) |
|
Лечение
Лечение
1. Консервативное лечение
1. Гемодинамическая и респираторная поддержка: кислородная терапия и вентиляция
Пероральные антикоагулянты без витамина К представляют собой небольшие молекулы, которые непосредственно ингибируют один активированный фактор свертывания, который является тромбином для дабигатрана и фактором ха для апиксабана, эдоксабана и ривароксабана. Благодаря их предсказуемой биодоступности и фармакокинетике, пероральные антикоагулянты без витамина К можно вводить в фиксированных дозах без обычного лабораторного мониторинга. По сравнению с антагонистами витамина К (АВК), при одновременном назначении пероральные антикоагулянты без витамина К с другими лекарственными средствами меньше взаимодействий.
При использовании АВК, антикоагулянтную терапию с НФГ, НМГ или фондапаринуксом следует продолжать параллельно с пероральным антикоагулянтом в течение ± 5 дней и до тех пор, пока значение международного нормализованного отношения (МНО) не станет 2,0–3,0 в течение 2 последующих дней. Варфарин может быть начат в дозе 10 мг у более молодых здоровых (например, в возрасте <60 лет) пациентов, и в дозе около 5 мг у пожилых пациентов. Суточная доза коррегируется в соответствии с МНО в течение следующих 5–7 дней с целью достижения уровня МНО 2,0–3,0.
В ниже приведенной таблице предоставлены данные о дозах и длительности антикоагулянтной терапии (Таблица 7.)
| Нефракционный гепарин основной препарат лечения в комбинации с вит. K Антагонист (АВК), при возможности использовать низкомолекулярные гепарины или пентасахариды, указанные ниже. |
Антикоагулянтная терапия
|
Низкомолекулярный гепарин и пентасахарид (фондапаринукс) одобрен для лечения ТЭЛА
|
||
|
|
Дозировка
|
Интервал
|
|
Эноксапарин (Enoxaparin)
|
1,0 мг / кг или
1,5 мг / кг а |
Каждые 12 часов
Один раз в деньа |
|
Тинзапарин (Tinzaparin )
|
175 ЕД / кг
|
Один раз в день
|
|
Дальтепарин (Dalteparin)
|
100 МЕ / кгб или
200 МЕ / кгб |
Каждые 12 часовб
Один раз в день |
|
Надропарин (Nadroparin)в
|
86 МЕ / кг или
171 МЕ / кг |
Каждые 12 часов
Один раз в день |
|
Фондапаринукс (Fondaparinux)
|
5 мг (масса тела <50 кг);
7,5 мг (масса тела 50-100 кг); 10 мг (масса тела> 100 кг) |
Один раз в день
|
-
Все схемы вводят подкожно.
-
МЕ = международных единиц; НМГ = низкомолекулярный гепарин.
-
а) инъекции эноксапарина один раз в сутки в дозе 1,5 мг / кг, предназначен для стационарного (больничного) лечения ТЭЛА в Соединенных Штатах и в некоторых, но не во всех, странах Европы.
-
б) В случае больных раковыми заболеваниями, дается дальтепарин в дозе 200 МЕ / кг массы тела (максимум, 18 000 МЕ) один раз в день в течение 1 месяца, затем 150 МЕ / кг один раз в день в течение 5 месяцев. По истечении этого срока, антикоагулянтная терапия вводиться под прикрытием антагониста витамина К или НМГ следует продолжать неограниченно или пока рак не будет считаться вылеченным.
-
в) Надропарин одобрен для лечения ТЭЛА в некоторых, но не во всех, странах Европы.
Вливание нефракционированного гепарина следует прекратить во время введения стрептокиназы или урокиназы; и может быть продолжено при ртАП инфузии (рекомбинантный тканевый активатор плазминогена). У пациентов, получающих НМГ или фондапаринукс, происходит тромболизис, и инфузию НФГ следует делать не раньше, чем через 12 часов после последней инъекции НМГ (два раза в день), или позже 24 часов после последней инъекций НМГ или фондапаринукса (один раз в день). Учитывая риск кровотечения, связанный с тромболизисом и возможность того, что необходимо будет немедленно прекратить или получить обратный антикоагулянтный эффект гепарина, разумно будет продолжить антикоагулянтную терапию с НФГ в течение нескольких часов после окончания тромболитической терапии до перехода на НМГ или фондапаринукс. Большая часть противопоказаний к тромболизису может считаться относительной в случае ТЭЛА высокого риска (жизнеугрожающей). (Таблица 8.)
Тромболитическая терапия. Тромболитическая терапия должна проводиться только в специализированных центрах (до 2-х дней с момента постановки диагноза)
|
Утвержденные тромболитические схемы для ТЭЛА
|
|
|
Стрептокиназа
|
250 000 МЕ как ударной дозы в течении 30 мин, затем 100 000 МЕ/ч в течении 12-24 часов
|
|
ускоренный режим: 1,5 миллиона МЕ в течении 2 часов
|
|
|
Урокиназа
|
4400 МЕ/кг как ударной дозы в течении 10 мин, затем 4400 МЕ/кг/ч течении 12-24 часов
|
|
ускоренный режим: 3 миллиона МЕ в течении 2 часов
|
|
|
Рекомбинантн ый тканевой активатор плазминогена
|
100 мг в течении 2 часов или
|
|
0,6 мг/кг в течении 15 мин. (макс. Доза 50 мг)
|
|
|
Противопоказания к тромболитической терапии
|
|
Абсолютные противопоказания
|
|
геморрагический инсульт или инсульт неясного генеза в любой момент времени
|
|
ишемический инсульт (в предыдущие 6 месяцев)
|
|
повреждения центральной нервной системы или новообразования
|
|
недавние большие травмы/ операции/ черепно-мозговые травмы (в предыдущие 3 недели)
|
|
желудочно-кишечное кровотечение в течение последнего месяца
|
|
известный риск кровотечения
|
|
Относительные противопоказания
|
|
транзиторная ишемическая атака (в предыдущие 6 месяцев)
|
|
Лечение пероральными антикоагулянтами
|
|
беременность, или первая неделя после родов
|
|
Не заживающее место пункции
|
|
травматическая реанимация
|
|
стойкая гипертензия (САД > 180 мм.рт.ст.)
|
|
прогрессирующее заболевания печени
|
|
|
Продолжительность антикоагулянтной терапии.
|
Рекомендации по продолжительности антикоагулянтной терапии
|
Класса
|
Уровеньб
|
|
Для пациентов с ТЭЛА с вторичными по отношению к временным (обратимые) фактором риска, пероральные антикоагулянты рекомендуется употреблять в течение 3 месяцев.
|
I
|
B
|
|
Для пациентов с неспровоцированной ТЭЛА, пероральные антикоагулянты рекомендуются, по крайней мере, 3 месяца.
|
I
|
A
|
|
Длительный курс пероральных антикоагулянтов следует назначать для пациентов с первым эпизодом неспровоцированной ТЭЛА и низким риском кровотечения.
|
IIa
|
B
|
|
Антикоагулянтную терапию на неопределенный срок (длительно) рекомендуется для пациентов со вторым эпизодом неспровоцированной ТЭЛА.
|
I
|
B
|
|
Ривароксабан (20 мг один раз в день), дабигатрана (150 мг два раза в день, или 110 мг два раза в день для пациентов > 80 лет или находящихся под сопутствующим лечением верапамилом) или Апиксабан (2,5 мг два раза в день) в случае продления лечения антикоагулянтами необходимо назначать в качестве альтернативы АВК (за исключением, пациентов с тяжелой почечной недостаточностью)в
|
IIa
|
Bг
|
|
При длительном получении антикоагулянтов, лечение должны быть пересмотрено с добавлением регулярных интервалов, для того чтобы пациент мог продолжать прием препаратов, сохраняя баланс между риском и пользой
|
I
|
C
|
|
Пациенты, которые отказываются принимать или не переносят любую форму пероральных антикоагулянтов, аспирин может назначаться длительно для профилактики вторичных ВТЭ.
|
IIb
|
B
|
|
Для пациентов с ТЭЛА и раком, следует назначить НМГ подкожно и откорректировать под массу больного в течение первых 3-6 месяцев.
|
IIa
|
B
|
|
Для пациентов с ТЭЛА и раком, при длительном получении антикоагулянтов (за первые 3-6 месяцев) следует оставить прием на неопределенный срок или до излечения от рака.
|
IIa
|
C
|
б - Уровень доказательности
в - Многолетние данные о пациентах, принимающих новые пероральные антикоагулянты для вторичной профилактики ТЭЛА еще не доступны
г - B относится к доказательствам доступным для каждого препарата в отдельности
7. Лечение ТЭЛА при беременности
После родов лечение гепарином можно заменить на АВК. Лечение антикоагулянтами следует продолжать не менее 6 недель после родов и с минимальным общим периодом в 3 месяца. АВК можно назначать кормящим матерям.
Тромболизис нельзя использовать в перипартальный период, за исключением критических ситуаций. (Таблица 11.)
Таблица. 11.
Беременность
|
Расчетная доза облучения, поглощаемая при процедурах, используемых для диагностики ТЭЛА
|
||
|
Исследование
|
Расчетная доза облучение плода (мЗв)
|
Расчетная доза радиационного облучения тканей молочной железы матери (мЗв)
|
|
Рентгенограмма грудной клетки
|
<0.01
|
0.01
|
|
Перфузионная сцинтиграфия легких с помощью Technetium-99m меченными альбуминами
Низкая доза: 40 МБк Высокая доза: 200 МБк |
0.11–0.20 0.20–0.60 |
0.28–0.50 1.20 |
|
Вентиляционное сканирование легких
|
0.10–0.30
|
<0.01
|
|
Компьютерная томография (ангиография)
|
0.24–0.66
|
10–70
|
|
Рекомендации по ТЭЛА при беременности
|
класс
|
уровень
|
|
При подозрение на ТЭЛА во время беременности диагностическая оценка формально гарантируется утвержденными методами
|
I
|
C
|
|
Измерение D-димера может быть выполнена для того, чтобы избежать ненужного облучения, а отрицательный результат имеет такую же клиническую значимость, как и у небеременных пациентов.
|
IIb
|
C
|
|
Компрессионное УЗИ вен можно учитывать для того, чтобы избежать ненужного облучения, а диагноз проксимального ТГВ подтверждает ТЭЛА.
|
IIb
|
C
|
|
При беременности перфузионную сцинтиграфию можно рассматривать для исключения подозрения на ТЭЛА с нормальным рентгеном грудной клетки.
|
IIb
|
C
|
|
КТ (ангиография) следует рассматривать, если рентген грудной клетки является ненормальным или если сцинтиграфия легких не доступны.
|
IIa
|
C
|
|
НМГ откорректированный под массу тела является рекомендованной терапии во время беременности у пациентов без шока или гипотонии.
|
I
|
В
|
8. Ведение пациентов с ТЭЛА и со злокачественными новообразованиями
При рецидиве ВТЭ у пациентов с раком на АВК или НМГ может применяться максимальная разрешённая доза НМГ или установка кавафильтра. Венозные фильтры следует рассматривать, когда антикоагулянты применять невозможно ввиду кровотечений; однако, в этом случае растёт риск тромбоза фильтра. (Таблица 12.)
Таблица. 12.
ТЭЛА и онкопатология
|
Рекомендации
|
Классa
|
Уровеньb
|
|
У пациентов с ТЭЛА и онкопатологией следует отдать предпочтение назначению НМГ подкожно сообразно весу пациента перед АВК в течение первых 6 мес.
|
IIa
|
A
|
|
Следует назначать эдоксабан в качестве альтернативы НМГ в дозировках, соответствующих весу пациента, при отсутствии рака желудочно-кишечного тракта.
|
IIa
|
B
|
|
Следует назначать ривароксабан в качестве альтернативы НМГ в дозировках, соответствующих весу пациента, при отсутствии рака желудочно-кишечного тракта.
|
IIa
|
C
|
|
У пациентов с ТЭЛА и онкологическим заболеванием следует обсуждать пролонгированную антикоагулянтную терапию (свыше первых 6 мес.) c на неопределенный период или до излечения онкозаболевания.
|
IIa
|
B
|
|
У пациентов с раком ведение случайно обнаруженной ТЭЛА должно осуществляться, так же как и симптомной ТЭЛА при наличии тромбов сегментарных и более проксимальных ветвей легочной артерии, или единственной сегментарной ветви легочной артерии с сочетанием с ТГВ.
|
IIa
|
B
|
Медицинская реабилитация
Организация медицинской помощи больным с острой ТЭЛА
В случае обращения больных с острой ТЭЛА в любые медицинские учреждения, должна быть оказана медицинская помощь.
Госпитализация и оказание квалифицированной медицинской помощи должно проводиться во всех ургентных и интенсивных отделениях.
Прогноз
Прогноз
Для прогнозирования ранней (в стационаре или в течении 30 дней) смертности при острой ТЭЛА, должны быть приняты во внимание клиническое состояния пациента и сопутствующие заболевания. (Таблица 10.)
Таблица. 10. Прогноз.
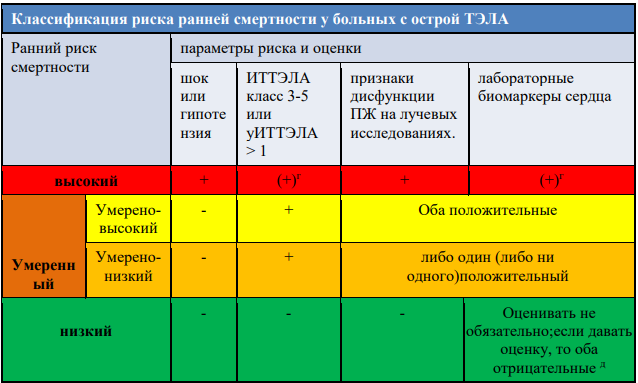
ТЭЛА = тромбоэмболия легочной артерии; ИТТЭЛА = индекс тяжести тромбоэмболии легочной артерии; ПЖ = правого желудочка; уИТТЭЛА = упрощенный индекс тяжести тромбоэмболии легочной артерии.
a) ИТТЭЛА Класс III - V показывает от умеренного до очень высокого 30-дневного риска смертности; уИТТЭЛА ≥1 пункт (ы) указывают на высокий риск 30-дневной смертности.
б) Эхокардиографические критерии дисфункции ПЖ включают расширение ПЖ и / или повышенние соотношения конечного диастолического диаметра между ПЖ-ЛЖ (в большинстве обследований, пороговое значение 0,9 или 1,0); гипокинезия свободной стенки ПЖ; увеличение скорости регургитации трехстворчатого клапана; или комбинации вышеперечисленного. На компьютерной томографии (КТ) ангиографии (при просмотре четырех камер сердца), ПЖ дисфункция определяется как увеличение конечного диастолического диаметр ПЖ к ЛЖ (с порогом 0,9 или 1,0).
в) маркеры повреждения миокарда (например, повышенный сердечный тропонин I или -T концентрации в плазме крови), или от сердечной недостаточности в вследствие (право) желудочковой дисфункции (повышенной концентрации натрийуретических пептидов в плазме).
г) Подсчет ИТТЭЛА (или уИТТЭЛА) и лабораторные обследования не считаются необходимыми у пациентов с гипотонией или шоком.
д) у пациентов с ИТТЭЛА класса I-II, или с уИТТЭЛА 0, и при повышении сердечных биомаркеров или признаков ПЖ дисфункции на томографии, должны классифицироваться по категории среднего низкого риска. Это может относиться к ситуациям, в которых результаты биомаркеров или томографии станут доступны до расчета клинического индекса тяжести.
Госпитализация
Организация медицинской помощи больным с острой ТЭЛА
В случае обращения больных с острой ТЭЛА в любые медицинские учреждения, должна быть оказана медицинская помощь.
Госпитализация и оказание квалифицированной медицинской помощи должно проводиться во всех ургентных и интенсивных отделениях.
Информация
Источники и литература
-
Клинические протоколы Министерства здравоохранения Кыргызской Республики
- Клинические протоколы Министерства здравоохранения Кыргызской Республики - 1. Raskob GE, Angchaisuksiri P, Blanco AN, Buller H, Gallus A, Hunt BJ, Hylek EM, Kakkar A, Konstantinides SV, McCumber M, Ozaki Y, Wendelboe A, Weitz JI. Thrombosis: a major contributor to global disease burden. Arterioscler Thromb Vasc Biol 2014;34:2363-2371. 2. Wendelboe AM, Raskob GE. Global burden of thrombosis: epidemiologic aspects. Circ Res 2016;118:1340-1347. 3. Keller K, Hobohm L, Ebner M, Kresoja KP, Munzel T, Konstantinides SV, Lankeit M. Trends in thrombolytic treatment and outcomes of acute pulmonary embolism in Germany. Eur Heart J 2020;41:522-529. 4. de Miguel-Diez J, Jimenez-Garcia R, Jimenez D, Monreal M, Guijarro R, Otero R, Hernandez-Barrera V, Trujillo-Santos J, Lopez de Andres A, Carrasco-Garrido P. Trends in hospital admissions for pulmonary embolism in Spain from 2002 to 2011. EurRespirJ 2014;44:942-950. 5. Dentali F, Ageno W, Pomero F, Fenoglio L, Squizzato A, Bonzini M. Time trends and case fatality rate of in-hospital treated pulmonary embolism during 11 years of observation in Northwestern Italy. Thromb Haemost 2016;115:399-405. 6. Lehnert P, Lange T, Moller CH, Olsen PS, Carlsen J. Acute pulmonary embolism in a national Danish cohort: increasing incidence and decreasing mortality. Thromb Haemost 2018;118:539-546. 7. Barco S, Woersching AL, Spyropoulos AC, Piovella F, Mahan CE. European Union-28: an annualised cost-of-illness model for venous thromboembolism. Thromb Haemost 2016;115:800-808. 8. Cohen AT, Agnelli G, Anderson FA, Arcelus JI, Bergqvist D, Brecht JG, Greer IA, Heit JA, Hutchinson JL, Kakkar AK, Mottier D, Oger E, Samama MM, Spannagl M; VTE Impact Assessment Group in Europe (VITAE). Venous thromboembolism (VTE) in Europe. The number of VTE events and associated morbidity and mortality. Thromb Haemost 2007;98:756-764. 9. Jimenez D, de Miguel-Diez J, Guijarro R, Trujillo-Santos J, Otero R, Barba R, Muriel A, Meyer G, Yusen RD, Monreal M; RIETE Investigators. Trends in the management and outcomes of acute pulmonary embolism: analysis from the RIETE registry. J Am Coll Cardiol 2016;67:162-170. 10. Agarwal S, Clark D III, Sud K, Jaber WA, Cho L, Menon V. Gender disparities in outcomes and resource utilization for acute pulmonary embolism hospitalizations in the United States. Am J Cardiol 2015;116:1270-1276. 11. Roy PM, Meyer G, Vielle B, Le Gall C, Verschuren F, Carpentier F, Leveau P, Furber A; EMDEPU Study Group. Appropriateness of diagnostic management and outcomes of suspected pulmonary embolism. Ann Intern Med 2006;144:157-164. 12. Jimenez D, Bikdeli B, Barrios D, Morillo R, Nieto R, Guerassimova I, Muriel A, Jara-Palomares L, Moores L, Tapson V, Yusen RD, Monreal M; RIETE Investigators. Management appropriateness and outcomes of patients with acute pulmonary embolism. Eur RespirJ 2018;51:1800445. 13. Wiener RS, Schwartz LM, Woloshin S. Time trends in pulmonary embolism in the United States: evidence of overdiagnosis. Arch Intern Med 2011;171:831-837. 14. Biss TT, Brandao LR, Kahr WH, Chan AK, Williams S. Clinical features and outcome of pulmonary embolism in children. BrJ Haematol 2008;142:808-818. 15. Andrew M, David M, Adams M, Ali K, Anderson R, Barnard D, Bernstein M, Brisson L, Cairney B, DeSai D. Venous thromboembolic complications (VTE) in children: first analyses of the Canadian Registry of VTE. Blood 1994;83:1251-1257. 16. Stein PD, Kayali F, Olson RE. Incidence of venous thromboembolism in infants and children: data from the National Hospital Discharge Survey. J Pediatr 2004;145:563-565. 17. van Ommen CH, Heijboer H, Buller HR, Hirasing RA, Heijmans HS, Peters M. Venous thromboembolism in childhood: a prospective two-year registry in The Netherlands. J Pediatr 2001;139:676-681. 18. McIntyre KM, Sasahara AA. The hemodynamic response to pulmonary embolism in patients without prior cardiopulmonary disease. Am J Cardiol 1971;28:288-294. 19. Smulders YM. Pathophysiology and treatment of haemodynamic instability in acute pulmonary embolism: the pivotal role of pulmonary vasoconstriction. Cardiovasc Res 2000;48:23-33. 20. Lankhaar JW, Westerhof N, Faes T J C, Marques K M J, Marcus JT, Postmus PE, Vonk-Noordegraaf A. Quantification of right ventricular afterload in patients with and without pulmonary hypertension. Am J Physiol Heart Circ Physiol 2006;291:H1731- H1737. 21. Marcus JT, Gan CT, Zwanenburg JJ, Boonstra A, Allaart CP, Gotte MJ, Vonk-Noordegraaf A. Interventricular mechanical asynchrony in pulmonary arterial hypertension: left-to-right delay in peak shortening is related to right ventricular overload and left ventricular underfilling. J Am Coll Cardiol 2008;51:750-757. 22. Mauritz GJ, Marcus JT, Westerhof N, Postmus PE, Vonk-Noordegraaf A. Prolonged right ventricular post-systolic isovolumic period in pulmonary arterial hypertension is not a reflection of diastolic dysfunction. Heart 2011;97:473-478. 23. Begieneman MP, van de Goot FR, van der Bilt IA, Vonk Noordegraaf A, Spreeuwenberg MD, Paulus WJ, van Hinsbergh VW, Visser FC, Niessen HW. Pulmonary embolism causes endomyocarditis in the human heart. Heart 2008;94:450-456. 24. Lankeit M, Jimenez D, Kostrubiec M, Dellas C, Hasenfuss G, Pruszczyk P, Konstantinides S. Predictive value of the high-sensitivity troponin T assay and the simplified Pulmonary Embolism Severity Index in hemodynamically stable patients with acute pulmonary embolism: a prospective validation study. Circulation 2011;124:2716-2724. 25. Lankeit M, Kempf T, Dellas C, Cuny M, Tapken H, Peter T, Olschewski M, Konstantinides S, Wollert KC. Growth differentiation factor-15 for prognostic assessment of patients with acute pulmonary embolism. Am J Respir Crit Care Med 2008;177:1018-1025. 26. Burrowes KS, Clark AR, Tawhai MH. Blood flow redistribution and ventilationperfusion mismatch during embolic pulmonary arterial occlusion. Pulm Circ 2011;1:365-376. 27. Konstantinides S, Geibel A, Kasper W, Olschewski M, Blumel L, Just H. Patent foramen ovale is an important predictor of adverse outcome in patients with major pulmonary embolism. Circulation 1998;97:1946-1951. 28. Harjola VP, Mebazaa A, Celutkiene J, Bettex D, Bueno H, Chioncel O, Crespo-Leiro MG, Falk V, Filippatos G, Gibbs S, Leite- Moreira A, Lassus J, Masip J, Mueller C, Mullens W, Naeije R, Nordegraaf AV, Parissis J, Riley JP, Ristic A, Rosano G, Rudiger A, Ruschitzka F, Seferovic P, Sztrymf B, Vieillard-Baron A, Yilmaz MB, Konstantinides S. Contemporary management of acute right ventricular failure: a statement from the Heart Failure Association and the Working Group on Pulmonary Circulation and Right Ventricular Function of the European Society of Cardiology. EurJ Heart Fail 2016;18:226-241. 29. Rogers MA, Levine DA, Blumberg N, Flanders SA, Chopra V, Langa KM. Triggers of hospitalization for venous thromboembolism. Circulation 2012;125:2092-2099. 30. Anderson FA Jr, Spencer FA. Risk factors for venous thromboembolism. Circulation 2003;107:I9-I16. 31. Ku GH, White RH, Chew HK, Harvey DJ, Zhou H, Wun T. Venous thromboembolism in patients with acute leukemia: incidence, risk factors, and effect on survival. Blood 2009;113:3911-3917. 32. Chew HK, Wun T, Harvey D, Zhou H, White RH. Incidence of venous thromboembolism and its effect on survival among patients with common cancers. Arch Intern Med 2006;166:458-464. 33. Timp JF, Braekkan SK, Versteeg HH, Cannegieter SC. Epidemiology of cancerassociated venous thrombosis. Blood 2013;122:1712-1723. 34. Blom JW, Doggen CJ, Osanto S, Rosendaal FR. Malignancies, prothrombotic mutations, and the risk of venous thrombosis. JAMA 2005;293:715-722. 35. Gussoni G, Frasson S, La Regina M, Di Micco P, Monreal M; RIETE Investigators. Three-month mortality rate and clinical predictors in patients with venous thromboembolism and cancer. Findings from the RIETE registry. Thromb Res 2013;131:24-30. 36. Blanco-Molina A, Rota L, Di Micco P, Brenner B, Trujillo-Santos J, Ruiz-Gamietea A, Monreal M; RIETE Investigators. Venous thromboembolism during pregnancy, postpartum or during contraceptive use. Thromb Haemost 2010;103:306-311. 37. Blanco-Molina A, Trujillo-Santos J, Tirado R, Canas I, Riera A, Valdes M, Monreal M; RIETE Investigators. Venous thromboembolism in women using hormonal contraceptives. Findings from the RIETE Registry. Thromb Haemost 2009;101:478- 482. 38. van Hylckama Vlieg A, Middeldorp S. Hormone therapies and venous thromboembolism: where are we now? J Thromb Haemost 2011;9:257-266. 39. Lidegaard Ø, Nielsen LH, Skovlund CW, Skjeldestad FE, Løkkegaard E. Risk of venous thromboembolism from use of oral contraceptives containing different progestogens and oestrogen doses: Danish cohort study, 2001-9. BMJ 2011;343:d6423. 40. de Bastos M, Stegeman BH, Rosendaal FR, Van Hylckama Vlieg A, Helmerhorst FM, Stijnen T, Dekkers OM. Combined oral contraceptives: venous thrombosis. Cochrane Database Syst Rev 2014;3:CD010813. 41. van Vlijmen EF, Wiewel-Verschueren S, Monster TB, Meijer K. Combined oral contraceptives, thrombophilia and the risk of venous thromboembolism: a systematic review and meta-analysis. J Thromb Haemost 2016;14:1393-1403. 42. Tricotel A, Collin C, Zureik M. Impact of the sharp changes in the use of contraception in 2013 on the risk of pulmonary embolism in France. J Thromb Haemost 2015;13:1576-1580. 43. Kemmeren JM, Algra A, Grobbee DE. Third generation oral contraceptives and risk of venous thrombosis: meta-analysis. BMJ 2001;323:131-134. 44. van Hylckama Vlieg A, Helmerhorst FM, Rosendaal FR. The risk of deep venous thrombosis associated with injectable depot- medroxyprogesterone acetate contraceptives or a levonorgestrel intrauterine device. Arterioscler Thromb Vasc Biol 2010;30:2297- 2300. 45. Sweetland S, Beral V, Balkwill A, Liu B, Benson VS, Canonico M, Green J, Reeves GK; Million Women Study Collaborators. Venous thromboembolism risk in relation to use of different types of postmenopausal hormone therapy in a large prospective study. J Thromb Haemost 2012;10:2277-2286. 46. Clayton TC, Gaskin M, Meade TW. Recent respiratory infection and risk of venous thromboembolism: case-control study through a general practice database. IntJ Epidemiol 2011;40:819-827. 47. Smeeth L, Cook C, Thomas S, Hall AJ, Hubbard R, Vallance P. Risk of deep vein thrombosis and pulmonary embolism after acute infection in a community setting. Lancet 2006;367:1075-1079. 48. Khorana AA, Kuderer NM, Culakova E, Lyman GH, Francis CW. Development and validation of a predictive model for chemotherapy-associated thrombosis. Blood 2008;111:4902-4907. 49. Dijk FN, Curtin J, Lord D, Fitzgerald DA. Pulmonary embolism in children. Paediatr Respir Rev 2012;13:112-122. 50. Piazza G, Goldhaber SZ. Venous thromboembolism and atherothrombosis: an integrated approach. Circulation 2010;121:2146- 2150. 51. Steffen LM, Cushman M, Peacock JM, Heckbert SR, Jacobs D R Jr, Rosamond WD, Folsom AR. Metabolic syndrome and risk of venous thromboembolism: longitudinal investigation of thromboembolism etiology. J Thromb Haemost 2009;7:746-751. 52. Severinsen MT, Kristensen SR, Johnsen SP, Dethlefsen C, Tjonneland A, Overvad K. Anthropometry, body fat, and venous thromboembolism: a Danish follow-up study. Circulation 2009;120:1850-1857. 53. Ageno W, Becattini C, Brighton T, Selby R, Kamphuisen PW. Cardiovascular risk factors and venous thromboembolism: a meta- analysis. Circulation 2008;117:93-102. 54. Piazza G, Goldhaber SZ, Lessard DM, Goldberg RJ, Emery C, Spencer FA. Venous thromboembolism in patients with symptomatic atherosclerosis. Thromb Haemost 2011;106:1095-1102. 55. Montecucco F, Mach F. Should we focus on "venous vulnerability" instead of "plaque vulnerability" in symptomatic atherosclerotic patients? Thromb Haemost 2011;106:995-996. 56. Gresele P, Momi S, Migliacci R. Endothelium, venous thromboembolism and ischaemic cardiovascular events. Thromb Haemost 2010;103:56-61. 57. Fox EA, Kahn SR. The relationship between inflammation and venous thrombosis - A systematic review of clinical studies. Thromb Haemost 2005;94:362-365. 58. Wattanakit K, Lutsey PL, Bell EJ, Gornik H, Cushman M, Heckbert SR, Rosamond WD, Folsom AR. Association between cardiovascular disease risk factors and occurrence of venous thromboembolism. A time-dependent analysis. Thromb Haemost 2012;108:508-515. 59. Enga KF, Braekkan SK, Hansen-Krone IJ, le Cessie S, Rosendaal FR, Hansen JB. Cigarette smoking and the risk of venous thromboembolism: the Tromsø Study. J Thromb Haemost 2012;10:2068-2074. 60. Sorensen HT, Horvath-Puho E, Lash TL, Christiansen CF, Pesavento R, Pedersen L, Baron JA, Prandoni P. Heart disease may be a risk factor for pulmonary embolism without peripheral deep venous thrombosis. Circulation 2011;124:1435-1441. 61. Prandoni P, Pesavento R, Sorensen HT, Gennaro N, Dalla Valle F, Minotto I, Perina F, Pengo V, Pagnan A. Prevalence of heart diseases in patients with pulmonary embolism with and without peripheral venous thrombosis: findings from a cross-sectional survey. Eur J Intern Med 2009;20:470-473. 62. Sorensen HT, Horvath-Puho E, Pedersen L, Baron JA, Prandoni P. Venous thromboembolism and subsequent hospitalisation due to acute arterial cardiovascular events: a 20-year cohort study. Lancet 2007;370:1773-1779. 63. PIOPED Investigators. Value of the ventilation/perfusion scan in acute pulmonary embolism. Results of the prospective investigation of pulmonary embolism diagnosis (PIOPED). JAMA 1990; 263:2753. 64. Stein PD, Terrin ML, Hales CA, et al. Clinical, laboratory, roentgenographic, and electrocardiographic findings in patients with acute pulmonary embolism and no pre-existing cardiac or pulmonary disease. Chest 1991; 100:598. 65. Stein PD, Saltzman HA, Weg JG. Clinical characteristics of patients with acute pulmonary embolism. Am J Cardiol 1991; 68:1723. 66. Stein PD, Beemath A, Matta F, et al. Clinical characteristics of patients with acute pulmonary embolism: data from PIOPED II. Am J Med 2007; 120:871. 67. Lucassen W, Geersing GJ, Erkens PM, et al. Clinical decision rules for excluding pulmonary embolism: a meta-analysis. Ann Intern Med 2011; 155:448. 68. Liesching T, O'Brien A. Significance of a syncopal event. Pulmonary embolism. Postgrad Med 2002; 111:19. 69. Castelli R, Tarsia P, Tantardini C, et al. Syncope in patients with pulmonary embolism: comparison between patients with syncope as the presenting symptom of pulmonary embolism and patients with pulmonary embolism without syncope. Vasc Med 2003; 8:257. 70. Coen M, Leuchter I, Sussetto M, et al. Progressive Dysphonia: Ortner Syndrome. Am J Med 2018; 131:e494. 71. Blanc JJ, L'Her C, Touiza A, et al. Prospective evaluation and outcome of patients admitted for syncope over a 1 year period. Eur Heart J 2002; 23:815. 72. Soteriades ES, Evans JC, Larson MG, et al. Incidence and prognosis of syncope. N Engl J Med 2002; 347:878. 73. Vanbrabant P, Van Ouytsel V, Knockaert D, Gillet JB. Diagnostic yield of syncope investigation (initiated) in the emergency department: a pilot study. Acta Clin Belg 2011; 66:110. 74. Saravi M, Ahmadi Ahangar A, Hojati MM, et al. Etiology of syncope in hospitalized patients. Caspian J Intern Med 2015; 6:233. 75. Keller K, Beule J, Balzer JO, Dippold W. Syncope and collapse in acute pulmonary embolism. Am J Emerg Med 2016; 34:1251. 76. Prandoni P, Lensing AW, Prins MH, et al. Prevalence of Pulmonary Embolism among Patients Hospitalized for Syncope. N Engl J Med 2016; 375:1524. 77. Verma AA, Masoom H, Rawal S, et al. Pulmonary Embolism and Deep Venous Thrombosis in Patients Hospitalized With Syncope: A Multicenter Cross-sectional Study in Toronto, Ontario, Canada. JAMA Intern Med 2017; 177:1046. 78. Costantino G, Ruwald MH, Quinn J, et al. Prevalence of Pulmonary Embolism in Patients With Syncope. JAMA Intern Med 2018; 178:356. 79. Badertscher P, du Fay de Lavallaz J, Hammerer-Lercher A, et al. Prevalence of Pulmonary Embolism in Patients With Syncope. J Am Coll Cardiol 2019; 74:744.
Информация
г. Бишкек Ул. Тоголок Молдо, 3, 720040,
Национальный Центр Кардиологии и Терапии
Тел: 996 312 62 56 79
E-mail: sooronbaev@inbox.ru
Главный внештатный пульмонолог МЗ КР Д.м.н.,
профессор Сооронбаев Т.М.
Венозная тромбоэмболия (ВТЭ);
Тромбоз глубоких вен (ТГВ);
D-димер;
Свертывающая система крови;
Тромб;
Легочное артериальное давление;
Правые отделы сердца;
Гипотония;
Десатурация;
Компьютерная томография (КТ) с контрастом;
УЗДС (ультразвуковое дуплексное сканирование);
Эхокардиография;
Факторы риска;
Реперфузия;
Антикоагулянтная терапия;
Тромболитическая терапия;
Эмболэктомия.
|
АВК
|
Антагонист витамина К
|
|
ИТТЭЛА
|
Индекс тяжести тромбоэмболии легочной артерии
|
|
КТ
|
Компьютерной томографии
|
|
МРА
|
Магнитно-резонансная ангиография
|
|
МЕ
|
Международные единицы
|
|
НМГ
|
Низкомолекулярный гепарин
|
|
НФГ
|
Нефракционированный гепарин
|
|
ПЖ
|
Правый желудочек
|
|
ТГВ
|
Тромбоз глубоких вен
|
|
ТЭЛА
|
Тромбоэмболия легочной артерии
|
|
УЗДГ
|
УЗИ вен нижних конечностей
|
|
УЗИ
|
Ультразвуковое исследование
|
|
уИТТЭЛА
|
Упрощенный индекс тяжести тромбоэмболии легочной артерии
|
|
ЭхоКГ
|
Эхокардиография
|
|
ртАП
|
Рекомбинантный тканевый активатор плазминогена
|
|
МНО
|
Международное нормированное отношение
|
|
ОПА
|
Оральный прямой антикоагулянт
|
|
АЧТВ
|
Активированное частичное тромбопластиновое время
|
|
КТ-АПГ
|
Компьютерная томография-ангиопульмонография
|
|
ВТЭ
|
Венозная тромбоэмболия
|
|
Д-димер
|
Д-димер — это белковый фрагмент, образующийся при растворении кровяного сгустка, который возникает при свертывании крови. Этот маркер используется для оценки активности системы свертывания крови и может быть полезен при диагностике тромбоэмболии, инфаркта миокарда и других состояний, связанных с повышенным образованием тромбов
|
|
МНО
|
Международное нормализованное отношение: система, созданная Всемирной организацией здравоохранения (ВОЗ) и Международным комитетом по тромбозам и гемостазу для отчетности о результатах тестов на свертываемость крови. Сокращенное МНО. В системе МНО все результаты стандартизируются. Например, человек, принимающий антикоагулянт варфарин, должен регулярно сдавать анализ крови для
измерения МНО. |
|
Эмболэктомия
|
Эмболэктомия — это хирургическая процедура, направленная на удаление эмбола из сосуда. Эмбол — это образование, которое закупоривает сосуд и может привести к серьезным последствиям, таким как инфаркт или инсульт. Эмболэктомия часто проводится в случаях тромбоэмболии легочной артерии, и ее целью является восстановление нормального кровотока и предотвращение дальнейших осложнений
|
|
Высокопоточная кислородная терапия
|
Высокопоточная кислородная терапия — это неинвазивный метод респираторной поддержки, при котором пациенту подается высокий поток теплого, увлажненного и обогащенного кислородом воздуха через носовые канюли или маску. Он обеспечивает подачу кислорода со скоростью потока, превышающей традиционную кислородную терапию, до 100 литров в минуту, и может обеспечить концентрацию кислорода, близкую к 100 %. Такая терапия помогает улучшить оксигенацию, уменьшить работу дыхания и повысить комфорт для пациентов с дыхательной недостаточностью или дистрессом.
|
Приложение A1.
Для обновления и своевременного пересмотра клинического руководства по диагностике и лечению ТЭЛА для всех уровней оказания медицинской помощи была создана мультидисциплинарная рабочая группа (МДРГ) из специалистов разного профиля.
Ответственные исполнители за клиническое содержание руководства по разделам
|
Ибраева Н.С.
|
Начальник УОМП и ЛП МЗКР (координатор)
|
|
Сооронбаев Т.М.
|
председатель рабочей группы, Главный пульмонолог МЗ, директор Национального центра кардиологии и терапии имени академика М.Миррахимова, д.м.н., профессор
|
|
Байсекеев Т.А.
|
к.м.н., заведующий отделения сосудистой хирургии НГМЗКР
|
|
Джузумалиева Г.С.
|
к.м.н., главный реаниматолог МЗКР
|
|
Кемелова Ж.К.
|
заведующая отделением пульмонологии и аллергологии с БИП НЦКиТ
|
|
Калбекова Ч.К.
|
заведующая отделением УКИР2 НЦКиТ
|
|
Мадемилов М. Ж.
|
врач пульмонолог НЦКиТ.
|
Ответственные исполнители осуществляли систематизацию и поиск ключевых рекомендаций из выбранных международных клинических руководств путем адаптации, предоставили обобщенные данные по ссылкам для формирования клинического содержания обновленного руководства.
В эту группу вошли представители специальностей, наиболее часто встречающие в повседневной практике оказанием медицинской помощи пациентам с ТЭЛА. Они были приглашены из ведущих организаций здравоохранения Кыргызской Республики. Приглашение медицинских консультантов и пациентов в состав разработчиков позволило обсудить применимость отдельных рекомендаций в реальной медицинской практике, а также вопросы применимости руководства в организациях здравоохранения амбулаторного и стационарного уровней Кыргызской Республики.
Протоколы согласительных заседаний мультидисциплинарной рабочей группы по разработке клинического руководства велись в соответствии с установленным порядком, ответственный за ведение протоколов – Таалайбекова А.Т. (секретарь КТО).
Все члены группы подписали декларацию о конфликте интересов.
Процесс утверждения клинического руководства 1 апреля 2024 года на совещании МДРГ принято решение обновить «матричное» руководство с полным описанием лучшей международной практики для повышения информированности специалистов, и дополнить национальное клиническое руководство краткими клиническими протоколами (алгоритмами или блок-схемами) в зависимости от уровней оказания медицинской специализированной помощи. Представить данные документы в удобном для использования формате, по мере возможности клинические протоколы упростить для практического использования, отразить клинические рекомендации для улучшения оснащения организаций здравоохранения – разработать стандарты, а также для мониторинга процесса внедрения разработанных документов разработать индикаторы для оценки выполнения стандартов (индикаторы ресурсного обеспечения, процесса и результативности) и для последующего мониторинга и оценки оказываемой помощи на местах для улучшения качества оказываемой медицинской помощи.
|
Миррахимов Э.М.
|
Заведующий кафедрой факультетской терапии КГМА имени И.К. Ахунбаева, д.м.н., профессор
|
|
Маасаидова А.Ю.
|
Заведующая отделением пульмонологии НГ МЗ КР
|
|
Омурова Ж.Н.
|
Заведующая кафедрой семейной медицины КГМИПК
|
|
Thomas Hess
|
Специалист по респираторной медицине, Швейцария
|
|
Джакубекова А.У.
|
Консультант МЗ КР по вопросам доказательной медицины и
разработки клинических руководств и протоколов. |
Методологами была проведена оценка методологического качества клинического руководства по логическому изложению, отражению наилучшей клинической практики в рекомендациях и применимости в клинической практике на местах согласно инструменту AGREE II.
МДРГ было принято решение о создании клинического руководства по диагностике и лечению ТЭЛА путем адаптирования для всех уровней здравоохранения Кыргызской Республики уже существующих международных руководств высокого методологического качества, основанных на принципах доказательной медицины.
Были установлены языковые ограничения, так как рабочая группа имела возможность изучать источники литературы только на английском и русском языках.
Найденные электронные базы данных по клиническим руководствам ипрактическим рекомендациям
|
Страна и название ресурса
|
Интернет-адрес
|
|
Международная ассоциация
|
|
|
International Society on Thrombosis and Haemostasis (ISTH): Published guidance
|
|
|
Соединенные Штаты Америки
|
|
|
Treatment of deep vein thrombosis and pulmonary embolism
|
|
|
American College of Chest Physicians (CHEST): Guideline and expert panel report on antithrombotic therapy for
VTE disease, second update (2021) |
|
|
Expert Consensus Panel: Results on direct oral anticoagulants in obese patients with venous thromboembolism
(2023) |
|
|
Канада
|
|
|
Thrombosis Canada: Clinical guides
|
|
|
Великобритания
|
|
|
National Institute for Health and Care Excellence (NICE): Clinical guideline on venous thromboembolic diseases – Diagnosis, management, and thrombophilia testing (2020, updated
2023) |
|
|
NICE: Interventional procedures guidance on percutaneous
thrombectomy for intermediate-risk or high-risk pulmonary embolism (2023) |
|
|
Европа
|
|
|
European Society of Cardiology (ESC)/European Respiratory Society (ERS): Guidelines for the diagnosis and management of acute pulmonary
embolism (2019) |
|
|
European Society of Medical Oncology (ESMO): Clinical practice guideline on
venous thromboembolism in cancer patients (2023) |
|
|
По лекарственным средствам
|
|
|
The Global Drug Database
|
|
|
Drugs.com
|
|
|
Medscape
|
|
В итоге поиска было найдено 14 клинических руководств.
Найденные клинич9. Организация медицинской помощи больным с острой ТЭЛА В случае обращения больных с острой ТЭЛА в любые медицинские учреждения, должна быть оказана медицинская помощь. Госпитализация и оказание квалифицированной медицинской помощи должно проводиться во всех ургентных и интенсивных отделениях.еские руководства были оценены МДРГ при помощи инструмента AGREE GRS.
|
|
Название руководства
|
Качество
|
Новизна
|
Применимость
|
Варианты
действий |
|
1
|
European Society of Cardiology
|
+++
|
+++
|
+++
|
Рекомендации по
|
|
|
(ESC)/European Respiratory
|
|
|
|
диагностике и
|
|
|
Society (ERS): Guidelines for the
|
|
|
|
лечению ТЭЛА,
|
|
|
diagnosis and management of acute
|
|
|
|
доступен на
|
|
|
pulmonary embolism (2019)
|
|
|
|
русском языке
|
|
2
|
American College of Chest Physicians (CHEST): Guideline and expert panel report on antithrombotic therapy for VTE disease, second update (2021)
|
+++
|
+++
|
+++
|
Рекомендации по диагностике и лечению ТЭЛА, доступен на
русском языке |
|
3
|
National Institute for Health and Care Excellence (NICE): Clinical guideline on venous thromboembolic diseases – Diagnosis, management, and thrombophilia testing (2020, updated 2023)
|
+++
|
+++
|
+++
|
Рекомендации по диагностике и лечению ТЭЛА, доступен на русском языке
|
Предпочтение для разработки руководства основывались на European Society of Cardiology (ESC)/European Respiratory Society (ERS), American College of Chest Physicians (CHEST), National Institute for Health and Care Excellence (NICE). По черновому варианту были получены комментарии и замечания специалистов. Обновление данного руководства предполагается 2027г и/или по мере появления новых данных.
Так как в найденных клинических руководствах МДРГ были отражены необходимые рекомендации по диагностике и лечению ТЭЛА, то дополнительный поиск медицинских публикаций по результатам мета анализов, систематических обзоров, РКИ и т.д. в международных базах не проводился.
Все ключевые рекомендации в клиническом руководстве выделены в рамки-боксы. Ключевые рекомендации с представлением их уровней доказательности и убедительности были адаптированы по шкале SIGN-50 на 4 уровня A, B, C, D.
|
А
|
Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты
|
|
В
|
Высококачественный (++) систематический обзор когортны или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки
|
|
С
|
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+)
|
|
D
|
Описание серии случаев или неконтролируемое исследование, или мнение экспертов
|
Данное национальное клиническое руководство дополнено алгоритмами, памяткой для пациентов, стандартами и индикаторами для мониторинга и аудита внедрения клинического руководства по диагностике и лечению ТЭЛА.
Задачи:
-
Внедрение в практику единых научно-обоснованных клинико-лабораторных критериев диагностики ТЭЛА на всех уровнях организаций здравоохранения КР.
-
Внедрение в практику научно-обоснованных принципов и подходов в лечении и ведении ТЭЛА на всех уровнях здравоохранения КР.
-
Применение единого алгоритма действий на всех уровнях оказания медицинской помощи пациентам с ТЭЛА:
-
своевременной диагностики заболевания;
-
правильного квалифицированного ведения и лечения ТЭЛА
-
-
Снижение риска развития и прогрессирования осложнений у пациентов с ТЭЛА
Клиническое руководство разработано для медицинских работников всех уровней ОЗ КР, принимающих участие в ведении, диагностике и лечении пациентов с ТЭЛА.
Ожидаемые результаты применения клинического руководства:
-
Улучшение качества диагностики будет способствовать своевременному выявлению и лечению ТЭЛА;
-
Рациональное лечение ТЭЛА будет способствовать сокращению осложнений и летальности, с последующей ее элиминацией.
Что такое тромбоэмболия легочных артерий (ТЭЛА)?
ТЭЛА — это закупорка одного или нескольких кровеносных сосудов, снабжающих кровью легкие. Чаще всего эти закупорки вызваны тромбами, которые образуются где-то еще и затем попадают в легкие. В редких случаях закупорка также может быть вызвана пузырьками воздуха, крошечными шариками жира или кусочками опухоли, которые попадают в легкие.
Большинство тромбов в легких фактически образуются в ногах или области таза, а затем попадают в легкие. Когда в глубоких венах ног образуется тромб, это называется «тромбоз глубоких вен» («ТГВ»). ТГВ может вызвать отек, боль, жар и покраснение в ноге. Если у вас есть какие-либо из этих симптомов, важно немедленно обратиться к врачу. Они могут провести анализы, чтобы выяснить, есть ли у вас тромб и где он находится. Существуют методы лечения, которые могут помочь предотвратить увеличение тромба и его попадание в легкие.
Каковы симптомы ТЭЛА? Общие симптомы включают в себя:
-
Одышка или проблемы с дыханием.
-
Острая, режущая боль в груди при вдохе или напряжении.
-
Кашель или кашель с кровью.
-
Учащенное сердцебиение.
Если у вас возникнут какие-либо из этих симптомов, особенно если они происходят в течение короткого периода времени (часы или дни) или быстро ухудшаются, вызовите скорую помощь. В больнице врачи могут провести анализы, чтобы выяснить, есть ли у вас тромб. Тромбы в легких могут привести к смерти. Вот почему важно действовать быстро и выяснить, есть ли тромб.
-
Анализ крови на D-димер. D-димер – это вещество в крови. Количество D-димера часто увеличивается у людей с тромбом в легких. Этот анализ крови часто проводится вместе с другими анализами.
-
КТ-ангиография легких («КТ») – КТ- ангиография легких представляет собой особый вид рентгеновского исследования. Во время этого теста в одну из вен вводится контраст. Контраст виден на рентгеновских снимках и может показать, заблокированы ли какие-либо кровеносные сосуды.
Как лечат ТЭЛА?
-
Если у вас образовался тромб, ваш врач назначит антикоагулянт, чтобы снизить риск образования новых тромбов в будущем. Вам нужно будет принимать лекарство не менее 3 месяцев (а иногда и дольше). Некоторым людям сначала вводят укол гепарина. Вы можете делать этот укол в течение нескольких дней или дольше, если по какой-то причине вы не можете принимать таблетки.
-
Лекарства не растворяют существующие тромбы, но предотвращают их увеличение. Они также помогают предотвратить образование новых тромбов. Важно принимать лекарство в течение нескольких месяцев, поскольку оно дает организму время растворить старый тромб. Это также важно, потому что люди, у которых есть тромб, подвергаются риску образования нового тромба, особенно в первые несколько месяцев.
-
Для предотвращения и лечения тромбов используются различные пероральные препараты (таблетки). К ним относятся апиксабан, дабигатран, эдоксабан, ривароксабан и варфарин. Каждое лекарство отличается дозой, частотой приема, стоимостью и тем, как на нее может повлиять ваша диета или другие лекарства. Ваш врач может поговорить с вами о ваших возможностях и предпочтениях.
Если ваш врач прописывает 1 из этих лекарств:
-
Принимайте точно так, как советует ваш врач. Если вы забыли или пропустили дозу, позвоните своему врачу, чтобы узнать, что делать. Когда вы начнете принимать лекарство, вам необходимо будет сдать анализ крови. Если вы принимаете варфарин, вам потребуется регулярно сдавать анализы крови, чтобы проверить свертываемость крови. Это важно, чтобы убедиться, что вы получили правильную дозу варфарина.
-
Следуйте инструкциям своего врача относительно диеты и лекарств. В зависимости от того, какое лекарство вы принимаете, вам, возможно, придется уделять особое внимание тому, что вы едите. Кроме того, некоторые другие лекарства могут влиять на действие этих лекарств.
-
Следите за признаками кровотечения. Аномальное кровотечение представляет собой риск при применении любого лекарства, используемого для предотвращения и лечения тромбов. Это потому, что, хотя эти лекарства помогают предотвратить образование опасных тромбов, они также затрудняют контроль кровотечения после травмы. Постарайтесь избежать травм и сразу же сообщите своему врачу, если у вас появятся признаки кровотечения.
Люди, которые не могут принимать лекарства для предотвращения и лечения тромбов или не получают достаточной пользы от лекарств, могут получить другое лечение. Это называется «фильтр нижней полой вены» («КАВА фильтр»). Нижняя полая вена — это крупная вена, по которой кровь от ног и нижней половины тела возвращается к сердцу. кава- фильтры проходят внутри нижней полой вены. Они фильтруют и улавливают любые большие сгустки, образующиеся под местом расположения фильтра. Ваш врач может предложить это, если:
-
Вы не можете безопасно принимать лекарства от тромбов.
-
У вас образуются тромбы даже во время приема лекарств от тромбов.
-
У вас возникла опасная проблема с кровотечением во время приема лекарства от тромбов.
-
Ваши легкие и сердце могут не справиться с еще одной ТЭЛА.
В некоторых случаях сильный тромб может вызвать низкое кровяное давление и даже шок. (Шок – это когда кровяное давление падает слишком низко, и к органам и тканям организма поступает недостаточно крови.) Если это произойдет, врачи могут дать лекарство для растворения тромба. Иногда его называют лекарством, разрушающим тромбы, и его вводят через катетер (небольшую трубку, вставленную в вену). В некоторых случаях врачи проводят операцию по удалению тромба.
Могу ли я сделать что-нибудь самостоятельно, чтобы предотвратить образование тромбов?
Например, люди, которые путешествуют на длительных рейсах на самолетах, подвергаются повышенному риску образования тромбов. Вот некоторые вещи, которые вы можете сделать, чтобы предотвратить образование тромба во время длительного перелета:
-
Вставайте и ходите хотя бы раз в час.
-
Не курите непосредственно перед поездкой.
-
Носите свободную, удобную одежду.
-
Меняйте положение сидя и часто двигайте ногами и ступнями.
-
Носите компрессионные чулки до колена.
-
Избегайте употребления алкоголя и лекарств, вызывающих сонливость, поскольку они могут ухудшить вашу способность передвигаться.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.