Тромбоэмболические осложнения в акушерстве
 Версия: Клинические протоколы МЗ РК - 2022 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2022 (Казахстан)
Акушерская эмболия (O88), Венозные осложнения в послеродовом периоде (O87), Венозные осложнения во время беременности (O22)
Акушерство и гинекология
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «13» января 2023 года
Протокол №177
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «13» января 2023 года
Протокол №177
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
ТРОМБОЭМБОЛИЧЕСКИЕ ОСЛОЖНЕНИЯ В АКУШЕРСТВЕ
Код(ы) МКБ-10:

Категория пациентов: беременные, роженицы, родильницы.
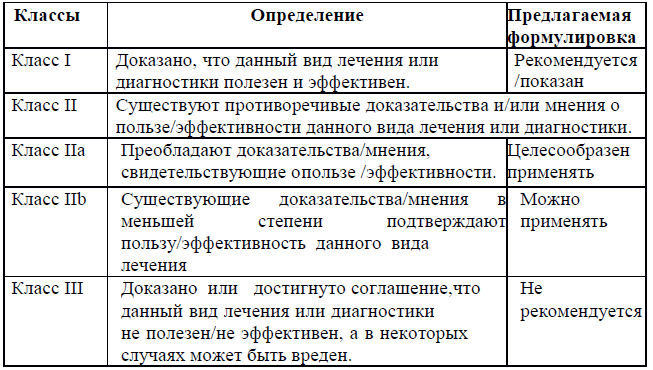
Шкала уровня доказательности:
Классы рекомендаций
Венозные тромбоэмболические осложнения (ВТЭО) – собирательное понятие, объединяющее тромбоз подкожных и глубоких вен и тромбоэмболию легочных артерий.
Тромбоз подкожных вен (ТПВ) – наличие тромба в поверхностной вене, которое обычно сопровождается клинически определяемым воспалением.
Тромбоз глубоких вен (ТГВ) – наличие тромба в глубокой вене, который может вызвать ее окклюзию.
Тромбоэмболия легочных артерий (ТЭЛА) — окклюзия ствола или ветвей легочной артерии частичками тромба, сформировавшимися в венах большого круга кровообращения или правых камерах сердца и занесенными в легочную артерию с током крови.
ВВОДНАЯ ЧАСТЬ:
Код(ы) МКБ-10:

Дата разработки/пересмотра протокола: 2015 год (пересмотр 2022 год).
Пользователи протокола: врачи скорой помощи, врачи общей практики, акушер-гинекологи, анестезиологи-реаниматологи, терапевты, кардиологи, интервенционные кардиологи, ангиохирурги, кардиохирурги, гематологи
Категория пациентов: беременные, роженицы, родильницы.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты, которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С |
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+).
Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию.
|
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
Классы рекомендаций
Классификация
Классификация тромбоза вен нижних конечностей [2]:
Тип I
Тромбоз дистальных отделов большой или малой подкожных вен либо их притоков. Тромботический процесс локализуется дистальнее коленного сустава при поражении большой подкожной вены и ниже сафено-поплитеального соустья при поражении малой подкожной вены. Угроза эмболии легочной артерии отсутствует. В дальнейшем тромбофлебит либо стихает, либо переходит в один из следующих типов.
Тип II
Тромбоз распространяется до сафено-феморального или сафено-поплитеального соустья, не переходя на бедренную/подколенную вену. Непосредственной угрозы эмболии легочного артериального русла еще нет, но она становится реальной в ближайшее время при проксимальном распространении тромбоза.
Тип III
Тромбоз, через устье подкожной вены, переходит на глубокую венозную систему. Верхушка такого тромба, как правило, носит неокклюзивный характер и флотирует (плавает) в кровотоке бедренной или подколенной вены. Тромб фиксирован к венозной стенке лишь в проксимальном отделе подкожной вены. Угроза легочной эмболии, в том числе и фатальной, весьма велика. В последующем подобный флотирующий тромб либо превращается в эмбол, либо становится пристеночным или окклюзивным тромбом магистральной глубокой вены. Дальнейшее распространение тромбоза по глубокой венозной системе в проксимальном и дистальном направлениях ведет к развитию протяженной окклюзии бедренно-подвздошного сегмента.
Тип V
Классификация по характеру проксимальной части тромба:
Тип IV
Тромбоз не распространяется на приустьевые отделы, но через несостоятельные перфорантные вены голени или бедра переходит на глубокую венозную систему. Наличие или отсутствие угрозы легочной эмболии у пациентов этой группы зависит в первую очередь от характера тромба (флотирующий, пристеночный или окклюзивный) в глубокой венозной магистрали.
Тип V
Любой из перечисленных вариантов тромбофлебита сочетается с изолированным симультанным тромбозом глубокой венозной системы как пораженной, так и контралатеральной конечности.
Классификация по характеру проксимальной части тромба:
Неэмболоопасные:
окклюзивный – тромботические массы полностью заполняют просвет вены;
пристеночный - верхушка тромба прикреплена к стенке сосуда, распространяется в проксимальном направлении, не перекрывая полностью просвет вены.
Эмболоопасные:
флотирующий – свободно расположенная в кровотоке проксимальная часть тромба, фиксированная лишь своим основанием. Эта форма тромбоза может вызвать ТЭЛА.
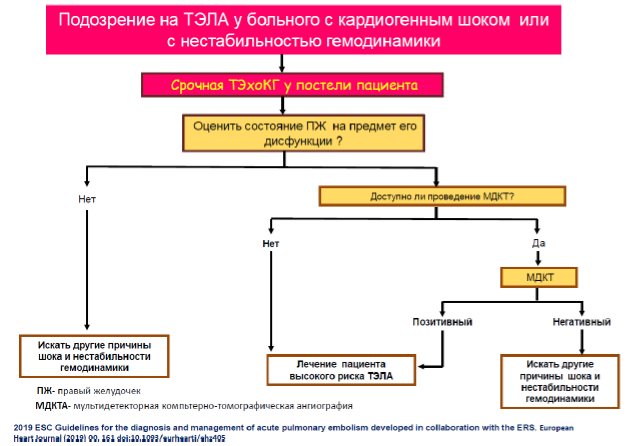
Классификация ТЭЛА согласно рекомендации Европейского общества кардиологов 2019 года
Диагностическая классификация при подозрении на ТЭЛА.
высокого риска;
низкого риска.
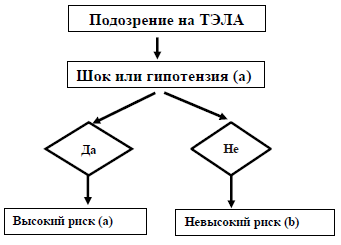

Рисунок 1. Диагностическая классификация при подозрении на ТЭЛА.
Примечание:
a – определяется как снижение уровня АД ниже 90 мм рт.ст. или падение на ≥40 мм рт.ст. в течение >15 минут при отсутствии новой аритмии, гиповолемии или сепсиса
b – на основании данных ожидаемой ТЭЛА-связанной госпитальной смертности или 30-дневной смертности.
Таблица 1. Критерии шока или гемодинамической нестабильности для верификации ТЭЛА высокого риска (присутствует один из следующих симптомов по время поступления больного).
В основе клинической классификации степени тяжести острой ТЭЛА лежит ранняя прогнозируемая госпитальная смертность или смертность в течение 30 дней в результате основного заболевания.
Таблица 2. Классификация больных с острой ТЭЛА, основанная на риске ранней смертности
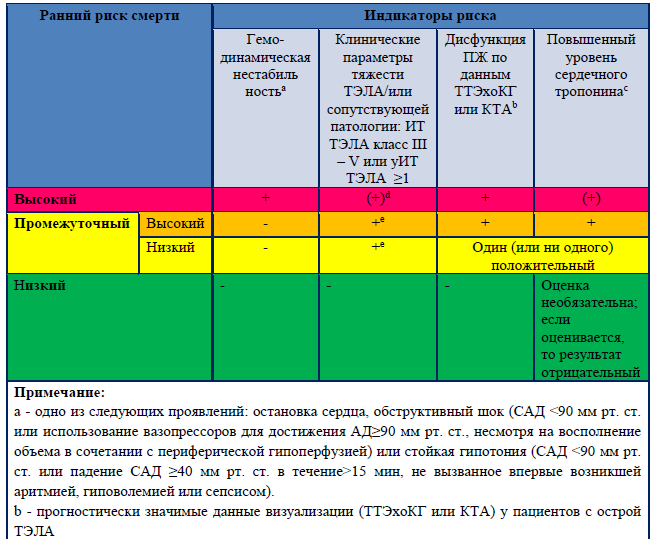

Таблица 1. Критерии шока или гемодинамической нестабильности для верификации ТЭЛА высокого риска (присутствует один из следующих симптомов по время поступления больного).
| Остановка сердечной деятельности | Клиника обструктивного шока | Стойкая гипотензия |
| Потребность в сердечно-легочной реанимации | САД <90 мм рт. ст. или потребность в вазопрессорах для достижения АД ≥90 мм рт.ст. и гипоперфузия жизненно важных органов (измененный психический статус; холодная и липкая кожа; олигурия /анурия; повышенный уровень лактата в сыворотке) | Систолическое АД <90 мм рт. ст. или падение САД≥40мм.рт.ст., продолжительностью более 15 минут не вызванное аритмией, гиповолемией или сепсисом |
В основе клинической классификации степени тяжести острой ТЭЛА лежит ранняя прогнозируемая госпитальная смертность или смертность в течение 30 дней в результате основного заболевания.
ТЭЛА высокого риска
ТЭЛА промежуточного риска
Промежуточный – высокий риск
Промежуточный – низкий риск
ТЭЛА низкого риска
Таблица 2. Классификация больных с острой ТЭЛА, основанная на риске ранней смертности


Классификация степени тяжести ТЭЛА.
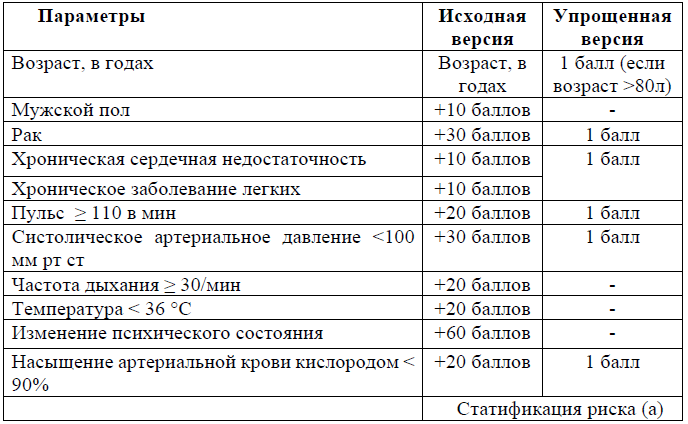
Оценка степени тяжести ТЭЛА – важный компонент для определения прогноза больных и выбора тактики лечения при острой ТЭЛА особенно у больных промежуточного риска для проведения своевременной спасательной ТЛТ и ранней выписки больных низкого риска. Существуют основная и упрощенная версии оценки индекса степени тяжести ТЭЛА (ИТ ТЭЛА) [1,11].
Таблица 3. Исходная и упрощенная версии индекса степени тяжести ТЭЛА [1,11]

Факторы риска:



Примечание: ВТЭ - венозная тромбоэмболия, ФР - факторы риска, СН - сердечная недостаточность, ФП - фибрилляция предсердий, СПИД - синдром приобретённого иммунодефицита.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ [1,2,3,4,5,6]
Диагностические критерии
Жалобы и анамнез
Тромбоз глубоких вен:
Жалобы:
острая распирающая боль в области икроножных мышц;
отек мышц стопы и голени;
цианоз кожи;
переполнение подкожных вен стопы;
повышение локальной температуры;
боли по ходу сосудистого пучка.
Анамнез:
наличие варикозной болезни;
тромбофилия;
привычное невынашивание беременности;
тромбоз глубоких вен и ТЭЛА в анамнезе;
Антифосфолипидный синдром;
применение ВРТ;
применение КОК и ЗГТ;
перенесенные недавно операции (до 1 месяца);
длительное нахождение пациента в постели;
перенесенные вирусные инфекции.
Таблица 4. Шкалы клинической вероятности ТЭЛА
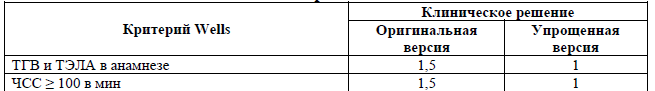
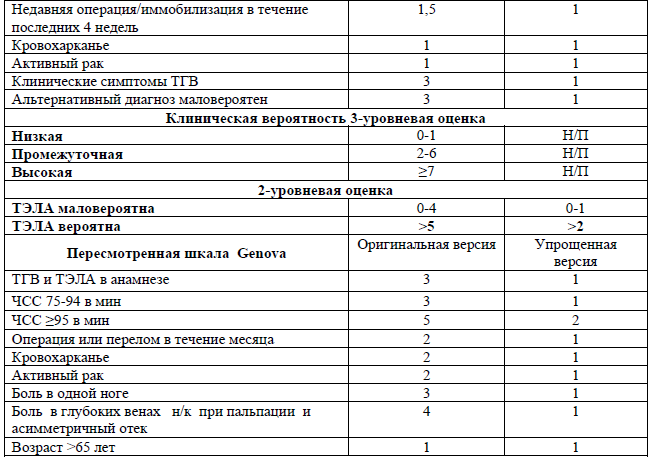

При тромбозе вен нижних конечностей:
Стандартные методы обследования (обычные лабораторные тесты, электрокардиография (ЭКГ), рентгенография органов грудной клетки) полезны только для исключения другой патологии.
Диагностический алгоритм:
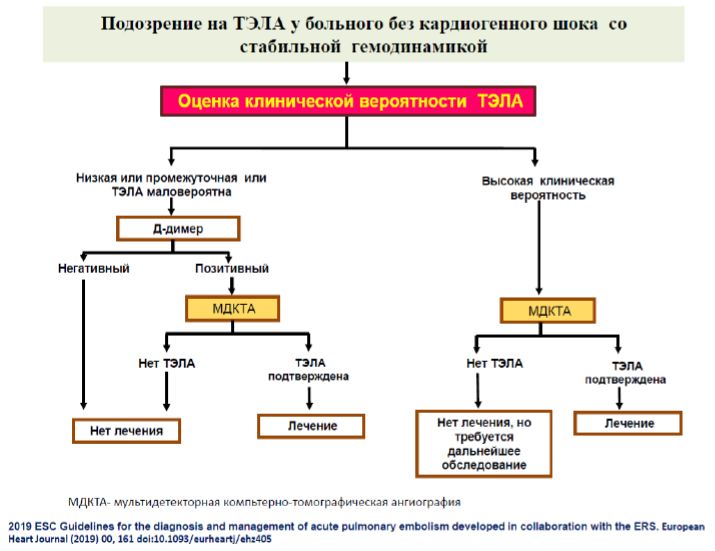
ТЭЛА:
Жалобы:
беспокойство, страх смерти, чувство стеснения в груди, тахикардия, головокружение, холодный пот, бледность
острые боли за грудиной, усиливающиеся при дыхании и кашле; боль в области сердца; боль в плечах, лопатках; чувство холода за грудиной
диспноэ, тахипное (одышка);
синкопе (кратковременная потеря сознания);
кашель; кровохарканье.
В связи с отсутствием специфичности указанных клинических жалоб и объективных данных диагноз ТЭЛА часто пропускается. Поэтому необходимо оценить клиническую вероятность ТЭЛА в случае, когда у пациента с подтвержденным диагнозом ТГВ или болями в одной ноге имеются жалобы на: одышку, тахикардию, кашель, боль в грудной клетке или загрудинную боль, повышение температуры тела, кровохарканье и синкопальное состояние.
Анамнез:
Важно оценить наличие провоцирующих факторов риска (ФР) в анамнезе больного, таких, как большая травма, хирургические вмешательства, эндопротезирование суставов, длительный постельный режим на фоне перелома нижних конечностей, повреждения спинного мозга, ревматоидного артрита, ХОБЛ, ХСН и онкологических заболеваний (лейкозы, рак легкого, опухоли желудочно-кишечного тракта, поджелудочной железы и рак головного мозга), недавно установленные центральные венозные катетеры, а также наличие беременности, особенно, после экстракорпорального оплодотворения, приема пероральных контрацептивов или заместительной гормональной терапии, переливание крови и компонентов крови , варикозной болезни н/к, привычное невынашивание беременности, преждевременной отслойки нормально-расположенной плаценты в анамнезе и диагностированной тромбофилии.
Оценка клинической вероятности:
Несмотря на низкую чувствительность, специфичность симптомов, данных осмотра и инструментальных обследований, требуется проведение обобщенного анализа всех полученных показателей для установления клинического диагноза. При этом использование правил вероятности позволяет классифицировать больных с подозрением на ТЭЛА на категорию большей клинической или предиагностической вероятности ТЭЛА, что, в конечном счете, позволяет правильно установить и подтвердить диагноз. Постдиагностическая (т.е. после компьютерной томографии) вероятность ТЭЛА зависит не только от результатов диагностических исследований, но также и от результатов предварительных предиагностических шкал вероятности, которые являются ключевым шагом в диагностике на протяжении всего алгоритма подтверждения ТЭЛА.
Таблица 4. Шкалы клинической вероятности ТЭЛА



Физикальные исследования
При тромбозе вен нижних конечностей:
Общий осмотр:
увеличение объема всей голени на 3–4 см и более;
цианоз кожных покровов;
переполнение подкожных вен стопы;
повышение локальной температуры.
боли в икроножных мышцах при давлении манжетки сфигмоманометра до 150 мм.рт.ст. (симптом Ловенберга);
болезненность по ходу сосудистого пучка отмечается отеки на стопе, голени, бедре;
усиление боли при тыльном сгибании стопы из-за натяжения икроножных мышц и сдавления вен (симптом Хоманса).
Пальпация:
боли по ходу сосудистого пучка;
болезненность голени при передне-заднем сдавлении (симптом Мозеса).
При ТЭЛА:
Общий осмотр:
цианоз кожных покровов;
установленный диагноз ТГВ;
пациент после остановки сердца и легочно-сердечной реанимации;
контроль ЧСС, АД и уровня сатурации кислорода.
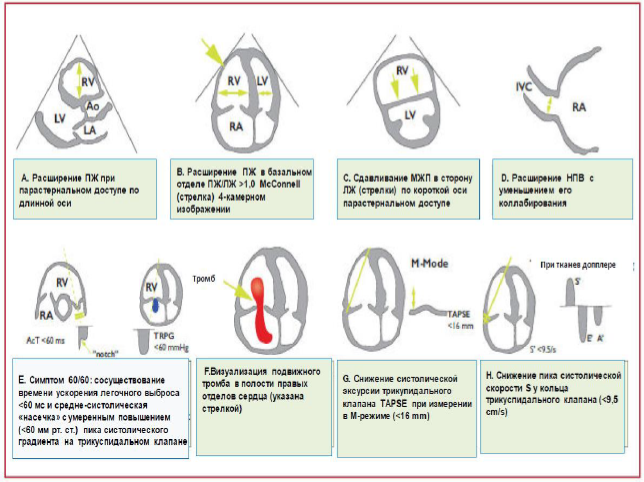
Рисунок 3. Графическое описание параметров ТТЭхоКГ при ТЭЛА
Лабораторная диагностика ТГВ и ТЭЛА:
Общий анализ крови – обратить внимание на возможность анемии, тромбоцитопении как индикаторов желудочно-кишечного кровотечения и для выбора антикоагулянтной терапии
Биохимические анализы – определение общего билирубина и его фракции, АЛТ, АСТ, ЩФ и креатинина для оценки наличия патологии печени и почек и рассчитать СКФ (скорость клубочковой фильтрации) как для выбора антикаогулянтной терапии и для оценки риска кровотечения.
Коагулограмма (фибриноген, протромбиновый индекс, АЧТВ, МНО) – для оценки активности системы гемостаза и адекватности терапии гепарином и АВК.
Кровь на маркеры тройного АФС - антитела к кардиолипину, волчаночный антикоагулянт, антитела к β – глобулину.
Кровь на тромбофилию на мутацию Лейдена, протромбина, на протеин С и S.
Определение D-димера, предпочтительно, с помощью высокочувствительного метода у пациентов с низкой или промежуточной клинической вероятностью или маловероятной ТЭЛА, чтобы уменьшить проведение необоснованных методов визуализации и облучения.
- Измерение Д-димера не рекомендовано для исключения или подтверждения ТЭЛА в период беременности, так как беременность сопровождается прогрессивным увеличением уровня Д-димера, который в силу невысокой специфичности в период беременности не является информативным.
- У больных с низкой клинической вероятностью или малой вероятностью ТЭЛА нормальный показатель D-димера при применении высоко – или умеренно чувствительных методов исключает наличие ТЭЛА. В группе пациентов с низкой или умеренной вероятностью диагностическая ценность Д-димера для исключения ТГВ составляет 99% среди пациентов в возрасте до 50 лет, однако его специфичность при подозрении на ТЭЛА неуклонно уменьшается у больных после 50 лет в результате естественного увеличения уровня Д-димера с возрастом. Поэтому рекомендуется скорректировать пороговый уровень Д-димера с учетом возраста (возраст х 10 мг/Л старше 50 лет), что позволяет увеличить его диагностическую специфичность на 34-46% при сохранении чувствительности более 97%.
- Измерение D-димера не рекомендуется пациентам с высокой клинической вероятностью, так как нормальные результаты являются ненадежными, чтобы исключить наличие ТЭЛА, даже при использовании высокочувствительного метода.
Определение маркеров повреждения миокарда (сердечные тропонины I или T), мозгового натрийуретического пептида (BNP) необходимы как для оценки индекса степени тяжести ТЭЛА, так и для определения ближайшего клинического прогноза.
- Повышение уровня тропонина в плазме выше верхней границы нормы (≥14 пг/мл) в острый период ТЭЛА сопровождается плохим прогнозом независимо от уровня стабильности гемодинамики.
Определение лактата в плазме позволяет оценить дисбаланс между доставкой и потребностью кислорода у больных с тяжелой формой ТЭЛА с гемодинамической нестабильностью. Повышенные уровни лактатов в плазме ≥2ммоль/л предсказывают осложнения, связанные с ТЭЛА, даже у пациентов с нормальными уровнями АД в начальной стадии заболевания.

Рисунок 2. Ультразвуковое исследование вен на уровне паховой складки.
Инструментальные исследования:
Кроме ЭКГ и рентгенографии легких необходимо проведение следующих обследований, с помощью которых можно выявить более специфические данные.
Пульсоксиметрия – для оценки сатурации кислорода и оценки степени дыхательной недостаточности и тяжести ТЭЛА.
Проведение КУЗИ (компрессионное ультразвуковое исследование) вен конечностей (см. рис 2) для диагностики проксимального ТГВ как нижних, так и верхних конечностей (после катетеризации подключичной вены) необходимо у больных, с подозрением на ТЭЛА. Наличие проксимального ТГВ у пациентов с подозрением на ТЭЛА является достаточным основанием для установки диагноза ТЭЛА и начала антикоагулянтной терапии без проведения дальнейших обследований. Поэтому проведение КУЗИ до КТ исследования является диагностическим методом выбора у пациентов с относительными противопоказаниями для КТ, особенно, у больных с почечной недостаточностью, аллергией на контрастное вещество или при беременности.
Наличие проксимального тромбоза вен по данным КУЗИ у больных с подозрением на ТЭЛА подтверждает диагноз ТЭЛА.
При наличии дистального ТГВ необходимо проведение дальнейших обследований для подтверждения ТЭЛА.
Необходимо повторить КУЗИ в течение 10 дней для оценки динамики размера тромба (желательно через каждые 2см по ходу вен).

Рисунок 2. Ультразвуковое исследование вен на уровне паховой складки.
Трансторакальная эхокардиография (при наличии условий):
Эхокардиографические косвенные признаки ТЭЛА представлены на рис. 3. на ЭхоКГ преобладают признаки правожелудочковой недостаточности, в виде увеличения размеров правого желудочка, снижения уровня TAPSE, а также увеличения размера нижней полой вены. Наиболее характерным ЭхоКГ признаком ТЭЛА является наличие синдрома 60/60, когда у пациента одновременно наблюдается укорочение времени легочного выброса, измеренного на выходном тракте ПЖ, <60сек, и уровня пика систолического градиента на трикуспидальном клапане ПЖ<60 мм рт. ст, что нередко сочетается с синдромом Макконнелла (снижение сократимости свободной стенки правого желудочка), однако эти признаки наблюдаются у 12% и 20% больных соответственно. На ЭхоКГ признаком неблагоприятного прогноза ТЭЛА является увеличение размера правого желудочка, соотношения размера ПЖ/ЛЖ ≥1,0 и уменьшение уровня TAPSE <16мм (Рисунок 3а,в). В дополнение к дисфункции ПЖ к эхокардиографическим признакам ранней смертности относятся наличие функционирующего шунта справа налево через открытое овальное отверстие и наличие тромба в правых отделах сердца. Наличие открытого овального отверстия также увеличивает риск развития ишемического инсульта в результате парадоксальной эмболии у пациентов с острой дисфункцией ПЖ при ТЭЛА.

Мультидетекторная компьютерно-томографическая ангиография с высоким разрешением в различных плоскостях и во времени с визуализацией артериальной системы стала методом выбора для диагностики при подозрении на ТЭЛА в клинической практике.
Вентиляционно-перфузионная сцинтиграфия (V/Q сцинтиграфия) является надежным и признанным диагностическим методом диагностики ТЭЛА. V/Q сцинтиграфия является безопасным из-за низкой дозы радиационного облучения, за исключением незначительного количества аллергических реакций. Метод основан на проведении перфузионного сканирования с одновременной вентиляцией легких с помощью различных трейсеров, таких, как: газовый ксенон-133, криптоновый газ – 81, меченый технецием -99m аэрозоли или меченые технеций 99m микрочастицы углерода – Технегаз. Будучи процедурой с низкой радиационной и контрастной нагрузкой, V/Q-сканирование может быть активно использовано в амбулаторных условиях, особенно, у больных с низкой клинической вероятностью и нормальной рентгенографией грудной клетки, у молодых, особенно, у беременных женщин, у пациентов с аллергическим анамнезом на контрастные вещества, при тяжелой почечной недостаточности, а также у пациентов с миеломой болезнью и парапротеиновой анемией.
Легочная ангиография (ЛА):
Легочная ангиография на протяжении десятилетий оставалась «золотым стандартом» для диагностики или исключения ТЭЛА, однако метод редко используется в настоящее время, так как с помощью менее инвазивной КТ-ангиографии можно получить точную информацию. В настоящее время ЛА чаще используется для определения направления катетера во время катетер-направленной терапии при острой ТЭЛА.
Стандартные методы обследования (обычные лабораторные тесты, электрокардиография (ЭКГ), рентгенография органов грудной клетки) полезны только для исключения другой патологии.
Показания для консультации специалистов:
кардиолог с целью верификации диагноза ТЭЛА;
кардиохирург с целью обсуждения тактики хирургического лечения тромбоза правых отделов сердца;
интервенционный кардиолог с целью проведения ангиопульмонографии и необходимости проведения катетернаправленой ТЛТ и неинвазивного удаления тромба из полости правых отделов (при наличии компетенции специалиста);
гематолог для выявления нарушении гемостаза и с целью коррекции тромболитической терапии;
сосудистый хирург с целью диагностики уровня поражения и определения лечения.
Диагностический алгоритм:


Дифференциальный диагноз
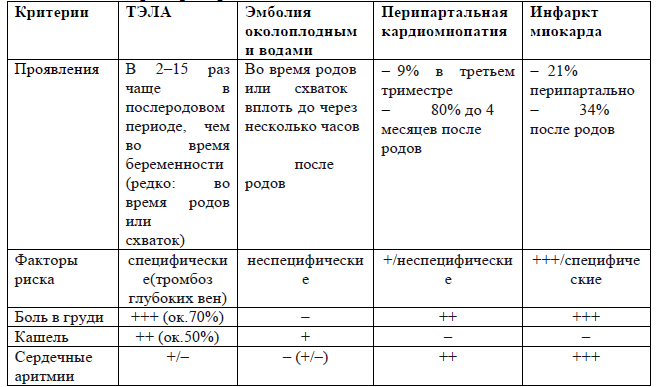
Дифференциальный диагноз
ТГВ:


ТЭЛА
Дифференциальный диагноз и обоснование дополнительных исследований:
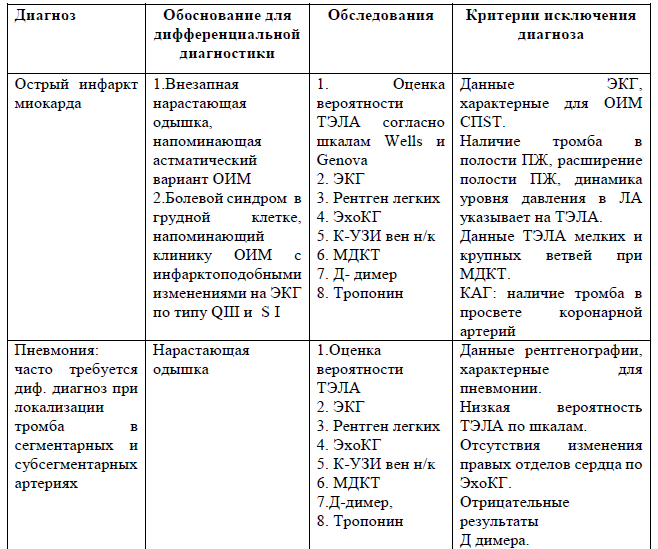
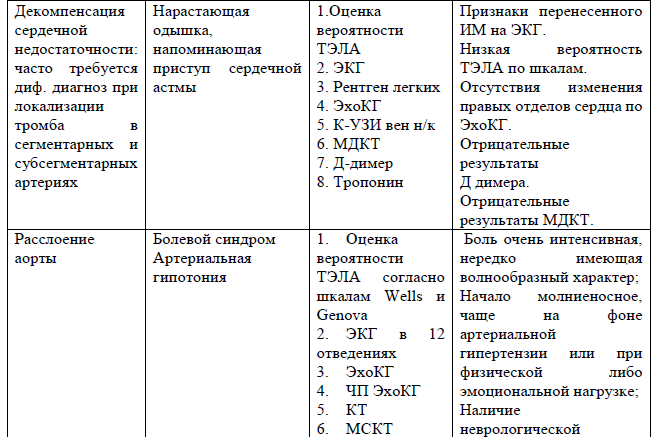
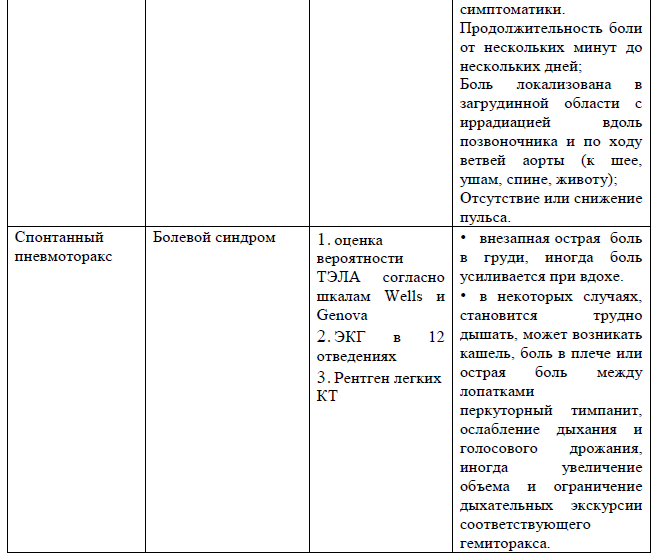
Клинические критерии различия:

Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ: нет.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ:
Карта наблюдения пациента, маршрутизация пациента (схемы, алгоритмы)
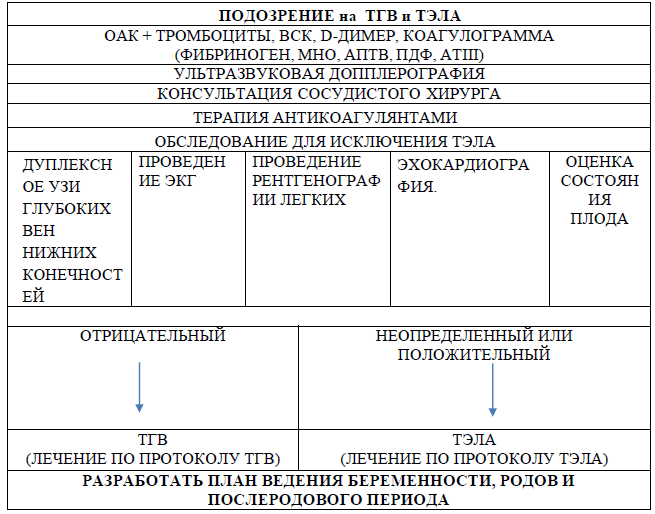
Маршрутизация пациента с подозрением на ТЭЛА во время беременности и в течение 6 недель после родов.
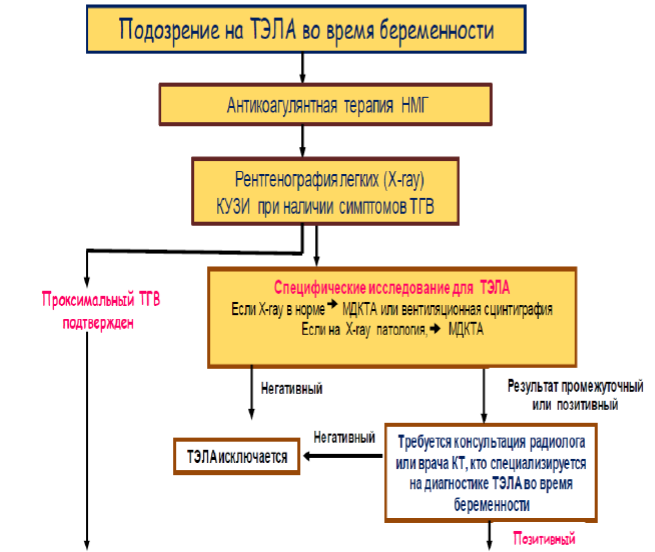
Всем беременным с диагностированным случаем ТГВ рекомендована консультация ангиолога или сосудистого хирурга и госпитализация в многопрофильный стационар.
Тактика ведения беременности и показания для прерывания беременности или родоразрешения определяются решением мультидисциплинарного консилиума в зависимости от конкретной клинической ситуации.
Немедикаментозное лечение:
При ТГВ:
обеспечить возвышенное положение нижней конечности (на начальном этапе);
обеспечить эластическую компрессию (чулки) нижних конечностей;
нет никаких и данных, что ранняя мобилизация больных с острым ТГВ увеличивает риск ТЭЛА, более того указывают, что ранняя мобилизация приводит к более быстрому регрессу отека нижней конечности и болевого синдрома.
При ТЭЛА: нет.
Рекомендации по лечению ТЭЛА
Медикаментозное лечение [15]
Рекомендации по лечению ТЭЛА
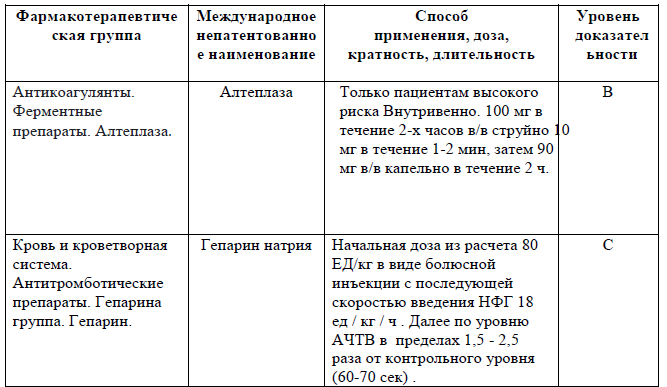
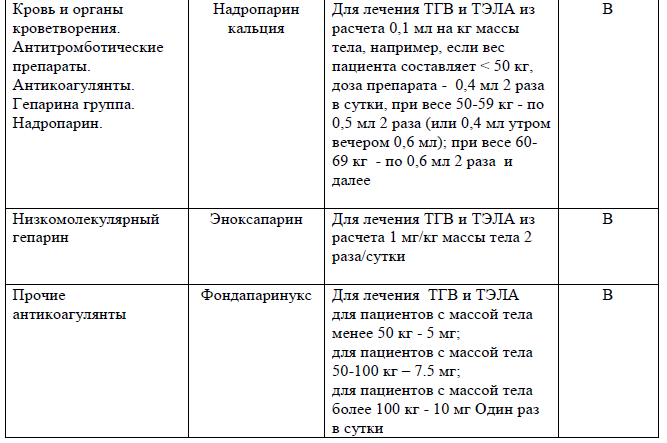
a - Однократная иньекция НМГ (эноксапарина, надропарина) возможна для больных во время беременности.
b - Фондапаринукс- препарат второй линии во время беременности для лечения ВТЭ (ТГВ и ТЭЛА) из-за отсутствия результатов РКИ, но может быть использовано в случае аллергии на НМГ, или при тромбоцитопении после решения врачебного консилиума.

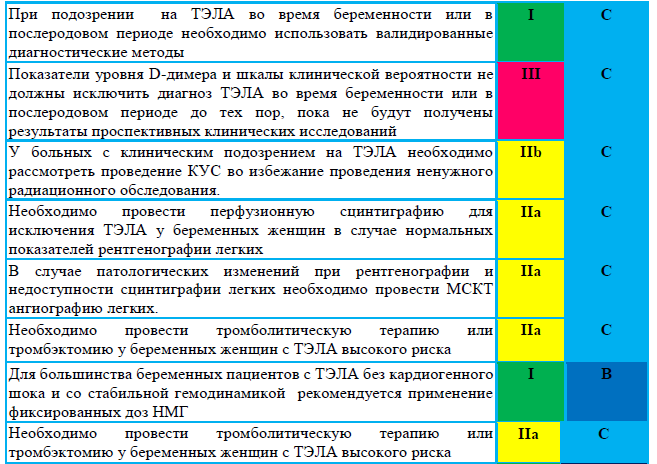

Терапевтические дозы антикоагулянтов: назначаются только в случае подтвержденного диагноза ТГВ и ТЭЛА.


Таблица 5. Режим дозирования гепарина

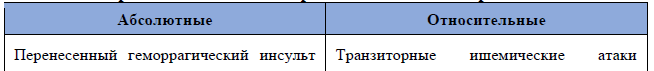
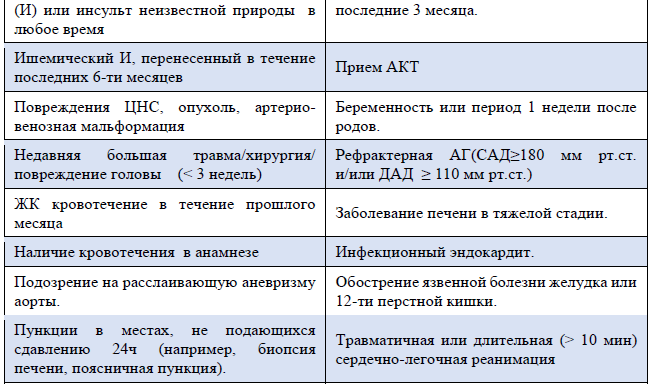
Таблица 6. Противопоказания к тромболитической терапии
Медикаментозное лечение, оказываемое на этапе скорой неотложной помощи:
Особую проблему представляет родоразрешение беременных, получающих антикоагулянтную терапию для лечения ВТЭ в связи с увеличением числа больших кровотечений
Послеродовое ведение:
Лекарственная терапия при кровотечениях, когда требуется срочная инактивация действия антикоагулянтов (гепарина, НМГ).
1. Свежезамороженная плазма (СЗП).
Заказ СЗП соответствующей АВ0 группы крови реципиента.
Если неизвестна группа крови пациента, универсальная СЗП — это СЗП группы АВ (без антител анти-А и анти-В). Начальная доза 10–20 мл/кг; решение о последующих трансфузиях на основании клинического состояния пациента и результатов исследования системы свёртывания крови.
Если гепарин вводился внутривенно капельно, необходимо прекратить его инфузию и ввести 25-30 мг протамина сульфата.
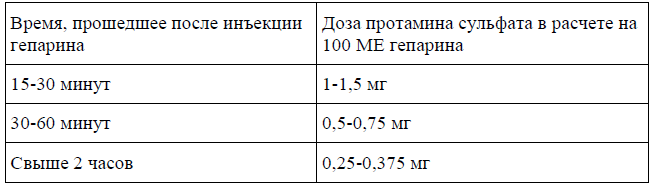
При подкожных инъекциях гепарина доза протамина сульфата составляет 1 - 1,5 мг на каждые 100 ME гепарина. Первые 25-50 мг протамина сульфата следует ввести внутривенно медленно, а оставшуюся дозу - внутривенно капельно в течение 8-16 часов. Возможно дробное введение протамина сульфата, что требует контроля активированного частичного тромбопластинового времени (АЧТВ). Например, если введено подкожно 20000 ME гепарина, через 2 часа происходит резорбция гепарина из комплексов с протамином по 3333 ME гепарина, в связи с этим следующая доза протамина сульфата составляет 33 мг.
В случае использования экстракорпорального кровообращения при оперативном вмешательстве доза протамина сульфата составляет 1,5 мг на каждые 100 ME гепарина.
2б. Протамина сульфат для нейтрализации низкомолекулярного гепарина (НМГ)
Сульфат протамина не способен полностью устранить антитромбическую активность НМГ: 1 мг протамина сульфата нейтрализует 100 ЕД анти-Ха активности и не более 60 % анти-Ха активности НМГ, поэтому необходима инфузия расчетной дозы протамина сульфата в течение нескольких часов или повторное введение половинной дозы протамина сульфата при сохраняющемся кровотечении. При выборе дозы протамина сульфата необходимо учитывать время, прошедшее после последней инъекции НМГ. Вводят протамина сульфат внутривенно или в виде инфузии медленно - 1 мг протамина сульфата на 100 анти-Ха ME недавно введенного НМГ. Через 8 ч после введения НМГ можно использовать половинную дозу протамина сульфата, через 12 ч введение препарата скорее всего не потребуется.
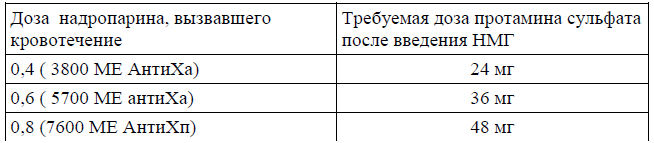
Надропарин. 6 мг сульфата протамина нейтрализует около 0,1 мл (950 МЕ анти-Xa) фраксипарина. А вторая инфузия 0,5 мг протамина на 1 мг надропарина может быть назначена, если АЧТВ, измеренное через 2–4 часа после первой инфузии, остается продолжительным.
Эноксапарин. 1 мг протамина сульфата нейтрализует антикоагулянтную активность 1 мг эноксапарина, если эноксапарин натрия вводился не более, чем за 8 ч до введения протамина. 0,5 мг протамина нейтрализует антикоагулянтный эффект 1 мг эноксапарина, если с момента введения последнего прошло более 8 ч или при необходимости введения 2-й дозы протамина. Если же после введения эноксапарин натрия прошло 12 ч и более, введения протамина не требуется. Однако даже при введении больших доз протамина сульфата анти-Ха-активность эноксапарина полностью не нейтрализуется (максимально на 60%).
2в. Протамин у пациентов с почечной и печеночной недостаточностью:
У пациентов с почечной недостаточностью легкой и средней степени тяжести (КК≥30 мл/мин и <60 мл/мин) снижение дозы не требуется, у пациентов с почечной недостаточностью тяжелой степени (КК <30 мл/мин) дозу следует снизить на 25 %.
У пациентов с печеночной недостаточностью протамина сульфат следует применять с осторожностью.
3. Препараты фактора VIIa свертывания крови.
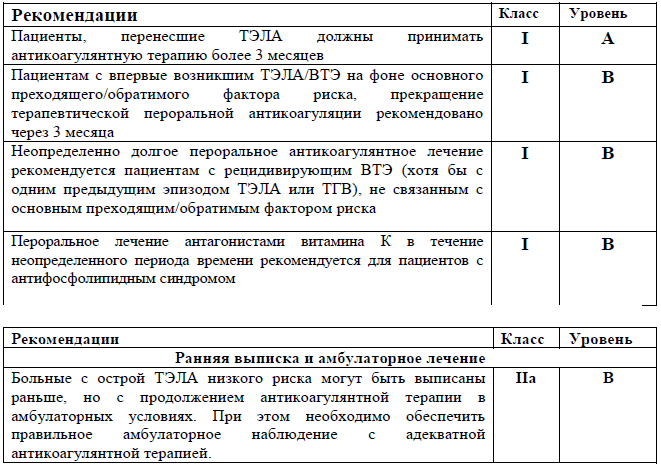
Рекомендации по длительности антикоагулянтной терапии после ТЭЛА у пациентов, не страдающих раком
Индикаторы эффективности лечения и безопасности методов диагностики и лечения:



Терапевтические дозы антикоагулянтов: назначаются только в случае подтвержденного диагноза ТГВ и ТЭЛА.


*Фондапаринукс – существует несколько наблюдательных исследований относительно применения фондапаринукса у беременных женщин, самое большое число благоприятных исходов у беременных женщин с данным препаратом — 65. Его применение рассматривается в случаях аллергии или нежелательных эффектах на применение НМГ. Одно исследование продемонстрировало незначительное проникновение фондапаринукса через плаценту, и дальнейшие исследования требуются для оценки риска аномалий развития.
Таблица 5. Режим дозирования гепарина

Тромболитическая (фибринолитическая) терапия (ТЛТ) следует применять только у пациенток с тяжелой гипотензией или шоком. После ТЛТ рекомендуется отказаться от нагрузочной дозы НФГ и вводить их в стартовой в 18 МЕ/кг/ч и тщательно корректировать дозу на основании значений АЧТВ. После стабилизации пациентки НФГ может быть заменен на НМГ.
Таблица 6. Противопоказания к тромболитической терапии


Медикаментозное лечение, оказываемое на амбулаторном уровне: нет.
Медикаментозное лечение, оказываемое на этапе скорой неотложной помощи:
при ТЭЛА и выраженном болевом синдроме – наркотические аналгетики: тримеперидин 2%-1,0 в/м или в/в, морфин 1%-1,0 в/м или в/в.
при необходимости - проведение реанимационных мероприятий.
Искусственная вентиляция легких при ТЭЛА:
Общие принципы ИВЛ:
Другие виды лечения:
Искусственная вентиляция легких при ТЭЛА:
Показания к переводу на ИВЛ:
отсутствие сознания (менее 10 баллов по шкале Глазго), тахипное более 25 в минуту, брадипноэ менее 10 в минуту, снижение сатурации ниже 90% при ингаляции увлажненного кислорода, снижение РаО2 ниже 80 мм.рт.ст., повышение РаСО2 выше 60 мм.рт.ст. или снижение ниже 30 мм.рт.ст;
Общие принципы ИВЛ:
предпочтительный режим вентиляции при отсутствии обструктивного синдрома – вентиляция по давлению с поддержкой самостоятельного дыхания (SIMV(P). Верхняя граница давления должна составлять < 30 см вод. ст.
не рекомендуется проведение длительной медикаментозной седации у больных на ИВЛ;
не рекомендуется применение миорелаксации у больных на ИВЛ, только кратковременно (менее 48 часов) при раннем ОРДС и при ИО менее 150 (УД 2С).
Хирургическое вмешательство, оказываемое в стационарных условиях только после решения мультидисциплинарной команды: ангиолога, тромбокардиолога, гинеколога, врача ОРИТ, сосудистого хирурга:
Хирургическое вмешательство:
Хирургическое вмешательство, оказываемое в стационарных условиях только после решения мультидисциплинарной команды: ангиолога, тромбокардиолога, гинеколога, врача ОРИТ, сосудистого хирурга:
флебэктомия;
тромбэктомия;
установка «Кава-фильтра».
Показания:
- абсолютные противопоказания к ТЛТ (УД – IIaC);
- рутинная установка кава-фильтров не рекомендуется (УД – IIIA).
Флотация тромба в венах нижних конечностей не является показанием для имплантации «Кава-фильтра».
Лечебная тактика во время беременности:
В случае острого ТГВ прерывание беременности и досрочное родоразрешение не рекомендуется:
для коррекции артериальной гипотонии/шока при ТЭЛА должны использоваться вазопрессоры (норэпинефрин 2-30 мкг/мин, эпинефрин, допамин) и инотропные препараты при дисфункции правого желудочка (добутамин 5 мкг/кг/мин, левосимендан);
при выраженном болевом синдроме – наркотические аналгетики: тримеперидин 2%-1,0 в/м или в/в, морфин 1%-1,0 в/м или в/в.
применение тромболитической терапии оправдано только у пациентов высокого риска смерти, В то время необходимо соблюдать осторожность в плане риска развития кровотечения (см таблицу противопоказания в ТЛТ терапии);
массивная инфузионная терапия для коррекции гемодинамических нарушений при ТЭЛА противопоказана.
Лечебная тактика на этапе родоразрешения
Особую проблему представляет родоразрешение беременных, получающих антикоагулянтную терапию для лечения ВТЭ в связи с увеличением числа больших кровотечений
Дородовое ведение:
возможен перевод больных с 36 недели на НФГ, в таких случаях необходимо прекратить НФГ за 4-6 ч до родов;
прием НМГ необходимо прекратить за 24- 36 ч до предполагаемого срока родов;
полная отмена требуется в случае применения региональной анестезии для снижения риска эпидуральной и спинальной гематомы;
эпидуральная анестезия не может быть использована в течение 12 часов после применения профилактической доза и в течение 24 часов после применения терапевтической дозы.
Послеродовое ведение:
Начало АКТ у больных с ТГВ или ТЭЛА зависит от метода родоразрешения, баланса риска развития тромботических осложнений, риска развития кровотечения и коллегиального решения многопрофильной команды.
Не следует вводить НМГ в течение, как минимум, 4 часов после удаления эпидурального катетера.
Можно рассмотреть применение временной профилактической дозы НМГ в послеоперационном периоде (после кесарева сечения) после оценки риска один раз, по крайней мере, через 4 часа с момента удаления эпидурального катетера, затем с интервалом не менее 8–12 часов ввести следующую профилактическую дозу с последующим переходом на терапевтическую дозу.
АКТ должно проводиться в течение не менее 6 недель после родов с минимальным общим сроком продолжительности лечения 3 месяца пероральных антикоагулянтов время кормления можно использовать НМГ и АВК. Не рекомендуется использование НОАК кормящим матерям.
Рекомендуется тесное сотрудничество между врачом-акушером, анестезиологом и лечащим врачом.
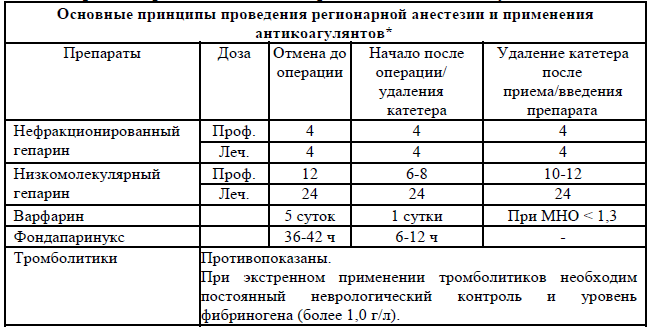
Важность соблюдения временного интервала во время проведения регионарной анестезии и применения антикоагулянтов
Важность соблюдения временного интервала во время проведения регионарной анестезии и применения антикоагулянтов

*- в акушерстве можно использовать только гепарин и НМГ.
Варфарин и дезагреганты противопоказаны по инструкции во время беременности и могут использоваться только при информированном согласии пациентки и специальных абсолютных показаниях, связанных с сопутствующими заболеваниями сердечно-сосудистой системы.
Лекарственная терапия при кровотечениях, когда требуется срочная инактивация действия антикоагулянтов (гепарина, НМГ).
1. Свежезамороженная плазма (СЗП).
Заказ СЗП соответствующей АВ0 группы крови реципиента.
Если неизвестна группа крови пациента, универсальная СЗП — это СЗП группы АВ (без антител анти-А и анти-В). Начальная доза 10–20 мл/кг; решение о последующих трансфузиях на основании клинического состояния пациента и результатов исследования системы свёртывания крови.
2. Протамина сульфат.
2а. Доза протамина сульфат при кровотечениях на фоне применения нефракционированного гепарина (НФГ).
Протамин нейтрализует действие гепарина, обладает гемостатическим и слабым антикоагуляционным свойствами. Активность выражается в единицах действии (ЕД). В 1 мл 1 % раствора должно содержаться не менее 750 ЕД; 1 мг (75 ME) нейтрализует примерно 80-100 ЕД гепарина. Раствор протамина сульфата вводят медленно внутривенно струйно или капельно. Скорость введения не должна превышать 5 мг в минуту (например, 50 мг препарата вводить в течение 10 минут), так как более быстрое введение может вызвать анафилактоидную реакцию. Доза препарата зависит от способа введения гепарина. Вычисленную дозу растворяют в 300-500 мл 0,9 % раствора натрия хлорида. Не следует вводить более 150 мг протамина сульфата в течение 1 часа.
При болюсных инъекциях гепарина доза протамина сульфата уменьшается в зависимости от времени, прошедшего от введения гепарина, так как последний непрерывно удаляется из организма.

Если гепарин вводился внутривенно капельно, необходимо прекратить его инфузию и ввести 25-30 мг протамина сульфата.
При подкожных инъекциях гепарина доза протамина сульфата составляет 1 - 1,5 мг на каждые 100 ME гепарина. Первые 25-50 мг протамина сульфата следует ввести внутривенно медленно, а оставшуюся дозу - внутривенно капельно в течение 8-16 часов. Возможно дробное введение протамина сульфата, что требует контроля активированного частичного тромбопластинового времени (АЧТВ). Например, если введено подкожно 20000 ME гепарина, через 2 часа происходит резорбция гепарина из комплексов с протамином по 3333 ME гепарина, в связи с этим следующая доза протамина сульфата составляет 33 мг.
В случае использования экстракорпорального кровообращения при оперативном вмешательстве доза протамина сульфата составляет 1,5 мг на каждые 100 ME гепарина.
2б. Протамина сульфат для нейтрализации низкомолекулярного гепарина (НМГ)
Сульфат протамина не способен полностью устранить антитромбическую активность НМГ: 1 мг протамина сульфата нейтрализует 100 ЕД анти-Ха активности и не более 60 % анти-Ха активности НМГ, поэтому необходима инфузия расчетной дозы протамина сульфата в течение нескольких часов или повторное введение половинной дозы протамина сульфата при сохраняющемся кровотечении. При выборе дозы протамина сульфата необходимо учитывать время, прошедшее после последней инъекции НМГ. Вводят протамина сульфат внутривенно или в виде инфузии медленно - 1 мг протамина сульфата на 100 анти-Ха ME недавно введенного НМГ. Через 8 ч после введения НМГ можно использовать половинную дозу протамина сульфата, через 12 ч введение препарата скорее всего не потребуется.
Надропарин. 6 мг сульфата протамина нейтрализует около 0,1 мл (950 МЕ анти-Xa) фраксипарина. А вторая инфузия 0,5 мг протамина на 1 мг надропарина может быть назначена, если АЧТВ, измеренное через 2–4 часа после первой инфузии, остается продолжительным.

Эноксапарин. 1 мг протамина сульфата нейтрализует антикоагулянтную активность 1 мг эноксапарина, если эноксапарин натрия вводился не более, чем за 8 ч до введения протамина. 0,5 мг протамина нейтрализует антикоагулянтный эффект 1 мг эноксапарина, если с момента введения последнего прошло более 8 ч или при необходимости введения 2-й дозы протамина. Если же после введения эноксапарин натрия прошло 12 ч и более, введения протамина не требуется. Однако даже при введении больших доз протамина сульфата анти-Ха-активность эноксапарина полностью не нейтрализуется (максимально на 60%).
2в. Протамин у пациентов с почечной и печеночной недостаточностью:
У пациентов с почечной недостаточностью легкой и средней степени тяжести (КК≥30 мл/мин и <60 мл/мин) снижение дозы не требуется, у пациентов с почечной недостаточностью тяжелой степени (КК <30 мл/мин) дозу следует снизить на 25 %.
У пациентов с печеночной недостаточностью протамина сульфат следует применять с осторожностью.
3. Препараты фактора VIIa свертывания крови.
Дальнейшее ведение:
Все пациенты с ТЭЛА высокого риска после стабилизации общего состояния (нормализация АД, ЧСС, сатурация кислорода) и после повторной оценки индекса тяжести ТЭЛА при уровне 1-2 степени могут быть выписаны на амбулаторное лечение под наблюдением акушер-гинеколога, кардиолога, терапевта.
Рекомендации по длительности антикоагулянтной терапии после ТЭЛА у пациентов, не страдающих раком

Вопросы профилактики ВТЭ у женщин до и после родов.
Согласно рекомендации Американской коллегии (2012), все женщины разделены на три категории в зависимости от необходимости проведения профилактики.
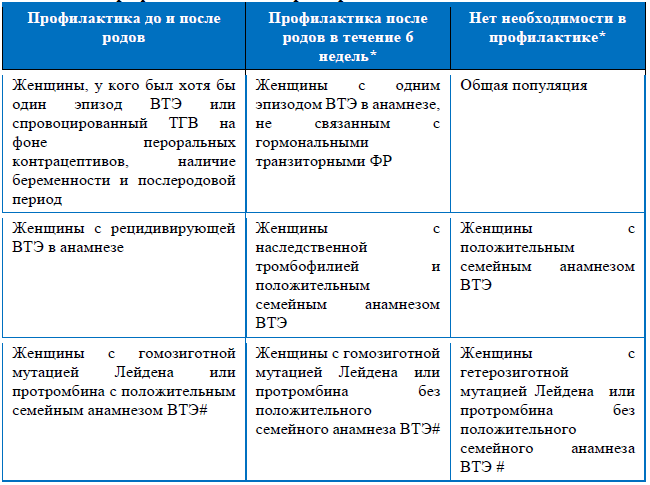
К первой группе относятся женщины, которые нуждаются в профилактике ВТЭ в течение всей беременности и после родов. К ним относятся беременные женщины, у кого был хотя бы один эпизод ВТЭ или спровоцированный ТГВ на фоне пероральных контрацептивов, женщины с рецидивирующей ВТЭ в анамнезе и с гомозиготной мутацией Лейдена или протромбина с положительным семейным анамнезом ВТЭ.
Ко второй группе относятся женщины, которые нуждаются в проведении только профилактики ВТЭ после родов. Это женщины с одним эпизодом ВТЭ в анамнезе, не связанным с применением гормональных препаратов, женщины с наследственной тромбофилией и положительным семейным анамнезом, женщины с гомозиготной мутацией Лейдена или протромбина без положительного семейного анамнеза ВТЭ.
И наконец группа женщин, которые не требуют проведения профилактики во время беременности и после родов. К этой группе относятся все женщины, даже с положительным семейным анамнезом, а также женщины с гетерогенной мутацией мутацией Лейдена или протромбина без положительного семейного анамнеза ВТЭ.
Более подробная информация представлена в таблице 7.
Таблица 7. Профилактика ВТЭ при беременности:
Таблица 7. Профилактика ВТЭ при беременности:

* Положительный семейный анамнез – наличие родства первой степени с больными ВТЭ
+ За исключением женщин, которые могут быть отнесены в группу более агрессивной профилактической стратегии в таблице.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения:
предупреждение ТЭЛА при ТГВ;
купирование и ликвидация ТЭЛА.Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации: нет.
Показания для экстренной госпитализации:
при подозрении и/или верификации острого ТГВ;
при подозрении и/или верификации ТЭЛА.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2022
- 1.Konstantinides S.V., Torbicki A., Agnelli G et al. 2014 ESC Guidelines on the diagnosis and management of acute pulmonary embolism. European Heart Journal (2014) 35, 3033–3080 doi:10.1093/eurheartj/ehu283 2.Konstantinides SV, Meyer G, Becattini C. et al 2019 ESC Guidelines for the diagnosis and management of acute pulmonaryembolism developed in collaboration with the European Respiratory Society (ERS) European Heart Journal (2020) 41, 543-603.doi:10.1093/eurheartj/ehz405 3. Сугралиев А.Б., Актаева Ш.С., Plinio C и др. Рекомендации по диагностике и лечению тромбоза глубоких вен и тромбоэмболии легочных артерий (методические рекомендации) Алматы 2021г. 4. American College of Obstetricians and Gynecologists (ACOG). Inherited thrombophilias in pregnancy. Washington (DC): American College of Obstetricians and Gynecologists (ACOG); 2010 Apr. 11 p. (Practice bulletin; no. 111). 5. Протокол диагностики и лечения МЗ РК «Тромбоэмболия легочной артерии» от 16 июля 2020 года Протокол №107 6. Bates SM, Greer IA, Middeldorp S, VTE, thrombophilia, antithrombotic therapy, and pregnancy: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines Сhest. 2012 Feb;141(2 Suppl):e691S-e736S. doi: 10.1378/chest.11-2300. 7. Казахстанский Национальный лекарственный Формуляр Приказ Министра здравоохранения Республики Казахстан от 23 августа 2022 года № ҚР ДСМ-88. Зарегистрирован в Министерстве юстиции Республики Казахстан 26 августа 2022 года № 29299. 7.World Health Organization 2021 Some rights reserved. This work is available under the Creative Commons Attribution-NonCommercial-ShareAlike 3.0 IGO licence (CC BY-NC-SA 3.0 IGO; https://creativecommons.org/licenses/by-nc-sa/3.0/igo). 8. British national formulary September 2020- March 2021 9. Food and Drug Administration, FDA U.S. Food and Drug Administration (fda.gov) 10. BMJ Best Practice BMJ Best Practice 11. Konstantinides S.V., Meyer G., Becattinin C., et al 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). European Heart Journal (2020) 41, 543-603. doi:10.1093/eurheartj/ehz405
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА
Список разработчиков протокола с указанием квалификационных данных:
1) Уразбаева Гульфайруз Галимовна – кандидат медицинских наук, акушер-гинеколог, Председатель Правления АО «Научный центр акушерства, гинекологии и перинатологии».
2) Мамедалиева Нагима Мусралиевна – доктор медицинских наук, профессор, акушер-гинеколог, главный научный сотрудник АО «Научный центр акушерства, гинекологии и перинатологии».
3) Сугралиев Ахметжан Бегалиевич – кандидат медицинских наук, кардиолог, заведующий кафедрой внутренних болезней с курсом пропедевтики ОАН «Казахский национальный медицинский университет имени С.Д. Асфендиярова», член Президиума Евразийской Ассоциации терапевтов, член Рабочей группы по тромбозам Европейского общества кардиологов.
4) Исенова Сауле Шайкеновна – доктор медицинских наук, акушер-гинеколог, заведующая кафедрой акушерства и гинекологии НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова».
5) Исина Гульжан Муратовна – доктор медицинских наук, акушер-гинеколог, профессор кафедры акушерства и гинекологии НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова».
6) Кожахметов Али Нурбатырович – доктор медицинских наук, анестезиолог-реаниматолог, заведующий отделением анестезиологии и реанимации городского роддома №4 г. Алматы.
7) Акшалова Асель Талгатбековна – PhD, врач клинический фармаколог АО «Научный центр акушерства, гинекологии и перинатологии».
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
1) Бапаева Гаури Биллахановна – доктор медицинских наук, профессор, акушер-гинеколог, Директор Департамента женского здоровья КФ UMC.
2) Жумадилов Агзам Шаймарданович – доктор медицинских наук, анестезиолог-реаниматолог, заместитель Председателя Правления РГП на ПХВ «Национальный координационный центр экстренной медицины».
3) Искаков Серик Саятович – кандидат медицинских наук (PhD), акушер-гинеколог, заведующий кафедрой акушерства и гинекологии №2 НАО «Медицинский университет Астана».
4) Миербеков Ергали Маматович – доктор медицинских наук, профессор, анестезиолог-реаниматолог АО «Национальный научный центр хирургии имени А.Н. Сызганова», президент РОО «Федерация анестезиологов и реаниматологов».
Указание условий пересмотра протокола: пересмотр протокола через 5 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.