Синдром Сезари
 Версия: Клинические рекомендации РФ 2024 (Россия)
Версия: Клинические рекомендации РФ 2024 (Россия)
Болезнь Сезари (C84.1)
Гематология, Дерматовенерология, Онкогематология
Общая информация
Краткое описание
Разработчик клинической рекомендации
- Общероссийская общественная организация "Российское общество дерматовенерологов и косметологов"
- Российское общество онкогематологов
- Национальное гематологическое общество
Одобрено Научно-практическим Советом Минздрава РФ
– размещенные в Рубрикаторе после 1 января 2024 года – с 1 января 2025 года.
Клинические рекомендации
Синдром Сезари
Год утверждения (частота пересмотра): 2024
Возрастная категория: Взрослые, Дети
Пересмотр не позднее: 2026
ID: 575
Определение заболевания или состояния (группы заболеваний или состояний)
Синдром Сезари (СС) представляет собой Т-клеточную лимфому кожи, характеризующуюся эритродермией, генерализованной лимфаденопатией и наличием в крови циркулирующих злокачественных Т-лимфоцитов (клеток Сезари).
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
C84.1 – Синдром Сезари.
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Стадирование синдрома Сезари проводится согласно пересмотренной TNM классификации, предложенной Международным обществом по лимфомам кожи и Европейской организацией по изучению и лечению рака (ISCL-EORTC staging system). Так как для пациентов с синдромом Сезари характерны эритродермия (Т4) и В2-вовлечение крови, они расцениваются как имеющие IVA или IVB стадию заболевания [9].
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Причины развития синдрома Сезари неизвестны. Иммунофенотипирование показало, что пролиферирующими злокачественными лимфоцитами, проникающими в кожу, при синдроме Сезари являются зрелые Т-лимфоциты центральной памяти, экспрессирующие CD3, CD4, CD45RO и CCR4 (маркеры зрелых Т-лимфоцитов памяти), а также CCR7, L-селектин и CD27 (маркеры Т-лимфоцитов центральной памяти) [1, 2]. Активацию пролиферации Т-лимфоцитов, приводящую к развитию этого заболевании и его прогрессированию, связывают с мутациями и/или хромосомными изменениями в генах, которые контролируют активность супрессоров опухолевого роста, эпигенетических регуляторов, сигнальных путей Т-лимфоцитов, а также дифференцировку, выживание и миграцию Т-лимфоцитов в кожу [3-5].
Злокачественная популяция Т-лимфоцитов вырабатывает интерлейкин-(ИЛ)-4 и ИЛ-10, что соответствует профилю Т-хелперов 2-го типа (Th2), и экспресирует маркер CD25 и белок Fox-P3 (forkhead box protein 3), что соответствует профилю Т-регуляторных лимфоцитов (Т-супрессоров) [6-8]. В результате смещения иммунных реакций в сторону Th2 и T-регуляторного профилей происходит подавление функции естественных киллерных и CD8-экспрессирующих Т-лимфоцитов, а также нарушение функции и дифференцировки дендритных клеток, что приводит к подавлению нормального иммунного ответа, в том числе на вирусные инфекции и новообразования [8].
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Синдром Сезари составляет менее чем 5% от всех первичных кожных лимфом. Болеют преимущественно люди пожилого возраста с преобладанием пациентов мужского пола, средний возраст начала заболевания составляет 60-65 лет [7, 9]
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Синдром Сезари начинается с развития эритродермии, которая сопровождается сильным зудом и/или шелушением. Выраженность эритродермии может быть различной -от розовато-красной до ярко-красной окраски кожных покровов. Впоследствии присоединяется ладонно-подошвенный гиперкератоз, алопеция и ониходистрофия. Пальпация выявляет увеличение периферических лимфатических узлов, которое может происходить как за счет дерматопатической лимфаденопатии, так и вследствие их вовлечения в опухолевый процесс [7, 10]. При лабораторных исследованиях обнаруживается наличие в периферической крови большое количество клеток Сезари.
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
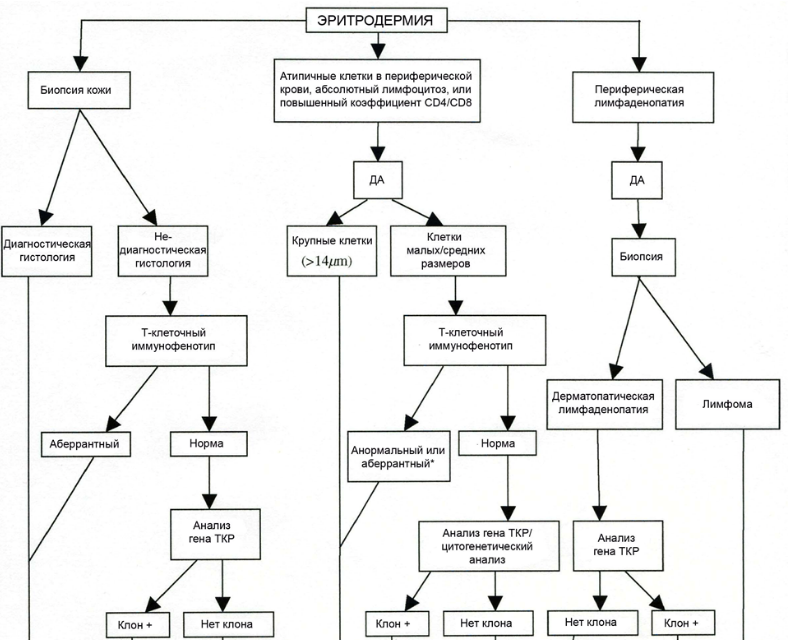
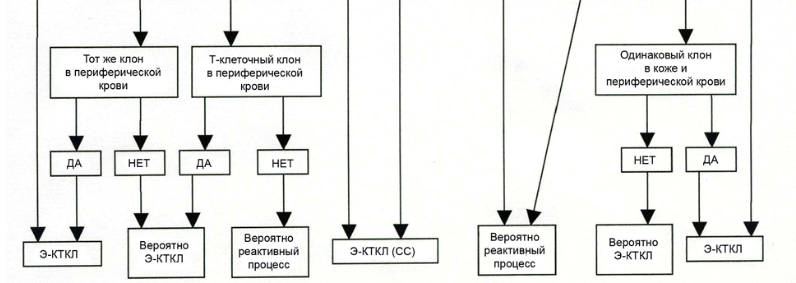
Международным обществом лимфом кожи (ISCL) и Европейской организацией по изучению и лечению рака (EORTC) выработаны следующие критерии диагностики синдрома Сезари (Приложение Г1) [9]:
- Отсутствие предшествующего грибовидного микоза
- Генерализованная эритродермия (диффузная эритема, покрывающая не менее 80% поверхности тела с/без шелушения)
- Наличие в крови доминантного клона Т-лимфоцитов (определяется при помощи ПЦР или Southernblot)
- Наличие одного или более следующих признаков:
-
абсолютное количество клеток Сезари в крови ≥ 1000 клеток/мм3
-
повышенное содержание CD3+ или CD4+ клеток в периферической крови с коэффициентом отношения CD4/CD8 ≥ 10 (определяется при помощи проточной цитометрии)
-
повышенное содержание CD4+ клеток в периферической крови с аберрантным иммунофенотипом, включающим отсутствие экспрессии CD7 (≥ 40% CD4+СD7- клеток) или CD26 (≥ 30% CD4+CD26- клеток).
1. Жалобы и анамнез
Жалобы и анамнез описаны в разделе «Клиническая картина».
2. Физикальное обследование
Данные физикального обследования описаны в разделе «Клиническая картина».
3. Лабораторные диагностические исследования
-
Рекомендуется пациентам с клиническими проявлениями синдрома Сезари для выявления в периферической крови лимфоцитов с признаками злокачественной трансформации (клеток Сезари) иммунофенотипирование периферической крови для выявления субпопуляционного состава лимфоцитов (основные и/или малые) [7, 16–19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2)
Комментарии: Для иммунофенотипирование периферической крови для выявления субпопуляционного состава лимфоцитов (основные и/или малые) используется кровь. Исследование проводится для выявления маркеров Т-лимфоцитов, циркулирующих в крови, – CD3, CD4, CD7, CD26. Т-лимфоциты с аберрантной экспрессией маркеров CD3, CD4, CD7, CD26 являются клетками Сезари. Диагностически значимым является абсолютное количество клеток Сезари в крови ≥ 1000 клеток/мм3 или содержание атипичных лимфоцитов >5%. При этом подсчитывается общее число лейкоцитов, общее число лимфоцитов, число атипичных лимфоцитов, приходящихся на 100 лимфоцитов. Диагностически значимым является также повышенное содержание CD3+ или CD4+ клеток периферической крови с коэффициентом отношения CD4/CD8 ≥ 10; повышенное содержание CD4+ клеток периферической крови с аберрантным иммунофенотипом, включающем отсутствие экспрессии CD7 (≥ 40% CD4+СD7- клеток) или CD26 (≥ 30% CD4+CD26- клеток) [18].
-
Рекомендуется пациентам с клиническими и гистологическими проявлениями синдрома Сезари для выявления признаков злокачественной трансформации лимфоцитов, инфильтрирующих кожу, патолого-анатомическое исследование биопсийного (операционного) материала кожи с применением иммуногистохимических методов [7, 11, 19, 20]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Необходимо определение маркеров CD2, CD3, CD4, CD5, CD7, CD8, CD20, CD30. Неопластические Т-лимфоциты при синдроме Сезари обычно экспрессируют CD3 и CD4, но не экспрессируют CD8. Потеря экспрессии CD7 (маркера всех Т-лимфоцитов) более чем 50% Т-лимфоцитами инфильтрата и наличие экспрессии белка программируемой гибели клеток 1 (PD-1) Т-лимфоцитами инфильтрата подтверждают диагноз синдрома Сезари при дифференциальной диагностике с эритродермиями, вызванными воспалительными заболеваниями [14]. Малое количество (менее 10%) CD8-положительных Т-лимфоцитов в составе кожного инфильтрата в биоптате кожи также указывает на диагноз синдрома Сезари [14].
-
Рекомендуется для подтверждения диагноза синдрома Сезари путем выявления преобладающего клона Т-лимфоцитов молекулярно-генетическое исследование Т-клеточной клональности (по генам бэта, гамма и дельта цепей Т-клеточного рецептора[7, 19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Для исследования T-клеточной клональности могут использоваться кровь и биопсийный материал кожи пациента. Доля биоптатов кожи пациентов с Т-клеточными лимфомами кожи, в которых обнаруживается моноклональная реаранжировка гена Т-клеточного рецептора (TCR) методом полимеразной цепной реакции, может зависеть от метода амплификации [7]. Описано выявление клонов Т-лимфоцитов методом полимеразной цепной реакции в биоптатах кожи 27 из 30 пациентов с синдромом Сезари [21]. Секвенирование биоптатов пораженной кожи пациентов с Т-клеточными лимфомами кожи считается более специфичным и чувствительным в обнаружении клона Т-лимфоцитов по сравнению с полимеразной цепной реакцией [22].
Поскольку моноклональность может быть выявлена в случае некоторых воспалительных заболеваний, результаты определения реаранжировки гена Т-клеточного рецептора необходимо рассматривать в сопоставлении с другими данными обследования пациента. Обнаружение идентичных клонов Т-лимфоцитов в коже и крови может указывать на синдром Сезари, но не на воспалительные причины эритродермии [23].
-
Рекомендуется просмотр мазка крови для анализа аномалий морфологии эритроцитов, тромбоцитов и лейкоцитов с целью подсчета клеток Сезари в мазке крови при необходимости определения их количества в крови в случае невозможности определить клетки Сезари с помощью проточной цитофлуометрии [7, 16-17, 27].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2)
Комментарии: Клетки Сезари в мазке крови определяются как клетки, имеющие ядра неправильной формы с множественными инвагинациями ядер, что придает им церебриформный вид. Различают 3 морфологических варианта клеток Сезари: мелкоклеточный (размер клеток от 8 до 11 мкм), крупноклеточный (размер клеток от 12 до 25 мкм) и двуядерный (клетки с двумя ядрами). В мазках крови необходимо определять абсолютное и относительное (процентное) число этих клеток в общей популяции лимфоцитов [25]. Выявление содержания клеток Сезари в крови ≥ 1000 клеток/мм3 подтверждает диагноз синдрома Сезари [18].
-
Рекомендуется общий (клинический) анализ крови развернутый для выявления заболеваний и состояний, являющихся противопоказаниями к проведению системной терапии синдрома Сезари и для контроля безопасности проводимой системной терапии метотрексатом**, интерферонами, вориностатом, хлорамбуцилом**, преднизолоном**, доксорубицином**, гемцитабином**, брентуксимабом ведотином** или ультрафиолетового облучения кожи [24, 25–31].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Лекарственные препараты, используемые для системной терапии синдрома Сезари, обладают нежелательными эффектами, выявление которых требует проведения общего (клинического) анализа крови.
Метотрексат** даже при применении в обычных терапевтических дозах может вызвать угнетение системы кроветворения (лейкопения, тромбоцитопения, анемия). Перед началом лечения метотрексатом**, во время терапии или при возобновлении терапии после перерыва необходимо проводить общий (клинический) анализ крови с подсчетом лейкоцитарной формулы и количества тромбоцитов. В процессе лечения метотрексатом** анализ крови проводят ежемесячно в первые 6 месяцев и не реже, чем каждые 3 месяца в дальнейшем, при повышении доз целесообразно повышать частоту обследований. В случае значительного снижения количества лейкоцитов или тромбоцитов лечение метотрексатом** немедленно прекращают и назначают симптоматическую поддерживающую терапию.
При применении интерферонов возможны изменения лабораторных показателей, проявляющиеся лейкопенией, лимфопенией, тромбоцитопенией, анемией. Для своевременного выявления отклонений от нормы лабораторных показателей, которые могут возникнуть в ходе терапии, общий клинический анализ крови необходимо повторять каждые 2 недели. При снижении числа тромбоцитов до значения менее 50х109/л, абсолютного числа нейтрофилов менее 0,50х109/л, лечение интерфероном рекомендуется прекратить.
Пациентам, получающим терапию препаратом вориностат , из-за возможности развития лейкопении, нейтропении, тромбоцитопении и анемии, следует проводить тщательный мониторинг параметров общего (клинического) анализа крови не реже 1 раза в 2 недели в первые 2 месяца лечения, впоследствии – ежемесячно.
Хлорамбуцил** может вызвать угнетение функции костного мозга, и поэтому во время лечения необходимо систематически (не менее 2–3 раз в неделю) производить общий анализ крови с подсчетом форменных элементов периферической крови. При применении в терапевтических дозах препарат угнетает выработку лимфоцитов и в меньшей степени влияет на количество нейтрофилов и тромбоцитов, а также на уровень гемоглобина. Нет необходимости прекращать прием препарата при первых признаках снижения количества нейтрофилов, однако следует помнить, что снижение количества нейтрофилов может продолжаться в течение 10 и более дней после приема последней дозы.
Необходимо контролировать общий анализ крови до начала и во время проведения терапии преднизолоном**.
В процессе лечения доксорубицином** необходимо проводить оценку гематологических показателей до и во время каждого цикла терапии, включая определение количества лейкоцитов, тромбоцитов, гемоглобина, форменных элементов крови.
Перед каждым введением препарата гемцитабин** необходимо контролировать клинический анализ крови с количественным подсчетом форменных элементов крови (тромбоцитов, лейкоцитов, нейтрофилов). При угнетении функции костного мозга необходимо приостановить лечение или скорректировать дозу препарата.
Поскольку при лечении брентуксимабом ведотином** могут развиться анемия, тромбоцитопения и тяжелая нейтропения, перед каждым введением препарата должен проводиться клинический анализ крови. Если в процессе лечения обнаруживается нейтропения, для ее контроля следует увеличить интервалы между дозами. В случае развития нейтропении 3 или 4 степени необходимо уменьшить дозу препарата вплоть до прекращения лечения.
-
Рекомендуется анализ крови биохимический общетерапевтический для диагностики заболеваний и состояний, являющихся противопоказаниями к проведению системной терапии синдрома Сезари вориностатом и для контроля безопасности проводимой системной терапии метотрексатом**, интерферонами, вориностатом, преднизолоном**, доксорубицином**, гемцитабином**, брентуксимабом ведотином** или фототерапии [24, 25–30].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Лекарственные препараты, используемые для системной терапии синдрома Сезари, обладают нежелательными эффектами, выявление которых требует проведения анализа крови биохимического общетерапевтического. Перед началом лечения метотрексатом** или при возобновлении терапии после перерыва необходимо определение активности аспартатаминотрансферазы и аланинаминотрансферазы в крови, проведение исследования уровня билирубина связанного (коньюгированного), билирубина свободного (неконьюгированного)и альбумина в крови. В процессе лечения метотрексатом** анализ биохимический общетерапевтический необходимо повторять (ежемесячно в первые 6 месяцев и не реже, чем каждые 3 месяца в дальнейшем, при повышении доз целесообразно повышать частоту обследований). Лечение метотрексатом** не следует начинать или необходимо приостанавливать в случае наличия или развития любых отклонений от нормальных показателей функциональных печеночных тестов. Обычно показатели нормализуются в течение 2 недель, после чего лечение может быть возобновлено. При применении интерферона возможны отклонения от нормы лабораторных показателей, проявляющиеся повышением активности аланинаминотрансферазы, щелочной фосфатазы, концентрации креатинина. Для своевременного выявления отклонений от нормы лабораторных показателей, которые могут возникнуть в ходе терапии интерфероном, биохимический анализ крови необходимо повторять каждые 4 недели. В случае появления признаков нарушения функции печени за больным необходимо установить тщательное наблюдение. При прогрессировании нарушений функции печени введение препарата следует прекратить. Пациентам, получающим терапию препаратом вориностат, из-за возможности увеличения плазменной концентрации креатинина/ развития гипокалиемии, повышения уровня глюкозы в крови следует проводить тщательный мониторинг параметров биохимического анализа крови, включая концентрации электролитов плазмы, а именно исследование уровня натрия, калия, общего кальция,хлоридов в крови, исследование уровня глюкозы и креатинина в крови не реже 1 раза в 2 недели в первые 2 месяца лечения, впоследствии – ежемесячно. Исследование уровня глюкозы в особенности необходим для пациентов с уже имеющимся диабетом или риском развития диабета. До начала и во время терапии преднизолоном** необходимо контролировать гликемию и содержание электролитов в плазме, а именно исследование уровня натрия, калия, общего кальция, хлоридов в крови, исследование уровня глюкозы в крови. В процессе лечения доксорубицином** необходимо проводить оценку печеночных функциональных тестов, а именно определение активности аспартатаминотрансферазы и аланинаминотрансферазы, щелочной фосфотазы в крови, проведение исследования уровня билирубина связанного (коньюгированного), билирубина свободного (неконьюгированного), креатинина и альбумина в крови. При применении доксорубицина** вследствие быстрого лизиса опухолевых клеток может наблюдаться гиперурикемия, в связи с чем пациентам во время терапии рекомендуется проводить исследование уровня мочевой кислоты и креатинина в крови, исследование электролитов, а именно калия и кальция в крови, а также профилактическое использование аллопуринола**. У пациентов, получающих терапию гемцитабином**, периодически необходимо проводить оценку функции печени, а именно определение активности аспартатаминотрансферазы и аланинаминотрансферазы, щелочной фосфотазы в крови, проведение исследования уровня билирубина связанного (коньюгированного), билирубина свободного (неконьюгированного), креатинина и альбумина в крови. У пациентов, проходящих лечение брентуксимабом ведотином**, необходимо регулярно контролировать функции печени, а именно определение активности аспартатаминотрансферазы и аланинаминотрансферазы, щелочной фосфотазы в крови, проведение исследования уровня билирубина связанного (коньюгированного), билирубина свободного (неконьюгированного), креатинина и альбумина в крови. Вне зависимости от анамнеза, уровень сывороточной глюкозы должен контролироваться путем назначения исследования уровня глюкозы в крови у всех получающих брентуксимаб ведотин** пациентов с зарегистрированным случаем гипергликемии.
-
Рекомендуется общий (клинический) анализ мочи для диагностики заболеваний и состояний, являющихся противопоказаниями к проведению системной терапии синдрома Сезари и для контроля безопасности проводимой системной терапии метотрексатом**, вориностатом, преднизолоном**, гемцитабином** или фототерапии [24, 25, 28].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Лекарственные препараты, используемые для системной терапии синдрома Сезари, обладают нежелательными эффектами, выявление которых требует проведения общего (клинического) анализа мочи. Поражение почек и мочевыводящих путей может быть обусловлено как прямым токсическим действием препаратов, так и активацией инфекции на фоне иммуносупрессии. На фоне терапии метотрексатом** возможна активация хронической инфекции, в том числе с поражением мочевыделительной системы [28]. Поскольку метотрексат** экскретируется преимущественно почками, у пациентов с нарушениями функции почек может наблюдаться повышение концентрации метотрексата в крови, следствием чего могут быть тяжелые побочные реакции. Необходимо тщательно контролировать состояние пациентов, у которых возможны нарушения функции почек (например, пожилых пациентов). У пациентов, получающих терапию вориностатом, возможно развитие протеинурии и гиперурикемии. Необходимо контролировать глюкозурию и возможность развития лейкоцитурии до начала и во время проведения терапии преднизолоном**. У пациентов, получающих терапию гемцитабином**, периодически необходимо проводить оценку функции почек из-за возможности развития острой почечной недостаточности и гемолитического уремического синдрома.
-
Рекомендуется при прогрессировании патологического процесса определение маркера агрессивного течения заболевания определение активности лактатдегидрогеназы в крови [19, 32]
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: Повышение активности лактатдегидрогеназы в крови указывает на агрессивное течение синдрома Сезари.
4. Инструментальные диагностические исследования
-
Рекомендуется при подозрении на поражение лимфатических узлов ультразвуковое исследование лимфатических узлов (одна анатомическая область) [33]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендуется пациентам с подозрением на поражение внутренних органов компьютерная томография органов грудной полости, органов малого таза у женщин, органов таза у мужчин, органов брюшной полости и забрюшинного пространства [34, 35]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: При прогрессировании синдрома Сезари возможно поражение органов грудной полости, поражение органов малого таза у женщи, органов таза у мужчин, органов брюшной полости и забрюшинного пространства
-
Рекомендуется для выявления пролиферативного поражения лимфатических узлов и внутренних органов при синдроме Сезари позитронная эмиссионная томография, совмещенная с компьютерной томографией с туморотропными РФП [34]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2)
Комментарии: Выявление изменений лимфатических узлов или внутренних органов, обусловленных патологической пролиферацией Т-лимфоцитов, свидетельствует о прогрессировании синдрома Сезари.
5. Иные диагностические исследования
При обследовании пациентов с синдромом Сезари проводится стадирование заболевания согласно рекомендациям ISLE-EORTC (Приложение Г1) [9].
-
Рекомендуется всем пациентам для верификации диагноза синдрома Сезари, а также при необходимости контроля эффективности терапии, патолого-анатомическое исследование биопсийного (операционного) материала кожи [7, 11]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Наиболее часто встречающимся морфологическим признаком синдрома Сезари является поверхностный периваскулярный или полосовидный инфильтрат из крупных лимфоцитов, которые могут проявлять признаки атипии (крупные, гиперхромные или конволютивные ядра) [12, 13]. Может присутствовать эпидермотропизм [13, 14]. Тем не менее, при синдроме Сезари гистологические признаки, позволяющие установить диагноз, часто отсутствуют. Гистологические признаки синдрома Сезари отсутствовали в 39% образцов, полученных от 41 пациента [13]. В другом исследовании эпидермотропизм отсутствовал или был минимально выражен у 19 из 31 пациентов с синдромом Сезари [15].
-
Рекомендуется при выявлении во время ультразвукового исследования признаков поражения лимфатических узлов патолого-анатомическое исследование биопсийного (операционного) материала лимфоузла [10]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Для проведения биопсии выбирают лимфатические узлы размером 1,5 см и более с плотной, неравномерной консистенцией (гистологическое исследование, проточная цитометрия, определение реарранжировки гена ТКР), биопсия выполняется врачами-специалистами с хирургической специализацией, в том числе врачом-онкологом/гематологом. Патолого-анатомическое исследование биопсийного (операционного) материала лимфоузла позволяет определить наличие специфического поражения лимфоузлов. При выявлении специфического поражения лимфатических узлов пациент направляется для дальнейшего ведения и лечения к врачу-гематологу или врачу-онкологу.
-
Рекомендуется пациентам с подозрением на поражение костного мозга патолого-анатомическое исследование биопсийного (операционного) материала костного мозга [10, 19]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Трепанобиопсия костного мозга выполняется врачами-специалистами, владеющими методикой забора трепанобиоптата костного мозга (врачами-хирургами, врачами-гематологами или врачами-онкологами). Патолого-анатомическое исследование биопсийного (операционного) материала костного мозга позволяет определить наличие специфического поражения костного мозга. При выявлении специфического поражения костного мозга пациент направляется для дальнейшего ведения и лечения к врачу-гематологу или врачу-онкологу.
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Выбор вида терапии при синдроме Сезари должен базироваться на определении степени тяжести заболевания (учитываются степень инфильтрации кожи, наличие/отсутствие кожных узлов, выраженность лимфаденопатии, степень интенсивности вовлечения крови, уровень лактатдегирогеназы и лейкоцитов в периферической крови), скорости его прогрессирования и влияния на качество жизни пациента. Принципы назначения терапии пациентам с синдромом Сезари:
- Подходы к лечению определяются массой опухоли и скоростью прогрессии
- По возможности необходимо избегать подавления иммунного ответа
- При необходимости системного лечения предпочтительно назначение иммуномодулирующей терапии, а не химиотерапии
- Комбинированная или мультимодальная (например, сочетание системной иммуномодулирующей и наружной) терапия более эффективна, чем любая монотерапия
- Своевременная диагностика и лечение инфекционных осложнений (иногда даже при отсутствии клинических признаков инфекционного процесса на коже) приводит к улучшению состояния пациента
Большое значение имеет лечение зуда, значительно снижающего качество жизни.
1. Консервативное лечение
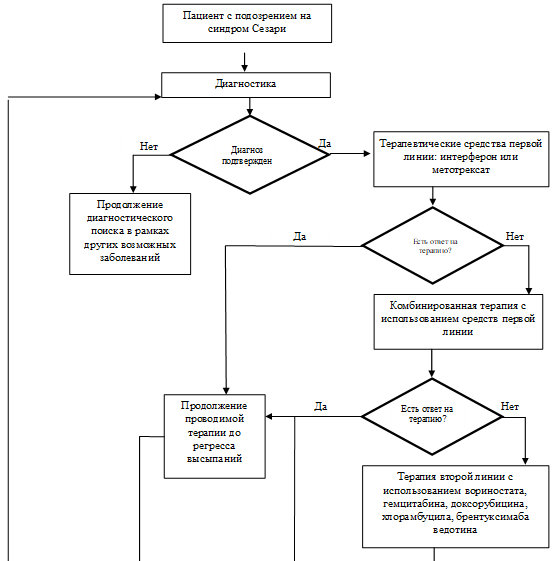
Выделяют терапию пациентов с синдромом Сезари первой линии и второй линии. Терапевтическими средствами первой линии начинают терапию пациентов с синдромом Сезари. В случае, если средство терапии первой линии недостаточно эффективно, возможна комбинированная терапия средствами первой линии.
Вторая линия терапии применяется при отсутствии ответа на лечение, рефрактерном течении заболевания или его прогрессировании, несмотря на проведенное лечение первой линии. Выбор лечения зависит от возраста пациента, степени тяжести поражения крови, общего соматического статуса и предыдущих методов терапии.
- Рекомендуются для терапии первой линии пациентов с синдромом Сезари интерфероны (в дозе 3–18 млн МЕ методом внутримышечного или подкожного введения лекарственного препарата для #интерферона альфа-2b** каждый день или три раза в неделю или в дозе 65-180 мкг методом подкожного введения лекарственного препарата для #пэгинтерферона альфа-2a** один раз в неделю) [7, 8, 30, 36, 37, 57].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: При непереносимости высоких доз интерфероны назначают 3–6 млн МЕ ежедневно или 3 раза в неделю. При применении препарата возможны отклонения от нормы лабораторных показателей, проявляющиеся лейкопенией, лимфопенией, тромбоцитопенией, анемией, повышением активности аланинаминотрансферазы, щелочной фосфатазы, концентрации креатинина, мочевой кислоты. В случае появления признаков нарушения функции печени за больным необходимо установить тщательное наблюдение. При прогрессировании симптомов введение препарата следует прекратить. На фоне длительного приема препарата возможны изменения со стороны щитовидной железы. У пациентов с заболеваниями щитовидной железы перед началом лечения необходимо проведение исследования уровня тиреотропного гормона (ТТГ) в крови, рекомендуется контролировать его уровень не реже 1 раза в 6 месяцев. Очень редко – сахарный диабет. При длительном применении, обычно после нескольких месяцев лечения, возможны нарушения со стороны органа зрения. До начала терапии рекомендуется провести офтальмологическое обследование. При жалобах на любые офтальмологические нарушения необходима немедленная консультация врача-офтальмолога. Пациентам с заболеваниями, при которых могут происходить изменения в сетчатке, например, с сахарным диабетом или артериальной гипертензией, необходимо проходить офтальмологический осмотр не реже 1 раза в 6 месяцев. Пациентам с заболеваниями сердечно-сосудистой системы и/или прогрессирующими онкологическими заболеваниями требуется тщательное наблюдение и периодическая регистрация электрокардиограммы. В случае появления изменений со стороны психической сферы и/или ЦНС, включая развитие депрессии, рекомендуется наблюдение врача-психиатра в период лечения, а также в течение 6 месяцев после его окончания.
или
#метотрексат** перорально в дозе менее 25-75 мг в неделю [7, 8, 36, 38,39]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Перед началом лечения #метотрексатом** или при возобновлении терапии после перерыва необходимо проводить общий (клинический) анализ крови развернутый, оценивать активность «печеночных» ферментов, концентрацию билирубина, альбумина сыворотки, а также прицельное рентгенографическое исследование органов грудной клетки и функциональные почечные тесты. При наличии клинических показаний назначают исследования с целью исключения и гепатита.
В процессе лечения #метотрексатом** (ежемесячно в первые 6 месяцев и не реже, чем каждые 3 месяца в дальнейшем, при повышении доз целесообразно повышать частоту обследований) проводят следующие исследования:
1. Осмотр ротовой полости и горла для выявления изменений слизистых оболочек.
2. Общий (клинический) анализ крови развернутый Даже при применении в обычных терапевтических дозах #метотрексат** может внезапно вызвать угнетение системы кроветворения. В случае значительного снижения количества лейкоцитов или тромбоцитов лечение #метотрексатом** немедленно прекращают и назначают симптоматическую поддерживающую терапию.
3. Функциональные печеночные пробы, а именно определение активности аспартатаминотрансферазы и аланинаминотрансферазы, щелочной фосфотазы в крови, проведение исследования уровня билирубина связанного (коньюгированного), билирубина свободного (неконьюгированного), креатинина и альбумина в крови. Особое внимание необходимо уделять выявлению признаков повреждения печени. Лечение #метотрексатом** не следует начинать или необходимо приостанавливать в случае любых отклонений результатов функциональных печеночных тестов или биопсии печени. Обычно показатели нормализуются в течение 2 недель, после чего лечение по решению может быть возобновлено.
4. Функциональные почечные пробы, а именно исследование уровня мочевины, мочевой кислоты, креатинина, а также уровня натрия, калия, общего кальция, хлоридов в крови и проведение общего (клинического) анализа мочи. Поскольку #метотрексат** экскретируется преимущественно почками, у пациентов с нарушениями функции почек может наблюдаться повышение концентрации #метотрексата** в крови, следствием чего могут быть тяжелые побочные реакции. Необходимо тщательно контролировать состояние пациентов, у которых возможны нарушения функции почек (например, пожилых пациентов).
5. Поскольку #метотрексат** оказывает воздействие на иммунную систему, он может изменять реакцию на вакцинацию и влиять на результаты иммунологических тестов. Особая осторожность необходима при лечении пациентов с неактивными, хроническими инфекциями (такими как опоясывающий лишай, туберкулез, вирусный гепатит В или С) ввиду их возможной активации. В период лечения #метотрексатом** не следует проводить вакцинацию живыми вакцинами.
В связи с возможностью активации хронической инфекции пациентам, которым планируется или проводится терапия #метотрексатом**, может потребоваться определение антител к поверхностному антигену (HBsAg) вируса гепатита B (Hepatitis B virus), определение антител к вирусу гепатита C (Hepatitis C virus) в крови с целью выявления противопоказаний к системной терапии #метотрексатом**.
- Рекомендуется при недостаточной эффективности монотерапии первой линии комбинированная терапия с применением лекарственных средств первой линии [7, 8, 36]:
#интерфероны (в дозах, указанных для первой линии терапии, методом подкожного введения лекарственного препарата для #пэгинтерферона альфа-2a**, и методом внутримышечного или подкожного введения лекарственного препарата для #интерферона альфа-2b**) в сочетании с фотохимиотерапией с внутренним применением фотосенсибилизаторов [7, 8, 36, 40, 41]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
или
#метотрексат** перорально в дозе не более 100 мг в неделю в сочетании с кортикостероидами, применяемыми в дерматологии [7, 8, 36,39]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
или
#интерфероны (в дозах, указанных для первой линии терапии, подкожно #пэгинтерферон альфа-2a**, внутримышечно или подкожно для #интерферон альфа-2b) в сочетании с #метотрексатом** перорально [7, 8, 36, 42]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
- Рекомендуется при неэффективности монотерапии первой линии или при неэффективности комбинированной терапии с применением средств первой линии терапия второй линии:
противоопухолевые препараты в сочетании с кортикостероидами системного действия [7, 8, 36]:
#хлорамбуцил** 2–6 мг в сутки перорально + #преднизолон** 20 мг в сутки перорально [7, 8, 36]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Во время терапии #хлорамбуцилом** следует учитывать возможность развития нежелательных явлений со стороны системы кроветворения, желудочно-кишечного тракта, мочевыделительной системы и прочие. Наиболее частыми нежелательными эффектами терапии #хлорамбуцилом** являются лейкопения (обратима, если прием препарата прекращен своевременно), тромбоцитопения, лимфопения, нейтропения, снижение содержания гемоглобина Необратимое угнетение функции костного мозга развивается крайне редко. Редко отмечаются гепатотоксическое действие токсико-аллергического генеза (гепатонекроз или цирроз, холестаз, желтуха), гиперурикемия или нефропатия, обусловленная повышенным образованием мочевой кислоты.
Во время терапии #преднизолоном** возможно развитие нежелательных явлений, требующих контроля, – снижение толерантности к глюкозе, «стероидный» сахарный диабет или манифестация латентного сахарного диабета, угнетение функции надпочечников, задержка жидкости и ионов натрия (периферические отеки), гипернатриемия, гипокалиемический синдром (гипокалиемия, аритмия, миалгия или спазм мышц, необычная слабость и утомляемость), в редких случаях – повышение активности «печеночных» трансаминаз и щелочной фосфатазы. Возможна также лейкоцитурия.
или
противоопухолевые препараты:
вориностат перорально по 400 мг ежедневно до достижения полного контроля (отсутствие признаков дальнейшего прогрессирования) или же до появления признаков неприемлемой токсичности [7, 8, 36, 43, 44]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Противопоказанием является детский возраст до 18 лет. При приеме вориностата возможно развитие тромбоцитопении и анемии, которые могут потребовать прекращения приема препарата или прекращения лечения. Возможно развитие лейкопении и нейтропении, требующих уменьшения дозы препарата. Отмечалось увеличение плазменной концентрации креатинина. Возможно также развитие гипокалиемии и увеличения плазменной концентрации креатинина, что может потребовать снижения дозы препарата. На фоне приема вориностата отмечались гипергликемия, в связи с чем может потребоваться назначение диеты и/или гипогликемической терапии. Возможно развитие протеинурии.
или
#доксорубицин** 20 мг/м2 внутривенно каждые 2 недели [7, 8, 36; 44]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Следует учитывать и контролировать нежелательные явления, которые могут возникнуть во время терапии #доксорубицином**, – лейкопения, нейтропения, тромбоцитопения и анемия, повышение активности «печеночных» трансаминаз, гипербилирубинемия. токсическое поражение сердца. Для снижения риска тяжелого токсического поражения сердца рекомендуется до начала и во время терапии #доксорубицином** проводить регулярный контроль кардиальных функций, включая оценку фракции выброса левого желудочка с помощью эхокардиографии или многоканальной радиоизотопной ангиографии, а также ЭКГ-контроль. Редким нежелательным явлением терапии #доксорубицином** является острая почечная недостаточность
или
#гемцитабин** 1200 мг/м2 в 1, 8 и 15 день 28-дневного цикла (3–6 курсов) [7, 8, 36; 44].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
или
#гемцитабин** в малых дозах с продолжительной инфузией в дозе 250 мг/м2 в течение 6 часов 1 раз в неделю [56]
Уровень убедительности рекомендаций С (уровень достоверности доказательств –4)
Комментарии: Следует учитывать и контролировать нежелательные явления, которые могут возникнуть во время терапии #гемцитабином**, – лейкопения (миелосупрессия обычно имеет легкую или умеренную степень и проявляется главным образом изменением концентрации гранулоцитов), тромбоцитопения, анемия, часто — фебрильная нейтропения, очень редко — тромбоцитоз. Возможно гепатотоксическое действие, проявляющееся повышением активности «печеночных» трансаминаз и щелочной фосфатазы, повышением концентрации билирубина, нечасто – с развитием печеночной недостаточности и смерти. Нежелательные явления со стороны мочеполовой системы очень часто – гематурия, протеинурия легкой степени, часто — острая почечная недостаточность, гемолитический уремический синдром.
- Рекомендуется пациентам 18 лет и старше при отсутствии или недостаточном эффекте после минимум одной линии предшествующей системной терапии и наличии экспрессии CD30 + антигена:
брентуксимаб ведотин** в дозе 1,8 мг/кг внутривенно каждый 21 день. Лечение проводят в течение 8 циклов, при достижении частичного ответа допускается проведение еще 8 циклов [31]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: При достижении постепенного клинического разрешения возможно продолжение терапии в сниженной дозе 1,2 мг/кг массы тела. При появлении побочных эффектов (наиболее часто – периферическая полинейропатия), допустимо снижение дозы до 1,2 мг/кг и увеличение интервала между циклами. При лечении брентуксимабом ведотином** может развиться анемия, тромбоцитопения и тяжелая пролонгированная (≥1 недели) нейтропения, и это может увеличить риск тяжелых инфекций. Были зарегистрированы случаи повышения уровней аланинаминотрансферазы и аспартатаминотрансферазы. Гипергликемия была зарегистрирована в клинических исследованиях у пациентов с увеличенным индексом массы тела, как с наличием, так и с отсутствием сахарного диабета в анамнезе.
2. Хирургическое лечение
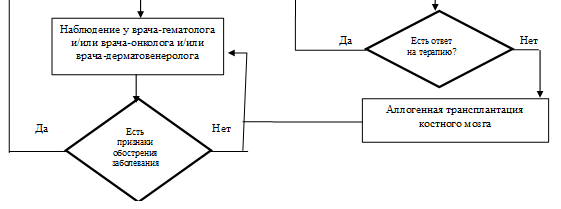
- Рекомендуется пациентам моложе 60 лет при агрессивном течении СС и при отсутствии эффекта от стандартных режимов терапии при условии достижения частичной или полной ремиссии на предтрансплантационном этапе, аллогенная трансплантация костного мозга при агрессивном течении синдрома Сезари [45–48].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Использование аллогенной трансплантации костного мозга не проводится пациентам пожилого возраста.
3. Иное лечение
- Рекомендуются пациентам с жалобами на зуд для уменьшения интенсивности зуда антигистаминные средства системного действия [49–51].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: При интенсивном зуде предпочтительным является парентеральное введение антигистаминных средств системного действия, согласно инструкции
- Рекомендуются пациентам с жалобами на боли анальгетики или нестероидные противовоспалительные и противоревматические препараты [52]:
парацетамол** перорально детям в возрасте от 12 лет и взрослым 500–1000 мг 2–4 раза в сутки [52]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
или
целекоксиб перорально в начальной дозе 400 мг, с последующим, при необходимости, приемом дополнительной дозы в 200 мг в первый день. В последующие дни – по 200 мг 2 раза в сутки [52] .
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Пациентам с синдромом Сезари при возникновении острого или хронического болевого синдрома необходимо провести диагностику причины болевого синдрома и последующую патогенетическую или симптоматическую терапию болевого синдрома в соответствии с существующими профильными рекомендациями [53, 54].
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- Методов реабилитации при синдроме Сезари не существует. Тем не менее, всем пациентам с синдромом Сезари на всех этапах терапии заболевания, а также после завершения лекарственного лечения рекомендована комплексная реабилитация, а также, при необходимости, поддерживающая терапия. [55].
Уровень убедительности рекомендаций ¬С (уровень достоверности доказательств – 5)
Комментарии: Реабилитация пациентов с синдромом Сезари должна охватывать не только медицинские, но и социально-психологические аспекты адаптации пациента к нормальной жизни. Такая реабилитация требует, кроме медицинской помощи, обязательного участия социальных работников и медицинских психологов. Программы реабилитации разрабатываются индивидуально, в зависимости от выявленных осложнений лекарственного лечения, сопутствующей патологии, социальных и психологических проблем.
Реабилитация при возникновении осложнений в течение заболевания и лечения проводится в рамках соответствующих нозологий.
Пациентам даются рекомендации вести здоровый образ жизни, исключить избыточную инсоляцию и тепловые физиМедицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Госпитализация
Организация оказания медицинской помощи
В рамках оказания первичной врачебной медико-санитарной помощи, врачи-терапевты участковые, врачи общей практики (семейные врачи) при выявлении у пациентов высыпаний на коже, кожного зуда, выявлении симптомов или признаков синдрома Сезари направляют пациента в медицинскую организацию дерматовенерологического профиля или кабинет врача-онколога/ врача-гематолога для оказания ему первичной специализированной медико-санитарной помощи, а также осуществляют оказание медицинской помощи в соответствии с рекомендациями медицинской организации дерматовенерологического профиля и/или врача онколога/ гематолога.
При невозможности оказания медицинской помощи в рамках первичной специализированной медико-санитарной помощи и наличии медицинских показаний пациент направляется в медицинскую организацию, оказывающую специализированную медицинскую помощь.
Специализированная, в том числе высокотехнологичная, медицинская помощь оказывается врачом-дерматовенерологом и/или врачом-гематологом и/или врачом-онкологом в стационарных условиях.
Показания для плановой госпитализации в медицинскую организацию:
1) Показания для оказания медицинской помощи в дневном стационаре:
- недостаточная эффективность лечения, проводимого в амбулаторных условиях
- обследование пациента, включающее биопсию и другие инвазивные вмешательства, в случаях, когда оно не может быть проведено амбулаторно.
2) Показания для оказания медицинской помощи в стационарных условиях:
- отсутствие эффекта от проводимого лечения в амбулаторных условиях;
- необходимость системной терапии;
- обследование пациента, включающее биопсию и другие инвазивные вмешательства, в случаях, когда оно не может быть проведено амбулаторно.
3) Показания к экстренной госпитализации в стационар медицинской организации, оказывающей специализированную, в том числе высокотехнологичную, медицинскую помощь по профилю «гематология» и «онкология»:
- Развитие тяжелой инфекции (необязательна госпитализация в гематологический стационар).
- Развитие угрожающих жизни цитопений (глубокой анемии, геморрагического синдрома, нейтропении).
- Развитие осложнений синдрома Сезари, угрожающих жизни.
- Развитие осложнений терапии, включая синдром лизиса опухоли, тяжелые инфузионные реакции, миелотоксический агранулоцитоз с лихорадкой и другие осложнения, угрожающие жизни.
Показания к выписке пациента из медицинской организации:
- частичный или полный регресс высыпаний.
- завершение курса лечения или одного из этапов оказания специализированной, в том числе высокотехнологичной, медицинской помощи, в условиях круглосуточного или дневного стационара при условии отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Методов профилактики синдрома Сезари в настоящее время не существует, поскольку неизвестен этиологический фактор(ы), ведущий к развитию заболевания. Диспансерное наблюдение врачом-гематологом или врачом-онкологом осуществляется в период лечения и после достижения ремиссии лимфомы. Обезболивание осуществляется в соответствии со стандартами оказания паллиативной помощи.
- Рекомендуется каждые 6 месяцев проведение обследования (физикальный осмотр с картированием кожи, УЗИ периферических лимфатических узлов, компьютерная томография органов грудной полости, брюшной полости и малого таза) [25].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: Тактика лечения рецидивов базируется на определении стадии заболевания, учитывается развитие резистентности к предыдущим видам терапии.
Информация
Источники и литература
-
Клинические рекомендации Российского общества онкогематологов
- Клинические рекомендации Российского общества онкогематологов - 1. Dummer R., Heald P.W., Nestle F.O. et al. Sezary syndrome T-cell clones display T-helper 2 cytokines and express the accessory factor-1 (interferon-gamma receptor beta-chain). Blood. 1996; 88 (4): 1383-1389. 2. Campbell J.J., Clark R.A., Watanabe R., Kupper T.S. Sezary syndrome and mycosis fungoides arise from distinct T-cell subsets: a biologic rationale for their distinct clinical behaviors. Blood. 2010; 116 (5): 767-771. 3. da Silva Almeida A.C., Abate F., Khiabanian H. et al. The mutational landscape of cutaneous T cell lymphoma and Sezary syndrome. Nat Genet. 2015; 47 (12): 1465-1470. 4. Wang L., Ni X., Covington K.R. et al. Genomic profiling of Sezary syndrome identifies alterations of key T cell signaling and differentiation genes. Nat Genet. 2015; 47 (12): 1426-1434. 5. Ungewickell A., Bhaduri A., Rios E. et al. Genomic analysis of mycosis fungoides and Sezary syndrome identifies recurrent alterations in TNFR2. Nat Genet. 2015; 47 (9): 1056-1060. 6. Berger C.L., Tigelaar R., Cohen J. et al. Cutaneous T-cell lymphoma: malignant proliferation of T-regulatory cells. Blood. 2005; 105 (4): 1640-1647. 7. Spicknall K.E. Sezary syndrome - clinical and histopathologic features, differential diagnosis, and treatment. Semin Cutan Med Surg 2018; 37: 18-23. 8. Olsen E.A., Rook A.H., Zic J. et al. Sezary syndrome: immunopathogenesis, literature review of therapeutic options, and recommendations for therapy by the United States Cutaneous Lymphoma Consortium (USCLC). J Am Acad Dermatol. 2011; 64 (2): 352 404. 9. Willemze R., Jaffe E.S., Burg G. et al. WHO-EORTC classification for cutaneous lymphomas. Blood. 2005; 105 (10): 3768-3785. 10. Kubica A.W., Davis M.D., Weaver A.L. et al. Sezary syndrome: a study of 176 patients at Mayo Clinic. J Am Acad Dermatol. 2012; 67 (6): 1189-1199. 11. Hristov A.C., Tejasvi T., Wilcox R.A. Mycosis fungoides and Sezary syndrome: 2019 update on diagnosis, risk-stratification, and management. Am J Hematol. 2019; 94: 1027-1041. 12. Sentis H.J., Willemze R., Scheffer E. Histopathologic studies in Sezary syndrome and erythrodermic mycosis fungoides: a comparison with benign forms of erythroderma. J Am Acad Dermatol. 1986; 15 (6): 1217-1226. 13. Trotter M.J., Whittaker S.J., Orchard G.E, Smith N.P. Cutaneous histopathology of Sezary syndrome: a study of 41 cases with a proven circulating T-cell clone. J Cutan Pathol. 1997; 24 (5): 286-291. 14. Klemke C.D., Booken N., Weiss C. et al. Histopathological and immunophenotypical criteria for the diagnosis of Sezary syndrome in differentiation from other erythrodermic skin diseases: a European Organisation for Research and Treatment of Cancer (EORTC) Cutaneous Lymphoma Task Force Study of 97 cases. Br J Dermatol. 2015; 173 (1): 93 105. 15. Diwan A.H., Prieto V.G., Herling M. et al. Primary Sezary syndrome commonly shows low-grade cytologic atypia and an absence of epidermotropism. Am J Clin Pathol. 2005; 123 (4): 510-515. 16. Morice W.G., Katzmann J.A., Pittelkow M.R. et al. A comparison of morphologic features, flow cytometry, TCR-Vbeta analysis, and TCR-PCR in qualitative and quantitative assessment of peripheral blood involvement by Sezary syndrome. Am J Clin Pathol. 2006; 125 (3): 364-374. 17. Feng B., Jorgensen J.L., Jones D. et al. Flow cytometric detection of peripheral blood involvement by mycosis fungoides and Sezary syndrome using T-cell receptor Vbeta chain antibodies and its application in blood staging. Mod Pathol. 2010; 23 (2): 284-295. 18. Olsen E., Vonderheid E., Pimpinelli N. et al. Revisions to the staging and classification of mycosis fungoides and Sezary syndrome: a proposal of the International Society for Cutaneous Lymphomas (ISCL) and the Cutaneous Lymphoma Task Force of the European Organization of Research and Treatment of Cancer (EORTC). Blood. 2007; 110 (6): 1713-1722. 19. Виноградова Ю.Е., Цыба Н.Н., Гилязитдинова Е.А. и др. Опыт лечения грибовидного микоза и синдрома Сезари в зависимости от стадий заболевания. Результаты собственных исследований и обзор литературы. Клиническая онкогематология 2009; 2 (4): 326-333. 20. Карамова А.Э., Чикин В.В., Знаменская Л.Ф., Воронцова А.А. Т-клеточные лимфомы кожи: дифференциальная диагностика эритродермических состояний. Вестник дерматологии и венерологии. 2019; 95 (5): 24-32. 21. Ponti R., Quaglino P., Novelli M. et al. T-cell receptor gamma gene rearrangement by multiplex polymerase chain reaction/heteroduplex analysis in patients with cutaneous T-cell lymphoma (mycosis fungoides/Sezary syndrome) and benign inflammatory disease: correlation with clinical, histological and immunophenotypical findings. Br J Dermatol. 2005; 153 (3): 565-573. 22. Kirsch I.R., Watanabe R., O’Malley J.T. et al. TCR sequencing facilitates diagnosis and identifies mature T cells as the cell of origin in CTCL. Sci Transl Med. 2015; 7 (308): 308ra158. 23. Vonderheid E.C. On the diagnosis of erythrodermic cutaneous T-cell lymphoma. J Cutan Pathol. 2006; 33 (Suppl 1): 27-42. 24. Mann B.S., Johnson J.R, Cohen M.H. et al. FDA approval summary: vorinostat for treatment of advanced primary cutaneous T-cell lymphoma. Oncologist 2007; 12 (10): 1247-1252. 25. Лезвинская Е.М., Вавилов А.М. Лимфопролиферативные опухоли кожи: руководство для врачей. - М.: Практическая медицина, 2010. - 366 с. 26. Wallace C.A., Sherry D.D. A practical approach to avoidance of methotrexate toxicity [editorial] J Rheumatol. 1995; 22: 1009-1012. 27. Wood G.S., Wu J. Methotrexate and pralatrexate. Dermatol Clin. 2015; 33 (4): 747-755. 28. Busger op Vollenbroek F.T., Doggen C.J., Janssens R.W., Bernelot Moens H.J. Dermatological guidelines for monitoring methotrexate treatment reduce drug-survival compared to rheumatological guidelines. PLoS ONE 2018; 13 (3): e0194401. 29. Ahmadzadeh A., Zamani N., Hassanian-Moghaddam H. et al. Acute versus chronic methotrexate poisoning; a cross-sectional study. BMC Pharmacol Toxicol 2019; 20 (1): 39. 30. Olsen E.A. Interferon in the treatment of cutaneous T-cell lymphoma. Dermatol Ther 2003; 16: 311-321. 31. Kim Y.H., Tavallaee M., Sundram U. et al. Phase II investigator-initiated study of brentuximab vedotin in mycosis fungoides and Sezary syndrome with variable CD30 expression level: a multi-institution collaborative project. J Clin Oncol. 2015; 33 (32): 3750-3758. 32. Talpur R., Singh L., Daulat S. et al. Long-term outcomes of 1,263 patients with mycosis fungoidesand Sezary syndrome from 1982 to 2009. Clin Cancer Res. 2012; 18 (18): 5051-5060. 33. Gobbi P.G., Broglia C., Carnevale Maffe G. et al. Lymphomatous superficial lymph nodes: limitations of physical examination for accurate staging and response assessment. Haematologica. 2002; 87 (11): 1151-1156. 34. Tsai E.Y., Taur A., Espinosa L. et al. Staging accuracy in mycosis fungoides and sezary syndrome using integrated positron emission tomography and computed tomography. Arch Dermatol. 2006; 142 (5): 577-584. 35. Toro J.R., Stoll H.L. Jr, Stomper P.C., Oseroff A.R. Prognostic factors and evaluation of mycosis fungoides and Sezary syndrome. J Am Acad Dermatol 1997; 37 (1): 58-67. 36. Trautinger F., Eder J., Assaf C. et al. European Organisation for Research and Treatment of Cancer consensus recommendations for the treatment of mycosis fungoides/Sezary syndrome - Update 2017. Eur J Cancer. 2017; 77: 57-74. 37. Виноградова Ю.Е. Применение интерферона-а при Т-клеточных лимфомах кожи. Гематология и трансфузиология 2012: 57 (3): 99-100. 38. Zackheim H.S. Epstein E.H. Jr. Low-dose methotrexate for the Sezary syndrome. J Am Acad Dermatol. 1989; 21 (4 Pt 1): 757-762. 39. Zackheim HS, Kashani-Sabet M, McMillan A. Low-dose methotrexate to treat mycosis fungoides: a retrospective study in 69 patients. J Am Acad Dermatol. 2003 Nov;49(5):873-8. doi: 10.1016/s0190-9622(03)01591-3. PMID: 14576667 40. Roenigk H.H. Jr, Kuzel T.M., Skoutelis A.P. et al. Photochemotherapy alone or combined with interferon alpha-2a in the treatment of cutaneous T-cell lymphoma. J Invest Dermatol 1990; 95 (6 Suppl); 198S-205S. 41. Kuzel T.M., Gilyon K., Springer E. et al. Interferon alfa-2a combined with phototherapy in the treatment of cutaneous T-cell lymphoma. J Natl Cancer Inst 1990; 82 (3); 203 207. 42. Aviles A., Nambo M.J., Neri N. et al. Interferon and low dose methotrexate improve outcome in refractory mycosis fungoides/Sezary syndrome. Cancer Biother Radiopharm 2007; 22 (6); 836-840. 43. Чернова Н.Г., Коломейцев О.А. Современные возможности оптимизации лечения грибовидного микоза и синдрома Сезари. Клиническая онкогематология. 2018;11 (1): 34-41. 44. Photiou L., van der Weyden C., McCormack C., Prince H.M. Systemic treatment options for advanced-stage mycosis fungoides and Sezary syndrome. Curr Oncol Rep. 2018; 20 (4):32. 45. Shiratori S., Fujimoto K., Nishimura M. et al. Allogeneic hematopoietic stem cell transplantation following reduced-intensity conditioning for mycosis fungoides and Sezary syndrome. Hematol Oncol 2016; 34 (1): 9-16. 46. Wu P.A., Kim Y.H., Lavori P.W. et al. A meta-analysis of patients receiving allogeneic or autologous hematopoietic stem cell transplant in mycosis fungoides and Sezary syndrome. Biol Blood Marrow Transplant 2009; 15 (8): 982-990. 47. Virmani P., Zain J., Rosen S.T., Hematopoietic stem cell transplantation for mycosis fungoides and Sezary syndrome. Dermatol Clin 2015; 33: 807-818. 48. Lechowicz M.J., Lazarus H.M., Carreras J. et al. Allogeneic hematopoietic cell transplantation for mycosis fungoides and Sezary syndrome. Bone Marrow Transplant 2014; 49 (11): 1360-1365. 49. Serrano L., Martinez-Escala M.E., Zhou X.A., Guitart J. Pruritus in cutaneous T-cell lymphoma and its management. Dermatol Clin 2018; 36: 245-258. 50. Schulz S., Metz M., Siepmann D. et al. Antipruritische Wirksamkeit einer hoch dosierten Antihistaminikatherapie. Hautarzt 2009; 60: 564-568. 51. Weisshaar E., Szepietowski J.C., Dalgard F.J. et al. European S2k guideline on chronic pruritus. Acta Derm Venereol. 2019; 99 (5): 469-506. 52. Левченко О.К. Опыт оказания противоболевой помощи в гематологическом стационаре. Российский журнал боли. 2019; 17 (1): 47-50. 53. Абузарова Г.Р, Невзорова Д.В., Кумирова Э.В. и др. Обезболивание взрослых и детей при оказании медицинской помощи. Методические рекомендации. ФГБОУ ВО РНИМУ им. Н.И.Пирогова Минздрава России, Москва, 2016, 94 с. 54. Абузарова Г.Р. и др. Лечение болевого синдрома у онкологических больных. Российские клинические рекомендации по диагностике и лечению злокачественны лимфопролиферативных заболеваний. Под редакцией И.В Поддубной, В.Г. Савченко, 2018, С.278-288. 55. Paul K.L. Rehabilitation and exercise considerations in hematologic malignancies. // Am. J. Phys. Med. Rehabil. 2011. Vol. 90, № 5 Suppl 1. P. S88-94. 56. Горенкова Л.Г., Пенская Е.А., Кравченко С.К., Ковригина А.М., Моисеева Т.Н., Воробьев А.И. Лечение резистентных форм грибовидного микоза и синдрома сезари. Клиническая онкогематология. Фундаментальные исследования и клиническая практика. 2017; 10 ( 3): 366-371 57. Gosmann J. et al. Use of Pegylated Interferon Alpha-2a in Cutaneous T-cell Lymphoma: A Retrospective Case Collection //Acta Dermato-venereologica. - 2023. - Т. 103.
Информация
Список сокращений
ПУВА – псорален+ультрафиолетовое облучение спектра А
РФП – радиофармпрепарат
ТОК – тотальное облучение кожи
ТКР – Т-клеточный рецептор
Э-КТКЛ – эритродермическая кожная Т-клеточная лимфома
Термины и определения
Синдром Сезари – Т-клеточная лимфома кожи, характеризующаяся эритродермией, генерализованной лимфаденопатией и наличием в крови циркулирующих злокачественных Т-лимфоцитов (клеток Сезари).
Факторами, влияющими на прогноз заболевания, являются:
-
возраст пациента
-
повышение уровня ЛДГ крови
-
поражение лимфатических узлов
-
степень тяжести вовлечения крови
Критерии оценки качества медицинской помощи
Критерии оценки качества медицинской помощи синдром Сезари (амбулаторный этап)
|
№
|
Критерии качества
|
Оценка выполнения
|
|---|---|---|
|
1
|
Пациенту с подозрением на синдром Сезари (СС) или с выявленным СС при первичном или повторном приеме, при контрольных исследованиях, а также при рецидиве или прогрессировании, выполнен общий (клинический) анализ крови развернутый для выявления заболеваний и состояний, являющихся противопоказаниями к проведению системной терапии метотрексатом**, пэгинтерфероном альфа-2a**, интерфероном альфа-2b**, вориностатом, хлорамбуцилом**, преднизолоном**, доксорубицином**, гемцитабином**, брентуксимаб ведотином** или ультрафиолетового облучения кожи
|
Да\Нет
|
|
2
|
Пациенту с подозрением на СС для верификации диагноза СС, а также при нееобходимости контроля эффективности терапии выполнено патолого-анатомическое исследование биопсийного (операционного) материала кожи.
|
Да\Нет
|
|
3
|
При наличии у пациента клинических и гистологических проявлений СС для выявления признаков злокачественной трансформации лимфоцитов, инфильтрирующих кожу, выполнено патолого-анатомическое исследование биопсийного (операционного) материала кожи с применением иммуногистохимических методов
|
Да\Нет
|
|
4
|
Пациенту с подозрением на СС или с выявленным СС, а также при рецидиве или прогрессировании, при установлении диагноза или для оценки эффективности в период терапии (при выявлении патологических изменений), выполнены инструментальные методы исследования (ультразвуковое исследование лимфатических узлов (одна анатомическая область), компьютерная томография органов грудной полости, компьютерная томография органов брюшной полости и забрюшинного пространства.
|
Да\Нет
|
|
5
|
Пациенту с подозрением на поражение костного мозга при установлении диагноза СС выполнено патолого-анатомическое исследование биопсийного (операционного) материала костного мозга
|
Да\Нет
|
|
6
|
Пациенту с впервые выявленным СС выполнено иммунофенотипирование периферической крови для выявления субпопуляционного состава лимфоцитов (основные и/или малые) и иммунофенотипирование гемопоэтических клеток-предшественниц в костном мозге
|
Да\Нет
|
|
7
|
Пациенту с впервые выявленным СС, при рецидиве или прогрессировании, выполнена системная терапия #метотрексатом**и/или интерферонами и/или вориностатом и/или #преднизолоном** и/или #доксорубицином** и/или #гемцитабином** и/или брентуксимабом ведотином** или комбинированная терапия интерферонами и фототерапией
|
Да\Нет
|
Критерии оценки качества медицинской помощи синдром Сезари (стационарный этап)
|
№
|
Критерии качества
|
Оценка выполнения
|
|---|---|---|
|
1
|
Пациенту с подозрением на синдром Сезари (СС) или с выявленным СС при первичном или повторном приеме, при контрольных исследованиях, а также при рецидиве или прогрессировании, выполнен общий (клинический) анализ крови развернутый для выявления заболеваний и состояний, являющихся противопоказаниями к проведению системной терапии метотрексатом**, пэгинтерфероном альфа-2a**, интерфероном альфа-2b**, вориностатом, хлорамбуцилом**, преднизолоном**, доксорубицином**, гемцитабином**, брентуксимаб ведотином** или ультрафиолетового облучения кожи
|
Да\Нет
|
|
2
|
Пациенту с подозрением на СС для верификации диагноза СС, а также при необходимости контроля эффективности терапии выполнено патолого-анатомическое исследование биопсийного (операционного) материала кожи (если не выполнено в амбулаторных условиях).
|
Да\Нет
|
|
3
|
При наличии у пациента клинических и гистологических проявлений СС для выявления признаков злокачественной трансформации лимфоцитов, инфильтрирующих кожу, выполнено патолого-анатомическое исследование биопсийного (операционного) материала кожи с применением иммуногистохимических методов (если не выполнено в амбулаторных условиях)
|
Да\Нет
|
|
4
|
Пациенту с подозрением на СС или с выявленным СС, а также при рецидиве или прогрессировании, при установлении диагноза или для оценки эффективности в период терапии (при выявлении патологических изменений), выполнены инструментальные методы исследования (ультразвуковое исследование лимфатических узлов (одна анатомическая область), компьютерная томография органов грудной полости, компьютерная томография органов брюшной полости и забрюшинного пространства), если не выполнено в амбулаторных условиях.
|
Да\Нет
|
|
5
|
Пациенту с впервые выявленным СС выполнено иммунофенотипирование периферической крови для выявления субпопуляционного состава лимфоцитов (основные и/или малые) и иммунофенотипирование гемопоэтических клеток-предшественниц в костном мозге (если не выполнено в амбулаторных условиях).
|
Да\Нет
|
|
6
|
Пациенту с впервые выявленным СС, при рецидиве или прогрессировании, выполнена системная терапия #метотрексатом**и/или интерферонами и/или вориностатом и/или #преднизолоном** и/или #доксорубицином** и/или #гемцитабином** и/или брентуксимабом ведотином** или комбинированная терапия интерферонами и фототерапией.
|
Да\Нет
|
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
-
Кубанов Алексей Алексеевич – академик РАН, доктор медицинских наук, профессор, президент Российского общества дерматовенерологов и косметологов.
-
Поддубная Ирина Владимировна – академик РАН, заслуженный деятель образования РФ, доктор медицинских наук, профессор, председатель Российского общества онкогематологов.
-
Белоусова Ирена Эдуардовна – доктор медицинских наук, член Российского общества дерматовенерологов и косметологов.
-
Самцов Алексей Викторович – доктор медицинских наук, профессор, Заслуженный деятель науки РФ, Заслуженный врач РФ, член Российского общества дерматовенерологов и косметологов.
-
Знаменская Людмила Федоровна – доктор медицинских наук, член Российского общества дерматовенерологов и косметологов.
-
Чикин Вадим Викторович – доктор медицинских наук, член Российского общества дерматовенерологов и косметологов.
-
Карамова Арфеня Эдуардовна – кандидат медицинских наук, член Российского общества дерматовенерологов и косметологов.
-
Кузьмин Алексей Александрович, главный врач КОГКБУЗ «Центр онкологии и медицинской радиологии», г. Киров.
-
Горенкова Лилия Гамилевна – кандидат медицинских наук, член общества Ассоциации содействия развитию гематологии и трансплантологии костного мозга «Национальное гематологическое общество».
-
Кравченко Сергей Кириллович – кандидат медицинских наук, член общества Ассоциации содействия развитию гематологии и трансплантологии костного мозга «Национальное гематологическое общество».
-
Стефанов Дмитрий Николаевич – научный сотрудник, зав. научно-организационным отделом, ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России, член Российского общества онкогематологов.
-
Чернова Наталья Геннадьевна – доктор медицинских наук, заведующий отделением гематологии и химиотерапии ГБУЗ «Московский многопрофильный клинический центр «Коммунарка» ДЗМ», член Национального гематологического общества.
-
Воронцова Анастасия Александровна - научный сотрудник, член Российского общества дерматовенерологов и косметологов.
Конфликт интересов: Авторы заявляют об отсутствии конфликта интересов.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
1. Врачи-специалисты: дерматовенерологи, гематологи, онкологи.
2. Преподаватели медицинских образовательных учреждений по специальности «Дерматовенерология», «Гематология», «Онкология»
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД)для методов диагностики (диагностических вмешательств)
|
УДД
|
Расшифровка
|
|---|---|
|
1
|
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа
|
|
2
|
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа
|
|
3
|
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая
|
|
5
|
Имеется лишь обоснование механизма действия или мнение экспертов
|
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД)для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
УДД
|
Расшифровка
|
|---|---|
|
1
|
Систематический обзор РКИ с применением мета-анализа
|
|
2
|
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа
|
|
3
|
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль»
|
|
5
|
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
|
Таблица 3. Шкала оценки уровней убедительности рекомендаций(УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР
|
Расшифровка
|
|---|---|
|
A
|
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
|
|
B
|
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
|
|
C
|
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
|
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года,а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учётом следующих нормативно-правовых документов:
1. Порядок оказания медицинской помощи по профилю «дерматовенерология», утвержденный Приказом Министерства здравоохранения Российской Федерации № 924н от 15 ноября 2012 г.
2. Порядок оказания медицинской помощи по профилю «гематология», утвержденный Приказом Министерства здравоохранения Российской Федерации № 930н от 15 ноября 2012 г.
3. Приказ Министерства здравоохранения РФ и Министерства труда и социальной защиты РФ от 31 мая 2019 г. N 345н/372н "Об утверждении Положения об организации оказания паллиативной медицинской помощи, включая порядок взаимодействия медицинских организаций, организаций социального обслуживания и общественных объединений, иных некоммерческих организаций, осуществляющих свою деятельность в сфере охраны здоровья".
4. Стадирование грибовидного микоза/синдрома Сезари согласно рекомендациям ISLE-EORTC (таблица 4).
Таблица 4. Стадирование грибовидного микоза/синдрома Сезари согласно рекомендациям ISLE-EORTC
|
Кожа
Т1 Ограниченные пятна, папулы, и/или бляшки, покрывающие <10% кожного покрова
Т1а – только пятна
Т1b – бляшки ± пятна
Т2 Пятна, папулы, и/или бляшки, покрывающие >10% кожного покрова
Т2а – только пятна
Т2b - бляшки ± пятна
Т3 Один или более узлов (≥1 см в диаметре)
Т4 Сливающаяся эритема, покрывающая ≥80% поверхности тела
Лимфатические узлы
N0 Нет увеличения периферических лимфатических узлов, их биопсия не требуется
N1 Периферические лимфатические узлы увеличены; гистопатология Dutchgrade 1 или NCILN0-2
N1a – клон-негативны
N1b – клон-позитивны
N2 Периферические лимфатические узлы увеличены; гистопатология Dutchgrade 2 или NCILN3
N2a – клон-негативны
N2b – клон-позитивны
N3 Периферические лимфатические узлы увеличены; гистопатология Dutchgrade 3-4 или NCILN4, клон-позитивны или негативны
NX Периферические лимфатические узлы увеличены, нет гистологического подтверждения
Внутренние органы
M0 Нет вовлечения внутренних органов
M1 Вовлечение внутренних органов (с уточнением органа и морфологическим подтверждением)
Кровь
B0 Отсутствие значительного вовлечения крови: атипичные (Сезари) клетки составляют ≤5% лимфоцитов периферической крови
B0a – клон-негативны
B0b – клон-позитивны
B1 Умеренное вовлечение крови: атипичные (Сезари) клетки составляют >5% лимфоцитов периферической крови
B1a – клон-негативны
B1b – клон-позитивны
B2 Значительное вовлечение крови: ≥1000/µL клеток Сезари с позитивным клоном
|
||||
|---|---|---|---|---|
|
Стадии
|
T
|
N
|
M
|
B
|
|
Ранние
IA
IB
IIA
Поздние
IIB
III
IIIA
IIIB
IVA1
IVA2
IVB
|
1
2
1,2
3
4
4
4
1-4
1-4
1-4
|
0
0
1,2
0-2
0-2
0-2
0-2
0-2
3
0-3
|
0
0
0
0
0
0
0
0
0
1
|
0,1
0,1
0,1
0,1
0,1
0
1
2
0-2
0-2
|
Приложение В. Информация для пациента
Тщательное соблюдение режима терапии, назначенной врачом, повышает ее эффективность.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента при синдроме Сезари не используются.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.