Синдром Ди Джорджи
Синдром делеции 22-й хромосомы; синдром del 22q11
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Синдром Ди Георга (D82.1)
Генетика, Иммунология, Кардиология, Кардиохирургия, Орфанные заболевания, Педиатрия
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «07» августа 2025 года
Протокол №237
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
СИНДРОМ ДИ ДЖОРДЖИ
Синдром Ди-Джорджи (синонимы: Синдром делеции 22-й хромосомы /синдром del 22q11 (при выраженных иммунологических изменениях СДД)) – это совокупность морфологических, иммунологических и неврологических изменений, которые являются следствием делеции длинного плеча одной копии 22-й хромосомы – del 22q11.2.
СДД представляет собой комплекс симптомов, состоящий из патологии лицевого скелета (расщелины твердого неба), врожденного порока сердца, иммунодефицита вследствие гипоплазии (аплазии) тимуса и гипокальциемии, как результат гипоплазии паращитовидной железы.
СДД вариабелен в количестве признаков и степени их выраженности, что и объясняет тот факт, что исторически этот синдром в литературе имеет порядка десятка различных названий, включая синдром Ди-Джорджи, синдром Ди Джорджи, САТСН 22, велокардиофациальный сидром, Шпринтцена синдром, Кайлера синдром, синдром лицевых и конотрункальных аномалий и т.д.
ВВОДНАЯ ЧАСТЬ
Код(ы) МКБ-10:
Дата разработки/пересмотра протокола: 2023 год.
Категория пациентов: взрослые, дети.
Сокращения, используемые в протоколе:
Шкала уровня доказательности:| Код | Название |
|
D 82.1
|
Синдром Ди Джорджи |
Дата разработки/пересмотра протокола: 2023 год.
Пользователи протокола: аллерголог-иммунолог, гематолог, кардиолог, кардиохирург, педиатр, терапевт, пульмонолог, врач общей практики.
Категория пациентов: взрослые, дети.
Сокращения, используемые в протоколе:
|
АИГА
|
аутоиммунная гемолитическая анемия |
| ВВИГ | внутривенные иммуноглобулины |
| ВИЧ | вирус иммунодефицита человека |
| ВЗК | воспалительные заболевания кишечника |
| ДНК | дезоксирибонуклеиновая кислота |
|
КТ
|
компьютерная томография |
| МКБ-10 | Международная классификация болезней 10-го пересмотра |
| МРТ | резонансная томография |
| ПЦР | полимеразная цепная реакция |
| РКИ | рандомизированные контролируемые исследования |
| Синдром del 22q11 | синдром делеции 22 хромосомы=синдром Ди Георга (синдром Ди Джорджи) |
|
СДД
|
синдром Ди Георга (Ди Джорджи) |
| ТТГ | тиреотропный гормон |
| Т4 | тироксин |
| ТКИН | тяжелый комбинированный иммунодефицит |
| УЗИ | ультразвуковое исследование |
| ЭКГ | электрокардиограмма |
| ЭхоКГ | эхокардиография |
| ЮРА | ювенильный ревматоидный артрит |
|
del 22q11.2
|
делеция длинного плеча 22 хромосомы локус 11.2 |
| САТСН 22 | Cardiac defects, Abnormal facies, Thymic hypoplasia, Cleft palate, Hypocalcemia, 22q deletion – порок сердца, лицевые аномалии, гипоплазия тимуса, расщелина неба, гипокальцемия, делеция 22 |
|
CD
|
субпопуляции лимфоцитов |
| FISH | fluorescent in situ hybridization - флуоресцентная гибридизация in situ 6 |
| IgG, IgА, IgМ | иммуноглобулины классов А, М, G |
| MLPA | генетическое исследование методом ПЦР, зависимый от мультиплексного лигирования амплификация зонда |
|
TREC
|
кольцевые ДНК-структуры Т-лимоцитов |
| TBX1 | Ген (T-BOX 1), расположенный на хромосоме 22 в регионе 22q11.21 |
| TUPLE 1 (HIRA) | ДНК зонд для генетического исследования синдрома Ди-Джорджи |
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты, которых могут быть распространены на соответствующую популяцию |
| В | Высококачественный (++) систематический обзор когортных или исследования случай-контроль или высококачественное (++) когортное или исследования случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С |
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+).
Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию.
|
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
Классификация
Классификация
Классификация СДД [1, 4, 6, 9]:
• полный синдром;
• частичный/не полный (случаи сочетания типичных признаков, но без проявлений выраженного иммунодефицита)
✓ достоверный частичный;
✓ вероятный частичный;
✓ возможный частичный.
Критерии для определения варианта СДД [1, 4, 6, 9]:
|
Вариант СДД
|
Критерии |
| СДД, полный синдром |
✓ Снижение/отсутствие CD3+ T-клеток (менее 50/мм³).
✓ Подтверждѐнная атимия в виде снижения ранних тимических мигрантов (CD3+CD45RA+CD62L+ кл/мм³ и/или TREC <100/100000 T-клеток.
✓ Гипопаратиреоз.
✓ Порок сердца.
|
| СДД, частичный/неполный синдром: | |
| СДД, достоверный частичный синдром |
• Снижение/отсутствие CD3+ Tклеток (менее 500/мм³) в течение первых трѐх лет жизни
• Один из следующих критериев:
✓ конотруктальный порок сердца и лабораторная или клинически выраженная гипокальциемия;
✓ конотруктальный порок сердца и делеция 22q11.2 хромосомы;
✓ лабораторная или клинически манифестированная гипокальциемия и делеция 22q11.2 хромосомы;
✓ конотруктальный порок сердца и лабораторная или клинически выраженная гипокальциемия и делеция 22q11.2 хромосомы.
|
| СДД, вероятный частичный синдром |
• Снижение CD3+ T-клеток (менее 1500/мм³) в течение первых трѐх лет жизни.
• Делеция 22q11.2 хромосомы.
|
| СДД, возможный частичный синдром |
• Снижение CD3+ T-клеток (менее 1500/мм³) в течение первых трѐх лет жизни.
• Один из следующих критериев:
✓ порок сердца;
✓ лабораторная или клинически выраженная гипокальциемия;
✓ дисморфизмы лица или расщепление нѐба.
|
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Диагностические критерии:
Жалобы и анамнез:
Жалобы и анамнез заболевания крайне разнообразные и различные по степени выраженности [2, 4, 7, 11, 13, 14, 16] и зависят от клинического варианта СДД (смотрите раздел «Физикальное обследование» настоящего клинического протокола).
Диагностический алгоритм:
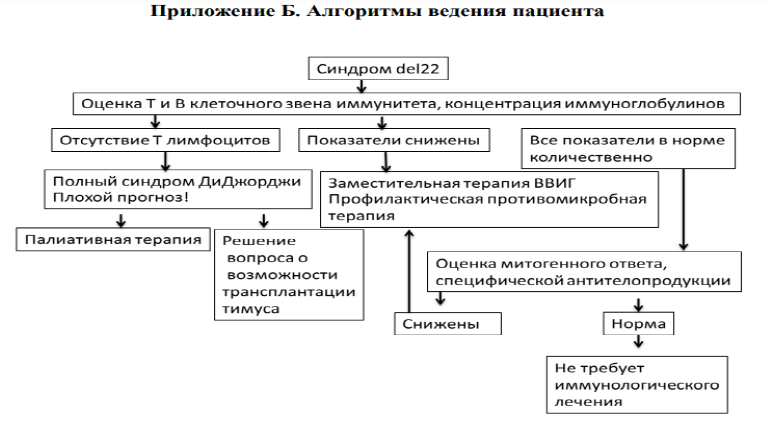
Физикальное обследование: [1, 2, 3, 7, 10, 12, 15, 16, 17]
• Задержка физического развития [1, 2, 7, 12], физическое развитие большинства пациентов низкое и дисгармоничное по весу;
• лицевой дисморфизм и другие стигмы дисэмбриогенеза широко вариабельны и не являются патогномоничными;
• характерные черты лица (удлиненное лицо, микрогнатия или ретрогнатия, широкая переносица, мелкие зубы, асимметрия лица при плаче, опущенные вниз уголки рта, глазной гипертелоризм, низко посаженные и деформированные ушные раковины, бульбообразный кончик носа) [3, 6, 12];
• пороки сердца не менее, чем в 80% случаев. Некоторые из пороков являются более патогномоничными: прерывание дуги аорты, общий артериальный ствол и тетрада Фалло являются наиболее частыми среди данной группы детей [7, 13];
• пороки развития дыхательной, пищеварительной, костно-мышечной и других систем;
• признаки дыхательной и сердечной недостаточности;
• иммунологические нарушения встречаются в 77% случаев. Инфекционные проявления вследствие дефекта иммунной системы иногда дебютируют не с рождения. Чаще других звеньев поражается Т-клеточное звено, что проявляется предрасположенностью к грибковым заболеваниям, пневмоцистной инфекции, некоторым бактериальным и вирусным инфекциям [1, 10, 12];
• поражение носоглоточного аппарата выявлено примерно в 70% случаев и проявляется в виде велофарингеальной недостаточности, вследствие которой у 36% пациентов отмечается затруднение глотания [7, 12, 15];
• расщепления нѐба, губы, раздвоения уздечки нѐба, гнусавым оттенком голоса [7, 12, 15];
• снижение обоняния [7, 12, 15];
• кондуктивная и/или сенсоневральная тугоухость [7, 12, 15];
• гипокальциемия/гипопаратиреоз может проявляться судорожным синдромом при выраженном дефиците кальция в младенческом возрасте, существует риск развития нефрокальциноза. В детском возрасте и у 20% взрослых развивается гипотиреоз, в детском возрасте иногда встречается гипертиреоз. Редко отмечается дефицит гормона роста [7, 14].
• задержка речевого и психомоторного развития наблюдается у 70—90% и проявляется с возрастом, однако тестирование пациентов с задержкой развития имеет смысл только в случаях сочетании с другими признаками;
• задержка умственного и речевого развития (встречается у подавляющего числа пациентов с данным синдромом);
• поведенческие и психические проблемы также могут встречаться у пациентов с СДД [2, 3, 12, 17]:
✓ в детском возрасте обычно отмечаются гиперактивность, тревожность, аутические и аффективные расстройства;
✓ в подростковом и взрослом возрасте у 10 – 30% с СДД отмечаются биполярные расстройства, шизофрения, шизоаффективные расстройства.
✓ повышен риск раннего старта (до 50 лет) болезни Паркинсона.
• нарушение выработки Т-клеток может предрасполагать к таким аутоиммунным заболеваниям, как ЮРА, ХТП, АИГА, ВЗК, болезнь Грейвса, аутоиммунный увеит, бронхиальная астма [1, 2, 12, 16].
Дополнительные лабораторные исследования:
Основные лабораторные исследования:
ОАК: снижение тромбоцитов, лимфопения[3,4]
Определение уровня ионизированного кальция: снижение уровня кальция [12]
Определение уровня паратиреоидного гормона: снижение уровня гипотиреоидного гормона [12]
Определение уровня сывороточных иммуноглобулинов IgA, IgM, IgG: норма или снижение уровня сывороточных иммуноглобулинов IgA, IgM, IgG
Дополнительные лабораторные исследования:
Определение уровня ТТГ и Т4 свободный: снижение уровня ТТГ и Т4 свободного [14]
Иммунофенотипирование лимфоцитов, включая определение количества наивных Т-лимфоцитов:
✓ Снижение Т лимфоцитов, возможна норма;
✓ Соотношение наивных Т-клеток / Т-клеток памяти понижено [1, 12, 18]
Исследование показателей специфических антител (к соответствующим возбудителям): снижение или норма показателей специфических антител [11, 12]
Оценка вакцинальных антител: снижение или норма вакцинальных антител.
Определение наличия вирусов гепатитов В и С, ВИЧ, цитомегаловируса, вируса Эпштейн-Барра (биоматериалы: моча, слюна) методом ПЦР: обнаружение вирусов [12, 14]. Микробиологическое исследование биосред при подозрении на сепсис: наличии бактериемии.
Проведение флюоресцентной гибридизации in situ (FISH) с ДНК-зондом TUPLE 1 (HIRA) с целью верификации генетического дефекта: наличие дефекта в гене [5, 7, 8, 9, 10, 20]
Прямое секвенирование по Сенгеру гена TBX1 или определение делеции/ дупликации в гене TBX1 методом MLPA с целью верификации генетического дефекта: наличие дефекта в гене, верификация диагноза [5, 7, 8, 9, 10, 20]
Исследование TREC методом ПЦР (показание: подозрением на полный синдром Ди Джорджи): TREC <100/100000 T-клеток [36, 37].
Комплексные молекулярные методы aSNP (анализ одиночных нуклеотидных полиморфизмов) и aCGH (сравнительная геномная гибридизация): наличие дефекта в гене [36, 37].
Дополнительные инструментальные исследования:
Основные инструментальные исследования:
ЭКГ: нарушение электрической проводимости сердца[3, 4, 7, 13]
Эхо КГ: наличие порока сердца[3, 4, 7, 13]
УЗИ органов мочевыделительной системы: выявление пороков развития органов мочевыделительной системы [12, 18]
Дополнительные инструментальные исследования:
Назофарингеальная эндоскопия: выявление пороков лицевого скелета[10, 12]
Аудиометрия: выявление снижения слуха[4]
Определение остроты зрения: снижение остроты зрения, наличие пороков развития органов зрения [3, 4, 15]
Лучевая диагностика МРТ/КТ: выявление хронических очагов инфекции [12]
Рентгенография придаточных пазух носа: выявление наличия инфекционных осложнений [12]
Ангиография: выявление пороков развития сосудов[12]
УЗИ органов брюшной полости: увеличение печени, селезенки.
Показания для консультации специалистов:
1) консультация кардиолога – пороки развития сердца, нарушения ритма;
2) консультация челюстно-лицевого хирурга –пороки развития челюстно-лицевого скелета;
3) консультация эндокринолога – я гипотиреоз и гипопаратиреоз;
4) консультация оториноларинголога – при наличии инфекционных осложнений верхних дыхательных путей;
5) консультация офтальмолога –пороки развития глаз, нарушения остроты зрения;
6) консультация психиатра – психические нарушения;
7) консультация невролога – судорожный синдром, задержка психо- моторного развития;
8) консультация генетика – врожденные пороки развития.
Диагностический алгоритм:

Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований
Таблица 5. Критерии дифференциальной диагностики СДД [12, 17, 21, 22]
|
Синдром
|
Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Синдром Смита-Лемли-Опица | Дисморфизм лица | Оценка объективного статуса | Наличие карликовости, отсутствие тяжелого инфекционного синдрома |
| определение уровня кальция, гормона паращитовидной железы | Показатели уровня кальция и гормона паращитовидной железы в пределах нормы | ||
| УЗИ тимуса или КТ грудного сегмента | Размеры тимуса в пределах нормы | ||
| Синдром CHARGE | Дисморфизм лица, высокий риск онкологических заболеваний, кисты верхней челюсти | Оценка объективного статуса | Наличие диморфизма лица отличные от СДД |
| определение уровня кальция, гормона паращитовидной железы | Показатели уровня кальция и гормона паращитовидной железы в пределах нормы | ||
| УЗИ тимуса или КТ грудного сегмента | Размеры тимуса в пределах нормы | ||
| Диабетическая эмбриопатия | Дисморфизм лица, короткая шея, пороки сердца, респираторная инфекция, судороги | определение уровня кальция, гормона паращитовидной железы | Показатели уровня кальция и гормона паращитовидной железы в пределах нормы |
| УЗИ тимуса или КТ грудного сегмента | Размеры тимуса в пределах нормы | ||
| ТКИН | Тяжелый инфекционный синдром, снижение уровня иммуноглобулинов, снижение Т-лимфоцитов, судороги | Оценка объективного статуса | Отсутствие порока сердца и аномалий черепа |
| определение уровня кальция, гормона паращитовидной железы | Показатели уровня кальция и гормона паращитовидной железы в пределах нормы | ||
| УЗИ тимуса или КТ грудного сегмента | Размеры тимуса в пределах нормы | ||
| Аладжилля синдром | аномальной формы черепа, асимметрии лица, низкая линия роста волос, расщепление нёба, раздвоенный язычок, верхнечелюстная гипоплазия, тугоухость, нарушение зрения, пороки сердца. | Оценка объективного статуса | Более тяжелая неврологическая патология и поражение зрения, брахидактилия, широкие пальцы, частичная кожная синдактилия 2 и 3 пальцев руки, дублированные дистальные фаланги большого пальца. |
| определение уровня кальция, гормона паращитовидной железы | Показатели уровня кальция и гормона паращитовидной железы в пределах нормы | ||
| УЗИ тимуса или КТ грудного сегмента | Размеры тимуса в пределах нормы |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ [1, 2, 3, 4, 11, 12]
Цель лечения:
• коррекция жизнеугрожающих морфологических дефектов;
• контроль за инфекционными эпизодами и компенсация иммунологических дефектов;
• профилактика аутоиммунных осложнений;
• обеспечение приближенных к нормальным росту и развитию ребенка, обеспечение хорошего качества жизни пациента;
• снижение частоты и тяжести бактериальных инфекций и предотвращение развития необратимых и тяжелых осложнений, а также жизнеугрожающих инфекций. Реализация этих целей становится возможной при достижении близких к нормальным претрансфузионных уровней IgG.
Немедикаментозное лечение:
Режим:
Режим:
• общий в период ремиссии;
• уменьшение контакта с инфекционными агентами.
Диета:
• повышенное содержание кальция;
• употребление продуктов, исключающих риск токсико-инфекции, кишечных инфекций, гельминтозов.
Заместительная терапия донорскими человеческим иммуноглобулином (УД – 4) [1, 3, 4, 12, 21].
Эффект насыщения определяется по уровню сывороточного IgG и оценка проводится по следующим критериям:
Медикаментозное лечение:
Заместительная терапия донорскими человеческим иммуноглобулином (УД – 4) [1, 3, 4, 12, 21].
Используются две формы иммуноглобулинов для заместительной терапии:
• Иммуноглобулин нормальный человеческий для внутривенного введения (ВВИГ);
• Иммуноглобулин нормальный человеческий для подкожного введения.
Заместительная иммуноглобулинотерапия используется следующим способом:
• режим насыщения до достижения целевого претрансфузионного уровня IgG (лицам с впервые выявленным диагнозом, либо лицам, не получавшим ранее адекватной заместительной терапии, а также после всех перенесенных серьезных инфекционных эпизодов);
• режим поддерживающей профилактической иммунотерапии: проводится только после достижении уровней IgG не ниже 6 – 8 г/л и при подавлении активности инфекционного процесса.
Длительность курса иммуноглобулинтерапии:
• при использовании ВВИГ в дозе 0,4 – 0,6 г/кг для поддерживающей терапии достаточно 1 раз в 3-4 недели;
• при использовании иммуноглобулинов для подкожного введения в дозе 0,5 мл (100 мг)/кг массы тела один раз в 1 или 2 недели.
Эффект насыщения определяется по уровню сывороточного IgG и оценка проводится по следующим критериям:
• > 10 г/л – хороший эффект;
• 8 – 10 г/л – удовлетворительный эффект;
• < 5 г/л – неудовлетворительный эффект.
Антибактериальная терапия проводится в зависимости от степени выраженности иммунологического дефекта:
• при наличии лимфопении, сопутствующих хронических очагах инфекции антибиотики назначаются с профилактической или лечебной целью [3,4,11].
Препаратами выбора являются:
• ко-тримоксазол (сульфаметоксазол+триметоприм) – 5 мг/кг/сут в два/три приема – 3 раза в неделю (ограничение в применении у детей до 3 лет);
• азитромицин 10 мг/кг/сут 1 раз в день – 3 раза в неделю (ограничение в применении у детей до 12 лет и массой тела менее 45 кг);
• амоксициллин+клавулановая кислота в дозе 40 мг/кг/сутки в два приема – ежедневно;
** В случае неэффективности или плохой переносимости данных режимов, может быть выбран любой другой антибактериальный препарат.
Хирургическое вмешательство:
Индикаторы эффективности лечения:
Противогрибковая терапия проводится при возникновении микозных осложнений и назначается с лечебной целью [3,4,11].
✓ Флуконазол 6 мг/кг/сут х 1 раз в день.
Перечень основных лекарственных средств [6,7,9,22]:
Перечень дополнительных лекарственных средств [3,4,11]:
Заместительная терапия препаратами кальция проводится с дополнительным назначением витамина D в возрастных дозировках для коррекции уровня электролитов [4, 11]. Рекомендовано мониторирование уровня кальция в течение жизни с последующей коррекцией доз препаратов [1,2,4,11,12].
Перечень основных лекарственных средств [6,7,9,22]:
|
Фармакотерапевтическая группа
|
МНН лекарственного средства | Способ и длительность применения | Уровень доказательности |
| Иммунологический препарат. Глобулин. | Иммуноглобулин G человеческий нормальный |
(содержание не менее 90%) Внутривенное медленное введение
Доза 0,4 до 0,8 г/кг в 3-4 недели, в зависимости от содержания иммуноглобулина у пациента.
Доза насыщения 8 г\кг.
Пожизненно! |
В |
| Иммунологический препарат. Глобулин. | Иммуноглобулин G человеческий нормальный |
(содержание не менее 90%) Подкожно Доза 100 мг/кг в неделю.
Возможно введение чаще для получения дозы насыщения.
Доза насыщения 8 г/кг.
Пожизненно! |
В |
|
Витамин D
|
Колекальциферол |
Перорально Взрослые и дети с 12 лет от 500 ME до 1000 ME витамина D (12,5–25 мкг или 0,0125–0,025 мг колекальциферола). Дети с рождения до
от 1 года– 500 МЕ/сутки;
от 1 года до 3 лет – 1500 Ме\сут;
от 3 года до 12 лет – 1000 МЕ/сутки.
|
С |
|
Фармакотерапевтическая группа
|
МНН лекарственного средства | Способ и длительность применения | Уровень доказательности |
| Противомикробное средство комбинированное | Триметоприм/ сульфаметоксазол** (расчет дозы по триметоприму) |
Перорально 5 мг/кг массы тела в
день или 2 раза в день ежедневно или 3 дня в неделю. Курсовая доза и длительность применения определяется врачом индивидуально в зависимости от состояния пациента
|
С |
| Антибиотик | Азитромицин** |
Перорально Дети 10 мг/кг массы тела 1 раз в неделю или 5 мг/кг массы тела через день 3 дня в неделю.
Взрослые 500 мг 1 раз в неделю
или 250 мг через день 3 раза в неделю
Курсовая доза и длительность применения определяется врачом индивидуально в зависимости от состояния пациента
|
С |
| Антибиотик | Амоксициллин** (при необходимости в сочетании с клавулановой кислотой) |
Перорально
Дети – 10- 20 мг/кг массы тела 1 или 2 раза / день
Взрослые 500 - 1000 мг 1 или 2 раза в день
Курсовая доза и длительность применения определяется врачом индивидуально в зависимости от состояния пациента
|
С |
| Противогрибковое средство | Флуконазол** |
Перорально
Дети 6 мг/кг массы тела в сутки Взрослые 150 мг 1 раз в день
Курсовая доза и длительность применения определяется врачом индивидуально в зависимости от состояния пациента
|
С |
Применение дополнительных лекарственных средств необходимо при возникновении осложнений и должна осуществляться согласно соответствующим действующим клиническим протоколам (пневмонии, бронхоэктатической болезни, НЯК, острого синусита, сепсиса и др.) (см соответствующие протоколы диагностики и лечения), но на фоне продолжающейся заместительной иммунной терапии.
Хирургическое вмешательство:
Хирургическое вмешательство проводится в зависимости от степени выраженности пороков сердца, лицевого скелета и гортани (УД -C) [1, 4, 10, 24, 25].
Наиболее часто коррекции подлежит пороки сердца, расщепление нѐба и верхней губы, лечение которых необходимо проводить в максимально короткие сроки с целью профилактики аспирации, провоцирующей развитие инфекций.
При проблемах с кормлением и глотанием вследствие дефекта велофарингеальной недостаточности рекомендуется установление гастростомы [11, 24].
Терапия и сопровождение невролога, логопеда, психиатра при задержке развития речи пациентам дошкольного возраста [12, 17]. Пациенты детского возраста наблюдаются с диагнозами: синдром дефицита внимания, гиперактивность, аутистические заболевания, фобии. Взрослые пациенты наблюдаются с диагнозами «психоз» или «шизофрения», «депрессия», «биполярный синдром».
Контрольное инструментальное обследование:
Другие виды лечения (УД – C) [12, 17].
Рекомендуется проведение трансплантация тимуса пациентам с синдромом делеции 22-й хромосомы при наличии выраженного Т-клеточного дефекта у пациентов с полным СДД, фенотипически похожим на тяжёлую комбинированную иммунную недостаточность, с выраженными иммунологическими нарушениями и высоким риском летального исхода в детском возрасте[26-30].
Терапия и сопровождение невролога, логопеда, психиатра при задержке развития речи пациентам дошкольного возраста [12, 17]. Пациенты детского возраста наблюдаются с диагнозами: синдром дефицита внимания, гиперактивность, аутистические заболевания, фобии. Взрослые пациенты наблюдаются с диагнозами «психоз» или «шизофрения», «депрессия», «биполярный синдром».
Дальнейшее ведение [35]:
Динамическое наблюдение по месту жительства у иммунолога-аллерголога, кардиолога, челюстно-лицевого хирурга, в процессе которого решаются вопросы поддерживающей заместительной терапии, минимизации побочных эффектов от проводимого лечения.
Контрольное обследование у иммунолога на республиканском уровне не менее 1 раза в 1 года, при снижении контроля заболевания возможно наличие онкологических и аутоиммунных осложнений.
Контрольное инструментальное обследование:
• ЭКГ – 1 раз в год;
• УЗИ брюшной полости, почек – 1 раз в год;
• ЭХО-сердца – 1 раз в год;
• денситометрия – 1 раз в год;
• рентгенография грудной клетки, КТ, МРТ – по показаниям.
При наличии сопутствующей патологии при наличии показаний осмотр следующих профильных специалистов:
• хирург – 1 раз в год
• стоматолог – 1 раз в год
• отоларинголог – 1 раз в год
• кардиолог – 1 раз в год
• гастроэнтеролог – 1 раз в год
• офтальмолог – 1 раз в год
• невролог – 1 раз в год.
Пациентам с делецией 22-й хромосомы рекомендуется проведение перинатальной диагностики и генетического консультирования с целью предотвращения рождения других детей с данным заболеванием [1, 2, 20].
Вакцинация [31, 32, 33, 34]
Вакцинации проводятся пациентам (взрослым и детям) с делецией 22-й хромосомы, за исключением пациентов с полным СДД.
Для оценки эффективности вакцинации необходим контроль специфических АТ к вакцинным штаммам микроорганизмов.
На фоне заместительной терапии иммуноглобулинами вакцинация не целесообразна.
Индикаторы эффективности лечения:
• поддержание претрансфузионных сывороточных уровней IgG выше 6-8 г/л;
• достижение клинической ремиссии заболевания;
• устранение или уменьшение инфекционных осложнений;
• восстановление утраченной трудоспособности;
• улучшение качества жизни пациентов.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ:
Стационарное лечение необходимо для коррекции порока сердца и/или дефектов лицевого скелета только, лечения клинических проявлений осложнений (лечение, которых проводится согласно соответствующим клинических протоколов диагностики и лечения).
Алгоритм ведения пациента:
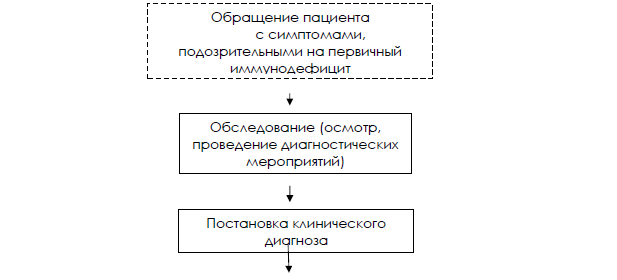
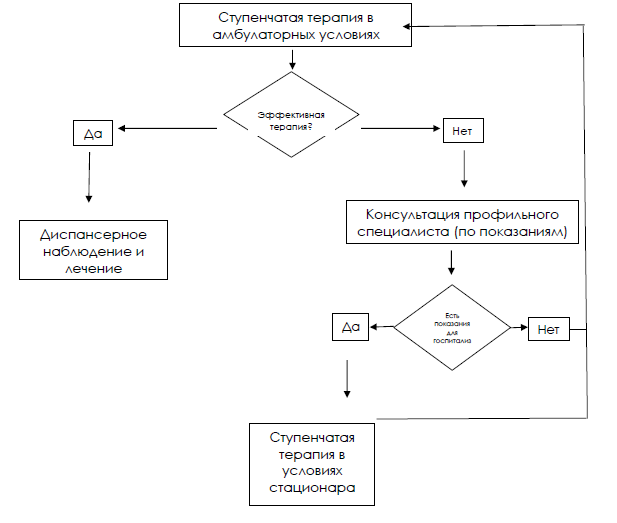
Карта наблюдения пациента, маршрутизация пациента:
Алгоритм ведения пациента:


Немедикаментозное лечение: см. Амбулаторный уровень.
Медикаментозное лечение: см. Амбулаторный уровень.
Хирургическое вмешательство: коррекции порока сердца и/или дефектов лицевого скелета.
Дальнейшее ведение [30, 35]:
Диспансерный учет у аллерголога – иммунолога по месту жительства.
Заместительная терапия иммуноглобулинами пожизненно.
Контрольное обследование и коррекция заместительной терапии 1 раз в год у иммунолога на республиканском уровне оказания лечебно-профилактической помощи.
Коррекция терапии у кардиолога по месту жительства.
Контрольное обследование у кардиохирурга после хирургической коррекции порока сердца.
Коррекция терапии у оториноларинголога по месту жительства.
Контрольное обследование у челюстно-лицевого хирурга после хирургической коррекции порока лицевого черепа.
Наблюдение у невролога или психотерапевта при наличии психоневрологической патологии.
Охранительный режим по инфекционным заболеваниям.
Ранняя этиотропная терапия инфекционных осложнений.
Индикаторы эффективности лечения:
• отсутствие инфекционных осложнений;
• поддержание уровня сывороточного иммуноглобулина G не менее 8 г+/л.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
• порок сердца и/или дефекты лицевого скелета с целью коррекции;
• отсутствие эффекта от проводимого лечения в амбулаторных условиях;
• развитие тяжелых инфекционных осложнений, не купируемых в амбулаторных условиях;
• наличие неинфекционных осложнений (онкология, аутоиммунные заболевания).
Показания для экстренной госпитализации:
• тяжелый инфекционный синдром;
• нарушение сердечной деятельности;
• аспирация.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- 1) Детская гематология/ Под ред: А.Г. Румянцева, А.А. Масчана, Е.В. Жуковской. Авторы: Айзенберг В.Л., Балашов Д.Н., Биккулова Д.Ш., и др.// Москва. Издательская группа «ГЭОТАР- Медиа» 2015 г. С. - 656. 2) Bassett AS et al. Practical Guidelines for Managing Patients with 22q11.2 Deletion Syndrome J Pediatr. 2011 August; 159(2): 332–9. 3) McDonald-McGinn D M, Sullivan K E. Chromosome 22q11.2 deletion syndrome (DiGeorge syndrome/velocardiofacial syndrome) Medicine (Baltimore) 2011;90(1):1–18. 4) Maggadottir SM, Sullivan KE. The diverse clinical features of chromosome 22q11.2 deletion syndrome (DiGeo 5) rge syndrome). J Allergy Clin Immunol Pract. 2013 NovDec;1(6):589-94. 6) Adam MP, Feldman J, Mirzaa GM, et al., editors.Seattle (WA): University of Washington, Seattle; 1993-2023. 7) Oh A K, Workman L A, Wong G B. Clinical correlation of chromosome 22q11.2 fluorescent in situ hybridization analysis and velocardiofacial syndrome. Cleft Palate Craniofac J. 2007;44(1):62–66. 8) Monteiro F P, Vieira T P, Sgardioli I C. et al. Defining new guidelines for screening the 22q11.2 deletion based on a clinical and dysmorphologic evaluation of 194 individuals and review of the literature. Eur J Pediatr. 2013;172(7):927–945. 9) Crowley B, Ruffner M, McDonald-McGinn DM, Sullivan KE. Variable immune deficiency related to deletion size in chromosome 22q11.2 deletion syndrome. Am J Med Genet A. 2018;176:2082-6. 10) Miller D T, Adam M P, Aradhya S. et al. Consensus statement: chromosomal microarray is a first-tier clinical diagnostic test for individuals with developmental disabilities or congenital anomalies. Am J Hum Genet. 2010;86(5):749–764. 11) Alexandra E. Lackey; Maria Rosaria Muzio. DiGeorge Syndrome. StatPearls Publishing; 2023 Jan. 12) Davies EG. Immunodeficiency in DiGeorge Syndrome and Options for Treating Cases with Complete Athymia. Front Immunol. 2013 Oct 31;4:322. 13) Bassett AS, McDonald-McGinn DM, Devriendt K, Digilio MC, Goldenberg P, Habel A, Marino B, Oskarsdottir S, Philip N, Sullivan K, Swillen A, Vorstman J. International 22q11.2 Deletion Syndrome Consortium. Practical guidelines for managing patients with 22q11.2 deletion syndrome. J Pediatr. 2011 Aug;159(2):332–9.e1. 14) Kobayashi D, Sallaam S, Humes RA. Tetralogy of Fallot with complete DiGeorge syndrome: report of a case and a review of the literature. Congenit Heart Dis. 2013 JulAug;8(4):E119-26. 26 15) Chinn IK, Markert ML. Induction of tolerance to parental parathyroid grafts using allogeneic thymus tissue in patients with DiGeorge anomaly. J Allergy Clin Immunol. 2011 Jun;127(6):1351-5. 16) Saffra N, Reinherz B. Keratoconus in an adult with 22q11.2 deletion syndrome. BMJ Case Rep. 2015 Jan 16;2015. pii: bcr2014203737. 17) Damlaj M, Séguin C. Refractory autoimmune hemolytic anemia in a patient with DiGeorge syndrome treated successfully with plasma exchange: a case report and review of the literature. Int J Hematol. 2014 Nov;100(5):494-7. 18) Fung WL, Butcher NJ, Costain G, Andrade DM, Boot E, Chow EW, Chung B, Cytrynbaum C, Faghfoury H, Fishman L, García-Miñaúr S, George S, Lang AE, Repetto G, Shugar A, Silversides C, Swillen A, van Amelsvoort T, McDonald-McGinn DM, Bassett AS (2015) Practical guidelines for managing adults with 22q11.2 deletion syndrome. Genet Med. 2015;17:599-609 19) Hacıhamdioğlu B, Hacıhamdioğlu D, Delil K. 22q11 deletion syndrome: current perspective. Appl Clin Genet. 2015 May 18;8:123-32. 20) van der Spek J, Groenwold RH, van der Burg M, van Montfrans JM. TREC Based Newborn Screening for Severe Combined Immunodeficiency Disease: A Systematic Review. J Clin Immunol. 2015 May. 35 (4):416-30. 21) Кузьменко Н.Б., Варламова Т.В., Мерсиянова И.В., Райкина Е.В., Бобрынина В.О., Щербина А.Ю. Молекулярно-генетическая диагностика первичных иммунодефицитных состояний. Вопросы гематологии\онкологии и иммунопатологии в педиатрии. 2016; 15(1):10-16. 22) Francisco A. Bonilla et al; International Consensus Document (ICON): Common Variable Immunodeficiency Disorders.J Allergy Clin Immunol Pract. 2016 ; 4(1): 38–59. 23) Bertini V, Azzarà A, Legitimo A, Milone R, Battini R, Consolini R, et al. Deletion Extents Are Not the Cause of Clinical Variability in 22q11.2 Deletion Syndrome: Does the Interaction between DGCR8 and miRNA-CNVs Play a Major Role?. Front Genet. 2017. 8:47. 24) Carotti A, Digilio MC, Piacentini G, Saffirio C, Di Donato RM, Marino B. Cardiac defects and results of cardiac surgery in 22q11.2 deletion syndrome. Dev Disabil Res Rev. 2008;14(1):35–42. 25) Leopold C, De Barros A, Cellier C, Drouin-Garraud V, Dehesdin D, Marie JP. Laryngeal abnormalities are frequent in the 22q11 deletion syndrome. Int J Pediatr Otorhinolaryngol. 2012;76(1):36–40. 26) Kirschner RE, Baylis AL. Surgical considerations in 22Q11.2 deletion syndrome. Clin Plast Surg. 2014;41(2):271–282. 27) Davies EG, Cheung M, Gilmour K, et al. Thymus transplantation for complete DiGeorge syndrome: European experience. J Allergy Clin Immunol. 2017;140(6):1660–1670.e16. 28) Ciupe SM, Devlin BH, Markert ML, Kepler TB. The dynamics of T-cell receptor repertoire diversity following thymus transplantation for DiGeorge anomaly. PLoS Comput Biol. 2009 Jun. 5(6):e1000396. 29) Markert ML, Devlin BH, Chinn IK, McCarthy EA, Li YJ. Factors affecting success of thymus transplantation for complete DiGeorge anomaly. Am J Transplant. 2008 Aug. 8(8):1729-36. 30) Markert ML, Devlin BH, Chinn IK, McCarthy EA. Thymus transplantation in complete DiGeorge anomaly. Immunol Res. 2009;44(1-3):61-70. 31) Al-Sukaiti N, Reid B, Lavi S, Al-Zaharani D, Atkinson A, Roifman CM, Grunebaum E. Safety and efficacy of measles, mumps, and rubella vaccine in patients with DiGeorge syndrome. J Allergy Clin Immunol. 2010 Oct;126(4):868-9 32) Azzari C, Gambineri E, Resti M, Moriondo M, Betti L, Saldias LR, et al. Safety and immunogenicity of measles-mumps-rubella vaccine in children with congenital immunodeficiency (DiGeorge syndrome). Vaccine. 2005 Feb 25. 23(14):1668-71. 33) Moylett EH, Wasan AN, Noroski LM, Shearer WT. Live viral vaccines in patients with partial DiGeorge syndrome: clinical experience and cellular immunity. Clin Immunol. 2004 Jul. 112(1):106-12. 34) Bakare N, Menschik D, Tiernan R, Hua W, Martin D. Severe combined immunodeficiency (SCID) and rotavirus vaccination: reports to the Vaccine Adverse Events Reporting System (VAERS). Vaccine. 2010 Sep 14;28(40):6609-12. 35) Приказ Министра здравоохранения Республики Казахстан № ҚР ДСМ-37 от 7 декабря 2018 года. О внесении изменений и дополнений в приказ Министра здравоохранения Республики Казахстан от 26 июня 2017 года № 446 «Об утверждении Стандарта организации оказания аллергологической и иммунологической помощи в Республике Казахстан»; 36) Jalali G, Vorstman J, Errami A, Vijzelaar R, Biegel J, Shaikh T, Emanuel B. Detailed analysis of 22q11.2 with a high density MLPA probe set, Hum Mutat 2008; 29(3): 433-40. doi: 10.1002/humu.20640; 37) Knutsen Р, Baker M, Markert M. Interpreting low T-cell receptor excision circles in newborns with DiGeorge anomaly: importance of assessing naive T-cell markers, J Allergy Clin Immunol 2011; 128(6):1375-6. doi: 10.1016/j.jaci.2011.08.019.
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1) Ковзель Елена Федоровна – доктор медицинских наук Республики Казахстан, доктор медицинских наук РК и РФ, аллерголог-иммунолог, заведующая Программой клинической иммунологии, аллергологии и пульмонологии Корпоративного фонда «University Medical Center».
2) Манжуова Ляззат Нурбопаевна – кандидат медицинских наук, заместитель председателя по научной работе АО «Научный центр педиатрии и детской хирургии».
3) Испаева Жанат Бахытовна – доктор медицинских наук, профессор, заведующая кафедрой аллергологии и клинической иммунологии НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова».
4) Бекмагамбетова Райхан Базарбаевна – лектор кафедры аллергологии и клинической иммунологии НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова».
Указание на отсутствие конфликта интересов: нет.
Указание условий пересмотра протокола: пересмотр не реже 1 раза в 5 лет и не чаще 1 раза в 3 года при наличии новых методов диагностики и лечения с уровнем доказательности.
5) Ермекбаева Бакытгуль Абкеновна – доктор медицинских наук, профессор, Назарбаев Университет, National Laboratory Astana, Центр наук о жизни, ведущий научный сотрудник, клинический фармаколог.
6) Муканова Шолпан Насыровна – независимый медицинский эксперт, менеджер здравоохранения высшей категории, сертифицированный методист по разработке клинических руководств, главный менеджер Департамента по медицинским и регуляторным вопросам Корпоративного фонда «University Medical Center».
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
Моренко Марина Алексеевна – доктор медицинских наук, аллерголог-иммунолог, профессор, заведующая кафедрой педиатрии НАО «Медицинский университет Астана».
Моренко Марина Алексеевна – доктор медицинских наук, аллерголог-иммунолог, профессор, заведующая кафедрой педиатрии НАО «Медицинский университет Астана».
Указание условий пересмотра протокола: пересмотр не реже 1 раза в 5 лет и не чаще 1 раза в 3 года при наличии новых методов диагностики и лечения с уровнем доказательности.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.