Саркома Капоши
 Версия: Клинические рекомендации РФ 2024 (Россия)
Версия: Клинические рекомендации РФ 2024 (Россия)
Болезнь, вызванная ВИЧ, с проявлениями саркомы Капоши (B21.0), Саркома Капоши (C46), Саркома Капоши других локализаций (C46.7), Саркома Капоши кожи (C46.0), Саркома Капоши лимфатических узлов (C46.3), Саркома Капоши множественных органов (C46.8), Саркома Капоши мягких тканей (C46.1), Саркома Капоши неба (C46.2), Саркома Капоши неуточненной локализации (C46.9)
Дерматовенерология, Онкология
Общая информация
Краткое описание
Разработчик клинической рекомендации
- Ассоциация онкологов России
- Общероссийская общественная организация "Российское общество дерматовенерологов и косметологов"
- Автономная некоммерческая организация "Восточно-Европейская группа по изучению сарком"
Одобрено Научно-практическим Советом Минздрава РФ
– размещенные в Рубрикаторе после 1 января 2024 года – с 1 января 2025 года.
Клинические рекомендации
Саркома Капоши
Год утверждения (частота пересмотра): 2024
Возрастная категория: Взрослые
Пересмотр не позднее: 2026
ID: 238
Определение заболевания или состояния (группы заболеваний или состояний)
В соответствии с определением ВОЗ Саркома Капоши представляет собой локально агрессивную пролиферацию эндотелия, которая обычно проявляется кожными изменениями в виде множественных пятен, бляшек или узелков, но также может поражать участки слизистых оболочек, лимфатические узлы и внутренние органы. СК всегда ассоциирована с инфекцией HHV8 и представляет собой пример индуцированной вирусом пролиферации сосудов. По классификации ВОЗ относится к разделу сосудистых опухолей.
Наиболее часто поражаются кожные покровы. Также могут поражаться слизистые оболочки, лимфатические узлы и внутренние органы, иногда без поражения кожных покровов. Изменения, затрагивающие головной мозг и кости встречаются редко даже при диссеминированном процессе [1,13, 14, 71-77]
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
По Международной статистической классификации болезней и проблем, связанных со здоровьем (далее - МКБ-10) такие опухоли классифицируются в соответствии с органом первичного происхождения.
Саркома Капоши (С46, В21.0)
С46.0 – СК кожи
С46.1 – СК мягких тканей
С46.2 - СК неба
С46.3 – СК лимфатических узлов
С46.7 – СК других локализаций
С46.8 – СК множественных органов
С46.9 – СК неуточненной локализации
В21.0 – Болезнь, вызванная ВИЧ, с проявлением СК
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Международная гистологическая классификация (классификация ВОЗ, опухоли костей и мягких тканей, 5 издание, 2020 год):
в соответствии с МКБ-0 морфологический код 9140/3[ 16,17]
− классическая СК (идиопатическая, спорадическая, европейская);
− эндемическая СК (африканская);
− эпидемическая СК, ассоциированная со СПИДом;
- СК на фоне иммуносупрессии (ятрогенная, возникающая при проведении иммуносупрессивной терапии, особенно после трансплантации органа).
Не существует общепринятой классификации по стадиям саркомы Капоши для классического, эндемического и иммуносупрессивного вариантов.
Рекомендуется разделять 3 клинические ситуации: 1) локально-распространенная неагрессивная форма, 2) локально-распространенная агрессивная форма и 3) диссеминированная форма СК [1, 2,14, 77].
Комментарий: Единственная утвержденная и валидированная система стадирования для СПИД-ассоциированной СК. Она была разработана комитетом по онкологии группы клинических исследований СПИДа еще в эру до появления комбинированной антиретровирусной терапии и включала в себя измерение степени распространенности болезни (T-tumor – опухоль) как локализованную или диссеминированную формы;по состоянию иммунной системы (I-immunodeficiency – состояние иммунодефицита) – по количеству CD4 клеток – высокое или низкое; по наличию или отсутствию симптомов и системных заболеваний (S-systemic – системные заболевания/ состояния) [1, 2, 3,16] В эру после появления комбинированной антиретровирусной терапии только T и S рекомендовано использовать для выявления пациентов с плохим прогнозом (таблица 1).
Таблица 1. Классификация стадирования СПИД-ассоциированной СК [1,2,3]
| Фактор |
Хороший прогноз
(все факторы)
|
Плохой прогноз
(один из факторов)
|
|---|---|---|
| Опухоль, T | T0: ограничена кожей и/или лимфоузлами и/или минимальные проявления со стороны полости рта (не узловая СК) |
Т1:отек или изъязвление, связанное с опухолью
Распространенная форма СК в полости рта
СК желудочно-кишечного тракта
СК другого органа за исключением лимфоузлов
|
| Иммунная система. I1 | I0: CD4+ клетки > 150/mL | I1: CD4+ клетки < 150/mL |
| Системные состояния/ заболевания. S |
S0:нет указания в анамнезе на оппуртонистические инфекции или афтозный стоматит
Нет симптомов «В»2
Общее состояние по шкале Карновского более 70
|
S1: есть указание в анамнезе на оппуртонистические инфекции или афтозный стоматит
Есть симптомы «В»2
Общее состояние по шкале Карновского менее 70
Другие ВИЧ-ассоциированные заболевания (неврологические болезни, лимфома)
|
|
1-в настоящее время данный параметр имеет меньшее клиническое значение с учетом наличия антиретровирусной терапии
2 - необъяснимая лихорадка, ночная потливость, непроизвольная потеря веса> 10% или диарея, сохраняющаяся> 2 недель.
|
||
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Причина развития cаркомы Капоши (СК) – вирус герпеса человека 8 типа (HHV-8, KSHV – Kaposhi sarсoma herpes virus) относится к подсемейству Gammaherpesvirinae, роду Rhadinovirus.
HHV-8 подразделяют на три варианта: А, В и С — на основании различий в нуклеотидных последовательностях субсегментов генома.
Вариант А связывают с классической СК и СПИД-ассоциированными поражениями кожи и внутренних органов, а В и С — с лимфопролиферативными заболеваниями (лимфомами, генерализованными лимфаденопатиями, болезнью Кастлемана).
Как у других герпес-вирусов, экспрессия генов зависит от стадии инфекции – латентной или литической. Во время латентной инфекции, геном HHV-8 представлен в виде эписомы и экспрессируются продукты 3 вирусных генов: ORF 72 (вирусный циклин D, угнетающий апоптоз инфицированных клеток), ORF 73 (LANA-1), и К13 (vFLIP). LANA-1 способствует распространению и транскрипции вируса в клетках за счет прикрепления ДНК HHV-8 к H1 гистону хроматина. LANA-1 угнетает транскрипционную активность р53, vFLIP защищает клетки, латентно инфицированные HHV-8 от апоптоза путем блокады Fas-рецептора и уничтожения цитотоксическими Т-лимфоцитами. Продукт гена ORF 50 (RTA) инициирует литическую фазу жизненного цикла HHV-8. После инициации литической репликации, генные продукты производятся в упорядоченной последовательности, типичной для других герпесвирусов человека. Установлено, что до 10% вирусов HHV-8, выявляемых в очагах СК, находятся в литической фазе, однако HHV-8 в лимфоцитах периферической крови выявляется, как правило, только у больных с выраженной иммуносупрессией (СПИД-ассоциированным и иммуносупрессивным типом заболевания). Ротоглотка является резервуаром наиболее выраженной репликации вируса; в слюне находится большое число копий вируса HHV-8.
HHV8 (ассоциированный с СК вирус герпеса), обнаруживается в клетках эндотелия при всех формах заболевания и представляет собой ДНК-вирус, кодирующий латентный ядерный антиген, продукт вирусного гена ORF73.
При секвенировании была выявлена взаимосвязь между генетическими вариантами HHV8 и по HHV8 передается в основном половым путем. ДНК HHV8 обнаруживается во всех формах СК (> 95% СК, связанных и не связанных со СПИДом) пуляциями пациентов (Европа, Африка, Северная Америка) Антитела против ядерных антигенов HHV8 появляются раньше, еще до клинических проявлений СК и могут быть обнаружены в периферической крови. Не все инфекции HHV8 приводят к клиническим проявлениям СК, а большинство первичных инфекций протекает бессимптомно Не у всех серопозитивных лиц развивается СК. Наличие инфекции HHV8 необходимо, но недостаточно для развития СК, которая является результатом комплексного сложного взаимодействия генетических, иммунологических и окружающих факторов.
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Частота распространения классической формы саркомы Капоши (СК) значительно варьирует в различных географических областях от 0,14 на 1 млн. жителей (как мужчин, так и женщин) до 10,5 на 1 млн. мужчин и 2,7 на 1 млн. женщин. Мужчины болеют в 3 раза чаще. Начало заболевания СК регистрируется в возрасте 35-39 лет у мужчин и в возрасте 25-39 лет у женщин Мужчины болеют в 3-10 раз чаще. Начало заболевания СК регистрируется в возрасте 50-70 лет [1, 2]. Большая частота СК наблюдается в странах, расположенных на побережье Средиземного моря и центральной Африки (эндемическая саркома Капоши). В развитых странах у пациентов, инфицированных вирусом иммунодефицита человека (ВИЧ) –1, частота выявляемости HHV-8 наиболее высока среди мужчин гомо- и бисексуальной ориентации.
Трансплантационная СК наблюдается при трансплантации органов, преимущественно при пересадке почки. Возможно развитие СК у пациентов, получающих иммуносупрессивную терапию при лечении аутоиммунных заболеваний. [3,4] Саркома Капоши является самой распространенной СПИД-ассоциированной опухолью у мужчин, практикующих гомосексуальные отношения и наблюдается у 20% больных СПИДом.
Одним из основных путей передачи HHV-8 является половой, риск инфицирования повышается с увеличением числа сексуальных партнеров и практикой нетрадиционных видов половых контактов. Неполовой механизм передачи вируса через слюну является общепризнанным и имеет важное значение в заражении детей в эндемических областях. Вертикальный путь передачи HHV-8 от матери к плоду во время беременности и родов не имеет большого значения для распространения вируса. Вирус HHV-8 также может передаваться через кровь, продукты крови, донорские органы после трансплантаций. Вирусный геном HHV-8 обнаруживается во всех элементах СК при всех стадиях заболевания независимо от клинического варианта. [1] Вирус широко распространен в популяции: примерно от 1-3% доноров крови в Северной Америке до 70% в регионах Африки, где HHV-8 является эндемичным, 90% ВИЧ-инфицированных имеют антитела к литическим белкам HHV-8, сывороточные антитела к этому вирусу у здоровых доноров из России обнаруживались в 9,6% случаев. Распространенность HHV-8 инфекции примерно отражает распространенность СК.
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
СК классическая (идиопатическая)
Типичная локализация проявлений при идиопатическом варианте СК – кожа дистальных отделов нижних конечностей. Характерно появление симметричных или ассиметричных пятнистых элементов синюшно-красного цвета, склонные к периферическому и постепенному вертикальному росту. В большинстве случаев определяется субъективно - асимптомное течение. При прогрессии СК, пятнистые элементы последовательно трансформируются в папулезные и бляшечные формы и реже узловые. Рост новообразований происходит медленно, без субъективных ощущений, некоторые годами могут оставаться неизменными в размерах, однако также описаны и быстро прогрессирующие формы. Появление болей может быть через 2-10 лет, при изъязвлении узлов, их Прогрессирование СК сопровождается диссеминацией поражений кожи и редко метастазированием в лимфатические узлы и слизистую ЖКТ [1].
СК эндемическая (африканская)
Преимущественно поражаются дети и молодые люди, характеризуется более «агрессивным» и молниеносным течением. При этом могут беспокоить появление большого числа болезненных подкожных узлов и язв, развивается нарушения внутренних органов.
СК, ассоциированная со СПИДом
Для этой формы характерно как быстрое течение, так и индолентное, зависит от уровня контроля ВИЧ инфекции. Вначале появляются высыпания на коже головы (носа, век, ушных раковин) и на туловище. Высыпания вначале безболезненные, далее сопровождаются болью и приводят к нарушению функции органов.
По локализации процесса встречаются как локализованные так и диссеминированные формы.
Клиническая картина характеризуется симптомо-комплексом зон поражения – кожные проявления или поражение висцеральных органов или слизистых.
СК на фоне иммуносупрессии
Кожные высыпания имеют ограниченный характер, не беспокоят. В дальнейшем распространение высыпаний сопровождается образованием узлов и их изъязвлением, что приводит к интенсивной локальной боли и напоминают проявления при СПИД-ассоцированной СК. Снижение дозы или отмена иммуносупрессивных препаратов приводит к полному регрессу кожных и висцеральных проявлений СК у 24-80% больных, однако возобновление их применения ведет к рецидиву заболевания.
Клинические проявления различных подтипов СК суммированы в таблице 2.
Таблица 2. Клинические проявления СК [6,14,17-21, 71-77].
| Вариант СК | Вовлечение кожных покровов | Вовлечение слизистых | Вовлечение внутренних органов | Вовлечение лимфоузлов |
|---|---|---|---|---|
| Классическая/ эндемическая СК | Индолентное, преимущественно на конечностях | <5% [1, 2] | <10% [3] | <10% [3] |
| СПИД-ассоциированная СК | Более распространенное и обширное [3] | 30-40% [4] | 20-40% [3, 4] | 25% [3, 4] |
| Пост-трансплантационная СК | Более распространенное и обширное [5] | 20% [5] | 20-50% [5] | 20-40% [5] |
Диагностика
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
1 Жалобы и анамнез
Течение и выраженность клинических симптомов зависит от варианта заболевания. Субъективные клинические проявления саркомы Капоши описаны в разделе «Клиническая картина».
2 Физикальное обследование
СК классическая (идиопатическая) (гендерных различий нет)
Критерии установления диагноза/состояния: на основании патогномоничных данных физикального обследования:
- на коже дистальных отделов нижних конечностей появляются одно- или двухсторонние синюшно-красные пятна диаметром 1-5 см с четкими границами, напоминающие гематому;
- далее элементы медленно растут, трансформируясь в плотные узелки (при слиянии формируют бляшки) и узлы;
- крупные узлы на нижних конечностях темнеют (из-за отложения гемосидерина) и изъязвляются, вызывая отторжение некротизированных тканей;
- по периферии узелков наблюдаются выраженные отеки с явлениями лимфостаза (в дальнейшем образуются участки фиброза);
- распространение высыпаний на другие участки тела, лимфатические узлы, слизистую оболочку полости рта и гениталий, внутренние органы (часто с бессимптомным течением)
- летальный исход при классической СК чаще наступает от других причин, т.к. болезнь наблюдается у лиц пожилого возраста и заболевание чаще всего развивается медленно.
СК эндемическая (африканская)
Критерии установления диагноза/состояния: на основании патогномоничных данных физикального обследования:
- СК проявляется узловым, «цветистым», инфильтративным и лимфаденопатическим вариантами;
- «цветистый», вегетирующий и инфильтративный варианты характеризуются более агрессивным течением с глубоким поражением дермы, подкожной клетчатки, мышц и костей;
- африканская СК может поражать детей, молодых людей и взрослых. У взрослого населения отмечается предрасположенность у мужского пола, у детского без половых различий. Кожа и слизистые оболочки поражаются в меньшей степени. Во взрослом возрасте часто отмечается поражение внутренних органов, у детей лимфатических узлов и внутренних органов. Может иметь молниеносное течение с очень быстрым прогрессированием.
СК эпидемическая (ассоциированная со СПИДом)
Критерии установления диагноза/состояния: на основании патогномоничных данных физикального обследования:
- Характерно быстрое течение с мультифокальным диссеминированием;
- первичные проявления СК на лице отмечаются чаще на коже носа, век, ушных раковин, на туловище - вдоль линий натяжения кожи;
- при отсутствии лечения диссеминированные элементы могут сливаться с образованием крупных бляшек, распространяющихся на кожу лица, туловища или конечностей, что нередко приводит к нарушениям функции органов;
- слизистая оболочка полости рта поражается у 10-15% больных. Наиболее типично расположение высыпаний в области твердого и мягкого неба и корня языка, где они быстро изъязвляются;
- часто наблюдается поражение глотки, которое может приводить к затруднению приема пищи, речи и дыхания;
- желудок и двенадцатиперстная кишка представляют собой места излюбленной локализации СК, и заболевание нередко сопровождается кровотечением и непроходимостью кишечника;
- при легочной форме СК могут наблюдаться респираторные симптомы: бронхоспазм, кашель и прогрессирующая дыхательная недостаточность.
СК на фоне иммуносупрессии
Критерии установления диагноза/состояния: на основании патогномоничных данных физикального обследования: развивается после трансплантации внутренних органов и обусловлена ятрогенным воздействием иммунодепрессантов (L04A);
- кожные проявления вначале имеют ограниченный характер, затем распространяются и напоминают высыпания эпидемической СК.
Снижение дозы или отмена иммунодепрессантов (L04A) приводит к полному регрессу кожных и висцеральных проявлений СК у 24-80% больных, однако возобновление их применения ведет к рецидиву заболевания.
3 Лабораторные диагностические исследования
Диагностика СК основана на данных физикального обследования – выявление типичных проявлений для соответствующих стадий СК, при дерматоскопии определяются синевато-красноватая окраска, «структура радуги», чешуйчатая поверхность и маленькие коричневые глобулы. Диагноз подтверждается патолого-анатомическим исследованием биопсийного (операционного) материала. Учитывая высокую частоту ассоциации заболевания со СПИДом необходимо проведения серологического исследование на ВИЧ. При подозрении на СК показано обследование на наличие специфических антител к HHV-8.
При диссеминированных формах показаны дополнительные лабораторные и инструментальные исследования для оценки висцеральных проявлений СК.
- Рекомендовано для подтверждения диагноза проводить патолого-анатомическое исследование биопсийного (операционного) материала кожи [1, 14].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5).
Комментарии: При патолого-анатомическом исследовании выделяют ангиоматозный, фибробластический и смешанный варианты СК. В пятнистых элементах определяется увеличение числа дермальных сосудов, окруженных эндотелиальными клетками, в прилегающих участках - отложения гемосидерина и экстравазальные эритроциты с умеренным периваскулярным инфильтратом. В бляшках при СК выявляется выраженная сосудистая пролиферация во всех структурах дермы, включая коллагеновые волокна. Характерным является наличие плотных тяжей и веретенообразных клеток между зазубренными сосудистыми клетками. В узлах больных СК определяются преимущественно веретеновидные клетки, участки ангиоматоза и плотные саркоматозные волокна. Воспалительный инфильтрат состоит из лимфоцитов, гистиоцитов и плазмоцитов. При СК иммуногистохимически выявляется экспрессия сосудистых маркеров CD31, CD34 и лимфоидных клеток D2-40 (подопланин) [1].
- Рекомендовано всем пациентам определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови и определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови для исключения ассоциации с ВИЧ- инфекцией [14, 45].
Уровень убедительности рекомендаций C (уровень достоверности доказательств 5).
- Рекомендовано всем пациентам с ВИЧ-ассоциированной СК исследование крови на наличие специфических антител к HHV-8 [14, 45].
Уровень убедительности рекомендаций C (уровень достоверности доказательств 5).
4 Инструментальные диагностические исследования
- Рекомендован осмотр всех кожных покровов и элементов подозрительных на саркому Капоши всем пациентам под увеличением (дерматоскопия) для первичной диагностики [39].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 4).
Комментарии: при дерматоскопии СК выявляются следующие дерматоскопические особенности: синевато-красноватая окраска (в 84% поражений), «структура радуги» (36%), чешуйчатая поверхность и маленькие коричневые глобулы (15%). Разноцветная структура радуги – наиболее значимый дерматоскопический паттерн, обнаруживаемый поляризованным дерматоскопом. Структура радуги не наблюдается в других сосудистых опухолях.
- Рекомендовано всем пациентам с саркомой Капоши для cтадирования и оценки распространенности СК проводить обследование пациентов в соответствии с таблицей 4. При диссеменированных формах или подозрении на наличие висцеральных проявлений СК, при наличии симптомов поражения желудочно-кишечного тракта, органов дыхания и костной системы, по показаниям, выполняются следующие исследования: эзофагогастродуоденоскопия, колоноскопия, бронхоскопия, магнитно-резонансная томография органов брюшной полости, компьютерная томография органов грудной полости, позитронная эмисионная томография совмещенная с компьютерной томографией с туморотропным РФП с контрастированием [14, 45, 71-76].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
5 Иные диагностические исследования
- Рекомендована консультация врача-онколога всем пациентам при выявлении любых форм СК, для определения тактики лечения. [43].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4).
- Рекомендовано назначение антиретровирусной терапии всем пациентам с саркомой Капоши и ВИЧ [14, 77].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Общие комментарии по лечению
Методы лечения саркомы Капоши зависят от клинической формы заболевания, размера поражений и вовлеченных в патологический процесс органов и/или систем, а также от состояния пациента по шкале ВОЗ/ECOG.
Несмотря на доказанную роль онкогенной герпесвирусной инфекции, вызываемой HHV-8, в патогенезе саркомы Капоши, J05AB нуклеозиды и нуклеотиды, кроме ингибиторов обратной транскриптазы (противогерпетические) не применяют вследствие их низкой эффективности [49].
- Рекомендовано при выявлении СК у пациентов, получающих иммунодепрессанты L04A, производить коррекцию дозы и /или схемы иммунодепрессантов [14, 49, 52, 77].
Уровень убедительности рекомендаций C (уровень достоверности доказательств 5).
1. Хирургическое лечение
- Рекомендовано для лечения локализованной формы СК последовательное хирургическое удаление ограниченных очагов СК, что позволяет в течение многих лет контролировать заболевание [1].
Уровень убедительности рекомендаций C (уровень достоверности доказательств 5)
Комментарии Необходимо принимать во внимание, что в связи с высокой частотой развития рецидивов необходимо его выполнять при наличии четко ограниченных опухолей и поверхностных опухолях. Не следует рассматривать данный вариант лечения как основной при обширных поражениях. Следует использовать принципы хирургии немеланомных злокачественных новообразований кожи с адекватным отступом и этапами пластической хирургии по необходимости. Следует проводить изучение хирургических краев. При положительном крае целесообразно выполнение повторного вмешательства. При расположении единичных образований на сложных анатомических зонах (лицо, кисть) следует отдавать предпочтение хирургическому иссечению с интраоперационным изучением краев резекции.
2. Лекарственное лечение
- Рекомендовано для лечения диссеминированных форм СК (в т.ч. с поражением внутренних органов) проведение лекарственной терапии классической СК:
#доксорубицин** 20 мг/м2 (липосомальный) каждые 3 недели, длительность лечения регламентируется достижением максимального эффекта и последующим проведением 2-х закрепляющих курсов химиотерапии [14, 15, 45, 77].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
- Рекомендовано для лечения диссеминированных форм СК
#Паклитаксел** 80мг/м2 еженедельно или 100 мг/м2 каждые 2 недели до достижения эффекта под контролем лабораторных и функциональных показателей [14, 15, 45, 77, 84-86].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
- Рекомендовано для лечения диссеминированных форм СК:
#помалидомид** 5 мг 1 раз/сут с 1-го по 21-й день, цикл каждые 28 дней [47, 48, 77]
Уровень убедительности рекомендаций В (уровень достоверности доказательств 3)
Комментарии: В клинических исследованиях #помалидомида** использовалась доза 5 мг / день и в качестве терапии первой линии. Однако #помалидомид** предоставляется в дозе 4 мг, и эксперты со-авторы КР в области лечения СК, а также эксперты NCCN считают, что 4мг это достаточная доза [54, 77].
- Рекомендовано проведение терапии интерфероном альфа-2b** при наличии противопоказаний к химиотерапии и/ или при неагрессивной не ассоциированной с ВИЧ-инфекцией саркоме Капоши:
# Интерферон альфа-2b** – 3 или 6 млн МЕ п/к 3 раза в неделю – 6 месяцев [14, 82]
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
- Не рекомендовано применение специфических антигерпетических препаратов: J05AB нуклеозиды и нуклеотиды, кроме ингибиторов обратной транскриптазы и J05AF нуклеозиды и нуклеотиды – ингибиторы обратной транскриптазы [15, 45]
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
- Рекомендовано в качестве терапии второй или последующих линий использовать следующие режимы:
1) #гемцитабин ** 1000 мг/м2 в/в в день 1 и день 8, цикл каждые 21 день либо 1200 мг в/в в день 1 и день 8, цикл каждые 21 день [2, 14, 26, 77, 80, 81]
Уровень убедительности рекомендаций С (уровень достоверности доказательств 4)
2) Этопозид** 50мг перорально в день в течении 7 дней, цикл 14 дней; после 2 циклов при удовлетворительной переносимости возможна эскалация дозы до 100мг р.о. в день в течении 7 дней, цикл каждые 14 дней [14, 28, 77]
Уровень убедительности рекомендаций C (уровень достоверности доказательств 5)
Комментарии: для лечения пациентов с саркомой Капоши доза этопозида** устанавливается индивидуально, в зависимости от линии терапии, гематологических показателей пациента и возраста пациента. В связи с редкой заболеваемостью большинство исследований лекарственной терапии были проведены для популяции пациентов с ВИЧ-инфекцией, где СК встречается чаще, однако данные по эффективности химиотерапии используются в том числе и для пациентов без ВИЧ. Указанные дозы лишь отчасти соответствуют зарегистрированной в РФ инструкции к таблетированному этопозиду**.
3) # Иматиниб** 400 мг в день р.о. длительно до 12 месяцев терапии с возможным увеличением дозы до 600 мг/день через 3 месяца, если отмечается стабилизация заболевания. [24, 29, 77]
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарий: данный режим изучался в исследовании II для пациентов с ВИЧ-ассоциированной саркомой Капоши, сообщество экспертов считает, что эти данные можно экстраполировать на пациентов с СК без ВИЧ в виду редкой встречаемости данной нозологической единицы. Что подтверждено внесением данной опции лечения в рекомендации NCCN.
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
- Рекомендовано для лечения диссеминированных форм саркомы Капоши при прогрессировании использовать монотерапию МКА-блокаторами PD1:
# пембролизумаб** 200 мг в/в капельно 1 раз в 21 день, длительно [60-62, 77].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 4)
3. Иные варианты локального лечения
- Рекомендовано для лечения локализованной формы СК только при наличии противопоказаний к хирургическому лечению или невозможности его выполнения:
Криодеструкция очагов СК на коже [6, 14, 77, 83]
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
- Рекомендовано для лечения локально-распространенных форм СК без висцеральных проявлений:
Аппликационная лучевая терапия с изготовлением и применением индивидуальных апликаторов. 3D -4D планирование, Интраоперационная лучевая терапия, Конформная дистанционная лучевая терапия, Конформная дистанционная лучевая терапия пучками нейтронов, протонов и тяжелых ионов [51]
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: выбор типа и полей облучения зависит от локализации и количества очагов СК.
Лучевая терапия является одним из самых эффективных методов локального лечения и используется для лечения всех вариантов локально-распространенных форм СК. Частота ответа на лучевую терапию варьирует от 47% до 99% [1-8,31-38]. Рекомендованные дозы лучевой терапии составляют 30-36Гр по 2-3Гр ежедневно. Назначения более 3Гр за фракцию совместно с системной терапии рекомендовано избегать для снижения риска отдаленных осложнений.
Использование лучевой терапии следует обсудить на междисциплинироном консилиуме. Радиотерапия при локализации процесса на подошвенной поверхности стопы и ладонной кисти ограничена побочными эффектами. Во всех случаях следует рассмотреть радиотерапию при неэффективности системной терапии и невозможности хирургии.
- Рекомендовано локальное лечение для лечения локализованной формы СК в неоперабельных случаях:
#Имихимод (5%) на очаги СК, 3 раза в неделю, не менее 16 недель [9, 14, 45, 53, 77-79]. Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
4. Обезболивание
Принципы обезболивания и оптимального выбора противоболевой терапии у пациентов с саркомой Капоши с хроническим болевым синдромом соответствуют принципам обезболивания, изложенным в клинических рекомендациях «Хронический болевой синдром у взрослых пациентов, нуждающихся в паллиативной медицинской помощи».
5. Сопутствующая терапия у больных саркомой Капоши
Принципы профилактики и лечения анемии у пациентов с саркомой Капоши соответствуют принципам, изложенным в клинических рекомендациях «Анемия при злокачественных новообразованиях», размещенным в рубрикаторе клинических рекомендаций Минздрава России https://cr.minzdrav.gov.ru
Принципы лечения и профилактики тошноты и рвоты у пациентов с саркомой Капоши соответствуют принципам, изложенным в методических рекомендациях «Профилактика и лечение тошноты и рвоты». Коллектив авторов: Владимирова Л.Ю., Гладков О.А., Королева И.А., Румянцев А.А., Семиглазова Т.Ю., Трякин А.А. и соавт. DOI: 10.18027/2224-5057-2023-13-3s2-2-29-44, https://rosoncoweb.ru/standarts/RUSSCO/2023/2023-38.pdf
Принципы лечения и профилактики костных осложнений у пациентов с саркомой Капоши соответствуют принципам, изложенным в методических рекомендациях «Патология костной ткани». Коллектив авторов: Багрова С.Г., Басин Е.М., Борзов К.А., Бычкова Н.М., Деньги- на Н. В., Копп М.В., Крылов В.В., Кочетова Т.Ю., Семиглазова Т.Ю. DOI: 10.18027/2224-5057-2023-13-3s2-2-44-59. https://rosoncoweb.ru/standarts/RUSSCO/2023/2023-39.pdf
Принципы профилактики и лечения фебрильной нейтропении у пациентов с саркомой Капоши соответствуют принципам, изложенным в методических рекомендациях «Фебрильная нейтропения». Коллектив авторов: Сакаева Д.Д., Борисов К.Е., Булавина И.С., Когония Л.М., Курмуков И.А., Орлова Р.В., Шабаева М.М. DOI: 10.18027/2224-5057-2023-13-3s2-2-60-68. https://rosoncoweb.ru/standarts/RUSSCO/2023/2023-40.pdf
Принципы профилактики и лечения гепатотоксичности у пациентов с саркомой Капоши соответствуют принципам, изложенным в методических рекомендациях «Гепатотоксичность». Коллектив авторов: Ткаченко П. Е., Ивашкин В. Т., Маевская. DOI: 10.18027/2224-5057-2023-13-3s2-2-69-82. https://rosoncoweb.ru/standarts/RUSSCO/2023/2023-41.pdf
Принципы профилактики и лечения сердечно-сосудистых осложнений у пациентов с саркомой Капоши соответствуют принципам, изложенным в методических рекомендациях «Кардиоваскулярная токсичность». Коллектив авторов: Виценя М.В., Агеев Ф.Т., Орлова Р.В., Полтавская М.Г., Потиевская В.И. DOI: 10.18027/2224-5057-2023-13-3s2-2-83-107. https://rosoncoweb.ru/standarts/RUSSCO/2023/2023-42.pdf
Принципы профилактики и лечения кожных осложнений у пациентов с саркомой Капоши соответствуют принципам, изложенным в методических рекомендациях «Дерматологические реакции». Коллектив авторов: Королева И.А., Болотина Л.В., Гладков О.А., Горбунова В.А., Ко- гония Л.М., Круглова Л.С., Орлова Е.В., Орлова Р.В. DOI: 10.18027/2224-5057-2023-13-3s2-2-108-131. https://rosoncoweb.ru/standarts/RUSSCO/2023/2023-43.pdf
Принципы нутритивной поддержки у пациентов с саркомой Капоши соответствуют принципам, изложенным в методических рекомендациях «Нутритивная поддержка». Коллектив авторов: Сытов А.В., Зузов С.А., Кукош М.Ю., Лейдерман И.Н., Обухова О.А., Потапов А.Л., Хотеев А.Ж. DOI: 10.18027/2224-5057-2023-13-3s2-2-132-142. https://rosoncoweb.ru/standarts/RUSSCO/2023/2023-44.pdf
Принципы профилактики и лечения нефротоксичности у пациентов с саркомой Капоши соответствуют принципам, изложенным в методических рекомендациях «Нефротоксочность». Коллектив авторов: Громова Е.Г., Бирюкова Л.С., Джумабаева Б.Т., Курмуков И.А. DOI: 10.18027/2224-5057-2023-13-3s2-2-153-166. https://rosoncoweb.ru/standarts/RUSSCO/2023/2023-47.pdf
Принципы профилактики и лечения тромбоэмболических осложнений у пациентов с саркомой Капоши соответствуют принципам, изложенным в методических рекомендациях «Тромбоэмболические осложнения». Коллектив авторов: Сомонова О.В., Антух Э.А., Варданян А.В., Громова Е.Г., Долгушин Б.И., Елизарова А.Л., Сакаева Д.Д., Сельчук В.Ю., Трякин А.А., Черкасов В.А. DOI: 10.18027/2224-5057-2023-13-3s2-2-167-178. https://rosoncoweb.ru/standarts/RUSSCO/2023/2023-48.pdf
Принципы профилактики и лечения последствий экстравазации лекарственных препаратов у пациентов с саркомой Капоши соответствуют принципам, изложенным в методических рекомендациях «Экстравазация противоопухолевых препаратов». Авторы: Буйденок Ю.В., Обухова О.А. DOI: 10.18027/2224-5057-2023-13-3s2-2-179-189. https://rosoncoweb.ru/standarts/RUSSCO/2023/2023-49.pdf
Принципы профилактики и лечения иммуноопосредованных нежелательных явлений у пациентов с саркомой Капоши соответствуют принципам, изложенным в методических рекомендациях «Иммуноопосредованные нежелательные явления». Коллектив авторов: Проценко С.А., Баллюзек М.Ф., Васильев Д.А., Жукова Н.В., Новик А.В., Носов Д.А., Петенко Н.Н., Семенова А.И., Харкевич Г.Ю., Юдин Д.И. DOI: 10.18027/2224-5057-2023-13-3s2-2-210-249. https://rosoncoweb.ru/standarts/RUSSCO/2023/2023-51.pdf
6. Диетотерапия
Диетотерапия не используется для лечения саркомы Капоши.
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Данные рекомендации сделаны на основании того, что во многих исследованиях доказано, что различные виды медицинской реабилитации значительно ускоряют функциональное восстановление, сокращают сроки пребывания в стационаре после операции и снижают частоту развития осложнений и летальных исходов у пациентов с другими злокачественными новообразованиями.
1. Предреабилитация
- Рекомендуется проведение предреабилитации всем пациентам с саркомой Капоши в целях ускорения функционального восстановления, сокращения сроков пребывания в стационаре после операции, снижения частоты развития осложнений и летальных исходов на фоне лечения меланомы. Предреабилитация включает физическую подготовку (ЛФК), психологическую и нутритивную поддержку, информирование пациентов [63].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5)
Комментарий: Целесообразно советовать пациенту увеличить физическую активность за 2 недели до операции в целях снижения сроков пребывания в стационаре и риска развития послеоперационных осложнений, а также повышения качества жизни в послеоперационном периоде [64].
2. Первый этап реабилитации
- Рекомендуется мультидисциплинарный подход при проведении реабилитации пациентов в онкодерматологии с включением двигательной реабилитации, психологической поддержки, работы со специалистами по трудотерапии (инструкторами по трудовой терапии) [65].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
- Рекомендуется раннее начало восстановительного лечения, поскольку оно улучшает функциональные результаты после операций в онкодерматологии [66].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
- Рекомендуется комплекс ЛФК в каждом конкретном случае разрабатывать индивидуально, исходя из особенностей и объема операции [67].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
3. Второй этап реабилитации
- Рекомендовано использовать методики, направленные на мобилизацию рубцов для профилактики формирования грубых рубцовых изменений, в том числе в глубоких слоях мягких тканей: глубокий медицинский массаж, упражнения на растяжку, ультразвуковую терапию с целью размягчения рубцовых изменений [68].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств –5).
4. Третий этап реабилитации
- Рекомендуется выполнение и постепенное расширение комплекса ЛФК с включением аэробной нагрузки, что улучшает результаты комбинированного лечения злокачественных новообразований и качество жизни [69].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
- Рекомендован медицинский массаж для улучшения качества жизни, уменьшения болевого синдрома, слабости [70].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5)
Госпитализация
Организация оказания медицинской помощи
При подозрении на саркому Капоши врач-дерматовенеролог выполняет диагностические исследования (осмотр кожи под увеличением (дерматоскопия), забор материала для патолого-анатомического исследования биопсийного (операционного) материала кожи).
При подозрении или выявлении у пациента саркомы Капоши врачи-дерамтовенерологи, а также врачи-терапевты, врачи-терапевты участковые, врачи общей практики (семейные врачи), врачи-специалисты, средние медицинские работники в установленном порядке направляют пациента на консультацию в центр амбулаторной онкологической помощи, а при отсутствии в первичный онкологический кабинет, поликлиническое отделение онкологического диспансера (онкологической больницы) для оказания ему первичной специализированной медико-санитарной помощи.
Консультация в центре амбулаторной онкологической помощи либо в первичном онкологическом кабинете, поликлиническом отделении онкологического диспансера (онкологической больницы) должна быть проведена не позднее 3 рабочих дней с даты выдачи направления на консультацию. Врач-онколог центра амбулаторной онкологической помощи (в случае отсутствия центра амбулаторной онкологической помощи врач-онколог первичного онкологического кабинета или поликлинического отделения онкологического диспансера (онкологической больницы организует взятие биопсийного (операционного) материала, а также организует выполнение иных диагностических исследований, необходимых для установления диагноза, включая распространенность онкологического процесса и стадию заболевания.
В случае невозможности взятия в медицинской организации, в составе которой организован центр амбулаторной онкологической помощи (первичный онкологический кабинет) биопсийного (операционного) материала, проведения иных диагностических исследований пациент направляется врачом-онкологом в онкологический диспансер (онкологическую больницу) или в медицинскую организацию, оказывающую медицинскую помощь пациентам с онкологическими заболеваниями.
Срок выполнения патологоанатомических исследований, необходимых для гистологической верификации злокачественных новообразований не должен превышать 15 рабочих дней с даты поступления биопсийного (операционного) материала в патологоанатомическое бюро (отделение).
Сроки проведения диагностических инструментальных и лабораторных исследований в случае подозрения на онкологическое заболевание не должны превышать сроков, установленных в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации, 7 рабочих дней со дня назначения исследований.
Диагноз онкологического заболевания устанавливается врачом-специалистом на основе результатов диагностических исследований, включающих в том числе проведение цитологической и (или) гистологической верификации диагноза, за исключением случаев, когда взятие биопсийного и (или) пункционного материала не представляется возможным.
Врач-онколог центра амбулаторной онкологической помощи (первичного онкологического кабинета) направляет пациента в онкологический диспансер (онкологическую больницу) или иную медицинскую организацию, оказывающую медицинскую помощь пациентам с онкологическими заболеваниями, в том числе подведомственную федеральному органу исполнительной власти (далее – федеральная медицинская организация), для уточнения диагноза (в случае невозможности установления диагноза, включая распространенность онкологического процесса и стадию заболевания), определения тактики лечения, а также в случае наличия медицинских показаний для оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
При онкологических заболеваниях, входящих в рубрики С37, C38, C40–C41, C45–C49, С58, D39, C62, C69–C70, С72, C74 МКБ-10, а также соответствующих кодам международной классификации болезней – онкология (МКБ-О), 3 издания 8936, 906-909, 8247/3, 8013/3, 8240/3, 8244/3, 8246/3, 8249/3 врач-онколог онкологического диспансера (онкологической больницы) или иной медицинской организации, оказывающей медицинскую помощь пациентам с онкологическими заболеваниями, для определения лечебной тактики организует проведение консультации или консилиума врачей, в том числе с применением телемедицинских технологий, в федеральных государственных бюджетных учреждениях, подведомственных Министерству здравоохранения Российской Федерации, оказывающих медицинскую помощь (далее в целях настоящего Порядка – национальные медицинские исследовательские центры).
В сложных клинических случаях для уточнения диагноза (в случае невозможности установления диагноза, включая распространенность онкологического процесса и стадию заболевания) в целях проведения оценки, интерпретации и описания результатов врач-онколог организует направление:
- цифровых изображений, полученных по результатам патоморфологических исследований, в патолого-анатомическое бюро (отделение) четвертой группы (референс-центр)[1] путем информационного взаимодействия, в том числе с применением телемедицинских технологий при дистанционном взаимодействии медицинских работников между собой;
- цифровых изображений, полученных по результатам лучевых методов исследований, в дистанционный консультативный центр лучевой диагностики, путем информационного взаимодействия, в том числе с применением телемедицинских технологий при дистанционном взаимодействии медицинских работников между собой;
- биопсийного (операционного) материала для повторного проведения патоморфологических, иммуногистохимических, и молекулярно-генетических исследований: в патолого-анатомическое бюро (отделение) четвертой группы (референс-центр), а также в молекулярно-генетические лаборатории для проведения молекулярно-генетических исследований.
Тактика лечения устанавливается консилиумом врачей, включающим врачей-онкологов, врача-радиотерапевта, врача-нейрохирурга (при опухолях нервной системы) медицинской организации, в составе которой имеются отделения хирургических методов лечения злокачественных новообразований, противоопухолевой лекарственной терапии, радиотерапии (далее – онкологический консилиум), в том числе онкологическим консилиумом, проведенным с применением телемедицинских технологий, с привлечением при необходимости других врачей-специалистов.
Диспансерное наблюдение врача-онколога за пациентом с выявленным онкологическим заболеванием устанавливается и осуществляется в соответствии с порядком диспансерного наблюдения за взрослыми с онкологическими заболеваниями.
С целью учета информация о впервые выявленном случае онкологического заболевания направляется в течение 3 рабочих дней врачом-онкологом медицинской организации, в которой установлен соответствующий диагноз, в онкологический диспансер или организацию субъекта Российской Федерации, исполняющую функцию регистрации пациентов с впервые выявленном злокачественным новообразованием, в том числе с применением единой государственной информационной системы в сфере здравоохранения. В случае подтверждения у пациента наличия онкологического заболевания информация об уточненном диагнозе направляется из онкологического диспансера или организации субъекта Российской Федерации, исполняющей функции регистрации пациентов с впервые выявленном злокачественным новообразованием, в медицинскую организацию, осуществляющую диспансерное наблюдение пациента
Специализированная, в том числе высокотехнологичная, медицинская помощь в медицинских организациях, оказывающих медицинскую помощь взрослому населению при онкологических заболеваниях, оказывается по медицинским показаниям, предусмотренным положением об организации оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
Специализированная, за исключением высокотехнологичной, медицинская помощь в медицинских организациях, подведомственных федеральным органам исполнительной власти, оказывается по медицинским показаниям, предусмотренным пунктом 5 порядка направления пациентов в медицинские организации и иные организации, подведомственные федеральным органам исполнительной власти, для оказания специализированной (за исключением высокотехнологичной) медицинской помощи, предусмотренного в приложении к положению об организации оказания специализированной, в том числе высокотехнологичной, медицинской помощи. (Пункт 5: для получения специализированной медицинской помощи в плановой форме выбор федеральной медицинской организации осуществляется по направлению лечащего врача.) В случае если в реализации Программы принимают участие несколько федеральных медицинских организаций, оказывающих специализированную медицинскую помощь при заболеваниях, состояниях (группе заболеваний, состояний), соответствующих заболеваниям, состояниям (группе заболеваний, состояний) пациента, лечащий врач обязан проинформировать пациента (законного представителя пациента) о возможности выбора федеральной медицинской организации, в том числе о возможных сроках ожидания специализированной медицинской помощи, которые могут превышать сроки ожидания, установленные программой государственных гарантий бесплатного оказания гражданам медицинской помощи.
Сроки ожидания оказания специализированной (за исключением высокотехнологичной) медицинской помощи не должны превышать сроков, установленных в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации, 7 рабочих дней.
При наличии у пациента с онкологическим заболеванием медицинских показаний для проведения медицинской реабилитации врач-онколог организует ее проведение в соответствии с порядком организации медицинской реабилитации взрослых.
При наличии у пациента с онкологическим заболеванием медицинских показаний к санаторно-курортному лечению врач-онколог организует его в соответствии порядком организации санаторно-курортного лечения.
Паллиативная медицинская помощь пациенту с онкологическими заболеваниями оказывается в соответствии с положением об организации оказания паллиативной медицинской помощи, включая порядок взаимодействия медицинских организаций, организаций социального обслуживания и общественных объединений, иных некоммерческих организаций, осуществляющих свою деятельность в сфере охраны здоровья.
При подозрении и (или) выявлении у пациента онкологического заболевания в ходе оказания ему скорой медицинской помощи его переводят или направляют в медицинские организации, оказывающие медицинскую помощь пациентам с онкологическими заболеваниями, для определения тактики ведения и необходимости применения дополнительно других методов специализированного противоопухолевого лечения.
Показаниями для госпитализации в медицинскую организацию в экстренной или неотложной форме являются:
1) наличие осложнений онкологического заболевания, требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме;
2) наличие осложнений лечения онкологического заболевания (хирургическое вмешательство, ЛТ, лекарственная терапия и т.д.), требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме
Показаниями для госпитализации в медицинскую организацию в плановой форме являются:
1) необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, а также проведение эндоскопических исследований при невозможности выполнить их амбулаторно, требуют последующего наблюдения в условиях круглосуточного или дневного стационара;
2) наличие показаний к специализированному противоопухолевому лечению (хирургическое вмешательство, ЛТ, в том числе контактная, ДЛТ и другие виды ЛТ, лекарственная терапия и др.), требующему наблюдения в условиях круглосуточного или дневного стационара.
Показаниями к выписке пациента из медицинской организации являются:
1) завершение курса лечения или одного из этапов оказания специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара при условии отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
2) отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара, установленной консилиумом медицинской организации, оказывающей онкологическую помощь;
3) в случаях несоблюдения пациентом предписаний или правил внутреннего распорядка лечебно-профилактического учреждения, если это не угрожает жизни пациента и здоровью окружающих;
4) необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи.
Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или предварительного осмотра пациента врачами-специалистами медицинской организации, в которую планируется перевод.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Диспансерному наблюдению подлежат взрослые с онкологическими заболеваниями, включенными в рубрики С00-D09 МКБ-10.
Диспансерное наблюдение организуется в центре амбулаторной онкологической помощи, либо в первичном онкологическом кабинете медицинской организации, онкологическом диспансере (онкологической больнице) или иных медицинских организациях, оказывающих медицинскую помощь больным с онкологическими заболеваниями.
Комментарии: На сегодняшний день нет единого мнения относительно частоты и интенсивности наблюдения за пациентами с саркомой Капоши. Целями наблюдения за пациентами следует считать раннее выявление рецидива заболевания, ранее выявление 2-х опухолей, а также психосоциальную поддержку пациентов.
Необходимый объем обследования в период наблюдения за пациентами с саркомой Капоши зависит от подтипа СК (таблица 4).
Таблица 4. Объем обследования в период наблюдения за пациентами с СК после окончания терапии
| Классическая эндемическая СК | СПИД-ассоциированная СК | Ятрогенная СК | |
|---|---|---|---|
| Клинический осмотр | ++ | ++ | ++ |
| Определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита ьчеловека ВИЧ- (Human immunodeficiency virus HIV 1) в крови, Определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови | - | - | - |
| Стандартные анализы крови | + | ++ | ++ |
| HHV-8 виремия | - | - | - |
| CD4 клетки | - | ++ | + |
| Патолого-анатомическое исследование | - |
-
|
-
|
| КТ всего тела | +- | +- | +- |
| Бронхоскопия | +- | +- | +- |
| Эндоскопическое исследование ЖКТ | +- | +- | +- |
|
Необходимость выполнения:
+ используют
- не используют
++ обязательно
+ - в зависимости от симптомов
|
|||
- Рекомендовано при диссеминированных формах, а также жизне-угрожающих клинических ситуациях (ВИЧ-ассоциированная СК с обширным поражением, формы СК после трансплантации органа) клинический осмотр и наблюдение не реже 1 раза в месяц и 1 раза в 3 месяца выполнение КТ всего тела до тех пор пока не будет достигнута стабилизация заболевания [1,14 ]
Уровень убедительности рекомендаций – С (уровень достоверности доказательств –5)
- Рекомендовано для классической формы СК с индолентным течением проводить клинический осмотр 1 раз в 6 - 12 месяцев [1,14]
Уровень убедительности рекомендаций – С (уровень достоверности доказательств –5)
Комментарий: задачей наблюдения является наиболее раннее выявление прогрессирования заболевания в целях раннего начала ХТ или ЛТ, или хирургического лечения в зависимости от выявленной ситуации.
Информация
Источники и литература
-
Клинические рекомендации Ассоциации онкологов России
- Клинические рекомендации Ассоциации онкологов России - 1. Friedman-Birnbaum R, Bergman R, Bitterman-Deutsch O, Weltfriend S, Lichtig C. Classic and iatrogenic Kaposi"s sarcoma. Histopathological patterns as related to clinical course. Am J Dermatopathol. 1993 Dec;15(6):523-7. PMID: 8311180. 2. PDQ® Adult Treatment Editorial Board. PDQ Kaposi Sarcoma Treatment. Bethesda, MD: National Cancer Institute. 3. Mbulaiteye SM, Engels EA. Kaposi"s sarcoma risk among transplant recipients in the United States (1993-2003). Int J Cancer. 2006 Dec 1;119(11):2685-91. 4. Stallone G., Schena A., Infante B. et al. Sirolimus for Kaposi"s sarcoma in renal-transplant recipients. N Engl J Med. 2005; 352 (13): 1317–1323. 5. Di Lorenzo G, Konstantinopoulos PA, Pantanowitz L, et al. Management of AIDS-related Kaposi"s sarcoma. Lancet Oncol. Feb 2008;8(2):167-76. 6. Kutlubay Z, Kucuktas M, Yardimci G, et al. Evaluation of effectiveness of cryotherapy on the treatment of cutaneous Kaposi"s sarcoma. Dermatol Surg. 2013 Oct;39(10):1502-6. 7. Tsao MN, Sinclair E, Assaad D, et al.: Radiation therapy for the treatment of skin Kaposi sarcoma. Ann Palliat Med 5 (4): 298-302, 2016. 8. Régnier-Rosencher E, Guillot B, Dupin N: Treatments for classic Kaposi sarcoma: a systematic review of the literature. J Am Acad Dermatol 68 (2): 313-31, 2013. 9. E Odyakmaz Demirsoy, D Bayramgürler, Ç Çağlayan, N Bilen, A Şikar Aktürk, R Kıran Imiquimod 5% Cream Versus Cryotherapy in Classic Kaposi Sarcoma/ Journal of cutaneous medicine and surgery, 2019. 10. Cianfrocca M, Lee S, Von Roenn J, Tulpule A, Dezube BJ, Aboulafia DM, et al. Randomized trial of paclitaxel versus pegylated liposomal doxorubicin for advanced human immunodeficiency virus-associated Kaposi sarcoma: evidence of symptom palliation from chemotherapy. Cancer. Aug 15 2010;116(16):3969-77. 11. Brinkhof MW, Pujades-Rodriguez M, Egger M. Mortality of patients lost to follow-up in antiretroviral treatment programmes in resource-limited settings: systematic review and meta-analysis. PLoS One. 2009 Jun 4;4(6):e5790. doi: 10.1371/journal.pone.0005790. PMID: 19495419; PMCID: PMC2686174. 12. Hu S.C., Ke C.L., Lee C.H. et al. // J. Eur. Acad. Dermatol. Venerol. – 2009. – Vol. 23, N 10. – P. 1128– 1132 Soft Tissue and Bone Tumours WHO Classification of Tumours, 5th Edition, Volume 3, WHO Classification of Tumours Editorial Board. 13. Soft Tissue and Bone TumoursWHO Classification of Tumours, 5th Edition, Volume 3, WHO Classification of Tumours Editorial Board,ISBN - 978-92-832-4502-5, Cree, Ian A. (EditorialBoard Chair). 14. Lebbe C, Garbe C, Stratigos AJ, Harwood C, Peris K, Marmol VD, Malvehy J, Zalaudek I, Hoeller C, Dummer R, Forsea AM, Kandolf-Sekulovic L, Olah J, Arenberger P, Bylaite-Bucinskiene M, Vieira R, Middleton M, Levy A, Eggermont AM, Battistella M, Spano JP, Grob JJ, Pages C; European Dermatology Forum (EDF), the European Association of Dermato-Oncology (EADO) and the European Organisation for Research and Treatment of Cancer (EORTC). Diagnosis and treatment of Kaposi"s sarcoma: European consensus-based interdisciplinary guideline (EDF/EADO/EORTC). Eur J Cancer. 2019 Jun;114:117-127. doi: 10.1016/j.ejca.2018.12.036. Epub 2019 May 13. PMID: 31096150. 15. Erin Reid, Gita Suneja et al, NCCN Clinical Practice Guidelines in Oncology, Version 3.2020 AIDS-Related Kaposi Sarcoma. 16. Krown SE, Testa MA, Huang J. AIDS-related Kaposi’s sarcoma: prospective validation of the AIDS Clinical Trials Group staging classification. AIDS Clinical Trials Group Oncology Committee. J Clin Oncol 1997;15:3085e92. 17. Brenner B, Weissmann-Brenner A, Rakowsky E, Weltfriend S, Fenig E, Friedman-Birnbaum R, et al. Classical Kaposi sarcoma: prognostic factor analysis of 248 patients. Cancer 2002;95:1982e7. 18. Zaraa I, Labbene I, El Guellali N, Ben Alaya N, Mokni M, Ben Osman A. [Kaposi’s sarcoma: epidemiological, clinical, anatomopathological and therapeutic features in 75 patients]. Tunis Med 2012;90:116e21. 19. Bower M, Dalla Pria A, Coyle C, Andrews E, Tittle V, Dhoot S, et al. Prospective stage-stratified approach to AIDS-related Kaposi’s sarcoma. J Clin Oncol 2014;32:409e14. 20. Nasti G, Martellotta F, Berretta M, Mena M, Fasan M, Di Perri G, et al. Impact of highly active antiretroviral therapy on the presenting features and outcome of patients with acquired immunodeficiency syndrome-related Kaposi sarcoma. Cancer 2003; 98:2440e6. 21. Frances C. Kaposi’s sarcoma after renal transplantation. Nephrol Dial Transplant 1998;13:2768e73. 22. Pellet C, Kerob D, Dupuy A, Carmagnat MV, Mourah S, Podgorniak MP, et al. Kaposi’s sarcoma-associated herpesvirus viremia is associated with the progression of classic and endemic Kaposi’s sarcoma. J Invest Dermatol 2006;126:621e7. 23. Jakob L, Metzler G, Chen KM, Garbe C. Non-AIDS associated Kaposi’s sarcoma: clinical features and treatment outcome. PLoS One 2011;6:e18397 24. Erin Reid, Gita Suneja et al, NCCN Clinical Practice Guidelines in Oncology, Version 1.2021 AIDS-Related Kaposi Sarcoma.25. Koon HB, Krown SE, Lee JY, Honda K, Rapisuwon S, Wang Z, Aboulafia D, Reid EG, Rudek MA, Dezube BJ, Noy A. Phase II trial of imatinib in AIDS-associated Kaposi"s sarcoma: AIDS Malignancy Consortium Protocol 042. J Clin Oncol. 2014 Feb 10;32(5):402-8. doi: 10.1200/JCO.2012.48.6365. Epub 2013 Dec 30. PMID: 24378417; PMCID: PMC3912327. 26. Strother RM, Gregory KM, Pastakia SD, Were P, Tenge C, Busakhala N, Jakait B, Schellhase EM, Rosmarin AG, Loehrer PJ. Retrospective analysis of the efficacy of gemcitabine for previously treated AIDS-associated Kaposi"s sarcoma in western Kenya. Oncology. 2010;78(1):5-11. doi: 10.1159/000292356. Epub 2010 Mar 6. PMID: 20215784 27. Reid E, Suneja G, Ambinder RF, Ard K, Baiocchi R, Barta SK, Carchman E, Cohen A, Crysler OV, Gupta N, Gustafson C, Hall A, Johung KL, Klopp A, LaCasce AS, Lin C, Mehta A, Menon MP, Morgan D, Nathwani N, Noy A, Ratner L, Rizza S, Rudek MA, Sanchez J, Taylor J, Tomlinson B, Wang CJ, Yendamuri S, Dwyer MA; CGC; Freedman-Cass DA. AIDS-Related Kaposi Sarcoma, Version 2.2019, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw. 2019 Feb;17(2):171-189. doi: 10.6004/jnccn.2019.0008. PMID: 30787130. 28. Hosseinipour MC, Kang M, Krown SE, Bukuru A, Umbleja T, Martin JN, Orem J, Godfrey C, Hoagland B, Mwelase N, Langat D, Nyirenda M, MacRae J, Borok M, Samaneka W, Moses A, Mngqbisa R, Busakhala N, Martínez-Maza O, Ambinder R, Dittmer DP, Nokta M, Campbell TB; A5264/AMC-067 REACT-KS Team. As-Needed Vs Immediate Etoposide Chemotherapy in Combination With Antiretroviral Therapy for Mild-to-Moderate AIDS-Associated Kaposi Sarcoma in Resource-Limited Settings: A5264/AMC-067 Randomized Clinical Trial. Clin Infect Dis. 2018 Jul 2;67(2):251-260. doi: 10.1093/cid/ciy044. PMID: 29365083; PMCID: PMC6030807. 29. Cao W, Vyboh K, Routy B, Chababi-Atallah M, Lemire B, Routy JP. Imatinib for highly chemoresistant Kaposi sarcoma in a patient with long-term HIV control: a case report and literature review. Curr Oncol. 2015 Oct;22(5):e395-9. doi: 10.3747/co.22.2635. PMID: 26628884; PMCID: PMC4608417. 30. Koon HB, Krown SE, Lee JY, Honda K, Rapisuwon S, Wang Z, Aboulafia D, Reid EG, Rudek MA, Dezube BJ, Noy A. Phase II trial of imatinib in AIDS-associated Kaposi"s sarcoma: AIDS Malignancy Consortium Protocol 042. J Clin Oncol. 2014 Feb 10;32(5):402-8. doi: 10.1200/JCO.2012.48.6365. Epub 2013 Dec 30. PMID: 24378417; PMCID: PMC3912327. 31. Stelzer KJ, Griffin TW. A randomized prospective trial of radiation therapy for AIDS-associated Kaposi’s sarcoma. Int J Radiat Oncol Biol Phys 1993;27:1057e61. 32. Singh NB, Lakier RH, Donde B. Hypofractionated radiation therapy in the treatment of epidemic Kaposi sarcoma–a prospective randomized trial. Radiother Oncol 2008;88:211e6. 33. Harrison M, Harrington KJ, Tomlinson DR, Stewart JS. Response and cosmetic outcome of two fractionation regimens for AIDS-related Kaposi’s sarcoma. Radiother Oncol 1998;46:23e8.34. Kigula-Mugambe JB, Kavuma A. Epidemic and endemic Kaposi’s sarcoma: a comparison of outcomes and survival after radiotherapy. Radiother Oncol 2005;76:59e62. 35. Yildiz F, Genc M, Akyurek S, Cengiz M, Ozyar E, Selek U, et al. Radiotherapy in the management of Kaposi’s sarcoma: comparison of 8 Gy versus 6 Gy. J Natl Med Assoc 2006;98:1136e9. 36. Caccialanza M, Marca S, Piccinno R, Eulisse G. Radiotherapy of classic and human immunodeficiency virus-related Kaposi’s sarcoma: results in 1482 lesions. J Eur Acad Dermatol Venereol 2008;22:297e302.Hamilton CR, Cummings BJ, Harwood AR. Radiotherapy of Kaposi’s sarcoma. Int J Radiat Oncol Biol Phys 1986;12:1931e5. 37. Hamilton CR, Cummings BJ, Harwood AR. Radiotherapy of Kaposi’s sarcoma. Int J Radiat Oncol Biol Phys 1986;12:1931e5. 38. Weshler Z, Loewinger E, Loewenthal E, Levinson R, Fuks Z. Megavoltage radiotherapy using water bolus in the treatment of Kaposi’s sarcoma. Int J Radiat Oncol Biol Phys 1986;12:2029e32. 39. Ertürk Yılmaz T, Akay BN, Okçu Heper A. Dermoscopic findings of Kaposi sarcoma and dermatopathological correlations. Australas J Dermatol. 2020 Feb;61(1):e46-e53. doi: 10.1111/ajd.13150. Epub 2019 Sep 8. PMID: 31495914. 40. Т.Фицпатрик,Р.Джонсон,К.Вулф Дерматология атлас-справочник 1999 . 41. А.А.Кубанова, В.И.Кисина Рациональная фармокотерапия заболеваний кожи и инфекций,передаваемых половым путем 2005 42. Казанцева К.В., Молочков А.В., Молочков В.А., Сухова Т.Е., Прокофьев А.А., Каприн А.Д., Галкин В.Н., Иванов С.А., Каплан М.А., Романко Ю.С., Попучиев В.В. Саркома Капоши: патогенез, клиника, диагностика и современные принципы лечения // Российский журнал кожных и венерических болезней. 2015. №1. 43. Karass M, Grossniklaus E, Seoud T, Jain S, Goldstein DA. Kaposi Sarcoma Inflammatory Cytokine Syndrome (KICS): A Rare but Potentially Treatable Condition. Oncologist. 2017 May;22(5):623-625. doi: 10.1634/theoncologist.2016-0237. Epub 2017 Apr 19. PMID: 28424322; PMCID: PMC5423516. 44. Hoffmann C, Sabranski M, Esser S. HIV-Associated Kaposi"s Sarcoma. Oncol Res Treat. 2017;40(3):94-98. doi: 10.1159/000455971. Epub 2017 Feb 9. PMID: 28259888. 45. В.В.Рассохин, А.Р.Крестьянинов Саркома Капоши. Диагностика и лечение//Практическая онкология, Т. 13, №2 – 2012 46. Zidan J, Robenstein W, Abzah A, Taman S. Treatment of Kaposi"s sarcoma with vinblastine in patients with disseminated dermal disease. Isr Med Assoc J. 2001 Apr;3(4):251-3. PMID: 11344835.47. Goncalves PH, Ziegelbauer J, Uldrick TS, Yarchoan R. Kaposi sarcoma herpesvirus-associated cancers and related diseases. Curr Opin HIV AIDS. 2017 Jan;12(1):47-56. doi: 10.1097/COH.0000000000000330. PMID: 27662501; PMCID: PMC6311702. 48. Polizzotto MN, Uldrick TS, Wyvill KM, Aleman K, Peer CJ, Bevans M, Sereti I, Maldarelli F, Whitby D, Marshall V, Goncalves PH, Khetani V, Figg WD, Steinberg SM, Zeldis JB, Yarchoan R. Pomalidomide for Symptomatic Kaposi"s Sarcoma in People With and Without HIV Infection: A Phase I/II Study. J Clin Oncol. 2016 Dec;34(34):4125-4131. doi: 10.1200/JCO.2016.69.3812. Epub 2016 Oct 31. Erratum in: J Clin Oncol. 2018 Jul 1;36(19):2008. doi: 10.1200/JCO.2018.79.3158. PMID: 27863194; PMCID: PMC5477825. 49. Казанцева К.В., Молочков А.В., Молочков В.А., Сухова Т.Е., Прокофьев А.А., Каприн А.Д., Галкин В.Н., Иванов С.А., Каплан М.А., Романко Ю.С., Попучиев В.В. Саркома Капоши: патогенез, клиника, диагностика и современные принципы лечения// РОССИЙСКИЙ ЖУРНАЛ КОЖНЫХ И ВЕНЕРИЧЕСКИХ БОЛЕЗНЕЙ No 1, 2015. 50. Карташова М. Г. Фотодинамическая терапия в лечении идиопатического типа саркомы Капоши// Дерматология №2 2009. 51. Карташова М. Г Современные подходы к диагностике и лечению идиопатического типа саркомы Капоши //Дерматология 2 — 2008. 52. Moray G, Başaran O, Yağmurdur MC, Emiroğlu R, Bilgin N, Haberal M. Immunosuppressive therapy and Kaposi"s sarcoma after kidney transplantation. Transplant Proc. 2004 Jan-Feb;36(1):168-70. doi: 10.1016/j.transproceed.2003.11.016. PMID: 15013336. 53. Htet KZ, Waul MA, Leslie KS. Topical treatments for Kaposi sarcoma: A systematic review. Skin Health Dis. 2022 Apr 8;2(2):e107. doi: 10.1002/ski2.107. PMID: 35677916; PMCID: PMC9168015. 54. Erin Reid et al. NCCN Guidelines Version 1.2021, Kaposi Sarcoma, 2/12/21 55. Brambilla L, Labianca R, Boneschi V, Fossati S, Dallavalle G, Finzi AF, Luporini G. Mediterranean Kaposi"s sarcoma in the elderly. A randomized study of oral etoposide versus vinblastine. Cancer. 1994 Nov 15;74(10):2873-8. doi: 10.1002/1097-0142(19941115)74:10<2873>3.0.co;2-1. PMID: 7954250. 56. Brambilla L, Boneschi V, Fossati S, Melotti E, Clerici M. Oral etoposide for Kaposi"s Mediterranean sarcoma. Dermatologica. 1988;177(6):365-9. doi: 10.1159/000248608. PMID: 2466707. 57. Tas F, Sen F, Keskin S, Kilic L. Oral etoposide as first-line therapy in the treatment of patients with advanced classic Kaposi"s sarcoma (CKS): a single-arm trial (oral etoposide in CKS). J Eur Acad Dermatol Venereol. 2013 Jun;27(6):789-92. doi: 10.1111/j.1468-3083.2011.04404.x. Epub 2011 Dec 20. PMID: 22188463.58. Oken M. M., Creech R. H., Tormey D. C., Horton J., Davis T. E., McFadden E. T., Carbone P. P. Toxicity and response criteria of the Eastern Cooperative Oncology Group // Am J Clin Oncol. ‒ 1982. ‒ T. 5, № 6. ‒ C. 649-55. 59. Karnofsky D. A., Burchenal J. H. The clinical evaluation of chemotherapeutic agents in cancer // Evaluation of chemotherapeutic agents / MacLeod C. ‒ New York: Columbia University Press, 1949. ‒ C. 191-205
- Клинические рекомендации Ассоциации онкологов России - 60. M. Silveira Vilbert, I. Hirsch, E.C. Koch, T. Pimentel Muniz, D. Pinheiro Xavier et al. Treatment of Kaposi sarcoma with immune-checkpoint inhibitors: A systematic review and single-arm meta-analysis. 775P, Vol.33, Suppl. 7, S895, Sep 2022.I:https://doi.org/10.1016/j.annonc.2022.07.901 61. Delyon J, Biard L, Renaud M, Resche-Rigon M, et al. PD-1 blockade with pembrolizumab in classic or endemic Kaposi"s sarcoma: a multicentre, single-arm, phase 2 study. Lancet Oncol. 2022 Apr;23(4):491-500. doi: 10.1016/S1470-2045(22)00097-3. Epub 2022 Mar 10. PMID: 35279271. 62. Lolli I, Valentini AM, Ricci AD, Armentano R. Anaplastic Classic Kaposi Sarcoma: PD-L1 Expression and Response to Immunotherapy: A Case Report and Review of the Literature. J Natl Compr Canc Netw. 2023 Apr 7;21(5):442-448.e2. doi: 10.6004/jnccn.2022.7091. PMID: 37028800. 63. Silver JK, Baima J: Cancer prehabilitation: an opportunity to decrease treatment-related morbidity, increase cancer treatment options, and improve physical and psychological health outcomes. Am J Phys Med Rehabil 2013, 92(8):715-727. 64. Nilsson H, Angeras U, Bock D, Borjesson M, Onerup A, Fagevik Olsen M, Gellerstedt M, Haglind E, Angenete E: Is preoperative physical activity related to post-surgery recovery? A cohort study of patients with breast cancer. BMJ open 2016, 6(1):e007997. 65. Siegel GW, Biermann JS, Chugh R, Jacobson JA, Lucas D, Feng M, Chang AC, Smith SR, Wong SL, Hasen J: The multidisciplinary management of bone and soft tissue sarcoma: an essential organizational framework. J Multidiscip Healthc 2015, 8:109-115. 66. Shehadeh A, El Dahleh M, Salem A, Sarhan Y, Sultan I, Henshaw RM, Aboulafia AJ: Standardization of rehabilitation after limb salvage surgery for sarcomas improves patients" outcome. Hematol Oncol Stem Cell Ther 2013, 6(3-4):105-111. 67. Cox CL, Montgomery M, Oeffinger KC, Leisenring W, Zeltzer L, Whitton JA, Mertens AC, Hudson MM, Robison LL: Promoting physical activity in childhood cancer survivors: results from the Childhood Cancer Survivor Study. Cancer 2009, 115(3):642-654. 68. Oren R, Zagury Al, Katzir O, Kollender Y, Meller I: Musculoskeletal Cancer Surgery. In., edn. Edited by Malawer. Dordrecht: Springer; 2013: 583-593.69. Segal R, Zwaal C, Green E, Tomasone JR, Loblaw A, Petrella T, Exercise for People with Cancer Guideline Development G: Exercise for people with cancer: a systematic review. Curr Oncol 2017, 24(4):e290-e315. 70. Boyd C, Crawford C, Paat CF, Price A, Xenakis L, Zhang W, Evidence for Massage Therapy Working G: The Impact of Massage Therapy on Function in Pain Populations-A Systematic Review and Meta-Analysis of Randomized Controlled Trials: Part II, Cancer Pain Populations. Pain Med 2016, 17(8):1553-1568. 71. O"Mahony D, Gandjbakche A, Hassan M, Vogel A, Yarchoan R. Imaging techniques for Kaposi"s sarcoma. J HIV Ther. 2008 Sep;13(3):65-71. PMID: 19039297; PMCID: PMC2600536. 72. Restrepo CS, Ocazionez D. Kaposi"s sarcoma: imaging overview. Semin Ultrasound CT MR. 2011 Oct;32(5):456-69. doi: 10.1053/j.sult.2011.03.007. PMID: 21963166. 73. Addula D, Das CJ, Kundra V. Imaging of Kaposi sarcoma. Abdom Radiol (NY). 2021 Nov;46(11):5297-5306. doi: 10.1007/s00261-021-03205-6. Epub 2021 Jul 13. PMID: 34255129; PMCID: PMC8502139. 74. Weprin L, Zollinger R, Clausen K, Thomas FB. Kaposi"s sarcoma: endoscopic observations of gastric and colon involvement. J Clin Gastroenterol. 1982 Aug;4(4):357-60. PMID: 7119413. 75. Aliaga Ramos J, Cedrón Cheng H, Pinto Valdivia J. Clinical and endoscopic findings of patients with cutaneous Kaposi sarcomaand gastrointestinal involvement. Experience in a single center of Lima-Peruin the last 3 years. Rev Gastroenterol Peru. 2019 Apr-Jun;39(2):123-126. English. PMID: 31333227. 76. Carmo J, Marques SC, Bispo M, Pinto D, Chagas C. Clinical and Endoscopic Features of Gastrointestinal Kaposi Sarcoma: A Single-Center Portuguese Experience over the Last Decade. GE Port J Gastroenterol. 2017 Sep;24(5):219-226. doi: 10.1159/000461592. Epub 2017 Apr 11. PMID: 29255756; PMCID: PMC5729958. 77. Erin Reid, Gita Suneja et al. NCCN Guidelines Version 1.2024 Kaposi Sarcoma. https://www.nccn.org/professionals/physician_gls/pdf/kaposi.pdf 78. Célestin Schartz NE, Chevret S, Paz C, Kerob D, Verola O, Morel P, Lebbé C. Imiquimod 5% cream for treatment of HIV-negative Kaposi"s sarcoma skin lesions: A phase I to II, open-label trial in 17 patients. J Am Acad Dermatol. 2008 Apr;58(4):585-91. doi: 10.1016/j.jaad.2007.11.005. Epub 2008 Feb 20. PMID: 18068265. 79. Benomar S, Boutayeb S, Benzekri L, Errihani H, Hassam B. Kaposi"s sarcoma responding to topical imiquimod 5% cream: a case report. Cases J. 2009 Sep 17;2:7092. doi: 10.1186/1757-1626-0002-0000007092. PMID: 20181188; PMCID: PMC2827081. 80. Brambilla L, Labianca R, Ferrucci SM, Taglioni M, Boneschi V. Treatment of classical Kaposi"s sarcoma with gemcitabine. Dermatology. 2001;202(2):119-22. doi: 10.1159/000051610. PMID:11306832. 81. Badalamenti G, Incorvaia L, Algeri L, Bonasera A, Dimino A, Scalia R, Cucinella A, Madonia G, Pomi FL, Galvano A, Gristina V, Toia F, Cordova A, Bazan V, Russo A. Safety and effectiveness of gemcitabine for the treatment of classic Kaposi"s sarcoma without visceral involvement. Ther Adv Med Oncol. 2022 Mar 26;14:17588359221086829. doi: 10.1177/17588359221086829. PMID: 35356263; PMCID: PMC8958699. 82. Costa da Cunha CS, Lebbe C, Rybojad M, Agbalika F, Ferchal F, Rabian C, Vignon-Pennamen MD, Calvo F, Morel P. Long-term follow-up of non-HIV Kaposi"s sarcoma treated with low-dose recombinant interferon alfa-2b. Arch Dermatol. 1996 Mar;132(3):285-90. doi: 10.1001/archderm.132.3.285. PMID: 8607632. 83. Curatolo P, Careri R, Simioni A, Campana LG. Cryotherapy, Imiquimod, and Electrochemotherapy Are Effective Options for Kaposi Sarcoma: A Call for Standardization to Allow for Comparisons and Informed Decisions. J Cutan Med Surg. 2020 Mar/Apr;24(2):218-219. doi: 10.1177/1203475419893302. PMID: 32208013. 84. Chao S, Lee Y, Tsao C. Treatment of classical type Kaposi"s sarcoma with paclitaxel. Anticancer Res 21: 571-574, 200. 85. Engin H, Celik I. Treatment of classical Kaposi"s sarcoma with visceral involvement by weekly paclitaxel. Clin Oncol (R Coll Radiol). 2002 Apr;14(2):178. doi: 10.1053/clon.2002.0058. PMID: 12069127. 86. Paksoy N, Khanmammadov N, Doğan İ, Ferhatoğlu F, Ahmed MA, Karaman S, Aydiner A. Weekly paclitaxel treatment in the first-line therapy of classic Kaposi sarcoma: A real-life study. Medicine (Baltimore). 2023 Feb 3;102(5):e32866. doi: 10.1097/MD.0000000000032866. PMID: 36749246; PMCID: PMC9901949.
Информация
Список сокращений
ВИЧ – вирус иммунодефицита человека
ВОЗ – всемирная организация здравоохранения
ЕД – единица действия
ЖКТ – желудочно-кишечный тракт
МКБ – Международная классификация болезней
МКБ-10 – Международная классификация болезней 10-го пересмотра
СК – саркома Капоши
СПИД – синдром приобретенного иммунодефицита
HHV-8 (human herpesvirus 8) – герпесвирус человека 8 типа
LANA-1 (latency-associated nuclear antigen-1) – ядерный антиген, ассоциированный с латентностью-1
ORF (opening reading frame) – открытая рамка считывания
vFLIP (viral FLICE-inhibitory protein) – вирусный белок, ингибирующий протеазу FLICE
** – жизненно необходимые и важнейшие лекарственные препараты
# – препарат, применяющийся не в соответствии с показаниями к применению противопоказаниями, способами применения и дозами, содержащимися в инструкции по применению лекарственного препарата (офф-лейбл)
Термины и определения
Саркома Капоши – мультицентрический неопластический процесс, развивающийся из эндотелия кровеносных и лимфатических сосудов, с преимущественным поражением кожных покровов и вовлечением внутренних органов.
HHV-8 (human herpesvirus 8, герпесвирус человека 8 типа) – гамма-герпесвирус, ассоциированный с саркомой Капоши.
ECOG (Eastern Cooperative Oncology Group) – шкала оценки общего состояния онкологического больного до начала лечения, в процессе и после его окончания по 5-степенной системе (рекомендована Восточной кооперативной онкологической группой).
Блокатор PD1 – моноклональное антитело, блокирующее взаимодействие между рецептором программируемой смерти (PD-1) и его лигандами.
Предреабилитация (prehabilitation) – реабилитация с момента постановки диагноза до начала лечения (хирургического лечения/химиотерапии/лучевой терапии).
Первый этап реабилитации – реабилитация в период специализированного лечения основного заболевания (включая хирургическое лечение/химиотерапию/лучевую терапию) в отделениях медицинских организаций по профилю основного заболевания.
Второй этап реабилитации – реабилитация в стационарных условиях медицинских организаций (реабилитационных центров, отделений реабилитации), в ранний восстановительный период течения заболевания, поздний реабилитационный период, период остаточных явлений течения заболевания.
Третий этап реабилитации – реабилитация в ранний и поздний реабилитационный периоды, период остаточных явлений течения заболевания в отделениях (кабинетах) реабилитации, физиотерапии, лечебной физкультуры, рефлексотерапии, мануальной терапии, психотерапии, медицинской психологии, кабинетах логопеда (учителя-дефектолога), оказывающих медицинскую помощь в амбулаторных условиях, дневных стационарах, а также выездными бригадами на дому (в том числе в условиях санаторно-курортных организаций).
Известные на сегодняшний день прогностические факторы, используемые для стадирования, приведены в таблице 5.
Таблица 5. Классификация стадирования СПИД-ассоциированной СК [1,2,3]
| Фактор |
Хороший прогноз
(все факторы)
|
Плохой прогноз
(один из факторов)
|
|---|---|---|
| Опухоль, T | T0: ограничена кожей и/или лимфоузлами и/или минимальные проявления со стороны полости рта (не узловая СК) |
Т1:отек или изъязвление, связанное с опухолью
Распространенная форма СК в полости рта
СК желудочно-кишечного тракта
СК другого органа за исключением лимфоузлов
|
| Иммунная система. I1 | I0: CD4+ клетки > 150/mL | I1: CD4+ клетки < 150/mL |
| Системные состояния/ заболевания. S |
S0:нет указания в анамнезе на оппуртонистические инфекции или афтозный стоматит
Нет симптомов «В»2
Общее состояние по шкале Карновского более 70
|
S1: есть указание в анамнезе на оппуртонистические инфекции или афтозный стоматит
Есть симптомы «В»2
Общее состояние по шкале Карновского менее 70
Другие ВИЧ-ассоциированные заболевания (неврологические болезни, лимфома)
|
|
1 - в настоящее время данный параметр имеет меньшее клиническое значение с учетом наличия антиретровирусной терапии
2 - необъяснимая лихорадка, ночная потливость, непроизвольная потеря веса> 10% или диарея, сохраняющаяся> 2 недель.
|
||
Критерии оценки качества медицинской помощи
Критерии оценки качества медицинской помощи приведены в табл. 6.
Таблица 6. Критерии оценки качества медицинской помощи
| № | Критерии качества | Оценка выполнения |
|---|---|---|
| 1 |
Проведено патолого - анатомическое исследование биопсийного (операционного) материала кожи
|
Да/ Нет |
| 2 | Выполнено исследование крови на наличие специфических антител к HHV-8 | Да/ Нет |
| 3 | Проведена консультация врача – онколога при выявлении саркомы Капоши для определения тактики лечения | Да/ Нет |
| 4 | Проведено определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови и определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови для исключения ассоциации с ВИЧ- инфекцией | Да/ Нет |
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
- Кубанов А.А., член-корреспондент РАН, доктор медицинских наук, профессор, директор ФГБУ «ГНЦДК» Минздрава России, президент Российского общества дерматовенерологов и косметологов.
- Снарская Е.С., доктор медицинских наук, профессор кафедры кожных и венерических болезней «Первого МГМУ им. И.М.Сеченова».
- Дубенский В.В., доктор медицинских наук, профессор, Заслуженный врач Российской Федерации, заведующий кафедрой дерматовенерологии с курсом косметологии ФГБОУ ВО Тверской ГМУ Минздрава России, г. Тверь, член Российского общества дерматовенерологов и косметологов.
- Дубенский В.В., кандидат медицинских наук, заместитель главного врача по медицинской части ГБУЗ «Центр специализированных видов медицинской помощи им. В.П. Аваева», профессор кафедры дерматовенерологии с курсом косметологии ФГБОУ ВО Тверской ГМУ Минздрава России, член Российского общества дерматовенерологов и косметологов.
- Жучков М.В., кандидат медицинских наук, заместитель главного врача по организационно-методической работе ГБУ РО «ОККВД».
- Феденко А.А., заведующий отделом лекарственного лечения опухолей МНИОИ им. П.А. Герцена-филиал ФГБУ «НМИЦ радиологии» Минздрава России
- Демидов Л.В., доктор медицинских наук, профессор, заведующий отделением опухолей кожи отдела лекарственного лечения ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина» Минздрава России, председатель правления Ассоциации специалистов по проблемам меланомы.
- Орлова К.В., кандидат медицинских наук, старший научный сотрудник отделения опухолей кожи отдела лекарственного лечения ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина» Минздрава России; член правления Ассоциации специалистов по проблемам меланомы
- Бохян Б.Ю., кандидат медицинских наук, старший научный сотрудник отдела общей онкологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, член Восточно-Европейской группы по изучению сарком
- Бухаров А.В., кандидат медицинских наук, старший научный сотрудник ФГБУ «НМИЦ радиологии» Минздрава России.
- Курильчик А.А., кандидат медицинских наук, ведущий научный сотрудник МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России, эксперт «Восточно-европейской группы по изучению сарком».
Блок по медицинской реабилитации:
- Бутенко A.B., д.м.н., профессор, председатель НС «Ассоциация специалистов по онкологической реабилитации»
- Обухова O.A., к.м.н., врач-физиотерапевт, заведующий отделением реабилитации ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, член Европейской ассоциации парентерального и энтерального питания (ESPEN), Российской ассоциации парентерального и энтерального питания (RESPEN);
- Семиглазова Т.Ю., д.м.н., ведущий научный сотрудник научного отдела инновационных методов терапевтической онкологии и реабилитации ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, доцент кафедры онкологии ФГБОУ ВО «СЗГМУ им. И.И. Мечникова» Минздрава России;
- Филоненко Е.В., д.м.н., профессор, заведующая центром лазерной и фотодинамической диагностики и терапии опухолей МНИОИ им. П.А. Герцена – филиала ФГБУ «НМИЦ радиологии» Минздрава России, врач-онколог;
Блок по организации медицинской помощи:
- Иванов Сергей Анатольевич, профессор РАН, доктор медицинских наук, директор МРНЦ им. А.Ф. Цыба - филиал ФГБУ «НМИЦ радиологии» Минздрава России, Московская область, Обнинск.
- Невольских A.A., д.м.н., профессор, заместитель директора по лечебной работе МРНЦ им. А.Ф. Цыба – филиала ФГБУ «НМИЦ радиологии» Минздрава России;
- Хайлова Ж.В., к.м.н., главный врач клиники МРНЦ им. А.Ф. Цыба – филиала ФГБУ «НМИЦ радиологии» Минздрава России.
- Геворкян Тигран Гагикович, заместитель директора НИИ КЭР ФГБУ «НМИЦ онкологии им.Н.Н. Блохина», Москва.
Конфликта интересов нет.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
- врачи-онкологи;
- врачи-хирурги;
- врачи-радиологи;
- врачи-генетики;
- врачи-дерматовенерологи;
- врачи-патологоанатомы;
- врачи-терапевты;
- врачи-терапевты участковые;
- врачи общей практики (семейные врачи);
- студенты медицинских вузов, ординаторы и аспиранты.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
| УДД | Расшифровка |
|---|---|
| 1 | Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
| 2 | Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
| 3 | Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая |
| 5 | Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
| УДД | Расшифровка |
|---|---|
| 1 | Систематический обзор РКИ с применением мета-анализа |
| 2 | Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа |
| 3 | Нерандомизированные сравнительные исследования, в т.ч. когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
| 5 | Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
| УУР | Расшифровка |
|---|---|
| A | Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
| B | Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
| C | Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учётом следующих нормативно-правовых документов:
- Приказ Минздрава России от 19.02.2021 № 116н «Об утверждении Порядка оказания медицинской помощи взрослому населению при онкологических заболеваниях».
- Приказ Минздрава России от 04.06.2020 № 548н «Об утверждении порядка диспансерного наблюдения за взрослыми с онкологическими заболеваниями».
- Приказ Минздрава России от 27.04.2021 № 404н «Об утверждении порядка проведения профилактического медицинского осмотра и диспансеризации определенных групп взрослого населения».
- Приказ Минздрава России от 10.05.2017 №203н «Об утверждении критериев оценки качества медицинской помощи».
- Распоряжение Правительства Российской Федерации от 12.10.2019 г. № 2406-р (в ред. от 24.12.2022) «Об утверждении перечня жизненно необходимых и важнейших лекарственных препаратов, а также перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи».
- Приказ Минздрава России от 28.02.2019 № 103н «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности, включаемой в клинические рекомендации информации» (зарегистрировано в Минюсте России 08.05.2019 № 54588).
- Методические рекомендации по проведению оценки научной обоснованности, включаемой в клинические рекомендации информации, ФГБУ «Центр экспертизы и контроля качества» Министерства здравоохранения Российской Федерации, 2019 г.
- Актуальные инструкции к лекарственным препаратам, упоминаемым в данных клинических рекомендациях, можно найти на сайте http://grls.rosminzdrav.ru.
Приложение Б. Алгоритмы действий врача
Блок-схема 1. Алгоритм ведения пациента
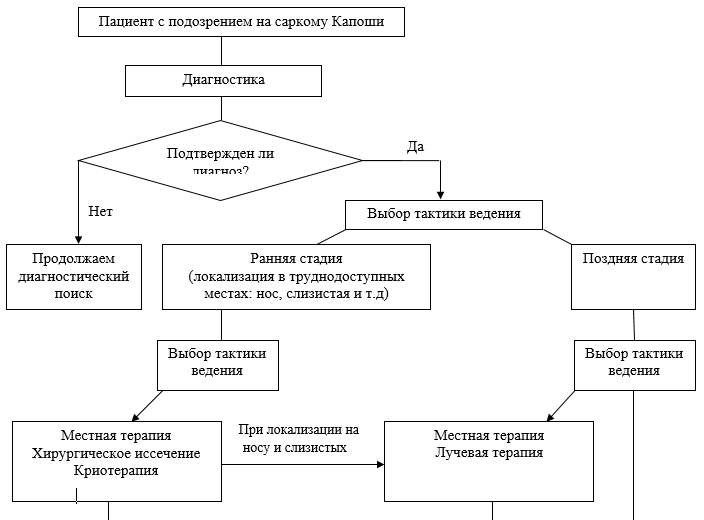
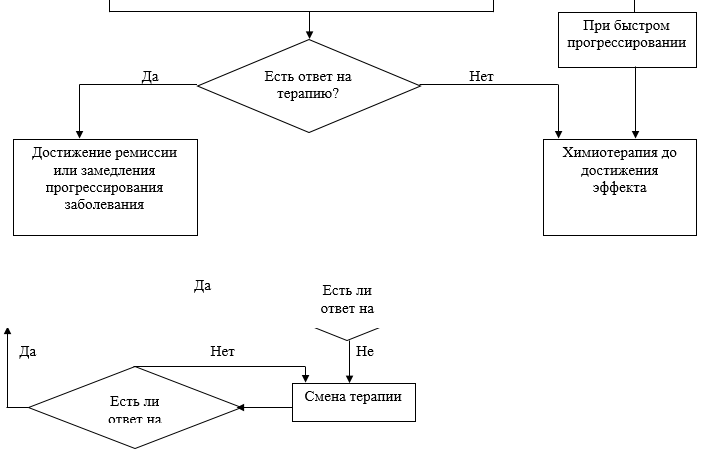
Приложение В. Информация для пациента
Рекомендации при осложнениях химиотерапии
При осложнениях химиотерапии необходимо связаться с врачом-онкологом (химиотерапевтом).
1. При повышении температуры тела до +38 °C и выше начать прием антибиотиков в соответствии с назначением врача-онколога.
2. При стоматите:
- диета – механическое, термическое щажение;
- часто (каждый час) полоскать полость рта отварами ромашки, коры дуба, шалфея, смазывать десна облепиховым (персиковым) маслом;
- обрабатывать полость рта по рекомендации врача-онколога.
3. При диарее:
- диета – исключить жирное, острое, копченое, сладкое, молочное, клетчатку. Можно употреблять нежирное мясо, мучное, кисломолочное, рисовый отвар. Обильное питье;
- принимать лекарственные препараты в соответствии с назначением врача-онколога
4. При тошноте принимать лекарственные препараты в соответствии с назначением врача-онколога.
Информация для пациента, получающего терапию моноклональными антителами – блокаторами PD1 (АТХ L01FF02, # пембролизумаб** (АТХ – L01XC18))
Своевременное взаимодействие с вашим лечащим врачом и медицинской̆ сестрой по поводу состояния вашего здоровья является важной составляющей помощи медицинской команде в защите вас в процессе лечения настолько безопасно, насколько это возможно.
Очень важно, чтобы любые симптомы (побочные явления), связанные с лечением блокаторами PD1 (АТХ L01FF02, # пембролизумаб** (АТХ – L01XC18)), были выявлены и излечены в самом начале их проявлений, это поможет предотвратить их переход в более тяжелые степени.
МКА-блокаторы PD1 (АТХ L01FF02, # пембролизумаб** (АТХ – L01XC18)) разработаны, чтобы помочь иммунной системе вашего организма бороться с опухолевым процессом. Наиболее частые побочные эффекты, с которыми Вы можете столкнуться в процессе лечения, являются результатом высокой активности иммунной системы. Такие побочные эффекты называются связанными с иммунной системой и отличаются от побочных эффектов, которые вы можете наблюдать при других видах лечения злокачественных опухолей.
Побочные явления, которые могут появиться у вас, обычно возникают в первые 12 нед лечения, но могут появиться и позже.
Очень важно, чтобы вы информировали вашего лечащего врача о любых симптомах, которые появились у вас во время лечения блокаторами PD1. Распознавание побочных эффектов на ранних стадиях дает возможность вашему лечащему врачу сразу же начать соответствующую терапию и предотвратить переход побочных явлений в более тяжелые степени.
Если после лечения МКА-блокаторами PD1 (АТХ L01FF02, # пембролизумаб** (АТХ – L01XC18)) у вас возникли симптомы из указанных ниже, пожалуйста, сообщите об этом вашему лечащему врачу незамедлительно.
Возможные побочные явления после терапии блокаторами PD1:
- увеличение числа актов дефекации до 2 и более в день или любая диарея в ночное время, любой стул со слизью и кровью;
- боль в животе или чувство озноба, а также боль, требующая медицинского вмешательства;
- красные болезненные глаза или желтоватая окраска белков глаз, затуманенный взгляд, воспаление или припухлость глаз;
- желтая окраска или покраснение кожи, зудящая сыпь, чувствительность кожи на солнце;
- вновь возникший кашель или одышка;
- усталость или сонливость;
- затрудненная концентрация внимания или спутанность сознания;
- головная боль, боль в теле или в месте опухоли;
- лихорадка (повышение температура тела до +38 °C);
- внезапное снижение или увеличение массы тела;
- вновь появившаяся эректильная дисфункция или потеря интереса к интимной жизни.
Пожалуйста, уделите особое внимание любым изменениям в актах дефекации. Записывайте количество актов каждый день. Диарея не всегда может проявляться в виде жидкого стула. Увеличение числа актов дефекации в день даже при твердом стуле потенциально может указывать на проблему.
Важно: побочные эффекты могут возникнуть в период от 1 нед до нескольких месяцев от начала лечения блокаторами PD1. Если у вас возник любой из вышеназванных симптомов, незамедлительно сообщите об этом вашему лечащему врачу или медицинской сестре.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Шкала оценки тяжести состояния пациента по версии ВОЗ/ECOG [58]
Название на русском языке: Шкала оценки тяжести состояния пациента по версии ВОЗ/ECOG
Оригинальное название: The Eastern Cooperative Oncology Group/World Health Organization Performance Status (ECOG/WHO PS)
Источник (официальный сайт разработчиков, публикация с валидацией): https://ecog-acrin.org/resources/ecog-performance-status
Oken MM, Creech RH, Tormey DC, Horton J, Davis TE, McFadden ET, Carbone PP: Toxicity and response criteria of the Eastern Cooperative Oncology Group. Am J Clin Oncol 1982, 5(6):649-655
Тип: шкала оценки
Назначение: описать уровень функционирования пациента с точки зрения его способности заботиться о себе, повседневной активности и физических способностях (ходьба, работа и т. д.).
Содержание:
| Балл | Описание |
|---|---|
| 0 | Пациент полностью активен, способен выполнять все, как и до заболевания (90–100 % по шкале Карновского) |
| 1 | Пациент неспособен выполнять тяжелую, но может выполнять легкую или сидячую работу (например, легкую домашнюю или канцелярскую работу, 70–80 % по шкале Карновского) |
| 2 | Пациент лечится амбулаторно, способен к самообслуживанию, но не может выполнять работу. Более 50 % времени бодрствования проводит активно – в вертикальном положении (50–60 % по шкале Карновского) |
| 3 | Пациент способен лишь к ограниченному самообслуживанию, проводит в кресле или постели более 50 % времени бодрствования (30–40 % по шкале Карновского) |
| 4 | Инвалид, совершенно не способен к самообслуживанию, прикован к креслу или постели (10–20 % по шкале Карновского) |
| 5 | Пациент мертв |
Ключ (интерпретация): приведен в самой шкале
Название на русском языке: Шкала Карновского
Оригинальное название (если есть): KARNOFSKY PERFORMANCE STATUS
Источник (официальный сайт разработчиков, публикация с валидацией): Karnofsky DA, Burchenal JH: The clinical evaluation of chemotherapeutic agents in cancer. In: Evaluation of chemotherapeutic agents. edn. Edited by MacLeod C. New York: Columbia University Press; 1949: 191-205
Тип: шкала оценки
Назначение: описать уровень функционирования пациента с точки зрения его способности заботиться о себе, повседневной активности и физических способностях (ходьба, работа и т. д.).
Содержание (шаблон):
| Шкала Карновского |
|---|
|
100— Состояние нормальное, жалоб нет
90— Способен к нормальной деятельности, незначительные симптомы или признаки заболевания
|
|
80— Нормальная активность с усилием, незначительные симптомы или признаки заболевания
70— Обслуживает себя самостоятельно, не способен к нормальной деятельности или активной работе
|
|
60— Нуждается порой в помощи, но способен сам удовлетворять большую часть своих потребностей
50— Нуждается в значительной помощи и медицинском обслуживании
|
|
40— Инвалид, нуждается в специальной помощи, в т.ч. медицинской
30— Тяжелая инвалидность, показана госпитализация, хотя смерть непосредственно не угрожает
|
|
20— Тяжелый больной. Необходимы госпитализация и активное лечение
10— Умирающий
|
| 0— Смерть |
Ключ (интерпретация): приведен в самой шкале
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.