Респираторный дистресс-синдром у новорожденных
 Версия: Клинические протоколы 2024 (Узбекистан)
Версия: Клинические протоколы 2024 (Узбекистан)
Синдром дыхательного расстройства у новорожденного (P22.0)
Неонатология, Педиатрия
Общая информация
Краткое описание
Приложение 1
к приказу № 290
от « 9» сентября 2024 года Министерства здравоохранения Республики Узбекистан
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ УЗБЕКИСТАН
ЦЕНТР РАЗВИТИЯ ПРОФЕССИОНАЛЬНОЙ КВАЛИФИКАЦИИ МЕДИЦИНСКИХ РАБОТНИКОВ
НАЦИОНАЛЬНЫЕ КЛИНИЧЕСКИЕ ПРОТОКОЛЫ ПО НОЗОЛОГИИ «РЕСПИРАТОРНЫЙ ДИСТРЕСС СИНДРОМ У НОВОРОЖДЕННЫХ»
ВВОДНАЯ ЧАСТЬ
Код по МКБ-10:
Ссылка: https://mkb-10.com/index.php?pid=15001
|
Р22.0
|
Синдром дыхательного расстройства у новорожденного
|
Дата разработки клинического протокола:
|
Дата разработки
|
01.07.2024
|
|
Планируемая дата обновления
|
проведение следующего пересмотра планируется в 2029 году, или по мере появления новых ключевых доказательств
|
Цель протокола: Целью национального клинического протокола является предоставление научно обоснованной информации с учетом современных требований доказательной медицины для создания единой комплексной и эффективной системы оказания медицинской помощи новорожденным детям с РДС. Меры по профилактике, своевременному выявлению и адекватному лечению этого заболевания позволят существенно улучшить качество медицинской помощи и уменьшить соответствующие расходы, увеличить выживаемость при минимизации таких осложнений как пневмоторакс, БЛД и другие.
Категория пациентов: недоношенные новорожденные с респираторным дистресс синдромом.
Целевая аудитория протокола: неонатологи, акушер гинекологи, педиатры, семейные врачи, студенты медицинских ВУЗов, магистры, клинические ординаторы и аспиранты. Данный протокол предназначен врачам, осуществляющим ведение, диагностику, лечение новорожденных с РДС.
ВЫВОДЫ:
1. Антенатальный уход:
-
Беременные с высоким риском преждевременных родов на сроке менее 28–30 недель должны быть переведены в перинатальные центры. (B1).
-
Пренатальная терапия ГК рекомендуется всем беременным с угрозой преждевременных родов начиная со срока, при котором плод считается жизнеспособным и до 34 недель беременности; (А1) см. протокол «Преждевременные роды».
-
Повторный курс кортикостероидной терапии может быть проведен при угрожающих преждевременных родах до 32 недель беременности, если первый курс был проведен по крайней мере 1-2 недели ранее (A2).
-
Рекомендуется назначение сульфата магния женщинам с угрожающими преждевременными родами до 32 недель. (А1).
-
Должен быть рассмотрен вариант краткосрочной токолитической терапии с целью завершения курса кортикостероидной терапии и/или обеспечения перевода женщины в перинатальный центр. (В1).
2. Стабилизация состояния недоношенных детей в родильном зале:
-
Отложите пережатие пуповины по крайней мере на 60 с, особенно у стабильных недоношенных младенцев. (А1).
-
Используйте систему с Т-образным коннектором, а не мешок и маску. (В1).
-
Стабилизируйте спонтанное дыхание недоношенных детей с помощью CPAP. (А1).
-
При апноэ начинайте масочную вентиляцию/вдувания при начальном давлении CPAP 6-8 см H2O и пиковом инспираторном давлении 20-25 см H2O. (D2).
-
Для титрования кислорода предпочтительнее использовать блендер. Использовать начальную FiO2: 0,30 для детей с ГВ менее 28 нед, 0,21-0,30 для детей с ГВ 28-31 нед, 0,21 для детей с ГВ 32 нед и старше.
-
Корректировка FiO2 в большую или меньшую сторону должна проводиться на основании данных пульсоксиметрии (B2).
-
Стремитесь к тому, чтобы SpO 2 составлял 80% или более к 5-минуте жизни. (C2).
-
Интубация должна быть выполнена только у детей, не реагирующих на вентиляцию с положительным давлением через лицевую маску или назальные канюли. (А1).
-
Подогрев и увлажнение кислородно-воздушной смеси, пластиковые пакеты /теплосберегающая упаковка, лучистые обогреватели следует использовать во время стабилизации у младенцев <32 недель беременности, чтобы снизить риск гипотермии. (А1).
3. Респираторная поддержка и сурфактант:
- По возможности используйте натуральный сурфактант, по методу LISA. (А1)
- Для более зрелых младенцев весом более 1,0 кг можно использовать сурфактант через ларингеальную маску. (B2).
- Если для стабилизации состояния недоношенного ребенка ГВ <30 нед потребовалась интубация трахеи, следует ввести сурфактант. (А2).
- Введение сурфактанта показано при прогрессировании РДС (FiO 2 > 0,3 при давлении CPAP ≥6 см H2O) или если УЗИ легких указывает на дефицит сурфактанта. (В2). Рассмотрите возможность снижения порогового значения FiO2 для очень незрелых младенцев.
- Вторая и третья дозы сурфактанта могут быть введены, если сохраняются признаки РДС. (А1).
- Как можно скорее начните CPAP или (s)NIPPV всем детям, подверженным риску РДС.(А1)
- В качестве альтернативного метода стартовой респираторной поддержки можно использовать HFNC, в случае его неэффективности обеспечить CPAP или NIPPV (В2).
- Если требуется МВ, используйте режимы, обеспечивающие защиту легких, такие как VTV или высокочастотную осцилляторную вентиляцию. (А1).
- Минимизируйте продолжительность МВ. (В2).
- При отлучении от МВ допускается наличие умеренной гиперкапнии, при pH выше 7,22. (C1).
- NO-терапия у недоношенных должна быть ограничена случаями тяжелых респираторных расстройств с документированной легочной гипертензией; терапия отменяется при отсутствии быстрого клинического эффекта (D2).
- Спонтанно дышащих новорожденных на фоне МВ следует экстубировать и перевести на CPAP, HFNC или NIPPV сразу после введения сурфактанта.
- BIPAP не дает преимуществ перед CPAP (А2). Однако, синхронизированная NIPPV, если она проводится через аппарат искусственной вентиляции легких, может снизить потребность в вентиляции или необходимости реинтубации и может снизить БЛД (A2).
- Раннее назначение кофеина применяется у детей ГВ <32 нед. для снижения риска перевода на ИВЛ (С1)
- Рассмотрите низкие дозы дексаметазона для облегчения экстубации у детей, находящихся на искусственной вентиляции легких более 1–2 недель. (А2).
- Целевое значение насыщения кислородом должно составлять от 90 до 94 %(В2) с пределами тревоги 89 % и 95 %.(Д2).
4. Поддерживающая терапия:
-
Температуру тела новорожденных рекомендуется поддерживать в пределах 36,5-37,5 °C (C1).
-
Начать парентеральное питание с рождения, начальный объем жидкости около 80 мл/кг/день, ограничить потребление натрия в течение первых нескольких дней. (C2).
-
Начать энтеральное кормление материнским молоком с первого дня, если ребенок стабилен. (В2).
-
Разумно используйте антибиотики и прекращайте прием антибиотиков как можно раньше, если исключен сепсис. (Д2)
-
Регулярно контролируйте артериальное давление, стремитесь к нормальной перфузии тканей, используйте инотропы, где это считается необходимым (рекомендуется ЭхоКГ), (С2) и поддерживайте гемоглобин на приемлемом уровне. (A2).
ОПРЕДЕЛЕНИЕ
«Респираторный дистресс-синдром» (РДС) новорожденного неинфекционное заболевание, представляющее расстройство дыхания у детей в первые дни жизни, обусловленное первичным дефицитом сурфактанта и незрелостью легких.
РДС является наиболее частой причиной возникновения дыхательной недостаточности в раннем неонатальном периоде у недоношенных новорожденных. Определена взаимосвязь между гестационным возрастом и массой тела ребенка при рождении с тяжестью течения заболевания.
РДС является наиболее частой причиной возникновения дыхательной недостаточности в раннем неонатальном периоде у недоношенных новорожденных. Определена взаимосвязь между гестационным возрастом и массой тела ребенка при рождении с тяжестью течения заболевания.
Эпидемиология
ЭПИДЕМИОЛОГИЯ
Распространенное неонатальное респираторное заболевание, наиболее часто встречающееся у недоношенных новорожденных, однако некоторые недоношенные дети также могут страдать, как правило, в возрасте от 34 до 37 недель.
В исследовании частота респираторного дистресс-синдрома составила 42% у младенцев весом 501–1500 г, 71% — у младенцев весом 501–750 г, 54% — у младенцев весом 751–1000 г, 36% — у младенцев весом 1001–1250 г и 22% — у младенцев весом 1251–1500 г среди 12 университетских больниц, участвующих в Неонатальной исследовательской сети Национального института здоровья детей и развития человека (NICHD). (5)
В исследовании частота респираторного дистресс-синдрома составила 42% у младенцев весом 501–1500 г, 71% — у младенцев весом 501–750 г, 54% — у младенцев весом 751–1000 г, 36% — у младенцев весом 1001–1250 г и 22% — у младенцев весом 1251–1500 г среди 12 университетских больниц, участвующих в Неонатальной исследовательской сети Национального института здоровья детей и развития человека (NICHD). (5)
Факторы и группы риска
ОСНОВНЫЕ ПРИЧИНЫ РАЗВИТИЯ РДС У НОВОРОЖДЕННЫХ ДЕТЕЙ:
Нарушение синтеза и экскреции сурфактанта альвеолоцитами 2-го типа, связанное с функциональной и структурной незрелостью легочной ткани; врожденный качественный дефект структуры сурфактанта.
Факторы риска.
Факторы риска.
|
Факторы повышающие риск развития РДС
|
Факторы, снижающие риск развития РДС
|
|
|
Клиническая картина
Cимптомы, течение
КЛИНИЧЕСКАЯ КАРТИНА
Неонатальный респираторный дистресс-синдром является распространенной причиной респираторного дистресса у новорожденного, проявляющегося в течение нескольких часов после рождения, чаще всего сразу после родов.
-
Тахипноэ, возникает обычно сразу после рождения или в первые часы жизни (брадипноэ, апноэ у глубоконедоношенных новорожденных);
-
Экспираторные шумы («стонущее дыхание»), обусловленные развитием компенсаторного спазма голосовой щели на выдохе;
-
Западение грудной клетки на вдохе (втягивание мечевидного отростка грудины, подложечной области, межреберий, надключичных ямок) с одновременным возникновением напряжения крыльев носа, раздувания щек (дыхание «трубача»);
-
Цианоз: центральный и/или периферический.
-
Ослабление дыхания в легких, крепитирующие хрипы при аускультации;
-
Нарастающая потребность в дополнительной оксигенации после рождения.
-
У младенца также могут развиться периферические отеки конечностей и проявиться признаки снижения диуреза.
-
При отсутствии лечения РДС симптомы постепенно ухудшаются в течение 48-72 часов, приводя к дыхательной недостаточности, и у ребенка могут развиться летаргия и апноэ.
Клиническая оценка тяжести дыхательных расстройств
Клиническая оценка тяжести дыхательных нарушений по Сильверман (Silverman) используется у недоношенных, имеет не столько с диагностической целью, сколько для оценки эффективности проводимой респираторной терапии или в качестве показания для ее начала. (См. Приложение № 1 Шкала Сильвермана).
Диагностика
ДИАГНОСТИКА
Перечень основных диагностических мероприятий
|
Обследование
|
Время проведения
|
ЦЕЛЬ
|
|
Неинвазивная пульсоксиметрия
|
Непрерывно
|
Измерение насыщения уровня гемоглобина кислородом в артериальной крови.
|
|
Общий анализ крови (Hb, Ht, лейкоциты, лейкоцитарная
формула, тромбоциты. |
6 – 12 часов жизни
|
Исключить инфекционный процесс
|
|
Сахар крови.
|
В первый час жизни, затем по показаниям.
|
Для исключения гипо- гипергликемии.
|
|
Газы крови и электролиты.
|
В течении первого часа жизни, затем по показаниям.
|
Для своевременной коррекции респираторных, метаболических и электролитных нарушений
|
|
Рентгенография органов грудной клетки
|
в первые сутки жизни показано всем новорожденным с дыхательными нарушениями.
По показаниям в любое время. Не ранее 6 часов от введения сурфактанта; контроль по показаниям |
Исключить другие причины дыхательной недостаточности, исключить синдром утечки воздуха.
|
|
Эхо КГ/УЗИ сердца.
|
по показаниям
|
исключить открытый артериальный проток, легочную гипертензию, врожденный порок сердца, сердечную недостаточность.
|
|
НСГ
|
По показаниям
|
с целью исключения внутрижелудочковых кровоизлияний, врожденных аномалии ЦНС.
|
|
бактериологическое исследование крови.
|
после рождения, до назначения антибактериальной терапии
|
С целью исключения сепсиса.
|
Перечень дополнительных диагностических мероприятий:
|
неинвазивный мониторинг газов крови (капнография, транскутаное исследование РО2 и РСО2)
|
Рекомендован непрерывный мониторинг во время проведения респираторной
поддержки |
Для своевременной коррекции респираторных нарушений.
|
|
СРБ
|
Не ранее 48 часов после рождения (см. протокол: Сепсис у новорожденных)
|
С целью исключения бактериальной инфекции, в дальнейшем при наличии показаний;
|
|
УЗИ легких
|
по показаниям
|
Оценка состояния легочной ткани, оценка потребности в сурфактантной терапии и исключит синдром утечки воздуха.
|
|
Биохимический анализ крови (электролиты, общий белок, альбумин, мочевина, креатинин, билирубин) коагулограмма.
|
по показаниям.
|
Исключение и/или коррекция метаболических нарушений, контороль функции почек и печени. оценка состояния системы гемостаза (свертывание крови), или показателей свертывания крови.
|
|
ПЦР и/или ИФА.
|
При необходимости
|
ПЦР и/или ИФА –при наличии показаний (задержка внутриутробного развития, тромбоцитопения/желтуха с первых суток жизни, наличие кальцификатов внутренних органов и/или головного мозга, вентрикуломегалия/гидроцефалия, высыпания на коже, гепатоспленомегалия), с целью исключения TORCH инфекции.
|
Ультразвук является дополнительным методом в диагностике и дифференциальной диагностике РДС. Освоение ультразвуковой диагностики и критериев классификации РДС имеет большое клиническое значение. (8).
Картина УЗИ легких. (См. приложение 2).
Рентгенограмма грудной клетки.
Рентгенологическая картина РДС зависит от тяжести заболевания – от небольшого снижения пневматизации до «белых легких». (См. приложение 3).
Рентгенологически РДС классифицируется в 4 стадии, согласно клиническому течению. (9)
I. Мелкогранулярные изменения легких (гранула = свободные от воздуха (ателектазированные) альвеолярные области.
II. Мелкогранулярные изменения легких+обогащенная аэрограмма бронхов на контурах сердца. Участки легких, стабильно остающиеся открытыми и содержащие воздух, хорошо видны на фоне не содержащей воздуха (ателектазированной) легочной ткани и не содержащего воздуха сердца.
III. Мелкогранулярные изменения легких + обогащенная аэробронхограмма на контурах сердца + нечеткое отграничение легочных полей от сердца и диафрагмы.содержание Содержание воздуха в легких, особенно в периферических областях, так сильно снижено, что стирается контраст с не содержащими воздух тканями сердца, диафрагмы и печени.
IV. «Белые легкие». Содержание воздуха в легких снижено настолько, что нет контраста с не содержащими воздух тканями сердца, диафрагмы и печени.
II. Мелкогранулярные изменения легких+обогащенная аэрограмма бронхов на контурах сердца. Участки легких, стабильно остающиеся открытыми и содержащие воздух, хорошо видны на фоне не содержащей воздуха (ателектазированной) легочной ткани и не содержащего воздуха сердца.
III. Мелкогранулярные изменения легких + обогащенная аэробронхограмма на контурах сердца + нечеткое отграничение легочных полей от сердца и диафрагмы.содержание Содержание воздуха в легких, особенно в периферических областях, так сильно снижено, что стирается контраст с не содержащими воздух тканями сердца, диафрагмы и печени.
IV. «Белые легкие». Содержание воздуха в легких снижено настолько, что нет контраста с не содержащими воздух тканями сердца, диафрагмы и печени.
Дифференциальный диагноз
ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ
|
Диагноз
|
Обоснование для дифференциальной диагностики
|
Обследования
|
Критерии исключения диагноза
|
|
Транзиторное тахипноэ новорожденных
|
Более характерно для доношенных, особенно после планового кесарево сечения. Симптомы сохраняются до 3х суток
|
Физикальные обследования, рентген.
|
В отличии от РДС при транзиторном тахипноэ на рентгеновском снимке органов грудной клетки характерно усиление бронхо-сосудистого рисунка, признаки жидкости в междолевых щелях/или плевральных синусах.
|
|
Пневмония. СГБ
|
Частота реализации пневмонии при РДС обратно пропорциональна гестационному возрасту (чем ниже ГВ, тем чаще реализуется пневмония) клинические проявления неспецифичны, могут преобладать дыхательные нарушения.
|
ОАК, С-реактивный белок; Бактериологическое исследование крови; Рентгенография органов грудной клетки;
|
Для РДС не характерны воспалительные изменения в ОАК, С-реактивный белок в пределах нормы. Характерно появление через 8-12 и 24 часа после рождения лейкоцитоза/лейкопении, нейтрофилеза/ нейтропении, повышение лейкоцитарного индекса≥0,2, и уровня Среактивного белка, обратить внимание на результаты бактериологического исследования крови. на рентгенограмме при пневмонии характерны очаговые изменения, интерстициальные или долевые инфильтраты.
|
|
Врожденная диафрагмальная грыжа.
|
Обычно диагностируется антенатально с помощью ультразвукового исследования.
|
Рентген, УЗИ лёгких
|
Признаки включают ладьевидный живот, уменьшение шумов дыхания с противоположной стороны от грыжи, смещение сердечных тонов с противоположной стороны от грыжи
|
|
Врожденная лобарная эмфизема легких.
|
Обычно диагностируется антенатально, реже в постнатальном периоде
|
Рентген, УЗИ лёгких
|
Увеличение объема и прозрачности одной из долей легких (чаще верхней доли слева), смещение органов средостения в противоположную сторону, признаки передней медиастинальной грыжи за счет перемещения перераздутой доли в сторону непораженного легкого, низкое стояние и уплощение купола диафрагмы на стороне поражения.
|
|
ВПС с цианозом.
|
Диагноз, как правило, ставится пренатально.
|
Рентген грудной клетки и ЭхоКГ.
|
Обычно сопровождается меньшей дыхательной недостаточностью, если только не присутствует стойкая легочная гипертензия. Респираторная поддержка и сурфактант не улучшают клиническое состояние ребенка. Течение не настолько тяжелое, при цианотичных ВПС цианоз рефрактерен к О2 терапии. Рентгенограмма грудной клетки характеризуется отсутствием диффузных ретикулозернистых образований, напоминающих матовое стекло, на воздушных бронхограммах/
|
Осложнения
ОСЛОЖНЕНИЯ
К острым осложнениям РДС относятся следующие (21):
- Пневмоторакс
- Инфекция
- Внутричерепное кровоизлияние и перивентрикулярная лейкомаляция
- Открытый артериальный проток (PDA) с увеличением шунтирования слева направо.
- Легочное кровотечение
- Некротический энтероколит (НЭК) и/или перфорация желудочно-кишечного тракта (ЖКТ)
К хроническим осложнениям РДС относятся следующие:
- Бронхолегочная дисплазия (БЛД)
- Ретинопатия недоношенных (РПН)
- Задержка неврологического развития является еще одним осложнением РДС, особенно у младенцев, которые долгое время находились на искусственной вентиляции легких.(22)
Лечение
СТАБИЛИЗАЦИЯ В РОДИЛЬНОМ ЗАЛЕ
Особенности оказания первичной и реанимационной помощи новорожденным из группы высокого риска по развитию РДС в родильном зале. (см. протокол реанимация и стабилизация новорожденных в родильном зале).
Профилактика гипотермии в родильном зале у недоношенных новорожденных.
- При ожидании рождения детей с ЭНМТ и ОНМТ температура в родильном зале должна составлять 28°С и более, плотно закрытые окна и двери.
- За 30 минут до предполагаемых родов включить столы с обогревом, и подготовить другие необходимые принадлежности. Основные мероприятия по обеспечению тепловой защиты проводятся в первые 30 секунд жизни в рамках начальных мероприятий первичной помощи новорожденному.
- Для контроля эффективности проводимых мероприятий и профилактики гипотермии всем недоношенным детям рекомендуется проводить непрерывный мониторинг температуры тела в родильном зале, а также фиксировать температуру тела ребенка при поступлении в блок интенсивной терапии.
- Во время стабилизации у младенцев <32 недель беременности следует использовать пластиковые пакеты или окклюзионную обертку под лучистыми обогревателями, чтобы снизить риск гипотермии и приведет к меньшему риску ВЖК. Следует также избегать гипертермии.
Техника использования пластикового пакета/пленки требует соблюдения общих принципов:
-
Используется термоустойчивый пластик пищевого класса.
-
Обсушивание кожи ребенка после рождения не проводится.
-
Туловище ребенка полностью помещается в пакет (оборачивается в пленку) сразу после рождения.
-
Поверхность головы ребенка дополнительно защищается пленкой/шапочкой.
-
Датчик пульсоксиметра присоединяется к правому запястью (предплечью) ребенка до помещения в пакет.
-
Все дальнейшие манипуляции, включая аускультацию, катетеризацию пупочных сосудов и прочее выполняются с минимальным нарушением целостности пакета/пленки.
-
Транспортировка новорожденного в ПИТ проводится в пакете/пленке.
Отсроченное пережатие пуповины
-
Если позволяет клиническое состояние, отложите пережатие пуповины минимум на 60 с (А1).
-
Рассмотрите возможность сцеживания пуповины у детей с ГВ >28 недель только в том случае, если отсроченное пережатие пуповины невозможно. (B2).
-
Примечание: Отсроченное пережатие пуповины до тех пор, пока легкие не аэрируются и не установится кровоток в левом предсердии, приводит к более плавному переходу и меньшим колебаниям артериального давления. Содействие переливанию плаценто-фетальной крови приводит к более высокому гематокриту, транзиторному повышение артериального давления с меньшей потребностью в инотропной поддержке и меньшему количеству внутрижелудочковых кровоизлияний. (10)
СТАБИЛИЗАЦИЯ ДЫХАНИЯ И МЕТОДЫ РЕСПИРАТОРНОЙ ТЕРАПИИ.
-
У спонтанно дышащих детей стабилизируйте дыхание с помощью CPAP: через маску или носовые катетеры. (A1)
-
При апноэ или брадикардии начните проводить ИВЛ. Следует использовать Т- систему, а не мешок Амбу и маску (B1).
-
Начинать следует с давления РЕЕР не менее 6 см H2Oст и PIP 20-25 см H2O (D2).
-
Аппараты BIPAP не дают преимуществ по сравнению с CPAP (A2).
-
Интубацию следует проводить только у младенцев, которые не реагируют на вентиляцию под положительным давлением через лицевую маску. (А1)
Кислород для реанимации должен контролироваться с помощью блендера, нагрев и увлажнение газов необходимы для предотвращения потери тепла.
Используйте начальное значение:
Используйте начальное значение:
-
FiO2 0,30 для детей со сроком беременности менее 28 недель,
-
0,21- 0,30 для детей со сроком беременности 28-31 неделя,
-
0,21 для детей со сроком беременности 32 недели и выше.
-
Корректировка FiO2 в большую или меньшую сторону должна проводиться на основании данных пульсоксиметрии (B2). Регистрация ЧСС и SpO2 начинается с первой минуты жизни, при этом пульсоксиметрический датчик устанавливается в области запястья или предплечья правой руки ребенка («предуктально»).
-
SpO2 80% или более (и частота сердечных сокращений >100/мин) должна быть достигнута в течение 5 минут (C2).
-
У недоношенных детей, получающих кислород, целевой уровень насыщения должен составлять от 90 до 94% (B2).
-
Пределы сигнализации должны быть установлены на 89% и 95% (D2).
-
Должны быть предусмотрены протоколы скрининга и лечения РН у недоношенных детей (А1).
Назальные канюли не показаны при лечении РДС, они полезны для доставки кислорода и при других патологиях. (11)
1.NCPAP
Обычно обеспечивается автономной системой доставки CPAP или «пузырьковыми» (BUBLE) системами NCPAP. Простота пузырьковых систем CPAP позволяет использовать их в условиях с низким доходом, при этом имеются некоторые доказательства их преимущества перед применением кислорода свободным потоком. (См. приложение 4. Алгоритм СРАР)
Общие характеристики.
-
Система, обеспечивающая CPAP, не имеет большого значения; однако в качестве интерфейса должны использоваться короткие биназальные канюли или маска, с начальным давлением около 6-8 см H2O (A2). Положительное давление в конце выдоха (ПДКВ) затем можно индивидуализировать в зависимости от клинического состояния, оксигенации и перфузии (D2).
Важно знать! Увеличение давления более 8 см вод. ст. вызывает пере растяжение лёгких и снижает сердечный венозный возврат у недоношенных детей.
-
Младенцы, получающие NCPAP, часто заглатывают воздух, что приводит к растяжению желудка и подъему диафрагмы, что требует декомпрессии с помощью желудочного зонда.
Обратите внимание! Эндотрахеальный CPAP не следует использовать, поскольку высокое сопротивление эндотрахеальной трубки усиливает ДН, особенно у недоношенных детей.
Преимущества:
- NCPAP менее инвазивен и вызывает меньшее повреждение легких.
- Системы NCPAP могут уменьшить ДН и улучшить рекрутирование легких у младенцев.
- Раннее применение NCPAP с раннем ведением сурфактанта у детей с респираторным дистресс-синдромом (РДС) может помочь предотвратить коллапс альвеол и дыхательных путей, и тем самым снизить потребность в искусственной вентиляции легких. (A1).
- NCPAP снижает частоту приступов обструктивного и смешанного апноэ у некоторых младенцев.
Показания:
-
CPAP или (s)NIPPV следует начинать с рождения у всех детей с риском развития РДС у детей с гестационным возрастом <30 недель, которым не требуется интубация для стабилизации (A1).
-
У младенецев (<32 недель) с минимальным респираторным дистресс-синдромом и потребностью (≥30%) в дополнительном кислороде (для предотвращения ателектаза).
-
Клинически значимые ретракции и/или дистресс после недавней экстубации
-
После экстубации (≤28 недель) для сохранения объема легких.
-
Во время отлучения от ИВЛ можно использовать HFNC в качестве альтернативы CPAP для некоторых детей с преимуществом меньшего травмирования носа (B2).
-
СРАР титруют, по клинической оценке ретракции и частоты дыхания, а также по наблюдению за насыщением кислородом. В этой ситуации NIPPV может быть альтернативой CPAP. Кроме того, у детей с более тяжелым РДС может быть рассмотрена (12) возможность интубации для введения сурфактанта с быстрой экстубацией с последующим СРАР (методика INSURE). Также необходимо учитывать LISA и MIST (см. Приложение 4)
Важно знать! При попытках самостоятельного вдоха у новорожденных - немедленное проведение СРАР ≥ 6,0 см вод. ст. Согласительная комиссия разрешает использование Т-систему для вентиляции младенцев с апноэ или брадикардией, в то время, как снижая риск развития бронхолегочной дисплазии в будущем, этим категориям детей рекомендуется по возможности воздерживаться от процедуры интубации в родильном зале. Исключение делается только для детей, которые не реагируют на вентиляцию легких с помощью лицевой маски или назальных канюль (А1).
Противопоказания NCPAP:
-
Прогрессирующая тяжелая дыхательная недостаточность, гиперкапния, комбинированный ацидоз, гипоксемия (рH<7,28 и PaCO2>50 мм рт.ст., FiO2>50%)
-
Новорожденные со следующей патологией: Диафрагмальная грыжа, трахеопищеводный свищ, атрезия хоан, дефект твердого и мягкого нёба, нарушение кровообращения с нарушением инотропной функции сердца, пневмоторакс.
-
Выраженное апноэ, брадикардия, нарушения кровообращения.
2. Высокопоточная назальная канюля.
HFNC позволяет доставлять расправляющее давление к дыхательным путям младенца с помощью более простого интерфейса для пациента. (13)
ВПНК (HFNC) может использоваться в качестве альтернативы CPAP для некоторых детей, с преимуществом меньшей травмы носа. Можно использовать ВПНК в качестве первой линии респираторной поддержки в центрах, способных предложить CPAP и/или NIPPV в качестве резервного варианта в случае неэффективности ВПНК. (B2).
Общие характеристики: ВПНК (HFNC) доставляют нагретый увлажненный воздух с начальной скоростью потока от 4 до 6 л/мин до максимальной 8 л/мин. Дотация кислорода должна контролироваться с помощью блендера.
Назальные канюли ВПНК (HFNC) обычно меньше по длине и диаметру, чем канюли, используемые для CPAP; не должны закрывать ноздри, занимать не более 50% внутреннего диаметра ноздрей, чтобы обеспечить достаточную утечку и защиту от высокого давления. Однако, в отличие от NCPAP, величина положительного давления, создаваемого ВПНК (HFNC), варьирует. (Приложение №5).
ВПНК (HFNC) может использоваться в качестве альтернативы CPAP для некоторых детей, с преимуществом меньшей травмы носа. Можно использовать ВПНК в качестве первой линии респираторной поддержки в центрах, способных предложить CPAP и/или NIPPV в качестве резервного варианта в случае неэффективности ВПНК. (B2).
Общие характеристики: ВПНК (HFNC) доставляют нагретый увлажненный воздух с начальной скоростью потока от 4 до 6 л/мин до максимальной 8 л/мин. Дотация кислорода должна контролироваться с помощью блендера.
Назальные канюли ВПНК (HFNC) обычно меньше по длине и диаметру, чем канюли, используемые для CPAP; не должны закрывать ноздри, занимать не более 50% внутреннего диаметра ноздрей, чтобы обеспечить достаточную утечку и защиту от высокого давления. Однако, в отличие от NCPAP, величина положительного давления, создаваемого ВПНК (HFNC), варьирует. (Приложение №5).
Преимущества
-
Механизм действия ВПНК (HFNC) подобен CPAP; с меньшей травмой носа, лучшей переносимостью и доступностью для ухода, контакта «кожа к коже» и кормления. (С1)
-
Более высокая скорость потока вымывает мертвое пространство носоглотки и замещает газ в выдохе в верхних дыхательных путях свежим газом, который насыщается кислородом, увлажняется, нагревается и обеспечивает положительное расширение дыхательных путей.
Показания:
-
Поддержка после экстубации
-
При отлучении от CPAP
-
В качестве альтернативы CPAP у стабильных недоношенных новорожденных (>32 недель)
Обратите внимание!
HFNC может использоваться в качестве альтернативы CPAP для некоторых детей на этапе отмены ИВЛ. (B2).
Противопоказания: см. Противопоказания NCPAP
Противопоказания: см. Противопоказания NCPAP
3. Неинвазивная назальная вентиляция с положительным давлением (NIPPV) предполагает инфуляцию, установленную на пиковом давлении, которая доставляется через назальные канюли или маску. Некоторые устройства пытаются синхронизировать надувание со спонтанным вдохом новорожденного. Возможность перехода на NIPPV снизит потребность в инвазивной МВ у некоторых младенцев (A1).
BIPAP не дает преимуществ перед CPAP; однако (s) NIPPV если он подается через аппарат искусственной вентиляции легких, может снизить потребность в вентиляции или реинтубации и может снизить БЛД. (A2)
Неинвазивная вентиляция с ранним введением сурфактанта по методике LISA считается оптимальным методом лечения детей с РДС (A1).
Неинвазивная вентиляция с ранним введением сурфактанта по методике LISA считается оптимальным методом лечения детей с РДС (A1).
Показания:
-
Апноэ недоношенных
-
После экстубации
-
Режим первичной вентиляции у недоношенных детей с РДС (менее 32 недель).
Рекомендуемые настройки для NIPPV:
Ч.Д. 20-30, PIP 16-25 и PEEP 6 смH2O. Настройки должны быть скорректированы в соответствии с клиническим состоянием каждого пациента и работой дыхания, до того, как они будут признаны адекватными.
Неэффективность критериев неинвазивной респираторной поддержки: (14).
Один или несколько из следующих критериев несмотря на соответствующие меры (правильное положение ребенка, очищение дыхательных путей - ноздри, глотки, адекватная терапия кофеином)
-
Тяжелое апноэ, требующее периодической вентиляции с помощью мешком и маски, или
-
Гиперкарбия, проявляющаяся в виде 2 последовательных газов крови с PaCO2>60 мм рт.ст. и PH <7,2 (с интервалом 30-60 минут), или
-
Увеличение потребности в FiO2 выше 30% для поддержания насыщения в пределах 90-95%
4. Неинвазивная высокочастотная осцилляторная вентиляция легких (nHFOV) Общие характеристики:
Применяет колебательную форму волны давления к дыхательным путям с помощью носового интерфейса.
Преимущества
Данных, сравнивающих nHFOV с другими более стандартными методами респираторной поддержки (например, nCPAP), немного, и они нуждаются в дальнейшем изучении (15).
Показания:
- Те же, что и NCPAP, NIPPV.
nHFOV является более дорогостоящим, чем другие более стандартные методы респираторной поддержки.
Противопоказания: см. противопоказания NCPAP.
nHFOV является более дорогостоящим, чем другие более стандартные методы респираторной поддержки.
Противопоказания: см. противопоказания NCPAP.
5. Двухуровневый nCPAP.
Общие характеристики:
Общие характеристики:
Двухуровневый CPAP, DuoPAP или BiPAP - вариант респираторной поддержки, промежуточный между CPAP и неинвазивной ИВЛ (NIPPV), при котором разница давления между инспираторной и экспираторной фазами незначительна, с верхним уровнем давления 9-11 см вод.ст. Обеспечивают два чередующихся уровня давления с большей продолжительностью (от 0,5 до 1,0 секунды для более высокого давления nCPAP), более низкой частотой циклов (от 10 до 30 вдохов в минуту) и более низким давлением, чем NIPPV (16)
Разница между двумя чередующимися уровнями CPAP довольно мала (<4 см H2O).
Разница между двумя чередующимися уровнями CPAP довольно мала (<4 см H2O).
Преимущества:
Данных недостаточно, чтобы определить, дает ли двухуровневый nCPAP какое-либо преимущество перед стандартным CPAP для респираторной поддержки у новорожденных. (17)
ЗАМЕСТИТЕЛЬНАЯ ТЕРАПИЯ СУРФАКТАНТОМ.
-
Если недоношенный ребенок на сроке беременности менее 30 недель нуждается в интубации для стабилизации состояния, ему следует ввести сурфактант (A2).
-
Младенцам с РДС, нуждающимся в лечении, следует вводить препарат сурфактанта животного происхождения (A1). Следует отметить, что применение LISA снижает потребность в эндотрахеальной вентиляции, развитие БЛД или летальный исход. В связи с этим у детей с самостоятельным дыханием более предпочтительным способом введения сурфактанта является методика LISA, но при условии освоения этой методики клиницистами (А1).
-
Сурфактант через ларингеальную маску может быть использован для более зрелых младенцев весом более 1,0 кг (B2).
-
Существует преимущество в выживаемости при использовании порактанта альфа в дозе 200 мг/кг по сравнению с порактантом альфа или берактантом в дозе 100 мг/кг (А1)
-
Недоношенным с РДС следует вводить сурфактант в качестве экстренной помощи на ранних стадиях заболевания. (А1). Введение сурфактанта показано при прогрессировании РДС (FiO 2 > 0,3 при давлении CPAP ≥6 см H 2 O) или если УЗИ легких (при условии хорошего владения методикой) указывает на дефицит сурфактанта. (B2).
-
Вторую, а иногда и третью дозу сурфактанта следует вводить, если имеются сохраняющиеся признаки РДС, такие как постоянная высокая потребность в кислороде, и исключены другие проблемы (A1). (Сделать рентген, УЗИ)
-
Сурфактант можно использовать при РДС, осложненным врожденной пневмонией (C1).
-
Терапия сурфактантом может улучшить оксигенацию после легочного кровоизлияния (C1).
-
Сурфактант может улучшить оксигенацию у младенцев с тяжелым синдромом аспирации мекония (B2).
СТРАТЕГИИ ИСКУССТВЕННОЙ ВЕНТИЛЯЦИИ ЛЕГКИХ.
(См.приложение 7)
Цель ИВЛ - обеспечить «приемлемые» газы крови путем вентиляции оптимальных легочных объемов (концепция открытых легких), избегая при этом перераздувания и ателектаза.
Цель ИВЛ - обеспечить «приемлемые» газы крови путем вентиляции оптимальных легочных объемов (концепция открытых легких), избегая при этом перераздувания и ателектаза.
-
ИВЛ должна применяться у детей с РДС при неэффективности методов неинвазивной респираторной поддержки (А1).
-
Режимы защиты легких, такие как VTV или высокочастотная колебательная вентиляция, должны быть первым выбором для детей с РДС, которым требуется МВ (А1).
-
Продолжительность МВ должна быть минимизирована (В2).
Показания для перевода на ИВЛ:
-
Сохранение или нарастание дыхательных нарушений с оценкой по Сильвермана 3 и более баллов на фоне проведения неинвазивной респираторной терапии
-
Повышение FiO2 >0,3 на фоне проведения неинвазивной респираторной терапии
-
Частые прерывистые апноэ без ответа на терапию метилксантином.
-
Апноэ, повторяющиеся более 4 раз в течении часа на фоне проведения неинвазивной респираторной терапии.
-
рН <7,2 на фоне проведения инвазивной респираторной терапии.
-
PaCO2 >60 мм рт.ст. на фоне проведения неинвазивной респираторной терапии.
-
шок
-
генерализованные судороги
-
легочное кровотечение
-
синдром утечки воздуха.
Общие характеристики:
- Аппарат ИВЛ должен быть с исправным датчикам потока, который позволяет измерять дыхательный объём и проводить синхронизированную вентиляцию.
- Режимы защиты легких, такие как вентиляция с целевым дыхательным объемом (VTV и высокочастотная вентиляция, являются режимами первого выбора у недоношенных с РДС, нуждающихся в ИВЛ (А1).
- VTV позволяет в режиме реального времени снижать давление по мере улучшения комплаенса легких, что приводит к уменьшению длительности ИВЛ, снижению возникновения синдрома утечек воздуха и частоты возникновения БЛД.
- Контроль дыхательного объема имеет важное значение для предотвращения развития синдромов утечки воздуха, особенно в период быстрого повышения комплаенса после введения сурфактанта.
- При наличии функции VTV: Гарантия объема должна быть начата сразу после того, как ребенок будет подключен к аппарату искусственной вентиляции легких, оснащенному системой контроля потока.
- Установите начальный дыхательный объем ~5 мл/кг с максимальным давлением на вдохе (PIP) на безопасном уровне, ~25-30 см вод.ст., коррегируйте начальный дыхательный объем в соответствии с оценкой работы дыхания и анализа газового состава крови. Необходимый дыхательный объем варьирует в пределах 5-7 мл/кг; этот диапазон имеет тенденцию к увеличению с повышением постнатального возраста.
- Режимы вентиляции, поддерживающие каждый спонтанный вдох пациента (PSV), более физиологичны в сравнении с использованием синхронизированной перемежающейся вентиляции (SIMV), если нет возможности вентиляции с гарантированным дыхательном объемом в ряде случаев безопаснее использовать SIMV, так как частота дыхания в этом режиме контролируется врачом.
- Планировать перевод ребенка на неинвазивную поддержку следует начинать сразу по стабилизации состояния, при наличии спонтанных дыхательных усилий. Значительной части новорожденных с РДС после терапии экзогенным сурфактантом достаточно очень короткого периода вентиляции.
При отлучении от ИВЛ разумно допускать умеренную степень гиперкапнии, если рН остается выше 7,22 (B2). Не допускайте pCO2 <4,7 кПа (35 мм рт. ст.) при проведении ИВЛ, чтобы уменьшить ишемию мозга (C1).
Предикторами успешной экстубации являются более высокая оценка по шкале Апгар на 5-й минуте и pH до экстубации, более низкая пиковая фракция вдыхаемого кислорода в течение первых 24 часов жизни, отсутствие потребности в дополнительной оксигенации и задержки внутриутробного развития, а также удовлетворительные показатели газового состава крови. Задержка экстубации у новорожденных не повышает шансы на дальнейший успех. Неудачная экстубация была связана со значительно более высокой вероятностью смертности и заболеваемости. (18).
Критерии экстубации: Экстубация возможна, когда МАР достигает примерно 7– 8 см водного столба при обычной вентиляции или МАР 8–9 см водного столба при HFOV и FiO2 >0,3. Экстубация пациента и перевод на неинвазивную респираторную поддержку с более высоким давлением CPAP 7-9 см вод.ст. или NIPPV повышает шансы на успех, хотя в настоящее время нет данных, подтверждающих какой-либо конкретный уровень CPAP с точки зрения влияния на долгосрочные результаты.(1)
КОФЕИН:
(20 мг/кг на нагрузку, 5-10 мг/кг на поддержание) следует использовать для облегчения отлучения от МВ (A).
Раннее назначение кофеина применяется у детей ГВ <32 нед. на неинвазивной респираторной поддержке для снижения риска перевода на ИВЛ (С1).
Терапия кофеином при стандартном режиме дозирования у новорожденных с массой тела <1251 г, отлучаемых от ИВЛ либо получающих терапию по поводу апноэ недоношенных, приводит к меньшей потребности в респираторной поддержке, меньшей частоте БЛД, а также к улучшению отдаленных неврологических исходов.
Оптимизация режима дозирования с постепенным увеличением дозировки кофеина с 5 до 8 мг/кг в сутки в течение нескольких недель после рождения рассматривается как способ эффективного поддержания фармакологического эффекта.
Раннее назначение кофеина применяется у детей ГВ <32 нед. на неинвазивной респираторной поддержке для снижения риска перевода на ИВЛ (С1).
Терапия кофеином при стандартном режиме дозирования у новорожденных с массой тела <1251 г, отлучаемых от ИВЛ либо получающих терапию по поводу апноэ недоношенных, приводит к меньшей потребности в респираторной поддержке, меньшей частоте БЛД, а также к улучшению отдаленных неврологических исходов.
Оптимизация режима дозирования с постепенным увеличением дозировки кофеина с 5 до 8 мг/кг в сутки в течение нескольких недель после рождения рассматривается как способ эффективного поддержания фармакологического эффекта.
НАЗНАЧЕНИЕ ГЛЮКОКОРТИКОИДОВ НЕДОНОШЕННЫМ ДЕТЯМ В ПЕРИОДЕ НОВОРОЖДЕННОСТИ
- Для облегчения экстубации у детей, которые остаются на МВ через 1-2 недели, следует рассмотреть возможность короткого курса дексаметазона в малых дозах (A2). Помните о повышающемся потенциальном риске долгосрочных неврологических проблем, перфорации желудочно-кишечного тракта и, особенно если их применять в течение первой недели жизни.
- Профилактическое назначение низких доз гидрокортизона от рождения также повышает шансы на выживание без БЛД и снижает потребность в лечении ОАП.
Протокол DART.
А. Критерии:
А. Критерии:
-
Вес при рождении: <1000 грамм или гестационный возраст при рождении 23-28 недель
-
Постнатальный возраст: не менее 14 дней жизни
-
При более чем 60% риске умеренной и тяжелой бронхолегочной дисплазии и смерти, с использованием калькулятора.
-
Не лечится по поводу активной инфекции или наличие признаков инфекции (нормальный общий анализ крови и/или СРБ до начала курса)
-
Отсутствие гемодинамически значимого ОАП
-
Документировать обсуждение и родительское согласие на инициацию протокола DART.
* Оценка риска БЛД: Используйте обновленный калькулятор результатов БЛД 2022 года на 14 и 28 день жизни: (20)
В. Протокол DART
Начните прием дексаметазона (энтеральным или парентеральным путем)
-
0,075 мг/кг/доза каждые 12 часов в течение трех дней (6 доз)
-
0,05 мг/кг/доза каждые 12 часов в течение трех дней (6 доз)
-
0,025 мг/кг/доза каждые 12 часов в течение двух дней (4 дозы)
-
0,025 мг/кг/доза каждые 24 часа в течение двух дней (2 приема)
-
(Всего 0,89 мг/кг за 10 дней)
С. Цели терапии:
-
Экстубация
-
Сроки экстубации: оценивать с 3-го по 7-й день после начала применения протокола DART
E. Оценка ответа на лечение:
-
Положительная реакция: возможность отменить настройки аппарата искусственной вентиляции легких (снижение FiO2 и снижение MAP), экстубировать и продолжить курс.
-
Плохой ответ или отсутствие ответа: невозможность отменить настройки аппарата искусственной вентиляции легких в течение 3 дней после начала лечения протокола DART
-
При плохом ответе или отсутствии ответа на протокол DART: отменить дексаметазон
-
Если рассматривается возможность повторного применения протокола DART, необходимо провести междисциплинарное совещание обязательным для обсуждения данного случая.
-
Повторный курс(ы) дексаметазона связан с ухудшением неврологического развития и плохим ростом и настоятельно не рекомендуются
ОБЕЗБОЛИВАНИЕ И СЕДАЦИЯ.
-
Опиоиды следует использовать выборочно, когда это показано клиническим заключением и оценкой показателей боли (D1).
-
Рутинное использование инфузий морфина или мидазолама у вентилируемых недоношенных детей не рекомендуется (A1)
-
Эндотрахеальные интубации в родильном зале часто являются экстренными и обычно не проводятся под седацией. [1]
АНТИБИОТИКИ.
-
У младенцев с РДС антибиотики следует применять разумно и прекращать прием на ранних стадиях, когда исключен сепсис (D1).
-
При назначении эмпирической АБТ предусматривается возможность отмены через 72 при отсутствии клинико-лабораторных и бактериологических данных, подтверждающих течение инфекционного процесса.
РАННЯЯ ПОДДЕРЖКА ЖИДКОСТЯМИ И ПИТАНИЕМ.
Выхаживание в инкубаторе с системой активного увлажнения позволяет снизить неощутимые потери воды более эффективно, чем выхаживание в открытой реанимационной системе.
-
Большинству детей следует начинать внутривенное введение жидкостей в объеме 70- 80 мл/кг/сутки в увлажненном инкубаторе, хотя некоторым очень незрелым детям может потребоваться больше (C2).
-
Корректировка проводится индивидуально в зависимости от баланса жидкости, изменения массы тела и уровня электролитов в сыворотке крови (D1).
-
Режим умеренного ограничения жидкости дает лучшие результаты, снижая частоту развития гемодинамически значимого ОАП, НЭК и БЛД.
-
Парентеральное питание должно быть начато с рождения. Аминокислоты 1,5-2 г/кг/сут. следует начинать с первого дня и быстро наращивать до 2,5-3,5 г/кг/сут (B). Липиды 1-2 г/кг/день следует начинать с 1-го дня и быстро наращивать до 4,0 г/кг/день по мере переносимости (C2).
-
Энтеральное питание материнским молоком должно быть начато с первого дня, если ребенок гемодинамически стабилен (B2).
-
Материнское молоко является предпочтительным вариантом для начала кормления. Для стабильных младенцев можно рано начать вводить небольшое количество (0,5-1 мл/кг/ч) грудного молока для начала энтерального питания.
УПРАВЛЕНИЕ АРТЕРИАЛЬНЫМ ДАВЛЕНИЕМ И ПЕРФУЗИЕЙ.
(СМ. ПРОТОКОЛ «ШОК У НОВОРОЖДЕННЫХ»).
ПОДДЕРЖАНИЕ ЦЕЛЕВОГО УРОВНЯ ГЕМОГЛОБИНА У НОВОРОЖДЕННЫХ С РДС ЯВЛЯЕТСЯ ВАЖНЫМ КОМПОНЕНТОМ ТЕРАПИИ.
Пороговые значения Hb для трансфузии эритроцитов могут быть установлены как:
-
12 г/дл (120 г/л; Ht <36%) для детей с тяжелыми кардиореспираторными нарушениями,
-
11 г/дл (110 г/л; Ht <30%) - для кислородозависимых пациентов и
-
7 г/дл (70 г/л; Ht <25%) - для пациентов старше 2 нед жизни, клиническое состояние которых стабильно (А2).
ГЕМОДИНАМИЧЕСКИ ЗНАЧИМЫЙ ФУНКЦИОНИРУЮЩИЙ АРТЕРИАЛЬНЫЙ ПРОТОК
(ГЗФАП) вызывает интерстициальный отек легких и снижение системного кровотока по мере уменьшения легочного сосудистого сопротивления после рождения. Функционирование гемодинамически значимого артериального протока связано с повышенным риском смерти, БЛД, ВЖК и НЭК.
-
Если принято решение о фармакологическом закрытии гемодинамически значимого ОАП, можно использовать индометацин, ибупрофен или парацетамол с одинаковой эффективностью (A2).
-
Парацетамол предпочтительнее при наличии тромбоцитопении или опасений по поводу функции почек (B2).
-
Ибупрофен и особенно индометацин повышают риск перфорации кишечника и желудочно-кишечного кровотечения, а также увеличивают вероятность развития острого повреждения почек. (1)
-
Рутинное закрытие ОАП у недоношенных не считается оптимальной тактикой
КОНТРОЛЬ ТЕМПЕРАТУРЫ ТЕЛА.
-
Поддержание нормальной температуры тела является важным показателем качества, поскольку гипотермия при поступлении связана с худшими исходами.
-
После поступления младенцев следует содержать в инкубаторах с сервоприводом, первоначально с относительно высокой влажностью, которую можно снизить по мере улучшения целостности кожи.
-
Периодический уход «кожа к коже» также является эффективным средством поддержания температуры, и его следует поощрять, поскольку они максимизируют связь и улучшают темпы роста и грудного вскармливания детей с ОНМТ.
МОНИТОРИНГ И ПОДДЕРЖИВАЮЩИЙ УХОД
Мониторинг витальных функций - важный элемент обеспечения качества помощи новорожденным с РДС.
-
Непрерывная пульсоксиметрия.
-
Важным условием оказания медицинской помощи новорожденным является наличие в постоянном доступе портативного ультразвукового аппарата.
-
Круглосуточный доступ к рентгенографическим методам диагностики, которые необходимы для подтверждения диагноза РДС и контроля правильного положения ЭТТ и сосудистых катетеров.
-
При возможности - ЭКГ
-
При возможности - определение etCO2 методом капнографии (для верификации корректного положения ЭТТ).
-
При возможности - для контроля кислотно-основного состояния (КОС) и газового состава крови "золотым стандартом" является артериальная кровь; при необходимости частых заборов устанавливают умбиликальный или периферический артериальный катетер.
РЕСУРСЫ, НЕОБХОДИМЫЕ ДЛЯ РЕАЛИЗАЦИИ ПРОТОКОЛА
|
Ресурсы
|
Функции/Важность
|
Примечание
|
|
Человеческие ресурсы
|
||
|
Неонатолог родильного отделения, отделения реанимации и интенсивной терапии новорожденных, отделения патологии новорожденных
|
Клиническая оценка состояния пациента
Выбор необходимых диагностических методов и лабораторных тестов Подтверждение диагноза Выбор профилактических мер Решение о лечении, согласно национальному протоколу Вызов специалистов для проведения консультаций Постоянное наблюдение. Консультирование родителей по вопросам профилактики, выбранной тактики лечения и состояния ребенка. Постоянное повышение своей профессиональной квалификации, в порядке, установленным законодательством. |
Обязательно
|
|
Медсестра
|
Уход за ребенком.
Оценка профиля риска. Немедикаментозное лечение факторов риска. Тщательный мониторинг клинического состояния ребенка и основных витальных показателей. Выполнение назначенных процедур, медикаментов, диагностических мероприятий. Своевременное информирование врача об изменении жизненно важных параметров. Стратегия по профилактике внутрибольничных инфекций. Постоянное повышение своей профессиональной квалификации, в порядке, установленным законодательством. |
Обязательно
|
|
Рентгенолог
|
Проведение рентгенологического обследования 24/7
|
Обязательно
|
|
Администратор
|
Содействие в реализации национального протокола.
Надзор за выполнением. Аудит. Помощь в оснащении материально- технической базы. |
Обязательно
|
| Лабораторные тесты | ||
|
Рекомендуется рутинный динамический мониторинг. Полезен для оценки изменений заболевания
|
Настоятельно рекомендуется (доказательства уровня С)
|
|
При парентеральном питании
|
Обязательно
|
|
До начала антибактериальной терапии
|
Обязательно
|
|
При наличии соответствующих нарушений
|
Обязательно
|
|
Диагностическое оборудование
|
||
|
Пульсоксиметрия
|
Непрерывный мониторинг сатурации
|
Настоятельно рекомендуется (доказательства уровня В)
|
|
Капнография - используется для верификации корректного положения ЭТТ.
Для своевременной коррекции респираторных нарушений. |
Настоятельно рекомендуется
|
|
Рентгенография грудной и брюшной полости
|
Оценка риска.
Подтверждение подозреваемого диагноза Принятие решения. Отслеживание прогрессирования заболевания. |
Настоятельно рекомендуется (доказательства уровня С)
|
|
Ультразвуковое исследование
(УЗИ внутренних органов, НСГ) |
Оценить потребность сурфактантной терапии и исключить синдром утечки воздуха, а также для диагностики патологии головного мозга
|
Настоятельно рекомендуется (доказательства уровня В)
|
|
Материалы для обучения пациентов
|
Информирование родителей/опекунов пациента
|
Желательно
|
Прогноз
ПРОГНОЗ (21).
Повышенная выживаемость в развитых странах резко отличается от выживаемости младенцев, в странах с низким уровнем дохода, где смертность недоношенных детей с РДС значительно выше, иногда приближается к 100%.
При адекватной вентиляционной поддержке в конечном итоге начинается выработка сурфактанта, а после начала выработки сурфактанта вместе с установлением диуреза РДС улучшается в течение 4 или 5 дней. Неонатальный респираторный дистресс- синдром является одной из основных причин преждевременной смерти, однако у значительной части выживших может развиться бронхолегочная дисплазия и возникнуть хронические легочные заболевания. Также важную роль в определении прогноза играет гестационный возраст, при котором у поздних недоношенных детей прогноз обычно лучше, чем у ранних недоношенных.
При адекватной вентиляционной поддержке в конечном итоге начинается выработка сурфактанта, а после начала выработки сурфактанта вместе с установлением диуреза РДС улучшается в течение 4 или 5 дней. Неонатальный респираторный дистресс- синдром является одной из основных причин преждевременной смерти, однако у значительной части выживших может развиться бронхолегочная дисплазия и возникнуть хронические легочные заболевания. Также важную роль в определении прогноза играет гестационный возраст, при котором у поздних недоношенных детей прогноз обычно лучше, чем у ранних недоношенных.
Профилактика
АНТЕНАТАЛЬНАЯ ПРОФИЛАКТИКА
- Матерей с высоким риском преждевременных родов на сроке беременности <28-30 недель следует переводить в перинатальные центры, имеющие опыт ведения РДС (B1).
- У женщин с одноплодной беременностью и короткой шейкой матки в середине беременности или предыдущими преждевременными родами следует использовать вагинальную терапию прогестероном для увеличения гестационного возраста при родах и снижения перинатальной смертности и заболеваемости (A1).
- У женщин с симптомами преждевременных родов следует рассмотреть возможность определения длины шейки матки и точного измерения биомаркеров, чтобы предотвратить ненужное применение токолитических препаратов и/или дородовых стероидов (B2).
- Клиницисты должны предложить один курс пренатальных кортикостероидов всем женщинам с высоким риском преждевременных родов, начиная с момента, когда беременность считается потенциально жизнеспособной с 24 полных недель и до 34 полных недель гестации, в идеале не позднее чем за 24 часа до родов (A1). Антенатальные кортикостероиды как показывает практика, повышает выживаемость, снижает риск РДС, НЭК и ВЖК. (7).
- При угрожающих преждевременных родах до 32 недель беременности можно провести один повторный курс стероидов, если первый курс был проведен не менее чем за 1-2 недели до этого (A2).
- Женщинам с угрозой родов до 32 недель беременности следует назначать MgSO4 (A1).
- Клиницистам следует рассмотреть возможность краткосрочного применения токолитических препаратов при очень недоношенной беременности для завершения курса пренатальных кортикостероидов и/или внутриутробного перевода в перинатальный центр (B1).
Информация
Источники и литература
-
Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2024
- Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2024 - 1. Sweet D.G., Carnielli V.P., Greisen G., Hallman M., Klebermass-Schrehof K., et al. European Consensus guidelines on the management of respiratory distress syndrome: 2022 update. 2. Lees MH, Цианоз новорожденного. Распознавание и клиническая оценка, J Pediatr. 1970;77(3):484. 3. Грант Дж. Б., Зальцман А. Р. Дыхательные функции легких. В: Учебник легочных заболеваний, 5-е изд., Баум Г.Л., Волински Э. (ред.), Литтл, Браун, Бостон, 1994. 4. МКБ 10 - Дыхательное расстройство у новорожденного [дистресс] (P22) (mkb10.com) 5. Smith PB, Ambalavanan N, Li L, Cotten CM, Laughon M, Walsh MC, Das A, Bell EF, Carlo WA, Stoll BJ, Shankaran S, Laptook AR, Higgins RD, Goldberg RN., Подкомитет по общей базе данных. Национальный институт детского здоровья, сеть исследований неонатологии и развития человека имени Юнис Кеннеди Шрайвер. Подход к младенцам, рожденным на 22–24 неделе беременности: связь с результатами более зрелых младенцев. Педиатрия. 2012 июнь; 129 (6):e1508-16 6. Child and Adolescent Health Service. Neonatology. GUIDELINE. Respiratory Distress Syndrome (RDS). Scope (Staff): Nursing and Medical Staff. 7. Roberts D, Brown J, Medley N, Dalziel SR.Antenatal corticosteroids for accelerating fetal lung maturation for women at risk of pretermbirth. Cochrane Database Syst Rev. 2017Mar 21; 3(3): CD004454. 8. Ultrasound diagnosis and grading criteria of neonatal respiratory distress syndrome.Jing Liu. Article: 2206943 | Received 26 May 2022, Accepted 20 Apr 2023, Published online: 04 May 2023 9. Roland R. Wauer. Surfactant in der Neonatologie.Prävention und Therapie des neonatalen Atemnotsyndroms mit Surfactant. 2011 .P. 15 10. Neonatal Clinical Practice Guidelines 2018-2021 by Elsie Constanza, M.D., Paediatrician & Neonatologist First Edition. 11. Можган Сабз , Скотт Тавернини , Кинешта Пиллэй , Коул Кристиансон , Коул Кристиансон , Изменчивость низкопоточной доставки кислорода с помощью назальной канюли, оцененная в репликах дыхательных путей новорожденных и младенцев , Исследования органов дыхания том 23, номер статьи: 333 (2022) 12. Ng EH, Shah V Руководство по заместительной терапии сурфактантом у новорожденных. Педиатр Здоровье ребенка. 2021;26(1):35. Epub 2021 1 февраля. 13. Чарльз С. Рёр , Брэдли А Йодер , , Питер Дж. Дэвис , Кевин Айвз. Доказательная поддержка и рекомендации по использованию назальных канюль с подогревом, увлажнением и высоким потоком в неонатологии: Oxford Nasal High-Flow Therapy Meeting, 2015, PMID : 27837753 14. Детская больница Джона Хопкинса. Рекомендации по неинвазивной первичной респираторной поддержке пациентов с респираторным дистресс-синдромом (РДС) по клиническому пути 15. Zhu XW, Zhao JN, Tang SF, Yan J, Shi Y Неинвазивная высокочастотная осцилляторная вентиляция в сравнении с назальным постоянным положительным давлением в дыхательных путях у недоношенных детей с респираторным дистресссиндромом средней и тяжелой степени: предварительный отчет. Педиатр Пульмонол. 2017;52(8):1038. Epub 2017 3 июля. 16. Каммингс Дж. Дж., Полин Р. А., Комитет по плодам и новорожденным, Американская академия педиатрии. Неинвазивная респираторная поддержка. Педиатрия. 2016;137(1) 17. О'Брайен К., Кэмпбелл С., Браун Л., Венгер Л., Шах В. Двухфазное непрерывное положительное давление в дыхательных путях через нос для младенцев (BP-NCPAP) в сравнении с потоком для младенцев NCPAP для облегчения экстубации у младенцев весом ≤1250 граммов: рандомизированное контролируемое исследование. БМС Педиатр. 2012;12:43. Epub 2012 4 апр 18. Chawla S, Natarajan G, Shankaran S, Carper B, Brion LP, Keszler M, et al. Markers of successful extubation in extremely preterm infants, and morbidity after failed extubation. J Pediatr. 2017 Oct; 189: 113–9. e2. 19. Doyle L.W., Davis P.G., Morley C.J., McPhee A., Carlin J.B.; DART Study Investigators. Low-dose dexamethasone facilitates extubation among chronically ventilatordependent infants: a multicenter, international, randomized, controlled trial. Pediatrics. 2006; 117 (1): 75-83. DOI: https://doi.org/10.1542/peds.2004-284314 20. https://neonatal.rti.org/index.cfm?fuseaction=BPD_Calculator2.start 21. Neonatal Respiratory Distress Syndrome. Sudeep Yadav; Brian Lee; Ranjith Kamity. Author Information and Affiliations. Last Update: July 25, 2023. 22. Sun H, Zhou Y, Xiong H, Kang W, Xu B, Liu D, Zhang X, Li H, Zhou C, Zhang Y, Zhou M, Meng Q. Прогноз для недоношенных детей с тяжелым респираторным дистресс-синдромом, получающих искусственную вентиляцию легких. 2015 апрель; 193 (2):249-54. PubMed
Информация
Состав рабочей группы по разработке клинического протокола:
|
1.
|
Насирова У.Ф.
|
Главный неонатолог МЗ РУз, заместитель директора по научной работе и инновации ЦРПКМР, д.м.н.
|
|
2.
|
Ахмедова Д.И.
|
Главный педиатр МЗ РУз, заведующая кафедрой Гос.Педиатрии №2 и народной медицины ТашПМИ, д.м.н., профессор
|
|
3.
|
Салихова К.Ш.
|
РСНПМЦ педиатрии, заместитель директора по научной работе, д.м.н.
|
|
4.
|
Касымова Н.А.
|
Заместитель директора РПЦ, к.м.н.
|
|
5.
|
Шамансуров Ш.Ш.
|
Главный детский невролог МЗ РУз, заведующий кафедрой детской неврологии ЦРПКМР, д.м.н., профессор
|
|
6.
|
Алимов А.В.
|
Профессор, д.м.н., Кафедра Неонатологии ЦРПКМР
|
|
7.
|
Усманова М.Ш.
|
Главный неонатолог г. Ташкента, РСНПМЦЗМиР филиаль города Ташкента
|
Список авторов и соавторов:
|
1.
|
Разикова М.З.
|
Ассистент кафедры Неонатологии ЦРПКМР
|
|
2.
|
Шамсиев Ф.М.
|
Профессор, главный детский пульмонолог Министерства здравоохранения Республики Узбекистан, РСНПМЦП
|
|
3.
|
Батманов А.Л.
|
Ассистент кафедры Неонатологии ЦРПКМР
|
|
4.
|
Саидумарова Д.С.
|
Ассистент кафедры Неонатологии ЦРПКМР
|
|
5.
|
Латипова Г.Г.
|
к.м.н., ассистент кафедры Неонатологии ЦРПКМР
|
|
6.
|
Султанова З.А.
|
К.м.н., РПЦ ОВНН
|
|
7.
|
Ходжамова Н.К.
|
Доцент кафедры Неонатология ТашПМИ
|
|
8.
|
Касимова У.Ш.
|
Зам.директора РСНПМЦЗМиР Ферганского филиала
|
|
9.
|
Исраилова Н.М.
|
Неонатолог клиники ТМА
|
|
10.
|
Усмонов С.К.
|
акушер-гинеколог
|
Рецензенты:
|
1.
|
Хатуна Ломаури
|
Доктор медицинских наук, Профессор, Заведующая Кафедрой Неонатологии Тбилисского Государственного Медицинского Университета, эксперт ВОЗ
|
|
2.
|
Татьяна Караус
|
Эксперт ВОЗ, к.м.н., Институт матери и ребенка Республики Молдова
|
|
3
|
Рахманкулова З.Ж.
|
Д.м.н., Профессор кафедры Неонатологии, ТашПМИ
|
Протокол был подготовлен в рамках проекта «ISHONCH. Uzbekistan Vision 2030», при финансовой поддержке ВОЗ и ЮНИСЕФ совместно с Министерством Здравоохранения Республики Узбекистан.
Мнения, выраженные в протоколе, принадлежат авторам и свободны от какого-либо влияния.
Методология разработки протокола:
Источники рекомендаций были дополнены текущими исследованиями доказательной медицины. Проведен поиск в различных медицинских базах данных, таких как: PubMed, Cochrane Library, UpTodate.
Национальный клинический протокол разработан на основе следующих документов:
Протокол разработан на основании клинического руководства «European Consensus Guidelines on the management of respiratory distress syndrome – 2022 update» (1), которое основывается на принципах доказательной медицины с учетом современных международных рекомендаций.
Список сокращений.
|
BiPAP (Bilevel positive airway pressure) -
|
двухуровневое положительное давление в дыхательных путях
|
|
СРАР (Continuous positive airway pressure) -
|
постоянное положительное давление в дыхательных путях
|
|
EtCO2 (End-tidal CO2) -
|
концентрация углекислого газа в конце выдоха
|
|
FiO2 (Fraction of inspired oxygen) -
|
фракция вдыхаемого кислорода
|
|
HFNC (High-flow nasal cannula) -
|
высокопоточные назальные канюли
|
|
Ht (Hematocrit) -
|
Гематокрит
|
|
IN-SUR-E (INtubation-SURfactant- Extubation) -
|
"интубация - введение сурфактанта - экстубация"
|
|
LISA (Less-invasive surfactant administration)
|
менее инвазивное введение сурфактанта
|
|
MAP (Mean airway pressure) -
|
среднее давление в дыхательных путях
|
|
MIST (Minimally invasive surfactant therapy)
|
минимально инвазивное введение сурфактанта
|
|
nHFOV (Nasal high-frequency oscillatory ventilation)
|
назальная высокочастотная вентиляция легких
|
|
NIPPV (Nasal intermittent positive pressure ventilation)
|
назальная перемежающаяся вентиляция с положительным давлением
|
|
NO (Nitric oxide) -
|
оксид азота
|
|
pСО2 -
|
парциальное давление углекислого газа
|
|
PEEP (Positive end-expiratory pressure) -
|
положительное давление в конце выдоха
|
|
PIP (Peak inspiratory pressure) -
|
пиковое инспираторное давление
|
|
PS (Pressure support) -
|
поддержка давлением
|
|
SIMV (Synchronized intermittent mandatory ventilation) -
|
синхронизированная перемежающаяся вентиляция
|
|
SpO2 (Peripheral saturation O2) -
|
уровень насыщения гемоглобина крови кислородом
|
|
VTV (Volume targeted ventilation) -
|
вентиляция с целевым дыхательным объемом
|
|
АБТ -
|
антибактериальная терапия
|
|
БЛД -
|
бронхолегочная дисплазия
|
|
ВЖК -
|
внутрижелудочковое кровоизлияние
|
|
ВЧО ИВЛ -
|
высокочастотная осцилляторная искусственная вентиляция легких
|
|
ГВ -
|
гестационный возраст
|
|
ГЗФАП -
|
гемодинамически значимый функционирующий артериальный проток
|
|
ДО
|
дыхательный объем
|
|
ИВЛ -
|
искусственная вентиляция легких
|
|
КОС
|
кислотно-основное состояние
|
|
НИВЛ
|
неинвазивная искусственная вентиляция легких
|
|
НЭК
|
некротизирующий энтероколит
|
|
ОАП
|
открытый артериальный проток
|
|
ОРИТН
|
отделение реанимации и интенсивной терапии новорожденных
|
|
РДС
|
респираторный дистресс-синдром
|
|
УЗИ
|
ультразвуковое исследование
|
|
ЧСС
|
частота сердечных сокращений
|
|
ЭКГ
|
Электрокардиография
|
|
ЭТТ
|
эндотрахеальная трубка
|
|
ПЦР
|
полимеразная цепная реакция.
|
|
МВ
|
механическая вентиляция
|
ШКАЛА ОЦЕНКИ КЛАССОВ УРОВНЯ УБЕДИТЕЛЬНОСТИ РЕКОМЕНДАЦИЙ (УУР) И УРОВНЕЙ ДОСТОВЕРНОСТИ ДОКАЗАТЕЛЬСТВ (УДД)
|
УДД
|
Критерии определения УУР
|
Итоговый УУР
|
|
Наиболее достоверные доказательства: систематические обзоры исследований с контролем референсным методом |
Одновременное выполнение двух условий:
1. Все исследования имеют высокое или удовлетворительное методологическое качество 2. Выводы исследований по интересующим исходам являются согласованными |
А |
|
Выполнение хотя бы одного из условий:
1. Не все исследования имеют высокое или удовлетворительное методологическое качество 2. Выводы исследований по интересующим исходам не являются согласованными |
В |
|
|
Выполнение хотя бы одного из условий:
1. Все исследования имеют низкое методологическое качество 2. Выводы исследований по интересующим исходам не являются согласованными |
С |
|
|
Отдельные исследования с контролем референсным методом |
Одновременное выполнение двух условий:
1. Все исследования имеют высокое или удовлетворительное методологическое качество 2. Выводы исследований по интересующим исходам являются согласованными |
А |
|
Выполнение хотя бы одного из условий:
1. Не все исследования имеют высокое или удовлетворительное методологическое качество 2. Выводы исследований по интересующим исходам не являются согласованными |
В |
|
|
Выполнение хотя бы одного из условий:
1. Все исследования имеют низкое методологическое качество 2. Выводы исследований по интересующим исходам не являются согласованными |
С |
|
|
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода
|
Выполнение хотя бы одного из условий:
1. Не все исследования имеют высокое или удовлетворительное методологическое качество 2. Выводы исследований по интересующим исходам не являются согласованными |
В |
|
Выполнение хотя бы одного из условий:
1. Все исследования имеют низкое методологическое качество 2. Выводы исследований по интересующим исходам не являются согласованными |
С |
ОСНОВНЫЕ ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ:
Газы крови: Контроль вентиляции (CO2), оксигенации (O2) и изменения кислотно- щелочного состояния наиболее точно определяются при исследовании газов артериальной крови.
Гипоксемия – снижение парциального напряжения кислорода в крови ниже 50 мм. рт.ст. (PaO2 <50 мм рт. ст.) Снижение PaO 2 вызывает тяжелые изменения обмена веществ, снижение легочного кровотока, поражение головного мозга и другие серьезные поражения.
Гипероксия - повышение парциального напряжения кислорода в крови выше 70 мм рт.ст. (PaO2> 70 мм рт.ст.). Повышение PaO2 более 120 мм рт.ст. вызывает ретролентальную фиброплазию и увеличивает риск развития бронхолегочной дисплазии. Нормальное значение РаО2 при дыхании атмосферным воздухом составляет 50 - 70 мм рт.ст.
Гиперкапния — повышение парциального напряжения углекислого газа в крови РаСО2 >50 мм рт.
Гипокапния – снижение парциального напряжения углекислого газа в крови РаСО2 < 30 мм рт.ст.
Гипоксия - снижение парциального напряжения кислорода в тканях, РН <7,28, РаСО2 > 50 мм рт.ст., FiO2 > 50%.
Постоянное положительное давление в дыхательных путях (CPAP) - означает обеспечение положительного давления в конце выдоха (PEEP) к носовым и/или ротовым отверстиям через интерфейс. Давление может создаваться вентилятором, гидрораспределителем или под гидрозатвором (пузырьковая система).
Назальная прерывистая вентиляция с положительным давлением (NIPPV) относится к обеспечению комбинации применения CPAP с периодическим повышением давления, применяемым через нос, без эндотрахеальной трубки. Он приводится в действие вентилятором и может быть синхронизирован или не синхронизирован.
Двухуровневый CPAP часто включается в состав NIPPV. Этот режим также сочетает CPAP с периодическим повышением давления через носовой интерфейс, но описывает чередование высоких и низких уровней CPAP. На обоих уровнях младенец дышит самостоятельно. Двухуровневый CPAP также называют назальным BiPAP и двухфазным назальным CPAP.
Назальная канюля с высоким потоком с подогревом (HHFNC) относится к обеспечению смеси кислорода и воздуха с помощью генератора потока, активного увлажнителя с подогревом, одинарного нагревательного контура и носовой канюли для ноздрей.
Короткие биназальные канюли представляют собой герметизирующие носовые интерфейсы, используемые для доставки CPAP или NIPPV.
Назальные маски представляют собой герметизирующие носовые интерфейсы, используемые для доставки CPAP или NIPPV.
Гипоксемия – снижение парциального напряжения кислорода в крови ниже 50 мм. рт.ст. (PaO2 <50 мм рт. ст.) Снижение PaO 2 вызывает тяжелые изменения обмена веществ, снижение легочного кровотока, поражение головного мозга и другие серьезные поражения.
Гипероксия - повышение парциального напряжения кислорода в крови выше 70 мм рт.ст. (PaO2> 70 мм рт.ст.). Повышение PaO2 более 120 мм рт.ст. вызывает ретролентальную фиброплазию и увеличивает риск развития бронхолегочной дисплазии. Нормальное значение РаО2 при дыхании атмосферным воздухом составляет 50 - 70 мм рт.ст.
Гиперкапния — повышение парциального напряжения углекислого газа в крови РаСО2 >50 мм рт.
Гипокапния – снижение парциального напряжения углекислого газа в крови РаСО2 < 30 мм рт.ст.
Гипоксия - снижение парциального напряжения кислорода в тканях, РН <7,28, РаСО2 > 50 мм рт.ст., FiO2 > 50%.
Постоянное положительное давление в дыхательных путях (CPAP) - означает обеспечение положительного давления в конце выдоха (PEEP) к носовым и/или ротовым отверстиям через интерфейс. Давление может создаваться вентилятором, гидрораспределителем или под гидрозатвором (пузырьковая система).
Назальная прерывистая вентиляция с положительным давлением (NIPPV) относится к обеспечению комбинации применения CPAP с периодическим повышением давления, применяемым через нос, без эндотрахеальной трубки. Он приводится в действие вентилятором и может быть синхронизирован или не синхронизирован.
Двухуровневый CPAP часто включается в состав NIPPV. Этот режим также сочетает CPAP с периодическим повышением давления через носовой интерфейс, но описывает чередование высоких и низких уровней CPAP. На обоих уровнях младенец дышит самостоятельно. Двухуровневый CPAP также называют назальным BiPAP и двухфазным назальным CPAP.
Назальная канюля с высоким потоком с подогревом (HHFNC) относится к обеспечению смеси кислорода и воздуха с помощью генератора потока, активного увлажнителя с подогревом, одинарного нагревательного контура и носовой канюли для ноздрей.
Короткие биназальные канюли представляют собой герметизирующие носовые интерфейсы, используемые для доставки CPAP или NIPPV.
Назальные маски представляют собой герметизирующие носовые интерфейсы, используемые для доставки CPAP или NIPPV.
Носовые канюли представляют собой длинные негерметизирующиеся интерфейсы, используемые для доставки HHFNC, CPAP или NIPPV (канюля® Рама, Fisher Paykel®)
Ацидемия – рН артериальной крови ниже нормального диапазона (менее 7,35).
Алкалиемия – рН артериальной крови выше нормального диапазона (более 7,45). Ацидоз – процесс, при котором рН внеклеточной жидкости снижается (увеличивается концентрация ионов водорода). Это может быть вызвано падением концентрации бикарбоната в сыворотке (HCO3) и/или повышением PCO2.
Алкалоз – процесс, который имеет тенденцию повышать pH внеклеточной жидкости (снижается концентрация ионов водорода). Это может быть вызвано повышением концентрации HCO3 в сыворотке крови и/или снижением PCO2.
Метаболический ацидоз – расстройство, при котором снижается концентрация HCO3 в сыворотке и pH крови.
Метаболический алкалоз — расстройство, при котором повышается концентрация HCO3 и pH.
Респираторный ацидоз — расстройство, при котором повышается артериальное РСО2 и снижается рН.
Респираторный алкалоз — расстройство, при котором снижается артериальное РСО2 и повышается рН.
Пульсоксиметрия SpO 2 - оптический метод определения процентного насыщения гемоглобина кислородом (SpO2). Толщина и цвет кожи не влияют на результаты измерения. Пульсоксиметры не требуют предварительной калибровки, работают стабильно, а погрешность измерений обычно не превышает 2-3%. Задержка реакции пульсоксиметра может варьироваться от 2-3 секунд до 1,5 минут в зависимости от скорости кровотока и времени обновления данных на экране дисплея.
Неинвазивный мониторинг углекислого газа – устройства для чрескожного мониторинга углекислого газа постоянно контролируют CO2 и могут отображать динамические изменения уровня pCO 2 в режиме реального времени.
Тахипноэ: учащенное дыхание из-за недостаточной оксигенации или вентиляции. Частота дыхания более> 60 вдохов/мин
Апноэ: задержка дыхания на 20 секунд и более при нормальной частоте сердечных сокращений или на 10 секунд при наличии брадикардии (частота сердечных сокращений менее 100 в минуту)
Цианоз – синеватое окрашивание тканей, возникающее, когда абсолютный уровень деоксигенированного гемоглобина в капиллярном русле превышает 3 г/дл. (2)
Центральный цианоз. Центральный цианоз проявляется, когда системная артериальная концентрация деоксигенированного гемоглобина (Hb) в крови превышает 5 г/дл (3,1 ммоль/л) (насыщение кислородом ≤85%)(3). Следует отметить, что у пациентов с тяжелой анемией (например, уровень гемоглобина <5 г/дл [3,1 ммоль/л]) цианоз может быть не сразу обнаружен.
Периферический цианоз. Пациенты с периферическим цианозом имеют нормальное системное артериальное насыщение кислородом. Однако повышенная экстракция кислорода приводит к широкой системной артериовенозной разнице по кислороду и увеличению деоксигенированной крови на венозной стороне капиллярного русла.
Ацидемия – рН артериальной крови ниже нормального диапазона (менее 7,35).
Алкалиемия – рН артериальной крови выше нормального диапазона (более 7,45). Ацидоз – процесс, при котором рН внеклеточной жидкости снижается (увеличивается концентрация ионов водорода). Это может быть вызвано падением концентрации бикарбоната в сыворотке (HCO3) и/или повышением PCO2.
Алкалоз – процесс, который имеет тенденцию повышать pH внеклеточной жидкости (снижается концентрация ионов водорода). Это может быть вызвано повышением концентрации HCO3 в сыворотке крови и/или снижением PCO2.
Метаболический ацидоз – расстройство, при котором снижается концентрация HCO3 в сыворотке и pH крови.
Метаболический алкалоз — расстройство, при котором повышается концентрация HCO3 и pH.
Респираторный ацидоз — расстройство, при котором повышается артериальное РСО2 и снижается рН.
Респираторный алкалоз — расстройство, при котором снижается артериальное РСО2 и повышается рН.
Пульсоксиметрия SpO 2 - оптический метод определения процентного насыщения гемоглобина кислородом (SpO2). Толщина и цвет кожи не влияют на результаты измерения. Пульсоксиметры не требуют предварительной калибровки, работают стабильно, а погрешность измерений обычно не превышает 2-3%. Задержка реакции пульсоксиметра может варьироваться от 2-3 секунд до 1,5 минут в зависимости от скорости кровотока и времени обновления данных на экране дисплея.
Неинвазивный мониторинг углекислого газа – устройства для чрескожного мониторинга углекислого газа постоянно контролируют CO2 и могут отображать динамические изменения уровня pCO 2 в режиме реального времени.
Тахипноэ: учащенное дыхание из-за недостаточной оксигенации или вентиляции. Частота дыхания более> 60 вдохов/мин
Апноэ: задержка дыхания на 20 секунд и более при нормальной частоте сердечных сокращений или на 10 секунд при наличии брадикардии (частота сердечных сокращений менее 100 в минуту)
Цианоз – синеватое окрашивание тканей, возникающее, когда абсолютный уровень деоксигенированного гемоглобина в капиллярном русле превышает 3 г/дл. (2)
Центральный цианоз. Центральный цианоз проявляется, когда системная артериальная концентрация деоксигенированного гемоглобина (Hb) в крови превышает 5 г/дл (3,1 ммоль/л) (насыщение кислородом ≤85%)(3). Следует отметить, что у пациентов с тяжелой анемией (например, уровень гемоглобина <5 г/дл [3,1 ммоль/л]) цианоз может быть не сразу обнаружен.
Периферический цианоз. Пациенты с периферическим цианозом имеют нормальное системное артериальное насыщение кислородом. Однако повышенная экстракция кислорода приводит к широкой системной артериовенозной разнице по кислороду и увеличению деоксигенированной крови на венозной стороне капиллярного русла.
Приложение 1.
Шкала Сильвермана (Silverman W.L., Andersen O.H., 1956).
Шкала Сильвермана (Silverman W.L., Andersen O.H., 1956).
|
Признак
|
0 балл
|
1 балл
|
2 балла
|
|
«Парадоксальное» дыхание
|
Нет
|
Отсутствие синхронности или минимальное опущение верхней части грудной клетки при подъёме передней брюшной стенки на вдохе
|
Заметное западение верхней части грудной клетки во время подъёма передней брюшной стенки на вдохе
|
|
Втяжение межреберий на
вдохе |
Нет
|
Лёгкое
|
Выраженное
|
|
Втяжение
мечевидного отростка на вдохе |
Нет
|
Лёгкое
|
Выраженное
|
|
Участие подбородка
при дыхании |
Нет
|
Опускание подбородка на вдохе, рот закрыт
|
Опускание подбородка на вдохе, рот открыт
|
|
Экспираторные шумы
|
Нет
|
Экспираторные шумы слышны при аускультации грудной клетки
|
Экспираторные шумы слышны при поднесении фонендоскопа ко рту или даже без фонендоскопа
|
1–3 балла— легкие дыхательные расстройства,
4–6 баллов— умеренные дыхательные расстройства,
7- 10 баллов— тяжелые дыхательные расстройства
Иллюстрированное представление оценки клинических признаков респираторного дистресса новорожденных детей, представленных шкале Сильвермана-Андерсена
4–6 баллов— умеренные дыхательные расстройства,
7- 10 баллов— тяжелые дыхательные расстройства
Иллюстрированное представление оценки клинических признаков респираторного дистресса новорожденных детей, представленных шкале Сильвермана-Андерсена
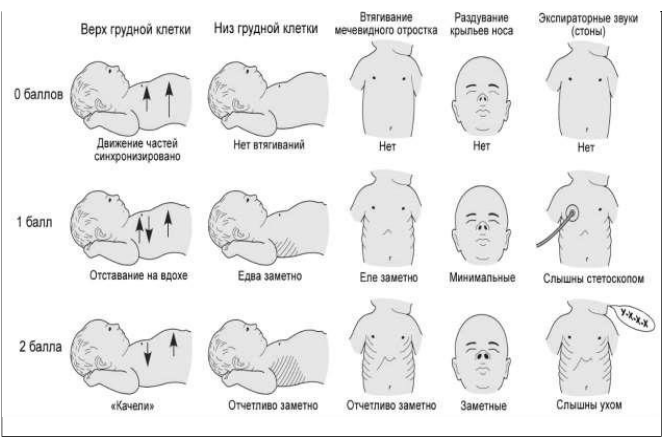
Приложение 2.
РЕНТГЕНОЛОГИЧЕСКИЕ КРИТЕРИИ ОЦЕНКИ СТЕПЕНИ ТЯЖЕСТИ РЕСПИРАТОРНОГО ДИСТРЕСС-СИНДРОМА НОВОРОЖДЕННЫХ
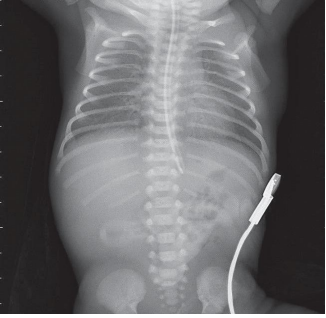
РДС 1 степени тяжести.
Мелкогранулярные изменения легких (гранула = свободные от воздуха (ателектазированные) альвеолярные области.
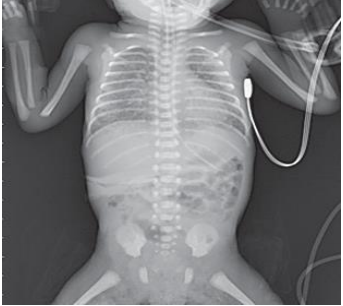
РДС 2 степени тяжести.
Мелкогранулярные изменения легких+обогащенная аэрограмма бронхов на контурах сердца. Участки легких, стабильно остающиеся открытыми и содержащие воздух, хорошо видны на фоне не содержащей воздуха (ателектазированной) легочной ткани и не содержащего воздуха сердца.
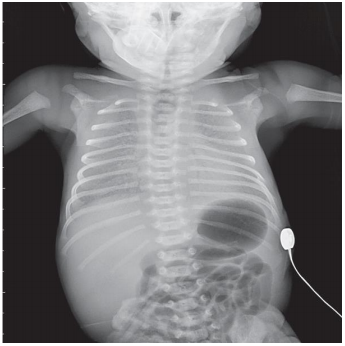
РДС 3 степени тяжести. Мелкогранулярные изменения легких + обогащенная аэробронхограмма на контурах сердца + нечеткое отграничение легочных полей от сердца и диафрагмы.содержание Содержание воздуха в легких, особенно в периферических областях, так сильно снижено, что стирается контраст с не содержащими воздух тканями сердца, диафрагмы и печени.
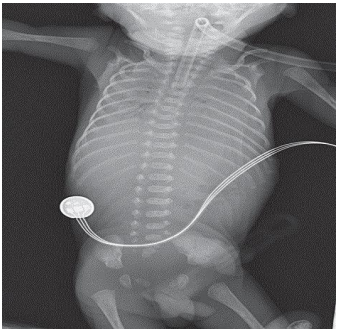
РДС 4 степени тяжести. «Белые легкие». Содержание воздуха в легких снижено настолько, что нет контраста с не содержащими воздух тканями сердца, диафрагмы и печени.
Приложение 3.
УЗИ легких.
УЗИ легких.
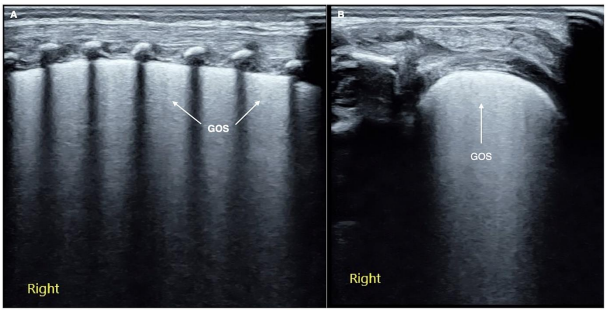
Рисунок 1. Перпендикулярное сканирование показывает, что плевральная линия утолщена и размыта, эхогенность в ближнем поле усилена, а эхогенность в дальнем поле значительно ослаблена, выглядя как матовое стекло (A). Параллельное сканирование показывает, что матовое стекло более очевидно в ближнем поле (B). GOS (признаки матового стекла) является характерным ультразвуковым признаком RDS I степени.
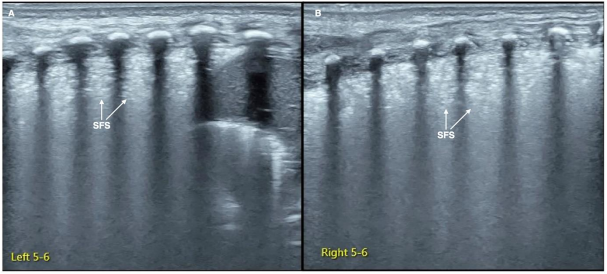
Рисунок 2. На УЗИ в В-режиме мы можем увидеть своего рода специфическую легочную консолидацию, которая характеризуется очевидным пятном и пятнистыми или тонкими линиями воздушных бронхограмм в области поражения, образуя признаки снежинки (SFS).
SFS- является характерным ультразвуковым признаком РДС II степени и выше.
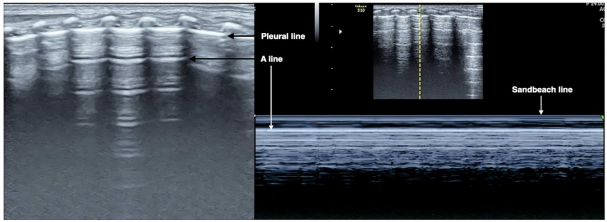
Рисунок 3. Нормальная картина УЗИ легких. На снимках в B-режиме и плевральная линия, и A-линия выглядят как гладкие, регулярные и гиперэхогенные линии, расположенные параллельно и на одинаковом расстоянии друг от друга, то есть как знак бамбука. На УЗИ в M-режиме выглядит как знак песчаного пляжа.
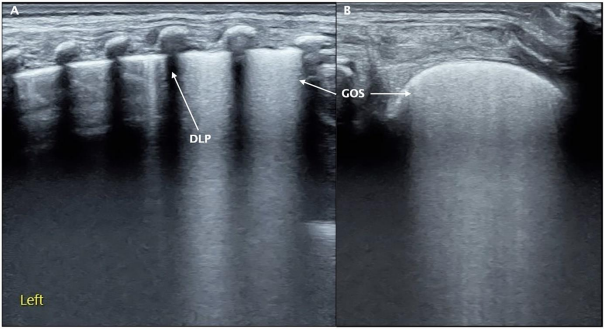
Рисунок 4. РДС I степени. Пациент с РДС I степени. УЗИ легких выявило легочную консолидацию, похожую на признаки матового стекла (GOS) в последних двух межреберных промежутках левого легкого и DLP двойная точка легкого между верхним и нижним легочными полями (A). GOS был более типичным, когда датчик сканировался вдоль межреберного промежутка параллельно (B).
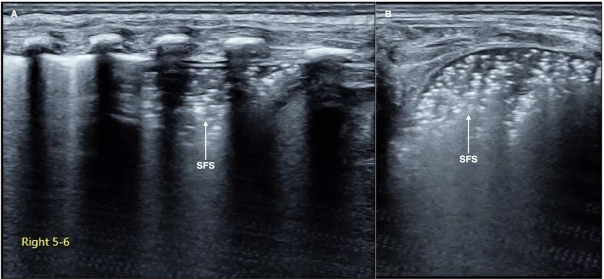
Рисунок 5. РДС II степени. Пациенты с РДС. УЗИ легких показало, что легочная консолидация, похожая на СФС, затронула только часть межреберья (правая 6-я область у этого пациента) правого легкого (A: перпендикулярное сканирование; B: параллельное сканирование).
УЗИ грудной клетки. Ультрасонография грудной клетки новорожденных все чаще используется в неонатологической практике для оценки заболеваний легких. Характерные ультразвуковые признаки РДС включают:
- Консолидация легких на воздушных бронхограммах. Консолидированные участки имеют неравномерную гипоэхогенность, а граница с окружающей легочной тканью четкая и легко различимая. Воздушные бронхограммы могут иметь плотную, крапчатую или снежинчатую форму. Обычно наблюдается двустороннее поражение, часто вовлекаются задние отделы легких. Степень консолидации коррелирует с тяжестью заболевания. При легком РДС консолидации могут ограничиваться субплевральной паренхимой легкого. Тяжелый РДС обычно имеет диффузное поражение («белое легкое»). Наличие уплотнений в легких является ключевым признаком, отличающим ультразвуковую картину РДС от транзиторного тахипноэ новорожденного (ТТН).
- Аномалии плевральной линии. Плевральная линия имеет ненормальный вид, А-линии исчезают.
- Интерстициальное поражение. В неконсолидированных областях легких могут наблюдаться признаки интерстициального поражения (например, B-линии кометного хвоста и картина альвеолярного интерстициального синдрома).
- Плевральные выпоты. Односторонние или двусторонние плевральные выпоты наблюдаются в 15–20 процентах случаев.
Эти результаты могут быть использованы для установления диагноза РДС и оценки степени тяжести.
Приложение 4.
КЛИНИЧЕСКИЙ ПРОТОКОЛ МЕДИЦИНСКОГО ВМЕШАТЕЛЬСТВА СОП
Проведение неинвазивной респираторной поддержки у новорожденных методом непрерывного положительного давления в дыхательных путях (СРАР)
Требования к проведению процедуры/вмешательства:
- На подготовительном этапе следует проверить наличие и функционирование оборудования, согласно оперативному контрольному списку-чек, лист.
- На каждых родах должен присутствовать как минимум 1 медработник, владеющий навыками начальной помощи и проведения вентиляции под положительным давлением, единственной обязанностью которого является оказание помощи новорожденному.
- При наличии значимых перинатальных факторов риска, повышающих вероятность расширенной реанимации должен быть немедленно доступен дополнительный персонал с навыками непрямого массажа сердца, интубации трахеи и катетеризации пупочной вены.
- На каждых родах должны быть легко доступны все материалы и оборудование, необходимые для выполнения всех этапов реанимации. Если ожидается рождение ребенка высокого перинатального риска, все соответствующие материалы и оборудование должны быть готовы к немедленному использованию.
Стандартные меры предосторожности:
- При проведении процедуры строго соблюдаются все положения инфекционного контроля по отношению к обработке родильного зала, палат интенсивной терапии, оборудования, материалов, используемых в процессе реанимации, рук персонала и т.д.
- Ситуация при проведении респираторной терапии новорожденных характеризуется высоким риском контакта с биологическими жидкостями человеческого организма (кровь, моча, стул, слюна, рвотные массы), которые следует расценивать как потенциально инфицированные. Поэтому перед началом реанимации новорожденного необходимо надеть стерильные перчатки. При выполнении процедур, связанных с вероятным разбрызгиванием капель крови или других биологических жидкостей, следует надевать маску, защитные приспособления для глаз и лица, халат и фартук.
Ранний СРАР/ РЕЕР
Методика СРАР как самостоятельый метод респираторной поддержки применяется:
- с профилактической целью с первых минут жизни - у новорожденных гестационного возраста ≤ 30 недели
- при наличии регулярного спонтанного дыхания (в том числе - стонущего, сопровождающегося втяжением уступчивых мест) и ЧСС > 100 уд/мин.
- СРАР в родильном зале проводится при помощи биназальных канюль, назальной или лицевой маски (РЕЕР +6 см FiO2 0,21-0,3).
- Если гестационный возраст >30 недель СРАР рекомендован по показаниям.
Критериями неэффективности СРАР считают:
- нарастание тяжести ДН.
- выраженное участие вспомогательной мускулатуры
- потребность в дополнительной оксигенации более 30%.
- РЕЕР +6 см
Тяжелый респираторный синдром требует перевода ребенка на ИВЛ и введения сурфактанта, ИВЛ в родильном зале проводится с созданием остаточного давления в конце выдоха РЕЕР +4-5 см Н2О.
Алгоритм изменения режимов СРАР при терапии РДС недоношенным с гестационным возрастом 26-28 недель
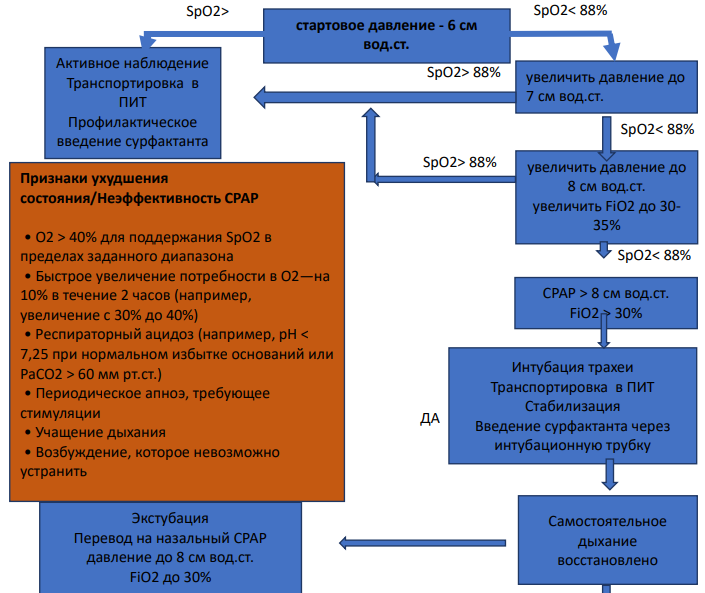

Приложение 5.
HFNC - Назальная канюля с высоким потоком
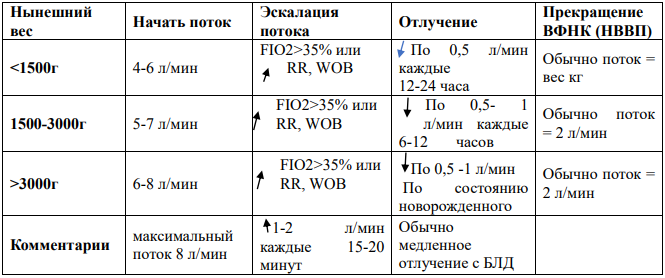
Приложение 6.
Стандартная операционная процедура
Малоинвазивное введение сурфактанта Методика LISA.
LISA – это аббревиатура выражения: Less Invasive Surfactant Administration, или «мало инвазивное введение сурфактанта»
LISA – это ряд методик, включающих введение сурфактанта через тонкий эндотрахеальный катетер при спонтанном дыхании больного с использованием CPAP (постоянное положительное давление в дыхательных путях).
Метод LISA позволяет:
Стандартная операционная процедура
Малоинвазивное введение сурфактанта Методика LISA.
LISA – это аббревиатура выражения: Less Invasive Surfactant Administration, или «мало инвазивное введение сурфактанта»
LISA – это ряд методик, включающих введение сурфактанта через тонкий эндотрахеальный катетер при спонтанном дыхании больного с использованием CPAP (постоянное положительное давление в дыхательных путях).
Метод LISA позволяет:
- Вводить сурфактант раньше
- Сохранить спонтанное дыхание ребенка
- Обеспечить синергизм CPAP и сурфактанта – нет необходимости прерывать СРАР
- Не зависеть от механической вентиляции
-
Соответствует целям лечения – обеспечить респираторную поддержку с защитой легких, так как удается:
- избежать МВ благодаря введению сурфактанта не по схеме InSurE
- избежать утраты эффективности CPAP путем раннего назначения сурфактанта
- избежать МВ за счет того, что CPAP не утрачивает эффективность
- Помогая избежать МВ, метод LISA, снижает вероятность БЛД, задержки психомоторного развития и других осложнений МВ
Почему метод LISA менее инвазивный?
- Катетер для LISA гораздо тоньше, чем эндотрахеальная трубка, и считается менее инвазивным
- Считается, что более тонкий катетер для LISA позволяет проводить процедуру без седации или под легкой седацией
- Считается, что отсутствие необходимости ручной вентиляции в сочетании с введением сурфактанта – это менее инвазивная процедура
Необходимое оснащение:
1. Стерильные перчатки
2. Стерильная пеленка
3. Ларингоскоп
4. Желудочный зонд 4 FR
5. Шприц объемом 5 мл
6. Шприц объемом 2 мл
7. Сурфактант
8. Атропина сульфат 1 мг/мл - 1 амп
9. Медицинский отсос
Описание пациента:
Самостоятельно дышащий новорожденный ребенок со сроком гестации 26-28 недель (и более) которому проводится неинвазивная респираторная поддержка в виде назального СРАР. С установленным желудочным зондом.
Методика проведения:
1. В процедуре участвуют 2 человека
2. Оцените состояние ребенка
3. Определите дозу вводимого сурфактанта и согрейте сурфактант
4. Вымойте руки и наденьте перчатки и средства защиты.
5. Наберите в шприц 5 мл дозу сурфактанта с дополнительным объемом воздуха, присоедините шприц к катетеру, катетер держите стерильным
6. Укутайте ребенка и придайте ему удобную позицию для ларингоскопии в инкубаторе или столике с обогревом
7. Шланги от назального СРАР должны находиться слева от головы ребенка
8. Оцените состояние ребенка (стабильный, сатурация выше 90%, пульс выше 100 уд. мин.)
9. Введите в рот ребенку 0,1 мл 20% раствора глюкозы
10. Аккуратно введите ларингоскоп и визуализируйте голосовую щель
11. Введите стерильный зонд, так чтобы конец располагался приблизительно на 2 см ниже голосовой щели, ассистент фиксирует шприц
12. Аккуратно извлеките ларингоскоп и 2-мя пальцами зафиксируйте катетер возле губ ребенка
13. Если у ребенка развилась брадикардия введите ВВ Атропин 20 мкг/кг
14. Проверьте состояние ребенка
15. Медленно и осторожно введите сурфактант в течение 2-3 минут, опорожните катетер остаточным воздухом из шприца
16. Ассистент параллельно проводит аспирационную пробу из желудочного зонда
17. Извлеките катетер
18. Проверьте состояние ребенка и верните его в исходное положение
2. Оцените состояние ребенка
3. Определите дозу вводимого сурфактанта и согрейте сурфактант
4. Вымойте руки и наденьте перчатки и средства защиты.
5. Наберите в шприц 5 мл дозу сурфактанта с дополнительным объемом воздуха, присоедините шприц к катетеру, катетер держите стерильным
6. Укутайте ребенка и придайте ему удобную позицию для ларингоскопии в инкубаторе или столике с обогревом
7. Шланги от назального СРАР должны находиться слева от головы ребенка
8. Оцените состояние ребенка (стабильный, сатурация выше 90%, пульс выше 100 уд. мин.)
9. Введите в рот ребенку 0,1 мл 20% раствора глюкозы
10. Аккуратно введите ларингоскоп и визуализируйте голосовую щель
11. Введите стерильный зонд, так чтобы конец располагался приблизительно на 2 см ниже голосовой щели, ассистент фиксирует шприц
12. Аккуратно извлеките ларингоскоп и 2-мя пальцами зафиксируйте катетер возле губ ребенка
13. Если у ребенка развилась брадикардия введите ВВ Атропин 20 мкг/кг
14. Проверьте состояние ребенка
15. Медленно и осторожно введите сурфактант в течение 2-3 минут, опорожните катетер остаточным воздухом из шприца
16. Ассистент параллельно проводит аспирационную пробу из желудочного зонда
17. Извлеките катетер
18. Проверьте состояние ребенка и верните его в исходное положение
Приложение 7.
Стратегия вентиляции при РДС.
CPAP: начинается с 5–6 см H2O и увеличивается до 7–8 см H2O. Риск пневмоторакса может увеличиваться при более высоких уровнях давления CPAP. СРАР титруют по клинической оценке ретракции и частоты дыхания, а также по наблюдению за насыщением кислородом. В этой ситуации NIPPV может быть альтернативой CPAP. Кроме того, у детей раннего возраста с более тяжелым РДС может быть рассмотрена iвозможность интубации для введения сурфактанта с быстрой экстубацией с последующей СРАР ( методика INSURE ). Также необходимо учитывать LISA и MIST (см. приложение N4).
Важно знать. Существуют предпосылки неудачи INSURE у очень недоношенных новорожденных на практике: Низкий гестационный возраст, низкая концентрация гемоглобина до введения сурфактанта. Предикторы длительной МВ могут также прогнозировать неудачу INSURE : низкий гестационный возраст, низкая оценка по шкале Апгар на 5 минуте, высокое FiO2, высокое рСО2, высокий уровень лактата, низкий рН, инотропные препараты, вводимые до интубации , и сурфактант, вводимый в течение 5 часов после рождениеii
Механическая вентиляция: используется, когда несоответствие V̇/Q̇ настолько велико, что повышенного FiO2 и CPAP недостаточно для поддержания газообмена, или у младенцев, которые устали от учащенного дыхания.
CPAP: начинается с 5–6 см H2O и увеличивается до 7–8 см H2O. Риск пневмоторакса может увеличиваться при более высоких уровнях давления CPAP. СРАР титруют по клинической оценке ретракции и частоты дыхания, а также по наблюдению за насыщением кислородом. В этой ситуации NIPPV может быть альтернативой CPAP. Кроме того, у детей раннего возраста с более тяжелым РДС может быть рассмотрена iвозможность интубации для введения сурфактанта с быстрой экстубацией с последующей СРАР ( методика INSURE ). Также необходимо учитывать LISA и MIST (см. приложение N4).
Важно знать. Существуют предпосылки неудачи INSURE у очень недоношенных новорожденных на практике: Низкий гестационный возраст, низкая концентрация гемоглобина до введения сурфактанта. Предикторы длительной МВ могут также прогнозировать неудачу INSURE : низкий гестационный возраст, низкая оценка по шкале Апгар на 5 минуте, высокое FiO2, высокое рСО2, высокий уровень лактата, низкий рН, инотропные препараты, вводимые до интубации , и сурфактант, вводимый в течение 5 часов после рождениеii
Механическая вентиляция: используется, когда несоответствие V̇/Q̇ настолько велико, что повышенного FiO2 и CPAP недостаточно для поддержания газообмена, или у младенцев, которые устали от учащенного дыхания.
Рекомендуется использовать режим VG в сочетании с вспомогательным управлением (A/C), SIMV или PSV- со следующими настройками iii:
- VT 4-6 мл/ кг
- Частота резервного дыхания от 30 до 60 в минуту
- Время вдоха 0,30-0,35 сек.
- ПДКВ 5-8 см H2O
- Поддержка давлением для достижения 50-75% установленного VT во время SIMV/резервных вдохов
- Когда состояние пациента улучшается, сначала уменьшается FiO2 и PIP или VT, чередуясь с частотой, в ответ на оценку результатов экскурсии грудной клетки, насыщения кислородом и газов крови.
- При вентиляции с гарантией целевого объема PIP будет автоматически уменьшаться в ответ на улучшение комплайнса;
- В режимах, инициируемых пациентом, частота поддержки вентилятора обычно не меняется, а для выключения аппарата ИВЛ используется прогрессивное снижение давления вдоха (PIP) .
- Экстубация обычно успешна, когда частота вентилятора составляет <20–25 вдохов в минуту или PIP составляет менее 16–18 см водного столба. MAP 7,0–8,0 см водяного столба для достижения желаемого VT.
Обратите внимание! Терапию цитратом кофеина следует начинать до экстубации , чтобы облегчить самостоятельное дыхание. Также рекомендуется давать по крайней мере за 30 минут до LISA iv.
Профилактический прием кофеина увеличивает вероятность успешной экстубации у новорожденных с очень низкой массой тела при рождении (1А). Кроме того, он используется для детей с высоким риском потребности в ИВЛ, находящихся на неинвазивной респираторной поддержке ( C1 ). Стандартный режим дозирования цитрата кофеина основан на нагрузочной дозе 20 мг/кг (эквивалентно 10 мг/кг основания кофеина) с последующей поддерживающей дозой 5–10 мг/кг (эквивалентно 2,5–5 мг/кг основания кофеина). Суточная доза начинается через 24 часа после нагрузочной дозы, вводят внутривенно или энтерально. Прекратите прием кофеина, когда ребенок достигнет постконцептуального возраста ПКВ между 32 и 34 неделями и в течение примерно пяти дней не было эпизодов апноэ, требующих вмешательства.
HFV считается целесообразным, когда МАР, необходимое для адекватного газообмена, превышает 10–11 см вод. ст. у детей младшего возраста. Параметры, выбранные оператором, включают MAP, частоту и амплитуду.
Профилактический прием кофеина увеличивает вероятность успешной экстубации у новорожденных с очень низкой массой тела при рождении (1А). Кроме того, он используется для детей с высоким риском потребности в ИВЛ, находящихся на неинвазивной респираторной поддержке ( C1 ). Стандартный режим дозирования цитрата кофеина основан на нагрузочной дозе 20 мг/кг (эквивалентно 10 мг/кг основания кофеина) с последующей поддерживающей дозой 5–10 мг/кг (эквивалентно 2,5–5 мг/кг основания кофеина). Суточная доза начинается через 24 часа после нагрузочной дозы, вводят внутривенно или энтерально. Прекратите прием кофеина, когда ребенок достигнет постконцептуального возраста ПКВ между 32 и 34 неделями и в течение примерно пяти дней не было эпизодов апноэ, требующих вмешательства.
HFV считается целесообразным, когда МАР, необходимое для адекватного газообмена, превышает 10–11 см вод. ст. у детей младшего возраста. Параметры, выбранные оператором, включают MAP, частоту и амплитуду.
- МАР составляет 10–16 см вод. ст., обычно на 1–2 см вод. ст. выше по сравнению с предыдущими настройками обычной вентиляции при переключении. Последующие корректировки выполняются в зависимости от потребности в кислороде и оптимизации расширения легких в зависимости от положения диафрагмы на рентгенограмме грудной клетки примерно до 8-9 задних ребер.
- Амплитуда — примерно в два раза больше МАР — настраивается на вибрацию грудной клетки/живота.
- Частота 8–15 Гц (нижний предел для доношенных детей, верхний предел для глубоко недоношенных детей; в большинстве клинических отчетов используется частота 10 Гц).
- Обычно достаточно потока от 8 до 15 л/мин.
Отлучение от HFO. Как правило, сначала снижают FiO2, а затем MAP с шагом 1-2 см вод. ст., когда FiO2 падает ниже 0,6. Амплитуда регулируется частой оценкой вибрации грудной клетки и определением газов крови. Частота обычно не регулируется, если иным образом не удается достичь адекватной оксигенации или вентиляции. В отличие от традиционной механической вентиляции, снижение частоты вдохов при вентиляции с HFO улучшит вентиляцию за счет воздействия доставляемого VT.
i Ng EH, Shah V Руководство по заместительной терапии сурфактантом у новорожденных. Педиатр Здоровье ребенка. 2021;26(1):35. Epub 2021 1 февраля.
ii Нис Брикс1, Анна Селлмер1, Мортен Сондергаард Йенсен1, Линда Вад Педерсен2 и Тине Бринк Хенриксен1,2 Предикторы неудачной интубации-сурфактанта-экстубации процедура: когортное исследование , BMC Pediatrics том 14 , Номер статьи: 155 (2014)
iii Антон Х. ван Каам , Даниэла Де Лука , Роланд Хентшель , Йерун Хаттен , Ричард Синделар , Ульрих Томе Люк Й.И. Циммерманн Способы и стратегии обеспечения традиционной ИВЛ у новорожденных Педиатрические исследования том 90, страницы 957–962 (2021)
iv https://www.clinicalguidelines.scot.nhs.uk/nhsggc-guidelines/nhsggc- guidelines/neonatology/less-invasive-surfactant-administration-lisa-neonatal-guideline/
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.