Рак мочевого пузыря
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Злокачественное новообразование пузыря (C67)
Онкология
Общая информация
Краткое описание
Одобрено
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «14» декабря 2023 года
Протокол №198
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
РАК МОЧЕВОГО ПУЗЫРЯ
Рак мочевого пузыря - распространенный тип злокачественного процесса, который берет начало из клеток, выстилающих внутреннюю поверхность мочевого пузыря (уротелиальных клеток).
Код(ы) МКБ-10:
Дата разработки/пересмотра протокола: 2018 г. (пересмотр 2023 г.)
Категории пациентов: взрослые.
Шкала уровня доказательности:
Рак мочевого пузыря - распространенный тип злокачественного процесса, который берет начало из клеток, выстилающих внутреннюю поверхность мочевого пузыря (уротелиальных клеток).
ВВОДНАЯ ЧАСТЬ
Код(ы) МКБ-10:
|
Код
|
Название |
|
C67
|
Злокaчественное новообрaзовaние мочевого пузыря |
| С67.0 | Треугольник мочевого пузыря |
| С67.1 | Купола мочевого пузыря |
| С67.2 | Боковой стенки мочевого пузыря |
|
С67.3
|
Передней стенки мочевого пузыря |
| С67.4 | Задней стенки мочевого пузыря |
| С67.5 | Шейка мочевого пузыря (внутреннего уретрального отверстия) |
| С67.6 | Мочеточникового отверстия |
|
С67.7
|
Первичного мочевого протока (урахуса) |
| С67.8 | Поражение мочевого пузыря, выходящие за пределы одной и более вышеуказанных локализаций |
| С67.9 | Мочевого пузыря неуточненной части |
Дата разработки/пересмотра протокола: 2018 г. (пересмотр 2023 г.)
Пользователи протокола: онкологи, хирурги, радиологи, гинекологи, урологи, врачи общей практики, терапевты, химиотерапевты.
Категории пациентов: взрослые.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследование случай-контроля с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов |
Классификация
Классификация [2,5]
Классификация ВОЗ [2]:
Папиллярная опухоль уротелия с низким злокачественным потенциалом (PUNLMP);
Папиллярный уротелиальный рак низкой степени злокачественности (LG - low grade);
Папиллярный уротелиальный рак высокой степени злокачественности (HG – high grade).
Согласно классификации ВОЗ – опухоли мочевого пузыря подразделяют на папиллому, папиллярную уротелиальную опухоль с низким злокачественным потенциалом, уротелиальный рак низкой и высокой степенью злокачественности.
Морфологическая классификация [1,5]:
Уротелиальная карцинома in situ;
Переходно-клеточный рак (с плоскоклеточной, железистой дифференцировкой);
Плоскоклеточный рак;
Мелкоклеточный рак;
Аденокарцинома;
Недифференцированный рак.
Классификация рака мочевого пузыря:
В настоящее время используется следующая классификация ВОЗ [9, 14]:
1. Уротелиальная карцинома
2. Уротелиальные карциномы с частичной плоскоклеточной и / или железистой или трофобластической дифференцировкой;
3. Микропапиллярный уротелиальный рак;
4. Гнездовой вариант (в том числе крупный гнездовой вариант) и микрокистозная уротелиальная карцинома;
5. Плазмацитоид, гигантская клетка, перстень, диффузный, недифференцированный;
6. Лимфоэпителиомоподобный;
7. Мелкоклеточные карциномы;
8. Саркоматоидные уротелиальные карциномы;
9. Нейроэндокринный вариант уротелиальной карциномы;
10. Некоторые уротелиальные карциномы с другими редкими дифференцировками.
Классификация TNM 2017 год [5]:
Т – первичная опухоль:
ТX – недостаточно данных для оценки первичной опухоли;
Т0 – признаки первичной опухоли отсутствуют;
Та – неинвазивная папиллярная карцинома;
Tis – преинвазивная карцинома: carcinoma in situ ("плоская опухоль");
Т1 – опухоль распространяется на субэпителиальную соединительную ткань;
Т2 – опухоль распространяется на мышцы;
Т2а – опухоль распространяется на поверхностную мышцу (внутренняя половина);
Т2b – опухоль распространяется на глубокую мышцу (наружная половина);
Т3 – опухоль распространяется на паравезикальную клетчатку:
Т3а – микроскопически;
Т3b – макроскопически (экстравезикальная опухолевая ткань);
Т4 – опухоль распространяется на одну из следующих структур:
T4a – опухоль распространяется на простату, матку или влагалище;
T4b – опухоль распространяется на стенки таза или брюшную стенку;
Примечание. Если при гистологическом исследовании не подтверждается инвазия мышцы, то считается, что опухоль поражает субэпителиальную соединительную ткань.
N – регионарные лимфатические узлы:
N – регионарные лимфатические узлы:
Регионарными для мочевого пузыря являются лимфоузлы малого таза ниже бифуркации общих подвздошных сосудов.
NX – определить состояние лимфатических узлов не представляется возможным;
N0 – метастазы в регионарных узлах не определяются;
N1 – метастазы в единичном (подвздошном, запирательном, наружном подвздошном, пресакральном) лимфатическом узле в малом тазе;
N2 – метастазы в нескольких (подвздошных, запирательных, наружных подвздошных, пресакральных) лимфатических узлах в малом тазе;
N3 – метастазы в одном общем подвздошном лимфатическом узле или более.
М – отдаленные метастазы:*
М – отдаленные метастазы:*
М0 – Признаки отдаленных метастазов отсутствуют;
M1a - Отдаленные метастазы, ограниченные лимфатическими узлами за пределами общих подвздошных узлов
M1b - Отдаленные метастазы, не являющиеся лимфатическими узлами
Соответствие клинических стадий категориям TNM [1] (УД – А):
G – гистопатологическая градация:
GX – степень дифференцировки не может быть установлена;
G1 – высокая степень дифференцировки;
G2 – средняя степень дифференцировки;
G3-4 – низкодифференцированные /недифференцированные опухоли.
Соответствие клинических стадий категориям TNM [1] (УД – А):
|
Стадия 0а
Стадия 0is
|
Ta
Tis
|
N0 | M0 |
| Стадия I | T1 | N0 | M0 |
| Стадия II |
T2a
T2b
|
N0
N0
|
M0
M0
|
| Стадия III |
Т3a–b
Т4а
|
N0
N0
|
M0
M0
|
| Стадия IV |
T4b
любая T
любая T
|
N0 N1,2,3
любая N
|
M0
M0
M1
|
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ [1,3]
Диагностические критерии
Жалобы и анамнез:
гематурия, макро или микрогематурия;
дизурические явления;
императивные позывы;
боли в надлобковой области;
слабость;
потливость по ночам;
субфебрильная температура;
похудание.
Физикальное обследование
локальная болезненность над лоном;
при бимануальном осмотре возможно прорастание в прямую кишку, предстательную железу у мужчин, инфильтрация данных структур;
у женщин при вагинальном осмотре инфильтрация передней стенки влагалища, шейки матки.
Дополнительные:

Лабораторные исследования [1,2]
Основные:
Общий анализ крови – наиболее характерно наличие анемии, разной степени выраженности; повышение СОЭ, лейкоцитоз;
Общий анализ мочи – микро-, макрогематурия, возможно: лейкоцитурия, бактериурия, протеинурия;
Тест на ЛТИ: АТР или IGRA тесты: должны быть отрицательными.
Дополнительные:
Биохимический анализ крови – гипопротеинемия, повышение креатинина, мочевины;
Коагулограмма – склонность к гиперкоагуляции.
Основные:
Алгоритм диагностики латентной туберкулезной инфекции (ЛТИ) перед назначением внутрипузырной БЦЖ-терапии и маршрут пациента
Инструментальные исследования [6,7]:
Основные:
Цистоскопия – определяется опухолевое образование на любой стенке мочевого пузыря в виде «цветной капусты» на ножке или на широком основании, одиночное или множественное, либо изменения могут быть в виде инфильтративного процесса, гиперемия стенки, буллезного отека слизиcтой. При технической возможности необходимо взять биопсию с образования и/или с подозрительных мест (при подозрении на карциному insitu материал необходимо брать из различных отделов мочевого пузыря (мультифокальная биопсия) и простатического отдела уретры. Предпочтительно проведение гистологического исследования - ТУР мочевого пузыря);
Цитологическое и/или гистологическое исследование биоптата из опухоли мочевого пузыря – определяются морфологические признаки рака, подтверждение диагноза злокачественного новообразования;
УЗИ органов малого таза – определяется экзофитная тень тканевой плотности в полости мочевого пузыря, неравномерное утолщение стенки, наличие или отсутствие метастазов в регионарные лимфатические узлы;
КТ или МРТ органов малого таза – определяется опухоль мочевого пузыря, а также увеличенные лимфатические узлы малого таза при распространенности процесса.
Дополнительные [1,2]:
ТРУЗИ мочевого пузыря – определяется степень инвазии опухолью стенки мочевого пузыря;
Обзорно – экскреторная урография – выявляется дефект накопления по стенке мочевого пузыря, а так же уротерегидронефроз на стороне поражения;
Цистография – отмечается дефект наполнения по стенке мочевого пузыря в области поражения;
Диагностический алгоритм: (схема)
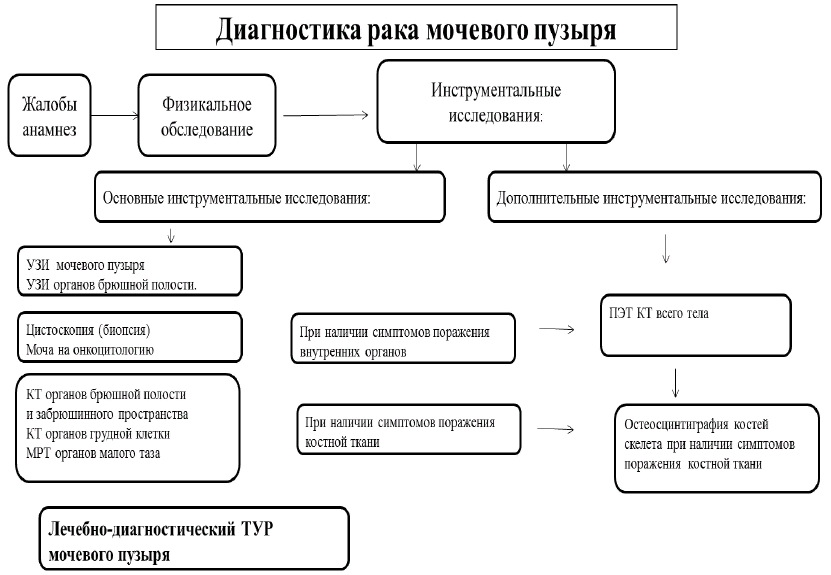
Показания для консультации специалистов:
Консультация фтизиатра – при наличии ЛТИ (латентной туберкулезной инфекции) и при подозрении на специфический процесс, а также при осложнениях во время проведения внутрипузырной БЦЖ-терапии;
Консультации узких специалистов при наличии сопутствующих заболеваний по показаниям.
Диагностический алгоритм: (схема)


Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований [3,5]:
|
Диагноз
|
Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Воспалительные заболевания мочевыводящих путей | При наличии воспаления применяют так же хирургическое лечение |
УЗИ мочевого пузыря
Цистоскопия
МРТ малого таза
|
Отсутствие образования |
| Нефрогенная метаплазия | При наличии образования ,так же гематурии проводится обследование |
УЗИ мочевого пузыря
Цистоскопия с биоспией
МРТ малого таза
|
Исключения по данным морфологии |
| Аномалии развития мочевыделительного тракта | Экстрофия мочевого пузыря, аномалии урахуса, агенезия, удвоение мочевого пузыря, дивертикул мочевого пузыря, врожденная контрактура шейки мочевого пузыря (болезнь Мариона). |
УЗИ мочевого пузыря
Цистоскопия
МРТ малого таза
|
Отсутствие образования по данным исследований |
| Плоскоклеточная метаплазия уротелия | Лейкоплакия мочевого пузыря |
УЗИ мочевого пузыря
Цистоскопия с биопсией
|
Исключения по данным морфологии |
| Доброкачественные эпителиальные образования мочевого пузыря | Это группа эпителиальных и неэпителиальных новообразований, исходящих из различных слоев стенки мочевого пузыря и растущих внутрь его полости. Неоплазии могут проявляться гематурией различной интенсивности, учащенным мочеиспусканием и ложными позывами, болезненностью. |
УЗИ мочевого пузыря
Цистоскопия с биоспией
МРТ малого таза
|
Отсутствие образования по данным исследований
Исключения по данным морфологии
|
| Туберкулез | Это одно из внелегочных проявлений заболевания, вызванного Mycobacterium tuberculosis и M. bovis. Болезнь чаще всего развивается как осложнение нефротуберкулеза у пациентов с сопутствующими хроническими патологиями мочевыводящей системы | Следует проводить ПЦР-диагностику для определения ДНК M. tuberculosis в осадке мочи, секрете простаты, эякуляте, отделяемом свищей. При подозрении на туберкулез больной должен быть направлен для полного фтизиоурологического обследования в противотуберкулезный диспансер | Диагноз УГТ достоверно исключен, если ни в одном образце ни одного вида патологического материала ни одним методом не найдена МБТ, патоморфологическое исследование биоптата не выявило признаков туберкулезного воспаления, на рентгенограммах нет признаков деструкции, объем мочевого пузыря в пределах физиологической нормы, провокационные пробы отрицательные, терапия ex juvantibus 1 типа дала положительный результат; отсутствуют свищи |
| Хронический цистит | Состояние, характеризующееся длительным воспалением стенки мочевого пузыря. | Лабораторные диагностика (анализы крови, мочи, включая посев на бактериальную флору) Ультразвуковая визуализация Рентгенологическая визуализация Флоуметрия Уретроцистоскопия Внутривенная урография |
Отсутствие образования по данным исследований
Исключения по данным морфологии
|
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ: нет.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Карта наблюдения пациента, маршрутизация пациента (схемы, алгоритмы):

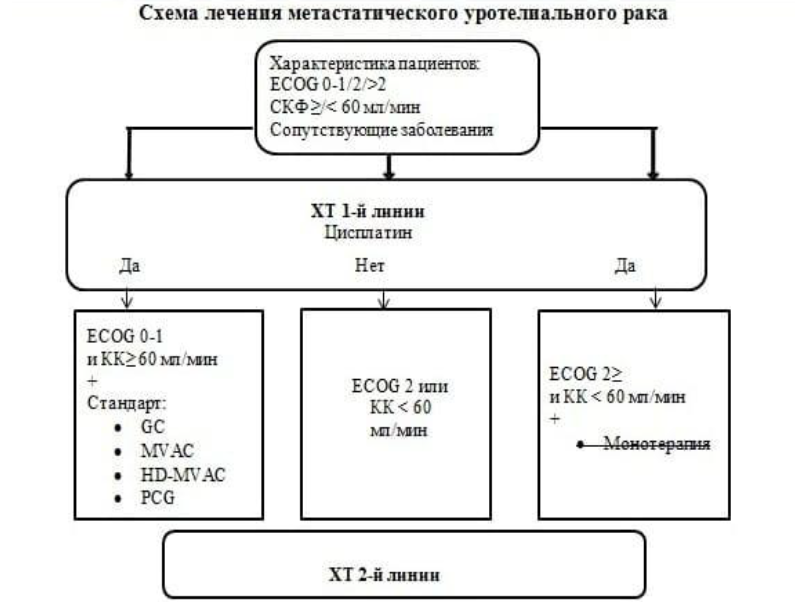

Немедикаментозное лечение:
Режим 1 (постельный) первые сутки после операции;
Режим 2 (полупостельный) 2-3 сутки после операции;
Режим 3 (общий) свободный режим;
Диета – стол №7.
Медикаментозное лечение [4; 12; 15]:
Внутрипузырная терапия:
Внутрипузырная химиотерапия;
Внутрипузырная БЦЖ-иммунотерапия.
Системная терапия
Пре и после оперативная ХТ (неоадьювантная [предпочитительна для рака мочевого пузыря] или адьювантная.
Первая линия системной терапии местнораспространенного или метастатического рака мочевого пузыря (Стадия IV) (Категория 2А, если не указано иное)
Вторая линия терапии местнораспространенного или метастатического рака мочевого пузыря (Стадия IV) (После терапиии препаратами платины)
Вторая линия терапии местнораспространенного или метастатического рака мочевого пузыря (Стадия IV) (После терапиии ингибиторами иммунных контрольных точек)
Симптоматическая терапия.
Внутрипузырная терапия (УД-А).
Внутрипузырная химиотерапия:
Внутрипузырная химиотерапия может применяться в сочетании с хирургическим лечением для профилактики рецидивов и прогрессирования после операции.
В настоящее время для внутрипузырного введения используются следующие химиопрепараты: доксорубицин, митомицин С, цисплатин и другие химиопрепараты.
В день проведения ТУР мочевого пузыря при предположительно немышечно- инвазивном раке мочевого пузыря, за исключением случаев, когда имеется подозрение на интра- либо экстраперитонеальную перфорацию мочевого пузыря, обычно при проведении обширных ТУР (опасность развития некроза паравезикальной клетчатки), показано:
Доксорубицин 50мг в 50мл 0,9% р-ра натрия хлорида внутрипузырно на 2ч (УД- В);
Эпирубицин 60-70 мг в 50мл 0,9% р-ра натрия хлорида внутрипузырно на 2ч (УД-В).
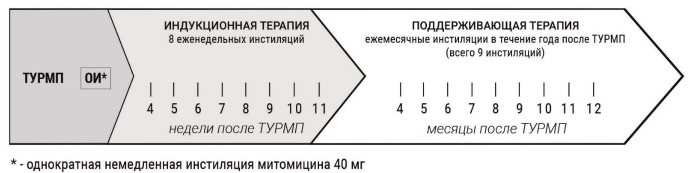

Схемы внутрипузырной химиотерапии [4]
(показано для пациентов с промежуточным риском прогрессирования):
Доксорубицин 50мг в 50мл 0,9% раствора Натрия хлорида внутрипузырно на 2ч еженедельно в течении 6-8 недель, затем ежемесячно до 1 года (УД-В);
Эпирубицин 60-70 мг в 50мл 0,9% раствора Натрия хлорида внутрипузырно на 2ч еженедельно в течении 6-8 недель, затем ежемесячно до 1 года (УД-В).
Внутрипузырная БЦЖ иммунотерапия [12]
(показана пациентам с промежуточным, высоким риском прогрессирования и при CIS) (УД-А):
Внутрипузырное введение БЦЖ проводят по следующей методике: Содержимое флакона (2х108-3х109 жизнеспособных единиц БЦЖ в одном флаконе) разводят в 50мл изотонического раствора хлорида натрия и вводят в мочевой пузырь на 2 часа. Для облегчения контакта препарата со всей поверхностью мочевого пузыря пациенту рекомендуется изменять положение тела через определенные промежутки времени.
Режим БЦЖ- иммунотерапии [12]:
Индукционный курс (через 3 недели после ТУР): 6 еженедельных введений (1 раз в неделю в течении 6 недель).
Поддерживающий курс: 3 еженедельных внутрипузырных вливаний на 3, 6, 12, 18, 24, 30, 36 месяцы.
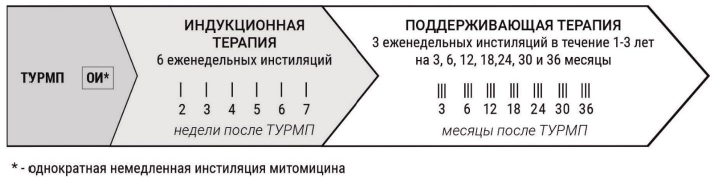

Противопоказания к внутрипузырному введению БЦЖ:
- Первые 2 недели после ТУР;
- ранее перенесенный туберкулез;
- резко положительная кожная реакция на пробу Манту;
- заболевания аллергической природы;
- положительная реакция на АТР или IGRA-тесты;
- первичный иммунодефицит, ВИЧ-инфицирование;
- емкость мочевого пузыря менее 150 мл;
- пузырно-мочеточниковый рефлюкс;
- тяжелые сопутствующие заболевания в стадии декомпенсации;
- иммуносупрессивная терапия (назначение БЦЖ допускается не ранее чем через 6мес. после завершения курса лечения);
- выраженный цистит или макрогематурия (до исчезновения симптомов);
- травматичная катетеризация или появление крови после катетеризации мочевого пузыря являются противопоказаниями для инстилляции БЦЖ в данный день.
Системная химиотерапия (УД-А):
GР (высокодозная схема)*
PРG
МVAC интенсивный
HD-МVAC/МVAC интенсивный
*Поддержка Г-КСФ 5мкг/кг с 1-го по 10-й дни.
Системная терапия [15]
Системная химиотерапия (УД-А):
Стандартом является полихимиотерапия по схеме «гемцитабин+цисплатин».
GР (стандартная схема).
Цисплатин 70мг/м2 в/в капельно 2-й день.
Гемцитабин 1000мг/м2 в/в капельно в 1,8,15-й день. Повторение цикла через 28 дней.
GР (высокодозная схема)*
Цисплатин 70мг/м2 в/в капельно в 1-й день.
Гемцитабин 2500мг/м2 в/в капельно в 1-й день . Повторение цикла через 14 дней.
*Поддержка Г-КСФ с 5-го по 9-й дни.
PРG
Паклитаксел 80мг/м2 в/в капельно в 1, 8-й дни Цисплатин 70мг/м2 в/в капельно в 1-й день.
Гемцитабин 1000мг/м2 в/в капельно в 1, 8-й дни Повторение цикла через 21 дней.
МVAC интенсивный
Метотрексат 30мг/м2 в/в в 1, 15, 22-й дни Винбластин 3мг/м2 в/в в 1, 15, 22-й дни. Доксорубицин 30мг/м2 в/в во 2-й день.
Цисплатин 70мг/м2 в/в капельно во 2-й день Повторение цикла через 28 дней.
HD-МVAC/МVAC интенсивный
Метотрексат 30мг/м2 в/в в 1-й день .
Винбластин 3мг/м2 в/в во 2-й день.
Доксорубицин 30мг/м2 в/в во 2-й день.
Цисплатин 70мг/м2 в/в капельно во 2-й день Повторение цикла через 14 дней.
*Поддержка Г-КСФ 5мкг/кг с 1-го по 10-й дни.
CMV
Цисплатин 100мг/м2 в/в капельно во 2-й день.
Метотрексат 30мг/м2 в/в в 1-й и 8-й дни.
Винбластин 4мг/м2 в/в в 1-й и 8-й дни.
М-CAVI
При невозможности назначения цисплатина следующие схемы (УД-В): GemCarbo
Гемцитабин 1000мг/м2 в/в капельно в 1, 8-й дни.
Карбоплатин AUC-5 в/в капельно в 1-й день.
М-CAVI
Метотрексат 30мг/м2 в/в в 1, 15, 22-й дни .
Винбластин 3мг/м2 в/в в 1, 15, 22-й дни.
Карбоплатин AUC-4,5 в/в капельно во 1-й день .
Повторение цикла через 28 дней.
Химиотерапия при редких гистологических формах РМП (плоскоклеточная карцинома, аденокарцинома, мелкоклеточная карцинома) (УД-В): [14]
Предпочтительно для плоскоклеточного РМП назначаются:
PF 5-фторурацил 1000мг/м2 в/в 96-часовая инфузия, 1-4 дни
Цисплатин 100мг/м2 в/в, 1 день.
Интервал 21-28 дней.
Доцетаксел 75мг/м2, в/в, кап 1 день
ЕС Этопозид 100мг/м2 1-3 дни
Паклитаксел 175мг/м2 в/в 1-й день.
Цисплатин 75мг/м2, в/в, 1-й день Интервал 21 день
Доцетаксел 75мг/м2, в/в, кап 1 день
Цисплатин 75 мг/м2, в/в, кап1 день. Интервал 21 день
ITP Паклитаксел 200мг/м2 3-часовая в/в инфузия 1-й день.
Цисплатин 75мг/м2, в/в 1-й день
Ифосфамид 1500мг/м2 в/в 1-3 дни
Интервал 21 день
Предпочтительно для аденокарциномы РМП назначаются:
FOLFOX-4
Оксалиплатин 85мг/м2 в/в в 250-500мл 5% раствор глюкозы – инфузия 2ч день 1, Кальция фолинат 200 мг/м2 в/в инфузия 2ч 1-2 дни
5-фтоурацил 400 мг/м2 в/в струйно 1-2 дни
5-фтоурацил 600 мг/м2 в/в 22 часовая инфузия 1-2 дни
Курсы повторят каждые 14 дней
Предпочтительно для мелкоклеточного РМП назначаются:
FOLFOX-6
Оксалиплатин 100мг/м2 в/в в 250-500мл 5% раствор глюкозы – инфузия 2ч день 1, Кальция фолинат 400 мг/м2 в/в инфузия 2ч 1 день
5-фтоурацил 400 мг/м2 в/в струйно 1 день
5-фтоурацил 2400 мг/м2 в/в 1 день – 46 часовая
Курсы повторят каждые 14 дней
Предпочтительно для мелкоклеточного РМП назначаются:
EP Этопозид 100мг/м2 1-3 дни
Цисплатин 80-100мг/м2, в/в 1-й день
Интервал 21 день
ЕС Этопозид 100мг/м2 1-3 дни
Карбоплатин AUC 5-6 в/в 1-й день
Интервал 21 день
Пре и после оперативная ХТ (неоадьювантная [предпочитительна для рака мочевого пузыря] или адьювантная
Первая линия системной терапии местнораспространенного или метастатического рака мочевого пузыря (Стадия IV) (Категория 2А, если не указано иное)
Вторая линия терапии местнораспространенного или метастатического рака мочевого пузыря (Стадия IV) (После терапиии препаратами платины)а,b (Категория 2А, если не указано иное)
Принципы системной терапии метастатического РМП [15]
Пре и после оперативная ХТ (неоадьювантная [предпочитительна для рака мочевого пузыря] или адьювантная
|
Предпочтительные режимы
DDMVAC (дозированный метотрексат, винбластин, доксорубицин, и цисплатин) с поддержкой факторов роста для 3-4 циклов
Гемцитабин и цисплатин 4 цикла |
|
Альтернативные режимы
CMV (Цисплатин, метотрексат, и Винбластин) 3 цикла
|
Первая линия системной терапии местнораспространенного или метастатического рака мочевого пузыря (Стадия IV) (Категория 2А, если не указано иное)
|
Характеристики пациентов
|
Рекомендации по лечению |
|
Подходящие для лечения Цисплатином
|
Предпочтительные режимы
Гемцитабин и цисплатин [I, A] [Категория 1] с последующей поддерживающей терапией авелумабом для опухолей, которые не прогрессировали на платиносодержащей ХТ [I, A]
DDMVAC с поддержкой факторов роста [Категория 1] с последующей поддерживающей терапией авелумабом для опухолей, которые не прогрессировали на платиносодержащей ХТ [Категория 1] |
| Неподходящие для лечения Цисплатином |
Предпочтительные режимы
Гемцитабин и карбоплатин с последующей поддерживающей терапией авелумабом
Атезолизумаб (только для пациентов с PD-L1 позитивными опухолями, которые не подходят для лечения любым платиносодержащим препаратом независимо от экспрессиии PD-L1)
Пембролизумаб (только для пациентов с PD-L1 позитивными опухолями, которые не подходят для лечения любым платиносодержащим препаратом независимо от экспрессиии PD-L1)
Альтернативные режимы
Гемцитабин
Гемцитабин и паклитаксел
У отдельных пациентов
Ифосфамид, доксорубицин и гемцитабин (для пациентов с хорошей функцией почек и хорошим физическим статусом)
|
Вторая линия терапии местнораспространенного или метастатического рака мочевого пузыря (Стадия IV) (После терапиии препаратами платины)а,b (Категория 2А, если не указано иное)
|
Предпочтительные режимы
Пембролизумаб (Категория 1)
|
Другие рекомендуемые режимы
Паклитаксел или доцетаксел
Гемцитабин
|
|
Альтернативные режимы
Иммуноонкологические препараты: Авелумаб
Ниволумаб*
Энфортумаб ведотин
Эрдафитиниб* c-(Только для пациентов, с мутациями генов FGFR3 или FGFR2)
|
У отдельных пациентов
Ифосфамид, доксорубицин, и гемцитабин
Гемцитабин и цисплатин
Гемцитабин и паклитаксел
|
*В соответствии с правилами применения незарегистрированных ЛС.
a Если ВБП>12 мес после лечения препаратами платины (например, Цисплатин или Карбоплатин, рассмотрите продолжение лечения препаратами платины, если пациент подходит для леченния)
b Также для лечения пациентов, кто в первой линии получал лечение препаратами не на основе платины или ингибиторы иммунных контрольных точек
c Эрдафитиниб* рекомендован во 2 линии в качестве альтернативной предпочтительной схемы для пациентов с местно-распространенным или метастатическим раком мочевого пузыря (категория 2 А) после платин-содержащей химиотерапии или иммунотерапии, имеющих FGFR3/FGFR2 генетические изменения [16].
Вторая линия терапии местнораспространенного или метастатического рака мочевого пузыря (Стадия IV) (После терапиии ингибиторами иммунных контрольных точек)
Последующие линии терапии местнораспространенного или метастатического рака мочевого пузыря (Стадия IV)
Химиотерапия второй линии [12; 15]
Вторая линия терапии местнораспространенного или метастатического рака мочевого пузыря (Стадия IV) (После терапиии ингибиторами иммунных контрольных точек)
|
Предпочтительные режимы
Энфортумаб ведотин
Гемцитабин/ Карбоплатин
|
Другие рекомендуемые режимы
Паклитаксел или доксатаксел
Гемцитабин
|
|
Предпочтительные режимы для подходящих для лечения препаратами платины и ранее не получавших ХТ
Гемцитабин и Цисплатин
DDMVAC с поддержкой факторов роста
|
У отдельных пациентов
Ифосфамид, доксорубицин, и гемцитабин
Гемцитабин и паклитаксел
|
Последующие линии терапии местнораспространенного или метастатического рака мочевого пузыря (Стадия IV)
|
Предпочтительные режимы
Энфортумаб ведотин (Категория 1)
Эрдафитиниб* a (Только для пациентов, с мутациями генов FGFR3 или FGFR2)
|
Другие рекомендуемые режимы
Паклитаксел или доксатаксел
Гемцитабин
Ифосфамид, доксорубицин, и гемцитабин
Гемцитабин и паклитаксел
Гемцитабин и цисплатин
|
*В соответствии с правилами применения ЛС незарегистрированных на территории РК.
a Эрдафитиниб* рекомендуется применять у пациентов с генетическими изменениями FGFR резистентных к платине опухолях или прогрессии на иммунотерапии или химиотерапии у пациентов с рецидивом распространенного/ метастатического уротелиального рака [1].
Химиотерапия второй линии [12; 15]
При клиренсе креатина менее 50-60 мл/мин или при прогрессировании заболевания менее чем через 6-12 месяцев после ХТ 1-й линии рекомендовано:
Винфлунин* - 320 мг/м2 в/в капельно раз в 21 день. В случае повышенного риска развития побочных явлений (клиренс креатинина менее 40-60 мл/мин, возраст старше 75 лет, состояние после ЛТ) следует начать с дозы 280 мг/м2.
*В соответствии с правилами применения незарегистрированных ЛС.
Рекомендовано применение карбоплатин-содержащей комбинации препаратов в качестве терапии первой линии только у пациентов, не подходящих для лечения цисплатином.
Рекомендовано поддерживающая монотерапия первой линии – Авелумаб у пациентов с местно-распространенной или метастатической уротелиальной карциномой (УК), без прогрессирования после химиотерапии на основе препаратов платины.
Рекомендовано назначение иммуноонкологических препаратов – пембролизумаб при невозможности проведения первой линии ХТ с включением цисплатина.
Химиотерапия при метастатическом РМП:
Рекомендовано применение цисплатин-содержащей комбинации препаратов в качестве терапии первой линии (при отсутствии противопоказаний).
Рекомендовано применение карбоплатин-содержащей комбинации препаратов в качестве терапии первой линии только у пациентов, не подходящих для лечения цисплатином.
Рекомендовано поддерживающая монотерапия первой линии – Авелумаб у пациентов с местно-распространенной или метастатической уротелиальной карциномой (УК), без прогрессирования после химиотерапии на основе препаратов платины.
Рекомендовано назначение иммуноонкологических препаратов – пембролизумаб при невозможности проведения первой линии ХТ с включением цисплатина.
Рекомендовано назначение препарата пембролизумаб при прогрессировании заболевания после первой линии ХТ.
Лечение пациентов с местнораспространённым или метастатическим уротелиальным раком, получавших ранее лечение PD-1/L1 ингибитором и химиотерапию на основе препаратов платины в неоадъювантном/адъювантном режиме, при местно-распространённом или метастатическом процессе проводится препаратом энфортумаб ведотин*. Рекомендуемая доза составляет 1,25 мг/кг (максимум до 125 мг для пациентов ≥100 кг), вводимая в виде внутривенной инфузии в течение 30 минут в дни 1, 8 и 15 28-дневного цикла до прогрессирования заболевания или неприемлемой токсичности.
Иммунотерапия:
Пембролизумаб – 200 мг в виде в/в инфузии в течение 30 минут каждые 3 недели (УД-А).
Авелумаб 10 мг / кг в / в в 1-й день каждые 2 нед.
Лечение пациентов с местнораспространённым или метастатическим уротелиальным раком, получавших ранее лечение PD-1/L1 ингибитором и химиотерапию на основе препаратов платины в неоадъювантном/адъювантном режиме, при местно-распространённом или метастатическом процессе проводится препаратом энфортумаб ведотин*. Рекомендуемая доза составляет 1,25 мг/кг (максимум до 125 мг для пациентов ≥100 кг), вводимая в виде внутривенной инфузии в течение 30 минут в дни 1, 8 и 15 28-дневного цикла до прогрессирования заболевания или неприемлемой токсичности.
Рекомендации:
Вторая линия ХТ
Энфортумаб ведотин показан пациентам с метастатическим раком мочевого пузыря с противопоказаниями к назначению платиносодержащей химиотерапии, имеющих прогрессирование заболевания во время или после лечения ингибитором PD-1 или PD-L1 в 1-й линии
Уровень доказательности 2А, степень рекомендаций А (сильная)
Эрдафитиниб* рекомендован во 2 линии в качестве альтернативной предпочтительной схемы для пациентов с местно-распространенным или метастатическим раком мочевого пузыря (категория 2 А) после платин-содержащей химиотерапии или иммунотерапии, имеющих FGFR3/FGFR2 генетические изменения
Эрдафитиниб* рекомендован во 2 линии в качестве альтернативной предпочтительной схемы для пациентов с местно-распространенным или метастатическим раком мочевого пузыря (категория 2 А) после платин-содержащей химиотерапии или иммунотерапии, имеющих FGFR3/FGFR2 генетические изменения
Третья линия ХТ
Энфортумаб ведотин показан пациентам с метастатическим раком мочевого пузыря, ранее получавших платиносодержащую химиотерапию и имеющих прогрессирование заболевания во время или после лечения ингибитором PD-1 или PD-L1
Уровень доказательности 1b, степень рекомендаций А (сильная)
Эрдафитиниб *рекомендуется применять у пациентов с генетическими изменениями FGFR резистентных к платине опухолях или прогрессии на иммунотерапии или химиотерапии у пациентов с рецидивом распространенного/ метастатического уротелиального рака.
При костных метастазах обосновано применение: [4]
Памидроновая кислота 90мг в/в 4-часовой инфузия 1 раз в 3-4 недели для снижения риска развития костных осложнений.
Золедроновая кислота в/в капельно в течение 15 минут 4 мг 1 раз в 3-4 недели для снижения риска развития костных осложнений. У пациентов с остеопорозом может быть назначена 1 инъекция 1 раз в три месяца.
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
Перечень дополнительных лекарственных средств (менее 100% вероятности применения):
*В соответствии с правилами применения незарегистрированных ЛС на территории РК.
Показания для экстренных операций или манипуляций:
Показания для плановых операций:
Противопоказания к оперативному лечению:
Лечение поверхностного рака мочевого пузыря (стадии Тis, Ta и T1)
При нарушении оттока мочи из верхних мочевых путей применяется:
Абляция фокусированным ультразвуком:
Абляция фокусированным ультразвуком (далее – ФУЗ) – при фокусированном ультразвуковом лечении не используется ионизирующее излучение. Лечение может быть дополнением к медикаментозной терапии, позволяя улучшить доставку лекарственных агентов к клеткам опухоли. Метод может быть использован при метастазах рака мочевого пузыря в кости.
Абляция фокусированным ультразвуком (далее – ФУЗ) – при фокусированном ультразвуковом лечении не используется ионизирующее излучение. Лечение может быть дополнением к медикаментозной терапии, позволяя улучшить доставку лекарственных агентов к клеткам опухоли. Метод может быть использован при метастазах рака мочевого пузыря в кости.
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
|
Фармакотерапевтическая группа
|
МНН лекарственного средства | Способ применения | Уровень доказательности |
| Алкилирующие агенты – комплексные соединения платины | Цисплатин | 75 мг/м2 1-й день, в/в | А |
| Карбоплатин | АUC 5-6 1-й день, в/в | С | |
| Препараты растительного и природного происхождения | Паклитаксел | 175 мг/м2 1-й день, в/в; | С |
| Микротрубочковые ингибиторы – таксаны | 80мг/м2 в/в капельно в 1, 8-й дни | ||
| Доцетаксел | 75мг/м2, в/в, кап 1 день | С | |
| Противоопухолевые антибиотики – антрациклины | Доксорубицин | 30мг/м2 в/в во 2-й день | С |
| Прочие противоопухолевые антибиотики | Митомицин С | внутрипузырно, по 20-60 мг 1 раз в неделю в течение 6-8 недель. | А |
| Антиметоболиты – аналоги цитидина | Гемцитабин | 1000 мг/м2 1-й, 8-й и 15-й день, в/в | А |
| Антиметоболиты – антифолаты | Метотрексат |
30мг/м2 в/в в 1, 15, 22-й дни;
30мг/м2 в/в в 1-й и 8-й дни;
30мг/м2 в/в в 1-й
|
В |
|
Винкоалакалоиды
|
Винбластин |
3мг/м2 в/в в 1, 15, 22-й дни;
3мг/м2 в/в во 2-й дни
|
В |
Перечень дополнительных лекарственных средств (менее 100% вероятности применения):
|
Фармакотерапевтическая группа
|
МНН лекарственного средства | Способ применения | Уровень доказательности |
|
Ингибиторы топоизомеразы 11
|
Этопозид | 100мг/м2 1-3 дни | С |
|
Комплексные соединения платины
|
Оксалиплатин | 85-100 мг/м2 в/в | С |
|
Фторпиримидины
|
5-фторурацил |
РF: 1000мг/м2 в/в 96-часовая инфузия, 1-4 дни;
OLFOX-4;
5-фтоурацил 400 мг/м2 в/в струйно 1-2 дни;
5-фтоурацил 600 мг/м2 в/в 22 часовая инфузия 1-2 дни
FOLFOX-6:
5-фтоурацил 400 мг/м2 в/в струйно 1 день;
5-фтоурацил 2400 мг/м2 в/в 1 день – 46 часовая
|
С |
| Антидот антагонистов фолиевой кислоты, модификатор биологического действия фторурацила | Кальция фолинат |
200 мг/м2 в/в инфузия 2ч 1-2 дни;
400 мг/м2 в/в инфузия 2ч 1 день
|
С |
| Алкилирующие агенты – хлорэтиламины | Ифосфамид | 1500мг/м2 в/в 1-3 дни | С |
| Моноклональное антитело, PD-L1 ингибитор | Авелумаб | 10 мг / кг в / в в 1-й день каждые 2 нед | А |
| Атезолизумаб | Внутривенно, медленно, по 1200 мг в течение 60 минут каждые 3 недели | В | |
| Моноклональное антитело, PD1 ингибитор | Пембролизумаб | 200 мг в виде в/в инфузии в течение 30 минут каждые 3 недели | А |
| Конъюгат моноклонального антитела и химиопрепарата | Энфортумаб ведотин | 1,25 мг/кг (максимум до 125 мг для пациентов ≥100 кг), в/в в течение 30 минут в дни 1, 8 и 15 каждого 28-дневного цикла | А |
| Ингибитор тирозинкиназы пан-FGFR | Эрдафитиниб* | Таб 4мг х 2 в сутки (8мг внутрь ежедневно с возможностью эскалации дозы до 9 мг) | В |
| Алкалоиды растительного происхождения | Винфлунин | 320 мг/м2 в/в капельно раз в 21 день | С |
| Ингибиторы костной резорбции | Памидроновая кислота | 90мг в/в 3-часовая инфузия 1 раз в 3-4 недели | С |
| Золедроновая кислота | 4 мг в/в капельно в течение 15 минут, 1 раз в 3-4 недели | С |
Хирургическое вмешательство [1,2,4]:
Показания для экстренных операций или манипуляций:
- Угрожающее жизни кровотечение из опухоли мочевого пузыря;
- Тампонада мочевого пузыря;
- Вторичный уретерогидронефроз с развитием постренальной олиго-анурии, пионефроз;
- Острая задержка мочи;
Показания для плановых операций:
- Морфологически верифицированная злокачественная опухоль мочевого пузыря.
- Опухоль мочевого пузыря, требующая морфологической верификации и стадирования.
Противопоказания к оперативному лечению:
- Тяжелые сопутствующие заболевания;
- Терминальная стадия ХПН;
- Глубокая анемия;
- Общие противопоказания к оперативному лечению;
Лечение поверхностного рака мочевого пузыря (стадии Тis, Ta и T1)
- Для Ta низкого риска после ТУРМП, рекомендуется наблюдение и возможность рассмотрения введения единственной дозы немедленной внутрипузырной химиотерапии в течение 24 часов после резекции. Немедленная внутрипузырная химиотерапия может сопровождаться 6-недельным индукционным курсом внутрипузырной химиотерапии. Иммунотерапия не рекомендуется этим пациентам из-за низкого риска прогрессирования заболевания.
- После ТУРМП пациенты с Ta высокого риска, полноценные опухоли могут лечиться внутрипузырным БЦЖ (предпочтительно), внутрипузырной химиотерапией или наблюдением.
- Для cT1ТУРМП Эти опухоли обрабатывают полной эндоскопической резекцией. У пациентов с высоким риском заболевания, особенно если полная резекция неясна из-за размера опухоли и ее расположения, отсутствие мышц в образце, наличие лимфоваскулярной инвазии или неадекватная постановка, настоятельно рекомендуется повторить ТУРМП. Если обнаружено остаточное заболевание cT1, лечение должно состоять из БЦЖ (категория 1) или цистэктомии.
- Если после второй резекции не обнаружено остаточного заболевания, рекомендуется внутрипузырная терапия БЦЖ (предпочтительная категория 1) или внутрипузырная химиотерапия.
- Для Tis Стандартная терапия для этого поражения - это резекция с последующей внутрипузырной терапией с БЦЖ. Если пациент неспособен переносить БЦЖ, можно рассмотреть возможность внутрипузырной химиотерапии, но данные, поддерживающие этот подход, ограничены.
ТУР - трансуретральная резекция
Показания:
- кровь в моче;
- учащенное либо затрудненное мочеиспускание;
- повторяющиеся симптомы цистита – рези в животе, частые позывы к мочеиспусканию, чувство неполного опорожнения мочевого пузыря. Противопоказания: - Относительное – устранимое – противопоказание – инфекции мочевыделительного тракта (операцию делают после устранения возбудителя).
Лечение больных мышечно-инвазивным раком мочевого пузыря, (стадии Т2– Т4):
- Стадирование (лечебно-диагностический ТУР, МРТ малого таза).
- Операция – радикальная цистэктомия (стандарт) (открытая, лапароскопическая, роботассистированная).
- Полихимиотерапия – проводится в неоадъювантном и/или адъювантном режимах (при pN+). Самостоятельная химиотерапия носит паллиативный характер.
- Дистанционная лучевая терапия – не относится к стандартному виду лечения, проводится при отказе больного от органоуносящей операции в самостоятельном варианте или в сочетании с химиотерапиией.Не проводится в виде неоадъювантного лечения. Может использоваться в качестве компонента мультимодальной терапии при органосохранном лечении.
- Трехкомпонентная (мультимодальная) терапия, включающая операцию (ТУР либо резекция мочевого пузыря), 2-4 курса ПХТ по схеме GC илиMVAC, и лучевую терапию. Используется у отобранной группы пациентов (T2N0M0) –может использоваться в качестве альтернативного лечения у информированных больных.
Показания к резекции мочевого пузыря:
Хирургическое лечение:
При инвазивном раке мочевого пузыря применяются органосохраняющие (ТУР при Т2а и резекция мочевого пузыря) и органоуносящие (радикальная цистэктомия) операции. ТУР может также использоваться в качестве паллиативного метода остановки кровотечения при поздних стадиях РМП.
Резекция мочевого пузыря. Резекция мочевого пузыря не является радикальной операцией и должна выполняться только при наличии противопоказаний к радикальной цистэктомии или при отказе больного от нее.
Показания к резекции мочевого пузыря:
одиночная инвазивная опухоль в пределах мышечной стенки мочевого пузыря, рак низкой степени злокачественности (LG или G2), первичная (не рецидивная) опухоль, расстояние от опухоли до шейки мочевого пузыря не менее 2см, отсутствие дисплазии и рака insitu при биопсии свободной от опухоли слизистой мочевого пузыря. Операция сочетается с обязательной тазовой лимфодиссекцией. Если при гистологическом исследовании в краях резекционной раны выявляются опухолевые клетки (R1), выполняется радикальная цистэктомия. При вовлечении в процесс устья мочеточника после резекции мочевого пузыря и удаления опухоли производится уретеронеоцистоанастомоз.
Показаниями к цистэктомии с созданием ортотопического мочевого пузыря являются [2-5], (УД – А):
Стандартной операцией при инвазивном раке мочевого пузыря является
радикальная цистэктомия.
Показаниями к цистэктомии с созданием ортотопического мочевого пузыря являются [2-5], (УД – А):
- возможность выполнения радикальной цистэктомии;
- нормальная функция почек (креатинин < 150 ммоль/л);
- отсутствие метастазов (N0M0);
- отрицательный результат биопсии простатического отдела уретры.
- Из методик операции наибольшее распространение получили методики Штудера (U.Studer), Хаутманна (E. Hautmann).
Показаниями являются:
Паллиативные операции у больных раком мочевого пузыря:
Показаниями являются:
1) угрожающие жизни кровотечения из опухоли мочевого пузыря;
2) острая задержка мочи;
3) нарушение оттока мочи из верхних мочевых путей и развитие почечной недостаточности, острый обструктивный пиелонефрит;
4) сопутствующие заболевания (заболевания сердечно-сосудистой системы, эндокринные нарушения и др.)
С целью остановки кровотечения применяют:
1) ТУР опухоли с остановкой кровотечения;
2) перевязка или эмболизация внутренних подвздошных артерий;
3) остановка кровотечения на открытом мочевом пузыре;
4) паллиативная цистэктомия.
При нарушении оттока мочи из верхних мочевых путей применяется:
1) чрескожная пункционная нефростомия;
2) открытая нефростомия;
3) уретерокутанеостомия;
4) надпузырное отведение мочи в изолированный сегмент тонкой кишки (операция Брикера и т.д.),
5) эпицистостомия.
Показания к лучевой терапии:
Противопоказания к лучевой терапии:
Лучевая терапия
Применение лучевой терапии как самостоятельного метода лечения у больных РМП не рекомендуется
Показания к лучевой терапии:
1) морфологически установленный диагноз злокачественного новообразования с инвазией в мышечный слой мочевого пузыря;
2) При отказе пациента от радикального удаления мочевого пузыря в плане мультимодального лечения после выполнения ТУР и 2-4 курсов ПХТ;
3) при рецидивах, продолженном росте опухоли или прогрессирование заболевания после ранее проведенного комбинированного или комплексного лечения.
Противопоказания к лучевой терапии:
1) декомпенсированное общее состояние по сопутствующей соматической патологии (сердечно сосудистая, дыхательная, мочеполовая, пищеварительная и т.п.);
2) общесоматическое инкурабельное состояние больного вызванное онкологическим процессом;
3) микроцистис, сморщенный мочевой пузырь (объем менее 100 мл);
4) предшествующее облучение таза, наличие остаточной мочи более 70 мл;
5) камни мочевого пузыря;
6) обострение цистита и пиелонефрита.
Способы лучевой терапии:
1) 1-мерная лучевая терапия (1DRT);
2) 2-х мерная конвенциальная (стандартная) лучевая терапия (2D RT);
3) 3-х мерная конформная лучевая терапия (3D CRT);
4) интенсивно-модулированная лучевая терапия (IMRT);
5) лучевая терапия, управляемая по изображениям (IGRT);
6) лучевая терапия, синхронизированная с дыханием (4DRT);
7) стереотаксическая радиохирургия (SRS);
8) стереотаксическая радиотерапия (SRT);
9) интраоперационная лучевая терапия (IORT);
10) брахитерапия (внутриполостная, внутритканевая), высокодозная, пульс-дозная брахитерапия.
Лучевая терапия (частный раздел)
При топометрии, планирование и при лечение пациентов проводится при пустом пузыре, что предпочтительно для ежедневной воспроизводимости.
Использование многопольного облучения на высокоэнергетические линейные ускорители. По возможности использовать ежедневное IGRT.
Одновременная химиолучевая терапия или лучевая терапия наиболее успешны для пациентов без гидронефроза и без обширной карциномы in situ, связанной с их опухолью, поражающей мышцы.
Пациенты со стадией Ta, T1 или Tis.
ДЛТ применяется только в случае неоднократно рецидивирующего заболевания Ta- T1, обычно после БЦЖ-терапии, но без обширных Tis, которые не являются кандидатами на цистэктомию, одновременная химиолучевая терапия может рассматриваться как потенциально лечебная альтернатива радикальной цистэктомии, которая является стандартным лечением.
Облучение всего мочевого пузыря с облучением лимфоузлов малого таза дозой 39,6-50,4 Гр с использованием обычного или ускоренного гиперфракционирования. Факультативное лечение на лимфатические узлы необязательно и должно учитывать сопутствующие заболевания пациента и риски токсичности для критических структур. Затем дополнительное воздействие на мочевой пузырь до общей СОД 60- 66 Гр. Для альтернативы традиционному фракционированию включают взятие всего мочевого пузыря до 55 Гр в 20 фракциях или использование интегрированного повышения дозы на участках расположения опухоли.
Одновременная химиолучевая терапия рекомендуется для дополнительного цитотоксичного воздействия на опухоль и может быть дана без существенной повышенной токсичности по сравнению с самостоятельной лучевой терапией. Одновременное применение 5-ФУ и митомицин С могут использоваться вместо цисплатина у пациентов с низкой или умеренной почечной функцией.
Неоперабельные метастатические заболевания
Одновременная химиолучевая терапия или лучевая терапия следует рассматривать как потенциально лечебную терапию для пациентов с неоперабельным метастатическим заболеванием. При назначении паллиативного излучения для метастатического рака мочевого пузыря или рецидивирующей опухоли таза следует учитывать сочетание излучения с радиочувствительной химиотерапией. Химиотерапия не должна использоваться одновременно с паллиативным излучением высокой дозы (> 3 Гр на фракцию).
Клинический объем лечения (СTV) должен включать весь мочевой пузырь с и все участки возможного распространения болезни в том числе региональные лимфатические узлы. Региональные лимфатические узлы включают обтураторные, внутренние и внешние подвздошные, перивизические, сакральные, пресакральные, подбиффуркационные узлы. Для участвующих узловых заболеваний общие подвздошные узлы являются участком вторичного поражения.
Для пациентов с pT3 / pT4 pN0- (чистый уротелиальный или первичный уротелий, смешанный с другими подтипами) рак мочевого пузыря после радикальной цистэктомии с выведением кишечного кондуита, возможность послеоперационной адъювантной тазовой лучевой терапии. Клинический объем лечения (СTV) должен включить остаточную микроскопическую болезнь, основанные на патологических результатах при операции, и может включать в себя ложе мочевого пузыря до СОД 54-60 Гр и тазовые лимфатические узлы до СОД 40 - 50,4 Гр.
Оценка состояния опухоли после завершения полной доза первичной химиолучевой терапии: через 2 - 3 месяца визуализация с помощью КТ грудной клетки / живота / таза с контраст - сканирование кости. Цистоскопическое наблюдение и биопсия также рекомендуются в качестве последующих после завершения полной дозы химиолучевой терапии.
В отобранных случаях с опухолью категории T4b может рассматриваться как метод выбора интраоперационная лучевая терапия.
Лучевая терапия в плане мультимодального лечения (сохранение органа) cT2 cN0.
ДЛТ СОД 66 до 70 Гр. Клинический объем лечения (СTV) должен включать области потенциального микроскопического распространения.
Возможна профилактическая лучевая терапия регионально-узловых бассейнов (паховые и нижние тазовые узлы для женских и дистальных мужских опухолей, тазовые лимфатические узлы для проксимальных мужских опухолей).
cT3-T4 или положительный лимфатический узел
Клинический объем лечения (СTV) должен включать области микроскопического распространения и регионарно-узловые бассейны (паховые и нижние тазовые узлы для женских и дистальных мужских опухолей, тазовые лимфатические узлы для ближних мужских опухолей). Повысить дозу на мочевой пузырь до 62-70 Гр и объемного узлового заболевания до 50-66 Гр, если это возможно. Доза, доставляемая к увеличенному объемному образованию, может быть ограничена в зависимости от ограничения толерантности тканей. Одновременную химиотерапию следует вводить для дополнительной цитотоксичности опухоли.
Рецидивирующее заболевание
Постоперационная адъювантная лучевая терапия
Поле лечения должно охватывать районы, подверженные риску сохранения остаточного микроскопического заболевания на основе патологических результатов при резекции, и может включать в себя резецирующий ложе, паховые лимфатические узлы и узлы тазовых лимфатических узлов. Районы, подверженные риску заражения остаточной микроскопической болезнью, должны получать от 45 до 50,4 Гр. EBRT. Принятые границы резекции и области экстранодального расширения должны быть увеличены до 54-60 Гр, если это возможно, исходя из нормальных ограничений ткани. Области валового остаточного заболевания должны быть увеличены до 66-70 Гр, если это возможно, исходя из нормальных ограничений ткани. Для дополнительной цитотоксичности опухоли следует учитывать одновременную химиотерапию с режимами, используемыми для лечения рака мочевого пузыря.
Рецидивирующее заболевание
Клинический объем мишени (CTV) должен включать распространение опухоли в подозрительных областях при 66-74 Гр (более высокая доза до 74 Гр для более крупной опухоли и неврологическая гистология), и рассмотрение может быть дано выборным регионально-узловым бассейнам (45-50,4 Гр), как обсуждалось выше, если это возможно на основе нормальных тканевых ограничений.
Лучевая терапия при метастазах в головной мозг.
Тотальное облучение головного мозга до С1 шейного позвонка:
1) РОД 2,0 Гр 5 фракций в неделю СОД 30-40 Гр;
2) РОД 2,5 Гр 5 фракций в неделю СОД 30-35 Гр;
3) РОД 3,0 Гр 5 фракций в неделю СОД 30-33 Гр;
4) РОД 4,0 Гр 5 фракций СОД 20 Гр.
Локальное облучение головного мозга
1) стереотаксическая радиохирургия (SRS) - РОД 10,0 – 30,0 Гр 1 фракция при размерах метастаза не более 3 см в диаметре;
2) стереотаксическая радиотерапия (SRT) – РОД 6,0-10,0 Гр 3-5 фракций при размерах метастаза от 3,0 до 6,0 см;
3) локальное облучение метастазов РОД 2,0-3,0 до СОД 20-60 Гр.
Лучевая терапия при метастазах в кости скелета.
1) РОД 2,0 Гр 5 фракций в неделю СОД 40-50 Гр;
2) РОД 2,5 Гр 5 фракций в неделю СОД 30-50 Гр;
3) РОД 3,0 Гр 5 фракций в неделю СОД 30-45 Гр;
4) РОД 4,0 Гр 3-5 фракций в неделю СОД 20-40 Гр;
5) РОД 8,0 Гр 1-3 фракции.
Схема лечения больных раком мочевого пузыря с отдаленными метастазами:
1) Стадирование;
2) Операция (индивидуализированно):
3) могут выполняться различные виды паллиативных операций с целью отведения мочи;
4) эндоскопические операции с целью остановки кровотечения;
5) при угрожающем жизни кровотечении может выполняться паллиативная цистэктомия, а при тяжелом состоянии эмболизация/перевязка внутренних подвздошных артерий.
Дальнейшее ведение [2] (см. приложение 2):
Объем наблюдений:
Цистоскопия с биопсией (после органосохраняющих операций), пальцевое исследование прямой кишки.
Рентгенография органов грудной клетки
Лабораторные исследования:
Сроки наблюдения:
По показаниям выполняются:
Рентгеновская компьютерная или магнитная резонансная томография;
Остеосцинтиграфия и рентгенография конкретных областей скелета при подозрении на метастатическое поражение.
УЗИ органов брюшной полости, забрюшинного пространства и малого таза;
Лабораторные исследования:
Общий анализ крови
Общий анализ мочи
Цитологическое исследование осадка мочи
Определение кислотно-щелочного равновесия после цистэктомии;
Сроки наблюдения:
Первый год – 1 раз в 3мес.;
Второй год – 1 раз в 6мес.;
В последующем, пожизненно – 1 раз в год.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе:
«ответ опухоли» - регрессия опухоли после проведенного лечения;
Полный эффект – исчезновение всех очагов поражения на срок не менее 4х недель.
Частичный эффект – большее или равное 50% уменьшение всех или отдельных опухолей при отсутствии прогрессирования других очагов.
Стабилизация – (без изменений) уменьшение менее чем на 50% или увеличение менее чем на 25% при отсутствии новых очагов поражения.
Прогрессирование – увеличение размеров одной или более опухолей более 25% либо появление новых очагов поражения[7] (УД – А).
безрецидивная выживаемость (трех и пятилетняя);
«качество жизни» включает кроме психологического, эмоционального и социального функционирования человека, физическое состояние организма больного.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
1) Наличие опухолевого процесса в мочевом пузыре верифицированного гистологически или/и цитологически;
2) Операбельный рак мочевого пузыря (I-IV стадии);
Показания для экстренной госпитализации:
3) Наличие опухолевого процесса в мочевом пузыре, требующее дополнительных инвазивных методов диагностики (лечебно-диагностическая ТУР).
Показания для экстренной госпитализации:
1) Выраженная, угрожающая макрогематурия, тампонада мочевого пузыря;
2) Острая задержка мочи.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- 1. Клинические рекомендации ESMO (утверждено группой по подготовке рекомендаций ESMO, август 2014 года). 2. «Клиническая онкоурология» под редакцией Б.П. Матвеева (Москва, 2018 год). Руководство по раку мочевого пузыря ЕАУ (Европейской Ассоциации Урологов), 2018 год. 3. Журнал Онкоурология 2015г - 2018г, Ежеквартальный научно-практический журнал. 4. Клинические рекомендации Европейской ассоциации урологов 2021 гг. 5. IARC, Cancer Today. Estimated number of new cases in 2020, worldwide, both sexes, all ages. 2021 [access date March 2021]. https://gco.iarc.fr/today/online-analysis-table 6. Burger, M., et al. Epidemiology and risk factors of urothelial bladder cancer. Eur Urol, 2013. 63: 234.https://pubmed.ncbi.nlm.nih.gov/22877502 7. Comperat, E., et al. Clinicopathological characteristics of urothelial bladder cancer in patients less than 40 years old. Virchows Arch, 2015. 466: 589. https://pubmed.ncbi.nlm.nih.gov/25697540 8. Veskimae, E., et al. What Is the Prognostic and Clinical Importance of Urothelial and Nonurothelial Histological Variants of Bladder Cancer in Predicting Oncological Outcomes in Patients with Muscle-invasive and Metastatic Bladder Cancer? A European Association of Urology Muscle Invasive and Metastatic Bladder Cancer Guidelines Panel Systematic Review. Eur Urol Oncol, 2019. 2: 625. https://pubmed.ncbi.nlm.nih.gov/31601522 9. Choi, W., et al. Identification of distinct basal and luminal subtypes of muscle-invasive bladder cancer with different sensitivities to frontline chemotherapy. Cancer Cell, 2014. 25: 152. https://pubmed.ncbi.nlm.nih.gov/24525232 10. Richard, P.O., et al. Active Surveillance for Renal Neoplasms with Oncocytic Features is Safe. J Urol, 2016. 195: 581. https://pubmed.ncbi.nlm.nih.gov/26388501 11. Comperat, E.M., et al. Grading of Urothelial Carcinoma and The New “World Health Organisation Classification of Tumours of the Urinary System and Male Genital Organs 2016”. Eur Urol Focus, 2019. 5: 457. https://pubmed.ncbi.nlm.nih.gov/29366854 12. Рупре, М.,и другие., Руководство по уротелиальной клеточной карциноме верхних мочевых путей. В:Руководящие принципы ЕАУ, опубликованные на 38й Ежегодный Конгресс Милан 2023. Офис рекомендаций Европейской ассоциации урологов, Арнем, Нидерланды. https://uroweb.org/guidelines/upper-urinary-tract-urothelial-cell-carcinoma 17 13. Гонтеро, П.,и другие.Рекомендации по немышечно-инвазивному раку мочевого пузыря (Ta, T1 и CIS). В: Руководящие принципы ЕАУ, опубликованные на 38й Ежегодный Конгресс Милан 2023. Офис рекомендаций Европейской ассоциации урологов, Арнем, Нидерланды. https://uroweb.org/guidelines/non-muscle-invasive-bladder-cancer 18 14. Гакис, Г.,и другие.Руководство EAU по первичной карциноме уретры. В:Руководящие принципы ЕАУ, опубликованные на 38йЕжегодный Конгресс Милан 2023. Офис рекомендаций Европейской ассоциации урологов, Арнем, Нидерланды. https://uroweb.org/guidelines/ muscle-invasive-and-metastatic-bladder-cancer. 15. Витжес, Дж. А.,и другие.Рекомендации Европейской ассоциации урологов по мышечно-инвазивному и метастатическому раку мочевого пузыря: Краткое изложение рекомендаций 2020 г. Евро Урол, 2021. 79: 82. 16. NCCN Guidelines Version 3.2023 по раку мочевого пузыря.
Информация
Сокращения, используемые в протоколе:
|
АТР
|
Аллерген туберкулезный рекомбинантный |
| БЦЖ | Бацилла Кальметта — Герена или BacillusCalmette—Guérin, BCG |
| КТ | компьютерная томография |
| МРТ | магнитно-резонансная томография |
|
ЛОР
|
оториноларинголог |
| ЛТИ | латентная туберкулезная инфекция |
| ЖКТ | желудочно-кишечный тракт |
| НПВС | нестероидные противовоспалительные препараты |
| ТРУЗИ | трансректальное ультразвуковое исследование |
| ТУР | трансуретральная резекция |
|
УД
|
уровень доказательности |
| УЗИ | ультразвуковое исследование |
| ЭКГ | электрокардиография |
|
РМ
|
Рак мочевого пузыря |
| LG | low grade (опухоли низкого риска) |
| HG | high grade (опухоли высокого риска) |
|
TNM
|
Tumor, Nodulus, Metastasis - международная классификация стадий
злокачественных новообразований
|
|
PD-L1
|
лиганд к рецептору PD1 иммунных клеток |
| GP | гемцитабин + цисплатин |
|
PРG
|
паклитаксел + цисплатин + гемцитабин |
| МVAC | метотрексат + винблатсин + доксорубицин + цисплатин |
| CMF | цисплатин + метотрексат + винбластин |
|
GemCarbo
|
гемцитабин + карбоплатин |
|
М-CAVI
|
метотрексат + винблатсин + карбоплатин |
| PF | фторурацил + цисплатин |
| ITP | ифосфамид + паклитаксел + цисплатин |
|
FOLFOX
|
оксалиплатин + кальция фолинат + фторурацил |
| EP | этопозид + цисплатин |
| EC | этопозид + карбоплатин |
|
DDMVAC
|
дозированный метотрексат + винбластин +доксорубицин и цисплатин |
|
CMV
|
цисплатин + метотрексат и винбластин |
| IGRT | лучевая терапия, управляемая по изображениям |
|
IGRA тест
|
тесты на высвобождение ИФН-γ |
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков:
1) Умурзаков Хусан Талипбаевич - PhD докторант, магистр медицины, руководитель центра онкоурологии АО «Казахский научно – исследовательский институт онкологии и радиологии».
2) Гасанов Зиё Бахшиевич - PhD докторант, врач онкоуролог, старший ординатор АО «Казахский научно – исследовательский институт онкологии и радиологии».
3) Онгарбаев Бахытжан Тулигенович – врач высшей категории, заместитель председателя по клинической работе АО «Казахский научно – исследовательский институт онкологии и радиологии».
4) Абдрахманов Рамиль Зуфарович – кандидат медицинских наук, руководитель Центра химиотерапии опухолей, Председатель химиотерапевтического совета АО «Казахский научно – исследовательский институт онкологии и радиологии».
5) Арыбжанов Давранкул Турсункулович – доктор медицинских наук, профессор, заместитель главного врача по лечебной работе ГКП на ПХВ «Областная мноопрофильная клиника» УЗ области Жетыcу, доцент кафедры хирургических дисциплин №1 АО «Южно - Казахстанская медицинская академия».
6) Новиков Игорь Игоревич - PhD докторант, магистр медицины. Заместитель директора по контролю качества оказания медицинских услуг ГКП на ПХВ «Алматинская региональная многопрофильная клиника».
7) Кабыкенов Асхат Амангелдынович - врач онкоуролог высшей категории, магистр медицины. ГКП на ПХВ « Центр ядерной медицины и онкологии гСемей
8) Рахманбердиева Эльвира Жайдаровна – врач, клинический фармаколог АО «Казахский научно – исследовательский институт онкологии и радиологии».
Указание на отсутствие конфликта интересов: нет
Рецензенты:
1) Шалекенов Булат Уахитович – доктор медицинских наук, профессор, заведующий кафедрой урологии и андрологии НАО «Казахский Национальный университет им. Аль-Фараби», уролог;
2) Кайдаров Бакыт Касенович – доктор медицинских наук, профессор кафедры онкологии НАО «Казахский Национальный медицинский университет им. С.Д.Асфендиярова», онколог.
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его разработки или при наличии новых методов с уровнем доказательности.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.