Предраковые заболевания шейки матки
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Дисплазия шейки матки неуточненная (N87.9), Карцинома in situ внутренней части шейки матки (D06.0), Карцинома in situ других частей шейки матки (D06.7), Карцинома in situ наружной части шейки матки (D06.1), Карцинома in situ шейки матки неуточненной части (D06.9), Новообразования неопределенного или неизвестного характера других женских половых органов (D39.7), Резко выраженная дисплазия шейки матки, не классифицированная в других рубриках (N87.2), Слабовыраженная дисплазия шейки матки (N87.0), Умеренная дисплазия шейки матки (N87.1)
Акушерство и гинекология, Онкология
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «17» марта 2026 года
Протокол № 248
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
ПРЕДРАКОВЫЕ ЗАБОЛЕВАНИЯ ШЕЙКИ МАТКИ
LSIL - low-grade squamous intraepithelial lesions – плоскоклеточное интраэпителиальное поражение низкой степени. LSIL включает койлоцитоз, CIN I и кондиломы шейки матки [1], [3].
HSIL – high-grade squamous intraepithelial lesions – плоскоклеточное интраэпителиальное поражение высокой степени [1], [2]. HSIL включают CIN II (умеренную дисплазию), CIN III (тяжелую дисплазию и преинвазивный рак (CIS)). HSIL относится к облигатному предраку шейки матки.
Цервикальные интраэпителиальные неоплазии (Cervical Intraepithelial Neoplasia - CIN) – это группа заболеваний, характеризующихся нарушением созревания, дифференцировки и стратификации многослойного плоского эпителия шейки матки. CIN трех степеней инициируются персистирующей инфекцией, вызванной вирусами папилломы человека высокого канцерогенного риска (ВПЧ ВР), которая поддерживает прогрессию повреждений до инвазии. CIN I характеризуется высокой вероятностью регрессии и не относится к предраку шейки матки, небольшая часть CIN I переходит в CIN II-III – истинные предраковые поражения. Возможно развитие CIN II-III без формирования CIN I. Они предшествуют раку шейки матки (РШМ) на протяжении нескольких лет и даже десятилетий. За столь длительный период CIN могут быть выявлены и излечены до развития инвазивного рака несложными органосохраняющими эксцизиями [1], [2], [3].
LSIL - low-grade squamous intraepithelial lesions – плоскоклеточное интраэпителиальное поражение низкой степени. LSIL включает койлоцитоз, CIN I и кондиломы шейки матки [1], [3].
HSIL – high-grade squamous intraepithelial lesions – плоскоклеточное интраэпителиальное поражение высокой степени [1], [2]. HSIL включают CIN II (умеренную дисплазию), CIN III (тяжелую дисплазию и преинвазивный рак (CIS)). HSIL относится к облигатному предраку шейки матки.
ВВОДНАЯ ЧАСТЬ
Код(ы) Международной классификации болезней 10-го пересмотра (далее – МКБ-10) / Международной классификации болезней 11-го пересмотра (далее – МКБ-11):
Дата разработки протокола: 2023 год.
| МКБ-10 | |
|
Код
|
Название |
|
N87.0
|
Слабовыраженная дисплазия шейки матки |
|
N87.1
|
Умеренная дисплазия шейки матки |
|
N87.2
|
Резко выраженная дисплазия шейки матки, неклассифицированная в других рубриках |
|
N87.9
|
Дисплазия шейки матки неуточненная |
|
D39.7
|
Новообразование неопределенного или неизвестного характера других женских половых органов |
|
D06.0
|
Карцинома in situ внутренней части шейки матки (эндоцервикса) |
|
D06.1
|
Карцинома in situ наружной части шейки матки (экзоцервикса) |
|
D06.7
|
Карцинома in situ других частей шейки матки |
|
D06.9
|
Карцинома in situ неуточненной части шейки матки |
| МКБ-11 | |
|
GA15.7
|
Плоскоклеточное интраэпителиальное поражение шейки матки низкой степени |
|
2E66.2
|
Интраэпителиальное плоскоклеточное поражение шейки матки высокой степени |
|
2E66.2
|
Цервикальная интраэпителиальная неоплазия III степени |
|
2E66.2
|
Цервикальная интраэпителиальная неоплазия II степени |
|
2E66.Y
|
Другая уточненная карцинома in situ шейки матки |
|
2E66.Z
|
Карцинома in situ шейки матки неуточненная |
|
GA15.Z
|
Приобретенные аномалии шейки матки неуточненные |
Дата разработки протокола: 2023 год.
Пользователи протокола: акушер-гинекологи, онкогинекологи.
Категория пациентов: взрослые.
Сокращения, используемые в протоколе:
Сокращения, используемые в протоколе:
|
АКК
|
аномальная кольпоскопическая картина |
|
ВПЧ
|
вирус папилломы человека |
|
ВПЧ-ВР
|
вирус папилломы человека высокого канцерогенного риска |
|
ЗТ
|
зона трансформации |
|
ПЦР
|
полимеразная цепная реакция |
|
ПЭЭ
|
петлевая электроэксцизия |
|
РШМ
|
рак шейки матки |
|
AGC
|
клетки цервикального (железистого) эпителия с атипией неясного значения |
|
ASC-US
|
клетки плоского эпителия с атипией неясного значения |
|
ASC-H
|
клетки плоского эпителия с атипией неясного значения, не исключающие наличия высокой степени интраэпителиальных изменений |
|
CIN I
|
слабая дисплазия (цервикальная интраэпителиальная неоплазия I степени) |
|
CIN II
|
умеренная дисплазия (цервикальная интраэпителиальная неоплазия II степени) |
|
CIN III
|
тяжелая дисплазия (цервикальная интраэпителиальная неоплазия III степени) |
|
CIS
|
carcinoma in situ |
|
HSIL
|
интраэпителиальные изменения плоского эпителия высокой степени, включают CIN II, CIN III, карциному in situ и случаи, подозрительные на наличие инвазии. |
|
LSIL
|
интраэпителиальные изменения плоского эпителия низкой степени, включают поражения, ассоциированные с HPV и CIN I. |
|
NILM
|
интраэпителиальные изменения и злокачественные процессы отсутствуют. В эту группу включены цитологические заключения о нормальном состоянии эпителия, а также о наличии различных не неопластических состояний (заболеваний) |
|
VIA
|
визуальный осмотр шейки матки после обработки уксусной кислотой |
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты, которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D |
Описание серии случаев или неконтролируемое исследование, или мнение экспертов.
|
Классификация
Классификация:
Система Bethesda, 2014 г.
ASCUS – клетки плоского эпителия с атипией неясного значения.
ASC-Н – клетки плоского эпителия с атипией неясного значения, не исключающие наличия высокой степени интраэпителиальных изменений.
LSIL – интраэпителиальные изменения плоского эпителия низкой степени, включают поражения, ассоциированные с HPV и CIN I.
НSIL – интраэпителиальные изменения плоского эпителия высокой степени, включают CIN II, CIN III, карциному in situ и случаи, подозрительные на наличие инвазии.
Плоскоклеточная карцинома.
AGC – клетки цервикального (железистого) эпителия с атипией неясного значения.
AIS – аденокарцинома in situ
Аденокарцинома
Соотношение классификаций предраковых поражений шейки матки
|
Система Папаниколау
|
Описательная система ВОЗ | CIN | Система Bethesda |
| Класс 1 (норма) | Отсутствие злокачественных клеток | Отсутствие неопластических изменений | Норма |
| Класс 2 (метаплазия эпителия, воспалительный тип) | Атипия, связанная с воспалением |
Реактивные изменения
клеток ASC: ASCUS;
ASC - Н
|
|
| Класс 3 (дискариоз) | Слабая дисплазия | CIN I Койлоцитоз | LSIL |
| Умеренная дисплазия | CIN II | HSIL | |
| Тяжелая дисплазия | CIN III | ||
| Класс 4 (клетки, подозрительные на рак или карцинома in situ) | Карцинома in situ | ||
|
Класс 5 (рак)
|
Инвазивная карцинома | Карцинома | Карцинома |
Клиническая картина
Cимптомы, течение
Клиническая картина: не имеют патогномоничных клинических проявлений.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Жалобы: CIN I/II/III, включая преинвазивный рак шейки матки (CIS), не имеют патогномоничных клинических проявлений [3-10].
Анамнез:
Рекомендуется всем пациенткам проведение анализа анамнестических данных с целью выявления факторов риска развития CIN [12] (уровень доказательности C).
Факторами риска развития CIN являются раннее начало половой жизни, большое число и частая смена половых партнеров, курение, сопутствующие половые инфекции, большое количество беременностей и родов, наличие иммунокомпрометирующих заболеваний (гепатита B, С, ВИЧ), иммуносупрессивная терапия, длительный прием комбинированных оральных контрацептивов (КОК – по анатомо-терапевтическо-химической классификации – прогестагены и эстрогены (фиксированные комбинации)). Необходимо уточнить возраст сексуального дебюта, число половых партнеров [6]. При «контактных» кровянистых выделениях из половых путей уточнить их длительность, наличие в анамнезе хирургических вмешательств на шейке матки, ВПЧ инфекции, оценить результаты ранее проведенного цервикального скрининга [14, 15].
Физикальные обследования
Гинекологический осмотр:
• состояние наружных половых органов;
У женщин c HSIL старше 50 лет и/или с зоной трансформации III типа целесообразно проведение конизации шейки матки с выскабливанием оставшейся части цервикального канала [5].
Не рекомендуется рутинно использовать МРТ органов малого таза в качестве метода диагностики предрака шейки матки. Однако этот метод рассматривается как перспективный в дифференциальной диагностике предрака и РШМ. Поскольку МРТ с использованием диффузно-взвешенных последовательностей позволяет выявить начальные признаки инвазии опухоли в строму шейки матки, характерные для ранней стадии РШМ [26].
Показания для консультации узких специалистов:
Схема -1. Диагностический алгоритм патологии шейки матки
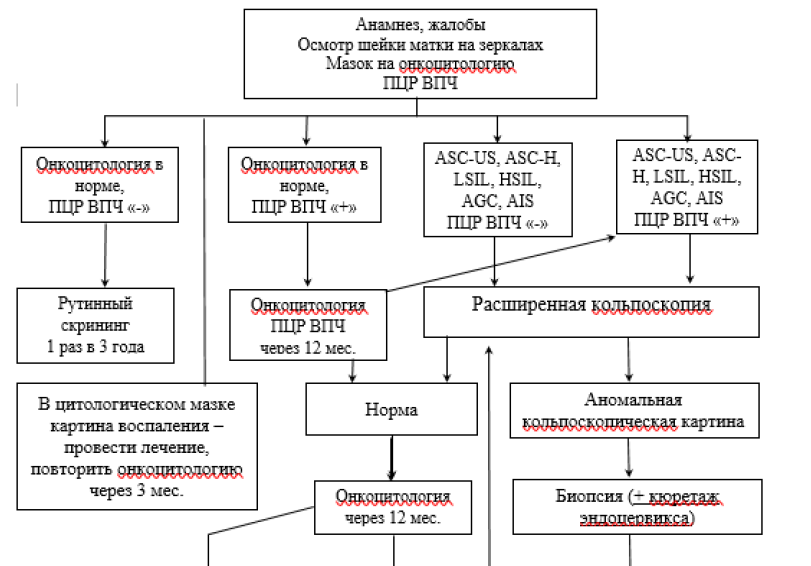
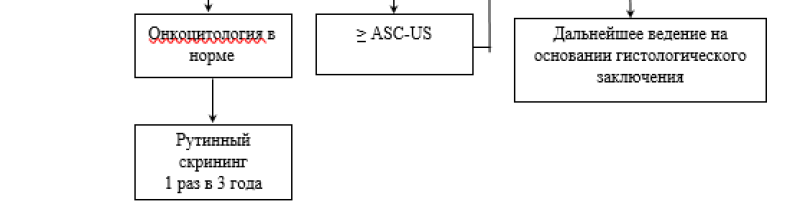
• осмотр влагалища и шейки матки на зеркалах;
• визуальная оценка шейки матки после обработки уксусной кислотой (VIA).
Ожидаемые результаты. Осмотр шейки матки в зеркалах не позволяет определить интраэпителиальные поражения шейки матки [12].
При визуальной оценке шейки матки с уксусной кислотой можно выявить поражения эпителия шейки матки или подозрение на рак шейки матки.
VIA должно выполняться обученным специалистом.
Техника: для проведения VIA медработник наносит на шейку матки 3–5% уксусную кислоту, а затем через 1–2 минуты смотрит, не появляются ли какие-либо белые изменения на шейке матки.
Тест VIA является положительным, если имеются приподнятые и утолщенные белые бляшки или ацетобелые области, которые сохраняются более одной минуты, обычно в области зоны трансформации.
VIA является отрицательным, если слизистая оболочка шейки матки не имеет изменений [4].
Медицинский работник должен заподозрить рак, если на шейке матки обнаружено образование или язва, напоминающая цветную капусту. В этих случаях VIA не проводится, и женщину необходимо направить непосредственно к онкологу-гинекологу [4].
Комментарии. Рекомендуется выполнить прицельную (при необходимости мультифокальную) кольпоскопически направленную биопсию шейки матки (punch-биопсия) с последующим патологоанатомическим исследованием биопсийного (операционного) материала шейки матки пациенткам с цитологическим заключением ASCUS, ASC-H, LSIL при наличии ВПЧ-ВР и аномальной кольпоскопической картине для подтверждения диагноза [26], [27], [28], [29] (уровень доказательности С). Поскольку у одной пациентки возможно наличие CIN разной степени тяжести, постановка диагноза на основании ограниченных биоптатов может быть затруднена [4]. Проведение мультифокальной точечной биопсии шейки матки (punch-биопсия) возможно под кольпоскопическим контролем у молодых женщин.
Бимануальный осмотр:
• консистенция влагалищной части шейки матки, состояние надвлагалищной части шейки матки
• размеры и форма матки;
• состояние придатков.
Ожидаемые результаты: отклонений от нормы может и не быть.
Основные лабораторные исследования:
Дополнительные лабораторные исследования:
Лабораторные диагностические исследования
Основные лабораторные исследования:
• цитологическое исследование цервикального мазка (традиционная или жидкостная) (уровень доказательности А).
• гистологическое исследование биоптата шейки матки (уровень доказательности А).
• молекулярно-биологическое исследование цервикального мазка (ПЦР на определение ВПЧ-ВР) (уровень доказательности С).
Ожидаемые результаты. Аномальный цитологический результат (по классификации Bethesda). Результат гистологического исследования может быть CIN I-III, CIS. По результатам ПЦР могут быть обнаружены ДНК ВПЧ высокого онкогенного риска.
Дополнительные лабораторные исследования:
• микроскопическое исследование влагалищных мазков для исключения воспалительных заболеваний органов малого таза.
• проведение скрининга на ИППП (Chlamydia trachomatis, Neisseria gonorrhoeae, Trichomonas vaginalis, Mycoplasma genitalium) методом ПЦР (при подозрении на инфекции).
• ИФА на ВИЧ
Ожидаемые результаты: отклонений от нормы может и не быть.
Рекомендуется проведение цитологического исследования микропрепарата шейки матки всем женщинам в возрасте от 21 до 65 лет с интервалом в 3 года с целью выявления предрака шейки матки [17], [18]. Возможно проведение цитологического исследования при обращении пациентки менее 21 года при половой жизни более 3 лет. Следует учитывать низкую воспроизводимость результатов повторных мазков, взятых течение 1,5 мес. после первичных, рекомендован пересмотр аномальных мазков. Около 10% традиционных цитологических мазков являются неадекватными, что связано с неправильной техникой забора материала и приготовления препарата [3], [15], [19], [20], [23]. Жидкостная цитология является более эффективной для выявления CIN, прежде, всего ввиду многократного уменьшения числа неадекватных мазков [12], [22], [23].
Ожидаемые результаты: отклонений от нормы может и не быть.
Рекомендуется проведение цитологического исследования микропрепарата шейки матки всем женщинам в возрасте от 21 до 65 лет с интервалом в 3 года с целью выявления предрака шейки матки [17], [18]. Возможно проведение цитологического исследования при обращении пациентки менее 21 года при половой жизни более 3 лет. Следует учитывать низкую воспроизводимость результатов повторных мазков, взятых течение 1,5 мес. после первичных, рекомендован пересмотр аномальных мазков. Около 10% традиционных цитологических мазков являются неадекватными, что связано с неправильной техникой забора материала и приготовления препарата [3], [15], [19], [20], [23]. Жидкостная цитология является более эффективной для выявления CIN, прежде, всего ввиду многократного уменьшения числа неадекватных мазков [12], [22], [23].
ВПЧ-тестирование рекомендовано для:
• включения в первый этап скрининга;
• диагностики CIN;
• оценки эффективности лечения и мониторинга больных после лечения;
• сортировки женщин с аномальными результатами мазков от ASC-US и более в возрасте от 25 до 65 лет;
• определения тактики у пациенток с мазками типа ASCUS;
• оценки эффективности эксцизионного лечения HSIL (CIN2-3/CIS) и микроинвазивного рака в случае органосохраняющих операций.
Отрицательный результат указывает на отсутствие инфекции ВПЧ, а положительный результат указывает на инфекцию одним или несколькими типами ВПЧ высокого риска.
Рекомендуется выполнить ПЦР отделяемого из цервикального канала ВПЧ с целью выявления риска РШМ в качестве скринингового метода у всех женщин старше 30 лет каждые 5 лет (у ВПЧ негативных женщин) и ежегодно у ВПЧ позитивных женщин (уровень доказательности C). ВПЧ-тестирование целесообразно проводить всем женщинам в качестве скринингового метода с 30 лет в сочетании с цитологическим исследованием цервикального образца (co-test) [24], [25].
Рекомендуется выполнить ПЦР отделяемого из цервикального канала на ВПЧ пациенткам с цитологическим заключением ASCUS, ASC-H, LSIL, HSIL вне зависимости от возраста [24] (уровень доказательности C). Целесообразно проведение генотипирования (частичного или полного) и определение вирусной нагрузки для оценки риска прогрессирования CIN до инвазии, а также для выбора тактики ведения и контроля эффективности лечения [24].
В таблице описаны уровни риска и путь скрининга, какое последующеенаблюдение необходимо для каждого уровня риска [3-10].
Определение уровней риска
Основные инструментальные исследования:
Дополнительные инструментальные исследования:
Рекомендуется выполнить ПЦР отделяемого из цервикального канала на ВПЧ на всю группу ВПЧ-ВР (не менее 12 типов) всем женщинам в возрасте от 30 до 65 лет с целью выявления группы риска предрака и РШМ [3].
Рекомендуется выполнить ПЦР отделяемого из цервикального канала ВПЧ с целью выявления риска РШМ в качестве скринингового метода у всех женщин старше 30 лет каждые 5 лет (у ВПЧ негативных женщин) и ежегодно у ВПЧ позитивных женщин (уровень доказательности C). ВПЧ-тестирование целесообразно проводить всем женщинам в качестве скринингового метода с 30 лет в сочетании с цитологическим исследованием цервикального образца (co-test) [24], [25].
Рекомендуется выполнить ПЦР отделяемого из цервикального канала на ВПЧ пациенткам с цитологическим заключением ASCUS, ASC-H, LSIL, HSIL вне зависимости от возраста [24] (уровень доказательности C). Целесообразно проведение генотипирования (частичного или полного) и определение вирусной нагрузки для оценки риска прогрессирования CIN до инвазии, а также для выбора тактики ведения и контроля эффективности лечения [24].
Для идентификации и типирования ВПЧ целесообразно использовать ПЦР с типоспецифическими и видоспецифическими праймерами для количественной оценки риска малигнизации — позволяет определить ту критическую концентрацию вируса (вирусную нагрузку), которая напрямую связана с риском малигнизации. При показателях уровня ДНК ВПЧ выше 5000 геномов вероятность развития РШМ высока [3-9].
В таблице описаны уровни риска и путь скрининга, какое последующеенаблюдение необходимо для каждого уровня риска [3-10].
Определение уровней риска
| Уровни риска | Результаты скринингового теста |
| Низкий риск | Онкогенные ВПЧ не обнаружены |
| Средний риск |
Онкогенный ВПЧ не обнаружен при отсутствии патологии шейки матки, выявленной при цитологическом исследовании; или Онкогенный ВПЧ не обнаружен при возможном или определенном низком уровне патологии, выявленном при цитологическом исследовании |
| Высокий риск |
Обнаружен онкогенный ВПЧ (независимо от результата цитологии); или Онкогенный ВПЧ обнаружен при возможном или определенном высоком уровне сквамозной или любой железистой патологии, выявленной при цитологическом исследовании |
Инструментальные диагностические исследования
Основные инструментальные исследования:
• Расширенная кольпоскопия (уровень доказательности B).
• Прицельная биопсия шейки матки (уровень доказательности C).
• Эндоцервикальное выскабливание (уровень доказательности C).
Ожидаемые результаты. При расширенной кольпоскопии может быть аномальная кольпоскопическая картина 1-2 степени. Результат гистологического исследования биоптата шейки матки может быть CIN I-III, CIS. Результат цитологического или гистологического исследований эндоцервикального соскоба может быть без атипических изменений или могут быть гиперплазия эндоцервикса, LSIL, HSIL, HGSIL и др. атипические изменения.
Дополнительные инструментальные исследования:
• УЗИ органов малого таза;
• МРТ органов малого таза с контрастированием (при подозрении на инвазию).
Ожидаемые результаты. По результатам УЗИ и МРТ органов малого таза каких-либо изменений может и не быть. Проводится с целью исключения инвазивного рака шейки матки.
Рекомендуется выполнить расширенную кольпоскопию для выявления измененных участков шейки матки (при визуальных изменениях шейки матки, при аномалиях в мазках ASCUS, ASC-H, LSIL, HSIL; при положительном тесте на ВПЧ-ВР), а также с целью выбора места и метода биопсии шейки матки для верификации диагноза [12], [25]. При отсутствии возможности проведения расширенной кольпоскопии возможно использование визуального метода VIA (осмотр шейки матки после обработки 3% раствором уксусной кислоты) [12].
Рекомендуется выполнить расширенную кольпоскопию для выявления измененных участков шейки матки (при визуальных изменениях шейки матки, при аномалиях в мазках ASCUS, ASC-H, LSIL, HSIL; при положительном тесте на ВПЧ-ВР), а также с целью выбора места и метода биопсии шейки матки для верификации диагноза [12], [25]. При отсутствии возможности проведения расширенной кольпоскопии возможно использование визуального метода VIA (осмотр шейки матки после обработки 3% раствором уксусной кислоты) [12].
Оценка измененных участков шейки матки при расширенной кольпоскопии [3-12, 17, 19]:
• аномальная неспецифическая кольпоскопическая картина;
• аномальная кольпоскопическая картина 1 степени;
• аномальная кольпоскопическая картина 2 степени.
Рекомендуется при результатах цитологии HSIL выполнить прицельную биопсию или эксцизию зоны трансформации (ЗТ) шейки матки (в зависимости от результатов кольпоскопии) с последующим выскабливанием цервикального канала и патологоанатомическим исследованием материала для подтверждения диагноза [28]. Уровень доказательности С.
У женщин c HSIL старше 50 лет и/или с зоной трансформации III типа целесообразно проведение конизации шейки матки с выскабливанием оставшейся части цервикального канала [5].
Эндоцервикальное выскабливание предполагает использование специального тонкого инструмента для получения ткани из канала шейки матки для микроскопического исследования. Он используется, когда:
• цитологический скрининг-тест считается положительным, но при кольпоскопии никаких отклонений не наблюдается – внутри канала может быть скрыто предраковое состояние или рак;
• аномальные железистые клетки видны при скрининговом тесте на основе цитологии;
• кольпоскопия предполагает аномалии, возникающие в канале;
• вся зона трансформации не видна (кольпоскопия оценивается как неудовлетворительная).
Не рекомендуется рутинно использовать МРТ органов малого таза в качестве метода диагностики предрака шейки матки. Однако этот метод рассматривается как перспективный в дифференциальной диагностике предрака и РШМ. Поскольку МРТ с использованием диффузно-взвешенных последовательностей позволяет выявить начальные признаки инвазии опухоли в строму шейки матки, характерные для ранней стадии РШМ [26].
Показания для консультации узких специалистов:
• консультация кардиолога. Цель: при наличии сопутствующей патологии ССС для оценки сердечно-сосудистой системы, выявления и минимизации рисков осложнений, а также для определения оптимального плана подготовки к вмешательству;
• консультация невропатолога. Цель: при сосудистых мозговых нарушениях, в том числе инсультах, травмах головного и спинного мозга, эпилепсии, миастении, нейроинфекционных заболеваниях, а также во всех случаях потери сознания для выявления и минимизации рисков осложнений, а также для определения оптимального плана подготовки к вмешательству;
• консультация гастроэнтеролога. Цель: при наличии сопутствующей патологии органов ЖКТ для выявления и минимизации рисков осложнений, а также для определения оптимального плана подготовки к вмешательству;
• консультация эндокринолог. Цель: при наличии сопутствующей патологии эндокринных органов для выявления и минимизации рисков осложнений, а также для определения оптимального плана подготовки к вмешательству;
NB! Консультация других узких специалистов по показаниям.
Диагностический алгоритм
Схема -1. Диагностический алгоритм патологии шейки матки


Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований
Основные заболевания для дифференциальной диагностики представлены в таблице
|
Диагноз
|
Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Эктропион | Выделения из половых путей в виде белей |
Осмотр шейки матки на зеркалах;
онкоцитология;
кольпоскопия.
|
При осмотре шейки матки определяется постравматический выворот слизистой цервикального канала с наличие радиарных борозд на влагалищной порции шейки матки.
Онкоцитология: нет интраэпителиальных поражений.
Кольпоскопическая картина эктропиона шейки матки.
|
|
Лейкоплакия шейки матки
|
Клинических проявлений нет. |
Осмотр шейки матки на зеркалах;
онкоцитология;
кольпоскопия;
прицельная биопсия с гистологическим исследованием.
|
При осмотре на поверхности шейки матки определяется белесоватое пятно или бляшка различных размеров, не удаляемое кончиком инструмента.
Онкоцитология: нет интраэпителиальных поражений.
Кольпоскопически: аномальная неспецифическая кольпоскопическая картина. Гистологическое заключение: гиперкератоз, паракератоз, акантоз.
|
| Цервицит | Обильные слизистые или гноевидные выделения из половых путей |
Осмотр шейки матки на зеркалах;
мазок на степень чистоты; онкоцитология;
кольпоскопия;
|
При осмотре шейка матки диффузно гипетрофированная, поверхность мелкобугристая, эпителий гиперемированный, рыхлый.
Большое количество лейкоцитов, кокковая или другая флора.
Онкоцитология: лейкоцитарная инфильтрация, картина воспаления.
Кольпоскопическая картина: признаки востпаления.
|
|
Рак шейки матки
|
АМК;
контактные кровянистые выделения из половых путей;
выделения из половых путей цвета «мясных помоев»
|
Осмотр шейки матки;
бимануальный осмотр;
биопсия шейки матки с гистологическим исследованием; эндоцервикальный кюретаж;
УЗИ органов малого таза;
МРТ органов малого таза
|
Наличие язвенного дефекта на шейке матки с инфильтрированными краями или наличие экзофитной опухоли в виде «цветной капусты» или бочкообразно гипертрофированная шейка матки плотной деревянистой консистенции.
УЗ-признаки образования шейки матки с локусами кровотока;
МРТ-признаки РШМ;
заключение гистологического исследования биоптата шейки матки – плоскоклеточная карцинома или другая гистологическая форма РШМ
|
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
Немедикаментозное лечение: нет.
Медикаментозное лечение: нет.
Медикаментозное лечение плоскоклеточных интраэпителиальных поражений в качестве самостоятельного метода не рекомендуется [6], [24], [40], [41]. Уровень доказательности А.
Хирургическое лечение на амбулаторном уровне может быть выполнено в объеме деструктивного и эксцизионного методов лечения.
Деструктивные методы лечения:
• криодеструкция шейки матки;
• радиоволновая абляция шейки матки;
• аргоноплазменная деструкция;
• лазерная вапоризация шейки матки.
Рекомендуется деструктивное или эксцизионное лечение (в зависимости от типа ЗТ) при сохранении поражений, соответствующих CIN I более 18-24 месяцев с целью профилактики прогрессирования [6], [24], [38]. Уровень доказательности C.
Эксцизионные методы лечения – punch-биопсия шейки матки, петлевая электроэксцизия (ПЭЭ) шейки матки.
Показания для проведения деструктивных методов лечения [3-12, 17, 19]:
• полная визуализация зоны трансформации (ЗТ) (I тип ЗТ – поражения ограничены эктоцервиксом);
• отсутствие кольпоскопических признаков поражения эктоцервикальных желез с погружением АБЭ в них; отсутствие данных о вовлечении эндоцервикса в патологический процесс;
• отсутствие хирургического лечения шейки матки в анамнезе;
• отсутствие расхождений между данными цитологического, кольпоскопического и патологоанатомического исследований.
В остальных случаях и при сохранении CIN I через 18-24 месяцев даже в возрасте моложе 24 лет показана эксцизия [3], [6], [15], [24], [28], [34].
Не рекомендуется проводить деструкцию эктопии, т.к. эктопия шейки матки является вариантом нормы и не требует лечения [28]. Уровень доказательности C.
Не рекомендуется лечить неосложненный эктропион шейки матки [28]. Уровень доказательности C.
Рекомендуется женщинам старше 40 лет с CIN I в биоптате эктоцервикса проводить петлевую эксцизию ЗТ в связи с риском синхронных тяжелых поражений, скрытых в канале, вследствие длительной персистенции ВПЧ ВКР [6], [35]. Уровень доказательности А.
Не рекомендуется проводить деструкцию эктопии, т.к. эктопия шейки матки является вариантом нормы и не требует лечения [28]. Уровень доказательности C.
Необоснованная деструкция эктопии и нормальной ЗТ в случае развития неоплазии не предупреждает прогрессию заболевания в скрытой части канала, но способствует трудностям в диагностике [1], [3], [6], [15].
Не рекомендуется лечить неосложненный эктропион шейки матки [28]. Уровень доказательности C.
Врожденный эктропион у ВПЧ негативных женщин является неопасным состоянием в отношении развития предрака и РШМ [1], [3], [15], [30].
Осложнения деструктивных методов лечения шейки матки:
Вид анестезии: местный.
Противопоказания к деструктивным методам лечения шейки матки:
• менструация;
• аномальные маточные кровотечения
• воспалительные заболевания мочеполовой системы;
• беременность;
• отсутствие цитологического (и/или гистологического) подтверждения патологического процесса;
• дисплазия или рак шейки матки в цервикальном канале.
Осложнения деструктивных методов лечения шейки матки:
• кровотечение;
• стеноз наружного зева;
• эндометриоз шейки матки.
Вид анестезии: местный.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЕ НА СТАЦИОНАРНОМ УРОВНЕ
Карта наблюдения пациента, маршрутизация пациента:
Медикаментозное лечение: нет.
Хирургическое лечение
Рекомендуется проводить хирургическое лечение при HSIL (CIN II, CIN III) – электроэксцизию шейки матки или конизацию в зависимости от типа ЗТ с последующим выскабливанием цервикального канала с целью исключения злокачественного процесса [3], [6], [15], [24], [38], [34]. Уровень доказательности C.
Рекомендуется при CIN III направлять пациенток к врачу онкогинекологу для выполнения конизации шейки матки с последующим выскабливанием цервикального канала и по показаниям – полости матки (сопутствующая патология эндометрия) [1], [3], [6], [26], [38]. Уровень доказательности C.
Показания к петлевой электроэксцизии и конизации шейки матки:
Осложнения ПЭЭ и конизации шейки матки:
Вид анестезии: местный или тотальная внутривенная анестезия.
Если в краях резекции шейки матки или соскобе из оставшейся части цервикального канала обнаруживается HSIL, рекомендован цитологический, кольпоскопический и ВПЧ контроль через 3 месяца. В таких случаях женщинам, завершившим репродуктивную функцию и/или с сопутствующей патологией матки, показано проведение тотальной гистерэктомии [6], [16].
При наличии аномальных результатов цитологии и/или аномальной кольпоскопической картины и/или позитивном ВПЧ с сохранением вирусной нагрузки показана повторная конизация, в некоторых случаях возможно проведение гистерэктомии [3], [5], [6], [38].
NB! Гистерэктомия по поводу HSIL проводится только после получения результата гистологического исследования конус-биоптата шейки матки с исключением инвазивного рака шейки матки.
Вид анестезии: эндотрахеальный наркоз.
Противопоказания к тотальной гистерэктомии: острые инфекционные заболевания (ОРВИ, пневмония и др.), острые воспалительные заболевания половых органов, сопутствующие заболевания внутренних органов (сердца, печени, почек) в стадии декомпенсации, нарушения гемостаза, большие размеры матки (более 12 недель).
Риски операции: кровотечение во время операции, кровотечение после операции, гематомы в малом тазу, травма мочевого пузыря, мочеточника или кишечника, инфекции, перикультит, инфекции раны, перитонит или сепсис, тромбоз вен нижних конечностей или тромбоэмболия легочных артерий, осложнения, связанные с анестезией: реакции на препараты для анестезии, риски сердечно-сосудистых осложнений, нарушения мочеиспускания, грыжи.
Алгоритмы действий врача при выявлении отдельных видов аномальных мазков и у отдельных групп пациенток представлены в приложении 1.
Дальнейшее ведение:
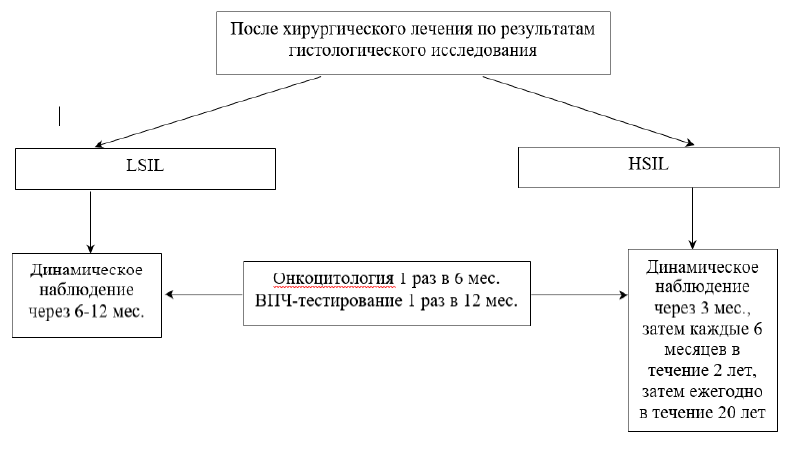
У молодых и/или планирующих беременность пациенток с морфологически подтвержденным диагнозом LSIL (признаки ВПЧ инфекции, койлоцитоз, CIN I) предпочтительна выжидательная тактика c динамическим наблюдением за состоянием шейки матки в течение 18-24 месяцев в виде цитологического контроля 1 раз в 6 месяцев и ВПЧ-тестирования 1 раз в 12 месяцев. Хирургическое лечение рекомендуется в случае отсутствия регрессии через 18-24 месяцев [1], [3], [6], [14], [15]. Уровень доказательности А.
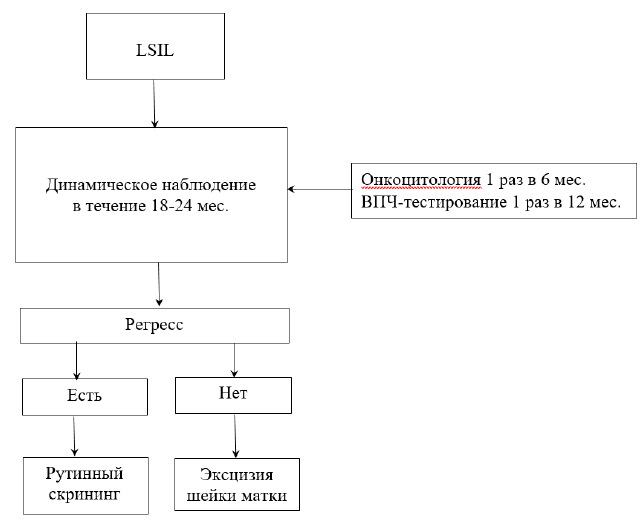
После хирургического лечения LSIL проводится цитологическое исследование микропрепарата шейки матки и ВПЧ-тестирование через 6-12 месяцев. После хирургического лечения HSIL первый co-test (цитологическое исследование и ВПЧ – тестирование) целесообразно выполнить через 3 месяца после хирургического лечения, затем каждые 6 месяцев в течение 2 лет, затем ежегодно в течение 20 лет [6].
В случае подозрения на остаточное поражение (рецидив) рекомендована расширенная кольпоскопия и реконизация с патологоанатомическим исследованием [55]; консультация врача-онколога (по показаниям). Для лечения рецидива CIN II/III предпочтительным методом является конизация, в некоторых случаях возможна гистерэктомия [6], [38].
Индикаторы эффективности лечения: NILM в цитологических мазках с шейки матки, отсутствие ВПЧ-ВР.

Немедикаментозное лечение: нет.
Медикаментозное лечение: нет.
Хирургическое лечение
При выявлении заболеваний шейки матки (CIN II/CIN III, CIS) оперативное лечение целесообразно проводить в стационарах 3 уровня в связи с изменениями топографо-анатомических взаимоотношений и возможными интраоперационными осложнениями.
Рекомендуется проводить хирургическое лечение при HSIL (CIN II, CIN III) – электроэксцизию шейки матки или конизацию в зависимости от типа ЗТ с последующим выскабливанием цервикального канала с целью исключения злокачественного процесса [3], [6], [15], [24], [38], [34]. Уровень доказательности C.
У женщин до 25 лет с диагнозом CIN II в биоптате при р16-негативном результате ИГХ допустимо динамическое наблюдение с использованием цитологического контроля, ВПЧ-тестирования и кольпоскопии 1 раз в 6 месяцев в течение 2 лет [36]. В случае отсутствие регресса, перейти к активной тактике (эксцизия шейки матки).
У пациенток с диагнозом CIN II в биоптате при р16-позитивном результате ИГХ рекомендована безотлагательная эксцизия шейки матки [37].
Рекомендуется при CIN III направлять пациенток к врачу онкогинекологу для выполнения конизации шейки матки с последующим выскабливанием цервикального канала и по показаниям – полости матки (сопутствующая патология эндометрия) [1], [3], [6], [26], [38]. Уровень доказательности C.
Показания к петлевой электроэксцизии и конизации шейки матки:
• аномальная цитологическая картина мазка (LSIL, HSIL, ASC-H, AGC, HGSIL, AIS, CIS);
• аномальная кольпоскопическая картина 1 степени без четких границ у наружного зева при ЗТ 2 и/или 3 типа при положительном тесте на ВПЧ;
• аномальная кольпоскопическая картина 2 степени при любой ЗТ;
• неудовлетворительная кольпоскопия (ЗТ 3 тип) с подозрением на поражение цервикального канала;
• преинвазивный рак;
• микроинвазивный рак (инвазия опухоли до 5 мм).
Противопоказания к ПЭЭ и конизации шейки матки:
• менструация;
• воспалительные заболевания мочеполовой системы;
• беременность;
• до 12 недель после родов;
• инвазивный рак.
Осложнения ПЭЭ и конизации шейки матки:
• кровотечение интраоперационное, в раннем и позднем послеоперационном периоде (на 10-20 дни);
• стеноз цервикального канала, внутреннего или наружного зева;
• вторичное инфицирование;
• эндометриоз шейки матки.
Вид анестезии: местный или тотальная внутривенная анестезия.
При патологоанатомическом подтверждении диагноза и отсутствии опухолевых клеток в краях резекции и соскобе из оставшейся части цервикального канала проведенный объем хирургического вмешательства считается адекватным.
Если в краях резекции шейки матки или соскобе из оставшейся части цервикального канала обнаруживается HSIL, рекомендован цитологический, кольпоскопический и ВПЧ контроль через 3 месяца. В таких случаях женщинам, завершившим репродуктивную функцию и/или с сопутствующей патологией матки, показано проведение тотальной гистерэктомии [6], [16].
При наличии аномальных результатов цитологии и/или аномальной кольпоскопической картины и/или позитивном ВПЧ с сохранением вирусной нагрузки показана повторная конизация, в некоторых случаях возможно проведение гистерэктомии [3], [5], [6], [38].
NB! Гистерэктомия по поводу HSIL проводится только после получения результата гистологического исследования конус-биоптата шейки матки с исключением инвазивного рака шейки матки.
Вид анестезии: эндотрахеальный наркоз.
Противопоказания к тотальной гистерэктомии: острые инфекционные заболевания (ОРВИ, пневмония и др.), острые воспалительные заболевания половых органов, сопутствующие заболевания внутренних органов (сердца, печени, почек) в стадии декомпенсации, нарушения гемостаза, большие размеры матки (более 12 недель).
Риски операции: кровотечение во время операции, кровотечение после операции, гематомы в малом тазу, травма мочевого пузыря, мочеточника или кишечника, инфекции, перикультит, инфекции раны, перитонит или сепсис, тромбоз вен нижних конечностей или тромбоэмболия легочных артерий, осложнения, связанные с анестезией: реакции на препараты для анестезии, риски сердечно-сосудистых осложнений, нарушения мочеиспускания, грыжи.
Пациентки после субтотальной гистерэктомии наблюдаются по стандартной схеме в зависимости от возраста.
Алгоритмы действий врача при выявлении отдельных видов аномальных мазков и у отдельных групп пациенток представлены в приложении 1.
Дальнейшее ведение:
У молодых и/или планирующих беременность пациенток с морфологически подтвержденным диагнозом LSIL (признаки ВПЧ инфекции, койлоцитоз, CIN I) предпочтительна выжидательная тактика c динамическим наблюдением за состоянием шейки матки в течение 18-24 месяцев в виде цитологического контроля 1 раз в 6 месяцев и ВПЧ-тестирования 1 раз в 12 месяцев. Хирургическое лечение рекомендуется в случае отсутствия регрессии через 18-24 месяцев [1], [3], [6], [14], [15]. Уровень доказательности А.

Рекомендуется наблюдение пациенток после хирургического лечения HSIL с проведением цитологического исследования микропрепарата шейки матки и ПЦР ВПЧ отделяемого из цервикального канала для раннего выявления рецидива [38]. Уровень доказательности С.
После хирургического лечения LSIL проводится цитологическое исследование микропрепарата шейки матки и ВПЧ-тестирование через 6-12 месяцев. После хирургического лечения HSIL первый co-test (цитологическое исследование и ВПЧ – тестирование) целесообразно выполнить через 3 месяца после хирургического лечения, затем каждые 6 месяцев в течение 2 лет, затем ежегодно в течение 20 лет [6].
В случае подозрения на остаточное поражение (рецидив) рекомендована расширенная кольпоскопия и реконизация с патологоанатомическим исследованием [55]; консультация врача-онколога (по показаниям). Для лечения рецидива CIN II/III предпочтительным методом является конизация, в некоторых случаях возможна гистерэктомия [6], [38].
Индикаторы эффективности лечения: NILM в цитологических мазках с шейки матки, отсутствие ВПЧ-ВР.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для экстренной госпитализации: нет.
Показания для плановой госпитализации: HSIL (CIN II, CIN III, CIS), подозрение на рак шейки матки для проведения широкой конус-биопсии шейки матки диагностическим выскабливанием цервикального канала; эксцизия шейки матки (при невозможности проведения в амбулаторных условиях, например, поражение шейки матки до сводов, предельное укорочение шейки матки, тяжелая экстрагенитальная патология, отказ от выполнения процедуры под местной анестезией и т.д.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- 1. WHO guideline for screening and treatment of cervical pre-cancer lesions for cervical cancer prevention, 2 edition. 6 July 2021.Available at:https://www.who.int/publications/i/item/9789240030824. 2. Monitoring national cervical cancer prevention and control programmes: quality control and quality assurance for visual inspection with acetic acid (VIA)-based programmes, WHO https://apps.who.int/iris/bitstream/handle/10665/79316/9789241505260 eng.pdf;jsessionid=7DD100FFE36D56FA17FCF4177DEFBAB6?sequence=1 3. Screening and treatment of pre-cancerous lesions for secondary prevention of cervical cancer Technology landscape, UNITAID,2019. Available at:https://unitaid.org/assets/Cervical_Cancer_Technology-landscape-2019.pdf 4. International Federation of Gynecology and Obstetrics (FIGO). Available at: https://www.figo.org/search/node?keys=cervical+cancer&advancedform=1&f[0]=language:en 5. The American Cancer Society Guidelines for the Prevention and Early Detection of Cervical Cancer, 2021. Available at:https://www.cancer.org/cancer/cervical-cancer/detectiondiagnosis-staging/cervical-cancer-screening-guidelines.html 6. Risk Factors for Cervical Cancer, ACS, 2022.Available at: https://www.cancer.org/cancer/cervical-cancer/causes-risks-prevention/risk-factors.html. 7. Updated Cervical Cancer Screening Guidelines, ACOG, April, 2021. Availableat: https://www.acog.org/clinical/clinical-guidance/practice-advisory/articles/2021/04/updatedcervical-cancer-screening-guidelines. 8. 2019 ASCCP Risk-Based Management Consensus Guidelines for Abnormal Cervical Cancer Screening Tests and Cancer Precursors. Available at https://journals.lww.com/jlgtd/Fulltext/2020/04000/2019ASCCP_Risk_Based_Managemen t_Consensus.3.aspx. 9. Shahida S. M. et al. Prevalence of Cervical Intraepithelial Neoplasia in four Upazila of Dhaka Division //Mymensingh medical journal: MMJ. – 2019. – Т. 28. – №. 3. – С. 655., Jul. 10. World Health Organization. Reproductive Health et al. Comprehensive cervical cancer control: a guide to essential practice. – World Health Organization, 2014. 11. Darragh T. M. et al. The lower anogenital squamous terminology standardization project for HPV-associated lesions: background and consensus recommendations from the College of American Pathologists and the American Society for Colposcopy and Cervical Path, Oct., doi: 10.5858/arpa. LGT200570. 12. Saslow D. et al. American Cancer Society, American Society for Colposcopy and Cervical Pathology, and American Society for Clinical Pathology screening guidelines for the prevention and early detection of cervical cancer //CA: a cancer journal for clinici, Jul., doi: 10.1097/LGT.0b013e31824ca9d5. 13. Bonde J. H. et al. Clinical Utility of Human Papillomavirus Genotyping in Cervical Cancer Screening: A Systematic Review //Journal of lower genital tract disease. – 2020. – Т. 24. – №. 1. – С. 1- 13.
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1) Шакирова Аида Фазыловна – кандидат медицинских наук, врач высшей квалификационной категории, заведующий центром женского здоровья ТОО «Национальный научный онкологический центр».
2) Укыбасова Талшын Мухадесовна – доктор медицинских наук, профессор, врач акушер-гинеколог высшей квалификационной категории, КАД женское здоровье Корпоративного фонда «University Medical Center».
3) Козгамбаева Ляззат Таласпаевна – кандидат медицинских наук, врач высшей квалификационной категории, заместитель директора по менеджменту качества медицинской помощи ГКП на ПХВ «Многопрофильный медицинский центр» Управление общественного здравоохранения города Астаны.
4) Олжатаева Гайни Оскеновна – врач высшей квалификационной категории, врач гинеколог-радиационный онколог центра лучевой терапии ТОО «Национальный научный онкологический центр».
5) Камзаева Назира Калдешевна – кандидат медицинских наук, врач акушер-гинеколог высшей квалификационной категории, КАД женское здоровье Корпоративного фонда «University Medical Center».
6) Игембаева Гульмира Исмаиловна – магистр медицины, врач первой квалификационной категории, ТОО «Национальный научный онкологический центр», онкогинеколог сектора онкогинекологии Центра многопрофильной хирургии.
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
Исенова Сауле Шайкеновна – доктор медицинских наук, профессор, заведующая кафедрой акушерства и гинекологии с курсом клинической генетики НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова»
Тулетова Айнур Серикбаевна – PhD, ассоциированный профессор, доцент кафедры акушерства и гинекологии №2 НАО «Медицинский университет Астана», руководитель ТОО «ANA Clinic», президент Национальной лиги эндометриоза.
Условие для пересмотра протокола: пересмотр не реже 1 раза в 5 лет и не чаще 1 раза в 3 года при наличии новых методов диагностики и лечения с уровнем доказательности.
Алгоритм обследования и ведения пациенток с патологией шейки матки, выявленной при скрининговом исследовании
Приложение 1
Алгоритм обследования и ведения пациенток с патологией шейки матки, выявленной при скрининговом исследовании
| ASC-US [59], [60] |
При наличии ASC-US показано ВПЧ-тестирование.
При отсутствии ВПЧ – ко-тестирование через 3 года.
При обнаружении ВПЧ – кольпоскопия. При выявлении АКК – биопсия, при их отсутствии – ко-тестирование через год.
При ASC-US с положительным ВПЧ-тестом может быть целесообразна сортировка женщин с помощью ИЦХ теста с окрашиванием на р16/Ki67
|
| > ASC-US, после хирургического лечения CIN [59], [60] | ВПЧ-тестирование и кольпоскопия по результатам которых определяется необходимость повторной эксцизии/конизации |
| ASC-H [59] |
ВПЧ-тестирование.
Кольпоскопия с последующей биопсией при АКК, в том числе у женщин моложе 25 лет.
|
| LSIL [61] |
ВПЧ-тестирование, кольпоскопия, при АКК – биопсия.
При отрицательном ВПЧ – повторное ко-тестирование через год.
При отрицательных результатах обоих тестов через год – повторный скрининг через 3 года.
|
| Беременные с LSIL [59] |
ВПЧ-тестирование.
Кольпоскопия.
При отсутствии подозрения на тяжелое поражение (HSIL) – повторное обследование после родов через 8-12 недель.
|
| HSIL [59] | Показана немедленная кольпоскопия. Сортировка на основании результатов повторных мазков или ВПЧ-статус недопустима. При полной визуализации ЗТ проводится петлевая электроэксцизия. При неполной визуализации ЗТ конизация с диагностической и лечебной целью. Деструкция очагов поражения недопустимы. |
| Беременные с HSIL [59] | Показана немедленная кольпоскопия. При отсутствии подозрения на инвазию рекомендовано наблюдение с цитологическим и кольпоскопическим контролем каждые 3 месяца. При подозрении на инвазию – немедленная биопсия. При отсутствии отрицательной динамики обследование через 8-12 недель после родов. |
| AGC [62] |
ВПЧ-тестирвоание.
Кольпоскопия.
Выскабливание цервикального канала, биопсия эндометрия у женщин старше 35 лет.
|
| AIS [62] |
ВПЧ-тестирвоание.
Кольпоскопия.
Конизация шейки матки с последующим выскабливанием цервикального канала и биопсия эндометрия у женщин старше 35 лет.
|
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.