Послеродовые инфекционные осложнения
 Версия: Клинические рекомендации РФ 2024 (Россия)
Версия: Клинические рекомендации РФ 2024 (Россия)
Общая информация
Краткое описание
- Российское общество акушеров-гинекологов
- Корпоративная некоммерческая организация "Ассоциация анестезиологов –реаниматологов"
- Ассоциация акушерских анестезиологов-реаниматологов
Одобрено Научно-практическим Советом Минздрава РФ
В соответствии с Правилами поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 –9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», утвержденных постановлением Правительства Российской Федерации от 19.11.2021 № 1968 с изменения, клинические рекомендации применяются следующим образом:
– размещенные в Рубрикаторе после 1 января 2024 года – с 1 января 2025 года.
Год утверждения: 2024
Пересмотр не позднее: 2026
Дата размещения: 19.07.2024
Статус: Действует
ID: 791
Определение заболевания или состояния (группы заболеваний или состояний)
Послеродовые инфекционные осложнения — заболевания, наблюдаемые у родильниц, непосредственно связанные с беременностью и родами и обусловленные бактериальной инфекцией (от момента родов до конца 6-й недели после родов). В данных клинических рекомендациях рассматриваются следующие основные послеродовые инфекционные осложнения: инфекции области хирургического вмешательства, послеродовой эндометрит, акушерский перитонит, послеродовой сепсис и септический шок.
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
O85 Послеродовой сепсис.
O86.0 Инфекция хирургической акушерской раны.
O86.1 Другие инфекции половых путей после родов.
O86.4 Гипертермия неясного происхождения, возникшая после родов.
O86.8 Другие уточненные послеродовые инфекции.
O88.3 Акушерская пиемическая и септическая эмболия.
O90.0 Расхождение швов после кесарева сечения.
O90.1 Расхождение швов промежности.
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Классификация ИОХВ [50] [1]:
-
поверхностная инфекция области хирургического вмешательства (вовлечение кожи и подкожно-жировой клетчатки);
-
глубокая инфекция области хирургического вмешательства (вовлечение мышц и фасций);
-
инфекция области хирургического вмешательства органа или полости.
Классификация послеродового эндометрита:
-
послеродовой эндометрит после самопроизвольных родов;
-
послеродовой эндометрит после кесарева сечения.
Классификация перитонита [2]:
На сегодняшний день в РФ общепризнанной является классификация перитонитов, предложенная В.С. Савельевым с соавт. и утвержденная на ХI съезде хирургов России в 2011 г.
1. Основной диагноз.
2. Характер развития.
2.1. Первичный.
2.1.1. Спонтанный перитонит у детей.
2.1.2. Спонтанный перитонит у взрослых.
2.1.3. Перитонит, связанный с определенными заболеваниями (туберкулез, сифилис, гонорея).
2.2. Вторичный.
2.3. Третичный.
3. Распространенность.
3.1. Местный (занимающий одну-две анатомические области).
3.1.1. Отграниченный (инфильтрации, абсцесс).
3.1.2. Не отграниченный.
3.2. Распространенный.
3.2.1. Диффузный (от трех до пяти анатомических областей или в пределах одного этажа брюшной полости).
3.2.2. Разлитой (более пяти анатомических областей или два этажа брюшной полости).
4. Экссудат и его примеси.
4.1. Характер экссудата: серозный, фибринозный, гнойный, геморрагический (и их сочетания).
4.2. Примеси: кишечное содержимое, желчь, моча, кровь.
5. Тяжесть состояния в зависимости от выраженности системной воспалительной реакции и полиорганной дисфункции (при возможности определяется в баллах на основании общепринятых шкал).
6. Осложнения.
6.1. Интраабдоминальные: оментит, несформированные кишечные свищи, абсцессы паренхиматозных органов, стресс-повреждения ЖКТ.
6.2. Со стороны передней брюшной стенки и забрюшинной клетчатки: нагноение операционной раны, флегмона брюшной стенки, флегмона забрюшинной клетчатки, эвентpация.
6.3. Экстраабдоминальные: тромбоз глубоких вен, ТЭЛА, пневмония, плеврит, медиастинит.
Согласно Третьему международного консенсусу определений сепсиса и септического шока – «Сепсис-3» (The third international consensus definitions for sepsis and septic shock (Sepsis-3), 2016), в настоящее время выделяют два состояния [3] [51]:
-
Сепсис.
-
Септический шок.
К основной форме может быть добавлено соответствующее уточнение в зависимости от возбудителя инфекции, локализации первичного очага, структуры полиорганной недостаточности.
Термин «тяжелый сепсис» является излишним и в настоящее время не используется.
[1] http://www.cdc.gov/nhsn/PDFs/pscManual/9pscSSIcurrent.pdf
[2] Абдоминальная хирургическая инфекция. Российские национальные рекомендации / Под редакцией академика РАН Б.Р. Гельфанда, академика РАН А.И. Кириенко, профессора Н.Н. Хачатрян. М.: Московское информационное агентство, 2018. 164 с.
[3] Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock 2021.
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Инфекция области хирургического вмешательства (ИОХВ) в большинстве случаев развивается через 4–7 дней после оперативного вмешательства [1]. ИОХВ является полиэтиологичным инфекционным осложнением. Staphylococcus aureus является наиболее распространенным микроорганизмом, достигая частоты 15–20%. Большое значение в этиологии имеют микроорганизмы вида Enterococcus и Escherichia coli [2].
Факторами риска развития ИОХВ после операции кесарева сечения являются: подкожная гематома, хориоамнионит, тяжелая экстрагенитальная патология, курение во время беременности, длина разреза >16,6 см, ИМТ>30–35 кг/м2, прием глюкокортикостероидов, толщина подкожно-жировой клетчатки >3 см, отсутствие антибиотикопрофилактики, гестационный сахарный диабет, продолжительность операции ≥38 мин, гипертензивные расстройства во время беременности, преждевременный разрыв плодных оболочек, кесарево сечения в анамнезе, экстренное кесарево сечение [1,3–9].
Общеизвестна зависимость проявлений ИОХВ от вирулентности и количества микроорганизмов. В патогенезе преимущественное значение имеют высоковирулентные микроорганизмы, которые приводят к локальному повреждению тканей и замедлению ее репарации [10,11]. Однако динамическое взаимодействие между организмом хозяина и патогена, которое приводит к развитию местных и системных проявлений, требует дальнейшего изучения.
Международным институтом раневой инфекции (International Wound Infection Institute) были определены стадии развития раневой инфекции [1].
-
Контаминация раны – это наличие в ране микроорганизмов, которое не приводит к местным или системным проявлениям [10] и завершается развитием ответных иммунных реакций, преимущественно процессов фагоцитоза.
-
Колонизация – это наличие ограниченного роста микроорганизмов, которое не приводит к местным или системным проявлениям [12]. При этом наблюдается некритическое количество микроорганизмов, которое не препятствует своевременной репарации раны.
-
Местная инфекция – это осложнение раневого процесса, при котором увеличение роста микроорганизмов приводит к местным и/или системным проявлениям [12].
-
Распространение инфекции – осложнение раневого процесса, при котором увеличение роста микроорганизмов приводит к их выходу за пределы раны [13].
-
Системная инфекция – осложнение раневого процесса, при котором распространение инфекции по всему организму через сосудистую или лимфатическую системы приводит к возникновению системной воспалительной реакции, сепсису и органной дисфункции.
Послеродовой эндометрит имеет полимикробную природу [14]. В 60–70% случаев инфекцию вызывают как представители аэробной, так и анаэробной флоры. Среди анаэробных возбудителей выделяют Peptostreptococcus, Peptococcus, Bacteroides, Prevotella и Clostridium. Представителями аэробных видов в первую очередь являются Streptococcaceae групп А и В, порядка Enterobacterales, Enterococcaceae, Staphylococcaceae, виды Proteus и Escherichia coli. Ткани матки, поврежденные при кесаревом сечении, особенно чувствительны к Streptococcus pyogenes и Staphylococcus aureus [15–18].
Факторами риска послеродового эндометрита являются: хориоамнионит, ИМТ>30 кг/м2, затяжные роды, преждевременный разрыв плодных оболочек, многократные влагалищные исследования в родах, инвазивная кардиотокография, мекониальные околоплодные воды, отсутствие антибиотикопрофилактики, молодой возраст матери, низкий социально-экономический статус, и бактериальная колонизация нижних отделов половых путей такими бактериями, как Streptococcus agalactiae, Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum, Gardnerella vaginalis [18–22].
Наиболее распространенным фактором риска послеродового эндометрита является кесарево сечение [23,24].
Данный риск возрастает в 21 раз, согласно одним данным [23], и в 30 раз – согласно другим данным в случае выполнения операции кесарева в экстренном порядке в родах [18].
Патогенез послеродового эндометрита в настоящее время остается до конца неизученным. Ранняя манифестация послеродового эндометрита чаще всего связана с микробной колонизацией околоплодных вод и децидуальной оболочки до родов [25].
Кроме того, существует взаимосвязь между воспалительно-инфекционными заболеваниями и замедлением инволютивных процессов в послеродовом периоде.
Основными путями распространения инфекции при послеродовом эндометрите являются:
а) восходящий;
б) гематогенный (диссеминация бактерий из первичного экстрагенитального очага);
в) лимфогенный (через систему региональных сосудов, чему способствуют обширные дефекты эндометрия и травмы половых органов);
г) интраамниальный, связанный с применением в клинической практике инвазивных методов исследования [26].
При физиологическом течении пуэрперального периода область плацентарной площадки представляет собой обширную асептическую рану. Наблюдаются инфильтрация раневой поверхности лейкоцитами, эпителизация и регенерация эндометрия без образования воспалительного инфильтрата и некроза [27]. При наличии предрасполагающих факторов наблюдается развитие воспалительного лимфоцитарного и лейкоцитарного инфильтрата в области раневой поверхности с постепенным переходом на область миометрия. При прогрессировании заболевания возможны переход воспалительного процесса на серозный покров матки, образование абсцесса малого таза, тромбофлебита таза, а также развитие акушерского перитонита [28].
Акушерский перитонит характеризуется полиэтиологичной природой. Согласно данным обсервационного исследования внутрибрюшных инфекций, во всем мире (CIAOW) отмечается рост числа резистентных микроорганизмов [29]. Основным этиологическим фактором могут быть Escherichia coli, Klebsiella pneumoniae, виды Enterococcus, виды Pseudomonas [30].
В патогенезе акушерского перитонита наблюдается смена острого провоспалительного ответа на смешанный противовоспалительный ответ со сбалансированными про- и противовоспалительными медиаторами. Дальнейшее наступление синдрома компенсаторного противовоспалительного ответа является одним из предрасполагающих факторов повышения восприимчивости организма ко вторичным инфекционным осложнениям [31]. Перитонит сопровождается стойким повышением внутрибрюшного давления, значение которого составляет ≥12 мм рт.ст. Синдром абдоминального компартмента характеризуется устойчивым повышением давления >20 мм рт.ст. в брюшной полости, ведущим к нарушению перфузии тканей и способствующим снижению функциональной активности органов вплоть до их недостаточности [32]. При этом отмечается взаимосвязь между возрастанием уровня внутрибрюшного давления и риском 28- и 90-дневной смертности [33].
Послеродовой сепсис является полиэтиологическим заболеванием, которое может быть вызвано большинством патогенных и условно-патогенных микроорганизмов. К основным возбудителям послеродового сепсиса относят: Streptococcus pyogenes, Escherichia coli, Streptococcus pneumoniae, Clostridium septicum, Morganella morganii, Staphylococcus aureus [34]. В настоящее время наблюдается увеличение частоты метициллинорезистентных штаммов Staphylococcus aureus как этиологического фактора послеродового сепсиса [37, 38].
К факторам риска послеродового сепсиса относятся: ожирение, нарушение углеводного обмена (нарушение толерантности к глюкозе, сахарный диабет), нарушение иммунного ответа (получение иммуносупрессивной терапии), анемия, воспалительные заболевания органов малого таза в анамнезе, проведение амниоцентеза и других инвазивных процедур во время беременности, серкляж, длительный безводный промежуток, родовой травматизм (разрывы влагалища), кесарево сечение, гематома послеоперационной раны, задержка остатков плацентарной ткани или плодных оболочек, инфекция, ассоциированная с β-гемолитическим стрептококком группы А у членов семьи пациента [36, 39–41].
Патогенез сепсиса на клеточном и молекулярном уровнях чрезвычайно сложен. Инвазия патогенов в организм приводит к активации врожденного иммунитета посредством процессов взаимодействия между патоген-ассоциированными молекулярными паттернами (PAMP) и паттерн-распознающими рецепторами (PRR), которые приводят к синтезу макрофагами провоспалительных цитокинов [40–42].
[1] International Wound Infection Institute (IWII). Wound infection in clinical practice. Wounds International 2016
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Несмотря на успешную борьбу с инфекцией в клинической медицине, сепсис и септический шок все еще являются одними из ведущих причин смерти, что связано со многими медицинскими, социальными и экономическими факторами [43–45].
Согласно данным ВОЗ (2014 г.), показатель материнской смертности в результате гнойно-септических осложнений в странах с низким и средним уровнем дохода составляет 10,7% и превышает более чем в два раза данный показатель в странах с высоким уровнем дохода (4,7%) [44].
По данным Глобального исследования материнского и неонатального сепсиса (GLOSS, 2020 г.), которое проходило в 52 странах, частота материнской инфекции составила 70,4 (95% ДИ 67,7–73,1) женщин на 1000 живорожденных детей, а частота неблагоприятных исходов (тяжелые акушерские осложнения «near miss» и материнская смерть) – 10,9 (95% ДИ 9,8–12,0) на 1000 живорожденных детей. Самые высокие значения наблюдались в странах с низким и средним уровнем дохода, а самые низкие – в странах с высоким уровнем дохода [46].
В Российской Федерации септические осложнения занимают пятое место в структуре материнской смертности. По данным Министерства здравоохранения РФ, доля септических осложнений имела тенденцию к росту в 2018 г. и составила 7,5% в структуре материнской смертности [1].
По данным статистического сборника Минздрава России (основные показатели здоровья матери и ребенка, деятельности службы охраны детства и родовспоможения в РФ), заболеваемость женщин распространенной послеродовой инфекцией и сепсисом составила в 2005 г. 1,31, в 2010 – 0,51, в 2015 – 0,19, в 2017 – 0,17, в 2018 – 0,18 на 1000 родов [2].
ИОХВ осложняет послеродовой период у 2–7% пациентов [47,48].
Послеродовой эндометрит является наиболее распространенной послеродовой инфекцией. Частота послеродового эндометрита после самопроизвольных родов составляет 1–3%, после оперативных родов путем операции кесарева сечения возрастает до 27% [20].
Среди женщин, которым была назначена антибиотикопрофилактика, частота послеродового эндометрита составляет примерно 7,0% в случае выполнения кесарева сечения после начала родовой деятельности и 1,5% – в случае плановой операции [49]. При отсутствии антибиотикопрофилактики частота послеродового эндометрита составляет примерно 18 и 4% соответственно [49].
Частота перитонита после кесарева сечения варьирует в различных стационарах от 0,1 до 1,5% [34].
[1] Материнская смертность в Российской Федерации в 2018 г. Методическое письмо МЗ РФ от 18.09.19 №15-4/и/2-8714.
[2] https://minzdrav.gov.ru/ministry/61/22/stranitsa-979/statisticheskie-i-informatsionnye-materialy/statisticheskiy-sbornik-2018-god
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Классическими признаками ИОХВ являются гиперемия, повышение местной температуры, отек тканей, болевой синдром, снижение репарации раны, появление гнойного отделяемого, присоединение неприятного запаха [52].
Скрытыми признаками ИОХВ могут быть избыточный рост грануляционной ткани, наличие патологических легко кровоточащих грануляций, увеличение раневой поверхности, возрастание болевого синдрома [52–55].
При распространении местной инфекции могут наблюдаться нарастание области гиперемии, расхождение краев раны, лимфаденит. Системные признаки неспецифичны и проявляются общей слабостью и потерей аппетита [13].
Основные симптомы послеродового эндометрита:
-
Фебрильная температура тела (>38ºC).
-
Тазовая боль или болезненность матки при пальпации.
-
Выделения с неприятным запахом или гнойные выделения из половых путей.
-
Субинволюция матки.
Дополнительные симптомы послеродового эндометрита:
-
Умеренное кровотечение из половых путей.
-
Неспецифические симптомы: слабость, озноб, снижение аппетита, головная боль [19,55].
Клиническая характеристика фаз течения перитонита:
-
Реактивная фаза (продолжительность 24 ч).
-
Токсическая фаза (продолжительность 24–72 ч).
-
Терминальная фаза (продолжительность свыше 7 ч).
В клинической картине акушерского перитонита рекомендовано выделять раннее начало (на 1–2-е сутки после операции), гипертермию (температура тела 39,0°С и выше), выраженную тахикардию, парез кишечника.
В зависимости от времени послеоперационного периода к концу 2-х суток развивается паралитическая непроходимость кишечника, с 3–4-х суток после операции отмечаются нарастание признаков интоксикации, экссудация в брюшную полость, транссудация в кишечник, на 4–9-е сутки развивается перитонит на фоне эндометрита и несостоятельности швов на матке, сопровождающихся обильными гнойными выделениями из влагалища и попаданием содержимого матки в брюшную полость [34,56].
Клинические признаки послеродового сепсиса:
-
Лихорадка, озноб.
-
Гипотермия.
-
Генерализованная макуло-папулезная сыпь.
-
Инъекция склер.
-
Тахикардия (более 90 ударов в минуту).
-
Тахипноэ.
-
Гипотензия.
-
Олигурия.
-
Слабость, снижение аппетита.
-
Нарушение сознания.
-
Диарея, рвота, боль в животе.
-
Признаки ИОХВ.
-
Субинволюция матки.
-
Патологические выделения из половых путей с неприятным запахом.
-
Симптомы инфекции мочевыводящих путей.
-
Отсутствие адекватного ответа организма на лечение [36, 39, 61].
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза ИОХВ [1]:
-
гнойное отделяемое из раны;
-
повышение температуры тела >38°С;
-
локализованная боль, отек, гиперемия, повышение местной температуры уплотнение в области послеоперационной раны.
Критерии установления диагноза послеродового эндометрита [2]:
-
лихорадка (>38°C);
-
болезненность матки;
-
тазовая и параметральная боль;
-
гнойные лохии;
-
лейкоцитоз по данным общего (клинического) анализа крови.
Критерии установления диагноза акушерского перитонита [3].
Для реактивной фазы характерны:
-
интенсивный болевой синдром, защитное напряжение мышц передней брюшной стенки;
-
рвота, возбуждение, тахикардия (100–120 в минуту), гипертензия, тахипноэ (24–28 в минуту);
-
лихорадка в пределах 38ºC.
-
умеренный лейкоцитоз со сдвигом лейкоцитарной формулы влево.
Для токсической фазы характерны:
-
превалирование признаков общей тяжелой интоксикации;
-
тахикардия (120 в минуту и выше), умеренная гипотензия, рвота застойным содержимым;
-
гектический характер лихорадки;
-
высокий лейкоцитоз, токсическая зернистость нейтрофилов, сдвиг формулы влево;
-
разлитой характер боли без четкой локализации.
Для терминальной фазы характерно:
-
прогрессирование перитонеального сепсиса.
Абдоминальный сепсис диагностируется в случае наличия инфекции и органных нарушений. На начальных этапах госпитализации органная дисфункция диагностируется при оценке по шкале qSOFA >2 баллов [58].
Критерии послеродового сепсиса [51]:
-
подтвержденная инфекция;
-
органная дисфункция (оценка два балла и более по шкале SOFA, см. ниже и в Приложении Г4);
Критерии септического шока:
-
персистирующая артериальная гипотензия, требующая вазопрессорной терапии для поддержания среднего артериального давления ≥65 мм рт. ст.;
-
уровень молочной кислоты (лактата) в крови >2 ммоль/л, несмотря на адекватную инфузионную терапию.
[1] http://www.cdc.gov/nhsn/PDFs/pscManual/9pscSSIcurrent.pdf
[2] WHO Recommendations for Prevention and Treatment of Maternal Peripartum Infections. Geneva: World Health Organization; 2015.
[3] Абдоминальная хирургическая инфекция. Российские национальные рекомендации / Под редакцией академика РАН Б.Р. Гельфанда, академика РАН А.И. Кириенко, профессора Н.Н. Хачатрян. М.: Московское информационное агентство, 2018. 164 с.
1. Жалобы и анамнез
-
Рекомендовано у всех пациентов при поступлении в стационар по поводу родоразрешения проводить сбор анамнеза и жалоб с целью оценки риска послеродовых инфекционных осложнений [59–61].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии. При сборе анамнеза особое внимание необходимо уделить наличию следующих факторов (см. также раздел Этиология и патогенез):
- перенесенные ранее гнойно-септические осложнения, в особенности связанные с беременностью, родами и гинекологическими заболеваниями;
- наличие очага хронической или острой инфекции;
- наличие иммунодефицитных состояний, а также состояний, потребовавших иммуносупрессивной терапии;
- наличие нарушений углеводного обмена (нарушение толерантности к глюкозе, сахарный диабет), ожирение;
- наличие вредных привычек;
- инвазивные манипуляции или оперативные вмешательства во время беременности;
- данные о длительном приеме антибактериальных препаратов;
- длительная госпитализация (более семи суток);
- наличие анамнестических данных о колонизации нижних отделов половых путей такими бактериями, как Streptococcus agalactiae, Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum, Gardnerella vaginalis.
При сборе жалоб особое внимание следует уделить жалобам на:
- головокружение,
- дезориентацию,
- слабость,
- одышку,
- боль и дискомфорт различной локализации,
- потливость,
- появление сыпи на кожных покровах,
- выделения из половых путей измененного цвета или запаха,
- лихорадку, озноб,
- учащённое сердцебиение,
- снижение мочеотделения,
- жидкий стул.
2. Физикальное обследование
-
Рекомендованы визуальный контроль состояния и пальпация кожи и мягких тканей в области послеоперационной раны после кесарева сечения, эпизиотомии и акушерских травм, а также в местах установки внутривенных канюль или инъекций с целью своевременной диагностики ИОХВ [59,62,63].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
-
С целью своевременного выявления послеродовых инфекционных осложнений, оценки гемодинамического статуса рекомендован мониторинг состояния пациентов в послеродовом периоде, включающий [64]:
- исследование пульса;
- термометрию общую;
- измерение частоты дыхательных движений;
- измерение артериального давления на периферических артериях [59,64,65,66].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
-
Рекомендовано при подозрении на послеродовую инфекцию с целью ее своевременной диагностики выполнение бимануального влагалищного исследования [67].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендована пальпация брюшной стенки при подозрении на акушерский перитонит с целью дифференциальной диагностики, определения тактики дальнейшего обследования и лечения [16,59,60,68–70].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии. При пальпации выявляется болезненность во всех областях живота, которая может быть более выраженной в проекции патологического процесса. Основными перитонеальными симптомами являются: симптом Щеткина–Блюмберга, симптом Менделя, симптом Воскресенского, симптом Бернштейна.
-
Рекомендована оценка состояния пациента с использованием одной из следующих шкал в качестве инструмента скрининга сепсиса и/или септического шока:
- на догоспитальном этапе и вне палаты интенсивной терапии [51,71–73]:
-
быстрой шкалы последовательной оценки органной недостаточности qSOFA (quick Sequential Organ Failure Assessment) (Приложение Г1) [51];
-
критериев синдрома системного воспалительного ответа SIRS (Приложение Г2) [74];
-
модифицированная акушерская шкала раннего предупреждения MEOWS (Приложение Г3) [75,76];
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
- в ОРИТ шкалы SOFA (Приложение Г4) [51].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: В систематическом обзоре и метаанализе 2018 г., в которые вошли 10 исследований и 229 480 пациентов, было показано, что шкала SIRS значительно превосходила qSOFA в диагностики сепсиса, а qSOFA была незначительно лучше SIRS в прогнозировании госпитальной смертности [71]. Несмотря на то что шкала qSOFA способствует быстрому выявлению пациентов, имеющих высокий риск неблагоприятных исходов и требующих эскалации терапии, нецелесообразно ее преимущественное применение по сравнению с другими шкалами (SIRS или MEWS) для скрининга органной дисфункции [71]. Необходимо помнить, что критерии SIRS часто совпадают с нормальными физиологическими параметрами во время беременности и в раннем послеродовом периоде [77]. В клинической практике с целью оценки органной дисфункции у беременных и женщин в послеродовом периоде также получила распространение шкала сепсиса в акушерстве (Sepsis in obstetrics score – SOS), которая является модификацией общепринятых шкал и учитывает физиологические изменения во время беременности, однако данных о ее эффективности сегодня недостаточно, необходимо проведение дальнейших исследований с целью оценки эффективности применения данной шкалы [78,79].
3. Лабораторные диагностические исследования
-
Рекомендован общий (клинический) анализ крови с исследованием уровня лейкоцитов в крови при подозрении на инфекционное послеродовое осложнение с целью своевременной диагностики [51,59,80–82].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
-
Рекомендовано микробиологическое (культуральное) исследование гнойного отделяемого на аэробные и факультативно-анаэробные микроорганизмы и иного биологического материала пациента (отделяемое женских половых органов, кровь на стерильность, перитонеальная жидкость, мокрота, ликвор, моча) с целью идентификации возбудителей, количественной оценки микробной обсемененности и определения чувствительности к антибактериальным препаратам [59,73,82].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии: Сбор биологических материалов рекомендовано проводить до назначения антибиотикотерапии во всех случаях, если это не приведет к задержке противомикробной терапии (не более 45 минут) [73,83]. Соответствующие рутинные микробиологические исследования всегда должны включать не менее 2 образцов крови (аэробная и анаэробная среда в каждом) [84]. Идентификация инфекционного агента при сепсисе представляет сложную задачу в связи с широким разнообразием возбудителей сепсиса, среди которых многие являются частью нормальной микрофлоры человека. В целях ускорения идентификации возбудителя, выявления некультивируемых микроорганизмов, а также идентификации факторов антибиотикорезистентности рекомендованы в качестве дополнительных к микробиологическому (культуральному) исследованию гнойного отделяемого на аэробные и факультативно-анаэробные микроорганизмы и иного биологического материала пациента методы молекулярно-биологического анализа – гибридизационные методы, полимеразная цепная реакция и протеомный анализ методом масс-спектрометрии (MALDI-TOF) [85–89]. Преимуществами данных методов являются сокращение времени анализа, возможность раннего выявления некультивируемых микроорганизмов, а также идентификации факторов антибиотикорезистентности [89]. В настоящее время данные методы диагностики малодоступны, но могут быть рекомендованы в качестве дополнительных при обеспечении лабораторий.
-
Рекомендовано при подозрении на сепсис исследование уровня лактата в сыворотке крови (исследование уровня молочной кислоты в крови) с целью его диагностики и выбора тактики лечения [59,83,90–95].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарии: Уровень молочной кислоты (лактата) не является прямым показателем перфузии тканей [96]. Повышение уровня лактата в крови может свидетельствовать о гипоксии тканей, усилении аэробного гликолиза и других факторах. Независимо от причины повышение уровня лактата ассоциировано с наиболее неблагоприятными исходами [97]. Если исходный уровень лактата >2 ммоль/л, целесообразно производить повторные исследования в течение каждых 2–4 ч до нормализации его уровня [90].
-
Рекомендовано при подозрении на послеродовое инфекционное осложнение с целью ранней диагностики исследование уровня С-реактивного белка в сыворотке крови [98–102].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3)
Комментарии: Несмотря на низкую специфичность, определение уровня С-реактивного белка обладает высокой чувствительностью на ранних стадиях сепсиса [98]. В исследовании выявлено, что у родильниц на третьи сутки послеродового периода чувствительность в отношении послеродового эндометрита уровня С-реактивного белка выше 60 мг/мл составила 79 % (95 % ДИ 68-86), специфичность - 93 % (95 % ДИ 85-98) [100]. По результатам ряда исследований также было выявлено, что первые два дня после родов уровень С-реактивного белка повышен, что может усложнить оценку наличия инфекции [101,103,104]. При доступности метода рекомендовано исследование уровня пресепсина в крови у пациентов с подозрением на сепсис или септический шок, а также у пациентов с подтверждённым диагнозом в целях контроля состояния пациента и своевременной коррекции терапии [105–107]. По данным метаанализа, в которое были включены 9 публикаций и 1561 пациент, показано, что пресепсин может служить эффективным диагностическим маркером, а также предиктором смерти при сепсисе (AUC составила 0,77 (95% ДИ 0,73–0,81) с объединенной прогностической чувствительностью (SEN) и специфичностью (SPE) (0,83 (95% ДИ 0,72–0,90) и 0,69 (95% ДИ 0,63–0,74) соответственно) [107].
-
При подозрении на сепсис или септический шок не рекомендовано исследование уровня прокальцитонина в крови для решения вопроса о начале антибактериальной терапии по сравнению с клинической оценкой [73,108–110].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. Исследование уровня прокальцитонина в крови рекомендовано лишь наряду с клинической оценкой для решения вопроса о длительности антибактериальной терапии у пациентов с сепсисом или септическим шоком в случае адекватного контроля за источником сепсиса и/или септического шока [73,108–110].
-
Рекомендован анализ крови биохимический общетерапевтический с целью своевременной диагностики органной дисфункции и выбора тактики лечения у пациентов с сепсисом [51,111].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендована коагулограмма (ориентировочное исследование системы гемостаза) с целью своевременной диагностики органной дисфункции и выбора тактики лечения у пациентов с сепсисом [82,111–115].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендовано исследование уровней натрия, калия, хлоридов в крови у пациентов с сепсисом и септическим шоком с целью выявления электролитных нарушений и коррекции терапии [59].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
4. Инструментальные диагностические исследования
-
Рекомендовано при возможности медицинской организации с целью оценки гемодинамического статуса и выбора тактики лечения у пациентов с сепсисом и/или септическим шоком проведениеэхокардиографии (ЭхоКГ) [116–119].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
-
Рекомендована пульсоксиметрия (мониторирование насыщения гемоглобина кислородом при помощи пульсоксиметра (SpO2)) для оценки степени гипоксемии у пациентов с сепсисом/септическим шоком [59,66,73,120–123].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: снижение SpO2 ниже 90% соответствует снижению PaO2 ниже 60 мм рт.ст. согласно кривой диссоциации оксигемоглобина [124].
-
Рекомендовано пациентам с подозрением на послеродовое инфекционное осложнение выполнение ультразвукового исследование органов малого таза (комплексного) и/или компьютерной томографии (КТ) органов малого таза и/или магнитно-резонансной томографии (МРТ) органов малого таза с целью дифференциальной диагностики, выявления абсцесса малого таза, гематомы, метротромбофлебита, параметрита [59,125–129].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. Эхографическая картина при послеродовом эндометрите обладает большим полиморфизмом, что не позволяет рекомендовать данный метод в качестве диагностического при послеродовом эндометрите [125,130,131]. Однако УЗИ органов малого таза имеет клиническое значение для обнаружения остатков плацентарной ткани и абсцесса малого таза [95, 97].
-
Рекомендовано при подозрении на акушерский перитонит выполнение ультразвукового исследования органов брюшной полости (комплексного) и/или КТ органов брюшной полости в целях установления диагноза [69,132–134].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии. В случае неубедительных данных УЗИ органов брюшной полости рекомендовано проведение КТ органов брюшной полости [135–137].
-
Рекомендовано пациентам с сепсисом/септическим шоком выполнение рентгенографии легких и/или КТ легких с целью оценки наличия повреждения легких, дифференциальной диагностики и выбора тактики респираторной терапии в случае наличия сепсис-индуцированного ОРДС [138–142].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии. Чувствительность рентгенографии легких при ОРДС в случае наличия билатеральных инфильтратов (ведущий симптом ОРДС) составляет около 75%, а специфичность – 70% [104, 105].
-
Рекомендовано у пациентов с септическим шоком использование инвазивного мониторинга гемодинамики для отслеживания сердечной деятельности и адекватности сердечного выброса с целью своевременных выявления нарушений кровообращения, коррекции тактики лечения, оценки ее эффективности при наличии возможности медицинской организации [144–148].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии: В настоящее время отсутствуют крупные рандомизированные исследования, сравнивающие инвазивный мониторинг артериального давления с неинвазивными методами. Принимая во внимание низкий уровень осложнений и, вероятно, более высокую точность измерения артериального давления, преимущества артериальных катетеров, вероятно, перевешивают риски. Однако, необходимо учитывать потенциально ограниченные ресурсы в некоторых странах и отсутствие высококачественных исследований по данному методу. Таким образом, группа экспертов дала слабую рекомендацию в пользу применения артериального катетера. Для сведения к минимуму риска осложнений артериальные катетеры следует незамедлительно удалять в случае, когда отсутствует необходимость в постоянном гемодинамическом мониторинге.
5. Иные диагностические исследования
-
Рекомендован прием (осмотр, консультация) врача-хирурга первичный пациентам с ИОХВ для оценки необходимости хирургического лечения [59,149].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
-
Рекомендован прием (осмотр, консультация) врача - клинического фармаколога первичный пациентам с сепсисом с целью коррекции проводимой терапии [59,150,151].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
1. Лечение ИОХВ
-
Рекомендовано при ИОХВ проведение антибактериальной терапии в комбинации с хирургической обработкой и санацией раны или инфицированной ткани [59,152–154].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Хирургическая обработка гнойно-некротического очага проводится с адекватным дренированием, удалением некротизированных тканей с целью предупреждения дальнейшего распространения инфекции. Кроме того, необходимо производить контроль путей распространения инфекции на уровне подкожно-жировой клетчатки, фасций, сухожилий и межмышечных пространств [152]. Рекомендовано наложение вторичных швов после хирургической обработки раны у пациентов с ИОХВ, что связано с более быстрой репарацией раны по сравнению с заживлением вторичным натяжением [155].
-
Рекомендовано в качестве стартовой антибактериальной терапии назначение эмпирической терапии антибактериальных препаратов системного действия [156–158].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Возможные эмпирические схемы антибактериальной терапии (в дальнейшем антибактериальная терапия может быть изменена на основании результата микробиологического исследования и чувствительности) [152]:
- пероральный прием - Амоксициллин + [Клавулановая кислота]** 875/125 мг каждые 12 ч;
- ципрофлоксацин** 500 мг каждые 12 ч + Метронидазол** 500 мг каждые 8 ч.;
2. Лечение послеродового эндометрита
-
Рекомендована при послеродовом эндометрите антибактериальная терапия антибактериальными препаратами системного действия [21, 26, 63].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии. Метаанализ 2015 г., который включил 40 рандомизированных испытаний и 4240 пациентов, показал, что комбинированная терапия, включающая внутривенное введение клиндамицина** c гентамицином**, показала более высокую эффективность при лечении послеродового эндометрита по сравнению с другими антибактериальными препаратами или комбинациями антибактериальных препаратов. Ни в одном из исследований не сообщалось о материнской смертности и различиях по частоте серьезных осложнений при применении различных групп антибактериальных препаратов [20].
Возможные схемы эмпирической антибактериальной терапии (в дальнейшем антибактериальная терапия может быть изменена на основании результата микробиологического исследования и чувствительности):
Перорально:
- Амоксициллин** 500 мг каждые 8 ч + Метронидазол** 500 мг каждые 8 ч [159];
- Амоксициллин + [Клавулановая кислота]** 875 мг+125 мг каждые 12 ч [159];
Внутривенно:
- Клиндамицин** 900 мг каждые 8 ч внутривенно + # Гентамицин** 5 мг/кг (для взрослых с нормальной функцией почек) внутривенно каждые 24 ч [20].
Использование карбапенемов возможно при получении результатов микробиологического исследования полирезистентных вариантов условно-патогенных микроорганизмов или при отсутствии клинической эффективности в течении 48-72 часов.
3. Лечение акушерского перитонита
-
Рекомендована при перитоните эмпирическая терапия антибактериальными препаратами системного действия [132].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. Ключевыми факторами эффективного лечения акушерского перитонита являются своевременная диагностика, адекватные реанимационные мероприятия, раннее начало антибактериальной терапии, контроль и санация источника инфекции, а также переоценка клинического ответа и соответствующая коррекция стратегии ведения [132].
Исследование по мониторингу тенденций устойчивости к противомикробным препаратам (SMART) предоставляет данные исследований in vitro о чувствительности к антимикробными препаратам грамотрицательных бактерий при внутрибрюшных инфекциях с 2002 г. [160]. Результаты локальных исследований резистентности и фармакоэпидемиологии противоинфекционных средств позволяют обеспечить адекватную антимикробную терапию [160,161]. Комитет экспертов ВОЗ рекомендует при осложненных инфекциях брюшной полости применение в качестве терапии первого выбора пиперациллин + [тазобактам], в качестве терапии второго выбора – меропенем** [1].
4. Лечение сепсиса, септического шока
Необходимо обратить внимание, что сегодня исследования по вопросам акушерского сепсиса по этическим причинам практически отсутствуют, принципы терапии акушерского сепсиса в значительной степени экстраполируются из общей популяции.
Ранняя целенаправленная интенсивная терапия повышает выживаемость пациентов с септическим шоком. Проведение неотложной терапии в течение первых 6 ч от начала реанимации способно снизить 28-дневную летальность.
Ключевым моментом тактики ведения пациентов с сепсисом является неотложность оказываемой медицинской помощи. Раннее выявление и незамедлительное лечение улучшают исходы заболевания [61, 89, 107–110].
4.1 Антибактериальная терапия
-
При подозрении на септический шок или высокую вероятность сепсиса у пациента рекомендовано начать эмпирическую терапию антибактериальными препаратами системного действия в течение 1 часа [72,73,165,166].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии. Своевременное раннее лечение высокими дозами внутривенных антибиотиков широкого спектра действия (антибактериальные препараты системного действия) повышает вероятность благоприятного исхода. Задержка адекватной антибактериальной терапии после развития клинической симптоматики сепсиса ассоциирована с увеличением смертности [166–169], а каждый час задержки адекватной антибактериальной терапии снижает выживаемость пациентов [110, 118]. При выборе эмпирической антимикробной терапии крайне важным является учет локальных данных. Результаты локальных исследований резистентности и фармакоэпидемиологии противоинфекционных средств позволяют обеспечить адекватную антимикробную терапию[160,161].
В 2019 г. ВОЗ начала глобальную кампанию, призывающую правительства применять разработанную классификацию антибиотиков AWaRe, которая представляет собой базу из антибактериальных препаратов, разделенных на три группы – доступа (Access), наблюдения (WAtch), резерва (REserve), с целью борьбы со снижением устойчивости к противомикробным препаратам[2]. Был принят новый целевой показатель на основании классификации AWaRe, который ставит задачу обеспечить на уровне страны не менее 60% используемых антибиотиков из группы доступа[3]. При наличии возможности эти данные следует учитывать при выборе противомикробной терапии.
-
Рекомендовано проводить антибактериальную терапию пациентам с клиническими признаками сепсиса или подтвержденным сепсисом в зависимости от анатомического места инфекции в соответствии с имеющимися клиническими рекомендациями по нозологическим формам [59].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии. Если развитие сепсиса связано с локализацией очага инфекции в матке, то выбор возможных схем антибактериальной терапии основан на рекомендациях лечения послеродового эндометрита.
Коррекцию антибактериальной терапии следует проводить на основании результатов культурального исследования через 48–72 ч после начала лечения при отсутствии улучшения клинико-лабораторных показателей, свидетельствующих о положительной динамике в течение заболевания и/или резистентности возбудителя к проводимой терапии [170].
-
Рекомендовано рассмотрение вопроса о деэскалационной стратегии антибактериальной терапии пациентам с клиническими признаками сепсиса или подтвержденным сепсисом после получения результатов микробиологического (культурального) исследования крови и других биологических материалов с определением чувствительности к антибактериальным препаратам [171–173].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии. Деэскалационная антибактериальная терапия не повышает смертность пациентов с сепсисом и/или септическим шоком [171–174], однако дает возможность ограничения использования антибиотиков широкого спектра действия, что имеет значение в борьбе с развитием устойчивости микроорганизмов к антибактериальным препаратам. В дальнейшем антибактериальную терапию пациентам следует корректировать на основании результата микробиологического исследования и чувствительности, если они доступны.
4.2 Инфузионная терапия
-
Рекомендовано внутривенное введение кристаллоидных растворов (B05BB: Растворы, влияющие на водно-электролитный баланс) в дозе 30 мл/кг в течение первых 3 ч терапии при развитии сепсиса и/или септического шока с обязательным контролем переносимости инфузии [73].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий. При нарастании признаков перегрузки правых отделов сердца рекомендованы снижение темпа инфузионной терапии и индивидуальный подбор объема вводимой инфузионной терапии [175].
-
Рекомендовано продолжать инфузионную терапию после начальной терапии под контролем динамических гемодинамических характеристик [73].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. ЦВД, систолическое артериальное давление и частота сердечных сокращений являются менее информативными показателями волемического статуса. Более показательными являются нарастание сердечного выброса в ответ на изменения внутригрудного давления или прирост ударного объема в ответ на болюсы в 1–3 мл/кг. При недоступности ЭхоКГ возможно проведение теста с поднятием ног на 45° в течение 60–90 секунд с приростом пульсового артериального давления более чем на 15% [176–178]. Недостаточно данных о преимуществах либеральной инфузионной стратегии по сравнению с ограничительной при сепсисе и септическом шоке в первые 24 ч в отношении снижения смертности [179].
-
Рекомендовано для инфузионной терапии пациентов с сепсисом и/или септическим шоком рассмотреть вопрос об использовании сбалансированных кристаллоидов (B05BB: Растворы, влияющие на водно-электролитный баланс) вместо изотонического раствора натрия хлорида** [73,180,181].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1)
Комментарии. В метаанализе 14 РКИ, в котором оценивалась эффективность инфузионной терапии для пациентов с сепсисом и септическим шоком, было показано, что применение сбалансированных кристаллоидов по сравнению с изотоническим раствором натрия хлорида было связано со снижением смертности пациентов с септическим шоком [180]. В кластерном рандомизированном исследовании «SMART» 2018 года 30-дневная смертность пациентов в критическом состоянии была ниже в группе с применением сбалансированных кристаллоидных растворов по сравнению с группой, где применялся физиологический раствор (ОШ 0,90; 95% ДИ=0,67-0,94) [181]. (приложение А3)
-
Рекомендовано дополнение инфузионной терапии альбумином человека** (B05AA - Кровезаменители и препараты плазмы крови) в случае повышенной потребности в инфузии кристаллоидных растворов (B05BB: Растворы, влияющие на водно-электролитный баланс) при развитии сепсиса и/или септического шока [180,182–184].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Комментарии: Применение альбумина человека** (B05AA - Кровезаменители и препараты плазмы крови) в качестве инфузионной терапии является безопасным [182], а также эффективным в снижении смертности пациентов с сепсисом и/или септическим шоком [138, 139].
-
Не рекомендовано применение гидроксиэтилкрахмала** (B05AA - Кровезаменители и препараты плазмы крови) у пациентов с сепсисом и септическим шоком в связи с высоким риском развития нежелательных явлений и летального исхода [73,180,185].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: Препараты гидроксиэтилкрахмала** противопоказаны к применению при сепсисе и септическом шоке, так как связаны с высоким риском летального исхода [180]. Кроме того, применение гидроксиэтилкрахмала** связано с повышением потребности заместительной почечной терапии у пациентов с сепсисом и септическим шоком [185].
4.3 Вазопрессорная терапия
-
У пациентов с септическим шоком рекомендовано применение норэпинефрина** (C01CA - Адренергические и дофаминергические средства) в качестве препарата первой линии вазопрессорной терапии для достижения целевого значения среднего артериального давления более 65 мм рт.ст. [186,187].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии. Немедленное восстановление перфузионного давления в жизненно важных органах является одной из ключевых задач реанимационных мероприятий у пациентов с сепсисом и/или септическим шоком. Применение норэпинефрина** связано с более низким показателем смертности, а также более низким риском развития аритмий у пациентов с септическим шоком по сравнению с допамином** [141, 142].
-
Для достижения целевого значения среднего артериального давления более 65 мм рт.ст. при недостаточной эффективности норэпинефрина** рекомендовано применение комбинации норэпинефрина** с эпинефрином** у пациентов с сепсисом и/или септическим шоком [73].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Не рекомендовано применение допамина** в качестве препарата первой линии вазопрессорной терапии у пациентов с сепсисом и/или септическим шоком [186].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: Исследования демонстрируют более низкие показатели смертности при применении норэпинефрина** у пациентов с септическим шоком по сравнению с допамином**. Кроме того, применение допамина** чаще вызывает нарушения сердечного ритма у пациентов с сепсисом и/или септическим шоком по сравнению с норэпинефрином** [142, 143].
-
У пациентов с септическим шоком и персистирующей гипоперфузией тканей, несмотря на адекватную инфузионную и вазопрессорную терапию, либо у пациентов с дисфункцией миокарда, установленной на основании etСО2 и ЭхоКГ, рекомендовано в качестве инотропной терапии добавление добутамина** (C01CX: Другие кардиотонические средства) к норэпинефрину** либо применение только эпинефрина** [73,190].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии. Несмотря на отсутствие рандомизированных плацебо-контролируемых исследований по оценке клинических исходов, применение добутамина** в качестве препарата выбора при инотропной терапии в исследованиях не показало увеличение смертности пациентов с сепсисом и/или септическим шоком. При этом инотропная терапия добутамином** с рутинным увеличением сердечного индекса до сверхнормальных значений не приводит к улучшению исходов у пациентов с сепсисом и/или септическим шоком [145, 146]. В настоящее время отсутствуют сравнительные исследования по эффективности добутамина** и эпинефрина**, согласно данным сетевого метаанализа, были получены одинаковые показатели смертности при применении как первого, так и второго препарата [190].
-
Не рекомендовано рутинное использование левосимендана** для терапии септического шока [73,193,194].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 1)
Комментарий. В метаанализе трех РКИ было показано, что левосимендан** не снижает смертность при септическом шоке по сравнению с отсутствием ионотропных препаратов (ОШ 0,87; 95% ДИ=0,59-1,28) [194]. Во другом метаанализе, основанном на 7 РКИ, было показано, что левосимендан не превосходит добутамин в отношении снижения смертности пациентов с септическим шоком(ОШ 0,80; 95% ДИ=0,48-1,33) [193]. Таким образом, результаты данных исследований не позволяют рекомендовать рутинное применение левосимендана** для терапии септического шока.
-
Рекомендовано у пациентов с септическим шоком начинать вазопрессорную терапию (C01CA: Адренергические и дофаминергические средства, C01CX: Другие кардиотонические средства) в периферические вены, а не откладывать начало терапии до тех пор, пока не будет обеспечен доступ к центральным венам [73,195,196].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендовано в случае отсутствия стабилизации гемодинамики у пациентов с септическим шоком после проведения инфузионной, вазопрессорной (C01CA: Адренергические и дофаминергические средства) и инотропной терапии (C01CX: Другие кардиотонические средства) внутривенное введение #гидрокортизона** [73,197–201].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1)
Комментарии. Рекомендовано внутривенное введение #гидрокортизона** в дозе не более 200 мг в сутки в дозировке 50 мг каждые 6 часов или в виде непрерывной инфузии. Начало терапии возможно при дозировке норэпинефрина** более 0,25 мкг/кг/мин на протяжении не менее чем 4 часов [198,199]. Применение глюкокортикоидов у пациентов с сепсисом, приводит к снижению риска смерти, а также значительному сокращению продолжительности пребывания в отделении интенсивной терапии и стационаре [202]. Рекомендована непрерывная внутривенная инфузия с целью предотвращения гипергликемии [202,203] и постепенное снижение глюкокортикоидов после прекращения вазопрессорной терапии [197].
4.4 Трансфузионная терапия
-
При снижении уровня гемоглобина ниже 70 г/л у пациентов с сепсисом и/или септическим шоком рекомендована трансфузия эритроцитарной массы (B05AX01: Эритроциты) [73].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии. Трансфузия эритроцитарной массы рекомендована в случае отсутствия таких отягощающих состояний, как ишемия миокарда, тяжелая гипоксемия, острое кровотечение [73]. Выбор в качестве порога уровня гемоглобина 90 г/л не приводит к повышению 30-дневной [204], 90-дневной выживаемости пациентов с сепсисом и/или септическим шоком [205].
-
Трансфузия свежезамороженной плазмы с целью коррекции нарушений свертывающей системы не рекомендована у пациентов с сепсисом и септическим шоком [73].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. При отсутствии кровотечения или планируемых инвазивных вмешательств трансфузия свежезамороженной плазмы не рекомендована [112].
-
Рекомендована трансфузия тромбоцитов (B05AX02: Тромбоциты) при их количестве в периферической крови менее 10×109/л и отсутствии кровотечения, а также при количестве менее 20×109/л и наличии высокого риска кровотечения у пациентов с сепсисом и септическим шоком [206,207].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Не рекомендовано рутинное применение антитромбина III (B01AB02 - Антитромбин III) для терапии пациентов с сепсисом и септическим шоком [208,209].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарий. Применение антитромбина не снижает смертность при сепсисе и септическом шоке, но повышает риск кровотечения [209].
4.5 Респираторная терапия
-
Рекомендовано начать диагностический поиск респираторных нарушений при SpO2 менее 95% у пациентов с сепсисом [210].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Для пациентов с дыхательной недостаточностью, вызванной сепсисом (без ОРДС), рекомендовано использовать низкий дыхательный объем по сравнению с вентиляцией с высоким дыхательным объемом [211] .
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: Имеются ограниченные данные о стратегиях вентиляции у пациентов с дыхательной недостаточностью, вызванной сепсисом, которые не соответствуют критериям ОРДС. Однако сепсис является независимым фактором риска развития ОРДС, и задержки в диагностике ОРДС могут привести к отсроченному использованию низких дыхательных объемов. Поэтому мы предлагаем использовать вентиляцию с низким дыхательным объемом у всех пациентов с сепсисом, которым проводится ИВЛ во избежание недостаточного или отложенного использования этого вмешательства. Кроме того, использование вентиляции с низким дыхательным объемом позволяет избежать риска повреждения легких, вызванного вентилятором, у пациентов с сепсисом, у которых был пропущен диагноз ОРДС.
-
Рекомендовано начало ИВЛ при остром повреждении легких и остром респираторном дистресс-синдроме у пациентов с сепсисом и септическим шоком [73,212–214].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Абсолютными показаниями для начала ИВЛ являются: отсутствие самостоятельного дыхания и патологические ритмы дыхания, нарушение проходимости верхних дыхательных путей, снижение PaO2/FiO2 менее 200 мм рт.ст., септический шок, нарушение гемодинамики с развитием жизнеугрожающих нарушений ритма, стойкой тахикардии и гипотензии. Наличие двух относительных показаний является показанием для начала ИВЛ: снижение PaO2/FiO2 менее 300 мм рт. ст., развитие септической энцефалопатии и отека головного мозга с угнетением сознания и нарушением функции внешнего дыхания, гиперкапния или гипокапния (РaCO2 менее 25 мм рт.ст.), тахипноэ более 40 в минуту и прогрессирующее увеличение минутного объема вентиляции, снижение жизненной емкости легких менее 10 мл/кг массы тела, снижение податливости менее 60 мл/см вод. ст., увеличение сопротивления дыхательных путей более 15 см вод. ст./л/с, усталость пациента, вовлечение вспомогательных дыхательных мышц [212–214].
-
При ИВЛ у пациентов с сепсисом и септическим шоком рекомендовано использовать стратегию с низким дыхательным объемом 6 мл/кг идеальной массы тела [73].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии. Использование дыхательного объема до 6 мл/кг приводит к снижению летальности и частоты вентилятор-ассоциированной пневмонии, ателектазов по сравнению с большими дыхательными объемами [211], использование дыхательного объема более 10 мл/кг идеальной массы тела приводит к увеличению органной дисфункции и длительности респираторной поддержки [215]. При анализе 10 РКИ, в которые были включены пациенты с ОРДС, было показано дозо- и времязависимое увеличение летальности при превышении целевых значений оксигенации более 6 мл/кг при любой тяжести ОРДС [216].
-
Рекомендовано использование верхнего предела давления плато, 30 см вод. ст. и снижение «движущего» давления легких (driving pressure — DP) менее 15 см вд. ст., при ИВЛ у пациентов с сепсис-индуцированным ОРДС [73,217,218].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
-
Рекомендовано использование высоких значений положительного давления в конце выдоха (PEEP) при ИВЛ у пациентов с сепсис-индуцированным ОРДС [219].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарии: Исследования, сравнивающие применение высоких и низких значений PEEP, показали снижение летальности при высоких значениях PEEP [219,220], достигающих 10–15 мбар [221,222].
4.6 Профилактика осложнений
-
Рекомендовано применение эмпирической противогрибковой терапии (противогрибковые препараты системного действия) у пациентов с сепсисом или септическим шоком и высоким риском реализации грибковой инфекции [73].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: К факторам рискам кандидозной инфекции относятся: наличие грибов рода Candida во множественных локусах [223], нейтропения [224], иммуносупрессия [225], тяжесть состояния (высокий балл по Apache II) [226], длительное пребывание в отделении реанимации и интенсивной терапии [227], наличие центрального венозного катетера или других внутрисосудистых устройств, наркозависимость, полное парентеральное питание, антибиотикотерапия препаратами широкого спектра [228], острое повреждение почек и гемодиализ [229]. Начало эмпирической противогрибковой терапии зависит от типа и количества факторов риска реализации грибковой инфекции у пациента, а также локальных данных инфекции [73].
-
Рекомендовано начало инсулинотерапии (АТХ A10A Инсулины и их аналоги) при уровне глюкозы в крови >180 мг/дл (>10 ммоль/л) при двукратном анализе у пациентов с сепсисом и/или септическим шоком [73,230–234].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Гипергликемия (>180 мг/дл), гипогликемия и повышенная вариабельность уровня глюкозы связаны с высокой смертностью пациентов в критическом состоянии [231]. В метаанализе 2017 г. было показано, что уровни глюкозы <110 и 110–144 мг/дл связаны с повышенным риском гипогликемии по сравнению с уровнями 144–180 и >180 мг/дл. При этом было выявлено отсутствие существенной разницы в риске гипогликемии при уровне гликемии 144–180 и >180 мг/дл [235]. Тем не менее в настоящее время рекомендовано начало введения инсулина (АТХ A10A Инсулины и их аналоги) при уровне глюкозы >180 мг/дл, что обусловлено повышенным риском гипогликемии [73].
-
Рекомендована комбинированная профилактика венозных тромбоэмболических осложнений с применением как медикаментозной, так и механической (компрессионные чулки с градуированной компрессией или переменная пневмокомпрессия) профилактики [73,236].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1)
Комментарии: Кокрейновский обзор показал, что комбинированная профилактика является более эффективной, чем любой из других методов, однако методологические особенности данного исследования не позволяют рассмотреть данную рекомендацию как сильную [236]. При сравнении препаратов нефракционированного гепарина (B01AB - Группа гепарина) и препаратов низкомолекулярного гепарина (НМГ) – (B01AB - Группа гепарина) в другом Кокрейновском обзоре было показано, что НМГ являются более эффективными в отношении снижения тромбоэмболических осложнений [237].
-
Рекомендована в качестве медикаментозной профилактики венозных тромбоэмболических осложнений применение препаратов НМГ (B01AB - Группа гепарина) пациентам с сепсисом и септическим шоком при отсутствии противопоказаний [73,238–240].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1)
Комментарии: Пациенты, находящиеся в ОРИТ, подвержены высокому риску тромбоэмболических осложнений, при этом частота тромбоза глубоких вен может достигать 10%, а тромбоэмболии легочной артерии – 2–4% [236,237,241].
4.7 Иные методы
-
После проведения успешной первичной реанимации рекомендована санация источника сепсиса и/или септического шока в течение не более 12 ч после постановки диагноза [242–245].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3)
-
Рекомендовано решение вопроса о гистерэктомии в случае отсутствия, помимо матки, других очагов инфекции, обусловливающих прогрессирование признаков полиорганной недостаточности и отсутствие эффекта от проводимой консервативной терапии [246–249].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
-
У пациентов с сепсисом и острым повреждением почек рекомендовано использование продленной или интермиттирующей заместительной почечной терапии [250,251].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1)
-
Применение заместительной почечной терапии не рекомендовано при увеличении уровня креатинина или олигурии в отсутствие других четких показаний для диализа [252–254].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 2)
-
Рутинное применение поликлональных и моноклональных иммуноглобулинов не рекомендовано в терапии пациентов с сепсисом и/или септическим шоком в связи отсутствием достаточных доказательств эффективности данной терапии, необходимо проведение дополнительных исследований [255].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1)
Комментарии: Эффективность терапии поликлональными и моноклональными иммуноглобулинами при сепсисе остается спорной и требует подтверждения в более крупных исследованиях [255].
-
Рутинное применение высокообъемной гемофильтрации не рекомендовано в терапии пациентов с сепсисом и/или септическим шоком в связи с низким качеством доказательств проведенных исследований, необходимо проведение дополнительных исследований для оценки эффективности терапии [256].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1)
-
Рутинное применение плазмафереза не рекомендовано в терапии пациентов с сепсисом и/или септическим шоком [257–260].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1)
Комментарии: Рутинное применение терапевтического плазмообмена не рекомендовано в лечении пациентов с сепсисом и/или септическим шоком, однако, при наличии специалистов и условий для проведения экстракорпоральных методов данный метод лечения может быть рассмотрен [261]. Экстракорпоральное очищение крови рассматривается как выгодная стратегия, позволяющая элиминировать медиаторы воспаления и микробные токсины, однако рандомизированные контролируемые исследования показали, что соотношение риск/выгода для большинства методик остается неопределенным, за исключением процедур селективной ЛПС-адсорбции с применением колонок с иммобилизированным полимиксином В и терапевтического плазмообмена [258,262]. Ретроспективное обсервационное исследование у взрослых пациентов с септическим шоком и полиорганной недостаточностью продемонстрировало улучшение 28-дневной выживаемости при применении дополнительного терапевтического плазмообмена по сравнению со стандартной терапией. Гемодинамика, органная дисфункция и баланс жидкости улучшились при дополнительном терапевтическом плазмообмене, а продолжительность пребывания в стационаре у выживших увеличилась [262]. Данные в рандомизированном контролируемом исследовании показали, что терапевтический плазмообмен в подгруппе пациентов с септическим шоком привел к быстрому улучшению гемодинамики [258]. Требуется проведение дальнейших многоцентровых рандомизированных исследований с адекватной мощностью для определения тактики лечения у пациентов с сепсисом и септическим шоком.
-
Рекомендовано проведение профилактики стрессовых язв желудочно-кишечного тракта при наличии факторов риска желудочно-кишечного кровотечения у пациентов с сепсисом и/или септическим шоком c применением препаратов ингибиторов протонного насоса и блокаторов H2-гистаминовых рецепторов [73,263].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: При этом последние метаанализы показали, что ингибиторы протонной помпы (A02BC Ингибиторы протонного насоса) более эффективны в отношении снижения частоты клинически значимых желудочно-кишечных кровотечений по сравнению с блокаторами H2-гистаминовых рецепторов (A02BA - Блокаторы H2-гистаминовых рецепторов) [264–266].
-
Рекомендовано раннее начало энтерального питания (в течение 72 ч) у пациентов с сепсисом и/или септическим шоком, для которых возможно энтеральное питание [73].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
[1] https://apps.who.int/iris/handle/10665/331990
Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Послеродовые инфекционные осложнения как правило являются инфекциями связанные с оказанием медицинской помощи (ИСМП). ИСМП в послеродовом периоде могут быть обусловлены как экзогенным, так и эндогенным инфицированием.
Основными формами ИСМП в послеродовом периоде являются:
-
Гнойно-септические инфекции родильниц (ГСИ родильниц): сепсис, инфекции соска и молочной железы, связанные с деторождением, острый перитонит, инфекция хирургической акушерской раны, расхождение швов после кесарева сечения, расхождение швов промежности, инфекции мочевых путей после родов, инфекции органов дыхания, осложняющие роды и послеродовой период.
-
Инфекции в области хирургического вмешательства (ИОХВ).
Каждый случай ИСМП подлежит регистрации в журнале учета инфекционных заболеваний по месту их выявления и месту инфицирования пациента в медицинских организациях, а также в территориальных органах, уполномоченных осуществлять федеральный государственный санитарно-эпидемиологический надзор. Учет всех случаев ИСМП ведется по месту инфицирования пациента.
В случае выявления ИСМП после выписки или перевода пациента в другой стационар, медицинская организация, выявившая ИСМП, должна передавать информацию в территориальные органы, уполномоченные осуществлять федеральный государственный санитарно-эпидемиологический надзор, которые в течение 12 часов передают информацию о зарегистрированных ИСМП в медицинскую организацию по месту предполагаемого инфицирования.
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
-
В настоящее время единые подходы к реабилитации пациентов с послеродовыми инфекционными осложнениями не разработаны. Рекомендовано придерживаться общих правил реабилитации пациентов после инфекционных заболеваний и сепсиса [267–269].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Госпитализация
Организация оказания медицинской помощи
Сепсис и септический шок являются состояниями, требующими проведения мероприятий по реанимации и интенсивной терапии пациентов, а также консультирования и дальнейшего мониторинга состояния пациента в акушерском дистанционном консультативном центре.
Оказание медицинской помощи в экстренной и неотложной формах осуществляется в два этапа:
-
вне медицинской организации – осуществляется выездной бригадой скорой медицинской помощи анестезиологии-реанимации для оказания экстренной и неотложной медицинской помощи женщинам в период беременности, родов, в послеродовом периоде и при гинекологической патологии, которая состоит из врачей анестезиологов-реаниматологов, владеющих методами ургентной диагностики, реанимации и интенсивной терапии в акушерстве и гинекологии; врачей акушеров-гинекологов, владеющих полным объемом хирургических вмешательств в акушерстве-гинекологии, и медицинских сестер-анестезистов, освоивших навыки оказания неотложной помощи в неонатологии и акушерстве-гинекологии, или в случае отсутствия выездной бригады скорой медицинской помощи анестезиологии-реанимации – бригадами скорой медицинской помощи;
-
в стационарных условиях – осуществляется в отделениях анестезиологии-реанимации медицинских организаций.
Основаниями для перевода родильниц в профильное отделение для дальнейшего наблюдения и лечения являются:
-
стойкое восстановление гемодинамики и спонтанного дыхания;
-
коррекция метаболических нарушений;
-
стабилизация жизненно важных функций.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
В настоящее время, учитывая развитие устойчивости к антибактериальным препаратам, должно быть произведено усиление мер, направленных на профилактику гнойно-септических осложнений в послеродовом периоде.
-
Рекомендовано информировать всех беременных и женщин в послеродовом периоде о необходимости своевременного обращения в медицинское учреждение в случае возникновения признаков инфекции [36, 63].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
-
Рекомендовано наблюдение за пациентами на протяжении всего послеродового периода в целях профилактики, своевременного выявления инфекционных осложнений и снижения материнской смертности [34,59,270].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
-
При разрывах промежности III и IV степени рекомендовано проведение антибиотикопрофилактики с целью профилактики гнойно-септических осложнений в послеродовом периоде [271].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
-
При ручном отделении плаценты и выделении последа рекомендовано проведение антибиотикопрофилактики с целью профилактики гнойно-септических осложнений в послеродовом периоде [67].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендованы соблюдать меры профилактики развития инфекционных осложнений в процессе родоразрешения (см. клинические рекомендации «Роды одноплодные, родоразрешение путем кесарева сечения», «Нормальная беременность») [61,272,273].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3)
-
Рекомендовано в целях профилактики послеродовой инфекции обеспечение эпидемиологической безопасности в медицинской организации, проведение профилактических мероприятий, выявления и регистрации в медицинской организации случаев возникновения инфекционных болезней, связанных с оказанием медицинской помощи [274].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2)
Комментарии: см. также приказ Минздрава России от 29.11.2021 № 1108н «Об утверждении порядка проведения профилактических мероприятий, выявления и регистрации в медицинской организации случаев возникновения инфекционных болезней, связанных с оказанием медицинской помощи, номенклатуры инфекционных болезней, связанных с оказанием медицинской помощи, подлежащих выявлению и регистрации в медицинской организации».
-
Рекомендовано медицинским работникам проявлять высокую клиническую настороженность в отношении инфекции, ассоциированной с β-гемолитическим стрептококком группы А, в целях профилактики послеродовой инфекции [275].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендовано в целях профилактики послеродовой инфекции проводить эпидемиологическое расследование внутри медицинской организации в случае, если за шестимесячный период в медицинской организации выявляются два или более эпизода послеродовой инфекции, ассоциированной с β-гемолитическим стрептококком группы А [276–278].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Информация
Источники и литература
-
Клинические рекомендации Российского общества акушеров-гинекологов
- 1. Olsen M.A. et al. Risk Factors for Surgical Site Infection After Low Transverse Cesarean Section// Infect. Control Hosp. Epidemiol. Cambridge University Press (CUP), 2008. Vol. 29, № 6. P.477–484. 2. Korol E. et al. A systematic review of risk factors associated with surgical site infections amongsurgical patients // PLoS ONE. PLoS One, 2013. Vol. 8, № 12. 3. Tran T.S. et al. Risk factors for postcesarean surgical site infection // Obstet. Gynecol. ObstetGynecol, 2000. Vol. 95, № 3. P. 367–371. 4. Avila C. et al. Association of smoking with wound complications after cesarean delivery // J.Matern. Neonatal Med. J Matern Fetal Neonatal Med, 2012. Vol. 25, № 8. P. 1250–1253. 5. De Vivo A. et al. Wound length and corticosteroid administration as risk factors for surgical-sitecomplications following cesarean section // Acta Obstet. Gynecol. Scand. Acta Obstet GynecolScand, 2010. Vol. 89, № 3. P. 355–359. 6. Vermillion ST et al. Wound infection after cesarean: Effect of subcutaneous tissue thickness //Obstet. Gynecol. Obstet Gynecol, 2000. Vol. 95, № 6. P. 923–926. 7. Killian C.A. et al. Risk Factors for Surgical-Site Infections Following Cesarean Section // Infect.Control Hosp. Epidemiol. Cambridge University Press (CUP), 2001. Vol. 22, № 10. P. 613–617. 8. Opøien H.K. et al. Post-cesarean surgical site infections according to CDC standards: Rates andrisk factors. A prospective cohort study // Acta Obstet. Gynecol. Scand. Acta Obstet GynecolScand, 2007. Vol. 86, № 9. P. 1097–1102. 9. Schneid-Kofman N. et al. Risk factors for wound infection following cesarean deliveries // Int. J.Gynecol. Obstet. John Wiley and Sons Ltd, 2005. Vol. 90, № 1. P. 10–15. 10. Eberlein T., Assadian O. Clinical use of polihexanide on acute and chronic wounds for antisepsisand decontamination // Skin Pharmacology and Physiology. Skin Pharmacol Physiol, 2010. Vol.23, № SUPPL. 1. P. 45–51. 11. James G.A. et al. Biofilms in chronic wounds // Wound Repair Regen. Wound Repair Regen,2008. Vol. 16, № 1. P. 37–44. 12. Siddiqui A.R., Bernstein J.M. Chronic wound infection: Facts and controversies // Clin. Dermatol.Clin Dermatol, 2010. Vol. 28, № 5. P. 519–526. 13. Leaper D.J. et al. Extending the TIME concept: What have we learned in the past 10 years? // Int.Wound J. Int Wound J, 2012. Vol. 9, № SUPPL. 2. P. 1–19. 14. Rouse C.E. et al. Postpartum endometritis and infection following incomplete or completeabortion: Case definition & guidelines for data collection, analysis, and presentation of maternal immunization safety data // Vaccine. Elsevier Ltd, 2019. Vol. 37, № 52. P. 7585–7595. 15. Morgan J., Roberts S. Maternal Sepsis // Obstetrics and Gynecology Clinics of North America.Obstet Gynecol Clin North Am, 2013. Vol. 40, № 1. P. 69–87. 16. Dalton E., Castillo E. Post partum infections: A review for the non-OBGYN // Obstet. Med. RoyalSociety of Medicine Press Ltd, 2014. Vol. 7, № 3. P. 98–102. 17. Seale A.C. et al. Estimates of the Burden of Group B Streptococcal Disease Worldwide forPregnant Women, Stillbirths, and Children // Clin. Infect. Dis. Oxford University Press, 2017. Vol.65, № suppl_2. P. S200–S219. 18. Maharaj D. Puerperal pyrexia: A review. Part II // Obstetrical and Gynecological Survey. ObstetGynecol Surv, 2007. Vol. 62, № 6. P. 400–406. 19. Karsnitz DB. Puerperal infections of the genital tract: A clinical review // Journal of Midwiferyand Women’s Health. John Wiley and Sons Inc., 2013. Vol. 58, № 6. P. 632–642. 20. Mackeen A.D. et al. Antibiotic regimens for postpartum endometritis // Cochrane Database ofSystematic Reviews. John Wiley and Sons Ltd, 2015. Vol. 2015, № 2. 21. Myles TD, Gooch J, Santolaya J. Obesity as an independent risk factor for infectious morbidity inpatients who undergo cesarean delivery // Obstet. Gynecol. Ovid Technologies (Wolters KluwerHealth), 2002. Vol. 100, № 5. P. 959–964. 22. Magann EF et al. Pregnancy, obesity, gestational weight gain, and parity as predictors ofperipartum complications // Arch. Gynecol. Obstet. Arch Gynecol Obstet, 2011. Vol. 284, № 4. P.827–836. 23. Burrows L.J., Meyn L.A., Weber A.M. Maternal morbidity associated with vaginal versuscesarean delivery // Obstetrics and Gynecology. Obstet Gynecol, 2004. Vol. 103, № 5 I. P. 907–912. 24. Boggess K.A. et al. Risk factors for postcesarean maternal infection in a trial of extended-spectrum antibiotic prophylaxis // Obstet. Gynecol. Lippincott Williams and Wilkins, 2017. Vol.129, № 3. P. 481–485. 25. Liu D. et al. Different regimens of penicillin antibiotics given to women routinely for preventinginfection after cesarean section: A systematic review and meta analysis // Medicine (UnitedStates). Lippincott Williams and Wilkins, 2018. Vol. 97, № 46. 26. Анохова Л.И. et al. Послеродовый эндометрит и его профилактика (обзор литературы). 2016.6–13 p. 27. Докудаева Ш.А. Современные представления об этиологии, патогенезе, клинике идиагностике послеродового эндометрита // Вестник Национального медико-хирургическогоЦентра им. Н. И. Пирогова. 2016. Vol. 11, № 4. P. 109–115. 28. Мартынов С.А., Адамян Л.В. Рубец на матке после кесарева сечения: терминологическиеаспекты // Гинекология. 2020. Vol. 22, № 5. P. 70–75. 29. Sartelli M. et al. Complicated intra-abdominal infections worldwide: The definitive data of theCIAOW Study // World J. Emerg. Surg. BioMed Central Ltd., 2014. Vol. 9, № 1. 30. Bassetti M. et al. A multicenter study of septic shock due to candidemia: Outcomes and predictorsof mortality // Intensive Care Med. Springer Verlag, 2014. Vol. 40, № 6. P. 839–845. 31. Osuchowski M.F. et al. Circulating Cytokine/Inhibitor Profiles Reshape the Understanding of theSIRS/CARS Continuum in Sepsis and Predict Mortality // J. Immunol. The American Associationof Immunologists, 2006. Vol. 177, № 3. P. 1967–1974. 32. Kirkpatrick A.W. et al. Update from the abdominal compartment society (WSACS) on intra-Abdominal hypertension and abdominal compartment syndrome: Past, present, and future beyondBanff 2017 // Anaesthesiology Intensive Therapy. Via Medica, 2017. Vol. 49, № 2. P. 83–87. 33. Reintam Blaser A. et al. Incidence, Risk Factors, and Outcomes of Intra-Abdominal Hypertensionin Critically Ill Patients - A Prospective Multicenter Study (IROI Study) // Crit. Care Med.Lippincott Williams and Wilkins, 2019. Vol. 47, № 4. P. 535–542. 34. Cantwell R et al. Saving Mothers’ Lives: Reviewing maternal deaths to make motherhood safer:2006-2008 // BJOG An Int. J. Obstet. Gynaecol. Wiley, 2011. Vol. 118. P. 1–203. 35. Reusch M. et al. Prevalence of MRSA colonization in peripartum mothers and their newborninfants // Scand. J. Infect. Dis. Taylor & Francis, 2008. Vol. 40, № 8. P. 667–671. 36. Hassoun A., Linden P.K., Friedman B. Incidence, prevalence, and management of MRSAbacteremia across patient populations-a review of recent developments in MRSA management andtreatment // Critical care (London, England). Crit Care, 2017. Vol. 21, № 1. P. 211. 37. Bowyer L. The Confidential Enquiry into Maternal and Child Health (CEMACH). SavingMothers’ Lives: reviewing maternal deaths to make motherhood safer 2003–2005. The SeventhReport of the Confidential Enquiries into Maternal Deaths in the UK // Obstet. Med. SAGEPublications, 2008. Vol. 1, № 1. P. 54–54. 38. Stefonek K.R., Maerz L.L., Nielsen M.P. Group A streptococcal puerperal sepsis preceded bypositive surveillance cultures // Obstet. Gynecol. Obstet Gynecol, 2001. Vol. 98, № 5. P. 846–848. 39. Barnham M.R.D., Weightman N.C. Bacteraemic Streptococcus pyogenes infection in the peri-partum period: Now a rare disease and prior carriage by the patient may be important // J. Infect.W.B. Saunders Ltd, 2001. Vol. 43, № 3. P. 173–176. 40. Raymond S.L. et al. Microbial recognition and danger signals in sepsis and trauma // Biochimicaet Biophysica Acta - Molecular Basis of Disease. Elsevier B.V., 2017. Vol. 1863, № 10. P. 2564–2573.
Информация
Список сокращений
|
APACHE II |
Acute Physiology and Chronic Health Evaluation – диагностические критерии острых и хронических физиологических нарушений |
|---|---|
|
FiO2 |
фракция кислорода во вдыхаемой смеси |
|
HFO |
High frequency oscillation – высокочастотная осцилляторная вентиляция лёгких |
|
MEOWS |
Modified Early Obstetric Warning System – модифицированная акушерская ранняя система предупреждения |
|
MEWS |
Modified Early Warning Score – модифицированная ранняя система предупреждения |
|
MODS |
Multiple Organ Dysfunction Score – шкала оценки полиорганной дисфункции |
|
MRSA |
methicillin-resistant Staphylococcus aureus – метициллинрезистентный золотистый стафилококк |
|
NEWS |
National Early Warning Score – национальная ранняя система предупреждения |
|
NO |
оксида азота |
|
PaO2 |
парциальное давление кислорода в артериальной крови |
|
PEEP |
Positive end-expiratory pressure – положительное конечно-экспираторное давление |
|
qSOFA |
quick Sequential Organ Failure Assessment – быстрая шкала последовательной оценки органной недостаточности |
|
SaO2 |
насыщение гемоглобина кислородом артериальной крови |
|
SCVO2 |
насыщение кислорода в центральной вене |
|
SIRS |
Systemic inflammatory response syndrome – синдром системного воспалительного ответа |
|
SOFA |
Sequential Organ Failure Assessment – шкала последовательной оценки органной недостаточности |
|
SOS |
Sepsis in obstetrics score – шкала сепсиса в акушерстве |
|
SSC |
Surviving Sepsis Campaign – Кампания по выживанию при сепсисе |
|
SvO2 |
насыщение кислорода в смешанной венозной крови |
|
SрO2 |
насыщение гемоглобина кислородом (по пульсоксиметру) |
|
FiO2 |
фракция кислорода во вдыхаемой смеси |
|
ВОЗ |
Всемирная организация здравоохранения |
|
ИВЛ |
искусственная вентиляция легких |
|
ИОХВ |
инфекция области хирургического вмешательства |
|
НИВЛ |
неинвазивная вентиляция легких |
|
НМГ |
низкомолекулярный гепарин |
|
ОРДС |
острый респираторный дистресс-синдром |
|
ОРИТ |
отделение реанимации и интенсивной терапии |
|
РКИ |
рандомизированное контролируемое испытание |
|
ПКТ |
прокальцитониновый тест |
|
САД |
среднее артериальное давление |
|
СРБ |
С-реактивный белок |
|
ЦВД |
центральное венозное давление |
|
ЧСС |
частота сердечных сокращений |
|
ЭхоКГ |
эхокардиография |
Термины и определения
Абдоминальный сепсис – это патологический процесс, в основе которого лежит системная воспалительная реакция организма на внутрибрюшную инфекцию, приводящая к остро возникшей органной дисфункции.
Абсцесс малого таза – абсцесс, локализующийся в прямокишечно-маточном пространстве и возникающий как осложнение острых воспалительных заболеваний, травм или операций на органах малого таза или брюшной полости.
Инфекция области хирургического вмешательства (ИОХВ) – осложнение раневого процесса, которое возникает в результате роста микроорганизмов и приводит к местным и/или системным проявлениям.
Материнский сепсис – это патологический процесс, в основе которого лежит системная воспалительная реакция организма на инфекцию, приводящая к остро возникшей органной дисфункции во время беременности, родов, постабортного или послеродового периода.
Острый респираторный дистресс-синдром (ОРДС) – остро возникающее диффузное воспалительное поражение паренхимы легких, развивающееся как неспецифическая реакция на различные повреждающие факторы и приводящее к формированию острой дыхательной недостаточности вследствие нарушения структуры легочной ткани и уменьшения массы аэрированной легочной ткани.
Перитонит – широкий комплекс патологических процессов, протекающих в просвете брюшной полости, в брюшине, подлежащих тканях (предбрюшинная клетчатка, стенки органов брюшной полости и их просветах), а также на уровне всех жизненно важных органов и систем (системная воспалительная реакция, сепсис, органные и системные дисфункции, шок).
Полиорганная недостаточность – тяжелая неспецифическая стресс-реакция организма, совокупность недостаточности нескольких функциональных систем, развивающаяся как терминальная стадия большинства острых заболеваний и травм.
Послеродовой эндометрит – это инфекционное воспаление эндометрия, возникающее в послеродовом периоде. Чаще всего в воспалительный процесс вовлекается также и миометрий.
Сепсис – это жизнеугрожающая органная дисфункция, возникающая вследствие нарушения регуляции ответа организма на инфекцию.
Септический шок – это разновидность сепсиса, при которой системная воспалительная реакция организма сопровождается не только органной дисфункцией, но и стойкой гипоперфузией тканей, не купируемой волемической нагрузкой и требующей вазопрессорной поддержки.
Хориоамнионит – инфекционное воспаление плодных оболочек и амниотической жидкости, вызванное полимикробными ассоциациями.
Критерии оценки качества медицинской помощи
Критерии оценки качества медицинской помощи. Инфекция области хирургического вмешательства.
|
№ |
Критерии качества |
Да/Нет |
|---|---|---|
|
1 |
Проведен визуальный контроль состояния и пальпация кожи и мягких тканей в области послеоперационной раны после кесарева сечения, эпизиотомии и акушерских травм, а также в местах установки внутривенных канюль или инъекций с целью своевременной диагностики ИОХВ |
Да/Нет |
|
2 |
Проведена антибактериальная терапия в комбинации с хирургической обработкой и санацией раны или инфицированной ткани |
Да/Нет |
Критерии оценки качества медицинской помощи. Послеродовой эндометрит.
|
№ |
Критерии качества |
Да/Нет |
|---|---|---|
|
1 |
Выполнено ультразвуковое исследование органов малого таза (комплексного) и/или компьютерная томография (КТ) органов малого таза и/или магнитно-резонансная томография (МРТ) органов малого таза с целью дифференциальной диагностики, выявления абсцесса малого таза, гематомы, метротромбофлебита, параметрита |
Да/Нет |
|
2 |
Проведена антибактериальная терапия антибиотиками широкого спектра действия |
Да/Нет |
Критерии оценки качества медицинской помощи. Акушерский перитонит.
|
№ |
Критерии качества |
Да/Нет |
|---|---|---|
|
1 |
Выполнено ультразвукового исследования органов брюшной полости (комплексного) и/или КТ органов брюшной полости при подозрении на акушерский перитонит с целью установки диагноза |
Да/Нет |
|
2 |
Проведена эмпирическая терапия антибиотиками широкого спектра действия |
Да/Нет |
Критерии оценки качества медицинской помощи. Послеродовой сепсис. Септический шок.
|
№ |
Критерии качества |
Да/Нет |
|---|---|---|
|
1 |
При подозрении на септический шок или высокую вероятность сепсиса начата эмпирическая терапия антибиотиками широкого спектра действия в течение 1 часа |
Да/Нет |
|
2 |
Выполнено микробиологическое (культуральное) исследование биологических сред на аэробные и факультативно-анаэробные микроорганизмы с целью идентификации возбудителей, количественной оценки микробной обсемененности и определения чувствительности к антибактериальным препаратам |
Да/Нет |
|
3 |
Выполнено исследование уровня лактата в сыворотке крови с целью диагностики сепсиса и выбора тактики лечения |
Да/Нет |
|
4 |
Проведена оценка состояния пациента с помощью шкал для скрининга сепсиса и/или септического шока |
Да/Нет |
|
5 |
Проведено внутривенное введение кристаллоидных растворов в дозе 30 мл/кг в течение первых 3 ч терапии при развитии сепсиса и/или септического шока с обязательным контролем переносимости инфузии |
Да/Нет |
|
6 |
Проведена ИВЛ при остром повреждении легких и остром респираторном дистресс-синдроме у пациентов с сепсисом и септическим шоком |
Да/Нет |
|
7 |
Проведена профилактика венозных тромбоэмболических осложнений пациентам с сепсисом и септическим шоком |
Да/Нет |
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
-
Кан Наталья Енкыновна – доктор медицинских наук, профессор, заместитель директора по научной работе ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Тютюнник Виктор Леонидович – доктор медицинских наук, профессор, в.н.с. центра научных и клинических исследований департамента организации научной деятельности, ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Хачатрян Зарине Варужановна – кандидат медицинских наук, врач акушер-гинеколог АО «Европейский медицинский центр» (г. Москва). Конфликт интересов отсутствует.
-
Абабков Сергей Геннадьевич – заведующий отделением анестезиологии и реанимации ГБУЗ СО «Екатеринбургский клинический перинатальный центр» (г. Екатеринбург). Конфликт интересов отсутствует.
-
Амирасланов Эльрад Юсифович – кандидат медицинских наук, заведующий акушерским отделением ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Артымук Наталья Владимировна – доктор медицинских наук, профессор, заведующая кафедрой акушерства и гинекологии имени профессора Г.А. Ушаковой ФГБОУ ВО «Кемеровский государственный медицинский университет» Минздрава России, главный внештатный специалист Минздрава России по акушерству, главный внештатный специалист Минздрава России по гинекологии, главный внештатный специалист Минздрава России по репродуктивному здоровью женщин в СФО (г. Кемерово). Конфликт интересов отсутствует.
-
Ахматова Анастасия Николаевна – кандидат медицинских наук, доцент кафедры акушерства и гинекологии с курсом перинатологии Российского университета дружбы народов, заслуженный деятель науки РФ (г. Москва). Конфликт интересов отсутствует.
-
Баранов Игорь Иванович – доктор медицинских наук, профессор, заведующий отделом научных и образовательных программ ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Белокриницкая Татьяна Евгеньевна – доктор медицинских наук, профессор, заведующая кафедрой акушерства и гинекологии ФПК и ППС ФГБОУ ВО «Читинская государственная медицинская академия» Минздрава России, заслуженный врач Российской Федерации, главный внештатный специалист Минздрава России по акушерству, главный внештатный специалист Минздрава России по гинекологии, главный внештатный специалист Минздрава России по репродуктивному здоровью женщин в ДФО (г. Чита). Конфликт интересов отсутствует.
-
Быков Аким Семёнович – кандидат медицинских наук, врач – анестезиолог-реаниматолог ГБУЗ СО «Екатеринбургский клинический перинатальный центр» (г. Екатеринбург). Конфликт интересов отсутствует.
-
Десятник Кирилл Александрович – врач акушер-гинеколог организационно-методического отдела ГБУЗ СО «Екатеринбургский клинический перинатальный центр» (г. Екатеринбург). Конфликт интересов отсутствует.
-
Долгушина Наталия Витальевна – доктор медицинских наук, профессор, заместитель директора – руководитель департамента организации научной деятельности ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Игнатьева Алла Александровна – кандидат медицинских наук, заведующий 2 акушерским физиологическим отделением ФГБУ "Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова" Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Климов Владимир Анатольевич – кандидат медицинских наук, руководитель службы организации медицинской помощи и информационного сервиса ФГБУ «НМИЦ АГП им. акад. В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Куликов Александр Вениаминович – доктор медицинских наук, профессор, вице-президент Ассоциации ААР, член правления ФАР, председатель комитета ФАР по вопросам анестезии и интенсивной терапии в акушерстве и гинекологии, профессор кафедры акушерства и гинекологии, трансфузиологии ФГБОУ ВО «Уральский государственный медицинский университет» Министерства здравоохранения РФ, г. Екатеринбург. Конфликт интересов отсутствует.
-
Мартиросян Сергей Валерьевич – кандидат медицинских наук, главный врач ГБУЗ СО «Екатеринбургский клинический перинатальный центр», доцент кафедры акушерства и гинекологии лечебно-профилактического факультета Уральского государственного медицинского университета (г. Екатеринбург). Конфликт интересов отсутствует.
-
Николаева Анастасия Владимировна – кандидат медицинских наук, главный врач ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Перевозкина Ольга Владимировна – кандидат медицинских наук, заведующая организационно-методическим отделом ГБУЗ СО «Екатеринбургский клинический перинатальный центр» (г. Екатеринбург). Конфликт интересов отсутствует.
-
Припутневич Татьяна Валерьевна – Член-корреспондент РАН, доктор медицинских наук, директор института микробиологии, антимикробной терапии и эпидемиологии ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России, профессор кафедры микробиологии и вирусологии Педиатрического факультета ФГБОУ ВП «РНИМУ им. Н.И. Пирогова», главный внештатный специалист по медицинской микробиологии Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Проценко Денис Николаевич – кандидат медицинских наук, доцент, заведующий кафедрой анестезиологии и реаниматологии ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Министерства здравоохранения РФ, главный врач ГБУЗ «ГКБ № 40» Департамента здравоохранения г. Москвы, главный внештатный анестезиолог-реаниматолог Департамента здравоохранения г. Москвы, член президиума Ассоциации ААР, г. Москва. Конфликт интересов отсутствует.
-
Прялухин Иван Александрович – кандидат медицинских наук, начальник отдела методологии проектов департамента организации проектной деятельности, ФГБУ «НМИЦ АГП им. академика В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Пырегов Алексей Викторович – доктор медицинских наук, профессор, заместитель главного врача по анестезиологии и реанимации ГБУЗ МО «Московский областной перинатальный центр», главный внештатный специалист МЗ МО по анестезиологии-реаниматологии в акушерстве. Конфликт интересов отсутствует.
-
Радзинский Виктор Евсеевич – доктор медицинских наук, профессор, член- корреспондент РАН, заведующий кафедрой акушерства и гинекологии с курсом перинатологии Российского университета дружбы народов, заслуженный деятель науки РФ (г. Москва). Конфликт интересов отсутствует.
-
Рогачевский Олег Владимирович – доктор медицинских наук, трансфузиолог, акушер- гинеколог, заведующий отделением экстракорпоральных методов лечения и детоксикации. ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Роненсон Александр Михайлович – кандидат медицинских наук, главный внештатный анестезиолог-реаниматолог в акушерстве и гинекологии Министерства здравоохранения Тверской области, заведующий отделением анестезиологии и реанимации ГБУЗ Тверской области «Областной клинический перинатальный центр имени Е.М. Бакуниной», ученый секретарь Ассоциации ААР, ассистент кафедры анестезиологии, реаниматологии и интенсивной терапии ФГБОУ ВО «Тверской государственный медицинский университет» Министерства здравоохранения РФ, г. Тверь. Конфликт интересов отсутствует.
-
Серов Владимир Николаевич – академик РАН, доктор медицинских наук, профессор, заслуженный деятель науки РФ, президент Российского общества акушеров-гинекологов, главный научный сотрудник ФГБУ "Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова" Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Трошин Павел Владимирович – врач анестезиолог-реаниматолог, ассистент кафедры анестезиологии и реаниматологии, ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Федорова Татьяна Анатольевна – доктор медицинских наук, заведующая отделом трансфузиологии и гемокоррекции ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Шабанова Наталья Евгеньевна – кандидат медицинских наук, доцент, заведующая отделением клинической фармакологии антимикробных и иммунобиологических препаратов, ФГБУ «НМИЦ АГП им. академика В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Шешко Елена Леонидовна – кандидат медицинских наук, доцент, руководитель департамента организации проектной деятельности, ФГБУ «НМИЦ АГП им. акад. В.И. Кулакова» Минздрава России (г. Москва). Конфликт интересов отсутствует.
-
Шифман Ефим Муневич – доктор медицинских наук, профессор, президент Ассоциации ААР, Вице-Президент ФАР, член Президиума ФАР, член правления Всемирного общества внутривенной анестезии (SIVA), член правления МНО анестезиологов-реаниматологов, заслуженный врач Республики Карелия, профессор кафедры анестезиологии и реаниматологии ФУВ ГБУЗ МО МОНИКИ им. М.Ф. Владимирского, г. Москва. Конфликт интересов отсутствует.
-
Шмаков Роман Георгиевич - доктор медицинских наук, профессор РАН, директор института акушерства ФГБУ "Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова" Минздрава России (г. Москва). Главный внештатный специалист Минздрава России по акушерству (г. Москва). Конфликт интересов отсутствует.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
-
врачи акушеры-гинекологи;
-
врачи анестезиологи-реаниматологи;
-
студенты; ординаторы, аспиранты акушеры-гинекологи; ординаторы, аспиранты анестезиологи-реаниматологи;
-
преподаватели, научные сотрудники.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД)для методов диагностики (диагностических вмешательств)
|
УДД |
Расшифровка |
|---|---|
|
1 |
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2 |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3 |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4 |
Несравнительные исследования, описание клинического случая |
|
5 |
Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД)для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
УДД |
Расшифровка |
|---|---|
|
1 |
Систематический обзор РКИ с применением мета-анализа |
|
2 |
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа |
|
3 |
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования |
|
4 |
Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
|
5 |
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР |
Расшифровка |
|---|---|
|
A |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
|
B |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
|
C |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года,а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Характеристика некоторых кристаллоидных растворов (B05BB: Растворы, влияющие на водно-электролитный баланс) для инфузионной терапии
|
Раствор |
Содержание в 1000 мл, ммоль/л |
Осмолярность, (мОсм) |
|||||
|---|---|---|---|---|---|---|---|
|
Na |
К |
Са |
Mg |
Сl |
Носители резервной щелочности |
|
|
|
Плазма крови |
136-143 |
3,5-5 |
2,38-2,63 |
0,75-1,1 |
96-105 |
- |
280-290 |
|
Интерстициальная жидкость |
145 |
4 |
2,5 |
1 |
116 |
- |
298 |
|
Натрия хлорид** |
154 |
- |
- |
- |
154 |
- |
308 |
|
Натрия хлорида раствор сложный [Калия хлорид+Кальция хлорид+Натрия хлорид] ** |
147 |
4 |
6 |
|
155 |
- |
309 |
|
Натрия лактата раствор сложный [Калия хлорид+Кальция хлорид+Натрия хлорид+Натрия лактат]** |
130 |
4 |
3 |
- |
109 |
Лактат 28 |
273 |
|
Калия хлорид+Кальция хлорид+Магния хлорид+Натрия ацетат+Натрия хлорид |
131 |
4 |
2 |
1 |
111 |
ацетат 30 |
280 |
|
Калия хлорид+Кальция хлорид+Магния хлорид+Натрия ацетат+Натрия хлорид+Яблочная кислота** |
140 |
4 |
2,5 |
1 |
127 |
малат 5,0, ацетат 24 |
304 |
|
Калия ацетат+Кальция ацетат+Магния ацетат+Натрия ацетат+Натрия хлорид** |
137 |
4 |
1.65 |
1,25 |
110 |
ацетат 3.674 |
291 |
|
Калия хлорид+Магния хлорид+Натрия ацетат+Натрия глюконат+Натрия хлорид |
140 |
5 |
- |
1,5 |
98 |
Малат, ацетат по 27 |
294 |
Приложение Б. Алгоритмы действий врача
Алгоритм диагностики сепсиса и септического шока
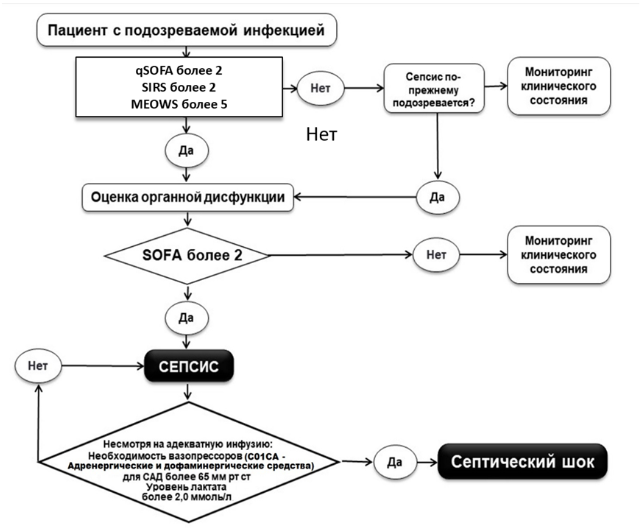
Начальная терапия сепсиса/септического шока
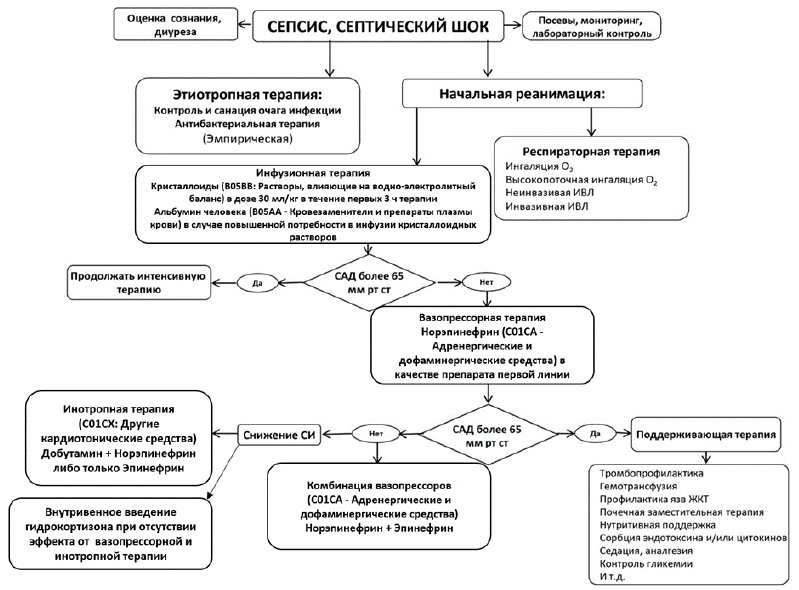
Алгоритм определения тактики санации очага (гистерэктомия)
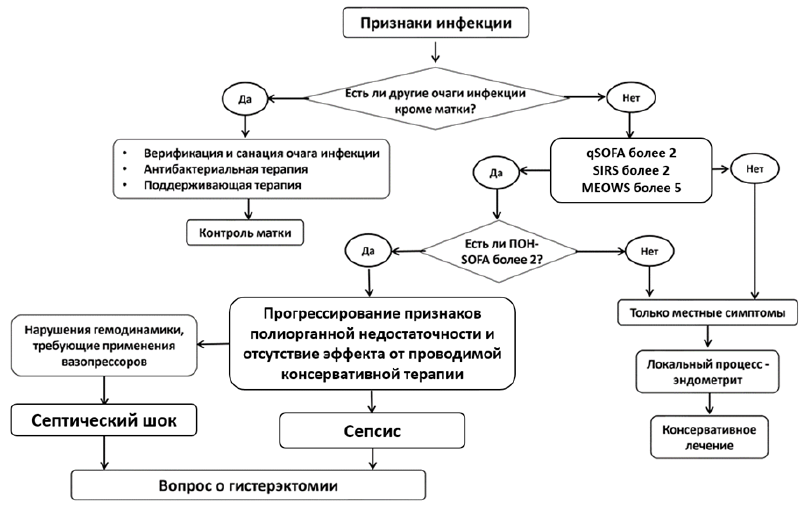
Приложение В. Информация для пациента
Что такое послеродовые инфекционные осложнения?
Послеродовые инфекционные осложнения – это группа инфекционных заболеваний, которые развиваются у женщин в послеродовом периоде и включают инфекции области хирургического вмешательства, инфекции молочных желез, послеродовой эндометрит, акушерский перитонит, сепсис и септический шок.
Каковы причины послеродовых инфекционных осложнений?
Причиной развития инфекции являются различные микроорганизмы. При развитии инфекции возникает активация клеточного и гуморального звеньев иммунной системы, а также ряд других биологических механизмов, которые приводят к ограничению очага инфекции и предотвращению ее распространения. Эти процессы называются воспалением.
Если ваша иммунная система слаба или инфекция особенно серьезна, возможно ее стремительное распространение на другие ткани и органы. Генерализация инфекции приводит к неблагоприятному воздействию воспаления на весь организм в целом. Воспаление служит причиной повреждения тканей, снижения кровотока, опасного падения артериального давления и снижения поступления кислорода к органам и тканям.
Каковы симптомы послеродовых инфекционных осложнений?
Для инфекции области хирургического вмешательства характерно наличие гнойного отделяемого из послеоперационной раны, локализованная боль, отечность, уплотнение в области раны, повышение как местной температуры, так и повышение температуры тела выше 38ºC.
Основным симптомом послеродового эндометрита является лихорадка с повышением температуры тела выше 38ºC. Кроме того, могут наблюдаться озноб, тазовые боли, выделения из половых путей с неприятным запахом или гнойные выделения, общее чувство дискомфорта или плохого самочувствия, головная боль, слабость, снижение аппетита. Как правило, в большинстве случаев послеродовой эндометрит диагностируется в течение 10 дней после родов.
Для начальной стадии акушерского перитонита характерны интенсивная боль в области живота, рвота, учащение пульса и дыхания, лихорадка с повышением температуры тела выше 38ºC.
Ранними симптомами сепсиса могут быть: высокая или низкая температура тела, озноб, учащенное сердцебиение и дыхание. Другими симптомами могут быть: спутанность сознания, невнятная речь, головокружение, обморок, тошнота, рвота, сильная боль в мышцах, выраженная одышка, снижение количества выделяемой мочи, бледность.
Как проводится лечение послеродовых инфекционных осложнений?
Лечение инфекции области хирургического вмешательства проводится комплексно и включает как хирургическую обработку области послеоперационной раны, так и антибактериальную терапию.
Лечение послеродового эндометрита в первую очередь включает антибактериальную терапию, а также применение дополнительных методов терапии под контролем клинических и лабораторных показателей.
В случае подозрения на акушерский перитонит и сепсис в первую очередь необходима безотлагательная госпитализация в стационар. Большинству пациентов необходимо оказание медицинской помощи в отделении интенсивной терапии.
Из-за повреждения жизненно важных органов исходы сепсиса могут быть крайне неблагоприятными. Однако при раннем выявлении и лечении в большинстве случаем происходит полное выздоровление. Лечение сепсиса проводится под контролем клинических и лабораторных показателей и включает антибактериальную, инфузионную (внутривенное введение растворов), кислородную терапию, санацию источника сепсиса и др. методы комплексной терапии.
Как происходит реабилитация после инфекционных осложнений послеродового периода?
После выписки домой пациенты могут испытывать выраженную усталость, снижение аппетита, потерю мышечной массы со снижением мышечного тонуса, общую слабость, хрупкость ногтей и зубов, сухость и шелушение кожи, истончение и выпадение волос, подавленное настроение. Для того, чтобы помочь восстановлению организма, необходим длительный отдых, правильный уход под наблюдением врача-акушера-гинеколога, врача-терапевта, врача-физиотерапевта и других специалистов.
Некоторые люди после сепсиса сталкиваются с депрессией, тревожным расстройством, отсутствием желания общения с окружающими. Преодолению данных проблем может помочь поддержка членов семьи и друзей, а также консультации специалистов.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Быстрая шкала последовательной оценки органной недостаточности qSOFA (quick Sequential Organ Failure Assessment)
Название на русском языке: быстрая шкала последовательной оценки органной недостаточности qSOFA
Оригинальное название: quick Sepsis Related Organ Failure Assessment, quickSOFA, qSOFA
Источник: Brabrand M., Havshøj U., Graham C. A. Validation of the qSOFA score for identification of septic patients: a retrospective study //European journal of internal medicine. – 2016. – Т. 36. – С. e35-e36., https://qsofa.org/research.php
Тип: шкала оценки
Назначение: скрининговая оценка наличия органной недостаточности, выявление пациентов с подозрением на инфекцию, которые подвергаются большему риску неблагоприятного исхода вне отделения интенсивной терапии (ОРИТ)
Содержание:
|
Показатель |
qSOFA, баллы |
|---|---|
|
Снижение АД (АД систолическое ≤100 мм рт ст) |
1 |
|
Увеличение частоты дыхания (≥22 дыханий/мин) |
1 |
|
Нарушение сознания (по шкале Глазго <15) |
1 |
Ключ (интерпретация):
— наличие 2 или более баллов qSOFA связано с большим риском смерти или длительного пребывания в отделении интенсивной терапии.
Приложение Г2. Критерии синдрома системного воспалительного ответа (SIRS)
Название на русском языке: Критерии синдрома системного воспалительного ответа
Оригинальное название: SIRS Criteria (Systemic Inflammatory Response Syndrome Criteria)
Источник: Fernando SM, Tran A, Taljaard M, et al. Prognostic Accuracy of the Quick Sequential Organ Failure Assessment for Mortality in Patients With Suspected Infection: A Systematic Review and Meta-analysis. Annals of Internal Medicine 2018 February 20, 168 (4): 266-275
Тип: шкала оценки
Назначение: скрининг для выявления пациентов с сепсисом
Содержание:
1. Температура тела >38°C или <36°С (Да = 1; Нет = 0)
2. Частота сердечных сокращений >90/мин (Да = 1; Нет = 0)
3. Частота дыхания >20 в минуту или PaCO2 менее 32 мм рт. ст. (4,3 кПа) (Да = 1; Нет = 0)
4. Количество лейкоцитов >12000 /мкл(>12 x109/л) или <4 000 /мкл (<4 x109/л) (Да = 1; Нет = 0)
Ключ (интерпретация):
— 0 или 1 балл: "Пациент не соответствует критериям SIRS"
— 2, 3 или 4 балла: "Пациент соответствует критериям SIRS. Обратите внимание, что это не диагностирует инфекцию"
Приложение Г3. Модифицированная акушерская ранняя система предупреждения (Modified Early Obstetric Warning System - MEOWS)
Название на русском языке: Модифицированная акушерская ранняя система предупреждения
Оригинальное название: Modified Early Obstetric Warning System, MEOWS
Источник (официальный сайт разработчиков, публикация с валидацией): Singh A. et al. Evaluation of maternal early obstetric warning system (MEOWS chart) as a predictor of obstetric morbidity: a prospective observational study // Eur. J. Obstet. Gynecol. Reprod. Biol. Elsevier Ireland Ltd, 2016. Vol. 207. P. 11–17.
Тип: шкала оценки
Назначение: раннее выявление сепсиса и других критических состояний в акушерстве
Содержание:
Ключ (интерпретация):
— Низкий риск – 1–4 балла
— Средний риск – 5–6 баллов
— Высокий риск – 7 и более баллов.
Любое одиночное значение в 3 балла указывает на крайнее отклонение от нормы, что должно относиться как минимум к группе среднего риска.
Приложение Г4. Шкала последовательной оценки органной недостаточности SOFA (Sequential Organ Failure Assessment)
Название на русском языке: Шкала последовательной оценки органной недостаточности SOFA
Оригинальное название: Sequential Organ Failure Assessment Score
Источник: Singer M, Deutschman CS, Seymour CW, et al: The third international consensus definitions for sepsis and septic shock (sepsis-3). JAMA 315:801–810, 2016. doi:10.1001/jama.2016.0287; Lambden S. et al. The SOFA score—development, utility and challenges of accurate assessment in clinical trials //Critical Care. – 2019. – Т. 23. – №. 1. – С. 1-9.
Тип: шкала оценки
Назначение: оценка органной недостаточности
Содержание:
|
Шкала SOFA |
0 |
1 |
2 |
3 |
4 |
|---|---|---|---|---|---|
|
Дыхание PaO2/FiO2, мм рт. ст. (кПа) |
≥400 (53.3) |
<400 (53.3) |
<300 (40) |
<200 (26.7) с респираторной поддержкой |
<*100 (13.3) с респираторной поддержкой |
|
Коагуляция Тромбоциты, х 103/мм3 |
≥150 |
<150 |
<100 |
<50 |
<20 |
|
Печень Билирубин, мг/дл (мкмоль/л) |
<1.2 (20) |
1.2-1.9 (20-32) |
2.0-5.9 (33-101) |
6.0-11.9 (102-204) |
>12.0 (204) |
|
Сердечно- cосудистая система Гипотензия |
АДср ≥70 мм рт. ст. |
АДср. <70 мм рт. ст. |
Допамин** <5 более 1 часа, или добутамин** (любая доза) |
Допамин** 5,1-15 более 1 часа, или эпинефрин** ≤0,1 более 1 часа, или норэпинефрин** ≤0,1 более 1 часа |
Допамин** >15 более 1 часа, или эпинефрин** >0,1 более 1 часа, или норэпинефрин** >0,1 более 1 часа |
|
ЦНС Шкала комы Глазго |
15 |
13-14 |
10-12 |
6-9 |
<6 |
|
Почки Креатинин, мг/дл, ммоль/л |
<1,2 (110) |
1,2-1,9 (110-170) |
2,0-3,4 (171-299) |
3,5-4,9 (300-440) Или |
>5.0 (440) |
|
Диурез, мл/сутки |
- |
- |
- |
<500 |
<200 |
Ключ (интерпретация):
SOFA индекс равен сумме всех шести показателей
- минимальный общий балл: 0
- максимальный общий балл: 24
- чем выше балл, тем больше дисфункция органа
- чем больше общий балл, тем сильнее полиорганная дисфункция.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.