Полип толстой и прямой кишки
 Версия: Клинические рекомендации РФ 2025 (Россия)
Версия: Клинические рекомендации РФ 2025 (Россия)
Общая информация
Краткое описание
Разработчик клинической рекомендации
Общероссийская общественная организация "Ассоциация колопроктологов России",
Ассоциация "Эндоскопическое общество "РЭндО"
Одобрено Научно-практическим Советом Минздрава России
Клинические рекомендации
Полип толстой и прямой кишки
Год утверждения (частота пересмотра): 2025
Пересмотр не позднее: 2027
ID:949_1
Возрастная категория: Взрослые, Дети
Определение заболевания или состояния (группы заболеваний или состояний)
Поскольку K63.5 полип толстой кишки и K62.1 полип прямой кишки обозначают не только доброкачественные эпителиальные новообразования, но и воспалительные, гамартомные и субэпителиальные образования, данные клинические рекомендации (КР) разработаны по диагностике и лечению доброкачественных эпителиальных новообразований (ДЭНо) ободочной и прямой кишки (ОиПК), которые составляют значимую часть подкласса заболеваний, объединенных в МКБ-10 единым кодом D12, а именно D12.0 – D12.8, а также D37.4. В настоящих НКР не рассматриваются ДЭНо заднего прохода (ануса) и анального канала (код D12.9), наследственные полипозные синдромы, а также неэпителиальные новообразования, так как они имеют ярко выраженную специфику в диагностике, лечении, профилактике и им посвящены отдельные КР.
ДЭНо ОиПК, к которым относятся все виды зубчатых новообразований, включая гиперпластические полипы, сидячие зубчатые полипы с дисплазией или без нее, традиционные зубчатые аденомы, а также эпителиальные неоплазии аденоматозного вида входят в группу «поверхностных» эпителиальных новообразований (ПЭНо) [1-5]. На авторитетном общемировом семинаре в Париже, в 2002 г. вышеописанные образования были отнесены к категории опухолей, глубина распространения которых ограничена слизистой оболочкой, либо подслизистой основой, то есть двумя внутренними, поверхностными по отношению к просвету кишки, слоями. Важно подчеркнуть, что в состав группы ПЭНо ОиПК были включены ранние колоректальные раки (КРР). Это решение принято единогласно, поскольку дифференциальная диагностика между ДЭНо и ранним КРР в рамках колоноскопии представляет собой сложную задачу. Тактические и методические подходы в лечении того и другого состояния во многом пересекаются, что обусловлено тем, что большинство ПЭНо ОиПК, включая значительную долю ранних КРР, поддаются радикальному удалению с помощью методов внутрипросветной эндоскопической хирургии. Эксперты отмечают, что успешное и окончательное подтверждение этих заболеваний возможно только после получения результатов патоморфологического исследования удаленной опухоли. Таким образом, выбор метода лечения имеет значительную роль в улучшении исходов и качества жизни пациентов [3].
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем

Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
В зависимости от размера ПЭНо ободочной и прямой кишки подразделяют на [50-52]:
− Миниатюрные (крошечные; мельчайшие; англ. – diminutive): до 5 мм включительно;
− Мелкие (маленькие; англ.- small): 6 – 9 мм;
− Средние (синонимы: средних размеров; среднеразмерные; англ. – intermediate): 10-19 мм;
− Большие (синонимы: крупные; англ. – large): 20 – 39 мм;
− Гигантские (англ. – giant): 40 мм и более.
*Аденомы размерами 10 мм и более и/или аденомы, которые содержат, по крайней мере, 20-25% ворсинчатого компонента и/или интраэпителиальную дисплазию высокой (тяжелой) степени, относят к «развитым» аденомам («advanced adenoma») [53].
В соответствии с модифицированной макроскопической классификацией эпителиальных опухолей Боррманна, предложенной им еще в 1926 году для описания внешнего вида и характера роста распространенных злокачественных опухолей (типы 1 – 4), поверхностные эпителиальные новообразования относятся к нулевому типу. Термин «тип 0» был выделен для того, чтобы отличать «поверхностные» полиповидные и неполиповидные эпителиальные опухоли (как доброкачественные, так и злокачественные) от распространенных [3, 54].
Парижская эндоскопическая классификация поверхностных эпителиальных новообразований толстой кишки 2002 года служит для более детальной и точной макроскопической оценки ПЭНо. Она используется для характеристики как доброкачественных эпителиальных опухолей и их предшественников, так и злокачественных опухолей, относимых во время эндоскопического исследования к типу 0 (табл. 1). Таким образом, в соответствии с внешним видом и характером роста ПЭНо различают возвышающиеся (полиповидные) ПЭНо – подтип 0-I, плоские (неполиповидные и неизъязвленные) ПЭНо – подтип 0-II, изъязвленные (язвенные, подрытые) ПЭНо – подтип 0-III [3, 55].
Таблица 1 Макроскопическая эндоскопическая классификация поверхностных эпителиальных новообразований (ПЭНо) пищеварительного тракта (тип 0)
|
Возвышающийся (полиповидный) тип |
0-I |
|
|---|---|---|
|
ПЭНо (полип) на ножке |
|
0-Ip |
|
ПЭНо (полип) на широком основании |
|
0-Is |
|
Плоский тип |
0-II |
|
|
ПЭНо плоско – приподнятое |
|
0-II а |
|
ПЭНо абсолютно плоское |
|
0-II b |
|
ПЭНо плоско – углубленное |
|
0-IIс |
|
Изъязвленный (язвенный; подрытый) тип |
0-III |
|
Кроме того, существуют смешанные формы ПЭНо, которые несут признаки двух типов, например: углубленно-приподнятые (0-IIc+IIa); приподнято-углубленные (0-IIa+IIc).
Латерально растущие (распространяющиеся/стелющиеся) опухоли (LST- Lateraly Spreading Tumor) – вид опухолей толстой кишки с особым стелющимся по слизистой оболочке кишки характером роста, что позволяет им достигать гигантского размера, без существенного увеличения высоты. Исходный/минимальный диаметр LST, который позволяет отнести их к этой категории стелющихся опухолей, составляет 10 миллиметров. Латерально растущие опухоли подразделяются на LST-G (Granular – гранулярные/зернистые) и LST-NG (NonGranular – негранулярные/гладкие), а каждую из них дополнительно делят на подтипы. LST-G подразделяется на гомогенный (LST-G-H) и смешанный узловой (LST-G-NM) подтипы; LST-NG подразделяется на плоский приподнятый (LST-NG-FE) и с псевдодепрессией (LST-NG-PD) подтипы [4, 55, 56].
Международная эндоскопическая классификация NICE (NBI International Colorectal Endoscopic) эпителиальных новообразований толстой кишки, 2009 г. основана на оценке цвета, микрососудистой архитектоники и рисунка поверхности эпителиальных новообразований толстой кишки при их осмотре в узком спектре света (NBI – Narrow Band Imaging) без увеличения [57, 58]. Согласно NICE классификации эпителиальные новообразования толстой кишки ранжируются на 3 типа, в соответствии с прогнозом их патоморфологического строения: тип 1 – гиперпластические и зубчатые полипы на широком основании; тип 2 – все аденомы, как с легкой, так и с тяжелой дисплазией, а также рак с минимальной глубиной инвазии в подслизистый слой; тип 3 – рак с глубокой инвазией [59].
В 2018 году группа японских экспертов ввели четвертую категорию разделив 2 тип на две подгруппы: 2A, включающую дисплазию легкой степени, и 2B, тяжелую степень дисплазии или ранний рак [60].
Универсальная эндоскопическая классификация опухолей толстой кишки в узкоспектральном режиме с увеличением: классификация JNET японской группы экспертов NBI. Согласно JNET классификации эпителиальные новообразования толстой кишки распределяются на 4 типа, в соответствии с прогнозом их патоморфологического строения: тип 1 – гиперпластические полипы/зубчатые образования на широком основании; тип 2А – внутрислизистая неоплазия низкой степени; тип 2В – внутрислизистая неоплазия высокой степени / рак с поверхностной инвазией в подслизистый слой; тип 3 – рак с глубокой инвазией [61, 62].
Классификация WASP (Workgroup Serrated Polyps And Polyposis – рабочей группы по зубчатым полипам и полипозу) [63]. Классификация WASP была создана для дифференциальной диагностики зубчатых новообразований на широком основании от гиперпластических полипов и от классических аденом по эндоскопическим критериям. На первом этапе дифференциальной диагностики используется классификация NICE, чтобы отличить ПЭНо 1 типа (зубчатое/гиперпластическое) от 2 типа (аденоматозное). На втором этапе у данных новообразований оценивается наличие или отсутствие эндоскопических признаков, характерных именно для зубчатых поражений.
К ним относятся:
1) облаковидная поверхность;
2) нечеткая граница;
3) неправильная форма;
4) «черные точки/пятнышки» внутри крипт (ямки II-О типа по T.Kimura).
Исходя из сочетания эндоскопических признаков делается вывод о предполагаемой морфологической структуре образования [64-66].
Классификация ямочного рисунка (микрорельефа) слизистой оболочки и эпителиальных новообразований толстой кишки по S. Kudo, 1994 г. Классификация применяется в эндоскопии высокого разрешения с хромоколоноскопией и увеличением. Различают семь основных типов ямочного рисунка и несколько дополнительных. Типы ямочного рисунка I и II характерны для неопухолевых изменений толстой кишки. При III и IV типе вероятность подслизистой инвазии достигает 4%, а при V типе – 41%. Типы IIIL, IIIS, IV, Vi, и VN предполагают наличие неоплазии с прогрессом от низкого к высокому риску злокачественного развития, где тип IIIS может соответствовать неоплазии высокой степени и раку; Vi – неоплазии высокой степени и раку, ограниченному слизистой оболочкой и поверхностными отделами подслизистого слоя; тип VN – аденокарциноме с глубокой инвазией. Риск малигнизации возрастает в следующей последовательности: IIIL
Классификация Всемирной Организации Здравоохранения (ВОЗ) опухолей ободочной и прямой кишки принята и опубликована в 2019 г. В классификации ВОЗ применяются морфологические коды Международной классификации онкологических заболеваний, третье издание, второй пересмотр (МКБ-О-3.2 / ICD-O-3.2). Опухоли закодированы в соответствии с их патоморфологическими характеристиками: /0 – доброкачественная опухоль; /1 – неустановленный, пограничный, либо неопределенный характер опухоли; /2 – рак “in situ” и интраэпителиальная неоплазия grade III; /3 – злокачественные опухоли, первичный очаг [68].
Доброкачественные эпителиальные опухоли и их предшественники
|
Зубчатая дисплазия низкой степени |
8213/0* |
|---|---|
|
Зубчатая дисплазия высокой степени |
8213/2* |
|
Гиперпластический полип, микровезикулярный тип |
|
|
Гиперпластический полип, бокаловидноклеточный |
|
|
Аденоматозный полип с дисплазией низкой степени |
8210/0* |
|
Аденоматозный полип с дисплазией высокой степени |
8210/2* |
|
Тубулярная аденома низкой степени |
8211/0* |
|
Тубулярная аденома высокой степени |
8211/2* |
|
Виллезная (ворсинчатая) аденома низкой степени |
8261/0* |
|
Виллезная (ворсинчатая) аденома высокой степени |
8261/2* |
|
Тубуловиллезная (тубуло-ворсинчатая) аденома низкой степени |
8263/0* |
|
Тубуловиллезная (тубуло-ворсинчатая) аденома высокой степени |
8263/2* |
|
Развитая (аdvanced) аденома |
|
|
Железистая интраэпителиальная неоплазия низкой степени |
8148/0 |
|
Железистая интраэпителиальная неоплазия высокой степени |
8148/2 |
* Коды, отмеченные звездочкой, одобрены комитетом IARC /WHO для ICD-O на его заседании в апреле 2019 года.
Согласованная международная Венская патоморфологическая классификация эпителиальных неоплазий толстой кишки впервые опубликована в 2000 г. [69]. Последний пересмотр Венской классификации, включающий в себя рекомендации по лечебной тактике, был опубликован в виде проекта в 2002 г. [70] и был рекомендован к повсеместному использованию (табл. 2) и (частично) принят в последней классификации опухолей пищеварительного тракта ВОЗ 2019 г. [2].
Таблица 2 Венская классификация эпителиальных неоплазий пищеварительного тракта; пересмотр [70] (Актуальная версия; утверждена в 2002 г.)
|
Категория |
Субкатегории и Диагноз |
Лечебная тактика |
|---|---|---|
|
1 |
Отсутствие неоплазии (Неоплазия / дисплазия не обнаружена). Данная категория включает в себя нормальный, реактивный, регенеративный, гиперпластический, атрофический и метапластический эпителий) |
Наблюдение по усмотрению врача, в зависимости от клинических показаний |
|
2 |
Неопределенность в отношении неоплазии / дисплазии. Диагностируется в тех случаях, когда неясно, имеются регенераторные изменения или неопластические. Диагностику затрудняют воспаление и артифициальные изменения |
Необходимо наблюдение и повторная биопсия, так как сущность процесса осталась неизвестной |
|
3 |
Неоплазия слизистой оболочки низкой степени Аденома низкой степени Дисплазия низкой степени (слабая дисплазия) |
Эндоскопическая резекция или наблюдение* |
|
4 |
Неоплазия слизистой оболочки высокой степени 4.1 Аденома/дисплазия высокой степени 4.2 Неинвазивный рак (рак «in situ») Неинвазивный означает доказанное отсутствие инвазии (прорастания) в собственную пластинку слизистой оболочки (за пределы базальной мембраны). 4.3 Подозрение на инвазивный рак. Трудно определить имеется инвазия в собственную пластинку слизистой оболочки или нет. 4.4 Внутрислизистый рак. Внутрислизистый означает, что имеется инвазия (прорастание) в собственную пластинку слизистой оболочки (за пределы базальной мембраны) или в мышечную пластинку слизистой оболочки |
Эндоскопическая или хирургическая локальная резекция* |
|
5 |
Инвазия рака в подслизистый слой |
Хирургическая резекция* |
*Выбор метода лечения зависит от общих размеров новообразования; глубины его инвазии, оцениваемой по данным лучевых методов, эндоскопии, и эндоУЗИ; от общих факторов, таких как возраст пациента и выраженность сопутствующих заболеваний.
Патоморфологическое стадирование малигнизированных полипов толстой кишки по R.C. Haggitt 1985 г. [71]. Согласно классификации R.C.Haggitt для полиповидных малигнизированных эпителиальных новообразований на ножке (Ip типа) различают 5 уровней инвазии [71, 72]:
Уровень 0 – отсутствие инвазии за пределы мышечной пластинки слизистой оболочки;
Уровень 1 – инвазия через собственную мышечную пластинку слизистой оболочки в подслизистый слой, ограниченная головкой полипа;
Уровень 2 – инвазия в подслизистый слой, достигающая шейки полипа;
Уровень 3 – инвазия в подслизистый слой, распространяющаяся на ножку полипа на любом ее уровне вплоть до основания;
Уровень 4 – инвазия в подслизистый слой кишечной стенки ниже уровня основания ножки полипа, независимо от глубины этой инвазии.
Для полиповидных малигнизированных эпителиальных новообразований на широком основании (Is типа) по R.C.Haggitt различают только 2 уровня раковой инвазии: нулевой и четвертый. Таким образом, по современным представлениям, уровень инвазии 1-3 по R.C. Haggitt, соответствует T1sm1, а уровень 4 может соответствовать, как поверхностной (T1sm1), так и более глубокой инвазии (T1sm2) в подслизистый слой. Классификацию Хаггит достаточно широко использовали до проведения Парижского семинара в 2002 г. и продолжают использовать для стадирования глубины инвазии в малигнизированных полипах на ножке (опухолях 0-Ip типа), но для оценки полиповидных опухолей на широком основании (0-Is типа) она неуместна.
Универсальное патоморфологическое стадирование глубины инвазии раннего рака (Т1) толстой кишки в подслизистый слой. Использовать оценку глубины инвазии раннего рака толстой кишки на широком основании, деля подслизистую основу на 3 субслоя равной толщины по S.Kudo, 1984 г. [73] или по R. Kikuchi, 1995 [74] возможно лишь в патологоанатомических образцах, содержащих целиком весь подслизистый слой и хотя бы часть собственного мышечного слоя толстой кишки, то есть в образцах, полученных при трансабдоминальной резекции сегмента кишки, либо при полнослойной эндоскопической резекции. Для полноценной оценки глубины инвазии опухоли в подслизистый слой после эндоскопической резекции опухоли, в том числе и с применением метода диссекции подслизистого слоя, достоверно использовать эти классификации невозможно. Именно поэтому, для удаленных препаратов, полученных путем резекции ПЭНо через эндоскоп, в 2002 году [3] была принята универсальная система оценки глубины инвазии в подслизистый слой в абсолютных величинах (микронах). Глубина инвазии в подслизистый слой условно разделена на два уровня: поверхностная (sm1) и глубокая (sm2), граница между ними находится на глубине 1000 µ (микрон). Именно эта система оценки сейчас наиболее широко используется в клинической практике и в научных исследованиях.
Вспомогательная классификация в системе TNM – R-классификация, которая предназначена для оценки полноты удаления опухоли. Она отражает эффективность проведенного вмешательства, влияет на выбор дальнейшей лечебной тактики и служит весомым фактором прогноза [75].
Различают нижепоименованные категории R:
RX – Оценить наличие резидуальной опухоли невозможно
R0 – Остаточная опухоль отсутствует
R1 – Микроскопическая остаточная опухоль
R2 – Макроскопическая остаточная опухоль [76].
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
В основе развития ПЭНо ОиПК лежит сочетание экзогенных и эндогенных факторов. На сегодняшний день доказана роль внешнего воздействия, включая влияние окружающей среды, низкую двигательную активность, так и особенностей питания, национальные диеты, кроме того, содержательный состав потребляемой пищи (продукты с высоким содержанием жиров, белков и низким количеством клетчатки), курение и регулярный прием алкоголя в развитии ПЭНо толстой кишки.
Эндогенные факторы:
- Возраст. Большое количество исследований демонстрируют, что распространенность аденом ободочной и прямой кишки предсказуемо увеличивается на 10–15% у лиц в возрасте от 50 до 75 лет [6-8]. Доброкачественные новообразования ободочной и прямой кишки у детей чаще встречаются в первом десятилетии жизни, при этом пик заболеваемости приходится на возраст от двух до пяти лет [9, 10];
- Пол. У мужчин частота выявления аденоматозных новообразований толстой кишки при скрининговой колоноскопии в 1,77 раза выше, чем у женщин [8]. К тому же, крупные эпителиальные образования толстой кишки (>9 мм) на 50% чаще наблюдаются у мужского населения по сравнению с женским [11]. В структуре заболеваемости у мужчин КРР составляет 10,9%, смертности — 9%. У женщин заболеваемость и смертность одинакова — по 9,5% [12];
- Наследственность. Прослеживается связь между ПЭНо и семейным анамнезом [13, 14]. Пациенты, у которых есть родственник первой степени родства с подтвержденным КРР, имеют повышенный риск развития полипов в толстой кишке, а также более высокий риск «развитых» аденом [15, 16]. Частота выявления КРР увеличивается в 1,76 раза у пациентов, у которых есть родственник первой линии родства с диагнозом КРР, даже после 80 лет [17]. Наследственные генетические патогенные варианты являются основным этиологическим фактором формирования ПЭНо при семейном аденоматозном полипозе толстой кишки (мутация в гене APC) и MutYH-ассоциированном полипозе (мутации в гене MutYH) [18]. По сравнению со взрослыми, КРР у детей встречается крайне редко. Наследственные синдромы предрасположенности к раку (ICSS) — группа заболеваний, при которых пациенты предрасположены к широкому спектру опухолей в результате патогенных мутаций в генах зародышевой линии, являются важной причиной КРР у детей [19];
- Воспалительные заболевания кишечника (ВЗК). Больные с ВЗК (язвенный колит – ЯК и болезнь Крона – БК) с поражением не менее 30% толстой кишки подвержены более высокому риску КРР, чем в общей популяции [20].
Патогенез формирования поверхностных эпителиальных новообразований толстой кишки до конца не исследован. Однако на сегодняшний день известны основные пути канцерогенеза колоректального рака. К традиционной модели относится последовательная хромосомная нестабильность, которая охватывает 70–90% случаев, сопровождаясь прогрессией от аденомы к карциноме. В то же время, путь зубчатой неоплазии, составляющий приблизительно 10% случаев, часто ассоциирован с мутациями онкогенов BRAF и KRAS, в то время как мутации гена APC встречаются значительно реже [21-27]. Кроме того, около 8% всех случаев КРР связаны с наследственными и семейными формами заболевания, такими как семейный аденоматозный полипоз толстой кишки и синдром Линча. Наконец, около 2% случаев развиваются на фоне длительного воспаления слизистой оболочки при воспалительных заболеваниях кишечника, которое имеет название колит-ассоциированный КРР [28-33].
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Распространенность эпителиальных новообразований толстой кишки колеблется от 20% в возрасте 45 лет до более чем 50%-60% к 85 годам [34-39]. Распространенность полипов толстой кишки у детей и подростков составляет от 0,08 до 6% [40, 41].
По результатам скрининговых колоноскопий определено, что полипы выявляются у 20%-53% лиц в возрасте 50 лет и старше, среди которых до 9,7% составляют «развитые» опухоли, определяемые как аденомы размером ≥10 мм или имеющие ворсинчатую структуру или высокую степень дисплазии эпителия [42-47]. По данным мета-анализа публикаций, включающих сведения о результатах колоноскопии, выполненной у лиц в возрасте ≥50 лет, полипы выявлены в 24% наблюдений, а распространенность «развитой» аденомы составляет около 4,5% [48]. Следует отметить, что частота аденом выше среди мужчин и увеличивается с возрастом [48, 49].
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
В большинстве случаев поверхностные эпителиальные новообразования ободочной и прямой кишки достаточно долго протекают бессимптомно и единственным способом их выявления служат скрининговые исследования. При достижении больших размеров ПЭНо толстой кишки возможно появление неспецифических клинических симптомов, таких как запоры или диарея, в том числе с выделением слизи, кровь в кале, спазмы и боли в животе с высоким уровнем их вариабельности.
Согласно данным некоторых научных публикаций частота обнаружения колоректальных полипов по данным колоноскопии у бессимптомных пациентов составляет от 18,2% до 46% [77, 78]. В исследовательской работе Xiaohua Long и др. превалирующую долю среди всех симптомов занимает диарея, составляющая 54,2%. Это объясняется тем, что большинство эпителиальных новообразований толстой кишки представляют собой аденомы, которые, имея крупные размеры, способны выделять большое количество слизи, вызывающие секреторную диарею. Кроме того, также отмечено, что женщины чаще сталкиваются с запорами, в то время как мужчины обычно жалуются на диарею или гематохезию [79].
В многочисленных исследованиях, посвященных ректальным кровотечениям, авторы акцентируют внимание на том, что гематохезия, в частности, является симптомом прогрессирующей аденомы толстой кишки. Данное клиническое проявление, характеризующееся выделением свежей крови из прямой кишки, может свидетельствовать о выраженной васкуляризации и повышенной склонности к кровотечениям, свойственным аденомам больших размеров или злокачественным новообразованиям [80-82].
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерием установки диагноза служит выявление ПЭН ободочной и/или прямой кишки по данным эндоскопического исследования или альтернативного инструментального метода обследования толстой кишки (Компьютерно-томографическая колоноскопия, УЗИ, МРТ).
1. Жалобы и анамнез
-
Рекомендуется тщательный сбор и оценка жалоб и анамнеза пациента, в том числе, с использованием анкетирования, с целью выявления факторов риска развития новообразований толстой кишки и формулировки показаний для дальнейшего дообследования [83, 88-91].
Для взрослых - Уровень убедительности рекомендации – B (уровень достоверности доказательств – 3).
Для детей - Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Основной причиной трудностей̆ своевременного выявления ПЭН толстой кишки служит отсутствие ранних и достоверных клинических проявлений этого заболевания у 46% пациентов [84, 86]. По результатам метаанализа данных популяционных скрининговых исследований, среди пациентов, перенесших колоноскопию, с использованием в качестве методов стратификации анкетирования для выявления в семейном анамнезе родственников с новообразованиями толстой кишки, частота выявления аденом (ADR) при колоноскопии составила 33,3% [87].
Вместе с тем, в рамках пилотных скрининговых исследований при положительном экспресс-исследовании кала на скрытую кровь иммунохроматографическим методом частота выявления аденом при колоноскопии составила 54,1%, а при высоком уровне риска по данным анкетирования – 67,3% [88, 91].
У детей наиболее частыми клиническими проявлениями являются гематохезия и ректальное кровотечение [89]. Нередко отмечаются жалобы на выпадение полиповидных образований через задний проход, с эпизодами ущемления и самоампутации полипа и последующим кровотечением [90].
2. Физикальное обследование
-
Пациентам с ПЭНо рекомендуется выполнение тщательного физикального осмотра, включая пальцевое ректальное исследование для исключения сопутствующей патологии анального канала и диагностики объемных новообразований в брюшной полости [92-95].
Для взрослых – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Для детей – Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Комментарии: Пальпация органов брюшной полости и пальцевое ректальное исследование позволяют заподозрить наличие новообразований ободочной и прямой кишки [92, 93]. Однако для достоверной диагностики требуется назначение инструментальных методов диагностики, таких как колоноскопия, УЗИ органов брюшной полости (комплексное), УЗИ прямой кишки трансректальное, компьютерная томография тонкой кишки с контрастированием МРТ [94, 95].
3. Лабораторные диагностические исследования
-
Рекомендуется выполнение общего (клинического) анализа крови и анализа крови биохимического общетерапевтического, коагулограммы (ориентировочного исследования системы гемостаза) с целью подбора препарата для подготовки толстой кишки к диагностическому и оперативному вмешательству и для оценки рисков интра- и послеоперационного кровотечения [90, 96-99].
Для взрослых – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Для детей – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Комментарии: Такие факторы риска как мужской пол (RR=1.64), гипертоническая болезнь (RR=1,54), прием антитромботических средств (RR=4,04), размер ПЭН более 10мм (RR=3,83), локализация ПЭН в правых отделах (RR=2,48) и применения для удаления новообразования метода мукозэктомии (RR=2,99) являются факторами риска развития послеоперационного кровотечения [98, 99]. Таким образом, у пациентов, длительно принимающих антитромботическую терапию необходим контроль коагулограммы, своевременная отмена антитромботических средств или назначение мост-терапии перед эндоскопическим удалением ПЭН [91].
4. Инструментальные диагностические исследования
-
Рекомендуется проведение колоноскопии во всех случаях положительного экспресс-исследования кала на скрытую кровь иммунохроматографическим методом, при высоком риске обнаружения полипов и рака по данным анкетирования, либо в случае ранее выявленного новообразования толстой кишки с целью определения тактики лечения [88, 91, 100-118].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Выполнение колоноскопии показано [100]:
1) Лицам, относящимся к группам риска:
− лицам с отягощенным семейным анамнезом по наследственным полипозам и колоректальному раку [101, 102];
− пациентам с семейным аденоматозным полипозом, синдромом Пейтца–Егерса, ювенильным полипозным синдромом и зубчатым полипозным синдромом [103-108];
− пациентам с ранее диагностированными эпителиальными новообразованиями толстой кишки [109];
− пациентам с воспалительными заболеваниями кишечника [109-111];
− пациентам, перенесшим радиационные и химиотерапевтические методы лечения заболеваний толстой кишки или соседних органов [112, 113].
2) Лицам с наличием следующих клинических проявлений, жалоб и симптомов [114, 115]:
− нарушение акта дефекации (запоры, диарея, неустойчивый стул);
− выделение крови при акте дефекации;
− патологические примеси в кале (слизь, гной);
− анемия;
− дискомфорт и боли в животе;
− потеря веса.
3) Лицам с подозрением/установленными заболеваниями/патологическими состояниями толстой кишки по результатам лабораторной и инструментальной диагностики:
− лица с положительным результатом экспресс-исследования кала на скрытую кровь иммунохроматографическим методом [116]
− опухоли дистального отдела толстой кишки, обнаруженные при ректороманоскопии [117].
− изменения толстой кишки, выявленные по результатам лучевых методов диагностики и толстокишечной эндоскопии видеокапсульной [117].
− заболевания смежных органов (эндометриоз, опухоли органов малого таза, забрюшинного пространства, органов брюшной полости) [118].
-
Выполнение плановой колоноскопии с целью диагностики эпителиальных доброкачественных новообразований ободочной и прямой кишки не рекомендуется во всех случаях, когда риск проведения исследования превышает его диагностическую ценность, а результаты исследования не влияют на выбор тактики и метода лечения пациента на момент выполнения колоноскопии и принятия этого решения [100].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Абсолютными противопоказаниями к проведению плановой колоноскопии служат: острая фаза нарушения мозгового кровообращения; острая фаза инфаркта миокарда; тяжелые степени сердечно-сосудистой, легочной и смешанной недостаточности (стадия декомпенсации), которые наблюдаются при ишемической болезни сердца, пороках сердца, массивной эмболии легочной артерии; нарушения ритма сердечной деятельности (особенно при нестабильных состояниях), такие как: пароксизмальная брадиаритмия, мерцательная аритмия с мерцанием предсердий или пароксизмы мерцательной аритмии, групповые желудочковые экстрасистолы в виде бигеминии или тригеминии, тяжелые степени поперечной блокады сердца; расслаивающая аневризма аорты или сердца.
Абсолютными противопоказаниями к проведению плановой колоноскопии также служат: сверхтяжелые (фульминантные) формы воспалительных заболеваний толстой кишки (язвенный колит, болезнь Крона, ишемический колит, радиационный колит); острые воспалительные инфильтраты брюшной полости (включая острый дивертикулит); подозрение на абсцесс брюшной полости, перитонит.
Относительными противопоказаниями к проведению колоноскопии служат: острые воспалительные заболевания аноректальной зоны (анальная трещина, геморрой в стадии обострения, тромбоз геморроидальных узлов, парапроктит); ранний послеоперационный период (хирургическое вмешательство на органах брюшной полости и малого таза); выраженная гепатоспленомегалия; напряженный асцит; гидроторакс, гидроперикард; тяжелые нарушения свертывающей системы крови; геморрагические васкулиты; беременность (особенно, второй — третий триместр).
-
До начала эндоскопического вмешательства рекомендуется получить информированное добровольное согласие пациента на проведение исследования и лечения с целью подтвердить, что пациент получил полную и понятную информацию о медицинском вмешательстве, включая цели, методы, риски и альтернативы, и добровольно соглашается на его проведение [119].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Каждому пациенту должны быть разъяснены в понятной форме как положительные стороны скринингового/диагностического исследования и оперативного вмешательства через эндоскоп, так и сопряженные с ним риски. Информирование должно включать объяснение цели вмешательства; подготовки и процесса исследования; обсуждение вопросов возможного возникновения дискомфорта, ранних и поздних осложнений; альтернативные методы исследования, а также преимущества колоноскопии по сравнению с другими методами. Перед оформлением информированного добровольного согласия (ИДС) лечащим врачом либо иным медицинским работником пациенту или его законному представителю предоставляется в доступной форме полная информация о целях, методах оказания медицинской помощи, связанном с ними риске, возможных вариантах видов медицинских вмешательств, о последствиях этих медицинских вмешательств, в т.ч. о вероятности развития осложнений, а также о предполагаемых результатах оказания медицинской помощи. ИДС оформляется в виде официального документа, подписывается пациентом или его законным представителем. Предлагается регистрировать количество пациентов, отказывающихся от колоноскопии в день исследования и во время проведения исследования, а также причины отказов.
-
Рекомендуется обеспечить адекватную подготовку пациента к колоноскопии с использованием специального рациона питания с низким содержанием клетчатки и препаратов, сертифицированных для подготовки к колоноскопии. Части пациентов также необходима коррекция общего статуса и нарушений, вызванных сопутствующими заболеваниями [120-137].
Для взрослых – Уровень убедительности рекомендации – В (уровень достоверности доказательств – 1).
Для детей – Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Комментарии: Эффективная подготовка пациента к колоноскопии является ключевым моментом для обеспечения качественного исследования [127, 137]. Качественная подготовка пациента обеспечивает возможность интубации слепой кишки, детального осмотра слизистой оболочки всех отделов толстой кишки и выявления патологических изменений, в т.ч. новообразований. В условиях неудовлетворительной подготовки выявление новообразований затруднено или невозможно [128]. В настоящее время существует множество различных схем подготовки пациента к эндоскопическим вмешательствам на толстой кишке. Трудности в подготовке возникают у пациентов, испытывающих затруднения при чтении инструкций; социально и экономически дезадаптированных; старческого возраста; находящихся в стационаре; обездвиженных; употребляющих опиаты; имеющих сахарный диабет, хронические запоры и операции на органах брюшной полости в анамнезе [129].
-
Для обеспечения эффективности диагностических и лечебных мероприятий в процессе колоноскопии, а также для минимизации осложнений рекомендуется оценивать качество подготовки пациента к колоноскопии по Бостонской шкале (Приложение Г1) и отражать степень подготовки кишки в протоколе/заключении эндоскопического исследования, это позволяет врачам-эндоскопистам убедиться в том, что пациент правильно подготовлен к процедуре, что, в свою очередь, влияет на точность результатов и безопасность лечения [138-142].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Комментарии: Бостонская шкала – многократно валидированная, удобная в повседневной работе и наиболее широко используемая в мире оценочная шкала [139-142]. Ее применение обеспечивает стандартизацию регистрации качества подготовки и осмотра толстой кишки в процессе колоноскопии. По Бостонской шкале качество очистки толстой кишки к колоноскопии может считаться адекватным при оценке 6 и более баллов, при условии, что оценка каждого из 3-х оцениваемых сегментов – не менее 2-х баллов [141, 142].
-
При выполнении колоноскопии для расправления просвета кишки рекомендуется использовать углекислый газ (CO2) [143, 144].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 1).
Комментарии: Углекислый газ не поддерживает горение и всасывается из просвета кишки в кровь в 13 раз быстрее, чем кислород и в 160 раз быстрее, чем азот. В связи с чем, применение его при эндоскопических вмешательствах предотвращает взрывы, неконтролируемую эмфизему и болевой синдром, связанные с выполненной манипуляцией [144].
-
Рекомендуется выводить колоноскоп из слепой кишки до анального отверстия в течение не менее 6 минут для качественного исследования толстой кишки [138, 145, 148].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Комментарии: Отмечается корреляция частоты выявления аденом (ЧВА) и времени извлечения колоноскопа от купола слепой кишки до анального отверстия. Частота выявления аденом (9,4% - 32,7%) зависит от времени извлечения эндоскопа (которое варьируется от 3,1 до 16,8 минут). При времени извлечения более 6 минут ЧВА статистически значимо выше, чем при более быстром осмотре толстой кишки (28,3% против 11,8%, р <0,001) [146, 147]. Оптимальное время выведения колоноскопа опытным специалистом, без учета выполнения уточняющей визуальной диагностики и биопсии, должно составлять не менее 10 минут; минимально допустимое время – не менее 6 минут [148].
-
Для выявления патологических изменений рекомендуется выполнять детальный осмотр терминального отдела подвздошной кишки и всей толстой кишки по мере извлечения колоноскопа [149-151].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Ротационная методика колоноскопии предусматривает минимальное расправление кишки газом на этапе проведения колоноскопа и, соответственно, не требует и не обеспечивает полноценного осмотра всех отделов и участков исследуемого органа. Детальный осмотр слизистой оболочки кишки выполняется в процессе извлечения колоноскопа из подвздошной/слепой кишки до анального канала [151].
В том случае, если в просвете кишки определяется остаточное кишечное содержимое, настоятельно рекомендуется очистить поверхность всех осматриваемых участков слизистой оболочки путем введения жидкости через инструментальный канал эндоскопа или, при наличии, через отдельный ирригационный канал эндоскопа при помощи помпы. При значительном количестве пенистого содержимого целесообразно использовать раствор пеногасителя (АТХ-группа: А03AX - другие препараты для функциональных желудочно-кишечных расстройств) [152-154].
-
Для проведения колоноскопии и выявления эпителиальных доброкачественных новообразований толстой кишки рекомендуется использовать видеоэндоскопы высокого разрешения с целью мультимодального осмотра и улучшения качества изображения [155-170].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Комментарии: Ретроспективные исследования продемонстрировали значительное увеличение показателя ЧВА при обследовании пациентов колоноскопами высокого разрешения. Так, в исследовании Buchner A.M. с соавт. сообщалось о повышении общего показателя ЧВА при осмотре толстой кишки на оборудовании высокой четкости по сравнению со стандарной колоноскопией с 24,3% до 28,8% (p=0.012), ЧВА аденом размером менее 5 мм при обследовании колоноскопами высокой четкости увеличилась с 16,9% до 19,9% (p=0.024) [155]. В двух ретроспективных когортных исследованиях [156, 157] сообщалось о значительном увеличении показателей ЧВА в аналогичных группах при выполнении колоноскопии высокого разрешения по сравнению со стандартной – на 8,2% (р = 0,02) и на 12,6% (р = 0,007), соответственно. В ряде исследований продемонстрировано, что использование технологии узкоспектрального изображения (NBI) не приводит к повышению показателя ЧВА, однако позволяет выявлять значительно большее количество аденом с плоским типом роста и аденом, локализованных в правых отделах ободочной кишки [158-160].
Эффективность узкоспектральной колоноскопии (NBI) в дифференциальной диагностике ПЭНо, определении его границ и проведении прицельной биопсии продемонстрирована в целом ряде исследований [161, 162]. Применение режима NBI при проведении колоноскопии позволяет провести дифференциальную диагностику ПЭНо по международным классификациям NICE и JNET (в режиме NBI + увеличение х70) [61, 163-165].
Исследование Yoshida N. et. al. показало, что другая цифровая технология контрастирования – LCI (Linked color imaging) улучшает показатели выявления колоректальных новообразований по сравнению с режимами белого света [166]. Suzuki S. et. al. опубликовал результаты крупного многоцентрового рандомизированного исследования, в котором было показано, что LCI улучшает показатель выявления аденом по сравнению с режимом белого света (58,7% против 46,7%; P<0,01) [167]. Другие исследования продемонстрировали, что применение режима BLI (blue laser imaging), по сравнению с осмотром в белом свете может улучшить выявляемость колоректальных полипов, особенно в отношении их местоположения, размера и морфологии. Классификации NICE и JNET могут применяться при использовании BLI для эндоскопической дифференциальной диагностики аденом и гиперпластических полипов [168, 169].
В крупном когортном исследовании, включавшем 1936 пациентов, установлен более высокий уровень показателя ЧВА при использовании технология i-SCAN, по сравнению со стандартной колоноскопией в белом свете [170]. Однако в других исследованиях не было никакого улучшения в уровне показателя выявления аденом. В настоящее время роль i-SCAN в улучшении показателя выявления аденом еще не доказана окончательно, и требуются более крупные проспективные исследования.
-
Для повышения частоты выявления аденом рекомендуется при колоноскопии дополнительно использовать программное обеспечение (искусственный интеллект), продемонстрировавшее воспроизводимый уровень точности автоматизированного выявления/детекции эпителиальных доброкачественных новообразований толстой кишки [171-175].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 1).
Комментарии: В систематическом обзоре был проведен анализ 6 рандомизированных контролируемых исследований для сравнения ЧВА при проведении колоноскопии с использованием и без использования CADe-системы (2480 человек в группе с применением CADe, 2482 – в контрольной группе) [171]. Результаты мета-анализа показали статистически значимое увеличение частоты выявления аденом в случае использования компьютерных систем автоматической детекции полипов и увеличения времени выведения колоноскопа. Другой систематический обзор с мета-анализом семи рандомизированных клинических исследований (2595 колоноскопий с применением CADe систем, 2622 стандартных колоноскопий) показал 80% увеличение среднего количества выявляемых аденом небольшого размера на одного пациента при применении средств автоматической компьютерной детекции, по сравнению со стандартной колоноскопией [172]. Правда, исследования, включенные в обзор, в основном, проведены в одной стране (КНР); также не указан уровень врачей-эндоскопистов, выполнявших колоноскопии. Мета-анализ шести рандомизированных контролируемых исследований (4996 случаев) показал более высокий уровень выявления аденом и полипов при колоноскопии с использованием искусственного интеллекта для плоских аденом и зубчатых образований на широком основании, хотя для полипов на ножке «стандартная» колоноскопия показала лучший результат [173]. Крупное мультицентровое рандомизированное контролируемое исследование (3059 пациентов, 1519 в группе проведения колоноскопии с использованием CADe системы, 1540 в контрольной группе стандартной колоноскопии) показало увеличение частоты выявленных аденом, как у эндоскопистов с опытом более 5000 проведенных колоноскопий, так и у менее опытных эндоскопистов [174]. Аналогичные результаты получены в исследованиях отечественных разработок [175].
-
Рекомендуется выполнение щипцовой биопсии злокачественной опухоли толстой кишки у пациентов старше 18 лет с забором не менее 6 прицельных биоптатов из наиболее подозрительных в плане злокачественности участков новообразования с целью определения гистологического типа опухоли, степени ее дифференцировки и для определения оптимальной тактики лечения [176, 177].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Комментарии: Для оценки оптимального количества биоптатов для увеличения диагностической точности гистологического исследования и снижения нагрузки на врачей-патоморфологов были проведены исследования. В одном из них, включающем 37 случаев КРР было показано, что забор 6 фрагментов опухоли, по сравнению с меньшим количеством, позволяет статистически значимо увеличить частоту гистологического подтверждения с 61% до 92% (p<0,02). Наибольшая прогностическая точность достигается при выполнении прицельной биопсии центральной части опухоли (96,1%) [177].
-
Для снижения риска развития колоректального рака при обнаружении поверхностного эпителиального новообразования толстой кишки без признаков глубокой инвазии рекомендуется его удаление с направлением на гистологическое исследование [169, 178-180, 181].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4) – для взрослых.
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5) – для детей.
Комментарии: ПЭН толстой кишки, подозрительные в отношении малигнизации требуют тщательной эндоскопической оценки, с адекватным отмыванием и осмотром всего новообразования с использованием видеоэндоскопа высокого разрешения с функцией виртуальной хромоскопии и увеличения, для выявления участков инвазивного роста. В диагностически сложных случаях рекомендуется выполнение хромоскопии, контрастного исследования органов желудочно-кишечного тракта и увеличением для оценки ПЭНо по классификации С. Кудо. При V типе ямок и отсутствии явных признаков глубокой инвазии предлагается удалить ПЭНо единым блоком и стадировать его по результатам морфологического исследования. Данные предоперационной биопсии поверхностного эпителиального образования толстой кишки не позволяют достоверно исключить наличие в нем микрофокусов аденокарциномы. Исследования, касающиеся биопсии злокачественных колоректальных новообразований показали, что частота ложноотрицательных результатов может достигать 18,5-86% [169]. По данным Sung HY в 39,8% случаев имелись расхождения морфологических диагнозов после щипцовой биопсии и резекции полипов толстой кишки (в исследование включено 996 полипов у 813 пациентов) [178]. Халин К. Д. с соавторами сообщает, что фокус аденокарциномы в поверхностном эпителиальном образовании толстой кишки при предоперационной биопсии был выявлен только в 16,6% случаев [179]. В исследовании Hah Y. сравнили щипцовую биопсию и резекционную методику. Факторами снижения диагностической точности биопсии были размер новообразований >3 см, наличие депрессии, макроскопический тип LST гранулярный смешанный. Общее число случаев расхождения морфологического диагноза составило 103 (57,5%) [180]. В том случае, если в силу любых медицинских, организационных, административных, юридических и иных обстоятельств удаление ПЭНо откладывается/переносится на этап повторной колоноскопии, в заключении протокола первичной колоноскопии рекомендуется указать, что морфологическое исследование новообразования будет выполнено после его удаления при повторной рекомендованной/запланированной колоноскопии [182].
В случае невозможности удалить ПЭН единым блоком в связи с недостаточным оснащением и/или опытом врача-эндоскописта, возможно выполнить репрезентативные снимки или видеозапись участка подозрительного на наличие инвазии (до принятия решения о биопсии) и подробно охарактеризовать его в протоколе исследования согласно общепринятым классификациям. Пациент должен быть направлен в экспертный центр для консультации более опытным специалистом или принятия решения о дальнейшей тактике лечения. Биопсия ободочной кишки эндоскопическая остается в резерве для ПЭН с подозрением на малигнизацию, если выполнить его удаление единым блоком и направить к более опытному специалисту невозможно [183-185].
При условии, если выполнить удаление новообразования единым блоком невозможно, то квалифицированный фото- и видеопротокол осмотра всего новообразования колоноскопом экспертного уровня зачастую имеет большее значение для диагностики, чем изолированная биопсия [183]. Если ПЭН подлежит эндоскопическому удалению, биопсию выполнять не следует, поскольку существует риск развития фиброза в подслизистом слое, что значительно затрудняет эндоскопическую резекцию новообразования. Частота развития фиброза после выполнения биопсии до стигает 77% [184]. Срок развития подслизистого фиброза соответствует 3 неделям после выполнения биопсии, в связи с чем, в случае выполнения биопсии, целесообразно решить вопрос о дальнейшей тактике лечения в течение указанного срока [185].
-
Для уменьшения риска контаминации и рассеивания опухолевых клеток рекомендуется щипцы и петли, применяемые для биопсии или удаления потенциально злокачественных новообразований у пациентов старше 18 лет, не использовать повторно в процессе текущего вмешательства, а забор фрагментов опухоли следует выполнять в конце исследования [186].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Комментарии: Проведенное исследование продемонстрировало, что рабочий канал колоноскопа во время выполнения биопсии был «загрязнен» жизнеспособными опухолевыми клетками, и что следующие чистые инструменты, введенные в канал, были контаминированы клетками, которые, как было показано, сохраняли свой пролиферативный потенциал. Таким образом, хотя вероятность ятрогенного переноса опухолевых клеток кажется низкой, он может служить причиной метахронного КРР, который потенциально возможно предотвратить и минимизировать путем соблюдения безопасного (с онкологических позиций) порядка и последовательности применения чресканальных инструментов при выполнении эндоскопических вмешательств [186].
-
Рекомендуется рассматривать в качестве метода окончательной дифференциальной диагностики эпителиальных доброкачественных и ранних злокачественных неоплазий ободочной и прямой кишки морфологическое исследование полностью удаленных поверхностных эпителиальных новообразований [1, 3, 70, 182].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Эпителиальные доброкачественные новообразования и ранний колоректальный рак ободочной и прямой кишки входят в одну группу поверхностных эпителиальных новообразований [3, 70]. Провести достоверную дифференциальную диагностику между ЭДНО и ранним КРР по результатам эндоскопического осмотра и даже по результатам щипцовой биопсии – нетривиальная задача. Именно поэтому, рекомендуется удалить, как доброкачественное ПЭНо, так и новообразование с подозрением на малигнизацию (но без признаков глубокой инвазии) единым блоком, что позволяет выполнить полноценное морфологическое исследование всего новообразования и, соответственно, провести завершающую дифференциальную диагностику [1, 182].
-
Рекомендуется извлекать все эпителиальные новообразования толстой кишки, удаленные методами эндоскопической полипэктомии, резекции слизистой или диссекции в подслизистом слое и направлять их на патолого-анатомическое исследование операционного материала для верификации гистологического строения и оценки радикальности удаления [187-194].
Уровень убедительности рекомендации – B (уровень достоверности доказательств – 1).
Комментарии: По данным метаанализа S.E. Mason с соавторами [187], существующие методики эндоскопического осмотра и анализа новообразований не в состоянии обеспечить безопасное применение стратегии «resect and discard» («резецировал и не извлекаю») для новообразований проксимальнее ректо-сигмоидного изгиба; все удаленные новообразования должны быть направлены на патолого-анатомическое исследование операционного материала. Для прецизионной оценки горизонтальной и вертикальной плоскостей резекции рекомендуется фиксация образований на плотной непромокаемой основе [188-192]. Незамедлительная фиксация операционного материала сразу после удаления позволяет сохранить форму, размеры и ориентацию новообразования, а также позволяет смоделировать расположение опухоли в организме (в т.ч. опухоли, удаленной по частям) и избежать скручивания макропрепарата во время фиксации в формалине [188, 193]. Кроме того, следует избегать чрезмерного растяжения препарата, для предотвращения искажения и повреждения слоев [188, 194]. Для предотвращения высыхания и возможной деформации препарата при невозможности незамедлительной фиксации и погружения в формалин, допускается смочить удаленную опухоль физиологическим раствором натрия хлорида** или накрыть ее влажной салфеткой. Циркулярные опухоли, удаленные единым блоком, могут быть размещены на цилиндрическом предмете подходящего диаметра (шприц и т.д.) для лучшей фиксации.
-
При эндоскопическом удалении поверхностных эпителиальных новообразований толстой кишки без подслизистой инвазии совершеннолетним пациентам рекомендуется считать их удаление радикальным при негативных краях резекции (вертикальная – Rv – и горизонтальная – Rh) для определения в последующем адекватных сроков наблюдения [195-197].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Комментарии: Эндоскопическое удаление поверхностных эпителиальных новообразований считается радикальным при удалении опухоли в пределах здоровых тканей (R0). Метаанализ показал, что факторами риска местного рецидива являются большой размер, резекция новообразований фрагментами, а также наличие резидуальной опухоли в краях резекции (Rv1 или Rh1) [197]. При невозможности достоверной оценки линии резекции (резекция фрагментами, выраженное коагуляционное повреждение краев при электроэксцизии) (Rx) рекомендовано причислять такую категорию пациентов в разряд лиц с существующим риском рецидива новообразования и сокращать для них интервал наблюдения [197, 198].
5. Иные диагностические исследования
-
Ректороманоскопию и сигмоидоскопию не рекомендуется применять в качестве самостоятельного метода скрининга ПЭН толстой кишки. Ректороманоскопию и сигмоидоскопию предлагается использовать для детального осмотра зоны анального канала, отключенной прямой кишки [199-202].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Гибкая сигмоидоскопия позволяет обследовать внутреннюю поверхность толстой̆ кишки на расстоянии до 60 см от анального отверстия, а ректороманоскопия (РРС) на уровень 20-25 см. С помощью этих методов, безусловно можно выявить ПЭНо левой половины ободочной и прямой кишки; они также используются для удаления ПЭНо или получения образцов ткани для прижизненного патолого-анатомического исследования биопсийного (операционного) материала [199, 200]. Относительными преимуществами РРС и сигмоидоскопии служит то, что на проведение исследований требуется меньше времени, частота осложнений при исследовании, не сопровождающемся проведением полипэктомии, несущественна; как правило, нет необходимости и в применении седативных препаратов. Однако, очевидным недостатком методов служит отсутствие возможности обследования значительной части толстой кишки, что делает их использование в качестве самостоятельного метода скрининга/диагностики ПЭНо толстой кишки все менее и менее значимым. Это связано и с растущим пониманием роли зубчатого пути канцерогенеза, преимущественно в правой половине кишки и с развитием эндоскопической техники и методики колоноскопии. Ведь в то время, как специфичность РРС и сигмоидоскопии для диагностики новообразований левой половины кишки очень высокая (98-100%), их чувствительность в отношении всей толстой кишки недопустимо низкая и находится в пределах от 35% до 70% для сигмоидоскопии и 10-20% для РРС [201, 202].
-
В диагностических целях толстокишечную эндоскопию видеокапсульную (ТЭВ) рекомендуется применять как дополняющий, либо самостоятельный/альтернативный метод эндоскопического исследования у пациентов с противопоказаниями к выполнению гибкой колоноскопии, либо с незавершенной гибкой колоноскопией, либо у пациентов, которые отказываются от проведения гибкой колоноскопии [203-209].
Для взрослых – Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Для детей – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: В случае отсутствия опухолевой обструкции ТЭВ можно рассматривать, как альтернативу компьютерно-томографическая колоноскопии для исследования проксимального отдела толстой кишки при незавершенной колоноскопии. В литературе сообщалось о результатах семи исследований с использованием ТЭВ. В 75–100% случаев ТЭВ были визуализированы отделы толстой кишки, не достигнутые при колоноскопии [203-206], при этом изменения слизистой оболочки были выявлены в 24% – 100% случаев. В исследовании Spada с соавт. сравнивали компьютерно-томографическую колоноскопию и ТЭВ у пациентов с неполной колоноскопией [207]. В этом исследовании при ТЭВ были выявлены полипы ≥ 6 мм у 24,5% пациентов (95% ДИ 16,6–34,4%), при компьютерно-томографической колоноскопии у 12,2% (95% ДИ 6,8–20,8%), с относительной чувствительностью 2,0 (95% ДИ 1,34 – 2,98), что свидетельствовало о более высокой чувствительности ТЭВ для диагностики образований ≥ 6 мм. Анализ диагностики эпителиальных образований большего размера показал, что при ТЭВ образования диаметром ≥ 10 мм выявлены у 5,1% пациентов (95% ДИ 1,9–12,1%), при компьютерно-томографической колоноскопии у 3,1% пациентов (95% ДИ 0,8–9,3%), с относительной чувствительностью 1,67 (95% ДИ 0,69–4,00). Чувствительность ТЭВ для выявления полипов >9 мм колеблется от 87% до 92,8%, а специфичность составляет около 92% [208, 209].
-
Для скрининга/диагностики ПЭНо толстой кишки рекомендуется использовать компьютерно-томографическую колоноскопию как самостоятельный/альтернативный метод у пациентов с противопоказаниями к выполнению колоноскопии, либо у пациентов, которые отказываются от ее проведения или при незавершенной колоноскопии [207, 210-214].
Для взрослых – Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Для детей – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Компьютерно-томографическая колоноскопия служит методом выбора из числа всех лучевых методов исследования для диагностики ПЭН толстой кишки. Точность диагностики колоректального рака и больших/распространенных эпителиальных образований аналогична оптической колоноскопии как у симптоматических, так и у бессимптомных пациентов, и значительно превосходит точность диагностики при ирригоскопии [207, 211, 213]. В японском мультицентровом исследовании, включающем 1177 пациентов, чувствительность и специфичность компьютерно-томографической колоноскопии для выявления образований толстой кишки размерами >9 мм достигли более 90% [210], но этот метод существенно уступает колоноскопии и толстокишечной эндоскопии видеокапсульной в выявлении плоских ПЭНо менее 10 мм [210]. Серьезным препятствием для использования компьютерно-томографической колоноскопии в скрининге пациентов с высоким риском является то, что плоские образования в кишке могут быть пропущены, а также возрастающую лучевую нагрузку на пациента при повторных иссследованиях [212, 213].
-
С целью диагностики и выявления новообразований толстой кишки рекомендуется использовать ирригоскопию с двойным контрастированием как дополняющий метод исследования у пациентов в ситуациях, когда сегмент толстой кишки невозможно осмотреть эндоскопически или с применением компьютерно-томографической колоноскопии [215-217].
Для взрослых – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Для детей – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Ирригоскопия с двойным контрастированием позволяет исследовать всю толстую кишку, с ее помощью можно выявить до 50% крупных ПЭНо, но ее чувствительность и специфичность существенно ниже показателей̆, получаемых при проведении колоноскопии и компьютерно-томографической колоноскопии [215]. Даже при наличии больших ПЭНо ирригоскопия обладает существенно более низкой чувствительностью (48%), чем колоноскопия; кроме того, она дает больше ложноположительных результатов чем колоноскопия [216, 217].
-
Эндосонографию толстой кишки (Эндо-УЗИ) и магнитно-резонансную томографию (МРТ) толстой кишки не рекомендуется применять в регулярной клинической практике как самостоятельный метод характеристики доброкачественных эпителиальных новообразований толстой кишки у пациентов старше 18 лет [218-223].
Уровень убедительности рекомендации – B (уровень достоверности доказательств – 1).
Комментарии: Для проведения дифференциального диагноза между доброкачественными и злокачественными ПЭН толстой кишки, оценки глубины инвазии и определения оптимального метода удаления новообразований рекомендуется, в первую очередь, ориентироваться на макроскопический тип новообразования, микроструктуру его поверхности и локализацию, но не на данные эндо-УЗИ и МРТ. Многоцентровое рандомизированное контролируемое исследование, сравнивающее хромэндоскопию с увеличением и эндо-УЗИ в стадировании раннего колоректального рака, не выявило преимуществ эндо-УЗИ, а общая точность составила 78% для обоих методов [218]. В четырех метаанализах, сравнивающих результаты эндо-УЗИ, КТ и МРТ в оценке T и N статуса первично выявленных новообразований прямой кишки, потенциально подлежащих эндоскопическому удалению, не было обнаружено существенных различий между этими методами [219-222]. Точность, как эндо-УЗИ, так и МРТ в разграничении стадии T1 от стадии T2 была существенно ограничена, при этом отмечался высокий риск «завышения» стадии опухолевого процесса. В случаях расхождения результатов Т-стадирования опухоли между оптической хромоэндоскопией и эндо-УЗИ/МРТ результаты визуальной оценки во время эндоскопического исследования предлагается считать приоритетными [223].
Эндо-УЗИ и/или МРТ могут помочь в оценке инвазии ПЭН прямой кишки в подслизистую основу, если при визуальной оценке новообразования имеется подозрение на его прорастание в подслизистый слой. Ультразвуковая эндоскопическая аппаратура последнего поколения позволяет с высокой точностью установить толщину анаплазированной ткани, подтвердить или исключить прорастание опухоли в подслизистый и мышечный слои кишечной стенки [223].
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Консервативное ведение пациентов
-
Консервативное ведение, а именно наблюдение, без удаления эпителиальных доброкачественных новообразований, рекомендуется пациентам при обнаружении миниатюрных (1 – 5 мм) гиперпластических полипов прямой кишки и ректосигмоидного перехода, как правило, множественных, при условии, что гиперпластический характер этих полипов с высокой степенью достоверности определен по данным эндоскопического осмотра с использованием увеличения в комбинации с виртуальной хромэндоскопией [181, 224, 225, 226].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4) – для взрослых.
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5) – для детей.
Комментарии: Гиперпластические полипы обладают крайне низким потенциалом малигнизации (менее 0,6%) [198]. Подавляющее большинство миниатюрных (≤5 мм) полипов прямой кишки и ректосигмоидного перехода являются именно гиперпластическими полипами [224, 225].
Эндоскопическое лечение пациентов
-
Рекомендуется эндоскопическое удаление всех поверхностных эпителиальных новообразований (ПЭНо) толстой кишки без эндоскопических признаков глубокой инвазии, кроме миниатюрных (1 – 5 мм) гиперпластических полипов прямой кишки и ректосигмоидного перехода [181, 226, 227-229].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Роль аденом и зубчатых образований в канцерогенезе, как и эффективность их удаления в прерывании последовательности развития рака толстой кишки доказана в многочисленных исследованиях [227-230].
Эпителиальные новообразования толстой кишки <10 мм
-
Рекомендуется использовать методику «холодной» щипцовой биопсии (ХЩБ) для удаления эпителиальных доброкачественных новообразований толстой кишки размером ≤ 2 мм [231-237].
Для взрослых – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 1).
Для детей – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: ХЩБ позволяет полностью удалить эпителиальное новообразование толстой кишки размером ≤ 2 мм в 95,5-100% случаев [232-234, 237]. По данным рандомизированных исследований, ХЩБ не уступает «холодной» петлевой полипэктомии по частоте полной резекции и превосходит ее по частоте извлечения удаленных образований [235, 236].
-
Не рекомендуется использовать методику «горячей» биопсии (ГБ) для удаления эпителиальных новообразований толстой кишки вне зависимости от их размеров [181, 237, 238, 239].
Для взрослых – Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Для детей – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: В рандомизированных исследованиях ГБ достоверно уступала «холодной» полипэктомии по частоте удаления в пределах здоровых тканей и приводила к более выраженному термическому повреждению биопсийного материала [238-240]. Удаление эпителиальных новообразований толстой кишки ≤5 мм методикой ГБ приводит к выявлению остаточной ткани новообразования в 10-17% случаев [241, 242].
-
Рекомендуется использовать методику «холодной» полипэктомии (ХП) в качестве основного метода удаления плоских (II типа) и полиповидных на широком основании (Is типа) эпителиальных новообразований толстой кишки размером <10 мм [243- 245].
Для взрослых – Уровень убедительности рекомендации – В (уровень достоверности доказательств – 1).
Для детей – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Согласно данным двух метаанализов, включавших 12 исследований (2481 пациентов, 4535 образований) и 8 исследований (1665 пациентов, 3195 образований) и сравнивающих результаты применения «горячей» полипэктомии (ГП) и «холодной» полипэктомии (ХП), не выявлено достоверной разницы по частоте удаления новообразований размером <10 мм в пределах здоровых тканей. Продолжительность процедуры, по данным обоих метаанализов, была достоверно выше при ГП [243, 244]. Несмотря на то, что отсроченное кровотечение возникало чаще после «горячей», чем после ХП, разница не достигала уровня статистически достоверных значений [244]. В тоже время, рандомизированное исследование, сравнивающее ХП и ГП у пациентов, находящихся на антитромботической терапии, показало достоверно более низкий риск отсроченного кровотечения в группе «холодной» полипэктомии [246].
-
Рекомендуется при подозрении на тяжелую дисплазию или раннюю карциному в эпителиальном новообразовании толстой кишки размером <10 мм удаление его с использованием методики эндоскопической резекции слизистой толстой кишки у пациентов старше 18 лет (ЭРСО/EMR) [247, 248].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Комментарии: ХП приводит к более поверхностному удалению эпителиальных новообразований толстой кишки, по сравнению с ГП: частота наличия мышечной пластинки слизистой в препарате не отличалась в группах ГП и ХП, однако ткани подслизистого слоя чаще выявлялись в препаратах после «горячей» полипэктомии [249]. По данным ретроспективного исследования, сравнивающего морфологические результаты ХП и ЭРСО, глубина резекции в гистологическом препарате (от уровня мышечной пластинки слизистой) в группах ХП и ЭРСО составили 76 и 338 мкм, соответственно (p <0.001) [250]. Частота удаления новообразований с положительными или не подлежащими морфологической оценке вертикальными краями резекции чаще наблюдалась в группе ХП, чем ЭРСО, 6% и 1%, соответственно (p <0.05) [250].
Эпителиальные новообразования толстой кишки 10-19 мм
-
Рекомендуется выполнять удаление плоских (II типа) и полиповидных на широком основании (Is типа) эпителиальных новообразований толстой кишки размером 10-19 мм методикой эндоскопической резекции слизистой толстой кишки (ЭРСО/EMR) или «горячей» (ГП), либо «холодной» полипэктомии (ХП) [245, 251, 252].
Для взрослых – Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Для детей – Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Комментарии: ЭРСО и ГП обладают сходной частотой полной резекции при удалении эпителиальных новообразований размером до 14 мм [241, 252]. Подслизистая инъекция раствора снижает риск глубокого термического повреждения кишечной стенки.
-
Рекомендуется выполнять эндоскопическую резекцию слизистой толстой кишки (ЭРСО/EMR) при удалении эпителиальных новообразований толстой кишки единым блоком или в пределах здоровых тканей с минимально возможным количеством ее фрагментов [252-254].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Комментарии: Эндоскопическое удаление эпителиальных новообразований толстой кишки фрагментами является независимым фактором риска местного рецидива [253]. Согласно крупному мультицентровому исследованию, частота местного рецидива повышалась только при удалении образования 3мя и более фрагментами [254]. Сроки возникновения рецидива также зависели от количества фрагментов: они были минимальными (3.8 ± 1.9 месяцев) при удалении опухоли 5ю и более фрагментами [253].
-
Рекомендуется для подслизистой инъекции при проведении эндоскопической резекции слизистой оболочки использовать как физиологический раствор натрия хлорида**, так и более вязкие растворы [245, 252, 254, 255].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 1).
Комментарии: Согласно данным метаанализа, использование более вязких растворов при выполнении ЭРСО повышает вероятность удаления единым блоком и снижает риск неполного удаления опухоли, не оказывая влияние на развитие осложнений [255].
-
Не рекомендуется выполнение рутинного профилактического клипирования дефекта слизистой с целью предупреждения отсроченного кровотечения после эндоскопического удаления эпителиальных новообразований толстой кишки у совершеннолетних больных [256, 257].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 1).
Комментарии: Согласно данным двух метаанализов, профилактическое клипирование дефекта слизистой с целью предупреждения отсроченного кровотечения не продемонстрировало преимуществ как в общей группе, так и при новообразованиях размером >20 мм [256, 257]. Профилактическое клипирование приводит к увеличению продолжительности вмешательства [258].
Эпителиальные новообразования толстой кишки >20 мм
-
Рекомендуется выбирать методику удаления плоского или полиповидного на широком основании эпителиального новообразования толстой кишки размером ≥20 мм в зависимости от предварительной эндоскопической оценки его морфологического строения у пациентов старше 18 лет [259, 260].
Уровень убедительности рекомендации – B (уровень достоверности доказательств – 2).
Комментарии: Выбор метода удаления (фрагментарная ЭРСО или ЭДПС) в зависимости от эндоскопической оценки морфологического строения опухоли позволяет избежать необходимости выполнения повторных хирургических вмешательств у ряда пациентов [259]. По сравнению с ЭРСО, ЭПДС ассоциирована с более высокой частотой полной резекции, а также с меньшим вовлечением латеральных краев резекции и рецидивом, обладает преимуществом в гистологической оценке препарата [260].
-
Рекомендуется проводить эндоскопическое удаление плоского или полиповидного на широком основании эпителиального новообразования ободочной кишки размером ≥20 мм с высоким/существенным риском наличия фокуса злокачественной опухоли единым блоком. Методом выбора является диссекция в подслизистом слое или гибридная диссекция в подслизистом слое у лиц старше 18 лет [261, 262].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
-
Рекомендуется проводить эндоскопическое удаление плоского или полиповидного на широком основании эпителиального образования ободочной кишки размером ≥ 20 мм без эндоскопических признаков глубокой инвазии методом эндоскопической резекции слизистой оболочки одним или нескольким фрагментами, или диссекцией в подслизистом слое у пациентов старше 18 лет, в зависимости от опыта лечебного учреждения [263-265].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Комментарии: Согласно метаанализу, при удалении новообразований размером ≥ 20 мм после ЭРСО фрагментами частота местного рецидива составляет 20% [266]. ЭДПС повышает вероятность полного удаления образования по сравнению с ЭРСО и снижает риск местного рецидива, однако эти преимущества достигаются за счет большего риска перфораций и увеличения продолжительности вмешательства. Потенциальная необходимость в хирургическом вмешательстве по поводу осложнений ЭДПС больше, чем по поводу осложнений ЭРСО [264, 267, 268].
По данным одного из самых крупных исследований, посвященных ЭРСО/EMR, риск местного рецидива после ЭРСО/EMR фрагментами составляет 16% и 4% через 4 и 16 месяцев после вмешательства, соответственно, причем размер рецидива был ≤5 мм в 71,7% случаев, а его эндоскопическое лечение успешным в 93,1% случаев [265]. Факторами риска развития местного рецидива после ЭРСО фрагментами явились размер новообразования >40 мм, массивное кровотечение во время вмешательства и наличие тяжелой дисплазии / HGD [269].
-
В случае отсутствия в медицинской организации достаточного опыта удаления «сложных» эпителиальных новообразований толстой кишки через эндоскоп (размером >40 мм, занимающих более 2/3 окружности кишки, рецидивных, с отсутствием «лифтинга») рекомендуется маршрутизировать совершеннолетнего пациента в учреждение экспертного уровня [270-272].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Комментарии: ЭРСО/EMR или ЭДПС/ESD при удалении сложных эпителиальных новообразований толстой кишки, проводимые в специализированных профильных центрах, являются эффективными и достаточно безопасными процедурами [270, 272].
-
Рекомендовано применение трансанальной эндоскопической микрохирургии (ТЭМ), как альтернативного метода локального удаления больших и гигантских эпителиальных новообразований прямой кишки у пациентов старше 18 лет [273, 274].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 1).
Комментарии: Опубликовано несколько метаанализов сравнивающих ТЭМ и ЭДПС/ESD для удаления крупных эпителиальных новообразований и раннего рака прямой кишки. Длительность выполнения ЭДПС/ESD была достоверно выше, чем ТЭМ, другие показатели, включая частоту осложнений, рецидивов и частоту удаления единым блоком, не отличались. Послеоперационный койко-день был больше в 1,6 раза после ТЭМ [275]. По данным другого метаанализа длительность вмешательства была ниже в группе ЭДПС/ESD, а длительность госпитализации – в группе ТЭМ [276]. Таким образом, данных, позволяющих сделать однозначный выбор в пользу того или иного типа вмешательства, недостаточно, и в настоящее время он зависит от опыта конкретной клиники и ее специалистов.
-
Рекомендуется (при наличии возможности и необходимого оборудования) маркировать маркером эндоскопическим BLACK EYE новообразования толстой кишки у больных после 18 лет, подозрительные на ранний рак, а также иные новообразования при ожидаемой сложности их обнаружения во время хирургического вмешательства и\или повторного эндоскопического обследования [275].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Комментарии: Эндоскопическая маркировка BLACK EYE в местах локализации подозрительных на наличие малигнизации новообразований, а также выявленного раннего рака, помогает идентифицировать место резекции при контрольной колоноскопии или во время хирургического вмешательства. Предпочтительно размечать более одной, как правило 2-3 метки, на разных стенках кишки дистальнее новообразования и подробно документировать детали инъекции (материал, объем, положение относительно новообразований) в протоколе исследования. Несмотря на то, что имеются сведения о возможных осложнениях после введения эндоскопической маркировки BLACK EYE, проявляющихся лихорадкой, болями в животе, и даже формированием абсцессов, показано, что введение BLACK EYE после предварительной подслизистой инъекции физиологического раствора натрия хлорида** является безопасным. Маркер эндоскопический BLACK EYE для эндоскопического татуажа на основе стерильных углеродных микрочастиц обладает лучшим профилем безопасности [275].
Эпителиальные новообразования толстой кишки на ножке
-
Рекомендуется использовать методику горячей полипэктомии (ГП) для удаления эпителиальных новообразований толстой кишки на ножке (тип 0-Ip), а также применение механического гемостаза (с помощью устройства для наложения лигатур однократного применения или клип-аппликатора) с целью профилактики непосредственного и отсроченного кровотечения при удалении полипов типа 0-Ip с размером головки ≥ 20 мм и/или ножки ≥ 10 мм в диаметре [181, 226, 245, 252, 276, 277].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 1) – для взрослых.
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5) – для детей.
Комментарии: Основным методом удаления полипов на ножке является ГП. Основным видом осложнений при удалении таких новообразований является отсроченное кровотечение. Такие способы механического гемостаза, как эндоскопическое лигирование или клипирование, снижают риск кровотечения после удаления эпителиальных новообразований на ножке [278, 279]. Наибольший эффект профилактики кровотечения продемонстрирован при новообразованиях на ножке размером >20 мм [280].
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Специфические меры реабилитации пациентов с доброкачественными новообразованиями ободочной и прямой кишки отсутствуют. Меры медицинской реабилитации после эндоскопического вмешательства направлены, как и после любого хирургического вмешательства, на максимально быстрое восстановление в послеоперационном периоде. Однако, они различны для пациентов после ЭПДС, ЭРСО и «холодной» петлевой полипэктомии и подразумевают ограничение физических нагрузок и диетические ограничения в течение 7-14 дней.
Госпитализация
Организация оказания медицинской помощи
Медицинская помощь пациентам с доброкачественными новообразованиями толстой кишки, за исключением медицинской помощи в рамках клинической апробации, в соответствии с федеральным законом от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» (с изменениями и дополнениями), организуется и оказывается:
1) В соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается Минздравом России;
2) В соответствии с приказом Минздрава России от 06.12.2017 № 974н «Об утверждении Правил проведения эндоскопических исследований», приказом Минздравсоцразвития России от 02.04.2010 № 206н «Об утверждении Порядка оказания медицинской помощи населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля», приказом Минздрава России от 15.11.2012 № 922н «Об утверждении Порядка оказания медицинской помощи взрослому населению по профилю "хирургия", приказом Минздрава России от 19.02.2021 № 116н "Об утверждении Порядка оказания медицинской помощи взрослому населению при онкологических заболеваниях», Приказом Минздрава России от 09.06.2020 № 560н «Об утверждении Правил проведения рентгенологических исследований», Приказом Минздрава России от 08.06.2020 № 557н "Об утверждении Правил проведения ультразвуковых исследований», Приказом Минздрава России от 18.05.2021 № 464н «Об утверждении Правил проведения лабораторных исследований»;
3) На основе настоящих клинических рекомендаций;
4) С учетом стандартов медицинской помощи, утвержденных Минздравом России.
Направление на диагностическое исследование при подозрении на наличие доброкачественного новообразования толстой кишки осуществляется в соответствии с приказом Минздрава России от 06.12.2017 № 974н «Об утверждении Правил проведения эндоскопических исследований», после предварительной оценки рисков предстоящего вмешательства.
Диагностика доброкачественных новообразований толстой кишки проводится в рамках оказания первичной специализированной медико-санитарной помощи лечения в амбулаторных условиях или условиях дневного стационара, при оказании медицинской помощи при санаторно-курортном лечении врачом-эндоскопистом и другими врачами-специалистами в эндоскопическом кабинете, который является структурным подразделением медицинской организации или иного учреждения, осуществляющего медицинскую деятельность, либо входит в состав эндоскопического отделения медицинской организации.
Во время диагностической колоноскопии может осуществляться тотальная биопсия ПЭНо размером до 10 мм методом холодной тотальной петлевой или щипцовой биопсии. Рекомендованное количество новообразований, подлежащих тотальной биопсии, не должно превышать 5 [298]. Частота развития осложнения при осуществлении тотальной биопсии методом холодной полипэктомии [299] в амбулаторных условиях составляет: 0,07% – перфорация, 0,14% – кровотечение, 0,07% – подслизистая гематома [300], что сопоставимо с осложнениями при диагностической колоноскопии без дополнительных вмешательств. Выполнение тотальной биопсии в амбулаторных условиях методом холодной полипэктомии [299] должно осуществляться врачом-эндоскопистом в эндоскопическом кабинете, который является структурным подразделением медицинской организации или иного учреждения, осуществляющего медицинскую деятельность, и входит в состав эндоскопического отделения медицинской организации. Обязательным условием удаления новообразований является наличие полноценного аппаратно-инструментального оснащения отделения эндоскопии средствами для эндоскопической коррекции осложнений. Рекомендуется весь материал, полученный при эндоскопической биопсии или эндоскопическом удалении новообразований и направляемый на прижизненную морфологическую диагностику, размещать во флаконе с достаточным количеством (не менее, чем 20-кратный объем от объема препарата) 10% раствора нейтрального (забуференного) формалина на срок не более, чем 24-48 часов (Приказ Министерства здравоохранения Российской Федерации от 24 марта 2016 г. № 179н «О Правилах проведения патолого-анатомических исследований»).
Правила выполнения, репрезентативный объем биопсийного материала, правила (стандарт) маркировки, порядок заполнения направления, порядок и сроки доставки в патологоанатомическое отделение, методическое обеспечение гистопатологического исследования (правила фиксации и окраски биоматериала, необходимость выполнения и характер иммуногистохимического исследования) и другие вопросы системно изложены в правилах проведения патологоанатомических исследований (Приказ Министерства здравоохранения Российской Федерации от 24 марта 2016 г. № 179н «О Правилах проведения патолого-анатомических исследований»).
При выявлении у пациента доброкачественного новообразования толстой кишки, требующего его удаления, врачи-колопроктологи, врачи-хирурги, врачи-онкологи, направляют пациента на госпитализацию для оказания первичной специализированной медико-санитарной помощи или специализированной медицинской помощи после предварительной оценки рисков предстоящего вмешательства.
Лечение пациентов с доброкачественными новообразованиями толстой кишки проводится в плановом порядке в эндоскопическом отделении медицинской организации в рамках оказания первичной специализированной медико-санитарной помощи в условиях дневного стационара по профилям «колопроктология», «онкология», «хирургия», а также в рамках оказания специализированной медицинской помощи по указанным профилям в условиях дневного или круглосуточного стационара.
Показанием для госпитализации в медицинскую организацию для оказания первичной специализированной медико-санитарной помощи в условиях дневного стационара является наличие поверхностного эпителиального новообразования (ПЭНо) Is и/или II типа размером менее 10 мм, в количестве до 10 штук, отсутствие рецидивных доброкачественных новообразований и признаков инвазии в подслизистый слой у пациентов с анестезиологическим риском I или II степени по шкале ASA (Приложение Г). Методы удаления – холодная или горячая полипэктомия. Госпитализация возможна при наличии у медицинской организации лицензии на оказание первичной медико-санитарной помощи в условиях дневного стационара по анестезиологии и реаниматологии.
Показаниями для госпитализации в медицинскую организацию для оказания специализированной медицинской помощи в условиях дневного стационара или стационара кратковременного пребывания являются: размер полипов на ножке (Ip): диаметра ножки менее 10 мм, размера его головки менее 20 мм, размер ПЭНо Is и/или II типа менее 20 мм, отсутствие рецидивных доброкачественных новообразований и признаков инвазии в подслизистый слой, количество образований – до 10, степень анестезиологического риска по шкале ASA – I или II. Методы удаления – холодная или горячая полипэктомия, а также эндоскопическая резекция слизистой оболочки. Госпитализация возможна при наличии у медицинской организации лицензии на оказание первичной медико-санитарной помощи в условиях дневного стационара или стационара кратковременного пребывания по анестезиологии и реаниматологии.
Показаниями для госпитализации в медицинскую организацию для оказания специализированной медицинской помощи в условиях круглосуточного стационара являются: полипы на ножке (Ip) диаметром более 10 мм, головка полипа размером более 20 мм, а также ПЭНо Is и/или II типа и латерально-стелющиеся опухоли размером более 20 мм. Госпитализация также показана при наличии более 10 новообразований, подлежащих удалению, подозрении на поверхностную инвазию или рецидивный характер новообразования, а также у пациентов с полипами любого размера и анестезиологическим риском по шкале ASA III и выше. Высокий риск их развития, таких как риск кровотечения, перфорации, также являются показаниями для направления в круглосуточный стационар. При нахождении пациента в условиях круглосуточного стационара ограничений по методам эндоскопического удаления ПЭНо нет. Госпитализация возможна при наличии у медицинской организации лицензии на оказание специализированной медицинской помощи в стационарных условиях по анестезиологии и реаниматологии (табл. 4).
Таблица 4. Организация оказания медицинской помощи пациентам с эпителиальными новообразованиями
|
Вид и условия оказания медицинской помощи |
Первичная специализированная медико-санитарная помощь (амбулаторная) |
Первичная специализированная медико-санитарная помощь (дневной стационар) |
Специализированная медицинская помощь (дневной стационар), стационар кратковременного пребывания |
Специализированная медицинская помощь (круглосуточный стационар) |
|---|---|---|---|---|
|
|
Показания для госпитализации |
|||
|
Размер и тип ПЭНо |
Is и/или II типа менее 10 мм |
Is и/или II типа менее 10 мм |
Полипы на ножке диаметром менее 10 мм (Ip); головка полипа менее 20 мм (Ip); ПЭНо Is и/или II типа менее 20 мм |
Полипы на ножке (Ip) более 10 мм; головка полипа более 20 мм; ПЭНо Is и/или II типа, LST более 20 мм |
|
Количество образований |
До 5 штук |
До 10 штук |
До 10 штук |
Не регламентировано |
|
Рецидивные новообразования и инвазия |
Не допустимо |
Не допустимо |
Не допустимо |
Подозрение на поверхностную инвазию или рецидивный характер новообразований |
|
Метод удаления ПЭНо |
Холодная тотальна петлевая или щипцовая биопсия |
Холодная полипэктомия, горячая полипэктомия |
Холодная и горячая полипэктомия. Эндоскопическая резекция слизистой оболочки |
Без ограничений |
|
Анестезиологический риск (ASA) |
I или II |
I или II |
I или II |
I, II, III и выше |
|
Дополнительные показания |
- |
- |
- |
Наличие высокого риска кровотечения или перфорации толстой кишки |
|
Оснащение медицинской организации |
Эндоскопический кабинет или эндоскопическое отделение |
Наличие лицензии на оказание первичной медико-санитарной помощи в условиях дневного стационара по анестезиологии и реаниматологии |
Наличие лицензии на оказание первичной медико-санитарной помощи в условиях дневного стационара или стационара кратковременного пребывания по анестезиологии и реаниматологии |
Наличие лицензии на оказание специализированной медицинской помощи в стационарных условиях по анестезиологии и реаниматологии. |
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Профилактика ДЭНо и снижение риска КРР подразумевает многогранный подход, который охватывает образ жизни, коррекцию вредных привычек и проведение скрининговых исследований. Методы профилактики ДЭНо и КРР разделяются на две категории: первичные профилактические методы, направленные на выявление и коррекцию факторов риска, и вторичные профилактические методы, подразумевающие диагностику (скрининг) и удаление эпителиальных новообразований толстой кишки.
Первичная профилактика ДЭНо и КРР включает в себя необходимость соблюдения определенного образа жизни, а также исключения факторов риска развития ДЭНо и КРР.
Существует корреляция между снижением риска развития ДЭНо, КРР и пищевым поведением человека, направленным на увеличение потребление овощей и фруктов, цельного зерна, исключение большого количества красного и переработанного мяса, пищи с высоким содержанием жиров, а также ограничение потребления алкоголя [281-283].
Для профилактики ДЭНо и КРР также необходима физическая активность, способствующая поддерживанию оптимальной массы тела и отказ от курения [281, 282].
Вторичная профилактика ДЭНо и КРР (скрининг) включает в себя диагностику и удаление ДЭНо толстой кишки, что позволяет снизить риск развития КРР [284].
-
Рекомендуется экспресс-исследование кала на скрытую кровь иммунохроматографическим методом больным старше 18 лет [283].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: к преимуществам анализа кала на скрытую кровь относят: неинвазивность, чувствительность к раку и аденомам составляет 79% и 30%, соответственно, и низкую стоимость [285, 286].
-
У лиц после 18 лет с положительным экспресс-исследованием кала на скрытую кровь иммунохроматографическим методом рекомендовано использовать скрининговую или диагностическую колоноскопию с выявлением и удалением всех ДЭНо [287].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарии: Колоноскопия является золотым стандартом скрининга КРР и является первичным методом обследования особенно у лиц с высоким риском развития КРР (наследственные синдромы, пациенты с длительным анамнезом воспалительных заболеваний толстой кишки) [287].
Первичная скрининговая колоноскопия должна проводиться по достижении 40-летнего возраста (Приказ Минздрава России от 27.04.2021 № 404н (ред. от 01.02.2022) «Об утверждении Порядка проведения профилактического медицинского осмотра и диспансеризации определенных групп взрослого населения») [48]. У пациентов, имеющих родственников первой линии с КРР, скрининговую колоноскопию необходимо выполнять в возрасте на 10 лет моложе, чем возраст кровного родственника на момент постановки диагноза КРР [288].
Сроки наблюдения за пациентами, у которых выполнено эндоскопическое электрохирургическое удаление эпителиальных новообразованиий толстой кишки обуславливаются морфологической характеристикой этих новообразований, а также методикой их удаления [289].
-
Рекомендуется при выборе интервала для выполнения повторной колоноскопии после удаления ДЭНо использовать критерии низкого и высокого риска развития КРР у лиц старше 18 лет [290-293].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 4).
Комментарии: пациентам с низким риском развития КРР: 1-4 аденомы <10 мм с дисплазией низкой степени с/без ворсинчатых компонентов, или с любым зубчатым полипом менее 10 мм без дисплазии) рекомендуется проводить повторную колоноскопию через 3 года [290, 291].
Контрольная колоноскопия через 1-2 года рекомендована пациентам высокого риска КРР: аденомы ≥10 мм при количестве аденом ≥5, зубчатые полипы ≥10мм, а также зубчатые полипы любого размера с дисплазией [291].
В случае если при первой контрольной колоноскопии не обнаружены полипы, требующие наблюдения, повторная колоноскопия выполнятся через 3 года. При выявлении на первой контрольной колоноскопии полипов, соответствующих высокому риску КРР, следующее эндоскопическое исследование проводится через 1-2 года (табл. 3) [292, 293].
Таблица 3 Интервалы между повторными колоноскопиями [290-297]
|
Первичная находка |
Колоноскопия после удаления опухоли через |
Повторная колоноскопия через |
Последующее наблюдение через |
|---|---|---|---|
|
Фрагментарная резекция аденомы |
3-6 месяцев |
1 год |
3 года |
|
Критерии высокого риска КРР |
1-2 года |
3 года |
По критериям риска |
|
Критерии низкого риска КРР |
3 года |
По критериям риска |
По критериям риска |
-
Рекомендуется при выборе сроков выполнения повторной колоноскопии после удаления ДЭНо учитывать способ выполненной полипэктомии [294-297].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Комментарии: В случае фрагментарной резекции полипа размером более 20 мм необходимо провести эндоскопический контроль через 3-6 месяцев, затем провести контрольную колоноскопию через 1 год. Это связано с тем, что фрагментарное удаление ДЭНо сопряжено с существенным риском рецидива опухоли и развития интервального КРР [294-297].
Информация
Источники и литература
-
Клинические рекомендации Ассоциации колопроктологов России
- 1. Schlemper RJ, Riddell RH, Kato Y, et al. The Vienna classification of gastrointestinal epithelial neoplasia. Gut. 2000;47(2):251-255. doi:10.1136/gut.47.2.251. 2. Nagtegaal ID, Odze RD, Klimstra D, et al. The 2019 WHO classification of tumours of the digestive system. Histopathology. 2020;76(2):182-188. doi:10.1111/his.13975. 3. The Paris endoscopic classification of superficial neoplastic lesions: esophagus, stomach, and colon: November 30 to December 1, 2002. Gastrointest Endosc. 2003;58(6 Suppl):S3-S43 . doi:10.1016/s0016-5107(03)02159-x. 4. Lambert R, Kudo SE, Vieth M, et al. Pragmatic classification of superficial neoplastic colorectal lesions. Gastrointest Endosc. 2009;70(6):1182-1199. doi:10.1016/j.gie.2009.09.015. 5. Bosman FT, World Health Organization, International Agency for Research on Cancer. World Health Organization classification of tumours. Lyon: IARC Press; 2010:417. 6. Sninsky JA, Shore BM, Lupu GV, et al. Risk factors for colorectal polyps and cancer. Gastrointest Endosc Clin N Am. 2022;32(2):195-213. doi:10.1016/j.giec.2021.12.008. 7. Peery AF, Crockett SD, Murphy CC, et al. Burden and cost of gastrointestinal, liver, and pancreatic diseases in the United States: Update 2021. Gastroenterology. 2022;162(2):621-644. doi:10.1053/j.gastro.2021.10.017. 8. Corley DA, Jensen CD, Marks AR, et al. Variation of adenoma prevalence by age, sex, race, and colon location in a large population: implications for screening and quality programs. Clin Gastroenterol Hepatol. 2013;11(2):172-180. doi:10.1016/j.cgh.2012.09.021. 9. Durno CA. Colonic polyps in children and adolescents. Can J Gastroenterol. 2007;21(4):233-9. Doi: 10.1155/2007/401674. 10. Soyer T. Polypoid disease of colon in children. Pediatr Surg Int. 2020;36(4):447-455. doi: 10.1007/s00383-020-04621-3. 11. Rex DK, Anderson JC, Butterly LF, et al. Quality indicators for colonoscopy. Gastrointest Endosc. 2024;100(3):352-381. doi:10.1016/j.gie.2024.04.2905. 12. Bray F, Ferlay J, Soerjomataram I, et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries [published correction appears in CA Cancer J Clin. 2020;70(4):313]. CA Cancer J Clin. 2018;68(6):394-424. doi:10.3322/caac.21492. 13. Wee CC, McCarthy EP, Phillips RS. Factors associated with colon cancer screening: the role of patient factors and physician counseling. Prev Med. 2005;41(1):23-29. doi:10.1016/j.ypmed.2004.10.010. 14. Winawer SJ, Zauber AG, Gerdes H, et al. Risk of colorectal cancer in the families of patients with adenomatous polyps. National Polyp Study Workgroup. N Engl J Med. 1996;334(2):82-87. doi:10.1056/NEJM199601113340203. 15. Samadder NJ, Curtin K, Tuohy TM, et al. Increased risk of colorectal neoplasia among family members of patients with colorectal cancer: a population-based study in Utah. Gastroenterology. 2014;147(4):814-821.e16. doi:10.1053/j.gastro.2014.07.006. 16. Abou Khalil M, Boutros M, Nedjar H, et al. Incidence rates and predictors of colectomy for ulcerative colitis in the era of biologics: results from a provincial database. J Gastrointest Surg. 2018;22(1):124-132. doi:10.1007/s11605-017-3530-y. 17. Samadder NJ, Smith KR, Hanson H, et al. Increased risk of colorectal cancer among family members of all ages, regardless of age of index case at diagnosis. Clin Gastroenterol Hepatol. 2015;13(13):2305-2311.e1. doi:10.1016/j.cgh.2015.06.040. 18. Шелыгин Ю.А., Кашников В.Н., Фролов С.А. et al. Молекулярно-генетическое исследование наследственной предрасположенности к разным формам полипоза толстой кишки. Колопроктология. 2013;1(43):9-14. 19. Shen Q, Zhou Y, Liu X, et al. Clinical and Genetic Characteristics of Pediatric Colorectal Cancer. Pediatr Blood Cancer. 2025 Apr;72(4):e31569. doi: 10.1002/pbc.31569. 20. Cairns SR, Scholefield JH, Steele RJ, et al. Guidelines for colorectal cancer screening and surveillance in moderate and high risk groups (update from 2002). Gut. 2010;59(5):666-689. doi:10.1136/gut.2009.179804. 21. Бакулин И.Г., Жарков А.В., Журавлева М.С. и др. Скрининг колоректального рака: состояние проблемы и перспективы. Профилактическая медицина. 2023;26(12):12-18. 22. Максимова П.Е., Голубинская Е.П., Сеферов Б.Д. и др. Колоректальный рак: эпидемиология, канцерогенез, молекулярно-генетические и клеточные механизмы резистентности к терапии (аналитический обзор). Колопроктология. 2023;22(2):160-171. doi:10.33878/2073-7556-2023-22-2-160-171. 23. Li J, Ma X, Chakravarti D, et al. Genetic and biological hallmarks of colorectal cancer. Genes Dev. 2021;35(11-12):787-820. doi:10.1101/gad.348226.120. 24. Dekker E, Tanis PJ, Vleugels JLA, et al. Colorectal cancer. Lancet. 2019;394(10207):1467-1480. doi:10.1016/S0140-6736(19)32319-0. 25. Boutin AT, Liao WT, Wang M, et al. Oncogenic Kras drives invasion and maintains metastases in colorectal cancer. Genes Dev. 2017;31(4):370-382. doi:10.1101/gad.293449.116. 26. Liao W, Overman MJ, Boutin AT, et al. KRAS-IRF2 axis drives immune suppression and immune therapy resistance in colorectal cancer. Cancer Cell. 2019;35(4):559-572.e7. doi:10.1016/j.ccell.2019.02.008. 27. Rashtak S, Rego R, Sweetser SR, et al. Sessile serrated polyps and colon cancer prevention. Cancer Prev Res (Phila). 2017;10(5):270-278. doi:10.1158/1940-6207.CAPR-16-0264. 28. Каприн А.Д., Старинский В.В., Шахзадова А.О. Злокачественные новообразования в России в 2020 году (заболеваемость и смертность). М.: МНИОИ им. П.А. Герцена — филиал ФГБУ «НМИЦ радиологии» Минздрава России; 2021. 29. Siegel RL, Miller KD, Goding Sauer A, et al. Colorectal cancer statistics, 2020. CA Cancer J Clin. 2020;70(3):145-164. doi:10.3322/caac.21601. 30. Clinton SK, Giovannucci EL, Hursting SD. The World Cancer Research Fund/American Institute for Cancer Research Third Expert Report on Diet, Nutrition, Physical Activity, and Cancer: Impact and Future Directions. J Nutr. 2020;150(4):663-671. doi:10.1093/jn/nxz268. 31. Sullivan T, Sullivan R, Ginsburg OM. Screening for cancer: considerations for low- and middle-income countries. In: Gelband H, Jha P, Sankaranarayanan R, et al, eds. Cancer: Disease Control Priorities. 3rd ed. Vol 3. The International Bank for Reconstruction and Development/The World Bank; 2015:211-222. doi:10.1596/978-1-4648-0349-9_ch12. 32. Navarro M, Nicolas A, Ferrandez A, et al. Colorectal cancer population screening programs worldwide in 2016: an update. World J Gastroenterol. 2017;23(20):3632-3642. doi:10.3748/wjg.v23.i20.3632. 33. Edwards BK, Ward E, Kohler BA, et al. Annual report to the nation on the status of cancer, 1975-2006, featuring colorectal cancer trends and impact of interventions (risk factors, screening, and treatment) to reduce future rates. Cancer. 2010;116(3):544-573. doi:10.1002/cncr.24760. 34. Sullivan BA, Noujaim M, Roper J. Cause, epidemiology, and histology of polyps and pathways to colorectal cancer. Gastrointest Endosc Clin N Am. 2022;32(2):177-194. doi:10.1016/j.giec.2021.12.001. 35. Kuntz KM, Lansdorp-Vogelaar I, Rutter CM, et al. A systematic comparison of microsimulation models of colorectal cancer: the role of assumptions about adenoma progression. Med Decis Making. 2011;31(4):530-539. doi:10.1177/0272989X11408730. 36. Arminski TC, McLean DW. Incidence and distribution of adenomatous polyps of the colon and rectum based on 1,000 autopsy examinations. Dis Colon Rectum. 1964;7(3):249-261. doi:10.1007/BF02626694. 37. Jass JR, Young PJ, Robinson EM. Predictors of presence, multiplicity, size and dysplasia of colorectal adenomas. A necropsy study in New Zealand. Gut. 1992;33(11):1508-1514. doi:10.1136/gut.33.11.1508. 38. Johannsen LG, Momsen O, Jacobsen NO. Polyps of the large intestine in Aarhus, Denmark. An autopsy study. Scand J Gastroenterol. 1989;24(7):799-806. doi:10.3109/00365528909089216. 39. Williams AR, Balasooriya BA, Day DW. Polyps and cancer of the large bowel: A necropsy study in Liverpool. Gut. 1982;23(10):835-842. doi:10.1136/gut.23.10.835. 40. Koninckx CR, Donat E, Benninga MA, et al. The use of fecal calprotectin testing in paediatric disorders: a position paper of the European Society for Paediatric Gastroenterology and Nutrition Gastroenterology Committee. J Pediatr Gastroenterol Nutr. 2021;72:617–640. doi: 10.1097/MPG.0000000000003046. 41. Thakkar K, Fishman DS, Gilger MA. Colorectal polyps in childhood. Curr Opin Pediatr. 2012;24:632–637. doi: 10.1097/MOP.0b013e328357419f. 42. Zauber AG, Winawer SJ, O’Brien MJ, et al. Colonoscopic polypectomy and long-term prevention of colorectal-cancer deaths. N Engl J Med. 2012;366(8):687-696. doi:10.1056/NEJMoa1100370. 43. Lieberman DA, Weiss DG, Bond JH, et al. Use of colonoscopy to screen asymptomatic adults for colorectal cancer. N Engl J Med. 2000;343(3):162-168. doi:10.1056/NEJM200007203430301. 44. Nishihara R, Wu K, Lochhead P, et al. Long-term colorectal-cancer incidence and mortality after lower endoscopy. N Engl J Med. 2013;369(12):1095-1105. doi:10.1056/NEJMoa1301969. 45. Heitman SJ, Ronksley PE, Hilsden RJ, et al. Prevalence of adenomas and colorectal cancer in average risk individuals: A systematic review and meta-analysis. Clin Gastroenterol Hepatol. 2009;7(12):1272-1278. doi:10.1016/j.cgh.2009.05.032. 46. Imperiale TF, Ransohoff DF, Itzkowitz SH, et al. Multitarget stool DNA testing for colorectal-cancer screening. N Engl J Med. 2014;370(14):1287-1297. doi:10.1056/NEJMoa1311194. 47. Kaminski MF, Wieszczy P, Rupinski M, et al. Increased rate of adenoma detection associates with reduced risk of colorectal cancer and death. Gastroenterology. 2017;153(1):98-105. doi:10.1053/j.gastro.2017.04.006. 48. Wong MCS, Huang J, Huang JLW, et al. Global prevalence of colorectal neoplasia: A systematic review and meta-analysis. Clin Gastroenterol Hepatol. 2020;18(3):553-561.e10. doi:10.1016/j.cgh.2019.07.015/ 49. Corley DA, Jensen CD, Marks AR, et al. Variation of adenoma prevalence by age, sex, race, and colon location in a large population: implications for screening and quality programs. Clin Gastroenterol Hepatol. 2013;11(2):172-180. doi:10.1016/j.cgh.2012.09.021. 50. Huck MB, Bohl JL. Colonic polyps: diagnosis and surveillance. Clin Colon Rectal Surg. 2016;29(4):296-305. doi:10.1055/s-0036-1584091.
Информация
Список сокращений
БДУ – без дополнительных уточнений (англ. NOS – not otherwise specified)
ВЗК – воспалительные заболевания кишечника (англ. IBD – inflammatory bowel disease)
ТЭВ – толстокишечная эндоскопия видеокапсульная
ВКС – видеоколоноскопия
ГБ – горячая биопсия (англ. – hot biopsy)
ГП – горячая полипэктомия (англ. – hot polypectomy)
ДЭНо – доброкачественное эпителиальное новообразование
ЖКТ – желудочно-кишечный тракт
КРР – колоректальный рак
КТ – компьютерная томография
МРТ – магнитно-резонансная томография
КР – клинические рекомендации
ОиПК – ободочная и прямая кишка
ПЭНо – поверхностное эпителиальное новообразование (англ.– superficial epithelial lesion)
ПЭТ – позитронно-эмиссионная томография
РКИ – рандомизированное клиническое исследование
РР – ранний рак
РРС – ректороманоскопия
АПС – аденоматозный полипозный синдром
УДД – уровень достоверности доказательств
УЗИ – ультразвуковое исследование
УУР – уровень убедительности рекомендаций
ХБ – холодная биопсия (англ. – cold biopsy)
ХП – холодная полипэктомия (англ. – cold polypectomy)
ЧВА – частота выявления аденом (англ. ADR – adenoma detection rate)
ЭДПС – эндоскопическая диссекция подслизистого слоя (англ. ESD – endoscopic submucosal dissection)
ЭРСО – эндоскопическая резекция слизистой оболочки (англ. EMR – endoscopic mucosal resection)
ASA (American Society of Anesthesiologists) – американское общество анестезиологов
** – жизненно необходимые и важнейшие лекарственные препараты
# – препарат, применяющийся вне показаний (офф-лейбл)
Термины и определения
Биопсия холодная щипцовая/петлевая – механическое (без использования электрического тока) удаление фрагмента биологической ткани биопсийными щипцами или полипэктомической петлей.
Биопсия горячая щипцовая/петлевая – удаление фрагмента биологической ткани биопсийными щипцами или полипэктомической петлей с использованием электрического тока.
Новообразование (синонимы: неоплазия; опухоль) – клон клеток, отличающихся от других тканей автономным ростом и соматическими мутациями [1].
Неоплазия интраэпителиальная – разновидность неинвазивной эпителиальной опухоли, термин, которым в согласованной Венской классификации эпителиальных неоплазий пищеварительного тракта заменены и определены термины аденома и дисплазия [2].
Полип (в широком смысле) – собирательный термин, прочно вошедший в повседневную профессиональную речь, как короткий, удобный для использования в практической работе термин, под которым понимается практически любое внутрипросветное новообразование. Собирательный термин «полип», преимущественно, используется для обозначения доброкачественных эпителиальных новообразований, но его используют и для обозначения образований иного происхождения (воспалительных, гамартомных, субэпителиальных/подслизистых), главным образом в ситуациях, когда истинная природа и происхождение образования до поры до времени непонятны/неизвестны. Этот дуализм определения нашел отражение и в кодировании заболевания по Международной статистической классификации болезней. В частности, в МКБ-10 оно кодируется и в классе II – «Новообразования» и в классе XI – «Болезни органов пищеварения». Поcле того, как на семинаре в Париже в 2002г. в отдельную категорию выделили неполиповидные – плоские (0-II типа) и изъязвленные (0-III типа) поверхностные эпителиальные новообразования стало очевидно, что целесообразно различать термин «полип» в его широком (описанном выше) и в узком значении.
Полип (в узком смысле), как синоним возвышающегося над поверхностью кишечной стенки ПЭНо (0-I типа) – термин, обозначающий эпителиальное новообразование, у которого высота превышает половину диаметра (критерий для миниатюрных образований), либо выступающее в просвет органа более чем на 2,5 миллиметра (диаметр чашек закрытых биопсийных щипцов), связанное со стенкой кишки ножкой или широким основанием.
Полип малигнизированный – полиповидное эпителиальное новообразование, с доказанным наличием раковых клеток в структуре. В отличие от термина «полиповидная форма рака» термин «малигнизированный полип» подчеркивает уверенность специалиста в том, что он имеет дело со злокачественной опухолью, предшественником которой был доброкачественный полип, часть которого, по-прежнему, сохраняет доброкачественное строение.
Ранний рак – раковая опухоль, ограниченная слизистой оболочкой или подслизистым слоем, вне зависимости от наличия или отсутствия метастазов в регионарных лимфатических узлах.
Субэпителиальное образование – собирательный термин, главным образом эндоскопический, характеризующий как опухолевое, так и неопухолевое очаговое объемное поражение толстой кишки, исходящее из любого слоя стенки органа, кроме эпителия. Термином «субэпителиальное образование/опухоль» постепенно замещается термин «подслизистое образование/опухоль», более точно отражая морфологию поражений, так как некоторые из них, например, исходящие из мышечной пластинки слизистой оболочки лейомиомы или нейроэндокринные опухоли, исходящие из глубоких отделов желез слизистой оболочки, строго говоря являются внутрислизистыми, хотя и выглядят при эндоскопичесом осмотре как «подслизистые».
Полипэктомия холодная – механическое (без использования электрического тока) удаление эпителиального новообразования полиэктомической петлей или биопсийными щипцами.
Полипэктомия горячая – удаление эпителиального новообразования полипэктомической петлей или биопсийными щипцами с использованием электрического тока.
Эндоскопическая диссекция подслизистого слоя (англ. ESD – endoscopic submucosal dissection) – разновидность внутрипросветной эндоскопической резекции новообразования, при которой процесс рассечения (диссекции) слизистой оболочки и подслизистого слоя выполняется через эндоскоп специально сконструированными электрохирургическими эндоножами под непосредственным контролем зрения.
Эндоскопическая резекция слизистой оболочки (англ. EMR – endoscopic mucosal resection) – термин, которым обозначают иссечение через эндоскоп (как правило полипэктомической петлей) в пределах неизмененных тканей фрагмента слизистой оболочки с расположенным в этом фрагменте новообразованием. Термин, в его классическом варианте, используют для обозначения удаления через эндоскоп неполиповидных ПЭНо с предварительным введением жидких субстанций в подслизистый слой.
Эпителиальное новообразование – доброкачественное или злокачественное новообразование, исходящее из эпителия слизистой оболочки органа.
Поверхностное эпителиальное новообразование (ПЭНо) – Эпителиальное новообразование глубина распространения, которого ограничена пределами слизистой, либо подслизистой оболочки, то есть двумя внутренними, поверхностными по отношению к просвету ЖКТ слоями.
Полиповидное (возвышающееся) ПЭНо (0-I тип) – эпителиальное новообразование, высота которого превышает половину его диаметра (критерий для миниатюрных образований), либо выступающее в просвет органа более чем на 2,5 миллиметра (диаметр чашек закрытых биопсийных щипцов), связанное со стенкой кишки ножкой или широким основанием.
Неполиповидное ПЭНо – эпителиальное новообразование, у которого высота не превышает половины его диаметра, либо не выступающее в просвет органа более чем на 2,5 миллиметра (диаметр чашек закрытых биопсийных щипцов). К ним относятся плоские (0-II тип) и изъязвленные (0-III тип) неоплазии.
Критерии оценки качества медицинской помощи

Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций


Преимущественно разработчики являются членами Ассоциация колопроктологов России и Российского эндоскопического общества.
Конфликт интересов: отсутствует у всех членов рабочей группы.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
-
Врачи – эндоскописты
-
Врачи – гастроэнтерологи
-
Врачи – хирурги
-
Врачи – детские хирурги
-
Врачи – онкологи
-
Врачи – колопроктологи
-
Врачи – патологоанатомы
-
Врачи – анестезиологи
Методы, использованные для сбора/селекции доказательств: поиск в электронных базах данных; анализ современных научных разработок по эпителиальным новообразованиям толстой кишки в РФ и за рубежом; обобщение практического опыта российских и зарубежных специалистов.
Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД |
Расшифровка |
|---|---|
|
1. |
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2. |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3. |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4. |
Несравнительные исследования, описание клинического случая |
|
5. |
Имеется лишь обоснование механизма действия или мнение экспертов |
Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
УДД |
Расшифровка |
|---|---|
|
1. |
Систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2. |
Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3. |
Нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4. |
Несравнительные исследования, описание клинического случая или серии случаев, исследование "случай-контроль" |
|
5. |
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР |
Расшифровка |
|---|---|
|
A |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
|
B |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
|
C |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учетом следующих нормативно-правовых документов:
-
Приказ Министерства здравоохранения Российской федерации от 15 ноября 2012 № 9222н «Об утверждении Порядка оказания медицинской помощи взрослому населению по профилю «хирургия»;
-
Приказ Министерства здравоохранения и социального развития РФ от 2 апреля 2010 г. № 206н "Об утверждении Порядка оказания медицинской помощи населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля" (с изменениями и дополнениями);
-
Приказ Минздрава России от 06.12.2017 № 974 «Об утверждении Правил проведения эндоскопических исследований»;
-
Приказ Министерства здравоохранения Российской Федерации от 24 марта 2016 г. № 179н "О Правилах проведения патолого-анатомических исследований";
-
Приказ Минздрава России от 20.12.2012 № 1177н (ред. от 17.07.2019) "Об утверждении порядка дачи информированного добровольного согласия на медицинское вмешательство и отказа от медицинского вмешательства в отношении определенных видов медицинских вмешательств, форм информированного добровольного согласия на медицинское вмешательство и форм отказа от медицинского вмешательства";
-
Приказ Минздрава России от 27.04.2021 № 404н (ред. от 01.02.2022) «Об утверждении Порядка проведения профилактического медицинского осмотра и диспансеризации определенных групп взрослого населения»);
-
Приказ Министерства здравоохранения РФ от 15 ноября 2012 г. № 928н "Об утверждении Порядка оказания медицинской помощи больным с острыми нарушениями мозгового кровообращения").
Приложение Б. Алгоритмы действий врача
Приложение Б1. Алгоритм действий врача-эндоскописта

Приложение Б2. Алгоритм действий врача-эндоскописта при выявлении эпителиальных латерально распространяющихся новообразований толстой кишки
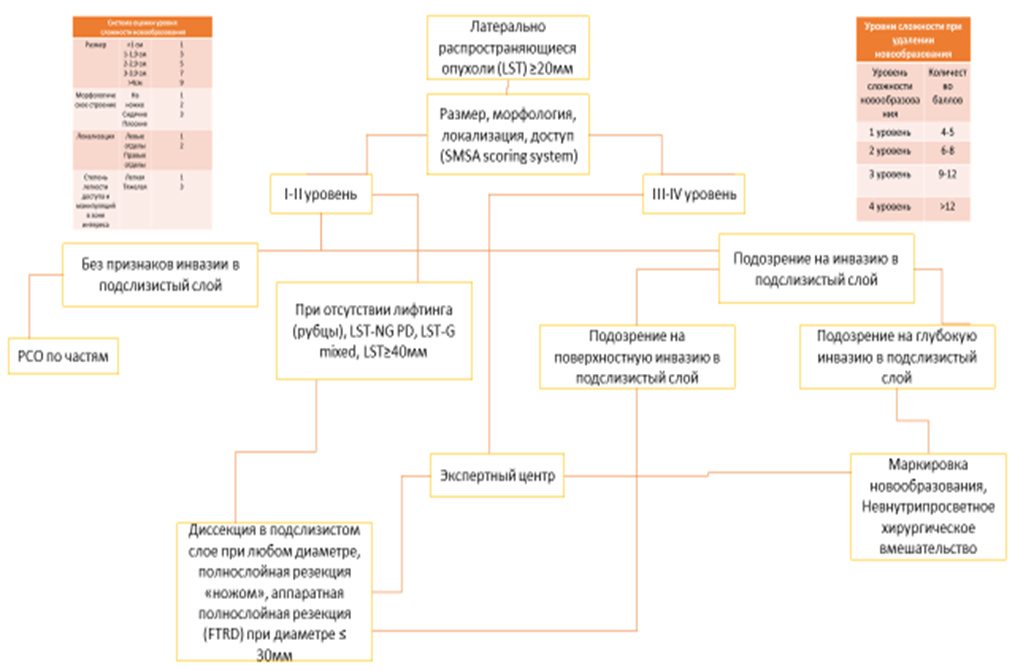
Приложение Б3. Алгоритм действий врача-эндоскописта при выявлении эпителиальных новообразований толстой кишки зубчатого вида
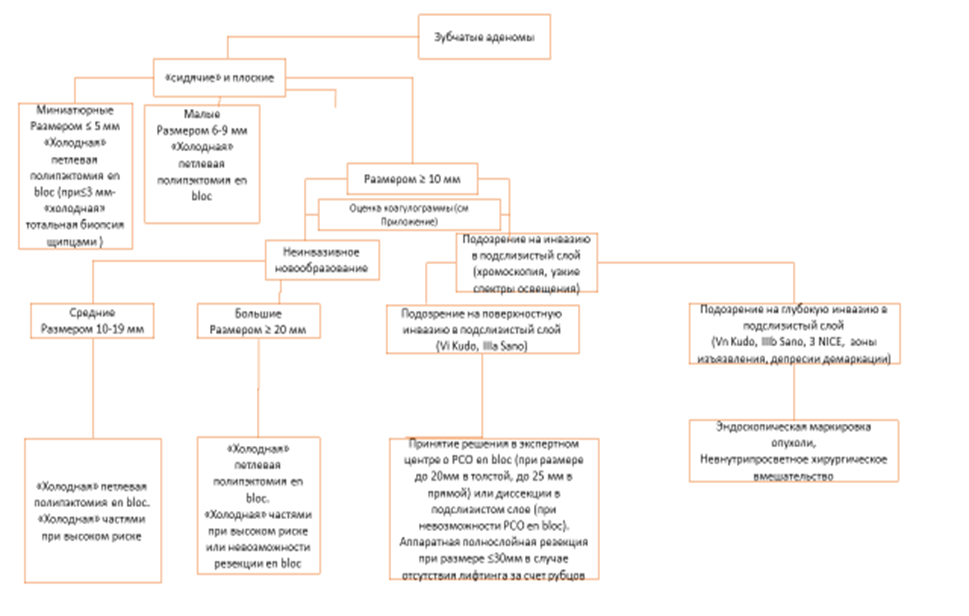
Приложение Б4. Тактика ведения пациентов при отсроченном кровотечении
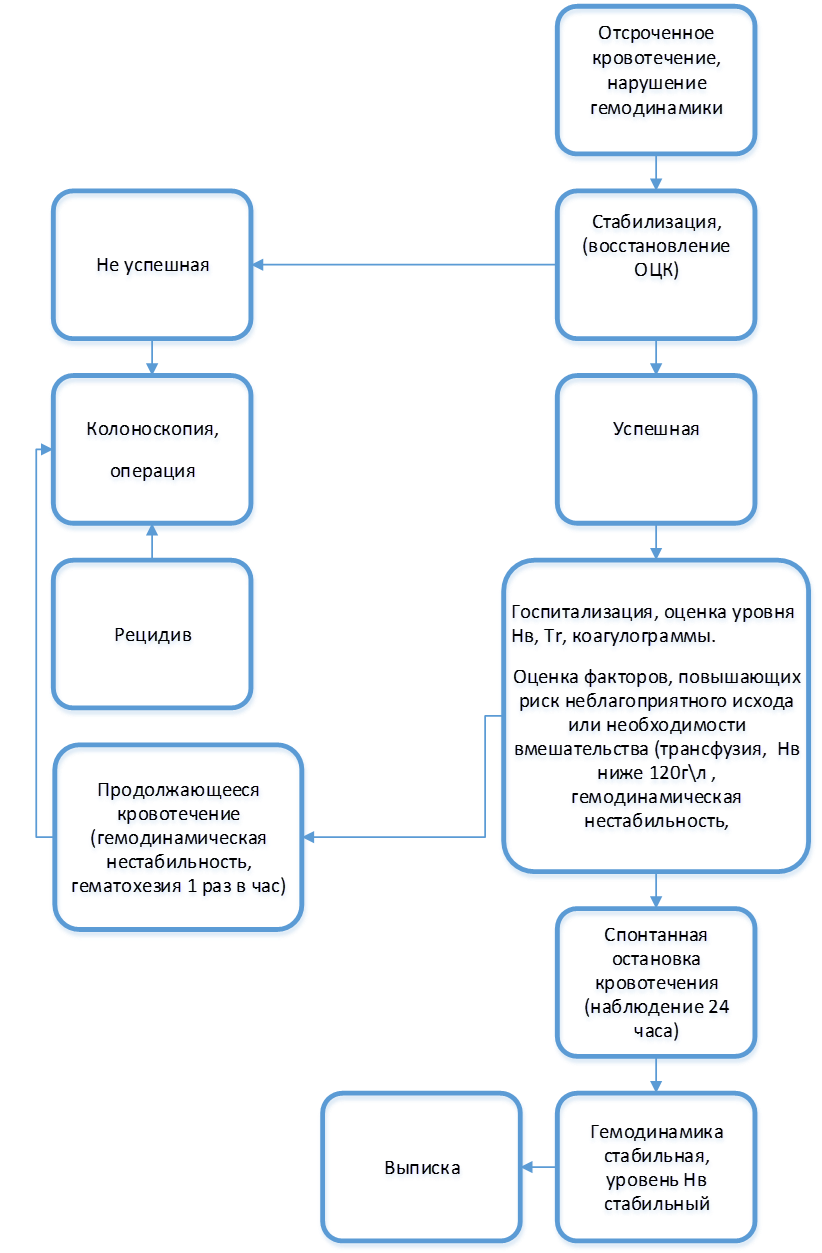
Приложение В. Информация для пациента
Что такое полипы толстой кишки?
Клетки слизистой оболочки кишечника регулярно обновляются, полная смена клеток внутреннего слоя происходит каждые 3-4 дня. Если этот процесс нарушается, на поверхности слизистой оболочки образуются локальные выросты - полипы.
Полип толстой кишки - доброкачественная опухоль, но к нему обращено пристальное внимание врачей-онкологов.
Классификация
Наиболее распространенная группа - аденоматозные полипы, т.н. аденомы. Причиной их возникновения является мутация гена APC. В результате мутации клетки начинают делиться быстрее и образуются излишние скопления клеток, появляются полипы. Важно отметить, что одной мутации APC-гена недостаточно, для злокачественного перерождения аденомы в рак, необходимо сочетание этой мутации с другими, в первую очередь гена р53, или KRas. Однако, риск возникновения рака при образовании полипов и APC-мутации возрастает.
В редких случаях люди уже рождаются с APC-мутацией всех клеток, в результате у них развивается заболевание – диффузный полипоз толстой кишки. При этом в кишечнике образуются сотни, или даже тысячи полипов. Такое состояние требует хирургического удаления толстой кишки, т.к. при появлении сопутствующих мутаций высок риск развития рака.
Аденомы классифицируются по гистологическому типу как: тубулярные и ворсинчатые, а также смешанные тубулярно-ворсинчатые.
Это заключение важно, так как ворсинчатый тип имеет большую склонность к злокачественному перерождению и требует более тщательного наблюдения, если полип не удалялся.
Другая классификация основывается на внешних особенностях и учитывает в первую очередь есть ли у полипа ножка, которая связывает его со стенкой кишки (по виду напоминает гриб). Или же для него характерна «сидячая», распластанная форма, что означает, что он прочно связан со стенкой. Здесь также есть различия, такие «сидячие» полипы чаще становятся злокачественными.
Другую группу полипов кишечника составляют зубчатые полипы, или зубчатые аденомы. Эта группа приобретает значение в последние годы. Название они получили, из-за характерного вида клеток под микроскопом. Внутри их ДНК образуются «CpG-островки», которые, не являясь собственно мутацией, способствуют злокачественной трансформации клетки при возможном влиянии ряда других мутагенных факторов. Зубчатые полипы бывают двух видов: мелкие – морфологически определяемые как гиперпластические и более крупные, распластанные формы, имеющие больший риск злокачественного перерождения.
Третья группа - это воспалительные полипы, которые часто сопровождают воспалительные заболевания кишечника (язвенный колит и болезнь Крона). Эти полипы являются видоизмененными рубцами и не несут в себе онкологического риска.
Последняя, четвертая группа – гамартомные полипы, клетки которых имеют искаженную структуру, как бы смешанных тканей. Данный тип полипов сочетается с наследственными синдромами и заболеваниями (ювенильный полипоз, синдром Пейца-Егерса и др.).
Факторы риска
Факторы риска развития полипов включают в себя все, что способствует мутациям в интенсивно делящихся клетках внутренней поверхности толстой кишки. Это в первую очередь наследственная предрасположенность (наличие полипов или рака толстой кишки у ближайших родственников). Пожилой возраст, после 50 лет риски появления полипов и рака толстой кишки возрастают.
Третья группа неблагоприятные факторы среды: курение, переедание, малоподвижный образ жизни, промышленная вредность, нервное перенапряжение и т.д. также часто сочетаются с полипами.
Отдельную группу образуют пациенты, длительно болеющие воспалительными заболеваниями кишечника, обнаружение у такого пациента аденомы, бывает тревожным сигналом и требует тщательного, регулярного наблюдения.
Клинические проявления
В большинстве случаев полипы не имеют симптомов и являются случайной находкой во время скрининговой колоноскопии.
Однако в ряде случаев крупный полип кровоточит, что проявляется кровотечениями из прямой кишки, или даже приводит к анемии.
Случаи кишечной непроходимости при доброкачественных полипах крайне редки.
Лечение
Удаляются полипы, как правило, через колоноскоп при помощи специальной петли, такая манипуляция называется полипэктомией.
Крупные полипы могут потребовать хирургической резекции целого сегмента толстой кишки, что проводится в операционной с разрезом стенки живота.
В настоящее время большее распространение получает метод удаления полипов «глубокой» диссекцией. При котором полип через колоноскоп удаляется вместе с прилегающей кишечной стенкой. Этот метод позволяет удалять крупные полипы малоинвазивно.
Удаленный полип подвергается осмотру под микроскопом, для окончательного точного определения типа и достоверного исключения очагов злокачественной трансформации.
Профилактика
После полипэктомии пациенты периодически проходят контрольные колоноскопии. Частота таких исследований зависит от размеров и типа удаленного полипа. При отсутствии новых полипов колоноскопию можно делать реже.
Для раннего выявления полипов рекомендуется после 50 лет сделать колоноскопию.
На предупреждение роста полипов влияет состав и нормы питания. Исследования показали, что употребление в пищу овощей (картофель, салат, капуста, бобовые), благодаря содержанию в них пищевых волокон, предотвращают развитие полипов и рака толстой кишки. Специалисты также советуют употреблять в пищу меньшее количество жиров, есть больше рыбы и "белого" мяса (например, птицы).
Отказ от курения, уменьшение употребления алкоголя, достижение нормального веса и повышение физической активности, также снижают риск роста полипов.
Заключение:
− Полип толстой кишки – это доброкачественная опухоль, но она может переродиться в рак.
− Наибольшую опасность, с точки зрения злокачественного перерождения, представляют аденомы и зубчатые полипы.
− Риск наличия полипов возрастает при обнаружении полипов у родственников и возрасте старше 50 лет.
− Обычно полипы выявляются и удаляются в процессе колоноскопии.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Бостонская шкала оценки качества подготовки кишечника
Название на русском языке: Бостонская шкала оценки качества подготовки кишечника.
Оригинальное название: The Boston Bowel Preparation Scale (BBPS).
Источник (официальный сайт разработчиков, публикация с валидацией): https://www.giejournal.org/article/S0016-5107(08)01988-3/abstract
Оригинальная публикация: Lai EJ, Calderwood AH, Doros G, Fix OK, Jacobson BC. The Boston bowel preparation scale: a valid and reliable instrument for colonoscopy-oriented research. Gastrointest Endosc. 2009 Mar;69(3 Pt 2):620-5. doi: 10.1016/j.gie.2008.05.057. Epub 2009 Jan 10. PMID: 19136102; PMCID: PMC2763922 [326].
Тип: шкала оценки.
Назначение: описать степень качества подготовки кишечника пациента к колоноскопии для повышения точности и надежности результатов колоноскопии.
Содержание (шаблон):
|
Балл |
Описание |
|---|---|
|
3 |
Вся слизистая оболочка оцениваемого сегмента толстой кишки хорошо видна на всем протяжении, отсутствуют даже незначительные остатки кишечного содержимого и непрозрачной/окрашенной жидкости |
|
2 |
Имеется небольшое количество окрашенного содержимого – остатков кишечного содержимого и/или непрозрачной жидкости, но в целом слизистая оболочка оцениваемого сегмента толстой кишки хорошо видна |
|
1 |
Видна только часть слизистой оболочки оцениваемого сегмента толстой кишки, но другие участки слизистой оболочки этого сегмента кишки малодоступны осмотру из-за наличия окрашенного содержимого – остаточного кишечного содержимого и/или непрозрачной жидкости |
|
0 |
Оцениваемый сегмент кишки не подготовлен к исследованию. Слизистая оболочка недоступна осмотру, так как ее невозможно отмыть от твердых/плотных каловых масс |
Ключ (интерпретация): приведен в самой шкале.
*В соответствии с авторскими условиями использования Бостонской шкалы, оценка подготовленности толстой кишки к эндоскопическому осмотру проводится после того, как эндоскопист провел отмывание и аспирацию содержимого!
Балльная оценка (от 0 до 3) используется для оценки качества подготовленности к эндоскопическому осмотру каждого из 3-х сегментов толстой кишки. Оценивается: правый сегмент толстой кишки; поперечный сегмент и левый сегмент толстой кишки. Каждому из оцениваемых сегментов толстой кишки выставляется балльная оценка в диапазоне от 0 до 3, при этом оценка в 2 и в 3 балла позволяет считать оцениваемый отдел кишки адекватно подготовленным для проведения эндоскопического осмотра; соответственно оценка в 0 и 1 балл – неадекватно подготовленным, не готовым для полноценного осмотра. После оценки каждого сегмента общая оценка подготовки кишки складывается из суммы баллов всех трех сегментов, таким образом, получается общий балл в пределах от 0 до 9. Суммарная максимальная оценка качества подготовленности толстой кишки к эндоскопическому осмотру составляет 9 баллов (идеальная подготовка), а минимальная оценка (ни один из сегментов кишки не подготовлен к осмотру) – 0 баллов.
Диапазон адекватной подготовленности толстой кишки к эндоскопическому осмотру составляет 6 – 9 баллов, при очень важном условии (!): качество подготовленности каждого из оцениваемых сегментов толстой кишки должно составлять не менее 2-х баллов.
Приложение Г2. Классификация «AGREE» нежелательных последствий/осложнений в эндоскопии пищеварительного тракта
| Нежелательные последствия отсутствуют |
v Телефонный контакт с врачом общей практики, с поликлиникой или с отделением эндоскопии без каких-либо дальнейших диагностических или лечебных мероприятий или
v Продленное (не более 3 часов) наблюдение за пациентом после вмешательства, без каких-либо диагностических или лечебных мероприятий
|
|
Категория I |
v Любое отклонение от стандартного «послеоперационного» периода, которое не требует специальной медикаментозной терапии, либо эндоскопического, радиологического или хирургического вмешательства v Неотложное поступление в приемный покой без каких-либо интервенционных вмешательств или v Госпитализация на срок до 24 часов без каких-либо интервенционных вмешательств или v Допустимое лечение – назначение медикаментов, таких как противорвотные препараты, жаропонижающие (АТХ-группа: N02BE - анилиды), анальгетики, электролиты (АТХ-группа: B05BB01- растворы, влияющие на водно-электролитный баланс) или v Допустимые диагностические исследования: лабораторные и лучевые |
|
Категория II |
v Требуется медикаментозное лечение препаратами (например, Антибактериальными препаратами системного действия, антитромботическими средствами и т.д.), не упомянутыми в категории I или v Требуется переливание крови или ее компонентов или v Госпитализация на срок более 24 часов |
|
Категория III IIIа IIIb |
Требуется эндоскопическое, радиологическое или хирургическое вмешательство Эндоскопическое или радиологическое вмешательство Хирургическое вмешательство |
|
Категория IV IVа IVb |
Требуется госпитализация в отделение реанимации/интенсивной терапии Недостаточность одного органа (включая диализ) Полиорганная недостаточность |
|
Категория V |
Смерть пациента |
Классификация AGREE – адаптированный для эндоскопии вариант классификации осложнений в хирургии Clavien-Dindo. По мнению 57 экспертов-эндоскопистов всего мира, принимавших участие в ее валидации, классификация AGREE проста – 86%, воспроизводима – 98%, логична – 98%, полезна – 96%. Верная категория осложнения была присвоена 84% всех тестовых клинических случаев. Осложнения определяются как все негативные последствия для пациента, которые препятствуют завершению запланированного вмешательства или вызывают любое отклонение от стандартного послеоперационного периода (в течение 30 дней!). Незапланированные события и явления во время вмешательства, которые не повлияли на стандартный послеоперационный период, не считаются осложнениями.
Приложение Г3. Шкала оценки физического состояния пациента перед операцией
ASA (American Society of Anaesthesiologists)
Название на русском языке: Шкала оценки физического состояния пациента перед операцией Американского общества анестезиологов
Оригинальное название: ASA Physical Status Classification System
Источник (официальный сайт разработчиков, публикация с валидацией): https://ekja.org/journal/view.php?doi=10.4097/kja.d.18.00224
Оригинальная публикация: De Cassai A, Boscolo A, Tonetti T, Ban I, Ori C. Assignment of ASA-physical status relates to anesthesiologists' experience: a survey-based national-study. Korean J Anesthesiol. 2019 Feb;72(1):53-59 [327].
Тип: шкала
Назначение: оценка физического состояния пациента перед операцией
Содержание (шаблон): для определения состояния пациента врач анестезиолог-реаниматолог использует следующие данные пациента: жалобы, анамнез, данные физикального обследования, результаты лабораторно-диагностических исследований, результаты инструментальных исследований.
Ключ (интерпретация): В зависимости от данных, полученных при сборе анамнеза и обследовании пациента, его относят к той или иной группе:
I – нормальный здоровый пациент (некурящий, не принимающий алкоголь на регулярной основе).
II – пациент с легкими системными заболеваниями средней тяжести течения (курильщик, алкоголик, беременная, ожирение с индексом массы тела от 30 до 40, артериальная гипертензия, компенсированный сахарный диабет, нетяжелые заболевания легких).
III – пациент с тяжелыми системными заболеваниями, ограничивающими функции. Одно или несколько средней степени тяжести (декомпенсированный или неконтролируемый сахарный диабет, терминальная хроническая почечная недостаточность, при этом пациент регулярно проходит процедуры гемодиализа, установлен электрокардиостимулятор, инфаркт миокарда более 3 месяцев назад, хроническая обструктивная болезнь легких, некомпенсированная артериальная гипертензия, ожирение с индексом массы тела > 40).
IV – пациент с выраженным заболеванием, которое представляет угрозу жизни на постоянной основе (инсульт и инфаркт миокарда < 3 месяцев назад, тяжелые поражения клапанного аппарата сердца, сепсис, синдром диссеминированного внутрисосудистого свертывания, тяжелые снижения фракции выброса левого желудочка, терминальная хроническая почечная недостаточность, при этом пациент проходит процедуры гемодиализа нерегулярно).
V – умирающий больной, который не выживет без операции (разрыв аорты, внутричерепное кровотечение с дислокацией, массивная травма, полиорганная недостаточность, ишемия кишечника в сочетании с тяжелой кардиальной патологией).
VI – зафиксирована смерть мозга, органы пациента взяты для последующей трансплантации.
Е – Экстренное вмешательство.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.