Острый коронарный синдром и инфаркт миокарда: протокол диагностики и лечения
 Версия: Клинические протоколы 2024 (Узбекистан)
Версия: Клинические протоколы 2024 (Узбекистан)
Некоторые текущие осложнения острого инфаркта миокарда (I23), Острый инфаркт миокарда (I21), Повторный инфаркт миокарда (I22)
Кардиология
Общая информация
Краткое описание
Приложение 1
к приказу № 290
от «9» сентября 2024 года
Министерства здравоохранения Республики Узбекистан
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ УЗБЕКИСТАН
РЕСПУБЛИКАНСКИЙ СПЕЦИАЛИЗИРОВАННЫЙ НАУЧНО-ПРАКТИЧЕСКИЙ МЕДИЦИНСКИЙ ЦЕНТР КАРДИОЛОГИИ
НАЦИОНАЛЬНЫЕ КЛИНИЧЕСКИЕ ПРОТОКОЛЫ ПО НОЗОЛОГИИ «ОСТРЫЙ КОРОНАРНЫЙ СИНДРОМ И ИНФАРКТ МИОКАРДА»
НАЦИОНАЛЬНЫЕ КЛИНИЧЕСКИЕ ПРОТОКОЛЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ ПО НОЗОЛОГИИ «ОСТРЫЙ КОРОНАРНЫЙ СИНДРОМ И ИНФАРКТ МИОКАРДА»
Вводная часть
Код(ы) МКБ-10:
|
Код
|
Название
|
|
I21
|
Острый инфаркт миокарда. Включено: инфаркт миокарда, уточненный как острый или установленной продолжительностью 4 недели (28 дней) или менее после возникновения острого начала
|
|
I21.0
|
Острый трансмуральный инфаркт передней стенки миокарда
|
|
I21.1
|
Острый трансмуральный инфаркт нижней стенки миокарда
|
|
I21.2
|
Острый трансмуральный инфаркт миокарда других уточненных локализаций
|
|
I21.3
|
Острый трансмуральный инфаркт миокарда неуточненной локализации
|
|
I21.4
|
Острый субэндокардиальный инфаркт миокарда
|
|
I21.9
|
Острый инфаркт миокарда неуточненный
|
|
I22
|
Повторный инфаркт миокарда
|
|
I22.0
|
Повторный инфаркт передней стенки миокарда
|
|
I22.1
|
Повторный инфаркт нижней стенки миокарда
|
|
I22.8
|
Повторный инфаркт миокарда другой уточненной локализации
|
|
I22.9
|
Повторный инфаркт миокарда неуточненной локализации
|
|
I23
|
Некоторые текущие осложнения острого инфаркта миокарда
|
|
I23.0
|
Гемоперикард как ближайшее осложнение острого инфаркта миокарда
|
|
I23.1
|
Дефект межпредсердной перегородки как текущее осложнение острого инфаркта миокарда
|
|
I23.2
|
Дефект межжелудочковой перегородки как текущее осложнение острого инфаркта миокарда
|
|
I23.3
|
Разрыв сердечной стенки без гемоперикарда как текущее осложнение острого инфаркта миокарда. Исключено: с гемоперикардом (I23.0)
|
|
I23.4
|
Разрыв сухожильной хорды как текущее осложнение острого инфаркта миокарда
|
|
I23.5
|
Разрыв сосочковой мышцы как текущее осложнение острого инфаркта миокарда
|
|
I23.6
|
Тромбоз предсердия, ушка предсердия и желудочка сердца как текущее осложнение острого инфаркта миокарда
|
|
I23.8
|
Другие текущие осложнения острого инфаркта миокарда
|
Код (ы) МКБ-11:
|
BA41
|
Острый инфаркт миокарда
|
|
BA41.0
|
Острый инфаркт миокарда с подъёмом ST
|
|
BA41.1
|
Острый инфаркт миокарда, без подъёма ST
|
|
BA41.Z
|
Острый инфаркт миокарда неуточненный
|
|
BA42
|
Последующий инфаркт миокарда
|
|
BA42.0
|
Последующий инфаркт миокарда, STEMI
|
|
BA42.1
|
Последующий инфаркт миокарда, NSTEMI
|
|
BA42.Z
|
Последующий инфаркт миокарда неуточненный
|
|
BA43
|
Коронарный тромбоз, не приводящий к инфаркту миокарда
|
|
BA4Z
|
Острая ишемическая болезнь сердца, неуказанная
|
|
BA50
|
Старый инфаркт миокарда
|
|
BA51
|
Ишемическая кардиомиопатия
|
|
BA5Z
|
Хроническая ишемическая болезнь сердца, неуточненная
|
|
BA60
|
Некоторые текущие осложнения после острого инфаркта миокарда
|
|
BA60.0
|
Синдром Дресслера
|
|
BA60.1.
|
Другой перикардит как текущее осложнение после острого инфаркта миокарда
|
|
BA60.2
|
Желудочковая аневризма как текущее осложнение после острого инфаркта миокарда
|
|
BA60.3
|
Дефект межжелудочковой перегородки как осложнение после острого инфаркта миокарда
|
|
BA60.4
|
Нарушение сердечной деятельности как текущее осложнение после острого инфаркта миокарда
|
|
BA60.5
|
Легочная эмболия как текущее осложнение после острого инфаркта миокарда
|
|
BA60.6
|
Разрыв папиллярной мышцы или хордовых тензиней как осложнение после острого инфаркта миокарда
|
|
BA60.7
|
Фрагмент тромба в виде современного осложнения после острого инфаркта миокарда
|
|
BA60.8
|
Аритмия как текущее осложнение после острого инфаркта миокарда
|
|
BA60.9
|
Кардиогенный шок, не связанный с механическими осложнениями, как текущее осложнение после острого инфаркта миокарда
|
|
BA60.Y
|
Другие уточненные текущие осложнения после острого инфаркта миокарда
|
|
BA60.Z
|
Некоторые современные осложнения после острого инфаркта миокарда неуточненные
|
Дата разработки и пересмотра протокола: 2023 год, дата пересмотра 2026 г. или по мере появления новых ключевых доказательств. Все поправки к представленным рекомендациям будут опубликованы в соответствующих документах.
Ответственное учреждение по разработке данного клинического протокола и стандарта: Республиканский специализированный научно-практический медицинский центр кардиологии (РСНПМЦК)
Пользователи протокола по данной нозологии:
кардиологи, реаниматологи, интервенционные кардиологи/рентгенхирурги, кардиохирурги, терапевты, врачи и фельдшеры скорой медицинской помощи, врачи общей практики и других специальностей. В процессе принятия клинических решений следует учитывать индивидуальные особенности и, в отдельных случаях, предпочтения пациента, а также надлежащие правила по использованию лекарственных средств и медицинского оборудования.
Категория пациентов в данной нозологии: взрослые
Основная часть.
Введение
Сердечно-сосудистые заболевания (ССЗ) остаются одной из ведущих причин смертности и выхода на инвалидность в трудоспособном возрасте. Ежегодно от ССЗ умирает 16,7 млн. человек, из них 7,4 млн. – от ишемической болезни сердца (ИБС) [4]. Клиническое обострение ИБС принято называть острым коронарным синдромом (ОКС) [1,2].
Острый коронарный синдром — временный «рабочий» диагноз, который необходим для первичной оценки, стратификации риска, выбора тактики лечения у больных с обострением ИБС. После непродолжительного периода наблюдения и диагностики, обычно не превышающего суток, становится ясно, о каком именно варианте обострения ИБС идет речь: нестабильной стенокардии, инфаркте миокарда (ИМ) без подъема сегмента ST, ИМ с подъемом сегмента ST, либо коронарную природу болевого синдрома исключают. Термин возник в связи с необходимостью оперативно, без промедления выбирать лечебную тактику до установления окончательного диагноза. Кроме того, все состояния, относимые к ОКС, объединены общими патогенетическими механизмами. С точки зрения особенностей развития процесса, возможности быстрой диагностики, выработки тактики лечения, оказалось удобным разделить ОКС на две группы в зависимости от изменений на исходной электрокардиограмме (ЭКГ): ОКС с подъемом сегмента ST (ОКСпST) и ОКС без подъема сегмента ST (ОКСбпST). При ОКСпST в большинстве случаев в дальнейшем развивается крупноочаговый инфаркт миокарда с формированием патологического зубца Q или без него. У больных с ОКСбпST обычно диагностируют нестабильную стенокардию или мелкоочаговый инфаркт миокарда [2].
Данные рекомендации, разработанные коллективом авторов, анализируют современные подходы к ОКС.
Острый коронарный синдром — временный «рабочий» диагноз, который необходим для первичной оценки, стратификации риска, выбора тактики лечения у больных с обострением ИБС. После непродолжительного периода наблюдения и диагностики, обычно не превышающего суток, становится ясно, о каком именно варианте обострения ИБС идет речь: нестабильной стенокардии, инфаркте миокарда (ИМ) без подъема сегмента ST, ИМ с подъемом сегмента ST, либо коронарную природу болевого синдрома исключают. Термин возник в связи с необходимостью оперативно, без промедления выбирать лечебную тактику до установления окончательного диагноза. Кроме того, все состояния, относимые к ОКС, объединены общими патогенетическими механизмами. С точки зрения особенностей развития процесса, возможности быстрой диагностики, выработки тактики лечения, оказалось удобным разделить ОКС на две группы в зависимости от изменений на исходной электрокардиограмме (ЭКГ): ОКС с подъемом сегмента ST (ОКСпST) и ОКС без подъема сегмента ST (ОКСбпST). При ОКСпST в большинстве случаев в дальнейшем развивается крупноочаговый инфаркт миокарда с формированием патологического зубца Q или без него. У больных с ОКСбпST обычно диагностируют нестабильную стенокардию или мелкоочаговый инфаркт миокарда [2].
Данные рекомендации, разработанные коллективом авторов, анализируют современные подходы к ОКС.
Определение:
Острый коронарный синдром (ОКС) – клиническое состояние, отражающее период обострения ишемической болезни сердца (ИБС), ведущим симптомом которого является боль в грудной клетке, инициирующая определенный диагностический и терапевтический каскад, начиная с регистрации ЭКГ на основании изменений которой дифференцируются 2 группы пациентов: с подъемом сегмента ST и без подъема сегмента ST.
Классификация
Классификация:
1. Пациенты с острой стойкой болью в грудной клетке и стабильной элевацией сегмента ST на ЭКГ (>20 мин) относятся к группе ОКС с подъѐмом сегмента ST, что отражает наличие острой тотальной окклюзии коронарной артерии. Основой лечения таких пациентов является немедленная реперфузия фармакологическая или методом первичной ангиопластики/стентирования (инфаркт миокарда с подъемом сегмента ST рассматривается в отдельном протоколе).
2. Пациенты с острой болью в грудной клетке, но без элевации сегмента ST на ЭКГ относятся к группе ОКС без подъема сегмента ST, что отражает наличие преходящей частичной окклюзии коронарной артерии или дистальной эмболизации фрагментами тромба или поврежденной бляшки. Изменения на ЭКГ могут быть в виде преходящей элевации сегмента ST (<20 мин), постоянной или преходящей депрессии сегмента ST, инверсии, нивелировании или псевдонормализации зубца Т или ЭКГ может быть нормальной.
2. Пациенты с острой болью в грудной клетке, но без элевации сегмента ST на ЭКГ относятся к группе ОКС без подъема сегмента ST, что отражает наличие преходящей частичной окклюзии коронарной артерии или дистальной эмболизации фрагментами тромба или поврежденной бляшки. Изменения на ЭКГ могут быть в виде преходящей элевации сегмента ST (<20 мин), постоянной или преходящей депрессии сегмента ST, инверсии, нивелировании или псевдонормализации зубца Т или ЭКГ может быть нормальной.
Формы острого коронарного синдрома.
Нестабильная стенокардия - острая ишемия миокарда, тяжесть и продолжительность которой недостаточны для развития некроза миокарда (нет диагностически значимых повышений уровней тропонина).
Инфаркт миокарда без подъема сегмента ST и с подъемом сегмента ST– острая ишемия миокарда, тяжесть и продолжительность которой приводит к некрозу миокарда.
Классификация нестабильной стенокардии.
- Впервые возникшая стенокардия (впервые возникшая стенокардия II-III функционального класса по классификации Канадского сердечно-сосудистого общества, длительностью не более 2 месяцев)
- Прогрессирующая (прогрессирование ранее стабильной стенокардии, по крайней мере до III функционального класса, возникшее в последние 2 месяца)
- Ранняя постинфарктная стенокардия (до 2 недель от развития ИМ) -Вазоспастическая стенокардия Принцметала
Острый инфаркт миокарда. Термин «повреждение миокарда» может быть использован при повышении уровня кардиального тропонина выше 99 перцентиля от верхней границы нормы. Повреждение миокарда считают острым, если отмечается нарастание или снижение уровня тропонина.
Рис. 1 Варианты ОКС
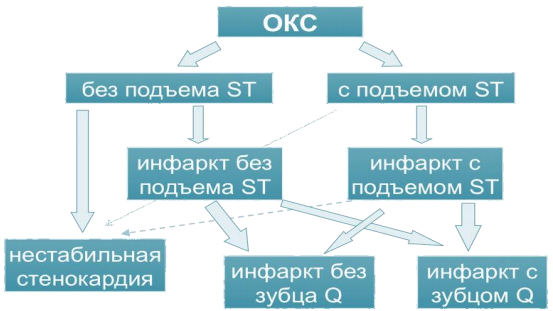
Настоящее руководство основано на принципах доказательной медицины. Основные наиболее важные положения подкреплены результатами крупных рандомизированных клинических исследований. Вместе с тем, допускаются рекомендации, основанные на мнении экспертов. В зависимости от обоснованности рекомендации делятся на 4 класса и 3 уровня доказательности данных (табл. 1 и 2).
Классификация инфаркта миокарда
На основании исходных изменений на ЭКГ (должно быть отражено в диагнозе):
1. ИМ с подъемом сегмента ST (к этой группе относят также остро возникшуюблокаду ЛНПГ).
2. ИМ без подъема сегмента ST.
На основании последующих изменений на ЭКГ (должно быть отражено в диагнозе):
1. ИМ с формированием патологических зубцов Q.
2. ИМ без формирования патологических зубцов Q.
На основании размера очага некроза (может быть отражено в диагнозе):
1. Крупноочаговый (в том числе трансмуральный) ИМ.
2. Мелкоочаговый ИМ.
На основании глубины поражения мышечного слоя (может быть отражено в диагнозе):
1. Субэндокардиальный.
2. Трансмуральный.
На основании локализации очага некроза (если известно, должно быть отражено в диагнозе):
1. ИМ с подъемом сегмента ST (к этой группе относят также остро возникшуюблокаду ЛНПГ).
2. ИМ без подъема сегмента ST.
На основании последующих изменений на ЭКГ (должно быть отражено в диагнозе):
1. ИМ с формированием патологических зубцов Q.
2. ИМ без формирования патологических зубцов Q.
На основании размера очага некроза (может быть отражено в диагнозе):
1. Крупноочаговый (в том числе трансмуральный) ИМ.
2. Мелкоочаговый ИМ.
На основании глубины поражения мышечного слоя (может быть отражено в диагнозе):
1. Субэндокардиальный.
2. Трансмуральный.
На основании локализации очага некроза (если известно, должно быть отражено в диагнозе):
1. ИМ передней стенки левого желудочка (передний ИМ).
2. ИМ боковой стенки левого желудочка (боковой ИМ).
3. ИМ верхушки сердца.
4. ИМ нижней стенки левого желудочка (нижний ИМ).
5. ИМ задней стенки ЛЖ (задний ИМ).
6. ИМ межжелудочковой перегородки.
7. ИМ правого желудочка.
8. ИМ предсердий.
9. Возможны сочетанные локализации: задненижний, переднебоковой и др.
Таблица 4.
Разделение по типу (ESC/ACCF/AHA/WHF, 2012, https://pubmed.ncbi.nlm.nih.gov/22991454/)
2. ИМ боковой стенки левого желудочка (боковой ИМ).
3. ИМ верхушки сердца.
4. ИМ нижней стенки левого желудочка (нижний ИМ).
5. ИМ задней стенки ЛЖ (задний ИМ).
6. ИМ межжелудочковой перегородки.
7. ИМ правого желудочка.
8. ИМ предсердий.
9. Возможны сочетанные локализации: задненижний, переднебоковой и др.
Таблица 4.
Разделение по типу (ESC/ACCF/AHA/WHF, 2012, https://pubmed.ncbi.nlm.nih.gov/22991454/)
|
Типы
|
Характеристика
|
|
1 тип
|
Спонтанный разрыв, изъязвление/эрозирование или расслоение, атеросклеротической бляшки, ведущее к последующему интракоронарному тромбозу в одной или нескольких артериях, резкому ограничению кровотока ниже поврежденной бляшки или дистальной тромбоцитарной эмболизации с последующим развитием некроза сердечной мышцы. Возможно, как на фоне имеющейся ИБС, так и в редких случаях, при непораженных коронарных артериях.
|
|
2 тип
|
Ситуации, когда повреждение миокарда обусловлены иными причинами, не относимыми к ИБС, например, эндотелиальной дисфункцией, спазмом коронарных артерий, эмболизацией коронарных артерий, тахи/брадиаритмиями, анемией, дыхательной недостаточностью, системной гипотонией, гипертензией в сочетании с гипертрофией миокарда левого желудочка и без нее.
|
|
3 тип
|
Внезапная сердечная смерть в сочетании с симптомами, позволяющими заподозрить ишемию миокарда, подтвержденную ишемическими изменениями на ЭКГ, вновь зарегистрированной блокадой ЛНПГ, в тех случаях, когда смерть произошла до момента взятия анализа крови на маркеры некроза
миокарда, до повышения их титров до диагностического уровня и во всех других случаях, когда анализ крови |
|
4 а тип
|
Инфаркт миокарда, связанный с ЧКВ, диагностируется при определении повышенного уровня тропонинов свыше 5×99 перцентиля ВГН у пациентов с нормальным исходным уровнем, либо нарастания его титра на 20% (при исходно повышенном уровне) и более от исходных значений. Дополнительным критерием диагноза служит (1) клиника стенокардии, (2) симптомы ишемии на ЭКГ, БЛНПГ, (3) окклюзия коронарной артерии по данным ангиографического исследования, феномен замедленного контрастирования в симптом связанной артерии, дистальная эмболизация коронарного русла, (4) визуализация зон аномального движения стенок сердца.
|
|
4 b тип
|
ИМ ассоциированный связанный с тромбозом ранее установленного стента, подтвержденный с помощью коронароангиографии либо аутопсии в сочетании с клиническими симптомами ишемии миокарда и типичной динамикой кардиоспецифических ферментов.
|
| 5 тип | ИМ, ассоциированный с операцией коронарного шунтирования, устанавливается на основании определения повышенного уровня тропонина, либо нарастания его титра на 20% и более от исходных значений. Дополнительным критерием служат появление патологического зубца Q на ЭКГ, вновь зарегистрированная БЛНПГ, ангиографически подтвержденная окклюзия шунта или нативной артерии, визуализация нового участка нежизнеспособного миокарда или новых очагов нарушения движения стенок, kибо появление новых зон гипокинезии и акинезии. |
Таблица 5.
Классификация тяжести ОИМ по Killip
Классификация тяжести ОИМ по Killip
|
Класс
|
Характеристика
|
|
I
|
Нет сердечной недостаточности
|
|
II
|
Влажные хрипы <50% легочных полей, III тон, легочная гипертензия.
|
|
III
|
Влажные хрипы >50% легочных полей. Отек легких
|
|
IV
|
Кардиогенный шок
|
Этиология и патогенез
Этиология и патогенез
В большинстве случаев (~95%) основными причинами ИБС являются анатомический, атеросклеротический и/или функциональный стеноз и/или микрососудистая дисфункция эпикардиальных сосудов [4]. Ишемическая болезнь сердца определяется наличием и ростом обструктивных или необструктивных атеросклеротических бляшек (АСБ).
Ишемия миокарда возникает, когда потребность миокарда в кислороде превышает его способность снабжаться кровотоком коронарной артерии.
Ишемия миокарда возникает, когда потребность миокарда в кислороде превышает его способность снабжаться кровотоком коронарной артерии.
Основные механизмы ишемии:
- снижение резерва коронарного кровотока (способности увеличивать коронарный кровоток при повышении метаболических потребностей миокарда), а также
- первичное снижение коронарного кровотока вследствие атеросклеротического стеноза.
Этиология поражения миокарда кислородом определяется тремя основными факторами:
-
напряжение стенок левого желудочка (ЛЖ);
-
частота сердечных сокращений (ЧСС);
-
сокращение миокарда.
Чем выше значение каждого из этих показателей, тем выше уровень потребления кислорода миокардом.
Клиническая картина
Cимптомы, течение
Клиническая картина
Жалобы и анамнез
Клинические проявления ОКС/ОИМ
-
Продолжительная (>20 мин) ангинозная боль в грудной клетке в покое: типичная боль в области сердца характеризуется дискомфортом или тяжестью за грудиной (стенокардия), иррадиирущей в левую руку, шею или челюсть, которая может быть преходящей (обычно продолжается несколько минут) или более длительной. Боль может сопровождаться потливостью, тошнотой, болью в животе, одышкой и обмороком. Нередко отмечаются атипичные проявления, такие как боль в эпигастральной области, диспепсия или изолированная одышка. Атипичные симптомы чаще отмечаются у пациентов пожилого возраста, у женщин, больных сахарным диабетом, хронической почечной недостаточностью или деменцией.
-
Впервые возникшая стенокардия напряжения (II или III ФК) (CCS) с анамнезом заболевания 1-2 месяца с тенденцией к прогрессированию клинической симптоматики. Приступы могут возникать при физической нагрузке и оставаться первое время относительно стереотипными, в других случаях приступы стенокардии быстро нарастают по частоте и интенсивности, вплоть до спонтанных приступов с длительностью от 5 до 15 минут и более.
-
Прогрессирующая стенокардия напряжения, по крайней мере, до III ФК: нарастание тяжести приступов стенокардии с прогрессирующим снижением толерантности к физической нагрузке, расширение зоны болей и их иррадиации, удлинение продолжительности приступов, снижение эффективности нитроглицерина [4], появление новых сопутствующих симптомов (одышки, перебоев в сердце, слабости, страха и т.д.).
-
Ранняя постинфарктная стенокардия, развившаяся в пределах 2-х недель после инфаркта миокарда.
Пациент с прогрессирующей или с впервые возникшей стенокардией давностью в несколько часов или суток потенциально намного более угрожаем в отношении развития ИМ или ВСС, чем пациент с аналогичными жалобами у которого нарастание симптомов произошло в последние 2-4 недели или менее 8 недель.
Пожилой возраст, мужской пол, семейный анамнез ИБС, диабет, гиперлипидемия, гипертензия, почечная недостаточность, предшествующее проявление ИБС, так же как поражения периферических и сонных артерий, повышают вероятность наличия ОКСбпST. Состояния, которые могут усугубить или ускорить развитие ОКСбпST, включают анемию, инфекции, воспалительный процесс, лихорадку, метаболические или эндокринные (в особенности щитовидной железы) нарушения.
Физикальное обследование: больных с подозрением на острый коронарный синдром мало информативно. Признаки сердечной недостаточности, гемодинамической или электрической нестабильности требуют быстрой диагностики и лечения. Аускультация сердца может выявить систолический шум вследствие ишемической митральной регургитации, которое ассоциировано с плохим прогнозом. Редко систолический шум может указывать на механическое осложнение (например, отрыв папиллярных мышц или дефект межжелудочковой перегородки) подострого и, возможно, недиагностированного ИМ.
Физикальное обследование может выявить признаки некоронарных причин болей в грудной клетке (например, ТЭЛА, острый аортальный синдром, миоперикардит, аортальный стеноз) или экстракардиальной патологии (например, пневмоторакс, пневмония или заболевания опорно-двигательного аппарата). В данном случае, наличие боли в грудной клетке, которая может быть воспроизведена пальпацией грудной клетки, имеет относительно высокую отрицательную предсказательную ценность для ОКСбпST. Согласно проявлениям, абдоминальные расстройства (например, спазм пищевода, эзофагит, язва желудка, холецистит, панкреатит) также могут рассматриваться в плане дифференциальной диагностики. Разница АД между верхней и нижней конечностями или между руками, нерегулярный пульс, расширение яремных вен, шумы в сердце, шум трения плевры, боль, воспроизводимая пальпацией грудной клетки или живота, предполагают постановку альтернативного диагноза. Бледность, потливость или тремор рук могут указывать на такие состояния, как анемия и тиреотоксикоз [4].
Необходимо оценить характер и продолжительность болевого синдрома. Для ишемии миокарда характерно наличие боли (дискомфорта) за грудиной с возможной иррадиацией в шею, нижнюю челюсть, левую руку. Сила болевого синдрома может быть различной, у отдельных больных он может сопровождаться страхом, возбуждением, выраженными вегетативными расстройствами. Менее характерны изолированная одышка, удушье, боль в верхних отделах живота, тошнота и рвота, слабость, спутанность сознания, сердцебиение, синкопе, а также проявления только в местах иррадиации. Атипичные проявления ишемии миокарда чаще встречаются у женщин, пожилых, больных с сахарным диабетом. Оценка реакции на нитроглицерин для определения связи симптомов с ишемией миокарда не рекомендуется, однако если после приема нитроглицерина симптомы купировались, необходимо повторно зарегистрировать ЭКГ (полное исчезновение подъемов сегмента ST свидетельствует в пользу коронарного спазма). Симптоматика может быть постоянной или волнообразной. Для определения показаний к реперфузионной терапии необходимо максимально точно выяснить время возникновения текущего ишемического эпизода – предположительного возникновения стойкой окклюзии коронарной артерии (при волнообразных симптомах за точку отсчета принимают начало наиболее сильного приступа, ставшего причиной обратиться за помощью).
Атипичные формы
В некоторых случаях интенсивный ангинозный приступ не является ведущим симптомом ИМ. Существует несколько вариантов нетипичного клинического течения ИМ.
Астматический вариант, при котором ведущий (иногда единственный) симптом — одышка, обусловленная левожелудочковой недостаточностью. Чаще такой вариант развивается у пожилых больных и при повторном ИМ. Одышка часто говорит о значительном объеме поражения миокарда.
Абдоминальный вариант ИМ чаще наблюдают при нижней локализации ИМ. Для него характерны боль в эпигастральной области и диспепсические явления — тошнота, рвота,метеоризм. При пальпации иногда наблюдают болезненность и напряжение брюшной стенки, затрудняющие постановку правильного диагноза. Нередко такие больные поступают в хирургические отделения с диагнозом «острый живот».
Церебральный вариант ИМ, при котором на первый план выходят неврологические симптомы, обусловленные различными причинами.
Ослабление сократительной функции ЛЖ и/или брадиаритмии приводят к уменьшению минутного объема сердца и перфузионного давления в артериях, кровоснабжающих головной мозг. У больных с исходной цереброваскулярной недостаточностью на фонеатеросклероза дополнительное снижение кровотока, связанное с ИМ, может привести к декомпенсации и развитию нарушения мозгового кровообращения. Другим клиническим проявлением гипоксии мозга может быть обострение или манифестация психических заболеваний. В редких случаях ИМ клинически протекает как острый психоз.
На фоне ИМ может развиться ишемический инсульт вследствие тромбоза церебральных артерий. Другой причиной ишемического инсульта может быть тромбоэмболия как осложнение тромбоза левого желудочка. Наконец, на фоне массивной антитромботической терапии, особенно, ТЛТ, возможно развитие геморрагического инсульта.
Аритмический вариант, при котором боль выражена незначительно или отсутствует. Больного беспокоят симптомы, связанные с нарушениями ритма и/или проводимости — ощущение сердцебиения, перебоев в работе сердца, слабость.
Бессимптомный (малосимптомный) вариант. Иногда ИМ протекает малосимптомно или бессимптомно. Около 50% случаев ИМ диагностируют ретроспективно, причем примерно половина из них протекает без болевого приступа. Частота бессимптомного ИМ с зубцом Q по разным данным составляет 9-37%. По данным регистра NRMI-2 (430 тыс. больных), около трети больных с ИМ поступают в стационар без болевого приступа. Эти больные либо не испытывают симптомов, либо у них наблюдают одышку, сердцебиение, тошноту, рвоту. Чаще бессимптомные или малосимптомные формы ИМ наблюдают у пожилых людей (особенно у женщин) и у больных сахарным диабетом.
Нетипичная локализация болей. У некоторых больных болевой синдром при ИМ носит нетипичный характер. Боль может иррадиировать в правую верхнюю конечность, нижние конечности, носить «корешковый характер» и т.д. В одном наблюдении среди больных, госпитализированных в связи с острой прокалывающей болью в грудной клетке, в 22% случаев обнаруживали ИМ. Следовательно, нетипичный вариант болевого синдрома — не редкость.
Диагностика
Диагностика заболевания.
Электрокардиограмма в 12 отведениях
При клиническом подозрении на ОКС/ОИМ необходимо как можно быстрее – в ближайшие 10 минут после контакта с медицинским работником – зарегистрировать ЭКГ как минимум в 12 отведениях. [2]. У всех больных с нижним ИМ необходимо регистрировать ЭКГ в прекардиальных отведениях с правой стороны для исключения инфаркта правого желудочка. Для ОКС характерно острое возникновение изменений на ЭКГ. Поэтому во всех случаях следует стремиться получить ЭКГ, зарегистрированные до настоящего ухудшения, и сопоставить их с текущей. При сохранении симптомов у больных, не имеющих измененийна ЭКГ, характерных для ОКС (ИМ)пST, необходимо регистрировать ЭКГ повторно, чтобыне пропустить появление критериев острого коронарного синдрома и, соответственно, возникновение показаний к реперфузионному лечению.
Признаком ИМ правого желудочка является элевация сегмента ST в отведениях V3R- V4R. В случае подозрения на ИМ задней локализации (высокоамплитудные зубцы R в отведениях V1–V3) следует зарегистрировать ЭКГ в дополнительных грудных отведениях V7 (левая задняя подмышечная линия), V8 (левая средне-лопаточная линия) или V9 (левая околопозвоночная линия). Признак ИМ задней локализации — элевация сегмента ST в этих отведениях. При блокаде ЛНПГ диагностика ИМ с помощью ЭКГ существенно затруднена. Блокада ЛНПГ не всегда свидетельствует об остром ИМ, однако у больных с клинической симптоматикой, подозрительной в отношении продолжающейся ишемии миокарда, является основанием для выбора стратегии ведения, аналогичной ОКС(ИМ)пST . [4]
Признаком ИМ правого желудочка является элевация сегмента ST в отведениях V3R- V4R. В случае подозрения на ИМ задней локализации (высокоамплитудные зубцы R в отведениях V1–V3) следует зарегистрировать ЭКГ в дополнительных грудных отведениях V7 (левая задняя подмышечная линия), V8 (левая средне-лопаточная линия) или V9 (левая околопозвоночная линия). Признак ИМ задней локализации — элевация сегмента ST в этих отведениях. При блокаде ЛНПГ диагностика ИМ с помощью ЭКГ существенно затруднена. Блокада ЛНПГ не всегда свидетельствует об остром ИМ, однако у больных с клинической симптоматикой, подозрительной в отношении продолжающейся ишемии миокарда, является основанием для выбора стратегии ведения, аналогичной ОКС(ИМ)пST . [4]
Для развивающегося ОКС(ИМ)пST характерны остро возникшие подъемы сегмента ST на уровне точки J как минимум в двух смежных отведениях ЭКГ продолжительностью не менее 20 минут, ≥0,1 мВ во всех отведениях, за исключением отведений V2-V3, где элевация сегмента ST должна составлять ≥0,2 мВ у мужчин в возрасте 40 лет и старше, ≥0,25 мВ у мужчин моложе 40 лет или 0,15 ≥мВ у женщин (при отсутствии гипертрофии левого желудочка или блокады левой ножки пучка Гиса). На основании изменений ЭКГ можно с высокой точностью судить о локализации ИМ (табл. 4)
Таблица 6.
Локализация инфаркта миокарда на основании электрокардиографии
Локализация инфаркта миокарда на основании электрокардиографии
|
Локализация
|
Отведения
|
|
Переднеперегородочный
|
V1–V3
|
|
Передневерхушечный
|
V3, V4
|
|
Переднебоковой
|
I, aVL, V5, V6
|
|
Боковой
|
aVL, V5, V6
|
|
Распространенный передний
|
I, aVL, V1–V6
|
|
Заднедиафрагмальный (нижний)
|
II, III, aVF
|
|
Заднебазальный
|
Высокая амплитуда R в V1–V3,
элевация сегмента ST в V7–V9 |
|
Заднебоковой
|
V5, V6, III, aVF
|
|
Инфаркт правого желудочка
|
V3R, V4R
|
|
Возможны другие сочетания локализаций ИМ, например: передний в сочетании с нижним
|
V1–V4, II, III, aVF
|
Для ИМ не характерна статичная «застывшая» ЭКГ. Важное отличие ЭКГ при ИМ - характерная динамика, заключающаяся в формировании патологического зубца Q или комплекса QS, постепенном снижении сегмента ST, образовании отрицательных зубцов T. Если изменения на ЭКГ имеют постоянный характер и не претерпевают указанной динамики, то наличие ИМ сомнительно.
Электрокардиографические признаки свершившегося инфаркта миокарда
-
Любой зубец Q в отведениях V2–V3 0,02 с, или комплекс QS в этих отведениях.
-
Зубец Q 0,03 с и амплитудой 0,1 мВ (1 мм) в отведениях I, II, aVL, aVF, V4–V6. Указанные изменения должны быть отмечены не менее чем в двух соседних отведениях.
-
Признаки заднего ИМ: зубец R в отведениях V1–V2 0,04 с, R/S в V1–V2 1. Положительный конкордантный зубец T в V1–V2. Необходимое условие — отсутствие нарушений внутрижелудочковой проводимости.
Таблица 7.
Атипичные изменения на ЭКГ, при которых у больных с сохраняющимися симптомами, возможно обусловленными ишемией миокарда, показана стратегия ведения, аналогичная первичномуЧКВ при несомненном ОКС(ИМ)пST.
Атипичные изменения на ЭКГ, при которых у больных с сохраняющимися симптомами, возможно обусловленными ишемией миокарда, показана стратегия ведения, аналогичная первичномуЧКВ при несомненном ОКС(ИМ)пST.
|
Блокада левой ножки пучка Гиса.
Признаки, улучшающие диагностику остро возникшей окклюзии коронарной артерии, характерной для ОКС(ИМ)пST (критерии Sgabossa):
|
|
Блокада правой ножки пучка Гиса.
Может затруднять диагностику трансмуральной ишемии миокарда |
|
Ритм ЭКС.
При электрической стимуляции правого желудочка на ЭКГ выявляется блокада левой ножки пучка Гиса и могут использоваться критерии Sgabossa, однако они менее специфичны. |
|
Изолированный задний ИМ.
|
|
Депрессии сегмента ST 0,1 мВ (1 мм) в 6 и более отведениях в сочетании с подъемами сегмента ST в отведениях aVR и/или V1
Предполагает многососудистое поражение коронарного русла или обструкцию ствола левой коронарной артерии. |
При ряде состояний возможные изменения на ЭКГ, характерные для ОКС(ИМ)пST.
Основные причины подъема сегмента ST.
-
Острый перикардит.
-
Синдром ранней реполяризации желудочков.
-
Блокада ЛНПГ (в отведениях V1–V2).
-
Гипертрофия левого желудочка (в отведениях V1–V2).
-
Аневризма левого желудочка.
-
Стенокардия Принцметала.
-
Синдром Бругада (элевация в V1–V2 и блокада правой ножки пучка Гиса).
-
Стресс-индуцированная кардиопатия (синдром Такоцубо).
-
Гиперкалиемия (V1–V2).
-
Травмы и опухоли сердца.
-
Гипотермия.
Основные причины глубоких зубцов Q и комплексов QS.
- Физиологические варианты зубца Q, обычно в отведениях III и aVF.
- Физиологические варианты низкоамплитудного зубца R, позиционные сдвиги: левосторонний пневмоторакс, декстракардия (низкоамплитудные зубцы R в левых грудных отведениях).
- Воспалительные и инфильтративные заболевания миокарда (миокардит, дилатационная кардио-миопатия, амилоидоз, саркоидоз, опухоли, склеродермия и т.д.).
- Тромбоэмболия легочной артерии (феномен Q3–S1).
- Гиперкалиемия.
- Гипертрофическая кардиомиопатия.
- Блокада ЛНПГ (низкоамплитудные зубцы R в отведениях V1–V2).
- Синдром пред возбуждения желудочков (синдром Вольффа–Паркинсона–Уайта).
Основные причины высокоамплитудного зубца R в правых грудных отведениях (дифференциальная диагностика заднего ИМ).
-
Физиологический зубец R в V1–V2.
-
Гипертрофия правого желудочка — отклонение электрической оси сердца вправо, сдвиг интервала ST–T в V1–V2, отсутствуют изменения в V7–V9.
-
Гипертрофия межжелудочковой перегородки; часто с признаками гипертрофии ЛЖ, отсутствуют изменения в V7–V9.
-
Блокада ПНБГ — расширенный комплекс QRS, широкий зубец S в V1, отсутствуют изменения вV7–V9.
-
Синдром Вольффа–Паркинсона–Уайта —короткий сегмент PQ, дельта -волна, отсутствуют изменения в V7–V9.
ЛАБОРАТОРНЫЕ ДИАГНОСТИЧЕСКИЕ ИССЛЕДОВАНИЯ.
МАРКЕРЫ ПОВРЕЖДЕНИЯ МИОКАРДА
Основное патогенетическое звено ИМ — некроз кардиомиоцитов, вследствие которого в периферический кровоток выходят внутриклеточные молекулы, которые в нормальных условиях не определяются или содержатся в низкой концентрации. Эти молекулы (в основном, белковой природы) называют маркерами повреждения миокарда. Повышение уровня маркеров повреждения миокарда — основной, необходимый критерий постановки диагноза ИМ. При первом контакте с больным диагноз ИМ ставят на основании типичной клинической картины и характерной динамики ЭКГ. Взятие крови для определения биомаркеров некроза миокарда (предпочтительно сердечного тропонина) следует производить как можно скорее, но их исходный уровень и динамика не влияют на выбор подхода к реперфузионному лечению и нужны для последующей верификации диагноза ИМ и стратификации риска неблагоприятного исхода. Для выявления ишемического некроза миокарда с помощью маркеров повреждения необходимо учитывать важное правило: для ИМ характерны не просто повышение уровня маркеров, а особая динамика, заключающаяся в появлении маркера (или существенном повышении концентрации), дальнейшем росте уровня с достижением максимального значения и постепенном снижении до нормальных значений. Если в течение длительного времени уровень маркера повреждения устойчиво повышен, следует искать другую причину, приведшую к выбросу маркера в периферический кровоток, не связанную с ИМ. Каждый маркер повреждения характеризует специфическое время появления в крови, достижения пиковых значений и нормализации значений. На эти временные параметры влияет ряд факторов, среди которых можно выделить восстановление коронарного кровотока. Характеристики основных маркеров повреждения миокарда приведены в табл. 7.
Основное патогенетическое звено ИМ — некроз кардиомиоцитов, вследствие которого в периферический кровоток выходят внутриклеточные молекулы, которые в нормальных условиях не определяются или содержатся в низкой концентрации. Эти молекулы (в основном, белковой природы) называют маркерами повреждения миокарда. Повышение уровня маркеров повреждения миокарда — основной, необходимый критерий постановки диагноза ИМ. При первом контакте с больным диагноз ИМ ставят на основании типичной клинической картины и характерной динамики ЭКГ. Взятие крови для определения биомаркеров некроза миокарда (предпочтительно сердечного тропонина) следует производить как можно скорее, но их исходный уровень и динамика не влияют на выбор подхода к реперфузионному лечению и нужны для последующей верификации диагноза ИМ и стратификации риска неблагоприятного исхода. Для выявления ишемического некроза миокарда с помощью маркеров повреждения необходимо учитывать важное правило: для ИМ характерны не просто повышение уровня маркеров, а особая динамика, заключающаяся в появлении маркера (или существенном повышении концентрации), дальнейшем росте уровня с достижением максимального значения и постепенном снижении до нормальных значений. Если в течение длительного времени уровень маркера повреждения устойчиво повышен, следует искать другую причину, приведшую к выбросу маркера в периферический кровоток, не связанную с ИМ. Каждый маркер повреждения характеризует специфическое время появления в крови, достижения пиковых значений и нормализации значений. На эти временные параметры влияет ряд факторов, среди которых можно выделить восстановление коронарного кровотока. Характеристики основных маркеров повреждения миокарда приведены в табл. 7.
Таблица 8.
Характеристики основных маркеров повреждения миокарда
Характеристики основных маркеров повреждения миокарда
| Маркер | Время появления показателя в крови, ч |
Время максимального значения показателя в крови, ч |
Длительность присутствия показателя в крови | Чувствительность | Специфичность |
|
Тропонин T
|
4–6
|
50
|
до 14 сут
|
100
|
95
|
|
Тропонин I
|
3–6
|
50
|
до 10 сут
|
100
|
95
|
|
Тропонин (высоко- чувствительный
тест) |
2–3 |
50 |
до 10 сут |
100 |
95 |
|
КФК-МВ
|
4–6
|
12
|
24–36 ч
|
88
|
90
|
|
КФК общая
|
6–8
|
8
|
36–48 ч
|
80-85
|
70
|
Сердечные тропонины
Тропонины — регуляторные белки, участвующие во взаимодействии актина и миозина. Тропонины I и T считают кардио специфичными. В связи с относительно небольшим молекулярным весом тропонины появляются в периферической крови при повреждении миокарда довольно быстро — через 3–6 ч. У абсолютного большинства здоровых лиц тропонин или не выявляется, или обнаруживается в минимальных количествах — от 0,01 до 0,1 мкг/мл. По чувствительности и специфичности сердечные тропонины превосходят все существующие маркеры повреждения. Тропонины рассматривают как предпочтительные маркеры для диагностики ИМ. Несмотря на высокую специфичность, при ряде заболеваний сердца и болезней, напрямую не связанных с сердцем, уровень сердечных тропонинов может быть повышен. Основные заболевания и состояния, при которых может повышаться тропонин, перечислены в приложении 1.
Для биохимической диагностики острого ИМ должны использоваться методы определения концентрации сердечного тропонина в крови, обеспечивающие коэффициент вариации определений 99-го перцентиля верхней границы нормы не выше 20% (оптимально – не выше 10%).
В настоящее время в клинической практике используют сердечные тропонины I и T реже КФК, КФК-MB (активность и концентрация). До сих пор по инерции используют одновременно тропонин и МВ-КФК, хотя в этом нет необходимости. Тропонин превосходит МВ-КФК по чувствительности, специфичности, диагностической точности. [4] Кроме того, возможна конфузная ситуация, когда уровень тропонина в норме, а МВ-КФК повышен.
МЕТОДЫ ВИЗУАЛИЗАЦИИ
Вследствие ишемии нарушается функция ЛЖ, как диастолическая, так и систолическая. Эти процессы можно объединить понятием потеря жизнеспособности. Другим признаком ишемии является нарушение перфузии миокарда. В настоящее время основные методы визуализации нарушений сократимости и перфузии при ИМ — ЭхоКГ, радионуклидные методы, КТ и МРТ.
Эхокардиография
С помощью ЭХО-КГ выявляют зоны нарушенной локальной сократимости миокарда, обусловленные тяжелой ишемией. Важно помнить, что нарушения локальной сократимости не являются абсолютным доказательством острого ИМ. Подобную картину можно встретить при ранее перенесенном ИМ, гибернации миокарда, миокардитах, предшествующих операциях на сердце, кардиомиопатиях и т.д. Отличительная особенность нарушения локальной сократимости при ранее перенесенном ИМ — истончение участка сердца в зоне рубца. При остром ИМ толщина пораженного участка не отличается от соседних участков миокарда. В сложных случаях может помочь контрастная ЭхоКГ, которая позволяет визуализировать субэндокардиальные отделы, оценивать перфузию миокарда, в том числе на микрососудистом уровне. Возможно использование тканевой допплерографии, которая количественно оценивает, как общую, так и локальную сократимость ЛЖ. Изменения, напоминающие нарушения локальной сократимости, наблюдают при асинхронном сокращении желудочков при блокаде ЛНПГ, синдроме предвозбуждения желудочков (синдром Вольффа–Паркинсона–Уайта). ЭхоКГ позволяет в сложных случаях установить локализацию и обширность ИМ. ЭхоКГ считают наиболее чувствительным методом для диагностики ИМ ПЖ, по своим диагностическим возможностям, превосходящим ЭКГ. Для оценки сократительной функции ЛЖ в период госпитализации проводят не менее двух раз — в первые сутки и ближе к выписке. ЭхоКГ — наиболее точный и доступный метод оценки сократимости ЛЖ при ИМ. При выраженном снижении сократительной функции (фракция выброса [ФВ] <35%) необходимо внимательно следить за симптомами сердечной недостаточности. Величина фракции выброса миокарда ЛЖ — существенный прогностический фактор и необходимый компонент при стратификации риска у больных ИМ. ЭхоКГ — основной метод диагностики ряда механических осложнений ИМ: разрыва межжелудочковой перегородки, разрыва свободной стенки или формирования аневризмы левого желудочка, дисфункции и отрыва папиллярных мышц, внутриполостного тромбоза.
Магнитно-резонансная томография (МРТ)
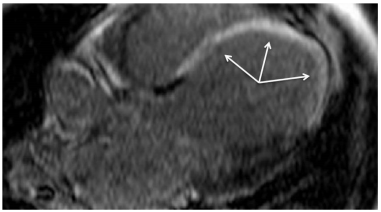
МРТ в динамическом (кино-) режиме позволяет точно, подобно ЭХО-КГ, оценить сократительную функцию миокарда и выявить участки нарушенной сократимости. Преимуществом МРТ является независимость от анатомических особенностей пациента и высокая разрешающая способность. Для выявления очагов инфаркта/фиброза и оценки перфузии миокарда используют парамагнитные контрастные вещества (гадолиний). Признаками поврежденного миокарда являются дефекты перфузии и отсроченное контрастирование (рис. 18). МРТ помогает в дифференциальной диагностике ОКС с рядом заболеваний миокарда, в частности с миокардитом. МРТ с гадолинием является важной методикой для дифференциального диагноза с неишемическим повреждением миокарда. Для ишемического повреждения характерно накопление контрастного препарата субэндокардиально или трансмурально; для неишемического (перикардит, миокардит) – субэпикардиально и интрамурально (Рис. 2).
Рис. 2. МРТ при ИМ. Стрелками указаны обширные зоны отсроченного контрастирования в миокардеЛЖ при ИМ передне-перегородочной локализации.
Мультиспиральная компьютерная томография (МСКТ)
При ОКС используют МСКТ рентген-контрастными препаратами. С помощью этого метода можно определить, как дефекты перфузии, так и очаги отсроченного контрастирования. В обоих случаях речь идет о выявлении необратимо поврежденных участков миокарда. Использование КТ особенно актуально в диагностически сложных случаях, особенно, когда есть подозрение на тромбоэмболию легочной артерии и диссекцию аорты. В последние 20 лет по мере усовершенствования оборудования возможности визуализации коронарных артерий с помощью МСКТ с введением контрастного препарата заметно увеличились. Метод позволяет оценить степень атеросклеротического поражения артерий, оценить выраженность кальциноза, в ряде случаев зафиксировать внутрикоронарный тромбоз, диссекцию стенки. МСКТ в отличии от КАГ позволяет измерить объем АСБ и обнаружить потенциально опасный признак АСБ – положительное ремоделирование. МСКТ коронарных артерий с контрастированием у больных с подозрением на ОКС позволяет провести быструю неинвазивную оценку изменений в артериях. МСКТ коронарных артерий может рассматриваться как альтернатива инвазивной ангиографии для исключения ОКС в случае низкой/промежуточной вероятности ИБС, когда тропонин и ЭКГ неинформативны. В случае наличия явных клинических и инструментальных признаков ОКСпST больному сразу должна быть выполнена КАГ, уточнять диагноз с помощью МСКТ нельзя.
Инвазивные методы обследования. Коронароангиография (КАГ)
КАГ — это инвазивное диагностическое исследование, выполняемое в условиях рентгено-операционной путем введения контрастного вещества в устья КА под рентгенологическим контролем.
Традиционно используется в диагностике ИБС и при стратификации риска осложнений, для выявления стенозов в КА, их локализации, протяженности и выраженности, а также, в ряде случаев, — для обнаружения участков нестабильности атеросклеротической бляшки.
Традиционно используется в диагностике ИБС и при стратификации риска осложнений, для выявления стенозов в КА, их локализации, протяженности и выраженности, а также, в ряде случаев, — для обнаружения участков нестабильности атеросклеротической бляшки.
КРИТЕРИИ ДИАГНОЗА ИНФАРКТ МИОКАРДА [3]
Инфаркт миокарда 1 и 2 типов
Уровень сердечного тропонина в крови >99-го перцентиля от верхней границы нормы у здоровых лиц как минимум однократно, повышение и/или снижение его концентрации в крови в сочетании как минимум с один признаком острой ишемии миокарда:
- Симптомы ишемии миокарда;
- Остро возникшие (или предположительно остро возникшие) ишемические изменения ЭКГ;
- Появление патологических зубцов Q на ЭКГ;
- Подтверждение с помощью методов визуализации наличия новых участков миокарда с потерей жизнеспособности или нарушением локальной сократимости в виде картины, характерной для ишемической этиологии;
- Выявление внутрикоронарного тромбоза при коронарной ангиографии или на аутопсии (для ИМ 1 типа).
Критерии диагностики острого ИМ 3 типа [2]
Сердечная смерть у больного с симптомами, указывающими на ишемию миокарда, сопровождающимися предположительно новыми ишемическими изменениями ЭКГ или фибрилляцией желудочков, в случаях, когда больной умирает до появления возможности взятия образцов крови или раньше, чем отмечается повышение активности биохимических маркеров некроза миокарда в крови, или наличие ИМ подтверждено на аутопсии. При выявлении на аутопсии ИМ в сочетании со свежим или недавно возникшим тромбом в инфаркт-связанной коронарной артерии ИМ 3 типа должен быть реклассифицирован в ИМ 1 типа.
Критерии диагностики острого ИМ 4А типа (первые 48 часов после процедуры чрескожного вмешательства). [2]
Повышение концентрации сердечного тропонина в крови более 5 раз >99-го перцентиля от верхней границы нормы у здоровых лиц у больных с исходно нормальным уровнем в крови (если до процедуры концентрация тропонина в крови была повышена и стабильна (вариация
≤20%) или снижалась, после процедуры она должен повыситься >20%) в сочетании как минимум с один признаком острой ишемии миокарда:
≤20%) или снижалась, после процедуры она должен повыситься >20%) в сочетании как минимум с один признаком острой ишемии миокарда:
- Остро возникшие ишемические изменения ЭКГ;
- Появление патологических зубцов Q на ЭКГ;
- Подтверждение с помощью методов визуализации наличия новых участков миокарда с потерей жизнеспособности или нарушением локальной сократимости в виде картины, характерной для ишемической этиологии;
- Ангиографические признаки, указывающие на ограничения коронарного кровотока, связанные с процедурой (диссекция КА, окклюзия/тромбоз крупной эпикардиальной/боковой ветви, разрушение коллатерального кровотока или дистальная эмболизация);
- Посмертное выявление тромба, связанного с процедурой, в целевой артерии, или макроскопически большая циркулярная область некроза.
Критерии диагностики острого инфаркта миокарда 4B типа [2]
Критерии острого ИМ 1 типа в сочетании с тромбозом стента, документированным при коронарной ангиографии или на аутопсии.
Критерии диагностики острого инфаркта миокарда 4С типа [2].
Критерии острого ИМ 1 типа, когда при коронарной ангиографии единственной причиной возникновения ИМ представляется рестеноз (не выявляются другие поражения, потенциально связанные с развившимся ИМ, нет признаков внутрикоронарного тромбоза).
Критерии диагностики острого инфаркта миокарда 5 типа (первые 48 часов после операции коронарного шунтирования) [2]
Повышение концентрации сердечного тропонина в крови более 10 раз >99-го перцентиля от верхней границы нормы у здоровых лиц у больных с исходно нормальным уровнем в крови (если до процедуры концентрация тропонина в крови была повышена и стабильна (вариация ≤20%) или снижалась, после процедуры она должен повыситься >20%) в сочетании как минимум с один признаком острой ишемии миокарда:
-
Появление патологических зубцов Q на ЭКГ;
-
Подтверждение с помощью методов визуализации наличия новых участков миокарда с потерей жизнеспособности или нарушением локальной сократимости в виде картины, характерной для ишемической этиологии;
-
Острая окклюзия шунта или нативной коронарной артерии, документированная при коронарной ангиографии.
Критерии диагностики ранее перенесенного инфаркта миокарда [2]
-
Патологические зубцы Q на ЭКГ (с наличием предшествующих симптомов или без них) при отсутствии не ишемических причин для появления патологических зубцов Q.
-
Подтверждение с помощью методов визуализации наличия участков миокарда с потерей жизнеспособности в виде картины, характерной для ишемической этиологии;
-
Морфологические находки, характерные для перенесенного инфаркта миокарда.
Рецидив инфаркта миокарда и повторный инфаркт миокарда
Под рецидивом ИМ понимают инцидент ИМ, который развивается в течение 28 дней после первоначального ИМ. Если ИМ развивается в более поздние сроки после говорят о повторном ИМ. Такое разделение носит условный характер и обусловлено эпидемиологическими причинами. Рецидив ИМ обычно проявляется ангинозным приступом, по характеру напоминающим приступ при первоначальном ИМ. Однако клинически рецидив ИМ может иметь отличия от первоначального ИМ. На ЭКГ возможна динамика в виде подъема или депрессии сегмента ST, изменения полярности зубца T, чаще в отведениях, где была динамика в острой фазе первоначального ИМ. Изменения на ЭКГ могут отсутствовать. Основной диагностический критерий, подтверждающий рецидив ИМ — повышение уровня маркеров повреждения миокарда. В случаях, когда значения биохимических маркеров некроза в крови еще остаются повышенными после недавно перенесенного ИМ, диагноз повторного ИМ выставляют при подъеме сердечного тропонина или МВ КФК не менее чем на 20% от уровня, отмеченного сразу после ангинозного приступа (при условии, что временной интервал до повторного анализа крови составляет, как минимум, 36 ч).
Таблица 9.
|
Рекомендации [2, https://cardio-eur.asia/media/files/clinical_recommendations/Eurasian_clinical_guidelines_for_the_diagnosis_and_treatment_of_acute_coronary_syndrome_with_ST_segment_elevation_(ACSpST)_rus_2019.pdf]
|
Класс
|
Уровень
|
|
ЭКГ как минимум в 12-ти отведениях должна быть зарегистрирована и интерпретирована как можно быстрее – максимально в первые 10 минут – на месте первого контакта с медицинским работником.
|
I
|
B
|
|
У всех больных с подозрением на ОКС(ИМ)пST рекомендуется как можно скорее начать мониторирование ЭКГ и обеспечить доступность дефибриллятора.
|
I
|
B
|
|
У всех больных как можно скорее следует выполнить взятие крови для определения уровня биомаркеров некроза миокарда, однако это не должно задерживать начало реперфузионого лечения.
|
I
|
C
|
|
Сердечные тропонины являются преимущественными маркерами повреждения для диагностики ИМ
|
I
|
C
|
|
У больных с подозрением на ИМ нажней задней локализации (и окклюзию огибающей коронарной артерии) следует зарегистрировать дополнительные отведения ЭКГ V7-V9.
|
IIa
|
B
|
|
У больных с нижним ИМ следует зарегистрировать дополнительные отведения ЭКГ V3R-V4R для выявления ИМ правого желудочка.
|
IIa
|
B
|
|
Если диагноз остается неясным, может быть рассмотрено выполнение ЭхоКГ до коронарной ангиографии.
|
IIa
|
C
|
|
Коронарная КТ-ангиография в случае очевидных признаков ОКСпST не рекомендуется.
|
III
|
C
|
Дифференциальный диагноз
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
На начальном периоде диагностики ОКС очень важно различать ИМ 1 типа и ИМ 2 типа, не связанный с обострением атеросклероза. Не менее актуально дифференцировать ИМ (ишемическое повреждение) от не ишемического повреждения. Если фиксируется увеличение уровня маркеров повреждения при повторном определении речь идет об остром повреждении миокарда. Стабильно высокий уровня маркеров является признаком хронического повреждения миокарда [2]. Для доказательств ишемической природы повреждения необходимо наличие клинических или инструментальных признаков ишемии (Рис. 3).
Рисунок 3. Причины повреждения миокарда. (модифицировано из Fourth universal definition of myocardial infarction 2018)
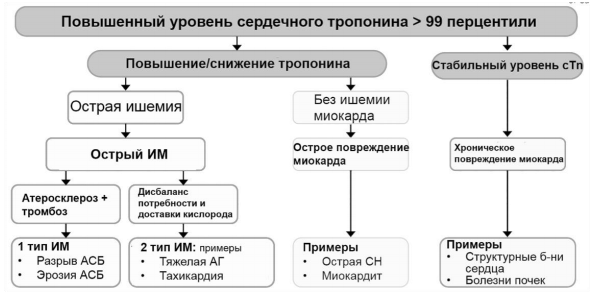
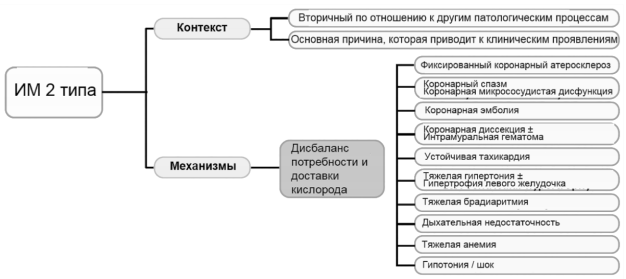
Рисунок 4. Основные причины ИМ 2 типа. (модифицировано из Fourth universal definition of myocardial infarction 2018)
Целый ряд заболеваний протекает с клинической картиной, напоминающей ОКС. Необходимо знать особенности клинической картины этих заболеваний, основные методы их диагностики. Ниже перечислены основные заболевания, с которыми приходится дифференцировать ОКСпST.
Расслаивающая аневризма аорты обычно начинается с приступа интенсивной боли в грудной клетке с иррадиацией в спину, часто похожей на боль при ИМ. При физикальном исследовании можно обнаружить грубый систолический шум на аорте, проводящийся на сонные артерии. При распространении расслоения до подключичных артерий отмечают асимметрию пульса. На ЭКГ признаков ишемии миокарда, как правило, не обнаруживают. В редких случаях в патологический процесс могут быть вовлечены устья коронарных артерий, и в этих ситуациях дифференциальная диагностика бывает особенно затруднена, [2] поскольку развивается типичный ангинозный приступ, а на ЭКГ возникают признаки ИМ. При малейших подозрениях на расслоение аорты показаны ЭхоКГ и/или КТ, МРТ. Важность дифференциальной диагностики между ИМ и расслоением аорты определяется также тактикой лечения, поскольку для эффективного лечения ИМ необходима ТЛТ, которая абсолютно противопоказана при расслоении аорты.[2]
Острый перикардит. Часто перикардиту предшествует простудное заболевание. Больные жалуются на боль в левой половине грудной клетки, связанную с дыханием и усиливающуюся на вдохе, зависящую от положения тела, обычно колющего, режущего характера, иногда по интенсивности сопоставимую с болевым синдромом при ИМ. При аускультации отмечают шум трения перикарда. На ЭКГ выявляют элевацию сегмента ST во многих отведениях (стандартные, грудные), имеющую конкордантный характер (в одном направлении с комплексом QRS). Патологических зубцов Q и комплексов QS нет. Возможно повышение показателей маркеров повреждения миокарда из-за повреждения субэпикардиальных зон миокарда. Иногда приходится исключать ОКС на основании КАГ [2].
При ТЭЛА боль часто бывает острой, плевритического характера и сопровождается одышкой, иногда кровохарканьем. При физикальном исследовании следует обратить внимание на состояние вен нижних конечностей (возможный источник эмболии). При аускультации в легких в первые сутки развития ТЭЛА можно не выслушать патологических изменений, однако при развитии инфарктной пневмонии появляются хрипы, ослабление дыхания. При рентгенографии органов грудной клетки до развития пневмонии отмечают обеднение сосудистого рисунка. На ЭКГ выявляют признаки перегрузки правых отделов сердца (феномен Q3–S1, блокада ПНБГ, P-pulmonale). Подтвердить диагноз можно с помощью вентиляционно-перфузионной сцинтиграфии легких, КТ с контрастированием легочных артерий (основной метод). Иногда проводят ангиографию легочных артерий. В большинстве случаев удается обнаружить источник тромбов. Признаком внутрисосудистого тромбообразования является повышение уровня D-димера. Этот анализ может быть использован в качестве скрининг-теста. Если уровень D-димера в пределах нормы, диагноз ТЭЛА маловероятен [2].
Острый миокардит. Иногда миокардиту предшествует простудное заболевание. Острый миокардит по сравнению с ИМ, как правило, развивается в более молодом возрасте. Болезнь может манифестировать с боли в грудной клетке. На ЭКГ возможно снижение амплитуды зубца R в грудных отведениях (даже комплексы QS), однако типичную для ИМ динамику изменений на ЭКГ наблюдают редко, и обычно она бывает связана с сопутствующим коронаритом. Для постановки правильного диагноза часто приходится проводить КАГ, при которой у больных миокардитом, как правило, не выявляют признаков выраженного коронарного атеросклероза.
Кардиомиопатия Такоцубо, стрессовая кардиопатия (от японского «такоцубо» — ловушка для осьминога) - транзиторное шарообразное расширение верхушки левого желудочка. Кардиопатия Такоцубо чаще всего манифестирует в виде ангинозного приступа. На ЭКГ могут элевации сегмента ST, иногда ишемические изменения ЭКГ отсутствуют. Основа диагноза – отсутствие ангиографических изменений в коронарных артериях в сочетании с верхушечным акинезом/дискинезом. Другая особенность - несоответствие между большой зоной поражения и незначительным повышением/отсутствием повышения уровня маркеров повреждения. Заболевание чаще встречается у женщин и, как правило, развивается после большого эмоционального напряжения. Функция левого желудочка обычно полностью восстанавливается в течение нескольких дней или недель. Этиология неизвестна, ведущую роль отводят вазоспазму и нарушению микроциркуляции.
Таблица 10.
Дифференциальная диагностика острого коронарного синдрома при наличии острой боли в грудной клетке
Дифференциальная диагностика острого коронарного синдрома при наличии острой боли в грудной клетке
|
Сердечные
|
Легочные
|
Сосудистые
|
Желудочно-кишечные
|
Ортопедические
|
Другие
|
|
Миокардиты
|
Легочная эмболия
|
Расслоение аорты
|
Эзофагит, рефлюкс
спазм |
Скелетно-мышечные
заболевания |
Тревожные расстройства.
|
|
Кардиомиопатииа |
(Напряженный) пневмоторакс
|
Симптомная аневризма аорты
|
Язва желудка, гастриты,
панкреатиты |
Травма сердца
|
Герпес Zoster |
|
Тахиаритмии
|
Бронхиты, пневмонии
|
Инсульт
|
Холециститы
|
Повреждение мышц,
воспаление |
Анемия
|
|
Острая сердечная
недостаточность |
Плевриты
|
|
|
Остеохондроз
|
|
|
Гипертонические кризы |
|
|
|
Патология шейного отдела позвоночника
|
|
|
Стеноз
аортального клапана |
|
|
|
|
|
|
Кардиомиопатия
такоцубо |
|
|
|
|
|
|
Коронарный
спазм |
|
|
|
|
|
|
Травма сердца
|
|
|
|
|
|
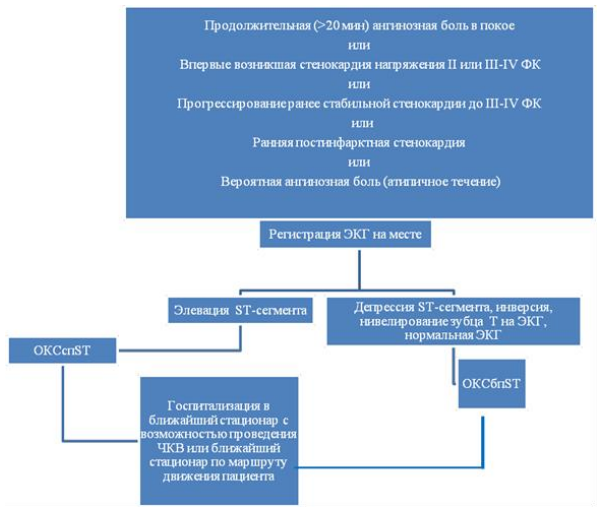
Диагностический алгоритм: (схема1)
(Рекомендации Европейского общества кардиологов по ведению пациентов с острым коронарным синдромом без стойкого подъема ST)
Лечение (амбулатория)
Тактика лечения на амбулаторном уровне:
В амбулаторных условиях лечение не проводится.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ.
К основным стратегиям восстановления коронарного кровообращения относятся:
1) механическая реперфузия - чрескожное коронарное вмешательство (ЧКВ) (см. стр 85);
2) фармакологическая реперфузия - догоспитальный и госпитальный тромболизис;
3) фармакоинвазивное лечение - тромболизис с последующей ранней ангиографией и механическим вмешательством, если оно показано.
1) механическая реперфузия - чрескожное коронарное вмешательство (ЧКВ) (см. стр 85);
2) фармакологическая реперфузия - догоспитальный и госпитальный тромболизис;
3) фармакоинвазивное лечение - тромболизис с последующей ранней ангиографией и механическим вмешательством, если оно показано.
Тромболитическая терапия
Троболитическая терапия (ТЛТ) — основной патогенетический метод лечения ИМпST. Тромболитические препараты способны устранить тромб, разрушая фибрин, образующий его основу. С помощью ТЛТ удается восстановить коронарную перфузию у 50–85% больных ИМ. Основной фактор, определяющий эффективность ТЛТ - время начала терапии. Чем раньше начата терапия и, соответственно, восстанавливается коронарный кровоток, тем больше польза от ТЛТ. Если ТЛТ проводят в течение первого часа от начала развития ИМ, эффект максимальный - до 30% ИМ могут быть «прерваны» [4]. По данным многих исследований, ТЛТ эффективна, если ее проводят в течение 12 ч ИМ. Максимально эффективна ТЛТ в первые 2-3 часа от начала симптомов ИМ. С 13 ч до 18 ч польза незначительна и недостоверна (снижение летальности до 1%), после 18 ч смысл в проведении ТЛТ отсутствует полностью [4]. Исключение составляют случаи, когда после 12 ч у больного сохраняется ангинозный приступ или тяжелая сердечная недостаточность. Тогда позднее проведение ТЛТ оправдано [4].
Если тромболитик активирует как свободный, так и связанный с фибрином плазмин, его принято называть фибрин-неспецифичным. Такими были первые тромболитики — стрептокиназа, урокиназа. Следующие поколения тромболитиков преимущественно влияют на плазмин, связанный с фибрином. Их называют фибрин-специфичными. Сегодня для лечения ИМпST в РФ используют тенектеплазу, альтеплазу, проурокиназу, стафилокиназу и стрептокиназу. Последняя является чужеродным белком и потенциально может приводить к аллергическим реакциям. Первые 4 препарата – производные активатора плазминогена тканевого или урокиназного типа. Это модифицированные белкичеловека и их преимущества заключаются в отсутствии антигенных свойств, которые позволяют повторно вводить эти препараты, если в этом возникает необходимость. Фибрин-специфические тромболитики реже вызывают аллергические реакции, при их использовании выше частота реперфузии, поэтому они являются предпочтительными по сравнению с препаратами первого поколения [4]. Основные характеристики тромболитиков и способ их применения представлены в приложении.
Если тромболитик активирует как свободный, так и связанный с фибрином плазмин, его принято называть фибрин-неспецифичным. Такими были первые тромболитики — стрептокиназа, урокиназа. Следующие поколения тромболитиков преимущественно влияют на плазмин, связанный с фибрином. Их называют фибрин-специфичными. Сегодня для лечения ИМпST в РФ используют тенектеплазу, альтеплазу, проурокиназу, стафилокиназу и стрептокиназу. Последняя является чужеродным белком и потенциально может приводить к аллергическим реакциям. Первые 4 препарата – производные активатора плазминогена тканевого или урокиназного типа. Это модифицированные белкичеловека и их преимущества заключаются в отсутствии антигенных свойств, которые позволяют повторно вводить эти препараты, если в этом возникает необходимость. Фибрин-специфические тромболитики реже вызывают аллергические реакции, при их использовании выше частота реперфузии, поэтому они являются предпочтительными по сравнению с препаратами первого поколения [4]. Основные характеристики тромболитиков и способ их применения представлены в приложении.
Показания к назначению тромболитической терапии
ТЛТ показана больным с болевым синдромом или дискомфортом в грудной клетке продолжительностью более 20 мин, не купируемым после приема нитратов или в покое при давности заболевания менее 12 ч и наличии на ЭКГ одного из нижеперечисленных признаков.
-
ЭКГ критериями для начала реперфузионной терапии являются предположительно вновь возникшие стойкие подъемы сегмента ST в точке J в двух смежных отведениях >= 0,1 мВ во всехотведениях, кроме V2-V3, где подъем ST должен быть >=0,2 мВ у мужчин >=40 лет, 0,25 мВ у мужчин <40 лет, или >= 0,15 мВ у женщин.
-
Остро возникшая блокада ЛНПГ (или предположительно остро возникшая), затрудняющая анализ сегмента ST.
-
Депрессия сегмента ST в передних прекардиальных отведениях в сочетании в высоким зубцом R и подъемом сегмента ST в дополнительных прекардиальных отведениях V7–V9.
Противопоказания к тромболитической терапии
Короткая успешная реанимация не является противопоказанием к ТЛТ. Продолжительная или травматичная, но успешная реанимация увеличивает риск геморрагических осложнений и является относительным противопоказанием к тромболизису. В таблице 8 представлены абсолютные и относительные противопоказания к тромболитической терапии.
Таблица 11.
Противопоказания к тромболитической терапии
Противопоказания к тромболитической терапии
|
Абсолютные
|
|
Геморрагический инсульт или инсульт неизвестного происхождения любой давности
|
|
Ишемический инсульт в предыдущие 6 мес.
|
|
Травма или опухоли головного мозга, артериовенозная мальфармация
|
|
Большая травма/операция/травма головы в течение предыдущего месяца
|
|
Желудочно-кишечное кровотечение в течение предыдущего мес.
|
|
Периодические кровотечения (исключая месячные)
|
|
Диссекция аорты
|
|
Некомпрессируемые пункции в течение последних 24 ч (биопсия печени, люмбарная пункция)
|
|
Относительные
|
|
Транзисторная ишемическая атака в течение предыдущих 6 мес.
|
|
Оральная антикоагулянтная терапия
|
|
Беременность или 1 неделя после родов
|
|
Резистентная гипертония (САД ≥180 мм рт.ст. и/или диастолическое АД >110 мм рт.ст.)
|
|
Тяжелое заболевание печени
|
|
Инфекционный эндокардит
|
|
Обострение язвенной болезни
|
|
Продолжительная или травматичная реанимация
|
Осложнения тромболизиса
Тромболитическая терапия в первые сутки сопряжена с риском развития церебрального кровоизлияния. Пожилой возраст, низкий вес, женский пол, цереброваскулярные заболевания в анамнезе и артериальная гипертензия при поступлении являются важными предикторами внутричерепного кровоизлияния. Частотавнутричерепных кровоизлияний составляет 0,9-1,0% [4]. В исследовании STREAM исходный риск внутричерепного кровоизлияния у пациентов старше 75 лет был снижен после коррекции протокола введения тенектеплазы с уменьшением дозы на 50%. Данные ряда исследований свидетельствуют о том, что большие нецеребральные кровотечения имели место у 4-13% пациентов [4]. Чаще всего источник кровотечений — места пункции сосудов, далее следуют желудочно-кишечный тракта и почки. Возможны и забрюшинные кровотечения в паранефральную клетчатку и по ходу подвздошно-поясничной мышцы, особенно при проведении ангиографии доступом через бедренную артерию. Для профилактики кровотечений следует избегать пункции некомпрессируемых артерий, а также не делать внутримышечных инъекций без крайней необходимости. Всем больным с язвенным анамнезом превентивно назначают блокаторы протонного насоса. При появлении признаков тяжелого кровотечения, сопровождаемого большой кровопотерей и нарушениемгемодинамики, необходимо экстренно предпринять ряд мер. Прежде всего, отменяют всю антикоагулянтную, антиагрегантную терапию, прекращают введение тромболитика. Быстро определяют показатели коагулограммы: протромбиновое время, активированное частичное тромбопластиновое время, уровень фибриногена, количество тромбоцитов. В качестве средств, нейтрализующих действие ТЛТ, вводят 10 ЕД криопреципитата, повышающего уровень фибриногена и VIII фактора, а также свежезамороженную плазму в качестве источника V и VIII факторов и плазмозамещающего раствора. Также назначают ингибитор плазминогена аминокапроновую кислоту по следующей схеме: внутривенно капельно 4–5 г, растворенных в 250 мл 0,9% раствора натрия хлорида, в течение часа, затемпри необходимости по 1 г (в 50 мл) каждый час в течение 8 ч или до полной остановки кровотечения. Больным, находящимся на терапии НФГ, дополнительно вводят протамина сульфат из расчета 1 мг на 100 ЕД гепарина [2].
При применении стрептокиназы может возникать гипотония, редко возможны выраженные аллергические реакции, поэтому следует избегать повторного ее использования.
Оценка достижения реперфузии инфаркт связанной артерии (ИСА) [2]
Для точной оценки достижения и степени коронарной реперфузии идеально подходит прямая визуализация - коронарная ангиография (КАГ). Согласно современным рекомендациям, даже после успешной (по косвенным признакам) ТЛТ, в течение 24 ч от начала заболевания проводят КАГ. Поэтому в специализированных центрах есть возможность у большинства больных достоверно судить об эффективности ТЛТ. КАГ позволяет не только констатировать факт реперфузии, но и оценить ее степень. В рамках исследования TIMI-I была разработана ангиографическая классификация степени восстановления коронарного кровотока.
Таблица 13.
Степени коронарного кровотока по критериям TIMI.
Степени коронарного кровотока по критериям TIMI.
|
0-степень. Отсутствие перфузии.
1-степень. Минимальная коронарная перфузия. Контраст проходит дистальнее места обструкции, однако дальше не поступает. Заполнение дистального русла отсутствует. Отсутствие антеградного поступления. 2-степень. Неполная коронарная перфузия. Полное контрастирование коронарной артерии дистальнее места обструкции. Однако отмечают задержку заполнения дистального русла и/или замедление пассажа контрастного вещества дистальнее зоны поражения (в сравнении с кровотоком в неизмененной артерии). 3-степень. Нормальная коронарная перфузия. Антеградный кровоток и вымывание контраста дистальнее места обструкции не отличаются от таковых в непораженном сосуде. При 0–1 степени коронарной перфузии тромболизис считают неудавшимся. 2–3 степени реперфузии говорят об успешном тромболизисе. |
Наблюдения показали, что ТЛТ успешна у 60–85% больных, идеальная реперфузия (3 степень по TIMI) — от 50 до 60% больных. Существует четкая прямая зависимость между степенью восстановления перфузии и прогнозом у больных ИМ.
О наличии реперфузии свидетельствует снижение сегмента ST >50% от исходного в отведении, где его подъем был максимальным, через 60-90 мин от начала ТЛТ. В таких случаях вероятность полного восстановления кровотока (TIMI 3) достигает 80%. Именно эти ЭКГ-критерии положены в основу определения тактики лечения больных с ОКСпST. Если через 60-90 мин отсутствуют критерии реперфузии, показана экстренная КАГ и реваскуляризация.
Таблица 14
[2, https://cardio-eur.asia/media/files/clinical_recommendations/Eurasian_clinical_guidelines_for_the_diagnosis_and_treatment_of_acute_coronary_syndrome_with_ST_segment_elevation_(ACSpST)_rus_2019.pdf]
[2, https://cardio-eur.asia/media/files/clinical_recommendations/Eurasian_clinical_guidelines_for_the_diagnosis_and_treatment_of_acute_coronary_syndrome_with_ST_segment_elevation_(ACSpST)_rus_2019.pdf]
|
Рекомендации
|
Класс
|
Уровень
|
|
ТЛТ проводится в первые 12ч от начала ИМ при невозможности выполнить пЧКВ в течение 120 мин от постановки диагноза ИМпST.
|
I
|
A
|
|
ТЛТ проводится с 12 до 24ч от начала ИМ при сохраняющейся ишемии, большой зоне поражения миокарда, гемодинамической нестабильности.
|
IIa
|
B
|
|
Если выбрана стратегия реперфузии с помощью ТЛТ, ее следует проводить незамедлительно, лучше на догоспитальном этапе
|
I
|
A
|
|
Предпочтительными являются фибрин- специфические тромболитики (альтеплаза, тенектеплаза, проурокиназа, стафилокиназа)
|
I
|
A
|
Феномен «NO-REFLOW»
Под феноменом no-reflow (в переводе с английского дословно: «нет восстановления кровотока») понимают отсутствие клинических и инструментальных признаков коронарной реперфузии, несмотря на восстановление проходимости артерии в области окклюзированной АСБ. На основании ангиографических данных можно выделить два варианта no-reflow. В первом случае наблюдают полное восстановление кровотока (TIMI- 3). Чаще наблюдают второй вариант: кровоток по инфаркт-связанной артерии неудовлетворительный (TIMI-1–2). Нарушение кровотока на уровне мелких артерий можно зафиксировать с помощью контрастной ЭхоКГ и контрастной КТ или МРТ, изотопных методов. Косвенными признаками no-reflow являются сохранение ангинозного приступа и отсутствие или минимальное снижение сегмента ST на ЭКГ. В основе no-reflow лежат разные механизмы: дистальная эмболизация фрагментами тромба и атероматозными массами, дисфункция, тромбоз и повреждение мелких артерий, вазоконстрикция на уровне мелких артерий, реперфузионное повреждение миокарда и т.д. Частота выявления феномена no-reflow варьирует в зависимости от диагностических критериев. 4% до 12–25%.Изучались различные лечебные подходы, уменьшающие проявления феномена no-reflow, но они оказались неэффективными.
Реперфузионное повреждение миокарда
Реперфузионное повреждение (РП) - патологический процесс, возникающий при восстановлении кровотока в ишемизированном миокарде, приводящий к миокардиальной, электрофизиологической и сосудистой дисфункции. Клиническими проявлениями реперфузионного повреждения могут быть:
-
реперфузионные аритмии;
-
систолическая дисфункция;
-
расширение зоны инфаркта вследствие гибели кардиомиоцитов.
Основываясь на механизмах РП, проводились попытки терапевтической защиты сердца. Для этой цели пытались использовать аденозин, глюкозо-инсулино-калиевую смесь, доноры оксида азота, ингибиторы эндотелина, ингибиторы Na+, K+-АТФазы, блокаторы системы комплемента и т.д. Существенного влияния на РП эта терапия не оказала.
Лечение.
Лекарственная терапия.
Лекарственная терапия.
Кислородотерапия. Обезболивание. Седация.
Кислородотерапия не только не приносит пользы больным с неосложненным ИМ, но даже может быть вредной, что предположительно обусловлено увеличением повреждения миокарда. Кислородотерапия показана больным с гипоксемией (SaO2 <90% или PaO2 <60 мм.рт.ст.). Дыхание кислородом проводят через носовые катетеры со скоростью 2-8 л/мин. Контролируют насыщение крови кислородом с помощью измерения сатурации.
Быстрое и полное устранение болевого синдрома, важно не только с точки зрения комфорта пациента, но и для снижения симпатической активности, приводящей к тахикардии и повышению АД. Отличительная особенность ангинозного приступа при ИМ слабая реакция или отсутствие реакции на нитроглицерин. Тем не менее, если ангинозный приступ не ослабевает через несколько минут после прекращения действия провоцирующего фактора (физическая нагрузка) или если он развился в покое, больному следует принять нитроглицерин в дозе 0,4-0,5 мг в виде таблеток под язык или аэрозоля (спрея). Если симптомы не исчезают через 5 мин, а препарат удовлетворительно переносится, можно использовать его повторно. В связи с опасностью гипотонии постоянно контролируют АД. Если боль в или дискомфорт грудной клетке сохраняются в течение 5 мин после повторного приема нитроглицерина, необходимо немедленно вызвать СМП. Если 2–3 приема нитроглицерина не уменьшают интенсивность приступа, дальнейший прием не имеет смысла. При наличии выраженного болевого синдрома основным препаратом для обезболивания является морфин [4] Помимо обезболивания морфин способствует уменьшению страха, возбуждения, снижает симпатическую активность, увеличивает тонус блуждающего нерва, уменьшает работу дыхания, вызывает расширение периферических артерий и вен (последнее особенно важно при отеке легких). Доза, необходимая для адекватного обезболивания, зависит от индивидуальной чувствительности, возраста, размеров тела. Перед использованием 10 мг морфина гидрохлорида или сульфата разводят как минимум в 10 мл 0,9% раствора хлорида натрия или дистиллированной воды. Первоначально следует ввести в/в медленно 2-4 мг лекарственного вещества. При необходимости введение повторяют каждые 5-15 мин по 2- мг до купирования боли или возникновения побочных эффектов, не позволяющих увеличить дозу. Назначение морфина приводит к замедлению начала действия антиагрегантов (клопидогрел, тикагрелор, прасугрел), что может отразиться на результатах лечения у некоторых пациентов [4].
При использовании морфина возможны следующие осложнения:
Кислородотерапия не только не приносит пользы больным с неосложненным ИМ, но даже может быть вредной, что предположительно обусловлено увеличением повреждения миокарда. Кислородотерапия показана больным с гипоксемией (SaO2 <90% или PaO2 <60 мм.рт.ст.). Дыхание кислородом проводят через носовые катетеры со скоростью 2-8 л/мин. Контролируют насыщение крови кислородом с помощью измерения сатурации.
Быстрое и полное устранение болевого синдрома, важно не только с точки зрения комфорта пациента, но и для снижения симпатической активности, приводящей к тахикардии и повышению АД. Отличительная особенность ангинозного приступа при ИМ слабая реакция или отсутствие реакции на нитроглицерин. Тем не менее, если ангинозный приступ не ослабевает через несколько минут после прекращения действия провоцирующего фактора (физическая нагрузка) или если он развился в покое, больному следует принять нитроглицерин в дозе 0,4-0,5 мг в виде таблеток под язык или аэрозоля (спрея). Если симптомы не исчезают через 5 мин, а препарат удовлетворительно переносится, можно использовать его повторно. В связи с опасностью гипотонии постоянно контролируют АД. Если боль в или дискомфорт грудной клетке сохраняются в течение 5 мин после повторного приема нитроглицерина, необходимо немедленно вызвать СМП. Если 2–3 приема нитроглицерина не уменьшают интенсивность приступа, дальнейший прием не имеет смысла. При наличии выраженного болевого синдрома основным препаратом для обезболивания является морфин [4] Помимо обезболивания морфин способствует уменьшению страха, возбуждения, снижает симпатическую активность, увеличивает тонус блуждающего нерва, уменьшает работу дыхания, вызывает расширение периферических артерий и вен (последнее особенно важно при отеке легких). Доза, необходимая для адекватного обезболивания, зависит от индивидуальной чувствительности, возраста, размеров тела. Перед использованием 10 мг морфина гидрохлорида или сульфата разводят как минимум в 10 мл 0,9% раствора хлорида натрия или дистиллированной воды. Первоначально следует ввести в/в медленно 2-4 мг лекарственного вещества. При необходимости введение повторяют каждые 5-15 мин по 2- мг до купирования боли или возникновения побочных эффектов, не позволяющих увеличить дозу. Назначение морфина приводит к замедлению начала действия антиагрегантов (клопидогрел, тикагрелор, прасугрел), что может отразиться на результатах лечения у некоторых пациентов [4].
При использовании морфина возможны следующие осложнения:
-
выраженная артериальная гипотензия; устраняется в горизонтальном положении в сочетании с поднятием ног (если нет отека легких). Если этого недостаточно, в/в вводится 0,9% раствор хлорида натрия. В редких случаях – прессорные препараты;
-
выраженная брадикардия в сочетании с артериальной гипотензией; устраняется атропином (в/в 0,5-1,0 мг);
-
тошнота, рвота; устраняется производными фенотиазина, в частности, метоклопрамидом (в/в 5-10 мг);
-
выраженное угнетение дыхания; устраняется налоксоном (в/в 0,1-0,2 мг, при необходимости повторно каждые 15 мин), однако при этом уменьшается и анальгезирующее действие препарата.
Опиаты могут ослаблять перистальтику кишечника и приводить к запорам. Препараты этой группы снижают тонус мочевого пузыря и затрудняют мочевыведение, особенно у мужчин с гипертрофией предстательной железы.
Для уменьшения страха обычно достаточно создать спокойную обстановку и ввести наркотический анальгетик. При выраженном возбуждении могут потребоваться транквилизаторы (например, диазепам в/в 2,5-10 мг). Важное значение для эмоционального комфорта больного имеет соответствующий стиль поведения персонала, разъяснение диагноза, прогноза и плана лечения. У больных с сохраняющимся беспокойством и нарушенным поведением, а также симптомами отмены при никотиновой зависимости также можно назначить транквилизаторы. При возбуждении и делирии достаточно эффективно и безопасно в/в введение галоперидола.
Таблица 15.
Кислородотерапии, обезболиванию, седация.
|
Рекомендации
|
Класс
|
Уровень
|
Источник
|
|
Кислородотерапия показана больным с гипоксемией (SaO2<90% или PaO2 <60 мм.рт.ст.)
|
I
|
С
|
4
https://car diocenter. uz/docs |
|
Кислородотерапия не показана больным со с уровнем сатурации > 90%
|
III
|
B
|
4
https://car diocenter. uz/docs |
|
При наличии выраженного болевого синдрома основным препаратом для обезболивания является морфин
|
I
|
С
|
4
https://car diocenter. uz/docs |
|
При наличии признаков выраженного беспокойства и возбуждения рекомендуется назначение транквилизаторов
|
IIa
|
C
|
4
https://car diocenter. uz/docs |
Антитромботическая терапия
1) Характеристика антитромботических препаратов антитромбоцитарные препараты (антиагреганты)
Тромбоциты играют ключевую роль в инициации и нарастании коронарного тромбоза. Поэтому лекарства, подавляющие функцию тромбоцитов, т.н. антиагреганты или антитромбоцитарные препараты являются важнейшей составляющей в патогенетической терапии ОКС. Антитромбоцитарные препараты эффективны в отношении ишемических событий как в остром периоде, так и при вторичной профилактике атеротромботических эпизодов. По меньшей мере три класса антиагрегантов доказали свою эффективность у больных ОКС (рис. 7). К ним относятся ацетилсалициловая кислота (АСК), ингибиторы Р2Y12 рецепторов тромбоцитов и блокаторы гликопротеиновых рецепторов IIb/IIIa. Следует упомянуть о новом классе антиагрегантов, пока еще не нашедших широкого клинического применения, – ингибиторах PAR-рецепторов тромбоцитов. Механизм действия этих препаратов связан с подавлением активации тромбоцитов, вызванной тромбином. Реальная клиническая значимость ингибиторов PAR-рецепторов пока не ясна. (Рис. 7)
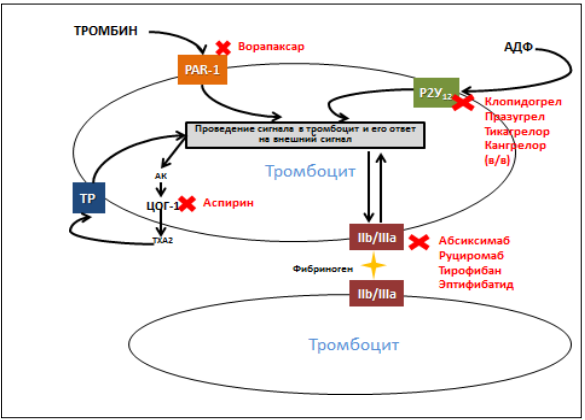
Рисунок 7. Механизмы действия антитромбоцитарных препаратов
АК – арахидоновая кислота; PAR-1 – рецептор, активируемый протеазами 1 типа; ТР – рецептор ктромбоксану; Р2Y12 – рецептор к АДФ (аденозиндифосфату); IIb/IIIa – гликопротеиновые рецепторы IIb/IIIa
2) Ацетилсалициловая кислота (АСК)
Необратимо ингибирует циклооксигеназу 1 типа, что приводит к уменьшению синтеза тромбоксана А2 в тромбоцитах, уменьшение его образования в свою очередь снижает активацию тромбоцитов (рис. 7). АСК необратимо действует на тромбоциты, поэтому ее эффект сохраняется на протяжении всего периода жизни этих клеток (около 7 дней).Эффективность АСК у больных ИМ, подвергшихся ТЛТ, подтверждена на основании результатов исследования ISIS-2 в 1988 г. [4]. У больных, принимавших АСК в дозе 160 мг/сут и получивших ТЛТ стрептокиназой, риск летального исхода снизился на 23%. Польза от назначения АСК в комбинации ингибиторами P2Y12 рецепторов тромбоцитов по сравнению с монотерапией ингибиторами P2Y12 рецепторов тромбоцитов не доказана. Проводятся исследования. На сегодняшний день рекомендовано назначать АСК при отсутствии противопоказаний всем больным ОКСпSTнезависимо от тактики лечения (первичная ЧКВ, ТЛТ или отсутствие реперфузионной терапии) [95]. При отсутствии регулярного приема АСК в предшествующие несколько суток начальная доза составляет 150 – 300 мг действующего вещества (для ускорения всасывания таблетку предпочтительно, разжевать). Стартовой терапии АСК с использованием покрытых и кишечнорастворимых форм следует избегать. При невозможности перорального приема допускается в/в путь введения препарата. Оптимальная нагрузочная доза точно не установлена, по-видимому, достаточно болюсного введения 75 – 150 мг (эти дозы эквивалентны 150 – 300 мг per os).
3) Ингибиторы P2Y12 рецепторов тромбоцитов
К этому классу препаратов относятся обратимые и необратимые блокаторы рецепторов тромбоцитов к АДФ. Среди них известны три производных тиенопиридина (не используемый в настоящее время тиклопидин, клопидогрел и прасугрел). Все они являются пролекарствами и должны пройти превращение в печени с помощью изоферментов цитохрома Р450 до образования коротко живущих активных метаболитов, которые необратимо модифицируют АДФ рецептор тромбоцитов. Тромбоциты, подвергнутые действию тиенопиридинов (также, как и действию АСК), не могут восстановить свою функцию на протяжении всего периода жизни (около 7 дней). Тикагрелор и кангрелор являются прямыми, обратимыми блокаторами Р2Y12 рецепторов, им не требуется метаболическая активация, а их антитромбоцитарный эффект напрямую зависит от присутствия препарата в кровотоке.
Клопидогрел
Клопидогрел (нагрузочная доза 300–600 мг, поддерживающая – 75 мг) является тиенопиридином второго поколения и представляет собой неактивное пролекарство, которое превращается в печени с помощью изоферментов цитохрома Р450 в активный метаболит. Установлено, что до 85% пролекарства гидролизуется эстеразами в неактивную форму, а оставшиеся 15% превращаются в активный метаболит, который селективно и необратимо инактивирует Р2Y12 рецептор и тем самым ингибирует АДФ-вызванную агрегацию тромбоцитов. Фармакодинамические и фармакокинетические исследования обнаружили межиндивидуальные различия в реакции на клопидогрел, связанные, прежде всего, с генетически детерминированной скоростью образования активного метаболита. Имеются доказательства того, что снижение чувствительности к клопидогрелу, определенное с помощью генотипирования или оценки остаточной реактивности тромбоцитов, может ассоциироваться с увеличением риска ишемических событий, главным образом - тромбозов стента после неотложных ЧКВ [4].
В исследовании CLARITY-TIMI 28 [4], включившем 3491 больных ИМ моложе 75 лет, подвергнутых тромботической терапии, кратковременное добавление клопидогрела (нагрузочная доза 300 мг, затем 75 мг/сут до 8 дней или до выписки из стационара), к аспирину снижало суммарную частоту случаев окклюзий инфаркт-связанной артерии, смертей и повторных ИМ на 36%. В крупном исследовании COMMIT (n= 45,852) [4] включение клопидогрела в схему консервативного лечения ИМ на срок до 4 недель снижало суммарную частоту ишемических исходов на 9%. Клопидогрел не изучался в сравнении с плацебо у больных, подвергаемых первичной ЧКВ. Известно, однако, что при неотложных вмешательствах более высокие дозы клопидогрела (нагрузочная 600 мг / поддерживающая 150 мг в течение недели) ассоциируются с меньшей частотой ишемических событий в сравнении с режимом приема препарата 300 мг / 75 мг в сут [4].
В исследовании CLARITY-TIMI 28 [4], включившем 3491 больных ИМ моложе 75 лет, подвергнутых тромботической терапии, кратковременное добавление клопидогрела (нагрузочная доза 300 мг, затем 75 мг/сут до 8 дней или до выписки из стационара), к аспирину снижало суммарную частоту случаев окклюзий инфаркт-связанной артерии, смертей и повторных ИМ на 36%. В крупном исследовании COMMIT (n= 45,852) [4] включение клопидогрела в схему консервативного лечения ИМ на срок до 4 недель снижало суммарную частоту ишемических исходов на 9%. Клопидогрел не изучался в сравнении с плацебо у больных, подвергаемых первичной ЧКВ. Известно, однако, что при неотложных вмешательствах более высокие дозы клопидогрела (нагрузочная 600 мг / поддерживающая 150 мг в течение недели) ассоциируются с меньшей частотой ишемических событий в сравнении с режимом приема препарата 300 мг / 75 мг в сут [4].
Прасугрел.
Прасугрел представляет собой тиенопиридин третьего поколения, который также, как клопидогрел необратимо блокирует Р2Y12 рецепторы тромбоцитов и является пролекарством, но с более быстрым превращением в печени, что обеспечивает более быстрый и сильный антитромбоцитарный эффект. В исследовании TRITON-TIMI 38 [4] прасугрел (насыщающая доза 60мг, поддерживающая – 10мг) сравнивался с клопидогрелом (300мг / 75мг) у больных ОКС, подвергаемых неотложным ЧКВ. Продолжительность лечения в сравниваемых группах составила 15 месяцев. Прасугрел продемонстрировал преимущество перед клопидогрелом в отношении суммарной частоты ишемических событий (сосудистая смерть, нефатальный ИМ и инсульт) - 9,3% и 11,2%, в основном за счет меньшей частоты ИМ. Однако, частота крупных, жизненно-опасных и смертельных кровотечений оказалась существенно выше. В целом, соотношение частоты ишемических событий и кровотечений оказалось в пользу прасугрела для большинства больных за исключением лиц старше 75 лет, с массой тела ниже 60 кг, а также перенесших инсульт или транзиторную ишемическую атаку. Для последней категории больных риск кровотечений оказался неприемлемо высоким, в связи с чем использование препарата у них не рекомендовано.
Тикагрелор
Тикагрелор – пероральный обратимый ингибитор Р2Y12 рецепторов тромбоцитов с периодом полувыведения в плазме до 12 часов. Помимо вышеописанного механизма тикагрелор ингибирует обратный захват аденозина клетками.
В исследовании PLATO [4] тикагрелор сравнивался с клопидогрелом у больных ОКС. В исследование вошли больные ОКСбпST средне-высокого риска, которые могли лечиться как инвазивно, так и консервативно, а также больные ОКСпST, подвергаемые первичной ЧКВ. Предшествующий прием клопидогрела не являлся критерием исключения. Насыщающие и поддерживающие дозы тикагрелора и клопидогрела составляли соответственно 180 мг /90 мг 2 раза в сутки и 300мг / 75мг 1 раз в сутки. Кроме того, при выполнении ЧКВ в группе клопидогрела допускался дополнительный прием 300 мг препарата до общей насыщающей дозы 600 мг. Медиана наблюдения составила 9 месяцев. Суммарная частота сосудистой смерти, ИМ и инсульта была ниже на фоне приема тикагрелора в сравнении с клопидогрелом: 9,8% и 11,7%. Было также обнаружено снижение случаев смерти от любых причин: 4,0% и 5,1%. Преимущества тикагрелора перед клопидогрелом сохранялись вне зависимости от исходного диагноза и стратегии лечения.
Крупных, не связанных с операцией коронарного шунтирования (КШ) кровотечений, оказалось больше в группе тикагрелора, чем в группе клопидогрела (4,5% и 3,8%), но разницы в частоте угрожающих жизни и фатальных кровотечений в сравниваемых группах не было. Помимо увеличения частоты не связанных с КШ кровотечений в группе тикагрелора чаще отмечались следующие побочные эффекты: одышка (без признаков бронхоспазма), брадикардия и повышение уровня мочевой кислоты и креатинина.
4) Ингибиторы гликопротеиновых рецепторов IIB/IIIA
Блокируют ключевой механизм агрегации тромбоцитов, а именно склеивание посредством связывания молекул фибриногена с активированными IIb/IIIa рецепторами тромбоцитов. Ингибиторы IIb/IIIa рецепторов преимущественно были изучены до появления клопидогрела, тикагрелора и широкого использования ЧКВ.В настоящее время на фоне стандартной ДАТТ дополнительное введение этих препаратов обычно не показано (как на догоспитальном этапе, так и во время ЧКВ) в связи с отсутствием явной пользы и увеличением риска кровотечений. Факторами, способствующими передозировке препаратов, являются пожилой возраст, женский пол, почечная недостаточность, малая масса тела, сахарный диабет и ХСН. Следует помнить, что применение ингибиторов IIb/IIIa рецепторов может вызывать тромбоцитопению. Блокаторы гликопротеина IIb/IIIa рецепторов тромбоцитов используются, в основном, как спасительное средство при тромботических осложнениях ЧКВ, либо высоком риске их развития (массивный тромб, феномен no-reflow и т.п.). Интракоронарное введение данных лекарств не имеет преимуществ перед внутривенным. Из препаратов этой группы используют абциксимаб, эптифибатид, тирофибан, и Российский препарат монофрам.
В исследовании PLATO [4] тикагрелор сравнивался с клопидогрелом у больных ОКС. В исследование вошли больные ОКСбпST средне-высокого риска, которые могли лечиться как инвазивно, так и консервативно, а также больные ОКСпST, подвергаемые первичной ЧКВ. Предшествующий прием клопидогрела не являлся критерием исключения. Насыщающие и поддерживающие дозы тикагрелора и клопидогрела составляли соответственно 180 мг /90 мг 2 раза в сутки и 300мг / 75мг 1 раз в сутки. Кроме того, при выполнении ЧКВ в группе клопидогрела допускался дополнительный прием 300 мг препарата до общей насыщающей дозы 600 мг. Медиана наблюдения составила 9 месяцев. Суммарная частота сосудистой смерти, ИМ и инсульта была ниже на фоне приема тикагрелора в сравнении с клопидогрелом: 9,8% и 11,7%. Было также обнаружено снижение случаев смерти от любых причин: 4,0% и 5,1%. Преимущества тикагрелора перед клопидогрелом сохранялись вне зависимости от исходного диагноза и стратегии лечения.
Крупных, не связанных с операцией коронарного шунтирования (КШ) кровотечений, оказалось больше в группе тикагрелора, чем в группе клопидогрела (4,5% и 3,8%), но разницы в частоте угрожающих жизни и фатальных кровотечений в сравниваемых группах не было. Помимо увеличения частоты не связанных с КШ кровотечений в группе тикагрелора чаще отмечались следующие побочные эффекты: одышка (без признаков бронхоспазма), брадикардия и повышение уровня мочевой кислоты и креатинина.
4) Ингибиторы гликопротеиновых рецепторов IIB/IIIA
Блокируют ключевой механизм агрегации тромбоцитов, а именно склеивание посредством связывания молекул фибриногена с активированными IIb/IIIa рецепторами тромбоцитов. Ингибиторы IIb/IIIa рецепторов преимущественно были изучены до появления клопидогрела, тикагрелора и широкого использования ЧКВ.В настоящее время на фоне стандартной ДАТТ дополнительное введение этих препаратов обычно не показано (как на догоспитальном этапе, так и во время ЧКВ) в связи с отсутствием явной пользы и увеличением риска кровотечений. Факторами, способствующими передозировке препаратов, являются пожилой возраст, женский пол, почечная недостаточность, малая масса тела, сахарный диабет и ХСН. Следует помнить, что применение ингибиторов IIb/IIIa рецепторов может вызывать тромбоцитопению. Блокаторы гликопротеина IIb/IIIa рецепторов тромбоцитов используются, в основном, как спасительное средство при тромботических осложнениях ЧКВ, либо высоком риске их развития (массивный тромб, феномен no-reflow и т.п.). Интракоронарное введение данных лекарств не имеет преимуществ перед внутривенным. Из препаратов этой группы используют абциксимаб, эптифибатид, тирофибан, и Российский препарат монофрам.
5) Антикоагулянтные препараты (антитромбины)
Задача антикоагулянтов в остром периоде ОКС подавить образование или активность ключевого фермента свертывания крови – тромбина и тем самым снизить риск тромботических осложнений. В настоящее время несколько антикоагулянтов для парентерального введения показали свою пользу у больных с ОКСпST (нефракционированный гепарин, эноксапарин, фондапаринукс и бивалирудин, (рис. 8).
Рисунок 8. Современные антикоагулянты
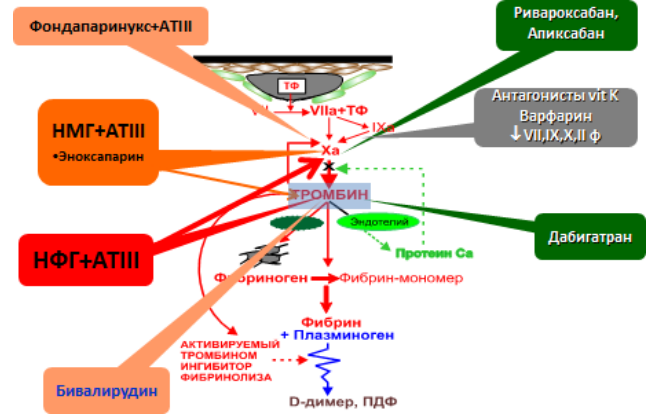
Сокращения: НФГ – нефракционированный гепарин, НМГ – низкомолекулярный гепарин, АТIII– антитромбин III, ПДФ – продукты деградации фибриногена и фибрина, ТФ – тканевой фактор, VII– VII фактор свертывания крови, IX– IX фактор свертывания крови, X– X фактор свертывания крови, II– II фактор свертывания крови (протромбин).
Евразийские клинические рекомендации по диагностике и лечению острого коронарного синдрома с подъемом сегмента ST.
Евразийские клинические рекомендации по диагностике и лечению острого коронарного синдрома с подъемом сегмента ST.
Парентеральные антикоагулянты
1) Нефракционированный гепарин (НФГ)
НФГ представляет собой гетерогенную смесь полисахаридов. Для осуществления антикоагулянтной активности НФГ в плазме крови необходим кофактор – антитромбинIII (АТIII). Связывание молекулы НФГ с АТIII приводит к конформационным изменениям антитромбина, и он превращается в быстродействующий ингибитор. При ОКСпST нефракционированный гепарин применяется для сопровождения реперфузионной терапии (ЧКВ или ТЛТ), а также для профилактики или лечения артериальных или венозных тромбозов и тромбоэмболий. Узкое терапевтическое окно НФГ предполагает внутривенный режим введения и индивидуальный подбор дозы в соответствии с весом пациента (подкожное введение рекомендуется только с целью профилактики венозных тромбозов).
Для поддержки первичной ЧКВ НФГ используют в виде внутривенных болюсных введений: первый болюс 70—100 ЕД/кг (50 - 70 МЕ/кг в сочетании с блокаторами гликопротеина IIb/IIIa), при необходимости введение НФГ повторяют в дозе 20 МЕ/кг. Возможен подбор дозы / мониторирование антикоагулятного действия НФГ путем определения активированного времени свертывания (АВС). Диапазон значений АВС составляет 250—350 с (200 – 250 в сочетании с блокаторами гликопротеина IIb/IIIa). Строгой доказательной базы в пользу такого подхода нет. В любом случае, определение АВС не должно задерживать выполнение реканализации инфаркт-связанной артерии при первичной ЧКВ. Для сопровождения ТЛТ НФГ вводится болюсом 60 ЕД/кг (максимально 4000 ЕД), затем сразу начинают инфузию со скоростью 12 ЕД/кг/ч (максимально 1000 ЕД/ч); в последующем подбор дозы осуществляют под контролем АЧТВ (увеличение до 50—70 с или в 1,5—2 раза выше контрольной величины для конкретной лаборатории), которое следует определять через 3, 6, 12 и 24 ч. [2]
НФГ представляет собой гетерогенную смесь полисахаридов. Для осуществления антикоагулянтной активности НФГ в плазме крови необходим кофактор – антитромбинIII (АТIII). Связывание молекулы НФГ с АТIII приводит к конформационным изменениям антитромбина, и он превращается в быстродействующий ингибитор. При ОКСпST нефракционированный гепарин применяется для сопровождения реперфузионной терапии (ЧКВ или ТЛТ), а также для профилактики или лечения артериальных или венозных тромбозов и тромбоэмболий. Узкое терапевтическое окно НФГ предполагает внутривенный режим введения и индивидуальный подбор дозы в соответствии с весом пациента (подкожное введение рекомендуется только с целью профилактики венозных тромбозов).
Для поддержки первичной ЧКВ НФГ используют в виде внутривенных болюсных введений: первый болюс 70—100 ЕД/кг (50 - 70 МЕ/кг в сочетании с блокаторами гликопротеина IIb/IIIa), при необходимости введение НФГ повторяют в дозе 20 МЕ/кг. Возможен подбор дозы / мониторирование антикоагулятного действия НФГ путем определения активированного времени свертывания (АВС). Диапазон значений АВС составляет 250—350 с (200 – 250 в сочетании с блокаторами гликопротеина IIb/IIIa). Строгой доказательной базы в пользу такого подхода нет. В любом случае, определение АВС не должно задерживать выполнение реканализации инфаркт-связанной артерии при первичной ЧКВ. Для сопровождения ТЛТ НФГ вводится болюсом 60 ЕД/кг (максимально 4000 ЕД), затем сразу начинают инфузию со скоростью 12 ЕД/кг/ч (максимально 1000 ЕД/ч); в последующем подбор дозы осуществляют под контролем АЧТВ (увеличение до 50—70 с или в 1,5—2 раза выше контрольной величины для конкретной лаборатории), которое следует определять через 3, 6, 12 и 24 ч. [2]
2) Низкомолекулярные гепарины (НМГ)
НМГ являются фрагментами нефракционированного гепарина, которые имеют ряд преимуществ перед НФГ: более быструю абсорбцию при подкожном введении, меньшую степень связывания с белками плазмы и тромбоцитами и поэтому обладают более предсказуемым дозозависимым действием. Они реже, чем НФГ вызывают гепарин- индуцированную тромбоцитопению (ГИТ). Важное преимущество НМГ перед НФГ — простота введения и отсутствие необходимости в регулярном коагулологическом контроле при использовании как профилактических, так и высоких (лечебных) доз.
Эноксапарин является единственным НМГ, рекомендованным для лечения больных ОКСпST. Эноксапарин, как и НФГ, может использоваться во время первичной ЧКВ, при введении тромболитика, а также для профилактики или лечения артериальных или венозных тромбозов и тромбоэмболий.
При ЧКВ у больных, до этого не получавших антикоагулянтов, эноксапарин вводят внутривенно болюсом 0,5 мг/кг вне зависимости от сопутствующего использования блокаторов гликопротеина IIb/IIIa и функции почек. Если ЧКВ выполняется на фоне предшествующей терапии эноксапарином, то в первые 8 часов после очередной п/к инъекции дополнительного антикоагулянта не требуется. Если до ЧКВ была сделана только одна подкожная инъекция эноксапарина или ЧКВ выполняется через 8-12 часов после подкожной инъекции – ввести внутривенно болюсом 0,3 мг/кг эноксапарина. [2]
При сопровождении тромболитической терапии эноксапарин назначается в дозе 30 мг в/в струйно; через 15 мин в дозе 1 мг/кг под кожу живота 2 раза в сутки (первые 2 дозы для п/к введения не должны превышать 100 мг). У лиц в возрасте 75 лет и старше первоначальная доза в/в не вводится, а поддерживающая уменьшается до 0,75 мг/кг (первые две подкожные дозы не должны превышать 75 мг).
Лечебные дозы эноксапарина (1 мг/кг под кожу живота 2 раза в сутки) применяют для профилактики кардиоэмболических осложнений и лечения артериальных тромбозов и эмболий. Для профилактики венозных тромбозов и эмболий рекомендованная доза эноксапарина составляет 40 мг 1 раз в сут [2]
Эноксапарин, как и другие НМГ, имеет почечный путь выведения из организма, поэтому у пациентов с клиренсом креатинина в пределах 15–30 мл/мин/1,73м2 требуется уменьшение лечебной дозы (1 мг/кг п/к 1 раз в сутки вне зависимости от возраста). Желательно при этом обеспечить мониторирование анти-Ха активности. Эноксапарин не рекомендуется больным с клиренсом креатинина <15 мл/мин/1,73 м2.
Эноксапарин является единственным НМГ, рекомендованным для лечения больных ОКСпST. Эноксапарин, как и НФГ, может использоваться во время первичной ЧКВ, при введении тромболитика, а также для профилактики или лечения артериальных или венозных тромбозов и тромбоэмболий.
При ЧКВ у больных, до этого не получавших антикоагулянтов, эноксапарин вводят внутривенно болюсом 0,5 мг/кг вне зависимости от сопутствующего использования блокаторов гликопротеина IIb/IIIa и функции почек. Если ЧКВ выполняется на фоне предшествующей терапии эноксапарином, то в первые 8 часов после очередной п/к инъекции дополнительного антикоагулянта не требуется. Если до ЧКВ была сделана только одна подкожная инъекция эноксапарина или ЧКВ выполняется через 8-12 часов после подкожной инъекции – ввести внутривенно болюсом 0,3 мг/кг эноксапарина. [2]
При сопровождении тромболитической терапии эноксапарин назначается в дозе 30 мг в/в струйно; через 15 мин в дозе 1 мг/кг под кожу живота 2 раза в сутки (первые 2 дозы для п/к введения не должны превышать 100 мг). У лиц в возрасте 75 лет и старше первоначальная доза в/в не вводится, а поддерживающая уменьшается до 0,75 мг/кг (первые две подкожные дозы не должны превышать 75 мг).
Лечебные дозы эноксапарина (1 мг/кг под кожу живота 2 раза в сутки) применяют для профилактики кардиоэмболических осложнений и лечения артериальных тромбозов и эмболий. Для профилактики венозных тромбозов и эмболий рекомендованная доза эноксапарина составляет 40 мг 1 раз в сут [2]
Эноксапарин, как и другие НМГ, имеет почечный путь выведения из организма, поэтому у пациентов с клиренсом креатинина в пределах 15–30 мл/мин/1,73м2 требуется уменьшение лечебной дозы (1 мг/кг п/к 1 раз в сутки вне зависимости от возраста). Желательно при этом обеспечить мониторирование анти-Ха активности. Эноксапарин не рекомендуется больным с клиренсом креатинина <15 мл/мин/1,73 м2.
Бивалирудин
Препарат представляет собой полусинтетический полипептид, состоящий из 20 аминокислот. Биливарудин в равной степени связывает свободный и связанный с тромбом тромбин, не инактивируется 4 фактором тромбоцитов и не нуждается в кофакторе - антитромбине. Бивалирудин обладает предсказуемой линейной фармакокинетикой и достигает пиковой концентрации после внутривенного болюса через 5 минут. Во время инфузии создается устойчивая концентрация, напрямую зависящая от дозы. Препарат быстро выводится из плазмы. Антикоагулянтный эффект зависит от дозы, показатели АЧТВ, тромбиновое время, АВС линейно нарастают с увеличением дозы, эффект проявляется через минуты после внутривенного болюса и у здоровых лиц прекращается примерно через 1 час после прекращения инфузии.
Бивалирудин применяется для сопровождения первичного ЧКВ. Предполагалось, что важное преимущество бивалирудина – уменьшение наклонности к кровотечениям, особенно при инвазивной тактике лечения. Данные о большей безопасности бивалирудина были получены в первую очередь при сравнении его с комбинацией НФГ и блокаторов гликопротеина IIb/IIIa. В исследованиях последних лет использовались современные блокаторы P2Y12 рецепторов и «спасительное» введение блокаторов гликопротеина IIb/IIIa, поэтому целесообразность использования бивалирудина вместо НФГ подвергается сомнению. Соответственно, при гепарин-индуцированной тромбоцитопении бивалирудин является препаратом первого выбора. [2]
Бивалирудин вводится в дозе 0,75 мг/кг в/в струйно с последующей инфузией со скоростью 1,75 мг/кг/ч. Выводится преимущественно почками и не рекомендован при клиренсе креатинина <30 мл/мин/1,73 м2. У больных с клиренсом креатинина 30—59 мл/мин доза для струйного введения остается прежней, а скорость инфузии следует уменьшить до 1,4 мг/кг/ч.
3) Пероральные антикоагулянты для длительного лечения больных, перенесших острый коронарный синдром.
Данные препараты включают антагонисты витамина К (АВК) и пероральные антикоагулянты прямого действия (ПОАК). Назначаются при наличии показаний к длительному антикоагулянтному лечению, таких, как фибрилляция предсердий (ФП), венозные тромбоэмболические осложнения (ВТЭО), механические и в ряде случаев – биологические протезы клапанов сердца, а также тромбоз полостей сердца (прежде всего ЛЖ). При ФП или ВТЭО могут использоваться как АВК, так и ПОАК, при наличии механического протеза клапана или тромбозе ЛЖ – АВК. [2]
В течение ближайших месяцев от момента ОКС антикоагулянт сочетают с одним или двумя антиагрегантными препаратами (более подробно – см раздел, посвященный многокомпонентной антитромботической терапии).
Ривароксабан – единственный антикоагулянт, назначение которого оправдано для дополнительного снижения риска атеротромботических осложнений у больных, получающих аспирин или сочетание аспирина с клопидогрелом. С этой целью следует использовать низкую – «сосудистую» дозу ривароксабана 2,5 мг 2 раза в сутки. Использование ривароксабана допустимо в сочетании с аспирином или комбинацией аспирина с клопидогрелом. [2] Опыта назначения ривароксабана с ДАТТ, включающей более мощные ингибиторы Р2Y12-рецепторов, пока нет и делать это до получения каких- либо новых данных не следует.
Таблица 16.
Дозировка антикоагулянтов у пациентов с нормальной и нарушенной почечной функцией.
В течение ближайших месяцев от момента ОКС антикоагулянт сочетают с одним или двумя антиагрегантными препаратами (более подробно – см раздел, посвященный многокомпонентной антитромботической терапии).
Ривароксабан – единственный антикоагулянт, назначение которого оправдано для дополнительного снижения риска атеротромботических осложнений у больных, получающих аспирин или сочетание аспирина с клопидогрелом. С этой целью следует использовать низкую – «сосудистую» дозу ривароксабана 2,5 мг 2 раза в сутки. Использование ривароксабана допустимо в сочетании с аспирином или комбинацией аспирина с клопидогрелом. [2] Опыта назначения ривароксабана с ДАТТ, включающей более мощные ингибиторы Р2Y12-рецепторов, пока нет и делать это до получения каких- либо новых данных не следует.
Таблица 16.
Дозировка антикоагулянтов у пациентов с нормальной и нарушенной почечной функцией.
|
Лекарство
|
|
Рекомендации
|
|
|
|
Функция почек в норме или ХБП 1-2 стадия (СКФ >30 мл/мин/1,73 м2)
|
4 стадия ХБП (СКФ 15-29 мл/мин/1,73 м2)
|
5 стадия ХБП (СКФ <15 мл/мин/1,73 м2)
|
|
Нефракционированный гепарин
|
До коронарной ангиографии: 60-70 МЕ/кг в/в (максимально 5000 МЕ) и инфузия (12-15 МЕ/ч) (максимально 1000 МЕ), целевое АЧТВ 1,5-2,5 от контрольного
Во время ЧКВ: 70-100 МЕ/кг в/в (50-70 МЕ/кг при сочетании с ингибитором ГП IIb/IIIa) |
Нет регулировки дозы
|
Нет регулировки дозы
|
|
Эноксапарин
|
1 мг/кг п/к 2 раза в день
|
1 мг/кг п/к 1 раз в день
|
Не рекомендуется
|
|
Фондапаринукс
|
2,5 мг п/к 1 раз в день
|
Не рекомендуется при СКФ <20 мл/мин/1,73 м2
|
Не рекомендуется
|
|
Бивалирудин*
|
0,75 мг/кг в/в болюсно, инфузия 1,75 мг/кг/ч
|
Болюс не подбирается, снижение скорости инфузии до 1 мг/кг/ч
|
На диализе, болюс не подбирается, снижение скорости инфузии до 0,25 мг/кг/ч
|
Неантитромботическая терапия
1) Нитраты
Польза от назначения нитратов всем больным ИМ не доказана. В крупных исследованиях ISSI-3 и ISIS-4 не показано положительное влияние на прогноз терапии нитратами как в виде внутривенной инфузии, так и перорально у больных с ИМ [4]. Рекомендуется внутривенная инфузия нитратов для симптоматического лечения больных с продолжающейся ишемии миокарда, артериальной гипертензией (АГ), СН, если нет противопоказаний (артериальная гипотония, ИМ ПЖ, использование ингибиторов фосфодиэстеразы V в предшествующие 48 часов). Критерий адекватно подобранной скорости введения (дозировки) при в/в инфузии нитратов – уровень систолического АД, который должен быть снижен на 10-15% у нормотоников и на 25-30% у лиц с АГ, но не ниже 100 мм рт. ст. Обычная начальная скорость введения нитроглицерина 10 мкг/мин. При ее неэффективности скорость инфузии увеличивается на 10-15 мкг/мин каждые 5-10 мин, пока не будет достигнут желаемый эффект. Если достичь целевого уровня снижения АД не удается, даже увеличив скорость инфузии нитроглицерина до 200 мкг/мин, то дальнейшее увеличение дозы не имеет смысла. Оптимальная продолжительность инфузии нитратов не более 24-48ч, т.к. в дальнейшем часто развивается толерантность. При развитии гипотонии обычно достаточно прекратить инфузию нитроглицерина, так как у препарата короткий период полувыведения. Реже приходится проводить стандартные мероприятия по увеличению притока крови к сердцу (приподнять нижние конечности, возможно в/в введение 0,9% раствора хлорида натрия, прессорных аминов). Противопоказанием к назначению нитратов является выраженная гипотония – систолическое АД<90 мм.рт.ст. При появлении головной боли назначают анальгетики и кофеин содержащие препараты. Внутрь нитраты при ИМ назначают только по показаниям, к которым, прежде всего, относят постинфарктную стенокардию. Иногда нитраты назначают по поводу сердечной недостаточности, хотя для этой цели лучше подходят ингибиторы АПФ. Для профилактики толерантности к нитратам их назначают прерывисто: промежуток времени между последним приемом препарата и первым приемом на следующий день должен быть не менее 12 ч (оптимально 16 ч)
2) Блокаторы бета-адренергических рецепторов (БАБ)
Убедительные данные об улучшении прогноза при назначении БАБ у больных с ОКСпST были получены, в основном, в дореперфузионную эру [4]. Польза рутинного назначения БАБ у больных, которые подверглись первичной ЧКВ, на основании РКИ и системных мета-анализов, не показана [4]. Вместе с тем, результаты некоторых регистров говорят о том, что назначение БАБ приводит к улучшению прогноза [4]. При наличии признаков сердечной недостаточности и/или выраженной дисфункции миокарда ЛЖ терапия БАБ приводит к выраженному улучшению симптоматики и прогноза [4]. Абсолютные противопоказания к использованию БАБ при ИМпST: кардиогенный шок, тяжелая обструктивная болезнь легких в стадии обострения, атриовентрикулярная (АВ) блокада II-III ст. у больных без функционирующего искусственного водителя ритма сердца, аллергия. Относительные противопоказания: клинические проявления СН, свидетельства наличия низкого сердечного выброса, систолическое АД <100 мм рт. ст., ЧСС <60 ударов в 1 мин, удлинение интервала PQ >0,24сек, обструктивная болезнь легких в анамнезе, наличие факторов риска возникновения кардиогенного шока.
Назначение БАБ на раннем этапе. Рекомендуется продолжить или начать применение одного из трех БАБ c доказанным положительным влиянием на смертность при хронической сердечной недостаточности со сниженной ФВ ЛЖ (метопролола сукцинат с замедленным высвобождением действующего вещества, карведилол или бисопролол). Гемодинамически стабильным пациентам БАБ могут быть назначены в первые 24ч после начала болезни. В ранние сроки ИМпST важнейшее значение имеет выбор приемлемой дозы препарата, которая не должна быть слишком большой при опасности возникновения осложнений (прежде всего – наличии СН). О достаточности дозы обычно судят по желаемой ЧСС. Она не должна быть ниже 44-46 ударов в 1 мин в ночные часы в покое. Первоначальная доза БАБ может быть введена в/в, особенно у больных с АГ, сохраняющейся ишемией, тахикардией при отсутствии признаков СН с последующим переходом на прием препаратов внутрь. Есть данные, что польза от БАБ выше, если терапия начата раньше [4]. У больных с существенным нарушением сократимости ЛЖ начинать лечение следует с минимальных доз бета-адреноблокаторов. Через 24-48 ч после исчезновения выраженной брадикардии, артериальной гипотензии, тяжелой СН, АВ блокады можно начать аккуратное титрование дозы препаратов для приема внутрь. При наличии исходных противопоказаний к БАБ возможность их назначения следует регулярно пересматривать. Следует воздержаться от назначения бета-адреноблокаторов с внутренней симпатомиметической активностью. Препараты и дозы для в/в введение (см. приложение 8).
Длительное назначение БАБ. Оптимальная продолжительность терапии БАБ является предметом обсуждения. В настоящее время нет убедительных свидетельств пользы продолжения рутинного применения БАБ через 1 год после ИМ у больных без хронической сердечной недостаточности со сниженной ФВ ЛЖ (исследования в этой области продолжаются) [4]. Больные с сердечной недостаточностью (СН) или сниженной фракцией выброса левого желудочка (<40%) должны принимать БАБ постоянно.
Назначение БАБ на раннем этапе. Рекомендуется продолжить или начать применение одного из трех БАБ c доказанным положительным влиянием на смертность при хронической сердечной недостаточности со сниженной ФВ ЛЖ (метопролола сукцинат с замедленным высвобождением действующего вещества, карведилол или бисопролол). Гемодинамически стабильным пациентам БАБ могут быть назначены в первые 24ч после начала болезни. В ранние сроки ИМпST важнейшее значение имеет выбор приемлемой дозы препарата, которая не должна быть слишком большой при опасности возникновения осложнений (прежде всего – наличии СН). О достаточности дозы обычно судят по желаемой ЧСС. Она не должна быть ниже 44-46 ударов в 1 мин в ночные часы в покое. Первоначальная доза БАБ может быть введена в/в, особенно у больных с АГ, сохраняющейся ишемией, тахикардией при отсутствии признаков СН с последующим переходом на прием препаратов внутрь. Есть данные, что польза от БАБ выше, если терапия начата раньше [4]. У больных с существенным нарушением сократимости ЛЖ начинать лечение следует с минимальных доз бета-адреноблокаторов. Через 24-48 ч после исчезновения выраженной брадикардии, артериальной гипотензии, тяжелой СН, АВ блокады можно начать аккуратное титрование дозы препаратов для приема внутрь. При наличии исходных противопоказаний к БАБ возможность их назначения следует регулярно пересматривать. Следует воздержаться от назначения бета-адреноблокаторов с внутренней симпатомиметической активностью. Препараты и дозы для в/в введение (см. приложение 8).
Длительное назначение БАБ. Оптимальная продолжительность терапии БАБ является предметом обсуждения. В настоящее время нет убедительных свидетельств пользы продолжения рутинного применения БАБ через 1 год после ИМ у больных без хронической сердечной недостаточности со сниженной ФВ ЛЖ (исследования в этой области продолжаются) [4]. Больные с сердечной недостаточностью (СН) или сниженной фракцией выброса левого желудочка (<40%) должны принимать БАБ постоянно.
3) Ингибиторы ангиотензин-превращающего фермента (ИАПФ), блокаторы рецепторов ангиотензина II (БРА), блокаторы рецептора альдостерона.
Эффективность ИАПФ у больных ИМ подтверждена результатами крупных РКИ: GISSI-3, ISIS-4, SMILE и т.д. [4] На фоне терапии ИАПФ уменьшается конечно- диастолический объем ЛЖ, улучшается сократительная способность ЛЖ и, как следствие, улучшаются качество жизни и прогноз. ИАПФ наиболее эффективны у больных с выраженной систолической дисфункцией ЛЖ, клиническими проявлениями сердечной недостаточности. У больных, относимых к группе низкого риска (сохраненная систолическая функция ЛЖ), польза ингибиторов АПФ не так очевидна.
Назначение ингибиторов АПФ/БРА на раннем этапе. У больных со стабильной гемодинамикой ИАПФ безопасно назначение ИАПФ в первые 24ч от начала заболевания [4]. Следует постепенно увеличивать дозу до рекомендуемой (целевой), которая поданным клинических исследований обеспечивает положительное влияние на прогноз, а если это невозможно, до максимально переносимой (см. приложение 9). Противопоказания для начала использования ингибиторов АПФ: систолическое АД <100 мм рт. ст., выраженная почечная недостаточность, гиперкалиемия, двусторонний стеноз почечных артерий, беременность, индивидуальная непереносимость. В случае непереносимости ингибиторов АПФ рекомендуется использовать блокаторы рецептора ангиотензина. Препаратом выбора считается валсартан, который по данным исследования VALIANT не уступал каптоприлу у больных ИМ, осложнившемся СН [4]. Начальная доза валсартана составляет 20 мг/сут; при хорошей переносимости дозу препарата постепенно увеличивают вплоть до 160 мг 2 раза в сутки.
Длительное назначение ингибиторов АПФ/БРА. Польза рутинного длительного назначения ингибиторов АПФ/БРА больным с сохранной функцией ЛЖ после ИМпST не доказана. Больным с СН, сниженной ФВ ЛЖ, сахарным диабетом должны получать постоянную терапию ингибиторами АПФ/БРА.
Рекомендуется использовать блокаторы рецептора альдостерона, в добавление к бета- адреноблокаторам и ингибиторам АПФ у больных с ИМпST и ФВ ЛЖ ≤40% в сочетании с СН или сахарным диабетом при условии, что нет почечной недостаточности и гиперкалиемии. Препарат этой группы эплеренон изучали у постинфарктных больных в исследовании EPHESUS. [4] У больных после ИМ с ФВ <40% и/или признаками сердечной недостаточности или СД принимали прием эплеренона привел к значительному снижению общей летальности. На основании исследования REMINDER предпочтительно назначать эплеренон в первые сутки от начала ИМ. [4] Альтернативой эплеренону может быть спиронолактон. [4] Противопоказания к назначению блокаторов рецептора альдостерона: уровень креатинина в крови у мужчин >2,5 мг/дл (220 мкмоль/л), у женщин >2,0 мг/дл (175 мкмоль/л), а также концентрация калия более 5 ммоль/л. Во время лечения контролируют уровень креатинина и калия к крови. Если уровень калия крови превышает 5,5 ммоль/л, препараты отменяют. Рекомендуется поддерживать концентрацию калия в крови в диапазоне 4,0-5,0 ммоль/л.
Длительное назначение ингибиторов АПФ/БРА. Польза рутинного длительного назначения ингибиторов АПФ/БРА больным с сохранной функцией ЛЖ после ИМпST не доказана. Больным с СН, сниженной ФВ ЛЖ, сахарным диабетом должны получать постоянную терапию ингибиторами АПФ/БРА.
Рекомендуется использовать блокаторы рецептора альдостерона, в добавление к бета- адреноблокаторам и ингибиторам АПФ у больных с ИМпST и ФВ ЛЖ ≤40% в сочетании с СН или сахарным диабетом при условии, что нет почечной недостаточности и гиперкалиемии. Препарат этой группы эплеренон изучали у постинфарктных больных в исследовании EPHESUS. [4] У больных после ИМ с ФВ <40% и/или признаками сердечной недостаточности или СД принимали прием эплеренона привел к значительному снижению общей летальности. На основании исследования REMINDER предпочтительно назначать эплеренон в первые сутки от начала ИМ. [4] Альтернативой эплеренону может быть спиронолактон. [4] Противопоказания к назначению блокаторов рецептора альдостерона: уровень креатинина в крови у мужчин >2,5 мг/дл (220 мкмоль/л), у женщин >2,0 мг/дл (175 мкмоль/л), а также концентрация калия более 5 ммоль/л. Во время лечения контролируют уровень креатинина и калия к крови. Если уровень калия крови превышает 5,5 ммоль/л, препараты отменяют. Рекомендуется поддерживать концентрацию калия в крови в диапазоне 4,0-5,0 ммоль/л.
4) Липид-снижающая терапия.
Многочисленные исследования по вторичной профилактике ИБС показали, что у больных ИБС, особенно перенесшим ОКС, терапия статинами приводит к улучшению прогноза. [4] Основываясь, прежде всего, на результатах исследования PROVE IT-TIMI 22, статины назначают сразу в больших дозировках и в ранние сроки от начала ОКС. [4].В этом исследовании больные получали аторвастатин в дозе 80 мг или правастатин в дозе 40 мг в сутки. На терапии статином было меньше ишемических осложнений. Объединенный анализ 26 крупных исследований показал, что интенсивная терапия статинами приводит к снижению риска сердечно-сосудистых осложнений [4]. У ряда больных общий холестерин и холестерин ЛПНП при первом измерении оказывается низким, иногда ниже целевых значений. По данным ретроспективного анализа у больных с низким холестерином ЛПНП (средний уровень 63 мг/дл), которым была назначена терапия статинами, частота летальности и сердечных осложнений был достоверно ниже, чем у больных, не получавших статины [6]. На основании этих данных рекомендуется начать как можно раньше или продолжить лечение статинами в высокой дозе вне зависимости от исходного уровня холестерина, если к ним нет противопоказаний. Препаратом выбора является аторвастатин в дозе 80 мг в сутки. Могут использоваться и другие статины, в частности, розувастатин в дозе 20-40мг/сут. При назначении статинов ориентируются на уровень холестерина, измеряемый в течение суток от начала развития ОКС. Было показано, что начиная со вторых суток и в последующие несколько недель, уровень холестерина может снижаться в связи с основным заболеванием и, соответственно, не отражать истинное состояние липидного обмена. В соответствии с Европейскими рекомендациями по лечению дислипидемий больные с ОКС относятся к категории очень высокого риска, целевой уровень холестерина ЛПНП у них составляет менее 1,4 ммоль/л (55 мг/дл) или снижение как минимум на 50% [7]. Эти рекомендации основаны да данных, согласно которым при достижении низких значений холестерина ЛПНП риск сердечно-сосудистых осложнений дополнительно снижается [4]. Терапия статинами обычно хорошо переносится, частота серьезных побочных эффектов не превышает 2% [4]. Возможно появление миалгии и мышечной слабости, которые появляются, в основном, в первые недели после начала терапии и обычно быстро проходит после отмены статина.[4] Рабдомиолиз с повышением уровня кретинкиназы более чем в 10 раз наблюдается очень редко [4]. Возможно биссимптомптомное повышение уровня трансаминаз в 3 и более раза, что требует снижения дозы или отмены препарата [4]. Следует помнить, что в острую фазу ИМ повышение уровня трансаминаз обусловлено некрозом кардиомиоцитов и не является причиной для отказа от назначения статинов. Статины повышают риск манифестации сахарного диабета, о чем больные должны быть проинформированы. Польза от назначения статинов превышает потенциальный риск развития сахарного диабета, и даже развитие диабета не является поводом для отмены статинов.[4] Для оценки эффективности терапии статинами следует определить уровень холестерина липопротеидов низкой плотности повторно через 4-6 недель после начала лечения [4]. Если не удается достигнуть целевых значений уровня холестерина липопротеидов низкой плотности на фоне терапии статинами в максимально переносимых дозы, рекомендовано назначить другие липид-снижающие препараты.
Эзетимиб является представителем нового класса гиполипидемических лекарственных средств, селективно ингибирующих абсорбцию холестерина в кишечнике. Эзетимиб, назначаемый в комбинации со статинами, снижает уровень общего холестерина, холестерина ЛПНП, триглицеридов и повышает уровень холестерина ЛПВП. В исследовании IMPROVE-IT изучали эзетимиб у больных после ИМ. Добавление эзетимибак 40 мг симвастатина привело к снижению частоты первичной конечной точки (кардиальная смертность, ИМ, нестабильная стенокардия с необходимостью повторной госпитализации, коронарной реваскуляризация и инсульт).[4] Эзетимиб рассматривают как препарат 2-й линии, который назначают в случае невозможности достигнуть целевых значений холестерина ЛПНП на максимально переносимых дозах статинов.
Ингибиторы пропротеиновой конвертазы субтилизин-кексинового типа 9 (proproteinconvertasesubtilisin/kexintype 9 - PCSK9) -широко исследуемый новый класс липид-снижающих препаратов. Эти препараты представляют собой моноклональные антитела против PCSK9 и вводятся подкожно. PCSK9 играет важную регуляторную роль в гомеостазе холестерина. Связывание PCSK9 с EGF-A доменом рецептора липопротеинов низкой плотности приводит к деградации рецептора. Уменьшение количества рецепторов липопротеинов низкой плотности, в свою очередь, вызывает пониженный метаболизм липопротеинов низкой плотности, что может привести к гиперхолестеринемии. Ингибиторы PCSK9 позволяют снизить уровень холестерина ЛПНП на 60%, что делает их наиболее сильными холестерин-снижающими препаратами. В исследовании FOURIER, в которое включали больных с различными клинически значимыми проявлениями атеросклероза, в том числе перенесших ИМ, показано, что препарат эволокумаб в комбинации со статинами по сравнению с монотерапией статинами приводил к снижению относительного риска первичной конечной точки (кардиальная смерть, ИМ, инсульт, госпитализация по поводу НС, коронарная реваскуляризация [4]. В исследовании ODYSSEY OUTCOMES изучался другой препарат этой группы алирокумаб у больных, недавно перенесших ОКС (от 4 до 52 недель до рандомизации). Ишемические осложненияи общая смертность в группе алирокумаба происходили на 15% реже по сравнению с плацебо. Преимущество алирокумаба было особенно выражено у пациентов, у которых исходный уровень холестерина ЛПНП был выше 100 мг/дл [4]. Эволокумаб и алирокумаб зарегистрированы и доступны в РФ. Ингибиторы PCSK9 можно рассматривать у больных с ОКС как дополнение к статинам (или альтернативу в случае непереносимости статинов) если не достигнут целевой уровень холестерин ЛПНП на максимально переносимых дозах статинов.
Ингибиторы пропротеиновой конвертазы субтилизин-кексинового типа 9 (proproteinconvertasesubtilisin/kexintype 9 - PCSK9) -широко исследуемый новый класс липид-снижающих препаратов. Эти препараты представляют собой моноклональные антитела против PCSK9 и вводятся подкожно. PCSK9 играет важную регуляторную роль в гомеостазе холестерина. Связывание PCSK9 с EGF-A доменом рецептора липопротеинов низкой плотности приводит к деградации рецептора. Уменьшение количества рецепторов липопротеинов низкой плотности, в свою очередь, вызывает пониженный метаболизм липопротеинов низкой плотности, что может привести к гиперхолестеринемии. Ингибиторы PCSK9 позволяют снизить уровень холестерина ЛПНП на 60%, что делает их наиболее сильными холестерин-снижающими препаратами. В исследовании FOURIER, в которое включали больных с различными клинически значимыми проявлениями атеросклероза, в том числе перенесших ИМ, показано, что препарат эволокумаб в комбинации со статинами по сравнению с монотерапией статинами приводил к снижению относительного риска первичной конечной точки (кардиальная смерть, ИМ, инсульт, госпитализация по поводу НС, коронарная реваскуляризация [4]. В исследовании ODYSSEY OUTCOMES изучался другой препарат этой группы алирокумаб у больных, недавно перенесших ОКС (от 4 до 52 недель до рандомизации). Ишемические осложненияи общая смертность в группе алирокумаба происходили на 15% реже по сравнению с плацебо. Преимущество алирокумаба было особенно выражено у пациентов, у которых исходный уровень холестерина ЛПНП был выше 100 мг/дл [4]. Эволокумаб и алирокумаб зарегистрированы и доступны в РФ. Ингибиторы PCSK9 можно рассматривать у больных с ОКС как дополнение к статинам (или альтернативу в случае непереносимости статинов) если не достигнут целевой уровень холестерин ЛПНП на максимально переносимых дозах статинов.
5) Блокаторы медленных кальциевых каналов
Пероральные нитраты, антагонисты кальция и другие антиангинальные препараты назначают только при сохранении ангинозных приступов, несмотря на терапию БАБ. Рутинное назначение антиангинальных препаратов после ОКС не приводит к улучшению прогноза и, следовательно, не показано [4]. В связи с возможностью неконтролируемой гипотонии следует избегать назначения нифедипина короткого действия у больных с ОКС [4]. Дилтиазем, верапамил и дигидропиридины 2-го поколения(амлодипин) можно назначать больным с постинфарктной стенокардией при недостаточной эффективности бета- адреноблокаторов и нитратов, или при невозможности контролировать артериальную гипертонию другими средствами. Дилтиазем и верапамил иногда используют для контроля сердечного ритма, реже для курирования суправентрикулярных аритмий в случае неэффективности/противопоказаний к бета- адреноблокаторам. Верапамил или дилтиазем могут использоваться только в отсутствие симптомов СН, существенной сократительной дисфункции ЛЖ, нарушений синоатриальной и АВ проводимости и брадиаритмий. Совместный прием верапамила и дилтиазема с бета-адреноблокаторами нежелателен.
6) Другие виды лечения: хирургические виды лечения по экстренным показаниям (см. соответствующий протокол по проведению кардиохирургических вмешательств).
Пациенты с одно-сосудистым поражением коронарных артерий должны подвергнуться ЧКВ во время коронарографии. Стратегия реваскуляризации отдельного пациента с ОКСбпST с многососудистым поражением должна быть обсуждена командой специалистов (Heart Team) и основываться на клиническом состоянии, тяжести и распространенности поражения сосудов, характеристик места поражения и шкале SYNTAX Если коронарная анатомия не позволяет провести ЧКВ, пациенты должны быть подвергнуты неотложному корнарному шунтированию.
Для некоторых пациентов может быть подходящим последовательный подход, состоящий из стентирования места поражения с последующим селективным КШ при доказательстве наличия ишемии и /или ФРК не инфаркт-зависимых артерий.
6) Другие виды лечения: хирургические виды лечения по экстренным показаниям (см. соответствующий протокол по проведению кардиохирургических вмешательств).
Пациенты с одно-сосудистым поражением коронарных артерий должны подвергнуться ЧКВ во время коронарографии. Стратегия реваскуляризации отдельного пациента с ОКСбпST с многососудистым поражением должна быть обсуждена командой специалистов (Heart Team) и основываться на клиническом состоянии, тяжести и распространенности поражения сосудов, характеристик места поражения и шкале SYNTAX Если коронарная анатомия не позволяет провести ЧКВ, пациенты должны быть подвергнуты неотложному корнарному шунтированию.
Для некоторых пациентов может быть подходящим последовательный подход, состоящий из стентирования места поражения с последующим селективным КШ при доказательстве наличия ишемии и /или ФРК не инфаркт-зависимых артерий.
Особенности лечения у отдельных групп пациентов [4, https://cardiocenter.uz/docs]
Рекомендации по периоперационному применению антиагрегантной терапии у пациентов с ОКС/ОИМ, нуждающихся в аортокоронарном шунтировании.
|
Рекомендации
|
Класс
|
Уровень
|
|
Рекомендованы ингибиторы P2Y12 независимо от стратегии реваскуляризации в дополнение к аспирину с продолжительностью применения 12 месяцев в отсутствии противопоказаний, таких как повышенный риск кровотечения.
|
I
|
А
|
|
Группе кардиологов (Heart Team) рекомендовано оценивать индивидуальные риски ишемии и кровотечения, а также определять сроки проведения АКШ, так же, как и ДАТ.
|
I
|
С
|
|
Рекомендовано осуществление АКШ без задержки пациентам с Гемодинамической нестабильностью, продолжающейся ишемией миокарда или очень высоким риском анатомии коронарных артерий, независимо от антиагрегантной терапии.
|
I
|
С
|
|
Аспирин рекомендован через 6-24 ч после АКШ в отсутствие продолжающегося кровотечения.
|
I
|
А
|
|
Рекомендовано продолжение приема низких доз аспирина несмотря на АКШ.
|
I
|
В
|
|
Стабилизированным пациентам, требующим проведение КШ и находящимся на ДАТ, должно быть рассмотрено прекращение приема тикагрелора и клопидогреля за 5 дней
|
IIа
|
В
|
|
Следует рассмотреть возобновление приема ингибиторов P2Y12 после АКШ, как только это станет безопасным
|
IIа
|
С
|
Рекомендации по лечению пациентов с ОКСбпST с сахарным диабетом
|
Рекомендации
|
Класс
|
Уровень
|
|
Контроль уровня глюкозы крови
|
|
|
|
Рекомендовано проверять всех пациентов с острый коронарный синдром без подъема сегмента ST на наличие диабета и часто мониторировать уровень глюкозы крови пациентам с установленным диабетом и гипергликемией при поступлении.
|
I
|
С
|
|
Сахароснижающая терапия должна быть рассмотрена пациентам с ОКС при уровне глюкозы >10 ммоль/л, с целью адаптации к сопутствующим заболеваниям, следует избегать эпизодов гипогликемии.
|
IIa
|
С
|
|
Менее строгий контроль глюкозы следует рассматривать как в острой фазе, так и при последующих наблюдениях у пациентов с более выраженными сердечно-сосудистыми заболеваниями, более старшего возраста, более длительным сроком диабета и с большим числом сопутствующих заболеваний.
|
IIa
|
С
|
|
Антитромботическое лечение и инвазивная стратегия
|
||
|
Рекомендовано назначать одинаковое антитромботическое лечение как пациентам с диабетом, так и без него
|
I
|
C
|
|
Инвазивная стратегия имеет преимущества над неинвазивной
|
I
|
A
|
|
Рекомендовано мониторировать функцию почек в течение 2-3 дней после коронарной ангиографии или ЧКВ пациентам с исходной почечной недостаточностью или на метформине
|
I
|
C
|
|
Пациентам, подвергшимся ЧКВ, предпочтительнее установка нового поколения стентов DES, чем BMS
|
I
|
A
|
|
Пациентам со стабилизированной ИБС с многососудистым поражением и приемлемым хирургическим риском предпочтительнее АКШ, чем ЧКВ.
|
I
|
A
|
|
Пациентам со стабильным многососудистым поражением и оценкой по шкале SYNTAX ≤22 баллов должно быть рассмотрено ЧКВ как альтернатива АКШ
|
IIа
|
B
|
Сокращения: BMS – голометаллический стент, DES - стент с лекарственным покрытием, КШ - коронарное шунтирование, ЧКВ - чрескожное коронарное вмешательство. *
Рекомендации по лечению пациентов с ОКС/ОИМ и хронической болезнью почек
|
Рекомендации
|
Класс
|
Уровень
|
|
Рекомендовано оценивать функцию почек по СКФ у всех пациентов
|
I
|
С
|
|
Рекомендовано назначать такую же антитромботическую терапию первой линии как пациентам с нормальной функцией почек, с соответствующей корректировкой дозы при наличии показаний.
|
I
|
B
|
|
В зависимости от степени нарушения почечной функции рекомендуется переход с парентеральной антикоагуляции на НФГ или на корректированные дозы фондапаринукса, эноксапарина и бивалирудина, также, как и ингибиторов гликопротеина IIb/IIIa.
|
I
|
B
|
|
Рекомендован переход с п/к или в/в антикоагуляции на инфузию НФГ, скорректированной по АЧТВ при СКФ <30 мл/мин/1,73 м2 (для фондапаринукса при СКФ <20 мл/мин/1,73 м2).
|
I
|
C
|
|
Пациентам, подвергающимся инвазивной стратегии, рекомендуется гидратация изотоническим солевым раствором и применение низко или изоосмолярного контрастного вещества (в минимальном объеме).
|
I
|
A
|
|
Коронарная ангиография и ЧКВ рекомендованы после тщательной оценки отношения риска-польза, особенно с учетом выраженности нарушения функции почек.
|
I
|
B
|
|
Пациентам, подвергшимся ЧКВ, предпочтительнее установка нового поколения стентов DES, чем BMS.
|
I
|
B
|
|
КШ предпочтительнее, чем ЧКВ, у пациентов с многососудистым поражением с приемлемым хирургическим риском и ожидаемой продолжительностью жизни более 1 года.
|
IIа
|
B
|
|
ЧКВ предпочтительнее, чем АКШ, у пациентов с многососудистым поражением с высоким хирургическим риском и ожидаемой продолжительностью жизни менее1 года
|
IIа
|
B
|
Рекомендации по лечению пациентов с ОКС/ОИМ с острой сердечной недостаточностью.
|
Рекомендации
|
Класс
|
Уровень
|
|
Рекомендовано проведении неотложной эхокардиографии для оценки функции ЛЖ, состояния клапанов и исключения механических осложнений.
|
I
|
С
|
|
Неотложная коронарография рекомендована пациентам с острой сердечной недостаточностью, со стойкими симптомами ишемии
(стенокардией), отклонениями сегмента ST, кардиогенным шоком. |
I
|
B
|
|
Неотложное ЧКВ рекомендовано пациентам с кардиогенным шоком при подходящей анатомии коронарных артерий.
|
I
|
B
|
|
Неотложное АКШ рекомендовано пациентам с кардиогенным шоком при наличии анатомии коронарных артерий, не подходящей для проведения ЧКВ.
|
I
|
B
|
|
Пациентам с механическими осложнениями ОКСбпST рекомендуется неотложное проведение кардиологического консилиума
|
I
|
C
|
|
Установка ВАБК должна быть рассмотрена пациентам с гемодинамической нестабильностью/кардиогенным шоком в связи с механическими осложнениями.
|
IIb
|
C
|
|
Кратковременная механическая поддержка кровообращения может быть рассмотрена пациентам с кардиогенным шоком.
|
IIb
|
С
|
|
Не рекомендуется рутинное применение ВАБК пациентам с кардиогенным шоком.
|
III
|
В
|
Рекомендации по лечению пациентов с ОКС/ОИМ с фибрилляцией предсердий.
|
Рекомендации
|
Класс
|
Уровень
|
|
Рекомендовано назначение антикоагулянтов всем пациентам при поступлении при отсутствии противопоказаний.
|
I
|
А
|
|
Всем пациентам с ФП и повышенным уровнем сердечного тропонина должны быть рассмотрены исследования по выявлению ишемии.
|
IIа
|
C
|
|
Пациенты с быстрой частотой сокращения желудочков
|
|
|
|
Электрическая кардиоверсия рекомендована пациентам с гемодинамической нестабильностью
|
I
|
С
|
|
Электрическая или фармакологическая кардиоверсия амиодароном рекомендованы пациентам при принятии решения о несрочном восстановлении синусового ритма (стратегия контроля ритма).
Этастратегия должна применяться пациентам с первым эпизодом ФП продолжительностью <48 ч (или пациентам в отсутствии данных за тромб в левом предсердии по данным ЧП-ЭХОКГ) или пациентам, находящимся в терапевтическом диапазоне на антикоагулянтах, по меньшей мере, 3 недели |
I
|
С
|
|
ПриФП у гемодинамически стабильных пациентов рекомендовано внутривенное введение β-блокаторов для снижения частого желудочкового ответа
|
I
|
C
|
|
Внутривенное назначение сердечных гликозидов может быть рассмотрено для контроля желудочковой частоты, если ответ на β-блокаторы не достаточен
|
IIb
|
C
|
|
При ФП у пациентов, не принимающих β-блокаторы и без признаков сердечной недостаточности может быть рассмотрено внутривенное назначение недигидропиридиновых антагонистов кальция (верапамила, дилтиазема) для снижения частого желудочкового ответа
|
IIb
|
C
|
Рекомендации по лечению пациентов с ОКС/ОИМ с тромбоцитопенией
|
Рекомендации
|
Класс
|
Уровень
|
|
Рекомендуется немедленное прекращение введения ингибиторов GPIIb/IIIa и/или гепарина (НФГ, НМГ, других продуктов гепарина) в случае тромбоцитопении <100000/μл (или >50% относительно снижение по сравнению с исходным количеством тромбоцитов), произошедшей во время лечения.
|
I
|
С
|
|
Пациентам, находившимся на лечении ингибиторами GPIIb/IIIa, рекомендовано переливание тромбоцитов в случае большого активного кровотечения или наличия асимптомной тромбоцитопении (<100000/μл)
|
I
|
C
|
|
Лечение антикоагулянтами, не относящимся к гепаринам, рекомендовано в случае документированной ГИТ или подозрении на ГИТ.
|
I
|
С
|
|
Для профилактики ГИТ рекомендовано применение антикоагулянтов с низким риском или отсутствием ГИТ или краткий курс НФГ или НМГ
|
I
|
С
|
* [Евразийские клинические рекомендации по диагностике и лечению острого коронарного синдрома с подъемом сегмента ST] стр. 100, 122,115, https://cardio-eur.asia/media/files/clinical_recommendations/Eurasian_clinical_guidelines_for_the_diagnosis_and_treatment_of_acute_coronary_syndrome_with_ST_segment_elevation_(ACSpST)_rus_20 19.pdf
Критерии оценки качества медицинской помощи
При оценке качества медицинской помощи, оказанной больным с ОКСпST необходимо учитывать совокупность различных факторов, включая своевременность оказания медицинской помощи, правильность выбора стратегии ведения больного, методов диагностики, лечения и реабилитации. Другими словами, оценка качества оказания медицинской помощи должна отражать соблюдение определенных стандартов, прежде всего, действующих Рекомендаций по диагностике и лечению ОКСпST с учетом особенностей конкретного медицинского учреждения (прежде всего возможности выполнения интервенционных методов диагностики и лечения), материально- технического оснащения, и индивидуальных особенностей каждого больного. Качество медицинской помощи отражают также показатели ключевых клинических результатов (исходов). Очевидно, что работа лечебного учреждения определяется многими существующими фактически территориальными, организационными, транспортными, логистическими, экономическими, материально-техническими и другими условиями, что может приводить к возникновению существенного разрыва между положениями действующих Рекомендаций по оказанию медицинской помощи и реальной клинической практикой. В связи с этим важно определить критерии, которые позволяли бы оценить качество оказания медицинской помощи пациенту с ОКСпST в данном лечебном учреждении и его отдельных подразделениях.
Общая организация помощи больному с ОКСпST
-
Наличие ЧКВ-центров с круглосуточной службой эндоваскулярных методов диагностики и лечения, организация которых оправдана с экономической и организационной точки зрения, если население региона, из которого происходит госпитализация, составляет более 200 000 человек. В крупных городах необходимое количество инвазивных центров: из расчета 1 центр на 400-500 тыс. населения;
-
Организация единой «сосудистой сети» (в данном городе, районе, области, крае и т.д.), куда включены все стационары, лицензированные на оказание медицинской помощи больным с ОКСпST, врачи и фельдшеры бригад СМП, сотрудники диспетчерских службах (с наличием единых протоколов - документов, регламентирующим ее оказание на всех этапах);
-
Существование единого легко запоминающегося номера телефона экстренной медицинской помощи для вызова бригады СМП или аналогичной неотложной службы;
-
Возможность догоспитальной незамедлительной интерпретации ЭКГ с принятием решения о скорейшем направлении больного в сосудистой центр с возможностью выполнения ЧКВ;
-
Наличие прямой связи между бригадой СМП или сотрудником диспетчерской службы и сосудистым центром для «догоспитального» оповещения о направлении туда больного с ОКСпST, для минимизации внутригоспитальной задержки при проведении ЧКВ;
-
Повсеместное оснащение бригад СМП дефибрилляторами и всем необходимым для проведения сердечно-легочной реанимации;
-
Проведение мониторирования и протоколирования времени всех этапов оказания медицинской помощи, прежде всего, времени до проведения реперфузии, (с периодическим анализом существующих задержек и их минимизацией);
-
Протоколирование (и периодический анализ) всех лекарственных препаратов, полученных больным до госпитализации (до проведения ЧКВ).
Показатели своевременности реперфузионной терапии
-
Процент больных с ОКСпST, поступивших в стационар в первые 12 часов от начала заболевания, которых проведена реперфузионная терапия: ЧКВ, ТЛТ, фармакоинвазивная стратегия;
-
Процент больных с ОКСпST, поступивших в стационар в первые 6 часов от начала заболевания, которых проведена реперфузионная терапия: ЧКВ, ТЛТ, фармакоинвазивная стратегия;
На догоспитальном этапе (процент больных):
-
<10 мин на регистрацию и интерпретацию ЭКГ
-
<90 мин с момента диагностики ОКСпST до восстановления кровотока в инфаркт-зависимой артерии при ЧКВ
-
<10 мин с момента диагностики ОКСпST до начала введения тромболитика, в случае невозможности транспортировки пациента в ЧКВ-центр в установленное время
В инвазивном стационаре (процент больных):
-
<10 мин на регистрацию и интерпретацию ЭКГ
-
<60 мин с момента диагностики ОКСпST до восстановления кровотока в инфаркт-зависимой артерии при ЧКВ
-
Для больных, переведенных из неинвазивного стационара (процент больных):
-
<90 мин с момента диагностики ОКСпST до восстановления кровотока в инфаркт-зависимой артерии при ЧКВ
-
<30 мин общего времени нахождения больного в неинвазивном стационаре с момента поступления, при принятии решении о переводе в ЧКВ-центр.
Оценка адекватности проводимой терапии в стационаре и после выписки:
-
процент больных, которым назначена ДАТТ, при отсутствии документированных противопоказаний к назначению ацелилсалициловой кислоты и / или блокатора P2Y12 рецепторов.
-
процент пациентов с ОКСпST, которым назначены статины в высоких дозах, при отсутствии документированных противопоказаний к их назначению
-
процент больных, с ФВЛЖ ≤40% или с клиническими признаками СН, которым назначены ингибиторы АПФ/блокаторы рецептора АТ2, при отсутствии документированных противопоказаний к их назначению
-
процент больных с ФВЛЖ ≤40% или с клиническими признаками СН, которым назначены бета-блокаторы, при отсутствии документированных противопоказаний к их назначению.
Анализ качества ведения больных в стационаре:
-
процент больных, которым проведена оценка риска по шкалам GRACE/TIMI/CRUSADE
-
процент больных, которым до выписки из стационара определена ФВ ЛЖ.
Оценка качества примененных немедикаментозных подходов к ведению больного в течение госпитального периода и после выписки из стационара:
-
процент больных, с которыми проведена беседа и даны письменные рекомендация по отказу от курения
-
процент больных, с которыми проведена беседа и даны письменные рекомендации по целесообразности приверженности к назначенному лечению, последующего медицинского наблюдения; которым разъяснены причины и факторы риска заболевания
-
процент больных, которые были включены в программы реабилитации
-
процент больных, которым даны письменные рекомендации по контролю приступов стенокардии
-
процент больных, которым объяснены алгоритмы действий при повторном обострении ИБС
Показатели клинических результатов (исходов) лечения:
-
Госпитальная летальность от ИМпST(с поправкой на сумму баллов по шкале GRACE)*
*При анализе госпитальной летальности целесообразно учитывать возраст, пол, сопутствующие тяжелые заболевания, исходную тяжесть состояния, наличие осложнений ИМ, реперфузионную терапию, лекарственную терапию.
Использование обозначенных выше критериев оценки качества могут помочь в выявлении общих системных и частных недостатков работы неотложной кардиологической службы, способствовать разработке подходов к ее дальнейшему улучшению, а значит оказанию более эффективной медицинской помощи каждому конкретному больному с ОКС/ОИМ.
Таблица 17.
Критерии качества специализированной медицинской помощи при остром коронарном синдроме
|
N
п/п |
Критерии качества
|
Оценка выполнения
|
|
1.
|
Выполнен осмотр врачом-кардиологом не позднее 5 минут от момента поступления в стационар
|
Да/Нет
|
|
2.
|
Выполнено электрокардиографическое исследование не позднее 10 минут от момента поступления в стационар
|
Да/Нет
|
|
3.
|
Выполнено определение уровня тропонинов I, T в крови и/или определение уровня и активности креатинкиназы в крови
|
Да/Нет
|
|
5.
|
Проведена (при остром коронарном синдроме с подъемом сегмента ST электрокардиограммы) терапия фибринолитическими лекарственными препаратами не позднее 30 минут от момента поступления в стационар (в случае, если терапия фибринолитическими лекарственными препаратами не проведена на догоспитальном этапе) или выполнено первичное чрескожное коронарное вмешательство не позднее 1 часа от момента поступления в стационар (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний)
|
Да/Нет
|
|
6.
|
Проведена терапия ингибиторами агрегации тромбоцитов
|
Да/Нет
|
|
7.
|
Проведена терапия ацетилсалициловой кислотой
|
Да/Нет
|
|
8.
|
Проведена терапия гиполипидемическими препаратами
|
Да/Нет
|
|
9.
|
Выполнено электрокардиографическое исследование до начала тромболитической терапии и через 1 час после окончания (в случае проведения тромболитической терапии)
|
Да/Нет
|
|
10.
|
Выполнено электрокардиографическое исследование до начала чрескожного коронарного вмешательства и через 30 минут после его окончания (при чрескожном коронарном вмешательстве)
|
Да/Нет
|
Медицинская реабилитация
ОБУЧЕНИЕ БОЛЬНОГО
Обучение больного является неотъемлемой частью реабилитации. Подробное разъяснение больному в доступной форме природы ИБС и ИМ, какие существуют направления профилактики, каким образом реагировать на изменения самочувствия и т.д., является крайне важным моментом, который существенным образом отражается на прогнозе. При разговоре с больным следует избегать непонятных медицинских терминов. Необходимо говорить на простом, доступном больному языке и перед переходом к следующей теме удостовериться, что больной все понял именно так, как вы хотели до него донести. Исходя из уровня знаний пациента о его заболевании, следует привлекать больного к совместной разработке реалистичного и приемлемого плана лечения. Врач должен знать ориентировочную стоимость месячного курса лечения и обязательно выяснить, может ли больной оплачивать лекарства. Лучше рекомендовать более дешевые и, возможно, менее эффективные препараты, чем формально предписать курс терапии, который больной не может себе позволить.
В разговоре с больным следует осветить следующие темы:
-
Необходимо разъяснить больному природу его заболевания и возможные причины, способствовавшие развитию ОКС.
-
Следует настоятельно рекомендовать прекратить курение. В связи с крайней важностью этого вопроса к нему нужно постоянно возвращаться.
-
Необходимо дать больному рекомендации по диете.
-
Следует убедиться, что больной ясно представляет себе необходимость выполнения предписаний врача, а именно: настроить больного на постоянный длительный прием препаратов, мотивируя рекомендации существенным улучшением качества жизни, уменьшением риска осложнений. Нужно подчеркнуть, что назначаемые препараты специально разработаны для длительного приема, обычно хорошо переносятся. Больной должен знать основные побочные эффекты препаратов и во всех случаях их развития сразу обращаться к врачу.
-
Следует проинструктировать пациента о лечебной тактике в случае возникновения приступа стенокардии: при развитии приступа стенокардии следует принимать нитроглицерин в виде спрея или таблеток. Если приступ не купируется, последующие приемы проводят с интервалом 5 мин под строгим контролем АД. Предпочтительно принять горизонтальное положение; если приступ на купируется в течение 5 мин, необходимо вызвать бригаду «скорой помощи».
-
Нужно описать больному признаки нестабильной стенокардии и необходимые меры по профилактике: при уменьшении толерантности к нагрузкам, учащении приступов, появлении приступов в покое, снижении эффективности антиангинальных препаратов следует безотлагательно обратиться к врачу.
-
Больному рекомендуют постоянно иметь при себе копию выписки из стационара и последнюю ЭКГ. В случае ухудшения состояния эти документы могут существенно помочь врачам сориентироваться в ситуации и выбрать оптимальную тактику лечения. После выписки больного с ИМ контрольный осмотр врача проводят в течение 3 сут, а в дальнейшем частота визитов к врачу зависит от состояния больного и последствий перенесенного ИМ. При стабильном состоянии частота визитов составляет 1 раз в месяц ев первые 6 мес., далее 1–2 раза в год.
Госпитализация
Показания для госпитализации с учетом видов оказания медицинской помощи:
Инфаркт миокарда с подъемом сегмента ST (ИМпST) в большинстве случаев обусловлен тромботической окклюзией крупной коронарной артерии. Незамедлительное восстановление коронарного кровотока - основной метод лечения ИМ, который позволяет уменьшить размер пораженного миокарда, и таким образом улучшить прогноз и качество жизни. Проведение эффективной и своевременной реперфузионной терапии – главная лечебно-организационная задача у этой категории больных.
При ИМ события происходят драматически быстро. После развития тромботической окклюзии крупной коронарной артерии ужу через 30 мин начинается гибель кардиомиоцитов. Через 3ч после начала ИМ погибает около 90% миокарда из зоны ишемии, через 6ч – почти 100% Раннее восстановление коронарного кровотока – краеугольный камень лечения ИМ. Очевидно, что именно время до восстановления коронарного кровотока в инфаркт связанной артерии в значительно большей степени определяет выживаемость пациентов, чем собственно метод реперфузии. Для эффективного лечения ИМ крайне важна организация логистики на каждом этапе, где возможна задержка, с целью сокращения времени от начала приступа до проведения реперфузионной терапии. Идеально, чтобы этот промежуток времени не превышал 1 ч. В этом случае эффективность восстановления кровотока максимальна, удается спасти основную часть миокарда из зоны риска [4].
Профилактика
К основным мерам, направленным на профилактику острого коронарного синдрома относят:
- Адекватный двигательный режим и (при необходимости) нормализация веса тела
- Питание с пониженным содержанием животных жиров, соли.
- Выявление лиц с АГ и подбор эффективного лечения до достижения целевых значений артериального давления. Динамический контроль артериального давления.
- Отказ от курения.
- У всех мужчин старше 40 лет и женщин после менопаузы, а также молодых пациентов с повышенным риском развития ИБС необходимо определение уровня холестерина и его фракций. При необходимости коррекция дислипидемии с помощью изменения рациона питания и медикаментозной терапии.
- Выявление и коррекция гипергликемии. Сахарный диабет - значимый фактор риска ИБС. Так, вероятность развития инфаркта миокарда (ИМ) у пациентов с СД 2 типа соответствует группе пациентов, уже перенёсших ИМ без СД
Алгоритм действий при сердечном приступе (для пациентов)
- Сесть или лечь с приподнятым изголовьем, снять галстук, расстегнуть ворот рубашки
- Обеспечить приток свежего воздуха в помещение
- Разжевать 1 таблетку (0, 5 г) ацетилсалициловой кислоты
- Положить под язык таблетку или капсулу (0,5 мг) нитроглицерина (капсулу предварительно раскусить)
- При сохранении боли через 5-7 минут повторно принznm еще 1 таблетку нитроглицерина и вызвать скорую помощь или незамедлительно обратиться на прием к врачу.
!!! Если после приема нитроглицерина боли исчезли и самочувствие улучшилось пациент все равно должен обратиться в поликлинику или вызвать скорую.
Информация
Источники и литература
-
Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2024
- Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2024 - 1. ACSIS (2007) Eur. Heart J., 28 (Abstr. Suppl.): 835. 2. Eurasian_clinical_guidelines_for_the_diagnosis_and_treatment_of_acute_coronary_syndrome_ with_ST_segment_elevation_(ACSpST)_rus_2019 3. Fourth universal definition of myocardial infarction (2018). Eur Heart J 2019; 40: 237-269. 4. Юрак-қон томир касалликлари бўйича миллий клиник баённомалар. Тошкент. 2023. 584 бет 5. Henning R. Andersen, M.D., Torsten T. Nielsen, M.D., Klaus Rasmussen, M.D., Leif Thuesen, M.D., Henning Kelbaek, M.D., Per Thayssen, M.D., Ulrik Abildgaard, M.D., Flemming Pedersen, M.D., Jan K. Madsen, M.D., Peer Grande, M.D., Anton B. Villadsen, M.D., Lars R. Krusell, M.D., Torben Haghfelt, M.D., Preben Lomholt, M.D., Steen E.Husted, M.D., Else Vigholt, M.D., Henrik K. Kjaergard, M.D., and Leif Spange Mortensen, M.Sc.for the DANAMI-2 Investigators. A comparison of coronary angioplasty with fibrinolytic therapy in acute myocardial infarction. N. Engl. J. Med. 2003;349:733–742. 6. Thomas T. Tsai, Brahmajee K. Nallamothu, Debabrata Mukherjee, Melvyn Rubenfire, Jianming Fang, Paul Chan,Eva Kline-Rogers, Amisha Patel, David F. Armstrong, Kim A. Eagle, A.D. Goldberg, Effect of statin use in patients with acute coronary syndromes and a serum low-density lipoprotein ≤80mg/dl. Am. J. Cardiol. 2005;96(11):1491–1493. 7. François Mach, Colin Baigent, Alberico L Catapano, Konstantinos C Koskinas, Manuela Casula, Lina Badimon, M John Chapman, Guy G De Backer, Victoria Delgado, Brian A Ference, Ian M Graham, Alison Halliday, Ulf Landmesser, Borislava Mihaylova, Terje R Pedersen, Gabriele Riccardi, Dimitrios J Richter, Marc S Sabatine, Marja-Riitta Taskinen, Lale Tokgozoglu, Olov Wiklund, ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk: The Task Force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS). European Heart Journal, ehz455, https://doi.org/10.1093/eurheartj/ehz455
Информация
В разработке клинического протокола и стандарта внесли вклад:
По организации процесса члены рабочей группы по направлению Кардиология:
-
Фозилов Х.Г. – директор РСНПМЦК, к.м.н., главный кардиолог МЗ
-
Низамов У.И. – заместитель директора по лечебной работе РСНПМЦК, PhD, кардиолог- консультант МЗ
-
Каримов А.М. – заместитель директора по филиалам РСНПМЦК, PhD, кардиолог- консультант МЗ
-
Курбанова Р.А. – заместитель главного врача РСНПМЦК
-
Толипова Ю.Ш. – доцент кафедры Кардиологии и геронтологии с курсом интервенционной кардологии и аритмологии Центра развития профессиональной квалификации медицинских работников, д.м.н., главный геронтолог МЗ
-
Ахматов Я.Р. – директор Каршинского филиала РСНПМЦК, к.м.н.
Список авторов:
-
Никишин А.Г. - доктор медицинских наук, руководитель лаборатории острого инфаркта миокарда Республиканского специализированного кардиологического научно- практического медицинского центра (РИКИАТМ) Министерства здравоохранения Республики Узбекистан.
-
Абдуллаева С.Я. - кандидат медицинских наук, научный сотрудник лаборатории острого инфаркта миокарда Республиканского специализированного кардиологического научно-практического медицинского центра (РИКИАТМ) Министерства здравоохранения Республики Узбекистан.
-
Якуббеков Н.Т. - кандидат медицинских наук, Республиканский научно-практический центр спортивной медицины. Заместитель директора по лечению.
Рецензенты:
-
Э.У. Асимбекова – ведущий научный сотрудник клинико-диагностического отделения Центра сердечно-сосудистой хирургии имени Бакулева Минздрава РФ, доктор медицинских наук.
-
А.Х. Абдуллаев – заведующий лабораторией реабилитации Республиканского центра специализированной терапии и медицинской реабилитации Министерства здравоохранения Республики Узбекистан, доктор медицинских наук.
Клинический протокол обсужден и рекомендован к утверждению путем достижения неформального консенсуса на заключительном Совещании рабочей группы с участием профессорско-преподавательского состава высших учебных заведений, членов ассоциации кардиологов Узбекистана, организаторов здравоохранения (коллектива ГУ РСНПМЦК и их заместителей), в онлайн-формате 1 ноября 2023 г.
Руководитель рабочей группы – к.м.н. Фозилов Х.Г,, директор РСНПМЦК, главный кардиолог МЗ
Клинический протокол рассмотрен и утвержден Ученым Советом Республиканского Специализированного Научно-Практического Медицинского Центра Кардиологии 25 сентября 2023 г., протокол №13.
Председатель Учёного Совета – к.м.н. Фозилов Х.Г.
Техническая экспертная оценка и редактирование:
-
Низамов У.И. – заместитель директора по лечебной работе РСНПМЦК, PhD, кардиолог- консультант МЗ
-
Каримов А.М. – заместитель директора по филиалам РСНПМЦК, PhD, кардиолог- консультант МЗ
Данный клинический протокол и стандарт был разработан при организационной и методической поддержки специалистов Министерства здравоохранения Республики Узбекистан под руководством заместителя министра д.м.н., Ф.Р. Шарипова, Начальника управления медицинского страхования Ш. Алмарданова, начальника отдела разработки клинических протоколов и стандартов д.м.н. С.А. Убайдуллаевой, Главных специалистов отдела разработки клинических протоколов и стандартов Ш.Р. Нуримова, С. Усманова и Г. Джумаевой.
Сокращения, используемые в протоколе:
Стент для коронарных артерий (КА) металлический непокрытый*** (МС) (голометаллический стент) — стент, представляющий собой металлический каркас из биологически инертного материала.
Доказательная медицина — надлежащее, последовательное и осмысленное использование современных наилучших доказательств (результатов клинических исследований) в процессе принятия решений о состоянии здоровья и лечении пациента.
Заболевание — возникающее в связи с воздействием патогенных факторов нарушение деятельности организма, работоспособности, способности адаптироваться к изменяющимся условиям внешней и внутренней среды при одновременном изменении защитно-компенсаторных и защитно-приспособительных реакций и механизмов организма.
Инструментальная диагностика — диагностика с использованием для обследования пациента различных приборов, аппаратов и инструментов.
Исход — любой возможный результат, возникающий от воздействия причинного фактора, профилактического или терапевтического вмешательства, все установленные изменения состояния здоровья, возникающие как следствие вмешательства.
Конфликт интересов — ситуация, при которой у медицинского или фармацевтического работника при осуществлении ими профессиональной деятельности возникает личная заинтересованность в получении лично либо через представителя компании материальной выгоды или иного преимущества, которое влияет или может повлиять на надлежащее исполнение ими профессиональных обязанностей вследствие противоречия между личной заинтересованностью медицинского работника или фармацевтического работника и интересами пациента.
Клиническое исследование — любое исследование, проводимое с участием человека в качестве субъекта для выявления или подтверждения клинических и/или фармакологических эффектов исследуемых продуктов и/или выявления нежелательных реакций на исследуемые продукты, и/или изучения их всасывания, распределения, метаболизма и выведения с целью оценить их безопасность и/или эффективность. Термины “клиническое испытание” и “клиническое исследование” являются синонимами.
Лабораторная диагностика — совокупность методов, направленных на анализ исследуемого материала с помощью различного специализированного оборудования.
Лекарственные препараты — лекарственные средства в виде лекарственных форм, применяемые для профилактики, диагностики, лечения заболевания, реабилитации, для сохранения, предотвращения или прерывания беременности.
Медицинское вмешательство — выполняемые медицинским работником и иным работником, имеющим право на осуществление медицинской деятельности, по отношению к пациенту, затрагивающие физическое или психическое состояние человека и имеющие профилактическую, диагностическую, лечебную, реабилитационную или исследовательскую направленность виды медицинских обследований и (или) медицинских манипуляций, а также искусственное прерывание беременности.
Острый инфаркт миокарда (ИМ) — острое повреждение (некроз) миокарда вследствие ишемии, подтвержденное характерной динамикой уровня биомаркеров в крови.
Доказательная медицина — надлежащее, последовательное и осмысленное использование современных наилучших доказательств (результатов клинических исследований) в процессе принятия решений о состоянии здоровья и лечении пациента.
Заболевание — возникающее в связи с воздействием патогенных факторов нарушение деятельности организма, работоспособности, способности адаптироваться к изменяющимся условиям внешней и внутренней среды при одновременном изменении защитно-компенсаторных и защитно-приспособительных реакций и механизмов организма.
Инструментальная диагностика — диагностика с использованием для обследования пациента различных приборов, аппаратов и инструментов.
Исход — любой возможный результат, возникающий от воздействия причинного фактора, профилактического или терапевтического вмешательства, все установленные изменения состояния здоровья, возникающие как следствие вмешательства.
Конфликт интересов — ситуация, при которой у медицинского или фармацевтического работника при осуществлении ими профессиональной деятельности возникает личная заинтересованность в получении лично либо через представителя компании материальной выгоды или иного преимущества, которое влияет или может повлиять на надлежащее исполнение ими профессиональных обязанностей вследствие противоречия между личной заинтересованностью медицинского работника или фармацевтического работника и интересами пациента.
Клиническое исследование — любое исследование, проводимое с участием человека в качестве субъекта для выявления или подтверждения клинических и/или фармакологических эффектов исследуемых продуктов и/или выявления нежелательных реакций на исследуемые продукты, и/или изучения их всасывания, распределения, метаболизма и выведения с целью оценить их безопасность и/или эффективность. Термины “клиническое испытание” и “клиническое исследование” являются синонимами.
Лабораторная диагностика — совокупность методов, направленных на анализ исследуемого материала с помощью различного специализированного оборудования.
Лекарственные препараты — лекарственные средства в виде лекарственных форм, применяемые для профилактики, диагностики, лечения заболевания, реабилитации, для сохранения, предотвращения или прерывания беременности.
Медицинское вмешательство — выполняемые медицинским работником и иным работником, имеющим право на осуществление медицинской деятельности, по отношению к пациенту, затрагивающие физическое или психическое состояние человека и имеющие профилактическую, диагностическую, лечебную, реабилитационную или исследовательскую направленность виды медицинских обследований и (или) медицинских манипуляций, а также искусственное прерывание беременности.
Острый инфаркт миокарда (ИМ) — острое повреждение (некроз) миокарда вследствие ишемии, подтвержденное характерной динамикой уровня биомаркеров в крови.
Острый коронарный синдром (ОКС) — термин, обозначающий любую группу клинических признаков или симптомов, позволяющих подозревать острый ИМ или нестабильную стенокардию.
Операция коронарного шунтирования (КШ) — наложение обходного анастомоза, позволяющего улучшить кровоток дистальнее гемодинамически значимого стеноза в КА. В зависимости от методики включает аортокоронарное, маммарокоронарное и другие виды шунтирования.
Состояние — изменения организма, возникающие в связи с воздействием патогенных и (или) физиологических факторов и требующие оказания медицинской помощи.
Синдром — устойчивая совокупность ряда симптомов с единым патогенезом.
Стент для КА, выделяющий лекарственное средство*** (СЛП) — стент, из структур которого выделяется антипролиферативное вещество, препятствующее образованию неоинтимы и за счет этого способствующее замедлению повторного стенозирования.
Уровень достоверности доказательств (УДД) — степень уверенности в том, что найденный эффект от применения медицинского вмешательства является истинным. [4].
Уровень убедительности рекомендаций (УУР) — степень уверенности в достоверности эффекта вмешательства и в том, что следование рекомендациям принесет больше пользы, чем вреда в конкретной ситуации [4].
Хирургическое лечение — метод лечения заболеваний путем разъединения и соединения тканей в ходе хирургической операции.
Чрескожное коронарное вмешательство (ЧКВ) — восстановление кровотока в стенозированном участке КА с использованием чрескожного введения необходимых для этого устройств. Включает чрескожную баллонную ангиопластику, коронарное стентирование и другие, менее распространенные методики. Как правило, если не указано иное, под ЧКВ подразумевают коронарное стентирование.
Операция коронарного шунтирования (КШ) — наложение обходного анастомоза, позволяющего улучшить кровоток дистальнее гемодинамически значимого стеноза в КА. В зависимости от методики включает аортокоронарное, маммарокоронарное и другие виды шунтирования.
Состояние — изменения организма, возникающие в связи с воздействием патогенных и (или) физиологических факторов и требующие оказания медицинской помощи.
Синдром — устойчивая совокупность ряда симптомов с единым патогенезом.
Стент для КА, выделяющий лекарственное средство*** (СЛП) — стент, из структур которого выделяется антипролиферативное вещество, препятствующее образованию неоинтимы и за счет этого способствующее замедлению повторного стенозирования.
Уровень достоверности доказательств (УДД) — степень уверенности в том, что найденный эффект от применения медицинского вмешательства является истинным. [4].
Уровень убедительности рекомендаций (УУР) — степень уверенности в достоверности эффекта вмешательства и в том, что следование рекомендациям принесет больше пользы, чем вреда в конкретной ситуации [4].
Хирургическое лечение — метод лечения заболеваний путем разъединения и соединения тканей в ходе хирургической операции.
Чрескожное коронарное вмешательство (ЧКВ) — восстановление кровотока в стенозированном участке КА с использованием чрескожного введения необходимых для этого устройств. Включает чрескожную баллонную ангиопластику, коронарное стентирование и другие, менее распространенные методики. Как правило, если не указано иное, под ЧКВ подразумевают коронарное стентирование.
Шкала уровня доказательности, на основе доказательной медицины.
В настоящем протоколе приведены доступные к настоящему дню клинические доказательства, моменты надлежащей практики, а также мнения экспертов. Рекомендации включают в себя материалы таких ведущих организаций, как Всемирная организация здравоохранения (WHO), Европейское общество кардиологов (ESC). Была проведена адаптация к местным условиям. Основным требованием при разработке протокола, включившего данные, основанные на лучшем мировом опыте, было использование материалов лучших руководств по данной теме, а также методологии строго отбора научных данных при формировании рекомендаций.
Таблица 1
Шкала оценки классов рекомендаций Европейского общества кардиологов
Шкала оценки классов рекомендаций Европейского общества кардиологов
|
Классы рекомендаций
|
Определение
|
Предлагаемая формулировка
|
|
Класс I |
Данные и/или всеобщее согласие, что конкретный метод лечения или вмешательство полезны, эффективны, имеют преимущества.
|
Рекомендуется/ показан
|
|
Класс II
|
Противоречивые данные и/или расхождение мнений о пользе/эффективности конкретного метода лечения или процедуры.
|
|
|
Класс IIa
|
Большинство данных/мнений говорит о пользе/ эффективности.
|
Целесообразно применять
|
|
Класс IIb
|
Данные/мнения не столь убедительно говорят о пользе/эффективности.
|
Можно применять
|
|
Класс III |
Данные и/или всеобщее согласие, что конкретный метод лечения или вмешательство не являются полезной или эффективной, а в некоторых случаях могут приносить вред.
|
Не рекомендуется |
Таблица 2
Шкала оценки уровней достоверности доказательств Европейского общества кардиологов
|
А
|
Данные многочисленных рандомизированных клинических исследований или метаанализов
|
|
B
|
Данные получены по результатам одного рандомизированного клинического исследования или крупных нерандомизированных исследований
|
|
C
|
Согласованное мнение экспертов и/или результаты небольших исследований, ретроспективных исследований, регистров
|
ПРИЛОЖЕНИЯ
Приложение 1. Причины повышения уровня сердечного тропонина в крови
Приложение 1. Причины повышения уровня сердечного тропонина в крови
|
Повреждение (некроз) миокарда из-за острой ишемии миокарда
- Изъязвление/разрыв атеросклеротической бляшки с тромбозом |
|
|
Повреждение (некроз) миокарда из-за острой ишемии миокарда за счет дисбаланса потребности и доставки кислорода
|
|
|
Снижение перфузии миокарда:
- Спазм КА - Дисфункция микрососудов - Эмболия в КА - Диссекция КА - Устойчивая брадиаритмия - Гипотония или шок - Дыхательная недостаточность - Тяжелая анемия |
Повышение потребности миокарда в кислороде:
- Устойчивая тахиаритмия - Тяжелая гипертония с или безгипертрофии ЛЖ |
|
Другие причины повреждения (некроза) миокарда
|
|
|
Сердечные причины:
- Сердечная недостаточность - Миокардит - Кардиомиопатия (любая) - Синдром Такоцубо - Процедуры реваскуляризации миокарда - Другие вмешательства на сердце - Катетерная аблация - Дефибрилляция - Контузия сердца |
Несердечные причины:
- Сепсис, инфекционное заболевание - ХБП - Инсульт - Субарахноидальное кровоизлияние - ТЭЛА, легочная гипертензия - Инфильтративные заболевания - Химиотерапевтические препараты - Критические состояния - Тяжелая физическая нагрузка |
Приложение 2. Оценка риска смерти в стационаре по критериям группы TIMI
|
Фактор риска
|
Число
баллов |
|
Возраст ≥75 лет
|
3
|
|
Возраст 65-74 года
|
2
|
|
САД <100 мм рт.ст.
|
3
|
|
ЧСС >100 уд/мин
|
2
|
|
Класс по KillipII-IV
|
2
|
|
Подъемы сегмента ST передней локализации или блокада ЛНПГ
|
1
|
|
СД, АГ или стенокардия в анамнезе
|
1
|
|
Масса тела <67 кг
|
1
|
|
Время начала лечения >4 часов от появления симптомов
|
1
|
|
Сумма баллов
|
Риск наступления летального исхода в ближайшие 30 суток*
|
|
0
|
0,8%
|
|
1
|
1,6%
|
|
2
|
2,2%
|
|
3
|
4,4%
|
|
4
|
7,3%
|
|
5
|
12,4%
|
|
6
|
16,1%
|
|
7
|
23,4%
|
|
8
|
26,8%
|
|
> 8
|
35,9%
|
Примечание: * - при условии проведения ТЛТ.
Приложение 3. Оценка риска смерти в стационаре с использованием шкалы GRACE.
|
Фактор риска
|
Число баллов
|
|
|
Возраст (лет)
|
|
|
|
≤30
|
0
|
|
|
30-39
|
8
|
|
|
40-49
|
25
|
|
|
50-59
|
41
|
|
|
60-69
|
58
|
|
|
70-79
|
75
|
|
|
80-89
|
91
|
|
|
≥90
|
100
|
|
|
ЧСС (ударов в минуту)
|
|
|
|
≤50
|
0
|
|
|
50-69
|
3
|
|
|
70-89
|
9
|
|
|
90-109
|
15
|
|
|
110-149
|
24
|
|
|
150-199
|
38
|
|
|
≥200
|
46
|
|
|
Систолическое АД (мм рт. ст.)
|
|
|
|
≤80
|
58
|
|
|
80-99
|
53
|
|
|
100-119
|
43
|
|
|
120-139
|
34
|
|
|
140-159
|
24
|
|
|
160-199
|
10
|
|
|
≥200
|
0
|
|
|
Класс по Killip
|
|
|
|
I
|
0
|
|
|
II
|
20
|
|
|
III
|
39
|
|
|
IV
|
59
|
|
|
Уровень креатинина в крови (мг/дл)
|
|
|
|
0-0,39
|
1
|
|
|
0,40-0,79
|
4
|
|
|
0,80-1,19
|
7
|
|
|
1,20-1,59
|
10
|
|
|
1,60-1,99
|
13
|
|
|
2,0-3,99
|
21
|
|
|
≥4,0
|
28
|
|
|
Другие факторы
|
|
|
|
Остановка сердца при поступлении
|
39
|
|
|
Смешения сегмента ST, инверсии зубца T
|
28
|
|
| Повышенный уровень маркеров некроза миокарда в крови* | 14 | |
|
Риск смерти в стационаре
|
Сумма баллов
|
|
|
Низкий (<1%)
|
≤125
|
|
|
Умеренный (1-3%)
|
126-154
|
|
|
Высокий (>3%)
|
≥155
|
|
Примечание: * при создании данной шкалы использовали сердечный тропонин «обычной» чувствительности.
Приложение 4. Оценка риска крупных кровотечений в стационаре с использованием шкалыCRUSADE
|
Фактор риска
|
Число баллов
|
|
ЧСС (уд/мин)
|
|
|
≤ 70
|
0
|
|
71—80
|
1
|
|
81—90
|
3
|
|
91—100
|
6
|
|
101—110
|
8
|
|
111—120
|
10
|
|
> 120
|
11
|
|
Систолическое АД (мм рт. ст.)
|
|
|
≤ 90
|
10
|
|
91—100
|
8
|
|
101—120
|
5
|
|
121—180
|
1
|
|
181—200
|
3
|
|
≥ 201
|
5
|
|
Гематокрит (%)
|
|
|
≤ 31,0
|
9
|
|
31,0—33,9
|
7
|
|
34,0—36,9
|
3
|
|
37,0—39,9
|
2
|
|
≥ 40,0
|
0
|
|
Клиренс креатинина (мл/мин)
|
|
|
≤ 15
|
39
|
|
> 15—30
|
35
|
|
> 30—60
|
28
|
|
> 60—90
|
17
|
|
> 90—120
|
7
|
|
> 120
|
0
|
|
Другие факторы
|
|
|
Женский пол
|
8
|
|
Сердечная недостаточность
|
7
|
|
Другое сосудистое заболевание
|
6
|
|
Сахарный диабет
|
6
|
|
Риск крупного кровотечения в стационаре
|
Сумма баллов
|
|
Очень низкий (3,1%)
|
≤ 20
|
|
Низкий (5,5%)
|
21—30
|
|
Умеренный (8,6%)
|
31—40
|
|
Высокий (11,9%)
|
41—50
|
|
Очень высокий (19,5%)
|
> 50
|
Приложение 5. Классификация острой сердечной недостаточности по Killip
|
Класс
|
Признаки
|
Госпитальная смертность*
|
|
I
|
Нет признаков сердечной недостаточности
|
2-3%
|
|
II
|
III тон, влажные хрипы в нижних отделах легких
|
5-12%
|
|
III
|
Отек легких, влажные хрипы выше углов лопаток
|
10-20%
|
|
IV
|
Кардиогенный шок
|
50-81%
|
*По Khot U. N. et al.
Приложение 6. Характеристика тромболитиков
|
ХАРАКТЕРИСТИКИ
|
АЛТЕПЛАЗА
|
ТЕНЕКТЕПЛАЗА
|
ПРОУРОКИНАЗА
|
СТАФИЛОКИНАЗА
|
СТРЕПТОКИНАЗА
|
|
Происхождение
|
рекомбинантная ДНК
|
рекомбинантная ДНК
|
рекомбинантная ДНК
|
pекомбинантный белок содержащий аминокислотную последовательность стафилокиназы
|
стрептококк группы C
|
|
Период полувыведения, мин
|
4–8
|
18–20
|
ОКОЛО 40
|
5,77 + 0,72
|
23–29
|
|
Метаболизм
|
ПЕЧЕНЬ
|
ПЕЧЕНЬ
|
ПЕЧЕНЬ
|
ПЕЧЕНЬ
|
ПЕЧЕНЬ
|
|
Способ применения
|
внутривенно в дозе 100 мг; сначала в дозе 15 мг болюсом, затем по 0,75 мг/кг массы тела в течение 30 мин., затем по 0,5 мг/кг массы тела в течение 60 мин
|
однократное внутривенное введение болюсом в дозе30–50 мг (0,5 мг/кг массы тела)
|
внутривенно болюсно по 2 млнме, затем в дозе
6 млн МЕ в видеинфузии в течение 60 мин |
однократное внутривенное введение болюсом в дозе 15 мг
|
внутривенная инфузия 1,5 млн ед в течение 60 мин)
|
|
Дополнительная антитромботическая терапия
|
аск внутрь в дозе 325 мг/сут, внутривенно
гепарин |
аск внутрь в дозе 325 мг/сут, внутривенно гепарин
|
аск внутрь в дозе325 мг/сут, внутривенно гепарин
|
аск внутрь в дозе 325 мг/сут, внутривенно гепарин
|
аск внутрь в дозе 325 мг/сут
|
|
Антигенность
|
нет
|
+
|
+
|
нет
|
+++
|
|
Специфичность для фибрина
|
++
|
+++
|
++
|
++++
|
НЕТ
|
|
Риск развития геморрагического инсульта
|
++
|
++
|
++
|
+
|
+
|
|
Риск развития системного кровотечения
|
++
|
+
|
++
|
+
|
+++
|
|
Эффективность восстановления нарушения
кровотока через 90 мин |
+++
|
+++
|
+++
|
+++
|
++
|
Приложение 7. Антитромботические средства при ИМпST
|
Препарат
|
Рекомендации по применению
|
|
Антиагреганты
|
|
|
АСК**
|
Внутрь; у ранее регулярно не принимавших первая доза 250 мг (разжевать и проглотить), со 2-х суток по 75-100 мг 1 раз/сут.
|
|
Клопидогрел**
|
Сопровождение первичного ЧКВ: внутрь; первая доза 600 мг (как можно быстрее), затем 75 мг 1 раз/сут (после стентирования у больных без
высокого риска кровотечений на 2-7-е сутки возможно применение в дозе 150 мг 1 раз/сут). Сопровождение ТЛТ: внутрь; первая доза 300 мг или 75 мг у больных старше 75 лет, со 2-х суток по 75 мг 1 раз/сут. Сопровождение ЧКВ вскоре после ТЛТ:в первые 24 ч от введения тромболитика не получившим нагрузочной дозы клопидогрела** принять 300 мг; после 24 ч от введения тромболитика не получившим нагрузочной дозы клопидогрела** принять 600 мг, получившим нагрузочную дозу 300 мг в первые сутки принять еще 300 мг Отсутствие реперфузионного лечения: внутрь; 75 мг 1 раз/сут; перед ЧКВ в более поздние сроки заболевания нагрузочная доза 600мг. |
|
Празугрел
|
Сопровождение первичного ЧКВ: внутрь; первая доза 60 мг, далее10 мг 1 раз в сутки.
|
|
Тикагрелор
|
Сопровождение первичного ЧКВ: внутрь; первая доза 180 мг, через12 часов по 90 мг 2 раза/сут (можно использовать у получивших нагрузочную дозу клопидогрела**).
|
|
Блокаторы ГП IIb/IIIa рецепторов тромбоцитов (используются для сопровождения ЧКВ)
|
|
|
Руциромаб (Монофрам®)^^^
|
В/в; 0,25 мг/кг в течение 3-5 мин за 10-30 мин до ЧКВ.
|
|
Антикоагулянты для парентерального введения^^
|
|
|
Рефракционированный гепарин
(гепарин натрия)** |
Сопровождение ТЛТ и другие показания к использованию лечебных доз антикоагулянтов: внутривенно; болюсом 60 ЕД/кг (максимально 4000 ЕД) сразу вслед за этим постоянная инфузия 12 ЕД/кг/ч (максимально 1000 ЕД/ч), в последующем подбор дозы, обеспечивающей увеличение АЧТВ до 50-70 секунд или в 1,5–2 раза выше контрольной величины для конкретной лаборатории (верхняя граница нормы или среднее нормальное значение у здоровых лиц); при сочетании с ТЛТ АЧТВ следует определить через 3, 6, 12 и 24 часа после начала инфузии НФГ**, длительность инфузии 24-48 часов.
Сопровождение ЧКВ: в/в болюсом 70-100 ЕД/кг, при необходимости повторно с целью поддерживать активированное время свертывания крови 250-350 сек; в сочетании с блокаторами гликопротеина IIb/IIIa тромбоцитов первый болюс 50-60 ЕД/кг, при необходимости повторно с целью поддерживать активированное время свертывания крови 200-250 сек. Первое определение АВС через 2-5 мин после болюса НФГ, затем каждые 20-30 мин на протяжении всей процедуры ЧКВ. При необходимости дополнительные болюсные введения НФГ 20 МЕ/кг. Применение НФГ** прекращается после успешного окончания процедуры. Устройство для введения катетеров может быть удалено из бедренной артерии через 4-6 ч при значениях АВС ≤150 с или раньше, если используется доступ через лучевую артерию. Профилактика венозного тромбоза и ТЭЛА: под кожу живота 5000ЕД 2-3 раз/сут, если нет необходимости в более высоких дозах антикоагулянтов (контроля АЧТВ не требуется). |
|
ивалирудин
|
Сопровождение первичного ЧКВ: в/в болюсом 0,75 мг/кг с последующей инфузией1,75 мг/кг/ч во время процедуры (при необходимости инфузию можно продолжить в той же дозе в течение4 ч, а затем в дозе 0,25 мг/кг/ч вплоть до 12 ч); при сниженном клиренсе креатинина скорость инфузии следует уменьшить в соответствии с инструкцией к препарату. У больных с клиренсом креатинина 30- 59 мл/мин размер болюса остается прежним, а скорость инфузии следует уменьшить до 1,4 мг/кг/ч; у больных с клиренсом креатинина <30 мл/мин или находящихся на диализе, бивалирудин противопоказан.
|
|
Эноксапарин натрия**
|
Сопровождение ТЛТ (у мужчин с уровнем креатинина в крови <2,5 мг/дл (221 мкмоль/л) и женщин с уровнем креатинина в крови <2,0 мг/дл (177 мкмоль/л): в/в болюс 30 мг; через 15 мин п/к живота в дозе1 мг/кг 2 раза/сут до 8-го дня болезни или выписки из стационара, если она произошла раньше (первые 2 дозы для п/к введения не должны превышать 100 мг). У лиц ≥75 лет первоначальная в/в доза препарата не вводится, а поддерживающая уменьшается до 0,75 мг/кг(первые 2 дозы не должны превышать 75 мг). При сниженной функции почек (клиренс креатинина <30 мл/мин) препарат вводится п/к в дозе 1 мг/кг один раз/сут вне зависимости от возраста.
Сопровождение первичного ЧКВ: в/в болюсом 0,5 мг/кг, при процедуре длительностью более 2 часов дополнительный болюс 0,25мг/кг. ЧКВ на фоне начатого введения лечебных доз эноксапарина натрия**: если после п/к инъекции препарата прошло не более 8 ч, дополнительного введения антикоагулянтов не требуется (если была сделана только одна подкожная инъекция эноксапарина натрия** – перед процедурой ввести в/в болюсом 0,3 мг/кг), после 12 ч от последней инъекции вовремя ЧКВ можно использовать любой антикоагулянт (в том числе эноксапарин натрия** в/в болюсом в дозе0,5-0,75 мг/кг). Устройство для введения катетеров может быть удалено из бедренной артерии через 6-8 ч после последней п/к инъекции эноксапарина натрия** и через 4 ч после в/в введения препарата. Профилактика венозного тромбоза и ТЭЛА: под кожу живота, 40 мг 1 раз/сут (если нет необходимости в болеевысоких дозах антикоагулянтов). |
|
Фондапаринукс натрия
|
Сопровождение ТЛТ стрептокиназой или отсутствие реперфузионного лечения (у больных с уровнем креатинина в крови <3,0 мг/дл или 265 мк моль/л): в/в болюсом 2,5 мг; со 2-х суток п/к живота в дозе 2,5 мг 1 раз/сут до 8-го дня болезни или выписки из стационара, если она произошла раньше. Противопоказан при клиренсе креатинина <20 мл/мин.
Профилактика венозного тромбоза и ТЭЛА: под кожу живота 2,5мг 1 раз/сут (если нет необходимости в более высоких дозах антикоагулянтов). |
Приложение 8. БАБ при ИМпST
|
Препарат
|
До за*
|
|
Лечение с 1-х суток заболевания
|
|
|
Метопролол
|
В/в медленно под контролем ЭКГ и АД по 5 мг 2-3 раза с интервалом как минимум 2 мин; через 15 мин после в/в введения внутрь до 50 мг каждые 6 ч в течение 48 ч, затем 2-3 раза/сут при применении меторолола сукцината или 1 раз/сут для пролонгированных лекарственных форм.
|
|
Пропранолол
|
В/в медленно под контролем АД и ЭКГ в дозе 0,1 мг/кг за 2- 3 приема с интервалами как минимум 2-3 мин; через 4 часа после в/в введения внутрь, обычная поддерживающая доза до 160 мг/сут за 4 приема.
|
|
Эсмолол
|
В/в инфузия под контролем ЭКГ и АД; нагрузочная доза 0,5 мг/кг в течение 1 мин, затем 0,05 мг/кг/мин в течение 4 мин, при недостаточном эффекте увеличение
|
|
|
скорости инфузии на 0,05 мг/кг/мин каждые 4 мин вплоть до 0,3 мг/кг/мин; если необходим более быстрый эффект, перед 2-м и 3-м увеличением дозы можно ввести дополнительные болюсы по 0,5 мг/кг. Гемодинамический эффект сохраняется 20–30 мин после прекращения введения. При переходе на прием других бета-адреноблокаторов внутрь через 1 ч после их первого назначения необходимо снизить дозу эсмолола на 50%; обычно эсмолол отменяют после перорального приема второй дозы бета-адреноблокатора, если за это время поддерживались надлежащие ЧСС и АД.
|
|
Лечение с более отдаленных сроков заболевания** &
|
|
|
Карведилол #
|
Внутрь; начальная доза 3,125-6,25 мг 2 раза/сут, при хорошей переносимости увеличение дозы с интервалом 3–10 суток до 25 мг 2 раза/сут.
|
|
Метопролол
|
Внутрь; начальная доза 12,5-25 мг 2-3 раза/сут, обычная поддерживающая доза до 200 мг за 2-3 приема (та же доза однократно при использовании пролонгированных лекарственных форм).
|
|
Бисопролол
|
Внутрь; начальная доза 1,125-2,5 мг 1 раза/сут, при хорошей переносимости увеличение дозы с интервалом 3–10 суток до 5-10 мг 1 раза/сут.
|
Приложение 9. Блокаторы ренин-ангиотензин-альдостероновой системы при ИМпST
|
Препарат
|
Доза*
|
|
Каптоприл
|
Внутрь; первая доза 6,25 мг, через 2 часа 12,5 мг, через 10-12 часов 25 мг; целевая доза 50 мг 2-3 раза/сут.
|
|
Лизиноприл
|
Внутрь; первая доза 5 мг, через 24 ч – 5 мг; целевая доза 10 мг 1 раз в сутки.
|
|
Зофеноприл
|
Внутрь; первая доза 7,5 мг, через 12 ч еще 7,5 мг, затем при систолическом АД >100 мм рт. ст. удвоение дозы каждые 12 ч до 30 мг 2 раза/сут; возможен более медленный режим титрования дозы – 7,5 мг 2 раза/сут в 1–2-е сутки, 15 мг 2 раза/сут на 3–4-е сутки, затем 30 мг 2 раза/сут.
|
|
Периндоприл&
|
Внутрь; 5 мг 1 раз/сут.
|
|
Рамиприл** &
|
Внутрь; начальная доза 1,25-2,5 мг; целевая доза 5 мг 2 раза/сут.
|
|
Трандолаприл**
|
Внутрь; начальная доза 0,5-1 мг; целевая доза 4 мг 1 раз/сут.
|
|
Эналаприл**
|
Внутрь; начальная доза 2,5 мг; целевая доза 10 мг 2 раза/сут.
|
|
Блокаторы рецептора ангиотензина II
|
|
|
Валсартан
|
Внутрь; первая доза 20 мг с постепенным увеличением до 160 мг 2 раза/сут.
|
|
Антагонисты альдостерона
|
|
|
Эплеренон#
|
Внутрь при уровне креатинина в крови у мужчин <2,5 мг/дл (220 мкмоль/л), <2,0 мг/дл (177 мкмоль/л) у женщин и уровень калия к крови <5 ммоль/л; первая доза 25 мг 1 раз/сут, при хорошей переносимости у больных, не принимающих амиодарон, дилтиазем или верапамил, в ближайшие 4 недели увеличение дозы до 50 мг 1 раз/сут.
|
Примечания: в пределах одной группы лекарственные средства перечислены по алфавиту; лечение иАПФ следует начать как можно раньше (с первых часов заболевания), как только стабилизируется гемодинамика (в частности, САД станет не <100 мм рт.ст.) и при отсутствии противопоказаний продолжать неопределенно долго;
* особенности подбора дозы у конкретного больного зависят от реакции АД, уровня креатинина и калия в крови; если достичь целевой дозы препарата не удается, следует использовать максимально переносимую дозу;
* особенности подбора дозы у конкретного больного зависят от реакции АД, уровня креатинина и калия в крови; если достичь целевой дозы препарата не удается, следует использовать максимально переносимую дозу;
Приложение 10. Нарушение функции почек и дозы антитромботических препаратов
|
Препарат
|
рСКФ 30-59 мл/мин/ 1,73 м2
|
рСКФ 15-29 мл/мин/ 1,73 м2
|
рСКФ <15 мл/мин/ 1,73 м2
|
|
Антитромбоцитарные препараты
|
|||
|
АСК
|
Обычная доза
|
Обычная доза
|
Обычная доза
|
|
Клопидогрел**
|
Обычная доза
|
Обычная доза
|
Использовать только в отдельных случаях (например, для профилактики тромбоза стента)
|
|
Прасугрел
|
|
|
Не рекомендуется
|
|
Тикагрелор**
|
Обычная доза
|
Обычная доза
|
Не рекомендуется
|
|
Руциромаб
|
Нет рекомендаций.
Учитывать общий риск геморрагических осложнений. |
||
|
Тирофибан
|
Обычная доза
|
Обычный болюс, уменьшить скорость инфузии до 0,05 мкг/кг/мин
|
Не рекомендуется
|
|
Антикоагулянты
|
|||
|
НФГ**
|
Обычная доза
|
Обычная доза
|
Обычная доза
|
|
Эноксапар ин натрия**
|
Обычная доза
|
Увеличить интервал между введением препаратов с 12 до 24 ч
|
Не рекомендуется
|
|
Фондапаринукс натрия
|
Обычная доза
|
Не рекомендуется при рСКФ <20 мл/мин/1,73 м2
|
Не рекомендуется
|
|
Бивалирудин
|
Обычная доза
|
Обычный болюс, уменьшить скорость инфузии до 1 мг/кг/ч
|
На диализе; обычный болюс, уменьшить скорость инфузии до 0,25 мг/кг/ч
|
|
Ривароксабан в дозе 2,5 мг 2 раза в сутки
|
Обычная доза
|
Обычная доза (использовать нежелательно)
|
Не рекомендуется
|
Приложение 11. Информированное согласие больного на медицинское вмешательство
Медицинское вмешательство – выполняемые медицинским работником по отношению к пациенту, затрагивающие физическое или психическое состояние человека и имеющие профилактическую, исследовательскую, диагностическую, лечебную, реабилитационную направленность виды медицинских обследований и (или) медицинских манипуляций.
1. Я,
(Ф.И.О. пациента или его законного представителя)
« » г. рождения, зарегистрированный(ая) по адресу
(адрес места жительства (пребывания) пациента либо его законного представителя
даю информированное согласие на предстоящее медицинское вмешательство в
(наименование медицинского учреждения)
2. В доступной для меня форме мне разъяснены возможные методы и варианты предстоящих медицинских вмешательств, их последствия, необходимость, цель и ожидаемые результаты предстоящего обследования, диагностики и/или лечения, в том числе вероятность развития осложнений, а также последствия отказа от медицинского вмешательства.
3. Я проинформирован, что точно предсказать результат и исход медицинского вмешательства невозможно. Я понимаю, что любое лечение или операция сопряжены с риском для жизни и могут привести к временной или постоянной, частичной или полной нетрудоспособности. Никакие гарантии относительно результатов медицинского вмешательства не предоставляются.
4. Я понимаю, что в процессе диагностических, лечебных и иных вариантов медицинских вмешательств могут возникнуть непредвиденные экстренные обстоятельства и осложнения, при которых я буду не в состоянии дать согласие на проведение необходимых экстренных действий (повторных операций или процедур). В таких ситуациях ход медицинского вмешательства может быть изменен врачами по их усмотрению.
5. Я знаю, что в целях максимальной эффективности предстоящего медицинского вмешательства я обязан поставить врача в известность о всех проблемах, связанных с моим здоровьем, наследственностью, в том числе об аллергических проявлениях, индивидуальной непереносимости лекарственных препаратов и продуктов питания, а также о курении табака, употреблении алкоголя, наркотических или токсических препаратов.
6. Я понимаю, что при проведении хирургического вмешательства возможна потеря крови и может возникнуть необходимость в переливании донорской крови или ее компонентов, на что я даю добровольное согласие. Я получил разъяснения от лечащего врача о цели переливания крови или ее компонентов, необходимости переливания, характере и особенностях процедуры, возможных последствиях, в случае развития которых я согласен на проведение всех нужных лечебных мероприятий. Я извещен о вероятном течении заболевания при отказе от переливания крови и ее компонентов.
7. Я согласен на запись моего лечебно-диагностического процесса на любые информационные носители, с использованием любых технических средств, а также на взятие у меня в диагностических и лечебных целях образцов биологических материалов, в том числе клеток, тканей, биологических жидкостей.
8. Мне разъяснено, что я имею право отказаться от одного или нескольких методов профилактики, диагностики, лечения и реабилитации при оказании медицинской помощи или потребовать его (их) прекращения, мне также разъяснены возможные последствия такого отказа.
9. Я разрешаю предоставлять информацию о моей болезни, прогнозе и лечении только:
4. Я понимаю, что в процессе диагностических, лечебных и иных вариантов медицинских вмешательств могут возникнуть непредвиденные экстренные обстоятельства и осложнения, при которых я буду не в состоянии дать согласие на проведение необходимых экстренных действий (повторных операций или процедур). В таких ситуациях ход медицинского вмешательства может быть изменен врачами по их усмотрению.
5. Я знаю, что в целях максимальной эффективности предстоящего медицинского вмешательства я обязан поставить врача в известность о всех проблемах, связанных с моим здоровьем, наследственностью, в том числе об аллергических проявлениях, индивидуальной непереносимости лекарственных препаратов и продуктов питания, а также о курении табака, употреблении алкоголя, наркотических или токсических препаратов.
6. Я понимаю, что при проведении хирургического вмешательства возможна потеря крови и может возникнуть необходимость в переливании донорской крови или ее компонентов, на что я даю добровольное согласие. Я получил разъяснения от лечащего врача о цели переливания крови или ее компонентов, необходимости переливания, характере и особенностях процедуры, возможных последствиях, в случае развития которых я согласен на проведение всех нужных лечебных мероприятий. Я извещен о вероятном течении заболевания при отказе от переливания крови и ее компонентов.
7. Я согласен на запись моего лечебно-диагностического процесса на любые информационные носители, с использованием любых технических средств, а также на взятие у меня в диагностических и лечебных целях образцов биологических материалов, в том числе клеток, тканей, биологических жидкостей.
8. Мне разъяснено, что я имею право отказаться от одного или нескольких методов профилактики, диагностики, лечения и реабилитации при оказании медицинской помощи или потребовать его (их) прекращения, мне также разъяснены возможные последствия такого отказа.
9. Я разрешаю предоставлять информацию о моей болезни, прогнозе и лечении только:
(доверенные лица)
10. Я ознакомлен со всеми пунктами настоящего документа, они мне понятны, о чем свидетельствует моя подпись ниже.
Подпись Дата « » г.
10. Я ознакомлен со всеми пунктами настоящего документа, они мне понятны, о чем свидетельствует моя подпись ниже.
Подпись Дата « » г.
Организационные аспекты протокола:
Конфликт интересов отсутствует
Данные экспертов (специалистов республики и зарубежных стран):
1. Никишин А.Г. - доктор медицинских наук, руководитель лаборатории острого инфаркта миокарда Республиканского специализированного кардиологического научно-практического медицинского центра (РИКИАТМ) Министерства здравоохранения Республики Узбекистан.
2. Абдуллаева С.Я. - кандидат медицинских наук, научный сотрудник лаборатории острого инфаркта миокарда Республиканского специализированного кардиологического научно-практического медицинского центра (РИКИАТМ) Министерства здравоохранения Республики Узбекистан.
3. Якуббеков Н.Т. - кандидат медицинских наук, Республиканский научно-практический центр спортивной медицины. Заместитель директора по лечению.
Условия пересмотра протокола: планируемая дата обновления 2026 г., или по мере появления новых ключевых доказательств
Конфликт интересов отсутствует
Данные экспертов (специалистов республики и зарубежных стран):
1. Никишин А.Г. - доктор медицинских наук, руководитель лаборатории острого инфаркта миокарда Республиканского специализированного кардиологического научно-практического медицинского центра (РИКИАТМ) Министерства здравоохранения Республики Узбекистан.
2. Абдуллаева С.Я. - кандидат медицинских наук, научный сотрудник лаборатории острого инфаркта миокарда Республиканского специализированного кардиологического научно-практического медицинского центра (РИКИАТМ) Министерства здравоохранения Республики Узбекистан.
3. Якуббеков Н.Т. - кандидат медицинских наук, Республиканский научно-практический центр спортивной медицины. Заместитель директора по лечению.
Условия пересмотра протокола: планируемая дата обновления 2026 г., или по мере появления новых ключевых доказательств
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.