Нейрофиброматоз у детей
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Нейрофиброматоз [незлокачественный] (Q85.0)
Онкология детская, Педиатрия
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «19» марта 2025 года
Протокол №228
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
НЕЙРОФИБРОМАТОЗ У ДЕТЕЙ
Нейрофиброматоз 1 типа (болезнь фон Реклингхаузена) – заболевание, наследуемое аутосомно-доминантно, характеризуещееся множественными пигментированными пятнами на коже цвета «кофе с молоком», пигментацией по типу «веснушек» на кожных складках (лентигинозными пятнами, которые возникают в местах, не подвергающихся воздействию солнца), доброкачественными новообразованиями (нейрофибромами, опухолями центральной нервной системы), костными аномалиями, изменениями радужной оболочки глаза (узелки Лиша) и целого ряда других симптомов[2]. Заболевание обусловлено мутацией гена NF1 на длинном плече 17 хромосомы (17q11.2) и кодирует синтез нейрофибромина.
Дата разработки протокола: 2023 год.
Категория пациентов: дети.
Нейрофиброматозы – группа наследственных заболеваний с аутосомно-доминантным типом наследования и полной пенетрантностью. Общим клиническим проявлением нейрофиброматозов является формирование множественных опухолей в тканях нейроэктодермального происхождения.
В настоящее время группа объединяет три типа нозологий, имеющих различную генетическую природу: нейрофиброматоз 1 типа (НФ1), нейрофиброматоз 2 типа и шванноматоз[1].
Нейрофиброматоз 1 типа (болезнь фон Реклингхаузена) – заболевание, наследуемое аутосомно-доминантно, характеризуещееся множественными пигментированными пятнами на коже цвета «кофе с молоком», пигментацией по типу «веснушек» на кожных складках (лентигинозными пятнами, которые возникают в местах, не подвергающихся воздействию солнца), доброкачественными новообразованиями (нейрофибромами, опухолями центральной нервной системы), костными аномалиями, изменениями радужной оболочки глаза (узелки Лиша) и целого ряда других симптомов[2]. Заболевание обусловлено мутацией гена NF1 на длинном плече 17 хромосомы (17q11.2) и кодирует синтез нейрофибромина.
Кожная/дермальная/локализованная/спорадическая нейрофиброма – самый распространенный тип (90%), возникает из мелких кожных нервов.
Локализованная интраневральная нейрофиброма – второй по распространенности тип нейрофибромы, злокачественные изменения редки.
Подкожная, внутримышечная нейрофибромы – встречается часто.
Диффузная нейрофиброма (поверхностная) – встречается нечасто, одиночные поражения, не связанные с каким-либо наследственным заболеванием (редко связанные с NF1), редкое злокачественное изменение.
Пигментная нейрофиброма – редкая форма, нет повышенного риска злокачественной трансформации.
ПН – является патогномоничным для нейрофиброматоза 1 типа (НФ 1), возникает из нескольких нервных пучков, до 5% риск злокачественной трансформации.
Глубокие ПН – около 60% случаев, чаще имеют узловое строение [6].
Поверхностные ПН – чаще диффузные, вовлекают кожу. Кожа над ПН может быть гипертрофирована, утолщена и/или гиперпигментирована.
Озлокачествление ПН может привести к развитию злокачественной опухоли оболочки периферических нервов (ЗООПН), которые имеют неблагоприятный прогноз:
характеризуются высокой частотой метастазирования. Часто вскоре после трансформации отмечаются метастазы в легкие;
вносят значимый вклад в смертность при НФ1 по причине высокой частоты рецидивирования, низкой частоты ответа на лечение, быстрого прогрессирования и высокой смертности;
5-летняя выживаемость у пациентов с НФ1 и ЗООПН и составляет 35–50%[7].
Нейрофиброматоз 2 типа – аутосомно-доминантное наследственное заболевание, которое наследуется или возникает спонтанно, характеризующееся образованием множественных доброкачественных опухолей, преимущественно шванном и менингиом, локализующихся в центральной нервной системе и по ходу периферических нервов. Заболевание обусловлено мутацией гена NF2 на длинном плече 22 хромосомы (22q12), кодирующего синтез белка мерлина который на клеточном уровне тормозит опухолевый рост клеточных мембран[3].
Шванноматоз – редкая форма нейрофиброматоза, характеризующаяся развитием множественных шванном (опухоли нервных оболочек) в спинном мозге и на периферических нервах, но несоответствующая критериям нейрофиброматоза 2 типа[4]. Заболевание обусловлено мутацией гена LZTR1, SMARCB1 – гене-суппрессоре опухолевого роста, который локализуется на длинном плече 22 хромосомы (22q11.23).
Код(ы) МКБ-10
Вводная часть
Код(ы) МКБ-10
|
Код
|
Название |
| Q85.0 | Нейрофиброматоз (незлокачественный) |
Дата разработки протокола: 2023 год.
Пользователи протокола: врачи общей практики, педиатры, детские онкологи и гематологи, детские неврологи, офтальмологи, оториноларингологи, хирурги.
Категория пациентов: дети.
Сокращения, используемые в протоколе:
ГЗП – Глиомы зрительного пути
ЗООПН – злокачественные опухоли оболочек периферических нервов;
КТ – Компьютерная томография;
МРТ – Магнитно-резонансная томография;
НФ – Нейрофиброматоз;
НФ1 – Нейрофиброматоз 1 типа;
НФ2 – Нейрофиброматоз 2 типа;
НЯО – Неопознанные яркие объекты;
ПН – Плексиформная нейрофиброма;
ПЭТ – Позитронно-эмисионная томография;
УЗИ – Ультразвуковое исследование;
РГ – Рентгенография;
РКИ – Рандомизированное клиническое исследование;
ШВН – Шванноматоз;
ЭКГ – Электрокардиограмма;
ЭхоКГ – Эхокардиография;
Шкала уровня доказательности:
Шкала уровня доказательности:
| А |
Высококачественный мета-анализ, систематический обзор рандомизированных
клинических исследований (РКИ) или крупное РКИ с очень низкой вероятностью
(++) систематической ошибки, результаты которых могут быть распространены на
соответствующую популяцию.
|
| В |
Высококачественный (++) систематический обзор когортных исследований или
исследований случай-контроль или Высококачественное (++) когортное
исследование или исследования случай-контроль с очень низким риском
систематической ошибки или РКИ с невысоким (+) риском систематической
ошибки, результаты которых могут быть распространены на соответствующую
популяцию.
|
| С |
Когортное или исследование случай-контроль или контролируемое исследование
без рандомизации с невысоким риском систематической ошибки (+), результаты
которых могут быть распространены на соответствующую популяцию или РКИ с
очень низким или невысоким риском систематической ошибки (++ или +),
результаты которых не могут быть непосредственно распространены на
соответствующую популяцию
|
| D |
Описание серии случаев или неконтролируемое исследование, или мнение
экспертов
|
Классификация
Классификация [1-9]
Клиническая классификация:
I. Нейрофиброматоз 1 типа (НФ1);
Подтипы:
кожная/дермальная/локализованная/спорадическая нейрофиброма;
локализованная интраневральная нейрофиброма;
подкожная нейрофиброма;
диффузная нейрофиброма (поверхностная);
внутримышечная нейрофиброма;
пигментная нейрофиброма;
плексиформная нейрофиброма (глубокая).
По характеру прогрессирования:
По морфологии и характеру роста:
По локализации:
глубокие ПН;
поверхностные ПН.
По характеру прогрессирования:
прогрессирующие ПН (увеличиваются в размере);
не прогрессирующие ПН (не увеличиваются в размере.
По морфологии и характеру роста:
узловые ПН;
диффузные ПН;
ПН-ассоциированные симптомы: симптомные, бессимптомные ПН-ассоциированные симптомы.
III. Шванноматоз.
II. Нейрофиброматоз 2 типа (НФ2);
III. Шванноматоз.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
|
NB!
При проведении диагностических исследований необходимо учитывать, что Нейрофиброматоз – генетическое заболевание, имеющее высокий риск развития злокачественного новообразования, которое характеризуется появлением и постепенным прогрессированием клинических симптомов с возрастом пациента с вовлечением новых органов и тканей.
Плексиформные нейрофибромы могут переродиться в злокачественные и являются наиболее частыми предвестниками возникновения злокачественных опухолей периферических нервных оболочек у людей с NF-1.
|
Клиническая картина НФ1 зависит от возраста (Рисунок 1 )[10].
Некоторые проявления заболевания являются врожденными и выявляются при рождении, однако другие развиваются в подростковом периоде или у взрослых, что затрудняет диагностику.
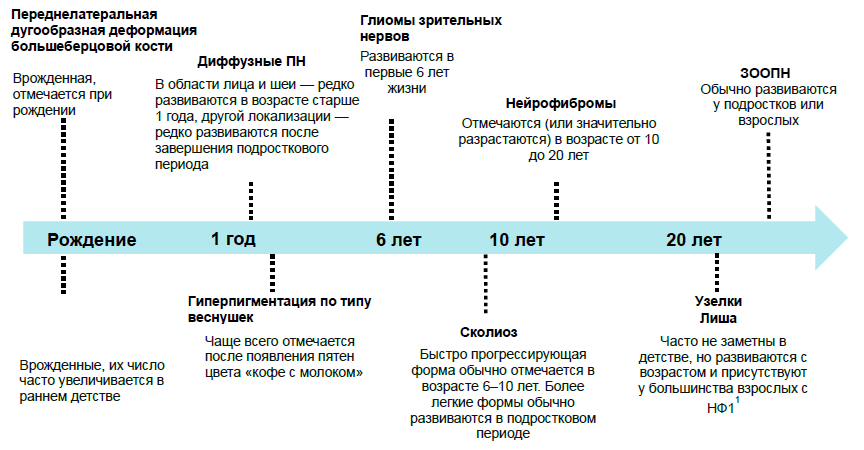
Рисунок 1. Зависимость клинической картины НФ1 от возраста.
НЕЙРОФИБРОМАТОЗ 1 ТИПА
Жалобы и анамнез [11-23]:
Диффузные ПН. Вовлекают протяженные участки нескольких нервов. Поверхностные диффузные ПН при пальпации могут напоминать «мешок с червями».
Пигментная нейрофиброма – микроскопически обнаруживаются меланинсодержащие пигментированные клетки.
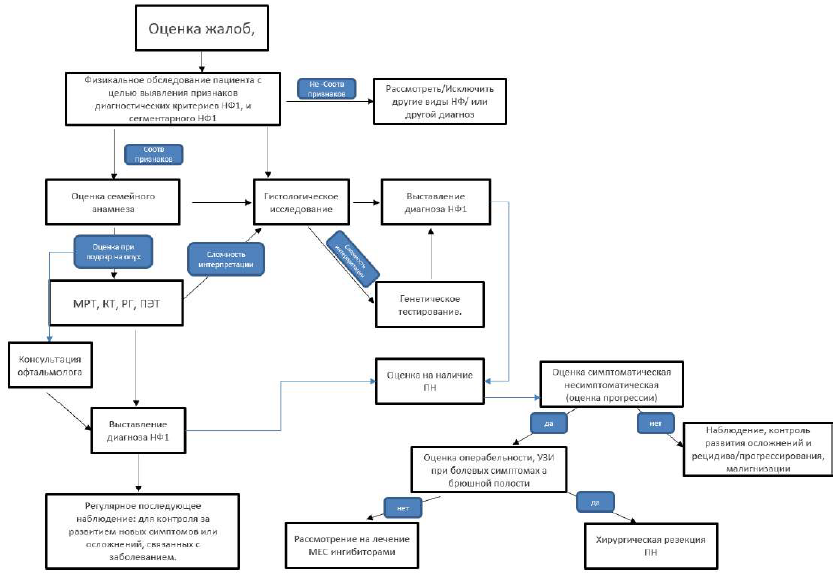
Диагностический алгоритм нейрофиброматоза 1 типа [5].
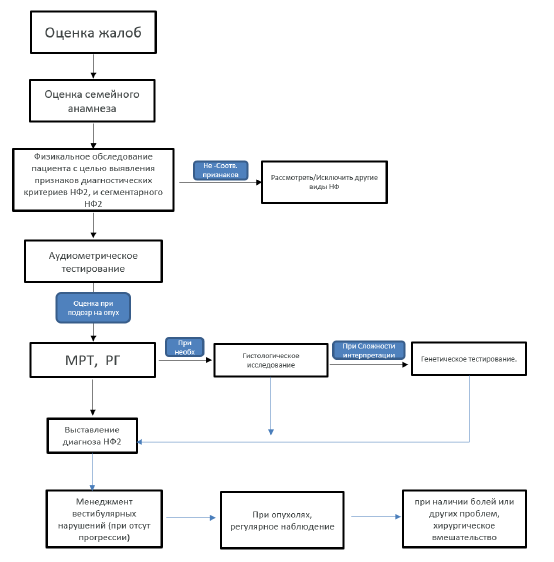
Диагностический алгоритм нейрофиброматоза 2 типа [12]
Диагностический алгоритм шванноматоза [4, 13, 16, 17]:
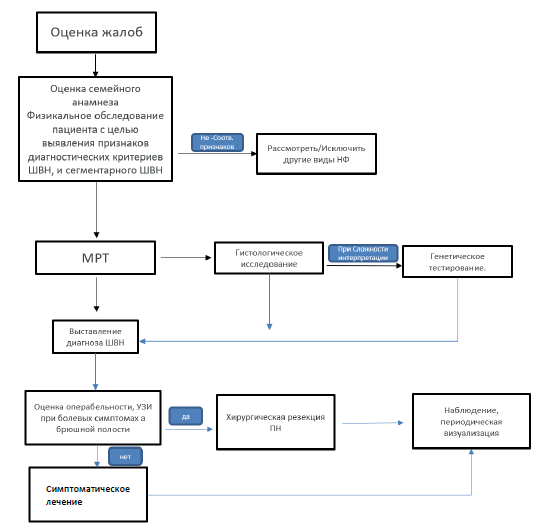

Рисунок 1. Зависимость клинической картины НФ1 от возраста.
Диагностические критерии
НЕЙРОФИБРОМАТОЗ 1 ТИПА
Жалобы и анамнез [11-23]:
Кожные проявления (пигментированные пятна на коже, в паховых и подмышечных областях);
Наличие опухолевых образований (кожные, подкожные, локальные различных размеров);
Нарушения со стороны зрения (снижение остроты зрения вплоть до полной утраты, сужение полей зрения, нечеткость зрения, двоение в глазах): глаукома, амблиопия, страбизм, слепота;
Блефароптоз, проптоз;
Судорожные припадки;
Повышение артериального давления;
Нарушение со стороны костной системы и опорно-двигательного аппарата: деформация костей, искривление позвоночника, двигательные нарушения (ограничение объема движений в суставах), боль при движении;
Мышечная слабость;
ПН-ассоциированные расстройства функции дыхания: ПН, растущие в области дыхательных путей, могут вызывать различные расстройства: храп, синдром ночного апноэ, легочную дисфункцию, обструкцию дыхательных путей;
Болевой синдром (головные боли, нейропатические боли):
- выраженный, требующий постоянного применения анальгетиков;
- в большинстве случаев полностью не купируется;
- может нарастать со временем, требуя увеличения объема применения анальгетиков;
- интенсивность боли может усиливаться на фоне физической активности.
Задержка или преждевременное половое созревание;
Ночной энурез – редко;
Кровотечения – редко, спонтанные, в результате травмы или во время операции, иногда массивные;
Нарушение когнитивных навыков, памяти, депрессия, эмоциональный стресс, связанный с болью, косметическими дефектами, дисфункцией органов, ограничением физических функций.
Анамнез: отягощенный семейный анамнез по нейрофиброматозу (наличие заболевания у родителей и у родственников) (50% случаев).
Кожная/дермальная/локализованная/спорадическая нейрофиброма медленно растущая, начинается в подростковом возрасте или у молодых людей и редко начинается в детстве, с годами увеличивается в размерах и количестве, злокачественное перерождение очень редко.
Локализованная интраневральная нейрофиброма – злокачественные изменения редки.
Диффузная нейрофиброма (поверхностная) – обычно наблюдается в раннем детстве и у молодых людей.
Плексиформная нейрофиброма – обычно считается, что она присутствует при рождении (врожденная). Увеличение объема ПН с течением времени может приводить к нарастанию тяжести двигательных расстройств.
Физикальное обследование [24-29]:
Общий осмотр: наличие опухолевых образований (опухоли оболочек периферических нервов: кожные, подкожные нейрофибромы, ПН; атипичные опухоли), измерение артериального давления.
Кожные нейрофибромы – единичные или множественные мягкие и мясистые образования на коже («шишки», «бугорки»), безболезненные, часто в дерме и подкожно, ≤2-5 см в диаметре, могут содержать жир no date).
Локализованная интраневральная нейрофиброма – визуально не обнаруживается.
Подкожные нейрофибромы – частое проявление, твердые и узловатые образования под кожей, единичные опухоли или цепочками. Они часто представляют собой форму плексиформных нейрофибром.
Диффузная нейрофиброма (поверхностная) – ощущается мягкой и эластичной структурой, выступающей наружу, в области кожи головы и шеи или туловища, имеет плохо очерченные края, невозможно сказать, где заканчивается опухоль. Обычно ассоциируется с диффузной гиперпигментацией, поэтому выглядит как очень большое мягкое пятно цвета кофе с молоком.
Внутримышечная нейрофиброма – обычно изолированные опухоли в мышцах, иногда могут возникать в виде плексиформных нейрофибром в виде цепочек или сетей, разрастания вдоль очень мелких нервов.
Плексиформные нейрофибромы: глубокое расположение, диффузное поражение по ходу крупного нерва и его ветвей.
Основные лабораторные исследования:
Диффузная плексиформная нейрофиброма:
проходит через кожу глубоко в ткани и мышцы;
нет четких границ;
имеет «мизинцы», проникающие в мышцы или другие ткани;
нелегко увидеть у младенцев;
может иметь большое пятно кофе с молоком «над» ним.
Пигментация кожных покровов:
наличие гиперпигментированных макул цвета «кофе с молоком» – как правило, формируются в раннем возрасте (при рождении);
наличие веснушек в подмышечных и паховых областях;
Пигментная нейрофиброма – пигментированные участки на коже.
Состояние костно-суставной системы:
дисплазии костей (наиболее часто – дисплазия большеберцовой кости);
прогрессирующий сколиоз;
псевдоартрозы (ложные суставы);
деформации костей;
Клинические характеристики ПН и других типов нейрофибром при НФ1 [30]
Дисплазия крыльев клиновидной кости — нарушение развития клиновидной кости (в средней части черепа, ближе к лицевой части), вызывающее деформацию лицевой части черепа (Рисунок 8).
Неврологические и когнитивные проявления:
головные боли;
судороги;
гипертензионно-гидроцефальный синдром;
задержка психо-моторного развития;
поведенческие проблемы;
специфические трудности в обучении;
синдром дефицита внимания и гиперактивности;
снижение интеллекта;
расстройства аутистического спектра.
Офтальмологические проявления (Рисунок 9 – 10):
изменения на радужной оболочке глаза (узелки Лиша) – 2 и более, формируются с возрастом;
аномалии сосудистой оболочки глаза (гамартомы);
снижение остроты зрения, сужение полей зрения, нечеткость зрения, двоение в глазах.
Эндокринные проявления:
задержка/преждевременное половое созревания.
Кардиологические проявления:
повышение артериального давления.
Клинические характеристики ПН и других типов нейрофибром при НФ1 [30]
| Плексиформные нейрофибромы | Кожные и подкожные нейрофибромы |
|
Врожденные или появляются в раннем возрасте
Увеличиваются в размере в детском или подростковом возрасте
Произрастают из клеток оболочки периферических нервов
Могут локализоваться в любых органах и тканях, где есть периферические нервы, в том числе:
глубокие ПН могут распространяться на кожу;
могут произрастать из оболочки периферических нервов кожи.
• При пальпации мягкие
• Некоторые поверхностные ПН могут напоминать
«мешок с червями» при пальпации
• Над поверхностными ПН могут отмечаться гиперпигментация и истончение кожи
Могут достигать крупных размеров (до нескольких десятков сантиметров)
|
Чаще появляются в период пубертата или во взрослом возрасте
С возрастом размеры и количество увеличиваются
Растут на терминальных ветвях нервов кожи
Локализация:
кожные нейрофибромы, локализация ограничена эпидермисом и дермой;
подкожные нейрофибромы располагаются в гиподерме
• Кожные нейрофибромы при пальпации мягкие, смещаются вместе с кожей
• Подкожные нейрофибромы при пальпации плотные, не смещаются, но кожа над ними смещается
Размеры чаще до нескольких сантиметров |
| Имеется риск малигнизации | Как правило, не малигнизируются |
Диагностические критерии НФ1 [24]:
|
Критерии типа A: Диагноз НФ1 устанавливается у детей здоровых родителей при наличии двух или более описанных ниже признаков:
|
|
| 1) |
Наличие 6 или более пятен цвета «кофе с молоком» (коричневых
пигментных пятен) диаметром более 5 мм у лиц препубертатного возраста и
более 15 мм у лиц постпубертатного возраста.
|
| 2) | Веснушки в подмышечной или паховой областях. |
| 3) |
Две или более нейрофибромы любого типа (кожная, подкожная) или одна плексиформная нейрофиброма (узловая, диффузная).
|
| 4) | Глиома зрительного нерва. |
| 5) |
Два и более узелка Лиша на радужной оболочке, выявленных при осмотре с помощью щелевой лампы, или ≥ 2 аномалий сосудистой оболочки глаза – определяемые как яркие пятнистые узелки, визуализируемые с помощью оптической когерентной томографии или лазерной сканирующей офтальмоскопии.
|
| 6) |
Характерные поражения костей: дисплазия крыла клиновидной кости, переднелатеральная дисплазия большеберцовой кости или псевдоартроз длинной трубчатой кости.
|
| 7) |
Гетерозиготная патогенная мутация в гене NF1 с долей вариантного аллеля 50%, выявляемая в непораженных тканях, таких как кровь.
|
|
Критерий типа В: Диагноз НФ1 устанавливается у детей родителей с установленным диагнозом НФ1 при наличии одного и более критериев типа А
|
|
|
NB!
Специфических изменений в общих лабораторных анализах крови при НФ1 не наблюдается!
|
ОАК – изменения соответственно сопутствующей патологии;
ОАМ – изменения соответственно сопутствующей патологии;
Биохимический анализ крови (общий белок, мочевина, креатинин, ЛДГ, АЛТ, АСТ, панкреатическая амилаза, общий и прямой билирубин) – изменения соответственно сопутствующей патологии;
Дополнительные лабораторные изменения:
Молекулярно-генетическое исследование [24, 25] – патогенные мутации в гене NF1 в 17q11.2, выявленные в любом источнике ДНК (образец венозной крови, биопсийный материал).
Рентгенография пораженных областей, позвоночника:
Основные инструментальные исследования [24, 31-33]:
Рентгенография пораженных областей, позвоночника:
специфические костные аномалии – дисплазия крыла клиновидной кости, переднелатеральная дисплазия большеберцовой кости или псевдоартроз длинной трубчатой кости;
признаки сколиоза;
псевдоартроз (ложные суставы);
деформации костей.
Ультразвуковое исследование органов брюшной полости, органов малого таза и очагов поражения: определяется опухоль, включая плексиформные нейрофибромы.
Магнитно-резонансная томография с внутривенным контрастированием (головного мозга, орбит, позвоночника, мягких тканей в очагах поражения) [24, 31-35]
Показания к проведению МРТ головного мозга
очаговая неврологическая симптоматика;
дебют эпилепсии;
головные боли (если становятся тяжелее и чаще);
признаки повышенного ВЧД (головная боль (если становятся тяжелее и чаще), нарушение зрения (снижение остроты зрения или сужение полей зрения), повышенная сонливость);
ТИА или ОНМК подобные симптомы;
снижение остроты зрения или сужение полей зрения;
задержка или преждевременное половое развитие;
плексиформные нейрофибромы головы и шеи (увеличение размеров или появление болевого синдрома), вдоль позвоночного столба;
энцефалопатия или нарушение когнитивных функций;
асимметрия конечностей.
При МРТ выявляются:
на Т1 взвешенных изображениях ПН изоинтенсивны или несколько гиперинтенсивны, в сравнении с мышечной тканью;
на Т2 взвешенных изображениях можно увидеть таргетный признак ПН – гиперинтенсивный очаг со снижением интенсивности сигнала в центре, напоминающий кольцо;
таргетные очаги могут быть единичными и множественными.
Таргетный признак чаще наблюдают при визуализации глубоких ПН;
важно оценивать протяженность поражения вовлеченного нерва. По ходу роста ПН может визуализироваться грубое диффузное утолщение нерва;
гиперинтенсивные поражения на Т2-взвешенной МРТ головного мозга [34-35];
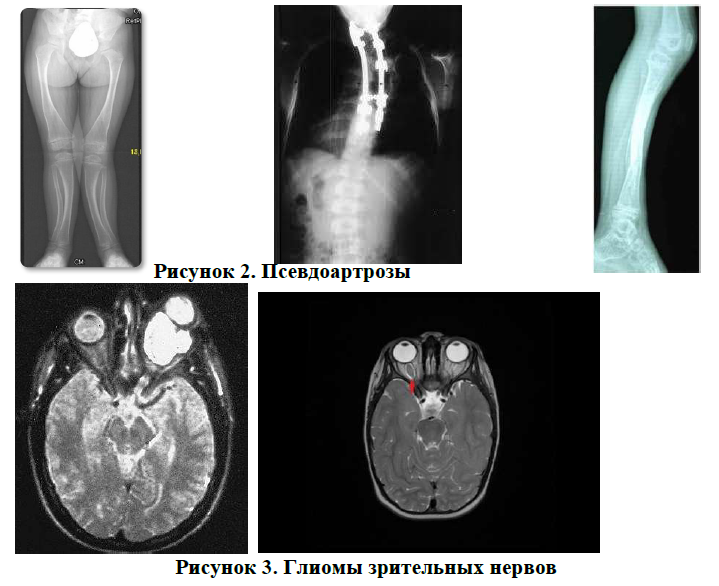
псевдоартрозы (Рисунок 2);
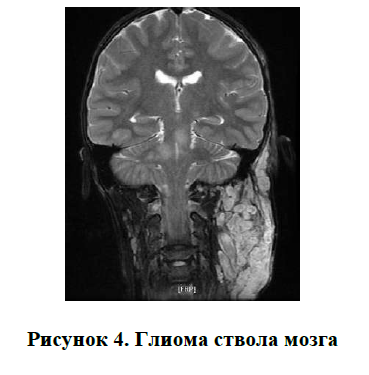
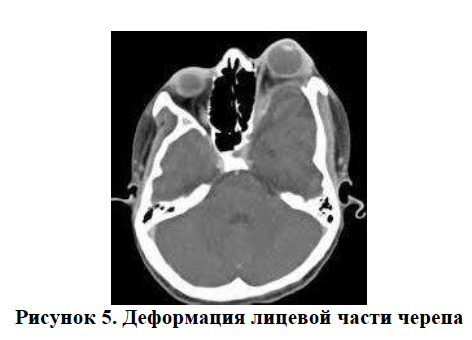
глиомы: зрительных нервов, ствола мозга (Рисунок 3, 4).
дисплазия крыльев клиновидной кости — деформация лицевой части черепа (Рисунок 5);
аневризмы и псевдоаневризмы на фоне сдавления кровеносных сосудов ПН, васкулопатии и нарушения гемостаза.



Локализованная интраневральная нейрофиброма – сегментарное, веретенообразное увеличение нерва, остаточные аксоны проходят через очаг поражения.
Узловая плексиформная нейрофиброма – может затрагивать корешки спинномозговых нервов, обычно растущие через межпозвонковые отверстия, с формированием интра-спинальных и экстраспинальных образований (гантелевидной опухоли). Интраспинальная часть может сжимать спинной мозг.
Диффузная плексиформная нейрофиброма (подкожные узелки или аморфные разрастания подлежащей кости или шванновских клеток) могут быть уродующими и приводить к дефициту дистальнее нейрофибромы.
Внутримышечная нейрофиброма – разрастания вдоль очень мелких нервов.
Плексиформные нейрофибромы: глубокое расположение, преимущественно внутренние/интраневральные расположение, диффузное поражение по ходу крупного нерва и его ветвей, также могут вовлекаться мелкие нервы и поверхностная кожа. Макроскопическое расширение нерва с развитием узловатой опухоли приводит к грубому патологическому состоянию, известному как «мешок с червями».
Признаки на Т2-взвешенной МРТ:
признак цели (низкая интенсивность сигнала в центре с кольцом высокой интенсивности сигнала на периферии).
истончение кортикального слоя трубчатых костей с псевдоартрозом или без такового)
Узловая плексиформная нейрофиброма (Рисунок 6)
обычно вовлекает нервы, отходящие от спинного мозга или от более крупных нервов (таких как седалищный нерв);
обычно увеличивает или утолщает нерв;
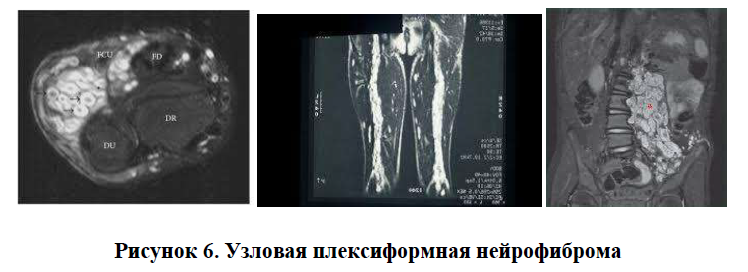
выглядит как небольшие скопления опухолей вдоль нерва

Эхокардиография – синусовый ритм, синусовая аритмия, умеренные диффузные изменения миокарда.
Биопсия опухолей, опухолевидных образований мягких тканей с последующим гистологическим исследованием [24,36-40] – при подозрении на ЗООПН при отсутствии четкой клинической картины, при стремительном увеличении ПН и устойчивом болевом синдроме – определяется малигнизация процесса.
Дополнительные инструментальные исследования:
Биопсия опухолей, опухолевидных образований мягких тканей с последующим гистологическим исследованием [24,36-40] – при подозрении на ЗООПН при отсутствии четкой клинической картины, при стремительном увеличении ПН и устойчивом болевом синдроме – определяется малигнизация процесса.
|
NB!
Не рекомендуется выполнять биопсию только для подтверждения диагноза ПН при НФ1типа!
Биопсийный материал может быть недостаточно информативным для подтверждения плексиформной нейрофибромы, потому что может не содержать достаточное количество материала и не отражать распространенность нейрофибромы.
|
Озлокачествление ПН может привести к развитию злокачественной опухоли оболочки периферических нервов (ЗООПН)
Быстрое увеличение размера или появление болезненности, связанной с ранее существующими бессимптомными ПН, может быть признаком трансформации в ЗООПН — опухоли, характеризующиеся:
• высокой целлюлярностью;
• многоочаговостью;
• атипичными ядрами клеток;
• высокой митотической активностью;
• некрозом опухоли.
Локализованная интраневральная нейрофиброма – иммуногистохимия нейрофиламентов и окраска по Бильшоуски показывают аксоны в центре поражения, часто содержит грубый преломляющий коллаген.
Диффузная нейрофиброма (поверхностная) – проходит через всю толщину кожи (от поверхности до основания кожи (подкожная фасция/жировая клетчатка), не проникает глубже фасции, неразрушающая/охватывает нормальные структуры (например, жировые клетки и аденексальные структуры), однородная матрица из тонкого фибриллярного коллагена, более короткие и круглые шванновские клетки, можно увидеть скопления псевдомейснеровских телесных структур.
Внутримышечная нейрофиброма – разрастания вдоль очень мелких нервов.
Плексиформные нейрофибромы: глубокое расположение, преимущественно внутренние/интраневральные расположение, диффузное поражение по ходу крупного нерва и его ветвей, также могут вовлекаться мелкие нервы и поверхностная кожа, имеют больше соединительной ткани/внеклеточного матрикса, чем у кожной формы нейрофибромы, которые разделяют нервные волокна.
Узловые ПН (Рисунок 7). Разрастание шванновских клеток вокруг волокон периферических нервов может привести к скручиванию нервных сегментов с формированием узловых структур. Узлы могут быть единичными или множественными, располагаясь плотно друг к другу или на некотором расстоянии друг от друга, как «бусы на нитке». Узловые ПН чаще поражают проксимальные корешки и растут вблизи внутренних органов, Фасцикулярный признак, может выглядеть как более крупная и более инфильтрирующая масса с дольчатыми краями с неоднородным усилением.
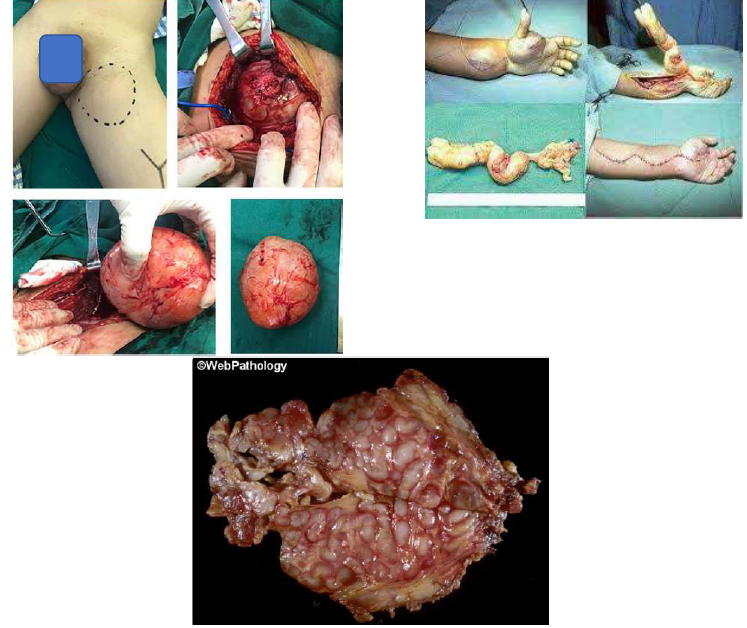

Рисунок 7. «Мешок с червями» (Узловая ПН)
Диффузные ПН. Вовлекают протяженные участки нескольких нервов. Поверхностные диффузные ПН при пальпации могут напоминать «мешок с червями».
Пигментная нейрофиброма – микроскопически обнаруживаются меланинсодержащие пигментированные клетки.
Электроэнцефалография показана пациентам с судорожным синдромом – определяется очаг судорожной готовности;
Компьютерная томография головного мозга, органов грудной клетки, органов брюшной полости и забрюшинного пространства [25,32,33]:
увеличение размера желудочков головного мозга;
наличие дисплазии крыльев клиновидной кости;
наличие опухоли (размер, локализация, распространенность, степень инвазии опухоли);
Основные лабораторные исследования:
Дополнительные лабораторные исследования:
наличие феохромоцитомы (нередко сопутствует НФ1).
Позитронно-эмиссионная томография [25,32,33]:
наличие признаков малигнизации ПН (активное накопление тканями опухоли 18F-фтордезоксиглюкозы).
Учитывая, что НФ1 является мультисистемным заболеванием, рекомендуются консультации профильных специалистов [24]:
детский невролог – для оценки неврологического статуса, при наличии очаговой неврологической симптоматики, эпилептических проявлениях;
детский онколог – при наличии опухолевых образований;
медицинский генетик – наличие наследственной патологии;
детский офтальмолог – при диагностированной глиоме зрительного пути;
детский оториноларинголог – при поражении верхних дыхательных путей, при поражении органов слуха;
детский травматолог-ортопед – при костно-суставной патологии;
детский эндокринолог – при преждевременном полового созревания или же его задержки;
детский кардиолог – при наличии нарушений со стороны сердечно-сосудистой системы (артериальная гипертензия);
детский хирург – при наличии опухолевого образования для оперативного лечения;
детский нейрохирург – при опухолях головного мозга, спинного мозга, слуховых нервов и других периферических нервов;
медицинский психолог – при нарушении когнитивных способностей;
детский психиатр – при психических нарушениях.
Жалобы и анамнез:
Анамнез: семейный анамнез по нейрофиброматозам.
Общий осмотр: наличие опухолевых образований (опухоли оболочек периферических нервов: кожные, подкожные нейрофибромы,);
НЕЙРОФИБРОМАТОЗ 2 ТИПА [41]
Жалобы и анамнез:
Жалобы на шум в ушах, нейросенсорную тугоухость и проблемы с равновесием, жалобы на симптомы, связанные с опухолью, проявляются в возрасте около 20 лет.
Жалобы у пациентов с менингиомами зависят от их локализации и включают головную боль, судороги или очаговые неврологические симптомы.
При наличии интраспинальных опухолей пациенты жалуются на боль, мышечную слабость и парестезии.
Анамнез: семейный анамнез по нейрофиброматозам.
Физикальное обследование:
Общий осмотр: наличие опухолевых образований (опухоли оболочек периферических нервов: кожные, подкожные нейрофибромы,);
Оценка кожных покровов: наличие гиперпигментированных пятен цвета «кофе с молоком» в небольшом количестве;
Неврологические и когнитивные проявления:
головокружение;
шум в ушах;
головные боли;
нейропатия, в том числе парез лицевого нерва;
Офтальмологические проявления:
аномалии сосудистой оболочки глаза (гамартомы);
различные нарушения зрения (катаракта).
Диагностические критерии нейрофиброматоза 2 типа [42]:
Диагностические критерии нейрофиброматоза 2 типа [42]:
|
Диагноз НФ2 устанавливается, когда у человека есть хотя бы один из следующих критериев
|
|
| I. | Двусторонние шванномы слуховых нервов |
| II. |
Идентичный патогенный вариант гена NF2 по крайней мере в 2 анатомически различных опухолях, связанных с НФ2 (шваннома, менингиома и/или эпендимома).
NB! Если фракция вариантного аллеля в непораженных тканях, таких как кровь <50%, диагноз — мозаичный НФ2.
|
| III. |
Наличие 2 больших или наличие 1 большого и 2 малых критериев, как описано ниже.
Большие критерии:
Наличие односторонней шванномы слухового нерва;
Наличие родственника первой линии родства, кроме брата и сестры, с установленным диагнозом НФ2;
2 или более менингиомы;
патогенный вариант* мутации гена NF2 в непораженных тканях, таких как кровь
NB! Если фракция вариантного аллеля в непораженных тканях, таких как кровь, составляет <50%, диагноз — мозаичный НФ2.
Малые критерии:
Следующие проявления следует учитывать больше 1 раза (например, 2 различных шванномы будут считаться 2 малыми критериями):
наличие эпендимомы и/или одной менингиомы;
шванномы (примечание: если в качестве большого критерия у пациента определяется односторонняя шваннома слухового нерва, то по крайней мере еще 1 шваннома должна располагаться в коже).
Следующие проявления следует учитывать только один раз (например, двусторонняя кортикальная катаракта считается одним малым критерием):
Ювенильная субкапсулярная или кортикальная катаракта, гамартома сетчатки, эпиретинальная мембрана у лиц в возрасте до 40 лет, менингиома.
|
* Если обнаружен вероятно патогенный вариант мутации, то молекулярно-генетическое исследование ткани опухоли на предмет мутации гена NF2 может повысить значение данной мутации до патогенного варианта
Основные лабораторные исследования:
|
NB!
Специфических изменений в общих лабораторных анализах для диагностики НФ2 не существует!
|
Набор лабораторных анализов аналогично таковым, как в НФ1.
Дополнительные лабораторные исследования:
Молекулярно-генетическое исследование: выявление патогенных мутаций в гене NF2 на длинном плече 22 хромосомы (22q12), выявляемые в любом источнике ДНК (образец венозной крови, биопсийный материал).
Основные инструментальные исследования [3, 43]:
Аудиометрическое исследование – тугоухость разных степеней, полная потеря слуха.
Магнитно-резонансная томография с внутривенным контрастированием (головного мозга, спинного мозга, лицевого черепа, очага поражения) – выявление шванном, менингиом, эпендимом.
Учитывая, что НФ2 является мультисистемным заболеванием, рекомендуются консультации профильных специалистов аналогично НФ 1[3, 44].
Жалобы и анамнез:
Анамнез: важно уточнить семейный анамнез по нейрофиброматозам.
Физикальное обследование:
Диагностические критерии шванноматоза [45]:
Основные лабораторные исследования:
Дополнительные лабораторные исследования:
Молекулярно-генетическое исследование – выявление патогенных мутаций в генах SMARCB1 и LZTR1 на длинном плече 22 хромосомы (22q11.23), выявленные в любом источнике ДНК (образец венозной крови, биопсийный материал).
Дополнительные инструментальные исследования [46, 47]:
Учитывая, что шванноматоз является мультисистемным заболеванием, рекомендуются консультации профильных специалистов аналогично НФ1 [16, 17].
Диагностический алгоритм пациентов с НФ:
Дополнительные инструментальные исследования [3, 43]:
Биопсия опухолей, опухолевидных образований мягких тканей с последующим гистологическим исследованием [24,34,37] – при подозрении на ЗООПН при отсутствии четкой клинической картины, при стремительном увеличении ПН и устойчивом болевой синдроме – определяется малигнизация процесса.
Учитывая, что НФ2 является мультисистемным заболеванием, рекомендуются консультации профильных специалистов аналогично НФ 1[3, 44].
ШВАННОМАТОЗ [4, 45-47]
Жалобы и анамнез:
боль различной локализации в зависимости от очага образования (тупая, ноющая или жгучая и может быть постоянной или прерывистой);
онемение;
головокружение, шум в ушах;
ощущение покалывания в пораженной области;
нарушения зрения (нечеткость зрения или двоение в глазах);
слабость или атрофию мышц в пораженной области;
в тяжелых случаях опухоли могут вызывать потерю функции в пораженной области, например, трудности с речью, глотанием или дыханием.
Анамнез: важно уточнить семейный анамнез по нейрофиброматозам.
Физикальное обследование:
Общий осмотр: мышечная слабость, наличие опухолевых образований (опухоли оболочек периферических нервов: кожные, подкожные нейрофибромы).
Неврологические и когнитивные проявления: нейропатия, нарушение речи, глотания, оценка нейропатического болевого синдрома; потеря рефлексов и нарушение чувствительности.
Офтальмологические проявления: различные нарушения зрения.
Диагностические критерии шванноматоза [45]:
|
Диагноз шванноматоза устанавливается, когда у пациента определяется один из следующих критериев:
|
|
| I. |
Наличие одной морфологически подтвержденной шванномы или гибридной опухоли оболочки нерва и патогенный вариант мутации генов SMARCB1 (или LZTR1) в непораженной* ткани, такой как кровь
|
| II. |
Обнаружение одного и того же патогенного варианта мутации генов SMARCB1 или LZTR1, определяемый в 2 шванномах или гибридных опухолях оболочки нерва.
|
* Если обнаружен вероятно патогенный вариант мутации, то молекулярно-генетическое исследование ткани опухоли на предмет мутации генов может повысить значение данной мутации до патогенного варианта.
Основные лабораторные исследования:
|
NB!
Специфических изменений в общих лабораторных анализах для диагностики НФ2 не существует!
|
Набор лабораторных анализов аналогично таковым, как в НФ1.
Дополнительные лабораторные исследования:
Молекулярно-генетическое исследование – выявление патогенных мутаций в генах SMARCB1 и LZTR1 на длинном плече 22 хромосомы (22q11.23), выявленные в любом источнике ДНК (образец венозной крови, биопсийный материал).
Основные инструментальные исследования [46, 47]:
Магнитно-резонансная томография с внутривенным
контрастированием (головного мозга, спинного мозга, очага поражения) – определяются множественные опухоли – шванномы.
Дополнительные инструментальные исследования [46, 47]:
Биопсия опухолей, опухолевидных образований мягких тканей с
последующим гистологическим исследованием [5,10,11] – при подозрении на ЗООПН при отсутствии четкой клинической картины, при стремительном увеличении ПН и устойчивом болевой синдроме – определяется малигнизация процесса.
Учитывая, что шванноматоз является мультисистемным заболеванием, рекомендуются консультации профильных специалистов аналогично НФ1 [16, 17].
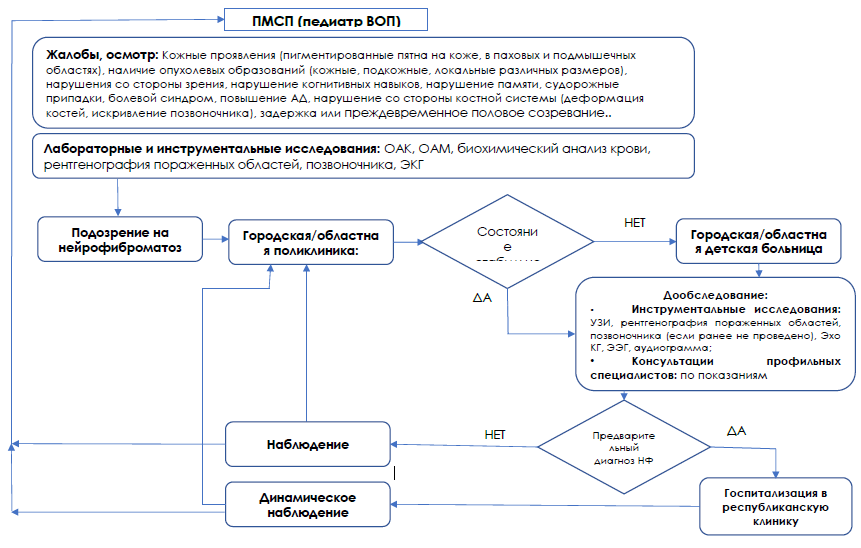
Диагностический алгоритм пациентов с НФ:

Диагностический алгоритм нейрофиброматоза 1 типа [5].

Диагностический алгоритм нейрофиброматоза 2 типа [12]

Диагностический алгоритм шванноматоза [4, 13, 16, 17]:

Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований нейрофиброматозов:
|
Диагноз
|
Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
|
Синдром Легиуса
|
пятна цвета «кофе с молоком», наличие веснушек в подмышечных и/или паховых областях, нейрофибромы
|
Молекулярно-генетическое исследование на выявление мутаций гена SPRED1 и в генах NF1, NF2, LZTR1, SMARSCB1
|
Отсутствие мутаций в генах NF1, NF2, LZTR1, SMARSCB1
|
|
Синдром Нунан
|
низкий рост, трудности в обучении
|
Молекулярно-генетическое исследование на выявление мутаций в генах NF1, NF2, LZTR1, SMARSCB1и мутаций генов:
BRAF
KRAS
LZTR1
MAP2K1
NRAS
PTPN11
RAF1
RIT1
SOS1
|
Отсутствие мутаций в генах NF1, NF2, LZTR1, SMARSCB1
|
|
Туберозный склероз
|
кожные поражения, судороги, когнитивные нарушения.
|
Молекулярно-генетическое исследование на выявление мутаций в гене TSC1 и TSC2, генах NF1, NF2, LZTR1, SMARSCB1
|
Отсутствие мутаций в генах NF1, NF2, LZTR1, SMARSCB1
|
|
Множественная эндокринная неоплазия типа 2B (MEN2B).
|
Нейрофибромы, пятна цвета кофе с молоком.
|
Молекулярно-генетическое исследование для выявления мутаций в генах NF1, NF2, LZTR1, SMARSCB1 и гена RET, определение уровня гормонов щитовидной железы
|
- Отсутствие мутаций в генах NF1, NF2, LZTR1, SMARSCB1
- отсутствие характерных изменений уровня гормонов щитовидной железы.
|
|
Синдром Мак Кьюна-Олбрайта
|
пятна цвета «кофе с молоком» и аномалии костей.
очаги фиброзной дисплазии в костях, гормональный дисбаланс (преждевременное половое созревание или гипертиреоз) |
- Молекулярно-генетическое исследование для выявления мутаций гена GNAS и генах NF1, NF2, LZTR1, SMARSCB1
|
- Отсутствие мутаций в генах NF1, NF2, LZTR1, SMARSCB1
|
|
Синдромом Протея
|
асимметричные разрастания невусов, соединительной ткани
|
- Молекулярно-генетическое исследование для выявления мутаций гена гена AKT1, генах NF1, NF2, LZTR1, SMARSCB1
|
- Отсутствие мутаций в генах NF1, NF2, LZTR1, SMARSCB1
|
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ [48-50]
Принцип лечения основывается на выборе терапии в зависимости от типа НФ[46]:
таргетная (патогенетическая) терапия – при НФ 1 типа;
симптоматическая терапия: НФ 1 и 2 типа, шванноматоз.
Немедикаментозное лечение [52,53]:
Диета: Без ограничений.
Режим: в зависимости от общего состояния.
Рекомендуются:
регулярные физические упражнения;
когнитивно-поведенческая терапия;
поддержка в обучении;
психологическая помощь;
физиотерапия и реабилитация.
Таргетная (патогенетическая) терапия
Показания к терапии селуметинибом:
Противопоказания
Таблица. Оценочная таблица Чайлд-Пью для определения тяжести цирроза печени
Антигипертензивная терапия
План динамического наблюдения пациентов с НФ на региональном (областном, городском) уровне [48]:
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе [51, 52]
Медикаментозное лечение [49,50]:
Таргетная (патогенетическая) терапия
Показания к терапии селуметинибом:
Препарат показан в качестве монотерапии для лечения симптомных неоперабельных плексиформных нейрофибром (ПН) у пациентов детского возраста от 3 лет и старше с нейрофиброматозом 1 типа (НФ1).
Противопоказания
гиперчувствительность к действующему веществу или к любому из вспомогательных веществ;
детский возраст до 3 лет;
нарушение функции печени в декомпенсированной стадии (класс C по шкале Чайлд – Пью).
Таблица. Оценочная таблица Чайлд-Пью для определения тяжести цирроза печени
| Параметр | 1 балл | 2 балла | 3 балла |
|
Билирубин, мкмоль/л (мг%)
|
менее 34 (2,0) | 34—51 (2,0—3,0) | более 51 (3,0) |
| Альбумин, г/л | более 35 | 28—35 | менее 28 |
|
ПТВ, (сек) или ПТИ (%)
|
1—4 (более 60) | 4—6 (40—60) | более 6 (менее 40) |
| Асцит | Нет |
Мягкий, легко поддаётся лечению
|
Напряжённый, плохо поддаётся лечению
|
|
Печеночная энцефалопатия
|
Нет | Лёгкая (I—II) |
Тяжёлая (III—IV) (рефрактерная)
|
Интерпретация: оценка нарушения функции печени в зависимости от суммы баллов:
Класс А: 5 – 6 баллов – компенсированная стадия;
Класс В: 7 – 9 баллов – субкомпенсированная стадия;
Класс С: 10 – 15 баллов – декомпенсированная стадия.
Препараты выбора: селуметиниб.
Перед началом терапии в обязательном порядке берется Информированное согласие пациента на проведение таргетной терапии селуметинибом (форма – в Приложении 1).
Длительность таргетной терапии зависит от клинической эффективности [49]. Оценка эффективности таргетной терапии проводится через 4 месяца от начала терапии.
Селуметиниб назначается детям старше 3 лет, в дозе 25 мг/м2 внутрь во время еды 2 раза в день с интервалом в 12 часов.
Длительность таргетной терапии зависит от клинической эффективности [49]. Оценка эффективности таргетной терапии проводится через 4 месяца от начала терапии.
Критерии клинической эффективности:
уменьшение размеров опухоли;
уменьшение или купирование боли;
улучшение неврологической симптоматики;
улучшение дыхания, глотания;
стабилизация зрения;
уменьшение тазовых нарушений;
уменьшение внешних деформаций;
увеличение объема движений суставов;
улучшение двигательных функций конечностей;
отсутствие прогрессирования НФ1 ПН;
отсутствие неприемлемой токсичности препарата.
Показания к завершению/прекращению таргетной терапии в виду ее неэффективности:
прогрессирование заболевания (увеличение объема плексиформной нейрофибромы более, чем на 20% от исходного);
злокачественная трансформация плексиформной нейрофибромы;
наличие другого злокачественного новообразования, требующего проведения химио- или лучевой терапии;
развитие окклюзии вены сетчатки;
явления кардиотоксичности препарата (симптоматическое снижение фазы выброса левого желудочка (ФВЛЖ) на ЭхоКГ или снижение ФВЛЖ 3 или 4 степени тяжести по CTCAE);
индивидуальная непереносимость компонентов лекарственного препарата.
|
NB!
Препараты повышающие концентрацию Селуметиниба в крови:
кларитромицин;
эритромици;
кларитромицин;
грейпфрутовый сок;
итраконазол;
кетоконазол;
флуконазол;
тиклопидин;
омепразол.
В случае, если избежать данной комбинации невозможно, следует проводить тщательное наблюдение за пациентами для выявления возможных нежелательных явлений и снизить дозу селуметиниба!
|
|
NB!
Препараты понижающие концентрацию Селуметиниба в крови:
фенитоин;
рифампицин;
карбамазепин;
препараты зверобоя.
Назначение указанных препаратов необходимо исключить!
|
Противосудорожная терапия
Противосудорожная терапия проводится в соответствии с клиническим протоколом «Эпилепсия у детей», одобренным Объединенной комиссией по качеству медицинских услуг Министерства здравоохранения Республики Казахстан от «15» апреля 2020 года Протокол № 90[54].
Антигипертензивная терапия
Антигипертензивная терапия проводится в соответствии с клиническим протоколом «Артериальная гипертензия у детей и подростков», одобренный Объединенной комиссией по качеству медицинских услуг Министерства здравоохранения Республики Казахстан от «10» ноября 2017 года Протокол № 32 [76].
Дозировка морфина:
Обезболивающая терапия
Препараты выбора:
парацетамол, кетопрофен;
трамадол;
морфин.
Дозировка морфина:
Начальные средние терапевтические дозы внутрь в зависисмости от возраста:
в возрасте от 1-12 мес. по 0,08-0,2 мг/кг каждые 4 часа;
в возрасте старше 12 мес. по 0,2-0,4 мг/кг через рот каждые 4 часа (может быть назначен каждые 6-8 часов у новорожденных или при почечной/печеночной недостаточности).
При переводе с перорального пути на другие – пользоваться правилами эквианальгетических доз (доза морфина для п/к введения в 2 раза меньше дозы, принимаемой через рот; доза морфина для в/в введения в 3 раза меньше дозы морфина, принимаемый через рот). Морфин назначать «по часам», а не «по требованию»: морфин короткого действия – каждые 4-6часов, морфин пролонгированного действия – каждые 8-12 часов.
Морфин короткого действия:
Стартовые дозы в зависимости от способа введения препарата:
внутрь или ректально в зависимости от возраста:
в возрасте от 1-3 мес. по 50 мкг/кг каждые 4 часа;
в возрасте от 3-6 мес. по 100 мкг каждые 4 часа;
в возрасте от 6 мес.-12 лет по 200мкг/кг каждые 4 часа;
в возрасте от 12-18 лет по 5-10 мг каждые 4 часа;
подкожно болюсно или в/в струйно (в течении минимум 5 мин) в зависимости от возраста:
в возрасте до 1 мес. по 25 мкг/кг каждые 6 часов;
в возрасте от 1-6 мес. по 100 мкг/кг каждые 6 часов;
в возрасте от 6 мес.-12 лет по 100 мкг/кг каждые 4 часа (максимально разовая стартовая доза 2,5 мг);
детям в возрасте от 12-18 лет по 2,5-5 мг каждые 4 часа (максимально суточная доза 20 мг в сутки);
продолжительная подкожная или в/в инфузия со скоростью в зависимости от возраста:
в возрасте до 1 мес. по 5 мкг/кг в час;
в возрасте от 1-6 мес. по 10 мкг/кг в час;
в возрасте от 6 мес.-18 лет по 20 мкг/кг в час (максимум 20 мг за 24 часа).
Увеличение разовой и суточной дозы:
вариант 1 – увеличить разовую дозу морфина для регулярного приема на 30- 50% от предыдущей дозы;
вариант 2 – суммировать все дозы морфина за последние 24 часа и разделить полученную сумму на 6, увеличить на это число каждую регулярную дозу, принимаемые каждые 4 часа, также необходимо увеличить дозу для купирования прорывной боли, так как увеличились регулярные дозы.
Перечень основных лекарственных средств: нет
Перечень дополнительных лекарственных средств:
Морфин пролонгированного (длительного) действия:
суточная доза равна суточной дозе морфина быстрого действия через рот;
разовая доза морфина пролонгированного действия равна половине его суточной дозы, для купирования прорывной боли использовать морфин быстрого действия.
Расчет морфина для купирования прорывной боли:
если при регулярном приеме боль появляется между дозами морфина, расписанными «по часам», назначить дозу морфина для купирования прорывной боли:
доза для купирования прорывной боли составляет 50-100% от той разовой, которая применяется каждые 4 часа, или рассчитывается как 1/6 от общей суточной дозы морфина, принимаемой в данный момент;
доза для купирования прорывной боли должна быть дана не ранее чем через 15-30 мин. от предыдущего приема препарата.
Отмена морфина: - отмена приема препарата постепенно на 1/3 каждые 3 дня
Перечень основных лекарственных средств: нет
Перечень дополнительных лекарственных средств:
|
Фармакотерапевтическая группа
|
МНН лекарственного средства | Способ применения | Уровень доказательности |
|
Противоопухолевое средство ингибитор протеинкиназы (ингибиторингибиторы митоген-активируемой протеинкиназы киназы 1 и 2 (MEK1 и MEK2))
|
Селуметиниб |
Перорально.
Расчет разовой дозы в зависимости от площади поверхности тела: 25 мг/м2 площади поверхности тела. Кратность: два раза в сутки (каждые 12 ч).
Длительность курса: длительно, под контролем эффективности терапии (смотрите Раздел 3.2 настоящего клинического протокола)
|
B[51, 52, 53] |
|
Неопиоидный анальгетик, жаропонижающее средство
|
Парацетамол |
Перорально.
Расчет разовой дозы: 10-15 мг/кг. Кратность приема: каждые 4 – 6 часов. Максимальная суточная доза составляет 60 мг/кг массы тела ребенка.
Длительность курса: при болях не более 5 дней
|
B[55] |
|
Нестероидное противовоспалительное средство
|
Кетопрофен |
Парентерально, в/м по 100 мг 1 – 2 раза/сут.
Максимальная суточная доза – 200 мг.
Длительность курса: при болях не более 5 дней
|
В [55] |
|
Анальгетическое опиоидное средство
|
Трамадол |
Перорально, парентерально.
При болевом синдроме в тяжелых случаях НФ1:
Детям в возрасте от 1 до 14 лет дозу устанавливают из расчета 1 – 2 мг/кг каждые 4 – 6 часов. Детям старше 14 лет разовая доза в зависимости от способа приема:
внутрь – 50 мг;
ректально – 100 мг;
в/в медленно или в/м – 50 – 100 мг.
Если при парентеральном введении эффективность недостаточна, то через 20-30 мин возможен прием внутрь в дозе 50 мг.
Максимальная доза: детям старше 14 лет независимо от способа введения – 400 мг/сут.
Длительность лечения определяется индивидуально в зависимости от купирования боли. |
B[55] |
|
Анальгетическое наркотическое средство
|
Морфин |
Рекомендации по применению смотрите в разделе 3.2 настоящего клинического протокола
|
B[55] |
Хирургическое вмешательство: не проводится.
Дальнейшее ведение:
Детям с Нейрофиброматозом (НФ1, НФ2, Шванноматозом) требуется постоянное динамическое наблюдение участковым врачом (педиатр, ВОП) под контролем профильных специалистов (онколог, невропатолог) по месту жительства.
План динамического наблюдения пациентов с НФ на региональном (областном, городском) уровне [48]:
|
Параметры
|
Частота проведения | Показания к обследованию |
| ОАК | 1 раз в 6 месяцев | Мониторинг общего состояния |
| ОАМ | 1 раз в 6 месяцев | Мониторинг общего состояния |
|
Биохимический анализ крови (общий белок, альбумин, мочевина, креатинин, ЛДГ, АЛТ, АСТ, КФК, липаза, панкреатическая амилаза, общий прямой билирубин, электролиты)
|
1 раз в 6 месяцев | Мониторинг общего состояния |
| 1 раз в 3 месяца | При терапии селуметинибом | |
| Коагулограмма | - | По показаниям |
| УЗИ | 1 раз в 6 месяцев |
Мониторинг общего состояния
|
| ЭКГ | 1 раз в 6 месяцев | Мониторинг общего состояния |
| ЭхоКГ |
1 раз в 3 месяца на протяжении 1-го года, далее 1 раз в 6 месяцев или чаще по показаниям
|
При терапии селуметинибом |
| МРТ |
1 раз в 6-12 месяцев по показаниям
|
Мониторинг общего состояния по назначению профильного специалиста;
При терапии селуметинибом в динамике.
|
| КТ, ПЭТ-КТ |
1 раз в 12 месяцев по показаниям
|
Мониторинг общего состояния
|
|
Молекулярно-генетическое исследование
|
Однократно | при планировании семьи* |
| Детский невролог |
1 раз в 3-6 месяцев при наличии неврологической симптоматики
|
Мониторинг общего состояния
|
| Детский онколог |
1 раз в 6-12 месяцев
|
Консультация на предмет выявления опухолевых образований;
Мониторинг имеющихся опухолей и появления новых
|
|
1 раз в 3-6 месяца на фоне терапии селуметинибом
|
- Оценка эффективности терапии;
- Оценка развития и степени НЯ.
- Коррекция дозировки препарата при необходимости.
|
|
| Детский офтальмолог | 1 раз в 6 месяцев |
Оценка степени нарушения зрения, связанных с НФ.
Мониторинг состояния зрения.
|
| 1 раз в 3 месяца |
При диагностированной глиоме зрительного пути - мониторинг глиомы
|
|
|
1 раз в 6 месяцев или чаще при появлении жалоб
|
Оценка состояния НЯ со стороны органа зрения на фоне терапии селуметинибом
|
|
| Детский ортопед |
- Первичный прием (на этапе установки диагноза)
- Далее 1 раз в 6 месяцев |
Оценка наличия проявлений НФ со стороны опорно-двигательного аппарата.
Мониторинг состояния опорно-двигательного аппарата. |
|
1 раз в 6 месяцев и чаще по показаниям
|
При наличии нарушений опорно-двигательного аппарата
|
|
| Детский эндокринолог |
- Первичный прием (на этапе установки диагноза)
-1 раз в 6 месяцев и чаще по показаниям |
Оценка наличия нарушений со стороны эндокринной систем
Мониторинг преждевременного полового созревания или же его задержки |
| Детский кардиолог |
- Первичный прием (на этапе установки диагноза)
-1 раз в 6 месяцев и чаще по показаниям |
Оценка наличия нарушений со стороны сердечно-сосудистой системы (артериальная гипертензия)
Мониторинг состояния сердечно-сосудистой системы |
|
1 раз в 3 месяца на протяжении 1-го года, далее 1 раз в 6 месяцев или чаще по показаниям
|
Мониторинг состояния сердечно-сосудистой системы при терапии селуметинибом
|
|
| Детский хирург |
- Первичный прием (на этапе установки диагноза)
- Далее 1 раз в год
|
Для решения вопроса оперативного лечения
Мониторинг состояния после оперативного лечения |
| Медицинский психолог |
- Первичный прием (на этапе установки диагноза)
- Далее 1 раз в год
|
Оценка нарушения когнитивных способностей и их мониторинг
|
| Детский психиатр |
- по показаниям при подозрении на наличие психических отклонений
|
При необходимости оценки психического состояния
|
|
Оториноларинголог, аудиолог
|
1 раз в 3 месяца |
При поражении верхних дыхательных путей, органов слуха и тугоухости;
|
| Нейрохирург | 1 раз в 3-6 месяцев |
При опухолях головного мозга, спинного мозга, слуховых нервов и других периферических нервов
|
* Всем пациентам с НФ и их семьям предлагается генетическое консультирование для обсуждения риска наследования, последствий диагноза для планирования семьи в будущем и возможностей пренатальной диагностики.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе [51, 52]
отсутствие прогрессирования заболевания (увеличение объема ПН не более чем на 20% от исходного);
уменьшение размера ПН;
улучшение внешнего вида при наружной локализации ПН;
купирование или снижение интенсивности болевого синдрома;
увеличение силы мышц и восстановление объема движений в вовлеченных суставах;
уменьшение выраженности осложнений, таких как судороги, повышенное артериальное давление;
уменьшение сдавления дыхательных путей или магистральных сосудов;
уменьшение проявлений миелопатии на фоне параспинальных ПН;
восстановление функции жевания, глотания, питания, речи;
снижение прогрессирования потери зрения вследствие сдавления органов орбиты ПН;
улучшение функции органов малого таза;
устранение других симптомов, вызванных ПН.
Лечение (стационар)
Тактика лечения на стационарном уровне [56, 57]:
На стационарном уровне определяется тактика лечения с привлечением специалистов мультидисциплинарной группы, определяется потребность в медикаментозной терапии и необходимость в хирургическом лечении. Важно, чтобы в мультидисциплинарную команду были включены хирурги для обсуждения возможности оперативного вмешательства в каждом случае.
Проводится хирургическое лечение кожных нейрофибром, плексиформных нейрофибром, коррекция сколиоза, дисплазии костей.
При жизнеугрожающих состояниях в результате обструкции дыхательных путей применяется трахеостомия и/или ИВЛ.
Для лечения синдрома ночного апноэ у пациентов с ПН применяется аппаратная терапия с помощью постоянного положительного давления в дыхательных путях (СРАР –терапия).
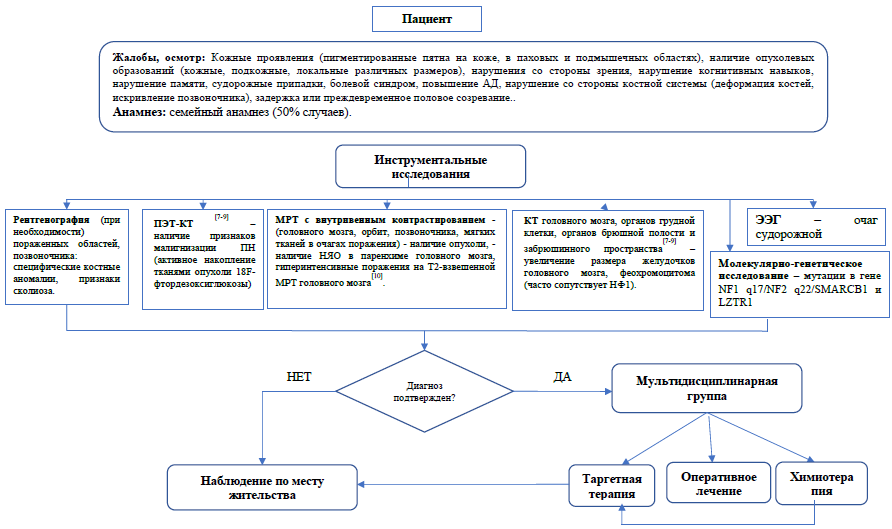
Карта наблюдения пациента, маршрутизация пациента:
Таргетная терапия назначается на амбулаторном уровне.
Диета: Первый день после операции – голод.
Режим: Постельный режим в послеоперационном периоде в зависимости от объема операции в среднем 1 – 5 дней.
Противопоказания к оперативному лечению:
Карта наблюдения пациента, маршрутизация пациента:

|
NB! Клинический диагноз нейрофиброматоза устанавливается на основании клинических данных согласно диагностическим критериям и результатам инструментальных исследований, преимущественно – по заключению МРТ, являющегося «золотым стандартом диагностики» НФ.
|
Мультидисциплинарная группа определяет тактику лечения пациента:
1) таргетная терапия;
2) химиотерапия;
3) оперативное лечение.
Таргетная терапия назначается на амбулаторном уровне.
Немедикаментозное лечение:
Диета: Первый день после операции – голод.
Далее – диета с физиологическим содержанием белков, жиров и углеводов, обогащенная витаминами, минеральными веществами с умеренным ограничением химических и механических раздражителей слизистой оболочки и рецепторного аппарата желудочно-кишечного тракта. Исключают острые закуски, приправы, пряности, ограничивают поваренную соль (6–8 граммов в день).
Блюда готовятся в отварном виде или на пару, протертые и не протертые.
Режим питания дробный, 5–6 раз в день.
Режим: Постельный режим в послеоперационном периоде в зависимости от объема операции в среднем 1 – 5 дней.
Медикаментозное лечение:
Медикаментозное лечение на стационарном уровне заключается в назначении химиотерапии, если было вынесено решение мультидисциплинарной группы.
Показания к химиотерапии: озлокачествление НФ 1 типа ПН.
Глиомы зрительного пути и другие глиомы низкой степени злокачественности[50] – ассоциированные с НФ1 глиомы низкой степени злокачественности у детей и подростков обычно протекают вяло. Лечение необходимо небольшому проценту пациентов, у которых развиваются симптоматические опухоли с клинически значимым ростом и прогрессирующей потерей зрения. Химиотерапия включает карбоплатин, винкристин и этопозид по схеме согласно Клиническому протоколу «Опухоли центральной нервной системы у детей» [57].
Злокачественные опухоли оболочек периферических нервов – проводят оценку стадии и лечат как злокачественные саркомы мягких тканей [57].
Нейрофиброматоз 2 типа, шванноматоз [46]: Лечение пациентов нейрофиброматозом 2 типа и шванноматоза симптоматическое: не существует методов лечения, направленных на основное заболевание.
Перечень дополнительных лекарственных средств (менее 100 % вероятности применения): смотрите Раздел Амбулаторный уровень настоящего клинического протокола.
Биопсия показана при подозрении на ЗООПН:
Показания к оперативному лечению:
Перечень основных лекарственных средств при медикаментозном лечении, имеющих 100 % вероятность применения: нет.
Перечень дополнительных лекарственных средств (менее 100 % вероятности применения): смотрите Раздел Амбулаторный уровень настоящего клинического протокола.
Хирургическое вмешательство [58-73]:
Биопсия показана при подозрении на ЗООПН:
стремительный рост и устойчивая боль ранее стабильной ПН;
признаки ЗООПН на МРТ, ПЭТ, ПЭТ/КТ.
Показания к оперативному лечению:
прогрессирование нейрофибромы;
некупирующийся болевой синдром;
кровотечение;
жизнеугрожающие состояния на фоне прогрессирующего увеличения в объеме опухолевой массы с компрессионным воздействием на близлежащие органы и ткани (сдавление трахеи, бронхов, магистральных сосудов, рядом расположенных рядом с опухолью органов, нервов и т.д.)
нарушение функции органа/-ов;
малигнизация;
косметические дефекты.
Структурные особенности ПН связаны с проблемами при проведении операции и риском для пациентов. Большинство ПН технически невозможно удалить радикально без угрозы значительных осложнений. Часто оперативное вмешательство выполняется с целью уменьшения объема опухолевой массы и купирования ПН-ассоциированных симптомов. Это может быть связано с тем, что ПН окружают жизненно важные органы или находятся в непосредственной близости от них, а также с инвазивностью или высокой васкуляризацией ПН.
|
NB!
До принятия решения о проведении операции важно провести тщательное обследование опухоли, чтобы оценить ее границы, степень интеграции в окружающие ткани и васкуляризации!
|
Виды оперативных вмешательств по поводу ПН:
тотальная резекция (15%);
околототальная резекция (23%);
субтотальная резекция (44%).
Противопоказания к оперативному лечению:
невозможность удаления опухоли из-за локализации в трудно доступном месте, контакте опухоли с жизненно важными органами, нервными стволами;
высокий риск кровотечения из-за обильной васкуляризации;
тяжелое общее состояние.
Костные аномалии:
Реконструктивные большие операции не проводятся.
Малоинвазивные операции:
временное блокирование зоны роста костей;
костная аутопластика при ложных суставах.
Сколиоз.
Проводится ортопедическое вмешательство (фиксация) или хирургическое вмешательство. Необходимость хирургического лечения дистрофического сколиоза может дополнительно усложнить клиническую картину лечения хронической боли у лиц с НФ1. Хирургическое вмешательство при сколиозе у детей производится в соответствии с клиническими протоколами
«Сколиозы у детей»[66], одобренный Объединенной комиссией по качеству медицинских услуг Министерства здравоохранения и социального развития Республики Казахстан от «28» июня 2016 года Протокол № 6;
«Сколиозы у детей»[66], одобренный Объединенной комиссией по качеству медицинских услуг Министерства здравоохранения и социального развития Республики Казахстан от «28» июня 2016 года Протокол № 6;
«Доброкачественные новообразования костей (педиатрия)»[67], рекомендованный Экспертным советом РГП на ПХВ «Республиканский центр развития здравоохранения» Министерства здравоохранения и социального развития Республики Казахстан от «12» декабря 2014 года Протокол № 9;
«Врожденные и приобретенные деформации позвоночника», одобренный Объединенной комиссией по качеству медицинских услуг Министерства здравоохранения Республики Казахстан от «25» мая 2017 года Протокол № 23[68].
Кожные и подкожные нейрофибромы [69].
Кожные и подкожные нейрофибромы не удаляются, если нет необходимости в удалении (например, боль, кровотечение, нарушение функции, обезображивание). Возможны различные варианты удаления, такие как хирургическое вмешательство, лазерное удаление или электродиссекция.
Плексиформные нейрофибромы [69-72].
При выраженной внешней дефигурации, болевом синдроме, сдавлении дыхательных путей, нервных стволов, компрессии ствола мозга, потери неврологической функции, ПН признается симптоматической и пациенту также возможно рекомендовать хирургическое лечение. Радикальное удаление опухоли сопряжено с риском необратимого повреждения нервов, поэтому радикальное хирургическое иссечение применяют редко. Также во многих случаях операция невозможна из-за тесного контакта опухоли с жизненно важными органами. ПН является высоко васкуляризированной опухолью, в связи с чем хирургическое вмешательство может быть ассоциировано с выраженной кровопотерей. Также возможно рассмотреть хирургическое лечение с целью эстетической коррекции после или в процессе медикаментозного лечения. В каждом клиническом случае показания и объем хирургического лечения определяется индивидуально.
У пациентов на фоне ПН данной локализации в некоторых случаях может потребоваться удаление глазного яблока[73].
Послеоперационные осложнения включают [74-75]:
замедленное/неполное заживление раны – местное лечение;
послеоперационная лихорадка – симптоматическая терапия;
рецидив/прогрессия – повторная операция;
развитие новых симптомов (часто – неврологический дефицит, нейропатии) – симптоматическая терапия;
повреждение нервов: потеря чувствительности и/или двигательных функций, онемение – симптоматическое лечение;
образование ложного сустава – костная аутопластика с последующей фиксацией металлоконструкцией;
патологический перелом – фиксация металлоконструкцией;
кровотечения с высоким риском массивного кровотечения – экстренная кровоостанавливающая терапия.
Дальнейшее ведение:
Всем пациентам после стационарного хирургического лечения проводится динамическое наблюдение и медицинcкая реабилитация согласно Клиническому протоколу «Второй этап. Реабилитация IIA. Профиль «Травматология и ортопедия (детская), динамическое наблюдение по месту жительства согласно рекомендаций Раздела Амбулаторное лечение настоящего клинического протокола.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе:
отсутствие прогрессирования заболевания (увеличение объема ПН не более чем на 20% от исходного);
уменьшение размера ПН, включая улучшение внешнего вида при наружной локализации ПН;
купирование или снижение интенсивности болевого синдрома;
увеличение силы мышц и восстановление объема движений в вовлеченных суставах;
уменьшение выраженности осложнений, таких как судороги, повышенное артериальное давление;
уменьшение сдавления дыхательных путей или магистральных сосудов;
уменьшение проявлений миелопатии на фоне параспинальных ПН;
восстановление функции жевания, глотания, питания, речи;
снижение прогрессирования потери зрения вследствие сдавления органов орбиты ПН;
улучшение функции органов малого таза;
устранение других симптомов, вызванных ПН.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
определение тактики лечения;
ухудшение состояния.
Показания для экстренной госпитализации:
некупирующийся болевой синдром;
судорожный синдром;
жизнеугрожающее состояние.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- 1) Le, C. and Bedocs, P.M. (2022). Neurofibromatosis. [online] PubMed. Available at: https://www.ncbi.nlm.nih.gov/books/NBK459329/. [Accessed 10 Jan. 2023]. 2) Rodrigues, L.O.C., Batista, P.B., Goloni-Bertollo, E.M., Souza-Costa, D. de, Eliam, L., Eliam, M., Cunha, K.S.G., Darrigo Junior, L.G., Ferraz Filho, J.R.L., Geller, M., Gianordoli-Nascimento, I.F., Madeira, L.G., Malloy-Diniz, L.F., Mendes, H.M., Miranda, D.M. de, Pavarino, E.C., Baptista-Pereira, L., Rezende, N.A., Rodrigues, L. de O. and Silva, C.M. da (2014). Neurofibromatoses: part 1 ? diagnosis and differential diagnosis. Arquivos de Neuro-Psiquiatria, 72(3), pp.241–250. doi:10.1590/0004- 282x20130241. 3) Asthagiri AR, Parry DM, Butman JA, Kim HJ, Tsilou ET, Zhuang Z, Lonser RR. Neurofibromatosis type 2. Lancet. 2009 Jun 6;373(9679):1974-86. doi: 10.1016/S0140- 6736(09)60259-2. Epub 2009 May 22. PMID: 19476995; PMCID: PMC4748851. 4) Schraepen C, Donkersloot P, Duyvendak W, Plazier M, Put E, Roosen G, Vanvolsem S, Wissels M, Bamps S. What to know about schwannomatosis: a literature review. Br J Neurosurg. 2022 Apr;36(2):171-174. doi: 10.1080/02688697.2020.1836323. Epub 2020 Dec 2. PMID: 33263426. 5) UpToDate. Available at: https://www.uptodate.com/contents/nf2-relatedschwannomatosis- formerly-neurofibromatosis-type-2 (Accessed: January 11, 2023). 6) www.mayoclinic.org. (n.d.). Neurofibroma - Overview - Mayo Clinic. [online] Available at: https://www.mayoclinic.org/diseases-conditions/neurofibroma/cdc- 20352978#:~:text=A neurofibroma is a type [Accessed 13 Jan. 2023]. 7) Hirbe A and Gutman D. Lancet Neurol 2014;13:834-843; Reilly K et al. J Natl Cancer Inst 2017;109:djx124.; Tonsgard J. Semin Pediatr Neurol 2006;13:2-7.; Farid M et al. The Oncologist 2014;19:193-201. 5. Yuan Z et al. Oncotarget 2017;8:104785- 104795 8) Friedrich et al. World Journal of Surgical Oncology 2005;3:1-6.; Blakeley J and Plotkin S. Neuro-Oncology 2016;18:624-638. Boyd K et al. J Am Acad Dermatol 2009;6:1-16.; Friedman J. J Child Neurol; Washington EN, Placket TP, Gagliano RA, Kavolius J, Person DA. Diffuse plexiform neurofibroma of the back: report of a case. Hawaii Med J. 2010;69(8):191-193; 2002;17:548-554.; Gross AM et al NEJM 2020;382:Suppl Protocol S1-S301; Friedman JM. Neurofibromatosis 1. 1998 Oct 2 [Updated 2022 Apr 21]. In: Adam MP, Mirzaa GM, Pagon RA, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2022. Электронный ресурс: https://www.ncbi.nlm.nih.gov/books/NBK1109/ дата обращения 15.06.2022 9) Friedrich R et al. World Journal of Surgical Oncology 2005;3:1-6. ;Blakeley J and Plotkin S. Neuro-Oncology 2016;18:624-638; Gerber P et al. Eur J Med Res 2009;14:102-105.; James H. Tonsgard, Clinical manifestations and management of neurofibromatosis type 1;; Semin Pediatr Neurol 13:2-7; 2006 Elsevie; Nguyen R, Kluwe L, Fuensterer C, Kentsch M, Friedrich RE, Mautner VF: Plexiform neurofibromas in children with neurofibromatosis type 1: frequency and associated clinical deficits. J Pediatr. 2011, 159: 652-5. 10) Rasmussen S and Friedman J. Am J Epidemiol 2000;151:33-40. 2. Friedman J. GeneReviews 2018;1-43 11) Legius, E., Messiaen, L., Wolkenstein, P., Pancza, P., Avery, R.A., Berman, Y., Blakeley, J., Babovic-Vuksanovic, D., Cunha, K.S., Ferner, R., Fisher, M.J., Friedman, J.M., Gutmann, D.H., Kehrer-Sawatzki, H., Korf, B.R., Mautner, V.-F., Peltonen, S., Rauen, K.A., Riccardi, V. and Schorry, E. (2021). Revised diagnostic criteria for neurofibromatosis type 1 and Legius syndrome: an international consensus recommendation. Genetics in Medicine, [online] 23(8), pp.1506–1513. doi:10.1038/s41436-021-01170-5. 12) Avery RA, Katowitz JA, Fisher MJ, Heidary G, Dombi E, Packer RJ, et al. Orbital/periorbital plexiform neurofibromas in children with neurofibromatosis type 1: multidisciplinary recommendations for care. Ophthalmology 2017;124(1):123-32. 13) Gross AM, Singh G, Akshintala S, Baldwin A, Dombi E, Ukwuani S, et al. Association of plexiform neurofibroma volume changes and development of clinical morbidities in neurofibromatosis 1. Neuro Oncol 2018;20(12):1643-51. Ejnell H, Järund M, Bailey M, Lindeman P. Airway obstruction in children due to plexiform neurofibroma of the larynx. J Laryngol Otol 1996;110(11):1065-68. 14) Plotkin SR, Davis SD, Robertson KA, Akshintala S, Allen J, Fisher MJ, et al. Sleep and pulmonary outcomes for clinical trials of airway plexiform neurofibromas in NF1. Neurology 2016;87(7 Suppl 1):S13-20. 15) Gross AM, Singh G, Akshintala S, Baldwin A, Dombi E, Ukwuani S, et al. Association of plexiform neurofibroma volume changes and development of clinical morbidities in neurofibromatosis 1. Neuro Oncol 2018;20(12):1643-51. Ejnell H, Järund M, Bailey M, Lindeman P. Airway obstruction in children due to plexiform neurofibroma of the larynx. J Laryngol Otol 1996;110(11):1065-68. 16) Szudek J, Birch P, Friedman JM. Growth in North American white children with neurofibromatosis 1 (NF1). J Med Genet 2000;37(12):933-8. 17) Gross AM, Singh G, Akshintala S, Baldwin A, Dombi E, Ukwuani S, et al. Association of plexiform neurofibroma volume changes and development of clinical morbidities in neurofibromatosis 1. Neuro Oncol 2018;20(12):1643-51. 18) Gross AM, Singh G, Akshintala S, Baldwin A, Dombi E, Ukwuani S, et al. Association of plexiform neurofibroma volume changes and development of clinical morbidities in neurofibromatosis 1. Neuro Oncol 2018;20(12):1643-51. Domingos ACB, Gomes MC, Nasr BP, Santos ACE Bladder Plexiform Neurofibroma in Neurofibromatosis Carrier: a Case Report. Revista Brasileira de Cancerologia 2018; 64(4): 579-583 19) Allen R, Epelman M, Cruz-Diaz O, Ellsworth P. Pelvic plexiform neurofibroma during bowel/bladder dysfunction in an NF1 pediatric patient: A case report. Urol Case Rep. 2021 May 21;38:101722. 20) Sawada Y. Hemorrhage into a plexiform neurofibroma induced by trauma: a rare complication of von Recklinghausen's disease. J Dermatol. 1987;14(4):378–81.; Tung TC, Chen YR, Chen KT, Chen CT, Bendor-Samuel R. Massive intratumor hemorrhage in facial plexiform neurofibroma. Head Neck. 1997;19(2):158–62; Miller J, Perotti V, Moore P. Massive spontaneous haemorrhage in a plexiform neurofibroma: A case report and discussion of the literature. J Clin Neurosci. 2020 Oct;80:229-231; Niddam J, Matheron C, La Padula S, Wolkenstein P, Meningaud JP. Hemostasis and Type 1 Neurofibromatosis. Plast Reconstr Surg Glob Open. 2017;5(7):e1414. Published 2017 Jul 26. Bergqvist, C., Servy, A., Valeyrie-Allanore, L. et al. Neurofibromatosis 1 French national guidelines based on an extensive literature review since 1966. Orphanet J Rare Dis 15, 37 (2020). 21) Lai JS, Jensen SE, Charrow J, Listernick R. Patient reported outcomes measurement information system and quality of life in neurological disorders measurement system to evaluate quality of life for children and adolescents with neurofibromatosis type 1 associated plexiform neurofibroma. J Pediatr 2019;206:190-6. 22) Copley-Merriman C, Yang X, Juniper M, Amin S, Yoo HK, Sen SS. Natural History and Disease Burden of Neurofibromatosis Type 1 with Plexiform Neurofibromas: A Systematic Literature Review. Adolesc Health Med Ther. 2021;12:55- 23) Published 2021 May 19. doi:10.2147/AHMT.S303456 24) Legius, E., Messiaen, L., Wolkenstein, P., Pancza, P., Avery, R.A., Berman, Y., Blakeley, J., Babovic-Vuksanovic, D., Cunha, K.S., Ferner, R., Fisher, M.J., Friedman, J.M., Gutmann, D.H., Kehrer-Sawatzki, H., Korf, B.R., Mautner, V.-F., Peltonen, S., Rauen, K.A., Riccardi, V. and Schorry, E. (2021). Revised diagnostic criteria for neurofibromatosis type 1 and Legius syndrome: an international consensus recommendation. Genetics in Medicine, [online] 23(8), pp.1506–1513. doi:10.1038/s41436-021-01170-5. 25) Bergqvist C. et al. NF France Network. Neurofibromatosis 1 French national guidelines based on an extensive literature review since 1966. Orphanet J Rare Dis. 2020 Feb 3;15(1):37. doi: 10.1186/s13023-020-1310-3. 26) UpToDate. Available at: https://www.uptodate.com/contents/nf2-relatedschwannomatosis- formerly-neurofibromatosis-type-2 (Accessed: January 11, 2023). 27) UpToDate. Available at: https://www.uptodate.com/contents/nf2-relatedschwannomatosis- formerly-neurofibromatosis-type-2 (Accessed: January 11, 2023). 28) Blakeley J and Plotkin S. Neuro-Oncology 2016;18:624-638. Friedrich R et al. World Journal of Surgical Oncology 2005;3:1-6.; Dogra B and Rana K. Indian Dermatol Online J 2013;4:195-198. Boyd K et al. J Am Acad Dermatol 2009;6:1-16. 29) Grover DSB, Kundra DR, Grover DH, Gupta DV, Gupta DR. Imaging diagnosis of plexiform neurofibroma- unravelling the confounding features: A report of two cases. Radiol Case Rep. 2021 Jul 17;16(9):2824-2833; Friedman J. J Child Neurol 2002;17:548-554.; Gross AM et al NEJM 2020;382:Suppl Protocol S1-S30; Grover D.S.B. et al. Imaging diagnosis of plexiform neurofibroma- unravelling the confounding features: A report of two cases. Radiol Case Rep. 2021 Jul 17;16(9):2824-2833. . 30) Tonsgard JH. Clinical manifestations and management of neurofibromatosis type 1. Semin Pediatr Neurol. 2006 Mar;13(1):2-7; Kehrer-Sawatzki H. et al. Clinical characterization of children and adolescents with NF1 microdeletions. Childs Nerv Syst 36, 2297–2310 (2020); 31) Neurofibromatosis Type 1 Workup: Laboratory Studies, Imaging Studies, Other Tests. [online] Available at: https://emedicine.medscape.com/article/1177266-workup#c4 [Accessed 3 Mar. 2023]. 32) Wilson M. et al. Diagnostic Accuracy of MRI for the Detection of Malignant Peripheral Nerve Sheath Tumors: A Systematic Review and Meta-Analysis. AJR Am J Roentgenol. 2021 Jul;217(1):31-39. doi: 10.2214/AJR.20.23403. 33) Carton, C., Evans, D.G., Blanco, I., Friedrich, R.E., Ferner, R.E., Farschtschi, S., Salvador, H., Azizi, A.A., Mautner, V., Röhl, C., Peltonen, S., Stivaros, S., Legius, E.,Oostenbrink, R., Brunet, J., Van Calenbergh, F., Cassiman, C., Czech, T., Gavarrete de León, M.J. and Giele, H. (2023). ERN GENTURIS tumour surveillance guidelines for individuals with neurofibromatosis type 1. eClinicalMedicine, 56, p.101818. doi: https://doi.org/10.1016/j.eclinm.2022.101818. 34) Russo C. et al. Non-Oncological Neuroradiological Manifestations in NF1 and Their Clinical Implications. Cancers (Basel). 2021 Apr 12; 13(8):1831. doi: 10.3390/cancers13081831. 35) Grover S.B. et al. Imaging diagnosis of plexiform neurofibroma- unravelling the confounding features: A report of two cases. Radiology case reports vol. 16,9 2824-2833. 17 Jul. 2021; Friedman JM. Neurofibromatosis 1. 1998 Oct 2 [Updated 2022 Apr 21]. In: Adam MP, Mirzaa GM, Pagon RA, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2022. https://www.ncbi.nlm.nih.gov/books/NBK1109/. 36) Russo C. et al. Non-Oncological Neuroradiological Manifestations in NF1 and Their Clinical Implications. Cancers (Basel). 2021 Apr 12; 13(8):1831. doi: 10.3390/cancers13081831. 37) Arshi A. et al. Malignant peripheral nerve sheath tumors of the head and neck: Demographics, clinicopathologic features, management, and treatment outcomes. Oral Oncol. 2015 Dec;51(12):1088-94. doi: 10.1016/j.oraloncology.2015.08.012. Epub 2015 Oct 9. PMID: 26442813. 38) Ortonne N, Wolkenstein P, Blakeley JO, Korf B, Plotkin SR, Riccardi VM, Miller DC, Huson S, Peltonen J, Rosenberg A, Carroll SL, Verma SK, Mautner V, Upadhyaya M, Stemmer-Rachamimov A. Cutaneous neurofibromas: Current clinical and pathologic issues. Neurology. 2018 Jul 10;91(2 Suppl 1):S5-S13; Friedman JM. Neurofibromatosis 1. 1998 Oct 2 [Updated 2022 Apr 21]. In: Adam MP, Mirzaa GM, Pagon RA, et al., editors. 39) GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993- 2022. Электронный ресурс: https://www.ncbi.nlm.nih.gov/books/NBK1109/ дата обращения 15.06.2022; Legius, E., Messiaen, L., Wolkenstein, P. et al. Revised diagnostic criteria for neurofibromatosis type 1 and Legius syndrome: an international consensus recommendation. Genet Med 23, 1506–1513 (2021). https://doi.org/10.1038/s41436-021-01170-5 40) Zhou, H. and Lu, H. (2021). A solitary giant neurofibroma of inguinal region: A case report. Science Progress, 104(1), p.003685042110042. doi:10.1177/00368504211004269. 41) Рында А.Ю., Олюшин В.Е., Ростовцев Д.М., Забродская Ю.М. Комплексное лечение пациента с нейрофиброматозом 2-го типа. Журнал неврологии и психиатрии им. С.С. Корсакова. 2020;120(8):98–104. https://doi.org/10.17116/jnevro202012008198 42) Plotkin, S.R., Messiaen, L., Legius, E., Pancza, P., Avery, R.A., Blakeley, J.O., Babovic-Vuksanovic, D., Ferner, R., Fisher, M.J., Friedman, J.M., Giovannini, M., Gutmann, D.H., Hanemann, C.O., Kalamarides, M., Kehrer-Sawatzki, H., Korf, B.R., Mautner, V.-F., MacCollin, M., Papi, L. and Rauen, K.A. (2022). Updated diagnostic criteria and nomenclature for neurofibromatosis type 2 and schwannomatosis: An international consensus recommendation. Genetics in Medicine, 24(9), pp.1967–1977. doi:https://doi.org/10.1016/j.gim.2022.05.007. 43) Brown R. Management of Central and Peripheral Nervous System Tumors in Patients with Neurofibromatosis. Curr Oncol Rep. 2023 Oct 31. doi: 10.1007/s11912- 023-01451-z. 44) Tiwari R, Singh AK. Neurofibromatosis Type 2. [Updated 2022 Oct 3]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK470350/ 45) Plotkin, S.R., Messiaen, L., Legius, E., Pancza, P., Avery, R.A., Blakeley, J.O., Babovic-Vuksanovic, D., Ferner, R., Fisher, M.J., Friedman, J.M., Giovannini, M., Gutmann, D.H., Hanemann, C.O., Kalamarides, M., Kehrer-Sawatzki, H., Korf, B.R., Mautner, V.-F., MacCollin, M., Papi, L. and Rauen, K.A. (2022). Updated diagnostic criteria and nomenclature for neurofibromatosis type 2 and schwannomatosis: An international consensus recommendation. Genetics in Medicine, 24(9), pp.1967–1977. doi:https://doi.org/10.1016/j.gim.2022.05.007. 46) Evans, D.G., Mostaccioli, S., Pang, D., Fadzil O Connor, M., Pittara, M., Champollion, N., Wolkenstein, P., Thomas, N., Ferner, R.E., Kalamarides, M., Peyre, M., Papi, L., Legius, E., Becerra, J.L., King, A., Duff, C., Stivaros, S. and Blanco, I. (2022). ERN GENTURIS clinical practice guidelines for the diagnosis, treatment, management, and surveillance of people with schwannomatosis. European Journal of Human Genetics, 30(7), pp.812–817. doi:10.1038/s41431-022-01086-x. 47) Tamura R. Current Understanding of Neurofibromatosis Type 1, 2, and Schwannomatosis. Int J Mol Sci. 2021 May 29;22(11):5850. doi: 10.3390/ijms22115850. PMID: 34072574; PMCID: PMC8198724. 48) David T. Miller, Debra Freedenberg, Elizabeth Schorry, Nicole J. Ullrich, David Viskochil, Bruce R. Korf, COUNCIL ON GENETICS, AMERICAN COLLEGE OF MEDICAL GENETICS AND GENOMICS, Emily Chen, Tracy L. Trotter, Susan A. Berry, Leah W. Burke, Timothy A. Geleske, Rizwan Hamid, Robert J. Hopkin, Wendy J. Introne, Michael J. Lyons, Angela E. Scheuerle, Joan M. Stoler; Health Supervision for Children With Neurofibromatosis Type 1. Pediatrics May 2019; 143 (5): e20190660. 10.1542/peds.2019-0660 49) Общая характеристика лекарственного препарата Коселуго (капсулы 10 мг, 25 мг). Регистрационное удостоверение РК-ЛС-5№026288 (10 мг), РК-ЛС-5№026289 (25 мг). Дата регистрации 01.10.2024. 50) Sait S. et al. Treatment of Pediatric Low-Grade Gliomas. Curr Neurol Neurosci Rep. 2023 Apr;23(4):185-199. doi: 10.1007/s11910-023-01257-3. 51) Gross A.M. et al. Selumetinib in Children with Inoperable Plexiform Neurofibromas // N. Engl. J. Med. N Engl J Med, 2020. Vol. 382, № 15. P. 1430–1442.
Информация
Организационные аспекты протокола
Список разработчиков протокола:
1) Жиенкулова Гульжанат Омаровна – кандидат медицинских наук, детский онколог/гематолог (координатор отделения Дневного стационара) отдел онкологии, Департамент Педиатрия КФ «UMC», г.Астана;
2) Нургалиев Даир Жванишевич – профессор, доктор медицинских наук, детский онколог-гематолог, кафедра детских болезней с курсами кардиоревматологии и гастроэнтерологии НАО «Медицинский университет Астана».
3) Абдилова Гульнара Калденовна – кандидат медицинских наук, высшая квалификационная категория, руководитель Республиканского центра детской онкологии и гематологии Научного центра педиатрии и детской хирургии МЗРК, г.Алматы;
4) Абильдинова Гульшара Жусуповна – доктор медицинских наук, профессор, главный внештатный генетик МЗ РК, руководитель лаборатории персонализированной геномной диагностики БМЦ УДП РК, г. Астана;
5) Идрисова Жаннат Рустемовна, доктор медицинских наук, профессор кафедры нервных болезней КазНМУ Асфендиярова, заведующая отделением Центр компетенции орфанных неврологических заболеваний у детей УК Аксай КазНМУ, г.Алматы;
Указание на отсутствие конфликта интересов: нет.
Рецензент: Ташенова Гульнара Талиповна – доктор медицинских наук, профессор, заведующая кафедрой детских болезней им. профессора Н.А. Барлыбаевой КазНМУ им.Асфендиярова, педиатр, онколог и гематолог.
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Информированное согласие пациента на проведение таргетной терапии селуметинибом
Пациент
ФИО (при наличии) пациента – полностью
Дата рождения: ____/____/_________ (дата, месяц, год рождения)
Даю свое согласие на проведение: ребенку/родственнику/подопечному (нужное подчеркнуть) таргетной терапии лекарственным препаратом:
1. Я информирован(а) о своем состоянии (состоянии ребенка, родственника, подопечного), о необходимости лечения.
Подпись:______________Дата:____/______/___________ Время:____
Если заполнил родственник/опекун/законный представитель пациента:
6) Жетимкаринова Гаухар Ерлановна – клинический фармаколог КФ «UMC»;
7) Орловский Владислав Николаевич – заведующий отделением Ортопедия №2 КФ «UMC», кандидат медицинских наук, высшая квалификационная категория;
8) Муканова Шолпан Насыровна, независимый медицинский эксперт, менеджер здравоохранения высшей категории, эксперт по методологии разработки клинических протоколов, начальник Отдела методологии и стандартизации бизнес процессов Департамента менеджмента качества КФ «UMC»;
9) Исатаева Нагима Мухамедрахимовна, кандидат медицинских наук, независимый медицинский эксперт, менеджер здравоохранения высшей категории, эксперт по методологии разработки клинических протоколов, главный менеджер Отдела методологии и стандартизации бизнес процессов Департамента менеджмента качества КФ «UMC».
Указание на отсутствие конфликта интересов: нет.
Рецензент: Ташенова Гульнара Талиповна – доктор медицинских наук, профессор, заведующая кафедрой детских болезней им. профессора Н.А. Барлыбаевой КазНМУ им.Асфендиярова, педиатр, онколог и гематолог.
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Приложение 1
Информированное согласие пациента на проведение таргетной терапии селуметинибом
Пациент
(родитель/опекун)______________________________________________________________________
ФИО (при наличии) пациента – полностью
Дата рождения: ____/____/_________ (дата, месяц, год рождения)
Даю свое согласие на проведение: ребенку/родственнику/подопечному (нужное подчеркнуть) таргетной терапии лекарственным препаратом:
_____________________________________________________________________________________ в
(Написано собственноручно)
_____________________________________________________________________________________
(Наименование медицинской организации)
1. Я информирован(а) о своем состоянии (состоянии ребенка, родственника, подопечного), о необходимости лечения.
2. Я уведомлен(а) о том, что дополнительные услуги, лекарственные средства и изделия медицинского назначения сверх гарантированного объема медицинской помощи государством, предоставляются за счет собственных средств, добровольного страхования или иных незапрещенных источников.
3. Мне в доступной форме разъяснена цель и альтернативные методы обследования и лечения, а также возможные последствия моего отказа от обследования и лечения.
4. Я уведомлен о возможных побочных или нежелательных явлении, которые могут возникнуть в результате терапии (паронихия, отслойка пигментного эпителия сетчатки, угревой дерматит, изменение состояния волос, отек, рвота, диарея, стоматит и др.).
5. Я знаю о праве отказаться от обследования и лечения при информировании меня о рисках для здоровья и подписании мной письменного отказа от предложенных вмешательств.
6. Я знаю о праве обратиться к другому врачу/ в другую организацию для получения альтернативного мнения о диагнозе и лечении.
7. Я знаю о том, что мое лечение координируется моим лечащим врачом.
8. Я знаю, что в моих интересах сообщить врачу обо всех имеющихся у меня (ребенка, родственника, подопечного) и известных мне проблемах со здоровьем, аллергиях, непереносимости лекарств, о наличии в прошлом или в настоящее время инфекционного гепатита, туберкулеза, венерических заболевании (в том числе сифилиса и ВИЧ-инфекции), а также о злоупотреблении алкоголем и/или пристрастии к наркотическим препаратам.
9. Я сообщаю о том, что у меня (ребенка, родственника, подопечного): нет аллергии.
Есть аллергия на: _______________________________________________________________
(Указать на какие лекарственные препараты, продукты и иное есть аллергия)
10. Я понимаю, что нарушение врачебных рекомендаций, несоблюдение режима, а также сокрытие информации о состоянии здоровья может привести к местным и общим осложнениям и другим неблагоприятным последствиям.
11. В случае возникновения во время обследования и лечения непредвиденных осложнений состояний, угрожающих моему здоровью, даю согласие на изменение тактики, плана обследования, лечения, включая отказ от его выполнения, с последующим информированием меня об этом.
12. Я даю добровольное согласие на предоставление сведений персонифицированного характера о пациенте и обработку личных данных с целью формирования и использования электронных информационных ресурсов здравоохранения.
13. Я ознакомлен(а) со всеми пунктами настоящего документа и согласен (на) с ними.
Подпись:______________Дата:____/______/___________ Время:____
Если заполнил родственник/опекун/законный представитель пациента:
___________________________________________________ Степень родства: ______________________
ФИО (при наличии) – полностью
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.