Миастения
 Версия: Клинические протоколы МЗ РК - 2024 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2024 (Казахстан)
Myasthenia gravis (G70.0), Myasthenia gravis и другие нарушения нервно-мышечного синапса (G70), Врожденная или приобретенная миастения (G70.2), Другие нарушения нервно-мышечного синапса (G70.8), Нарушение нервно-мышечного синапса неуточненное (G70.9), Токсические нарушения нервно-мышечного синапса (G70.1)
Неврология
Общая информация
Краткое описание
Одобрено
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «04» марта 2025 года
Протокол №226
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «04» марта 2025 года
Протокол №226
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАНОСТИКИ И ЛЕЧЕНИЯ
МИАСТЕНИЯ
Миастения – классическое аутоиммунное заболевание, клинические проявления которого в виде слабости и патологической мышечной утомляемости обусловлены явлениями аутоагрессии с образованием антител, направленных к различным антигенным мишеням периферического нейромоторного аппарата. Характерно бимодальное возрастное распределение заболеваемости миастенией с ранним началом в третьем десятилетии жизни (преимущественно женщины) и миастения с поздним началом у пожилых людей (преимущественно мужчины).
ВВОДНАЯ ЧАСТЬ
Код(ы) МКБ-10:
G70 Myasthenia gravis и другие нарушения нервно-мышечного синапса
G70.0 Myasthenia gravis
G70.1 Токсические нарушения нервно-мышечного синапса
G70.2 Врожденная или приобретенная миастения
G70.8 Другие нарушения нервно-мышечного синапса
G70.9 Нарушение нервно-мышечного синапса неуточненное
Дата разработки и пересмотра протокола: 2016 год (пересмотр 2024 год).
Пользователи протокола: неврологи, офтальмологи, ревматологи, торакальные хирурги, психологи, диетологи, физиотерапевты, эрготерапевты, логопеды, терапевты.
Категория пациентов: взрослые.
Сокращения, используемые в протоколе:
АД - Артериальное давление
АХЭП - Антихолинэстеразные препараты
АТ - Антитела
АХР - Ацетилхолиновые рецепторы
ИВЛ - Искусственная вентиляция легких
КМС - Конгенитальные миастенические синдромы
КТ - Компьютерная томография
МГ - Миастения Гравис
МРТ - Магнитно-резонансная томография
AchR - Ацетилхолиновый рецептор
MuSK - Мышечно-специфическая тирозинкиназа
LRP4 - Белок 4, ассоциированный с рецептором липопротеинов низкой плотности
ЦСЖ - Цереброспинальная жидкость
ЭКГ - Электрокардиография
Шкала уровня доказательности:
G70.0 Myasthenia gravis
G70.1 Токсические нарушения нервно-мышечного синапса
G70.2 Врожденная или приобретенная миастения
G70.8 Другие нарушения нервно-мышечного синапса
G70.9 Нарушение нервно-мышечного синапса неуточненное
Дата разработки и пересмотра протокола: 2016 год (пересмотр 2024 год).
Пользователи протокола: неврологи, офтальмологи, ревматологи, торакальные хирурги, психологи, диетологи, физиотерапевты, эрготерапевты, логопеды, терапевты.
Категория пациентов: взрослые.
Сокращения, используемые в протоколе:
АД - Артериальное давление
АХЭП - Антихолинэстеразные препараты
АТ - Антитела
АХР - Ацетилхолиновые рецепторы
ИВЛ - Искусственная вентиляция легких
КМС - Конгенитальные миастенические синдромы
КТ - Компьютерная томография
МГ - Миастения Гравис
МРТ - Магнитно-резонансная томография
AchR - Ацетилхолиновый рецептор
MuSK - Мышечно-специфическая тирозинкиназа
LRP4 - Белок 4, ассоциированный с рецептором липопротеинов низкой плотности
ЦСЖ - Цереброспинальная жидкость
ЭКГ - Электрокардиография
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортных или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с не высоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
Классификация
Классификация [2]:
По степени генерализации двигательных расстройств:
1. Локальная форма - глазная; бульбарная; туловищная; лицевая
2. Генерализованная форма: без бульбарных нарушений, с бульбарными нарушениями и генерализованные с нарушениями дыхания (периодическими дыхательными кризами)
По тяжести двигательных расстройств:
-
легкая форма;
-
среднетяжелая форма;
-
тяжелая форма.
По характеру течения миастенического процесса:
-
миастенические эпизоды;
-
миастеническое состояние;
-
прогрессирующее течение;
-
злокачественная форма
Клиническая классификация миастении MGFA (Myasthenia Gravis Foundatoin of America)
|
Класс І
|
Глазная форма. Любая слабость глазных мышц. Может быть слабость закрытия глаз. Сила всех остальных мышц — нормальная.
|
|
Класс ІІ
|
Легкая мышечная слабость (кроме глазных мышц). Может сопровождаться слабостью глазных мышц любой выраженности.
|
|
ІІ-А
|
Доминирует слабость мускулатуры конечностей и\или аксиальной мускулатуры. Может сопровождаться менее выраженной слабостью орофарингеальной мускулатуры.
|
|
ІІ-B
|
Доминирует поражение орофарингеальной мускулатуры и/или дыхательной мускулатуры. Может также включать менее выраженное или эквивалентное поражение мускулатуры конечностей и\или аксиальной мускулатуры.
|
|
Класс ІІІ
|
Умеренная мышечная слабость (кроме глазных мышц). Может сопровождаться слабостью глазных мышц любой выраженности.
|
|
ІІІ-А
|
Доминирует слабость мускулатуры конечностей и/или аксиальной мускулатуры. Может сопровождаться менее выраженной слабостью орофарингеальной мускулатуры
|
|
ІІІ-B
|
Доминирует поражение орофарингеальной мускулатуры и/или дыхательной мускулатуры. Может также включать менее выраженное или эквивалентное поражение мускулатуры конечностей и/или аксиальной мускулатуры
|
|
Класс ІV
|
Выраженная мышечная слабость (кроме глазных мышц). Может сопровождаться слабостью глазных мышц любой выраженности.
|
|
IV-A
|
Доминирует слабость мускулатуры конечностей и/или аксиальной мускулатуры. Может сопровождаться менее выраженной слабостью орофарингеальной мускулатуры.
|
|
IV-B
|
Доминирует поражение орофарингеальной мускулатуры и\или дыхательной мускулатуры. Может также включать менее выраженное или эквивалентное поражение мускулатуры конечностей и/или аксиальной мускулатуры
|
|
Класс V
|
Необходимость в интубации, сопровождающейся /или не сопровождающейся механической вентиляцией (кроме рутинного послеоперационного ведения). При использовании назогастрального зонда без интубации пациентов относят к классу IVB.
|
Диагностика
Методы, подходы и процедуры диагностики [1-3,4-11]:
Диагностические критерии:
Жалобы и анамнез:
-
слабость, патологическая утомляемость мышц, которая возникает после физической нагрузки и уменьшается после отдыха;
-
опущение век;
-
двоение предметов;
-
быстрая утомляемость жевательных мышц при пережевывании, длительном разговоре;
-
осиплость голоса, «носовой» оттенок голоса, его «затухание»;
-
нечеткость речи;
-
затрудненное глотание;
-
наличие в прошлом кратковременных эпизодов слабости и утомляемости, полностью/частично регрессировавших самопроизвольно/на фоне неспецифического лечения;
-
семейный анамнез, наличие у родственников нервно-мышечных, аутоиммунных и онкологических заболеваний.
Подгруппы антител к AchR-, MuSK- и LRP4-зависимым миастениям и связанные с ними клинические особенности
|
Подгруппы
|
Возраст
|
Пол
|
Гистология вилочковой железы
|
Дополнительные антитела
|
Клиническая картина
|
|
AchR
|
|
|
|
|
|
|
Ранее начало
|
<50
|
Ж> M
|
Гиперплазия
|
Редко
|
Часто глазная форма
|
|
Позднее начало
|
>50
|
M> Ж
|
Атрофия
|
Часто (антител к тетину и рианодиновым рецепторам)
|
Генерализованная Форма
|
|
Ассоциированная с тимомой
|
Любой, но часто >50
|
M> Ж
|
Тимома
|
Часто (антител к тетину, актину и рианодиновым рецепторам и др.)
|
Тяжелая генерализованная форма
|
|
MuSK
|
Обычно <50
|
Ж> M
|
Нормальная (гиперплазия у 23% больных с антителами к MuSK-CBA)
|
Редко
|
Тяжелая генерализованная форма
|
|
LRP4
|
Любой
|
Ж> M
|
Нормальная (гиперплазия у 31%больного с единичным поражением и 67% с сочетанием LRP4/AchRпозитивной), отсутствие тимомы
|
Редко (антитела к ацетихолиновым рецепторам и мышечной специфичной рецепторной тирозинкиназе)
|
Глазная или генерализованная форма средней степени тяжести; тяжелая форма при сочетанной LRP4/AchRпозитивной или LRP4/ MuSKпозитивной
|
Физикальное обследование:
Неврологический статус:
• глазодвигательные нарушения (птоз, диплопия). Птоз чаще двусторонний ассиметричный, утром выражен меньше, чем вечером. Диплопия усиливается при зрительной и физической нагрузке, на ярком свету, во второй половине дня, более выражена при взгляде вдаль.
• бульбарные нарушения: на фоне длительного разговора или во время приёма пищи голос приобретает гнусавый оттенок, появляется дизартрия, трудно выговаривать «Р», «Ш», «С», далее присоединяются нарушение глотания, поперхивания, попадание жидкой пищи в нос.
• дыхательные нарушения характеризуются затруднением вдоха, ослаблением кашлевого толчка, скоплением густой, вязкой слюны, которую невозможно сплюнуть.
• слабость жевательных мышц проявляется в виде утомления при жевании, иногда до отвисания нижней челюсти, больные во время еды поддерживают челюсть и помогают себе при жевании рукой.
• слабость мимической мускулатуры: амимия, губы полностью не смыкаются.
• характерна слабость проксимальных мышц конечностей, усиление слабости при нагрузке (подъеме по лестнице, при быстрой ходьбе и беге), уменьшение слабости утром и после отдыха.
• слабость мышц туловища и шеи чаще встречается у больных пожилого возраста и выражается в согнутой позе и свисающей голове
• вегетативно-трофические нарушения в виде сухости кожи и слизистых, парестезий, нарушений сердечного ритма, непереносимости ортостатических нагрузок и др. - выявляется у 10% больных миастенией
Характеристика симптомов при миастеническом и холинергическом кризах [2]
Неврологический статус:
• глазодвигательные нарушения (птоз, диплопия). Птоз чаще двусторонний ассиметричный, утром выражен меньше, чем вечером. Диплопия усиливается при зрительной и физической нагрузке, на ярком свету, во второй половине дня, более выражена при взгляде вдаль.
• бульбарные нарушения: на фоне длительного разговора или во время приёма пищи голос приобретает гнусавый оттенок, появляется дизартрия, трудно выговаривать «Р», «Ш», «С», далее присоединяются нарушение глотания, поперхивания, попадание жидкой пищи в нос.
• дыхательные нарушения характеризуются затруднением вдоха, ослаблением кашлевого толчка, скоплением густой, вязкой слюны, которую невозможно сплюнуть.
• слабость жевательных мышц проявляется в виде утомления при жевании, иногда до отвисания нижней челюсти, больные во время еды поддерживают челюсть и помогают себе при жевании рукой.
• слабость мимической мускулатуры: амимия, губы полностью не смыкаются.
• характерна слабость проксимальных мышц конечностей, усиление слабости при нагрузке (подъеме по лестнице, при быстрой ходьбе и беге), уменьшение слабости утром и после отдыха.
• слабость мышц туловища и шеи чаще встречается у больных пожилого возраста и выражается в согнутой позе и свисающей голове
• вегетативно-трофические нарушения в виде сухости кожи и слизистых, парестезий, нарушений сердечного ритма, непереносимости ортостатических нагрузок и др. - выявляется у 10% больных миастенией
Характеристика симптомов при миастеническом и холинергическом кризах [2]
|
Миастенический криз
|
Холинергический криз
|
|
Дисфункция симпатической и парасимпатической иннервации
|
|
|
Активация симпатической иннервации:
Мидриаз Угнетение слюноотделения, слюна густая, вязкая, сухость во рту Сухость слизистых и кожи Расширение бронхов, уменьшение выделения слизи Тахикардия, артериальная гипертензия Ослабление перистальтики кишечника. Атония, запоры Побледнение кожи, сужение сосудов |
Активация парасимпатической иннервации; мускариновые эффекты:
Миоз Усиление слюноотделения, слюна жидкая и водянистая Ринорея, слезотечение, повышение потоотделения Сужение бронхов, увеличение трахеобронхиальной секреции Брадикардия, артериальная гипотония Усиление перистальтики кишечника, спазмы, диарея, рвота, тенезмы Покраснение кожи, расширение сосудов |
|
Никотиновые эффекты
|
|
|
-
|
Фасцикуляции мышц, мышечные спазмы, тремор
|
Фармакологические пробы [2].
Проба с введением антихолинэстеразных препаратов. Неостигмина сульфат, 1,5 мл 0,05% раствора, или пиридостигмина бромид в дозе 10 мг вводят подкожно при весе больного 50-60 кг, в дозе 2,0 мл или 20 мг — при весе 60-80 кг соответственно и 2,5мл или 30 мг — при весе от 80 до 100 кг. При возникновении мускариновых эффектов антихолинэстеразных препаратов после оценки эффективности теста вводят атропин в дозе 0,2-0,5 мл 0,1 % раствора. Оценка теста проводится в интервале от 30-40 до 90 мин после введения препарата. При полной и неполной компенсации двигательных нарушений пробу считают позитивной, при частичной -сомнительной, при отсутствии реакции – негативной [2].
Тест со льдом (The Ice-Pack Test) высокоспецифичный тест для лежачих больных, который можно использовать у пациентов с птозом и подозрением на миастению.
Тест проводят следующим образом. Стерильные латексные перчатки наполняют льдом (температура от 0 до 4 °С) и кладут на закрытые веки обоих глаз на 2-5 минут, следя за тем, чтобы растаявший лед не вытекал на глаза и кожу. Для объективной регистрации результатов теста можно сделать фотоснимки до и после его проведения. Тест считают положительным, если глазная щель расширяется больше, чем на 2 мм по сравнению с исходной (птоз улучшается на 2 мм или больше) [12].
Лабораторные исследования [7,13-15]:
Основные лабораторные исследования:
• Иммуноферментный анализ на антитела к ацетилхолиновому рецептору, который является чувствительным и специфическим маркером миастении.
Положительный результат при титре антител> 0,45 нмоль/л.
• Иммуноферментный анализ на антитела к специфической мышечной тирозинкиназе, назначают при подозрении на серонегативную миастению.
Положительный результат при титре антител> 0,4 ед/мл.
• Определение электролитов крови – снижение показателей калия крови;
• Гормоны щитовидной железы: и тиреотоксикоз, и гипотиреоз могут усиливать слабость при миастении;
• Биохимический анализ крови – для измерения концентрации С-реактивного белка, альбумина, глюкозы, уровень калия и магния, мочевины и креатинина.
Дополнительные лабораторные исследования:
• Непрямая реакция иммунофлюоресценции на антитела к скелетным мышцам служат чувствительным клинико-лабораторным маркером тимомы у пациентов с миастенией, а также миастении с поздним началом. Референсные значения <20.
Инструментальные исследования [15,16]:
Основные инструментальные исследования:
• Непрямая ритмическая супрамаксимальная стимуляции мышц (RNS)с регистрацией М-ответа (декремент-тест) позволяет оценить функциональное состояние нервно-мышечной передачи. Обследование больных миастенией позволяет при ритмической стимуляции мышц выявить снижение амплитуд М-ответов. Значения декремента М-ответа до 10% свидетельствуют об отсутствии нарушений нервно-мышечной передачи. Выявление декремента амплитуды и площади М-ответа больше 10% при повторной ритмической стимуляции нерва низкой(3имп/с) и высокой (50 имп/с) частотой с применением функциональных и фармакологических проб указывает на изменения, характерные для миастении.
• КТ/МРТ органов средостения, при необходимости с контрастированием: для исключения/подтверждения патологии вилочковой железы (тимома, гиперплазия вилочковой железы) с целью определения дальнейшей тактики лечения.
Дополнительные инструментальные исследования:
• Электромиография одиночного мышечного волокна (Single Fiber EMG) -высокоточный метод диагностики миастении. Измеряет нервно-мышечное дрожание, то есть латентную вариабельность деполяризации мышечных волокон, принадлежащих к одной и той же двигательной единице. При миастении сниженная амплитуда потенциала концевой пластинки (ПКП) удлиняет время достижения порога срабатывания (увеличение дрожания) и потенциал действия (ПД) мышечных волокон могут быть заблокирован.
Консультация профильных специалистов:
Проба с введением антихолинэстеразных препаратов. Неостигмина сульфат, 1,5 мл 0,05% раствора, или пиридостигмина бромид в дозе 10 мг вводят подкожно при весе больного 50-60 кг, в дозе 2,0 мл или 20 мг — при весе 60-80 кг соответственно и 2,5мл или 30 мг — при весе от 80 до 100 кг. При возникновении мускариновых эффектов антихолинэстеразных препаратов после оценки эффективности теста вводят атропин в дозе 0,2-0,5 мл 0,1 % раствора. Оценка теста проводится в интервале от 30-40 до 90 мин после введения препарата. При полной и неполной компенсации двигательных нарушений пробу считают позитивной, при частичной -сомнительной, при отсутствии реакции – негативной [2].
Тест со льдом (The Ice-Pack Test) высокоспецифичный тест для лежачих больных, который можно использовать у пациентов с птозом и подозрением на миастению.
Тест проводят следующим образом. Стерильные латексные перчатки наполняют льдом (температура от 0 до 4 °С) и кладут на закрытые веки обоих глаз на 2-5 минут, следя за тем, чтобы растаявший лед не вытекал на глаза и кожу. Для объективной регистрации результатов теста можно сделать фотоснимки до и после его проведения. Тест считают положительным, если глазная щель расширяется больше, чем на 2 мм по сравнению с исходной (птоз улучшается на 2 мм или больше) [12].
Лабораторные исследования [7,13-15]:
Основные лабораторные исследования:
• Иммуноферментный анализ на антитела к ацетилхолиновому рецептору, который является чувствительным и специфическим маркером миастении.
Положительный результат при титре антител> 0,45 нмоль/л.
• Иммуноферментный анализ на антитела к специфической мышечной тирозинкиназе, назначают при подозрении на серонегативную миастению.
Положительный результат при титре антител> 0,4 ед/мл.
• Определение электролитов крови – снижение показателей калия крови;
• Гормоны щитовидной железы: и тиреотоксикоз, и гипотиреоз могут усиливать слабость при миастении;
• Биохимический анализ крови – для измерения концентрации С-реактивного белка, альбумина, глюкозы, уровень калия и магния, мочевины и креатинина.
Дополнительные лабораторные исследования:
• Непрямая реакция иммунофлюоресценции на антитела к скелетным мышцам служат чувствительным клинико-лабораторным маркером тимомы у пациентов с миастенией, а также миастении с поздним началом. Референсные значения <20.
Инструментальные исследования [15,16]:
Основные инструментальные исследования:
• Непрямая ритмическая супрамаксимальная стимуляции мышц (RNS)с регистрацией М-ответа (декремент-тест) позволяет оценить функциональное состояние нервно-мышечной передачи. Обследование больных миастенией позволяет при ритмической стимуляции мышц выявить снижение амплитуд М-ответов. Значения декремента М-ответа до 10% свидетельствуют об отсутствии нарушений нервно-мышечной передачи. Выявление декремента амплитуды и площади М-ответа больше 10% при повторной ритмической стимуляции нерва низкой(3имп/с) и высокой (50 имп/с) частотой с применением функциональных и фармакологических проб указывает на изменения, характерные для миастении.
• КТ/МРТ органов средостения, при необходимости с контрастированием: для исключения/подтверждения патологии вилочковой железы (тимома, гиперплазия вилочковой железы) с целью определения дальнейшей тактики лечения.
Дополнительные инструментальные исследования:
• Электромиография одиночного мышечного волокна (Single Fiber EMG) -высокоточный метод диагностики миастении. Измеряет нервно-мышечное дрожание, то есть латентную вариабельность деполяризации мышечных волокон, принадлежащих к одной и той же двигательной единице. При миастении сниженная амплитуда потенциала концевой пластинки (ПКП) удлиняет время достижения порога срабатывания (увеличение дрожания) и потенциал действия (ПД) мышечных волокон могут быть заблокирован.
Консультация профильных специалистов:
-
консультация торакального хирурга – установление/исключения объемного образования средостения (тимома);
-
консультация терапевта – установление/исключение терапевтического заболевания, онкопатологии внутренних органов (артериальная гипертензия, злокачественное новообразование, пневмония);
-
консультация эндокринолога – установление/исключение заболевания щитовидной железы;
-
консультация онколога – установления онкологического заболевания, проявление паранеопластического синдрома.
-
консультация офтальмолога – осмотр глазного дна для исключения патологии глаза, признаков внутричерепной гипертензии, застоя дисков зрительных нервов.
-
мультидисциплинарная группа- невролог, кардиолог, пульмонолог.
Диагностический алгоритм [16]:
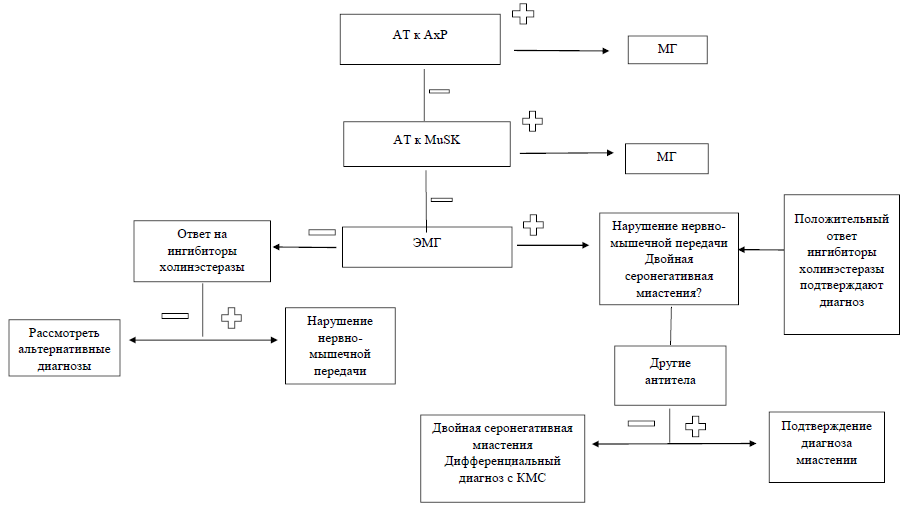
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных методов исследования [17-26]:
| Диагноз | Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Миопатии (мышечные дистрофии, врожденные миопатии, воспалительные, метаболические, токсические миопатии) | Прогрессирующая мышечная слабость | Повышение активности КФК в крови; возможно увеличение СОЭ; биопсия мышц | Мышечная слабость при миопатиях более выражена в проксимальных отделах и носит симметричный характер, характерны затруднения при поднимании рук, вставании со стула, подъеме по лестнице; возможны мышечные боли, мышечная гипотрофия или псевдогипертрофии; миотонический феномен |
| Полинейропатии (идиопатические воспалительные; наследственные; полинейропатии при метаболических расстройствах, экзогенных интоксикациях, системных и инфекционных заболеваниях, вакцинациях, злокачественных новообразованиях) | Мышечная слабость, быстрая утомляемость | В спинномозговой жидкости белковоклеточная диссоциация (в определенные сроки заболевания); при ЭНМГ – признаки демиелинизации и аксонопатии | Характерны периферические тетрапарезы, арефлексия, нарушения чувствительности по типу «носков» и «перчаток», вегетативные проявления |
| Миастенический синдром Ламберта Итона (МСЛИ) при бронхогенной карциноме (реже при раке предстательной железы, лимфоме, лейкозе). | Мышечная слабость, утомляемость | Детальный сбор анамнеза; КТ органов грудной клетки; специфические онкомаркеры | Типичным признаком МСЛИ является слабость и утомляемость проксимальных отделов ног и тазового пояса, в меньшей степени характерны слабость в проксимальных отделах рук, также редки глазодвигательные нарушения, расстройства глотания и речи. Характерно развитие «сухого» синдрома в связи с дисфункцией автономной вегетативной нервной системы (нарушения саливации, потоотделения, ортостатическая гипотензия). Своеобразным проявлением МСЛИ является снижение или отсутствие сухожильных рефлексов и несоответствие жалоб больных на мышечную слабость и отсутствия снижения мышечной силы в исследуемых мышцах |
| Митохондриальные энцефаломиопатии, синдром Кирнса Сейра | 2-х сторонний птоз, наружный офтальмопарез, мышечная утомляемость в проксимальных отделах конечностей | Повышение уровня белка в ЦСЖ; ЭКГ – атриовентрикулярная блокада различной степени | Заболевание обычно проявляется в детском возрасте, не позднее 2-го десятилетия жизни, типична пигментная ретинопатия, мозжечковая атаксия, нарушения проводимости сердца. Течение медленно прогрессирующее |
| Конгенитальные миастенические синдромы | Мышечная слабость | Слабость в окулярных, бульбарных и туловищных мышцах проявляются в младенчестве или раннего детства, положительного семейного анамнеза. Негатативный тест на антитела к ацетилхолиновым рецепторам. | Группа наследственных нейромышечных заболеваний, обусловленных мутацией генов, ответственных за образование и функциональное состояние ацетилхолиновых рецепторов, ионных каналов, энзимов, обеспечивающих надежность проведения возбуждения с нерва на мышцу. |
| Нарушение мозгового кровообращения в вертебробазилярной системе | Бульбарный синдром, офтальмоплегия | Магнитно-резонансная томография головного мозга, осмотр глазного дна, консультация терапевта, инфекциониста. |
- острое начало, обусловленное физическим и/или эмоциональным перенапряжением на фоне высокого артериального давления; - наличие предшествующего сосудистого анамнеза; - наличие на МРТ сканах признаков сосудистого заболевания головного мозга - на глазном дне – ангиопатия сосудов сетчатки, гиперемия; - подтверждение терапевтом артериальной гипертензии; - отсутствие динамичности бульбарных нарушений и реакции на введение антихолинэстеразных препаратов |
| Стволовой энцефалит | Бульбарные проявления, диплопия | Магнитно-резонансная томография головного мозга, осмотр глазного дна, исследование ликвора |
- Для клинического течения стволового энцефалита характерно острое начало. - Определяются очаговые неврологические симптомы, альтернирующие синдромы - При исследовании глазного дна –признаки внутричерепной гипертензии, застоя дисков зрительных нервов - В анализах спинномозговой жидкости – воспалительные изменения - МРТ головного мозга – очаговое поражение головного мозга воспалительного характера |
| Объемный процесс головного мозга | Опухоли головного мозга стволовой локализации некоторое время могут иметь латентный период и проявляться мышечной слабостью. | Магнитно-резонансная томография головного мозга с контрастированием, осмотр глазного дна, консультация нейрохирурга. |
- подострое развитие общемозгового цефалгического синдрома - на МРТ-сканах наличие объемного образования головного мозга; - на глазном дне – признаки внутричерепной гипертензии, явления застойных дисков зрительных нервов; - подтверждение наличия объемного образования головного мозга нейрохирургом; отсутствие динамичности бульбарных нарушений и реакции на введение антихолинэстеразных препаратов |
| Боковой амиотрофический склероз (БАС) | признаки центрального и/или периферического паралича, отсутствие чувствительных и тазовых расстройств, клинические симптомы миастении, нарушения нервно- мышечной передачи и реакции на введение антихолинэстеразных препаратов. | Электронейромиография (ЭНМГ) | - при ЭНМГ исследовании выявляются характерные для БАС признаки денервации и реиннервации, а также наличие большого количества потенциалов фасцикуляций |
Лечение (амбулатория)
Тактика лечения на амбулаторном уровне [1, 16, 27-39, 46-52]:
Основные принципы лечения миастении определяются такими направлениями:
- компенсация нервно-мышечной передачи;
- коррекция аутоиммунных нарушений;
- влияние на вилочковую железу.
1) Немедикаментозное лечение:
Режим: общий.
Диета: стол №15.
2) Медикаментозное лечение:
Перечень основных лекарственных средств (имеющих 100 % вероятность применения):
2) Медикаментозное лечение:
Перечень основных лекарственных средств (имеющих 100 % вероятность применения):
| Фармакотерапевтическая группа | МНН лекарственного средства | Способ применения | УД |
| Антихолинэстеразное средство | Пиридостигмина бромид | Перорально в начальной дозе: 30-60 мг 3 раза в день поддерживающая доза: 60- 120 мг 4 раза в день начало действия: 30-60 минут | А |
| Глюкокортикостероид | Преднизолон | Перорально в начальной дозе: 20-60 мг в день поддерживающая доза: 20-60 мг в день с медленным снижением начало действия: 10-20дней | А |
| Иммунодепрессивное средство | Циклоспорин | Перорально в начальной дозе: 100мг 2 раза в день поддерживающая доза: 3-5 мг/кг в день, разделенная на 2 приема, начало действия: 1-3 месяца | А |
| Иммунодепрессивное средство, антиметаболит | Азатиоприн | Перорально в начальной дозе: 50мг в день, поддерживающая доза: 150 мг в день или 2-3 мг/кг в день, начало действия: 6-18 месяцев | А |
| Иммунодепрессивное средство | Микофенолат мофетил | Перорально в начальной дозе: 500 мг в день поддерживающая доза: 500- 1500 мг 2 раза в день, начало действия:3-12 месяцев | В |
| Ингибиторы активности комплемента – антитела моноклональные. | Экулизумаб | Внутривенно капельно в начальной дозе: 900 мг/нед. в течение 4 недель, поддерживающая доза: 1200 мг каждые 2 недели начало действия: 2-12 недель | В |
| Противоопухолевое средство, антиметаболит | Метотрексат | Перорально в начальной дозе: начальная доза: 2,5 мг/нед поддерживающая доза: 15-25 мг /нед начало действия: 6-12 месяцев | В |
Перечень дополнительных лекарственных средств (менее 100 % вероятности применения):
| Фармакотерапевтическая группа | МНН лекарственного средства | Способ применения | УД |
| Глюкокортикостероид | Метилпреднизолон | Перорально в начальной дозе: от 4 до 16 мг в день поддерживающая доза: 32-64 мг в день с медленным снижением начало действия: 10- 20дней | В |
| Противоопухолевое средство – антитела моноклональные | Ритуксимаб | Внутривенно капельно в начальной дозе: 1г каждые 2 недели, разделенные на 2 приема или 375 мг/м2 площади поверхности тела (ППТ) еженедельно в течение 4 недель поддерживающая доза: повторять курс повторно через 6 месяцев при необходимости начало действия: 1-3 месяцев | С |
| Противоопухолевое средство, алкилирующее соединение | Циклофосфамид | Внутривенно в начальной дозе: 0,5-1,5 г/м2 площади поверхности тела (ППТ) или 50-100 мг/сут перорально поддерживая доза: 0,5- 1г/м2 ППТ ежемесячно или50-100 мг/сут перорально | С |
| Ингибиторы активности комплемента – антитела моноклональные. | Равулизумаб |
Вводится внутривенно. Дозирование основано на массе тела пациента: нагрузочная дозы (1 доза на 2 недели): • пациентам с массой тела от 40-59 кг - 2400 мг • пациентам от 60-99 кг 2700 мг пациентам с массой тела 100кг и больше 3000 мг через 2 недели поддерживающие дозы 1 раз в 8 недель в зависимости от массы тела. • пациентам с массой тела от 40-59 кг поддерживающая доза 3000 мг пациентам от 60-99 кг 3300 мг пациентам с массой тела 100 кг и больше 3600 мг. Препарат вводится на стационарном уровне. |
В |
Ведение пациентов с миастенией во время беременности [45]
- Пиридостигмин считается безопасным при беременности, можно продолжить прием без изменений при наступлении беременности.
- Преднизолон является препаратом выбора иммуносупрессивной терапии во время беременности. Преднизолон следует продолжать только тем женщинам, которые нуждаются в этом лечении для контроля своего заболевания. Предпочтительнее поддерживать суточную дозу преднизолона ниже 20 мг.
- Микофенолата мофетил, метотрексат и циклофосфамид обладают тератогенным действием, избегать применения этих препаратов у всех женщин с миастенией, которые потенциально могут забеременеть (в возрасте 16–50 лет). Эти препараты следует отменить более чем за 3 месяца до зачатия. - Внутривенный иммуноглобулин используется при обострении миастении во время беременности. Терапевтический эффект сохраняется около 3 месяцев.
- Женщины с миастенией, перенесшие тимэктомию, имеют меньший риск обострений миастении во время беременности, а также меньший риск рождения детей с неонатальной миастенией.
- Прием фолиевой кислоты рекомендуется перед зачатием и во время беременности женщинам с миастенией так же, как и без миастении.
Рекомендации по назначению ингибиторов контрольных точек иммунитета (ИКИ)
К ингибиторам контрольных точек иммунитета (ИКИ) относятся: ипилимумаб, пембролизумаб, атезолизумаб, ниволумаб. Имеющаяся миастения не является абсолютным противопоказанием к использованию ИКИ, по крайней мере, у пациентов с хорошо контролируемым заболеванием (минимальные проявления или без них).
Однако у этих пациентов:
- Нужно избегать назначения комбинированной терапии (анти-CTLA-4 плюс моноклональные антитела против PD-1/PD-L1), учитывая более высокий риск тяжелых нежелательных явлений, связанным с иммунитетом.
- Обязателен тщательный клинический мониторинг, особенно дыхательной и бульбарной функции.
- Хотя терапевтический ответ на ИКИ кажется менее удовлетворительным у пациентов, получающих иммунодепрессанты, лечение миастении следует продолжать и возобновить у пациентов, которые находились в ремиссии до лечения ИКИ.
- Раннее интенсивная терапия высокими дозами глюкокортикостероидов в сочетании с плазмаферезом или внутривенным введением иммуноглобулина может потребоваться пациентам, у которых развились явные проявления миастении во время приема ИКИ. Решение об отмене ИКИ зависит от онкологического статуса.
- [51]
Рекомендации по назначению ритуксимаба и экулизумаба [51]:
Ритуксимаб следует рассматривать как ранний вариант терапии у пациентов с положительными антителами к MuSK, которые имеют неудовлетворительный ответ на начальную иммунотерапию. Ритуксимаб следует рассматривать при рефрактерной миастении, если другие иммунодепрессивные препараты неэффективны или есть непереносимость. Экулизумаб применяется при тяжелой рефрактерной миастении с положительными антителами к AChR.
Экулизумаб следует рассматривать после того, как применение других иммунотерапевтических средств оказалось безуспешным в достижении целей лечения.
Равулизумаб используется в качестве хронической иммунотерапии для пациентов с генерализованным миастенией, с положительным результатами к антителам к AChR. Время начала действия этого агента составляет от одной до двух недель, поэтому его можно также использовать в качестве промежуточной терапии к иммунотерапии замедленного действия у пациентов, у которых особенно желательно избегать или сводить к минимуму использование глюкокортикоидов.
Равулизумаб также применяется при тяжелой рефрактерной миастении с положительными антителами к AChR.
Равулизумаб также следует рассматривать после того, как применение других иммунотерапевтических средств оказалось безуспешным в достижении целей лечения.
Клинико-лабораторные критерии для назначения равулизумаба при генерализованной форме миастении гравис (гМГ):
1. Критерии включения:
1. Генерализованная форма миастении гравис, подтвержденная клиническим диагнозом, с наличием антител к ацетилхолиновому рецептору (серопозитивный вариант).
2. Возраст пациента старше 18 лет.16
1. Критерии включения:
1. Генерализованная форма миастении гравис, подтвержденная клиническим диагнозом, с наличием антител к ацетилхолиновому рецептору (серопозитивный вариант).
2. Возраст пациента старше 18 лет.16
2. Показания к назначению на фоне недостаточной эффективности стандартной терапии:
1. Недостаточная эффективность текущей терапии антихолинэстеразными препаратами, глюкокортикостероидами (ГКС) и/или иммуносупрессорами (азатиоприн, микофенолата мофетил и другие). Недостаточная эффективность определяется сохранением выраженных клинических симптомов, оцениваемых по шкале MG-ADL ≥6 баллов, несмотря на проводимую терапию.
2. Непереносимость стандартной терапии (ГКС, иммуносупрессоров) или развитие нежелательных явлений, препятствующих увеличению доз препаратов до терапевтических уровней.
3. Наличие сопутствующих заболеваний, препятствующих повышению доз ГКС или иммуносупрессоров до терапевтических доз, при сохранении симптомов (MG-ADL ≥6 баллов).
4. Рецидивирующее или тяжелое течение гМГ с обострениями и/или кризами, требующее регулярной резервной терапии:
• плазмаферез,
• введение внутривенного иммуноглобулина (IVIG),
• развитие осложнений от вышеуказанной терапии (например, нарушения электролитного баланса, инфекционные осложнения, катетер-ассоциированные осложнения).
3. Условия назначения:
1. Пациент должен иметь документально подтвержденную вакцинацию против менингококковой инфекции.
2. Назначение равулизумаба возможно только при соблюдении строгих требований к предтерапевтическому скринингу и мониторингу пациента в процессе лечения, включая оценку состояния иммунного статуса.
Примечания: Равулизумаб рекомендуется для применения в специализированных центрах, имеющих опыт лечения миастении гравис и возможность проведения мультидисциплинарного наблюдения.
Хирургическое вмешательство: нет.
Дальнейшее ведение:
Наблюдение профильными специалистами на уровне консультативно-диагностической помощи: сроки наблюдения - пожизненно, периодичность осмотров - 2 раза в год, необходимый минимум лабораторных и диагностических исследований – электронейромиография 2 раза в год, КТ органов грудной клетки, МРТ органов средостения по показаниям (1 раз в год) [54].
Индикаторы эффективности лечения: - полная или достаточная компенсации двигательных нарушений - отсутствие бульбарных и дыхательных нарушений 4.
Лечение (стационар)
Тактика лечения на стационарном уровне:
Алгоритм ведения пациента с миастеническим кризом
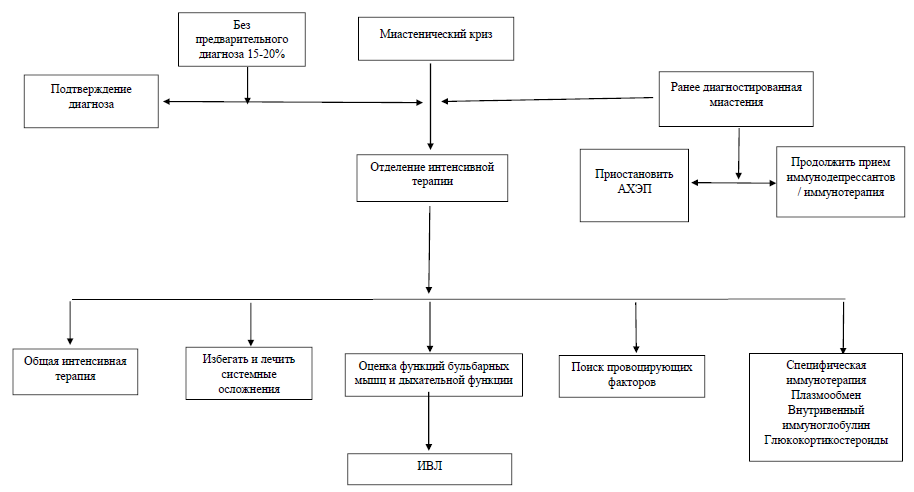
Немедикаментозное лечение:
Режим: постельный, палатный.
Режим: постельный, палатный.
Диета: при ИВЛ - рациональное парентеральное или зондовое питание.
Медикаментозное лечение [40,41]:
Лечение миастенических кризов должно быть направлено на компенсации нарушений нервно-мышечной передачи и коррекцию иммунных расстройств.
Медикаментозное лечение [40,41]:
Лечение миастенических кризов должно быть направлено на компенсации нарушений нервно-мышечной передачи и коррекцию иммунных расстройств.
Миастенический криз — неотложное состояние, характеризующееся угнетением дыхания вследствие слабости мышц диафрагмы и риском аспирации вследствие выраженной слабости орофарингеальной мускулатуры.
Холинергический криз — это состояние, имеющее особый механизм развития, обусловленный избыточной активацией никотиновых и мускариновых холинорецепторов вследствие передозировки антихолинестеразными препаратами.
Искусственная вентиляция легких
В качестве первого мероприятия предполагает необходимость адекватного дыхания с помощью принудительной ИВЛ.
Показания к переводу на ИВЛ:
- нарушение ритма дыхания;
- цианоз;
- возбуждение;
- потеря сознания;
- участие вспомогательной мускулатуры;
- изменение величины зрачков отсутствие реакции на введение АХЭ препаратов.
NB! В период проведения искусственной вентиляции легких полностью исключается введение антихолинэстеразных препаратов, проводится интенсивное лечение интеркуррентных заболеваний и патогенетическое лечение миастении.
NB! Через 16-24 ч после начала ИВЛ, при условии ликвидации клинических черт холинергического или смешанного кризов, следует провести пробу с введением неостигмина метилсульфата. При положительной реакции на введение неостигмина метилсульфата можно прервать ИВЛ и, убедившись в возможности адекватного дыхания, перевести больного на прием оральных антихолинэстеразных препаратов.
При отсутствии положительной реакции на введение неостигмина метилсульфата необходимо продолжить ИВЛ, повторяя пробу через каждые 24-36 ч [2].
При холинергическом кризе для устранения мускаринового эффекта ацетилхолина вводят атропин [43].
Перечень основных лекарственных средств (имеющих 100 % вероятность применения):
| Фармакотерапевтическая группа | МНН лекарственного средства | Способ применения | УД |
| Антихолинэстеразное средство | Неостигмина метилсульфат | Для непрерывной внутривенной инфузии от 0,002 до 0,012 мг/кг/час [42] | А |
| Иммуноглобулины, человеческий нормальный | Иммуноглобулин | Внутривенно в начальной дозе: 2 г/кг на 2–5 дней внутривенно поддерживающая доза:0,4-1 г/кг каждые 1-6 месяцев | В |
| Глюкокортикостероиды | Преднизолон | Внутривенно в начальной дозе – 1-2 мг/кг в сутки в 4-6 приемов, поддерживающая – 0,3- 0,6 мг/кг/сут | А |
| Ингибиторы активности комплемента – антитела моноклональные | Экулизумаб | Внутривенно капельно в начальной дозе: 900 мг/нед. в течение 4 недель, поддерживающая доза: 1200 мг каждые 2 недели начало действия: 2-12 недель. | В |
Перечень дополнительных лекарственных средств (менее 100 % вероятности применения) [2,53] :
| Фармакотерапевтическая группа | МНН лекарственного средства | Способ применения | УД |
| Калия препарат | Калия хлорид | При кризах внутривенно 70 мл 4% раствора на 400 мл 5% раствора глюкозы или физиологического раствора капельно медленно (со скоростью 20-30 капель в минуту) | С |
| Диуретическое калийсберегающее средство | Спиронолактон | При кризе внутрь 0,05 г 3-4 раза в день | С |
| М-холиноблокатор | Атропин | 2 мг внутривенно | С |
| Глюкокортикостероиды | Метилпреднизолон | Внутривенно в начальной дозе – от 4 мг до 48 мг в сутки в 4-6 приемов, высокие дозы при кризах от 200 до 1000 мг | В |
| Ингибиторы активности комплемента – антитела моноклональные. | Равулизумаб | Вводится внутривенно Дозирование основано на массе тела пациента: нагрузочная дозы (1 доза на 2 недели): • пациентам с массой тела от 40-59 кг - 2400 мг • пациентам от 60-99 кг 2700 мг • пациентам с массой тела 100кг и больше 3000 мг через 2 недели поддерживающие дозы 1 раз в 8 недель в зависимости от массы тела. • пациентам с массой тела от 40-59 кг поддерживающая доза 3000 мг пациентам от 60-99 кг 3300 мг пациентам с массой тела 100кг и больше 3600 мг | В |
Критерий назначения внутривенного иммуноглобулина (ВВИГ) и плазмообмена [29]
- Краткосрочная терапия умеренной и тяжелой миастении с целью обеспечить быстрое улучшение и служить переходным лечением к преднизолону или другим иммунодепрессантам с медленным началом действия;
- Поддерживающее лечение у пациентов с плохим ответом или непереносимостью нескольких иммунодепрессантов;
- В качестве предоперационной терапии для улучшения силы пациента;
- Плазмообмен предпочтительнее при миастеническом кризе из-за его более быстрого начала действия;
- Для обеспечения долгосрочного улучшения следует добавлять иммунодепрессанты или назначать их в более высоких дозах, чем до обострения миастении.
Клинико-лабораторные критерии для назначения равулизумаба при генерализованной форме миастении гравис (гМГ):
1. Критерии включения:
1. Генерализованная форма миастении гравис, подтвержденная клиническим диагнозом, с наличием антител к ацетилхолиновому рецептору (серопозитивный вариант).
2. Возраст пациента старше 18 лет.
2. Показания к назначению на фоне недостаточной эффективности стандартной терапии:
1. Недостаточная эффективность текущей терапии антихолинэстеразными препаратами, глюкокортикостероидами (ГКС) и/или иммуносупрессорами (азатиоприн, микофенолата мофетил и другие). Недостаточная эффективность определяется сохранением выраженных клинических симптомов, оцениваемых по шкале MG-ADL ≥6 баллов, несмотря на проводимую терапию.
2. Непереносимость стандартной терапии (ГКС, иммуносупрессоров) или развитие нежелательных явлений, препятствующих увеличению доз препаратов до терапевтических уровней.
3. Наличие сопутствующих заболеваний, препятствующих повышению доз ГКС или иммуносупрессоров до терапевтических доз, при сохранении симптомов (MG-ADL ≥6 баллов).
4. Рецидивирующее или тяжелое течение гМГ с обострениями и/или кризами, требующее регулярной резервной терапии:
• плазмаферез,
• введение внутривенного иммуноглобулина (IVIG),
• развитие осложнений от вышеуказанной терапии (например, нарушения электролитного баланса, инфекционные осложнения, катетер-ассоциированные осложнения).
Условия назначения:
1. Пациент должен иметь документально подтвержденную вакцинацию против менингококковой инфекции.
2. Назначение равулизумаба возможно только при соблюдении строгих требований к предтерапевтическому скринингу и мониторингу пациента в процессе лечения, включая оценку состояния иммунного статуса.
Примечания: Равулизумаб рекомендуется для применения в специализированных центрах, имеющих опыт лечения миастении гравис и возможность проведения мультидисциплинарного наблюдения.
Назначение препарата: Изначальное введение препарата равулизумаб возможно в условиях стационара, а также с использованием стационарзамещающих технологий, в кабинетах генно-инженерной биологической терапии. После инфузии препарата за состоянием пациента следует наблюдать в течение одного часа.
Хирургическое вмешательство [1, 44]:
Рекомендации по тимэктомии (операция по удалению вилочковой железы)
У пациентов без тимомы с генерализованной миастенией с АТ к АхР, в возрасте 18-50 лет, тимэктомия рассматривается на ранних стадиях заболевания для улучшения клинического течения и сведению к минимуму дозы и продолжительности иммунотерапии, а также потребности в госпитализации при обострении заболевания.
Тимэктомия должна быть настоятельно рекомендована пациентам с генерализованной миастенией с АТ с АхР, если они не реагируют на первоначальную иммунотерапию или имеют непереносимые побочные эффекты от этой терапии
Тимэктомия при миастении является плановой операцией и выполняется, когда пациент стабилен и может безопасно пройти процедуру, при которой послеоперационная боль и механические факторы могут ограничивать дыхательную функцию
Тимэктомия рекомендуется пациентам с генерализованной миастенией без определяемых антител к АхР, если они не отвечают адекватно на иммуносупрессивную терапию, или чтобы избежать/свести к минимуму непереносимые побочные эффекты от иммуносупрессивной терапии. Тимэктомия не показана пациентам с антителами к MuSK, LRP4 и агрину.
Тимэктомия должна быть настоятельно рекомендована пациентам с генерализованной миастенией с АТ с АхР, если они не реагируют на первоначальную иммунотерапию или имеют непереносимые побочные эффекты от этой терапии
Тимэктомия при миастении является плановой операцией и выполняется, когда пациент стабилен и может безопасно пройти процедуру, при которой послеоперационная боль и механические факторы могут ограничивать дыхательную функцию
Тимэктомия рекомендуется пациентам с генерализованной миастенией без определяемых антител к АхР, если они не отвечают адекватно на иммуносупрессивную терапию, или чтобы избежать/свести к минимуму непереносимые побочные эффекты от иммуносупрессивной терапии. Тимэктомия не показана пациентам с антителами к MuSK, LRP4 и агрину.
Противопоказания к тимэктомии: тяжелые соматические заболевания пациентов, а также острая фаза миастении (выраженные, не компенсируемые бульбарные нарушения, а также нахождение больного в состоянии криза) [1, 44].
Дальнейшее ведение [54]:
Наблюдение профильными специалистами на уровне консультативно-диагностической помощи: сроки наблюдения - пожизненно, периодичность осмотров - 2 раза в год, необходимый минимум лабораторных и диагностических исследований – электронейромиография 2 раза в год, КТ органов грудной клетки, МРТ органов средостения по показаниям (1 раз в год).
Индикаторы эффективности лечения:
Дальнейшее ведение [54]:
Наблюдение профильными специалистами на уровне консультативно-диагностической помощи: сроки наблюдения - пожизненно, периодичность осмотров - 2 раза в год, необходимый минимум лабораторных и диагностических исследований – электронейромиография 2 раза в год, КТ органов грудной клетки, МРТ органов средостения по показаниям (1 раз в год).
Индикаторы эффективности лечения:
- компенсация витальных нарушений;
- устранение метаболических нарушений, возникающих вследствие гипоксии и оксидантного стресса;
- снятие обострения миастенического процесса;
- полная или достаточная компенсации двигательных нарушений на фоне АХЭ препаратов.
Госпитализация
Показания для госпитализации с указанием типа госпитализации:
1) Показания для плановой госпитализации:
- пациенты с неполной компенсацией двигательных нарушений;
- пациенты с частичной компенсацией двигательных нарушений.
2) Показания для экстренной госпитализации: миастенический, холинергический криз.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2024
- Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2024 - 1. Narayanaswami P., Sanders 2. D.S., Wolfe G., Benatar M., Cea G., Evoli Aet al.International Consensus Guidance for Management of Myasthenia Gravis: 2020 Update//Neurology, 2020 3. Санадзе А.Г. Миастения и миастеническиесиндромы: руководство, 2-е изд., испр. //М.: ГЭОТАР-Медиа, 2019. 4. Avidan N, Le Panse R, Berrih-Aknin S, Miller A. Genetic basis of myasthenia gravis - A comprehensive review. J Autoimmun.2014;52:146–53. 5. Wang S., Breskovska I., Gandhy S., Punga A.R., Guptill J.T., Kaminski H.J. Advances in autoimmune myasthenia gravis management // Published in final edited form as: Expert Rev Neurother. 2018 Jul; 18(7): 573–588. 6. Dresser L., Wlodarski R., Rezania K., Soliven B. Myasthenia Gravis: Epidemiology, Pathophysiology and Clinical Manifestations // J Clin Med. 2021 Jun; 10(11): 2235. 7. Hehir M.K., Silvestri N.J. Generalized Myasthenia Gravis: Classification, Clinical Presentation, Natural History, and Epidemiology // Neurol Clin 2018 May;36(2):253-260. 8. Lazaridis К., Tzartos S.J. Autoantibody Specificities in Myasthenia Gravis; Implications for Improved Diagnostics and Therapeutics // Front Immunol. 2020; 11: 212. 9. Frykman H., Kumar Р., Oger J. Immunopathology of Autoimmune Myasthenia Gravis: Implications for Improved Testing Algorithms and Treatment Strategies // Front. Neurol., 09 December 2020 10. CaoМ., KonecznyI., Vincent A. Myasthenia Gravis With Antibodies Against Muscle Specific Kinase: An Update on Clinical Features, Pathophysiology and Treatment//Front. Mol. Neurosci., 02 September 2020 11. Rodolico C.,Bonanno C., Toscano A., Vita G. MuSK-Associated Myasthenia Gravis: Clinical Features and Management//Front. Neurol., 23 July 2020 12. Silvestri N. J., & Wolfe G. I. (2018). Myasthenia Gravis: Classification and Outcome Measurements. Myasthenia Gravis and Related Disorders, 307–318. 13. Rousseff R.T. Diagnosis of Myasthenia Gravis // J Clin Med. 2021 Apr; 10(8): 1736. 14. Chou CC, Su IC, Chou IJ, Lin JJ, Lan SY, Wang YS, Kong SS, Chen YJ, Hsieh MY, Hung PC, Wang HS, Chou ML, Lin KL. Correlation of anti-acetylcholine receptor antibody levels and long-term outcomes of juvenile myasthenia gravis in Taiwan: a case control study // BMC Neurol. 2019 Jul 18;19(1):170 15. Marino M, Basile U, Spagni G, Napodano C, Iorio R, Gulli F, Todi L, Provenzano C, Bartoccioni E, Evoli A. Long-Lasting Rituximab-Induced Reduction of Specific-But Not Total-IgG4 in MuSK-Positive Myasthenia Gravis. Front Immunol 2020 May 5;11:613. 16. Чухловина М. Диагностика и лечение миастении (возрастные аспекты). Издательство: СпецЛит, 2018 г. 17. Evoli A, Antonini G, Antozzi C. et al. Italian recommendations for the diagnosis and treatment of myasthenia gravis. Neurol Sci 2019; 40:1111–1124. 18. Nicolau S., Kao J.C., Liewluck T. Trouble at the junction: When myopathy and myasthenia overlap // Muscle Nerve 2019 Dec;60(6):648-657. 19. Ciafaloni E. Myasthenia Gravis and Congenital Myasthenic Syndromes // Continuum (MinneapMinn) 2019 Dec;25(6):1767-1784. 20. Kukulka N.,Bailey E.,Yelam A., Nagarajan E., Govindarajan R. Myasthenia Gravis Mimicking Stroke - Implications of Cognitive Errors and Clinical Factors // NeurologyApril 09, 2019; 92 21. Romano A.E, Al-Qudah Z, Kaminski H.J, et al. Concurrent Paraspinous Myopathy and Myasthenia Gravis // J Clin Neuromuscul Dis 2017;18:218–22 22. Tanovska N., Novotni G., Sazdova-Burneska S., Kuzmanovski I, Boshkovski B. Myasthenia Gravis and Associated Diseases // Open Access Maced J Med Sci 2018 Mar 5;6(3):472-478. 23. DjibaB., Diagne N., Dieng M., Faye A. et al.Myasthenia Associated with Other Autoimmune Diseases: A Series of Cases//Open Journal of Internal Medicine > Vol.10 No.1, March 2020 24. Santos-LasaosaS., López-Bravo A., Garcés-Redondo M.Amyotrophic lateral sclerosis and myasthenia gravis overlap syndrome: 3 new cases//Neurología, 2020 Vol. 35. Issue 8. 25. Propson A., Qureshi S., Farooq M. Inflammatory Myopathy with Superimposed Myasthenia Gravis – A Rare Overlap Syndrome (1016)// Neurology, April 14, 2020; 94 26. Uchio N., Taira K., Ikenaga C., Kadoya M. et al. Inflammatory myopathy with myasthenia gravis//Neurol NeuroimmunolNeuroinflamm. 2019 Mar; 6(2): e535. 27. Menon S.R.,Mokkath N.R. Myasthenia gravis masquerading as acute stroke: a case report// PanAfr Med J2020 Dec 2;37:305. 28. Электронная версия Примерного перечня ВОЗ об основных лекарственных средствах - на английском языке https://www.who.int/ru 29. Кокрановская библиотека https://www.cochranelibrary.com 30. HehirIIM.K., Li Y. Diagnosis and Management of Myasthenia Gravis//Continuum (MinneapMinn)2022 Dec 1;28(6):1615-1642. 31. Cortés-Vicente Е., Gallardo Е., Velasco R.A. Illa I. Myasthenia Gravis TreatmentUpdates//Current Treatment Options in Neurology, 2020 22(8) 32. Farmakidis C., Pasnoor M., Dimachkie MM, Barohn RJ. Treatment of Myasthenia Gravis // Neurol Clin. 2018 May;36(2):311-337. 33. Abuzinadah AR, Jabari D, Jawdat O, Pasnoor M, Glenn M, Herbelin L, et al. Satisfactory response with achieving maintenance low-dose prednisone in generalized myasthenia gravis // J Clin Neuromuscul Dis. (2018) 20:49–59. 34. Fortin E, Cestari DM, Weinberg DH. Ocular myasthenia gravis: an update on diagnosis and treatment // CurrOpinOphthalmol. (2018) 29:477–84. 35. Marino M, Bartoccioni E, Alboini PE, Evoli A. Rituximab in myasthenia gravis: a “to be or not to be” inhibitor of T cell function // Ann NY Acad Sci. (2018) 1413:41–48. 36. Beecher G, Anderson D, Siddiqi ZA. Rituximab in refractory myasthenia gravis: extended prospective study results // Muscle Nerve. (2018) 58:452–5. 37. Landon-Cardinal O, Friedman D, Guiguet M, Laforêt P, Heming N, Salort –Campana E, et al. Efficacy of rituximab in refractory generalized anti-AChR myasthenia gravis // J Neuromuscul Dis. (2018) 5:241–9. 38. Muppidi S, Utsugisawa K, Benatar M, Murai H, Barohn RJ, Illa I, et al. Long-term safety and efficacy of eculizumab in generalized myasthenia gravis // Muscle Nerve. (2019) 60:14–24. 39. Andersen H, Mantegazza R, Wang JJ, O'Brien F, Patra K, Howard F, Jr, et al. Eculizumab improves fatigue in refractory generalized myasthenia gravis // Qual Life Res. (2019) 28:2247–54. 40. Farrugia M.E., Goodfellow J.A. A Practical Approach to Managing Patients With Myasthenia Gravis—Opinions and a Review of the Literature//Front. Neurol., 07 July 2020 41. Harjana L.T., Hardiono. Myasthenia Crisis Vs Cholinergic Crisis: Challenges in Crisis Management Without Plasmapheresis or Intravenous Immunoglobulin (IVIG) // Indonesian Journal of Anesthesiology and Reanimation. Volume 2, Number 2, July 2020: 53-58 42. Лобзин С.В., Соколова М.Г., Шавуров В.А., Зуев А.А. Неотложная помощь пациентам с миастенией при кризах // Скорая медицинская помощь. — 2019. — №2. 43. Prado Jr. M.B., Adiao K.J. Acetylcholinesterase Inhibitors in Myasthenic Crisis: A Systematic Review of Observational Studies//Neurocrit Care. 2021 Jul 22: 1–17. 44. Adeyinka А; KondamudiN.P.Cholinergic Crisis// StatPearls Publishing; 2021 45. Evoli A., Meacci E. An update on thymectomy in myasthenia gravis // Expert Review of Neurotherapeutics. Apr 2019. 46. Gilhus N.E. Treatment considerations in myasthenia gravis for the pregnant patient // Expert Review of Neurotherapeutics. 2023 Feb 20;1-9. 47. Vu, T., Meisel, A., Mantegazza, R., Annane, D., Katsuno, M., Aguzzi, R., Enayetallah, A., Beasley, K.N., Rampal, N. and Howard, J.F. (2022). Terminal Complement Inhibitor Ravulizumab in Generalized Myasthenia Gravis. NEJM Evidence, 1(5). doi: https://doi.org/10.1056/evidoa2100066. 48. Vanoli, F. and Mantegazza, R. (2023). Ravulizumab for the treatment of myasthenia gravis. Expert Opinion on Biological Therapy, 23(3), pp.235–241. doi: https://doi.org/10.1080/14712598.2023.2185131. 49. Vu, T., Ortiz, S., Katsuno, M. et al. Ravulizumab pharmacokinetics and pharmacodynamics in patients with generalized myasthenia gravis. J Neurol (2023). https://doi.org/10.1007/s00415-023-11617-1. 50. ANNEX I SUMMARY OF PRODUCT CHARACTERISTICS. (n.d.). Available at: https://www.ema.europa.eu/en/documents/product-information/ultomiris-epar-productinformation_en.pdf. 51. HIGHLIGHTS OF PRESCRIBING INFORMATION. (n.d.). Available at: https://www.accessdata.fda.gov/drugsatfda_docs/label/2022/761108s023lbl.pdf. 52. UpToDate. Bird, S. (2023). [online] Uptodate.com. Available at: https://www.uptodate.com/contents/overview-of-the-treatment-of-myasthenia-gravis. 53. Sánchez-Tejerina, D., Sotoca, J., Llaurado, A., López-Diego, V., Juntas-Morales, R. and Salvado, M. (2022). New Targeted Agents in Myasthenia Gravis and Future Therapeutic Strategies. Journal of Clinical Medicine, 11(21), p.6394. 54. Гусев Е.И. Коновалов А.Н., Скворцова В.И. Неврология и нейрохирургия. Учебник в 2-х томах 4-е издание, дополненное // ГЭОТАР-Медиа, 2015 55. Приказ Министра здравоохранения Республики Казахстан от 23 октября 2020 года № ҚР ДСМ-149/2020. Об утверждении правил организации оказания медицинской помощи лицам с хроническими заболеваниями, периодичности и сроков наблюдения, обязательного минимума и кратности диагностических исследований.
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА:
Список разработчиков протокола:
1) Нургужаев Еркын Смагулович – доктор медицинских наук, профессор кафедры нервных болезней НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова», председатель «Ассоциация неврологов Республики Казахстана».
1) Нургужаев Еркын Смагулович – доктор медицинских наук, профессор кафедры нервных болезней НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова», председатель «Ассоциация неврологов Республики Казахстана».
2) Туруспекова Сауле Тлеубергеновна – доктор медицинских наук, профессор, Президент ОФ «Save our brain Central Asia research fund» SoBCARF, Член ОО «Ассоциации неврологов Республики Казахстан», Лиги неврологов PrimWFN, ESO, WSO, AD/PD, IPA, ISPRM, НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова», заведующая кафедрой нервных болезней, главный невролог Министерства здравоохранения Республики Казахстан.
3) Кудебаева Айгерим Жангильдыевна – старший преподаватель кафедры неврологии НУО «Казахстанско-Российский медицинский университет».
4) Атантаева Эльмира Балабековна – кандидат медицинских наук, доцент кафедры нервных болезней НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова».
5) Демесинова Баян Косболовна - ассистент кафедры нервных болезней НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова».
6) Жаркинбекова Назира Асановна - кандидат медицинских наук, профессор, АО «Южно-Казахстанская медицинская академия», заведующая кафедрой неврологии, психиатрии, реабилитиологии и нейрохирургии, главный внештатный невролог Управления Здравоохранения Туркестанской области, председатель Южно-Казахстанской ассоциации неврологов «Азия Нейро».
7) Жумаханов Даурен Бахытбекович – клинический нейрофизиолог центра нейрофизиологии и реабилитации Neurolab.
8) Ажар Таниберген– ассистент кафедры клинической фармакологии НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова».
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
1) Хайбуллин Талгат Нурмуханович – доктор медицинских наук, профессор, профессор кафедры неврологии, офтальмологии и оториноларингологии НАО «Медицинский университет Семей», врач-невролог высшей категории, член ОО «Ассоциация неврологов», «Лиги неврологов Казахстана» prim.
2) Лисник Виталий Стельянович – доктор-хабилитат медицинских наук, профессор кафедры неврологии Государственного университета медицины и фармации имени Николая Тестемицану (г. Кишинев, Республика Молдова). Председатель Общества неврологов Республики Молдова. Профессор консультант отделения невро-мышечных заболеваний Института Неврологии, Член комитета по образованию Европейской Академии неврологии, Делегат от Республики Молдова в WAN и EAN.
Указание условий пересмотра протокола: пересмотр не реже 1 раза в 5 лет и не чаще 1 раза в 3 года при наличии новых методов диагностики и лечения с уро
внем доказательности.
4) Атантаева Эльмира Балабековна – кандидат медицинских наук, доцент кафедры нервных болезней НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова».
5) Демесинова Баян Косболовна - ассистент кафедры нервных болезней НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова».
6) Жаркинбекова Назира Асановна - кандидат медицинских наук, профессор, АО «Южно-Казахстанская медицинская академия», заведующая кафедрой неврологии, психиатрии, реабилитиологии и нейрохирургии, главный внештатный невролог Управления Здравоохранения Туркестанской области, председатель Южно-Казахстанской ассоциации неврологов «Азия Нейро».
7) Жумаханов Даурен Бахытбекович – клинический нейрофизиолог центра нейрофизиологии и реабилитации Neurolab.
8) Ажар Таниберген– ассистент кафедры клинической фармакологии НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова».
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
1) Хайбуллин Талгат Нурмуханович – доктор медицинских наук, профессор, профессор кафедры неврологии, офтальмологии и оториноларингологии НАО «Медицинский университет Семей», врач-невролог высшей категории, член ОО «Ассоциация неврологов», «Лиги неврологов Казахстана» prim.
2) Лисник Виталий Стельянович – доктор-хабилитат медицинских наук, профессор кафедры неврологии Государственного университета медицины и фармации имени Николая Тестемицану (г. Кишинев, Республика Молдова). Председатель Общества неврологов Республики Молдова. Профессор консультант отделения невро-мышечных заболеваний Института Неврологии, Член комитета по образованию Европейской Академии неврологии, Делегат от Республики Молдова в WAN и EAN.
Указание условий пересмотра протокола: пересмотр не реже 1 раза в 5 лет и не чаще 1 раза в 3 года при наличии новых методов диагностики и лечения с уро
внем доказательности.
Приложение 1
Лекарственные препараты, которые не следует назначать или использовать с осторожностью [1].
| Препарат | Комментарий |
| Аминогликозиды (гентамицин, неомицин, тобрамицин) | Применяются при грамотрицательных бактериальных инфекциях. Может ухудшить течение миастении. Применять осторожно, если нет альтернативного лечения |
| Бета-блокаторы | Обычно назначают при артериальной гипертензии, заболеваниях сердца и мигрени. Может ухудшить течение миастении. Применять осторожно. |
| Ботулинический токсин | Блокатор пресинаптических нервно-мышечных соединений. Избегать применения при миастении. |
| Хлорохин и гидроксихлорохин | Применяется для лечения и профилактики малярии и при некоторых аутоиммунных заболеваниях. Может вызвать развитие миастении denovo или усугубить течение текущей миастении. Использовать только в случае необходимости и наблюдать за развитием ухудшения состояния. |
| Кортикостероиды | Входит в основную схему лечения миастении, но может вызвать ухудшение состояния в течение первых 2-х недель. Необходимо тщательное наблюдение. |
| Дефероксамин | Хелатирующий агент, используемый при гемохроматозе. Может ухудшить течение миастении |
| Пеницилламин | Применяется при болезни Вильсона-Коновалова и редко при ревматоидном артрите. В значительной мере является причиной развития миастении. Избегать применения |
| Фторхинолоны (ципрофлоксацин, левофлоксацин, моксифлоксацин и офлоксацин) | Антибиотики широкого спектра действия, которые вызывают ухудшение течения миастении. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США определило предупреждение «черного ящика» – рекомендация для потребителей о том, что лекарство может иметь серьезные и потенциально опасные побочные эффекты. Избегать использования или применять с осторожностью. |
| Ингибиторы контрольных точек иммунитета (ипилимумаб, пембролизумаб, атезолизумаб и ниволумаб) | Применяются при некоторых видах рака. Может вызвать развитие миастении denovo или усугубить течение текущей миастении. Применять с осторожностью в зависимости от онкологического статуса. |
| Йодсодержащие контрастные вещества | Имеются данные о возникновении повышенной утомляемости при миастении, однако современные контрастные вещества кажутся более безопасными. Применять осторожно и наблюдать за состоянием. |
| Макролиды (эритромицин, азитромицин и кларитромицин) | Антибиотики назначаются при грамположительных бактериальных инфекциях. Может ухудшить течение миастении. Избегать использования или применять с осторожностью. |
| Магний | Потенциально опасен при внутривенном введении, например, при эклампсии на поздних сроках беременности или при гипомагниемии. Применять только в случае крайней необходимости и наблюдать за состоянием. |
| Прокаинамид | Применяется при нарушениях сердечного ритма. Может ухудшить течение миастении. Применять с осторожностью. |
| Хинин | Иногда применяется при крампи. Использование запрещено, за исключением лечения малярии в США. |
| Статины (аторвастатин, правастатин, розувастатин и симвастатин) | Используется для снижения уровня холестерина в крови. Редко, но может ухудшить или ускорить развитие миастении. Внимательно оценить возможность ухудшения миастении в начале лечения статинами. |
| Телитромицин | Антибиотик применяется при внебольничной пневмонии. Препарат гепатотоксичен и повышает риск удлинения интервала QTс. Вызывает тяжелое ухудшение состояния, часто высокую смертность при миастении. Согласно предупреждению «черного ящика» Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США, противопоказан к использованию при миастении. Препарат снят с большинства международных рынков. Не применять при миастении. |
| Живые аттенуированные вакцины (корь, паротит, краснуха, ветряная оспа, грипп, полиомиелит, аденовирусы типов 4 и 7, Зоставакс (вакцина против опоясывающего герпеса), ротавирус, брюшной тиф, оспа и желтая лихорадка) | Не влияют на миастению, но противопоказаны пациентам, получающим иммуносупрессивную терапию, из-за риска побочных реакций. |
Приложение 2
Количественная шкала оценки тяжести клинических проявлений миастении QMGS (quantitative myasthenia gravis score)
|
Показатель
|
0 (отсутствует)
|
1 (умеренная )
|
2 (средняя)
|
3 (тяжёлая)
|
|
Диплопия при боковом взгляде влево или вправо, с
|
61
|
11-60
|
1-10
|
Спонтанно
|
|
Птоз (взгляд вверх), с
|
61
|
11-60
|
1-10
|
Спонтанно
|
|
Мышцы лица
|
Нормальное закрытие века
|
Полное, слабое, некоторое сопротивление некоторое усилие
|
Полное, без сопротивления
|
Неполное
|
|
Глотание 1 /2 стакана воды
|
Нормальное
|
Минимальное покашливание или прочистка горла
|
Тяжелый кашель, удушье или носовая регургитация
|
Не может глотать
|
|
Разговор после счета вслух от 1 до 50 (начало дизартрии)
|
Отсутствует
|
на 30-49 дизартрия
|
на 10-29 дизартрия
|
на 9 дизартрия
|
|
Вытягивание правой руки (90 градусов сидячее положение), c
|
240
|
90-239
|
10-89
|
0-9
|
|
Вытягивание левой руки (90 градусов сидячее положение), c
|
240
|
90-239
|
10-89
|
0-9
|
|
ЖЁЛ, % от должного
|
˃ 80
|
65-79
|
50-64
|
<50
|
|
Динамометрия справа, кг:
- мужчины - женщины |
>45
>30 |
15-44
10-29 |
5-14
5-9 |
0-4
0-4 |
|
Динамометрия слева, кг:
- мужчины - женщины |
>35
>25 |
15-34
10-24 |
5-14
5-9 |
0-4
0-4 |
|
Подъем головы (в положении лежа на спине 45 градусов)
|
120
|
30-119
|
1-29
|
0
|
|
Вытягивание правой ноги (в положении лежа на спине 45 градусов)
|
100
|
31-99
|
1-30
|
0
|
|
Вытягивание левой ноги (в положении лежа на спине 45 градусов)
|
100
|
31-99
|
1-30
|
0
|
Приложение 3
Шкала оценки силы мышц конечностей (A. Szobor)
|
0 баллов
|
Движения в мышце отсутствуют.
|
|
1 балл
|
Минимальные движения в мышце, но вес конечности пациент не удерживает.
|
|
2 балла
|
Пациент удерживает вес конечности, но сопротивление, оказываемое исследователю, минимально
|
|
3 балла
|
Пациент оказывает сопротивление усилиям изменить положение конечности, но оно незначительно.
|
|
4 балла
|
Пациент хорошо сопротивляется усилиям изменить положение конечности, но 20 имеется некоторое снижение силы.
|
|
5 баллов
|
Сила мышцы соответствует возрастной и конституциональной норме обследуемого.
|
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.