Изосерологическая несовместимость крови матери и плода
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Общая информация
Краткое описание
Одобрено
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Изосерологическая несовместимость крови матери и плода [5] – гуморальный иммунный ответ резус – отрицательной матери на эритроцитарные антигены резус-положительного плода, при котором образуются антирезусные антитела.
Изоиммунизация [2,5] – процесс образования аллоиммунных антиэритроцитарных антител к антигенам эритроцитов, отсутствующих у данного пациента. Эти антитела вызывают гемолиз эритроцитов, что приводит к гемолитической болезни плода и новорождённых. Резус-изоиммунизация, в основном, развивается при несовместимости крови матери и плода по антигену RhD. Также ГБП может развиться при несовместимости крови матери и плода по антигенам С, с, E, e и др [4,5].
Гемолитическая болезнь плода и новорожденного [5] – заболевание, характеризующееся гемолизом эритроцитов плода и новорожденного под воздействием антиэритроцитарных антител матери, проникающих в кровоток плода через плацентарный барьер, при несовместимости крови матери и плода по эритроцитарным антигенам, и проявляющееся развитием анемии, увеличением числа бластных форм эритроцитов, гипербилирубинемии.
Внутриутробная внутрисосудистая гемотрансфузия плоду [5] – терапевтический кордоцентез с внутрисосудистым переливанием отмытых лейкофильтрованных облученных эритроцитов О (I) первой группы, Rh (-) отрицательным фактором крови в сроке беременности до 34 недель.
ВВОДНАЯ ЧАСТЬ
Код(ы) МКБ-10:
|
Код
|
Название |
| О36.0 | Резус-иммунизация, требующая предоставления медицинской помощи матери. |
| О36.1 | Другие формы иммунизации, требующие предоставления медицинской помощи матери. |
| О36.2 | Водянка плода, требующая предоставления медицинской помощи матери |
Дата разработки протокола: 2014 год (пересмотр 2023 год).
Сокращения, используемые в протоколе:
| HBSAg | поверхностный антиген вируса гепатита B, «австралийский» антиген) |
| АВ0 | система групп крови человека |
| В/в | внутривенно |
| В/м | внутримышечно |
| ВИЧ | вирус иммунодефицита человека |
| ВПК | внутриутробное переливание крови |
| ГБН | гемолитическая болезнь новорожденного |
| ГБП | гемолитическая болезнь плода |
| ИПД | инвазивная пренатальная диагностика |
| КТГ | кардиотокография |
| МППК | маточно – плодово – плацентарный кровоток |
| ОЗПК | операция заменного переливания крови |
| ПССК | пиковая систолическая скорость кровотока |
| СМА | средне – мозговая артерия |
| УЗИ | ультразвуковое исследование |
| ФМТ | фето – материнская трансфузия |
| ЭКГ | электрокардиограмма |
| Ig | иммуноглобулин |
| МоМ | английская аббревиатура термина “multiple of median”, отражает степень отклонения показателя от среднего значения (медианы) |
| Rh (D) | резус D |
Пользователи протокола: акушеры-гинекологи.
Категория пациентов: беременные, роженицы и родильницы.
Шкала уровня доказательности: Соотношение уровней доказательности и градаций рекомендаций, разработанные Оксфордским Центром доказательной медицины [1]
| Уровни доказательности | Градации рекомендаций | |
| Систематический обзор, клинические исследования, отдельное клиническое исследование | I | А |
| Систематический обзор когортных исследований, или отдельное когортное исследование | II | В |
| Исследование типа "случай-контроль" (отдельное, либо систематический обзор нескольких) | III | В |
| Описание серии случаев, низкокачественные когортные исследования | IV | С |
| Мнение экспертов без точной критической оценки | V | D |
Классификация
Клиническая классификация:
Клиническая классификация изосерологической несовместимость крови матери и плода [1 - 3]:
По срокам реализации:
- Гемолитическая болезнь плода;
- Гемолитическая болезнь новорожденного.
По виду конфликта:
- При несовместимости эритроцитов матери и плода по системе Резус;
- При несовместимости по системе АВ0 (групповая несовместимость);
- При несовместимости по редким системам крови.
По клиническим проявлениям выделяют следующие формы ГБН:
- Анемическая (анемия без желтухи и водянки);
- Желтушная (анемия с желтухой);
- Отёчная (тяжелая анемия с водянкой). Наиболее тяжелая и прогностически неблагоприятная форма гемолитической болезни новорождённого;
- Осложнённая (ядерная желтуха – билирубиновая интоксикация, энцефалопатия, синдром сгущения желчи, геморрагический синдром; поражение почек, надпочечников и др.).
Клинические формы ГБП по уровню гемоглобина/гематокрита у плода:
- Легкая анемия – дефицит гемоглобина до 20 г/л по сравнению со средними значениями для данного срока (Hb < 0.84МоМ). Легкая анемия свидетельство начала гемолиза эритроцитов плода на более поздних сроках гестации.
- Умеренно тяжелая анемия – дефицит гемоглобина 20-70 г/л (Hb 0.65 < МоМ).
- Тяжелая анемия – дефицит гемоглобина более 70 г/л (Hb < 0.55МоМ).
Клинические классификация ГБП по формам:
- Анемическая;
- Отёчная (тяжелая анемия с водянкой).
Осложнения резус конфликтной беременности:
- Инвалидизация новорожденных;
- Мертворождение;
- Преждевременные роды.
Риски резус конфликтной беременности:
- Для плода: недоношенность, инфицирование, отёчная форма ГБП;
- Для беременной: кровотечение, преждевременные роды, хориоамнионит.
Диагностика
Диагностические критерии:
Жалобы:
- снижение интенсивности шевелений в случаях тяжелой анемии и водянки плода, что является признаком снижения двигательной активности плода на фоне развившейся сердечной недостаточности.
При указании в анамнезе на [13,15,18]:
- самопроизвольное прерывание беременности после 7 недели беременности;
- аборты (медицинские, медикаментозные);
- внематочная беременность;
- угрожающий аборт с кровотечением;
- пузырный занос;
- антенатальное кровотечение;
- необъяснимая (неиммунная) водянка плода в анамнезе.антенатальная гибель плода, мертворождение, смерть детей от гемолитической болезни у пациенток с резус-сенсибилизацией в предыдущих беременностях;
- особенности родоразрешения (кесарево сечение, ручное обследование полости матки, ручное отделение плаценты и выделение последа, акушерские щипцы, поворот плода на головку при тазовом предлежании);
- выявление антиэритроцитарных антител в сроке до 12 недель беременности;
- раннее появление признаков ГБП и тяжесть ГБН, особенности лечения ГБН (заменное переливание крови, трансфузия компонентов крови, инфузионная терапия, фототерапия, внутриутробная гемотрансфузия плоду в предыдущую беременность);
- гемотрансфузия в анамнезе без учета резус-принадлежности женщинам с резус-отрицательной кровью;
- инвазивные диагностические и лечебные вмешательства (биопсия ворсин хориона, плацентоцентез, амниоцентез, кордоцентез, серкляж, амниодренирование, интраамниальное внедрение шунта, эмбриоредукция, лазерная коагуляция сосудистых анастомозов при синдроме трансфузии монохориальных близнецов) в данную беременность;
- закрытая травма брюшной полости в данную беременность;
- антенатальная гибель плода в данную беременность;
- ретрохориальная/ плацентарная гематома в данную беременность.
Физикальное обследование: без особенностей.
Основные лабораторные исследования [4- 8,13,18,19]:
- Определение группы крови и резус принадлежности беременной: резус отрицательная принадлежность крови.
- Определение группы крови и резус принадлежности крови супруга/биологического отца плода: резус положительная принадлежность крови.
- Определение в крови беременной наличия антител, их титр:
обнаружение в крови беременной анти Rh-антител, что свидетельствует о сенсибилизации организма (качественно и количественно);
резус отрицательная принадлежность крови плода
ВАЖНО! При определении резус(D)-отрицательной принадлежности крови плода дальнейшее медицинское наблюдение и оказание медицинской помощи осуществляется без риска развития резус(D)-иммунизации или ГБП и ГБН (как при физиологической беременности)!
резус(D)-положительная принадлежность плода
Неинвазивное типирование Rh (D) гена плода в первом триместре используется для предотвращения рутинного введения анти-Rh (D) иммуноглобулина во время беременности.
- Идентификация антиэритроцитарных антител с определением их субклассов IgG1, IgG3и концентрации [6,16,19] (венозная кровь, метод реакции агглютинации): риск гемолиза высокой степени.
- Фенотипирование антигенного состава крови обоих супругов (антигены С, Е, Kell и другим системам крови) [5,7,10,16,19] (венозная кровь, метод реакции агглютинации): иммуноконфликт по нескольким антигенам.
Нормативные показатели Hb и Ht у плода в различные сроки гестации представлены в Таблице 1.
Таблица 1 Показатели гемоглобина и гематокрита у здоровых плодов [13]:
|
Срок беременности (недель) |
24 – 25 |
26 – 29 |
30 – 33 |
34 |
|
Hb (г/л) |
113 ± 17 |
125 ± 9 |
129 ± 12 |
144 ± 13 |
|
Ht (%) |
35 ± 3 |
38 ± 3 |
39 ± 3 |
44 ± 5 |
Основные инструментальные исследования [5,13, 16,17,18,19]:
УЗИ плода: увеличение толщины плаценты, многоводие, гепато – спленомегалия плода, асцит, гидроторакс, гидроперикард, подкожный отек (двойной контур).
УЗИ плода иммуноконфликтным беременным проводится в следующие сроки беременности:
начиная с 18 – недель;
далее 1 раз в месяц;
непосредственно перед родоразрешением.
У каждой беременной сроки повторных УЗИ сканирований назначаются индивидуально. При необходимости интервал между исследованиями сокращается до 1 – 2 недель, а при тяжелых формах заболевания – до 1–3 дней.
Допплерометрия МППК и СМА (УД I/A) [5,7,8,11,12,16,17]: увеличение максимальной скорости кровотока в СМА, выраженной в МоМ, 1,5 и более с высокой чувствительностью и специфичностью свидетельствует о развитии у плода гипердинамического типа кровообращения, характерного для тяжелой анемии, требующей вмешательства в течение беременности (Рис. 1).
неопределенной резус(D)-принадлежности крови плода.
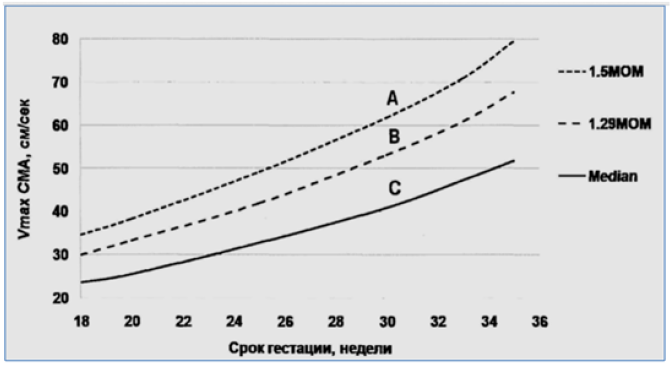
С – отсутствие у плода анемии;
В – отсутствие у плода умеренно тяжелой/тяжелой анемии;
А – наличие у плода умеренно тяжелой/тяжелой анемии.
Алгоритм действий в зависимости от ПССК в СМА [5,6,7,16]:
- ПССК в СМА в зоне «С»:
мониторинг допплера исследования каждые 2 недели;
с 36 недели беременности показана комплексная оценка состояния плода (КТГ и допплерометрия кровотока в артерии пуповины и СМА) 1 раз в неделю;
родоразрешение в соответствие с акушерской ситуацией в сроке беременности 38/+ недель;
- ПССК в СМА в зоне «В»:
мониторинг допплера 1 раз в неделю;
с 36 недели беременности показана комплексная оценка состояния плода ( КТГ и допплерометрия МППК и СМА) каждые 2 – 3 дня
родоразрешение согласно акушерской ситуацией в зависимости от предшествующего анамнеза, связанного с ГБН, предпочтительно в сроке беременности 37 – 38 недель;
- ПССК СМА в зоне «А»: В зависимости от срока беременности:
срок гестации менее 34 недель (начиная с 24 недель, в более ранние сроки - по показаниям) – кордоцентез и последующая внутриутробная гемотрансфузия отмытых лейкофильтрованных облученных эритроцитов О (I) Rh (-) отрицательной принадлежности крови;
срок гестации более 34 – 36 недель – родоразрешение.
Кардиотокография:
при среднетяжёлой и тяжёлой формах ГБП – монотонный ритм;
при отёчной форме ГБП – «синусоидальный» ритм.
Показания для консультации специалистов: нет.
Диагностический алгоритм [3, 10, 11]:
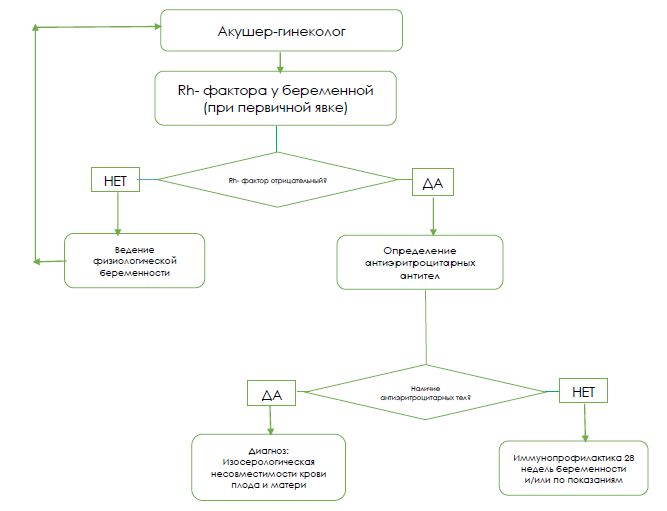

Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных диагностических исследований:
|
Диагноз |
Обоснование для дифференциальной диагностики |
Обследования |
Критерии исключения диагноза |
|
Неимунная водянка плода |
Водянка плода |
Анамнез |
ГБН в акушерском анамнезе беременной |
|
Определение группы крови и резус принадлежности беременной |
Резус-отрицательная принадлежность крови |
||
|
Определение антирезусных антител |
Наличие антиэритроцитарных антител |
||
|
Внутриутробная анемия одного из плодов при фето – фетальном трансфузионном синдроме при многоплодной беременности с монохориальным типом плацентации |
Водянка одного из плодов |
Анамнез |
ГБН в акушерском анамнезе беременной |
|
Определение группы крови и резус принадлежности беременной |
Резус-отрицательная принадлежность крови |
||
|
Определение антирезусных антител |
Наличие антиэритроцитарных антител |
||
|
Другие виды внутриутробной анемии плода, обусловленные инфекциями (ЦМВ, парвовирус и тд) |
Допплерометрия: ускорение кровотока в СМА |
Анамнез |
ГБН в акушерском анамнезе беременной |
|
Определение группы крови и резус принадлежности беременной , антиэритроцитарных антител. |
Резус-отрицательная принадлежность крови |
||
|
ПЦР на инфекции. |
Наличие антиэритроцитарных антител |
Лечение (амбулатория)
Формирование групп риска резус отрицательных беременных.
I группа риска: Беременные с резус отрицательной принадлежностью крови без титра антител.
II группа риска: Беременные с резус отрицательной принадлежностью крови с титром антител без признаков ГБП.
Профилактические мероприятия [4,5,6,13,16]
Основные цели профилактических мероприятий:
профилактика сенсибилизации к Rh(D) (специфическая и неспецифическая);
формирование групп риска сенсибилизированных беременных, исходя из данных анамнеза, показателя антирезусных антител и данных дообследования;
своевременная диагностика ГБП;
своевременное направление на лечение или родоразрешение в стационар.
|
Практические рекомендации: Меры по предотвращению сенсибилизации к Rh(D) (УД II|/В) [4,5,6,8,13,19,23] |
|
| Первый приоритет: |
● Определение антирезусных антител на ранних сроках беременности: при 1-м визите (при постановке на «Д» учет); далее контроль в динамике 1 раз в 4 недели. NB! Более частое определение анти-Rh-антител нецелесообразно! ● Определение резус-фактора новорожденного в пуповинной крови e резус(D)-отрицательных родильниц ● Профилактика резус-изоиммунизации (УД I|/A): в первые 72 часа после родов антирезус Rho[D] иммуноглобулином человека в послеродовом периоде резус иммунизированной родильнице при рождении резус положительного новорожденного. |
| Второй приоритет: |
Профилактика резус-изоиммунизации:
при отсутствии антирезусных антител резус отрицательной беременной показана в дозе, согласно инструкции к препарату (1250 – 1500 МЕ – 250 – 300 мкг), внутримышечно в 28-34 недели беременности.
NB! После антенатального профилактического введения aнти-Rh(D)-иммуноглобулина в течение 12 недель возможно выявление следовых уровней титра анти-Rh-антител! (1В) [4, 8, 13] при неблагоприятном завершении беременности и отсутствии антирезусных антител (после хирургического аборта более 12 недель беременности, выкидыша, внематочной беременности, пузырного заноса, неразвивающейся беременности, антенатальной гибели плода); после кровотечения, травмы живота во время беременности и/или гибели плода, после лазерной коагуляции сосудистых анастомозов при синдроме трансфузии близнецов (TTTS) во втором или третьем триместре беременности. |
| Низкий приоритет: |
Профилактика резус-изоиммунизации:
после инвазивной пренатальной диагностики (625 МЕ (125 мкг); при наружном повороте плода (500 МЕ; 100 мкг). Перед медикаментозным абортом пациенткам с неизвестным резус-фактором рекомендуется проводить резус-тестирование, при наличии показаний следует вводить резус-иммуноглобулин. В ситуациях, когда резус-фактор и введение резус-иммуноглобулина недоступны или могут значительно отсрочить медикаментозный аборт, рекомендуется совместное принятие решений, чтобы пациентки могли сделать осознанный выбор в отношении лечения. |
● Сохранение первой и последующих беременностей у женщин с резус – отрицательной принадлежностью крови.
● На этапе стационара – предотвращение переливания любых препаратов компонентов донорской крови пациенткам с резус отрицательной принадлежностью без учета резус-принадлежности крови донора.
Медикаментозное лечение:
ВАЖНО! Профилактические мероприятия являются гарантией предупреждения рождения детей с ГБ.
ВАЖНО! Введение анти-Д иммуноглобулина снижает число сенсибилизированных женщин.
Специфическая профилактика [4,5,6,7,11,13,18]: Введение анти-резус Rho (D) иммуноглобулина пациенткам с резус-отрицательной кровью без явлений сенсибилизации в соответствии с показаниями согласно Таблицы 2.
Таблица 2 Показания к специфической профилактике анти-резус Rho (D) иммуноглобулином
|
Показания
|
Дозировка анти-резус Rho (D) иммуноглобулина | |
| 1. |
Планово:
|
|
| 1) | Отсутствие резус-изоиммунизации беременной | Внутримышечно введение в сроке 28 – 34 недели одной дозы анти-Rh(D) – иммуноглобулина в дозе: 1250 – 1500 МЕ – 250 – 300 мкг (УД A/I)[4,5,13,18] |
| 2) | При отсутствии резус-иммунизации родильницы и рождении резус-положительного ребенка | Внутримышечно введение родильнице в течение 72 часов после родов одной дозы анти-Rh(D) – иммуноглобулина в дозе: 1250 – 1500 МЕ – 250 – 300 мкг. (УД А/ I)[4,5,13] |
| 2. | Дополнительно: | |
| 1) |
После проведения следующих инвазивных диагностических и лечебных вмешательств во время беременности (УД II/B):
ИПД (биопсия хориона, амниоцентез, кордоцентез);
акушерские кровотечения на любом сроке;
цервикальный серкляж;
повороты плода на головку при тазовом предлежании;
состояния после перенесенной абдоминальной травмы во время беременности;
при внутриматочных процедурах (амниодренирование, внедрение шунта, эмбриоредукция, после лазерной коагуляции сосудистых анастомозов при синдроме трансфузии монохориальных близнецов).
|
Внутримышечно введение в зависимости от срока беременности (УД II/B) [5,6,13]:
I триместр – 625 МЕ (125 мкг);
II и III триместры – 1250 - 1500 МЕ (250 – 300 мкг)
|
| 2) |
При неудачном завершении беременности: внематочной беременности, медикаментозном, инструментальном прерывании беременности;
самопроизвольном и медицинском прерывании беременности;
трофобластической болезни; антенатальной гибели плода
|
1250 – 1500 МЕ (250 – 300 мкг) (УД II/B) [5,6,13] |
| 3) | Объем ФМТ (расчет методом Клейхауэра-Бетке) |
В зависимости от объема ФМТ: не более 25 мл – 1500 МЕ (300 мкг); 25–50 мл – 3 000 МЕ (600 мкг) (УД II/B) [5,6,13] |
| 4) | отслойка плаценты, ручного обследования послеродовой матки и операции кесарева сечения, сопровождающегося массивной кровопотерей (при отсутствии технической возможности определить объем ФМТ методом Клейхауэра-Бетке) | Двойная дозировка: 2500 – 3000 МЕ (500 – 600 мкг) (УД II/B) [5,6,13] |
ВАЖНО!
После антенатального профилактического введения aнти-Rh(D)-иммуноглобулина в течении последующих 12 недель возможно выявление следовых уровней титра анти-Rh-антител, что не требует каких либо действий со стороны врача и проведение скрининговых исследований, ввиду ложно-положительных результатов, делает нецелесообразными (УД 4/С) [4]!
Перечень основных лекарственных средств:
|
Фармакотерапевтическая группа
|
МНН лекарственного средства | Способ применения | Уровень доказательности |
| Иммуноглобулин | Анти-D иммуноглобулин человека (human anti-D immunoglobulin) | В/м, однократно, дозировка в зависимости от показаний в соответствии с Таблицей 2 | УД А/I [4,5,7,8,11,13] |
Дальнейшее ведение:
Неспецифическая профилактика [1-13]:
● Сохранение первой и последующих беременностей у женщин с резус-отрицательной принадлежностью крови;
● После ВПК продолжить динамический мониторинг за состоянием плода по допплеру ПССК в СМА и УЗИ;
● Родильницы и новорожденные перенесшие ВПК через 6 месяцев после родоразрешения обследуются на наличие вирусов гепатитов (HBSAg, Анти HCV), ВИЧ.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе:
● отсутствие тяжелых форм ГБП;
● возможность пролонгирования беременности до более зрелого гестационного возраста плода и рождение жизнеспособных новорожденных;
● неосложненное течение адаптационного периода у новорожденных (отсутствие тяжелой формы ГБН, РДС);
● улучшение перинатальных исходов, выживаемость новорожденных, снижение перинатальной смертности.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Алгоритм принятия решений в зависимости от группы риска беременной
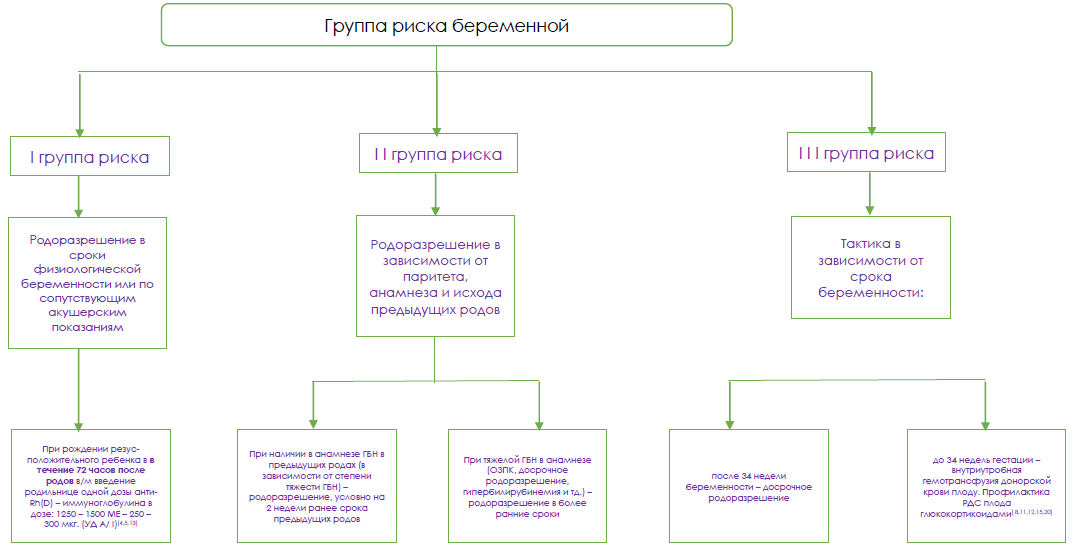
Основные цели лечения в условиях стационара:
● Пролонгирование беременности до более зрелого гестационного возраста плода и рождение жизнеспособных новорожденных;
● Улучшение перинатальных исходов:
Гормональная терапия с целью профилактики РДС плода глюкокортикоидами[ 8,11,12,15,20]:
Глюкокортикостероиды:
Перечень основных лекарственных средств:
|
Фармакотерапевтическая группа
|
МНН лекарственного средства | Способ применения | Уровень доказательности |
| Иммуноглобулин | Анти-D иммуноглобулин человека (human anti-D immunoglobulin) | В/м, однократно, дозировка в зависимости от показаний в соответствии с Таблицей 2 | УД А/I [4,5,7,8,11,13] |
Перечень дополнительных лекарственных средств:
|
Фармакотерапевтическая группа
|
МНН лекарственного средства | Способ применения | Уровень доказательности |
| Глюкокортикостероиды | Дексаметазон |
4-кратное введение по 6 мг в/м через каждые 12 ч.
Курс: 2 дня
|
УД В [8,11,12,15,20 |
| Бетаметазон |
2-кратное введение по 12 мг в/в через каждые 12ч.
Курс: 1 день
|
Хирургическое вмешательство:
Кордоцентез [5,8,12,15,16]:
Показания для проведения кордоцентеза:
увеличение максимальной скорости кровотока в СМА до 1.5 МоМ и выше (данные допплерометрии)
Внутриутробная внутрисосудистая гемотрансфузия плоду проводится с целью (УД B)[5,8,12,14,15,16]:
повышения уровня гемоглобина и гематокрита выше критического;
снижения риск развития отечной формы гемолитической болезни;
обеспечения возможности пролонгирования беременности.
Показания для проведения внутриутробной внутрисосудистой гемотрансфузии плоду:
тяжелая анемия (Hb менее 70 г/л)
Расчет объема донорской крови для ВПК [22]:
Формула расчета объема донорской крови для ВПК:
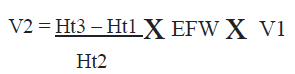
V2 – объем крови для предстоящего переливания (в мл);
V1 – фетоплацентарный объем крови, соответствующий данному сроку беременности (150 мл/кг);
EFW – масса плода (кг);
Ht1 – величина гематокрита плода (в %);
Ht2 – величина гематокрита донора (в %);
Ht3 – желаемая величина гематокрита плода (в %).
● Повторные внутриутробные гемотрансфузии [12,15,16]: плоду определяются сроком беременности на момент предыдущего переливания, величины конечного гематокрита плода и динамики изменений МССК СМА.
● Родоразрешение в зависимости от акушерской ситуации:
При отсутствии абсолютных показаний для оперативного родоразрешения, возможны вагинальные роды методом индукции родовой деятельности (Смотрите клинический протокол «Индукция родов»);
Оперативное родоразрешение путем кесрево сечения (Смотрите клинический протокол «Кесарево сечение»).
● Неспецифическая профилактика [14]:
Сохранение первой и последующих беременностей у женщин с резус-отрицательной принадлежностью крови.
Проведение переливаний любых компонентов донорской крови пациенткам с резус отрицательной принадлежностью с учетом резус-принадлежности крови донора
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе:
● Пролонгирование беременности до более зрелого гестационного возраста плода и рождение жизнеспособных новорожденных.
● Неосложненное течение адаптационного периода у новорожденных (отсутствие тяжелой формы ГБН, РДС, инвалидизации).
● Улучшение перинатальных исходов, выживаемость новорожденных, снижение перинатальной смертности.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для экстренной госпитализации.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- 1) Шотландская межвузовская сеть руководящих принципов. Руководство для разработчиков. Краткое справочное руководство. Ноябрь 2015 2) Obstetrics & gynecology, 5th edition. | Chichester, West Sussex : John Wiley & Sons Ltd., 2017. 3) Horvath S. et al. Society of Family Planning committee consensus on Rh testing in early pregnancy //Contraception. – 2022. 4) Prophylactic use of Rh D immunoglobulin in pregnancy care, National Blood Authority, 2021. Website: www.blood.gov.au 5) Delaney M., Matthews D.S. Hemolytic disease of fetus and newborn: managing the mother, fetus and newborn. Hematology Am.Soc.Hematol.Educ.Programme. - 2015. - Dec.5.2015(l): 146-151. 6) Visser GH, Thommesen T, Di Renzo GC, Nassar AH, Spitalnik SL, FIGO Safe Motherhood & Newborn Health Committee. FIGO/ICM guidelines for preventing Rhesus disease: A call to action. Int J Gynecol Obstet. 2021;152:144–147. https://doi.org/10.1002/ ijgo.13459 7) Management of Alloimmunization During Pregnancy, ACOG PRACTICE BULLETIN, Number 192, March 2018 8) Society of Maternal and Fetal Medicine (SMFM): Fetus at risk of anemia - diagnosis and treatment. Am. J. Obstet. Gynecol. June 2015; 212(6):697-710. 9) Targeted antenatal anti-D prophylaxis for RhD-negative pregnant women: a systematic review. Runkel B, Bein G, Sieben W, Sow D, Polus S, Fleer D.BMC Pregnancy Childbirth. 2020 Feb 7;20(1):83. doi: 10.1186/s12884-020-2742-4. 10) Резус-изоиммунизация. Гемолитическая болезнь плода. Клинические рекомендации. ООО «Российское общество акушеров-гинекологов» (РОАГ). Москва, 2020 г. 11) ACOG Practice Bulletin No.192: Management of Alloimmunization during Pregnancy. March 2018 12) Sahoo, T., Sahoo, M., Gulla, K.M. et al. Rh Alloimmunisation: Current Updates in Antenatal and Postnatal Management. Indian J Pediatr 87, 1018–1028 (2020). https://doi.org/10.1007/s12098-020-03366-0 13) Visser GH, Carlo Di Renzo G, Glob. libr. women's med., 2022 ISSN: 1756-2228; DOI 10.3843/GLOWM.418863 14) Prevention of Rh D alloimmunization. Practice Bulletin No. 181. American College of Obstetricians and Gynecologists. Obstet Gynecol 2017;130:p57–70.Fetal middle cerebral artery Doppler to time intrauterine transfusion in red-cell alloimmunization: a randomized trial. 15) Dodd JM, Andersen C, Dickinson JE, Louise J, Deussen A, Grivell RM, Voto L, Kilby MD, Windrim R, Ryan G; MCA Doppler Study Group. Ultrasound Obstet Gynecol. 2018 Mar;51(3):306-312. doi: 10.1002/uog.18807. Epub 2018 Feb 5. 16) Cionca O. et al. Rh incompatibility and the pregnancy outcome of Rh negative women //Obstetrica si Ginecologie. – 2019. – Т. 67. – №. 2. 17) Burki F. et al. Comparison of Middle Cerebral Artery Doppler and Cord. Blood Hemoglobin in the Diagnosis of Fetal Anemia among Rh-negative Pregnant Women //Journal of Sheikh Zayed Medical College (JSZMC). – 2022. – Т. 13. – №. 01. – С. 3-6. 18) Red Blood Cell Alloimmunization in the Pregnant Patient Jennifer Webb ⁎, Meghan Delaney Children's National Health System, Washington, D.C., USA The George Washington University, Departments of Pediatrics & Pathology, Washington, DC, USA, 19 July 2018. 19) Приказ Министра здравоохранения Республики Казахстан от 20 октября 2020 года № ҚР ДСМ - 140/2020 «Об утверждении номенклатуры, правил заготовки, переработки, контроля качества, хранения, реализации крови, ее компонентов, а также правил переливания крови, ее компонентов». Зарегистрирован в Министерстве юстиции Республики Казахстан 22 октября 2020 года № 21478. 20) Roberts D., Brown J., Medley N., Dalziel S.R. Antenatal corticosteroids for accelerating fetal lung maturation for women at risk of preterm birth. Cochrane database Syst Rev. 2017; 3:CD004454. 21) Magann E.F., Haram K., Ounpraseuth S., Mortensen J.H., Spencer H.J., Morrison J.C. Use of antenatal corticosteroids in special circumstances: a comprehensive review. Acta Obstet Gynecol Scand. 2017; 96(4):395–409/ 22) Carolien Zwiers, Inge van Kamp, Dick Oepkes & Enrico Lopriore. Intrauterine transfusion and non-invasive treatment options for hemolytic disease of the fetus and newborn – review on current management and outcome Carolien Zwiers, Inge van Kamp, Dick Oepkes & Enrico Lopriore/ Expert Review of Hematology, 10:4, 337-344. 23) Society of Family Planning committee consensus on Rh testing in early pregnancy/ Sarah Horvatha,Vinita Goya, Sarah Traxler, Sarah Prager a Department of Obstetrics and Gynecology, Pennsylvania State University College of Medicine, Hershey Medical Center, Pennsylvania b Population Research Center, University of Texas at Austin, Austin, TX, United States c Planned Parenthood Northl Central States, Saint Paul, Minnesota, United States d University of Washington School of Medicine, Seattle, WA, United State/ DOI: 10.1016/j.contraception.2022.07.002.
Информация
Список разработчиков протокола с указание квалификационных данных:
Указание на отсутствие конфликта интересов: нет.
Указание условий пересмотра протокола: пересмотр не реже 1 раза в 5 лет и не чаще 1 раза в 3 года при наличии новых методов диагностики и лечения с уровнем доказательности.
Определение RhD гена [4-6,9,12,14,19] – неинвазивное определение резус-генотипа плода в конце первого триместра беременности путем пренатального тестирования свободной ДНК плода в образцах крови матери.
Чувствительность и специфичность данного метода 98-100% [4,5,6].
Определение RhD гена в периферической крови беременной с резус отрицательной принадлежностью крови в сроке с 11+0 до 32 недель беременности.
Для определение RhD гена плода используется периферическая венозная кровь беременной женщины, из которой выделяется свободно циркулирующая дезоксирибонуклеиновая кислота плода.
Метод определения резус D-принадлежности крови плода выполняется только к антигену D [5,6].
Показания [4,5,6].
в случае неизвестной принадлежности крови биологического отца ребенка.
наличие резус положительной принадлежности крови биологического отца ребенка.
Возможность неинвазивного определения Rh-генотипа плода у резус-отрицательных беременных женщин позволяет:
снизить затраты на ведение беременности;
избежать многократного скринингового определения резус-антител;
обеспечить профилактическое применение антирезусной иммунопрофилактики только при резус-положительном генотипе плода.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.