Злокачественные новообразования губы
 Версия: Клинические рекомендации РФ 2024 (Россия)
Версия: Клинические рекомендации РФ 2024 (Россия)
Общая информация
Краткое описание
Разработчик клинической рекомендации
Общероссийская общественная организация "Российское общество специалистов по опухолям головы и шеи",
Общероссийская общественная организация «Российское общество клинической онкологии»,
Общероссийская общественная организация «Федерация специалистов по лечению заболеваний головы и шеи»,
Некоммерческая организация "Ассоциация онкологических организаций Сибири и Дальнего Востока
ID: 553_2
Возрастная категория: Взрослые
Определение заболевания или состояния (группы заболеваний или состояний)
- неблагоприятные метеорологические факторы (длительная солнечная инсоляция, резкие колебания температуры);
- вредные привычки: курение, особенно в сочетании с употреблением крепкого алкоголя, жевание различных смесей (нас, орех бетель и т.д.);
- фоновые процессы: плоские лейкоплакии, эритроплакии, хронические язвы и трещины губ, хейлиты [1, 2].
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
Кодирование по МКБ-0, 4-е издание, 2010 г.: опухоли губы
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Клиническая классификация

- Глубина инвазии не является толщиной опухоли.
Символ сN указывает на наличие или отсутствие метастазов в регионарных лимфатических узлах (ЛУ) по данным клинико-инструментальных исследований


Таблица 1 - Группировка по стадиям
| Стадия | 0 | I | II | III | IVА | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| T | In situ | T1 | T2 | T3 | T1 | T2 | T3 | Т1 | Т2 | Т3 | Т4а | Т4а | T4a |
| N | N0 | N0 | N0 | N0 | N1 | N1 | N1 | N2 | N2 | N2 | N0 | N1 | N2 |
| M | M0 | M0 | N0 | M0 | M0 | M0 | M0 | M0 | M0 | M0 | M0 | M0 | M0 |
| Стадия | IVВ | IVС | |
|---|---|---|---|
| T | любое Т | T4b | любое T |
| N | N3 | любое N | любое N |
| M | M0 | M0 |
M1 |
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
1. Жалобы и анамнез
- Рекомендуется тщательный сбор жалоб и анамнеза у пациента с целью выявления факторов, которые могут повлиять на выбор тактики лечения [1, 5].
2. Физикальное обследование
- Рекомендуется всем пациентам проводить тщательный физикальный осмотр, включающий осмотр и пальпацию (бимануальную) очага поражения и регионарных ЛУ, оценку нутритивного статуса с целью определения распространенности опухолевого процесса и принятия решения о необходимости коррекции нутритивного статуса [1, 5].
3. Лабораторные диагностические исследования
- Рекомендуется всем пациентам выполнять: общий (клинический) анализ крови развернутый, анализ крови биохимический общетерапевтический, общий (клинический) анализ мочи, коагулограмму (ориентировочное исследование системы гемостаза) в целях выявления факторов, которые могут повлиять на выбор тактики лечения [1, 5].
4. Инструментальные диагностические исследования
- Пациентам с ЗНО губы рекомендуется выполнять биопсию слизистой полости рта, пункцию тканей полости рта, получение соскоба с эрозивно-язвенных элементов кожи и слизистых оболочек с последующим цитологическим исследованием соскобов эрозий, язв, ран, свищей, цитологическим исследованием микропрепарата тонкоигольной аспирационной биопсии с целью морфологической верификации опухолевого процесса, [1, 5, 6].
- При неясности цитологического исследования пациентам с ЗНО губы рекомендуется выполнение патологоанатомического исследования биопсийного (операционного) материала тканей полости рта, патологоанатомическое исследование биопсийного (операционного) материала тканей полости рта с применением гистобактериоскопических методов, патологоанатомическое исследование биопсийного (операционного) материала тканей полости рта с применением иммуногистохимических методов с целью морфологической верификации опухолевого процесса [1, 5, 6].
- Рекомендуется всем пациентам с ЗНО губы выполнить УЗИ ЛУ шеи с пункцией пальпаторно неизмененных ЛУ с целью исключения или подтверждения вовлечения регионарных лимфоколлекторов в опухолевый процесс [1, 5].
- Рекомендуется всем пациентам с ЗНО губы выполнение УЗИ первичного очага для определения толщины опухоли и дальнейшего планирования объема операции на лимфоколлекторах шеи. [7, 8].
- Рекомендуется всем пациентам с ЗНО губы выполнить компьютерную томографию (КТ) и/или магнитно-резонансную томографию (МРТ) пораженной области с внутривенным контрастированием для оценки первичной распространенности и глубины инвазии опухолевого процесса, наличия костной инвазии на нижнюю/верхнюю челюсти, основание черепа [1, 5].
- Рекомендуется выполнить компьютерную томографию органов грудной полости или компьютерную томографию органов грудной полости с внутривенным болюсным контрастированием всем пациентам с ЗНО губы при распространенном раке с поражением регионарных ЛУ с целью выявления отдаленных метастазов [1, 5].
- Рекомендуется выполнить сцинтиграфию костей всего тела при подозрении на метастатическое поражение костей скелета с целью уточнения распространенности опухолевого процесса [112].
- Рекомендуется выполнить позитронную эмиссионную томографию костей совмещенную с компьютерной томографией всего тела / позитронную эмиссионную томографию совмещенную с компьютерной томографией с туморотропными РФП / позитронную эмиссионную томографию совмещенную с компьютерной томографией с туморотропными РФП с контрастированием при стадиях III–IV с целью исключения отдаленных метастазов, а также для оценки эффективности лечения (в случае консервативного лечения на I этапе) и по индивидуальным показаниям [5, 9].
5. Иные диагностические исследования
- Рекомендуется проводить патолого-анатомическое исследование биопсийного (операционного) материала ткани губы с целью определения дальнейшей тактики лечения, при этом в морфологическом заключении рекомендуется отразить следующие параметры [5]:
- размеры и распространенность первичной опухоли;
- глубина инвазии первичной опухоли;
- гистологическое строение опухоли;
- степень дифференцировки опухоли;
- наличие периваскулярной, перилимфатической, периневральной инвазии (отрицательный результат также должен быть констатирован);
- статус регионарных ЛУ (рN) с указанием общего числа исследованных и пораженных лимфоузлов, признаков экстранодального распространения опухоли (ENE+/−);
- микроскопическая оценка краев резекции c указанием расстояния до ближайшего края резекции в мм [4,5].
- При нерезектабельных процессах и планировании паллиативного лечения определение экспрессии белка PDL1 иммуногистохимическим методом.
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
1. Общие принципы лечения в зависимости от стадии
- Рекомендуется рассматривать хирургическое вмешательство как основной метод радикального лечения больных раком губы, при этом удаление образования следует выполнять с одномоментной пластикой при необходимости [1, 10, 11, 12].
- T1–T2, N0 при глубине инвазии опухоли ˂2 мм рекомендуется выполнение оперативного вмешательства только на первичном очаге, выполнение шейной диссекции не рекомендуется [5; 13].
- T1-T2, N0 при глубине инвазии опухоли >4 мм рекомендовано выполнение оперативного вмешательства на первичном очаге и селективной лимфодиссекции (минимально уровни 1−3) [5; 13].
- T3,T4a, N0, любое T1-4a N1-3 Рекомендуется выполнение оперативного вмешательства на первичном очаге с лимфаденэктомией шейной [5, 17].
- При невозможности оперативного вмешательства (отказ пациента и/или наличие абсолютных противопоказаний) рекомендуется проведение дистанционной лучевой терапии опухоли губы / химиолучевой терапии (ХЛТ) [14].
- При невозможности оперативного вмешательства (отказ пациента и/или наличие абсолютных противопоказаний) рекомендовано проведение внутритканевой лучевой терапии опухоли на первичном очаге в комбинации с ДЛТ/ХЛТ [14].
- При невозможности оперативного вмешательства (отказ пациента и/или наличие абсолютных противопоказаний) при небольших опухолевых процессах (T1−T3) рекомендовано проведение фотодинамической терапии на первичный очаг в самостоятельном варианте или в комбинации с ДЛТ/ХЛТ [15].
- Пациентам с ЗНО губы рекомендуется проведение хирургического лечения при отсутствии абсолютных противопоказаний на I этапе [1, 5, 10, 18, 19, 20, 21, 22].
- Пациентам с ЗНО губы рекомендуется проведение послеоперационной одновременной ХЛТ в случае выявления при плановом патолого-анатомическом исследовании операционного материала таких неблагоприятных гистологических признаков, как положительные края резекции либо экстракапсулярное распространение метастаза/зов [1, 5, 10, 18, 19, 20, 21, 22].
- Пациентам с ЗНО губы рекомендуется в качестве альтернативы выполнение повторного оперативного вмешательства в случае выявления при плановом патолого-анатомическом исследовании операционного материала положительного края резекции [1, 5, 10, 18, 19, 20, 21, 22].
- Пациентам с ЗНО губы рекомендуется проведение послеоперационной ЛТ или одновременной ХЛТ при выявлении таких неблагоприятных гистологических признаков, как периневральная/периваскулярная/лимфатическая инвазия, pT3/pT4, множественные регионарные метастазы [1, 5, 10, 18, 19, 20, 21, 22].
- Пациентам с ЗНО губы рекомендуется проведение одновременной ХЛТ/ЛТ при невозможности оперативного вмешательства [1, 5, 10, 18, 19, 20, 21, 22].
- При T4bN0−3 или нерезектабильных регионарных метастазах, или других стадиях при абсолютных противопоказаниях для хирургического лечения рекомендуется выбор метода лечения в зависимости от общего состояния по шкале оценки общего состояния онкологического больного по версии Восточной объединенной группы онкологов (ECOG) [1, 5]:
- При локальном рецидиве или остаточной опухоли после хирургического лечения без предшествующей дистанционной лучевой терапии рекомендовано хирургическое вмешательство с достижением свободного от опухоли края резекции (R0) или одновременная ХЛТ, или проведение полихимиотерапии с последующей ДЛТ/ХЛТ [1, 5, 10, 18].
- Пациентам с ЗНО губы рекомендовано хирургическое вмешательство с обсуждением вопроса о повторной лучевой или одновременной ХЛТ в случае резектабельности опухоли при локальном рецидиве или остаточной опухоли после проведенной дистанционной лучевой терапии [1, 5].
- Пациентам с ЗНО губы рекомендована повторная дистанционная лучевая терапия / одновременная ХЛТ либо лекарственная терапия, либо симптоматическое лечение в случае нерезектабельности опухоли при локальном рецидиве или остаточной опухоли после проведенной дистанционной лучевой терапии [1, 5].
- При ECOG 0–1 пациентам с раком губы рекомендуется комбинация полихимиотерапии или монохимиотерапии. Возможны хирургическое лечение (при возможности достижения всех отдаленных метастазов и резектабельности первичной опухоли с достижением R0) или ДЛТ/ХЛТ на область отдаленного метастазирования и при отсутствии рецидива/остаточной опухоли в области первичного очага и в зонах регионарного метастазирования. При невозможности – наилучшая поддерживающая терапия [5].
- При ECOG 2 пациентам с раком губы рекомендуется монохимиотерапия или иммунотерапия или наилучшая поддерживающая терапия [5].
- При ECOG 3 пациентам с раком губы рекомендуется наилучшая поддерживающая терапия [5].
2. Принципы лучевой терапии
- Рекомендована дистанционная лучевая терапия на первичный очаг и клинически определяемые регионарные метастазы 66−70 Гр (1,8−2,2 Гр/фракция) ежедневно с понедельника по пятницу в течение 6−7 недель (нед), на локорегионарную область, включая регионарные ЛУ 44−54 Гр (1,8−2,0 Гр/фракция) [1, 5].
- С целью излечения больного рака губы рекомендована внутритканевая лучевая терапия опухолей губы в самостоятельном варианте рекомендуется при T1-2 [5, 14].
- Рекомендуется низкодозовая (LDR) внутритканевая лучевая терапия опухолей губы (0,4-0,5 Гр/ч) [113]:
- Рекомендуется высокодозовая (HDR) внутритканевая лучевая терапия опухолей губы [113]:
Техника внутритканевой лучевой терапии основана на классических системах для интерстициальной брахитерапии (Парижская, Манчестерская или Нью-Йоркская). При подготовке к БТ используется трехмерное планирование (3D) – используются компьютеры и программное обеспечение для расчета и отображения изодоз и их интеграции с изображениями облучаемых тканей, полученным при компьютерной томографии. Расположение источников должно быть параллельным и равноудаленным, на расстоянии от 1 до 1,5 см.
- Послеоперационная дистанционная лучевая терапия рекомендована при стадиях pТ3–4 и N2–3, а также у отдельных пациентов со стадиями pT1–2, N0–1 (при наличии неблагоприятных признаков, положительный или близкий край резекции) [1, 5].
При R0 – на область удаленной первичной опухоли и регионарных метастазов подводится доза 60 Гр (1,8−2,0 Гр/фракция).
При R+ суммарная доза излучения составляет 66 Гр (1,8−2,0 Гр/фракция).
На локорегионарную область, включая неизмененные регионарные ЛУ, суммарная доза составляет 44−50 Гр (2,0 Гр/фракция), на пораженные метастазами ЛУ – 54–63 Гр (1,8-2,0 Гр/фракция)
- В качестве послеоперационного лечения пациентам с раком губы при прорастании опухолью капсулы ЛУ и/или при положительном крае резекции и/или наличии факторов (первичная стадия pT3 или pT4; N2 или N3, наличие периневральной инвазии и/или эмболов в лимфатических сосудах), а также при сочетании двух и более неблагоприятных факторов (первичная стадия pT3 или pT4; N2 или N3, наличие периневральной инвазии и/или эмболов в лимфатических сосудах) рекомендована одновременная ХЛТ на основе препаратов платины: цисплатин** в дозе 100 мг/м2 каждые 3 недели и ЛТ [1, 5].
При микроскопической остаточной опухоли (R1) рекомендованная суммарная доза излучения составляет 66 Гр (1,8−2,0 Гр/фракция).
На локорегионарную область, включая неизмененные регионарные ЛУ, суммарная доза составляет 44−50 Гр (2,0 Гр/фракция), на пораженные метастазами ЛУ – 54–63 Гр (1,8-2,0 Гр/фракция).
3. Принципы системной химиотерапии
- Пациентам с ЗНО губы (для лечения рецидивных, первично-неоперабельных опухолей или метастатического опухолевого процесса, при отсутствии возможности проведения ХЛТ), рекомендуется поли- или монохимиотерапия для улучшения выживаемости пациентов (таблица №1) [5, 23, 27, 29, 31, 34, 36, 38, 39, 116 - 123].
Таблица №1.
Режимы терапии плоскоклеточного рака головы и шеи.
| Название режима | Схема проведения | |
|---|---|---|
| PF+ Cet | Цисплатин** 75–100 мг / м2 в / в в 1‑й день + #фторурацил** 1000 мг / м2 / сут. в / в 96‑часовая инфузия в 1–4‑й дни, каждые 3 нед. + цетуксимаб** 400 мг / м2 (нагрузочная доза), далее — 250 мг / м2 в / в еженедельно. После 6 циклов ХТ завершается, и в случае отсутствия прогрессирования рекомендовано продолжить поддерживающую терапию #цетуксимабом** 250 мг / м2 в / в еженедельно [23] | |
| DС+ Cet | #Доцетаксел** 75 мг / м2 в /в в 1‑й день + цисплатин** 75 мг / м2 в / в в 1‑й день, каждые 3 нед. + цетуксимаб** 400 мг / м2 (нагрузочная доза) в / в, далее — 250 мг / м2 в / в еженедельно. После 4 циклов ХТ завершается, и в случае отсутствия прогрессирования рекомендовано продолжить поддерживающую терапию #цетуксимабом** 500 мг / м2 в / в 1 раз в 2 недели [116] | |
| Цисплатин + Cet | Цисплатин** 75–100 мг / м2 1 раз в 3 недели (не более 6-8 введений) + цетуксимаб** 400 мг / м2 (нагрузочная доза) в / в в 1 день, далее — 250 мг / м2 в / в еженедельно до прогрессирования или непереносимой токсичности. [27] | |
| Pacli + Carbo + Cet 1 | #Паклитаксел** 80 мг / м2 в / в еженедельно + карбоплатин** AUC 2,0 в / в еженедельно + цетуксимаб** 400 мг / м2 в / в (2‑часовая инфузия) в 1‑й день 1‑го цикла, далее — 250 мг / м2 в / в еженедельно. После завершения ХТ в случае отсутствия прогрессирования рекомендовано продолжить поддерживающую терапию #цетуксимабом**250 мг / м2 в / в еженедельно. Количество введений цитостатиков определяется индивидуально [121, 122] | |
| PF 2 | Цисплатин** 75–100 мг / м2 в / в в 1‑й день + #фторурацил** 1000 мг / м2 / сут. в / в 96‑часовая инфузия в 1–4‑й дни, каждые 3 нед. [117] | |
| Карбоплатин** AUC- 5 в / в в 1‑й день + #фторурацил** 1000 мг / м2 в / в 96‑часовая инфузия в 1–4‑й дни, каждые 3 нед. Общее число циклов 6, при отсутствии токсичности и нарастающей положительной динамике может быть увеличено до 8. Общее число циклов 6, при отсутствии токсичности и нарастающей положительной динамике может быть увеличено до 8.[29] | ||
| Pacli +Carbo 2 | #Паклитаксел** 175 мг / м2 в / в в 1‑й день + карбоплатин** AUC- 5–6 в / в в 1‑й день каждые 3 нед. Общее число циклов 6, при отсутствии токсичности и нарастающей положительной динамике может быть увеличено до 8.[121] | |
| #Паклитаксел** 60–80 мг / м2 в / в еженедельно + карбоплатин** AUC- 2 в / в еженедельно до прогрессирования или неприемлемой токсичности, но не более 18 недель. [117] | ||
| DС 2 | #Доцетаксел** 75 мг / м2 в / в в 1‑й день + цисплатин** 75 мг / м2 в / в в 1‑й день, каждые 3 нед. Общее число циклов 6, при отсутствии токсичности и нарастающей положительной динамике может быть увеличено до 8. [120,121] | |
| Ниволумаб3 | Ниволумаб** 3 мг / кг в / в 1 раз в 2 нед. или 240 мг 1 раз в 2 нед. или 480 мг 1 раз в 4 нед. 60‑минутная инфузия (первое введение), далее — 30‑минутная инфузия до прогрессирования или неприемлемой токсичности, но не более 2 лет [36] | |
| Пембролизумаб 4 | Пембролизумаб 200 мг в / в 1 раз в 3 нед. (30‑минутная инфузия) или 400 мг 1 раз в 6 нед. до прогрессирования или неприемлемой токсичности, но не более 2 лет [38], [39], [118] | |
| PF + Пембролиз-умаб 5 | Пембролизумаб** 200 мг + карбоплатин** AUC 5 или цисплатин** 100 мг / м2 + #фторурацил** 1000 мг / м2 1–4 дни 1 раз в 3 недели (6 циклов), далее пембролизумаб** 200 мг 1 раз в 3 недели или 400 мг 1 раз в 6 нед. Максимум — до 35 введений в целом [123] | |
| Монотерапия для пациентов в общем состоянии по ECOG> 2 баллов | ||
| Цисплатин** 60–70 мг / м2 в / в 1 раз в 3 нед. Количество введений определяется индивидуально, но целесообразность длительности более 6-8 введений представляется сомнительной.[121] | ||
| Карбоплатин** AUC 5–6 в / в 1 раз в 3 нед. или карбоплатин** AUC 2 в / в еженедельно. Количество введений определяется индивидуально. [119] | ||
| #Паклитаксел** 175 мг / м2 в / в 1 раз в 3 нед. или #паклитаксел** 80 мг / м2 в / в еженедельно. Количество введений определяется индивидуально. [31] | ||
| #Доцетаксел** 70–75 мг / м2 в / в 1 раз в 3 нед. Количество введений определяется индивидуально. [121] | ||
| #Капецитабин** 2000 мг / м2 внутрь в 2 приема в 1–14‑й дни, перерыв 1 неделя или #капецитабин** 2000 мг / сут. внутрь ежедневно в метрономном режиме. Длительность терапии определяется индивидуально. [121] | ||
| #Метотрексат** 40 мг / м2 в / в еженедельно. Количество введений определяется индивидуально6. [29] | ||
| #Цетуксимаб** 400 мг / м2 в / в (2‑часовая инфузия) в 1‑й день 1‑го курса, далее — 250 мг / м2 в / в еженедельно [34] | ||
- При прогрессировании на фоне платиносодержащей схемы химиотерапии (таблица №1) или после ее окончания рекомендуется ниволумаб** 3 мг / кг в / в 1 раз в 2 нед (30- или 60-минутная инфузия) до прогрессирования или неприемлемой токсичности [36]
- При прогрессировании на фоне платиносодержащей схемы химиотерапии (таблица №1) или после ее окончания рекомендуется #пембролизумаб** 200 мг в / в 1 раз в 3 нед (30-минутная инфузия) до прогрессирования или неприемлемой токсичности [37, 38; 39]
- При прогрессии после платиносодержащей терапии рекомендуется #афатиниб** 40 мг в день (эффективность при плоскоклеточном раке головы и шеи оценена только по данным зарубежных исследований) [40]
Дистанционная лучевая терапия на первичный очаг и клинически определяемые регионарные метастазы – 70 Гр (2,0 Гр/фракция) ежедневно с понедельника по пятницу в течение 7 нед, на клинически неизмененные ЛУ − 46-50 Гр (2,0 Гр/фракция), цисплатин** в дозе 100 мг/м2 на фоне гипергидратации в 1, 22 и 43-й дни ЛТ (суммарная доза во время ЛТ – 300 мг/м2) [41].
- Оценка. Рекомендована оценка всех пациентов до лечения хирургом-онкологом, специализирующимся на опухолях головы и шеи, которому следует предпринять следующие действия: рассмотреть адекватность биопсийного материала, стадирования и визуализации опухолевого процесса (КТ, МРТ) для определения степени распространения опухоли, исключить наличие синхронной первичной опухоли, оценить текущий функциональный статус и возможность назначения потенциального хирургического лечения; если первичное лечение было нехирургическим, разработать проспективный план наблюдения, который будет включать адекватное обследование зубов, питания и здорового образа жизни, а также вмешательства и любые другие дополнительные исследования, которые необходимы для полной реабилитации [1, 5].
- Оценка операбельности. Рекомендована оценка наличия поражения опухолью структур, при котором отмечается плохой прогноз или процесс классифицируется как стадия Т4b (например, неоперабельность, ассоциированная с технической невозможностью получить чистые края резекции): значительное поражение крыловидно-небной ямки, тяжелые тризмы из-за инфильтрации опухолью крыловидных мышц; макроскопическое распространение опухоли на основание черепа (например, эрозия крыловидных пластинок или основной кости, расширение овального отверстия и др.); возможная инвазия (охват) стенки общей или внутренней сонной артерии [1, 5].
- Удаление первичного очага. По возможности рекомендовано выполнять удаление первичной опухоли единым блоком [1, 5].
- Края резекции. Рекомендовано достигать статуса R0 при хирургическом лечении [1, 5, 42].
- Рекомендовано с целью радикального хирургического лечения при высокой вероятности или наличии метастазов в ЛУ шеи выполнять всем пациентам профилактическую ипсилатеральную лимфаденэктомию шейную. При локализации опухоли на срединной линии или переходе опухоли за срединную линию рекомендована двусторонняя лимфаденэктомия шейная [1, 5].
5. Иное лечение
- С целью коррекции ксеростомии рекомендуются обильное питье, заменители слюны (например, растворы с фосфатом кальция, гели, содержащие лизоцим, лактоферрин и пероксидазу), ополаскиватели полости рта, не содержащие спирт, стимуляторы слюноотделения и вкуса (например, жевательная резинка с ксилитолом, леденцы с сорбитолом/яблочной кислотой, ксилитолом) [43, 44].
6. Диетотерапия
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- Рекомендуется проводить мероприятия по медицинской реабилитации пациентов c раком губы специалистам мультидисциплинарной реабилитационной команды специалистов (МДРК) [45, 124].
- Рекомендуется для повышения эффективности мероприятий по медицинской реабилитации и приверженности пациента к лечению специалистам мультидисциплинарной реабилитационной команды планировать продолжительность и интенсивность реабилитационных мероприятий в соответствии с целями реабилитационной терапии, конкретными потребностями и состоянием пациента, по согласованию с ним и его семьей/опекуном [45, 124].
- Рекомендуется, чтобы индивидуальная программа реабилитации пациента с раком губы включала мультидисциплинарный подход в диагностике состояния пациента и возможность коррекции структуры, функции, ограничения активности и участия, а также личностных факторов, факторов окружающей среды в категориях Международной классификации функционирования (МКФ) [45, 124, 125].
- С целью улучшения качества жизни пациентов с раком губы рекомендуется использовать мультидисциплинарный подход в реабилитации [45, 124].
- Рекомендован регулярный скрининг питания и нутритивная поддержка, включая (при необходимости) кормление тяжелобольных пациентов через рот и/или назогастральный зонд, при проведении противоопухолевого лечения по поводу рака губы, и пациентам с ожидаемой выживаемостью более нескольких месяцев [47].
- У пациентов с раком губы с ожидаемой продолжительностью жизни менее нескольких месяцев рекомендуется снижение инвазивности нутритивных вмешательств, при этом при планировании нутритивной поддержки предпочтение следует отдавать диетическому консультированию и сиппинговому энтеральному питанию [47].
- У пациентов с ЗНО губы с ожидаемой выживаемостью менее нескольких недель рекомендуется уход и симптоматическая терапия, ориентированная на комфорт, включая облегчение жажды и голода [47].
- У пациентов с ЗНО губы, получающих противоопухолевое лечение, рекомендуется соблюдать суточный калораж 25-30 ккал/кг массы тела в сутки, а необходимое количество белка – 1,2-2 г белка на 1 кг массы тела в сутки [47].
- Рекомендовано обеспечение пациентов с ЗНО губы витаминами и минеральными добавками в количествах, приблизительно равных рекомендуемой суточной норме, с целью коррекции нутритивного статуса [48].
- У пациентов с ЗНО губы рекомендуется применение мультимодального подхода, направленного на облегчение симптомов, влияющих на потребление пищи, обеспечение адекватного потребления энергии и питательных веществ, минимизацию катаболических изменений, поддержку физической активности и оказание психологической и социальной поддержки с целью коррекции нутритивной недостаточности и улучшения качества жизни. [47].
- У пациентов с ЗНО губы рекомендовано на первом этапе проводить диетическое консультирование с целью увеличения потребления энергии, белка и других необходимых нутриентов [47].
- Парентеральное питание рекомендуется при полном отсутствии функции ЖКТ, либо в случае, если не удается покрыть необходимые потребности в энергии и белке энтеральным питанием (сиппинговым/зондовым) [47].
- У пациентов с ЗНО губы рекомендовано сочетание нутритивной поддержки с повышением уровня физической активности для профилактики саркопении [47].
- У пациентов с ЗНО губы с целью улучшения аппетита рекомендовано применение глюкокортикоидов короткими курсами (до 2-3 недель). [47].
- С целью повышения аппетита и массы тела у пациентов с кахексией рекомендовано назначение гестагенов. Необходимо учитывать риск развития побочных эффектов, включая тромбоэмболические осложнения [47].
- Пациентам с раком губы рекомендовано повышение и поддержание достаточного уровня физической активности с целью улучшения качества жизни [49].
- Рекомендован комплексный подход к психологической поддержке пациентов с раком губы на весь период лечения с целью улучшения качества жизни, раннего выявления и уменьшения уровня тревоги и депрессии [50].
- Рекомендован мультидисциплинарный подход к реабилитации пациентов с раком губы с обязательным включением в него психологической реабилитации на весь период лечения с целью улучшения качества жизни [51].
- Рекомендовано использовать телемедицинские технологии в реабилитации пациентов с раком губы на всех этапах лечения с целью улучшения качества жизни [52].
1. Пререабилитация
- Проведение пререабилитации рекомендовано всем пациентам со злокачественными опухолями головы и шеи, которым планируется специализированное лечение, так как значительно ускоряет функциональное восстановление, сокращает сроки пребывания в стационаре после операции и снижает частоту развития осложнений и летальных исходов на фоне лечения онкологического заболевания. Пререабилитация включает в себя лечебную физическую культуру (ЛФК), психологическую и нутритивную поддержку, информирование пациентов [53].
- Программы профилактической гимнастики и обучение тактике глотания до начала лечения рекомендовано с целью уменьшения нарушения глотания при проведении комплексной противоопухолевой терапии [54, 55].
- Рекомендовано мониторирование питательного статуса у пациентов, которые имеют достоверную потерю массы тела (5 % от исходной массы тела за предыдущий месяц или 10 % от исходной массы тела за предшествующие 6 мес), а также при нарушении функции глотания вследствие болевого синдрома или опухолевого поражения [56].
- Пациентам со злокачественными новообразованиями головы и шеи и риском нутритивной недостаточности рекомендована нутритивная поддержка, проводимая на амбулаторном этапе и продолженная в течение всего периода обследования, вплоть до проведения оперативного вмешательства, так как снижает число послеоперационных осложнений и длительность госпитализации. При сохранении перорального приема пищи предпочтение отдается высокобелковым готовым смесям, суточная дозировка не менее 400 мл/сут. При невозможности перорального приема пищи проводят зондовое, парентеральное или смешанное питание согласно расчетной потребности [58].
- При мальнутритивном статусе или риске развития нутритивной недостаточности пациентам со злокачественными новообразованиями головы и шеи на дооперационном этапе рекомендована адекватная питательная поддержка в течение как минимум 7 сут, так как снижает число послеоперационных осложнений и длительность пребывания в стационаре [59].
- У пациентов с ЗНО губы рекомендована физическая предреабилитация с включением аэробных тренировок, дыхательных и силовых упражнений для улучшения функциональных долгосрочных результатов [60].
- Рекомендованы раннее выявление и коррекция саркопении у пациентов с раком губы для улучшения результатов терапии основного заболевания и улучшения общей выживаемости [61].
2. Реабилитация при хирургическом лечении
I ЭТАП РЕАБИЛИТАЦИИ
- Рекомендовано использование протоколов fast track rehabilitation (быстрый путь) и ERAS (Enhanced recovery after surgery – ускоренное восстановление после операции), включающих комплексное обезболивание, раннее начало энтерального питания, отказ от рутинного использования катетеров и дренажей, ранняя мобилизация пациентов с 1−2-х послеоперационных суток (активизация и вертикализация), так как является безопасным, уменьшает длительность пребывания в стационаре, снижает число нехирургических осложнений и не увеличивает общее количество послеоперационных осложнений [62, 63].
- Рекомендовано пациентам с ЗНО губы купирование болевого синдрома в раннем послепоперационном периоде путем сочетания обезболивающей терапии и физиотерапии [66].
- Восстановление функции глотания возможно за счет восстановления двигательной функции сохранных анатомических структур, а также подвижности пересаженных тканей при адекватно выполненной пластике. Для восстановления функции глотания рекомендованы упражнения на увеличение объема движения и силы мышц и усиление произвольного контроля над временем и координацией глотка. [67, 68].
- У пациентов с ЗНО губы для создания компенсаторных механизмов речепроизводства рекомендуется применение артикуляционных упражнений в динамике и статике с постепенным увеличением нагрузки с целью улучшения функциональных результатов и качества жизни [69].
- Рекомендовано раннее начало физической реабилитации с включением упражнений на сопротивление у пациентов с парезом добавочного нерва после шейной лимфаденэктомии [70].
- Рекомендовано постепенное увеличение диапазона активных и пассивных движений в плечевом суставе для профилактики адгезивного капсулита у пациентов с парезом добавочного нерва после фациально-футлярного иссечения клетчатки шеи [71].
- Рекомендовано раннее ортезирование для снижения нагрузки на трапецевидную мышцу и область плеча у пациентов с парезом добавочного нерва после фациально-футлярного иссечения клетчатки шеи [71].
- С целью улучшения заживления послеоперационной раны у пациентов с ЗНО губы рекомендована низкоинтенсивная лазеротерапия [72]. .
II ЭТАП РЕАБИЛИТАЦИИ
- Рекомендовано выполнение комплексов ЛФК при афазии, дизартрии и для уменьшения спастики после проведения радикального хирургического лечения по поводу рака головы и шеи, так как оно безопасно, способствует быстрейшему восстановлению физической формы и улучшает качество жизни больного [73].
- Поддержание стабильной массы тела и активный образ жизни рекомендованы с целью увеличения сроков общей выживаемости у пациентов, перенесших хирургическое лечение [74].
III ЭТАП РЕАБИЛИТАЦИИ
- Пациентам с ЗНО губы рекомендовано поддержание высокого уровня физической активности после завершения лечения с целью улучшения функциональных результатов [75].
- Пациентам с ЗНО губы рекомендовано увеличение и поддержание высокого уровня физической активности с целью улучшения общей выживаемости [75,76].
- С целью преодоления тризма (тонического спазма группы жевательных мышц), который приводит к ограничению подвижности височно-нижнечелюстного сустава, пациентам с ЗНО губы рекомендованы упражнения, регулирующие степень открытия рта [77].
- Рекомендовано выполнение комплекса упражнений в сочетании с механотерапией для лечения тризма у пациентов с ЗНО губы [78].
- Рекомендовано проведение низкоинтенсивной лазеротерапии на область жевательной мускулатуры и височно-нижнечелюстной сустав с целью коррекции тризма у пациентов с ЗНО губы [79].
- Рекомендовано информирование пациентов с ЗНО губы после расширенных операций с/без ЛТ о возможности возникновения вторичной лимфедемы с целью раннего обращения к специалистам [80].
- Рекомендован регулярный скрининг пациентов с ЗНО губы после расширенных операций с/без ЛТ с целью раннего выявления вторичной лимфедемы области головы и шеи [80].
- Рекомендовано направление пациента с ЗНО губы после расширенных операций с/без ЛТ к специалисту по лечению вторичной лимфедемы в случае ее выявления в ходе скрининга [80]
- Рекомендовано обучение пациентов с ЗНО губы после расширенных операций с/без ЛТ методике самомассажа, выполнению комплекса ЛФК, уходу за кожей с целью профилактики и лечения вторичной лимфедемы области головы и шеи [81].
- У пациентов с ЗНО губы рекомендован комплексный подход к лечению вторичной лимфедемы области головы и шеи с включением компрессионной терапии, упражнений, ухода за кожей, ручного лимфодренажа и обучения пациентов самоконтролю [82].
- С целью лечения лимфедемы области головы и шеи у пациентов с ЗНО губы рекомендован массаж шеи, волосистой части головы и лица медицинский [83].
- Физиотерапия, включая специальный комплекс упражнений и компрессионное воздействие, также рекомендована у пациентов с ЗНО губы с целью коррекции лимфедемы [84, 85].
- Низкоинтенсивная лазеротерапия в комбинации с полной противозастойной терапией рекомендуется пациентам с ЗНО губы с целью уменьшения отека [86].
3. Реабилитация при лекарственном лечении
- Противоопухолевое лечение рака головы и шеи вызывает психологический дистресс, тревогу, депрессию, что ухудшает качество жизни пациентов. Выполнение упражнений с нагрузкой рекомендовано для уменьшения слабости, улучшения качества жизни и психологического состояния пациентов, получающих адьювантную химиотерапию [87].
- Для уменьшения утомляемости и повышения выносливости на фоне проведения ХЛТ рекомендовано проведение ЛФК. Оптимальный эффект дают аэробные упражнения средней интенсивности в сочетании с упражнениями на сопротивление [90, 91].
- Сочетание ЛФК с психологической поддержкой рекомендовано у пациентов с ЗНО губы для лечения слабости на фоне химиотерапии [91].
- Рекомендовано сочетание нутритивной поддержки и физической реабилитации на фоне системной терапии с целью улучшения качественного состава тела и физических функций у пациентов ЗНО губы [92].
- Рекомендовано выполнение комплекса ЛФК (общий массаж медицинский, терренное лечение) для коррекции патологической усталости на фоне системной терапии у пациентов с ЗНО губы [93].
- Рекомендована физическая активность умеренной интенсивности с включением в комплекс упражнений на сопротивление для коррекции патологической утомляемости на фоне системной терапии у пациентов с ЗНО губы [93].
- Рекомендована аэробная нагрузка, такая, как ходьба и упражнения на сопротивление в домашних условиях для улучшения качества жизни и контроля патологической утомляемости у пациентов с ЗНО губы [93].
- Рекомендована йога для коррекции патологической усталости и улучшения качества жизни на фоне системной терапии у пациентов с ЗНО губы [93].
- Рекомендовано информирование и психологическое консультирование пациентов с ЗНО губы и членов их семей для профилактики развития патологической усталости и перехода ее в хроническую фазу [93].
- Рекомендована когнитивно-поведенческая терапия (психотерапия) пациентам с ЗНО губы на фоне системной терапии для коррекции патологической усталости [93].
- Рекомендован массаж медицинский для коррекции патологической утомляемости на фоне системной терапии ЗНО губы [94].
- Пациентам с ЗНО губы рекомендована ЛФК с включением упражнений на координацию для профилактики токсической периферической полинейропатии [95].
- Рекомендована ЛФК, направленная на улучшение координации и мелкой моторики, которая должна начинаться одновременно с началом нейротоксичной терапии, самое позднее одновременно с манифестацией первых проявлений периферической полинейропатии [95].
- Рекомендовано применение локальной криотерапии для профилактики токсической периферической полинейропатии на фоне системной терапии у пациентов с ЗНО губы [95].
- Рекомендовано применение локальной компрессионной терапии для профилактики симптомов периферической полинейропатии на фоне системной терапии у пациентов с ЗНО губы [95].
- Рекомендована иглорефлексотерапия для коррекции периферической полинейропатии на фоне системной терапии у пациентов с ЗНО губы [95].
- Рекомендована ЭЭГ-БОС-терапия (neurofeedback) (тренировка с биологической обратной связью по электроэнцефалографии при заболеваниях периферической нервной системы), для коррекции периферической полинейропатии на фоне системной терапии у пациентов с ЗНО губы [95].
- Рекомендован общий массаж медицинский для лечения периферической полинейропатии на фоне системной терапии ЗНО губы [96].
4. Реабилитация при лучевой терапии
- Рекомендовано раннее начало нутритивной поддержки на фоне лучевой терапии для улучшения показателей пищевого статуса и уменьшения длительности госпитализации у пациентов с ЗНО губы [97]
- Рекомендовано проведение регулярной оценки функции глотания у пациентов с ЗНО губы в процессе ЛТ с целью раннего выявления дисфагии и своевременного изменения тактики энтерального питания [98].
- Рекомендовано проведение низкоинтенсивной лазеротерапии весь период ЛТ для профилактики развития радиоиндуцированного дерматита более 2 степени у пациентов с ЗНО губы [99].
- Рекомендован комбинированный подход к профилактике мукозита на фоне лучевой терапии у пациентов с ЗНО губы [100].
- Рекомендовано полоскание полости рта растворами с #бензидамином (полоскание ротовой полости #бензидамином 15 мл в течение 2 мин. 4-8 раз в день до, во время и в течение 2-х недель после завершения ЛТ) для профилактики мукозита полости рта на фоне всего курса ЛТ на область головы и шеи у пациентов с ЗНО губы [100, 126].
- Рекомендовано применение низкоинтенсивной лазеротерапии на полость рта для профилактики мукозита полости рта на фоне ЛТ ЗНО губы в течение всего периода ЛТ/ХЛТ [100].
- Рекомендовано начало ЛФК одновременно с началом ХЛТ, направленных на улучшение функции глотания с целью профилактики дисфагии у пациентов с ЗНО губы [80].
- Рекомендовано применение низкоинтенсивной лазеротерапии для профилактики острой дисфагии, уменьшения потребности в парентеральном питании и кратности применения опиоидов в процессе лучевой терапии у пациентов с ЗНО губы [101].
- Рекомендовано информирование пациентов о возможности развития ксеростомии на фоне ЛТ ЗНО губы, поощрение гигиены полости рта для профилактики осложнений на фоне нее [102].
- Рекомендована аккупунктура для профилактики ксеростомии на фоне ЛТ на область головы и шеи у пациентов с ЗНО губы [102].
- Рекомендованы местные средства, в том числе искусственная слюна для улучшения качества жизни пациентов с ксеростомией на фоне ЛТ на область головы и шеи [102].
- Рекомендована акупунктура с целью коррекции симптомов ксеростомии на фоне ХЛТ на область головы и шеи у пациентов с ЗНО губы [103].
- Рекомендована чрескожная короткоимпульсная электростимуляция области слюнных желез для коррекции симптомов ксеростомии после ЛТ опухолей головы и шеи у пациентов с ЗНО губы[102].
- Рекомендовано применение иглорефлексотерапии (воздействие на точки акупунктуры другими физическими факторами) для коррекции болевого синдрома и уменьшения дозы анальгетиков у пациентов с ЗНО губы на фоне ЛТ [104]
- Рекомендовано проведение гипербарической оксигенации с целью уменьшения субъективных симптомов ксеростомии, улучшения глотания, речи и общего качества жизни у пациентов с ЗНО губы [105].
Прогноз
Дополнительная информация (в томчисле факторы, влияющие на исходзаболевания или состояния)
Факторами, влияющими на прогноз заболевания являются:
Госпитализация
Организация оказания медицинской помощи
Медицинская помощь, за исключением медицинской помощи в рамках клинической апробации, в соответствии с Федеральным законом от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», организуется и оказывается:
-
в соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается уполномоченным Федеральным органом исполнительной власти;
-
в соответствии с порядком оказания помощи по профилю «онкология», обязательным для исполнения на территории Российской Федерации всеми медицинскими организациями;
-
на основе настоящих клинических рекомендаций;
-
с учетом стандартов медицинской помощи, утвержденных уполномоченным Федеральным органом исполнительной власти.
Первичная специализированная медико-санитарная помощь оказывается врачом-онкологом и иными врачами-специалистами в центре амбулаторной онкологической помощи либо в первичном онкологическом кабинете, поликлиническом отделении онкологического диспансера (онкологической больницы).
При подозрении или выявлении у пациента онкологического заболевания врачи-терапевты, врачи-терапевты участковые, врачи общей практики (семейные врачи), врачи-специалисты, средние медицинские работники в установленном порядке направляют пациента на консультацию в центр амбулаторной онкологической помощи либо в первичный онкологический кабинет, поликлиническое отделение онкологического диспансера (онкологической больницы) для оказания ему первичной специализированной медико-санитарной помощи.
Консультация в центре амбулаторной онкологической помощи либо в первичном онкологическом кабинете, поликлиническом отделении онкологического диспансера (онкологической больницы) должна быть проведена не позднее 5 рабочих дней с даты выдачи направления на консультацию. Врач-онколог центра амбулаторной онкологической помощи (в случае отсутствия центра амбулаторной онкологической помощи врач-онколог первичного онкологического кабинета или поликлинического отделения онкологического диспансера (онкологической больницы организует взятие биопсийного (операционного) материала, а также организует выполнение иных диагностических исследований, необходимых для установления диагноза, включая распространенность онкологического процесса и стадию заболевания.
В случае невозможности взятия в медицинской организации, в составе которой организован центр амбулаторной онкологической помощи (первичный онкологический кабинет, биопсийного (операционного) материала, проведения иных диагностических исследований пациент направляется лечащим врачом в онкологический диспансер (онкологическую больницу) или в медицинскую организацию, оказывающую медицинскую помощь пациентам с онкологическими заболеваниями.
Срок выполнения патологоанатомических исследований, необходимых для гистологической верификации злокачественных новообразований не должен превышать 15 рабочих дней с даты поступления биопсийного (операционного) материала в патологоанатомическое бюро (отделение).
Сроки проведения диагностических инструментальных и лабораторных исследований в случае подозрения на онкологическое заболевание не должны превышать сроков, установленных в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации.
Диагноз онкологического заболевания устанавливается врачом-онкологом, а при злокачественных новообразованиях лимфоидной, кроветворной и родственных им тканей, входящих в рубрики МКБ-10 С81-С96, также врачом-гематологом.
Врач-онколог центра амбулаторной онкологической помощи (первичного онкологического кабинета) направляет пациента в онкологический диспансер (онкологическую больницу) или иную медицинскую организацию, оказывающую медицинскую помощь пациентам с онкологическими заболеваниями, в том числе подведомственную федеральному органу исполнительной власти (далее – федеральная медицинская организация), для уточнения диагноза (в случае невозможности установления диагноза, включая распространенность онкологического процесса и стадию заболевания), определения тактики лечения, а также в случае наличия медицинских показаний для оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
При онкологических заболеваниях, входящих в рубрики С37, C38, C40–C41, C45–C49, С58, D39, C62, C69–C70, С72, C74 МКБ-10, а также соответствующих кодам международной классификации болезней – онкология (МКБ-О), 3 издания 8936, 906-909, 8247/3, 8013/3, 8240/3, 8244/3, 8246/3, 8249/3 врач-онколог онкологического диспансера (онкологической больницы) или иной медицинской организации, оказывающей медицинскую помощь пациентам с онкологическими заболеваниями, для определения лечебной тактики организует проведение консультации или консилиума врачей, в том числе с применением телемедицинских технологий, в федеральных государственных бюджетных учреждениях, подведомственных Министерству здравоохранения Российской Федерации, оказывающих медицинскую помощь (далее в целях настоящего Порядка – национальные медицинские исследовательские центры).
В сложных клинических случаях для уточнения диагноза (в случае невозможности установления диагноза, включая распространенность онкологического процесса и стадию заболевания) в целях проведения оценки, интерпретации и описания результатов врач-онколог организует направление:
- цифровых изображений, полученных по результатам патоморфологических исследований, в патолого-анатомическое бюро (отделение) четвертой группы (референс-центр) путем информационного взаимодействия, в том числе с применением телемедицинских технологий при дистанционном взаимодействии медицинских работников между собой;
- цифровых изображений, полученных по результатам лучевых методов исследований, в дистанционный консультативный центр лучевой диагностики, путем информационного взаимодействия, в том числе с применением телемедицинских технологий при дистанционном взаимодействии медицинских работников между собой;
- биопсийного (операционного) материала для повторного проведения патоморфологических, иммуногистохимических, и молекулярно-генетических исследований: в патолого-анатомическое бюро (отделение) четвертой группы (референс-центр), а также в молекулярно-генетические лаборатории для проведения молекулярно-генетических исследований.
Тактика лечения устанавливается консилиумом врачей, включающим врачей-онкологов, врача-радиотерапевта, врача-нейрохирурга (при опухолях нервной системы) медицинской организации, в составе которой имеются отделения хирургических методов лечения злокачественных новообразований, противоопухолевой лекарственной терапии, радиотерапии (далее - онкологический консилиум), в том числе онкологическим консилиумом, проведенным с применением телемедицинских технологий, с привлечением при необходимости других врачей-специалистов.
Диспансерное наблюдение врача-онколога за пациентом с выявленным онкологическим заболеванием устанавливается и осуществляется в соответствии с порядком диспансерного наблюдения за взрослыми с онкологическими заболеваниями.
С целью учета информация о впервые выявленном случае онкологического заболевания направляется в течение 3 рабочих дней врачом-онкологом медицинской организации, в которой установлен соответствующий диагноз, в онкологический диспансер или организацию субъекта Российской Федерации, исполняющую функцию регистрации пациентов с впервые выявленном злокачественным новообразованием, в том числе с применением единой государственной информационной системы в сфере здравоохранения.
Специализированная, в том числе высокотехнологичная, медицинская помощь в медицинских организациях, оказывающих медицинскую помощь взрослому населению при онкологических заболеваниях, оказывается по медицинским показаниям, предусмотренным положением об организации оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
Специализированная, за исключением высокотехнологичной, медицинская помощь в медицинских организациях, подведомственных федеральным органам исполнительной власти, оказывается по медицинским показаниям, предусмотренным пунктом 5 порядка направления пациентов в медицинские организации и иные организации, подведомственные федеральным органам исполнительной власти, для оказания специализированной (за исключением высокотехнологичной) медицинской помощи, предусмотренного в приложении к положению об организации оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
Сроки ожидания оказания специализированной (за исключением высокотехнологичной) медицинской помощи не должны превышать сроков, установленных в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации.
При наличии у пациента с онкологическим заболеванием медицинских показаний для проведения медицинской реабилитации врач-онколог организует ее проведение в соответствии с порядком организации медицинской реабилитации взрослых.
При наличии у пациента с онкологическим заболеванием медицинских показаний к санаторно-курортному лечению врач-онколог организует его в соответствии порядком организации санаторно-курортного лечения.
Паллиативная медицинская помощь пациенту с онкологическими заболеваниями оказывается в соответствии с положением об организации оказания паллиативной медицинской помощи, включая порядок взаимодействия медицинских организаций, организаций социального обслуживания и общественных объединений, иных некоммерческих организаций, осуществляющих свою деятельность в сфере охраны здоровья.
При подозрении и (или) выявлении у пациента онкологического заболевания в ходе оказания ему скорой медицинской помощи его переводят или направляют в медицинские организации, оказывающие медицинскую помощь пациентам с онкологическими заболеваниями, для определения тактики ведения и необходимости применения дополнительно других методов специализированного противоопухолевого лечения.
Показаниями для госпитализации в медицинскую организацию в экстренной или неотложной форме являются:
-
наличие осложнений онкологического заболевания, требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме;
-
наличие осложнений лечения (хирургическое вмешательство, ЛТ, лекарственная терапия и т.д.) онкологического заболевания.
Показаниями для госпитализации в медицинскую организацию в плановой форме являются:
-
необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, требующих последующего наблюдения в условиях круглосуточного или дневного стационара;
-
наличие показаний к специализированному противоопухолевому лечению (хирургическое вмешательство, ЛТ, в том числе контактная, ДЛТ и другие виды ЛТ, лекарственная терапия и др.), требующему наблюдения в условиях круглосуточного или дневного стационара.
Показаниями к выписке пациента из медицинской организации являются:
-
завершение курса лечения или одного из этапов оказания специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара при условии отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
-
отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара, установленной консилиумом медицинской организации, оказывающей онкологическую помощь при условии отсутствия осложнений основного заболевания и/или лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
-
в случаях несоблюдения пациентом предписаний или правил внутреннего распорядка лечебно-профилактического учреждения, если это не угрожает жизни пациента и здоровью окружающих;
-
необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи.
Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или предварительного осмотра пациента врачами-специалистами медицинской организации, в которую планируется перевод.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- Рекомендуется соблюдать следующие периодичность и методы наблюдения после завершения лечения по поводу рака губы:
В первый год физикальный осмотр и сбор жалоб проводить каждые 1−3 мес, 2-й год – 2−6 мес, на сроке 3−5 лет – 1 раз в 4−8 мес. После 5 лет с момента операции визиты проводятся ежегодно или при появлении жалоб. У пациентов с высоким риском рецидива перерыв между обследованиями может быть сокращен. Объем обследования:
- анамнез и физикальное обследование;
- УЗИ ЛУ шеи с двух сторон, органов брюшной полости и малого таза;
- КТ области головы и шеи по показаниям, а также при недоступности зоны адекватному физикальному осмотру;
- рентгенография/КТ органов грудной клетки каждые 12 мес;
- определение уровня тиреотропного гормона каждые 6–12 мес, если проводилось облучение шеи с целью оценки функции щитовидной железы [1, 4].
- Рекомендуется наблюдение у стоматолога до, во время и после специализированного лечения с целью оценки состояния полости рта, риска развития кариеса и пародонтоза, удаления проблемных зубов, профилактики радиоиндуцированного остеонекроза, устранения потенциальных источников инфекции, мотивации пациента к поддержанию гигиены полости рта. Проблемные зубы должны быть удалены не менее чем за 2 нед до начала специализированного лечения [44, 79-84].
- Рекомендуются всем пациентам после окончания лучевой терапии с целью профилактики кариеса применять ежедневно длительно местные средства с фтором – 0,4% гель с фторидом олова или 1,1 % гель с фторидом натрия (NaF) (эффективность ниже фторида олова), или комбинацию - 0,4% гель с фторидом олова, 0,32% зубной порошок с NaF и препараты-заменители слюны с фосфатом кальция [44, 79, 80, 81, 82, 83, 84].
Информация
Источники и литература
-
Клинические рекомендации Ассоциации онкологов России
- Клинические рекомендации Ассоциации онкологов России - 1. Алиева С.Б., Алымов Ю.В., Кропотов М.А. и др. Рак губы. Онкология. Клинические рекомендации. Под ред. М.И. Давыдова. М.: Издательская группа РОНЦ, 2015. С. 17‒20 2. Пачес А.И. Опухоли головы и шеи. 5-е изд., доп. и перераб. М.: Практическая медицина, 2013. С. 105‒12 3. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой Состояние онкологической помощи населению России в 2021 году. − М.: МНИОИ им. П.А. Герцена − филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2022. − илл. – 239 с 4. Shah J.P., Patel S. G., Singh B. Head and neck surgery and oncology. 4thеdn. P. 204 5. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®). Cancer of the Lip. Version 1.2022 6. Richards, D. (2015). Adjunctive tests cannot replace scalpel biopsy for oral cancer diagnosis. Evidence-Based Dentistry, 16(2), 46–47 7. Babu N.H., Devi B.V.L., Kadiyala S. et al. Accuracy of preoperative ultrasonography in measuring tumor thickness and predicting the incidence of cervical lymph node metastasis in oral cancer. J Dr NTR Univers Health Sci 2018;7(4):241−4 8. Wouter L. Lodder, Hendrik J. Teertstra, Ing B. Tan et al. Tumour thickness in oral cancer using an intra-oral ultrasound probe. Eur Radiol 2011;21(1):98–106 9. Fleming A.J., Smith S.P., Paul C.M. et al. Impact of [18F]-2-fluorodeoxyglucose-positron emission tomography/computed tomography on previously untreated head and neck cancer patients. Laryngoscope 2007;117(7):1173‒9 10. Ellis M.A., Graboyes E.M., Wahlquist A.E., et al. Primary Surgery vs Radiotherapy for Early Stage Oral Cavity Cancer. Otolaryngology– Head and Neck Surgery 2018, Vol. 158(4) 649–659 11. McCombe D., MacGill K., Ainslie J. et al. Squamous cell carcinoma of the lip: a retrospective review of the Peter MacCallum Cancer Institute experience 1979‒88. Aust N Z J Surg 2000;70(5):358‒61 12. De Visscher J.G., van den Elsaker K., Grond A.J. et al. Surgical treatment of squamous cell carcinoma of the lower lip: evaluation of long-term results and prognostic factors ‒ a retrospective analysis of 184 patients. J Oral Maxillofac Surg 1998;56:814‒20 13. Bhandari, K., Wang, D., Li, S., Jiang, B., Guo, Y., Koirala, U., & Du, X. (2014). Primary cN0 lip squamous cell carcinoma and elective neck dissection: Systematic review and meta-analysis. Head & Neck, 37(9), 1392–1400 14. Mazeron J.J., Ardiet J.M., Haie-Méder C. et al. GEC-ESTRO recommendations for brachytherapy for head and neck squamous cell carcinomas. Radiother Oncol 2009;91(2):150−6 15. Kübler A.C., de Carpentier J., Hopper C. et al. Treatment of squamous cell carcinoma of the lip using Foscan-mediated photodynamic therapy. Int J Oral Maxillofac Surg 2001;30(6):504−9 16. De Visscher J.G., Botke G., Schakenraad J.A., van der Waal I. A comparison of results after radiotherapy and surgery for stage I squamous cell carcinoma of the lower lip. Head Neck 1999;21:526‒30 17. Chone, C. T., Magalhães, R. S., Etchehebere, E., Camargo, E., Altemani, A., & Crespo, A. N. (2008). Predictive value of sentinel node biopsy in head and neck cancer. Acta Oto-Laryngologica, 128(8), 920–924 18. Babington S., Veness M.J., Cakir B. et al. Squamous cell carcinoma of the lip: is there a role for adjuvant radiotherapy in improving local control following incomplete or inadequate excision? ANZ J Surg 2003;73:621‒5 19. De Visscher J.G., Grond A.J., Botke G., van der Waal I. Results of radiotherapy for squamous cell carcinoma of the vermilion border of the lower lip. A retrospective analysis of 108 patients. Radiother Oncol 1996;39:9‒14 20. Bernier J., Cooper J.S. Chemoradiation after surgery for high-risk head and neck cancer patients: how strong is the evidence?, Oncologist 2005;10(3):215−24 21. Bernier J., van Glabbeke M., Domenge C. et al. Results of EORTC phase III trial 22931 comparing, postoperatively, radiotherapy (RT) to concurrent chemo-radiotherapy (RT−CT) with high dose cisplatin in locally advanced head and neck (H & N) carcinomas (SCC). Eur J Cancer 2001 22. Cooper J.S., Zhang Q., Pajak T.F. et al. Long-term follow-up of the RTOG 9501/intergroup phase III trial: postoperative concurrent radiation therapy and chemotherapy in high-risk squamous cell carcinoma of the head and neck. Int J Radiat Oncol Biol Phys 2012;84(5):1198−205 23. Vermorken J.B., Mesia R., Rivera F. et al. Platinum-based chemotherapy plus cetuximab in head and neck cancer. N Engl J Med 2008;359:1116−27 24. Posner M.R., Hershock D.M., Blajman C.R. et al. Cisplatin and fluorouracil alone or with docetaxel in head and neck cancer. N Engl J Med 2007;357:1705−15 25. Болотина Л. В., Владимирова Л. Ю., Деньгина Н. В., Новик А. В., Романов И. С. Практические рекомендации по лечению злокачественных опухолей головы и шеи // Злокачественные опухоли: Практические рекомендации RUSSCO #3s2, 2021 (том 11). С. 71–82 26. Hitt R., Lopez-Pousa A, Martinez-Trufero J et al. Phase III study comparing cisplatin plus fluorouracil to paclitaxel, cisplatin, and fluorouracil induction chemotherapy followed by chemoradiotherapy in locally advanced head and neck cancer. J Clin Oncol 2005;23(34):8636−45 27. Burtness B., Goldwasser M.A., Flood W. et al. Phase III randomized trial of cisplatin plus placebo compared with cisplatin plus cetuximab in metastatic/recurrent head and neck cancer: an Eastern Cooperative Oncology Group study. J Clin Oncol 2005;23:8646−54 28. Schöffski, P., Catimel, G., Planting et al. (1999). Docetaxel and cisplatin: An active regimen in patients with locally advanced, recurrent or metastatic squamous cell carcinoma of the head and neck. Annals of Oncology, 10(1), 119–122 29. Forastiere A.A., Metch B., Schuller D.E. et al. Randomized comparison of cisplatin plus fluorouracil and carboplatin plus fluorouracil versus methotrexate in advanced squamous-cell carcinoma of the head and neck: a Southwest Oncology Group study. J Clin Oncol 1992;10:1245−51 30. Jacobs C., Lyman G., Velez-Garcia E. et al. A phase III randomized study comparing cisplatin and fluorouracil as single agents and in combination for advanced squamous cell carcinoma of the head and neck. J Clin Oncol 1992;10:257−63 31. Grau J.J., Caballero M., Verger E. et al. Weekly paclitaxel for platin-resistant stage IV head and neck cancer patients. Acta Otolaryngol 2009;129:1294−9 32. Catimel, G., Verweij, J., Mattijssen, V., et al (1994). Docetaxel (Taxotere®): An active drug for the treatment of patients with advanced squamous cell carcinoma of the head and neck. Annals of Oncology, 5(6), 533–537 33. Guardiola E., Peyrade F., Chaigneau L. et al. Results of a randomised phase II study comparing docetaxel with methotrexate in patients with recurrent head and neck cancer. Eur J Cancer 2004;40:2071−6 34. Vermorken J.B., Trigo J., Hitt R. et al. Open-label, uncontrolled, multicenter phase II study to evaluate the efficacy and toxicity of cetuximab as a single agent in patients with recurrent and/or metastatic squamous cell carcinoma of the head and neck who failed to respond to platinum-based therapy. J Clin Oncol 2007;25:2171−7 35. Martinez-Trufero J., Isla D., Adansa J.C. et al. Phase II study of capecitabine as palliative treatment for patients with recurrent and metastatic squamous head and neck cancer after previous platinum-based treatment. Br J Cancer 2010;102:1687−91 36. Ferris R., Blumenschein G., Fayette J. et al. Nivolumab for recurrent squamous-cell carcinoma of the head and neck. N Engl J Med 2016;375:1856‒67 37. Ye W., Schmitt, N. C. (2019). Pembrolizumab for recurrent/metastatic head and neck cancer: equally promising for Asian patients? Annals of Translational Medicine, 7(S1), S14–S14. doi:10.21037/atm.2019.01.46 38. Сohen, E. E. W., Soulières, D., Le Tourneau, C., et al. (2018). Pembrolizumab versus methotrexate, docetaxel, or cetuximab for recurrent or metastatic head-and-neck squamous cell carcinoma (KEYNOTE-040): a randomised, open-label, phase 3 study. The Lancet. doi:10.1016/s0140-6736(18)31999-8 39. Сhow L.Q., Haddad R., Gupta S. et al. Antitumor activity of pembrolizumab in biomarker-unselected patients with recurrent and/or metastatic head and neck squamous cell carcinoma: results from the phase Ib KEYNOTE-012 expansion cohort. J Clin Oncol 2016;34(32):3838‒45 40. Machiels J.P., Haddad R.I., Fayette J. et al. Afatinib versus methotrexate as second-line treatment in patients with recurrent or metastatic squamous-cell carcinoma of the head and neck progressing on or after platinum-based therapy (LUX-Head & Neck 1): an open-label, randomised phase 3 trial. Lancet Oncol 2015;16:583−94 41. Noronha V., Joshi A., Patil V.M. et al. Once-a-week versus once-every-3-weeks cisplatin chemoradiation for locally advanced head and neck cancer: a phase III randomized noninferiority trial. J Clin Oncol 2018; 36‒11:1064‒72 42. Looser K.G., Shah J.P., Strong E.W. The significance of “positive” margins in surgically resected epidermoid carcinomas. Head Neck Surg 1978;1(2):107–11 43. Gorsky M., Epstein J.B., Parry J. et al. The efficacy of pilocarpine and bethanechol upon saliva production in cancer patients with hyposalivation following radiation therapy. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2004;9792):190‒5 44. Jensen S.B., Pedersen A.M., Vissink A. et al. A systematic review of salivary gland hypofunction and xerostomia induced by cancer therapies: management strategies and economic impact. Support Care Cancer 2010;18(8):1061‒79 45. Иванова Г.Е., Мельникова Е.В., Шмонин А.А., Вербицкая Е.В., Аронов Д.М., Белкин А.А., Беляев А.Ф., Бодрова Р.А., Бубнова М.Г., Буйлова Т.В., Мальцева М.Н., Мишина И.Е., Нестерин К.В., Никифоров В.В., Прокопенко С.В., Сарана А.М.О., Стаховская Л.В., Суворов А.Ю., Хасанова Д.Р., Цыкунов М.Б. и др. Пилотный проект "Развитие системы медицинской реабилитации в Российской Федерации": Предварительные результаты реализации на первом и втором этапах медицинской реабилитации. Вестник восстановительной медицины. 2017. N 2 (78). С. 10 - 15. 46. Приказ Министерства здравоохранения РФ от 31 июля 2020 г. N 778н "О Порядке организации медицинской реабилитации взрослых" Зарегистрировано в Минюсте РФ 25 сентября 2020 г. Регистрационный N 60039. 47. Arends J, Strasser F, Gonella S, Solheim TS, Madeddu C, Ravasco P, Buonaccorso L, de van der Schueren MAE, Baldwin C, Chasen M, Ripamonti CI; ESMO Guidelines Committee. Electronic address: clinicalguidelines@esmo.org. Cancer cachexia in adult patients: ESMO Clinical Practice Guidelines☆. ESMO Open. 2021 Jun;6(3):100092. doi: 10.1016/j.esmoop.2021.100092. PMID: 34144781; PMCID: PMC8233663. 48. Muscaritoli M, Arends J, Bachmann P, Baracos V, Barthelemy N, Bertz H, et al. ESPEN practical guideline: Clinical Nutrition in cancer. Clinical Nutrition. 2021.40; p. 2898-2913. 49. Burgos-Mansilla, B.; Galiano-Castillo, N.; Lozano-Lozano, M.; Fernández-Lao, C.; Lopez-Garzon, M.; Arroyo-Morales, M. Effect of Physical Therapy Modalities on Quality of Life of Head and Neck Cancer Survivors: A Systematic Review with Meta-Analysis. J. Clin. Med. 2021, 10, 4696. https://doi.org/ 10.3390/jcm10204696 50. Kar A, M R A, Bhaumik U, Rao VUS. Psychological issues in head and neck cancer survivors: Need for addressal in rehabilitation. Oral Oncol. 2020 Nov;110:104859. doi: 10.1016/j.oraloncology.2020.104859. Epub 2020 Jun 18. PMID: 32564916 51. Elaldi R, Roussel LM, Gal J, Scheller B, Chamorey E, Schiappa R, Lasne-Cardon A, Louis MY, Culié D, Dassonville O, Poissonnet G, Saada E, Benezery K, Babin E, Bozec A. Correlations between long-term quality of life and patient needs and concerns following head and neck cancer treatment and the impact of psychological distress. A multicentric cross-sectional study. Eur Arch Otorhinolaryngol. 2021 Jul;278(7):2437-2445. doi: 10.1007/s00405-020-06326-8. Epub 2020 Sep 8. PMID: 32901366 52. Dias JF, Oliveira VC, Borges PRT, et al Effectiveness of exercises by telerehabilitation on pain, physical function and quality of life in people with physical disabilities: a systematic review of randomised controlled trials with GRADE recommendations British Journal of Sports Medicine 2021;55:155-162 53. Silver J.A., Baima J. Cancer prehabilitation: anopportunity to decrease treatment-related morbidity, increase cancer treatment options, and improve physical and psychological health outcomes. Am J Phys Med Rehabil 2103;92(8):715‒27 54. Govender R., Smith C.H., Gardner B. Et al. Improving swallowing outcomes in patients with head and neck cancer using a theory-based pretreatment swallowing intervention package: protocol for a randomised feasibility study. BMJ Open 2017;7(3):e014167 55. Clarke P., Radford K., Coffey M., Stewart M. Speech and swallow rehabilitation in head and neck cancer: United Kingdom National Multidisciplinary Guidelines. J Laryngol Otol 2016;130(S2):176‒80 56. Cнеговой А.В., Бесова Н.С., Веселов А.В. и др. Практические рекомендации по нутритивной поддержке у онкологических больных. Злокачественные опухоли 2016;4(2):434−450 57. Сolevas A.D., Yom S.S., Pfister D.G. et al. NCCN Guidelines Insights: head and neck cancers. Version 1.2018. J Natl Compr Canc Netw 2018;16(5):479−90 58. Arends J., Bachmann P., Baracos V. et al. ESPEN guidelines on nutrition in cancer patients. Clin Nutr 2017;36(1):11−48 59. Talwar, B., Donnelly, R., Skelly, R., & Donaldson, M. (2016). Nutritional management in head and neck cancer: United Kingdom National Multidisciplinary Guidelines. The Journal of Laryngology & Otology, 130(S2), S32–S40 60. Linda Denehy, Lara Edbrooke, The Role of Exercise Before Cancer Treatment, Seminars in Oncology Nursing, 2022, 151330, ISSN 0749-2081, https://doi.org/10.1016/j.soncn.2022.151330 61. Takenaka Y, Takemoto N, Oya R, Inohara H. Prognostic impact of sarcopenia in patients with head and neck cancer treated with surgery or radiation: A meta-analysis. PLoS One. 2021 Oct 29;16(10):e0259288. doi: 10.1371/journal.pone.0259288. PMID: 34714876; PMCID: PMC8555817 62. Hubera G.F., Dort J.C. Reducing morbidity and complications after major head and neck cancer surgery: the (future) role of enhanced recovery after surgery protocols. Curr Opin Otolaryngol Head Neck Surg 2018, 26(2):73−5 63. Coyle, M. J., Main, B., Hughes, C., et al. (2016). Enhanced recovery after surgery (ERAS) for head and neck oncology patients. Clinical Otolaryngology, 41(2), 118–126. doi:10.1111/coa.12482 64. Midgley A.W., Lowe D., Levy A.R. et al. Exercise program design considerations for head and neck cancer survivors. Eur Arch Otorhinolaryngol 2018;275(1):169−79 65. Guru K., Manoor U.K., Supe S.S. A comprehensive review of head and neck cancer rehabilitation: physical therapy perspectives. Indian J Palliat Care. 2012;18(2):87−97 66. Swarm R.A., Abernethy A.P., Anghelescu D.L. et al. Adult cancer pain. J Natl Compr Canc Netw 2013;11(8):992−1022 67. Wall L.R., Ward E.C., Cartmill B., Hill A.J. Physiological changes to the swallowing mechanism following (chemo) radiotherapy for head and neck cancer: a systematic review. Dysphagia 2013;28(4):481–93 68. Govender R., Smith C.H., Taylor S.A. et al. Swallowing interventions for the treatment of dysphagia after head and neck cancer: a systematic review of behavioural strategies used to promote patient adherence to swallowing exercises. BMC Cancer 2017;17(1):43 69. Starmer, H. M., Ayoub, N., Byward, C., et al. (2017). The impact of developing a speech and swallow rehab program: Improving patient satisfaction and multidisciplinary care. The Laryngoscope, 127(11), 2578–2581
Информация
Термины и определения
-
размеры и распространенность первичной опухоли;
-
глубина инвазии первичной опухоли;
-
степень дифференцировки опухоли;
-
наличие/отсутствие периваскулярной, перилимфатической, периневральной инвазии;
-
статус регионарных ЛУ (рN) (метастазы в ЛУ шеи вдвое снижают выживаемость больных)
-
экстранодальное распространение опухоли;
-
статус краев резекции (R0-1)
Критерии оценки качества медицинской помощи
|
№
|
Критерии качества
|
Оценка выполнения
|
|---|---|---|
|
1.
|
Выполнена биопсия опухоли и/или измененных регионарных ЛУ с последующим патолого-анатомическом исследованием биопсийного материала (при установлении диагноза)
|
Да/Нет
|
|
2.
|
Выполнено УЗИ ЛУ шеи (при установлении диагноза)
|
Да/Нет
|
|
3.
|
Выполнено КТ/МРТ пораженной области с в/в контрастированием для оценки распространенности опухолевого процесса
|
Да/Нет
|
|
4.
|
Выполнено КТ органов грудной клетки при распространенном раке с поражением регионарных ЛУ
|
Да/Нет
|
|
5.
|
Выполнено патолого-анатомическое исследование операционного материала ( препарата удаленных тканей) (при хирургическом вмешательстве)
|
Да/Нет
|
|
6.
|
Выполнена шейная лимфодиссекция при хирургическом вмешательстве при распространенности заболевания, соответствующего стадиям T3,T4a, N0, любое T1−4a N1−3
|
Да/Нет
|
-
Поляков Андрей Павлович, д.м.н., доцент, заведующий отделением микрохирургии МНИОИ им. П.А. Герцена - филиал ФГБУ «НМИЦ радиологии» Минздрава России, член Общероссийской общественной организации «Российское общество специалистов по опухолям головы и шеи»
-
Кульбакин Денис Евгеньевич, д.м.н., заведующий отделением опухолей головы и шеи НИИ онкологии Томского НИМЦ
-
Агабабян Татев Артаковна, заведующая отделением лучевой диагностики МРНЦ им. А.Ф. Цыба — филиала ФГБУ «НМИЦ радиологии» Минздрава России, к.м.н., Обнинск https://orcid.org/0000-0002-9971-3451
-
Алиева Севил Багатуровна, д.м.н., ведущий научный сотрудник отделения радиационной онкологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, член Общероссийской общественной организации «Российское общество специалистов по опухолям головы и шеи».
-
Алымов Юрий Владимирович, к.м.н., врач-онколог отделения хирургических методов лечения №5 (эндокринной онкологии) НИИ клинической онкологии им. Н.Н. Трапезникова ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, исполнительный директор Общероссийской общественной организации «Российское общество специалистов по опухолям головы и шеи»; ORCID: https://orcid.org/0000-0002-6851-9867
-
Артемьева Анна Сергеевна, к.м.н., врач-патоморфолог, руководитель научной лаборатории морфологии опухолей ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, доцент отделения дополнительного профессионального образования НМИЦ онкологии им. Н.Н. Петрова
-
Бойко Анна Владимировна, д.м.н., профессор, заведующая отделением лучевой терапии с модификацией МНИОИ им. П.А. Герцена – филиала ФГБУ «НМИЦ радиологии» Минздрава России.
-
Болотин Михаил Викторович, к.м.н., научный сотрудник отделения хирургического № 11 опухолей верхних дыхательно-пищеварительных путей ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, член Общероссийской общественной организации «Российское общество специалистов по опухолям головы и шеи».
-
Болотина Лариса Владимировна, д.м.н., доцент РАН, заведующая отделением химиотерапии МНИОИ им. П.А. Герцена – филиала ФГБУ «НМИЦ радиологии» Минздрава России. Председатель группы опухолей головы и шеи практических рекомендаций Российского общества клинической онкологии, член Правления.
-
Виноградов Вячеслав Вячеславович, д.м.н., профессор, руководитель научно-клинического отдела лор-онкологии ФГБУ «Научно-клинический центр оториноларингологии» ФМБА России.
-
Владимирова Любовь Юрьевна, д.м.н., профессор, руководитель отдела лекарственного лечения опухолей, ФГБУ «НМИЦ онкологии» МЗ РФ
-
Геворков Артем Рубенович, к.м.н., с.н.с., врач-радиотерапевт отделения лучевой терапии с модификацией МНИОИ им. П.А. Герцена - филиала ФГБУ «НМИЦ радиологии» Минздрава России, член Общероссийской общественной организации «Российское общество специалистов по опухолям головы и шеи»
-
Гиршович Михаил Маркович, к.м.н., врач-радиотерапевт ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России; https://orcid.org/0000-0002-7925-9570
-
Гулидов Игорь Александрович, заведующий отделом лучевой терапии МРНЦ им. А.Ф. Цыба- филиал ФГБУ «НМИЦ радиологии» Минздрава России
-
Гузь Александр Олегович, к.м.н., врач-онколог, заведующий отделением опухолей головы и шеи ГБУЗ «Челябинский областной клинический центр онкологии и ядерной медицины»
-
Дайхес Николай Аркадьевич, член-корр. РАН, д.м.н., профессор, директор ФГБУ «Научно-клинический центр оториноларингологии» ФМБА России.
-
Дронова Екатерина Леонидовна, врач-радиолог ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, член Общероссийской общественной организации «Российское общество специалистов по опухолям головы и шеи».
-
Енгибарян Марина Александровна, д.м.н., заведующая отделением опухолей головы и шеи ФГБУ «НМИЦ онкологии» МЗ РФ, член Общероссийской общественной организации «Российское общество специалистов по опухолям головы и шеи».
-
Игнатова Анастасия Валерьевна, к.м.н., врач-онколог отделения хирургических методов лечения №5 НИИ клинической онкологии им. Н.Н. Трапезникова ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, член Общероссийской общественной организации «Российское общество специалистов по опухолям головы и шеи», ассистент кафедры общей и клинической стоматологии ФГАОУ ВО РУДН. ORCID: https://orcid.org/0000-0002-6796-0968
-
Клименко Вероника Викторовна, к.м.н., врач клинико-диагностического отделения ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России; https://orcid.org/0000-0003-1079-4492
-
Корниецкая Анна Леонидовна, к.м.н., старший научный сотрудник отделения химиотерапии отдела лекарственного лечения опухолей МНИОИ им. П.А. Герцена – филиала ФГБУ «НМИЦ радиологии» Минздрава России.
-
Костромина Екатерина Викторовна, к.м.н., врач ультразвуковой диагностики, врач-рентгенолог отделения лучевой диагностики, научный сотрудник научного отделения диагностической и интервенционной радиологии ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» МЗ РФ, доцент кафедры лучевой диагностики и медицинской визуализации ФП и ДПО ФГБОУ ВО СПбГМУ; https://orcid.org/0000-0002-4245-687X
-
Красильникова Лариса Анваровна, к.м.н., врач-цитолог ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России
-
Кропотов Михаил Алексеевич, д.м.н., заведующий отделением хирургическим отделением №10 опухолей головы и шеи ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России
-
Кутукова Светлана Игоревна, д.м.н., доцент, ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет имени академика И.П. Павлова» Министерства здравоохранения Российской Федерации, СПб ГБУЗ «Городской клинический онкологический диспансер»
-
Мордовский Александр Валентинович – к.м.н., научный сотрудник отделения микрохирургии МНИОИ им. П.А. Герцена – филиала ФГБУ «НМИЦ радиологии» Минздрава России
-
Мудунов Али Мурадович, д.м.н., профессор РАН, заведующий отделением хирургических методов лечения № 10 опухолей головы и шеи ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, президент Общероссийской общественной организации «Российское общество специалистов по опухолям головы и шеи»
-
Мусин Шамиль Исмагилович, к.м.н., заведующий хирургическим отделением N6 ГАУЗ РКОД Минздрава РБ
-
Подвязников Сергей Олегович, д.м.н., профессор, ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, вице-президент Общероссийской общественной организации «Российское общество специалистов по опухолям головы и шеи».
-
Полькин Вячеслав Викторович, к.м.н. заведующий отделения лучевого и хирургического лечения заболеваний головы, шеи МРНЦ им. А.Ф. Цыба - филиала ФГБУ «НМИЦ радиологии» Минздрава России
-
Пономарева Ольга Игоревна, врач-рентгенолог отделения радиотерапии НМИЦ онкологии им. Н.Н. Петрова; https://orcid.org/0000-0002-7004-9630
-
Раджабова Замира Ахмед-Гаджиевна, д.м.н., доцент РАН, заведующий отделением опухолей головы и шеи ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, доцент отделения дополнительного профессионального образования НМИЦ онкологии им. Н.Н. Петрова https://orcid.org/0000-0002-6895-0497
-
Решетов Игорь Владимирович, д.м.н., профессор, академик РАН, заведующий кафедрой онкологии, радиотерапии и реконструктивной хирургии Первого Московского медицинского университета им. И.М. Сеченова, президент Общероссийской общественной организации «Федерация специалистов по лечению заболеваний головы и шеи»
-
Романов Илья Станиславович, д.м.н, старший научный сотрудник отделения онкоэндокринологии ФГБУ «НМИЦ Онкологии им. Н.Н. Блохина», доцент кафедры онкологии ФДПО, РНИМУ им Н.И. Пирогова
-
Рубцова Наталья Алефтиновна, д.м.н., заведующая отделом лучевой диагностики МНИОИ им. П.А. Герцена – филиал «НМИЦ радиологии» Минздрава России. Главный внештатный специалист по лучевой и инструментальной диагностике Минздрава России по Центральному федеральному округу Российской Федерации.
-
Рудык Андрей Николаевич, к.м.н., врач-онколог онкологического отделения №5 (опухолей головы и шеи) ГАУЗ «Республиканский клинический онкологический диспансер Министерства здравоохранения Республики Татарстан имени профессора М.З.Сигала», и.о. заведующего кафедрой челюстно-лицевой хирургии и хирургической стоматологии, доцент кафедры онкологии, радиологии и паллиативной медицины КГМА - филиал ФГБОУ ДПО РМАНПО Минздрава России, доцент кафедры хирургических болезней постдипломного образования ИФМиБ ФГАОУ ВО "Казанский (Приволжский) федеральный университет", г. Казань.
-
Семиглазова Татьяна Юрьевна, д.м.н., профессор, заведующий научным отделом инновационных методов терапевтической онкологии и реабилитации ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России
-
Степанова Александра Михайловна, заведующая отделением реабилитации МНИОИ им. П.А. Герцена - филиала ФГБУ «НМИЦ радиологии» Минздрава России
-
Сукорцева Наталья Сергеевна, ассистент кафедры онкологии, реконструктивной хирургии и радиотерапии, врач онколог Университетской клинической больницы №1 Сеченовского университета
-
Ткаченко Елена Викторовна, к.м.н., заведующий отделением краткосрочной противоопухолевой лекарственной терапии, научный сотрудник научного отдела инновационных методов терапевтической онкологии и реабилитации ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, https://orcid.org/0000-0001-6375-8335
-
Фалалеева Наталья Александровна, заведующий отделом лекарственного лечения злокачественных новообразований МРНЦ им. А.Ф. Цыба- филиал ФГБУ «НМИЦ радиологии» Минздрава России
-
Феденко Александр Александрович, д.м.н., профессор РАН, заведующий Отделом лекарственного лечения опухолей МНИОИ им. П.А. Герцена-филиал ФГБУ «НМИЦ радиологии» Минздрава России
-
Хмелевский Евгений Витальевич, д.м.н., профессор, заведующий отделом лучевой терапии МНИОИ им. П. А. Герцена - филиал ФГБУ «НМИЦ радиологии» Минздрава России, врач-радиотерапевт МНИОИ им. П. А. Герцена - филиал ФГБУ «НМИЦ радиологии» Минздрава России.
-
Ходжибекова Малика Маратовна, д.м.н., врач-радиолог отделения радионуклидной диагностики МНИОИ им. П.А. Герцена – филиал «НМИЦ радиологии» Минздрава России.
-
Цырлина Евгения Владимировна, к.м.н., врач-эндокринолог отделения функциональной диагностики ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России
-
Чойнзонов Евгений Лхамацыренович, д.м.н., профессор, академик РАН, директор НИИ онкологии Томского НИМЦ, заведующий кафедрой онкологии ФГБОУ ВО СибГМУ Минздрава России, член Общероссийской общественной организации «Российское общество специалистов по опухолям головы и шеи»
-
Яковлева Лилия Павловна, к.м.н., врач-онколог, заведующая центром диагностики и лечения опухолей головы и шеи ГБУЗ МКНЦ имени А.С. Логинова МЗ РФБлок Организация оказания медицинской помощи
-
Геворкян Тигран Гагикович, заместитель директора ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России
-
Иванов Сергей Анатольевич, д.м.н., профессор РАН, директор МРНЦ им. А.Ф. Цыба - филиала ФГБУ «НМИЦ радиологии» Минздрава России
-
Невольских Алексей Алексеевич, д.м.н., заместитель директора по лечебной работе МРНЦ им. А.Ф. Цыба – филиала ФГБУ «НМИЦ радиологии» Минздрава России.
-
Хайлова Жанна Владимировна, к.м.н., заместитель директора по организационно-методической работе МРНЦ им. А.Ф. Цыба - филиал ФГБУ "НМИЦ радиологии" Минздрава России.
Приложение А2. Методология разработки клинических рекомендаций
-
Врачи-онкологи
-
Врачи-хирурги
-
Врачи-радиологи
-
Студенты медицинских вузов, ординаторы и аспиранты
Таблица 2.
Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств).
|
УДД
|
Расшифровка
|
|---|---|
|
1
|
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа
|
|
2
|
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа
|
|
3
|
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода, или нерандомизированные сравнительные исследования, в том числе когортные
|
|
4
|
Несравнительные исследования, описание клинического случая
|
|
5
|
Имеется лишь обоснование механизма действия или мнение экспертов
|
Таблица 3.
Шкала оценки уровней достоверности доказательств (для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств).
|
УДД
|
Расшифровка
|
|---|---|
|
1
|
Систематический обзор рандомизированных клинических исследований с применением метаанализа
|
|
2
|
Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа
|
|
3
|
Нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай−контроль»
|
|
5
|
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
|
Таблица 4.
Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств).
|
УУР
|
Расшифровка
|
|---|---|
|
A
|
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
|
|
B
|
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
|
|
C
|
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
|
Порядок обновления клинических рекомендаций
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Приложение Б. Алгоритмы действий врача
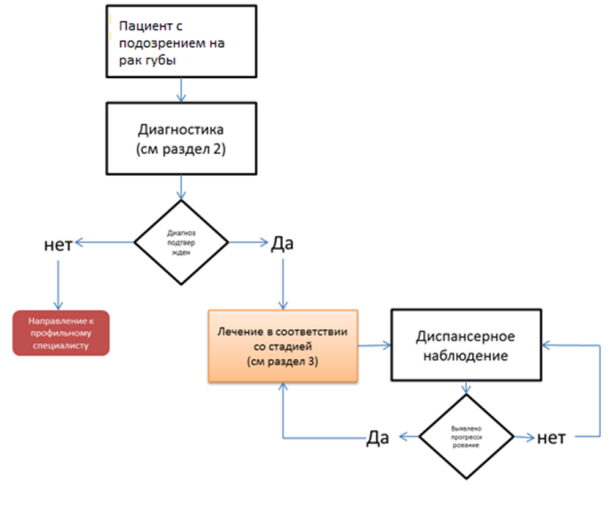
Рекомендации относительно образа жизни и питания должны быть индивидуализированы с учетом объема проведенного лечения, рисков и выраженности осложнений, особенностей пациента.
Преимущества отказа от табакокурения и потребления алкоголя
-
Более высокие показатели выживаемости
-
Большая эффективность лечения
-
Меньшее количество и выраженность побочных эффектов противоопухолевого лечения (сердечно-легочные осложнения, утомляемость, снижение массы тела, мукозиты, потеря вкуса)
-
Ускоренное восстановление общего состояния после лечения
-
Ниже риск рецидива
-
Меньший риск вторых опухолей
-
Меньший риск инфекций
-
Выше качество жизни
При осложнениях химиотерапии/химиолучевой терапии − связаться с врачом-онкологом, врачом-радиологом.
-
При повышении температуры тела до 38 °C и выше:начать прием антибиотиков (J01: Антибактериальные препараты системного действия) по назначению врача
-
При стоматите:диета – механическое, термическое и химическое щажение, а также применение лечебного питания ‒ по рекомендации врача;частое полоскание рта (каждый час) – ромашки аптечной цветки, дуба кора, шалфей лекарственного листья, смазывать рот облепиховым (персиковым) маслом;обрабатывать полость рта по рекомендации врача.
-
При диарее:диета – исключить жирное, острое, копченое, сладкое, молочное, клетчатку. Можно нежирное мясо, мучное, кисломолочное, рисовый отвар. Обильное питье;принимать препараты по назначению врача.
-
При тошноте:Принимать препараты по назначению врача.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1.
|
Баллы
|
Состояние больного
|
|---|---|
|
0
|
Больной полностью активен, способен выполнять все, как и до заболевания (90 - 100% по шкале Карновского)
|
|
1
|
Больной не способен выполнять тяжелую, но может выполнять легкую или сидячую работу (например, легкую домашнюю или канцелярскую работу, 70 - 80% по шкале Карновского)
|
|
2
|
Больной лечится амбулаторно, способен к самообслуживанию, но не может выполнять работу. Более 50% времени бодрствования проводит активно - в вертикальном положении (50 - 60% по шкале Карновского)
|
|
3
|
Больной способен лишь к ограниченному самообслуживанию, проводит в кресле или постели более 50% времени бодрствования (30 - 40% по шкале Карновского)
|
|
4
|
Инвалид, совершенно не способен к самообслуживанию, прикован к креслу или постели (10 - 20% по шкале Карновского)
|
|
5
|
Смерть
|
Приложение Г2.
|
Таблица 1. Начальный скрининг
|
|||
|---|---|---|---|
|
1
|
ИМТ < 20,5 кг/м2?
|
Да/нет
|
|
|
2
|
Была ли у пациента потеря массы тела за последние 3 месяца?
|
Да/нет
|
|
|
3
|
Уменьшилось ли потребление пищи пациентом за последнюю неделю?
|
Да/нет
|
|
|
4
|
Есть ли у пациента тяжелое заболевание?
|
Да/нет
|
|
|
Да: Если при ответе на вопросы таблицы 1 получен хотя бы один положительный ответ, необходимо перейти к вопросам таблицы 2.
Нет: Если при ответе на вопросы таблицы 1 получены все отрицательные ответы, необходимо еженедельно проводить повторный скрининг
|
|||
|
Таблица 2. Финальный скрининг
|
|||
|
Степень тяжести нарушений пищевого статуса
|
Тяжесть заболевания (~ повышение потребности организма в белке и нутриентах)
|
||
|
0 баллов
|
Нормальный пищевой статус
|
0 баллов
|
Обычные потребности организма в белке и нутриентах
|
|
Легкая степень
1 балл
|
снижение массы тела > 5% за 3 мес. или прием пищи менее 50 - 75% от обычного объема на предшествующей неделе
|
Легкая степень
1 балл
|
Перелом бедра, пациенты с хроническими заболеваниями, особенно с осложнениями в острой фазе: цирроз печени, ХОБЛ, хронический гемодиализ, диабет, онкология
|
|
Средняя степень
2 балла
|
снижение массы тела > 5% за 2 мес. или ИМТ 18,5 - 20,5 + нарушение общего состояния пациента
или прием пищи менее 50 - 75% от обычного объема на предшествующей неделе
|
Средняя степень
2 балла
|
Большая абдоминальная хирургическая операция, инсульт, тяжелая пневмония, злокачественные гематологические опухоли
|
|
Тяжелая степень
3 балла
|
снижение массы тела > 5% за 1 мес. (> 15% за 3 мес.) или ИМТ < 18,5 + нарушение общего состояния пациента или прием пищи 0 - 25% от обычного объема на предшествующей неделе
|
Тяжелая степень
3 балла
|
Травма головы, пересадка костного мозга, пациенты, находящиеся в ОРИТ
|
Клиническая интерпретация степеней тяжести заболевания
2 балла: пациент находится на постельном режиме из-за заболевания, например, после проведенного хирургического вмешательства на брюшной полости. Потребность в белке в значительной степени повышена, однако может быть покрыта за счет применения специализированных продуктов питания и искусственного питания;
3 балла: пациент находится в ОРИТ на ИВЛ и другие тяжелые состояния. Потребности в белке максимально увеличены и не могут быть покрыты с помощью клинического (искусственного) питания. Значительно усилен распад белка и потеря азота.
Общий балл = баллы за степень тяжести нарушений пищевого статуса + баллы за тяжесть заболевания.
Если возраст 70 лет и старше, добавить 1 балл.
Ключ (интерпретация)
Менее 3 баллов - еженедельная оценка. Если планируется большое оперативное вмешательство, обсуждается превентивный план нутритивной поддержки.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.