Желудочковые аритмии: протокол диагностики и лечения
 Версия: Клинические протоколы 2024 (Узбекистан)
Версия: Клинические протоколы 2024 (Узбекистан)
Возвратная желудочковая аритмия (I47.0), Другая и неуточненная преждевременная деполяризация (I49.4), Другие нарушения сердечного ритма (I49), Другие уточненные нарушения сердечного ритма (I49.8), Желудочковая тахикардия (I47.2), Нарушение сердечного ритма неуточненное (I49.9), Остановка сердца (I46), Пароксизмальная тахикардия (I47), Пароксизмальная тахикардия неуточненная (I47.9), Преждевременная деполяризация желудочков (I49.3), Фибрилляция и трепетание желудочков (I49.0)
Кардиология
Общая информация
Краткое описание
Приложение
к приказу № 107
от 29 марта 2024 года
Министерства здравоохранения Республики Узбекистан
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ УЗБЕКИСТАН
РЕСПУБЛИКАНСКИЙ СПЕЦИАЛИЗИРОВАННЫЙ НАУЧНО-ПРАКТИЧЕСКИЙ МЕДИЦИНСКИЙ ЦЕНТР КАРДИОЛОГИИ
НАЦИОНАЛЬНЫЕ КЛИНИЧЕСКИЕ ПРОТОКОЛЫ ПО НОЗОЛОГИИ «СИНДРОМ ЖЕЛУДОЧКОВЫХ АРИТМИЙ»
НАЦИОНАЛЬНЫЕ КЛИНИЧЕСКИЕ ПРОТОКОЛЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ ПО НОЗОЛОГИИ «ЖЕЛУДОЧКОВЫЕ АРИТМИИ»
Коды по МКБ-10:
| Код | Название |
| I 46 | Остановка сердца |
| I 46.0 | Остановка сердца с успешным восстановлением сердечной деятельности |
| I 46.1 | Внезапная сердечная смерть, так описанная |
| I 46.9 | Остановка сердца неуточненная |
| I 47 | Пароксизмальная тахикардия |
| I 47.0 | Возвратная желудочковая аритмия |
| I 47.2 | Желудочковая тахикардия |
| I 47.9 | Пароксизмальная тахикардия неуточненная |
| I 49 | Другие нарушения сердечного ритма |
| I 49.0 | Фибрилляция и трепетание желудочков |
| I 49.3 | Преждевременная деполяризация желудочков |
| I 49.4 | Другая и неуточненная деполяризация |
| I 49.8 | Другие уточненные нарушения сердечного ритма |
| I49.9 | Нарушение сердечного ритма неуточненное |
Введение
На сегодняшний день, несмотря на применение современных передовых методов лечения и диагностики сердечно-сосудистых заболеваний во всем мире, уровень смертности от инфаркта миокарда (ИМ) и его осложнений остается высоким. По данным Всемирной организации здравоохранения (ВОЗ), в 2019 году во всем мире было зарегистрировано 18,6 миллиона смертей от сердечно - сосудистых заболеваний (ИБС), причем 85% из них были вызваны инфарктом миокарда (ИМ) и инсультом. Несомненно, наиболее частым клиническим состоянием является ИМ. От 25% до 50% пациентов, перенесших ИМ, умирают из-за желудочковой тахикардии или фибрилляции желудочков, приводящей к внезапной аритмической смерти (ВСС). Во всем мире в течение года происходит около 6 миллионов внезапных остановок сердца (ВОС) с вероятностью выживания не более 10%. ВСС - это состояние, связанное с сердцем, которое проявляется в виде потери сознания в течение 1 часа после появления естественных острых клинических симптомов без внешних воздействий и заканчивается летальным исходом. В этом случае болезнь сердца может быть известна или неизвестна заранее, но смерть всегда наступает неожиданно. Ситуация усугубляется тем фактом, что ВСС как социальная проблема возникает внезапно, смерть наступает после первых клинических признаков (6-10 минут) в течение определенного периода времени, и в большинстве случаев наблюдается во сне и без свидетелей, а также ограниченными возможностями оказания неотложной помощи.
Желудочковые нарушения ритма сердца (ЖНРС) или Желудочковая тахиаритмия (ЖТА) – обобщенное название расстройств сердечного ритма, при которых источник эктопической активности или круга риентри находится ниже пучка Гиса, т. е. в его ветвях, сети Пуркинье или в миокарде желудочков.
Дата разработки и пересмотра протокола: 2023 год, дата пересмотра 2026 г. или по мере появления новых ключевых доказательств. Все поправки к представленным рекомендациям будут опубликованы в соответствующих документах.
Ответственное учреждение по разработке данного клинического протокола и стандарта: Республиканский специализированный научно-практический медицинский центр кардиологии (РСНПМЦК)
Пользователи протокола:
1. Кардиологи;
2. Терапевты;
3. Врачи общей практики;
4. Врачи скорой и неотложной помощи;
5. Врачи-лаборанты;
6. Организаторы здравоохранения;
7. Клинические фармакологи;
8. Студенты, клинические ординаторы, магистранты, аспиранты, преподаватели медицинских вузов;
Категории пациентов: больные с сердечно - сосудистыми заболеваниями, в частности заболеваний АГ, ИБС, ОИМ, кардиомиопатии осложнённые нарушением ритма сердца.
Классификация
Классификации желудочковых аритмий
Классификация ЖА по данным ЭКГ (ESC/ACC/AHA, 2006)
ЖЭ (одиночные, парные, мономорфные, полиморфные).
ЖТ:
- неустойчивая ЖТ (3 и более ЖЭ подряд длительностью не более 30 сек);
- устойчивая ЖТ (продолжительностью более 30 сек или требует купирования вследствие гемодинамических нарушений);
фасцикулярная левожелудочковая тахикардия;
полиморфная ЖТ типа «пируэт» («torsade de pointes»);
Двунаправленная ЖТ
ТЖ;
ФЖ.
Классификация ЖЭ В.Lown и M.Wolf (1971.)
1. Редкие одиночные мономорфные экстрасистолы <30 ЖЭ/час:
- 1А – <1 ЖЭ/мин
- 1В – >1 ЖЭ/мин
2. Частые одиночные мономорфные экстрасистолы >30 ЖЭ/час
3. Полиморфные экстрасистолы
4. Повторные формы ЖА:
- 4А – парные (куплеты)
- 4В – групповые (залпы), включающие короткие эпизоды ЖТ
5. Ранние ЖЭ – типа «R на T».
Классификация желудочковых нарушений ритма по J.T. Bigger (1984г).
Доброкачественные – неустойчивые нарушения ритма сердца, отсутствие органической патологии сердца.
Потенциально злокачественные – неустойчивые нарушения ритма сердца, наличие органической патологии сердца.
Злокачественные – устойчивые пароксизмы ЖТ, ТЖ или ФЖ на фоне органической патологии миокарда (высокий риск ВСС).
По частоте сердечных сокращений в минуту:
По продолжительности тахикардии:
По характеру клинического течения тахикардии:
По этиологии (наличие или отсутствие основного структурного заболевания сердца):
На практике с диагностической и прогностической целью удобно выделять следующие виды ЖА:
По частоте сердечных сокращений в минуту:
От 51 до 100 – ускоренный идиовентрикулярный ритм.
От 100 до 250 – ЖТ.
Свыше 250 – ТЖ и ФЖ.
По продолжительности тахикардии:
Устойчивая – длительностью >30 сек.
Неустойчивая – длительностью <30 сек.
По характеру клинического течения тахикардии:
Пароксизмальные
Непароксизмальные (непрерывно рецидивирующие/некупирующиеся ЖТ и электрический шторм)
По этиологии (наличие или отсутствие основного структурного заболевания сердца):
Идиопатические желудочковые аритмии при отсутствии структурного заболевания сердца («доброкачественные»).
Большое значение для клинической практики имеет риск-стратификация ЖНРС.
Таблица 3. Классификация желудочковых аритмий Lown-Wolf (1971)
Желудочковые аритмии при отсутствии явного структурного заболевания сердца при наличии врожденных синдромов или т. н. каналопатий – «злокачественные»: синдром удлиненного интервала QT, синдром Бругада, катехоламинзависимая полиморфная желудочковая тахикардия, синдром короткого интервала QT, синдром ранней реполяризации желудочков.
Желудочковые аритмии при отсутствии явного структурного заболевания сердца при наличии обратимых метаболических или лекарственных причин (например, вторичный синдром удлиненного интервала QT).
Желудочковые аритмии при наличии структурного заболевания сердца.
Большое значение для клинической практики имеет риск-стратификация ЖНРС.
Таблица 3. Классификация желудочковых аритмий Lown-Wolf (1971)
| Критерии стратификации риска | Доброкачественные ЖА | Потенциально злокачественные ЖА | Злокачественные ЖА |
| Риск ВСС |
Низкий
|
Средний | Высокий |
| Клиника | Сердцебиение | Сердцебиение | Сердцебиение и синкопальные состояния |
| Органическое поражение сердца | Нет | Есть | Есть |
| Желудочковая экстрасистолия | Редкая или средняя | Средняя или частая | Средняя или частая |
| Парная ЖЭ или ЖТ | Обычно нет | Неустойчивая ЖТ | Устойчивая ЖТ |
| Цель лечения | Уменьшение симптомов | Уменьшение симптомов, снижение летальности | Снижение летальности, подавление аритмии, уменьшение симптомов |
Диагностика
Диагностика
Жалобы:
ощущение неправильного ритма сердца; сердцебиение, которое сопровождается головокружением, слабостью, одышкой, болями в области сердца, перебоями, паузами в сокращениях сердца, эпизодами потери сознания.
Анамнез:
Наличие в анамнезе АГ, ИБС, ХСН, заболевания периферических артерий. У большинства из больных при сборе анамнеза находят различные заболевания миокарда. Пациенты обычно имеют тяжелое заболевание сердца, которое может еще осложниться комплексной желудочковой эктопией (состоящей из частых ЖЭ, неустойчивых ЖТ или тех и других вместе). При выяснении наследственности важно обратить внимание больного на наличие случаев необъяснимой внезапной смерти родственников молодого возраста, а также наличие в семье родственников, страдающих ЖА, имеющих имплантируемые кардиоустройства.
Физикальное обследование:
Всем обследуемым пациентам рекомендуется проводить следующие стандартные измерения, в соответствии с действующими рекомендациями:
антропометрические показатели (рост, вес, индекс массы тела, окружность талии);
термометрия и оценка состояния кожных покровов;
оценка наличия отеков и их распространенности;
определение уровня систолического и диастолического АД;
пальпация пульса на периферических артериях с оценкой частоты и регулярности ритма;
оценка набухания и пульсации шейных вен, что может свидетельствовать о наличии венозного застоя;
аускультация сердца, сонных, почечных и бедренных артерий для выявления патологических шумов;
пальпация щитовидной железы: размеры, болезненность, подвижность.
В дополнение к основным показателям рекомендовано оценивать специфические изменения с целью исключения обратимых причин, которые потенциально могут быть ассоциированы с желудочковыми нарушениями ритма.
Выявление признаков гемодинамической нестабильности (снижения артериального давления) рекомендовано при физикальном обследовании пациентов с пароксизмальными нарушениями ритма сердца.
При подавляющем большинстве ЖНРС при физикальном обследовании пациентов вне пароксизма какие-либо изменения не отмечаются. Экстрасистолы могут быть отмечены при подсчёте пульса, измерении артериального давления или аускультации сердца пациента.
При частой ЖЭ аускультативно выявляется аритмичная сердечная деятельность, наличие дефицита пульса. При приступе ЖТ при пальпации пульса отмечается частый (от 100 до 220 в 1 мин) и в основном правильный ритм, наличие патологических шумов, признаков сердечной недостаточности (хрипы в легких, ритм галопа), снижение АД вплоть до отсутствия пульсации периферических артерий и исчезновения АД и сердечных тонов при переходе ЖТ в ФЖ. В случае ВСС наблюдается следующее: через 15-20 секунд от начала ФЖ больной теряет сознание; через 40-50 секунд – развивается однократное тоническое сокращение скелетных мышц; расширяются зрачки; дыхание урежается и прекращается через 2-4 мин.
Лабораторные исследования: позволяют выявить факторы риска развития ЖА (электролитные нарушения, эндокринные заболевания, анемические состояния), наличие дислипидемии при клинике ИБС, состояние свертывающей системы крови при приеме антикоагулянтов.
Дополнительные лабораторные исследования проводятся в зависимости от коморбидного фона.
Основные инструментальные методы исследования:
Лабораторные исследования: позволяют выявить факторы риска развития ЖА (электролитные нарушения, эндокринные заболевания, анемические состояния), наличие дислипидемии при клинике ИБС, состояние свертывающей системы крови при приеме антикоагулянтов.
Основные лабораторные исследования:
Общий анализ крови - проводится при впервые диагностируемых ЖА, ежегодно и при ухудшении состояния больного.
Общий анализ мочи – проводится при впервые диагностируемых ЖА, ежегодно и при ухудшении состояния больного.
Определение глюкозы натощак – проводится при впервые диагностируемых ЖА, ежегодно и при ухудшении состояния больного.
Биохимическое исследование крови (билирубин, ACT, АЛТ, креатинин) – проводится при впервые диагностируемых ЖА, ежегодно и при ухудшении состояния больного.
Калий и натрий крови – определяются при впервые диагностируемых ЖА, ежегодно и при ухудшении состояния больного.
Гормоны щитовидной железы (ТТГ, Т3 свободный, Т4 свободный, антиТПО) – исследуются при впервые диагностируемых ЖА, при лечении амиодароном ежегодно, при ухудшении состоянии вероятно обусловленном приемом амиодарона.
Липидный спектр (общий холестерин, ЛПВП, ЛПНП, коэффициент атерогенности, триглицериды) – исследуется при впервые диагностируемых ЖА, ежегодно и при ухудшении состояния больного.
Коагулограмма (по показаниям – при предшествующем приеме антикоагулянтов, патологии свертывающей системы крови в анамнезе (кровотечения/тромбозы)
Тест толерантности к глюкозе (по показаниям – при наличии признаков абдоминального ожирения, АГ, дислипидемии)
Гликолизированный гемоглобин (по показаниям – при наличии гипергликемии натощак более 5,6 ммоль/л, признаков метаболического синдрома)
Дополнительные лабораторные исследования проводятся в зависимости от коморбидного фона.
Инструментальные исследования
Основные инструментальные методы исследования:
1. ЭКГ стандартная 12-канальная.
ЖЭ – преждевременное сокращение, перед которым отсутствует зубец Р, комплекс QRS по продолжительности 0,12 с и более, по форме напоминает блокаду ножки пучка Гиса, противоположной стороне возникновения экстрасистолы. Расположение сегмента ST и зубца Т экстрасистолы дискордантно направлению основного зубца комплекса QRS'. Вслед за ЖЭ возникает полная компенсаторная пауза (дополняет интервал сцепления ЖЭ до удвоенного RR основного ритма), исключая случаи вставочных ЖЭ при редком ритме, при котором интервал RR не нарушается. К сложным формам ЖЭ относятся парные, политопные, ранние («R на T») ЖЭ, а также аллоритмия.
ЖТ – участок ритма на ЭКГ из трех и более эктопических комплексов с ЧСС обычно в пределах 140-220 в мин, комплексы QRS при этом широкие, деформированные, более 0,12 с, напоминающие блокаду ножек пучка Гиса с дискордантным расположением сегмента ST и зубца T. Наличие АВ-диссоциации – полного разобщения частого ритма желудочков (комплексов QRS') и нормального синусового ритма предсердий (зубцов Р') с изредка регистрирующимися одиночными неизмененными комплексами QRST синусового происхождения («захваченные» сокращения желудочков).
Полиморфная ЖТ типа «пируэт» - частота желудочкового ритма составляет 150-250 в мин, ритм неправильный с колебаниями интервалов R-R в пределах 0,2-0,3 с. Комплексы QRS широкие, деформированные, большой амплитуды, их продолжительность превышает 0,12 с. Амплитуда и полярность желудочковых комплексов меняется в течение короткого времени.
ТЖ – на ЭКГ регистрируются ритмичные высокоамплитудные расширенные электрические отклонения желудочков, напоминающие синусоидальную кривую, с частотой 200-300 в минуту, зубцы Т не определяются, изолиния не регистрируется.
ФЖ – частые (до 200-500 в мин), но нерегулярные беспорядочные волны, отличающиеся друг от друга различной формой и амплитудой, без определяющихся зубцов.
2. ХМЭКГ 3- или 12-канальное (суточное или многосуточное). Позволяет не только выявить наличие ЖА соответственно указанным выше ЭКГ-критериям, но и определить их плотность, суточное распределение, связь с ощущениями пациента, при совместной регистрации с монитором измерения АД – возможно выявить факт падения АД в момент аритмии. Также возможно осуществлять оценку эффекта лекарственной терапии АПП, работу имплантированных кардиоустройств.
4. Проба с физической нагрузкой – по показаниям проводятся тредмил-тест/ВЭМ; имеет большое значение в провокации ЖА коронарогенного происхождения и, наоборот, уменьшение числа идиопатических ЖЭ при физической нагрузке. Тредмил-тест/ВЭМ позволяют спровоцировать желудочковые тахиаритмии, которые не удается диагностировать при использовании ХМЭКГ или электростимуляции сердца (например, катехоламинергическая ЖТ). Нагрузочные тесты не используются для провокации ЖА при синдроме WPW. Нагрузочные пробы проводятся по показаниям при оснащении кабинета функциональной диагностики амбулаторного звена средствами для оказаниям реанимационной помощи).
5. УЗДГ сосудов шеи и экстракраниальных артерий проводится по показаниям для дифференциальной диагностики синкопальных состояний, в случае трудности ЭКГ-выявления пароксизмов ЖА.
6. ЧПЭФИ проводится по показаниям для поиска ДППЖС; дифференциальной диагностики тахикардий с широкими комплексами QRS во время приступа, зарегистрированного при амбулаторном обращении пациента.
Дополнительные инструментальные методы исследования проводятся в зависимости от коморбидного фона.
2. ХМЭКГ 3- или 12-канальное (суточное или многосуточное). Позволяет не только выявить наличие ЖА соответственно указанным выше ЭКГ-критериям, но и определить их плотность, суточное распределение, связь с ощущениями пациента, при совместной регистрации с монитором измерения АД – возможно выявить факт падения АД в момент аритмии. Также возможно осуществлять оценку эффекта лекарственной терапии АПП, работу имплантированных кардиоустройств.
3. ЭхоКГ трансторакальная в целях уточнения характера первичного заболевания сердца, характеристики состояния миокарда левого желудочка и межжелудочковой перегородки, определения наличия и распространенности зон а- и дискинезии в левом желудочке, его фракции выброса, структуры миокарда правого желудочка, клапанной патологии, наличия врожденных и приобретенных пороков сердца. В случае развития идиопатических ЖА при проведении ЭхоКГ может не выявляться структурных аномалий сердца.
4. Проба с физической нагрузкой – по показаниям проводятся тредмил-тест/ВЭМ; имеет большое значение в провокации ЖА коронарогенного происхождения и, наоборот, уменьшение числа идиопатических ЖЭ при физической нагрузке. Тредмил-тест/ВЭМ позволяют спровоцировать желудочковые тахиаритмии, которые не удается диагностировать при использовании ХМЭКГ или электростимуляции сердца (например, катехоламинергическая ЖТ). Нагрузочные тесты не используются для провокации ЖА при синдроме WPW. Нагрузочные пробы проводятся по показаниям при оснащении кабинета функциональной диагностики амбулаторного звена средствами для оказаниям реанимационной помощи).
5. УЗДГ сосудов шеи и экстракраниальных артерий проводится по показаниям для дифференциальной диагностики синкопальных состояний, в случае трудности ЭКГ-выявления пароксизмов ЖА.
6. ЧПЭФИ проводится по показаниям для поиска ДППЖС; дифференциальной диагностики тахикардий с широкими комплексами QRS во время приступа, зарегистрированного при амбулаторном обращении пациента.
Дополнительные инструментальные методы исследования проводятся в зависимости от коморбидного фона.
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований
Чаще всего дифференциальный диагноз проводится по наличию синдрома пароксизмального расстройства ритма либо по синдрому утраты сознания. Наиболее трудным вопросом является дифференциальная диагностика тахиаритмий с широкими комплексами QRS, которые иногда возможно различить с аберрантными комплексами при НЖТ только при проведении электрофизиологического исследования. В таблицах ниже сводные данные по основным электрокардиологическим и клиническим диагнозам, которые необходимо рассматривать при дифференциальной диагностике жизнеугрожающих ЖА
Таблица 4. Основные методы обследования, применяемые при ЖА*
|
Наименование исследования
|
Кто будет переведен |
Учреждение
|
УДД | Источник |
| ЭКГ | Kардиолог | Всех степенях МЗ | I A | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| ХМЭКГ | Функционалый кардиолог | Район, область, Республика | I В | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| Тредмил тест | Функционалый кардиолог | Район, область, Республика | I В | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| ЭХОКГ | Функционалый кардиолог | Район, область, Республика | I В | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| Электрофизиологические исследования | Электрофизиолог | Республика | IIа C | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
*- Эти обследования проводятся наряду с основными обследованиями при заболеваниях.
Таблица 5. Дифференциальная диагностика пароксизмальных аритмий по ЭКГ-критериям
|
Диагноз
|
Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| ЖТ | Ширококомплексные пароксизмальные тахикардии | ЭКГ, ХМЭКГ, ЧПЭФИ, ВСЭФИ | Трудно выделяемые желудочковые комплексы, частое отсутствие изоэлектрического интервала, наличие сливных, захваченных комплексов, АВ- диссоциации. Положительный критерий Верекей – высокий з. R в aVR. |
| НЖТ с БНПГ | Ширококомплексные пароксизмальные тахикардии | ЭКГ, ХМЭКГ, ЧПЭФИ, ВСЭФИ | На ЭКГ часто присутствует з. Р разнообразной морфологии, отсутствуют сливные и захваченные комплексы во время приступа, нет АВ- диссоциации. На ХМЭКГ вне приступа возможно разрешение БНПГ с возвращением желудочковому комплексу обычной морфологии. |
| НЖТ при WPW | Ширококомплексные пароксизмальные тахикардии | ЭКГ, ХМЭКГ, ЧПЭФИ, ВСЭФИ | На ЭКГ покоя вне приступа наличие дельта-волны, укорочение интервала PQ менее 0,12 с, деформация и расширение QRS комплекса. Наличие ДПЖС при ЧПЭФИ, ВСЭФИ. |
| ФП/ТП | Пароксизмальная форма с высокой ЧСЖ | ЭКГ, ХМЭКГ, ЧПЭФИ, ВСЭФИ | Неправильный ритм на ЭКГ/ХМЭКГ при ФП с ЧСЖ 75-180 в мин, частотой предсердных сокращений до 300-600 в мин, отсутствие з. Р, волны f, различная амплитуда з. R. При ТП возможно наличие правильного ритма (при правильной форме проведения), пилообразные волны F, ЧСЖ 75-170 в мин. |
| АВ-блокада | Внезапная потеря сознания | ЭКГ, ХМЭКГ, ЧПЭФИ, ВСЭФИ | Постепенное удлинение/фиксированный удлиненный интервал PQ, периодическое выпадение комплекса QRSТ, при полной АВ-блокаде – разобщенный ритм предсердий и водителей ритма II или III порядка. |
| СССУ | Внезапная потеря сознания, приступы пароксизмальных тахикардий. | ЭКГ, ХМЭКГ, ЧПЭФИ, ВСЭФИ | Эпизоды выпадения комплексов PQRSТ, возможно с замещающими ритмами и комплексами, эпизоды sinus arrest. На ХМЭКГ возможно наличие эпизодов тахикардии- брадикардии. |
| СУИQT | Внезапная потеря сознания, приступы пароксизмальных тахикардий | ЭКГ, ХМЭКГ | Удлинение интервала QTc свыше 0,44 с без изменений во время нагрузки, учащении ЧСС. Угроза развития полиморфной ЖТ типа «пируэт». |
Таблица 6. Дифференциальная диагностика пароксизмальных аритмий по клиническим данным
|
Диагноз
|
Обоснование для дифференциальной диагностики | Обследование | Критерии исключения диагноза |
| Эпилепсия | Внезапная потеря сознания | КТ/МРТ головного мозга, ЭЭГ, осмотр невролога. | Отсутствие расстройств ритма на ЭКГ/ХМЭКГ. Наличие специфических признаков по данным ЭЭГ, лучевых методов диагностики. |
| ОНМК/ТИА | Внезапная потеря сознания | КТ/МРТ головного мозга, осмотр невролога. | Отсутствие расстройств ритма на ЭКГ/ХМЭКГ. Наличие специфических признаков по данным лучевых методов диагностики. |
| Тяжелый стеноз отверстия аортального клапана. | Внезапная потеря сознания | ЭхоКГ | Ограничение площади отверстия аортального клапана менее 1 см2, макс. градиент давления >65 мм рт. ст., средний – >50 мм рт. ст. |
| ГКМП с обструкцией ВТЛЖ | Внезапная потеря сознания, приступы пароксизмальных тахикардий | ЭхоКГ | На ЭхоКГ выявляется массивная (>15 мм) гипертрофия миокарда левого желудочка, отношение толщины МЖП к ЗСЛЖ >1,3. Градиента давления в ВТЛЖ >45 мм рт ст. |
| Простой вазовагальный обморок | Внезапная потеря сознания | СМАД, тилт-тест, кардиоритмография с вегетативными тестами. | Отсутствие расстройств ритма на ЭКГ/ХМЭКГ. Эпизоды гипотонии по СМАД в утренние часы, при ортостазе. Кардиоингибиторный (с асиситолией или без нее), смешанный типы ответов при тилт-тесте. |
| Синдром гиперчувствительности каротидного синуса | Внезапная потеря сознания | Массаж каротидного синуса под контролем АД, ритмограммы. | Отсутствие расстройств ритма на ЭКГ/ХМЭКГ, кардиоингибиторный (с асистолией), вазодепрессорный или смешанный тип ответа на пробу. |
| Психиатрические заболевания | Внезапная потеря сознания или имитация такового | Осмотр психиатра | Отсутствие расстройств ритма на ЭКГ/ХМЭКГ. Специфические признаки психических расстройств, частые падения с обилием жалоб и отсутствием физикальных отклонений. |
| Медикаментозно- индуцированная гипотония | Внезапная потеря сознания | СМАД | Чаще возникает у пожилых пациентов при приеме полнодозовой комбинированной антигипертензивной терапии, связана с недавним приемом очередной дозы лекарств, на СМАД определяется избыточное снижение АД после приема препарата; провоцируется чаще в утренние часы при подъеме с постели после ночного сна. |
Лечение (амбулатория)
Тактика лечения на амбулаторном уровне
Немедикаментозное лечение
Немедикаментозное (без медикаментозного) лечение (элементы здорового образа жизни, правильное-альтернативное питание, режим дня и сна, диета) проводится у пациентов по основному заболеванию, которое привело к данной патологии.
Таблица 8. Дополнительные антиаритмические препараты для купирования ЖТ
Хирургические способы лечения в амбулаторных условиях не проводятся.
Медикаментозное лечение
В целях мониторинга и контроля безопастоности медикаментозной терапии в амбулаторных условиях необходимо вести динамическое наблюдение индивидуально по каждому принимаемому препарату (в частности, контроль интервала QT/QTc при приеме антиаритмических препаратов III группы, динамическое увеличение ширины QRS при приеме препаратов I С группы), ЭКГ, ЭКГ, суточную ХМЭКГ, содержание калия в крови, контроль функции почек и исследования, специфичные для основного заболевания. Пациенты с имплантируемыми устройствами регулярно обследуются на работоспособность устройства в специализированных центрах 3 раза за первый год лечения и 2 раза за 2 года.
Каждый из известных противоаритмических препаратов обладает одним из представленных выше эффектов в качестве доминирующего, что позволяет отнести его к тому или иному классу.
Основные медикаментами в лечении ЖНР являются антиаритмические средства. В настоящее время принята классификация противоаритмических препаратов по E.M.Vaughan Williams в модификации B. N. Singh и D. C. Harrison. Эта классификация позволяет разделить все известные в настоящее время противоаритмические препараты на 4 класса, в зависимости от их способности:
1. угнетать деполяризацию (фазу 0 потенциала действия) в тканях с «быстрым» ответом;
2. блокировать симпатические влияния на сердце;
3. увеличивать продолжительность потенциала действия, замедляя процессы реполяризации;
4. замедлять деполяризацию в тканях с «медленным» ответом.
Каждый из известных противоаритмических препаратов обладает одним из представленных выше эффектов в качестве доминирующего, что позволяет отнести его к тому или иному классу.
1. Антиаритмические препараты I класса (препараты, блокирующие натриевые каналы).
2. Бета-адреноблокаторы: антиаритмические препараты II класса.
3. Антиаритмические препараты III класса: препараты, блокирующие калиевые каналы.
4. Блокаторы «медленных» кальциевых каналов: антиаритмические препараты IV класса.
Таблица 7. Основные антиаритмические препараты для длительной терапии с целью профилактики желудочковой экстрасистолии и рецидива ЖТ
| Фармако-терапевтическая группа | Международное название препарата | Способ применения |
УДД
|
Источник |
| III группа антиаритических препаратов | Амиодарон | 200 мг 3 раза в день в течение 1 недели, далее 200 мг по 2 раза в день в течение 1-2 недели, после перейти на поддерживающую дозу по 200 мг в сутки | I A (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| Соталол* |
80-120 мг 2 раза в сутки
Максимальная доза 320 мг в сутки
|
IIa C (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ | |
| II группа антиаритических препаратов | Атенолол | 25-100 мг 1-2 раза в день | I A (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| бисопролол | 2,5-10 мг 1 разв день | I A (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ | |
| карведилол | 3,125-25 мг 2 раза в день | I A (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ | |
| Метопролол | 25-100 мг 1-2 раза в день | I A (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ | |
| Пропанолол | 10-40 мг 4 раза в день | I A (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ | |
| I В группа антиаритмических препаратов | Фенитоин* | 400-600 мг в сутки | III C (1) | https://pubmed.ncbi.nlm.nih.gov/26320108/ |
| I С группа антиаритмических препаратов | Пропафенон | 150-300 мг 1 таблетка 3 раза в день | IIb B (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| Аллапинин | 25-50 мг 3 раза в день | IIb B (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ | |
| Этацизин | 25-100 мг 3 раза в день | IIb C (1) | https://pubmed.ncbi.nlm.nih.gov/26320108/ | |
| IV гурух антиаритмических препаратов | Верапамил | 240-480 мг/сут. | IIb B (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| Дилтиазем* | 120-360 мг/сут | IIb C (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
* - на момент 2023 г. данные препараты не зарегистрированы в Узбекистане. В скобках указаны ссылки на литературный источник.
Таблица 8. Дополнительные антиаритмические препараты для купирования ЖТ
|
Фармако-терапевтическая группа
|
Международное название препарата | Способ применения | УДД | Источник |
| Препараты калия |
Калия хлорид 4% -10 мл
или
препараты, содержащие калий
|
в/в на дозаторе или в инфузии раствором глюкозы, максимальная суточная доза 100 мл/сут, по 1 таблетке 3 раза в день под контролем концентрации калия в крови | III C (2) | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| Препараты магния |
Магния сулфат 25% -10 мл,
Магния цитрат 400 мг,
Препараты, содержащие магний
|
в/в на дозаторе или в инфузии раствором глюкозы, максимальная суточная доза 100 мл/сут,
по 1 таблетке 3 раза в день под контролем концентрации магния в крови
|
III В (2) | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
Хирургические способы лечения в амбулаторных условиях не проводятся.
Лечение (стационар)
Тактика медикаментозной терапии на стационарном уровне
Важнейшим условием успешного лечения ЖА и предотвращения ВСС является эффективное лечение основного заболевания сердца и сопутствующих заболеваний. ИБС является основной патологией сердца, являющейся причиной ЖТА и ВСС. Лечение основного заболевания, являющегося причиной возникновения ЖТА и ВСС, должно осуществляться в соответствии с действующими КР по рассматриваемым заболеваниям/состояниям.
Таблица 9. Основные антиаритмические препараты лечения желудочковой экстрасистолии, ЖНР и ЖТ в условиях стационара
|
Фармако-терапевтическая группа
|
Международное название препарата | Способ применения | УДД | Источник |
| III группа антиаритмических препаратов | Амиодарон |
200 мг 3 раза в день в течение 1 недели, далее 200 мг по 2 раза в день в течение 1-2 недели, после перейти на поддерживающую дозу по 200 мг в сутки,
При неустойчивой гемодинамике в/в струйно 5 мг/кг в течение 15-20 мин, сўнгра в/в капельно: 1 мг/мин — 6 часов, затем по 0,5 мг/мин — 18 часов (до 1200 мг в сутки)
|
I A (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| Соталол* |
80-120 мг 2 раза в сутки
Максимальная доза 320 мг в сутки
|
IIa C (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ | |
| II группа антиаритмических препаратов | Атенолол | 25-100 мг 1-2 раза в день | I A (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| бисопролол | 2,5-10 мг 1 разв день | I A (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ | |
| карведилол | 3,125-25 мг 2 раза в день | I A (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ | |
| Метопролол | 25-100 мг 1-2 раза в день | I A (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ | |
| Пропанолол | 10-40 мг 4 раза в день | I A (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ | |
| I A группа антиаритмических препаратов | Прокаинамид* | в/в струйно по 10-17 мг/кг в течение 20-50 мин, затем при необходимости в/в капельно по 1-4 мг/мин. | IIb B (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| I В группа антиаритмических препаратов | Фенитоин* | 400-600 мг/сут | III C (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| Лидокаин | 1-2 мг/кг в/в (100-200 мг) в течение 3-5 мин, при необходимости продолжать в дозе 1-4 мг/мин в/в капельно | IIb B (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ | |
| I С группа антиаритмических препаратов | Пропафенон | 150-300 мг по 1 таблетке 3 раза в день | IIb B (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| Аллапинин | 25-50 мг 3 раза в день | IIb B (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ | |
| Этацизин | 25-100 мг по 1 таблетке 3 раза в день | IIb С (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ | |
| IV группа антиаритмических препаратов | Верапамил |
240-480 мг/сут.
Инъекционно: в/в струйно 2,5-5 мг при необходимости повторять каждые 15-30 мин
|
IIb B (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| Дилтиазем* | 120-360 мг/сут | IIb B (1) | https://pubmed.ncbi.nlm.nih.gov/33091602/ | |
| Другой антиаритмик | Трифосаденин | В/в струйно 10 мг в течение 2 с. Через 2 мин возможно повторное введение 20 мг в течение 2 с, затем через 2 мин 30 мг в течение 2 с. | IIb С (1) | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
* - на момент 2023 г. данные препараты не зарегистрированы в Узбекистане. В скобках указаны ссылки на литературный источник.
Таблица 10. Особенности основных антиаритмических препаратов для длительной терапии с целью профилактики рецидивов ЖТ и ЖЭ
|
Антиаритмический препарат (класс)
|
Показания | Частые побочные эффекты | Противопоказания | Источник |
| Амиодарон (III) | ЖЭ, ЖТ, ФЖ, в том числе у пациентов с ХСН, патологической (>1,4 см) ГЛЖ, ПИКС |
Кардиальные: Гипотензия, брадикардия, АВ-блокады, ЖТ типа TdP, замедление ритма ЖТ ниже порога детекции ИКД, возрастание порога дефибрилляции
Некардиальные: кератопатия, гипо- и гипертиреоз, рвота, запор,фотосенсибилизация, атаксия, головокружение, периферическая нейропатия, тремор, лекарственный гепатит, цирроз печени, фиброз легких, пневмонит
|
QT >480 мс до начала терапии,
ХСН III-IV ФК NYHA,
Синусовая брадикардия, СА-блокада II-III ст.,
АВ-блокада II-III ст. при отсутствии имплантиро-ванного ЭКС
|
https://pubmed.ncbi.nlm.nih.gov/27222591/ |
|
Бета-адреноблокаторы (II):
Бисопролол,
Карведилол,
Метопролол,
Пропанолол
|
ЖЭ, ЖТ, в том числе у пациентов с ХСН, патологической ГЛЖ (>1,4 см), ПИКС, врожденный LQTS, катехоламин-эргическая полиморфная ЖТ |
Кардиальные: Брадикардия, гипотензия, АВ-блокада, усугубление ХСН. Некардиальные: Головокружение, усталость, бронхообструктивный синдром, тревожные расстройства, депрессия, диарея, сексуальные расстройства, гипогликемия при инсулинзависимом СД |
СА-блокада II-III ст., АВ-блокада II-III ст., синусовая брадикардия (в отсутствии ЭКС), артериальная гипотония, ХСН IV ФК, бронхообструктивный синдром | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| Соталол (III) | ЖЭ, ЖТ, ФЖ | СА-блокада II-IIIст., АВ-блокада II-III ст., синусовая брадикардия (в отсутствии ЭКС), артериальная гипотония, ХСН III-IV ФК, патологическая (>1,4 см) ГЛЖ, в остром периоде ИМ, бронхообструктивный синдром |
Кардиальные: брадикардия, гипотензия, усугубление ХСН, ЖТ типа TdP
Некардиальные: как у бета-адреноблокаторов
|
https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| Прокаинамид (IA) | ЖТ у пациентов без структурной патологии сердца и ХСН | Синусовая брадикардия ≤50 уд/мин, угнетение АВ-проведения (блокады II-III ст.), QRS >160 мс, QT ≥500 мс | Артериальная гипотония, брадикардия, нарушения АВ-проводимости, нарушения в/ж проводимости, возрастание порога дефибрилляции, ЖТ типа пируэт | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| Лидокаин (IB) | ЖТ у пациентов в остром периоде ИМ, ЖТ вследствие интоксикации сердечными гликозидами, после кардиохирургических операций | Значимо не влияет на интервалы ЭКГ. Может сокращать QTc | Делирий, психоз, эпилептические припадки, тремор, дизартрия (при дозах капельного введения 1 г/сут. и более) | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| Пропафенон (IC) | ЖЭ, ЖТ (в отсутствии структурного поражения сердца) |
Кардиальные: СА-блокада, АВ-блокада, расширение комплекса QRS до 25%, отрицательный инотропный эффект, усугубление ХСН, увеличение порогов стимуляции и дефибрилляции сердца. Аритмогенное действие – мономорфная ЖТ, ФЖ. Некардиальные: головокружение, утомляемость, сухость во рту, тошнота, диарея, тремор, нечеткость зрения, нарушения функции печени |
СА-блокада II-III ст., АВ-блокада II-III ст., синусовая брадикардия (в отсутствии ЭКС), тяжелые нарушения внутрижелудочкового проведения (QRS >140 мс), ТП (при отсутствии терапии препаратами, блокирующими АВ-проведение), ИБС, ПИКС, ХСН любого ФК, снижение ФВЛЖ, болезни клапанного аппарата сердца с нарушением гемодинамики, синдром Бругада, наследственный синдром удлиненного интервала QT | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| Лаппаконитина гидробромид (IC) | https://pubmed.ncbi.nlm.nih.gov/33091602/ | |||
| Диэтиламино-пропионил-этоксикарбонил-аминофенотиазина гидрохлорид (IC) | https://pubmed.ncbi.nlm.nih.gov/27222591/ | |||
| Верапамил (IV) Дилтиазем (IV) | ЖТ (из выносящего тракта ПЖ, ЛЖ; фасцикулярная ЖТ) |
Кардиальные: гипотензия, отеки, АВ-блокада, синусовая брадикардия, усугубление ХСН у пациентов со сниженной ФВЛЖ
Некардиальные: головная боль, сыпь, гиперплазия десен, запор, диспепсия
|
СА-блокада II-III ст., АВ-блокада II-III ст., синусовая брадикардия (в отсутствии ЭКС), ХСН, снижение ФВЛЖ, ФП/ТП у пациентов с синдромом WPW | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| Трифосаденин | «Идиопатические» ЖТ: Из выносящего тракта ПЖ, ЛЖ. Фасцикулярная ЖТ | Головная боль, головокружение, тахикардия, тошнота, полиурия | Арест синусового узла или АВ- блокада II-III ст. (кратковременно). Возможно развитие пароксизма ФП. Одышка, бронхоспазм | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
Таблица 11. Особенности дополнительных антиаритмических препаратов для длительной терапии с целью профилактики рецидивов ЖТ и ЖЭ
|
Антиаритмический препарат
|
Показания | Частые побочные эффекты | Противопоказания | Источник |
| Магния сульфат | Удлинения интервала QTc | Со стороны сердца: гипотензия | Артериальная гипотония | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| Калия хлорид и препраты Калия | Гипокалиемия | Со стороны сердца: брадикардия, гипотензия, АВ блокада, гиперкалиемия | Гиперкалиемия, тяжелая почечная недостаточность | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
При определении лечебного подхода у пациентов с ЖА основываются на наличии или отсутствии структурной патологии сердца. Перечень основных ААП, показания к назначению, дозы и побочные эффекты приведены в Приложении. Их использование варьируется в зависимости от задач – купирование приступа ЖТ или профилактическое назначение.
Антиаритмическая терапия ЖА у пациентов без структурной патологии сердца/ДЛЖ
У пациентов без структурной патологии сердца/ДЛЖ медикаментозное лечение ЖА не рекомендовано, т.к. у этих пациентов низкий риск ВСС и не требуется её профилактика [1] (ЕОК IIIА)
В отсутствие структурной патологии сердца так называемая «идиопатическая» ЖА может быть представлена в виде одиночной, парной ЖЭ, пробежек ЖТ, а также аналогичных проявлений желудочковой парасистолии. С позиции риска ВСС пациенты без структурной патологии сердца имеют благоприятный прогноз вне зависимости от вида ЖА, общего количества ЖЭ в сутки и величины интервала сцепления ЖЭ.
У пациентов без структурной патологии сердца/ДЛЖ лекарственное лечение ЖЭ рекомендовано в случаях, когда аритмия сопровождается клинической симптоматикой либо приводит к дилатации полостей сердца и снижению сократимости миокарда ЛЖ на фоне частой ЖА, превышающей 15% от общего количества сердечных сокращений в сутки по данным ХМЭКГ (ЕОК IС).
Для лечения ЖА у пациентов без структурной патологии сердца/ДЛЖ рекомендовано назначение бета-адреноблокаторов, блокаторов «медленных» кальциевых каналов с прямым влиянием на сердце (верапамила), а также ААП I и III классов по классификации E.M.Vaughan-Williams в модификации B.N.Singh и D.C.Harrison [2] (ЕОК IIaB).
Наиболее эффективными средствами лечения ЖЭ являются антиаритмические препараты IC класса (пропафенон, этацизин аллапинин, а также ААП III класса (соталол и амиодарон) [1].
У пациентов без структурной патологии сердца/ДЛЖ наличие пароксизмов мономорфной ЖТ (идиопатической ЖТ) не увеличивает риск ВСС и не требует её медикаментозной профилактики [1] (ЕОК IА).
С позиции риска ВСС в большинстве случаев пациенты с идиопатическими ЖТ имеют благоприятный прогноз жизни, однако данные аритмии могут сопровождаться выраженными нарушениями системной гемодинамики (обморок, отёк лёгких), а при длительно персистирующем течении – приводить к прогрессирующему снижению сократимости миокарда и развитию тахикардиомиопатии. Эти состояния при отсутствии эффективного антиаритмического лечения могут представлять опасность для жизни пациентов.
При наличии ЖТ у пациентов без структурной патологии сердца для профилактики повторного возникновения устойчивых приступов рекомендовано назначение бета- адреноблокаторов, верапамила, а также ААП I и III класса [3] (ЕОК IIaB).
Выбор препарата для ААТ с целью профилактики рецидивов ЖТ должен осуществляться с учётом индивидуальных провоцирующих факторов и характерных для разных форм ЖТ изменений ЭКГ. Бета-адреноблокаторы являются препаратами выбора при ЖТ, провоцируемых физической нагрузкой. Профилактический приём верапамила целесообразен для лечения непароксизмальной ЖТ и предупреждения пароксизмов фасцикулярной левожелудочковой тахикардии. Наиболее эффективными средствами предупреждения рецидивов пароксизмальной мономорфной ЖТ являются ААП I и III класса .
Антиаритмическая терапия желудочковой эктопической активности у пациентов со структурной патологией сердца/ДЛЖ
Лекарственная ААТ ЖЭ у пациентов со структурной патологией сердца/ДЛЖ рекомендована в случаях, когда аритмия сопровождается клинической симптоматикой либо приводит к дилатации полостей сердца и снижению сократимости миокарда ЛЖ на фоне частой ЖА, превышающей 15% от общего количества сердечных сокращений в сутки по данным ХМЭКГ (ЕОК IС).
При наличии ЖА у пациентов со структурной патологией сердца/ДЛЖ повышен риск ВСС и рекомендуется проведение ААТ для её профилактики (ЕОК IА).
У пациентов со структурной патологией сердца риск ВСС зависит от характера ЖА и выраженности ДЛЖ. Наличие у пациентов со структурным поражением сердца частой ЖЭ (>10 ЖЭ в час), множественных форм ЖА (парной ЖЭ, пробежек ЖТ) и/или сниженной сократительной функции ЛЖ (значение ФВЛЖ <40%) сопряжено с повышенным риском ВСС.
Для лечения пациентов со структурным поражением миокарда/ДЛЖ, имеющих повышенный риск ВСС и нуждающихся в её первичной или вторичной профилактике, рекомендовано назначение препаратов группы бета-адреноблокаторов с учётом противопоказаний к их применению и возможных побочных эффектов (ЕОК IА).
Применение ААТ (за исключением бета-адреноблокаторов) не рекомендовано для снижения риска ВСС у пациентов со структурной патологией сердца/ДЛЖ (ЕОК IIIА).
Использование ААП IC класса (блокаторы натриевых каналов) и блокаторов «медленных» кальциевых каналов у пациентов со структурной патологией сердца/ДЛЖ может приводить к увеличению риска возникновения жизнеугрожающих ЖТА и ВСС, а также прогрессированию явлений СН; а применение ААП III класса (блокаторы калиевых каналов) у таких пациентов не улучшает их прогноз.
У пациентов с имплантированными СРТ-устройствами, применение лекарственной ААТ рекомендовано для подавления частой ЖЭ в случаях, когда она приводит к снижению процента навязанного бивентрикулярного ритма ниже рекомендованного уровня (ЕОК IIa B).
В качестве ААТ ЖЭ у пациентов со структурной патологией сердца/ДЛЖ рекомендовано назначение бета-адреноблокаторов, соталола, амиодарона, либо комбинации бета-адреноблокаторов и амиодарона (ЕОК IА).
Бета-адреноблокаторы необходимо рассматривать в качестве основы ААТ ЖА. Соталол более эффективен, чем бета-адреноблокаторы, подавляет ЖА, однако его применение не рекомендовано пациентам, имеющим значения ФВЛЖ <20%, гипертрофию миокарда ЛЖ >14 мм, а также признаки СН. Амиодарон в качестве монотерапии и в комбинации с бета-адреноблокаторами представляет собой наиболее эффективный ААП для лечения ЖА у пациентов со структурной патологией сердца. В то же время, его применение сопряжено с наиболее высоким риском развития тяжёлых побочных эффектов. Вследствие этого, амиодарон целесообразно назначать при неэффективности или невозможности применения других ААП.
Не рекомендовано применение антиаритмических препаратов I класса и блокаторов «медленных» кальциевых каналов для лечения ЖЭ у пациентов со структурным поражением сердца/ДЛЖ (ЕОК IIIА).
ААП I класса не должны применяться для лечения ЖЭ у пациентов с ИБС, в т. ч. переживших ИМ, а также у пациентов с другими формами сердечной патологии, приводящими к снижению сократительной функции ЛЖ (значения ФВ ЛЖ <40%) и/или проявлениям хронической СН. Назначение ААП I класса также противопоказано пациентам, имеющим ГЛЖ (толщина миокарда левого желудочка >14 мм). Блокаторы «медленных» кальциевых каналов (верапамил и дилтиазем) малоэффективны в лечении ЖА у пациентов со структурным поражением сердца и могут ухудшать прогноз пациентов с ДЛЖ и СН.
Оценку эффективности и безопасности подавления ЖА при помощи ААТ у пациентов со структурной патологией сердца/ДЛЖ рекомендовано проводить под контролем повторного ХМЭКГ, выполненного на фоне приёма ААТ в терапевтической дозе в течение времени, достаточного для наступления ААЭ назначаемых лекарств (ЕОК IIaС).
Титрование бета-адреноблокаторов целесообразно проводить на 3-5 сутки их приёма, соталола – на 5-7 сутки, амиодарона – не ранее, чем через 5 недель. Назначение каждого последующего ААП должно проводиться не ранее, чем через 5 периодов полувыведения предыдущего, для амиодарона – не ранее, чем через 1,5 месяца после его отмены. Для оценки эффективности тестируемых ААП рекомендуется использовать следующие критерии: при приёме ААП в терапевтической дозе регистрируется снижение общего количества ЖЭ более, чем на 50% и/или уменьшение количества часов в сутки, в течение которых регистрировалась ЖЭ более, чем в 2 раза от такового, проводившегося в условиях отсутствия ААТ. Параллельно с этим у пациентов должно регистрироваться уменьшение количества парных ЖЭ в 10 раз и более, а также полное устранение пробежек ЖТ.
Назначение амиодарона или комбинации амиодарона с бета-адреноблокаторами рекомендовано при наличии приступов ЖТ/ФЖ у пациентов со структурной патологией сердца или ДЛЖ, если они отказываются от имплантации ИКД либо эта операция не может быть выполнена по каким-либо другим причинам.
У пациентов, нуждающихся в первичной и вторичной профилактике ВСС, амиодарон или его комбинированное применение с бета-адреноблокаторами являются единственной лекарственной альтернативой ИКД, способной предупреждать возникновение ЖТ/ФЖ и увеличивать продолжительность жизни пациентов.
Лечение пациентов с пароксизмами ЖТ/ФЖ должно проводиться параллельно с выявлением и устранением индивидуальных патогенетических факторов, лежащих в основе возникновения аритмических приступов. ЕОК IС
патогенетическими факторами, провоцирующими возникновение ЖТ, являются аритмогенное действие лекарственных препаратов, электролитные нарушения (гипокалиемия, гипомагниемия) и острая ишемия миокарда.
Купирование устойчивых пароксизмов желудочковой тахикардии
Алгоритм купирования пароксизмов ЖТ представлен в Приложении. Дозы препаратов для купирования пароксизмов ЖТ представлены в Приложении.
При остановке кровообращения (ЖТ с отсутствием пульса или ФЖ) ключевым элементом реанимации является экстренная электрическая дефибрилляция сердца [1, 4] (ЕОК I С).
При ФЖ/ЖТ с отсутствием пульса после трех неэффективных разрядов дефибриллятора рекомендовано внутривенное болюсное введение 300 мг амиодарона на фоне продолжения СЛР с целью повышения эффективности проводимых реанимационных мероприятий и предупреждения немедленных рецидивов ЖТ/ФЖ (ЕОК I А).
Внутривенное введение лидокаина на фоне продолжения СЛР рекомендуется в случае неэффективности дефибрилляции или непрерывного рецидивирования аритмии для повышения шансов купирования ФЖ и предупреждения немедленных рецидивов ЖТ/ФЖ в случае, если амиодарон недоступен (ЕОК IIaB).
Внутривенное введение эпинефрина 1 мг каждые 3-5 мин. после введения первой дозы рекомендовано в ходе оказания СЛР, до восстановления эффективного кровообращения, независимо от ритма, сопровождающего остановку кровообращения, с целью повышения эффективности проводимых реанимационных мероприятий (ЕОК IIb A).
Время введения первой дозы эпинефрина зависит от сердечного ритма, сопровождающего остановку кровообращения:
При остановке кровообращения (ЖТ с отсутствием пульса или ФЖ) рекомендуется незамедлительное проведение комплекса сердечно-легочных реанимационных мероприятий (СЛР) [1] (ЕОК I С).
При остановке кровообращения (ЖТ с отсутствием пульса или ФЖ) ключевым элементом реанимации является экстренная электрическая дефибрилляция сердца [1, 4] (ЕОК I С).
При ФЖ/ЖТ с отсутствием пульса после трех неэффективных разрядов дефибриллятора рекомендовано внутривенное болюсное введение 300 мг амиодарона на фоне продолжения СЛР с целью повышения эффективности проводимых реанимационных мероприятий и предупреждения немедленных рецидивов ЖТ/ФЖ (ЕОК I А).
Введение дополнительных 150 мг амиодарона рекомендовано после 5 неэффективных разрядов дефибриллятора.
Внутривенное введение лидокаина на фоне продолжения СЛР рекомендуется в случае неэффективности дефибрилляции или непрерывного рецидивирования аритмии для повышения шансов купирования ФЖ и предупреждения немедленных рецидивов ЖТ/ФЖ в случае, если амиодарон недоступен (ЕОК IIaB).
Внутривенное введение эпинефрина 1 мг каждые 3-5 мин. после введения первой дозы рекомендовано в ходе оказания СЛР, до восстановления эффективного кровообращения, независимо от ритма, сопровождающего остановку кровообращения, с целью повышения эффективности проводимых реанимационных мероприятий (ЕОК IIb A).
Применение более высоких доз препарата не обладает преимуществом по сравнению со стандартной дозой 1 мг.
Время введения первой дозы эпинефрина зависит от сердечного ритма, сопровождающего остановку кровообращения:
при ритмах, подлежащих дефибрилляции или кардиоверсии, первая доза эпинефрина вводится после трех неэффективных разрядов дефибриллятора;
при ритмах, не подлежащих лечению разрядом дефибриллятора (электромеханическая диссоциация и асистолия) первая доза эпинефрина вводится немедленно после установки внутривенного доступа.
Экстренная электрическая кардиоверсия рекомендована при ЖТ, сопровождающейся острыми нарушениями гемодинамики (симптомная артериальная гипотензия, синкопальное/пресинкопальное состояние, признаки острой ишемии миокарда, отёк лёгких/острая СН) (ЕОК IB).
При оказании неотложной медицинской помощи пароксизмы тахикардии с широкими комплексами QRS рекомендуется расценивать как ЖТ за исключением ситуаций, когда диагноз наджелудочковой тахикардии (НЖТ) не вызывает сомнения (ЕОК IС).
Интерпретация тахикардии с широкими комплексами QRS как наджелудочковой только на основании отсутствия острых нарушений гемодинамики является распространённой клинической ошибкой. ААП, используемые для купирования ЖТ, эффективны и при НЖТ, в то время как препараты, применяемые для купирования НЖТ (верапамил) могут вызывать снижение АД и приводить к острым нарушениям гемодинамики у пациентов с ЖТ.
Внутривенное введение Прокаинамида рекомендуется для купирования пароксизмов ЖТ, протекающих без острых нарушений гемодинамики (ЕОК IIaА).
Внутривенное введение Амиодарона рекомендуется для купирования пароксизмов ЖТ, протекающих без острых нарушений гемодинамики (ЕОК IIbB).
Внутривенное введение бета-адреноблокаторов (Метопролол, Эсмолол) рекомендуется для купирования и предотвращения непрерывного рецидивирования ЖТ/ФЖ, провоцируемой ишемией миокарда (ЕОК IIaB).
Внутривенное введение верапамила рекомендуется для купирования ЖТ, но только в случае, если диагноз верапамил-чувствительной ЖТ не вызывает сомнений (ЕОК IaB).
Особой, нечасто встречающейся формой пароксизмальной мономорфной ЖТ является фасцикулярная левожелудочковая тахикардия, в основе которой лежит механизм reentry с участием в цепи циркуляции волны возбуждения задненижнего разветвления левой ножки пучка Гиса (иногда передневерхнего разветвления). Комплексы QRS во время пароксизма имеют конфигурацию, характерную для блокады правой ножки пучка Гиса с отклонением ЭОС влево. Участие проксимальных структур системы Гиса-Пуркинье в формировании механизма тахикардии является причиной других ее особенностей: 1) продолжительность комплексов QRS редко превышает 120 мс; 2) пароксизмы могут инициироваться не только желудочковыми, но и предсердными экстрасистолами; 3) верапамил высоко эффективен в купировании этой тахикардии (по этим причинам ее обозначают также как «верапамил-чувствительную ЖТ», а в/в применение верапамила служит не только способом устранения пароксизмов, но и своеобразным диагностическим лекарственным тестом, надежно подтверждающим именно такой механизм тахикардии); 4) отчетливый анатомический субстрат ЖТ – задне-нижняя ветвь левой ножки пучка Гиса, как участник цепи риентри, – зона высокоэффективной катетерной аблации при этой форме тахикардии. Фасцикулярная левожелудочковая тахикардия выявляется, как правило, у молодых лиц, не имеющих признаков органического заболевания сердца, что принципиально отличает их от подавляющего большинства других пациентов с пароксизмами ЖТ, и по тяжести клинических проявлений приступов, и по прогнозу жизни с позиции риска ВСС.
Внутривенное введение трифосаденина рекомендуется для купирования ЖТ, но только в случае, если диагноз аденозин-чувствительной ЖТ не вызывает сомнений (ЕОК IС).
Чувствительной к трифосаденину является тахикардия, исходящая из выносящего тракта ПЖ. Для такой тахикардии типичны характерная морфология комплексов QRS на ЭКГ, частота ритма во время тахикардии в пределах от 100 до 150 в минуту, непрерывное рецидивирование. Гораздо реже аналогичная форма тахикардии может возникать в выносящем тракте ЛЖ. Помимо трифосаденина, данные формы тахикардии также являются чувствительными и к верапамилу.
Трифосаденин может вызывать снижение АД и приводить к острым нарушениям гемодинамики, а также потенцировать «феномен обкрадывания» и усугублять ишемию миокарда, поэтому противопоказан пациентам с другими формами ЖТ.
Введение лекарств не должно прерывать СЛР и задерживать такие вмешательства, как дефибрилляция или кардиоверсия.
Экстренная электрическая кардиоверсия рекомендована при ЖТ, сопровождающейся острыми нарушениями гемодинамики (симптомная артериальная гипотензия, синкопальное/пресинкопальное состояние, признаки острой ишемии миокарда, отёк лёгких/острая СН) (ЕОК IB).
При оказании неотложной медицинской помощи пароксизмы тахикардии с широкими комплексами QRS рекомендуется расценивать как ЖТ за исключением ситуаций, когда диагноз наджелудочковой тахикардии (НЖТ) не вызывает сомнения (ЕОК IС).
Интерпретация тахикардии с широкими комплексами QRS как наджелудочковой только на основании отсутствия острых нарушений гемодинамики является распространённой клинической ошибкой. ААП, используемые для купирования ЖТ, эффективны и при НЖТ, в то время как препараты, применяемые для купирования НЖТ (верапамил) могут вызывать снижение АД и приводить к острым нарушениям гемодинамики у пациентов с ЖТ.
Внутривенное введение Прокаинамида рекомендуется для купирования пароксизмов ЖТ, протекающих без острых нарушений гемодинамики (ЕОК IIaА).
Внутривенное введение Амиодарона рекомендуется для купирования пароксизмов ЖТ, протекающих без острых нарушений гемодинамики (ЕОК IIbB).
Внутривенное введение бета-адреноблокаторов (Метопролол, Эсмолол) рекомендуется для купирования и предотвращения непрерывного рецидивирования ЖТ/ФЖ, провоцируемой ишемией миокарда (ЕОК IIaB).
Внутривенное введение верапамила рекомендуется для купирования ЖТ, но только в случае, если диагноз верапамил-чувствительной ЖТ не вызывает сомнений (ЕОК IaB).
Особой, нечасто встречающейся формой пароксизмальной мономорфной ЖТ является фасцикулярная левожелудочковая тахикардия, в основе которой лежит механизм reentry с участием в цепи циркуляции волны возбуждения задненижнего разветвления левой ножки пучка Гиса (иногда передневерхнего разветвления). Комплексы QRS во время пароксизма имеют конфигурацию, характерную для блокады правой ножки пучка Гиса с отклонением ЭОС влево. Участие проксимальных структур системы Гиса-Пуркинье в формировании механизма тахикардии является причиной других ее особенностей: 1) продолжительность комплексов QRS редко превышает 120 мс; 2) пароксизмы могут инициироваться не только желудочковыми, но и предсердными экстрасистолами; 3) верапамил высоко эффективен в купировании этой тахикардии (по этим причинам ее обозначают также как «верапамил-чувствительную ЖТ», а в/в применение верапамила служит не только способом устранения пароксизмов, но и своеобразным диагностическим лекарственным тестом, надежно подтверждающим именно такой механизм тахикардии); 4) отчетливый анатомический субстрат ЖТ – задне-нижняя ветвь левой ножки пучка Гиса, как участник цепи риентри, – зона высокоэффективной катетерной аблации при этой форме тахикардии. Фасцикулярная левожелудочковая тахикардия выявляется, как правило, у молодых лиц, не имеющих признаков органического заболевания сердца, что принципиально отличает их от подавляющего большинства других пациентов с пароксизмами ЖТ, и по тяжести клинических проявлений приступов, и по прогнозу жизни с позиции риска ВСС.
Верапамил может вызывать снижение АД и приводить к острым нарушениям гемодинамики, поэтому противопоказан пациентам сдругими формами ЖТ.
Внутривенное введение трифосаденина рекомендуется для купирования ЖТ, но только в случае, если диагноз аденозин-чувствительной ЖТ не вызывает сомнений (ЕОК IС).
Чувствительной к трифосаденину является тахикардия, исходящая из выносящего тракта ПЖ. Для такой тахикардии типичны характерная морфология комплексов QRS на ЭКГ, частота ритма во время тахикардии в пределах от 100 до 150 в минуту, непрерывное рецидивирование. Гораздо реже аналогичная форма тахикардии может возникать в выносящем тракте ЛЖ. Помимо трифосаденина, данные формы тахикардии также являются чувствительными и к верапамилу.
Трифосаденин может вызывать снижение АД и приводить к острым нарушениям гемодинамики, а также потенцировать «феномен обкрадывания» и усугублять ишемию миокарда, поэтому противопоказан пациентам с другими формами ЖТ.
Лечение желудочковых аритмий при остром коронарном синдроме
ЖЭ и неустойчивая ЖТ часто отмечаются у пациентов с ОКС, особенно во время первичного коронарного вмешательства при ИМ с подъемом сегмента ST (т. н. реперфузионные аритмии). Они редко приводят к нарушению гемодинамики и не требуют специфической терапии. Длительно сохраняющаяся и частая ЖА может свидетельствовать о необходимости дальнейшей реваскуляризации (например, повторной ангиографии/ЧКВ) [3, 5]. Если неустойчивая ЖТ сопровождается нарушением гемодинамики, следует рассмотреть назначение амиодарона (300 мг в/в струйно) [2]. Повторная стойкая ЖТ, особенно полиморфного характера, или повторная ФЖ могут быть признаком неполной реперфузии или возврата острой ишемии. В таких случаях следует рассмотреть выполнение экстренной коронарографии. Повторная полиморфная ЖТ с переходом в ФЖ может отвечать на терапию бета-адреноблокаторами. Уменьшению числа эпизодов ЖТ или ФЖ также способствует глубокая седация. Для быстрого подавления гемодинамически значимых ЖА можно использовать амиодарон (150-300 мг в/в струйно).
Применение других антиаритмических препаратов при ОКС (например, прокаинамид, пропафенон) не рекомендовано [7] (ЕОК III B).
С целью профилактики ЖА у пациентов со структурной патологией сердца рекомендуется назначать бета-адреноблокаторы (ЕОК I aB).
Назначение бета-адреноблокаторов внутрь для профилактики ЖА и ВСС рекомендовано для всех пациентов с ОКС во время госпитализации и после выписки, при отсутствии противопоказаний (ЕОК I B).
Лечение бета-адреноблокаторами рекомендовано при повторных эпизодах полиморфной ЖТ т.к. ААТ устойчивой ЖТ должна быть направлена на максимальную симпатическую блокаду [7] (ЕОК I B).
Применение амиодарона рекомендовано для устранения симптомов ЖА у пациентов после ИМ, однако такая терапия не влияет на показатели смертности.
Внутривенное введение амиодарона рекомендовано для лечения полиморфной ЖТ, ассоциированной с ОКС (ЕОК I C).
Коррекция нарушений электролитного баланса рекомендована пациентам с повторными эпизодами ЖТ или ФЖ для купирования и профилактики приступов аритмии (ЕОК I C).
Внутривенное введение лидокаина рекомендовано для лечения повторных эпизодов стойкой ЖТ или ФЖ, не отвечающей на терапию бета-адреноблокаторами или амиодароном, а также при наличии противопоказаний к лечению амиодароном [5, 7] (ЕОК IIb C)
Электрическая дефибрилляция. Электрическая стимуляция
Экстренная электрическая кардиоверсия или дефибрилляция рекомендована пациентам с устойчивой ЖТ или ФЖ для купирования приступа аритмии [1-5] (ЕОК I C).
Если остановка сердца произошла в лечебном учреждении, необходимо сразу выполнить дефибрилляцию, поскольку в этом случае выше вероятность того, что причиной остановки сердца была стойкая ЖТА. При этом дефибрилляцию начинают с максимальной мощности. Для лечебных учреждений самым удобным вариантом являются полуавтоматические дефибрилляторы. В/в введение амиодарона повышает эффективность дефибрилляции и/или предотвращает повторные эпизоды ЖТ или ФЖ в острых случаях.
Электрическая кардиоверсия рекомендована пациентам с мономорфной ЖТ и нестабильной гемодинамикой для купирования приступа аритмии и восстановления эффективной сердечной деятельности (ЕОК IС).
Электрическая кардиоверсия рекомендуется для купирования пароксизма ЖТ, не сопровождающегося острыми нарушениями гемодинамики, при неэффективности ААТ, противопоказании к их применению, а также в случае, если лечащий врач и пациент отдают предпочтение этому способу восстановления ритма (ЕОК IIb C).
Учащающая стимуляция желудочков рекомендована для купирования мономорфной ЖТ и ТЖ и восстановления эффективной сердечной деятельности [4-8] (ЕОК IIa C).
Кратковременная «залповая» стимуляция желудочков «пачками» из 8-10 импульсов с частотой, превышающей частоту ЖТ (burstpacing) для купирования мономорфной ЖТ может быть проведена с использованием системы временной трансвенозной стимуляции сердца (при наличии центрального венозного доступа), либо с помощью имплантированных устройств (ЭКС, ИКД, имплантируемых СРТ-устройств). Данный метод неэффективен для купирования ФЖ и полиморфной ЖТ типа torsade de pointes.
Трансвенозная катетерная учащающая стимуляция по типу «овердрайв» рекомендована в том случае, если возникают частые повторные эпизоды ЖТ, несмотря на лечение ААП, а катетерная аблация у данного пациента невозможна (ЕОК I C).
Временная трансвенозная стимуляция рекомендована пациентам с симптомами синусовой брадикардии для профилактики возникновения ЖТ/ФЖ, несмотря на лечение препаратами с положительным хронотропным эффектом (ЕОК I C).
Временная трансвенозная стимуляция рекомендована пациентам с симптомами тяжелой АВ-блокады без стабильного замещающего ритма для профилактики возникновения ЖТ/ФЖ (ЕОК I C)
Далее приводятся алгоритмы по купированию ЖТ.
Рис. 1. АЛГОРИТМ КУПИРОВАНИЯ ПАРОКСИЗМА ЖЕЛУДОЧКОВОЙ ТАХИКАРДИИ
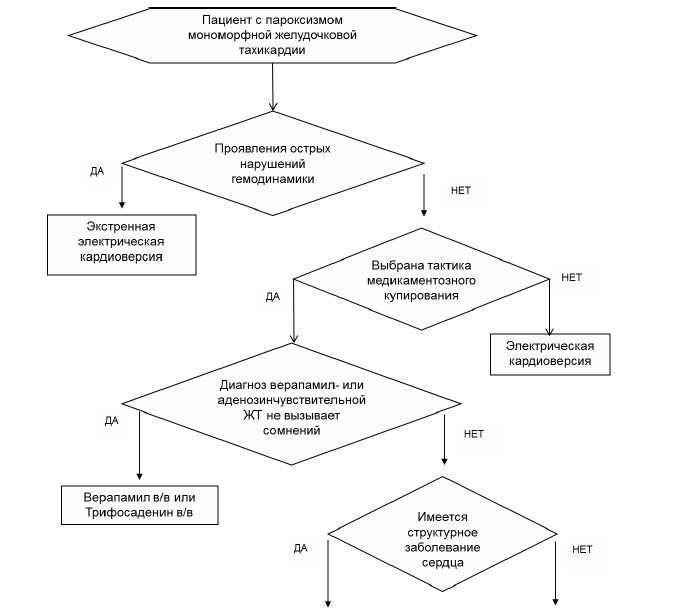
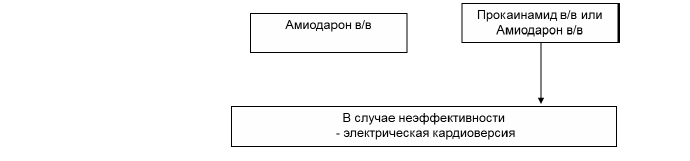
Рис 2. ЛЕЧЕНИЕ РЕЦИДИВИРУЮЩЕЙ ЖТ У ПАЦИЕНТОВ С ИБС И НЕИШЕМИЧЕСКОЙ КАРДИОМИОПАТИЕЙ
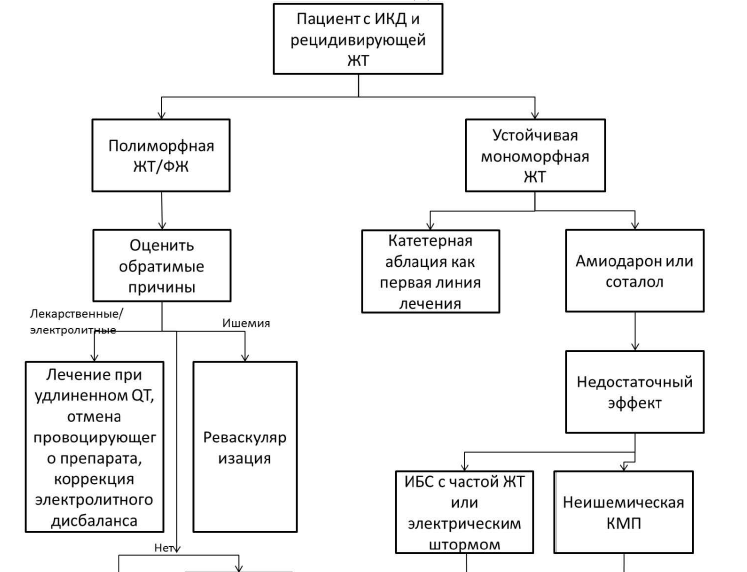
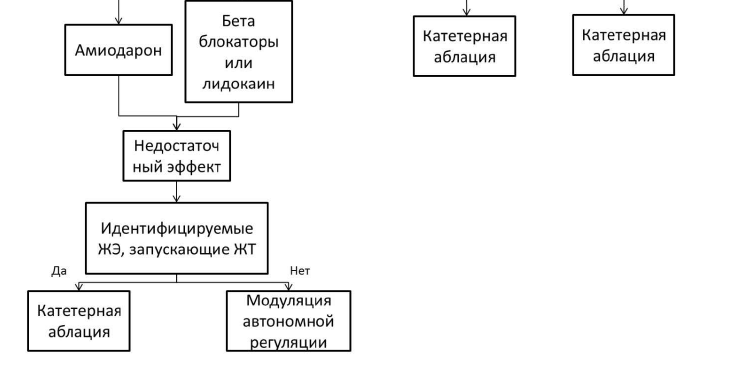
Здесь не включена информация по постстационарному наблюдению, то есть что должен делать Семейный врач после стационарного лечения, «Д» наблюдения, реабилитации и профилактики осложнений.
Особенности терапии основного заболевания при ЖА.
1. Лечение ИБС. Острый коронарный синдром и острый инфаркт миокарда.
Частота ЖА при ОКС на госпитальном этапе в последние десятилетия снизилась, главным образом за счет ранней и активной реваскуляризации и своевременной адекватной фармакотерапии. Тем не менее, у 6% пациентов с ОКС в первые 48 часов с момента появления симптомов развиваются ЖТ или ФЖ, чаще всего до или во время реперфузии. Устранению ЖА в этой ситуации способствуют быстрая и полная реваскуляризация коронарных артерий, нефармакологические вмешательства (кардиоверсия, дефибрилляция, стимуляция и катетерная аблация) и фармакотерапия (антиаритмические и другие препараты) [1]
Если на ЭКГ до или сразу после реанимационных мероприятий отмечается подъем сегмента ST, необходима экстренная ангиография и реваскуляризация, как и всем пациентам с ИМ с подъемом сегмента ST. Однако даже при отсутствии подъема сегмента ST вполне возможно обструктивное или даже тромботическое поражение инфаркт-ассоциированной коронарной артерии, что отмечается в 25-85% случаев [1,5]. Учитывая высокую распространенность окклюзий коронарных артерий и возможные сложности интерпретации ЭКГ после остановки сердца, следует рассмотреть выполнение коронароангиографии всем пациентам, пережившим остановку сердца вне стен лечебного учреждения, сразу после поступления в приемный покой или отделение интенсивной терапии для исключения несердечных причин остановки сердца [2].
В случае ОКС и повторной стойкой и/или гемодинамически значимой ЖТ или ФЖ быстрая и успешная реваскуляризация имеет ключевое значение для профилактики последующих аритмий и должна выполняться без промедления [1,2].
Для всех пациентов с болями за грудиной рекомендуется сокращать время между появлением симптомов и первым контактом с врачом, а также от первого контакта с врачом до реперфузии [1,3] (ЕОК IA).
При развитии клинической смерти рекомендуется выполнять основные и дополнительные реанимационные мероприятия в соответствии с алгоритмами, разработанными Европейским (ERC) советом по реанимации [1,4] (ЕОК IB).
Экстренная коронарография, при необходимости с реваскуляризацией, рекомендована пациентам с повторными эпизодами ЖТ или ФЖ, когда не удается исключить ишемию миокарда [1,2,3] (ЕОК IC).
При ИМ с подъемом сегмента ST рекомендуется экстренная реперфузия для уменьшения ишемического повреждения и электрической нестабильности миокарда [7] (ЕОК IA ).
Пациентам с ИМ без подъема сегмента ST из группы высокого риска, в том числе с угрожающими жизни ЖА, рекомендуется коронарная ангиография и при необходимости коронарная ангиопластика в течение 2 ч после поступления для уменьшения ишемического повреждения и электрической нестабильности миокарда [1,5] (ЕОК IC).
Для устранения ишемии миокарда, которая может присутствовать у пациентов с повторными эпизодами ЖТ или ФЖ, рекомендуется экстренная реваскуляризация коронарных артерий [1] (ЕОК IC)
Госпитализация в отделение интенсивной терапии рекомендовано для пациентов, выживших после остановки сердца вне стен лечебного учреждения и находящихся в коматозном состоянии, без электрокардиографических признаков ИМ с подъемом сегмента ST на ЭКГ после реанимации (ЕОК IIaB).
У пациентов, выживших после остановки сердца вне стен лечебного учреждения и находящихся в коматозном состоянии, при отсутствии данных за некоронарные причины рекомендовано срочное выполнение (<2 ч) коронароангиографии, особенно у пациентов с нестабильной гемодинамикой (ЕОК IIaB).
Острая ишемия является причиной электрической нестабильности и провоцирует возникновение ЖА при ОКС. Для уменьшения вероятности ЖТ/ФЖ при ОКС рекомендуется назначение бета-адреноблокаторов в раннем периоде. В некоторых случаях помогает компенсация гипомагниемии и гипокалиемии. Статины уменьшают смертность среди пациентов с ИБС, главным образом за счет предотвращения повторных коронарных событий, и являются частью стандартного лечения таких пациентов. Возникновение фибрилляции желудочков в раннем периоде (т. е. в течение 48 часов) при ОКС сопровождается пятикратным повышением риска госпитальной смертности.
2. Стратификация риска ВСС в острый период инфаркта миокарда.
Большинство исследований, в которых оценивали целесообразность неинвазивных способов стратификации риска, проводились на пациентах с выраженным снижением ФВЛЖ (<40%) или в смешанных группах. Результаты для пациентов с ФВЛЖ>40% либо не сообщались, либо подгруппы таких пациентов были настолько малы, что не позволяли выполнить достоверный анализ и интерпретировать полученные данные. В настоящий момент нет достаточно специфичных и чувствительных неинвазивных методов стратификации риска у пациентов, перенесших ИМ и имеющих нормальную ФВЛЖ. Есть ограниченные данные, полученные в подгруппах больших исследований, что программируемая желудочковая стимуляция может применяться для стратификации риска после ИМ у пациентов с ФВЛЖ >40% [1].
Большинство исследований, в которых оценивали целесообразность неинвазивных способов стратификации риска, проводились на пациентах с выраженным снижением ФВЛЖ (<40%) или в смешанных группах. Результаты для пациентов с ФВЛЖ>40% либо не сообщались, либо подгруппы таких пациентов были настолько малы, что не позволяли выполнить достоверный анализ и интерпретировать полученные данные. В настоящий момент нет достаточно специфичных и чувствительных неинвазивных методов стратификации риска у пациентов, перенесших ИМ и имеющих нормальную ФВЛЖ. Есть ограниченные данные, полученные в подгруппах больших исследований, что программируемая желудочковая стимуляция может применяться для стратификации риска после ИМ у пациентов с ФВЛЖ >40% [1].
Неинвазивные методы (например, оценка альтернации зубца T, дисфункции вегетативной системы или сигнал-усредненной ЭКГ) не рекомендуются для стратификации риска в ранний период после ИМ [7] (ЕОК IIIB).
Ранняя (до выписки) оценка ФВЛЖ рекомендована всем пациентам, перенесшим острый ИМ [8] (ЕОК IB).
При сниженной фракции ФВЛЖ (<35%) рекомендуется повторная оценка через 6-12 недель после ИМ с целью определения необходимости имплантации кардиовертера-дефибриллятора (ИКД) для первичной профилактики ВСС (ЕОК IC).
В особых случаях, например, при неполной реваскуляризации, предшествующем нарушении ФВЛЖ и появлении аритмии спустя 48 часов от развития ОКС, можно рассмотреть раннюю (<40 дней) установку ИКД или временное (<40 дней) применение носимого кардиовертера-дефибриллятора. При этом следует учитывать тип ЖА (мономорфная, полиморфная, ЖТ или ФЖ), а также длину цикла ЖТ (нестойкие короткие циклы и нестойкие длинные циклы). Если выполняется программируемая стимуляция, дополнительно оценивают индукцию и тип индуцируемой аритмии (мономорфная ЖТ, полиморфная ЖТ, ФЖ).
Реваскуляризация коронарных артерий рекомендуется для снижения риска ВСС у пациентов с ФЖ и предшествующими ей признаками ишемии миокарда. ЕОК IB
3. Аневризма левого желудочка. Ишемическая кардиомиопатия. Хроническая сердечная недостаточность.
Частота развития и тяжесть ЖА возрастают по мере утяжеления СН, однако прогностическое значение ЖА для оценки риска внезапной смерти пока неясно. Оптимальная медикаментозная терапия ингибиторами АПФ (или ангиотензина II антагонистами при непереносимости ингибиторов АПФ), бета-адреноблокаторами или антагонистами альдостерона рекомендована пациентам с СН и систолической дисфункцией ЛЖ (ФВЛЖ ≤ 35-40%) для снижения общей смертности и риска ВСС [1].
Частота развития и тяжесть ЖА возрастают по мере утяжеления СН, однако прогностическое значение ЖА для оценки риска внезапной смерти пока неясно. Оптимальная медикаментозная терапия ингибиторами АПФ (или ангиотензина II антагонистами при непереносимости ингибиторов АПФ), бета-адреноблокаторами или антагонистами альдостерона рекомендована пациентам с СН и систолической дисфункцией ЛЖ (ФВЛЖ ≤ 35-40%) для снижения общей смертности и риска ВСС [1].
Хирургическое лечение ЖТ. Данный раздел расписан в протоколе «Желудочковые аритмии: протокол медицинских вмешательств».
Особые клинические состояния
1. Желудочковая тахикардия из выходного отдела сердца
Выполнение катетерной аблации ЖТ/ЖЭ из области ВОПЖ рекомендовано при наличии симптомов и/или в случае неэффективности ААТ (к примеру, бета-адреноблокаторов), а также у пациентов с нарушением систолической функции ЛЖ на фоне частой ЖТ/ЖЭ (ЕОК IB).
Пациентам с ЖТ-ВТПЖ/ЖЭ рекомендована катетерная аблация в качестве метода первого выбора, тогда как при ЖТ-ВТЛЖ/ЖЭ ее выполнение следует рассматривать только при отсутствии эффекта ААТ.
Лечение ААП IC класса (блокаторы натриевых каналов) рекомендовано при наличии симптомов пациентам с ЖТ из ВОЛЖ, области аортального клапана или эпикардиальной ЖТ/ЖЭ (ЕОК IC).
Выполнение катетерной аблации для лечения ЖТ/ЖЭ из ВОЛЖ, области аортального клапана или эпикардиальной ЖТ/ЖЭ рекомендовано у симптомных пациентов при неэффективности приема ≥1 ААП IC класса, а также при нежелании пациентов находиться на долгосрочной ААТ (ЕОК IIaB).
Катетерная аблация для лечения ЖТ/ЖЭ из синусов Вальсальвы рекомендована только при неэффективности ААТ IC класса (ЕОК IC).
Эпикардиальный подход для аблации ЖТ/ЖЭ рекомендован только после неэффективной эндокардиальной аблации ВТ-ЖТ/ЖЭ (ЕОК IC).
Большинство очаговых эпикардиальных ЖТ возникают в непосредственной близости от больших сердечных вен или коронарных артерий, и главным риском такой процедуры является повреждение коронарной артерии.
2. Идиопатическая левожелудочковая тахикардия
Чаще всего встречается фасцикулярная ЖТ с локализацией цепи риентри в области разветвлений задней ветви левой ножки пучка Гиса (> 90%), изредка – передней ветви, которая развивается главным образом у молодых людей без структурной патологии сердца. Методом первого выбора для лечения таких пациентов в специализированных центрах является катетерная аблация, поскольку заболевание встречается в основном у лиц молодого возраста, и длительное медикаментозное лечение в этом случае неэффективно. Частота рецидивов тахикардии после успешной аблации колеблется от 0 до 20% ЖТ с циркуляцией возбуждения по ножкам пучка Гиса обычно наблюдается у пациентов с ранее существовавшими нарушениями внутрижелудочкового проведения, включая удлинение интервала H-V и блокаду ножки пучка Гиса. Такая тахикардия хорошо поддается лечению с помощью катетерной аблации, по крайней мере в специализированных центрах. Чаще всего выполняют аблацию правой ножки, реже левой ножки пучка Гиса, результатом чего является отсутствие индуцируемой ЖТ и, по сути, полное излечение от ЖТ.
3. Желудочковая тахикардия из папиллярных мышц
Если лечение ЖТ/ЖЭ из области папиллярных мышц ААП IC класса и/или бета-адреноблокаторами оказалось неуспешным, рекомендована катетерная аблация, которая обычно дает нужный эффект (ЕОК IC).
У небольшого числа пациентов идиопатическая ЖТ или ЖЭ могут возникать в области папиллярных мышц ПЖ или ЛЖ. Для ЖТ, источником которой является задняя папиллярная мышца ЛЖ, характерна морфология по типу блокады правой ножки пучка Гиса, смещение оси QRS вверх вправо или влево и длительность QRS >150 мс. Однако при картировании и выполнении аблации в зоне папиллярных мышц достаточно сложно достичь стабильного положения катетера, в связи с чем рекомендуется транссептальный доступ в ряде случаев и контроль с помощью внутрисердечной эхокардиографии. Успешная аблация может осложняться митральной регургитацией, которая, однако, встречается редко.
4. Желудочковая тахикардия из области кольца митрального или трехстворчатого клапана
При отсутствии эффекта от лечения ЖТ/ЖЭ из области кольца митрального или трехстворчатого клапана ААП IC класса и/или бета-адреноблокаторами рекомендована катетерная аблация (в специализированных центрах) (ЕОК IC) [1].
Около 5% всех идиопатических ЖТ и ЖЭ возникают в области кольца митрального клапана [80, 81, 82]. Для них характерна морфология блокады правой ножки пучка Гиса, персистирующая волна S в отведении V6 и расположение переходной зоны в отведении V1, а в некоторых случаях и между отведениями V1 и V2. Порядка 8% всех идиопатических ЖТ и ЖЭ возникают в области кольца трехстворчатого клапана. В этом случае отмечают морфологию блокады левой ножки и отклонение оси QRS влево.
5. Идиопатическая фибрилляция желудочков
Имплантация ИКД рекомендована пациентам, пережившим эпизод идиопатической ФЖ для лечения ЖТ/ФЖ и профилактики ВСС. ЕОК IВ
При наличии рецидивирующей ЖЭ-индуцированной ФЖ и показаний к ИКД-терапии рекомендовано для лечения ЖТ/ФЖ и профилактики ВСС выполнение катетерной аблации опытными специалистами (ЕОК IВ) [6].
При наличии ЖЭ, являющейся причиной электрического шторма, для лечения ЖТ/ФЖ и профилактики ВСС рекомендовано выполнение катетерной аблации опытными специалистами (ЕОК IIaВ) [3].
6. Катетерная аблация у пациентов со структурной патологией сердца/ДЛЖ
У пациентов с ДЛЖ и стойкой ЖТ патофизиологический механизм аритмии во многих случаях заключается в формировании круга риентри на фоне рубцовых изменений, и целью аблации является критический перешеек в области этого круга. ЖТ у таких пациентов чаще всего имеет мономорфный характер. В настоящее время нет единого мнения о выборе критериев эффективности процедуры. Более предпочтительной конечной точкой может быть отсутствие любых индуцируемых ЖТ. В случае развития электрического шторма выполнение катетерной аблации может способствовать его прекращению, а также снизить частоту повторных эпизодов по сравнению с медикаментозной терапией.
В целом, успех процедуры в каждом конкретном случае зависит от размеров постинфарктного рубца, который можно оценить по областям низкого вольтажа при электроанатомическом картировании. Необходимым условием является выполнение аблации бригадой опытного специализированного центра.
Выполнение неотложной катетерной аблации в специализированных и опытных центрах рекомендовано пациентам с непрерывной ЖТ или электрическим штормом, приводящим к повторному нанесению шоков ИКД (ЕОК I B).
Назначение амиодарона или катетерная аблация рекомендованы пациентам с повторными шоками ИКД вследствие устойчивой ЖТ (ЕОК I B).
Рекомендовано назначение амиодарона или выполнения катетерной аблации после регистрации первого эпизода устойчивой ЖТ у пациентов с ИКД (ЕОК IIA B).
У пациентов с ДЛЖ, направленным на катетерную аблацию ЖА, препроцедурная или внутрипроцедурная визуализация рекомендуется для исключения тромбоза полостей сердца (ЕОК I B).
У пациентов с неишемической или ишемической КМП, направленных на катетерную аблацию ЖТ, рекомендована МРТ-визуализация миокарда для повышения эффективности вмешательства и снижения вероятности рецидивов ЖТ (ЕОК IIa B).
У пациентов с рубец-ассоциированной ЖТ рекомендована аблация субстрата для повышения эффективности вмешательства и снижения вероятности рецидивов ЖТ (ЕОК I B).
Рекомендовано мультиэлектродное картирование высокой плотности для более полной характеристики аритмогенной ткани во время катетерной аблации рубец-ассоциированной ЖТ для повышения эффективности вмешательства и снижения вероятности рецидивов ЖТ (ЕОК IIа B).
7. Желудочковая экстрасистолия у пациентов со структурной патологией сердца/ДЛЖ
У пациентов со структурной патологией сердца/ДЛЖ с частой симптомной ЖЭ или НУЖТ рекомендовано выполнение катетерной аблации (ЕОК IIа B)
При наличии ДЛЖ, ассоциированной с ЖЭ, рекомендовано проведение катетерной аблации (ЕОК IIа B).
8. Аритмогенная кардиомиопатия правого желудочка
Пациентам с АКПЖ для профилактики ВСС рекомендуют воздержаться от участия в соревновательных видах спорта (ЕОК I С).
Бета-адреноблокаторы в максимально переносимой дозе рекомендованы в качестве терапии первой линии пациентам с АКПЖ для устранения симптомов у пациентов с частой ЖЭ и НУЖТ (ЕОК I С).
Имплантация ИКД для вторичной профилактики ВСС рекомендована пациентам с АКПЖ с внезапной остановкой сердца в анамнезе и ЖТ с нарушениями гемодинамики (ЕОК I С).
Для устранения симптомов у пациентов АКПЖ с частой ЖЭ и НУЖТ, которые не переносят бета-адреноблокаторы или имеют противопоказания к ним, рекомендовано назначение амиодарона (ЕОК IIа С).
Выполнение катетерной аблации рекомендовано в специализированном центре у пациентов АКПЖ с частой симптомной ЖЭ/ЖТ, не отвечающей на медикаментозную терапию, в целях устранения симптомов и предотвращения срабатываний ИКД.
Рекомендована имплантация ИКД у пациентов с АКПЖ и устойчивой ЖТ без выраженных нарушений гемодинамики, с учетом рисков ИКД (включая риск отдаленных осложнений) и пользы такой терапии для пациента (ЕОК IIа B).
Имплантация ИКД рекомендована у взрослых пациентов с АКПЖ с одним или более факторов риска ЖА при ожидаемой продолжительности жизни свыше одного года, после тщательного обследования, с учетом риска отдаленных осложнений, а также влияния ИКД на образ жизни, социально-экономический статус и психическое здоровье пациента (ЕОК IIb C).
К факторам риска относят необъяснимые обмороки, частые эпизоды НУЖТ, семейный анамнез ВС в молодом возрасте, тяжелое поражение ПЖ, выраженное расширение QRS, наличие позднего гадолиниевого усиления при МРТ (в т. ч. с вовлечением ЛЖ), ДЛЖ, индукцию ЖТ во время ЭФИ.
Для стратификации риска ВСС рекомендовано выполнение эндокардиального ЭФИ с программированной стимуляцией желудочка (ЕОК IIb C).
9. Синдром удлиненного интервала QT
Средний возраст манифестации клинических проявлений – 14 лет. Годовой показатель ВСС у пациентов с нелеченным СУИQT составляет от 0,3 до 0,9%, тогда как синкопе возникают у 5% в год. Генетический скрининг выявляет патологические мутации в 75% случаев СУИQT в трех основных генах (KCNQ1, KCNH2 и SCN5A – типы СУИQT 1, 2 и 3 соответственно), что составляет 90% положительно генотипированных случаев. Стратификация индивидуального риска осуществляется с учетом клинических, электрокардиографических и генетических параметров. К профилактическому применению ИКД следует подходить индивидуально у всех пациентов группы высокого риска, в частности у женщин с генотипом LQT2 и QTc >500 мс, у пациентов с QTc >500 мс и признаками электрической нестабильности, а также у пациентов с генетическим профилем высокого риска (носительство двух мутаций, в том числе синдрома Джервелла-Ланге-Нильсена и синдрома Тимоти). На сегодняшний день нет данных, свидетельствующих о прогностической значимости инвазивного ЭФИ с программированной стимуляцией желудочков у пациентов с СУИQT.
Следующие мероприятия по коррекции образа жизни рекомендованы всем пациентам с диагностированным СУИQT:
Избегать приема медикаментов, способствующих удлинению интервала QT (перечень на сайте www.crediblemeds.org).
Корректировать нарушения электролитного баланса (гипокалиемию, гипомагниемию, гипокальциемию), которые могут развиваться на фоне диареи, рвоты или метаболических нарушений.
Избегать специфических триггеров аритмии (активное плавание, особенно при 1-м типе синдрома удлиненного интервала QT, и воздействие громких звуков при 2-м типе заболевания).
Выявление и устранение причин удлинения интервала QT (прежде всего, отмена любых лекарственных средств, способных удлинять интервал QT, если таковые применяются, коррекция электролитных нарушений, устранение брадикардии) рекомендовано пациентам с полиморфной ЖТ типа torsade de pointes (ЕОК IIa).
Пациентам с СУИQT для профилактики ВСС рекомендован прием бета-адреноблокаторов (ЕОК IB).
Назначение бета-адреноблокаторов для профилактики ВСС рекомендовано у носителей генетической мутации LQTS с нормальным QT-интервалом (ЕОК IIa B).
Временная ЭКС с частотой ≥100 имп/мин рекомендуется для укорочения интервала QT и предупреждения рецидивов полиморфной ЖТ типа torsade de pointes при отсутствии эффекта от введения магния сульфата (ЕОК I С).
Временная стимуляция может быть проведена с использованием системы трансвенозной электрической стимуляции сердца. Навязывание более высокой частоты сокращений сердца приводит к укорочению интервала QT и способствует предотвращению рецидивов полиморфной ЖТ типа torsade de pointes. Продолжительность ЭКС определяется временем, необходимым для устранения причины удлинения интервала QT, например, временем экскреции того или иного препарата, явившегося причиной удлинения интервала QT.
Если причиной удлинения интервала QT с развитием полиморфной ЖТ типа torsade de pointes является брадикардиия (например, при полной АВ-блокаде), ЭКС должна быть первым и основным этапом лечения, а при наличии соответствующих возможностей сразу же рекомендуется постоянная ЭКС с имплантацией искусственного водителя ритма сердца.
В случае возникновения полиморфной ЖТ типа torsade de pointes у пациентов с имплантированными кардиостимуляторами, ИКД или СРТ-устройствами возможно временное изменение базовой частоты стимуляции имплантированного устройства.
С целью купирования полиморфной ЖТ типа torsade de pointes применение ААП (особенно ААП IA и III класса) не рекомендовано (ЕОК III C).
Внутривенное введение магния сульфата рекомендовано для предупреждения рецидивов полиморфной ЖТ типа torsade de pointes (ЕОК IС)
Имплантация ИКД в сочетании с приемом бета-адреноблокаторов рекомендована пациентам с СУИQT, пережившим остановку сердца (ЕОК IB)
Имплантацию ИКД в сочетании с приемом бета-адреноблокаторов следует рекомендовать пациентам с СУИQT и синкопальными состояниями и/или ЖТ на фоне приема адекватной дозы бета-адреноблокаторов.
Выполнение грудной левосторонней симпатической денервации сердца рекомендовано у симптомных пациентов с СУИQT в следующих случаях:
Прием бета-адреноблокаторов неэффективен, плохо переносится, либо имеются противопоказания.
ИКД-терапия противопоказана или имеется отказ пациента.
Пациенты с имплантированным ИКД на фоне приема бета-адреноблокаторов продолжают испытывать множественные разряды дефибриллятора (ЕОК IIa С).
Лечение ранолазином (45 мг/ч в течение 3 часов, затем 90 мг/ч в течение 5 часов) рекомендовано в качестве дополнительной терапии с целью уменьшения длительности интервала QT у пациентов с СУИQT 3-го типа и увеличением QTc >500 мс (ЕОК IIb С).
Имплантация ИКД рекомендована в дополнение к терапии бета-адреноблокаторами у асимптомных носителей патологической мутации в генах KCNH2 или SCN5A при увеличении QTc >500 мс (ЕОК IIb С).
10. Синдром короткого интервала QT (СКИQT)
Синдром характеризуется уменьшенной продолжительностью реполяризации сердца, которая является субстратом для развития жизнеугрожающих аритмий. Идентифицированы пять генов, связанных с СКИQT: KCNH2, KCNQ1, KCNJ2, CACNA1C и CACNB2b. Но положительный результат генетического скрининга остается невысоким (всего 20%). Заболевание является летальным во всех возрастных группах, включая детей в первые месяцы жизни, и вероятность первой остановки сердца к возрасту 40 лет составляет 40%. Весьма вероятно, что СКИQT является недодиагностированным состоянием в общей популяции.
Показания к применению ИКД в каждом случае рассматривают индивидуально, учитывая семейный анамнез и наличие укороченного QTc, однако для общих рекомендаций на данный момент недостаточно данных.
На сегодняшний день нет данных о том, что программированная стимуляция желудочков позволяет прогнозировать аритмические события у пациентов с СКИQT.
Имплантация ИКД для профилактики ВСС рекомендована пациентам с СКИQT, которые:
Пережили остановку сердца и/или
Имеют документированную спонтанную устойчивую ЖТ. (ЕОК IС)
Назначение соталола рекомендовано для профилактики ВСС у пациентов с диагностированным синдромом короткого интервала QT, имеющих показания к ИКД-терапии, в случае, когда данная процедура противопоказана или имеется отказ пациентов (ЕОК IIb С).
Назначение соталола рекомендовано для профилактики ВСС у асимптомных пациентов с диагностированным СКИQT, имеющих семейный анамнез ВСС (ЕОК IIb С).
Следующие мероприятия по коррекции образа жизни рекомендованы всем пациентам с диагностированным синдромом Бругада:
Имплантация ИКД рекомендована пациентам с диагностированным синдромом Бругада, которые:
Имплантация ИКД рекомендована у пациентов со спонтанными ЭКГ-проявлениями 1-го типа синдрома Бругада и синкопальными состояниями в анамнезе (ЕОК IIa С).
11. Синдром Бругада
Синдром Бругада – каналопатия с доминантным наследованием и различной пенетрантностью, зависимой от возраста и пола: клинические проявления заболевания встречаются чаще у взрослых и в 8 раз чаще у мужчин, чем у женщин. ФЖ встречается в среднем возрасте 41±15 лет, но может возникать в любом возрасте, обычно во время отдыха или сна. Лихорадка, чрезмерное употребление алкоголя и обильное питание – это триггеры, которые позволяют выявить ЭКГ 1-го типа и предрасполагают к ФЖ. Синдром Бругада диагностируется у пациентов с подъемом сегмента ST с морфологией 1-го типа ≥2 мм в одном или нескольких правых прекордиальных отведениях V1 и/или V2, расположенных во втором, третьем или четвертом межреберье, возникающих либо спонтанно, либо после провокационного лекарственного теста с внутривенным введением ААП IC класса (такого как прокаинамид), или при регистрации ЭКГ в верхних прекордиальных отведениях (межреберных промежутках на 1-2 ребра выше положений электродов в V1 и V2.
Единственная возможность снизить риск ВСС при синдроме Бругада заключается в использовании ИКД, который рекомендован всем пациентам с подтвержденной ЖТ или ФЖ и при спонтанном появлении ЭКГ 1-го типа, а также при наличии обмороков в анамнезе.
Следующие мероприятия по коррекции образа жизни рекомендованы всем пациентам с диагностированным синдромом Бругада:
Избегать приема медикаментов, которые могут провоцировать элевацию сегмента ST в правых грудных отведениях (www.brugadadrugs.org).
Избегать избыточного употребления алкоголя и переедания.
Немедленно принять меры для снижения температуры тела при возникновении лихорадки любого генеза (ЕОК IС).
Имплантация ИКД рекомендована пациентам с диагностированным синдромом Бругада, которые:
Пережили остановку сердца и/или
Имеют документированную спонтанную устойчивую ЖТ (ЕОК IС)
Имплантация ИКД рекомендована у пациентов со спонтанными ЭКГ-проявлениями 1-го типа синдрома Бругада и синкопальными состояниями в анамнезе (ЕОК IIa С).
Имплантация ИКД рекомендована у пациентов с диагностированным синдромом Бругада, у которых развивается ФЖ во время программированной желудочковой стимуляции в двух точках с 2-мя или 3-мя экстрастимулами (ЕОК IIb С).
Выполнение катетерной аблации рекомендовано у пациентов с наличием в анамнезе электрического шторма или повторных мотивированных срабатываний ИКД с нанесением шоков (ЕОК IIb С).
12. Катехоламинергическая полиморфная ЖТ
Это редкое наследственное аритмогенное заболевание, характеризующееся адренергически-индуцируемой двунаправленной и полиморфной ЖТ. Заболеваемость имеет предполагаемую распространенность 1 на 10 000. Были идентифицированы два генетических типа КПЖТ. Клинические проявления КПЖТ обычно возникают в первом десятилетии жизни и вызваны физической активностью или эмоциональным стрессом. Диагностика является сложной задачей, поскольку пациенты с КПЖТ имеют нормальную ЭКГ и эхокардиограмму; для установления диагноза рекомендуется ХМЭКГ и/или тест с физической нагрузкой, во время которого появляются предсердные и желудочковые аритмии (двунаправленная или полиморфная ЖТ).
Независимыми прогностическими факторами для аритмических событий в случае КПЖТ являются выявление заболевания в детском возрасте, отсутствие терапии бета- адреноблокаторами и персистирующие сложные аритмии. Первая линия терапии КПЖТ включает неселективные бета-адреноблокаторы (без внутренней симпатомиметической активности) и модификацию образа жизни с ограничением физических нагрузок.
Левосторонняя симпатическая денервация сердца оказывает определенный эффект при КПЖТ у пациентов, которые не переносят бета-адреноблокаторы. Пациентам, пережившим остановку сердца, рекомендованы прием бета- адреноблокаторов и ИКД-терапия; если такое лечение по результатам стресс-теста не позволяет достичь полного контроля аритмии, следует рассмотреть комбинированную ААТ.
Имплантация ИКД возможна у пациентов с КПЖТ, которые не отвечают на лечение бета-адреноблокаторами. При программировании ИКД увеличивают продолжительность детекции ЖТ, поскольку нанесение разрядов может быть болезненным и способствовать повышению симпатического тонуса и провоцировать повторные эпизоды аритмии, что в конечном итоге ведет к возникновению порочного круга с рецидивирующими ЖА, вплоть до смертельного исхода.
Всем пациентам с диагностированной КПЖТ рекомендуется избегать соревновательных видов спорта, силовых тренировок и стрессовых ситуаций (ЕОК I С).
Прием бета-адреноблокаторов рекомендован для лечения аритмии и профилактики ВСС всем пациентам с диагностированной КПЖТ, учитывая наличие документированной спонтанной или стресс-индуцированной ЖА (ЕОК IС).
Имплантация ИКД дополнительно к приему бета-адреноблокаторов в сочетании или без ААП I или III класса рекомендована для лечения аритмии и профилактики ВСС пациентам с диагностированной КПЖТ, пережившим остановку сердца, имеющим в анамнезе повторные синкопальные состояния или эпизоды полиморфной/двунаправленной ЖТ, несмотря на оптимальную медикаментозную терапию (ЕОК IС).
Терапия бета-адреноблокаторами рекомендована родственникам пациента для профилактики ВСС при выявлении генетических мутаций, даже при отрицательном результате нагрузочного тестирования (ЕОК IIa С).
Выполнение грудной левосторонней симпатической денервации сердца рекомендовано у пациентов с диагностированной КПЖТ и повторными синкопальными состояниями, полиморфной/двунаправленной ЖТ, несколькими мотивированными срабатываниями ИКД с нанесением разрядов на фоне изолированного приема бета-адреноблокаторов или в сочетании с ААП I или III класса, а также при наличии непереносимости или противопоказаний к их приему (ЕОК IIb С).
13. Применение имплантируемого кардиовертера-дефибриллятора у пациентов с врожденными пороками сердца
Имплантация ИКД рекомендована пациентам с ВПС с устойчивыми симптомными пароксизмами ЖТ (ЕОК IB).
Пациентам должно быть выполнено инвазивное исследование гемодинамики и инвазивное ЭФИ. Необходимо рассмотреть возможность применения альтернативных методов лечения, таких как катетерная аблация или хирургическое вмешательство для устранения ЖТ. В случаях невозможности устранения ЖТ данными методами показана имплантация ИКД.
Применение ИКД рекомендовано у пациентов с ВПС и обмороками неизвестного происхождения в сочетании с тяжелой дисфункцией желудочков и/или индуцируемой устойчивой ЖТ/ФЖ при проведении эндоЭФИ (ЕОК IIaB).
Имплантация ИКД рекомендована взрослым пациентам с ВПС и ДЛЖ (ФВ <35%), симптомной ХСН на фоне оптимальной медикаментозной терапии с II или III ФК по NYHA (ЕОК IC).
Имплантация ИКД рекомендована у некоторых пациентов с тетрадой Фалло и несколькими факторами риска ВСС, включая ДЛЖ, неустойчивую ЖТ, QRS >180 мс или индуцируемую устойчивую ЖТ при ПСЖ (ЕОК IIaB).
Имплантация ИКД рекомендована у пациентов с тяжелой дисфункцией единственного желудочка или системного правого желудочка при наличии других факторов риска, включая неустойчивую ЖТ, ХСН II или III ФК по NYHA и выраженную регургитацию на системном АВ-клапане (ЕОК IIbB).
14. Воспалительные, ревматические поражения сердца и его клапанного аппарата, болезни накопления
Пациентов с угрожающими жизни устойчивыми ЖТА и клиническим подозрением на миокардит/перикардит рекомендуется направлять в специализированные центры, где возможны мониторинг гемодинамики, катетеризация сердца и эндомиокардиальная биопсия, а также применение устройств механической поддержки сердечно-легочной деятельности и специфических методов лечения аритмий (ЕОК IC).
Временный кардиостимулятор рекомендован пациентам с брадикардией и/или блокадой сердца, которые провоцируют ЖА во время острой фазы миокардита/панкардита (ЕОК IC).
Рекомендовано назначение ААТ пациентам с симптомной неустойчивой или устойчивой ЖТ во время острой фазы миокардита (ЕОК IIaC).
Рекомендовано при воспалительных заболеваниях сердца рассмотреть вопрос об имплантации ИКД или кардиостимулятора после разрешения острой фазы (ЕОК IIaC).
Применение ИКД у пациентов с устойчивой ЖТ и нарушениями гемодинамики целесообразно после разрешения острой фазы в случае развития вторичной кардиомиопатии, если ожидаемая продолжительность жизни составляет более одного года с хорошим функциональным статусом.
Рекомендовано применение дефибриллятора носимой системы длительной регистрации сердечного ритма (носимого дефибриллятора) для поддержки в период выздоровления или до установки ИКД пациентам с воспалительными заболеваниями сердца и остаточной тяжелой дисфункцией ЛЖ и/или электрической нестабильностью желудочка (ЕОК IIa C).
Рекомендовано рассмотреть вопрос о раннем применении ИКД у пациентов с гигантоклеточным миокардитом или саркоидозом, имеющих устойчивую ЖА с нарушением гемодинамики или переживших остановку сердца, учитывая плохой прогноз при данных заболеваниях, если ожидаемая продолжительность жизни составляет более одного года с хорошим функциональным статусом (ЕОК IIb C).
Наличие персистирующей воспалительной инфильтрации миокарда (по данным иммуногистохимического анализа) и/или аномальных скоплений фиброзной ткани (по данным МРТ) после острого миокардита можно рассматривать как дополнительный маркер высокого риска ВСС при воспалительных заболеваниях сердца. При остром и молниеносном миокардите в дополнение к медикаментозной терапии рекомендуется агрессивная поддержка гемодинамики с помощью чрескожной системы сердечно-легочной поддержки или внутриаортальной баллонной контрпульсации, чтобы сохранить жизнь пациента в тяжелую, но преодолимую острую фазу заболевания. Переход к чрескожной системе сердечно-легочной поддержки необходим в том случае, если рефрактерная ЖТ или ФЖ не отвечает на несколько попыток дефибрилляции (от трех до пяти).
Имплантацию ИКД рекомендуется отложить до разрешения острой фазы миокардита. Поскольку в это время миокардит уже может полностью разрешиться, показания к ИКД и временные рамки остаются спорными, даже после острой фазы заболевания.
При злокачественной ЖА или блокаде сердца при гигантоклеточном миокардите, болезни Лайма (клещевой боррелиоз), дифтерийном миокардите либо саркоидозе сердца рекомендована имплантация ИКД в раннем периоде, учитывая высокий риск аритмической смерти и потребность в трансплантации сердца.
У пациентов с подтвержденной устойчивой ЖТ неясной этиологии, сопровождающейся клинической симптоматикой, также следует исключить диагноз миокардита. МРТ у таких пациентов может показать аномальные участки фиброзной ткани в толще миокарда, чаще всего в субэпикардиальной и интрамуральной зонах.
16. Поражение клапанов сердца
15. Эндокардит
Появление ЖА у пациентов с инфекционным эндокардитом свидетельствует об очень плохом прогнозе. Однако каких-либо специальных рекомендаций по лечению аритмий в этой группе пациентов нет. Формирование абсцесса в области фиброзного кольца клапана (чаще аортального, реже митрального) может привести к блокаде сердца I или II степени. При первом эпизоде блокады сердца у пациента с эндокардитом следует сразу исключить абсцесс сердца.
Хирургическое лечение рекомендовано при остром нарушении гемодинамики в связи с остро возникшей аортальной регургитацией на фоне эндокардита, которое может привести к устойчивой ЖТ (ЕОК IIb C).
16. Поражение клапанов сердца
Поражение клапанов сердца, по всей вероятности, является главной причиной около 7% обращений для установки ИКД в целях вторичной профилактики. Было показано, что для пациентов с поражением клапанов сердца, которым устанавливают ИКД в целях первичной или вторичной профилактики ВСС, характерны такая же частота обоснованных срабатываний ИКД и такие же показатели смертности, что и для пациентов с ИБС или ДКМП.
ИКД рекомендован пациентам с заболеваниями клапанов сердца, которые после хирургической реконструкции клапана имеют показания к первичной или вторичной профилактике ВСС (ЕОК I C).
Хирургическая коррекция острой аортальной регургитации, возникшей на фоне эндокардита и сопровождающейся устойчивой ЖТ, рекомендована при отсутствии противопоказаний к такому методу лечения.
Выполнение ЭФИ с катетерной аблацией рекомендовано у пациентов, у которых после операции на клапане сердца появилась ЖТ, в целях выявления и устранения ЖТ с циркуляцией возбуждения по ножкам пучка Гиса (ЕОК IIa C).
17. Лечение ЖТ во время беременности
Лечение бета-адреноблокаторами рекомендуется во время беременности и в послеродовом периоде пациенткам с СУИQT или КПЖТ (ЕОК I C).
Назначение метопролола, пропранолола или верапамила во время беременности внутрь рекомендуется для длительной терапии идиопатической устойчивой ЖТ (ЕОК I C).
Экстренная электрическая кардиоверсия во время беременности рекомендуется для купирования аритмии при устойчивой ЖТ, особенно с нарушением гемодинамики (ЕОК I C).
При наличии соответствующих показаний выполнение имплантации ИКД рекомендуется во время беременности (ЕОК I C).
Внутривенное введение соталола или прокаинамида во время беременности рекомендовано для экстренной конверсии мономорфной устойчивой ЖТ без нарушений гемодинамики (ЕОК IIa C).
Внутривенное введение амиодарона во время беременности рекомендовано для экстренной конверсии мономорфной устойчивой ЖТ с нарушением гемодинамики, рефрактерной к электрической кардиоверсии или не отвечающей на медикаментозную терапию (ЕОК IIa C).
Выполнение катетерной аблации во время беременности рекомендовано для лечения рефрактерных к медикаментозной терапии и плохо переносимых тахикардий (ЕОК IIb C).
Беременность ассоциирована со значительным риском неблагоприятных событий у женщин со структурной патологией сердца. У женщин с врожденным СУИQT отмечают существенное повышение риска сердечных событий в послеродовом периоде (в течение 40 недель после родов), в связи с чем им необходимо применение бета-адреноблокаторов во время беременности и в послеродовом периоде. У женщин с синдромом Бругада беременность, роды и послеродовый период обычно проходят без дополнительных рисков. Риск повторной ЖТ выше у пациенток с ЖТ в анамнезе и структурной патологией сердца.
18. Аритмии, связанные с послеродовой кардиомиопатией
Послеродовая (перипартальная) кардиомиопатия характеризуется развитием систолической ДЛЖ и СН на поздних сроках беременности или в течение нескольких месяцев после родов. Следствием послеродовой кардиомиопатии могут быть сложные ЖА и внезапная остановка сердца. У всех пациенток с впервые возникшей ЖТ в последние 6 недель беременности или в раннем послеродовом периоде следует исключить послеродовую кардиомиопатию.
При развитии угрожающих жизни ЖТА прибегают к электрической кардиоверсии. Применение ИКД у пациенток с ЖА или низкой ФВЛЖ следует стандартным рекомендациям. При этом следует учитывать высокую частоту (50%) спонтанного разрешения дилатационной кардиомиопатии после родов
19. Обструктивное апноэ сна.
Рекомендуется рассматривать в качестве причины при дифференциальной диагностике брадиаритмий синдром ночного апноэ (ЕОК IIa B).
Рекомендуется рассматривать ночное апноэ и снижение сатурации кислорода как факторы риска ВСС у пациентов с нарушением дыхания во время сна (ЕОК IIb C).
Результаты последних исследований указывают на связь обструктивного ночного апноэ с повышенной смертностью. Показано, что обструктивное ночное апноэ с уменьшением средней ночной сатурации кислорода <93%, и минимальная ночная сатурация кислорода <78% являются независимыми факторами риска ВСС. По этой причине диагностика обструктивного ночного апноэ должна входить в алгоритм обследования для стратификации риска ВСС. Наиболее частыми НРС при синдроме ночного апноэ-гипопноэ являются синусовая брадикардия, синусовые паузы, АВ-блокады 1-й и 2-й степени типа Мобитц I, а также частые ЖЭ.
20. Гипертрофическая кардиомиопатия
При ГКМП отмечается значительное утолщение стенки ЛЖ, которое не может быть объяснено исключительно условиями повышенной нагрузки на ЛЖ. Данное определение относится к детям и взрослым и не предполагает никаких специфических этиологических причин.
Общая годовая смертность от ССЗ и смертность или частота срабатываний ИКД по поводу ЖТ/ФЖ у взрослых пациентов с ГКМП составляет 1-2 и 0,81% соответственно. Другими основными причинами сердечно-сосудистой смерти при ГКМП являются ХСН, тромбоэмболии и АВ-блокада. Калькулятор риска ВСС в течение 5 лет (Risk-ICD) расположен в интернете по адресу: http://doc2do.com/hcm/webHCM.html.
Пациентам с ГКМП ввиду высокого риска ВСС не рекомендуется участие в соревновательных видах спорта (ЕОК I C).
Рекомендуется имплантация ИКД у пациентов с ГКМП, перенесших остановку сердца по причине ЖТ или ФЖ, или у пациентов со спонтанной устойчивой ЖТ, приводящей к потере сознания или нарушению гемодинамики, при ожидаемой продолжительности жизни >1 года (ЕОК I B).
Стратификация риска у пациентов с ГКМП рекомендуется с использованием калькулятора Risk-ICD для оценки риска смерти в течение 5 лет у пациентов >16 лет без анамнеза устойчивой ЖТ (приводящей к нарушению гемодинамики или потере сознания) или ФЖ (ЕОК I B).
Пятилетний риск внезапной смерти рекомендуется оценивать при первоначальном обследовании пациента, а также каждые 1-2 года или при изменении клинического статуса (ЕОК I B).
Имплантация ИКД рекомендуется пациентам с предполагаемым 5-летним риском внезапной смерти ≥6% и ожидаемой продолжительностью жизни >1 года после подробного клинического обследования с оценкой риска последующих осложнений и влияния ИКД на образ жизни, социально-экономический статус и психологическое здоровье (ЕОК IIa B).
Имплантация ИКД рекомендована в отдельных группах пациентов с 5-летним риском ВСС от ≥4 до <6% и ожидаемой продолжительностью жизни >1 года после подробного клинического обследования с оценкой риска последующих осложнений и влияния ИКД на образ жизни, социально-экономический статус и психологическое здоровье (ЕОК IIb B).
Имплантация ИКД рекомендована у отдельных пациентов с 5-летним риском ВСС <4% при наличии клинических характеристик с доказанным прогностическим значением, и когда в результате оценки риска последующих осложнений и влияния ИКД на образ жизни, социально-экономический статус и психологическое здоровье предполагается общее положительное влияние имплантации ИКД (ЕОК IIb B).
Госпитализация
Показания к госпитализации в зависимости от вида оказания медицинской помощи
1) показания к плановой госпитализации:
Рекомендуется в зависимости от общего состояния основного заболевания (см. Тип планового лечения, указанный в клиническом протоколе основного заболевания)
2) показания к госпитализации в отделение неотложной помощи:
Пароксизмы желудочковой тахикардии (гемодинамически застойные и нестабильные типы)
Состояния предсинкопии и обморока неопределенной этиологии
Пациенты, перенесшие внезапную остановку сердца сразу после соответствующей реанимации
Информация
Источники и литература
-
Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2024
- 1. Юрак-қон томир касалликлари бўйича миллий клиник баённомалар. Тошкент. 2023. 584 бет 2. Клинические рекомендации. Желудочковые нарушения ритма. Желудочковые тахикардии и внезапная сердечная смерть. Российское кардиологическое общество (РКО) при участии Всероссийского научного общества специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции (ВНОА), Всероссийской общественной организации «Ассоциации детских кардиологов России», Общества холтеровского мониторирования и неинвазивной электрокардиологии. Министерство здравоохранения Российской Федерации 2020 год 3. Клинический протокол диагностики и лечения желудочковых нарушений ритма сердца и профилактики внезапной сердечной смерти. Министерство здравоохранения и социального развития Республики Казахстан. 2016 год. 4. 2020 APHRS/HRS expert consensus statement on the investigation of decedents with sudden unexplained death and patients with sudden cardiac arrest, and of their families. Heart Rhythm, Vol 18, No 1, January 2021. Pages e1-e50 5. 2019 HRS/EHRA/APHRS/LAHRS expert consensus statement on catheter ablation of ventricular arrhythmias. Heart Rhythm, Vol 17, No 1, January 2020. Pages e1-e154 6. 2017 AHA/ACC/HRS Guideline for Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death. Circulation. 2018;138:e272–e391 7. 2015 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: The Task Force for the Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death of the European Society of Cardiology (ESC) Endorsed by: Association for European Paediatric and Congenital Cardiology (AEPC), European Heart Journal, Volume 36, Issue 41, 1 November 2015, Pages 2793–2867 8. Piepoli M.F., Hoes A.W., Agewall S., et al; Authors/Task Force Members. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Eur Heart J. 2016; 37:2315–2381. doi:10.1093/eurheartj/ehw106.
Информация
В разработке клинического протокола и стандарта внесли вклад:
По организации процесса члены рабочей группы по направлению Кардиология:
1. Фозилов Х.Г. – директор РСНПМЦК, к.м.н., главный кардиолог МЗ
2. Низамов У.И. – заместитель директора по лечебной работе РСНПМЦК, PhD, кардиолог-консультант МЗ
3. Каримов А.М. – заместитель директора по филиалам РСНПМЦК, PhD, кардиолог-консультант МЗ
4. Курбанова Р.А. – заместитель главного врача РСНПМЦК
5. Толипова Ю.Ш. – доцент кафедры Кардиологии и геронтологии с курсом интервенционной кардологии и аритмологии Центра развития профессиональной квалификации медицинских работников, д.м.н., главный геронтолог МЗ
6. Ахматов Я.Р. – директор Каршинского филиала РСНПМЦК, к.м.н.
Рецензенты:
Список авторов:
1. Курбанов Р.Д. – академик АНРУз, профессор, д.м.н., главный консультант РСНПМЦК
2. Муллабаева Г.У. – д.м.н., научный руководитель лаборатории малоинвазивной хирургии и послеоперационной реабилитации РСНПМЦК
3. Нуриллаева Н.М. – д.м.н., заведующий кафедры внутренних болезней №1 ТМА
4. Кеворков А.Г. – к.м.н., в.н.с. лаборатории Аритмий сердца РСНПМЦК
5. Турсунов Э.Я. – м.н.с. лаборатории Аритмий сердца РСНПМЦК
6. Расулов А.Ш. – м.н.с. лаборатории Аритмий сердца РСНПМЦК
Рецензенты:
Асимбекова Э.У. – д.м.н., в.н.с. отделения клинической диагностики ФГБУ НМИЦ им Бакулева МЗРФ
Абдуллаев А.Х. - д.м.н. руководитель лаборатории реабилитации РСНПМЦТиМР МЗРУз
Клинический протокол рассмотрен и утвержден Ученым Советом Республиканского Специализированного Научно-Практического Медицинского Центра Кардиологии 25 сентября 2023 г., протокол №13.
Техническая экспертная оценка и редактирование:
Основная терминология
Коррекцию факторов риска требуется проводить не только пациенту, но и членам его семьи. Она осуществляется путем реализации программ семейной первичной профилактики и воспитания, составленных лечащим врачом:
Неотложные состояния, требующие вызова скорой медицинской помощи
Клинический протокол обсужден и рекомендован к утверждению путем достижения неформального консенсуса на заключительном Совещании рабочей группы с участием профессорско-преподавательского состава высших учебных заведений, членов ассоциации кардиологов Узбекистана, организаторов здравоохранения (коллектива ГУ РСНПМЦК и их заместителей), в онлайн-формате 1 ноября 2023 г.
Руководитель рабочей группы – к.м.н. Фозилов Х.Г, директор РСНПМЦК, главный кардиолог МЗ
Клинический протокол рассмотрен и утвержден Ученым Советом Республиканского Специализированного Научно-Практического Медицинского Центра Кардиологии 25 сентября 2023 г., протокол №13.
Председатель Учёного Совета – к.м.н. Фозилов Х.Г.
Техническая экспертная оценка и редактирование:
1. Низамов У.И. – заместитель директора по лечебной работе РСНПМЦК, PhD, кардиолог-консультант МЗ
2. Каримов А.М. – заместитель директора по филиалам РСНПМЦК, PhD, кардиолог-консультант МЗ
Данный клинический протокол и стандарт был разработан при организационной и методической поддержке под руководством заместителя министра д.м.н., Ф.Р. Шарипова, Начальника управления медицинского страхования Ш.К.Алмарданова, начальника отдела разработки клинических протоколов и стандартов д.м.н. С.А. Убайдуллаевой, Главных специалистов отдела разработки клинических протоколов и стандартов Ш.Р.Нуримова, С.К.Усманова и Г.Т.Джумаевой.
Список сокращений
ААТ антиаритмическая терапия
АВ атриовентрикулярный
АКПЖ аритмогенная кардиомиопатия правого желудочка
АЛЖ аневризма левого желудочка
ВАС внезапная аритмическая смерть
ВПС врожденный порок сердца
ВОС внезапная остановка сердца
ВСС внезапная сердечная смерть
ВСЭФИ внутрисердечное электрофизиологическое исследование
ВТЛЖ выходной тракт левого желудочка
ВТПЖ выходной тракт правого желудочка
ГКМП гипертрофическая кардиомиопатия
ДКМП дилатационная кардиомиопатия
ЕОК Европейское общество кардиологов
ЖТА желудочковая тахиаритмия
ЖТ желудочковая тахикардия
ЖЭ желудочковая экстрасистола
ИКД имплантируемый кардиовертер-дефибриллятор
КПЖТ катехоламинергическая полиморфная желудочковая тахикардия
КТ/ МСКТ мультиспиральная компьютерная томография
ХРЛЖ хиругическая реконструкция левого желудочка
МРТ магнитно-резонансная томография
НУЖТ неустойчивая желудочковая тахикардия
ОКС острый коронарный синдром
ПСВТ пароксизмальная суправентрикулярная тахикардия
ПСЖ программируемая стимуляция желудочков
РКИ рандомизированное контролируемое исследование
СВНС синдром внезапной необъяснимой смерти
СРЛ сердечно-легочная реанимация
СРТ сердечная ресинхронизирующая терапия
СРТ-Д сердечная ресинхронизирующая терапия-дефибриллятор
СРТ-П сердечная ресинхронизирующая терапия-пейсмейкер (кардиостимулятор)
СУИ QT синдром удлиненного интервала
QT СКИQT синдром короткого интервала
QT СУ-ЭКГ сигнал-усредненная ЭКГ
УЖТ устойчивая желудочковая тахикардия
ФВЛЖ фракция выброса левого желудочка
ФЖ фибрилляция желудочков
ФК функциональный класс
ФП фибрилляция предсердий
ХМЭКГ Холтеровское мониторирование электрокардиограммы
ХСН хроническая сердечная недостаточность
ЧКВ чрескожное коронарное вмешательство
ЧСС частота сердечных сокращений
ЭКГ электрокардиограмма
ЭМД электромеханическая диссоциация
ЭХОКГ эхокардиография
NYHA New York Heart Association QTc корригированный интервал
QT WPW-синдром Синдром Wolf-Parkinson-White
Данный клинический протокол и стандарт был разработан при организационной и методической поддержке под руководством заместителя министра д.м.н., Ф.Р. Шарипова, Начальника управления медицинского страхования Ш.К.Алмарданова, начальника отдела разработки клинических протоколов и стандартов д.м.н. С.А. Убайдуллаевой, Главных специалистов отдела разработки клинических протоколов и стандартов Ш.Р.Нуримова, С.К.Усманова и Г.Т.Джумаевой.
Список сокращений
ААТ антиаритмическая терапия
АВ атриовентрикулярный
АКПЖ аритмогенная кардиомиопатия правого желудочка
АЛЖ аневризма левого желудочка
ВАС внезапная аритмическая смерть
ВПС врожденный порок сердца
ВОС внезапная остановка сердца
ВСС внезапная сердечная смерть
ВСЭФИ внутрисердечное электрофизиологическое исследование
ВТЛЖ выходной тракт левого желудочка
ВТПЖ выходной тракт правого желудочка
ГКМП гипертрофическая кардиомиопатия
ДКМП дилатационная кардиомиопатия
ЕОК Европейское общество кардиологов
ЖТА желудочковая тахиаритмия
ЖТ желудочковая тахикардия
ЖЭ желудочковая экстрасистола
ИКД имплантируемый кардиовертер-дефибриллятор
КПЖТ катехоламинергическая полиморфная желудочковая тахикардия
КТ/ МСКТ мультиспиральная компьютерная томография
ХРЛЖ хиругическая реконструкция левого желудочка
МРТ магнитно-резонансная томография
НУЖТ неустойчивая желудочковая тахикардия
ОКС острый коронарный синдром
ПСВТ пароксизмальная суправентрикулярная тахикардия
ПСЖ программируемая стимуляция желудочков
РКИ рандомизированное контролируемое исследование
СВНС синдром внезапной необъяснимой смерти
СРЛ сердечно-легочная реанимация
СРТ сердечная ресинхронизирующая терапия
СРТ-Д сердечная ресинхронизирующая терапия-дефибриллятор
СРТ-П сердечная ресинхронизирующая терапия-пейсмейкер (кардиостимулятор)
СУИ QT синдром удлиненного интервала
QT СКИQT синдром короткого интервала
QT СУ-ЭКГ сигнал-усредненная ЭКГ
УЖТ устойчивая желудочковая тахикардия
ФВЛЖ фракция выброса левого желудочка
ФЖ фибрилляция желудочков
ФК функциональный класс
ФП фибрилляция предсердий
ХМЭКГ Холтеровское мониторирование электрокардиограммы
ХСН хроническая сердечная недостаточность
ЧКВ чрескожное коронарное вмешательство
ЧСС частота сердечных сокращений
ЭКГ электрокардиограмма
ЭМД электромеханическая диссоциация
ЭХОКГ эхокардиография
NYHA New York Heart Association QTc корригированный интервал
QT WPW-синдром Синдром Wolf-Parkinson-White
Таблица 1. Классы рекомендаций (ЕОК)
|
Классы
|
Определение |
| Класс I | Данный метод лечения/диагностический подход должен быть использован, польза от его применения существенно превышает сопутствующие риски |
| Класс IIa | Применение данного метода лечения/диагностического подхода целесообразно, польза от его применения превышает сопутствующие риски |
| Класс IIb | Данный метод лечения/диагностический подход может быть использован в определённых ситуациях, польза от его применения превышает сопутствующие риски или сопоставима с ними |
| Класс III | Данный метод лечения/диагностический подход не должен быть использован, т.к. он не оказывает пользы или может причинить вред. |
Таблица 2. Уровни доказательности данных
|
Уровень
|
Доказательная база |
| Уровень А | Доказательства получены в нескольких рандомизированных контролируемых исследованиях или мета-анализах этих исследований |
| Уровень В | Доказательства получены в одном рандомизированном контролируемом клиническом исследовании или крупных не рандомизированных исследованиях |
| Уровень С | В основе клинической рекомендации лежит мнение (соглашение) экспертови/или результаты небольших исследований, данные регистров |
Определения:
Желудочковые нарушения ритма сердца (ЖНРС) или Желудочковая тахиаритмия (ЖТА) – обобщенное название расстройств сердечного ритма, при которых источник эктопической активности или круга риентри находится ниже пучка Гиса, т. е. в его ветвях, сети Пуркинье или в миокарде желудочков.
Неустойчивая желудочковая тахикардия (НУЖТ) – 3 и более комплекса QRS, продолжительностью <30 сек.
Устойчивая желудочковая тахикардия – ЖТ, продолжительностью ≥ 30 сек.
Мономорфная ЖТ – ЖТ при наличии одинаковой конфигурации QRS-комплексов
Полиморфная ЖТ – нестабильная, меняющаяся конфигурация QRS-комплексов
Электрический шторм – более 3 эпизодов ЖТ/ФЖ в течение 24 часов
Трепетание желудочков – ритмичные, высокоамплитудные, уширенные электрические отклонения желудочков с частотой более 250 в мин., волны Т не определяются.
Фибрилляция желудочков – хаотическая электрическая активность в виде полиморфных осцилляций, постоянно изменяющихся по своей конфигурации, амплитуде, продолжительности и частоте, диапазон которой составляет от 300 и выше в 1 мин.
Внезапная смерть – непредвиденное смертельное событие, не связанное с травмой и возникающее в течение 1 ч с момента появления симптомов у практически здорового человека. Если смерть произошла без свидетелей, о внезапной смерти говорят в том случае, если погибший находился в удовлетворительном состоянии за 24 ч до смерти.
Внезапная сердечная смерть (ВСС) – термин применяется, если внезапная смерть возникла у субъекта с известным при жизни врожденным или приобретенным потенциально фатальным заболеванием сердца, или патология сердечно-сосудистой системы была выявлена на аутопсии и могла быть причиной смерти, или если очевидные экстракардиальные причины смерти по данным аутопсии не выявлены, и нарушение ритма служит наиболее вероятной причиной смерти.
Внезапная остановка сердца (ВОС) – непредвиденная остановка кровообращения, возникающая в течение 1 ч с момента появления острых симптомов, которая была устранена с помощью успешных реанимационных мероприятий (например, дефибрилляции) – «предотвращенная остановка сердца».
Идиопатическая желудочковая тахиаритмия – событие, когда клиническое обследование пациента не позволило выявить заболевания, потенциально ассоциированные с желудочковой тахиаритмией.
Первичная профилактика ВСС – мероприятия, направленные на снижение риска ВСС у лиц, имеющих повышенный риск ВСС, но без анамнеза угрожающих жизни аритмий или предотвращенной остановки сердца.
Вторичная профилактика ВСС – мероприятия, направленные на снижение риска ВСС у лиц, имеющих анамнез угрожающих жизни аритмий или предотвращенной остановки сердца
Таблица 12. Критерии оценки качества медицинской помощи
| № | Критерий качества | УДД | Оценка выполнения | Источник |
| 1 | Пациенту с остановкой кровообращения/синкопальным эпизодом выполнено ЭКГ и при диагностировании пароксизма ЖТ/ФЖ выполнены реанимационные мероприятия и экстренная кардиоверсия/дефибрилляция. | IIB | Да/нет | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| 2 | Пациенту с устойчивой желудочковой тахикардией выполнено купирование аритмии (медикаментозное, ЭИТ). | IIB | Да/нет | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| 3 | Выполнено ЭКГ-исследование покоя в 12-ти отведениях и/или холтеровское мониторирование ЭКГ (ХМЭКГ) пациентам при прохождении обследования на предмет выявления желудочковых аритмий (ЖА). | IA | Да/нет | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| 4 | Выполнено эхокардиографическое исследование и/или другие визуализирующие исследования для оценки функции ЛЖ и выявления структурной патологии сердца у пациента с ЖА. | IA | Да/нет | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| 5 | Начата/продолжена терапия бета-адреноблокаторами в лечении всех категорий пациентов со структурным поражением миокарда/дисфункцией ЛЖ, имеющих повышенный риск ВСС и нуждающихся в её первичной или вторичной профилактике. | IA | Да/нет | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| 6 | Проведена оптимальная медикаментозная терапия ингибиторами АПФ (или ангиотензина II антагонистами при непереносимости ингибиторов АПФ), бета-адреноблокаторами и антагонистами альдостерона пациентам с ХСН и систолической дисфункцией ЛЖ (ФВЛЖ≤35–40%) с целью снижения общей смертности и риска ВСС. | IA | Да/нет | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| 7 | При повторных срабатываниях/шоках ИКД*** вследствие устойчивой ЖТ проведена антиаритмическая терапия, при неэффективности или невозможности которой пациент направлен на консультацию к врачу, специализирующемуся на диагностике и лечении нарушений ритма сердца (кардиологу, сердечно-сосудистому хирургу, врачу рентгенэндоваскулярной диагностики и лечения) для решения вопроса о необходимости выполнения катетерной аблации. | IIB | Да/нет | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| 8 | Пациент с сохраняющейся дисфункцией левого желудочка (ФВЛЖ – 35% и менее) и сердечной недостаточностью (II или III ФК по NYHA), через 40 дней после инфаркта миокарда, направлен на консультацию к врачу, специализирующемуся на диагностике и лечении нарушений ритма сердца (кардиологу, сердечно-сосудистому хирургу, врачу рентгенэндоваскулярной диагностики и лечения) или в специализированный кардиологический центр для решения вопроса о необходимости имплантации ИКД***. | IA | Да/нет | https://pubmed.ncbi.nlm.nih.gov/27222591/ |
| 9 | При непрерывной некупирующейся ЖТ или электрическом шторме, приводящим к многократному повторному нанесению шоков ИКД***, с врачом, специализирующимся на диагностике и лечении нарушений ритма сердца (кардиологом, сердечно-сосудистом хирургом, врачом рентгенэндоваскулярной диагностики и лечения) обсуждена необходимость катетерной аблации в специализированных и опытных центрах. | IIB | Да/нет | https://pubmed.ncbi.nlm.nih.gov/33091602/ |
| 10 | При безуспешности медикаментозной терапии, сохранении приступов ЖТ, наличии дисфункции ЛЖ, ассоциированной с желудочковой экстрасистолией, пациент направлен на консультацию к врачу, специализирующемуся на диагностике и лечении нарушений ритма сердца (кардиологу, сердечно-сосудистому хирургу, врачу рентгенэндоваскулярной диагностики и лечения) или в специализированный кардиологический центр для решения вопроса о необходимости катетерной аблации для профилактики рецидивов аритмии и повторных срабатываний ИКД. | IB | Да/нет |
https://pubmed.ncbi.nlm.nih.gov/27222591/ |
Информация для пациента
Желудочковые нарушения ритма
Желудочковые тахикардии и внезапная сердечная смерть
Основная терминология
Желудочковые нарушения ритма или желудочковые тахиаритмии – обобщенное название расстройств сердечного ритма, при которых источник патологической электрической активности находится в ткани желудочков сердца.
Внезапная смерть – непредвиденное смертельное событие, не связанное с травмой и возникающее в течение 1 часа с момента появления симптомов у практически здорового человека. Если смерть произошла без свидетелей, о внезапной смерти говорят в том случае, если погибший находился в удовлетворительном состоянии за 24 часа до смерти.
Внезапная сердечная смерть (ВСС) – термин применяется, если внезапная смерть возникла у пациента с известным при жизни врожденным или приобретенным потенциально фатальным заболеванием сердца, или патология сердечно-сосудистой системы была выявлена посмертно и могла быть причиной смерти, или если очевидные внесердечные причины смерти не были выявлены, и нарушение ритма служит наиболее вероятной причиной смерти.
Социальная значимость
Внезапная сердечная смерть как необратимый исход и результат внезапной остановки сердца достигает 50% среди других исходов у лиц 35–50 лет, преимущественно мужского пола, однако в последнее время наблюдается тенденция к увеличению доли лиц женского пола, а также подросткового и юношеского возраста.
Почти в половине случаев остановка сердца у лиц старше 40 лет происходит без известных заболеваний сердца, однако большинство из них при этом имеют недиагностированную ишемическую болезнь сердца (ИБС). Снижение заболеваемости ИБС и другими видами сердечной патологии привело к уменьшению количества случаев ВСС почти на 40%. Существует генетическая предрасположенность к внезапной смерти. Описано прогностическое значение семейного анамнеза внезапной смерти – при наличии одного случая внезапной смерти в семье относительный ее риск возрастает практически вдвое, а при двух случаях внезапной смерти в семье риск увеличивается в 9 раз.
Бдительность по отношению к электрокардиографическим (ЭКГ) и эхокардиографическим признакам наследственных аритмогенных заболеваний является важной частью клинической практики и позволяет своевременно выявить лица с высоким риском ВСС. Скрининг ближайших родственников жертв внезапной смерти позволяет выявить лица в зоне риска, назначить соответствующее лечение и тем самым предотвратить другие случаи внезапной смерти в этой семье.
Коррекция сердечно-сосудистых факторов риска неблагоприятных исходов
Пациент должен знать об имеющихся у него и членов его семьи сердечно-сосудистых факторах риска — курении, избыточной массе тела, психоэмоциональном стрессе, малоподвижном образе жизни, повышенном уровне холестерина. Влияние указанных факторов риска может быть снижено. Особенно важна коррекция изменяемых факторов риска при наличии у пациента и членов его семьи некорригируемых факторов риска, к которым относятся: наличие в семейном анамнезе внезапной сердечной смерти, ранних мозговых инсультов, инфарктов миокарда, сахарного диабета; также к данным факторам относят мужской пол, пожилой возраст, физиологическую или хирургическую менопаузу у женщин.
Клинические проявления
Клинические проявления желудочковых тахиаритмий могут существенно различаться – от абсолютной бессимптомности до сердцебиения, дискомфорта в груди, загрудинной боли, удушья, головокружения, пресинкопальных и синкопальных состояний. Учащенное сердцебиение, предобморочное состояние и обмороки – три наиболее важных симптома, которые требуют визита к врачу и дополнительного обследования.
Коррекция сердечно-сосудистых факторов риска неблагоприятных исходов
Коррекцию факторов риска требуется проводить не только пациенту, но и членам его семьи. Она осуществляется путем реализации программ семейной первичной профилактики и воспитания, составленных лечащим врачом:
Индекс массы тела (Кетле) = масса тела в килограммах/(рост в м2);
Индекс талия/бедра (ИТБ): ИТБ = ОТ/ОБ, где ОТ (окружность талии) – наименьшая окружность, измеренная над пупком; ОБ (окружность бедер) – наибольшая окружность, измеренная на уровне ягодиц;
Интерпретация уровня холестерина плазмы:
- целевой уровень холестерина липопротеинов низкой плотности (ЛПНП) для пациентов с очень высоким риском <1,8 ммоль/л или его снижение не менее чем на 50% от исходного уровня, если он находился в диапазоне 1,8-3,5 ммоль/л (70-135 мг/дл);
- целевой уровень холестерина ЛПНП для пациентов с высоким риском <2,6 ммоль/л или его снижение не менее чем на 50% от исходного уровня, если он находился в диапазоне 2,6-5,2 ммоль/л (100-200 мг/дл);
- целевой уровень холестерина ЛПНП для пациентов с низким и умеренным риском <3 ммоль/л;
- Липопротеины высокой плотности (ЛПВП) >1,2 ммоль/л (у женщин), >1,0 ммоль/л (у мужчин);
- Целевой уровень триглицеридов <1,7 ммоль/л.
Уровень глюкозы в плазме крови натощак не выше 6,1 ммоль/л;
Уровень мочевой кислоты сыворотки крови <420 мкмоль/л (у мужчин), <360 мкмоль/л (у женщин).
Базовые советы пациенту и его семье
1. Достаточным считается сон не менее 7 часов в сутки;
2. Масса тела должна приближаться к идеальной (ИМТ менее 25 кг/м2). Для этого суточная калорийность пищи в зависимости от массы тела и характера работы должна составлять от 1500 до 2000 ккал. Потребление белка – 1 г/кг массы тела в сутки, углеводов – до 50г/сут, жиров – до 80 г/сут.
3. Желательно вести дневник питания; пациенту настоятельно рекомендуется избегать жирных, сладких блюд, отдавать предпочтение овощам, фруктам, злаковым и хлебу грубого помола;
4. Ограничение потребления соли до 5 г/сутки;
5. Следует употреблять в пищу продукты, богатые калием (свежие фрукты, овощи, курага, печеный картофель);
6. Необходимо прекратить или ограничить курение;
7. Потребление алкоголя следует ограничить до 30 мл/сут в пересчете на абсолютный этанол;
8. Согласование с лечащим врачом индивидуально приемлемых для пациента нагрузок: пешие прогулки, езда на велосипеде, ходьба на лыжах, работа в саду;
9. Психоэмоциональный стресс на производстве и в быту контролируется правильным образом жизни. Следует ограничить продолжительность рабочего дня и домашних нагрузок, избегать ночных смен, командировок;
10. Юношам, занимающимся спортом, нельзя злоупотреблять пищевыми добавками для наращивания мышечной массы и исключить прием анаболических стероидов.
Советы пациенту с имплантированным кардиовертером-дефибриллятором и/или устройством сердечной ресинхронизирующей терапии
Запрещается подвергаться воздействию мощных магнитных и электромагнитных полей, а также непосредственному воздействию любых магнитов вблизи места имплантации;
Запрещается подвергаться воздействию электрического тока;
Выполнение магнитно-резонансной томографии (МРТ) запрещено; исключение составляют системы ИКД и СРТ-Д (электроды и устройство), имеющие отметку о МРТ-совместимости;
Запрещается наносить удары в грудь в область имплантации ИКД/СРТ-Д, пытаться смещать аппарат под кожей;
Запрещается садиться за руль транспортного средства в первые 3 месяца после имплантации ИКД/СРТ-Д, а также в течение 3 месяцев после обоснованного срабатывания ИКД;
Запрещается применять монополярную электрокоагуляцию при хирургических вмешательствах (в т.ч. эндоскопических), применение биполярной коагуляции должно быть максимально ограничено;
Следует ограничить применение перфораторов и электродрелей, а также газонокосилок; косить вручную и колоть дрова необходимо с осторожностью, по возможности лучше отказаться от данного вида деятельности;
Нежелательны большие нагрузки на плечевой пояс;
Можно пользоваться компьютером и подобными ему устройствами, в том числе портативными;
Можно выполнять любые рентгеновские исследования, в том числе компьютерную томографию;
Можно работать по дому или на земельном участке, использовать электроинструмент, при условии его исправности;
Можно заниматься спортом, избегая контактно-травматических видов;
Пациент с ИКД/СРТ-Д должен своевременно являться к врачу для проверки устройства с использованием соответствующего программатора;
Пациент с ИКД/СРТ-Д должен знать название, модель имплантированного устройства; крайне желательно всегда иметь при себе паспорт, информационные данные об ИКД/СРТ-Д.
Советы пациенту после проведения интервенционного лечения желудочковых нарушений ритма
Ограничение среднетяжелых, тяжелых физических нагрузок в течение от одного до трех месяцев после интервенционного лечения желудочковых нарушений ритма;
Строгое соблюдение двигательного режима, рекомендаций по приему медикаментозных препаратов;
Регулярное посещение лечащего врача с оценкой состояния здоровья, ЭКГ-контролем не реже 1 раза в 6 месяцев;
При возникновении приступа аритмии, сопровождающегося головокружением, слабостью, потерей сознания, учащенным сердцебиением, - вызов скорой медицинской помощи; желательна ЭКГ-фиксация нарушений ритма;
По показаниям, рекомендациям лечащего врача может быть необходимо проведение контрольного эхокардиографического исследования, суточного мониторирования ЭКГ.
Принципы наблюдения пациента у лечащего врача
Плановые визиты к лечащему врачу для контроля состояния здоровья показаны в среднем 1 раз в полгода;
Пациенту желательно знать названия и дозировки принимаемых препаратов;
Целесообразно проведение ЭКГ-контроля при визите к лечащему врачу;
При ухудшении самочувствия рекомендован внеплановый осмотр лечащего врача.
Неотложные состояния, требующие вызова скорой медицинской помощи
При возникновении эпизода аритмии, сопровождающегося головокружением, слабостью, предобморочным состоянием, потерей сознания, учащенным сердцебиением показан вызов скорой медицинской помощи для контроля и стабилизации состояния, определения показаний к возможной госпитализации в стационар;
При возникновении эпизодов предобморочных состояний, потери сознания рекомендован вызов скорой медицинской помощи для контроля и стабилизации состояния, определения показаний к возможной госпитализации в стационар;
При возникновении срабатываний ИКД/СРТ-Д рекомендован вызов скорой медицинской помощи для контроля и стабилизации состояния, определения показаний к возможной госпитализации в стационар;
Пациентам с возникшими осложнениями после катетерной аблации рекомендована скорейшая госпитализация в специализированный стационар для проведения необходимых лечебно-диагностических мероприятий.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.