Глутаровая ацидурия тип I
 Версия: Клинические рекомендации РФ 2024 (Россия)
Версия: Клинические рекомендации РФ 2024 (Россия)
Общая информация
Краткое описание
Разработчик клинической рекомендации
- Ассоциация медицинских генетиков
- Союз педиатров России
- Национальная ассоциация детских реабилитологов
Одобрено Научно-практическим Советом Минздрава РФ
– размещенные в Рубрикаторе после 1 января 2024 года – с 1 января 2025 года.
Клинические рекомендации
Возрастная категория: Взрослые, Дети
Пересмотр не позднее: 2026
ID: 406
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
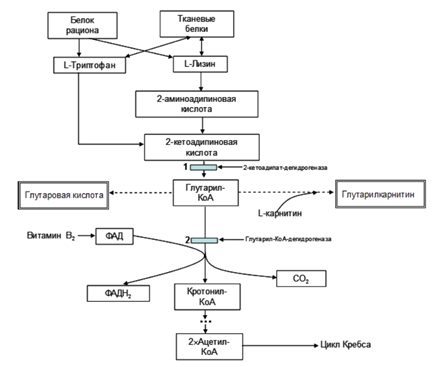
ФАД – флавинадениндинуклеотид, ФАДН2 - восстановленной форма ФАД, КоА – коэнзим А, СО2 – углекислый газ.
Рис.1 - Схема метаболических процессов, приводящих к развитию глутаровой ацидурии тип 1: метаболические блоки выделены голубым цветом, патологические метаболиты выделены двойной рамкой.
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
ГА1 обычно дебютирует в раннем детском возрасте - от 3 до 36 месяцев, с пиком манифестации от 6 до 18 месяцев. В 75% случаев наблюдается энцефалитоподобный вариант заболевания. У 75-80% пациентов первым симптомом болезни может быть макроцефалия, которая отмечается с рождения или развивается в первые месяцы жизни. Энцефалитоподобный вариант заболевания наблюдается в 75% случаев. Нередко первые проявления болезни в виде энцефалитоподобного криза возникают на фоне таких провоцирующих факторов как черепно-мозговая травма, хирургические вмешательства, длительный период голодания, кроме того, острый энцефалопатический криз может возникнуть у детей в возрасте первых 6 лет во время любого инфекционного заболевания, протекающего с повышением температуры тела, а также фебрильной реакции в поствакцинальном периоде, которые сопровождаются высоким уровнем процесса катаболизма [28]. Через 24-72 часа от воздействия «провоцирующего» фактора остро развивается симптоматика в виде лихорадки, эпизодов срыгивания или неукротимой рвоты, кишечных расстройств, эпилептических приступов, часто происходит угнетение сознания до сопора и комы, в результате развивающегося отека и набухания мозга, что может привести к быстрому летальному исходу. Спустя несколько дней или недель после криза могут отмечаться различные типы гиперкинезов (хореиформные, хореоатетоидные, баллистические, дистонические), которые могут быть генерализованными, фокальными или распределяться по гемитипу, а также сочетаться с изменением мышечного тонуса по спастическому типу. Заболевание носит волнообразный характер: после перенесенных энцефалитоподобных кризов происходит медленное, но не полное восстановление неврологических нарушений. В последующем у пациентов с грубым дистоническим синдромом часто формируются вторичные осложнения, такие как гипотрофия, хронический аспирационный синдром, подвывихи суставов и выраженный болевой синдром [6, 12].
В 25% случаев заболевание имеет подострое, доброкачественное течение. На первом году жизни дети наблюдаются с задержкой психомоторного развития, а в дальнейшем происходит постепенная утрата ранее приобретенных навыков, и присоединяются различные виды гиперкинезов в сочетании со спастичностью. Дистонические гиперкинезы приводят к нарушению ходьбы, письма и речевых функций. Многие пациенты длительное время наблюдаются у неврологов со спастико-гиперкинетической формой детского церебрального паралича. Подострое течение заболевания может осложняться метаболической декомпенсацией, появлением новых неврологических симптомов или усилением имеющейся клиники.
Другими частыми симптомами являются профузное потоотделение, эпизоды немотивированной лихорадки, эпилептические приступы. У некоторых пациентов наблюдаются атактические расстройства, очень редко встречаются миоклонии и тремор, офтальмопарез, косоглазие. У большинства пациентов интеллект не страдает или наблюдаются легкие когнитивные нарушения. Среди симптомов со стороны органа зрения нередко обнаруживают кровоизлияния в сетчатку, катаракту и пигментную дегенерацию сетчатки. У нелеченых пациентов смертельный исход наступает в течение первого десятилетия жизни на фоне тяжелого метаболического криза или в результате развития Рейе-подобного синдрома.
У ряда пациентов с ГА1 на первом году жизни в 10-30% случаев возникают субдуральные кровоизлияния, как правило, после перенесенной легкой черепно-мозговой травмы. У пациентов с субдуральными гематомами и/или битемпоральными арахноидальными кистами в сочетании с макроцефалией и дистониями должны быть проведены исследования для исключения ГА1. Диагноз ГА1 должен быть обязательно исключен лабораторными методами у пациентов с предполагаемым синдромом «тряски младенца» («Shaken baby syndrome») [2, 9].
Клинико-диагностические критерии, позволяющие заподозрить ГА1 представлены в Приложении А4.
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
1. Жалобы и анамнез
- отягощенный семейный анамнез (наличие в семье пациента с подтвержденным диагнозом ГА1, наличие в семье случая синдрома «внезапной смерти младенца»)
- Внезапное ухудшение состояния (в виде утраты ранее приобретенных двигательных навыков, появления насильственных движений конечностей, дистонических атак) на фоне полного здоровья или ОРВИ, при оперативных вмешательствах, черепно-мозговой травме;
- близкородственный брак;
- эпизоды лихорадки;
- плохой аппетит;
- нарушения вскармливания;
- частые срыгивания;
- неукротимую рвоту;
- угнетение сознания;
- судороги;
- вялость, слабость, сонливость;
- беспокойное поведение, плаксивость;
- повышенное потоотделение;
- нарушение координации движений;
- непроизвольные/насильственные движения;
- дистонические атаки;
- клиника спастико-гиперкинетической формы детского церебрального паралича;
2. Физикальное обследование
Дети первых 3 лет жизни
- макроцефалия;
- выступающие лобные бугры;
- гепатомегалия;
- задержка моторного и психо-речевого развития;
- изменение мышечного тонуса по типу дистонии;
- экстрапирамидные нарушения: изменения мышечного тонуса по типу ригидности и различные типы гиперкинезов (хореиформные, хореоатетоидные, баллистические, дистонические) разной локализации (фокальные, генерализованные, гемитип);
- спастический тетрапарез (повышение сухожильных рефлексов, наличие патологических стопных знаков, спастическая походка и др.);
- периодическая атаксия, тремор;
- судороги;
После 3 лет
- макроцефалия;
- задержка моторного и психо-речевого развития;
- изменение мышечного тонуса по типу дистонии;
- экстрапирамидные нарушения: ригидность и различные типы гиперкинезов: торсионные, орофациальные, хореиформные, хореоатетоидные, баллистические;
- спастический тетрапарез (повышение сухожильных рефлексов, наличие патологических стопных знаков, спастическая походка и др.);
- периодическая атаксия, тремор;
- судороги;
- периферическая невропатия;
- психиатрические нарушения;
- профузное потоотделение;
- повторные эпизоды необъяснимой лихорадки (гиперпирексические кризы);
- анорексия;
- инсомнии;
- гипогликемии на фоне длительной голодной паузы;
- гепатомегалия;
- редко рабдомиолиз.
Подробно данные физикального обследования описаны в разделе «клиническая картина».
3. Лабораторные диагностические исследования
- Рекомендуется комплексное определение концентрации на аминокислоты и ацилкарнитины в крови методом тандемной масс-спектрометрии пациентам с клиническими проявлениями, характерными для ГА1 с целью биохимической диагностики заболевания [2, 7, 4, 14].
- Рекомендуется определение в биологических жидкостях (моча) органических кислот методом газовой хроматографии с масс-спектрометрией (Комплексное определение содержания органических кислот в моче методом тандемной масс-спектрометрии) пациентам с клиническими проявлениями, характерными для ГА1, с целью биохимической диагностики заболевания [4, 14].
- Рекомендуется определение вариантов генов в образце биологического материала другом или неуточненном, неклассифицированные в других рубриках, методом секвенирования по Сенгеру (03.Я99.18.999.039) и/или методом таргетного высокопроизводительного секвенирования (03.Я99.18.998.041) и/или методом высокопроизводительного секвенирования (03.Я99.18.999.041) и/или методом полимеразной цепной реакции (03.Я99.18.999.048) и/или методом множественной лигазно-зависимой амплификации зондов (03.Я99.18.999.059) (выявление биаллельных патогенных вариантов в гене GCDH) пациентам с повышенной концентрацией глутарилкарнитина (С5DC), глутаровой и 3-OH-глутаровой кислот с целью подтверждения диагноза ГА1 [21].
- Рекомендуется проведение общего (клинического) анализа крови развернутого (гемоглобин, количество эритроцитов, цветовой показатель, количество лейкоцитов, тромбоцитов, лейкоцитарная формула и скорость оседания эритроцитов) всем пациентам с ГА1 и при подозрении на заболевание для оценки основных параметров кроветворения и наличия воспалительных процессов [37, 51, 52].
- Рекомендуется проведение общего (клинического) анализа мочи всем пациентам с ГА1 с целью оценки состояния почек [34].
- Рекомендовано пациентам с ГА1 проведение биохимического анализа крови общетерапевтического (содержание глюкозы, показатели кислотно-основного равновесия, общего белка, белковых фракций, альбумина, С реактивного белка, общего билирубина, холестерина, триглицеридов, липопротеидов низкой и высокой плотности (исследование уровня липопротеинов в крови), щелочной фосфатазы, креатинина, мочевины, аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), креатинфосфокиназы, кальция общего и ионизированного, натрия, калия, неорганического фосфора, железа, ферритина, магния), с целью оценки состояния печени, почек, баланса важнейших нутриентов при диетотерапии, кальциево-фосфорного обмена и выявления отклонений важных биохимических показателей для дальнейшей коррекции [21].
- Рекомендуется мониторинг клинических и лабораторных показателей (кислотно-основного состояния крови, глюкоза, электролиты (калий, натрий, кальций ионизированный, хлор) в период метаболического криза каждые 4-6 часов или раньше при наличии ухудшения или улучшений состояния пациентам с ГА1 в период метаболического криза с целью оценки состояния и своевременной коррекции терапии [21].
4. Инструментальные диагностические исследования
- Рекомендуется проведение магнитно-резонансной томографии (МРТ) головного мозга и/или компьютерная томография головного мозга всем пациентам с подозрением на ГА1 с диагностической целью и для выявления нейрохирургической патологии [7, 11, 13, 19, 20].
- Рекомендуется проведение электроэнцефалографии (ЭЭГ) пациентам с ГА1 при наличии неврологической симптоматики для выявления эпилептической активности [7, 35].
- Рекомендуется проведение ультразвукового исследования (УЗИ) органов брюшной полости пациентам с ГА1 для выявления поражения печени [36, 52].
- Рекомендуется оценка состояния почек с проведением ультразвукового исследования (УЗИ) почек пациентам с ГА1 для выявления структурных нарушений [37].
- Рекомендуется исследование минеральной плотности костной ткани – (Рентгеноденситометрия) пациентам для диагностики остеопении, выявления группы риска и принятия лечебно-профилактических мер [21, 53].
- Рекомендуется проведение офтальмоскопии пациентам с целью своевременного обнаружения офтальмологической патологии [38].
5. Иные диагностические исследования
- Рекомендуются в ведении пациентов с ГА1 использовать мультидисциплинарный подход в виду того, что заболевание характеризуется поражением многих органов и систем, требует комплексной терапии, что диктует необходимость совместного ведения пациента специалистами разных профилей [28].
Дифференциальная диагностика
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
- Рекомендуется патогенетическая диетотерапия с исключением высокобелковых продуктов, богатых лизином и триптофаном, обязательным использованием специализированных продуктов на основе смесей аминокислот без указанных патогенетически значимых аминокислот пациентам с установленным диагнозом ГА1 с целью предотвращения образования нейротоксических метаболитов [1, 3, 7, 18, 19, 20].
2. Медикаментозная терапия
- Рекомендуется пожизненно патогенетическая терапия #левокарнитином пациентам с ГА1 с целью выведения токсичных метаболитов и коррекции вторичной недостаточности карнитина [1, 2, 7, 16, 19, 20, 65].
3. Хирургическое лечение
- Рекомендуется хирургическое лечение субдуральных гидром и арахноидальных кист, гидроцефалии и других патологий пациентам с ГА1 по показаниям с целью стабилизации состояния при нейрохирургической патологии [7, 19, 20].
- Рекомендуется хирургическое лечение костных деформаций (тяжелые контрактуры, вывих бедра и др.) пациентам с ГА1 по показаниям с целью стабилизации и улучшения состояния при ортопедической патологии [2, 7, 39].
- Рекомендуется при планировании хирургического вмешательства по возможности избегать голодания, применять инфузии декстрозы** и удвоить дозировку левокарнитина [21].
4. Иное лечение
- Рекомендуется при возникновении лихорадки выше 38,5 назначать ибупрофен**или парацетамол**[28].
- Рекомендуется при возникновении инфекционных и интеркуррентных заболеваний назначать лечение согласно соответствующим клиническим рекомендациям (инфекционные заболевания). Антибактериальную терапию назначают в зависимости от предполагаемого патогенного агента в возрастных дозах [21].
- Рекомендуется фармакотерапия экстрапирамидных нарушений препаратами из группы миорелаксантов центрального действия, пациентам с ГА1 по показаниям с целью коррекции неврологический нарушений [2,16,21, 55].
Длительность лечения определяется индивидуально – от нескольких недель до нескольких месяцев [59]. Начальная доза #тригексифенидила** не должна превышать 0,5–1 мг/сут.
У взрослых с дистонией #тригексифенидил** обычно начинают с дозы 2мг х 2-3 р/сут с постепенным повышением на 2мг каждую 1-2 недели (чаще каждые 2 недели), обычно до достижения 21,5 мг [62].
- Рекомендуется ботулинотерапия пациентам с ГА1 по показаниям с целью коррекции неврологический нарушений (дистонии, спастичности) [7, 16, 20, 39].
- Рекомендуется терапия эпилептических приступов с индивидуальным подбором противоэпилептических препаратов пациентам с ГА1 с целью коррекции симптоматики [7, 16, 19, 20].
- Не рекомендуется назначение препаратов солей вальпроевой кислоты** пациентам с ГА1 с целью предотвращения ухудшения состояния [2, 7, 16, 20, 21].
Лечение в период метаболического криза
Основными триггерами декомпенсации (факторами, вызывающие распад белка) являются
- Голодание
- Инфекционные процессы, особенно протекающие со рвотой, диареей
- Лихорадка (любой этиологии)
- Интенсивные физические упражнения
- Нарушение диеты (избыточное потребление белка)
Необходимо проведение тщательной клинической оценки состояния пациента, включая измерение артериального давления и оценку комы по шкале Глазго при подозрении на развитие метаболического криза.
- восстановление катаболического статуса, путем назначения высокоэнергетической инфузионной терапии (декстроза** в сочетании с инсулинами и их аналогами);
- ограничение образования органических кислот, путем снижения поступления белка натуральных продуктов или полное их исключение (по возможности в течение 24 часов используют только специализированные продукты на основе смесей аминокислот)[28];
- введение высокодозного Левокарнитина;
- восстановление кислотно-щелочного состояния крови.
Подробные клинические и лабораторные показатели приведены в приложении А10.
- Рекомендуется коррекция патогенетической диетотерапии и доз левокарнитина пациентам с ГА1 в период метаболического криза с целью стабилизации состояния [7, 19, 20].
#Левокарнитин вводится внутривенно –150-200 мг/кг/24 ч в виде 2 -4 раздельных доз или болюсно по 100 мг/кг в течение 30 минут с последующей медленной внутривенной инфузией по 4 мг/кг/ч. (максимальная доза 6 г/сут)[66].
Если внутривенное введение невозможно, возможен пероральный прием 200 мг/кг/сутки дробно.
- Рекомендуется инфузионная терапия в стационаре пациентам с ГА1 в период метаболического криза с целью предотвращения развития тяжелых неврологических нарушений [7, 19, 20].
Инфузионная терапия включает:
- Рекомендуется применение аминокислотных смесей без лизина и триптофана (или с низким содержанием триптофана) всем пациентам с ГА1 в период метаболического криза с целью восполнения потребности в белке за счет белкового эквивалента без патогенетически значимых аминокислот [28, 55].
- Рекомендуется при рвоте применять противорвотные средства #Ондансетрон** в дозе 0,1- 0,15 мг/кг/сутки) в возрастных дозах с целью купирования симптома [55, 56, 57, 58].
- Рекомендуется при отечном синдроме дегидратационная терапия Фуросемидом** в возрастных дозах по клинической ситуации с целью нормализации водного баланса [55].
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- Рекомендуется участие специалиста по физической реабилитации при ведении пациентов с ГА1 для коррекции неврологических нарушений по типу детского церебрального паралича, медицинского психолога и дефектолога с целью проведения психолого-педагогической коррекции [21, 28, 48].
- Рекомендуется консультации логопеда пациентам с ГА1 с целью проведения мероприятий, направленных на улучшение речевых функций и коррекции дисфагии [21, 28, 48].
Госпитализация
Организация оказания медицинской помощи
- проведение диагностики и лечения, требующие продолжительного (дневное или круглосуточное пребывание) медицинского наблюдения и мониторинга клинико-лабораторных показателей;
- необходимость проведения различных видов экспертиз или обследования в медицинской организации при невозможности проведения их в амбулаторных условиях (в том числе оформление заключения федерального консилиума/врачебной комиссии).
Показания для экстренной госпитализации в медицинскую организацию:
- острые угрожающие для жизни и развития осложнений состояния, в том числе метаболический криз, требующие неотложного лечения, в том числе интенсивной терапии, а также круглосуточного медицинского наблюдении и проведения специальных видов обследования и лечения.
Показания к выписке пациента из медицинской организации:
- отсутствие угрозы для жизни пациента и угрозы развития осложнений, требующих неотложного лечения при завершение диагностических мероприятий.
- стабилизация состояния и основных клинико-лабораторных показателей патологического процесса, отсутствие необходимости в продолжительном медицинском наблюдении (дневное или круглосуточное пребывание);
- необходимость перевода больного в другое медицинское учреждение или учреждение социального обеспечения.
Особенности организации оказания медицинской помощи пациентам с ГА1
- Пациенты с ГА1 часто госпитализируются в отделение патологии детей раннего возраста, неврологическое, инфекционное отделения или реанимацию в состоянии энцефалитоподобного криза (первичного или повторного). Продолжительность госпитализации зависит от скорости верификации диагноза, коррекции метаболических нарушений путем проведения интенсивной терапии и начала патогенетической диетотерапии, а также от сроков появления положительной динамики со стороны центральной нервной системы и других органов, скорости восстановления биохимических показателей и в среднем составляет 21 день.
- После выписки из стационара ребенок должен находиться на этапе амбулаторно-поликлинического наблюдения у врача-педиатра, врача-невролога, врача-генетика, больные пациенты с симптоматической эпилепсией нуждаются в наблюдении врача-эпилептолога. Консультации других специалистов (врач-офтальмолог, врач-ортопед, врач ЛФК и др.) назначаются по показаниям.
- Ежегодно пациентам должны проходить углубленную диспансеризацию в условиях дневного стационара (длительность госпитализации не менее 10 суток), где также осуществляются необходимые реабилитационные мероприятия.
- Реабилитационные мероприятия, включающие лечебную физкультуру и физиотерапевтические процедуры необходимо проводить каждые 3 месяца.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
1. Профилактика
- Рекомендуется первичная и повторная консультация врача-генетика после установления диагноза ГА1 пациенту или его официальным представителям с целью разъяснений генетического риска, обсуждения возможностей пренатальной и преимплантационной диагностики [50].
- Рекомендовано пациентам с ГА1 проводить профилактическую вакцинацию по национальному календарю прививок с соблюдением мер предосторожности, в том числе, на фоне строгого выполнения диетических и лечебных назначений с целью формирования иммунной защиты организма от инфекций и предотвращения развития энцефалитоподобных кризов [7, 40].
2. Диспансерное наблюдение
- Рекомендуется комплексное определение концентрации на аминокислоты в крови у пациентов с ГА1 с целью профилактики недостаточности питания [19, 21].
- Рекомендуется исследование уровня свободного карнитина и ацилкарнитинов в крови всем пациентам с ГА1 для выявления вторичной карнитиновой недостаточности [28].
- Рекомендуется регулярный контроль общего (клинического) анализа крови всем пациентам с целью мониторинга нутритивного статуса [28].
- Рекомендуется всем пациентам проведение анализа крови биохимического общетерапевтического (содержание глюкозы, показатели кислотно-основного равновесия, общего белка, белковых фракций, альбумина, С реактивного белка, общего билирубина, холестерина, триглицеридов, липопротеидов низкой и высокой плотности (исследование уровня липопротеинов в крови), щелочной фосфатазы, креатинина, мочевины, аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), креатинфосфокиназы, кальция общего и ионизированного, натрия, калия, неорганического фосфора, железа, ферритина, магния) с целью оценки состояния печени, почек, баланса важнейших нутриентов при диетотерапии, кальциево-фосфорного обмена и выявления отклонений важных биохимических показателей для дальнейшей коррекции [21].
- Рекомендуется проведение общего (клинического) анализа мочи всем пациентам с ГА1 с целью контроля лабораторных показателей [7, 34].
- Рекомендуется проведение нейрорадиологического исследования головного мозга (МРТ/КТ головного мозга) пациентам с ГА1 по показаниям с целью визуализации изменений головного мозга [29, 30].
- Рекомендуется исследование минеральной плотности костной ткани – (Рентгеноденситометрия) у пациентов с ГА1 для диагностики остеопении, выявления группы риска по остеопорозу и принятия лечебно-профилактических мер [21].
- Рекомендуется проведение электроэнцефалографии (ЭЭГ) пациентам с ГА1 при наличии неврологической симптоматики для выявления эпилептической активности [7, 35].
- Рекомендуется проведение ультразвукового исследования (УЗИ) органов брюшной полости пациентам с ГА1 для выявления патологии печени [36, 52].
- Рекомендуется проведение офтальмоскопии пациентам с целью своевременного обнаружения офтальмологической патологии [38].
- Рекомендуется пациентам с ГА1 проведение коррекции лечебного питания и симптоматической терапии с целью исключения белково-энергетической недостаточности [1,3,7,18,1,20]
- Рекомендуются при наблюдении пациентов с ГА1 с целью коррекции терапии и динамического мониторинга применять мультидисциплинарный подход [28].
- Рекомендуется обязательное наблюдение врача-невролога всем пациентам для оценки тяжести неврологических нарушений и их последующей коррекции [2,7,16,19,20].
- экстрапирамидные нарушения (более чем в 95% случаев, развиваются после перенесенного острого токсико-метаболического криза);
- эпилептические приступы (4-40%);
- субдуральные кровоизлияния (10-30%);
- двусторонние арахноидальные кисты
- Рекомендуется обучение родителей правилам организации терапии в межприступный период и в период угрозы метаболического криза пациентов с ГА1 с целью предотвращения развития повторных энцефалитоподобных кризов [55].
Информация
Источники и литература
-
Клинические рекомендации Российского общества медицинских генетиков
- Клинические рекомендации Российского общества медицинских генетиков - 1. Михайлова С. В., Захарова Е. Ю., Петрухин А. С. Нейрометаболические заболевания у детей и подростков: диагностика и подходы к лечению / - 2-е изд., перераб. и доп. - М. : Литтерра, 2017. - 368 с. - (Серия "Практические руководства"). - ISBN 978-5-4235-0254-6.
2. Михайлова С. В., Захарова Е. Ю., Бобылова М. Ю., и др. Глутаровая ацидурия тип 1: клиника, диагностика и лечение. Журнал неврологии и психиатрии им.С.С.Корсакова. 2007-N 10.-С.4-12 3. MP 2.3.1.2432-08 "Нормы физиологических потребностей в энергии и пищевых веществах для различных групп населения Российской Федерации" (утв. Главным государственным санитарным врачом РФ 18 декабря 2008 г.). 4. Baric I., Wagner P., Feyh P. et al. Sensitivity and specificity of free and total glutaric acid and 3-hydroxyglutaric acid measurements by stable-isotope dilution assays for the diagnosis of glutaric aciduria type I. //J. Inher. Metab. Dis. ― 1999. ―V. 22. ― P. 867-882
5. Biery B.J., Stein D.E., Morton D.H. et al. Gene Structure and Mutations of Glutaryl-Coenzyme A. Dehydrogenase: Impaired Association of Enzyme Subunits That is Due to an A421V Substitution Causes Glutaric Acidemia Type I in the Amish. // Am. J. Hum.
Genet. ― 1996. ―V. 59. ― P. 1006-1011. 6. Bjugstad K.B., Goodman S.I., Freed C.R. Age at symptom onset predicts severity of motor impairment and clinical outcome of glutaric acidemia type I. //J. Pediatr. ― 2000. ― V.137. ―P. 681-686.
7. Boy N., Mühlhausen C., Maier E.M. Proposed recommendations for diagnosing and managing individuals with glutaric aciduria type I: second revision. J Inherit Metab Dis. 2016 Nov 16. [Epub ahead of print] 8. Brismar J., and Ozand P.T. CT and MR of the brain in glutaric acidemia type I: a review of 59 published cases and a report of 5 new patients. // AJNR Am. J. Neuroradiol. ―1995. ― V.16. ― P.675-683.
9. Caffey J. The whiplash shaken infant syndrome: manual shaking by the extremities with whiplash-induced intracranial and intraocular bleedings, linked with residual permanent brain damage and mental retardation. //Pediatrics. ― 1974. ― V.54. ― P. 396-403. 10. Chalmers R.A., Bain M.D., Zschocke J. Riboflavin-responsive glutaryl CoA dehydrogenase deficiency. //Mol. Genet. Metab. ―2006. ― V.88. ― P.29-37. 11. Chow C.W., Haan E.A., Goodman S.I. et al. Neuropathology in glutaric acidaemia type 1. // Acta. Neuropathol. ― 1988. ― V.76. ― P.590-594. 39
12. Corral I., Martinez C.J.C., Martinez-Pardo M. et al. Glutaric aciduria type 1: diagnosis in adulthood and phenotypic variability. //Neurologia. ―2001. ―V.16. ― P.377-380. 13. Desai N.K., Runge V.M., Crisp D.E. Magnetic resonance imaging of the brain in glutaric acidemia type I: a review of the literature and a report of four new cases with attention to the basal ganglia and imaging technique. //Invest. Radiol. ― 2003. ―V.38. ― P.489-496. 14. Forstner R., Hoffman G.F., Gassner I. et al. Glutaric aciduria type 1: ultrasonographic demonstrations of early signs. //Pediatr. Radiol. ― 1999. ―V.29. ―P.138-143. 15. Funk C.B., Prasad A.N., Frosk P. et al. Neuropathological, biochemical and molecular findings in a glutaric acidemia type 1 cohort. //Brain. ― 2005. ―V.128. ― P.711-722. 16. Goodman S.I. Prenatal diagnosis of glutaric acidemias. // Prenat. Diagn. ― 2001. ―V. 21. ― P. 1167-1168.
17. Hoffmann G.F., Athanassopoulos S., Burlina A.B., et al. Clinical Course, Early Diagnosis, Treatment, and Prevention of Disease in Glutaryl-CoA Dehydrogenase Deficiency. // Neuropediatr. ― 1996. ―V. 27. ―P. 115-123. 18. Hoffmann G.F., Zschocke J. Glutaric aciduria type I: From clinical, biochemical and molecular diversity to successful therapy. //J. Inher. Metab. Dis. ―1999. ―V. 22. ―P. 381-
19. Phyllis B. Acosta Nutrition Management of Patient with Inherited Metabolic Disorders-Jones and Bartlett Publishers- 2010 p.476. 20. S. Kolker,E. Christensen,J.V. Leonard et al. Guideline for the diagnosis and management of glutaryl-CoAdehydrogenase deficiency (glutaric aciduria type I) J. Inher. Metab. Dis. -2007- 30:5–22
21. Kölker, S., Christensen, E., Leonard, J.V. et al. Diagnosis and management of glutaric aciduria type I – revised recommendations. J Inherit Metab Dis 2011.vol 34 No.3:677-694. https://doi.org/10.1007/s10545-011-9289-5 22. World Health Organization (1985): Energy and protein requirements. Report of a Joint FAO/WHO/UNU Expert Consultation (1985). WHO Tech Rep Ser No 724, Geneva. 23. Online Mendelian Inheritance in Man/ An Onlaine Catalog of Human Genes and Genetic Disorders Update 23 November 2016 - www.omim.org. 24. Boy N, Mengler K, Thimm E, Schiergens KA, Marquardt T, Weinhold N, et al. Newborn screening: a disease-changing intervention for glutaric aciduria type 1. Ann Neurol. 2018;83:970–979.
25. Tsai FC, Lee HJ, Wang AG, Hsieh SC, Lu YH, Lee MC, Pai JS, Chu TH, Yang CF, Hsu TR, Lai CJ, Tsai MT, Ho PH, Lin MC, Cheng LY, Chuang YC, Niu DM. Experiences during newborn screening for glutaric aciduria type 1: diagnosis, treatment, genotype, phenotype, and outcomes. J Chin Med Assoc. 2017;80:253–61.40
26. Boy N., Mengler K., Heringer-Seifert J. et al. Impact of newborn screening and quality of therapy on the neurological outcome in glutaric aciduria type 1: a meta-analysis. Genet Med 23, 13–21 (2021). https://doi.org/10.1038/s41436-020-00971-4 27. Gerards M, Sallevelt SC, Smeets HJ. Leigh syndrome: resolving the clinical and genetic heterogeneity paves the way for treatment options. Mol Genet Metab. 2016;117:300–12. 28. Boy N, Mühlhausen C, Maier EM, Heringer J, Assmann B, Burgard P, Dixon M, Fleissner S, Greenberg CR, Harting I, Hoffmann GF, Karall D, Koeller DM, Krawinkel MB, Okun JG, Opladen T, Posset R, Sahm K, Zschocke J, Kölker S, et al. Proposed recommendations for diagnosing and managing individuals with glutaric aciduria type I: second revision. JInheritMetabDis. 2017b;40:75–101. 29. Vester ME, Visser G, Wijburg F, van Spronsen FJ, Williams M, van Rijn RR. Occurrence of subdural hematomas in Dutch glutaric aciduria type 1 patients. Eur J Pediatr. 2016;175:1001–6.
30. Boy N, Garbade SF, Heringer J, Seitz A, Kölker S, Harting I. Patterns, evolution, and severity of striatal injury in insidious-vs acute-onset glutaric aciduria type 1. J Inherit Metab Dis. 2019;42:117–27. 31. Kurkina, M.V., Mihaylova, S.V., Baydakova, G.V. et al. Molecular and biochemical study of glutaric aciduria type 1 in 49 Russian families: nine novel mutations in the GCDH gene. MetabBrainDis 35, 1009–1016 (2020). https://doi.org/10.1007/s11011-020-00554-x
32. MortonDH, BennettMJ, SeargeantLE, NichterCA, KelleyRI. Glutaric aciduria type I: a common cause of episodic encephalopathy and spastic paralysis in the Amish of Lancaster County, Pennsylvania. Am J Med Genet. 1991;41:89–95 33. BasingerAA, BookerJK, FrazierDM, KoeberlDD, SullivanJA, MuenzerJ.
Glutaricacidemiatype 1 inpatientsofLumbeeheritagefromNorthCarolina. MolGenetMetab. 2006;88:90–92.
34. Kölker S, Garcia-Cazorla A, Valayannopoulos V, Lund AM, Burlina AB, Sykut-Cegielska J, Wijburg FA, Teles EL, Zeman J, Dionisi-Vici C. The phenotypic spectrum of organic acidurias and urea cycle disorders. Part 1: the initial presentation. J Inherit Metab Dis. 2015a;38:1041–57 35. Fujimoto S, Shibata I, Sugiyama N, Ohba S, Togari H, Wada Y. Unique electroencephalographic change of acute encephalopathy in glutaric aciduria type 1.
Tohoku J Exp Med. 2000 May;191(1):31-8. doi: 10.1620/tjem.191.31. PMID: 10896037. 36. Monavari AA, Naughten ER. Prevention of cerebral palsy in glutaric aciduria type 1 by dietary management. Arch Dis Child. 2000 Jan;82(1):67-70. doi: 10.1136/adc.82.1.67.
PMID: 10630918; PMCID: PMC1718171.:
37. du Moulin M, Thies B, Blohm M, Oh J, Kemper MJ, Santer R, Mühlhausen C. Glutaric Aciduria Type 1 and Acute Renal Failure: Case Report and Suggested Pathomechanisms. 41
JIMD Rep. 2018;39:25-30. doi: 10.1007/8904_2017_44. Epub 2017 Jul 12. PMID: 28699143; PMCID: PMC5953902.
38. Kafil-Hussain NA, Monavari A, Bowell R, Thornton P, Naughten E, O'Keefe M. Ocular findings in glutaric aciduria type 1. J PediatrOphthalmol Strabismus. 2000 Sep-Oct;37(5):289-93. PMID: 11020111 39. Imerci A, Strauss KA, Oleas-Santillan GF, Miller F. Orthopaedic manifestations of glutaric acidemia Type 1. J ChildOrthop. 2020 Oct 1;14(5):473-479. 40. Kevin A. Strauss, Katie B. Williams, Vincent J. Carson, Laura Poskitt, Glutaric acidemia type 1: Treatment and outcome of 168 patients over three decades, Molecular Genetics and Metabolism,Volume 131, Issue 3, 2020, Pages 325-340, ISSN 1096-7192, https://doi.org/10.1016/j.ymgme.2020.09.007. 41. Fernández-Alvarez E, Nardocci N. Update on pediatric dystonias: etiology, epidemiology, and management. Degener Neurol Neuromuscul Dis. 2012;2:29-41. Published 2012 Apr 11. doi:10.2147/DNND.S16082 42. McClelland, V.M.; Bakalinova, D.B.; Hendriksz, C.; Singh, R.P. Glutaric aciduria type 1 presenting with epilepsy. Dev. Med. Child Neurol. 2009, 51, 235–239. [Google Scholar] [CrossRef] [PubMed] 43. Jovic, N.J.; Kosac, A.; Koprivsek, K. L-2-hydroxyglutaric aciduria: A case report.
SrpskiArhiv za CelokupnoLekarstvo 2014, 142, 337–341. [Google Scholar] [CrossRef] [PubMed][Green Version] 44. Periasamy, V.; Rudwan, M.; Yadav, G.; Khan, R.A. Epilepsy in a young adult caused by L-2-hydroxyglutaric aciduria: A case report. Med. Princ. Pract. Int. J. Kuwait Univ. Health Sci. Cent. 2008, 17, 258–261. [Google Scholar] [CrossRef] [PubMed] 45. Mete, A.; Isikay, S.; Sirikci, A.; Ozkur, A.; Bayram, M. Eyelid myoclonia with absence seizures in a child with l-2 hydroxyglutaric aciduria: Findings of magnetic resonance imaging. Pediatr. Neurol. 2012, 46, 195–197. [Google Scholar] [CrossRef] [PubMed] 46. Seijo-Martinez, M.; Navarro, C.; Castro del Rio, M.; Vila, O.; Puig, M.; Ribes, A.; Butron, M. L-2-hydroxyglutaric aciduria: Clinical, neuroimaging, and neuropathological findings.
Arch. Neurol. 2005, 62, 666–670. [Google Scholar] [CrossRef] [PubMed] 47. Calik, M.; Tuncer, F.N.; Sarikaya, S.; Karakas, O.; Cece, H.; Iscan, A. A case of l-2 hydroxyglutaric aciduria presenting as febrile seizure. Genet. Couns. 2014, 25, 363–367. [Google Scholar] [PubMed] 48. Leema P Cornelius, Vivekasaravanan Raju, Asir Julin Pediatric glutaric aciduria type 1: 14 cases, diagnosis and management Annals of Indian academy of neurology 2021 Vol. 24 Issue: 1 P.: 22-26 49. Iona Novak, Catherine Morgan, Michael Fahey, Megan Finch-Edmondson, Claire Galea, Ashleigh Hines, , State of the Evidence Traffic Lights 2019: Systematic Review of 42
Interventions for Preventing and Treating Children with Cerebral Palsy. Current Neurology and Neuroscience Reports (2020) 20: 3 https://doi.org/10.1007/s11910-020-1022-z 50. Larson A, Goodman S. Glutaric Acidemia Type 1. 2019 Sep 19. In: Adam MP, Ardinger HH, Pagon RA, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2021. Available from: https://www.ncbi.nlm.nih.gov/books/NBK546575/ 51. Kölker et al. J Inherit Metab Dis 30: 5-22, 2007b; J Inherit Metab Dis 34: 677-694, 2011, Boy, N., Mühlhausen, C., Maier, E.M., Heringer, J., Assmann, B., Burgard, P., Dixon, M., Fleissner, S., Greenberg, C.R., Harting, I., Hoffmann, G.F., Karall, D., Koeller, D.M., Krawinkel, M.B., Okun, J.G., Opladen, T., Posset, R., Sahm, K., Zschocke, J., Kölker, S. and (2017), Proposed recommendations for diagnosing and managing individuals with glutaric aciduria type I: second revision. J Inherit Metab Dis, 40: 75-101. https://doi.org/10.1007/s10545-016-9999-9,
52. Landmann E, Kreuder J, Gortner L, Neugebauer M, Reiter A, Blütters-Sawatzki R.
Effloreszenzen und Blutbildveränderungenbeieinem 9 MonatealtenSäuglingmitGlutarazidurieTyp I [Cutaneous lesions and blood count changes
in a 9-month old girl with glutaric aciduria type I]. KlinPadiatr. 2001 Mar-Apr;213(2):74-5. German. doi: 10.1055/s-2001-12880. PMID: 11305196. 53. Hakim M., Martin D., Beebe A., KlamarJ., Tobias J. Perioperative Management of a Patient With Glutaric Aciduria. Journal of Medical Cases, North America, 6, may. 2015.
Available at:
. Dateaccessed: 05 Apr. 2021. 54. Hedlund GL, Longo N, Pasquali M. Glutaric acidemia type 1. Am J Med Genet Part C Semin Med Genet 2006. 142C:86–94 55. Kölker S, Christensen E, Leonard JV, Greenberg CR, Burlina AB, Burlina AP, Dixon M, Duran M, Goodman SI, Koeller DM, Müller E, Naughten ER, Neumaier-Probst E, Okun JG, Kyllerman M, Surtees RA, Wilcken B, Hoffmann GF, Burgard P. Guideline for the diagnosis and management of glutaryl-CoA dehydrogenase deficiency (glutaric aciduria type I). J Inherit Metab Dis. 2007 Feb;30(1):5-22. doi: 10.1007/s10545-006-0451-4. Epub 2007 Jan 3. PMID: 17203377. 56. Emergency Protocol Glutaric Aciduria Type 1. 2019 FamiliasGA association(https://familiasga.com/wp-content/uploads/2020/05/GLUTARIC-ACIDURIA-TYPE-1-EMERGENCY-PROTOCOL-EN.pdf) 57. StraussK.A., PuffenbergerE.G., Robinson D.L. and MortonD.H. (2003), Type I glutaric aciduria, part 1: Natural history of 77 patients. Am. J. Med. Genet., 121C: 38-52. https://doi.org/10.1002/ajmg.c.20007 58. Mehta N, Kaur G. Anesthetic Management for Fracture Head of Radius in a Child with Glutaric Aciduria type-1. Anesth Essays Res. 2018 Apr-Jun;12(2):601-603. doi: 10.4103/aer.AER_34_18. PMID: 29962642; PMCID: PMC6020594.43 59. Luc QN, Querubin J. Clinical Management of Dystonia in Childhood. Paediatr Drugs. 2017 Oct;19(5):447-461 60. Sanger TD, Bastian A, Brunstrom J, Damiano D, Delgado M, Dure L, Gaebler-Spira D, Hoon A, Mink JW, Sherman-Levine S, Welty LJ; Child Motor Study Group. Prospective open-label clinical trial of trihexyphenidyl in children with secondary dystonia due to cerebral palsy. J Child Neurol. 2007 May;22(5):530-7 61. Rice J, Waugh M-C. Pilot study on trihexyphenidyl in the treatment of dystonia in children with cerebral palsy. J. Child Neurol. 2009;24:176–82 62. Lang AE. High dose anticholinergic therapy in adult dystonia. Can J Neurol Sci. 1986 Feb;13(1):42-6 63. Bohn E, Goren K, Switzer L, Falck-Ytter Y, Fehlings D. Pharmacological and neurosurgical interventions for individuals with cerebral palsy and dystonia: a systematic review update and meta-analysis. Dev Med Child Neurol. 2021 Mar 27 64. Неонатальный скрининг: национальное руководство / под ред. С.И. Куцева. Москва : ГЭОТАР-Медиа, 2023. — 360 с. — (Серия «Национальные руководства»). — DOI: 10.33029/9704-7737-3-NEO-2023-1-360 65. Захарова Е. Ю., Михайлова С. В., Зарубина В.В. и др. Практические аспекты терапии при глутаровой ацидурии типа 1. Нервно-мышечные болезни, 2021-Т11 (4).-С.12-25 66. British Inherited Metabolic Disease Group protocol Glutaric aciduria type 1 – acute decompensation, standard version, 2016 (https://bimdg.org.uk/store/guidelines/ER-GA1-v4_549337_05042017.pdf) 67. Burlina AP, Zara G, Hoffmann GF, Zschocke J, Burlina AB (2004) Management of movement disorders in glutaryl-CoA dehydrogenase deficiency : Anticholinergic drugs and botulinum toxin as additional therapeutic options. J Inherit Metab Dis 27:911–915 68. Mühlhausen C., Hoffmann G. F., Strauss K. A. et al //Maintenance treatment of glutaryl-CoA dehydrogenase deficiency . Inherit. Metab. Dis. 27 (2004) 885^892. https://doi.org/10.1023/B:BOLI.0000045773.07785.83
- Клинические рекомендации Российского общества медицинских генетиков - 1. Михайлова С. В., Захарова Е. Ю., Петрухин А. С. Нейрометаболические заболевания у детей и подростков: диагностика и подходы к лечению / - 2-е изд., перераб. и доп. - М. : Литтерра, 2017. - 368 с. - (Серия "Практические руководства"). - ISBN 978-5-4235-0254-6.
2. Михайлова С. В., Захарова Е. Ю., Бобылова М. Ю., и др. Глутаровая ацидурия тип 1: клиника, диагностика и лечение. Журнал неврологии и психиатрии им.С.С.Корсакова. 2007-N 10.-С.4-12 3. MP 2.3.1.2432-08 "Нормы физиологических потребностей в энергии и пищевых веществах для различных групп населения Российской Федерации" (утв. Главным государственным санитарным врачом РФ 18 декабря 2008 г.). 4. Baric I., Wagner P., Feyh P. et al. Sensitivity and specificity of free and total glutaric acid and 3-hydroxyglutaric acid measurements by stable-isotope dilution assays for the diagnosis of glutaric aciduria type I. //J. Inher. Metab. Dis. ― 1999. ―V. 22. ― P. 867-882
5. Biery B.J., Stein D.E., Morton D.H. et al. Gene Structure and Mutations of Glutaryl-Coenzyme A. Dehydrogenase: Impaired Association of Enzyme Subunits That is Due to an A421V Substitution Causes Glutaric Acidemia Type I in the Amish. // Am. J. Hum.
Genet. ― 1996. ―V. 59. ― P. 1006-1011. 6. Bjugstad K.B., Goodman S.I., Freed C.R. Age at symptom onset predicts severity of motor impairment and clinical outcome of glutaric acidemia type I. //J. Pediatr. ― 2000. ― V.137. ―P. 681-686.
7. Boy N., Mühlhausen C., Maier E.M. Proposed recommendations for diagnosing and managing individuals with glutaric aciduria type I: second revision. J Inherit Metab Dis. 2016 Nov 16. [Epub ahead of print] 8. Brismar J., and Ozand P.T. CT and MR of the brain in glutaric acidemia type I: a review of 59 published cases and a report of 5 new patients. // AJNR Am. J. Neuroradiol. ―1995. ― V.16. ― P.675-683.
9. Caffey J. The whiplash shaken infant syndrome: manual shaking by the extremities with whiplash-induced intracranial and intraocular bleedings, linked with residual permanent brain damage and mental retardation. //Pediatrics. ― 1974. ― V.54. ― P. 396-403. 10. Chalmers R.A., Bain M.D., Zschocke J. Riboflavin-responsive glutaryl CoA dehydrogenase deficiency. //Mol. Genet. Metab. ―2006. ― V.88. ― P.29-37. 11. Chow C.W., Haan E.A., Goodman S.I. et al. Neuropathology in glutaric acidaemia type 1. // Acta. Neuropathol. ― 1988. ― V.76. ― P.590-594. 39
12. Corral I., Martinez C.J.C., Martinez-Pardo M. et al. Glutaric aciduria type 1: diagnosis in adulthood and phenotypic variability. //Neurologia. ―2001. ―V.16. ― P.377-380. 13. Desai N.K., Runge V.M., Crisp D.E. Magnetic resonance imaging of the brain in glutaric acidemia type I: a review of the literature and a report of four new cases with attention to the basal ganglia and imaging technique. //Invest. Radiol. ― 2003. ―V.38. ― P.489-496. 14. Forstner R., Hoffman G.F., Gassner I. et al. Glutaric aciduria type 1: ultrasonographic demonstrations of early signs. //Pediatr. Radiol. ― 1999. ―V.29. ―P.138-143. 15. Funk C.B., Prasad A.N., Frosk P. et al. Neuropathological, biochemical and molecular findings in a glutaric acidemia type 1 cohort. //Brain. ― 2005. ―V.128. ― P.711-722. 16. Goodman S.I. Prenatal diagnosis of glutaric acidemias. // Prenat. Diagn. ― 2001. ―V. 21. ― P. 1167-1168.
17. Hoffmann G.F., Athanassopoulos S., Burlina A.B., et al. Clinical Course, Early Diagnosis, Treatment, and Prevention of Disease in Glutaryl-CoA Dehydrogenase Deficiency. // Neuropediatr. ― 1996. ―V. 27. ―P. 115-123. 18. Hoffmann G.F., Zschocke J. Glutaric aciduria type I: From clinical, biochemical and molecular diversity to successful therapy. //J. Inher. Metab. Dis. ―1999. ―V. 22. ―P. 381-
19. Phyllis B. Acosta Nutrition Management of Patient with Inherited Metabolic Disorders-Jones and Bartlett Publishers- 2010 p.476. 20. S. Kolker,E. Christensen,J.V. Leonard et al. Guideline for the diagnosis and management of glutaryl-CoAdehydrogenase deficiency (glutaric aciduria type I) J. Inher. Metab. Dis. -2007- 30:5–22
21. Kölker, S., Christensen, E., Leonard, J.V. et al. Diagnosis and management of glutaric aciduria type I – revised recommendations. J Inherit Metab Dis 2011.vol 34 No.3:677-694. https://doi.org/10.1007/s10545-011-9289-5 22. World Health Organization (1985): Energy and protein requirements. Report of a Joint FAO/WHO/UNU Expert Consultation (1985). WHO Tech Rep Ser No 724, Geneva. 23. Online Mendelian Inheritance in Man/ An Onlaine Catalog of Human Genes and Genetic Disorders Update 23 November 2016 - www.omim.org. 24. Boy N, Mengler K, Thimm E, Schiergens KA, Marquardt T, Weinhold N, et al. Newborn screening: a disease-changing intervention for glutaric aciduria type 1. Ann Neurol. 2018;83:970–979.
25. Tsai FC, Lee HJ, Wang AG, Hsieh SC, Lu YH, Lee MC, Pai JS, Chu TH, Yang CF, Hsu TR, Lai CJ, Tsai MT, Ho PH, Lin MC, Cheng LY, Chuang YC, Niu DM. Experiences during newborn screening for glutaric aciduria type 1: diagnosis, treatment, genotype, phenotype, and outcomes. J Chin Med Assoc. 2017;80:253–61.40
26. Boy N., Mengler K., Heringer-Seifert J. et al. Impact of newborn screening and quality of therapy on the neurological outcome in glutaric aciduria type 1: a meta-analysis. Genet Med 23, 13–21 (2021). https://doi.org/10.1038/s41436-020-00971-4 27. Gerards M, Sallevelt SC, Smeets HJ. Leigh syndrome: resolving the clinical and genetic heterogeneity paves the way for treatment options. Mol Genet Metab. 2016;117:300–12. 28. Boy N, Mühlhausen C, Maier EM, Heringer J, Assmann B, Burgard P, Dixon M, Fleissner S, Greenberg CR, Harting I, Hoffmann GF, Karall D, Koeller DM, Krawinkel MB, Okun JG, Opladen T, Posset R, Sahm K, Zschocke J, Kölker S, et al. Proposed recommendations for diagnosing and managing individuals with glutaric aciduria type I: second revision. JInheritMetabDis. 2017b;40:75–101. 29. Vester ME, Visser G, Wijburg F, van Spronsen FJ, Williams M, van Rijn RR. Occurrence of subdural hematomas in Dutch glutaric aciduria type 1 patients. Eur J Pediatr. 2016;175:1001–6.
30. Boy N, Garbade SF, Heringer J, Seitz A, Kölker S, Harting I. Patterns, evolution, and severity of striatal injury in insidious-vs acute-onset glutaric aciduria type 1. J Inherit Metab Dis. 2019;42:117–27. 31. Kurkina, M.V., Mihaylova, S.V., Baydakova, G.V. et al. Molecular and biochemical study of glutaric aciduria type 1 in 49 Russian families: nine novel mutations in the GCDH gene. MetabBrainDis 35, 1009–1016 (2020). https://doi.org/10.1007/s11011-020-00554-x
32. MortonDH, BennettMJ, SeargeantLE, NichterCA, KelleyRI. Glutaric aciduria type I: a common cause of episodic encephalopathy and spastic paralysis in the Amish of Lancaster County, Pennsylvania. Am J Med Genet. 1991;41:89–95 33. BasingerAA, BookerJK, FrazierDM, KoeberlDD, SullivanJA, MuenzerJ.
Glutaricacidemiatype 1 inpatientsofLumbeeheritagefromNorthCarolina. MolGenetMetab. 2006;88:90–92.
34. Kölker S, Garcia-Cazorla A, Valayannopoulos V, Lund AM, Burlina AB, Sykut-Cegielska J, Wijburg FA, Teles EL, Zeman J, Dionisi-Vici C. The phenotypic spectrum of organic acidurias and urea cycle disorders. Part 1: the initial presentation. J Inherit Metab Dis. 2015a;38:1041–57 35. Fujimoto S, Shibata I, Sugiyama N, Ohba S, Togari H, Wada Y. Unique electroencephalographic change of acute encephalopathy in glutaric aciduria type 1.
Tohoku J Exp Med. 2000 May;191(1):31-8. doi: 10.1620/tjem.191.31. PMID: 10896037. 36. Monavari AA, Naughten ER. Prevention of cerebral palsy in glutaric aciduria type 1 by dietary management. Arch Dis Child. 2000 Jan;82(1):67-70. doi: 10.1136/adc.82.1.67.
PMID: 10630918; PMCID: PMC1718171.:
37. du Moulin M, Thies B, Blohm M, Oh J, Kemper MJ, Santer R, Mühlhausen C. Glutaric Aciduria Type 1 and Acute Renal Failure: Case Report and Suggested Pathomechanisms. 41
JIMD Rep. 2018;39:25-30. doi: 10.1007/8904_2017_44. Epub 2017 Jul 12. PMID: 28699143; PMCID: PMC5953902.
38. Kafil-Hussain NA, Monavari A, Bowell R, Thornton P, Naughten E, O'Keefe M. Ocular findings in glutaric aciduria type 1. J PediatrOphthalmol Strabismus. 2000 Sep-Oct;37(5):289-93. PMID: 11020111 39. Imerci A, Strauss KA, Oleas-Santillan GF, Miller F. Orthopaedic manifestations of glutaric acidemia Type 1. J ChildOrthop. 2020 Oct 1;14(5):473-479. 40. Kevin A. Strauss, Katie B. Williams, Vincent J. Carson, Laura Poskitt, Glutaric acidemia type 1: Treatment and outcome of 168 patients over three decades, Molecular Genetics and Metabolism,Volume 131, Issue 3, 2020, Pages 325-340, ISSN 1096-7192, https://doi.org/10.1016/j.ymgme.2020.09.007. 41. Fernández-Alvarez E, Nardocci N. Update on pediatric dystonias: etiology, epidemiology, and management. Degener Neurol Neuromuscul Dis. 2012;2:29-41. Published 2012 Apr 11. doi:10.2147/DNND.S16082 42. McClelland, V.M.; Bakalinova, D.B.; Hendriksz, C.; Singh, R.P. Glutaric aciduria type 1 presenting with epilepsy. Dev. Med. Child Neurol. 2009, 51, 235–239. [Google Scholar] [CrossRef] [PubMed] 43. Jovic, N.J.; Kosac, A.; Koprivsek, K. L-2-hydroxyglutaric aciduria: A case report.
SrpskiArhiv za CelokupnoLekarstvo 2014, 142, 337–341. [Google Scholar] [CrossRef] [PubMed][Green Version] 44. Periasamy, V.; Rudwan, M.; Yadav, G.; Khan, R.A. Epilepsy in a young adult caused by L-2-hydroxyglutaric aciduria: A case report. Med. Princ. Pract. Int. J. Kuwait Univ. Health Sci. Cent. 2008, 17, 258–261. [Google Scholar] [CrossRef] [PubMed] 45. Mete, A.; Isikay, S.; Sirikci, A.; Ozkur, A.; Bayram, M. Eyelid myoclonia with absence seizures in a child with l-2 hydroxyglutaric aciduria: Findings of magnetic resonance imaging. Pediatr. Neurol. 2012, 46, 195–197. [Google Scholar] [CrossRef] [PubMed] 46. Seijo-Martinez, M.; Navarro, C.; Castro del Rio, M.; Vila, O.; Puig, M.; Ribes, A.; Butron, M. L-2-hydroxyglutaric aciduria: Clinical, neuroimaging, and neuropathological findings.
Arch. Neurol. 2005, 62, 666–670. [Google Scholar] [CrossRef] [PubMed] 47. Calik, M.; Tuncer, F.N.; Sarikaya, S.; Karakas, O.; Cece, H.; Iscan, A. A case of l-2 hydroxyglutaric aciduria presenting as febrile seizure. Genet. Couns. 2014, 25, 363–367. [Google Scholar] [PubMed] 48. Leema P Cornelius, Vivekasaravanan Raju, Asir Julin Pediatric glutaric aciduria type 1: 14 cases, diagnosis and management Annals of Indian academy of neurology 2021 Vol. 24 Issue: 1 P.: 22-26 49. Iona Novak, Catherine Morgan, Michael Fahey, Megan Finch-Edmondson, Claire Galea, Ashleigh Hines, , State of the Evidence Traffic Lights 2019: Systematic Review of 42
Interventions for Preventing and Treating Children with Cerebral Palsy. Current Neurology and Neuroscience Reports (2020) 20: 3 https://doi.org/10.1007/s11910-020-1022-z 50. Larson A, Goodman S. Glutaric Acidemia Type 1. 2019 Sep 19. In: Adam MP, Ardinger HH, Pagon RA, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2021. Available from: https://www.ncbi.nlm.nih.gov/books/NBK546575/ 51. Kölker et al. J Inherit Metab Dis 30: 5-22, 2007b; J Inherit Metab Dis 34: 677-694, 2011, Boy, N., Mühlhausen, C., Maier, E.M., Heringer, J., Assmann, B., Burgard, P., Dixon, M., Fleissner, S., Greenberg, C.R., Harting, I., Hoffmann, G.F., Karall, D., Koeller, D.M., Krawinkel, M.B., Okun, J.G., Opladen, T., Posset, R., Sahm, K., Zschocke, J., Kölker, S. and (2017), Proposed recommendations for diagnosing and managing individuals with glutaric aciduria type I: second revision. J Inherit Metab Dis, 40: 75-101. https://doi.org/10.1007/s10545-016-9999-9,
52. Landmann E, Kreuder J, Gortner L, Neugebauer M, Reiter A, Blütters-Sawatzki R.
Effloreszenzen und Blutbildveränderungenbeieinem 9 MonatealtenSäuglingmitGlutarazidurieTyp I [Cutaneous lesions and blood count changes
in a 9-month old girl with glutaric aciduria type I]. KlinPadiatr. 2001 Mar-Apr;213(2):74-5. German. doi: 10.1055/s-2001-12880. PMID: 11305196. 53. Hakim M., Martin D., Beebe A., KlamarJ., Tobias J. Perioperative Management of a Patient With Glutaric Aciduria. Journal of Medical Cases, North America, 6, may. 2015.
Available at:
Информация
Список сокращений
Термины и определения
Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
| № п/п | Критерии оценки качества | Оценка выполнения |
|---|---|---|
| 1. | Выполнено комплексное определение концентрации на аминокислоты и ацилкарнитины в крови методом тандемной масс-спектрометрии (при установлении диагноза) | Да/Нет |
| 2. | Выполнено комплексное определение содержания органических кислот в моче (при установлении диагноза) | Да/Нет |
| 3. | Выполнено молекулярно-генетическое исследование мутаций в гене GCDH (при установлении диагноза) | Да/Нет |
| 4. | Выполнен прием (осмотр, консультация) врача-генетика первичный (при установлении диагноза) | Да/Нет |
| 5. | Выполнено назначение левокарнитина (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний) | Да/Нет |
| 6. | Выполнено назначение специализированного продукта лечебного питания, лишенного лизина и триптофана**** | Да/Нет |
Критерии оценки качества специализированной медицинской помощи
| № п/п | Критерии оценки качества | Оценка выполнения |
|---|---|---|
| 1. | Проведено лечение левокарнитином (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний) | Да/Нет |
| 2. | Выполнено назначение специализированного продукта лечебного питания, лишенного лизина и триптофана**** | Да/Нет |
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
- Врачи-генетики;
- Врачи общей врачебной практики (семейные врачи);
- Врачи- педиатры;
- Врачи-терапевты;
- Врачи-диетологи;
- Врачи-неврологи;
- Врачи-офтальмологи;
- Врачи-травматологи-ортопеды;
- Врачи-эпилептологи;
- Врачи-психиатры;
- Врачи-нефрологи;
- Врачи функциональной диагностики;
- Врачи-лабораторной генетики;
- Врачи клинической лабораторной диагностики;
- Студенты медицинских ВУЗов;
- Обучающиеся в ординатуре.
Таблица 1 Шкала оценки уровней достоверности доказательств (УДД)для методов диагностики (диагностических вмешательств)
| УДД | Расшифровка |
|---|---|
| 1 | Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
| 2 | Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
| 3 | Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая |
| 5 | Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД)для методов профилактики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
| УДД | Расшифровка |
|---|---|
| 1 | Систематический обзор РКИ с применением мета-анализа |
| 2 | Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа |
| 3 | Нерандомизированные сравнительные исследования, в т.ч. когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
| 5 | Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки уровней убедительности рекомендаций(УУР) для методов профилактики, диагностики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
| УУР | Расшифровка |
|---|---|
| A | Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
| B | Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
| C | Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций.
- Федеральный закон "Об основах охраны здоровья граждан в Российской Федерации" (N 323-ФЗ от 21.11.2011).
- Постановление Правительства РФ от 30 июля 1994 г. N 890 "О государственной поддержке развития медицинской промышленности и улучшении обеспечения населения и учреждений здравоохранения лекарственными средствами и изделиями медицинского назначения" (с изменениями и дополнениями)
- Приказ Минздрава России от 21 апреля 2022 года № 274н «Об утверждении Порядка оказания медицинской помощи пациентам с врожденными и (или) наследственными заболеваниями»
- Постановление Правительства от 26 апреля 2012 г. № 403 "О порядке ведения Федерального регистра лиц, страдающих жизнеугрожающими и хроническими прогрессирующими редкими (орфанными) заболеваниями, приводящими к сокращению продолжительности жизни граждан или их инвалидности, и его регионального сегмента"
- Приказ Минздрава России от 10 мая 2017 г. № 203н «Об утверждении критериев оценки качества медицинской помощи)»
- Приказ Министерства здравоохранения Российской Федерации от 15 декабря 2014 г. № 834н «Об утверждении унифицированных форм медицинской документации, используемых в медицинских организациях, оказывающих медицинскую помощь в амбулаторных условиях, и порядков по их заполнению»
- Приказ Минздрава России от 12 ноября 2021 г. № 1051н «Об утверждении порядка дачи информированного добровольного согласия на медицинское вмешательство и отказа от медицинского вмешательства, формы информированного добровольного согласия на медицинское вмешательство и формы отказа от медицинского вмешательства»
- Приказ Минздрава России от 24 ноября 2021 г. № 1094н "Об утверждении порядка назначения лекарственных препаратов, форм рецептурных бланков на лекарственные препараты, порядка оформления указанных бланков, их учета и хранения, форм бланков рецептов, содержащих назначение наркотических средств или психотропных веществ, порядка их изготовления, распределения, регистрации, учета и хранения, а также правил оформления бланков рецептов, в том числе в форме электронных документов"
- Приказ Минздрава России от 16 мая 2019 г. № 302н "Об утверждении Порядка прохождения несовершеннолетними диспансерного наблюдения, в том числе в период обучения и воспитания в образовательных организациях"
- Распоряжение Правительства РФ от 31 декабря 2018 г. № 3053-р "Об утверждении перечней медицинских изделий, имплантируемых в организм человека при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи и отпускаемых по рецептам на медицинские изделия при предоставлении набора социальных услуг"
- Приказ Министерства здравоохранения РФ от 6 июня 2013 г. N 354н "О порядке проведения патологоанатомических вскрытий" (зарегистрирован Министерством юстиции Российской Федерации 16 декабря 2013 г., регистрационный N 30612).
Основные нормативно-правовые акты, регулирующие оказание паллиативной медицинской помощи
- Федеральный закон от 12.11.2011 №323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации" (статья 36. Паллиативная медицинская помощь)
- Приказ Минздрава России № 345н, Минтруда России от 31.05.2019 № 372н «Об утверждении положения об организации оказания паллиативной медицинской помощи, включая порядок взаимодействия медицинских организаций, организаций социального обслуживания и общественных объединений, иных некоммерческих организаций, осуществляющих свою деятельность в сфере охраны здоровья».
- Приказ Минздрава России № 348н от 31 мая 2019 года «Об утверждении перечня медицинских изделий, предназначенных для поддержания органов и систем организма человека, предоставляемых для использования на дому».
- Приказ Минздрава России № 505н от 10 июля 2019 года «Об утверждении Порядка передачи от медицинской организации пациенту (его законному представителю) медицинских изделий, предназначенных для поддержания функций органов и систем организма человека, для использования на дому при оказании паллиативной медицинской помощи».
- Приказ МЗ РФ № 831 от 3 октября 2019 года «Об утверждении ведомственной целевой программы «Развитие системы оказания паллиативной медицинской помощи».
Прочие нормативно-правовые документы, с учетом которых разработаны клинические рекомендации:
- Международная классификация болезней, травм и состояний, влияющих на здоровье (МКБ – 10);
- Приказ МЗ РФ от 2 мая 2023 г. № 205н «Об утверждении номенклатуры должностей медицинских работников и фармацевтических работников».
- Приказ Минздравсоцразвития РФ от 23 июля 2010 г. № 541н «Об утверждении Единого квалификационного справочника должностей руководителей, специалистов и служащих, раздел «Квалификационные характеристики должностей работников в сфере здравоохранения».
- Федеральный закон от 25.12.2018 № 489-ФЗ «О внесении изменений в статью 40 Федерального закона "Об обязательном медицинском страховании в Российской Федерации" и Федеральный закон "Об основах охраны здоровья граждан в Российской Федерации" по вопросам клинических рекомендаций».
- Приказ Минздрава России № 103н от 28.02.2019 г. «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности, включаемой в клинические рекомендации информации».
- Приказ Минздрава России от 13.10.2017 N 804н "Об утверждении номенклатуры медицинских услуг".
- Приказ Министерства труда и социальной защиты РФ от 27 августа 2019 г. N 585н "О классификациях и критериях, используемых при осуществлении медико-социальной экспертизы граждан федеральными государственными учреждениями медико-социальной экспертизы";
- Приказ Министерства здравоохранения и социального развития Российской Федерации «О порядке применения лекарственных средств у больных по жизненным показаниям» от 9 августа 2005 г. № 494
- Информационное письмо Минздрава России по возможности закупки лекарственного препарата по торговому наименованию (https://www.rosminzdrav.ru/news/2019/12/18/13043-minzdrav-podgotovil-informatsionnoe-pismo-po-vozmozhnosti-zakupki-lekarstvennogo-preparata-po-torgovomu-naimenovaniyu);
- Распоряжение Правительства РФ от 11.12.2023 N 3551-р «Об утверждении перечня специализированных продуктов лечебного питания для детей-инвалидов»
Приложение А4. Клинико-диагностические критерии, позволяющие заподозрить глутаровую ацидурию тип 1 [16]
| Вероятность диагноза | Низкая | Умеренная | Высокая |
|---|---|---|---|
| Клинические критерии |
-Макроцефалия;
-Выступающие лобные бугры;
-Нарушения вскармливания
-Задержка двигательного развития
|
-Рейе-подобные эпизоды (острая метаболическая энцефалопатия)
-энцефалитоподобные эпизоды,
-гиперкинетическая форма детского церебрального паралича.
-периодическая атаксия
|
-Острая энцефалопатия
-прогрессирующие экстрапирамидные нарушения
-орофациальные дискинезии
|
| Семейный анамнез |
Не отягощен
|
Синдром «внезапной смерти младенца» или смертельный исход от некупируемых судорог в семье | Наличие в семье больного с подтвержденным диагнозом ГА тип 1, наличие смертельного исхода в семье от острого симметричного некроза базальных ганглиев |
|
Нейрорадио-
логические критерии
|
-атрофия/гипоплазия
лобных отделов
-задержка миелинизации
-вентрикуломегалия
-расширение субарахноидальных
пространств
|
-Субдуральные скопления
-атрофия/гипоплазия височных отделов
-лейкоэнцефалопатия (подростки, взрослые)
-изолированное поражение бледного шара
|
-Лобно-височная атрофия
головного мозга,
-изолированные симметричные некрозы базальных ганглиев (бледного шара и хвостатых ядер)
|
Приложение A5. Нейрорадиологические изменения (МРТ) головного мозга у пациентов с глутаровой ацидурией тип 1
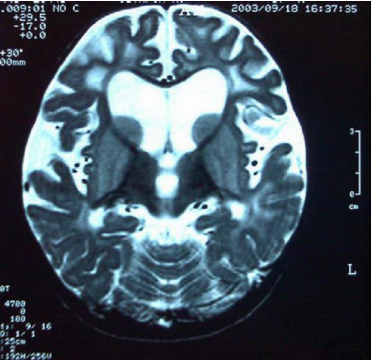
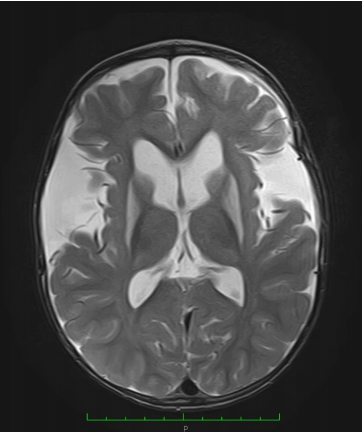
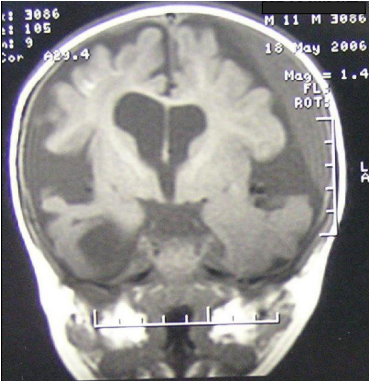
Рисунок. Субдуральные гематомы [2]
Приложение A6. Специализированные продукты на основе аминокислот без лизина и триптофана
| Наименование продукта | Белок (экв.) г |
Жир,
г
|
Углеводы, г | Энергетическая ценность, ккал |
Возраст
применения
|
|---|---|---|---|---|---|
|
Специализированный продукт сухой для диетического лечебного питания детей первого года жизни, больных глутаровой ацидурией, «Нутриген 14
-trp,- lys»****
|
14 | 23 | 50,4 | 472 | от 0 до 1 года |
| Специализированный продукт сухой для диетического лечебного питания детей старше одного года, больных глутаровой ацидурией, "Нутриген 20-trp, -lys"**** | 20 | 18 | 50,8 | 445 | старше 1 года |
|
Специализированный продукт сухой для диетического лечебного питания детей старше одного года, больных глутаровой ацидурией, «Нутриген 40
--trp,- lys»****
|
40 | 13 | 32,2 | 406 | старше 1 года |
|
Специализированный продукт сухой для диетического лечебного питания детей старше одного года, больных глутаровой ацидурией, «Нутриген 70
-trp,- lys»****
|
70 | 0 | 5,8 | 303 | старше 1 года |
| Специализированный продукт детского диетического лечебного питания для детей первого года жизни от 0 до 12 месяцев в качестве основного питания и в качестве дополнительного питания для детей до 3 лет "GA1 Анамикс Инфант"**** | 13,1 | 23 | 49,8 | 466 | от 0 до 1 года |
| Специализированный продукт диетического лечебного питания "XLYS, TRY Глутаридон"**** | 79 | - | 4 | 332 | старше 1 года |
Приложении A7. Ориентировочная потребность в лизине и триптофане у пациентов с глутаровой ацидурией тип 1 в зависимости от возраста
| Возраст больных | Суточная потребность в аминокислотах мг/кг массы тела | |
|---|---|---|
| Лизин | Триптофан | |
| 0 - 3 мес | 80-100 | 10-20 |
| 3 - 6 мес | 70-90 | 10-15 |
| 6 - 9 мес | 60-80 | 10-12 |
| 9 - 12 мес | 50-70 | 10-12 |
| 1 – 4 года | 55-65 | 8-12 |
| 4 – 7 лет | 45-55 | 7-11 |
| 7 – 11 лет | 35-45 | 4-10 |
| Девушки 11- 15 лет | 30-40 | 4-6 |
| Девушки 15- 18 лет | 20-30 | 3-5 |
| Юноши 11- 15 лет | 30-40 | 4-6 |
| Юноши 15- 18 лет | 35-45 | 6-8 |
Приложение A8. Рекомендуемые нормы потребления белка и среднее содержание лизина в различных пищевых продуктах (справочная информация для составления лечебного рациона пациентам с глутаровой ацидурией тип 1)
Таблица 1 - Рекомендуемые нормы потребления белка для здоровых детей различного возраста [1,3,18,22]
| Возраст |
RDA США
(г/кг/сутки)
|
ВОЗ
(г/кг/сутки)
|
Евросоюз
(г/кг/сутки)
|
Россия
|
|---|---|---|---|---|
| 0-6 мес | 2,2 | 1,38 | - | 2,2 (г/кг/сутки) |
| 6-12 мес | 1,6 | 1,21 | 1,6 | 2,6-2,9 (г/кг/сутки) |
| 1-2 года | - | - | - | 36 г/сут* |
| 2-3 года | - | - | - | 42 г/сут |
| 1-3 года | 1,2 | 0,97 | 1,1 | - |
| 4-6 лет | 1,1 | 0,84 | 1,0 | 54 г/сут |
| 7-10 лет | 1,0 | 0,8 | 1,0 | 63 г/сут |
| Мальчики 11-14 лет | 1,0 | 0,79 | 1,0 | 75 г/сут |
| Мальчики14-18 лет | 0,9 | 0,69 | 0,9 | 87 г/сут |
| Девочки 11-14 лет | 1,0 | 0,76 | 0,95 | 69 г/сут |
| Девочки 14-18 лет | 0,8 | 0,64 | 0,85 | 76 г/сут |
Таблица 2 - Среднее содержание лизина в белках различных продуктов [18,20].
| Продукты |
Содержание лизина
(% от общего белка)
|
Лизин/белок
(мг/г белка)
|
|---|---|---|
| Рыба | 9 | 90 |
| Мясо и мясные продукты | 8 | 80 |
| Грудное молоко | 8 | 80 |
| Коровье молоко и молочные продукты | 7 | 70 |
| Яйца | 6 | 60 |
| Картофель | 6 | 60 |
| Соя и соевые продукты | 6 | 60 |
| Орехи | 2-8,5 | 20-85 |
| Фрукты | 2-6,5 | 40-65 |
| Овощи | 4-6,5 | 20-65 |
| Хлеб и зерновые продукты | 2-4 | 20-40 |
Приложение A9. Комплекс обязательных мероприятий, которые должны быть проведены пациенту после установления диагноза глутаровая ацидурия тип 1
| Возраст больных детей | ||||||
|---|---|---|---|---|---|---|
| 0-6 месяцев | 7-12 месяцев | 1-3 года | 4-6 лет | Старше 6 лет | ||
| Диетотерапия | ||||||
|
Лизин белка натуральных продуктов мг/кг/сут
|
100
|
90
|
80-60
|
60-50
|
Избегать чрезмерного поступления белка. Употреблять продукты с низким содержанием лизина
(Deweyetal 1996)
|
|
| Триптофан белка натуральных продуктов мг/кг/сут | 20 | 17 | 17-13 | 13 | 13 | |
| Белок натуральный (г/кг/сут) | 1,4-1,3 | 1,5-1,3 | 1,4-1,3 | 1,3-1.1 | 1,3-1,1 | |
| Белок за счет СП* (г/кг/сут) | 1,3-0,8 | 1,0-0,8 | 0,8 | 0,8 | 0,8 | |
| Белок (общий) (г/кг/сут) | 2,7-2,1 | 2,5-2,1 | 2,2-2,1 | 2,1-1,9 | 2,1-1,9 | |
| Энергетическая ценность (ккал/кг/сут) | 115-80 | 95-80 | 95-80 | 90-78 | 90-78 | |
| Микронутриенты (%) | ≥100 | ≥100 | ≥100 | ≥100 | >100 | |
| Основная метаболическая терапия | ||||||
| Карнитин мг/кг/сут | 100 | 100 | 100 | 50-100 | 30-50 | |
Приложение A10. Основные принципы терапии в условиях стационара
| А. Восстановление энергетической потребности | ||||
|---|---|---|---|---|
| Калории | Повышение энергетической потребности до 120% от возрастной нормы | |||
| 120% (расчет диеты на ккал/кг/день)1 | 0-6 месяцев | 7-12 месяцев | 1-3 года | 4-6лет |
| 98-128 | 96-109 | 98-109 | 96-98 | |
| Б. Внутривенная инфузионная терапия | ||||
| Декстроза** | 8-15 г/кг/сут | |||
| Жиры 20% (по показаниям), при отсутствии метаболического ацидоза | Начальная доза 1-2 г/кг/день, если возможно, повышение дозы до 2-3 г/кг/день | |||
| Коррекция электролитных нарушений | Солевые растворы и/или растворы электролитов | |||
| Инсулинотерапия |
При гипергликемии выше 10 ммоль/л и/или глюкозурии возможно введение Инсулина и его аналогов
(контролировать уровень калия в крови)
|
|||
| Левокарнитин | 150-200 мг/кг/сутки | |||
| С. Потребность в белке | ||||
| Натуральный белок | Полное исключение белка максимально на 24-часа, с постепенным возвратом до минимально безопасного уровня в течение 48-72 часов. Если ребенок находится на низкобелковой диете без приема аминокислотных смесей, осуществляют постепенное введение белка в течение 24 -48часов. | |||
| Аминокислотные смеси (без лизина) | Аминокислотные смеси назначают per os или через назогастральный зонд в дозе 0,8-1,3 г/кг/день | |||
| Д. Фармакотерапия | ||||
| Жаропонижаю-щая терапия | При повышение температуры выше 38,5С – ибупрофен**и парацетамол**в возрастной дозе | |||
|
Антибактериаль-
ная терапия
|
Назначают в зависимости от предполагаемого патогенного агента в возрастных дозах | |||
| Противорвотные средства | метоклопрамид** или #ондансетрон**в возрастной дозировке | |||
|
Дегидратацион-
ная терапия
|
Если диурез менее, чем 3-4 мл/кг/день, назначают фуросемид**в возрастной дозировке (не более чем, 3-4 инъекции в день) (следить за электролитными нарушениями в крови) | |||
| Натрия гидрокарбонат |
В случае декомпенсированного метаболического ацидоза, возможно назначение Натрия гидрокарбоната**
внутривенно (под контролем рН и Na+ в крови) или перорально.
|
|||
|
Антиэпилепти-
ческая терапия
|
При судорогах возможно назначения стандартной антиэпилептической терапии в зависимости от типа судорожных приступов с использованием таких препаратов как фенобарбитал** леветирацетам**, ламотриджин, топирамат**, фенитоин**, карбамазепин** и клоназепам** в возрастных дозах. Нзаначение препаратов вальпроевой кислоты** нежелательно. | |||
| Е. Контроль жизненно-важных функций и лабораторных показателей | ||||
| Жизненно-важные функции | Частота сердечных сокращений, частота дыхательных движений, контроль артериального давления, температуры, диуреза. При угнетении сознания- оценка уровня сознания по шкале Глазго. | |||
| Кровь | Уровень глюкозы, рН и газы крови, электролиты (калий, натрий, кальций ионизированный, хлор). | |||
| Биохимические параметры | Обоснование назначений | Частота исследований (возраст) | ||
|---|---|---|---|---|
| От 0 до 1 года | 1-6 лет | Старше 6 лет | ||
| Аминокислоты (в крови) | Оценка общего аминокислотного статуса | Каждые 1-2 месяца | Каждые 3-6 месяца | Каждые 6 -12 месяцев |
|
Уровень карнитина
(в крови)
|
Профилактика вторичного истощения карнитинового пула, контроль осложнений | Каждые 2 месяца | Каждые 3месяца | Каждые 6-12 месяцев |
| Общий анализ крови + ферритин | Плановый контроль .Регулярное наблюдение, избегайте истощения запасов железа, фолиевой кислоты или кобаламина | Каждые 6 месяцев | Каждые 6 месяцев | Каждые 6 -12 месяцев |
| Альбумин крови | Нутритивный статус | Если существуют опасения по поводу статуса питания и у детей с проблемами питания | ||
| Кальций и фосфор крови, щелочная фосфатаза | Состояние костной ткани * | Каждые 3 месяца | Каждые 6 месяцев | Каждые 12 месяцев |
|
Аспартатаминотрансфераза
Аланинаминотрасфераза
Гамма-глутамилтранспептидаза
|
Плановый контроль, профилактика метаболической декомпенсации | Каждые 3 месяца | Каждые 6 месяцев | Каждые 12 месяцев |
| Нейрорадиологическое исследование головного мозга (МРТ/КТ) | Контроль структурных изменений головного мозга | При установлении диагноза, а также после перенесенного энцефалитоподобногокриза, появления прогрессирующей неврологической симптоматики | ||
Приложение A12. Мероприятия, направленные на предотвращение развития повторных энцефалитоподобных кризов
| Мероприятия | Содержание мероприятия и методы их реализации |
|---|---|
| Образование и обучение родителей | Родители должны быть осведомлены о клиническом течении заболевания и его осложнениях. Они должны быть четко информированы о тактике терапии во время развивающегося энцефалитоподобного криза. |
| Лечебно-просветительская работа | Необходимо обеспечить в обязательном порядке индивидуальным протоколом основной метаболической и интенсивной инфузионной терапии родителей, врачей детской поликлиники по месту жительства пациента. Родители должны быть обеспечены литературой по клинической картине и лечению ГА1. В лечебном протоколе должен быть указан номер телефона лечащего врача, с которым можно связаться в любое необходимое для пациента время. |
| Экстренная медицинская помощь на дому | Родители должны иметь все необходимые лекарственные средства для начала интенсивной терапии на дому. |
| Обеспечение преемственности в лечении (детская поликлиника, районные больницы, метаболический центр) | Врачи детских поликлиник/районных больниц по месту жительства пациента, должны быть поставлены в известность о пациентах с ГА1, и инструктированы по тактике лечения. Индивидуальный протокол по лечению пациента должен быть отослан в поликлинику/стационар по месту жительства, незамедлительно после установления диагноза. Интенсивное лечение должно быть начато до перевода в специализированный метаболический центр, хорошо владеющий лечением данной патологии. |
| Медицинская помощь в выходные, праздничные дни и отпускной период | При выезде ребенка на отдых (в регионы вдали от дома), необходимо отправить по месту пребывания больного ребенка протокол индивидуального лечения, номер телефона лечащего врача. |
| Медицинская помощь во время инфекционных заболеваний | При возникновении инфекционных заболеваний и повышении температуры тела до 38,50С родители пациента как можно скорее, должны поставить в известность о случившемся лечащего врача. |
| Медицинская помощь при плановых хирургических вмешательствах | При плановом хирургическом вмешательстве врачи хирурги, анестезиологи должны быть информированы о клиническом течении заболевания, лечащий врач должен отправить в хирургический стационар протокол послеоперационного ведения пациента. Основными рекомендациями являются: избегать голодания, назначение растворов глюкозы и двойной дозы карнитина |
Приложение Б. Алгоритмы действий врача
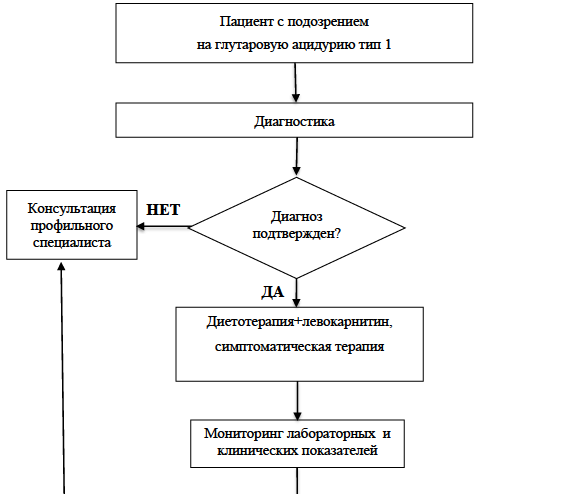
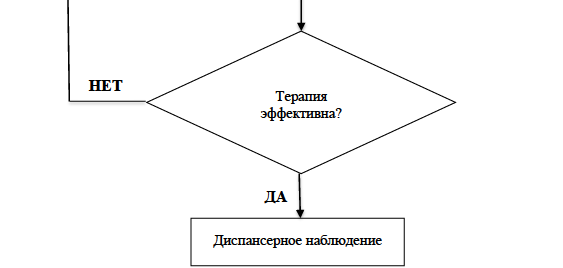
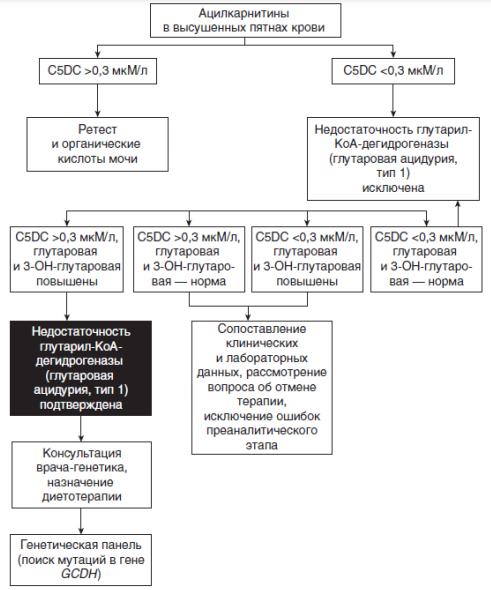
Алгоритм проведения скрининга на глутаровую ацидурию типа I
Приложение В. Информация для пациента
Что такое глутаровая ацидурия тип 1?
Основные цели диетотерапии:
- Нормальное физическое и интеллектуальное развитие.
- Прибавка в весе и росте, в соответствие с возрастом.
- Предупреждение катаболических ситуаций, которые могут привести к метаболическим кризам
Если у ребенка нет признаков метаболического криза или инфекционного заболевания лечение проводят в стандартном, поддерживающем режиме, при котором потребление лизина с пищей строго контролируется, и ребенок получает специализированную лечебную смесь (без лизина, с низким содержанием триптофана), чтобы обеспечить достаточное количество белка для роста и развития.
- длительное голодание
- инфекция
- тяжелая физическая и эмоциональная нагрузка
Первые симптомы метаболического криза: повышенная сонливость, изменение поведения, раздражительность, снижение аппетита. Часто криз провоцирует инфекция, поэтому первые проявления могут начинаться лихорадкой, тошнотой, диареей, рвотой. Может наблюдаться снижение сахара в крови. Если своевременно не начать лечение у ребенка может появиться одышка, судороги и кома.
Необходимо в срочном порядке госпитализировать ребенка в клинику для обеспечения приема большого количества калорий, уменьшение или исключение белка для предотвращения, а также дополнительный прием карнитина. для проведения инфузионной терапии. Метаболические кризы - очень опасны. Именно в этот период могут развиться необратимые повреждения головного мозга.
| Исследование | Регулярность исследования |
|---|---|
| Коррекция диетотерапии (проводят врачи-генетики или врачи-диетологи) | 1 р/мес на 1 году жизни, далее 1 р/3 мес и по показаниям до 3 лет; 1 р 6 мес после 3 лет |
| ультразвуковое исследование (УЗИ) органов брюшной полости | 1 раз в год |
| проведение электроэнцефалографии (ЭЭГ) | 1 раз в год |
| проведение биохимического анализа крови | каждые 3 месяца пациентам до года, каждые 6 месяцев пациентам от 1 года до 6 лет, каждые 12 месяцев пациентам старше 6 лет |
| общий анализ крови | каждые 6 месяцев пациентам до 6 лет, каждые 6-12 месяцев пациентам старше 6 лет. |
| определение уровня свободного карнитина и аминокислот | каждые 1-2 месяца пациентам до года, каждые 3 - 6 месяцев у детей младше 6 лет, каждые 6 -12 месяцев пациентам старше 6 лет. |
Как пациенты с ГА1 получают лечение в Российской Федерации?
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.