ВИЧ-инфекция у беременных
 Версия: Клинические рекомендации РФ 2025 (Россия)
Версия: Клинические рекомендации РФ 2025 (Россия)
Общая информация
Краткое описание
Разработчик клинической рекомендации
Российское общество акушеров-гинекологов
Общественная организация "Российская ассоциация специалистов перинатальной медицины"
Национальная вирусологическая ассоциация
Московское общество акушеров-гинекологов
Одобрено Научно-практическим Советом Минздрава России
Клинические рекомендации
ВИЧ-инфекция у беременных
Год утверждения (частота пересмотра): 2025
Пересмотр не позднее: 2027
ID:717_2
Возрастная категория: Взрослые
Определение заболевания или состояния (группы заболеваний или состояний)
Болезнь, вызванная вирусом иммунодефицита человека, или ВИЧ-инфекция (англ. Human Immunodeficiency Virus Infection, HIV-infection) - медленно прогрессирующее антропонозное заболевание с контактным путём передачи, характеризующееся поражением иммунной системы с развитием синдрома приобретённого иммунодефицита (СПИД). Клиническими проявлениями несостоятельности иммунной системы являются оппортунистические инфекции, злокачественные новообразования, дистрофические и аутоиммунные процессы, что при отсутствии специфического лечения ведет к гибели инфицированного человека.
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
В Международной классификации болезней и проблем, связанных со здоровьем, 10-го пересмотра (МКБ-10) предусмотрены коды для различных состояний и медицинских услуг, связанных с ВИЧ-инфекцией. Кодирование предназначено для статистического учёта и не предполагает определение тяжести течения или прогноза заболевания. При практическом использовании кодов МКБ им могут соответствовать различные категории или стадии в клинических классификациях ВИЧ-инфекции [5,6,16].
Ниже приводятся состояния и медицинские услуги, связанные с ВИЧ-инфекцией, в соответствии с МКБ-10.
Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], проявляющаяся в виде инфекционных и паразитарных болезней (B20):
B20.0 - Болезнь, вызванная ВИЧ, с проявлениями микобактериальной инфекции;
B20.1 - Болезнь, вызванная ВИЧ, с проявлениями других бактериальных инфекций;
B20.2 - Болезнь, вызванная ВИЧ, с проявлениями цитомегаловирусного заболевания;
B20.3 - Болезнь, вызванная ВИЧ, с проявлениями других вирусных инфекций; B20.4 - Болезнь, вызванная ВИЧ, с проявлениями кандидоза;
B20.5 - Болезнь, вызванная ВИЧ, с проявлениями других микозов;
B20.6 - Болезнь, вызванная ВИЧ, с проявлениями пневмонии, вызванной P. jirovecii;
B20.7 - Болезнь, вызванная ВИЧ, с проявлениями множественных инфекций;
B20.8 - Болезнь, вызванная ВИЧ, с проявлениями других инфекционных и паразитарных болезней;
B20.9 - Болезнь, вызванная ВИЧ, с проявлениями неуточненных инфекционных и паразитарных болезней.
Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], проявляющаяся в виде злокачественных новообразований (B21):
B21.0 - Болезнь, вызванная ВИЧ, с проявлениями саркомы Капоши;
B21.1 - Болезнь, вызванная ВИЧ, с проявлениями лимфомы Беркитта;
B21.2 - Болезнь, вызванная ВИЧ, с проявлениями других неходжкинских лимфом;
B21.3 - Болезнь, вызванная ВИЧ, с проявлениями других злокачественных новообразований лимфатической, кроветворной и родственных им тканей;
В21.7 - Болезнь, вызванная ВИЧ, с проявлениями множественных злокачественных новообразований;
B21.8 - Болезнь, вызванная ВИЧ, с проявлениями других злокачественных новообразований;
B21.9 - Болезнь, вызванная ВИЧ, с проявлениями неуточненных злокачественных новообразований.
Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], проявляющаяся в виде других уточненных болезней (B22):
B22.0 - Болезнь, вызванная ВИЧ, с проявлениями энцефалопатии;
B22.1 - Болезнь, вызванная ВИЧ, с проявлениями лимфатического интерстициального пневмонита;
B22.2 - Болезнь, вызванная ВИЧ, с проявлениями изнуряющего синдрома;
B22.7 - Болезнь, вызванная ВИЧ, с проявлениями множественных болезней, классифицированных в других рубриках.
Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], проявляющаяся в виде других состояний (B23):
B23.0 - Острый ВИЧ-инфекционный синдром;
B23.1 - Болезнь, вызванная ВИЧ, с проявлениями (персистентной) генерализованной лимфаденопатии;
В23.2 - Болезнь, вызванная ВИЧ, с проявлениями гематологических и иммунологических нарушений, не классифицированных в других рубриках;
B23.8 - Болезнь, вызванная ВИЧ, с проявлениями других уточненных состояний;
В24 - Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], неуточненная;
F02.4 - Деменция при болезни, вызванной вирусом иммунодефицита человека [ВИЧ] (В22.0);
О98.7 - Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], осложняющая беременность, деторождение и послеродовой период;
R75 - Лабораторное обнаружение вируса иммунодефицита человека [ВИЧ];
Z11.4 - Специальное скрининговое обследование с целью выявления инфицирования вирусом иммунодефицита человека [ВИЧ];
Z20.6 - Контакт с больным и возможность заражения вирусом иммунодефицита человека [ВИЧ];
Z21 - Бессимптомный инфекционный статус, вызванный вирусом иммунодефицита человека [ВИЧ];
Z71.7 - Консультирование по вопросам, связанным с вирусом иммунодефицита человека [ВИЧ];
Z83.0 - В семейном анамнезе болезнь, вызванная вирусом иммунодефицита человека [ВИЧ].
Основными кодами статистического наблюдения МКБ-10, используемыми в Российской Федерации при составлении медицинской отчётности о больных ВИЧ - инфекцией (форма № 61), являются коды В20-В24. Поскольку в настоящее время научно доказано отсутствие возможности носительства вируса иммунодефицита человека, а обнаружение в организме человека ВИЧ свидетельствует о наличии заболевания с различной скоростью прогрессирования, использование кода Z21 в отношении пациентов с лабораторно подтвержденным диагнозом некорректно. Вместо него рекомендуется использование кода В23.
На практике у многих пациентов с бессимптомной ВИЧ-инфекцией имеется увеличение лимфатических узлов, состояние таких пациентов может соответствовать категории В23.1. У большинства регистрируются иммунологические нарушения (снижение количества CD4 у многих пациентов, а инверсия соотношения CD4/CD8 - почти у всех) или гематологические изменения (лимфопения, анемия, тромбоцитопения). Для таких пациентов целесообразно использовать код по МКБ-10 В23.2.
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Согласно действующей в России классификации ВИЧ-инфекции (РК, 2006) [3,5], стадия и фаза заболевания устанавливаются только на основании клинических проявлений.
Уровень ВН и CD4 не является критерием для определения клинической стадии или фазы заболевания.
Российская клиническая классификация ВИЧ-инфекции
1. Стадия инкубации.
2. Стадия первичных проявлений.
Варианты течения:
А. Бессимптомное;
Б. Острая ВИЧ-инфекция без вторичных заболеваний;
В. Острая ВИЧ-инфекция с вторичными заболеваниями.
3. Субклиническая стадия.
4. Стадия вторичных заболеваний.
4А. Потеря массы тела менее 10%, грибковые, вирусные, бактериальные поражения кожи и слизистых, повторные фарингиты, синуситы, опоясывающий лишай.
Фазы:
— прогрессирование на фоне отсутствия АРТ, на фоне АРТ;
— ремиссия (спонтанная, после АРТ, на фоне АРТ).
4Б. Потеря массы тела более 10%, необъяснимая диарея или лихорадка более мес., повторные стойкие вирусные, бактериальные, грибковые, протозойные поражения внутренних органов, локализованная саркома Капоши, повторный или диссеминированный опоясывающий лишай.
Фазы:
— прогрессирование на фоне отсутствия АРТ, на фоне АРТ;
— ремиссия (спонтанная, после АРТ, на фоне АРТ).
4В. Кахексия. Генерализованные вирусные, бактериальные, микобактериальные, грибковые, протозойные, паразитарные заболевания, в том числе: кандидоз пищевода, бронхов, трахеи, легких; пневмоцистная пневмония; злокачественные опухоли; поражения центральной нервной системы.
Фазы:
— прогрессирование на фоне отсутствия АРТ, на фоне АРТ;
— ремиссия (спонтанная, после АРТ, на фоне АРТ).
5. Терминальная стадия.
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Вирус иммунодефицита человека (ВИЧ), впервые выделенный в 1983 году, относится к семейству ретровирусов (Retroviridae). В семействе ретровирусов выделяют два подсемейства - онковирусов (Oncoviridae) и медленных лентивирусов (Lentivirus). К первому подсемейству отнесены вирусы, вызывающие лейкозы: Т-клеточную лейкемию и хронический волосатоклеточный лейкоз, а также вирус лейкемии крупного рогатого скота. ВИЧ относится к подсемейству лентивирусов.
В настоящее время описаны два серотипа вируса: ВИЧ-1 и ВИЧ-2, различающиеся по структурным и антигенным характеристикам. Наибольшее эпидемиологическое значение имеет ВИЧ-1, доминирующий в современной пандемии и имеющий наибольшее распространение на территории Российской Федерации. ВИЧ-2 встречается преимущественно в странах Западной Африки. Попадая в организм человека, ВИЧ поражает различные органы и ткани, но, в первую очередь, клетки, несущие маркер CD4. Рецептор CD4 имеют, главным образом, Лимфоциты-хелперы, играющие центральную роль в иммунном ответе, а также клетки нервной системы (нейроглии), моноциты, макрофаги, эндотелий сосудов, клетки Лангерганса и т. д.
Поражение Т-лимфоцитов-хелперов (CD4) приводит к нарушению межклеточных взаимодействий внутри иммунной системы, ее функциональной несостоятельности, постепенному истощению и, как результат, - прогрессирующему иммунодефициту.
Результатом нарушений в иммунной системе является снижение сопротивляемости организма. Развивается широкий спектр заболеваний: вторичные (оппортунистические) инфекции, онкологические, гематологические, аутоиммунные и лимфопролиферативные заболевания.
Характерным проявлением ВИЧ-инфекции является хроническое воспаление с поражением всех органов и систем: аутоиммунные реакции, болезни иммунных комплексов и метаболические нарушения приводят к поражению эндотелия сосудов и соединительной ткани с развитием кардиоваскулярной, неврологической, эндокринной и костно-суставной патологии. Всё это обуславливает полиорганность поражений и разнообразие клинической симптоматики.
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Источником инфекции является человек, инфицированный ВИЧ, в любых стадиях заболевания. Роль инфицированного человека, как источника инфекции, возрастает в раннюю и позднюю стадии болезни (стадия первичных проявлений и стадия вторичных заболеваний с выраженным нарушением иммунореактивности) [1-6].
Пути передачи вируса: естественный (половой, от матери ребенку) и искусственный (парентеральный - инъекционный, трансфузионный, трансплантационный, в том числе при попадании зараженного материала на поврежденную кожу и слизистые оболочки глаз, носа и ротовой полости).
Вирус передаётся через кровь, сперму, секрет влагалища, грудное молоко.
Половой путь - в последние годы является доминирующим в распространении ВИЧ-инфекции. Вероятность заражения коррелирует с количеством половых партнеров человека и повышается при воспалительных и диспластических заболеваниях половых органов и прямой кишки.
Передача ВИЧ от матери ребенку - может произойти при любом сроке беременности, во время родов и при грудном вскармливании. В основном, передача инфекции происходит в последние недели беременности и во время родов. Без профилактики частота передачи ВИЧ от матери ребенку составляет около 40%.
Парентеральный путь реализуется попаданием ВИЧ-инфицированного материала во внутренние среды организма при медицинских, парамедицинских и ритуальных вмешательствах. Среди парентеральных вмешательств наибольшую степень риска заражения имеет внутривенное введение крови. Высокий риск инфицирования существует при: внутривенном введении ПАВ нестерильными шприцами и иглами; переливании ВИЧ-инфицированной крови и ее препаратов; использовании медицинского и немедицинского инструментария, загрязненного биологическими жидкостями человека, инфицированного ВИЧ. Кроме того, факторами заражения могут быть органы и ткани доноров, используемые для трансплантации.
По данным ВОЗ, в 2019 г. в мире зарегистрированы 38,0 млн человек с ВИЧ-инфекцией. В 2018 году - 37,8 млн человек, соответственно. Наиболее пораженным регионом является Африканский регион - здесь в 2019 г. проживает более двух третей (25,7 млн человек) от общего числа больных ВИЧ-инфекцией. К ключевым группам населения подвергающихся повышенному риску инфицирования ВИЧ, независимо от типа эпидемии или местных условий относятся: МСМ; лица, употребляющие инъекционные ПАВ; находящиеся в местах лишения свободы и других условиях изолированного пребывания; работники коммерческого секса.
Согласно данным Министерства здравоохранения Российской Федерации в 2020 г. охват тестированием на ВИЧ-инфекцию населения России составил 24,7%, в 2019 году - 28,5%, в 2018 году - 26,8%. В 2020 г. заболеваемость ВИЧ составляла 41,1 на 100 тыс. населения страны, в 2019 г. - 54,6 на 100 тыс., в 2018 - 58,6 на 100 тыс.
В 2019 г. наивысшие уровни распространенности заболевания отмечены в Кемеровской, Свердловской, Иркутской, Оренбургской, Самарской, Тюменской, Томской областях, Пермском, Красноярском, Алтайском крае [7]. За последние годы наметилась тенденция активного вовлечения женщин в эпидемию ВИЧ-инфекции, и возросла роль полового пути передачи у женщин детородного возраста, что усугубляет проблему передачи ВИЧ-инфекции от матери ребенку во время беременности и родов [8].
В 2019 г. отмечается положительная динамика в охвате трехэтапной профилактике передачи ВИЧ-инфекции от матери ребенку с 88,7% в 2017 году, 90,8% в 2018 году до 92,4%. В 2020 году зарегистрировано 681 новых случаев ВИЧ -инфекции среди детского населения, в 2019 году - 852, в 2018 году - 977 новых случаев (в возрасте от 0 до 17 лет) [7].
Заражение детей ВИЧ-инфекцией более, чем в 90% случаев происходит при перинатальном контакте с ВИЧ-инфицированной матерью и при сохранении грудного вскармливания [9-11]. Вероятность передачи ВИЧ-инфекции от матери ребенку без проведения профилактических мероприятий составляет до 40 % [11,12].
Риск заражения детей внутриутробно и во время родов оценивается в 15-30%, при грудном вскармливании - 5-15%, повышается при инфицировании женщины в период беременности и на поздних стадиях заболевания. Перинатальная передача ВИЧ от матери ребенку у женщин с уровнем СИ4+лимфоцитов ниже 350 мкл-1 осуществляется в 80 % случаев [13,14].
Своевременное начало и эффективность профилактики передачи ВИЧ-инфекции от матери ребёнку при благоприятно протекающей беременности снижают риск инфицирования ребенка до 1% [10,12].
Частота преждевременных родов в группе ВИЧ-инфицированных беременных женщин составляет 17,1%, а в группе, где произошло перинатальное инфицирование - 43,9% [15]. Патологическое течение беременности, особенно угроза ее прерывания, повышают вероятность инфицирования ребенка до 2-3%, что существенно увеличивает значимость качественной и эффективной акушерско-гинекологической помощи ВИЧ-инфицированным беременным [10]. Современные подходы определяют срок начала АРТ - или до беременности, или на 13 нед. беременности. При этом риск перинатальной передачи ВИЧ-инфекции снижается до минимальных значений. Начало АРТ на 14 - 27 нед. увеличивает риск передачи ВИЧ-инфекции от матери ребенку в 2,3 раза, с 28 нед. и позднее - в 4,5 раза [10].
На эффективность профилактики передачи ВИЧ-инфекции от матери ребенку оказывает существенное влияние преемственность в работе территориальных центров профилактики и борьбы со СПИДом и МО по своевременному выявлению ВИЧ-инфекции у женщин репродуктивного возраста, раннему началу АРТ у ВИЧ- инфицированных женщин во время беременности, проведению ППМР у ВИЧ- инфицированных женщин во время родов и новорожденному, выбору способа родоразрешения.
Мероприятия по профилактике передачи ВИЧ-инфекции от матери ребенку осуществляются при добровольном информированном согласии женщины. Индивидуальный подбор схемы АРТ, медицинское наблюдение, профессиональная психологическая поддержка во время беременности и родов определяют состояние здоровья и качество жизни будущего ребёнка.
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Клиническая картина заболевания ВИЧ-инфекция описана в клинических рекомендациях «ВИЧ-инфекция у взрослых». Планирование и ведение беременности у женщины с ВИЧ-инфекцией описано в главе 3.1, 7. Родоразрешение у беременной с ВИЧ-инфекцией описано в главе 3.2 данных клинических рекомендаций.
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Для диагностики ВИЧ-инфекции во время беременности применяются стандартные методы выявления антител к ВИЧ (ИФА, ИХЛА, ИБ) [17-24]. Основой профилактики передачи ВИЧ-инфекции от матери ребенку является своевременность выявления ВИЧ-инфекции у женщин детородного возраста, постановка на диспансерный учет, назначение АРТ.
-
Рекомендуется всем женщинам фертильного возраста, всем беременным, обследование на ВИЧ-инфекцию с целью исключения инфицирования ВИЧ [25-27].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 1).
-
Рекомендуется половому партнёру беременной обследование на ВИЧ-инфекцию с целью исключения инфицирования ВИЧ [25-27].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 2).
Комментарии: беременным, с целью исключения инфицирования ВИЧ, проводить обследование на ВИЧ-инфекцию двукратно - при постановке на учёт по беременности и в третьем триместре беременности, на сроке гестации в 34-36 недель [125].
Комментарии: обследование на наличие ВИЧ-инфекции во время беременности проводится:
— после получения добровольного информированного согласия женщины (Приложение А3.1);
— только при наличии документа, удостоверяющего личность женщины (за исключением случаев оказания экстренной помощи) [125].
-
Рекомендуется дополнительное обследование на ВИЧ-инфекцию, до истечения 36 недели беременности, женщинам:
— имеющим ВИЧ-инфицированных партнеров и беременным, употребляющим ПАВ;
— проживающим в наиболее пораженных субъектах (пораженность беременных более 1%) [29];
— беременным с признаками или симптомами острой ВИЧ-инфекции (например, лихорадка, лимфаденопатия, кожная сыпь, миалгия, головные боли, язвы во рту, лейкопения, тромбоцитопения, повышенный уровень трансаминаз).
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 3).
-
Рекомендуется прохождение добровольного обследования в наркологическом диспансере по месту жительства в случае, если беременная отрицает употребление ПАВ, но имеются убедительные признаки их употребления [30,31].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
1. Жалобы и анамнез
См. клинические рекомендации «ВИЧ-инфекция у взрослых».
При сборе анамнеза врач-акушер-гинеколог уточняет сведения о приеме беременной ПАВ.
-
Рекомендуется врачу акушеру-гинекологу направить письменный запрос в МО наркологического профиля по месту жительства беременной женщины, в случае если беременная подтверждает употребление ПАВ, состоит под наблюдением в наркологическом диспансере, уточнить срок употребления ПАВ, способ употребления, дату последнего употребления ПАВ, наличие в анамнезе передозировок, лечения наркозависимости, прохождения реабилитации [30,31].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
2. Физикальное обследование
См. клинические рекомендации «ВИЧ-инфекция у взрослых».
3. Лабораторные диагностические исследования
3.1. Диагностика ВИЧ-инфекции до и во время беременности
-
Рекомендуется количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР у беременных:
— при получении сомнительных результатов тестирования на антитела к ВИЧ, полученных стандартными методами (ИФА, ИБ);
— при получении отрицательных результатов исследования антител к вирусу иммунодефицита человека ВИЧ-1/2 и антигена р24 (Human immunodeficiency virus HIV 1/2 + Ag p24) в крови в случае, если беременная женщина относится к группе высокого риска по ВИЧ-инфекции (употребление ПАВ внутривенно, незащищенные половые контакты с ВИЧ-инфицированным партнером в течение последних 6 месяцев) [32-36].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
-
Рекомендуется проведение беременной до- и послетестового консультирования с обязательным разъяснением следующих вопросов [37]:
— пути передачи и способы защиты от заражения ВИЧ-инфекцией;
— методы профилактики передачи ВИЧ-инфекции от матери ребенку;
— интерпретация результатов обследования на ВИЧ-инфекцию;
— риск передачи ВИЧ-инфекции от матери ребенку во время беременности, родов, при грудном вскармливании, при пережевывании пищи для ребенка, при облизывании ниблера;
При выявлении ВИЧ-инфекции:
— необходимость проведения химиопрофилактики передачи ВИЧ-инфекции ребенку;
— возможные исходы беременности у ВИЧ-инфицированных женщин при отсутствии ППМР;
— необходимость последующего диспансерного наблюдения за матерью и ребёнком в территориальном Центре СПИД;
— необходимость информирования полового партнера о результатах обследования на ВИЧ-инфекцию;
— уголовная ответственность за заражение другого лица ВИЧ-инфекцией (полового партнера, ребенка).
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 3).
Комментарии: консультирование проводится для формирования приверженности беременных к добровольному обследованию на ВИЧ-инфекцию. Консультирование проводится в МО, где проводилось тестирование.
Информация о проведении до- и послетестового консультирования беременной вносится в индивидуальную карту беременной и родильницы (форма 111/у) [22-24].
При дотестовом консультировании врач-акушер-гинеколог (по месту наблюдения беременной) устанавливает дату очередного визита беременной для выдачи результатов обследования и послетестового консультирования.
При выявлении положительного результата лабораторного обследования на ВИЧ, врач акушер-гинеколог женской консультации или уполномоченный сотрудник МО:
— не позднее 12 часов с момента получения положительного результата анализа на ВИЧ подает в установленном порядке в территориальный Центр СПИД форму 058/у "Экстренное извещение об инфекционном заболевании, пищевом, остром профессиональном отравлении, необычной реакции на прививку";
— осуществляет активный вызов беременной для консультирования (результаты обследования по телефону не сообщаются). В индивидуальной карте беременной и родильницы (форма 111/у) делается соответствующая запись.
При явке беременной врач акушер-гинеколог или уполномоченный сотрудник МО [22-24]:
— осуществляет послетестовое консультирование при выявлении ВИЧ-инфекции;
— рекомендует обследование половых партнеров ВИЧ-инфицированной беременной на ВИЧ-инфекцию;
— указывает в обменной карте результат обследования на ВИЧ, в том числе дату, номер исследования;
— направляет беременную в территориальный Центр СПИД для постановки на диспансерный учет и назначения химиопрофилактики передачи ВИЧ-инфекции от матери ребенку, оформляет соответствующее направление формы 057/у-04;
— передает информацию о направлении беременной телефонограммой в территориальный Центр СПИД;
— устанавливает срок следующей явки беременной на прием в женскую консультацию;
— в случае неявки беременной женщины в установленный срок организует активное приглашение на прием в женскую консультацию и информирует телефонограммой территориальный Центр СПИД о нарушении режима диспансерного наблюдения по беременности.
Женщине с выявленной ВИЧ-инфекцией необходимо заполнить бланк «Информирования о выявлении ВИЧ-инфекции» (Приложение А3.2).
Направление в территориальный Центр СПИД осуществляется при получении первого положительного результата исследования к ВИЧ-1/2 и антигена р24 (Human immunodeficiency virus HIV 1/2 + Ag p24) в крови, повторных и уточняющих обследований в условиях женской консультации не проводится. При этом женщине разъясняется необходимость проведения комплекса дополнительных лабораторных исследований для уточнения ВИЧ-статуса.
Информация, полученная медицинскими работниками о положительном результате тестирования на ВИЧ-инфекцию беременной, роженицы, родильницы, проведении ППМР, совместном наблюдении женщины со специалистами Центра профилактики и борьбы со СПИД субъекта Российской Федерации, перинатальном контакте по ВИЧ-инфекции у новорожденного, не подлежит разглашению, за исключением случаев, предусмотренных действующим законодательством [23,24].
Дальнейшее наблюдение беременной с установленным диагнозом ВИЧ-инфекции осуществляется совместно врачом-инфекционистом Центра профилактики и борьбы со СПИД субъекта Российской Федерации и врачом-акушером- гинекологом женской консультации по месту жительства. При невозможности направления (наблюдения) беременной женщины в Центр профилактики и борьбы со СПИД субъекта Российской Федерации наблюдение осуществляет врач-акушер-гинеколог по месту жительства при методическом и консультативном сопровождении врача-инфекциониста Центра профилактики и борьбы со СПИД [23,24].
-
Рекомендуется обследование на ВИЧ половых партнеров ВИЧ- инфицированной беременной с представлением результатов в женскую консультацию. Обследование партнеров проводится при постановке беременной на диспансерный учет, или в любое время до родов [27].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
Комментарии: при получении положительного результата исследования партнера, необходимо организовать его направление в территориальный центр профилактики и борьбы со СПИДом, одновременно, в территориальный центр профилактики и борьбы со СПИДом подается форма 058/у «Экстренное извещение об инфекционном заболевании, пищевом, остром профессиональном отравлении, необычной реакции на прививку» (с пометкой - партнер беременной), не позднее 12 ч. от момента выявления [22-24].
3.2. Диагностика ВИЧ-инфекции в родильном отделении
-
Рекомендовано беременной в родильном отделении исследование суммарных антител к вирусу иммунодефицита человека ВИЧ-1/2 и антигена р24 (Human immunodeficiency virus HIV 1/2 + Agp 24) в крови для диагностики ВИЧ-инфекции, при:
— отсутствии обменной карты;
— отсутствии в обменной карте результатов обследования на ВИЧ -инфекцию;
— отсутствии в обменной карте печати медицинского учреждения;
— предъявлении обменной карты неустановленного образца;
— неразборчивом заполнении в обменной карте результатов обследования на ВИЧ - инфекцию;
— отсутствии в обменной карте результатов обследования на ВИЧ -инфекцию в третьем триместре беременности;
— при отрицательном результате обследования на ВИЧ -инфекцию: отсутствие информации о дате проведения и номере исследования;
— при отрицательном результате обследования на ВИЧ - наличие данных эпидемиологического анамнеза: употребление ПАВ женщиной; незащищенные половые контакты с партнером - потребителем парентеральных ПАВ; незащищенные половые контакты с ВИЧ-инфицированным партнером [25,26].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 1).
Комментарии: в наиболее пораженных субъектах (пораженность более 1%) обследование беременных с применением комбинированных тест-систем с одновременным выявлением суммарных антител ВИЧ-1,2 и антигена р24 ВИЧ-1 экспресс-методом в родильном отделении можно назначать в 100% случаев независимо от результатов исследования антител классов М, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1/2 и антигена р24 (Human immunodeficiency virus HIV 1/2 + Ag p24) в крови в ходе диспансерного наблюдения [38-40].
-
Рекомендовано проведение у беременной в родильном отделении экспресс-тестирования на ВИЧ-инфекцию при получении информированного добровольного согласия женщины, для проведения химиопрофилактики ППМР в родах. Врач-акушер-гинеколог разъясняет необходимость тестирования на ВИЧ. При отказе от обследования соответствующая информация отражается в медицинской документации [23,24,41,42].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: обследование на ВИЧ с использованием диагностических экспресс-тест систем проводится в лаборатории или приемном отделении родильного дома медицинскими работниками, прошедшими специальную подготовку в строгом соответствии с инструкцией, прилагаемой к экспресс-тесту [23,24,41,42]. Желательно проведение экспресс-тестирования на ВИЧ до рождения ребёнка для проведения химиопрофилактики ППМР в родах.
-
Рекомендовано женщинам, не прошедшим тестирование на ВИЧ до или во время родов, провести исследование в послеродовом периоде [28].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 1).
-
Рекомендовано при подозрении на острую ВИЧ-инфекцию у женщины дополнительно проводится количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР [43].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
-
Рекомендовано родильнице и ее новорожденному ребенку продлить период пребывания в родильном доме при положительном результате экспресс-тестирования на ВИЧ до получения результатов обследования на ВИЧ-инфекцию [18,19,22-24].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 3).
Комментарии: при получении положительного результата обследования на ВИЧ-инфекцию экспресс-методом, для проведения верификационного исследования, ту же порцию крови необходимо направить в скрининговую лабораторию Центра СПИД. Лабораторное отделение Центра СПИД проводит верификационное исследование в максимально короткий срок (не более 24 часов с момента поступления образца).
При получении результата исследования информация немедленно передается в акушерский стационар, направивший образец биоматериала [22-24,41,42].
-
Рекомендуется сопровождение тестирования роженицы на ВИЧ в акушерском стационаре с дотестовым и послетестовым консультированием, включающим информацию о значении тестирования, методах ППМР (применение антиретровирусных препаратов (по АТХ-классификации: противовирусные препараты системного действия), способе родоразрешения, особенностях вскармливания новорожденного (после рождения ребенок не прикладывается к груди и не вскармливается материнским молоком, а переводится на искусственное вскармливание)) [37].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 3).
Комментарий: в целях диагностики ВИЧ инфекции необходимо использовать комбинированные тест-системы с одновременным выявлением антител ВИЧ-1,2 и антигена р24 ВИЧ -1. Для минимизации ложноположительных и ложноотрицательных результатов тестирования, необходимо использовать тест-системы с наилучшими характеристиками аналитической и диагностической чувствительности и специфичности по выявлению антител ВИЧ-1,2 и антигена р24 ВИЧ-1 [221-224].
-
Рекомендуется исследование уровня антител классов М, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1/2 и антигена р24 (Human immunodeficiency virus HIV 1/2 + Ag p24) в крови у беременных с неизвестным ВИЧ-статусом с целью сокращения серологического окна. Каждое исследование на ВИЧ с применением простых/быстрых тестов должно сопровождаться обязательным параллельным исследованием той же порции крови на ВИЧ стандартными методами ИФА, ИХЛА, ИБ или направлением пациента на обследование на ВИЧ стандартными методами [25,26].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 1).
-
Рекомендуется родильнице исключить грудное вскармливание, до получения результатов обследования на ВИЧ стандартными методами (ИФА, ИХЛА, ИБ) для исключения передачи ВИЧ-инфекции от матери ребенку [44-46].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
Комментарии: не подавлять лактацию, проводить сцеживание грудного молока [44-46].
3.3. Исследования при установленном диагнозе
-
Рекомендуется беременной до назначения АРТ проведение медицинского осмотра и лабораторных исследований для индивидуального подбора АРВП, включающих:
— исследование CD4+ лимфоцитов [47-51];
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
— количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР [47-51];
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
— оценка потребности в профилактике оппортунистических инфекций [52];
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
— скрининговые лабораторные исследования на вирус гепатита В, вирус гепатита C и туберкулез [53-55] (см. соответствующие клинические рекомендации);
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
— скрининговые лабораторные исследования на ИППП, вызываемые такими возбудителями как таких Treponema pallidum, Chlamydia trachomatis, Trichomonas vaginalis и Neisseria gonorrhea [56,57] (см. соответствующие клинические рекомендации);
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
— общий (клинический) анализ крови, анализ крови биохимический общетерапевтический, общий (клинический) анализ мочи для оценки функции почек и печени [58,59];
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
— выявление аллели 5701 локуса В главного комплекса гистосовместимости человека (HLA B*5701), если планируется использование ABC** [60,61];
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
— результаты предыдущих и текущих молекулярно-генетических исследований плазмы крови на наличие мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) к АРВП [62].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
-
Рекомендуется беременной назначение лабораторных исследований для мониторинга НЯ на фоне приема АРВП [63-65].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 3).
-
Рекомендован беременной анализ крови биохимический общетерапевтический для контроля функции печени до начала АРТ, через 4 недели и 12 недель от начала АРТ, далее 1 раз в 12 недель [63-65].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 3).
-
Рекомендуется исследование уровня глюкозы в крови женщинам на сроке от 24 до 28 недель беременности, получающим АРТ [66].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
-
Рекомендуется исследование уровня глюкозы в крови на ранних сроках беременности для женщин, получающим схемы на основе ИП [66].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
-
Рекомендуется контролировать уровень РНК ВИЧ в плазме крови беременных с ВИЧ-инфекцией:
— во время первого дородового визита [47-51];
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
— через 4 недели после начала (или изменения) режима АРТ [47,67];
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
— 1 раз в 4 недели до снижения уровня РНК ВИЧ ниже порога чувствительности теста [47,67];
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
— затем не реже одного раза в 12 недель во время беременности [47].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
-
Рекомендуется для оценки иммунного статуса беременной исследование СD4+-лимфоцитов, ИРИ по соотношению CD4/CD8:
— при первичном обследовании ВИЧ-инфицированной беременной [47-51];
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
— при проведении АРТ: через 4 и 12 недель от начала лечения, далее - 1 раз в 12 недель [47].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
-
Рекомендуется беременным с РНК ВИЧ в плазме крови выше порогового значения для стандартного тестирования устойчивости, проведение молекулярно-генетического исследования плазмы крови для определения наличия мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1):
— перед началом АРТ у ранее не получавших АРВП;
— перед началом АРТ у ранее получавших АРТ;
— перед изменением схем АРТ у женщин с низкой эффективностью АРТ во время беременности [69].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
-
Рекомендовано беременным при назначении АРТ проводить до начала АРТ, через 4 и 12 недель от начала АРТ, далее 1 раз в 12 недель мониторинг побочных эффектов лечения и проявлений различных осложнений, включающий:
— общий (клинический) анализ крови;
— общий (клинический) анализ мочи [3,4,69-71].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
-
Рекомендовано у женщин во время беременности при снижении CD4 ниже 200 кл/мкл. проведение дополнительных лабораторных исследований на диагностику цитомегаловирусной инфекции (определение антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови, молекулярно-биологическое исследование крови на цитомегаловирус (Cytomegalovirus)), диагностика токсоплазмоза (определение антител класса G (IgG) и M (IgM) к токсоплазме (Toxoplasma gondii) в крови) [225].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
4. Инструментальные диагностические исследования
Постановка диагноза ВИЧ-инфекции не подразумевает специального инструментального обследования.
-
Не рекомендуется проведение амниоцентеза женщинам с определяемой ВН ВИЧ. По клиническим показаниям проведение амниоцентеза ВИЧ- инфицированной беременной возможно только после начала эффективной схемы АРТ при достижении неопределяемой ВН ВИЧ [72-75].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
-
Рекомендовано при постановке на диспансерное наблюдение проведение всем пациенткам:
— регистрация электрокардиограммы для диагностики заболеваний сердечно-сосудистой системы [76,77];
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
— ультразвуковое исследование органов брюшной полости (комплексное) для диагностики заболеваний ЖКТ [78].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
5. Иные диагностические исследования
Постановка диагноза ВИЧ-инфекции не подразумевает иных методов обследования.
-
Рекомендуется беременным при постановке на диспансерное наблюдение до назначения АРТ провести:
— оценку необходимости иммунизации против HAV, HBV, гриппа, пневмококка [79-82];
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
— оценку депрессивности и повышенной тревожности, потребность в поддерживающей терапии (например, консультация врача-психиатра, врача психиатра-нарколога) [83-89].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
-
Рекомендовано всем беременным осмотр врачом акушер-гинекологом 1 раз в 4 недели до снижения ВН ниже уровня определения, затем 1 раз в 3 мес. в месяц (предшествует осмотру врачом-инфекционистом с целью более точного установления срока беременности) [3,5,90,91].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
-
Рекомендовано беременным провести приемы врачей-специалистов с целью оценки состояния и раннего выявления сопутствующих заболеваний [3,5,90,91]:
— прием врача-терапевта однократно при постановке на диспансерное наблюдение, а также при наличии соматической патологии (см. Клинические рекомендации « ВИЧ-инфекция у взрослых»);
— прием врача-офтальмолога, врача-оториноларинголога, врача-невролога, врача стоматолога-терапевта при наличии поражения органов зрения, ЛОР-органов, неврологической симптоматики, патологии полости рта;
— прием врача-фтизиатра однократно при наличии положительных результатов скрининга на туберкулез;
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: пациентке также проводятся консультации иных врачей специалистов при наличии соответствующих симптомов или при установленном диагнозе.
— прием врача-психиатра (психотерапевта, нарколога), медицинского психолога, социального работника при употреблении женщиной ПАВ;
— прием медицинского психолога.
В соответствии с приказом от 17 февраля 2020 года № 69н/95н «Об утверждении Порядка оказания медицинскими организациями услуг по правовой, психологической и медико-социальной помощи женщинам в период беременности» пациенткам (в т.ч. с выявленной ВИЧ-инфекцией) положено назначить однократно консультацию медицинского психолога или психолога, имеющего высшее профессиональное образование по специальностям "медицинская психология", "клиническая психология" или "психолог" (далее - специалист, оказывающий психологическую помощь).
На этапе первичной медико-санитарной помощи врач-акушер-гинеколог взаимодействует со специалистами кабинета медико-социальной помощи женской консультации (специалистом по социальной работе, психологом) в части осуществления мероприятий по предупреждению абортов, проведения консультаций по вопросам социальной защиты женщин, обращающихся по поводу прерывания нежеланной беременности, формирования у женщины сознания необходимости вынашивания беременности и дальнейшей поддержки в период беременности и после.
К основным видам деятельности специалиста, оказывающего психологическую помощь, относится психологическое консультирование, психологическая диагностика, психологическая коррекция и профилактика.
Специалист, оказывающий психологическую помощь, осуществляет:
-
оценку психоэмоционального состояния женщины;
-
формирование атмосферы доверия и взаимодействия;
-
направление женщины к врачу-психиатру (врачу - психотерапевту);
-
профилактику отказов от новорожденных;
-
выявление послеродовой депрессии.
Тактика ведения пациентки, необходимость и количество повторных консультаций определяется в индивидуальном порядке только специалистом, оказывающим психологическую помощь.
При выявлении специалистом, оказывающим психологическую помощь, признаков наличия психопатологии у беременной пациентки с ВИЧ-инфекцией, необходимо назначить консультацию врача-психотерапевта (врача-психиатра) для узкоспециализированной оценки состояния пациентки.
При положительном заключении в отношении психического статуса пациентки, врачом-психотерапевтом (врачом-психиатром) определяется дальнейшая тактика ведения в индивидуальном порядке, включая углубленную диагностику психического статуса, решение вопроса о необходимости медикаментозного лечения, сроках наблюдения и количестве дополнительных консультаций.
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
1. АРТ во время беременности (первый этап профилактики).
Особенности диспансерного наблюдения ВИЧ-инфицированных беременных
Рекомендуемый протокол медицинского наблюдения ВИЧ-инфицированных беременных представлен в Приложении Б8.
Мероприятия по предотвращению отказов ВИЧ-инфицированных женщин от проведения ППМР представлены в Приложении Б12.
Для ВИЧ-инфицированных женщин предусмотрено проведение стандартного антенатального медицинского наблюдения [22-24,92-94].
Врач-инфекционист территориального Центра СПИД назначает АРВП с целью проведения ППМР, проводит медицинское обследование пациентки, включая определение ВН ВИЧ в плазме крови и исследование СD4+лимфоцитов в установленные сроки [106,108-111] (А2).
Коррекцию схемы АРТ в первом триместре беременности осуществляет врач- инфекционист территориального Центра СПИД [10].
-
Рекомендуется проведение пренатального консилиума с привлечением специалиста по акушерству и гинекологии, специалиста по наркологии, специалиста по проблемам диагностики и лечения ВИЧ-инфекции для решения вопроса о возможности пролонгирования беременности в случае, если беременная состоит под диспансерным наблюдением в наркологическом диспансере, или подтверждает употребление ПАВ, или имеются убедительные признаки их употребления беременной [30,31].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарий: при решении пренатального консилиума о пролонгировании беременности либо при отказе беременной от прерывания беременности, мониторинг беременности осуществляется врачом-акушером-гинекологом в женской консультации, врачом-психиатром-наркологом в наркологическом диспансере по месту жительства [22,24,92-94].
-
Рекомендуется назначение химиопрофилактики передачи ВИЧ-инфекции от матери ребёнку всем ВИЧ-инфицированным беременным независимо от уровня ВН ВИЧ и количества СD4+-лимфоцитов, включая ВИЧ-инфицированных беременных с неопределяемой ВН (элитные контроллеры) [95].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
Комментарий: при назначении АРВП с целью проведения ППМР ВИЧ- инфицированная беременная заполняет информированное согласие на проведение ППМР [22-24,92-94,96] (Приложение А3.3).
-
Рекомендуется проведение консультирования при назначении АРТ ВИЧ - инфицированной женщине в период беременности или выявлении беременности у ВИЧ-инфицированной женщины, уже получающей АРТ, с разъяснением значимости АРТ как единственной и необходимой меры, обеспечивающей возможность рождения здорового ребёнка, а также влияния лечения на состояние здоровья матери и будущего ребёнка [37].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 3).
Комментарий: необходимо дать разъяснения по следующим вопросам [22,24,92-94,96]:
— высокий риск прогрессирования ВИЧ-инфекции во время беременности без АРТ;
— необходимость АРТ для предотвращения перинатальной передачи ВИЧ;
— необходимость АРТ для снижения риска передачи ВИЧ половым путем партнерам, не инфицированным ВИЧ;
— необходимость строгого соблюдения режима дозирования АРВП, для эффективности АРТ, снижения риска формирования резистентности, и риска перинатальной передачи ВИЧ;
— возможные НЯ на приём АРВП для женщин, плода и новорожденных, включая лекарственные взаимодействия;
— ограниченные данные о долгосрочных исходах применения некоторых АРВП во время беременности для детей раннего возраста.
Необходимо информировать женщину о высоком риске инфицирования ребенка во время беременности в случае отказа от проведения ППМР, а также порядок ее возможного привлечения к уголовной ответственности в случае рождения ребенка ВИЧ-инфицированным [22,97].
При выборе схемы АРТ для беременной необходимо учитывать [98]:
— возможные тератогенные эффекты и другие краткосрочные и долгосрочные неблагоприятные воздействия на плод или новорожденного, включая преждевременные роды, мутагенность и канцерогенность;
— доступные данные по безопасности и исходам применения препарата при беременности;
— изменения плазменной концентрации АРВП при беременности, а также возможные побочные эффекты для женщины, особенно те, которые могут обостриться во время беременности;
— возможные лекарственные взаимодействия с препаратами сопутствующей терапии;
— результаты тестирования на генотипическую резистентность и анамнез применения АРТ;
— сопутствующие заболевания;
— способность пациента соблюдать режим АРТ, а также удобство применения АРВП.
-
Рекомендуется продолжать схему АРТ во время беременности ВИЧ-инфицированным женщинам, получавшим АРТ до беременности, при условии, что режим хорошо переносится, безопасен и эффективен в подавлении репликации вируса [99-102].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
-
Рекомендуется беременным заменить в схеме АРТ препараты, не рекомендуемые во время беременности [103].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
-
Рекомендовано беременным назначение АРВП, из предшествующих схем АРТ, имеющих вирусологическую эффективность, безопасность применения во время беременности, хорошую переносимость, отсутствие НЯ для беременных, которые ранее получали АРТ, но прервали прием АРВП. Учитывать имеющиеся результаты тестирования на резистентность ВИЧ к АРВП [99];
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
-
Рекомендовано беременным до начала АРТ провести молекулярно-генетическое исследование плазмы крови на наличие мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) при определяемой ВН ВИЧ [62].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
-
Рекомендовано беременным начать АРТ до получения результатов тестирования на резистентность ВИЧ к АРВП. После получение результатов исследования, следует скорректировать схему АРТ [99-102].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
-
Рекомендовано беременным повторить молекулярно генетическое исследование плазмы крови на наличие мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) и оценить другие факторы, включающие приверженность АРТ, сопутствующие заболевания и лекарственные взаимодействия при неэффективности АРТ [62].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
-
Рекомендуется назначать АРТ ВИЧ-инфицированной беременной, как можно раньше, на любом сроке беременности [99-102].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
-
Рекомендовано беременным осуществлять выбор АРВП для ППМР с учетом безопасности их применения и [99] (см. Прил. Б4-Б5).
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
Комментарии: Препараты выбора - см. приложения А3.5 - А3.7.
Категории АРВП и схемы АРТ для использования во время беременности включают:
— Предпочтительные: лекарственные препараты или их комбинации для АРТ беременных, если данные клинических испытаний у взрослых продемонстрировали эффективность и долгосрочность с незначительными НЯ и простотой использования, а данные ПК для беременных доступны для определения дозировки. Кроме того, имеющиеся данные должны указывать на благоприятный баланс риска и пользы для препарата или комбинации препаратов по сравнению с другими вариантами АРВП; оценка рисков и преимуществ должна включать результаты для женщин, плода и новорождённых.
— Альтернативные: лекарственные препараты или их комбинации для АРТ беременных, когда данные применения у взрослых показывают эффективность, а данные применения у беременных ограничены. Некоторые альтернативные АРВП или схемы АРТ могут иметь известные риски токсичности или тератогенности, которые компенсируются другими преимуществами применения у беременных с ВИЧ или ВИЧ-инфицированных женщин, планирующих беременность.
-
Не рекомендуются, за исключением особых обстоятельств: препараты, которые не рекомендуются для первоначальной АРТ женщинам, ранее не получавшим АРТ, из-за ограниченных данных по безопасности и эффективности их применения во время беременности. Однако, при определённых обстоятельствах, возможно применение указанных АРВП во время беременности для женщин, ранее получавших данные АРВП, при их хорошей переносимости и высокой эффективности [99].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
-
Не рекомендуются беременным препараты и их комбинации с низкой вирусологической эффективностью или с риском развития серьезных НЯ для матери или плода [99].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
-
Рекомендуется назначение АРТ беременным, с включением в схему не менее 3-х АРВП: два НИОТ и бустированный ИП (или небустированный ИИ или ННИОТ) [103].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
-
Рекомендуется беременным выбор схемы АРТ с учетом следующих рекомендаций:
— исключить прием EFV** до 8 недель беременности в связи с риском формирования ДНТ плода [104-108];
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
— исключить прием DTG** до 8 недель беременности в связи с риском формирования ДНТ плода [104-108];
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 3).
— при наступлении беременности у ВИЧ-инфицированных женщин, получающих DTG**, необходима консультация по рискам и преимуществам продолжения приема DTG** или перехода на другую схему АРТ [106];
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
— назначать NVP** только при количестве CD4 <250 мкл-1 [108];
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
-
Не рекомендуется беременным [12,96,98,103,106,109-121] (4С):
— NVP** не получавшим АРТ, в связи с высоким риском развития НЯ, необходимости вводного дозирования и низкого барьера к развитию резистентности. Однако, при хорошей переносимости препарата до беременности, возможно, что АРТ с NVP** во время беременности будет безопасным и эффективным [108];
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
— назначать ATV** без бустера - RTV**;
— назначать беременным FPV**, RTV** (как единственный ИП), SQV**;
— назначать схемы АРТ с двумя препаратами или схема АРТ с тремя НИОТ (например, ABC/ZDV/3TC**);
— назначать DTG/ЗТС** и DTG/RPV, так как нет данных о применении во время беременности. Необходима коррекция схемы АРТ при наступлении беременности [69].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
— назначать схемы, содержащие EVG/С, что связано с фармакокинетическими изменениями и низкой эффективностью во 2 и З триместрах беременности. При наступлении беременности следует рассмотреть вопрос о переходе на более эффективный режим, рекомендованный для беременных [110]. Если один из этих режимов будет продолжен, необходимо контролировать ВН каждые 4-8 недель;
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
— назначение TAF**-содержащих схем беременным, ранее не получавшим АРТ. Возможно продолжение лечения TAF**-содержащей схемой во время беременности женщинам, ранее получившим TAF**, при его эффективности и отсутствии НЯ [226,227].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 3).
-
Рекомендуется продолжить приём АРТ по ранее назначенной схеме при наступлении беременности у ВИЧ-инфицированной женщины, постоянно получающей АРТ, при условии ее эффективности и отсутствия противопоказаний для применения данных АРВП у беременных [99] (2А).
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
-
Рекомендуется проведение АРТ в период беременности (первый этап) ВИЧ-инфицированным половым партнерам ВИЧ-серонегативной беременной вне зависимости от наличия у него показаний к началу АРТ на протяжении всей ее беременности и грудного вскармливания ребенка в целях снижения риска заражения беременной и передачи ВИЧ-инфекции от матери к ребенку [122-124] (2А).
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
2. Профилактика ППМР в родах (второй этап профилактики)
Перед началом профилактических мероприятий роженица подписывает информированное согласие установленного образца [22-24,125] (Приложение А3).
При сроке беременности 36-37 недель беременности формулируется полный клинический диагноз и определяется место планового родоразрешения (Приказ МЗ РФ от 20.10.2020 № 1130н).
Для обеспечения ППМР в акушерском стационаре постоянно должен иметься необходимый запас АРВП.
Проведение ППМР у женщины в период родов осуществляет врач-акушер- гинеколог, ведущий роды, в соответствии с рекомендациями по ППМР [124,125].
Необходимо учитывать схему АРТ, назначенную женщине, при лечении послеродового маточного кровотечения для исключения межлекарственных взаимодействий.
-
Рекомендуется проведение ППМР в учреждениях родовспоможения:
— ВИЧ-инфицированным роженицам [126,127];
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
Комментарии:
- роженицам с положительным результатом экспресс-тестирования на ВИЧ- инфекцию;
- при невозможности проведения экспресс-тестирования или своевременного получения результатов стандартного теста на антитела к ВИЧ у роженицы;
- роженицам с отрицательным результатом экспресс-тестирования на ВИЧ - потребителям ПАВ и/или имеющим партнёра -потребителя ПАВ (в течение 12 недель до родов);
- роженицам с отрицательным результатом экспресс-тестирования на ВИЧ, имевшим половые контакты с известным ВИЧ-инфицированным (в течение 12 недель до родов) [125];
-
Рекомендуется после родов продолжить прием ранее назначенной схемы АРТ ВИЧ-инфицированным беременным, получающим APT [147].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
-
Рекомендуется назначение ВИЧ-инфицированным беременным, не получающим APT, поступающим за сутки и более до родов в акушерский стационар [22,215-217].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
-
Рекомендовано роженицам применение ZDV** в форме раствора для внутривенного введения с начала родовой деятельности в дозе 0,002 г (0,2 мл) /кг в течение первого часа родов, далее 0,001 г (0,1 мл) /кг в ч до момента отделения ребенка от матери (пересечения пуповины) во время родов для ППМР [126].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 1).
Комментарии: противопоказанием является резистентность ВИЧ к ZDV** или НЯ на приём ZDV** в анамнезе. В этом случае в родах продолжается подобранная схема лечения без ZDV**.
Схема приготовления раствора и расчет скорости введения определяются в соответствии со справочной таблицей (Приложение А3.9).
-
Рекомендуется при ведении родов у ВИЧ-инфицированных женщин не превышать продолжительность безводного периода более 4 часов [129-131].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 3).
-
Не рекомендуется во время родов у ВИЧ-инфицированной женщины, проведения процедур, повышающих риск инфицирования плода: родовозбуждение, родостимуляция, перинео-(эпизио)томию, наложение акушерских щипцов, вакуум-экстракцию плода. Назначение данных процедур производится по жизненным показаниям [132-136].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
Комментарии: искусственный разрыв плодных оболочек может выполняться по стандартным акушерским показаниям у ВИЧ-инфицированных женщин с неопределяемой ВН ВИЧ, которые получают АРТ [137].
-
Рекомендуется проведение плановой операции кесарева сечения у ВИЧ-инфицированных женщин при следующих условиях [132-136]:
— уровень ВН ВИЧ выше 1 000 копий/мл в последнем анализе перед родами;
— отсутствие результатов определения ВН ВИЧ перед родами;
— отсутствие АРТ во время беременности и/или невозможности проведение АРТ в родах.
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
Комментарии: при невозможности проведения химиопрофилактики в родах кесарево сечение может быть самостоятельной профилактической процедурой, снижающей риск заражения ребенка ВИЧ-инфекцией в период родов, при этом его проводить не рекомендуется при безводном промежутке более 4 часов.
Окончательное решение о способе родоразрешения женщины с ВИЧ-инфекцией принимается врачом-акушером-гинекологом, ведущим роды, в индивидуальном порядке, с учетом состояния матери и плода, сопоставляя в конкретной ситуации пользу от снижения риска заражения ребенка при проведении операции кесарева сечения с вероятностью возникновения послеоперационных осложнений и особенностей течения ВИЧ-инфекции [22,24,128].
-
Рекомендуется оперативное родоразрешение ВИЧ -инфицированным беременным проводить в 38 недель беременности в плановом порядке [132-136].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
Комментарии: при проведении операции кесарева сечения внутривенное введение раствора ZDV назначается за 4 ч до начала оперативного вмешательства в тех же дозах, что и при естественном родоразрешении и прекращается в момент отделения ребенка от матери (пересечения пуповины) [126].
-
Не рекомендуется плановое кесарево сечение, для ППМР у женщин, получающих АРТ с ВН ВИЧ <1000 копий/мл, из-за низкого уровня перинатальной передачи в этой группе [132-136].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
-
Рекомендуется после родов у ВИЧ-инфицированных женщин продолжение и пожизненное назначение АРТ [164-167] (А1). Решение вопроса о коррекции схемы АРТ принимается врачом-инфекционистом Центра СПИД [99].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2).
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
См. клинические рекомендации «ВИЧ-инфекция у взрослых».
Госпитализация
Организация оказания медицинской помощи
Организация оказания медицинской помощи по диагнозу ВИЧ-инфекция - см. клинические рекомендации «ВИЧ-инфекция у взрослых».
Тактика родов, сроки госпитализации в акушерский стационар у беременных с ВИЧ-инфекцией по результатам исследования крови количественным методом ПЦР РНК ВИЧ-1 у женщины на сроке беременности 34-36 недель определены в главе 3.2.
Информация
Источники и литература
-
Клинические рекомендации Российского общества акушеров-гинекологов
- 1. Gallo R.C. и др. Frequent detection and isolation of cytopathic retroviruses (HTLV-III) from patients with AIDS and at risk for AIDS // Science. 1984. № 4648 (224). С. 500-503. 2. Popovic M. [и др.]. Detection, isolation, and continuous production of cytopathic retroviruses (HTLV-III) from patients with AIDS and pre-AIDS // Science. 1984. № 4648 (224). C. 497-500. 3. Бартлетт Дж. [и др.]. Клинические аспекты ВИЧ-инфекции // ГРАНАТ изд. - 2013. 696 с. 4. Либман Г., Макадон Х. Дж. ВИЧ-инфекция // ГЭОТАР-Медиа, 2013. 560 c. 5. Покровский В.В. ВИЧ-инфекция и СПИД. Национальное руководство // ГЭОТАР-Мед-е изд., 2020. 696 с. 6. Беляков Н.А. [и др.]. Эпидемиология ВИЧ инфекции. Место мониторинга, научных и дозорных наблюдений, моделирования и прогнозирования обстановки // ВИЧ-инфекция и иммуносупрессии, Том 11, № 2. 2019. 7. Нечаева О.Б. Эпидемическая ситуация по ВИЧ-инфекции в России на период начала действия Государственной стратегии противодействия распространению ВИЧ-инфекции // Туберкулез и болезни лёгких. 2021. Т. 99. № С. 15-24. 8. Прохорова О.Г., Ножкина Н.В. Развитие профилактики и медико - социальной помощи ВИЧ-инфицированным женщинам и детям в Свердловской области // Вестник РГМУ. 2013. № 5-6. C. 106-110. 9. Мазус А.И. [и др.]. Современные рекомендации по диагностике и лечению ВИЧ-инфекции у детей и подростков // Педиатрия. 2019. (№1). C. 1 5 1-158. 10. Володин Н.Н. [и др.]. Рекомендации по проведению профилактики передачи ВИЧ-инфекции от матери ребёнку / Володин Н.Н., Адамян Л.В., Курцер М.А., Мазус А.И., Кузьмин В.Н. [и др.]., Российская ассоциация специалистов перинатальной медицины, 2015. 11. Flynn M Patricia и др. Prevention of mother-to-child HIV transmission in resource-limited settings // UpToDate. 2016. Т. Topic 3799. № Version 13.0. 12. Cooper E. R. [и др.]. Combination antiretroviral strategies for the treatment of pregnant HIV-1-infected women and prevention of perinatal HIV-1 transmission // Journal of Acquired Immune Deficiency Syndromes. 2002. № 5 (29). 13. WHO Global guidance on criteria and processes for validation: elimination of mother-to-child transmission of Hiv and Syphilis monitoring / WHO, 2021. 14. Kassa G.M. Mother-to-child transmission of HIV infection and its associated factors in Ethiopia: a systematic review and meta-analysis // BMC Infect Dis. 2018. (18). C. 216. 15. Самарина А.В., Беляков Н.А. Реализация подходов по снижению перинатальной передачи ВИЧ // ВИЧ-инфекция и иммуносупрессии. 2014. Т. 6 № 2. C. 7-24. 16. Клиническая классификация ВИЧ-инфекции. Приложение к Инструкции по заполнению годовой формы государственного федерального статистического наблюдения № 61 "Сведения о контингентах больных ВИЧ-инфекцией", утвержденной Приказом Минздравсоцразвития России от 17.03.2006 г. № 166. 17. Havens P.L. [и др.]. HIV Testing and Prophylaxis to Prevent Mother-to-Child Transmission in the United States // Pediatrics. 2008. № 5 (122). C. 1127-1134. 18. Branson B.M. [и др.]. Revised recommendations for HIV testing of adults, adolescents, and pregnant women in health-care settings. // MMWR. Recommendations and reports: Morbidity and mortality weekly report. Recommendations and reports / Centers for Disease Control. 2006. № RR-14 (55). 19. Chou R. [и др.]. Screening for HIV in pregnant women: Systematic review to update the 2005 U.S. Preventive Services Task Force recommendation // Annals of Internal Medicine. 2012. № 10(157). 20. Moyer V. A. Screening for HIV: U.S. Preventive Services Task Force recommendation statement // Annals of Internal Medicine. 2013. № 1 (159). 21. ACOG Committee Opinion Number 752 Prenatal and Perinatal Human Immunodeficiency Virus Testing // Obstetrics and Gynecology. 2018. № 3 (132). С. e138-e142. 22. Приказ департамента здравоохранения города Москвы от 17.08.2018 г. № 563 «О дальнейшем совершенствовании мероприятий по профилактике перинатальной передачи ВИЧ-инфекции в медицинских организациях государственной системы здравоохранения города Москвы». 23. Постановление Главного государственного санитарного врача РФ от 28.01.2021 № 4 "Об утверждении санитарных правил и норм СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней". 24. Приказ Минздрава России от 20.10.2020 № 1130н "Об утверждении Порядка оказания медицинской помощи по профилю "акушерство и гинекология". 25. Smallwood M. [и др.]. Evaluation of a rapid point of care test for detecting acute and established HIV infection, and examining the role of study quality on diagnostic accuracy: A Bayesian meta-analysis // PLoS ONE. 2016. № 2 (11). 26. Yoo S.J. [и др.]. Meta-analysis for the pooled sensitivity and specificity of antihuman immunodeficiency virus Ab rapid tests // Korean Journal of Laboratory Medicine. 2009. № 4 (29). С. 345-352. 27. Rosenberg N.E. [и др.]. Recruiting male partners for couple HIV testing and counseling in Malawi's option B+ programme: An unblinded randomised controlled trial // The Lancet HIV. 2015. № 11 (2). C. e483-e491. 28. Drake A.L. [и др.]. Incident HIV during Pregnancy and Postpartum and Risk of Mother-to-Child HIV Transmission: A Systematic Review and Meta-Analysis // PLoS Medicine. 2014. № 2 (11). 29. Liao C. [и др.]. Missed opportunities for repeat HIV testing in pregnancy: Implications for elimination of mother-to-child transmission in the United States // AIDS Patient Care and STDs. 2017. № 1 (31). C. 20-26. 30. Thorne C., Newell M.-L. Injecting drug use in pregnant HIV-infected women in Europe. // Medycyna wieku rozwojowego. 2006. № 4 (10). C. 1005-16. 31. Shankaran S. [и др.]. Impact of maternal substance use during pregnancy on childhood outcome // Seminars in Fetal and Neonatal Medicine. 2007. № 2 (12). С. 143150. 32. Yoo S.J. [и др.]. Meta-analysis for the pooled sensitivity and specificity of antihuman immunodeficiency virus Ab rapid tests // Korean Journal of Laboratory Medicine. 2009. № 4 (29). C. 345-352. 33. Tan W.S. [и др.]. Sensitivity of HIV rapid tests compared with fourth-generation enzyme immunoassays or HIV RNA tests // AIDS. 2016. № 12 (30). C. 1951-1960. 34. Sarinoglu R.C. [и др.]. Evaluation of enzyme immunoassay (EIA), immunoblot and HIV RNA polymerase chain reaction test results in the diagnosis of human immunodeficiency virus (HIV) infection // Mikrobiyoloji Bulteni. 2019. № 4 (53). C. 401 -407. 35. Wu S. [и др.]. Prevalence of HIV Indeterminate Western Blot Tests and Followup of HIV Antibody Sero-Conversion in Southeastern China // Virologica Sinica. 2019. № 4 (34). C. 358-366. 36. Zaaijer H.L. [и др.]. Validation of a new immunoblot assay (LiaTek HIV III) for confirmation of human immunodeficiency virus infection // Transfusion. 1998. № 8 (38). C. 776-781. 37. Hodgson I. [и др.]. A systematic review of individual and contextual factors affecting ART initiation, adherence, and retention for HIV-infected pregnant and postpartum women // PLoS ONE. 2014. № 11 (9). 38. Yee L.M. [и др.]. Sustainability of Statewide Rapid HIV Testing in Labor and Delivery // AIDS and Behavior. 2018. № 2 (22). C. 538-544. 39. Scott R.K., Crochet S., Huang C.C. Universal Rapid Human Immunodeficiency Virus Screening at Delivery: A Cost-Effectiveness Analysis // Infectious Diseases in Obstetrics and Gynecology. 2018. (2018). 40. Branson B.M. [и др.]. Laboratory testing for the diagnosis of HIV infection : updated recommendations - Guidelines and Recommendations // Centers for disease control and prevention. 2014. 41. Donovan M., Palumbo P. Diagnosis of HIV: Challenges and strategies for HIV prevention and detection among pregnant women and their infants // Clinics in Perinatology. 2010. № 4 (37). 42. Read J.S. [и др.]. Diagnosis of HIV-1 infection in children younger than 18 months in the United States // Pediatrics. 2007. № 6 (120). С. е 1547- е 1562. 43. Burgard M. [и др.]. Performance of HIV-1 DNA or HIV-1 RNA tests for early diagnosis of perinatal HIV-1 infection during anti-retroviral prophylaxis // Journal of Pediatrics. 2012. № 1 (160). С. 60-66. 44. Read J.S. Late postnatal transmission of HIV-1 in breast-fed children: An individual patient data meta-analysis // Journal of Infectious Diseases. 2004. № 12 (189). С. 2154-2166. 45. White A.B. [и др.]. Antiretroviral interventions for preventing breast milk transmission of HIV // Cochrane Database of Systematic Reviews. 2014. № 10. 46. Graybill L.A. [и др.]. Incident HIV among pregnant and breast-feeding women in sub-Saharan Africa: A systematic review and meta-analysis // AIDS. 2020. № 5 (34). С. 761-776. 47. Babiker A. [и др.]. Human immunodeficiency virus type 1 RNA level and CD4 count as prognostic markers and surrogate end points: A meta-analysis // AIDS Research and Human Retroviruses. 2000. № 12 (16). C. 1123-133. 48. Fox M., McCarthy O., Over M. A Novel Approach to Accounting for Loss to Follow-Up when Estimating the Relationship between CD4 Count at ART Initiation and Mortality // PLoS ONE. 2013. № 7 (8). 49. Baillargeon J., Grady J., Borucki M. J. Immunological predictors of HIV-related survival // International Journal of STD and AIDS. 1999. № 7 (10). C. 467-470. 50. Kebede M., Zegeye D.T., Zeleke B.M. Predicting CD4 count changes among patients on antiretroviral treatment: Application of data mining techniques // Computer Methods and Programs in Biomedicine. 2017. (152). C. 149-157.
Информация
Список сокращений
АЛТ - аланинаминотрансфераза
АРВП - антиретровирусные препараты (по АТХ-классификации: противовирусные препараты системного действия)
АРТ - антиретровирусная терапия
АСТ - аспартатаминотрансфераза
ВИЧ - вирус иммунодефицита человека
ВМИ - внутриматочная инсеминация
ВН - вирусная нагрузка - количество копий РНК ВИЧ в 1 мл биосубстрата
ВОЗ - Всемирная организация здравоохранения
ВРТ - вспомогательные репродуктивные технологии
ДКП - доконтактная профилактика
ДН - диспансерное наблюдение
ДНК - дезоксирибонуклеиновая кислота
ДНТ - дефект нервной трубки
ЖКТ - желудочно-кишечный тракт
ИБ - иммунноблотинг
ИИ - ингибиторы интегразы ВИЧ (по АТХ-классификации: ингибиторы интегразы)
ИКСИ - интрацитоплазматическая инъекция сперматозоида
ИМТ - индекс массы тела
ИП - ингибиторы протеазы ВИЧ (по АТХ-классификации: ингибиторы протеаз)
ИППП - инфекции, передающиеся половым путем
ИРИ - иммунорегуляторный индекс
ИС - иммунный статус
ИС - ингибиторы слияния (фузии) ВИЧ (по АТХ-классификации: прочие противовирусные препараты)
ИФА - иммуноферментный анализ
ИХА - иммунохроматографический анализ
ИХЛА - иммунохемилюминесцентный анализ
КТ - компьютерная томография
ЛЖВ - люди, живущие с ВИЧ-инфекцией
МКБ-10 - Международная классификация болезней и проблем, связанных со здоровьем, 10-го пересмотра
МО - медицинская организация
МРТ - магнитно-резонансная томография
МСМ - мужчины, практикующие секс с мужчинами
НИОТ - нуклеоз(т)идные ингибиторы обратной транскриптазы ВИЧ (по АТХ- классификации: нуклеозиды и нуклеотиды - ингибиторы обратной транскриптазы)
ННИОТ - ненуклеозидные ингибиторы обратной транскриптазы ВИЧ (по АТХ- классификации: ненуклеозидные ингибиторы обратной транскриптазы)
НЯ - нежелательные явления
ОАК - общий (клинический) анализ крови
ОАМ - общий (клинический) анализ мочи
ПАВ - психоактивные вещества
ПК - концентрация в плазме крови
ПМП - паллиативная медицинская помощь
ППМР - профилактика передачи от матери ребенку
ПЦР - полимеразная цепная реакция
РК - Российская классификация ВИЧ-инфекции
РНК - рибонуклеиновая кислота
СПИД - синдром приобретенного иммунодефицита
УЗИ - ультразвуковое исследование
ФК - фармакокинетика
ФКД - фиксированная комбинация доз
ХВГВ - хронический вирусный гепатит В
ХВГС - хронический вирусный гепатит С
ХП - химиопрофилактика
ЭКО - экстракорпоральное оплодотворение
3TC** - Ламивудин**
ABC** - Абакавир**
ABC/3TC** - Абакавир + Ламивудин** (ФКД)
ABC/ZDV/3TC** - Абакавир + Зидовудин + Ламивудин ** (ФКД)
ATV** - Атазанавир**
BIC/FTC/TAF** - Биктегравир + Тенофовира алафенамид + Эмтрицитабин**
CD - кластер дифференцировки (англ. Cluster of Differentiation)
CD4 - CD4+ лимфоциты (Т-лимфоциты с рецептором CD4+)
CD8 - CD8+ лимфоциты (Т-лимфоциты с рецептором CD8+)
COBI** (С) - Кобицистат + Тенофовира алафенамид + Элвитегравир + Эмтрицитабин** (ФКД)
COBI/TAF/EVG/FTC** - Кобицистат + Тенофовира алафенамид + Элвитегравир + Эмтрицитабин** (ФКД)
DOR** - Доравирин**
DOR/3TC/TDF** - Доравирин + Ламивудин + Тенофовир** (ФКД)
DRV** - Дарунавир**
DTG** - Долутегравир**
DTG/3TC - Долутегравир + Ламивудин
EFV** - Эфавиренз**
ESV** - Элсульфавирин**
ETR** - Этравирин**
EVG/COBI/FTC/TDF** - Элвитегравир + Кобицистат + Эмтрицитабин + Тенофовир**
PhAZT** - Фосфазид**
FDA - Управление по контролю качества пищевых продуктов и лекарственных препаратов США
FPV** - Фосампренавир**
FTC** - Эмтрицитабин **
HAV - вирусный гепатит А
HBV - вирусный гепатит В
HLA - человеческий лейкоцитарный антиген
HLA-B*5701 - аллель 5701 локуса В главного комплекса гистосовместимости человека
IGRA - interferon gamma release assay, анализ выявления гамма-интерферона
LPV/r** - Лопинавир + Ритонавир** (ФКД)
MVC** - Маравирок**
NVP** - Невирапин**
RAL** - Ралтегравир**
RPV - Рилпивирин
RPV/TDF/FTC** - Рилпивирин + Тенофовир + Эмтрицитабин** (ФКД)
RTV, r** - Ритонавир**
SQV** - Саквинавир**
TAF** - Тенофовира алафенамид**
TDF** - Тенофовир**
TDF/FTC/EFV - Тенофовир + Эмтрицитабин + Эфавиренз
ZDV** - Зидовудин**
2КР - двухкомпонентный режим
Термины и определения
Антиретровирусная терапия (АРТ) - этиотропная терапия инфекции, вызванной вирусом иммунодефицита человека (ВИЧ-инфекции), позволяющая добиться контролируемого течения заболевания, назначаемая пожизненно и основанная на одновременном использовании нескольких антиретровирусных препаратов (по АТХ-классификации: противовирусные препараты системного действия), действующих на разные этапы жизненного цикла ВИЧ.
Бесплодие - заболевание, характеризующееся невозможностью достичь клинической беременности после 12 месяцев регулярной половой жизни без контрацепции вследствие нарушения способности субъекта к репродукции, либо индивидуальной, либо совместно с его/ее партнером.
Вспомогательные репродуктивные технологии - методы лечения бесплодия, при применении которых отдельные или все этапы зачатия и раннего развития эмбрионов осуществляются вне материнского организма (в том числе с использованием донорских и (или) криоконсервированных половых клеток, тканей репродуктивных органов и эмбрионов, а также суррогатного материнства).
Вирус иммунодефицита человека (ВИЧ) - возбудитель ВИЧ-инфекции из семейства ретровирусов, вызывающий постепенное развитие иммунодефицита.
Вирусная нагрузка (ВН) - количество вируса в материале пациента (плазма, ликвор и т.д.), определяемое с помощью полимеразной цепной реакции (ПЦР) и выраженное в количестве копий рибонуклеиновой кислоты (РНК) ВИЧ в 1 мл плазмы.
Вирусная супрессия - цель АРТ, заключающаяся в снижении и поддержании вирусной нагрузки ниже уровня, выявляемого имеющимися тестами.
«Всплеск (подскок) виремии» (blip) - однократный подъем вирусной нагрузки до уровня менее 200 копий/мл после неопределяемой.
Генотипирование - метод, основанный на непрямой оценке лекарственной устойчивости путем сравнения консенсусной последовательности РНК ВИЧ с последовательностью РНК ВИЧ, полученной от пациента.
Детский возраст - с рождения до 17 лет 11 месяцев 29 дней.
Иммунный статус (ИС) - оценка состояния иммунной системы. При ВИЧ- инфекции исследуют процентное содержание и абсолютное количество иммунных клеток регуляторного звена (хелперные Т-лимфоциты и супрессорные Т- лимфоциты) и эффекторного звена (цитотоксические Т-лимфоциты), наиболее важных в патогенезе заболевания. Используется для мониторинга естественного течения ВИЧ-инфекции и оценки эффективности АРТ.
Иммуноблоттинг (ИБ) - лабораторный иммунологический метод определения антител в крови к различным белкам ВИЧ. Вследствие высокой специфичности используется как подтверждающий метод после получения положительного результата на этапе скрининга.
Иммунорегуляторный индекс (ИРИ) - соотношение абсолютного количества CD4 и CD8. У здоровых лиц значение ИРИ равно или выше 1. При ВИЧ-инфекции происходит инверсия показателя за счет снижения доли CD4; прогрессирование поражения иммунной системы сопровождается снижением ИРИ. Используется в прогностических целях.
Иммуноферментный анализ (ИФА) и иммунохемилюминесцентный анализ (ИХЛА) - лабораторные иммунологические методы качественного определения в крови суммарных антител к ВИЧ. Вследствие высокой чувствительности используются в качестве скрининговых методов.
Иммунохроматографический анализ (ИХА) - лабораторный иммунологический метод анализа, основанный на принципе тонкослойной хроматографии и включающий реакцию между антигеном и соответствующем ему антителом в биологических материалах. Проводится с помощью специальных тест-полосок, панелей или тест-кассет.
Индекс массы тела (ИМТ) - величина, позволяющая оценить степень соответствия массы человека и его роста и, тем самым, косвенно оценить, является ли масса недостаточной, нормальной или избыточной. Важен при определении адекватных доз фармакологических препаратов. Индекс массы тела рассчитывается по формуле: ИМТ (кг/м2) = m h2, где m - масса тела в кг, h - рост в м.
Интрацитоплазматическая инъекция сперматозоидов (ИКСИ) - процедура, во время которой один сперматозоид вводят в цитоплазму ооцита.
Искусственная инсеминация (внутриматочная инсеминация) - процедура, во время которой обработанная в лабораторных условиях сперма вводится в полость матки с целью достижения беременности.
Криоконсервация - процесс медленного замораживания или витрификации для сохранения биологического материала (например, гамет, зигот, эмбрионов на стадии дробления, бластоцист или ткани гонад) при экстремально низких температурах.
Люди, живущие с ВИЧ-инфекцией (ЛЖВ) - собирательное понятие, определяющее принадлежность человека (людей) к группе инфицированных ВИЧ.
Младенческий возраст - от 0 до 12 месяцев жизни.
Неопределяемый уровень ВН - уровень вирусной нагрузки ВИЧ ниже порога определения тест-системы или менее 50 копий/мл (рекомендуется использовать тест-системы с порогом чувствительности 50 копий / мл).
«Низкоуровневая виремия» - повторяющиеся значения вирусной нагрузки в интервале 50-1000 копий / мл (low level viremia). «Низкоуровневая виремия» является предиктором развития лекарственной устойчивости ВИЧ.
Овариальная стимуляция (стимуляция яичников) - фармакологическая терапия с целью индуцировать развитие фолликулов в яичниках. Ее можно использовать для двух целей: 1) для запланированного полового контакта или инсеминации; 2) при вспомогательных репродуктивных технологиях, для получения нескольких ооцитов при пункции фолликулов.
Определяемый уровень ВН ВИЧ - уровень вирусной нагрузки ВИЧ выше порога определения тест-системы (рекомендуется использовать тест-системы с порогом чувствительности 50 копий/мл).
Паллиативная медицинская помощь (ПМП) - медицинская помощь, направленная на улучшение качества жизни граждан, страдающих неизлечимыми прогрессирующими заболеваниями и состояниями, которые, как правило, приводят к преждевременной смерти, а также заболеваниями в стадии, когда исчерпаны возможности радикального лечения.
Перенос эмбриона - введение в полость матки эмбриона на любой стадии развития эмбриона с 1 по 7 день после экстракорпорального оплодотворения или ИКСИ.
Перинатальный контакт по ВИЧ-инфекции - контакт ребенка с ВИЧ- инфицированной матерью на протяжении периода гестации, родов и грудного вскармливания.
Профилактика перинатальной передачи ВИЧ-инфекции - комплекс мероприятий по предупреждению ВИЧ-инфицирования ребенка в период беременности, родов, послеродовом периоде. Включает медикаментозные методы (химиопрофилактика) и немедикаментозные (оперативное родоразрешение).
Полимеразная цепная реакция (ПЦР) - лабораторный метод качественного и количественного определения генетического материала ВИЧ, основанный на использовании уникальности нуклеотидных последовательностей участков РНК/ДНК. Обладает высокой чувствительностью и специфичностью. Качественное определение дезоксирибонуклеиновой кислоты (ДНК) ВИЧ в лимфоцитах крови используется у взрослых для раннего выявления ВИЧ- инфекции в установленном/предполагаемом периоде «серологического окна» (в первые недели после инфицирования, когда количество вырабатываемых специфических антител к ВИЧ в организме заразившегося человека недостаточно для выявления). Количественное определение РНК ВИЧ используется при выборе препаратов в составе схем АРТ, для оценки эффективности АРТ и с прогностической целью (см. «Вирусная нагрузка»).
Редукция эмбриона/плода - вмешательство с целью уменьшения числа плодных яиц или эмбрионов/плодов при многоплодной беременности.
Селективный перенос одного эмбриона - перенос одного (единственного) эмбриона, выбранного из когорты имеющихся эмбрионов.
Серодискордантные пары - пары, поддерживающие продолжительные сексуальные взаимоотношения, в которых только один из партнеров имеет ВИЧ- инфекцию.
Суррогатная мать - женщина, которая вынашивает плод после переноса донорского для нее эмбриона.
CD4 - СD4+-Т-лимфоциты - антигенраспознающие Т-лимфоциты-хелперы, обязательный компонент индукции гуморального ответа на Т-зависимые антигены.
CD8 - CD8+-Т-лимфоциты - Т-цитотоксические лимфоциты (Т-киллеры) лизируют клетки-мишени, несущие чужеродные антигены или изменённые аутоантигены.
Экстракорпоральное оплодотворение - последовательность манипуляций, включающая экстракорпоральное оплодотворение ооцитов. Оно включает традиционную инсеминацию in vitro и интрацитоплазматическую инъекцию сперматозоидов.
Элитный контроллер - лицо, относящееся к небольшой группе ВИЧ- инфицированных пациентов, которым удаётся сдерживать вирусную репликацию без антиретровирусной терапии, в связи с чем, несмотря на достоверную серологическую инфицированность, вирусная РНК в плазме крови методом ПЦР не обнаруживается Распространённость элитных контроллеров, обладающих способностью к длительному подавлению репликации вируса, составляет менее 1%, временный контроль наблюдается несколько чаще.
Критерии оценки качества медицинской помощи
|
№ п/п |
Критерий качества |
Оценка выполнения (Да/Нет) |
|---|---|---|
|
1. |
Выполнено подтверждающее исследование с раздельным определением антител к индивидуальным белкам ВИЧ-1 и ВИЧ-2 или определение РНК ВИЧ-1 в случае положительного результата определения суммарных антител к вирусу иммунодефицита человека 1, 2 типов и антигена p24 ВИЧ |
Да/Нет |
|
2. |
Выполнено исследование уровня антител классов М, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1/2 и антигена р24 (Human immunodeficiency virus HIV 1/2 + Agp24) в крови у беременной в родильном отделении при наличии показаний |
Да/Нет |
|
3. |
Выполнен прием (осмотр, консультация) врача-инфекциониста первичный |
Да/Нет |
|
3. |
Выполнено установление клинического диагноза в течение 10 дней с момента обращения |
Да/Нет |
|
4. |
Выполнено количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР во время первого дородового визита |
Да/Нет |
|
5. |
Выполнено количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР через 4 недели от начала или смены антиретровирусной терапии и на 36-й неделе беременности у пациентки посещавшей центр СПИД в указанные сроки беременности |
Да/Нет |
|
6. |
Выполнено исследование CD4+ лимфоцитов при установлении диагноза у пациентки, посещавшей центр СПИД при первичном обследовании |
Да/Нет |
|
7. |
Выполнено исследование CD4+ лимфоцитов через 4 недели от начала или смены антиретровирусной терапии у пациентки посещавшей центр СПИД в указанные сроки беременности |
Да/Нет |
|
8. |
Выполнен прием (осмотр, консультация) врача-акушера-гинеколога первичный |
Да/Нет |
|
9. |
Выполнено назначение лекарственных антиретровирусных препаратов при заболевании, вызываемом вирусом иммунодефицита человека (ВИЧ-инфекции) не позднее 13-й недели беременности (при своевременной постановке на диспансерный учет) |
Да/Нет |
|
10. |
Выполнено определение антител классов M, G (IgM, IgG) к вирусу гепатита С (Hepatitis C virus) в крови, антигена вируса гепатита В (НBsAg Hepatitis B virus) в крови (при их отсутствии ранее (в крови) |
Да/Нет |
|
11. |
Выполнено молекулярно-генетическое исследование плазмы крови на наличие мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) (при доказанной вирусологической неэффективности лечения и достаточном для проведения резистентности уровне вирусной нагрузки) |
Да/Нет |
|
12. |
Выполнено внесение информации об отказе пациентки от химиопрофилактики передачи ВИЧ от матери к ребенку в медицинскую документацию |
Да/Нет |
|
13. |
Выполнено внесение информации о согласии пациента с проведением химиопрофилактики передачи ВИЧ от матери к ребенку в медицинскую документацию |
Да/Нет |
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Адамян Лейла Вагоевна - академик РАН, профессор, заслуженный деятель науки РФ, заместитель директора по научной работе ФГБУ «Научный центр акушерства, гинекологии и перинатологии им. В.И. Кулакова» Минздрава России, главный внештатный специалист по акушерству и гинекологии Министерства здравоохранения Российской федерации, заведующий кафедрой репродуктивной медицины и хирургии ФПДО «МГМСУ имени А.И. Евдокимова», член Российского обществ акушеров-гинекологов (г. Москва).
Баранов Игорь Иванович - доктор медицинских наук, профессор, заведующий организационно-методическим отделом Службы научно-организационного обеспечения ФГБУ «Научный центр акушерства, гинекологии и перинатологии им. В.И. Кулакова» Минздрава России, член Российского обществ акушеров- гинекологов (г. Москва).
Белова Елена Геннадьевна - кандидат медицинских наук, врач-инфекционист отделения профилактики ВИЧ-инфекции Московского городского центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Бессараб Тимур Петрович - кандидат медицинских наук, заведующий отделением профилактики ВИЧ-инфекции Московского городского центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Влацкая Юлия Федоровна - кандидат медицинских наук, заведующая амбулаторно-поликлиническим педиатрическим отделением Московского городского центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Володин Николай Николаевич - доктор медицинских наук, академик РАН, президент ОО «Российская ассоциация специалистов перинатальной медицины».
Гейне Маргарита Дмитриевна - врач клинической лабораторной диагностики Центральной лаборатории диагностики ВИЧ-инфекции Московского городского центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Денисова Елена Владимировна - врач-терапевт отделения профилактики ВИЧ- инфекции центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Иванников Евгений Васильевич - заведующий поликлиническим отделением Московского городского центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Коноплянников Александр Георгиевич - доктор медицинских наук, профессор кафедры акушерства и гинекологии педиатрического факультета РГМУ.
Кузьмин Владимир Николаевич - доктор медицинских наук, профессор кафедры акушерства и гинекологии ФГБОУ ВО «МГМСУ им. А.И. Евдокимова» Минздрава России (г. Москва).
Курцер Марк Аркадьевич - доктор медицинских наук, академик РАН, заведующий кафедрой акушерства и гинекологии Педиатрического факультета ФГБОУ ВО «РНИМУ им. Н.И. Пирогова», Председатель Президиума Московского общества акушеров-гинекологов.
Литвинова Наталья Геннадьевна - врач-инфекционист поликлинического отделения Московского городского центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Мазус Алексей Израилевич - доктор медицинских наук, руководитель Московского городского центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы и Международного центра вирусологии Медицинского института РУДН, главный внештатный специалист по ВИЧ-инфекции Министерства здравоохранения РФ и Департамента здравоохранения города Москвы, председатель правления НП «Национальная вирусологическая ассоциация».
Митюрина Елена Викторовна - кандидат медицинских наук, старший научный сотрудник научно-клинического отделения ВРТ им. Ф. Паулсена старшего ФГБУ «НМИЦ АГП им. В.И. Кулакова».
Набиулина Динара Ринатовна - врач-инфекционист поликлинического отделения Московского городского центра профилактики и борьбы со СПИД Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Назаренко Татьяна Алексеевна - профессор, доктор медицинских наук, директор Института репродуктивной медицины ФГБУ «НМИЦ АГП им. В.И. Кулакова».
Оленев Антон Сергеевич - кандидат медицинских наук, главный внештатный специалист по акушерству и гинекологии, заведующий филиалом «Перинатальный центр» ГБУЗ «Городская клиническая больница № 24 ДЗМ», член Междисциплинарной ассоциации специалистов репродуктивной медицины.
Ольшанский Александр Яковлевич - кандидат медицинских наук, заведующий Центральной лабораторией диагностики ВИЧ-инфекции Московского городского центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы.
Перминова Светлана Григорьевна - доктор медицинских наук, доцент, ведущий научный сотрудник научно-клинического отделения ВРТ им. Ф. Паулсена старшего ФГБУ «НМИЦ АГП им. В.И. Кулакова».
Серебряков Егор Михайлович - заведующий организационно-методическим отделом Московского городского центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Спасский Максим Евгеньевич - врач-психотерапевт отделения профилактики ВИЧ-инфекции центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Тугланова Бэла Мухамедовна - врач-инфекционист отделения профилактики ВИЧ-инфекции центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Цыганова Елена Валерьевна - кандидат медицинских наук, главный внештатный специалист по проблемам ВИЧ-инфекции Центрального Федерального округа, заместитель главного внештатного специалиста по инфекционным болезням Департамента здравоохранения города Москвы, заведующая научно-клиническим отделом Московского городского центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Шимонова Татьяна Евгеньевна - кандидат медицинских наук, врач-эпидемиолог Московского городского центра профилактики и борьбы со СПИДом Департамента здравоохранения города Москвы, член НП «Национальная вирусологическая ассоциация».
Конфликт интересов. Все члены рабочей группы подтвердили отсутствие финансовой поддержки / конфликта интересов, о котором необходимо сообщить.
Приложение А2. Методология разработки клинических рекомендаций
Методы, использованные для оценки качества и силы доказательств:
-
обзоры опубликованных мета-анализов;
-
систематические обзоры с таблицами доказательств;
-
консенсус экспертов;
-
оценка значимости в соответствии с рейтинговой схемой (схемы прилагаются).
Рекомендации обсуждены и одобрены членами Национальной ассоциации специалистов в области профилактики, лечения и диагностики ВИЧ-инфекции, рабочей группой Профильной комиссии по проблемам диагностики и лечения ВИЧ-инфекции Минздрава России.
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме. Доказательной базой для рекомендаций явились публикации, вошедшие в Кокрейновскую библиотеку, базы данных EMBASE, PUBMED и MEDLINE. Оценка значимости рекомендаций приведена в соответствии с классификацией уровней их достоверности и доказательности (рейтинговой схемой).
Метод, использованный для формулирования рекомендаций - консенсус экспертов.
Методы валидизации рекомендаций:
-
внутренняя экспертная оценка;
-
анализ соответствия нормативной базе;
-
внешняя экспертная оценка.
Методология анализа доказательств
Отбор публикаций как потенциальных источников доказательств по уровню валидности каждого исследования.
Влияние доказательности, присваиваемой публикации, на силу вытекающих из неё рекомендаций.
Для сведения к минимуму потенциальных ошибок вследствие субъективного фактора каждое исследование оценивалось независимо, по меньшей мере, двумя независимыми членами рабочей группы. Какие-либо различия в оценках обсуждались всей группой в полном составе. При невозможности достижения консенсуса привлекались независимые эксперты из числа наиболее опытных специалистов территориальных центров по профилактике и борьбе со СПИДом.
Целевая аудитория данных клинических рекомендаций - специалисты, имеющие высшее медицинское образование по следующим специальностям:
-
инфекционные болезни;
-
терапия;
-
общая врачебная практика (семейная медицина);
-
акушерство и гинекология;
-
эпидемиология;
-
клиническая лабораторная диагностика.
Клинические рекомендации могут использоваться при разработке учебно-методических комплексов для подготовки и повышения квалификации врачей. Шкалы оценки уровней достоверности доказательств (УДД) для методов диагностики, профилактики, лечения и реабилитации (диагностических, профилактических, лечебных, реабилитационных вмешательств) и шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств).
Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД |
Расшифровка |
|---|---|
|
1. |
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2. |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3. |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4. |
Несравнительные исследования, описание клинического случая |
|
5. |
Имеется лишь обоснование механизма действия или мнение экспертов |
Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
УДД |
Расшифровка |
|---|---|
|
1. |
Систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2. |
Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа |
|
3. |
Нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4. |
Несравнительные исследования, описание клинического случая или серии случаев, исследование «случай-контроль» |
|
5. |
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР |
Расшифровка |
|---|---|
|
А |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
|
В |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
|
С |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций - один раз в два года.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
ВИЧ-инфекция и законодательство Российской Федерации
Федеральный закон от 21.11.2011 г. № 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации".
Федеральный закон от 24.11.1995 г. № 181-ФЗ (ред. от 29.07.2018) "О социальной защите инвалидов в Российской Федерации".
Федеральный закон от 30.03.1995г. № 38-ФЗ "О предупреждении распространения в Российской Федерации заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ-инфекции)".
Приказ Министерства здравоохранения Российской Федерации от 08.11.2012 года № 689н "Об утверждении порядка оказания медицинской помощи взрослому населению при заболевании, вызываемом вирусом иммунодефицита человека (ВИЧ-инфекции)".
Приказ Министерства здравоохранения РФ от 2 октября 2019 г. № 824н “Об утверждении Порядка организации оказания высокотехнологичной медицинской помощи с применением единой государственной информационной системы в сфере здравоохранения”.
Постановление Главного государственного санитарного врача РФ от 28.01.2021 № 4 "Об утверждении санитарных правил и норм СанПиН 3.3686 -21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней".
Приказ Минздрава России от 20.10.2020 № 1130н "Об утверждении Порядка оказания медицинской помощи по профилю "акушерство и гинекология".
Приказ департамента здравоохранения города Москвы от 17.08.2018 г. № 563 «О дальнейшем совершенствовании мероприятий по профилактике перинатальной передачи ВИЧ-инфекции в медицинских организациях государственной системы здравоохранения города Москвы».
Приложение А3.1. Информированное согласие на проведение обследования на ВИЧ-инфекцию.
Я, _____________________________________________________________________________
(фамилия, имя, отчество)
___________________ года рождения, настоящим подтверждаю, что на основании предоставленной мне информации, свободно и без принуждения, отдавая отчет о последствиях обследования, принял решение пройти тестирование на антитела к ВИЧ. Для этой цели я соглашаюсь сдать анализ крови.
Я подтверждаю, что мне разъяснено, почему важно пройти тестирование на ВИЧ, как проводится тест и какие последствия может иметь тестирование на ВИЧ.
Я проинформирован, что:
- тестирование на ВИЧ проводится в Центре СПИД и других медицинских учреждениях. Тестирование по моему добровольному выбору может быть добровольным анонимным (без предъявления документов и указания имени) или конфиденциальным (при предъявлении паспорта, результат будет известен обследуемому и лечащему врачу). В государственных медицинских учреждениях тестирование на ВИЧ проводится бесплатно;
- доказательством наличия ВИЧ-инфекции является присутствие антител к ВИЧ в крови обследуемого лица. Вместе с тем, в период между заражением и появлением антител к ВИЧ (так называемое "серонегативное окно", обычно 3 месяца) при тестировании не обнаруживаются антитела к ВИЧ и обследуемое лицо может заразить других лиц; - ВИЧ-инфекция передается только тремя путями:
- парентеральный - чаще всего при употреблении наркотиков, но может передаваться также при использовании нестерильного медицинского инструментария, переливания компонентов крови, нанесении татуировок, пирсинге зараженным инструментом,
использовании чужих бритвенных и маникюрных принадлежностей;
- при незащищенных сексуальных контактах;
- от инфицированной ВИЧ матери к ребенку во время беременности, родов и при грудном вскармливании.
Приложение А3.2. Информирование о выявлении ВИЧ-инфекции
Информирование о выявлении ВИЧ-инфекции
Я, _______________________________________________________________
(фамилия, имя, отчество)
___________________ года рождения, настоящим подтверждаю, что получил информацию о выявлении у меня ВИЧ-инфекции; мне разъяснено что означает этот диагноз.
Я проинформирован, что:
- присутствие антител к ВИЧ, эпидемиологических и клинических данных является доказательством наличия ВИЧ-инфекции;
- для диспансерного наблюдения, уточнения стадии заболевания и назначения лечения мне необходимо обратиться в Центр по профилактике и борьбе со СПИД. Мне разъяснено, что:
- ВИЧ-инфицированным оказываются на общих основаниях все виды медицинской помощи по клиническим показаниям в соответствии с законодательством Российской Федерации об охране здоровья граждан;
- ВИЧ-инфицированные граждане Российской Федерации обладают на ее территории всеми правами и свободами и исполняют обязанности в соответствии с Конституцией Российской Федерации, законодательством Российской Федерации;
- в настоящее время в России существует бесплатное обследование и лечение (антиретровирусная терапия) для нуждающихся инфицированных ВИЧ. Для наблюдения и лечения мне рекомендовано немедленно обратиться в территориальный Центр СПИД. Антиретровирусная терапия не позволяет излечиться от ВИЧ-инфекции, но останавливает размножение вируса, существенно продлевает жизнь больному и уменьшает вероятность передачи от него заболевания. ВИЧ-инфицированным беременным женщинам важно как можно раньше обратиться в Центр СПИД и начать принимать специальные лекарства для предотвращения заражения будущего ребенка;
- ВИЧ-инфекция передается только тремя путями:
-
При незащищенных сексуальных контактах.
-
Через кровь - чаще всего при употреблении наркотиков, но может передаваться также при использовании нестерильного медицинского инструментария, переливании компонентов крови, нанесении татуировок, пирсинге зараженным инструментом, использовании чужих бритвенных и маникюрных принадлежностей.
-
От инфицированной ВИЧ матери к ребенку во время беременности, родов и при грудном вскармливании.
- заражение ВИЧ в быту при рукопожатиях, пользовании общей посудой, бассейном, туалетом, совместном приеме пищи, а также при укусах насекомых не происходит;
- я должен/должна соблюдать меры предосторожности, чтобы не инфицировать ВИЧ других людей. Защитить других от заражения ВИЧ- инфекцией можно, если не иметь с ними опасных контактов (люди не должны иметь контакты с кровью, выделениями половых органов и грудным молоком инфицированного ВИЧ человека). Мне дана рекомендация информировать половых партнеров о наличии у меня ВИЧ-инфекции, всегда и правильно пользоваться презервативами. Следует оградить других людей от контактов с кровью инфицированного ВИЧ человека, пользоваться только индивидуальными предметами личной гигиены (бритвами, маникюрными принадлежностями, зубными щетками) и при необходимости стерильными медицинскими инструментами, не употреблять наркотики;
- инфицированные ВИЧ не могут быть донорами крови, биологических жидкостей, органов и тканей.
- Существует уголовная ответственность за заведомое поставление другого лица в опасность заражения ВИЧ-инфекцией либо заражение другого лица ВИЧ- инфекцией (ст. 122 Уголовного кодекса Российской Федерации, Собрание законодательства Российской Федерации);
- с вопросами можно обратиться в территориальный центр СПИД.
______________________________ подпись обследуемого на ВИЧ _______________ дата
Приложение А3.3. Информированное согласие на проведение химиопрофилактики передачи ВИЧ-инфекции от матери ребенку во время беременности и родов
Информированное согласие на проведение химиопрофилактики передачи ВИЧ-инфекции от матери ребенку во время беременности и родов
Я _____________________________________________________________ (фамилия, имя, отчество полностью),
__________________ года рождения, настоящим подтверждаю свое добровольное согласие на прием лекарственных препаратов, действие которых направлено на предотвращение заражения моего будущего ребенка вирусом иммунодефицита человека или/и лечение ВИЧ-инфекции.
Я подтверждаю, что мне в доступной форме разъяснено, почему прием данных лекарств необходим, разъяснено действие назначаемых мне и моему будущему ребенку препаратов.
Я проинформирована, что:
- назначенные мне препараты снижают количество вируса в моем организме и предотвращают заражение ВИЧ-инфекцией;
- соблюдение режима приема препаратов снижает вероятность заражения будущего ребенка;
- тем не менее даже при абсолютном соблюдении всех правил приема препаратов полной гарантии предотвращения заражения будущего ребенка нет, риск заражения ребенка составляет до 1%;
- при отказе от приема назначенных лекарств или нарушениях режима их приема риск заражения возрастает до 40%;
- все назначаемые мне и моему будущему ребенку лекарственные препараты разрешены к применению в России;
- как и любое лекарственное средство, назначенные мне и моему будущему ребенку препараты могут вызывать некоторые побочные реакции, о возможном появлении которых я информирована;
- если вследствие приема назначенных мне лекарств возникнет угроза моему здоровью или здоровью будущего ребенка, химиопрофилактика/лечение могут быть прекращены по решению лечащего врача;
- что прикладывание моего ребенка к груди и/или кормление его моим грудным молоком является поставлением ребенка в опасность заражения ВИЧ- инфекцией;
- что искусственное вскармливание - безопасный метод вскармливания моего ребенка.
Я обязуюсь:
- проходить медицинское обследование для контроля действия назначенных мне препаратов по установленному графику, заполнять предусмотренные для этого анкеты, сдавать анализы;
- принимать назначенные мне лекарственные препараты строго в соответствии с предписанием лечащего врача;
- сообщать лечащему врачу обо всех нарушениях в приеме назначенных мне препаратов или прекращении их приема по каким-либо причинам;
- сообщать лечащему врачу обо всех изменениях в состоянии моего здоровья и делать это незамедлительно (в течение суток), если я считаю, что эти изменения связаны с приемом назначенных мне препаратов;
- не принимать, не посоветовавшись с лечащим врачом, назначившим мне химиопрофилактику/лечение, какие-либо другие лекарственные препараты (даже если они назначаются другим врачом). Если же прием этих лекарств неизбежен (например, в неотложных или экстренных случаях), обязательно сообщать об этом лечащему врачу.
Подпись пациента ______________________________ Дата: _____________________
Подпись лечащего врача __________________________ Дата: _____________________
Приложение А3.4. Установленные FDA категории риска применения лекарственных средств во время беременности
Установленные FDA категории риска применения лекарственных средств во время беременности


Приложение А3.5. Использование АРВП у беременных с ВИЧ-инфекцией: данные ФК и токсичности при беременности человека и рекомендации по применению во время беременности
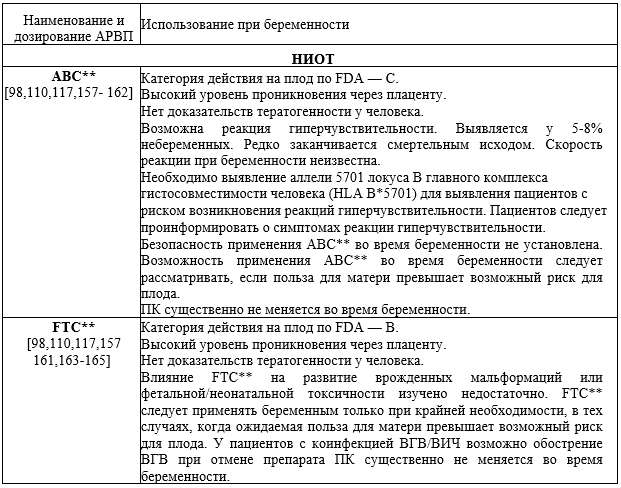
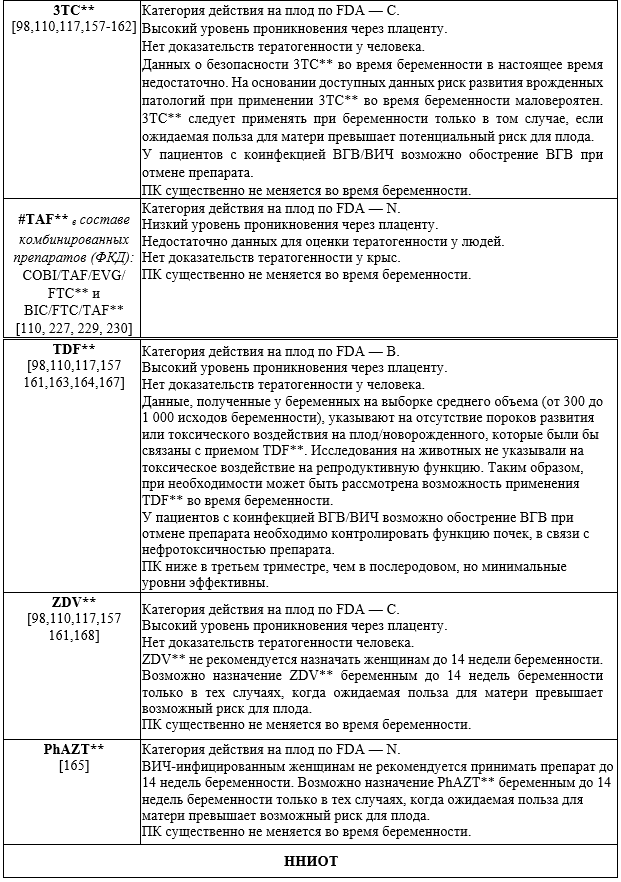
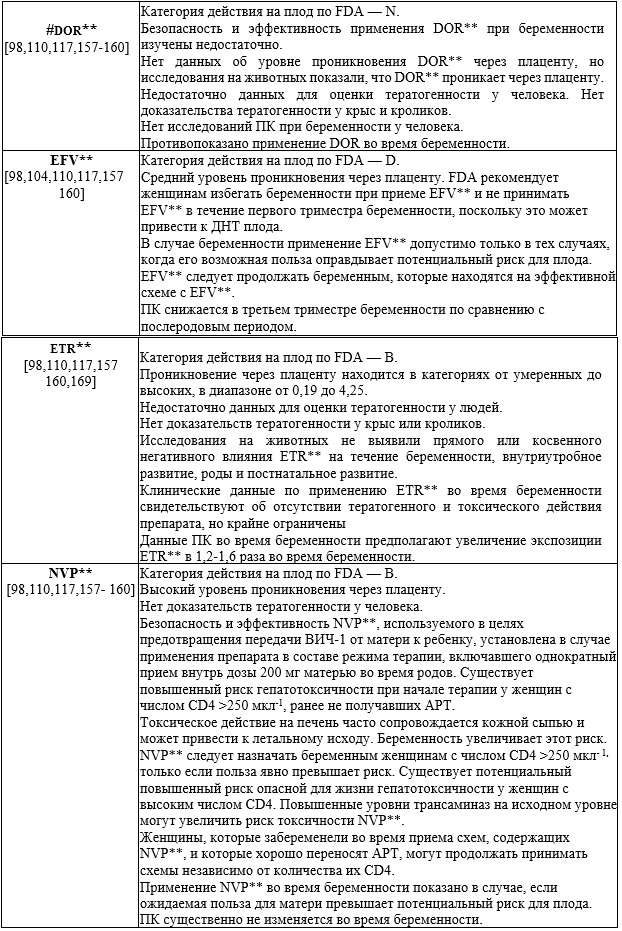
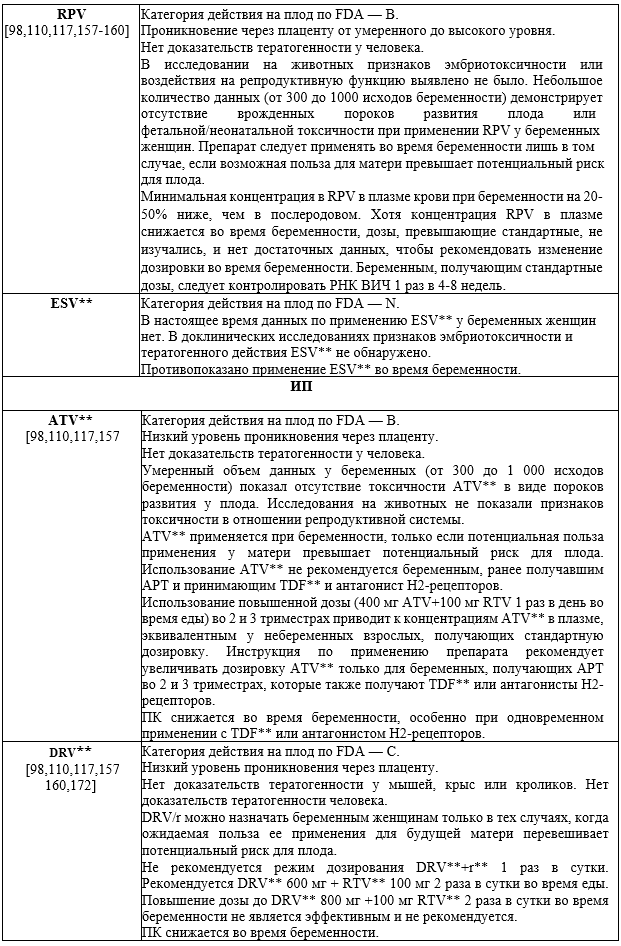
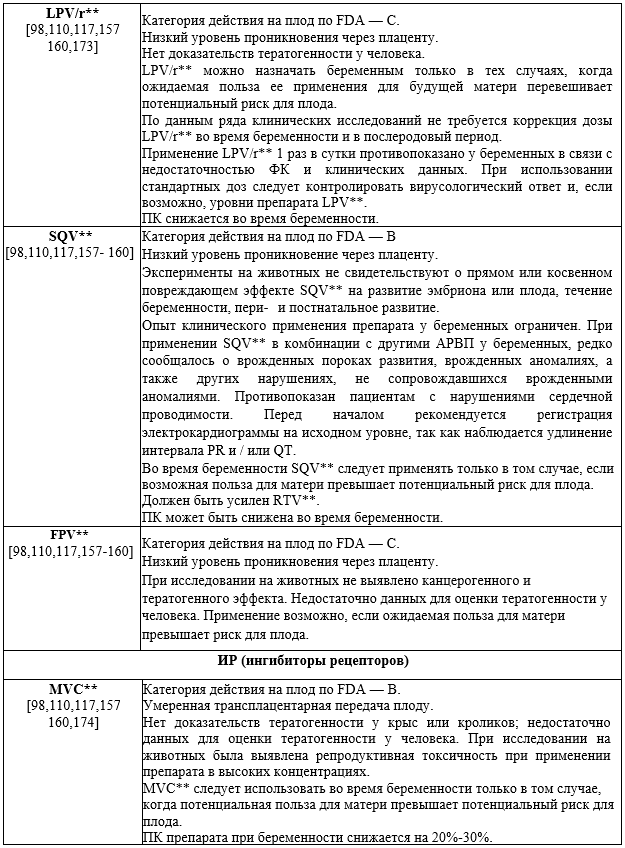
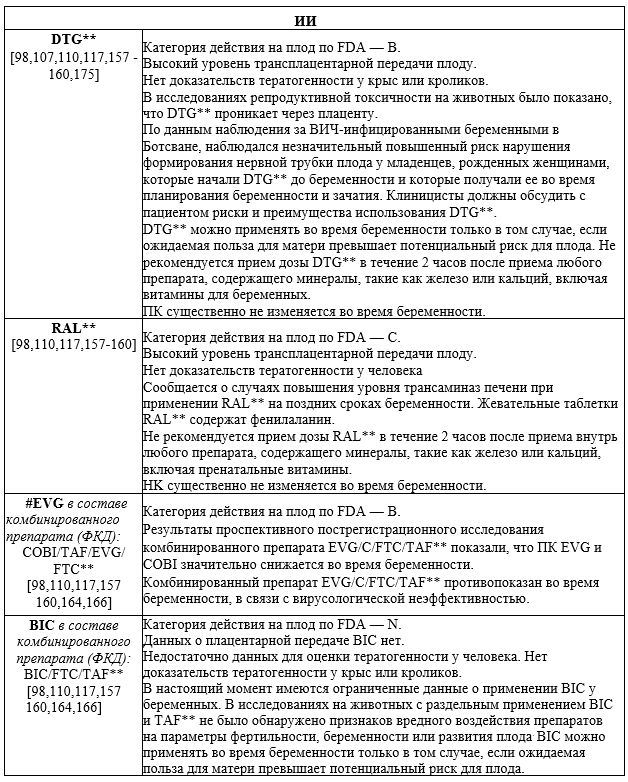

Приложение А3.6. Схемы АРВП для беременных, не получавших АРТ
Схемы АРВП для беременных, не получавших АРТ [12,96,98,106,109-121]

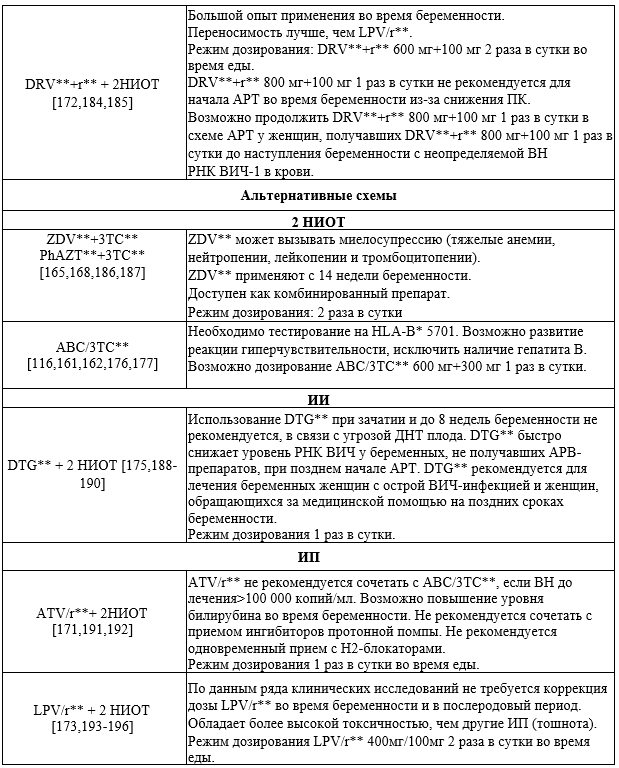
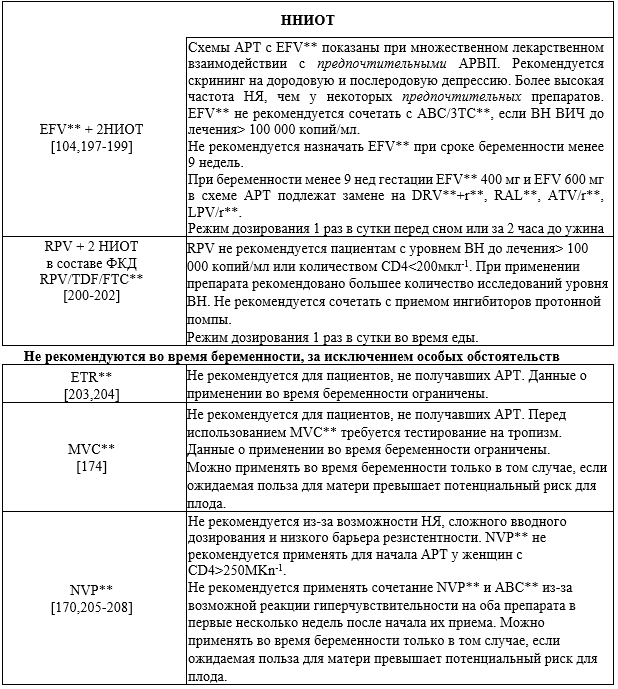
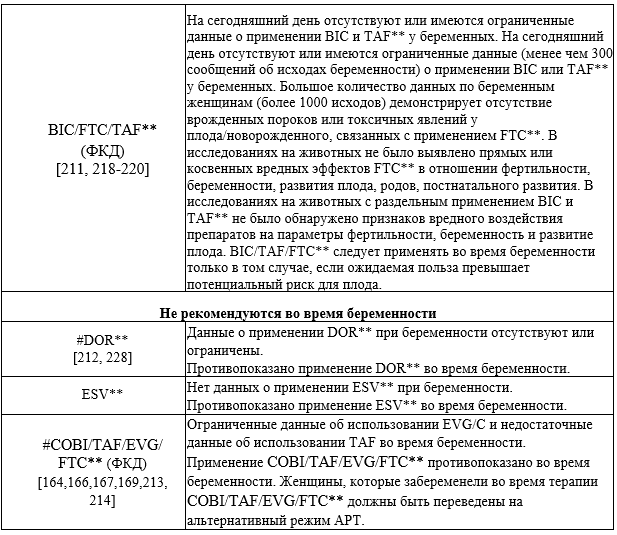
Приложение А3.7. Рекомендации по применению АРВП у ВИЧ-инфицированных беременных женщин и ВИЧ-инфицированных женщин, планирующих беременность [12,96,98,106,109-121]
|
АРВП |
Беременные, ранее не получавшие АРТ |
Продолжение для беременных с эффективной схемой АРТ |
Беременные, ранее получавшие АРТ |
Смена АРТ при низкой эффективности |
Женщины, планирующие беременность |
|---|---|---|---|---|---|
|
ИИ |
|||||
|
DTG** |
применение до 8 недель беременности противопоказано |
рассмотреть возможность перехода на другую схему АРТ в связи с риском развития ДНТ плода |
обсудить с пациенткой риски и преимущества использования DTG**; DTG** можно применять во время беременности только в том случае, если ожидаемая польза для матери превышает потенциальный риск для плода |
применение до 8 недель беременности противопоказано |
обсудить с пациенткой риски и преимущества использования DTG**; DTG** можно применять во время беременности только в том случае, если ожидаемая польза для матери превышает потенциальный риск для плода. |
|
RAL** |
предпочтительная схема |
продолжать |
предпочтительная схема |
предпочтительная схема |
предпочтительная схема |
|
ИП |
|||||
|
DRV**+r ** 600 мг + 100 мг |
предпочтительная схема |
продолжать |
предпочтительная схема |
предпочтительная схема |
предпочтительная схема |
|
LPV/r** |
альтернативная схема |
продолжать |
продолжать |
альтернативная схема |
альтернативная схема |
|
ННИОТ |
|||||
|
EFV** |
применение до 9 недель беременности не рекомендуется |
продолжать |
альтернативная схема |
альтернативная схема |
альтернативная схема |
|
RPV в составе ФКД |
альтернативная схема |
продолжать |
альтернативная схема |
альтернативная схема |
альтернативная схема |
|
#DOR** |
противопоказано |
противопоказано |
противопоказано |
противопоказано |
противопоказано |
|
#ESV** |
противопоказано |
противопоказано |
противопоказано |
противопоказано |
противопоказано |
|
#ETR** |
не рекомендуется |
продолжать |
не рекомендуется, за исключением особых обстоятельств |
не рекомендуется, за исключением особых обстоятельств |
не рекомендуется, за исключением особых обстоятельств |
|---|---|---|---|---|---|
|
#NVP** |
не рекомендуется |
продолжать |
не рекомендуется, за исключением особых обстоятельств |
не рекомендуется, за исключением особых обстоятельств |
не рекомендуется, за исключением особых обстоятельств |
|
НИОТ |
|||||
|
ABC** |
предпочтительная схема |
продолжать |
предпочтительная схема |
предпочтительная схема |
предпочтительная схема |
|
FTC** |
предпочтительная схема |
продолжать |
предпочтительная схема |
предпочтительная схема |
предпочтительная схема |
|
3TC** |
предпочтительная схема |
продолжать |
предпочтительная схема |
предпочтительная схема |
предпочтительная схема |
|
TDF** |
предпочтительная схема |
продолжать |
предпочтительная схема |
предпочтительная схема |
предпочтительная схема |
|
ZDV** |
альтернативная схема |
продолжать |
альтернативная схема |
альтернативная схема |
альтернативная схема |
Антагонист CCRS-рецепторов (по АТХ-классификации: прочие противовирусные препараты)
|
MVC** |
не рекомендуется |
продолжать |
не рекомендуется, за исключением особых обстоятельств |
не рекомендуется, за исключением особых обстоятельств |
не рекомендуется, за исключением особых обстоятельств |
|---|---|---|---|---|---|
|
Схемы ФКД |
|||||
|
TDF/ FTC/ EFV/ |
альтернативная схема (EFV**) |
продолжать |
альтернативная схема (EFV**) |
альтернативная схема (EFV**) |
альтернативная схема (EFV**) |
|
FTC/ RPV/ TDF** |
альтернативная схема (RPV) |
продолжать |
альтернативная схема (RPV) |
альтернативная схема (RPV) |
альтернативная схема (RPV) |
|
BIC/ TAF/ FTC** |
недостаточно данных (BIC, TAF**) |
недостаточно данных (BIC, TAF**), следует применять во время беременности только в том случае, если ожидаемая польза превышает потенциальный риск для плода |
недостаточно данных (BIC, TAF**), следует применять во время беременности только в том случае, если ожидаемая польза превышает потенциальный риск для плода |
недостаточно данных (BIC, TAF**), следует применять во время беременности только в том случае, если ожидаемая польза превышает потенциальный риск для плода |
недостаточно данных (BIC, TAF**), следует применять во время беременности только в том случае, если ожидаемая польза превышает потенциальный риск для плода |
|
#DOR/ 3TC/ TDF** |
противопоказан (DOR**) |
противопоказан (DOR**) |
противопоказан (DOR**) |
противопоказан (DOR**) |
противопоказан (DOR**) |
|
#EVG/ COBI/ FTC/ TDF** |
противопоказан | противопоказан | противопоказан | противопоказан | противопоказан |
|---|---|---|---|---|---|
|
#DTG/ 3TC (2КР) |
не рекомендуется |
не рекомендуется, сменить схему АРТ или добавить дополнит-ный АРВП |
не рекомендуется |
не рекомендуется |
не рекомендуется |
Приложение А3.8. Регламент основных осмотров и обследований ВИЧ-инфицированных беременных при диспансерном наблюдении в территориальном центре профилактики и борьбы со СПИДом
|
Врачи-специалисты |
Кратность обследования |
Дополнительные сведения |
|---|---|---|
|
Консультации врачей-специалистов обязательные |
||
|
врач-инфекционист |
1 раз в 4 недели до снижения ВН ниже уровня определения, затем 1 раз в 12 недель |
при назначении обследования, по его результатам (назначение АРТ), для оценки переносимости АРТ |
|
врач-терапевт |
однократно |
дополнительно по показаниям |
|
врач-офтальмолог |
по показаниям |
|
|
врач-оториноларинголог |
по показаниям |
|
|
врач-невролог |
по показаниям |
|
|
врач стоматолог-терапевт |
по показаниям |
|
|
врач акушер-гинеколог |
1 раз в 4 недели до снижения ВН ниже уровня определения, затем 1 раз в 12 недель |
осмотр врачом акушером-гинекологом предшествует осмотру врачом- инфекционистом с целью более точного установления срока беременности |
|
врач-фтизиатр |
однократно |
дополнительно по показаниям |
|
дополнительные консультации специалистами |
по показаниям |
врач-психиатр (психотерапевт, нарколог), психолог, социальный работник |
|
Лабораторная диагностика обязательная |
||
|
Общий (клинический) анализ крови |
до начала АРТ, через 4 и 12 недель от начала АРТ, далее 1 раз в 12 недель. |
дополнительно по показаниям |
|---|---|---|
|
Общий (клинический) анализ мочи |
до начала АРТ, через 4 и 12 недель от начала АРТ, далее 1 раз в 12 недель |
дополнительно по показаниям |
|
Анализ крови биохимический общетерапевтический |
до начала АРТ, через 4 и 12 недель от начала АРТ, далее 1 раз в 12 недель. |
дополнительно по показаниям |
|
лабораторное обследование на наличие заболеваний, передающихся половым путём |
1 (при постановке на учёт) |
дополнительно по показаниям |
|
Количественное определение РНК ВИЧ-1 в плазме крови методом ПЦР |
до начала АРТ, через 4 недели от начала или смены АРТ, далее 1 раз в 4 недели до снижения РНК ВИЧ до неопределяемых значений, далее не реже 1 раза в 12 недель и на 36 неделе беременности |
дополнительно по показаниям |
|
Анализ на ИС (исследование CD4+ лимфоцитов, исследование CD8+ лимфоцитов, ИРИ по соотношению, CD4/CD8) |
через 4 и 12 недель от начала АРТ, далее 1 раз в 12 недель; |
дополнительно по показаниям |
Дополнительные лабораторные исследования
|
ПЦР-диагностика ВГВ и ВГС |
1 (при постановке на учёт) |
при обнаружении в ИФА указанных инфекций |
|---|---|---|
|
диагностика ВПГ, ВЭБ, ЦМВ, токсоплазмоза |
по показаниям |
|
|
Молекулярно-генетическое исследование плазмы крови на наличие мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) к АРВП |
по показаниям |
|
|
Др. лабораторные исследования |
по показаниям |
|
|
Инструментальные исследования обязательные |
||
|
Регистрация электрокардиограммы |
по показаниям |
|
|
Ультразвуковое исследование органов брюшной полости (комплексное). |
по показаниям |
|
|
Др. инструментальные исследования |
по показаниям |
|
Приложение А3.9. Инструкция по проведению профилактики передачи ВИЧ-инфекции от матери ребенку в родильных домах (отделениях)
Инструкция по проведению профилактики передачи ВИЧ -инфекции от матери ребёнку в родильных домах (отделениях)
При поступлении беременной в родильное отделение, женщина продолжает приём АРТ, назначенной во время беременности. Если женщина не принимала АРТ, то ей назначается:
- Зидовудин/Ламивудин** (МНН: Зидовудин + Ламивудин**) 0,3г/0,15г
1 таблетка 2 раза в день;
- Лопинавир/Ритонавир** (МНН: Лопинавир + Ритонавир**) 0,2г/0,05 г
3 таблетки 2 раза в день, через 12 ч;
- в день родов - Ламивудин** 0,15 г 1 таблетка каждые 12 ч, Лопинавир/Ритонавир** (МНН: Лопинавир + Ритонавир**) 0,2г/0,05г 3 таблетки
каждые 12 ч.
С началом родовой деятельности: Зидовудин** внутривенно капельно 2 мг/кг в течение 1 ч (доза насыщения), 1 мг/кг/ч (поддерживающая доза) в течение всей родовой деятельности до пересечения пуповины. Порядок приготовления раствора Зидовудина**: в 500 мл раствора 5% декстрозы** добавляют 2 флакона (40 мл) раствора Зидовудина** для инъекций 10 мг/мл. Полученная концентрация составляет 0,0008 г/мл (0,8 мг/мл).
Соотношение объёмов ZDV** для в/в введения и 5% р-ра декстрозы**
|
Количество флаконов зидовудина** 200 мг/20 мл для внутривенного введения |
Объем раствора декстрозы** 5% |
Итоговый объем раствора |
|---|---|---|
|
1 флакон (20 мл) |
80 мл |
100 мл |
|
2 флакона (40 мл) |
160 мл |
200 мл |
|
3 флакона (60 мл) |
240 мл |
300 мл |
|
4 флакона (80 мл) |
320 мл |
400 мл |
Схема дозирования препарата Зидовудин** для внутривенной инфузии
|
Вес женщины (кг) |
Доза насыщения (мл/ч) |
Количество (кап/мин) |
Поддерживающая доза (мл/ч) |
Количество (кап/мин) |
|---|---|---|---|---|
|
до 50 |
125 |
40 |
62,5 |
20 |
|
51 - 60 |
150 |
50 |
75 |
25 |
|
61 - 70 |
175 |
60 |
87,5 |
30 |
|
71 - 80 |
200 |
70 |
100 |
35 |
|
81 - 90 |
225 |
80 |
112,5 |
40 |
|
91 - 100 |
250 |
90 |
125 |
45 |
1. При операции кесарева сечения инфузии начинаются за 4 ч до операции и продолжаются до пересечения пуповины.
Приложение А3.10. Информированное согласие на проведение ребенку антиретровирусной терапии с целью предотвращения перинатального заражения ВИЧ-инфекцией
Информированное согласие на проведение ребенку антиретровирусной терапии с целью предотвращения перинатального заражения ВИЧ-инфекцией
(подписывает законный представитель ребенка)
Я ________________________________________________________________ (фамилия, имя, отчество полностью)
настоящим подтверждаю свое добровольное согласие на лечение ребенка
__________________________________________________________________ (фамилия, имя, отчество полностью)
________________________ (дата рождения) лекарственными препаратами, направленными на предотвращение заражения ребенка ВИЧ-инфекцией от матери.
Я подтверждаю, что мне разъяснено:
- почему проведение данного лечения необходимо моему ребенку;
- действие назначаемых моему ребенку препаратов;
- как необходимо давать моему ребенку назначенные препараты;
- возможное побочное действие препаратов, назначенных моему ребенку;
- что мой ребенок должен проходить регулярные обследования, в том числе сдавать кровь, для диагностики ВИЧ-инфекции и оценки безопасности назначенного лечения и выявления возможного побочного действия лекарств;
- в какие сроки я должна приводить ребенка на обследование;
- что профилактический эффект может быть достигнут при неукоснительном соблюдении всех рекомендаций, данных мне лечащим врачом.
Я осознаю, что:
- при отсутствии химиопрофилактики передачи ВИЧ -инфекции от матери ребенку вероятность заражения составляет до 40%;
- назначение антиретровирусных препаратов (по АТХ -классификации: противовирусные препараты системного действия) позволяет снизить вероятность ВИЧ-инфицирования ребенка до 1%;
- если вследствие проведения лечения возникнет угроза здоровью моего ребенка, я буду проинформирована об этом для принятия решения о целесообразности дальнейшего его проведения;
- если вследствие проведения лечения возникнет угроза жизни моего ребенка, это лечение может быть прекращено по решению лечащего врача. В этом случае мне должны быть разъяснены причины этого решения;
- все лекарственные препараты, назначаемые моему ребенку, разрешены к применению в России;
- как и любое лекарственное средство, назначенные моему ребенку препараты могут вызывать некоторые побочные реакции, информация о которых предоставлена мне моим лечащим врачом.
Я обязуюсь:
- по установленному графику приводить своего ребенка на медицинское обследование для контроля воздействия назначенных ему препаратов, заполнять предусмотренные для этого анкеты, давать разрешение на взятие крови на анализы;
- давать назначенные моему ребенку лекарственные препараты строго в соответствии с предписанием лечащего врача;
- выполнять рекомендации лечащего врача по уходу за моим ребенком, его кормлению;
- не прикладывать ребенка к груди и не кормить его моим грудным молоком;
- сообщать лечащему врачу обо всех нарушениях в приеме назначенных моему ребенку препаратов или прекращении лечения по каким-либо причинам;
- сообщать лечащему врачу обо всех изменениях в состоянии здоровья моего ребенка и делать это незамедлительно (в течение суток), если я считаю, что эти изменения связаны с приемом препаратов, назначенных моему ребенку;
- не посоветовавшись с лечащим врачом, не давать моему ребенку какие-либо лекарственные препараты и не делать прививки (даже если лекарства и прививки назначаются другим врачом). Если же прием этих лекарств неизбежен (например, в экстренных случаях), незамедлительно сообщать об этом лечащему врачу;
- сообщить врачу, назначившему моему ребенку лекарственные препараты в экстренных случаях, что ребенок получает препараты для профилактики заражения ВИЧ-инфекцией.
Подпись законного представителя ребенка: ________________ Дата: ________________
Подпись лечащего врача ____________________________ Дата: _________________
Приложение А3.11. Уведомление об ответственности за отказ от профилактики передачи
Уведомление об ответственности за отказ от профилактики передачи ВИЧ-инфекции от матери ребенку
Мне_____________________________________________________________________ г.р., (фамилия имя отчество) разъяснены медицинские и юридические последствия отказа от профилактики передачи от матери ребенку для здоровья моего и моего ребенка. Вероятность передачи ВИЧ от матери к ребенку без проведения профилактических мероприятий составляет до 40%.
Регулярный прием мною антиретровирусных препаратов снижает риск заражения ребенка ВИЧ-инфекцией от матери до 1%.
Такого снижения можно добиться при сочетании приема антиретровирусных препаратов во время беременности, родов и в послеродовый период и ряда немедикаментозных мер, в том числе полной замены грудного вскармливания искусственным.
Отказ от приема мной антиретровирусных препаратов может повлечь за собой ухудшение состояния здоровья, прогрессию заболевания, выраженное снижение иммунитета, присоединение тяжелых, опасных для жизни оппортунистических заболеваний.
Мне разъяснено, что при грудном вскармливании и отказе от проведения ребенку антиретровирусной терапии существует непосредственная угроза жизни и здоровью моего ребенка, заключающаяся в возможности заражения его ВИЧ- инфекцией.
Мне разъяснено, что в этом случае, в соответствии с частью 5 статьи 20 Федерального закона от 21.11.2011 № 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации" при отказе родителей от медицинской помощи, необходимой для спасения жизни ребенка, медицинская организация имеет право обратиться в суд для защиты интересов ребенка.
Согласно Семейному кодексу, медицинская организация обязана сообщить в органы опеки и попечительства с передачей моих персональных данных для проведения дальнейших действий в целях защиты прав ребенка в соответствии с действующим законодательством.
Статьи Уголовного и Семейного кодекса и Федерального закона об основах охраны здоровья граждан зачитаны мне вслух.
Подпись пациента ______________________ Дата: __________________________
Подпись лечащего врача ______________________ Дата: __________________________
Подпись заведующего отделением______________________ Дата:_______________________
(Ф.И.О., разборчиво) (подпись)
Приложение А3.12. Мероприятия по предотвращению отказов ВИЧ-инфицированных женщин по проведению профилактики передачи ВИЧ-инфекции от матери ребенку
-
Отказы женщин от проведения профилактики передачи ВИЧ-инфекции от матери ребенку обусловлены наличием в СМИ информации СПИД-диссидентской направленности, отрицанием своего ВИЧ-статуса (иногда совместно с ВИЧ- инфицированным партнером), страхом развития побочных эффектов от приема препаратов.
-
В целях обеспечения возможности своевременной защиты прав ребенка на жизнь и здоровье женщинам предлагается подписать согласие на передачу сведений, составляющих врачебную тайну в установленном законом порядке в иные медицинские организации, органы опеки, попечительства и патронажа в целях обеспечения его прав и законных интересов ребенка.
-
При появлении отказа рекомендуется:
- прием пациентки максимально возможным числом врачей, психологом, социальным работником, юрисконсультом с отражением разъяснительной работы в медицинской документации;
- приглашение женщины на повторные визиты.
-
Женщина должна быть предупреждена об ответственности за отказ от медицинской помощи, влекущий за собой угрозу жизни или здоровью несовершеннолетнего с отражением медицинской документации (ст. 125 и ст. 156 Уголовного кодекса РФ, ч. 5, ст. 20 Федерального закона от 21.11.2011 г. № 323- ФЗ «Об основах охраны здоровья граждан в Российской Федерации»).
-
Рекомендуется заполнение формы уведомления об ответственности за отказ от профилактики передачи ВИЧ-инфекции от матери ребёнку (Приложение А3.9.). Если мать отказывается его подписать, то документ читается матери вслух и заверяется двумя подписями медработников.
-
Медицинские учреждения в обязательном порядке информируют органы опеки и попечительства о матерях, отказывающихся от проведения профилактики ребенку (по месту фактического нахождения ребенка) (ч. 3 ст. 56 Семейного кодекса РФ).
-
В исключительных случаях (отказ от профилактики новорожденному) органы опеки и попечительства могут применить ст. 77 Семейного Кодекса РФ об отобрании ребенка при непосредственной угрозе его здоровью с целью организации проведения дальнейших действий по защите здоровья ребёнка.
Приложение Б. Алгоритмы действий врача
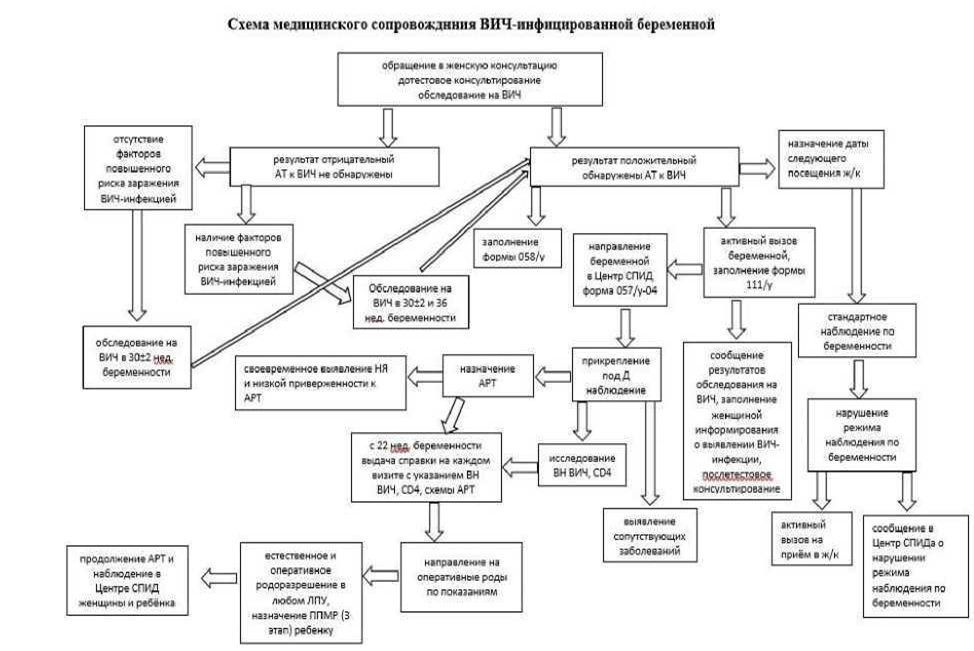
Приложение В. Информация для пациента
После постановки диагноза ВИЧ-инфекции проводится беседа с беременной женщиной о заболевании, его прогнозе, влиянии на беременность и здоровье будущего ребенка и предполагаемой схеме лечения. Проводится беседа в доступной для нее форме, при необходимости с привлечением психолога. Разъясняется необходимость назначения АРТ не позднее 13 -й недели беременности, далее в родах и новорожденному ребенку для профилактики перинатальной передачи ВИЧ-инфекции.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Опросник для определения факторов риска неприверженности у пациентов с ВИЧ-инфекцией
Название на русском: Опросник для определения факторов риска неприверженности у пациентов с ВИЧ-инфекцией.
Источник: Федяева О.Н., Сирота Н.А. Факторы риска неприверженности антиретровирусной терапии у больных ВИЧ-инфекцией и способы их выявления. Медицинский Совет. 2014;(7):77-79.
Тип (подчеркнуть):
шкала оценки
индекс
вопросник
другое (уточнить)
Назначение: определения факторов риска неприверженности АРВТ у пациентов с ВИЧ-инфекцией
Содержание и интерпретация:
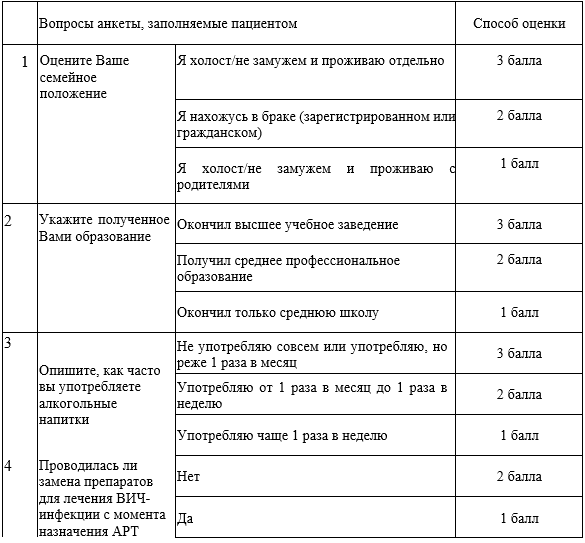
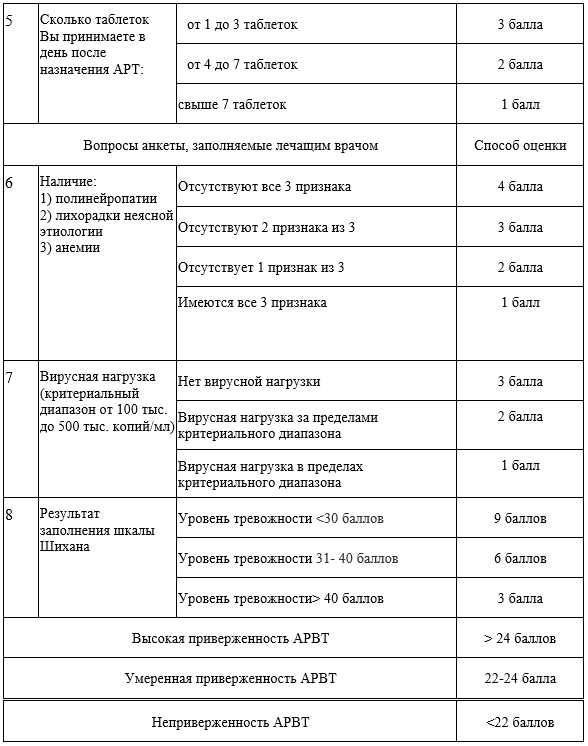
Приложение Г2. Шкала самооценки тревоги Д.Шихана
Название на русском языке: Шкала самооценки тревоги Д. Шихана
Оригинальное название: Sheehan Patient-Rated Anxiety Scale - (SPRAS),
(David V. Sheehan, 1983).
Источник: Sheehan D.V., Sheehan Kr. // Int. J. Psycriat. Med, - 1983. - N 12. - P. 243266.
Тип (подчеркнуть):
шкала оценки
индекс
вопросник
другое (уточнить):
Назначение: для скрининговой диагностики и самодиагностики расстройств тревожного спектра у взрослых лиц.
Содержание (шаблон): определите, насколько Вас беспокоили в течение последней недели указанные ниже симптомы. Отметьте номер Вашего ответа на бланке ответов.
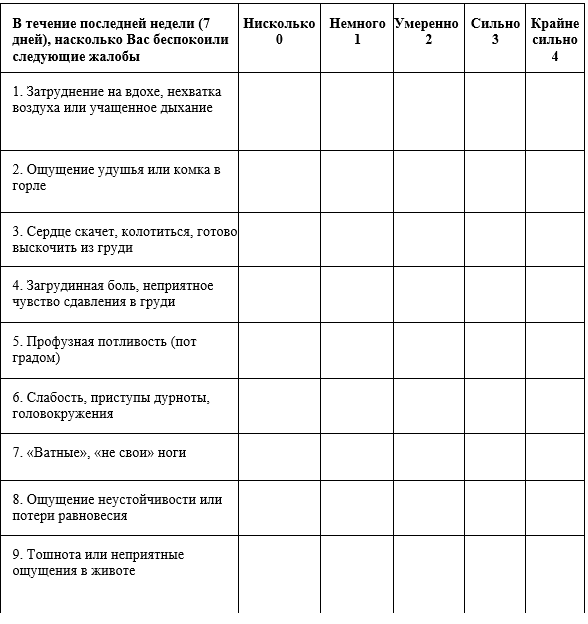
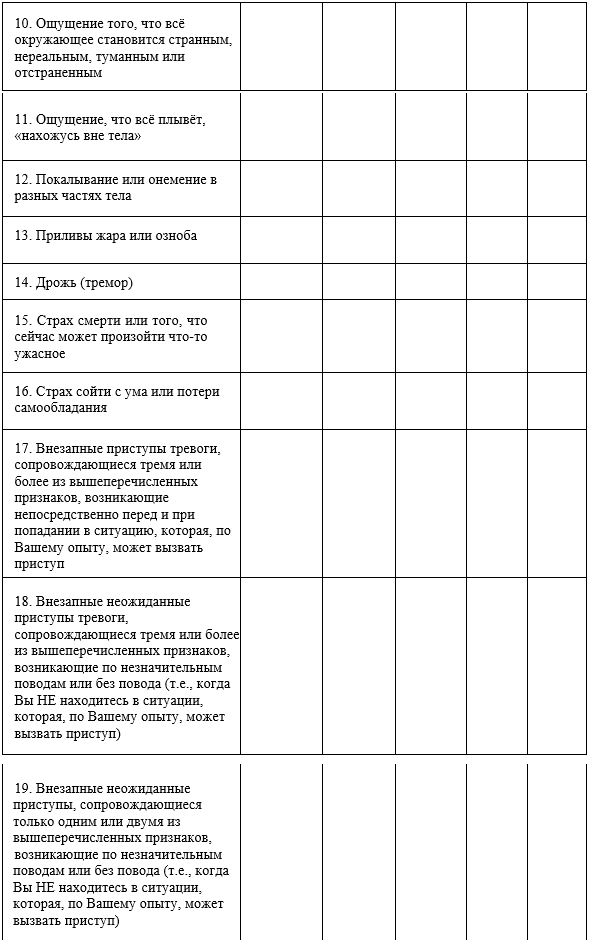


Ключ (интерпретация):
Общий балл по шкале равен сумме баллов всех пунктов. Таким образом, общий балл может находиться в диапазоне от 0 до 140.
0-29 - отсутствие клинически выраженной тревоги, 30-79 - клинически выраженная тревога, 80 и выше - тяжелое тревожное расстройство, паническое расстройство.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.