Бронхиальная астма у детей
 Версия: Клинические протоколы КР 2023 (Кыргызстан)
Версия: Клинические протоколы КР 2023 (Кыргызстан)
Астма (J45), Астматический статус [status asthmaticus] (J46)
Аллергология детская, Педиатрия, Пульмонология детская
Общая информация
Краткое описание
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ КЫРГЫЗСКОЙ РЕСПУБЛИКИ
НАЦИОНАЛЬНЫЙ ЦЕНТР ОХРАНЫ МАТЕРИНСТВА И ДЕТСТВА
КЫРГЫЗСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ им. И.К. АХУНБАЕВА
РЕСПУБЛИКАНСКИЙ ЦЕНТР РАЗВИТИЯ ЗДРАВООХРАНЕНИЯ И ИНФОРМАЦИОННЫХ ТЕХНОЛОГИЙ
Приложение 1
к приказу МЗ КР № 542
от 11.05.2023 г.
БРОНХИАЛЬНАЯ АСТМА У ДЕТЕЙ диагностика, ведение и лечение
Клиническое руководство для всех уровней здравоохранения
Клиническое руководство по диагностике, лечению и ведению бронхиальной астмы у детей
Клиническая проблема
Бронхиальная астма у детей
Название документа
Клиническое руководство по диагностике, лечению и ведению бронхиальной астмы у детей разработано для специалистов здравоохранения всех уровней здравоохранения
Этапы оказания помощи
Амбулаторный и стационарный уровни оказания медицинской помощи
Цель создания Клинического руководства
Внедрение и организация системы единого подхода по диагностике, лечению и ведению бронхиальной астмы у детей, основанного на международных клинических руководствах высокого методологического качества и адаптированных к местным условиям.
Целевые группы
Семейные врачи, врачи первичного, вторичного и третичного уровня здравоохранения, педиатры, врачи других специальностей; организаторы здравоохранения; специалисты, контролирующие качество оказания медицинской помощи (МАК, Фонд ОМС при МЗ КР и другие).
Клиническое руководство применимо к детям с бронхиальной астмой, обратившихся на амбулаторный уровень и стационарное лечение.
Дата создания: февраль 2022 - март 2023
Данное клиническое руководство разработано на основании новых обновленных данных по наилучшей клинической практике по бронхиальной астме у детей, в дальнейшем будет обновляться по мере появления новых доказательств.
Заболеваемость бронхиальной астмой в Кыргызской Республике
ВВЕДЕНИЕ
Бронхиальная астма (БА) - одно из самых распространенных заболеваний в мире, и количество больных увеличивается, особенно среди детей. Распространенность симптомов БА в детском возрасте колеблется от 0 до 30% в зависимости от популяции, с наибольшим уровнем в Австралии, Новой Зеландии, Шотландии и Англии.
Большинство пациентов, страдающих БА, хорошо отвечают на традиционную терапию, достигая контроля заболевания. Однако существенная часть больных (20–30%) имеет сложные для терапии фенотипы БА (тяжелая атопическая БА, БА при ожирении, БА с поздним дебютом, БА с фиксированной бронхиальной обструкцией) и может быть рефрактерна к традиционной терапии. У них отмечается высокая частота обострений и обращений за неотложной медицинской помощью [1, 2].
Впервые на основании анкетирования детей по международной программе ISAAC (под руководством д.м.н., проф. Иманалиевой Ч.А., 2003) установлено, что вероятность наличия БА в г. Бишкек составляет от 12,2% до 14,6% (среди детей 6-7 и 13-14 лет соответственно) [3].
Заболеваемость бронхиальной астмой в Кыргызской Республике
(2017-2020 гг., по данным центра электронного здравоохранения МЗ КР )
Заболеваемость бронхиальной астмой в Кыргызской Республике у детей до 14 лет
| Года | Зарегистрировано всего больных | Зарегистрировано больных впервые в жизни | ||||||
| Взрослые и подростки | Дети до 14 лет | Взрослые и подростки | Дети до 14 лет | |||||
| Абс. | На 100 тыс. | Абс. | На 100 тыс. | Абс. | На 100 тыс. | Абс. | На 100 тыс. | |
| 2017 | 8154 | 194,0 | 858 | 43,0 | 1239 | 29,5 | 257 | 12,9 |
| 2018 | 8308 | 194,6 | 960 | 46,8 | 1360 | 31,9 | 316 | 15,4 |
| 2019 | 7862 | 181,1 | 1000 | 47,3 | 773 | 17,8 | 311 | 14,7 |
| 2020 | 7235 | 164,1 | 788 | 36,3 | 572 | 13,0 | 170 | 7,8 |
Заболеваемость бронхиальной астмой в Кыргызской Республике у детей до 14 лет
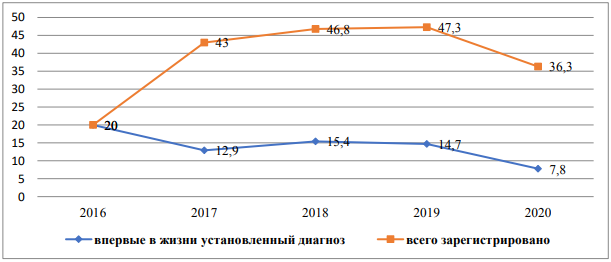
Рис. 1. Заболеваемость БА у детей по данным центра электронного здравоохранения МЗ КР, на 100 тыс. населения (2017-2020 гг.)
Болезни органов дыхания в структуре общей заболеваемости [4]
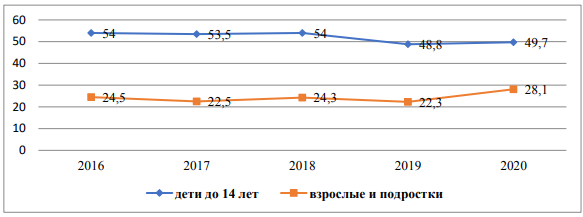
Рис. 2. Доля болезней органов дыхания от % общей заболеваемости в Кыргызской Республике на 100 тыс. населения, 2016-2020 гг.
С 2005 г. изданы три клинических руководства/протокола: «БА у детей для первичного звена здравоохранения» (2005 г.), «Ведение детей с болезнями органов дыхания» (2010 г.) и «Бронхиальная астма у детей» (2013 г.), в которых учитывались рекомендации, имеющие доказательную основу по диагностике, лечению и профилактике БА у детей.
Несмотря на то, что были определены критерии диагностики и лечения БА у детей, тем не менее, на сегодняшний день имеется стереотип использования необоснованных рекомендаций, не имеющих доказательную базу.
Данное клиническое руководство (КР) – дополненная и переработанная версия клинического руководства и протокола по лечению БА у детей.
Особенностью настоящего КР является объединение протоколов по лечению обострения БА и дальнейшему ведению детей с БА на амбулаторном и стационарном уровнях здравоохранения с учетом обновленных рекомендаций, основанных на доказательной медицине.
КР предназначено для медицинских работников всех уровней ОЗ КР, принимающих участие в ведении, диагностике, лечении, реабилитации и профилактики детей с БА, а также специалистов, контролирующих качество оказания медицинской помощи (Фонд ОМС).
Задачи:
Целевая группа руководства
Клиническое руководство разработано для медицинских работников всех уровней ОЗ КР, принимающих участие в ведении, диагностике, лечении и ведению БА у детей.
ОПРЕДЕЛЕНИЕ
КОДИРОВАНИЕ ПО МКБ-10 [7]
ЦЕЛИ И ЗАДАЧИ
СОЗДАНИЯ РУКОВОДСТВА ПО БРОНХИАЛЬНОЙ АСТМЕ У ДЕТЕЙ
Цель: Повышение знаний, умений и навыков врачей/медицинских работников всех специальностей в оказании качественной квалифицированной медико-санитарной помощи больным детям с БА на всех уровнях здравоохранения Кыргызской Республики (КР) с учетом обновленных руководств/протоколов, имеющих доказательную основу.
Задачи:
1. Внедрение в практику единых научно-обоснованных клинико-лабораторных критериев диагностики, научно-обоснованных принципов и подходов в лечении и ведении БА у детей на всех уровнях организаций здравоохранения КР.
2. Применение единого алгоритма действий на всех уровнях оказания медицинской помощи больным детям с БА у детей для:
- своевременной диагностики заболевания;
- правильного квалифицированного ведения и лечения болезни в зависимости от формы и течения заболевания.
3. Снижение риска развития и прогрессирования осложнений у детей с БА.
Целевая группа руководства
Клиническое руководство рекомендуется использовать для оказания квалифицированной качественной помощи при БА у детей.
Клиническое руководство разработано для медицинских работников всех уровней ОЗ КР, принимающих участие в ведении, диагностике, лечении и ведению БА у детей.
Ожидаемые результаты применения национального клинического руководства:
- Улучшение качества диагностики будет способствовать своевременному выявлению, следовательно, лечению БА у детей;
- Рациональное лечение и профилактика БА будут способствовать сокращению осложнений, снижению материальных и иных затрат у больного и государства.
ОПРЕДЕЛЕНИЕ
Бронхиальная астма (БА) - заболевание, сопровождающееся хроническим воспалением бронхов, их гиперреактивностью и периодически возникающими приступами затрудненного дыхания или удушья, в результате распространенной бронхиальной обструкции, обусловленной бронхоконстрикцией, гиперсекрецией слизи, отеком стенки бронхов. Бронхиальная обструкция (под влиянием лечения или спонтанно) обратима [3].
КОДИРОВАНИЕ ПО МКБ-10 [7]
J45 – Бронхиальная астма:
J45.0 – Бронхиальная астма с преобладанием аллергического компонента
J45.1 – Неаллергическая бронхиальная астма
J45.8 – Смешанная бронхиальная астма
J45.9 – Бронхиальная астма неуточненная
J46 – Астматический статус
Классификация
КЛАССИФИКАЦИЯ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ
Классификация БА по фенотипам [1-4]
Определение фенотипических особенностей заболевания является требованием времени, так как персонализированная медицина на основании отбора пациентов (выделение субпопуляций/кластеров/фенотипов БА) предусматривает использование ряда диагностических тестов и при подтверждении предполагаемого фенотипа – таргетную терапию, и персонифицированные методы профилактики [1].
Аллергическая БА: наиболее легко распознаваемый фенотип, при котором БА обычно начинается в детстве, связана с наличием других аллергических заболеваний (атопический дерматит, аллергический ринит, пищевая аллергия) у пациента или родственников. Для этого фенотипа характерно эозинофильное воспаление дыхательных путей. Пациенты с аллергической БА обычно хорошо отвечают на терапию ингаляционными глюкокортикостероидами (ИГКС).
Неаллергическая БА: встречается преимущественно у взрослых, не связана с аллергией. Профиль воспаления дыхательных путей у пациентов с данным фенотипом может быть эозинофильным, нейтрофильным, смешанным или малогранулоцитарным. В зависимости от характера воспаления пациенты с неаллергической астмой могут не отвечать на терапию ИГКС.
Классификация бронхиальной астмы по степени тяжести
Классификация БА по степени тяжести у пациентов с впервые выявленной БА проводится на основании клинической картины. Классификацию по тяжести БА целесообразно использовать диагностике и определения начальной терапии [1-4]. У пациентов с впервые выявленной БА классификация по степени тяжести проводится на основании клинической картины.
Классификация бронхиальной астмы по степени тяжести [1-4]
| Характеристики | Легкая интермиттирующая БА | Легкая персистирующая БА | Персистирующая БА средней тяжести | Тяжелая персистирующая БА |
| Дневные симптомы | Реже 1 раза в неделю | Чаще 1 раза в неделю, но реже 1 раза в день | Ежедневные симптомы; Ежедневное использование КДБА | Ежедневные симптомы; Ограничение физической активности |
|
Ночные
симптомы
|
Не чаще 2-х раз в месяц | Не чаще 2-х раз в месяц | Чаще 1 раза в неделю | Частые |
| Обострения | Короткие | Могут снижать физическую активность и нарушать сон | Могут приводить к ограничению физической активности и нарушению сна | Частые |
| Функциональные показатели | ОФВ1 или ПСВ ≥ 80% от должного | ОФВ1 или ПСВ ≥ 80% от должного | ОФВ1 или ПСВ 60- 80% от должного | ОФВ1 или ПСВ ≤60% от должного |
| Разброс ПСВ | Разброс ПСВ или ОФВ1 < 20% | Разброс ПСВ или ОФВ1 20-30% | Разброс ПСВ или ОФВ1 > 30% | Разброс ПСВ или ОФВ1 > 30% |
Примечание: Достаточно наличия одного из перечисленных критериев тяжести соответствующей группы, чтобы отнести пациента к более тяжелой степени тяжести.
Классификация обострений БА по степени тяжести
Пациенты с любой степенью тяжести БА могут иметь легкие, среднетяжелые или тяжелые обострения. У ряда пациентов с интермиттирующей БА наблюдаются тяжелые 2 2 и угрожающие жизни обострения на фоне длительных бессимптомных периодов с нормальной легочной функцией. Степень тяжести обострений БА устанавливается по клиническим критериям, для того, чтобы отнести пациента к более тяжелой категории достаточно наличие хотя бы одного из соответствующих критериев.
Под астматическим статусом понимают эпизод острой дыхательной недостаточности (ОДН) вследствие обострения БА. В современных классификациях астматический статус эквивалентен понятиям «жизнеугрожающая астма» (сопорозное состояние) и «астма, близкая к фатальной» (гипоксемическая кома).
Определение степени тяжести обострений БА [1]
| Степени тяжести | Критерии |
| Легкое обострение БА или обострение БА средней степени тяжести |
|
| Тяжелое обострение БА |
|
| Жизнеугрожающая астма |
Наличие любого из нижеперечисленных признаков:
Клинические признаки:
Инструментальные изменения:
|
| Астма, близкая к фатальной |
|
Необходимо зарегистрировать следующие клинические признаки:
- Частота пульса - нарастающая тахикардия обычно свидетельствует об ухудшении астмы; падение пульса при угрожающей жизни астме является претерминальным событием.
- Частота дыхания и степень одышки - слишком сильная одышка, чтобы закончить предложение на одном дыхании или покормить.
- Использование вспомогательных дыхательных мышц - лучше всего определяется при пальпации мышц шеи.
- Количество хрипов, которые могут стать двухфазными или менее явными с увеличением обструкции дыхательных путей обструкции
- Степень возбуждения и уровень сознания - всегда успокаивайте пациента.
Оценка тяжести обострений у детей до 5 лет [1]
| Симптомы | Средней тяжести | Тяжелое* |
| Изменение сознания | Нет | Возбуждение, заторможенность или сонливость |
| Пульсоксиметрия (SaO2)** | >92% | <92% |
| Речь*** | Предложениями | Отдельными словами |
| Частота пульса | <100 в минуту |
>180 в минуту (0–3 года)
>150 в минуту (4–5 лет)
|
| Частота дыхания | ≤ 40 в минуту | >40 в минуту |
| Центральный цианоз | Отсутствует | Вероятен |
| Интенсивность свистящего дыхания | Варьирует | Возможно «немое легкое» |
Примечание: * Любой из этих признаков указывает на тяжелое обострение астмы.
** Перед оксигенотерапией или назначением бронходилататора.
*** Необходимо принимать во внимание уровень развития ребенка.
Тяжесть БА у пациентов, получающих лечение, оценивается ретроспективно, исходя из необходимого для контроля симптомов и обострений объема терапии.
Классификация БА по степени тяжести у пациентов, уже получающих лечение
| Степень тяжести | Определение (ступень терапии) | Получаемое лечение |
| Легкая БА | Астма, которая хорошо контролируется терапией 1 ступени | Низкие дозы ИГКС-КДБА по потребности или низкие дозы ИГКС или АЛТР |
| БА средней тяжести | Астма, которая хорошо контролируется терапией ступени 3 | Низкие дозы ИГКС/ДДБА |
| Тяжелая БА | Астма, требующая терапии ступени 4 и 5, для того чтобы сохранить контроль, или БА, которая остается некотролируемой, несмотря на терапию ступени 5 | Средние или высокие дозы ИГКС/ДДБА, тиотропия бромида, или фиксированная комбинация ИГКС/ДДБА/ДДАХ, таргентная терапия и/или СГКС |
Для определения эффекта проводимой терапии и коррекции используют классификацию БА по уровню контроля через 1 месяц от начала терапии.
Классификация бронхиальной астмы по уровню контроля [1-4]
|
Клинические признаки за последние
4 недели (да/нет)
|
Бронхиальная астма по уровню контроля | ||
| Хорошо контролируемая | Частично контролируемая | Неконтролируемая | |
|
Дневные симптомы чаще 2-х раз в неделю
Для детей до 6 лет – чаще, чем 1 раз в неделю
|
Нет признаков | 1-2 признака | 3-4 признака |
| Ночные пробуждения из-за БА | |||
|
Потребность в препарате для купирования симптомов чаще 2-х раз в неделю*
Для детей до 6 лет – чаще, чем 1 раз в неделю
|
|||
|
Любое ограничение активности из-за БА
Для детей до 6 лет - бегает, играет меньше, чем другие дети; быстро устает от ходьбы/ игры
|
|||
Примечание: * за исключением использования бронходилататоров (препараты для лечения обструктивных заболеваний дыхательных путей) перед физической нагрузкой.
У детей 6-11 лет возможно применение специальных вопросников по оценке астмы для уточнения правильности оценки контроля, факторов риска, сопутствующих заболеваний (АСТ-тест).
Факторы и группы риска
ФАКТОРЫ РИСКА ВОЗНИКНОВЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ [5-8]
В развитии БА у детей имеет значение комплексное воздействие ряда внутренних и внешних факторов, приведенных в табл. 1.
Факторы риска бронхиальной астмы у детей
| Внутренние факторы | Внешние факторы |
|
|
В целом 13% случаев БА у детей можно отнести за счёт загрязнения воздуха автомобилями – «traffic-related air pollution» (Achakulwisut et al, Lancet Plan Health 2019) [4].
Диагностика
ДИАГНОСТИКА БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ [1-4]
Диагностика БА у детей основана на оценке клинических симптомов, наличии факторов риска развития БА при исключении других причин бронхиальной обструкции.
Центральное место во всех определениях занимает наличие симптомов (более одного - хрипы, одышка, стеснение в груди, кашель) и переменной обструкции воздушного потока [SIGN,2021]:
- Единого диагностического теста для астмы не существует.
- Диагноз ставится на основании клинической оценки, подкрепленной объективными тестами, которые призваны продемонстрировать переменную обструкцию воздушного потока или наличие воспаления дыхательных путей.
|
С
|
Диагноз БА устанавливается на основании:
|
Жалобы у детей
|
Жалобы [5-8]:
|
Ключевые симптомы БА [5-8]
|
Ключевые анамнестичекие данные [5-8]
|
При сборе анамнеза следует обсудить весь набор симптомов за последние 3-4 месяца, обратив особое внимание на те, которые беспокоили в течение 2-х предшествующих недель. Свистящее дыхание должно быть подтверждено врачом, поскольку родители могут неправильно интерпретировать звуки, издаваемые их ребенком при дыхании.
ОСОБЕННОСТИ ДИАГНОСТИКИ БРОНХИАЛЬНОЙ АСТМЫ В РАЗНЫЕ ВОЗРАСТНЫЕ ПЕРИОДЫ [3]
Дети первых двух лет жизни
Для детей от 0 до 2 лет с БА характерна наследственная отягощенность по аллергическим заболеваниям (особенно по материнской линии), высокая распространенность аллергических проявлений со стороны кожных покровов и аллергических реакций на пищевые продукты и медикаменты, отчетливый эффект бронхолитической терапии.
Во время острой респираторной вирусной инфекции у таких детей в ранние сроки развивается выраженный бронхообструктивный синдром. Однако на практике ни один из указанных признаков в отдельности, а также уровень общего иммуноглобулина Е (IgE) не может служить достоверным дифференциально-диагностическим критерием острого бронхита с бронхообструктивным синдромом и БА.
Дети 2–5 лет
Ключевым критерием диагностики БА в этом возрасте является персистирование симптомов на протяжении последнего года, за исключением случаев только пыльцевой сенсибилизации (Табл.5).
Наиболее частые триггеры – респираторные вирусы, аллергены (клещи домашней пыли, эпидермальные аллергены, пыльца аллергенных растений, пищевые), а также физическая нагрузка.
Характеристики, позволяющие заподозрить бронхиальную астму у детей в возрасте 5 лет и младше
|
Признак
|
Характеристики, позволяющие заподозрить БА
|
|
Кашель
|
Рецидивирующий или стойкий непродуктивный кашель, который может обостряться в ночное время или сопровождаться свистящими хрипами или затруднением дыхания.
Кашель возникает при физической нагрузке, смехе, плаче, у сенсибилизированных больных при контакте с аллергенами (кошка, собака), в сезон цветения аллергенных растений, при вирусной инфекции у больных БА или воздействии табачного дыма в отсутствие явной респираторной инфекции |
|
Свистящие хрипы
|
Рецидивирующие свистящие хрипы, в том числе возникающие во сне или при воздействии таких провоцирующих факторов, как физическая активность, смех, плач или воздействие табачного дыма или загрязненного воздуха
|
|
Затрудненное или тяжелое дыхание или одышка
|
Возникает при физической нагрузке, смехе или плаче и при воздействии других отмеченных выше триггеров
|
|
Снижение активности
|
Ребенок бегает, играет и смеется с меньшей интенсивностью, чем другие дети; быстрее устает при прогулке (просится на руки)
|
|
Личный или семейный анамнез
|
Другие аллергические заболевания (атопический дерматит или аллергический ринит)
Бронхиальная астма у ближайших родственников |
|
Пробное лечение низкими дозами ИГКС и КДБА
по потребности |
Клиническое улучшение в течение 2–3 месяцев терапии, направленной на контроль заболевания, и ухудшение состояния после ее прекращения
|
Дети 6–12 лет
В данной возрастной группе вирусиндуцированная астма остается частой формой заболевания.
Подростки старше 12 лет
БА может дебютировать в подростковом возрасте. При этом частым проявлением у них является бронхоспазм, вызванный физической нагрузкой.
Следует также учитывать, что пациенты нередко курят, а страх удушья формирует тревожность, чувство отверженности, подкрепляемые переживаниями своего отличия от сверстников.
НАЧАЛЬНАЯ СТРУКТУРИРОВАННАЯ КЛИНИЧЕСКАЯ ОЦЕНКА [1]
Прогностическая ценность отдельных симптомов или признаков невелика, поэтому следует провести структурированную клиническую оценку данных физикального обследования и анамнеза.
Показатели первоначальной структурированной клинической оценке включают:
Эпизодические симптомы
В данной возрастной группе вирусиндуцированная астма остается частой формой заболевания.
Подростки старше 12 лет
БА может дебютировать в подростковом возрасте. При этом частым проявлением у них является бронхоспазм, вызванный физической нагрузкой.
Следует также учитывать, что пациенты нередко курят, а страх удушья формирует тревожность, чувство отверженности, подкрепляемые переживаниями своего отличия от сверстников.
НАЧАЛЬНАЯ СТРУКТУРИРОВАННАЯ КЛИНИЧЕСКАЯ ОЦЕНКА [1]
Прогностическая ценность отдельных симптомов или признаков невелика, поэтому следует провести структурированную клиническую оценку данных физикального обследования и анамнеза.
Показатели первоначальной структурированной клинической оценке включают:
Эпизодические симптомы
-
Наличие более одного из таких симптомов, как свистящее дыхание, одышка, чувство стеснения в груди и кашель, возникающих приступообразно, с периодами полного отсутствия (или минимальной выраженности) между приступами. Кашель как изолированный симптом при этом не учитывается. Например:
- подтвержденные документально острые приступы бронхиальной обструкции, вызванные вирусной инфекцией или воздействием аллергена, с симптоматическим и объективным улучшением со временем и/или на фоне назначенного лечения
- астматические приступы, спровоцированные вирусной инфекцией или воздействием аллергенов, усиливаются физическими упражнениями и холодным воздухом, а также эмоциями или смехом
- Подтверждение обструктивного характера приступов одышки более низкими показателями ОФВ₁ или ПСВ по сравнению с бессимптомными периодами в анамнезе
Характер хрипов, определенных при аускультации
- Исключение стридора или дистанционных хрипов при обструктивном бронхите.
- Исключение астмы при исчезновении аускультативной симптоматики при наличии других объективных симптомов.
Динамика суточной симптоматики
- Признаки астмы усиливаются ночью или ранним утром.
Атопический анамнез
- Атопический анамнез ребенка (например, экзема или аллергический ринит) или семейный анамнез астмы и/или атопических болезней, подтвержденный повышениями аллерген-специфического IgE, положительными кожными прик-тестами на аэроаллергены или эозинофилией.
Отсутствие данных, позволяющих предположить альтернативный диагноз (ХОБЛ, дисфункцию дыхания, ожирение).
Первоначальная оценка
|
С
|
Рекомендуется собрать структурированный анамнез у детей с подозрением на БА[5-8], в частности:
|
|
С
|
НЕ РЕКОМЕНДУЕТСЯ учитывать симптомы без результатов объективного теста для диагностики астмы [5-8]
НЕ РЕКОМЕНДУЕТСЯ учитывать только атопические расстройства в анамнезе |
|
D
|
Рекомендуется предположить наличие астмы на основании следующих результатов структурированной клинической оценки:
|
|
С
|
Рекомендуется провести аускультацию всех детей с подозрением на астму для определения экспираторных хрипов и других причин нарушения дыхания. Следует заметить, что нормальные результаты обследования не исключают наличие астмы у ребенка [5-8]
|
Дети младше 6 лет
Диагностика БА у детей младше 6 лет затруднена из-за [3-4]:
- невозможности проведения исследования функции легких и
- совпадение симптомов ОРВИ (обструктивного бронхита) с симптомами астмы.
|
С
|
Диагноз у детей младше 6 лет основывается на [5-8]:
1. анамнезе (повторяющиеся приступы хрипов, кашля, затрудненного дыхания и чувства стеснения в груди); 2. физикальном обследовании, подтверждающим наличие обструкции дыхательных путей (например, свистящее дыхание), которая уменьшается или исчезает после применении бета-агонистов короткого действия (КДБА); 3. отсутствии альтернативного заболевания. |
Свистящие хрипы являются наиболее специфическим признаком астмы.
- свистящие хрипы - это пронзительный свистящий звук, обычно слышимый на выдохе, который
- требует подтверждения данными физикального обследования (аускультацией), поскольку свистящее дыхание может сопровождать состояния, не связанные с астмой.
Дети старше 6 лет
|
С
|
Диагноз у детей 6-18 лет основывается на:
1. клиническом анамнезе (повторяющиеся эпизоды хрипов, кашля, затрудненного дыхания и чувства стеснения в груди); 2. документированных доказательствах обратимой обструкции или гиперреактивности бронхов при определении функции легких; 3. если определение функции легких недоступно, в качестве возможного маркера обратимой обструкции дыхательных путей можно использовать наличие хрипов или одышки, которые исчезают при использовании КДБА. В то же время определение функции легких следует провести при первой же возможности. |
|
D (˃12 лет; ˂5 лет)
В (5-12 лет)
|
При каждом обследовании рассчитывайте риск будущих приступов астмы путем сбора анамнеза о предыдущих приступах, объективной оценки текущего контроля астмы и анализа использования лекарственных средств [5-8]
|
|
С
|
Диагноз астмы у детей основан на определении характерных респираторных симптомов и результатах тестов ФВД при отсутствии альтернативных объяснений полученным результатам [5-8]
|
Оценка вероятности БА [1]
|
Уровень высокого риска
|
Фактор риска
|
|
Значительно повышенный риск
|
Анамнез предыдущих приступов астмы
Постоянные симптомы астмы |
|
Умеренно повышенный риск
|
Недостаточно оптимальный режим приема лекарств (соотношение количества препаратов/рецептов для контроля астмы к общему количеству препаратов/рецептов для лечения астмы <0,5153)
Сочетанное (коморбидное) атопическое/аллергическое заболевание Семья с низким уровнем дохода Дефицит витамина D |
|
Незначительно повышенный риск
|
Более молодой возраст (до 3-х лет)
Пассивное курение Ожирение Низкий уровень образования родителей |
|
Нет повышенного риска
|
Пол
Городские жители |
|
Неясно (доказательства неоднозначны)
|
Снижение функции легких
Повышение FeNO при плановых обследованиях Положительные кожные аллерготесты Аллергоанамнез |
Высокая вероятность [1]
Дети с типичной клинической картиной, включающей повторяющиеся эпизоды симптомов (приступы), хрипы при аускультации, с положительным атопическим анамнезом и данными об обратимой обструкции в прошлом (без каких-либо признаков, позволяющих предположить альтернативный диагноз), имеют высокую вероятность БА.
При высокой вероятности астмы:
- зарегистрируйте пациента как вероятного больного БА и начните контролируемый курс лечения ингаляционными кортикостероидами (как правило, в течение шести недель);
- оцените состояние пациента с помощью валидированного опросника симптомов, подтвержденных тестами функции легких (ОФВ1 при посещении клиники или пикфлоуметрией в домашних условиях для регистрации наличия/отсутствия симптомов).
- подтвердите диагноз БА при хорошем симптоматическом и объективном ответе на лечение астмы и обоснуйте;
- если реакция слабая или неоднозначная, проверьте правильность техники проведения и режима использования ингаляций, в случае отсутствия погрешностей назначьте дополнительные обследования и рассмотрите альтернативные диагнозы.
Низкая вероятность [1]
Дети, у которых не отмечается ни одного из положительных признаков первоначальной структурированной клинической оценке или у которых наблюдаются симптомы, указывающие на альтернативный диагноз, имеют низкую вероятность БА.
- Если вероятность БА низка и/или более вероятен альтернативный диагноз, подтвердите альтернативный диагноз; пересмотрите диагноз астмы, если клиническая картина изменится или альтернативный диагноз не подтвердился.
- В случае пересмотра диагноза БА проведите или направьте на дополнительные исследования для уточнения диагноза астмы.
Промежуточная вероятность [1]
Дети, которые имеют некоторые типичные признаки БА при первоначальной структурированной клинической оценке или которые плохо реагируют на начало лечения под наблюдением врача имеют промежуточную вероятность развития БА.
|
D
|
Спирометрия с положительной пробой с КДБА является предпочтительным первоначальным тестом для исследования промежуточной вероятности БА у детей [1-4]
|
|
D
|
У детей с промежуточной вероятностью БА и обструкцией дыхательных путей, выявленных с помощью спирометрии, рекомендуется провести тест с КДБА и/или начать лечение под контролем показателей функции легких и данных объективного исследования [1-4]
|
|
D
|
У детей с промежуточной вероятностью астмы и нормальными результатами спирометрии рекомендуется провести тест с КДБА и/или измерение FeNO для выявления эозинофильного воспаления [1-4]
|
|
D
|
Детям старше 1 года с промежуточной вероятностью астмы, которым невозможно провести спирометрию, рекомендуется [1-4]:
|
Клинические признаки, увеличивающие и уменьшающие вероятность наличия БА [1]
|
Клинические признаки, повышающие вероятность наличия БА
|
Клинические признаки, уменьшающие вероятность наличия БА
|
|
Наличие более одного из следующих симптомов - хрипы, удушье, чувство заложенности в грудной клетке и кашель, особенно в случаях: ухудшения симптомов ночью и рано утром; возникновения симптомов при физической нагрузке, воздействии аллергенов и холодного воздуха; возникновения симптомов после приема ацетилсалициловой кислоты или бета-адреноблокаторов;
Наличие атопических заболеваний в анамнезе; Наличие БА и/или атопических заболеваний у родственников; Распространенные сухие свистящие хрипы при выслушивании (аускультации) грудной клетки; Низкие показатели ПСВ или ОФВ (ретроспективно или в серии исследований), необъяснимые другими причинами; Эозинофилия периферической крови, необъяснимая другими причинами. |
Выраженные головокружения, потемнение в глазах, парестезии;
Хронический продуктивный кашель при отсутствии свистящих хрипов или удушья; Постоянно нормальные результаты обследования грудной клетки при наличии симптоматики; Изменение голоса (осиплость); Возникновение симптомов исключительно на фоне простудных заболеваний; Заболевания сердца; Нормальные показатели ПСВ или спирометрии при наличии клинических проявлений |
Вероятность БА у детей младше 5 лет [1]
|
Признак
|
Характеристики, позволяющие заподозрить БА
|
|
Кашель
|
Рецидивирующий или стойкий непродуктивный кашель, который может обостряться в ночное время или сопровождаться свистящими хрипами или затруднением дыхания.
Кашель возникает при физической нагрузке, смехе, плаче, у сенсибилизированных больных при контакте с аллергенами (кошка, собака), в сезон цветения аллергенных растений, при вирусной инфекции у больных БА или воздействии табачного дыма в отсутствие явной респираторной инфекции |
|
Свистящие хрипы
|
Рецидивирующие свистящие хрипы, в том числе возникающие во сне или при воздействии таких провоцирующих факторов, как физическая активность, смех, плач или воздействие табачного дыма или загрязненного воздуха
|
|
Затрудненное или тяжелое дыхание или одышка
|
Возникает при физической нагрузке, смехе или плаче и при воздействии других отмеченных выше триггеров
|
|
Снижение активности
|
Ребенок бегает, играет и смеется с меньшей интенсивностью, чем другие дети; быстрее устает при прогулке (просится на руки)
|
|
Личный или семейный анамнез
|
Другие аллергические заболевания (атопический дерматит или аллергический ринит)
Бронхиальная астма у ближайших родственников |
|
Пробное лечение низкими дозами ИГКС и КДБА
по потребности |
Клиническое улучшение в течение 2–3 мес терапии, направленной на контроль заболевания, и ухудшение состояния после ее прекращения
|
Шкала риска астмы у детей (PARS - Pediatric Asthma Risk Score) — это первая система непрерывной оценки для прогнозирования риска развития астмы у детей младшего возраста.
Шкала оценки риска развития бронхиальной астмы у детей (PARS) [1]
|
|
Нет
|
Да
|
Кол-во баллов
|
|
Диагностировалась ли астма у кого-нибудь из родителей ребенка?
|
0
|
2
|
|
|
Была ли у ребенка диагностирована экзема (атопический дерматит) в возрасте от рождения до 3 лет?
|
0
|
2
|
|
|
Ранняя одышка. Отмечались у ребенка ли дистанционные хрипы на в возрасте в возрасте до 3 лет?
|
0
|
3
|
|
|
Хрипы в здоровом состоянии.
Отмечались ли дистанционные хрипы при отсутствии признаков респираторной инфекции? |
0
|
3
|
|
|
Наличие аллергии. Проводилось ли ребенку кожное тестирование на аллергию (прик-тесты)?
|
0
|
2
|
|
|
Общий итог
|
|
|
|
Интерпретация шкалы по оценке риска развития БА [1]
|
Баллы
|
Риск астмы
|
Интерпретация
|
|
|
0
|
3%
|
Низкий риск
|
Риск развития БА к 7 годам при наличии баллов от 0 до 4 (1 из 9)
|
|
2
|
6%
|
||
|
3
|
8%
|
||
|
4
|
11%
|
||
|
5
|
15%
|
Промежуточный риск
|
Риск развития БА к 7 годам при наличии баллов от 5 (1 из 7) до 8 (1 из 3-х)
|
|
6
|
19%
|
||
|
7
|
25%
|
||
|
8
|
32%
|
||
|
9
|
40%
|
Высокий риск
|
Риск развития БА к 7 годам при наличии баллов от 9 (2 из 5) до 14 (4 из 5)
|
|
10
|
49%
|
||
|
11
|
58%
|
||
|
12
|
66%
|
||
|
14
|
79%
|
||
ФИЗИКАЛЬНОЕ ОБСЛЕДОВАНИЕ [1]
|
Характерные изменения при объективном осмотре:
|
Примечание: *В межприступный период без клинических симптомов болезни аускультативно могут прослушиваться сухие свистящие хрипы при форсированном дыхании, которые свидетельствуют о наличии явлений скрытого бронхоспазма.
**Если диагноз неясен, дайте одну дозу быстродействующего бронхолитического средства (сальбутамол). Ребенку с тяжелой БА может потребоваться быстрое последовательное введение нескольких доз бронхолитического средства, прежде чем станет заметен его эффект [3].
ИНСТРУМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ ИЛИ ТЕСТЫ [1]
1. Пульсоксиметрия (SpO2)
Точные измерения насыщения кислородом (SpO2) необходимы для оценки состояния всех детей с дистанционными хрипами.
Пульсоксиметры должны быть доступны для использования всеми медицинскими работниками, оценивающими острую БА на амбулаторном и стационарном уровнях.
1. Пульсоксиметрия (SpO2)
Точные измерения насыщения кислородом (SpO2) необходимы для оценки состояния всех детей с дистанционными хрипами.
Пульсоксиметры должны быть доступны для использования всеми медицинскими работниками, оценивающими острую БА на амбулаторном и стационарном уровнях.
|
В
|
Рекомендуется госпитализировать детей с SpO2 <92% после первоначального лечения бронхолитиками [SIGN, 2019]
|
2. Спирометрия у детей в возрасте ≥ 6 лет
|
С
|
Рекомендуется считать специфичным для диагностики БА объем форсированного выдоха за 1 секунду (ОФВ1)/форсированная жизненная емкость легких (ФЖЕЛ) < 70% с 12%-ным улучшением ОФВ1 после КДБА [5-8]
|
ПРИМЕЧАНИЕ. Отрицательные результаты спирометрии не обязательно исключают диагноз БА, особенно если у ребенка нет симптомов или его состояние хорошо контролируется противоастматическими препаратами.
Особенности спирометрии:
- Наиболее целесообразно проводить этот тест, когда у пациентов есть симптомы БА.
- Выполнение спирометрии является важной частью диагностического процесса, хотя у 30% пациентов с диагноз астмы не подтверждается при проведении тестирования функции легких.
- Детям младше 6 лет часто не могут надежно провести спирометрию.
|
С
|
Рекомендуется использовать спирометрию в качестве начального исследования для выявления и оценки степени тяжести обструкции дыхательных путей у всех пациентов с подозрением на БА
|
Исследование функции внешнего дыхания (спирометрия) для детей старше 5 лет (см. приложение 2).
Комментарии: Повторные исследования функции легких часто более информативны, чем единичное обследование. Нормальные показатели спирометрии (или пикфлоуметрии) не исключают диагноза БА.
|
D
|
Рекомендуется проводить качественную спирометрию с использованием нижней границы нормы, чтобы продемонстрировать обструкцию дыхательных путей, обеспечить исходный уровень для оценки реакции на начало лечения и исключения альтернативных диагнозов.
|
3. Тесты бронхиальной гиперреактивности
- Если спирометрия в норме, а подозрение на БА сохраняется, можно провести провокацию физической нагрузкой или бронходилатационый тест, особенно если ребенок не реагирует на стандартную терапию астмы.
- Указанные тесты целесообразны для исключения диагноза у пациента с симптомами БА.
|
С
|
Рекомендуется выполнить бронходилатационный тест всем пациентам с БА для определения степени обратимости обструкции под влиянием бронхорасширяющих препаратов.
|
|
Рекомендуется оценивать обратимость бронхиальной обструкции у детей с БА старше 5-6 лет в тесте с бронхолитиком (2 дозы = 200 мкг сальбутамола) по приросту ОФВ1 более 12% и при этом абсолютный прирост составляет 200 мл и более
|
Показания для проведения теста:
- Атипичные симптомы БА или любое другое заболевание с бронхиальной обструкцией;
- Плохой контроль над БА (плохая функция легких, стойкие симптомы астмы) или тяжелые обострения БА (≥ 1 курса системных стероидов в год), несмотря на достаточные дозы ингаляционных кортикостероидов (при правильной технике и соблюдении режима лечения)
- Пациенту и/или лицам, контролирующим его лечение, требуется детальная оценка и управление потенциальными триггерами окружающей среды.
1. Пикфлоуметрия
Пикфлоуметрия – это метод функциональной диагностики, предназначенный для оценки проходимости бронхиальных путей, который позволяет измерять только один параметр – пиковую скорость выдоха (ПСВ).
|
С
|
НЕ РЕКОМЕНДУЕТСЯ для диагностики бронхиальной астмы у детей
|
|
D
|
Рекомендуется использовать пикфлоуметр для оценки пиковой скорости выдоха (ПСВ) у пациентов с клиническими симптомами БА, у которых нет возможности провести спирометрию или дополнительные диагностические тесты и рекомендуется выполнять в течение по меньшей мере 2-х недель для подтверждения вариабельности скорости воздушного потока
|
Диагноз БА при выявлении повышенной средней суточной вариабельности ПСВ (>13% у детей) у пациентов с типичными респираторными симптомами подтверждает диагноз БА.
Результаты мониторинга ПСВ с применением исследований неспровоцированных дыхательных объемов и потоков с использованием пикфлоуметра должны интерпретироваться с учетом клинической ситуации, поскольку вариабельность ПСВ может быть повышена при заболеваниях, с которыми чаще всего проводится дифференциальная диагностика БА.
Пикфлоуметры идеально подходят для использования пациентами старше 5 лет в домашних условиях. В целях диагностики наиболее информативен ежедневный мониторинг ПСВ в течение 2–3 недель. Следует помнить, что пикфлоуметрия является менее точным методом диагностики по сравнению со спирометрией.
Результаты мониторинга ПСВ с применением исследований неспровоцированных дыхательных объемов и потоков с использованием пикфлоуметра должны интерпретироваться с учетом клинической ситуации, поскольку вариабельность ПСВ может быть повышена при заболеваниях, с которыми чаще всего проводится дифференциальная диагностика БА.
Пикфлоуметры идеально подходят для использования пациентами старше 5 лет в домашних условиях. В целях диагностики наиболее информативен ежедневный мониторинг ПСВ в течение 2–3 недель. Следует помнить, что пикфлоуметрия является менее точным методом диагностики по сравнению со спирометрией.
2. Рентген грудной клетки
|
С
|
Рекомендуется для дифференциальной диагностики (исключение аспирации инородного тела, объемных образований легких, поражения плевры, врожденных пороков развития, бронхоэктазов и т.д.)
|
|
С
|
Рекомендуется сравнить результаты диагностических тестов во время периодов обострения и ремиссии, чтобы выявить изменения во времени
|
|
D
|
Рекомендуется проводить рентгенографию органов грудной клетки в прямой проекции пациентам с обострением БА для исключения медиастинальной эмфиземы или пневмоторакса, при подозрении на пневмонию, клинических признаках угрожающего жизни обострения, необходимости механической вентиляции легких
|
Аллергологическое обследование [3]:
|
Дополнительные методы обследования [3]:
|
Фибробронхоскопия (исключение аспирации инородного тела, врожденных пороков развития и т.д.).
|
|
Общий (клинический) анализ крови. В анализах крови при БА характерных изменений нет. Часто выявляется эозинофилия, однако ее нельзя считать патогномоничным симптомом.
|
|
В мокроте у детей с БА могут выявляться эозинофилы, спирали Куршмана, кристаллы Шарко-Лейдена.
|
|
Компьютерная бронхофонография (может быть использована у детей младше 5 лет).
|
|
Уровень оксида азота в выдыхаемом воздухе (FеNO) - для обнаружения аллергического воспаления дыхательных путей. Показатель FеNO повышен при эозинофильной БА и ассоциируется с хорошим краткосрочным ответом на ИГКС. Нормальные значения FеNO, особенно в момент, когда симптоматика отсутствует, не исключают диагноз БА.
|
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ [1]
Диагностические показания для направления
На любом этапе диагностического алгоритма может потребоваться направление на дополнительные исследования и/или консультация специалиста.
Направьте детей на дополнительное обследование и консультацию специалиста, если:
Диагностические показания для направления
На любом этапе диагностического алгоритма может потребоваться направление на дополнительные исследования и/или консультация специалиста.
Направьте детей на дополнительное обследование и консультацию специалиста, если:
- диагноз неясен;
- плохой ответ на контролируемое начало лечения БА;
- тяжелый/опасный для жизни приступ БА.
Индикаторы других заболеваний:
- Необъяснимые клинические признаки (например, очаговые признаки, аномальный голос или «кряхтение», дисфагия, инспираторный стридор);
- Симптомы присутствуют с рождения или перинатальные проблемы с легкими;
- Тяжелая инфекция верхних дыхательных путей;
- Постоянный продуктивный кашель;
- Семейный анамнез необычного бронхолегочного заболевания.
|
С
|
НЕ РЕКОМЕНДУЮТСЯ следующие диагностические тесты на БА:
|
|
С
|
Рекомендуется использовать кожные прик-тесты на аэроаллергены или тесты на специфические IgE для выявления триггеров после постановки официального диагноза БА
|
|
С
|
Рекомендуется определить уровень калия в крови при длительном использовании сальбутамола и др. адреномиметиков (риск гипокалиемии!)
|
1. Определение фракционного выдыхаемого оксид азота (FeNO) [1]
На сегодняшний день изучены различные аспекты клинического использования определения уровня оксида азота (FeNO) в выдыхаемом воздухе:
На сегодняшний день изучены различные аспекты клинического использования определения уровня оксида азота (FeNO) в выдыхаемом воздухе:
- Выявление повышенного уровня выдыхаемого оксида азота рекомендуется в качестве скринингового теста при диагностике бронхиальной астмы, в том числе, при эпидемиологических исследованиях.
- Нормализация уровня выдыхаемого оксида азота в процессе лечения используется для оценки эффективности базисной противовоспалительной терапии бронхиальной астмы и индивидуальной оптимизации дозировок используемых препаратов.
- Стойкое повышение уровня выдыхаемого оксида азота может свидетельствовать о низком комплайнсе (приверженности) пациента с бронхиальной астмой вследствие несоблюдения режима базисной терапии, погрешностей ингаляционной техники или неадекватном объеме базисного противовоспалительного лечения
-
Повышение уровня выдыхаемого оксида азота помогает спрогнозировать обострение бронхиальной астмы до появления клинических симптомов и характерных функциональных нарушений.
Определение содержания FeNO в составе выдыхаемого газа производится при помощи аппаратов – газоанализаторов. Пациент выдыхает из легких воздух в специальный, портативный прибор — газоанализатор.
|
С
|
НЕ РЕКОМЕНДУЕТСЯ рутинно использовать FeNO для мониторинга контроля астмы [5-8]
|
Дифференциальный диагноз
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ
|
Исключить другие распространенные и редкие нозологии при наличии следующих признаков:
|
ЗАБОЛЕВАНИЯ, С КОТОРЫМИ НЕОБХОДИМО ДИФФЕРЕНЦИРОВАТЬ БРОНХИАЛЬНУЮ АСТМУ [4]
|
При отсутствии бронхиальной обструкции
|
При наличии бронхиальной обструкции
|
|
|
ФОРМУЛИРОВКА ДИАГНОЗА БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ [1-4]
В диагнозе должны быть указаны:
- этиология (если установлена);
- степень тяжести;
- уровень контроля;
- сопутствующие заболевания, которые могут оказать влияние на течение БА;
- при наличии – обострение с указанием его степени тяжести.
Примеры формулировки диагноза:
|
Диагноз: J45.0 Бронхиальная астма, атопическая форма, легкое персистирующее течение, впервые выявленная, неконтролируемая, период обострение
|
|
Диагноз: J45.0 Бронхиальная астма, атопическая форма, легкое персистирующее течение, частично-контролируемая, период обострение.
Сопутствующий диагноз: Аллергический ринит, интермитирующее легкое течение, период обострение. Сенсибилизация (пыльце деревьев).
|
|
Диагноз: J45.0 Бронхиальная астма, атопическая форма, средней степени персистирующее течение, неконтролируемая, период обострение.
Сопутствующий диагноз: Аллергический ринит, персистирующее средней степени течение, период обострение. Сенсибилизация бытовая (домашняя пыль), пыльцевая (луговые: ежа, тимофеевка, райграсс; сорные: полынь горькая, полынь обыкновенная, амброзия).
|
|
Диагноз: J45.0 Бронхиальная астма, атопическая форма, тяжелое персистирующее течение, неконтролируемая, период тяжелого обострения.
Сопутствующий диагноз: Аллергический ринит, персистирующее, средней степени течение, период обострение. Сенсибилизация бытовая (домашняя пыль), пыльцевая (луговые: ежа, тимофеевка, райграсс; сорные: полынь горькая, полынь обыкновенная, амброзия). Атопический дерматит, эриматозно-скамозной формы, средне-тяжелой степени, пищевой сенсибилизации
|
|
Диагноз: J45.0 Бронхиальная астма, тяжелая персистирующая, неконтролируемая, жизнеугрожающая.
Сопутствующий диагноз: Аллергический ринит, персистирующее тяжелой степени течение, период обострение. Сенсибилизация бытовая (домашняя пыль), медикаментозная аллергия (антибиотики цефтриаксонового ряда).
|
Лечение
ЛЕЧЕНИЕ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ [1-4]
Целью лечения БА является достижение и длительное поддержание контроля над клиническими проявлениями заболевания.
4 компонента лечения БА:
- Компонент 1. Сотрудничество между пациентом (семьей пациента) и медицинским работником.
- Компонент 2. Выявление факторов риска БА и уменьшение их воздействия.
- Компонент 3. Оценка уровня контроля, терапия и мониторирование БА.
- Компонент 4. Лечение обострений БА.
КОМПОНЕНТ 1
РАЗВИТИЕ СОТРУДНИЧЕСТВА МЕЖДУ ПАЦИЕНТОМ И МЕДИЦИНСКИМ РАБОТНИКОМ
|
D
|
Рекомендуется сотрудничать с пациентом, родителями или лицами, ухаживающими за ребенком и медицинскими работниками для обсуждения и согласования цели лечения, разработки индивидуального плана лечения и оценки результатов лечения (не реже 2 раз в год)
|
Внедрение образовательных программ, включающих управляемое ведение БА с участием самих пациентов и их родителей, призвано улучшить исходы заболевания (Kneale et al, Thorax 2019) [4]:
- Снижение посещений отделений неотложной помощи.
- Меньше госпитализаций.
- Меньше дней с ограниченной активностью.
|
D
|
Рекомендуется обучить пациента/родителей/лиц, ухаживающих за ребенком правилам как:
|
|
С
|
Рекомендуется включать в программу обучения методы физической реабилитации всех пациентов с БА
|
Комментарии: Программа обучения пациентов с БА должна включать предоставление информации о заболевании, составление индивидуального плана лечения для пациента, и обучение технике управляемого самоведения.
Физическая реабилитация улучшает сердечно-легочную функцию. В результате проведения тренировки при физической нагрузке увеличивается максимальное потребление кислорода и увеличивается максимальная вентиляция легких. По имеющимся наблюдениям применение тренировки с аэробной нагрузкой, плавание, тренировка инспираторной мускулатуры с пороговой дозированной нагрузкой улучшают течение БА.
КОМПОНЕНТ 2
ВЫЯВЛЕНИЕ ФАКТОРОВ РИСКА БРОНХИАЛЬНОЙ АСТМЫ И УМЕНЬШЕНИЕ ИХ ВОЗДЕЙСТВИЯ [1]
Для улучшения контроля над БА и снижения потребности в лекарственных препаратах пациенты должны принимать меры по ограничению контакта с факторами риска астмы.
У значительной части пациентов существует представление о том, что многочисленные экологические, диетические и иные факторы могут быть триггерами БА и исключение этих факторов может улучшить течение заболевания и уменьшить объем медикаментозной терапии.
В настоящее время существуют лишь небольшое количество мероприятий, которые можно рекомендовать для профилактики БА, так как в развитии этого заболевания участвуют сложные и до конца не выясненные механизмы. Доказательств того, что нефармакологическими методами возможно влиять на течение БА недостаточно и требуется проведение широкомасштабных клинических исследований.
Уменьшение воздействия на пациентов некоторых категорий факторов/триггеров позволяет улучшить контроль над БА и снизить потребность в лекарствах.
|
Есть ли у пациента имеются какие-либо из следующих факторов риска:
|
|
D
|
Рекомендуется использовать стратегию по устранению поддающихся изменению факторов риска (например, исключение пассивного курения, устранение воздействия аллергенов и т. д.)
|
Рекомендации по профилактике БА приведены в Приложении 3.
Вакцинация
Вакцинацию против пневмококковой инфекции (ПИ) рекомендуется проводить согласно национальному календарю прививок.
|
С
|
Рекомендуется проведение вакцинации против ПИ пациентам с БА, сопутствующим хроническим бронхитом, эмфиземой легких, частых рецидивах респираторной инфекции, длительным приемом ингаляционных и системных ГКС
|
КОМПОНЕНТ 3
ОЦЕНКА УРОВНЯ КОНТРОЛЯ БРОНХИАЛЬНОЙ АСТМЫ, ТЕРАПИЯ И МОНИТОРИРОВАНИЕ БРОНХИАЛЬНОЙ АСТМЫ [1]
Уровень контроля БА (табл. 4) оценивается с целью определения эффективности терапии и коррекции объема терапии.
Оценить уровень контроля БА позволяет тест по контролю над астмой (приложение 4).
Оценка контроля над астмой
|
С
|
Рекомендуется проводить оценку контроля симптомов БА и факторов риска приступов БА во время постановки диагноза, при создании/изменении плана лечения и мониторинге результатов лечения [5-8]
|
|
D
|
Рекомендуется заполнять чек-лист по контролю симптомов астмы [5-8]
|
Чек-лист по контролю симптомов БА [5-8]
|
Наличие симптомов последние 4 недели
|
Да
(1 балл) |
Нет
(0 баллов) |
|
Симптомы БА больше, чем 2 раза в неделю
|
|
|
|
Наличие ночных симптомов БА
|
|
|
|
Симптомы требуют бронходилятации (больше, чем 2 раза в неделю)
|
|
|
|
Ограничение активности
|
|
|
|
МСВ1 или скорость выдоха ˂80%
|
|
|
|
Общий балл
|
|
|
Интерпретация полученных баллов:
0 баллов = хорошо контролируемые симптомы астмы
1-2 балла = частично контролируемые симптомы астмы
≥ 3 баллов = неконтролируемые симптомы астмы
ЛЕЧЕНИЕ БРОНХИАЛЬНОЙ АСТМЫ [1]
Аэрозольные системы для доставки препаратов:
- дозированные аэрозольные ингаляторы (ДАИ), бесфреоновые ДАИ, ДАИ, активируемые вдохом;
- комбинация дозированных ингаляторов со спейсерами;
- дозированные порошковые ингаляторы (ДПИ): однодозовые капсульные, мультидозовые резервуарные, мультидозовые блистреные;
- небулайзеры: струйные или компрессорные (конвекционный, активируемые вдохом, синхронизованные с дыханием), ультразвуковые;
- новые виды ингаляционных систем: жидкостной дозированный ингалятор, имеет компактный дизайн и снабжен цифровым счетчиком доз.
Прежде чем начинать новую лекарственную терапию, практикующие врачи должны проверить приверженность к существующим методам лечения, проверить технику ингаляции и использование спейсера, а также устранить триггерные факторы.
Препараты первой помощи при приступе БА
Детям с диагнозом БА следует назначить бронходилятаторы короткого действия для купирования симптомов. Для пациентов с нечастыми кратковременными хрипами эпизодическое использование броходилататоров короткого действия может быть единственным необходимым лечением.
Бронходиляторы короткого действия:
- Ингаляционные короткодействующие ингаляционные β2-агонисты (КДБА);
- Блокаторы М-холинорецепторов (ингаляционный ипратропия бромид);
- Метилксантины (ингибиторы фосфодиэстеразы) – аминофиллин, теофиллин®.
Короткодействующие ингаляционные β2-агонисты действуют быстрее и/или с меньшим количеством побочных эффектов, чем альтернативные препараты.
Хороший контроль астмы связан с минимальной потребностью или отсутствием потребности в КДБА. КДБА следует использовать только по мере необходимости для облегчения симптомов.
|
А
|
Рекомендуется назначать бронходилятаторы короткого действия для купирования симптомов по мере необходимости [5-8]
|
|
А
|
Рекомендуется провести оценку состояния БА при назначении более одного бронходилятаторов короткого действия в месяц и неудовлетворительном контроле [5-8]
|
Ингаляционные β2-агонисты:
- Короткого действия (КДБА) – сальбутамол, фенотерол, тербуталин;
-
Длительного действия (ДДБА) – сальметерол, формотерол, индекатерол (не рекомендуется в качестве монотерапии, только в комбинации с ИГКС).
|
В
|
Рекомендуется назначать детям в возрасте от 5 до 12 лет ДДБА или АЛТР в качестве начальной дополнительной терапии и назначать ДДБА только тем пациентам, которые уже принимают ингаляционные кортикостероиды (ИГКС), и следует продолжать принимать ИГКС [SIGN, 2021]
|
Меры предосторожности
Среди побочных эффектов адреномиметиков при бесконтрольном и частом применении следует также отметить:
Среди побочных эффектов адреномиметиков при бесконтрольном и частом применении следует также отметить:
- синдром «рикошета» - усиление бронхоспазма вследствие β2- блокирующего действия метаболитов адреномиметиков;
- синдром «замыкания легких» - обусловленный отеком слизистой бронхов в результате повышения проницаемости капилляров из-за излишней стимуляции β2-рецепторов и дилатации сосудов бронхов.
Следует отметить, что в развитии толерантности к адреномиметикам или усиления бронхоспазма на фоне их приема, кроме указанных синдромов может иметь значение снижение ответа β2-рецепторов в результате отсутствия контроля лечения, а также феномена «холодного аэрозоля», высокой скорости ингаляции препарата, действия растворителей.
Регулярная профилактическая терапия
Лекарства оцениваются по их способности улучшать симптомы, улучшать функции легких и предотвращать приступы астмы при приемлемом профиле безопасности.
Ингаляционные глюкокортикостероиды (ИГКС)
К ним относятся следующие препараты:
- беклометазона дипропионат;
- флутиказон;
- будесонид;
- флунизолид;
- триамцинолон;
- циклесонид.
|
В
|
Рекомендуется назначение ИГКС в качестве профилактического препарата для достижения целей лечения [5-8]
|
|
В
|
Рекомендуется назначение ИГКС при наличии следующих признаков для детей в возрасте до 5 лет и детей 5-12 лет [5-8]:
|
|
В
|
Рекомендуется назначение ИГКС, т.к. являются препаратами первого выбора для профилактики [5-8]
|
У многих неатопических детей в возрасте до 5 лет с повторяющимися эпизодами хрипов, вызванных вирусами (ОРВИ), хрипы не переходят в хроническую атопическую астму. Большинству из них не требуется лечения ИГКС.
Начальная доза ИГКС
Рекомендуется подбирать дозу ИГКС до самой низкой, при которой сохраняется эффективный контроль над астмой (не менее 1 месяца).
Начинать лечение пациентов с дозы ИГКС, соответствующей тяжести заболевания. Разумной начальной дозой ИГКС у детей должна быть низкая доза (Приложение 6).
При легкой и умеренной астме начало приема высоких доз ИГКС и их постепенное снижение не приносит пользы.
Частота назначения ИГКС
|
А
|
Рекомендуется назначение ИГКС первоначально 2 раза в день
|
Циклесонид только назначается один раз в день.
|
В
|
Рекомендуется назначение ИГКС 1 раз в день в той же общей суточной дозе при хорошем контроле БА
|
Безопасность применения ИГКС [SIGN, 2021]
|
D
|
Рекомендуется проводить мониторинг роста у детей с БА (использовать таблицы физического развития рост/вес) ежегодно
|
|
С
|
Рекомендуется использовать самую низкую дозу ИГКС для поддержания контроля БА
|
|
D
|
Рекомендуется для детей, получающих лечение средними или высокими дозами ИГКС:
|
|
D
|
Рекомендуется проверить биохимические показатели и уровень глюкозы в венозной крови при развитии шока или нарушении сознания детям, получающим ИГКС [5-8]. У пациентов, получающих ИГКС возможно развитие надпочечниковой недостаточности и может потребоваться назначение гидрокортизона внутримышечно.
|
|
С
|
Рекомендуется прекратить назначение ИГКС детям до 5 лет, если симптомы не изменились через 2 месяца [5-8]
|
Альтернативные лекарственные средства
|
В
|
Рекомендуется назначение антагонистов лейкотриеновых рецепторов (АЛТР) детям младше 5 лет, которые не могут принимать ИГКС, в качестве профилактической терапии [5-8]
|
|
С
|
Рекомендуется назначение кромогликата натрия ИЛИ недокромила натрия детям в возрасте 5-12 лет в качестве альтернативной терапии [5-8]
|
Недокромил натрия рекомендован для детей старше 5 лет. Нет четких доказательств пользы кромогликата натрия у детей в возрасте младше 5 лет
Теофиллины оказывают некоторое благоприятное воздействие.
Теофиллины оказывают некоторое благоприятное воздействие.
|
С
|
НЕ РЕКОМЕНДУЕТСЯ назначение антигистаминных средств и кетотифена как альтернативная профилактическая терапия
|
|
В
|
Рекомендуется назначение ингаляционного β2-агониста длительного действия (ДДБА) или АЛТР детям старше 5 лет в качестве начальной дополнительной терапии
|
Обзор применения ДДБА у детей младше 12 лет, используемых в сочетании с ИГКС, в контроле над астмой риски ухудшения невелики, перевешивают любые очевидные риски.
|
D
|
Рекомендуется рассмотреть альтернативные варианты лечения, если контроль БА недостаточный при приеме низкой дозы ИГКС плюс ДДБА* или АЛТР [5-8]:
|
* Комбинированный препарат (ИГКС + ДДБА)
Лечение бронхиальной астмы подразделяется на 5 ступеней в зависимости от степени тяжести и объема терапии. На каждой последующей ступени объем терапии увеличивается.
Ступенчатая терапия бронхиальной астмы [1-4]
Если текущая терапия не обеспечивает контроля над БА, необходимо увеличивать объем терапии (переход на более высокую ступень) до достижения контроля.
|
С
|
Рекомендуется уменьшить объема поддерживающей терапии при сохранении контроля над симптомами БА в течение 3 месяцев и более [5-8]
|
|
С
|
Рекомендуется увеличение объема терапии (т.е. увеличение доз или добавление других препаратов) с учетом их безопасности, доступности и удовлетворенности пациента при частичном контроле над симптомами БА [5-8]
|
Некоторым пациентам может потребоваться применение ИГКС в средней дозе, если астма не контролируется низкими дозами, несмотря на хорошую приверженность и правильную технику.
Высокие дозы ИГКС (в сочетании с ДДБА или отдельно) необходимы небольшой доле больных БА. Их длительное применение приводит к увеличению риска локальных и системных побочных эффектов, что требует сопоставления с потенциальной пользой (Приложение 6) [1].
СТУПЕНЬ 1
Высокие дозы ИГКС (в сочетании с ДДБА или отдельно) необходимы небольшой доле больных БА. Их длительное применение приводит к увеличению риска локальных и системных побочных эффектов, что требует сопоставления с потенциальной пользой (Приложение 6) [1].
СТУПЕНЬ 1
В настоящее время всем детям с БА рекомендуется применять противовоспалительную терапию (низкие дозы ИГКС) симптоматически или регулярно для снижения риска тяжелых обострений БА.
|
В
|
Рекомендуется на ступени 1 назначать в качестве базисной терапии:
|
Предпочтение в доставке ИГКС отдается небулайзерной терапии у детей (с 6 месяцев – будесонид суспензия, с 6 лет – также бекламетазона дипропионат через спейсер, с 1 года – флутиказона пропионат со спейсером).
|
В
|
НЕ РЕКОМЕНДУЕТСЯ монотерапия КДБА
|
Меры предосторожности по КДБА
Чрезмерное использование КДБА является небезопасным:
- применение ≥3 ингаляторов КДБА в год увеличивает риск обострений БА [5-8];
- применение ≥12 ингаляторов КДБА в год связано с повышенным риском смерти по причине БА;
- Регулярное или частое применения КДБА связано с нежелательными явлениями;
- Снижение чувствительности β-адренорецепторов, снижение бронхопротекции, рикошет гиперреактивности, снижение бронхолитического ответа.
СТУПЕНЬ 2
|
В
|
Рекомендуется начинать лечение со ступени 2 больным с персистирующей бронхиальной астмой, ранее не получавших поддерживающей терапии
|
|
А
|
Рекомендуется на ступени 2 назначать:
|
|
D
|
Рекомендуется постоянное наблюдение семейного врача и специалиста аллерголога/пульмонолога детям с БА, получающим ≥400 мкг в день БДП или его эквивалента (Приложение 6)
|
Комментарии: В случае присоединения интеркуррентного заболевания такие пациенты должны использовать конкретные письменные рекомендации.
СТУПЕНЬ 3
|
В
|
Рекомендуется начинать лечение со ступени 3 больным с наличием выраженных симптомов бронхиальной астмы (при неконтролируемой астме) [5-8]
|
|
А
|
Рекомендуются на ступени 3 назначать:
Детям старше 5 лет
Детям младше 5 лет
|
|
А
|
У детей старше 5 лет на ступени 3 лечения БА в качестве базисной терапии рекомендуются низкие/средние дозы ИГКС (Приложение 6) или в комбинации с ДДБА или в комбинации с АЛТР [1, 7].
|
|
С
|
У детей младше 5 лет в качестве дополнения к терапии ИГКС рекомендуются АЛТР.
|
|
В
|
При наличии у пациента с БА, получающего терапию ИГКС, ограничений по применению ДДБА (нежелательных эффектов, противопоказаний или индивидуальной непереносимости) в качестве альтернативы ДДБА рекомендуется использовать тиотропия бромид в жидкостном ингаляторе.
|
|
Комментарии: Тиотропия бромид (Код АТХ: R03BB04) в ингаляторе, содержащем раствор, зарегистрирован в КР для лечения больных БА с 6 лет. Препарат назначают при сохранении симптомов на фоне приема ИГКС или ИГКС/ДДБА [3].
|
|
А
|
Назначение тиотропия бромида (Код АТХ: R03BB04) в жидкостном ингаляторе рекомендуется в дополнение к терапии ИГКС/ДДБА у пациентов с частыми и/или тяжелыми обострениями БА [3].
|
|
Комментарии: Показанием к назначению тиотропия бромида служит наличие 2-х и более обострений в год или наличие хотя бы 1 обострения, потребовавшего назначения СГКС или госпитализации.
|
СТУПЕНЬ 4
|
А
|
Рекомендуются перепроверить диагноз, оценить приверженность к назначенным препаратам, проверить технику ингаляции и использование спейсера, если контроль остается плохим при применении очень низких доз ИГКС в сочетании с комбинированным ингалятором с ДДБА, прежде чем увеличить дозы препаратов.
|
Если целесообразно более интенсивное лечение, можно рассмотреть следующие альтернативы.
- Если после добавления ДДБА улучшения не произошло, отмените ДДБА и попробуйте увеличить до средней дозы ИГКС (общая доза беклометазона 400 мкг в день или эквивалент);
- Если при добавлении ДДБА наблюдается улучшение, но контроль остается недостаточным - продолжить ДДБА и увеличить дозу ИГКС с очень низкой до низкой (используя комбинированный ингалятор) (общая доза беклометазона 400 мкг в день или эквивалент) или продолжать ДДБА и очень низкие дозы ИГКС (комбинированный ингалятор) и рассмотреть возможность применения АЛТР.
Если симптомы не исчезают направить на стационарный уровень.
|
В
|
Рекомендуется назначать средние дозы ИГКС (суточная доза беклометазона 800 мкг или эквивалентная) только на стационарном уровне
|
|
В
|
Рекомендуется проверить соблюдение техники и дозировки ингаляций, использование спейсера, а также устранить триггерные факторы, прежде чем изменять терапию
|
|
Если контроль остается недостаточным при применении низких доз ИГКС (общая доза беклометазона 400 мкг в день или эквивалентная) в сочетании ДДБА, можно рассмотреть следующие вмешательства:
ИЛИ
ИЛИ
|
Если пробное дополнительное лечение неэффективно, отмените препарат (или в случае увеличения дозы ИГКС, уменьшите до исходной дозы).
|
В
|
Рекомендуется назначать пробный прием высоких доз ИГКС (более 800 мкг в день) под наблюдением специалистов, прежде чем переходить на пероральные ГКС
|
Дети, принимающие высокие дозы ИГКС, должны иметь при себе «стероидную карточку», чтобы включить в нее план экстренной заместительной терапии стероидами во время нереспираторного интеркуррентного заболевания.
Высокие дозы ИГКС могут применяться с помощью ДАИ со спейсером или через небулайзер.
|
D
|
Рекомендуется информировать и инструктировать пациентов с БА о том, что необходимо вести дневник по применению ИГКС
|
Прежде чем приступить к непрерывному или частому применению пероральных ГКС, направьте детей с неадекватно контролируемой астмой к специалисту.
- Используйте ежедневный пероральный ГКС в самой низкой дозе, обеспечивающей адекватный контроль.
- Поддерживать терапию средними дозами ИГКС (беклометазон 800 мкг/день или эквивалент)
- Рассмотрите другие варианты лечения, чтобы свести к минимуму потребность в пероральных стероидах.
Пациенты, длительное время принимающие стероиды в таблетках (например, более трех месяцев) или нуждающиеся в частых курсах стероидов в таблетках (например, три-четыре в год), будут подвергаться риску системных побочных эффектов, поэтому может потребоваться мониторинг.
Пероральные ГКС следует назначать в начале лечения острых приступов астмы у детей. Пероральный преднизолон один раз в день является стероидом выбора при приступах астмы у детей, если пациент не может переносить дозу:
- Детям до 2 лет - 10 мг преднизолона в сутки;
- Детям в возрасте 2-5 лет - 20 мг преднизолона в сутки;
- Детям старше 5 лет - 30–40 мг преднизолона в сутки.
Те, кто уже получает поддерживающие стероиды в таблетках, должны получать преднизолон в дозе 2 мг/кг в сутки до максимальной дозы 60 мг.
|
D
|
Рекомендуется повторить дозу преднизолона у детей, у которых рвота, и рассмотреть возможность в/в введения ГКС
|
Обычно достаточно лечения до трех дней, но продолжительность курса должна соответствовать количеству дней, необходимых для выздоровления. В снижении дозы нет необходимости, если курс стероидов не превышает 14 дней.
|
D
|
НЕ РЕКОМЕНДУЕТСЯ назначать ГКС детям младше 5 лет, когда триггером является вирус
|
|
В
|
Рекомендуется назначить комбинацию низких доз ИГКС (будесонид или беклометазон/формотерол) в качестве поддерживающей терапии и для купирования симптомов подросткам с БА, имеющим ≥1 обострения за предшествующий год для снижения частоты обострений
|
|
В
|
Рекомендуется увеличить дозу ИГКС до максимальной в сочетании с ДДБА и/или добавлением АЛТР пациентам с БА старше 12 лет при недостаточном контроле БА на фоне использования 800 мкг БДП или его эквивалента в день [5-8]
|
|
В
|
Рекомендуется увеличить дозу ИГКС до максимальной в сочетании с ДДБА или добавлением АЛТР детям 5-12 лет с неконтролируемым течением БА на фоне терапии 400 мкг (по бекламетазону) или его эквивалента в день
|
У детей всех возрастов, которые получают специализированную медицинскую помощь, можно назначить более высокие дозы ИГКС (> 800 мкг/сутки) прежде чем перейти к ступени 5.
СТУПЕНЬ 5
|
С
|
Рекомендуется направить к специалисту (аллерголог, пульмонолог), занимающемуся лечением тяжелой БА всех детей с персистирующими симптомами или обострениями БА, несмотря на правильную технику ингаляции и хорошую приверженность лечению, соответствующему 4-й ступени лечения БА
|
МОНИТОРИНГ ЛЕЧЕНИЯ БА
Для поддержания контроля над заболеванием с использованием минимального объема терапии и наименьших доз препаратов, способствующих снижению затрат и риска нежелательных лекарственных реакций, необходимо постоянное наблюдение за больными.
|
D
|
Рекомендуется оценивать уровень контроля над симптомами БА при каждом осмотре и необходимость изменения лечения
|
|
D
|
Рекомендуется мотивировать пациентов/родителей пациентов вести «Дневник контроля БА» (с определением АСТ-теста) для оценки уровня контроля над симптомами БА (см. Приложение 4)
|
|
D
|
Рекомендуется проводить наблюдения за пациентом с БА в следующем порядке:
|
|
D
|
Рекомендуется оценить технику ингаляций (см. Приложение 5) и мероприятия по уменьшению факторов риска (см. Приложение 3)
|
|
В
|
Рекомендуется оценить приверженность пациента к назначенному лечению, проверить количество используемого КДБА, ИГКС (проверить соблюдение техники и дозировки ингаляций, использование спейсера, а также устранить триггерные факторы)
|
|
D
|
Рекомендуется проводить осмотр полости рта, т.к. при приеме ИГКС возможно развитие стоматита.
Рекомендуется гигиена полости рта и полоскание рта после приема ИГКС. |
|
D
|
Рекомендуется проводить измерение роста и веса при каждом посещение и оценивать физическое развитие по таблицам стандартных отклонений (Вес/Возраст, Рост/Возраст, Вес/Рост).
|
|
В
|
Рекомендуется постепенно уменьшать объем терапии, переходя на более низкую ступень лечения, если контроль БА поддерживается в течение 3 месяцев
|
Предостережения!
Повышенный риск побочных эффектов возникает при применении следующих доз или выше: беклометазон 400 мкг/день; будесонид 800 мкг/день; флутиказон 400 мкг/день.
Высокие эквивалентные дозы беклометазона 800 мкг или выше несут риск надпочечниковой недостаточности (нарушение сознания, гипогликемия), особенно при нереспираторных интеркуррентных заболеваниях. Обратитесь к специалисту (аллергологу, пульмонологу), если пациент принимает эту дозу. Нельзя резко прекращать прием лекарств. Необходимы стероидная карта (препарат, дозировка, длительность применения) и план неотложной терапии (преднизолон перорально 0,2 мг/кг/день или гидрокортизон внутримышечно 4 мг/кг каждые 6-8 часов).
|
D
|
Рекомендуется проводить офтальмологический осмотра детям, длительно принимающим высокие дозы ИКГС (риск развития катаракты)
|
Дети, получающие средние или высокие дозы ИГКС, должны находиться под наблюдением врача ГСВ (или педиатра) в течение всего периода лечения. Конкретные письменные рекомендации по заместительной терапии ГКС в случае тяжелого интеркуррентного заболевания должны быть частью плана лечения (стероидная карта = план лечения + неотложная терапия при развитии острой надпочечниковой недостаточности).
КОМПОНЕНТ 4
ЛЕЧЕНИЕ ОБОСТРЕНИЙ БРОНХИАЛЬНОЙ АСТМЫ
|
Для обострения (приступа) БА характерны:
|
Цель лечения обострений БА:
- быстрое устранение бронхиальной обструкции и гипоксемии;
- предотвращение дальнейших рецидивов.
Основные мероприятия по лечению обострений:
- повторные ингаляции бронхолитиков быстрого действия;
- раннее применение СГКС (системные ГКС);
- кислородотерапия.
|
D
|
Рекомендуется оценивать степень тяжести обострения БА:
|
Оценка степени тяжести обострения (приступа) БА для детей
|
Показатель
|
Легкая
|
Средней тяжести
|
Тяжелая
|
Жизнеугрожающая астма (угроза остановки дыхания)
|
|
Одышка
|
При ходьбе, Могут лежать
|
При разговоре;
у детей плач становится тише и короче, возникают затруднения при кормлении Предпочитает сидеть |
В покое.
Дети прекращают принимать пищу. Сидят, наклоняясь вперед |
|
|
Речь
|
Предложениями
|
Фразами
|
Словами
|
|
|
Уровень бодрствования
|
Может быть возбужден
|
Обычно возбужден
|
Обычно возбужден
|
Заторможен или в состоянии спутанного сознания
|
|
Частота дыхания
|
Учащено
|
Учащено
|
Свыше 30 в мин
|
|
|
Нормальная частота дыхания у детей:
Возраст Нормальная частота дыхания <2 мес. <60 в минуту 2–12 мес. <50 в минуту 1–5 лет <40 в минуту 6-8 лет <30 в минуту |
||||
|
Участие вспомогательной дыхательной мускулатуры и втяжение яремной ямки
|
Нерезко выражено
|
Выражено
|
Резко выражено
|
Парадоксальные движения грудной и брюшной стенок
|
|
Свистящие хрипы
|
Умеренные, обычно в конце выдоха
|
Выраженные сухие хрипы
|
Резко выраженные
|
Немое легкое (хрипы не прослушиваются)
|
|
Частота пульса, в минуту
|
<100
|
100-120
|
>120
|
Брадикардия
|
|
Нормальная частота пульса у детей:
грудного возраста 2–12 мес. <160 в минуту младшего возраста 1–2 лет <120 в минуту дошкольного и школьного возраста 2–8 лет <110 в минуту |
||||
|
ПСВ после начального применения бронхолитика в % от должного или от индивидуального лучшего показателя
|
Более 80%
|
60-80%
|
<60%
|
<60%
|
|
Sр02
|
>95%
|
91-95%
|
<90%
|
<90%
|
COVID-19 И БРОНХИАЛЬНАЯ АСТМА У ДЕТЕЙ [8, 9, 10, 11, 12]
|
В
|
Рекомендуется продолжать принимать предписанные лекарства от астмы, в частности, ингаляционные кортикостероиды (ИГКС) и пероральные кортикостероиды (ОГКС), если они были назначены пациентам с БА[5-8]
|
|
В
|
Рекомендуется составить письменный план действий по усилению контролирующей и облегчающей терапии, если течение БА становится тяжелым [5-8]
|
|
С
|
НЕ РЕКОМЕНДУЕТСЯ использовать небулайзеры, т.к. увеличивают риск передачи вируса другим больным и медицинским работникам [5-8]
|
|
С
|
НЕ РЕКОМЕНДУЕТСЯ проводить спирометрию у больных с подтверждённым / предполагаемым COVID-19 [5-8]
|
Спирометрия может распространять вирусные частицы и подвергать персонал и пациентов риску заражения.
|
В
|
Рекомендуется соблюдать правила инфекционного контроля, если необходимы процедуры с использованием аэрозольной терапии [5-8]
|
Лечение (амбулатория)
ЛЕЧЕНИЕ ОБОСТРЕНИЯ АСТМЫ В АМБУЛАТОРНЫХ УСЛОВИЯХ [1-4]
| В | Рекомендуется назначить КДБА по 2-4 вдоха детям до 5 лет (через лицевую маску или спейсер из пластиковой бутылки объемом 750 мл, см. приложение 5) и по 1-2 вдоха детям старше 5 лет (через спейсер заводского изготовления или спейсер из пластиковой бутылки объемом 1 литр, см. приложение 5) повторяющихся каждые 20 минут в течение часа соответственно клиническому ответу |
Если применение КДБА полностью купирует приступ (для детей старше 5 лет ПСВ возвращается к значению, превышающему 80% от должной или наилучшей индивидуальной величины), и это улучшение сохраняется в течение 3-4 часов, то необходимость в дополнительных лекарственных препаратах отсутствует.
Если дыхательная недостаточность купирована, и у ребенка нет учащенного дыхания, рекомендуйте матери давать ребенку в домашних условиях сальбутамол из дозированного аэрозольного ингалятора через спейсер (который можно изготовить самостоятельно из пластиковой бутылки) [5].
| В | Рекомендуется добавить ипратропия бромид (250 мкг/доза смешивается с физиологическим раствором через небулайзер), если симптомы не поддаются лечению КДБА |
Повторные дозы ипратропия бромида используют для лечения детей, которые плохо отвечают на КДБА.
Если ингаляции КДБА требуются чаще чем каждые 4 часа, то следует отменить ДДБА.
| D | Рекомендуется госпитализировать ребенка, если симптомы не контролируются КДБА и назначить кислородотерапию, если дыхательная недостаточность сохраняется |
Дополнительные дозы бронходилататоров даются по мере необходимости во время ожидания врача при выраженных симптомах.
Во время доставки ребенка с тяжелым приступом БА в отделение неотложной помощи назначается бронхолитик + суспензия будесонида через небулайзер с кислородом.
| В | Рекомендуется назначить суспензию будесонида через небулайзер при неэффективности бронходилататоров у детей с 6 мес. возраста |
Необходимо индивидуализировать дозу препарата в зависимости от тяжести и ответной реакции пациента.
| В |
Рекомендуется перед госпитализацией назначить преднизолон перорально в дозе из расчета 1 мг/кг.
Если ребенок не может глотать, ГКС следует ввести внутримышечно или внутривенно в дозе 1-2 мг/кг (преднизолон) или 0,5-0,6 мг/кг (дексаметазон)
|
В случае невозможности госпитализации ребенка, необходимо продолжить лечение кортикостероидами (1 мг/кг/сутки) в течение 3-х дней
При необходимости длительность курса должна увеличиваться до стабилизации состояния.
| В | Рекомендуется назначить базисную терапию ИГКС после купирования приступов астмы (снижение потребности в β2-агонистах быстрого действия и увеличение ПСВ) |
Лечение обострений БА на догоспитальной этапе у детей 6-11 лет [5-8]
Показания для лечения БА на догоспитальном этапе:
Нетяжелые обострения со снижением ПСВ на 25-50%, ночными пробуждениями из-за БА и повышенной потребности в КДБА.
При отсутствии ответа или сомнениях – направление в интенсивную терапию.
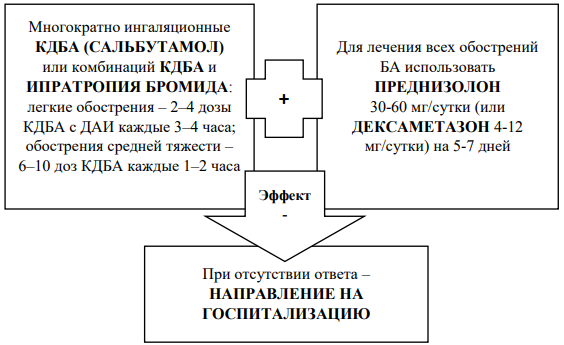
Лечение обострений БА на догоспитальном этапе у детей 5 лет и младше [1]
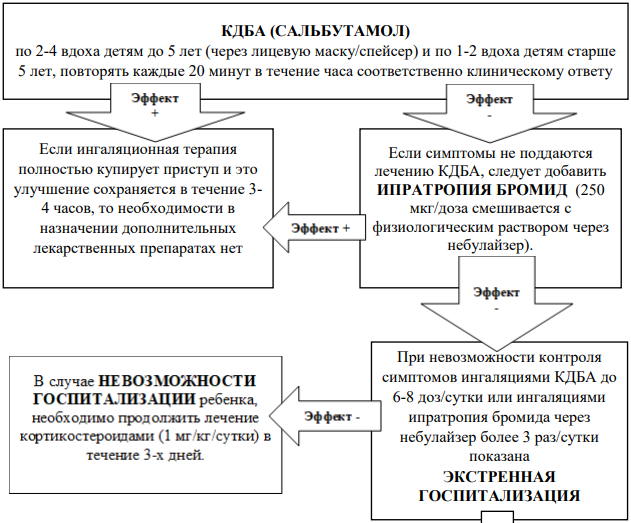

| В | Рекомендуется назначить при легкой степени БА - 2–4 дозы КДБА с ДАИ каждые 3–4 часа + ИГКС через небулайзер |
| В | Рекомендуется назначить при средней тяжести БА - 6–10 доз КДБА каждые 1–2 часа + ИГКС через небулайзер |
При легком и умеренном обострении - короткодействующие бронхолитики в ДАИ + спейсер или небулайзер с подбором дозы.
При отсутствии ответа или сомнениях – направление в интенсивную терапию.
| В | Рекомендуется назначить системные ГКС при всех обострениях - преднизолон 30-60 мг/сутки (или дексаметазон 4-12 мг/сутки) на 5-7 дней |
АЛГОРИТМ ЛЕЧЕНИЯ ОБОСТРЕНИЯ АСТМЫ В АМБУЛАТОРНЫХ УСЛОВИЯХ У ДЕТЕЙ 6-11 ЛЕТ

Лечение обострений БА на догоспитальном этапе у детей 5 лет и младше [1]
|
Показания:
|
|
Лечение:
|
АЛГОРИТМ ЛЕЧЕНИЯ ОБОСТРЕНИЯ АСТМЫ В АМБУЛАТОРНЫХ УСЛОВИЯХ У ДЕТЕЙ 5 ЛЕТ И МЛАДШЕ


ГОСПИТАЛИЗАЦИЯ ДЕТЕЙ С ОБОСТРЕНИЕМ БРОНХИАЛЬНОЙ АСТМОЙ [3, 4]
| Состояние и ФВД через 1 час от начала терапии более значимы, чем исходное состояние. |
|
Показания к госпитализации:
|
Лечение (стационар)
ЛЕЧЕНИЕ ОБОСТРЕНИЯ АСТМЫ В СТАЦИОНАРЕ [1]
Детям, принятым на лечение в стационар, немедленно назначьте кислород, быстродействующее бронхолитическое средство и первую дозу кортикостероидных препаратов.
1. Кислородотерапия.
Детям, принятым на лечение в стационар, немедленно назначьте кислород, быстродействующее бронхолитическое средство и первую дозу кортикостероидных препаратов.
1. Кислородотерапия.
Оксигенотерапия проводится для поддержания адекватного уровня газов крови.
|
В
|
Рекомендуется подавать кислород младенцам и детям в возрасте до 5 лет с гипоксемией через назальные канюли
|
При отсутствии назальных канюлей, в качестве альтернативных методов подачи могут использоваться назальные или носоглоточные катетеры.
|
С
|
НЕ РЕКОМЕНДУЕТСЯ подавать кислород через лицевые маски или дыхательные мешки
|
|
В
|
Рекомендуется подавать кислород через плотно прилегающую маску или носовые канюли детям с угрожающей жизни БА и SрO2 <94% для достижения нормальной сатурации
|
2. Ингаляционные β2-агонисты короткого действия (КДБА)
|
А
|
Рекомендуется назначить:
ИЛИ
|
При необходимости в тяжелых случаях можно давать через каждый час в течение 2-4 часов, т.е. до улучшения состояния больного (клинические симптомы, ПСВ, SрO2).
Техника ингаляции сальбутамолом через небулайзер
Производительность небулайзера должна составлять как минимум 6–9 л/мин. Рекомендуется использовать воздушный компрессор, ультразвуковой ингалятор или кислородный баллон, но в случаях угрожающей жизни бронхиальной астмы должен обязательно применяться кислород. Если указанных выше приспособлений нет в наличии, используйте ингалятор со спейсером. Также можно использовать простой в обращении ножной насос, однако это менее эффективно.
|
Техника ингаляции сальбутамолом из дозированного аэрозольного ингалятора через спейсер
Выпускаются спейсеры объемом 750 мл.
|
2. Комбинированные ингаляционные бронходилятаторы
|
D
|
Рекомендуется назначить комбинированные ингаляционные бронходилятаторы – ипратропия бромид + фенотерола гидробромид (раствор для небулайзерной терапии):
|
Техника применения раствора и аэрозоля комбинированного бронхолитика
|
3. 0,1% (1:1000) раствор эпинефрина (адреналина)
|
D
|
Рекомендуется ввести подкожно 0,1% (1:1000) раствор эпинефрина в дозе 0,01 мл/кг (максимально до 0,3 мл), которую нужно точно набрать в шприц объемом 1 мл, если ингаляционные методы невозможны
|
Техника выполнения инъекции эпинефрина
-
Детям в возрасте старше 2-х лет п/к инъекции проводят в наружную сторону бедра или в верхний наружный квадрант ягодицы, на достаточном расстоянии от седалищного нерва.
-
Для выполнения инъекций детям более раннего возраста или детям с тяжелым нарушением питания используйте среднюю часть наружной стороны бедра или место над дельтовидной мышцей плеча.
|
Введите иглу (23–25 калибра) под углом 45° в подкожную жировую клетчатку.
|
4. Глюкокортикостероиды (ГКС)
|
D
|
Рекомендуется назначить преднизолон перорально в дозе из расчета 0,5-1 мг/кг, если ребенок может пить и глотать.
Рекомендуется назначить ГКС в/в или в/м в дозе из расчета 1-2 мг/кг. |
Как только больной сможет принимать препараты внутрь, дайте преднизолон в табл. 0,5-1мг/кг в течение 3 дней с последующей одномоментной отменой.
Преднизолон используется в дозе 20 мг для детей в возрасте от 2 до 5 лет и в дозе от 30 до 40 мг для детей старше 5 лет. У детей, уже получающих стероиды перорально, преднизолон назначается из расчета 2 мг/кг до максимальной дозы 60 мг.
|
С
|
Рекомендуется назначить системные ГКС всем детям старше 2 лет с тяжелым обострением БА [5-8]
|
Если у ребенка наблюдалась рвота, преднизолон назначается повторно. Возможно внутривенное введение ГКС в случаях, когда пероральный прием препарата затруднен или невозможен. Обычно достаточно лечения пероральным преднизолоном в течение трех дней, но длительность его приема может быть увеличена до 14 дней для полного купирования симптомов.
При необходимости длительность курса должна увеличиваться до стабилизации состояния. Затем следует назначить базисную терапию ИГКС.
5. Сульфат магния
Внутривенное введение сульфата магния может дать дополнительный лечебный эффект у детей с тяжелой бронхиальной астмой, получающих бронхолитические и кортикостероидные препараты. Сульфат магния является более безопасным препаратом при лечении тяжелого приступа бронхиальной астмы, чем аминофиллин. Как более широко доступное лекарственное средство сульфат магния может применяться у детей, которые не реагируют на лечение препаратами, описанными выше.
|
D
|
Рекомендуется ввести внутривенно однократно в течение 20 минут 50% раствор сульфата магния в дозе из расчета 0,1 мл/кг (50 мг/кг)
|
6. Аминофиллин
При неэффективности терапии вышеизложенными мероприятиями, необходимо ввести препараты второго ряда - аминофиллин (под контролем ЭКГ).
|
D
|
Рекомендуется ввести внутривенно аминофиллин детям старше 2-х лет только с тяжелой или угрожающей жизни астмой, не отвечающим на максимальные дозы ингаляционных бронхолитиков и СГКС, находящихся на лечении в отделении интенсивной терапии
|
Техника введения аминофиллина
|
Меры предосторожности!
Аминофиллин не рекомендуется назначать при легких или среднетяжелых приступах бронхиальной астмы. Его следует использовать как препарат резерва для тех детей, состояние которых не улучшается после нескольких доз быстродействующего бронхолитического средства, вводимых через короткие промежутки времени вместе с пероральным преднизолоном.
Аминофиллин не рекомендуется назначать при легких или среднетяжелых приступах бронхиальной астмы. Его следует использовать как препарат резерва для тех детей, состояние которых не улучшается после нескольких доз быстродействующего бронхолитического средства, вводимых через короткие промежутки времени вместе с пероральным преднизолоном.
7. Антибиотики
|
В
|
НЕ РЕКОМЕНДУЕТСЯ назначать антибиотики детям с обострением БА только при бактериально подтвержденной инфекции [5-8]
|
АЛГОРИТМ ЛЕЧЕНИЯ ОБОСТРЕНИЯ АСТМЫ В СТАЦИОНАРЕ
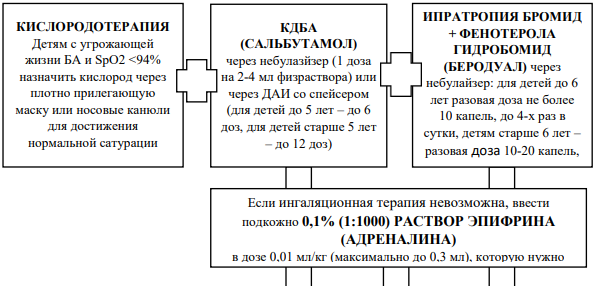
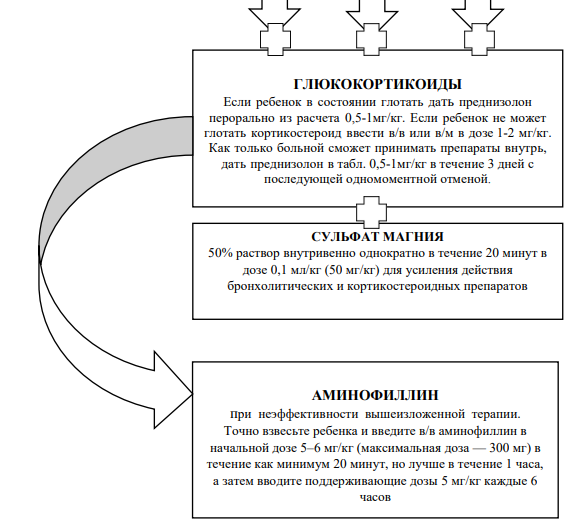
Лечение обострений бронхиальной астмы на госпитальном этапе у детей 6-11 лет [1]
Лечение в стационарах с ОРИТ.
|
В
|
Рекомендуется подавать кислород объемом 4-5 л через назальные канюли при SрО2<90% [5-8]
|
|
D
|
Рекомендуется назначить КДБА или комбинацию КДБА и ипратропия бромида:
|
|
С
|
Рекомендуется назначить перорально преднизолон в дозе 40-50 мг/1 раз/сутки на 5-7 дней [5-8].
При невозможности приёма per os из-за выраженной одышки или респираторной поддержки назначить парентерально ГКС |
|
С
|
Рекомендуется отменять СГКС только на фоне назначения ИГКС [5-8]
|
|
С
|
Рекомендуется назначить эпинефрин п/к, в/м при неотложном лечении анафилаксии или ангионевротического отека [5-8]
|
|
D
|
Рекомендуется назначить магния сульфат 2 г в/в в течение 20 мин однократно при рефрактерных к КДБА обострениях [5-8]
|
|
В
|
Рекомендуется провести неинвазивную вентиляцию легких (НИВЛ) при тяжелой одышке, гиперкапнии, признаках повышенной работы дыхательной мускулатуры, но без утомления мышц и без нарушения сознания [5-8]
|
|
Показания к ИВЛ:
|
|
В
|
Не рекомендуется назначать при обострении БА [5-8]:
|
Лечение обострений бронхиальной астмы на госпитальном этапе у детей 5 лет и младше [1]
|
С
|
Рекомендуется назначить терапию СГКС преднизолоном 1-2 мг/кг/сутки (максимум/сутки 60 мг) 3 дня, до 14 дней для полного купирования симптомов при тяжелых обострениях БА или при отсутствии эффекта от бронхолитической терапии в течение1 часа [5-8]
|
|
С
|
Рекомендуется назначить суспензию будесонида через небулайзер детям старше 6 месяцев как альтернатива СГКС [5-8]
|
|
С
|
Рекомендуется начать кислородотерапию через плотно прилегающую маску или назальные канюли при угрожающей жизни БА и SрO2 <94% [5-8]
|
|
С
|
НЕ РЕКОМЕНДУЕТСЯ назначать аминофиллин в/в и антибиотики [5-8]
|
Лечение обострений бронхиальной астмы на госпитальном этапе у детей в возрасте младше 2 лет [1]
|
D
|
Рекомендуется назначить ингаляционно ипратропия бромид в комбинации с ингаляционным β2-агонистом детям младше 2-х лет с обострением средней и тяжелой степени тяжести и при неудовлетворительном ответе на начальное лечение КДБА
|
|
В
|
Рекомендуется использовать небулайзер или ДАИ + спейсер у детей младше 2-х лет для лечения легкого и среднетяжелого обострения БА [5-8]
|
|
С
|
НЕ РЕКОМЕНДУЮТСЯ использовать оральные β2-агонисты для купирования обострения БА у детей младше 2-х лет [5-8]
|
|
В
|
Рекомендуется назначать ингаляционный будесонид через небулайзер в средних и высоких дозах, СГКС внутрь (преднизолон – 10 мг) продолжительностью до 3 дней для купирования среднетяжелых и тяжелых приступов БА в условиях стационара у детей до 2-х лет [5-8]
|
Поддерживающее лечение
|
D
|
Рекомендуется проводить ежедневный контроль получаемой жидкости в соответствующем его возрасту объеме
|
|
Общая суточная потребность в жидкости ребенка до 5 лет рассчитывается по следующей формуле:
100 мл/кг на первые 10 кг массы тела, затем 50 мл/кг на следующие 10 кг, далее 25 мл/кг на каждый последующий килограмм. Например, ребенок весом 8 кг должен получать: 8 x 100 мл = 800 мл в сутки; а ребенок весом 15 кг должен получать (10 x 100) + (5 x 50) = 1250 мл в сутки [5]. |
|
D
|
Рекомендуется поощрять грудное вскармливание, прием жидкостей перорально, адекватное дополнительное кормление маленького ребенка, как только он сможет принимать пищу
|
Критерии перевода в ОРИТ из соматического отделения:
а. Больные с тяжелым обострением астмы и отсутствием положительного эффекта от начальной терапии в течение 2-3-х часов.
б. Больные с обострением астмы, угрожающим жизни (астматический статус).
в. Нестабильное течение астмы с эпизодами госпитализации в ОРИТ в анамнезе.
г. Любые признаки тяжелого обострения.
д. Снижение сатурации кислорода на фоне проводимой терапии.
Критерии перевода из ОРИТ в соматическое отделение:
а. Полное купирование астматического статуса
а. Больные с тяжелым обострением астмы и отсутствием положительного эффекта от начальной терапии в течение 2-3-х часов.
б. Больные с обострением астмы, угрожающим жизни (астматический статус).
в. Нестабильное течение астмы с эпизодами госпитализации в ОРИТ в анамнезе.
г. Любые признаки тяжелого обострения.
д. Снижение сатурации кислорода на фоне проводимой терапии.
Критерии перевода из ОРИТ в соматическое отделение:
а. Полное купирование астматического статуса
б. Улучшение состояние больного (клинических симптомов, ПСВ, SAO2).
НАБЛЮДЕНИЕ ПРИ ГОСПИТАЛИЗАЦИИ
НАБЛЮДЕНИЕ ПРИ ГОСПИТАЛИЗАЦИИ
|
|
D
|
Рекомендуется проведение рентгенографии грудной клетки для исключения пневмоторакса, если ребенок не реагирует на описанное выше лечение, или его состояние резко ухудшается
|
ПОКАЗАНИЯ К ВЫПИСКЕ [2]:
|
Достижение контроля симптомов;
|
Рекомендации при выписке пациента из стационара [2]:
|
В
|
Рекомендуется назначить КДБА по потребности с постепенным переходом на базовый препарат, назначенный до начала обострения [5-8]
|
|
В
|
Рекомендуется назначить или продолжить ИГКС [5-8]
|
|
С
|
Рекомендуется провести обучение по правильному использованию ингалятора, спейсера, составить план самоведения и самооценки [5-8]
|
|
D
|
Рекомендуется обратиться к семейному врачу по месту жительства в течение 24 часов после выписки
|
Информация
Источники и литература
-
Клинические протоколы Министерства здравоохранения Кыргызской Республики
- Клинические протоколы Министерства здравоохранения Кыргызской Республики - 1. Британские рекомендации по диагностике и медикаментозному лечению астмы у детей, SIGN, 2019. 2. Астма: диагностика, мониторинг и лечение хронической астмы, NICE, 2021 3. Бронхиальная астма. Клинические рекомендации. Сокращенный вариант. МЗ Российской федерации. МОО Российское респираторное общество. Российская Ассоциация Аллергологов и Клинических иммунологов Союз педиатров России. Москва. 2021. 4. Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention, 2022. 5. Карманный справочник «Оказание стационарной помощи детям. Руководство по ведению наиболее распространенных болезней детского возраста». Всемирная организация здравоохранения. Второе издание. Бишкек. 2017. 6. Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention for adults and children older than 5 years. A Pocket Guide For Health Professionals. Updated May 2022. 7. icd.who.int/browse10/2019/en (официальный сайт МКБ-10 на сайте Всемирной организации здравоохранения). 8. Akenroye AT, Wood R, Keet C. Asthma, biologics, corticosteroids, and coronavirus disease 2019. Ann Allergy Asthma Immunol 2020; 125:12. 9. Crimi C, Impellizzeri P, Campisi R, et al. Practical considerations for spirometry during the COVID-19 outbreak: Literature review and insights. Pulmonology 2021; 27:438. 10. Hussein MH, Elshazli RM, Attia AS, et al. Asthma and COVID-19; different entities, same outcome: a meta-analysis of 107,983 patients. J Asthma 2021; :1. 11. Rosenthal JA, Awan SF, Fintzi J, et al. Asthma is associated with increased risk of intubation but not hospitalization or death in coronavirus disease 2019. Ann Allergy Asthma Immunol 2021; 126:93. 12. Yang JM, Koh HY, Moon SY, et al. Allergic disorders and susceptibility to and severity of COVID-19: A nationwide cohort study. J Allergy Clin Immunol 2020; 146:790.
Информация
Адрес для переписки с рабочей группой
Кыргызская Республика, г. Бишкек
ул. Тоголока Молдо, 1 А, НЦОМиД
Тел: (996-312), 66-05-00
Тел: (996-312), 66-04-49
e-mail: masheraliev@mail.ru
Ашералиев М.Э.
e-mail: boriakiny@gmail.com
Борякин Ю.В.
Данное клиническое руководство может использоваться в публикациях с соответствующей ссылкой.
СПИСОК СОКРАЩЕНИЙ
АД - артериальное давление
АЛТР - антагонисты лейкотриеновых рецепторов
АСИТ - аллерген-специфическая иммунотерапия
БА - бронхиальная астма
БГР - бронхиальная гиперреактивность
БДП - беклометазона дипропионат
БО - бронхиальная обструкция
ГКС - глюкокортикостероиды
ГСВ - группа семейных врачей
ГЭРБ - гастроэзофагеальная рефлюксная болезнь
ДАИ - дозированный аэрозольный ингалятор
ДДБА - длительнодействующие β2–агонисты
ДИ - дозированный ингалятор
ДМ - доказательная медицина
ДПИ - дозированный порошковый ингалятор
ИВЛ - искусственная вентиляция легких
ИГКС - ингаляционные кортикостероиды
КБД - коэффициент бронходилатации
КГМА - Кыргызская Государственная Медицинская Академия им. И.К. Ахунбаева
КДБА - короткодействующие β2–агонисты
КП - клинический протокол
КР - клиническое руководство
КС - Карманный справочник «Оказание стационарной помощи детям. Руководство по ведению наиболее распространенных болезней детского возраста»
МАК - медицинская аккредитационная комиссия
МЗ КР - министерство здравоохранения Кыргызской Республики
МСВ - максимальная скорость выдоха
НВЛ - неинвазивная вентиляция легких
НВПС - нестероидные противовоспалительные средства
НЦОМиД - Национальный центр охраны материнства и детства
НЯ - нежелательные явления
ОДН - острая дыхательная недостаточность
ОРИТ - отделение реанимации и интенсивной терапии
ОФВ - объём форсированного выдоха
ОФВ1 - объем форсированного выдоха за 1–ю секунду
ПИ - пневмококковая инфекция
ПКВ - пневмококковая конъюгированная вакцина
ППВ-23 - пневмококковая полисахаридная 23-валентная вакцина
ПСВ - пиковая скорость выдоха
РКИ - рандомизированные контролируемые исследования
РЦРЗ и ИТ - Республиканский Центр развития здравоохранения и информационных технологий
СГКС - системные глюкокортикостероиды
УДД - уровни достоверности доказательств
ФЖЕЛ - форсированная жизненная емкость легких Фонд ОМС – фонд обязательного медицинского страхования
ХОБЛ - хроническая обструктивная болезнь легких
ЦСМ - центр семейной медицины
ЧСС - частота сердечных сокращений
АСТ - Asthma Control Test (тест по контролю над астмой)
BPAP - Biphasic positive airway pressure
сАСТ - Children’s Asthma Control Test (тест по контролю астмы у детей)
CPAP, - Constant Positive Airway Pressur
ACQ - Asthma Control Questionnaire (вопросник по оценке контроля астмы) фракция оксида азота в выдыхаемом воздухе
FDA - Food and Drug Administration (управление по санитарному надзору за качеством пищевых продуктов и медикаментов США)
FiO2 - (fraction of inspired oxygen) фракция кислорода во вдыхаемой газовой смеси
GINA - Global Initiative for Asthma (Глобальная инициатива по астме)
GPP - Good Practice Points (сложившаяся клиническая практика)
IgE - Immunoglobulin E (иммуноглобулины класса Е)
PaO2 - Pressure of Oxygen (парциальное напряжение кислорода в артериальной крови)
PaСO2 - Pressure of Carbon Dioxide (парциальное напряжение углекислого газа в артериальной крови)
SрO2 - Percentage of Saturation Oxygen of Blood Hemoglobin (насыщение гемоглобина кислородом)
Тh2 - (T-helpers 2) Т-лимфоциты хелперы 2 типа
ОСНОВНЫЕ ТЕРМИНЫ И ПОНЯТИЯ
Бронхиальная гиперреактивность – функциональное нарушение, проявляющееся эпизодами бронхиальной обструкции под воздействием стимулов, безопасных для здорового человека.
Обострение бронхиальной астмы – эпизоды нарастающей одышки, кашля, свистящих хрипов, или заложенности в грудной клетке, требующие изменений обычного режима терапии.
Астматический статус - эпизод острой дыхательной недостаточности вследствие обострения БА.
Астмоидное дыхание – дыхание, характеризующееся высокими, свистящими звуками при выдохе Эти звуки обусловлены спастическим сужением дистальных отделов дыхательных путей. Для того, чтобы услышать астмоидное дыхание, даже в легких случаях, расположите свое ухо рядом со ртом ребенка и послушайте дыхание, когда ребенок спокоен, или используйте фонедоскоп (КС).
Атопия – наследственно обусловленная гиперчувствительность немедленного типа с повышенной выработкой IgE-антител к аллергену, повышенным количеством Fc-рецепторов для этих антител на тучных клетках, особенностями распределения тучных клеток и повышенной проницаемостью тканевых барьеров.
Таргетная терапия бронхиальной астмы ‒ это вид лечения моноклональными антителами, направленный на установление контроля над тяжелой бронхиальной астмой.
Фенотип – совокупность характеристик организма, развивающаяся в результате взаимодействия генетических факторов и окружающей среды.
Эндотип - субтип болезни, определяемый отличительным патобиологическим механизмом.
Ответственные за клиническое содержание по амбулаторному и стационарному ведению бронхиальной астмы у детей
Ответственные исполнители осуществляли систематизацию и поиск ключевых рекомендаций из выбранных международных клинических руководств путем адаптации, предоставили обобщенные данные по ссылкам для формирования клинического содержания о руководства.
Медицинские консультанты по разделам руководства:
Все члены группы подписали декларацию о конфликте интересов.
Процесс утверждения клинического руководства
От непосредственных пользователей были получены отзывы для улучшения формата представления ключевых рекомендаций, удобству применения и возможности использования ключевых рекомендаций на местах в виде кратких блок-схем и чек-листов.
Ответственный исполнитель осуществлял систематизированный поиск имеющихся международных клинических руководств, критическую оценку найденных руководств, методологическая поддержка при формировании ключевых рекомендаций по представленной информации от МДРГ, формирование методологического содержания разработанного руководства.
Методологическая помощь
Оценка клинического содержания клинического руководства (рецензенты)
Рецензенты проводили независимую оценку клинического руководства и алгоритмов по клиническому содержанию рекомендаций согласно обновленным данным по диагностике и лечению бронхиальной астмы с позиции наилучшей клинической практики, применяемой в других странах.
Оценка методологического качества клинического руководства
Методологами была проведена оценка методологического качества клинического руководства по логическому изложению, отражению наилучшей клинической практики в рекомендациях и применимости в клинической практике на местах согласно инструменту AGREE II.
Декларация конфликта интересов
Рабочей мультидисциплинарной группой было принято решение о разработке национального клинического руководства по диагностике, лечению и ведению бронхиальной астмы у детей путем адаптирования уже разработанных международных клинических руководств высокого методологического качества, основанных на принципах доказательной медицины для всех уровней здравоохранения Кыргызской Республики.
Найденные электронные базы данных по клиническим руководствам и практическим рекомендациям
Дополнительный поиск информации не проводился, т.к. было найдено достаточно клинических руководств по диагностике и лечению бронхиальной астмы у детей.
Характеристика отобранных клинических рекомендаций по бронхиальной астме у детей
СОСТАВ РАБОЧЕЙ МУЛЬТИДИСЦИПЛИНАРНОЙ ГРУППЫ ПО СОЗДАНИЮ РУКОВОДСТВА
Для создания клинического руководства по диагностике, лечению и ведению бронхиальной астмы у детей была создана междисциплинарная группа разработчиков. Это было обусловлено тем, что:
1. Бронхиальная астма - это заболевание, к диагностике, лечению и профилактике которого привлекаются специалисты различных звеньев и отраслей медицины, в первую очередь аллергологи, педиатры и семейные врачи.
2. Создание такой группы позволило включить в процесс разработки рекомендаций все заинтересованные стороны и рассмотреть проблему с разных позиций.
3. Создание междисциплинарной группы позволило исключить личную заинтересованность разработчиков, что значительно снизило риск возникновения систематической ошибки
Ответственные за клиническое содержание по амбулаторному и стационарному ведению бронхиальной астмы у детей
Маймерова Г.Ш. - директор НЦОМиД, д.м.н., с.н.с. (руководитель рабочей группы)
Боронбаева Э.К. - и.о. доцента кафедры пропедевтики детских болезней им. Т.И. Покровской КГМА им. И. Ахунбаева, к.м.н.
Ашералиев М.Е. - заведующий отд. аллергологии НЦОМиД, д.м.н., профессор (заместитель руководителя рабочей группы)
Молдогазиева А.С. - доцент кафедры госпитальной педиатрии с курсом неонатологии им. Д.К. Кудаярова КГМА имени И. Ахунбаева, к.м.н.
Борякин Ю.В. - доцент кафедры госпитальной педиатрии с курсом неонатологии им. Д.К. Кудаярова КГМА имени И. Ахунбаева, к.м.н.
Джанузакова Н.Э. - ассистент кафедры госпитальной педиатрии с курсом неонатологии им. Д.К. Кудаярова КГМА имени И. Ахунбаева, к.м.н.
Омушева С.Э. - старший научный сотрудник отделения аллергологии НЦОМиД, к.м.н.
Ответственные исполнители осуществляли систематизацию и поиск ключевых рекомендаций из выбранных международных клинических руководств путем адаптации, предоставили обобщенные данные по ссылкам для формирования клинического содержания о руководства.
Медицинские консультанты по разделам руководства:
Нажимидинова Г.Т. - доцент кафедры педиатрии, акушерства и гинекологии Международной высшей школы медицины УНПК МУК
Черикчиева К.Б. - клинический руководитель ГСВ ЦСМ №7 г.Бишкек, врач высшей категории.
Бектурсунов Т.М. - и.о. доцента кафедры пропедевтики детских болезней им. Т.И. Покровской КГМА им. И. Ахунбаева, к.м.н. (ответственный за перевод на государственный язык);
В эту группу вошли представители специальностей, наиболее часто встречающие в повседневной практике с бронхиальной астмой. Они были приглашены из ведущих организаций здравоохранения Кыргызской Республики. Приглашение медицинских консультантов в состав разработчиков позволило обсудить применимость отдельных рекомендаций в реальной медицинской практике, а также вопросы применимости руководства в организациях здравоохранения амбулаторного и стационарного уровней Кыргызской Республики.
Протоколы согласительных заседаний мультидисциплинарной рабочей группы по разработке клинического руководства велись в соответствии с установленным порядком, ответственным за ведение протоколов была Омушева С.Э., старший научный сотрудник отделения аллергологии НЦОМиД, к.м.н.
Все члены группы подписали декларацию о конфликте интересов.
Декларация конфликта интересов
Перед началом работы по разработке национального клинического руководства по бронхиальной астме у детей, на рабочем совещании согласительной комиссии, все члены рабочей группы дали согласие сообщить в письменной форме о наличии финансовых взаимоотношений с фармацевтическими компаниями. Никто из членов авторского коллектива не заявил о наличии коммерческой заинтересованности или другого конфликта интересов с фармацевтическими компаниями или другими организациями, производящими продукцию для диагностики и лечения бронхиальной астмы
Процесс утверждения клинического руководства
На совещании мультидисциплинарной рабочей группы принято решение разработать руководство с полным описанием лучшей международной практики для повышения информированности специалистов, и дополнить национальное клиническое руководство краткими клиническими протоколами или алгоритмами или блок-схемами в зависимости от уровней оказания медицинской специализированной помощи. Представить данные документы в удобном для использования формате, по мере возможности клинические протоколы упростить для практического использования, отразить клинические рекомендации для улучшения оснащения организаций здравоохранения. Также рассмотреть разработку стандартов и индикаторов для последующего мониторинга и оценки оказываемой медицинской помощи на местах для улучшения качества оказываемой медицинской помощи.
На расширенном заседании с членами МДРГ был обсужден финальный формат и клиническое содержание подготовленной версии клинического руководства и решено обсудить подготовленные разделы руководства для окончательной компановки.
Также было принято решение на утверждение подготовить и клинические протоколы или алгоритмы, стандарты и индикаторы для оценки оказываемой медицинской помощи при бронхиальной астме у детей.
Процесс апробации клинического руководства
В течении 2022 были подготовлены алгоритмы и клинические протоколы для различных уровней здравоохранения. В течение 2022 разработанные алгоритмы и клинические протоколы были апробированы в регионах при обучении членами мультидисциплинарной группы по бронхиальной астме у детей.
От непосредственных пользователей были получены отзывы для улучшения формата представления ключевых рекомендаций, удобству применения и возможности использования ключевых рекомендаций на местах в виде кратких блок-схем и чек-листов.
Ответственная за методологическое содержание руководства и формирование клинических рекомендаций по результатам обсуждения
Зурдинова А.А. - д.м.н., профессор, главный внештатный клинический фармаколог МЗ КР, специалист по ДМ
Ответственный исполнитель осуществлял систематизированный поиск имеющихся международных клинических руководств, критическую оценку найденных руководств, методологическая поддержка при формировании ключевых рекомендаций по представленной информации от МДРГ, формирование методологического содержания разработанного руководства.
Методологическая помощь
Матоморова А.А. - зав. отделом ДМиМТ, ЦРЗиМТ при МЗ КР
Оценка клинического содержания клинического руководства (рецензенты)
Узаков О.Ж.
Батырханов Ш.К.
Рецензенты проводили независимую оценку клинического руководства и алгоритмов по клиническому содержанию рекомендаций согласно обновленным данным по диагностике и лечению бронхиальной астмы с позиции наилучшей клинической практики, применяемой в других странах.
Оценка методологического качества клинического руководства
Шараева А.Т. - доцент каф. базисной и клинической фармакологии КРСУ, к.м.н., эксперт-методолог
Методологами была проведена оценка методологического качества клинического руководства по логическому изложению, отражению наилучшей клинической практики в рекомендациях и применимости в клинической практике на местах согласно инструменту AGREE II.
Декларация конфликта интересов
Никто из членов авторского коллектива не имел коммерческой заинтересованности или другого конфликта интересов с фармацевтическими компаниями или другими организациями, производящими продукцию для диагностики, лечения и профилактики бронхиальной астмы у детей.
СТРАТЕГИЯ ПОИСКА ИНФОРМАЦИИ
В связи с актуальностью проблемы на сегодняшний день в мире разработано и обновлено большое количество разнообразных клинических руководств, консенсусов, стандартов и пр., посвященных диагностике, лечению и ведению бронхиальной астмы у детей.
Рабочей мультидисциплинарной группой было принято решение о разработке национального клинического руководства по диагностике, лечению и ведению бронхиальной астмы у детей путем адаптирования уже разработанных международных клинических руководств высокого методологического качества, основанных на принципах доказательной медицины для всех уровней здравоохранения Кыргызской Республики.
ОПИСАНИЕ ПРОЦЕССА ПОИСКА И ОЦЕНКИ СУЩЕСТВУЮЩИХ КЛИНИЧЕСКИХ РУКОВОДСТВ ПО БРОНХИАЛЬНОЙ АСТМЕ У ДЕТЕЙ
Поиск клинических руководств по бронхиальной астме у детей осуществлялся в международных доступных электронных базах данных в сети Интернет.
Найденные электронные базы данных по клиническим руководствам и практическим рекомендациям
| Страна и название ресурса | Интернет - адрес |
| Международные организации | |
| GINA |
https://ginasthma.org/wp-content/uploads/2020/04/GINA-2020-full-report_-final-_wms.pdf
https://ginasthma.org/wp-content/uploads/2020/04/Main-pocket-guide_2020_04_03-final-wms.pdf
|
| Великобритания | |
| National Institute for Clinical Excellence (NICE) | https://www.nice.org.uk/guidance/ng80 |
| British Columbia | https://www2.gov.bc.ca/gov/content/health/practitioner-professional-resources/bc-guidelines/asthma-children#:~:text=Diagnosis%20and%20Management.-,Key%20Recommendations,medication%20daily%20and%20not%20intermittently. |
| Scottish Intercollegiate Guidelines Network (SIGN) | https://www.guidelines.co.uk/respiratory/sign-and-bts-management-of-asthma-in-children-guideline/454880.article |
| South West Devon Formulary Guide, NHS | https://southwest.devonformularyguidance.nhs.uk/formulary/chapters/3.-respiratory/asthma--paed |
| Европа | |
| Europe Respiratory Society | https://erj.ersjournals.com/content/early/2021/04/16/13993003.04173-2020 |
| Австралия | |
| The Royal Children’s Hospital Melbourne | https://www.rch.org.au/clinicalguide/guideline_index/Asthma_Acute/ |
| Россия | |
| Министерство здравоохранения РФ | https://spulmo.ru/upload/rekomendacyi_bronh_astma_21_23.pdf |
Дополнительный поиск информации не проводился, т.к. было найдено достаточно клинических руководств по диагностике и лечению бронхиальной астмы у детей.
Найденные клинические руководства были оценены мультидисциплинарной рабочей группой.
Критерии включения/исключения публикаций
В связи с тем, что изначально рабочая группа провела четкие ограничения по вопросам, которые необходимо было включать в клиническое руководство, в качестве опорных клинических руководств нами выбраны только те, которые были выполнены с применением принципов доказательной медицины, с учетом градации рекомендаций и уровнями доказательств и посвященные диагностике и лечению бронхиальной астмы у детей.
При подготовке руководства были установлены временные ограничения для клинических руководств с 2016 по 2021 год. Использовались руководства, разработанные для лечения БА у детей. Были установлены языковые ограничения, так как рабочая группа имела возможность изучать источники литературы только на английском и русском языках.
Оценка найденных клинических рекомендаций и доказательств
В результате проведённого поиска было найдено 4 клинических руководства, освещающих вопросы диагностики и лечения бронхиальной астмы у детей, которые содержали необходимую информацию, соответствующую задаче рабочей группы.
Характеристика отобранных клинических рекомендаций по бронхиальной астме у детей
| № | Название руководства | Качество | Новизна | Применимость | Варианты действий |
| 1 | Бронхиальная астма. Клинические рекомендации. МЗ Российской федерации, 2021 [3] | + | + | + | Отдельные рекомендации по классификации, МКБ-10, ведению БА |
| 2 | Британские рекомендации по диагностике и медикаментозному лечению астмы у детей, SIGN, 2019 [1] | + | + | + | Взята за основу при разработке, рекомендации по диагностике, лечению, профилактике БА |
| 3 | Руководство по лечению и профилактике астмы у взрослых и детей старше 5 лет, GINA, 2022 [4] | + | - | + | Отдельные рекомендации по диагностике и лечению БА |
| 4 | Астма: диагностика, мониторинг и лечение хронической астмы, NICE, 2021 [2] | + | + | + | Рекомендации диагностике, оценка тяжести и ведению БА |
Предпочтение для разработки руководства основывались на данных международных согласительных документов по БА – GINA, SIGN, NICE, РФ. По черновому варианту были получены комментарии и замечания специалистов. Обновление данного руководства предполагается по мере появления новых данных.
Так как в найденных клинических руководствах мультидисциплинарной рабочей группой были найдены необходимые рекомендации по диагностике, лечению и ведению бронхиальной астмы у детей (БА), то дополнительный поиск медицинских публикаций по результатам мета-анализов, систематических обзоров, РКИ и т.д. в международных базах не проводился.
Шкала уровней доказательности и градации рекомендаций
В связи с тем, что на сегодняшний день имеются доказательства по различным вмешательствам (диагностике, лечению и ведению) БА, основные клинические рекомендации представлены на основании рекомендаций выбранных международных руководств, которые были приняты за основу группой разработчиков национального руководства при обсуждении (с использованием метода Делфи).
Все ключевые рекомендации в клиническом руководстве выделены в рамки-боксы. Ключевые рекомендации с представлением их уровни доказательности и убедительности были адаптированы по шкале SIGN-50 на 4 уровня A, B, C, D.
Данное национальное клиническое руководство дополнено краткими клиническими протоколами для амбулаторного и стационарного уровней здравоохранения, алгоритмами, справочником лекарственных средств, чек-листами (см. Приложения 1-16).
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки |
| С | Когортное исследование или случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+) |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов |
Данное национальное клиническое руководство дополнено краткими клиническими протоколами для амбулаторного и стационарного уровней здравоохранения, алгоритмами, справочником лекарственных средств, чек-листами (см. Приложения 1-16).
Приложение 1.
ПИКФЛОУМЕТРИЯ: ПРИМЕНЕНИЕ И ТЕХНИКА
| Для диагностики БА важную роль играет измерение пиковой скорости выдоха, которая позволяет оценить препятствие воздушному потоку и помогает диагностировать астму, следить за ее течением. |
| Показатели пикфлуометрии важны, так как пациенты и врачи не всегда могут правильно оценить тяжесть симптомов астмы. |
| Устойчивое превышение показателя максимальной скорости выдоха более 80% от наилучшего индивидуального свидетельствует хорошем контроле БА. |
| А | Пикфлуометрия является наиболее удобным и информативным средством контроля за эффективностью лечения и решения вопроса о потребности в бронхолитиках при ежедневном фиксировании показателей максимальной скорости выдоха. |
| Кому показана пикфлоуметрия? Всем больным детям астмой старше 5 лет. |
 |
Пикфлоуметр - это портативный прибор, который служит для измерения пиковой скорости выдоха (ПСВ), т.е. максимальной скорости воздушного (МСВ) потока при форсированном выдохе.
Имеется большое разнообразие пикфлоуметров, но техника использования одинакова для всех. Для младших детей важно использовать пикфлоуметр, определяющий низкий поток. Производитель обычно указывает, на какой возраст рассчитан данный прибор.
|
Техника измерения ПСВ у детей:
|
Как определить индивидуальную норму ПСВ?
| С | При оценке ПСВ следует ориентироваться на среднестатистические нормы для данной популяции, а в идеале – на лучший показатель данного больного, измеренный в период стабильного состояния |
|
Должные значения ПСВ в зависимости от роста (л/мин)*
| Рост | 109 | 112 | 114 | 117 | 119 | 122 | 124 | 127 | 130 | 132 | 135 | 137 |
| ПСВ | 147 | 160 | 173 | 187 | 200 | 214 | 227 | 240 | 254 | 267 | 280 | 293 |
| Рост | 140 | 142 | 145 | 147 | 150 | 152 | 155 | 158 | 160 | 163 | 165 | 167 |
| ПСВ | 307 | 320 | 334 | 347 | 360 | 373 | 387 | 400 | 413 | 427 | 440 | 454 |
* Polger G., Promedhat V. Pulmonary Function Testing in Children: Techniques Standards. Philadelphia Pa; W.B. Saunders Company, 1971.
Величина показателей ПСВ зависит от тяжести обострения БА:
|
Приложение 2
СПИРОМЕТРИЯ
| Спирометрия – метод измерения легочных объемов или изменений легочных объемов по отношению к оси времени или потока. |
|
Основные спирометрические показатели:
|
| Результаты спирометрии выражаются в процентах от должной величины. В этих целях используются показатели нормы с учетом возраста, пола, веса, роста больного. Эти показатели информируют о наличии рестриктивных или обструктивных нарушений дыхания, а также об их выраженности. |
|
Показания для проведения спирометрии:
1. Диагностика заболеваний легких у детей старше 5 лет с бронхообструктивным синдромом.
2. Контроль эффективности лечения.
3. Данные спирометрии применяются в предоставлении инвалидности детям с тяжелой астмой.
|
|
Противопоказания для проведения спирометрии:
1. Острые респираторные инфекции – не менее двух недель после выздоровления (4 недели при пневмонии, вызванной атипичными возбудителями).
2. Детям младше 5 лет.
|
|
Подготовка больного к спирометрии:
Если исследование выполняется с диагностической целью, прием лекарственных препаратов должен быть прекращен за определенное время до исследования:
Если исследование проводится с целью контроля эффективности лечения, пациент должен продолжать прием назначенных ему лекарственных препаратов и в период исследования.
|
| Для исследования обратимости обструкции проводится проба с КДБА (сальбутамолом) в разовой дозе 400 мкг. Дозированные аэрозольные ингаляторы должны использоваться со спейсером. Повторное спирометрическое исследование необходимо провести через 15–30 мин после ингаляции КДБА [1]. |
| Бронходилатационный тест считается положительным, если после ингаляции бронходилататора коэффициент бронходилатации (КБД) по ОФВ1 составляет не менее 12%, и при этом абсолютный прирост составляет 200 мл и более [1]. |
|
Формула для расчета КБД:
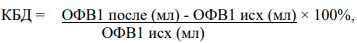
где ОФВ1 исх - значение спирометрического показателя до ингаляции бронходилататора, ОФВ1 после - значение показателя после ингаляции бронходилататора.
Абсолютный прирост (мл) = ОФВ1 после(мл) - ОФВ1 исх(мл).
|
| Тесты на обратимость с применением бронходилататоров или терапевтические пробы с применением ИГКС у диагностически неясных пациентов должны проводиться с применением одного и более объективных методов оценки. |
| Использование ОФВ1 или ПСВ как основных методов оценки обратимости или ответа на терапию находит более широкое использование у пациентов с исходной бронхиальной обструкцией. Использование данных параметров у пациентов с исходно нормальными показателями легочной функции ограничено в применении, т.к. в этом случае отсутствует резерв улучшения этих параметров. |
| Прирост ОФВ1 ≥ 200 мл или 12% в ответ на пробу с β2-агонистом или терапевтический курс кортикостероида может служить подтверждением диагноза БА. Пробное прекращение терапии может оказывать помощь в случае сомнений. |
Приложение 3.
ПЕРЕЧЕНЬ ФАКТОРОВ РИСКА И МЕРОПРИЯТИЯ ПО УДАЛЕНИЮ ПРИЧИН ОБОСТРЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ
| Факторы риска | Действия |
| Пищевые аллергены | При наличии сенсибилизации исключить пищевые продукты с высокой аллергизирующей активностью: коровье молоко, рыба, яйца, орехи, мед, грибы, мясо птиц, клубника, черная смородина, ежевика, малина, дыня, хурма, гранаты, шоколад, кофе, какао, горчица, виноград. |
| Аллергены клеща домашней пыли |
- Удаление коллекторов пыли в жилых комнатах (мягкая мебель, мягкие игрушки, шерстяные ковры, книги на открытых полках).
- Проведение антикарицидных мероприятий (покрытие подушек, матрацев непроницаемым синтетическим материалом, еженедельная стирка белья, уборка пылесосом, инсоляция/замораживание постельных принадлежностей.
|
| Табачный дым (если пациент курит активно или пассивно) | Избегать контакта с табачным дымом. Пациенты и их родители не должны курить. |
| Аллергены животных |
- Удалить животных из дома или хотя бы из спальни.
- Регулярное купание домашнего животного.
|
| Аллергены тараканов |
- Тщательно и часто убирать дом.
- Использовать пестициды, однако при этом надо убедиться, что ребенка нет дома во время обработки.
|
| Аллергены пыльцы растений |
- Закрытие окон и форточек в дневное время, отсутствие букетов и цветущих растений в жилых комнатах.
- Не выходить на улицу в солнечную, сухую и ветреную погоду.
- Носить солнцезащитные очки.
- Уменьшение выездов за город и отказ от прогулок в парках.
- Войдя в помещение принять душ (или обмыть открытые участки тела) и сменить одежду
|
| Грибковые аллергены Плесень внутри помещения | При наличии сенсибилизации исключить из рациона питания продукты, содержащие грибки: острые сыры, квашенные, соленые или моченые овощи (капуста, огурцы, помидоры, грибы, яблоки, др.), квас и пиво, копченое мясо и рыбу, шампанское, вино, виноград, сухофрукты, кисломолочные продукты, дрожжевое тесто и черный хлеб. Уменьшить влажность в доме. Обеспечить хорошую вентиляцию. Удалить домашние цветы. |
| Физическая активность | Не ограничивать физическую активность ребенка. При наличии обострений болезни, связанных с физической нагрузкой, с профилактической целью рекомендуется прием β2-агонистов короткого действия |
| Лекарства | Следует избегать, если их применение вызывают симптомы болезни. |
ПЕРВИЧНАЯ ПРОФИЛАКТИКА БРОНХИАЛЬНОЙ АСТМЫ
| Мероприятия | Результаты исследований | Рекомендации |
| Элиминация аллергена | Данные об эффективности влияния мероприятий по обеспечению гипоаллергенного режима внутри жилья на вероятность развития БА противоречивы. | Нет достаточных доказательств для рекомендаций. |
| Кормление грудью | Существуют доказательства протективного эффекта в отношении раннего развития БА. | Грудное кормление должно поощряться из-за многих его преимуществ. Оно может играть роль в предотвращении раннего развития БА у детей |
| Молочные смеси | Нет исследований достаточной продолжительности по влиянию применения молочных смесей на раннее развитие БА. | В отсутствие доказанных преимуществ молочных смесей нет основания рекомендовать их использование как стратегию предотвращения БА у детей. Алгоритм назначения молочных смесей определяется отсутствием или наличие аллергии к белкам коровьего молока у ребенка |
| Пищевые добавки | Существует очень ограниченное число исследований потенциального протективного эффекта рыбьего жира, селена и витамина Е, принимаемых во время беременности. | Нет достаточных доказательств для рекомендаций каких-либо дополнений к диете беременных как средства профилактики БА. |
| Иммунотерапия (специфическая иммунотерапия) АСИТ | Необходимо большее число исследований для подтверждения роли иммунотерапии в профилактике развития БА. | АСИТ может предотвращать развитие БА у лиц с аллергическим ринитом. |
| Микроорганизмы | Ключевая область для исследований с длительным периодом наблюдения для того, чтобы установить эффективность в отношении профилактики БА. | Нет достаточных доказательств того, что использование пробиотиков матерью во время беременности снижает риск развития БА у ребенка. |
| Отказ от курения | Исследования выявляют ассоциацию между курением матери и увеличением риска заболевания ребенка. | Родителям и будущим матерям должны быть даны советы в отношении неблагоприятного влияния курения на ребенка, в том числе и риска развития БА. |
ДИЕТИЧЕСКИЕ РЕКОМЕНДАЦИИ ПРИ БРОНХИАЛЬНОЙ АСТМЕ
| Мероприятия | Результаты исследований | Рекомендации |
| Пищевые продукты и добавки | Сульфиты (консерванты, которые часто входят в состав лекарств и таких пищевых продуктов как картофельные чипсы, креветки, сухофрукты, пиво и вино) нередко причастны к развитию тяжелых обострений БА | В случае доказанной аллергии на пищевой продукт или пищевую добавку исключение этого продукта может привести к снижению частоты обострений БА. |
| Ожирение | Исследования показывают взаимосвязь между увеличением массы тела и симптомами БА | Пациентам с избыточной массой тела рекомендуется снижение веса для улучшения состояния здоровья и течения БА. |
ВТОРИЧНАЯ ПРОФИЛАКТИКА БРОНХИАЛЬНОЙ АСТМЫ
| Мероприятия | Результаты исследований | Рекомендации |
| Поллютанты | Исследования показывают взаимосвязь между загрязнением воздуха (повышение концентрации озона, окислов азота, аэрозолей кислот и взвесей твердых частиц) и ухудшением течения БА. | У пациентов с контролируемой БА обычно отсутствует необходимость избегать неблагоприятных условий внешней среды. Больным с плохо контролируемой БА рекомендуется воздержаться от интенсивной физической нагрузки в холодную погоду, при пониженной атмосферной влажности, высоком уровне загрязнения воздуха. |
| Клещи домашней пыли | Меры по снижению концентрации клеща домашней пыли помогают уменьшить количество клещей, но нет доказательств изменения тяжести течения БА при снижении их концентрации. | В активно настроенных семьях могут быть полезны комплексные меры по уменьшению концентрации клеща домашней пыли. |
| Домашние животные | Нет контролируемых исследований, посвященных уменьшению тяжести БА после удаления домашних животных. Однако если в семье есть больной БА, заводить домашнее животное не стоит. | Нет оснований для дачи рекомендаций. |
| Курение | Активное и пассивное курение оказывает негативное влияние на качество жизни, функцию легких, потребность в препаратах неотложной помощи и долговременный контроль при использовании ингаляционных стероидов | Пациентам и членам их семей необходимо объяснять опасность курения для больных БА и оказывать помощь в отказе от курения. |
| Аллерген-специфическая иммунотерапия | Проведение специфической иммунотерапии положительно влияет на течение БА. | Необходимость иммунотерапии должна рассматриваться у пациентов с БА при невозможности избегать экспозиции клинически значимого аллергена. Необходимо информировать пациента о возможности серьезных аллергических реакций на иммунотерапию |
Приложение 4
ОЦЕНКА КОНТРОЛЯ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ
АСТ-тест (Asthma Control Test) - опросник для определения уровня контроля БА
| Оценивают за последние 4 недели (1 месяц). |
Тест по контролю над астмой у детей в возрасте 4-11 лет
(Children Asthma Control Test)
|
| Вопрос | Ответы | Баллы |
| 1. Как у тебя дела с астмой сегодня? | Очень плохо | 0 |
| Плохо | 1 | |
| Хорошо | 2 | |
| Очень хорошо | 3 | |
| 2. Как сильно астма мешает тебе бегать, заниматься физкультурой? | Очень мешает, я совсем не могу делать то, что мне хочется | 0 |
| Мешает, и это меня расстраивает | 1 | |
| Немножко мешает, но это ничего | 2 | |
| Не мешает | 3 | |
| 3. Кашляешь ли ты из-за астмы? | Да, все время | 0 |
| Да, часто | 1 | |
| Да, иногда | 2 | |
| Нет, никогда | 3 | |
| 4. Просыпаешься ли ты по ночам из-за астмы? | Да, все время | 0 |
| Да, часто | 1 | |
| Да, иногда | 2 | |
| Нет, никогда | 3 | |
| На следующие вопросы ответьте самостоятельно, без участия ребенка. | ||
| 5. Как часто за последние 4 недели Ваш ребенок испытывал какие-либо симптомы астмы в дневное время? | Ни разу | 5 |
| 1-3 дня | 4 | |
| 4-10 дней | 3 | |
| 11-18 дней | 2 | |
| 19-24 дня | 1 | |
| Каждый день | 0 | |
| 6. Как часто за последние 4 недели у Вашего ребенка было свистящее дыхание из-за астмы в дневное время? | Ни разу | 5 |
| 1-3 дня | 4 | |
| 4-10 дней | 3 | |
| 11-18 дней | 2 | |
| 19-24 дня | 1 | |
| Каждый день | 0 | |
| 7. Как часто за последние 4 недели Ваш ребенок просыпался по ночам из-за астмы? | Ни разу | 5 |
| 1-3 дня | 4 | |
| 4-10 дней | 3 | |
| 11-18 дней | 2 | |
| 19-24 дня | 1 | |
| Каждый день | 0 | |
Оценка результатов АСТ теста
|
|
Если Ваш ребенок набрал 19 баллов или меньше, это может означать, что его астма контролируется недостаточно эффективно.
|
|
Если Ваш ребенок набрал 20 баллов или больше, возможно, его астму удается эффективно контролировать. Однако при оценке контроля астмы лечащий врач Вашего ребенка может принимать во внимание и другие факторы. Поэтому следует поговорить с врачом о том, как чувствует себя Ваш ребенок в связи с астмой.
Астма непредсказуема. Может казаться, что симптомы астмы у ребенка легкие, или, что их совсем нет; однако они могут ярко проявиться в любой момент.
|
Тест по контролю над астмой у детей от 12 лет и старше
(Children Asthma Control Test)
| Дети от 12 лет и старше отвечают на все вопросы самостоятельно. |
| Вопрос | Ответы | Баллы |
| 1. Как часто за последние 4 недели астма мешала Вам выполнять обычный объем работы в учебном заведении, на работе или дома? | Все время | 1 |
| Очень часто | 2 | |
| Иногда | 3 | |
| Редко | 4 | |
| Никогда | 5 | |
| 2. Как часто за последние 4 недели Вы отмечали у себя затрудненное дыхание? | Чаще, чем раз в неделю | 1 |
| Раз в день | 2 | |
| От 3-х до 6-ти раз | 3 | |
| 1 или 2 раза в неделю | 4 | |
| Ни разу | 5 | |
| 3. Как часто за последние 4 недели Вы просыпались ночью или раньше обычно из-за симптомов астмы (свистящего дыхания, кашля, затрудненного дыхания, чувства стеснения или боли в груди)? | 4 ночи в неделю или чаще | 1 |
| 2-3 ночи в неделю | 2 | |
| Раз в неделю | 3 | |
| 1 или 2 раза | 4 | |
| Ни разу | 5 | |
| 4. Как часто за последние 4 недели Вы использовали быстродействующий ингалятор (например: Вентолин, Сальбутамол, Саламол, Беродуал, Беротек, Атровен) или небулайзер с лекарством (Беродуал, Вентолин, Беротек или др.)? | 3 раза в день или чаще | 1 |
| 1 или 2 раза в день | 2 | |
| 2 или 3 раза в неделю | 3 | |
| 1 раз в неделю или реже | 4 | |
| Ни разу | 5 | |
| 5. Как бы Вы оценили, насколько Вам удалось контролировать астму за последние 4 недели? | Совсем не удалось контролировать | 1 |
| Плохо удавалось контролировать | 2 | |
| В некоторой степени удавалось контролировать | 3 | |
| Хорошо удавалось контролировать | 4 | |
| Полностью удавалось контролировать | 5 |
Оценка результатов АСТ теста
|
В каждом вопросе выберите ответ по 5 бальной системе, сложите баллы и запишите полученный итоговый балл.
Принесите тест на прием к врачу и обсудите с ним итоговый балл.
|
|
Если Ваш ребенок набрал 19 балов или меньше, это может означать, что его астма контролируется недостаточно эффективно.
|
|
Если Ваш ребенок набрал 20 балов или больше, возможно, его астму удается эффективно контролировать. Однако при оценке контроля астмы лечащий врач Вашего ребенка может принимать во внимание и другие факторы. Поэтому следует поговорить с врачом о том, как чувствует себя Ваш ребенок в связи с астмой.
Астма непредсказуема. Может казаться, что симптомы астмы у ребенка легкие, или, что их совсем нет; однако они могут ярко проявиться в любой момент.
|
УРОВНИ КОНТРОЛЯ СИМПТОМОВ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ ДО 6 ЛЕТ
| Уровни контроля | |||
| В течение последних 4-х недель ребенок имел: |
Хороший
контроль
|
Частичный контроль |
Нет
контроля
|
| Дневные симптомы более чем несколько минут, более чем 1 раз в неделю | Ничего из перечисленного | 1-2 симптома | 3-4 симптома |
| Ограничивает ли астма физическую активность (бегает/играет меньше других детей, легче устает во время прогулки/игры) | |||
| Использование препаратов для купирования симптомов более чем один раз в неделю | |||
| Наличие ночных пробуждения или ночного кашля из-за астмы | |||
ОЦЕНКА КОНТРОЛЯ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ СТАРШЕ 6 ЛЕТ, ПОДРОСТКОВ И ВЗРОСЛЫХ
| А. Контроль симптомов астмы | ||||
| Уровень контроля | ||||
| За последние 4 недели у пациента отмечались: | Хорошо контролируемая | Частично контролируемая | Не контролируемая | |
| Дневные симптомы чаще, чем 2 раза в неделю | ДА ☐ НЕТ☐ | Ничего из перечисленного | 1-2 из перечисленного | 3-4 из перечисленного |
| Ночные пробуждения из-за БА | ДА ☐ НЕТ☐ | |||
| Потребность в препарате для купирования симптомов чаще, чем 2 раза в неделю | ДА ☐ НЕТ☐ | |||
| Любое ограничение активности из-за БА | ДА ☐ НЕТ☐ | |||
| В. Факторы риска для неблагоприятных исходов | ||||
|
Оценивать факторы риска с момента постановки диагноза и периодически, особенно у пациентов с обострениями.
Функция легких не учитывается при оценке контроля симптомов (но снижение ОФВ1 учитывается как фактор риска обострений).
Измерять функцию легких в начале терапии, затем спустя 3-6 месяцев лечения препаратами для длительного контроля с целью определения лучшего персонального ОФВ1 пациента, и затем периодически для оценки риска.
|
||||
Другие важные независимые факторы риска обострений:
|
||||
|
Факторы риска для развития фиксированной обструкции дыхательных путей:
|
||||
|
Факторы риска для развития нежелательных побочных эффектов лекарств:
|
||||
Приложение 5
ИНГАЛЯЦИОННАЯ ТЕХНИКА
| В | Рекомендуется назначать ингаляторы только после того, как пациенты прошли обучение по использованию устройства и показали удовлетворительную технику ингаляции [1]. |
| D | Выбор ингаляционного устройства для терапии стабильной БА рекомендуется основывать на предпочтении пациента и оценке правильности использования ингалятора [1]. |
| В | При назначении пациентам с БА тиотропия бромида** (Код АТХ: R03BB04) в качестве средства доставки рекомендуется использовать жидкостной ингалятор [1]. |
| В | У детей от 0 до 5 лет в качестве предпочтительного способа доставки бронхолитиков или ИГКС рекомендуется ДАИ + спейсер [1]. |
Краткая характеристика основных способов доставки ингаляционных лекарственных средств и техника ингаляций
|
Основные преимущества ингаляционного введения ЛС следующие:
|
|
Недостатки дозированных ингаляторов включают слишком высокую скорость ингаляции, в результате чего большая часть ингалируемой дозы оседает в ротоглотке, невозможность назначения больших доз препарата и сложность ингаляционной техники. Считается, что около 70-80% детей имеют трудности при использовании препарата в виде дозированного аэрозоля.
Для устранения данных недостатков были разработаны различные устройства, предназначенные для уменьшения зависимости эффективности доставки препарата от техники ингаляции: спейсер, спейсер с лицевой маской.
|
|
Системы для ингаляционного введения препаратов:
|
| А |
Выбор типа ингалятора для детей с бронхиальной астмой
(с учетом эффективности доставки препарата, экономической эффективности, безопасности, простоты и удобства применения)
|
| Возрастная группа | Предпочтительный тип ингалятора | Альтернативный тип ингалятора |
| Младше 4-х лет | ДАИ плюс соответствующий спейсер с лицевой маской | Небулайзер с лицевой маской |
| 4-6 лет | ДАИ плюс соответствующий спейсер с мундштуком | Небулайзер с мундштуком |
| Старше 6 лет | ДПИ, или активируемый с дыханием ДАИ, или ДАИ со спейсером и мундштуком | Небулайзер с мундштуком |
|
Техника проведения ингаляции с помощью ДАИ:
|
|
Рекомендуется применение ДАИ со спейсером.
Использование спейсера:
|
|
Техника ингаляции через спейсер:
Оптимальной техникой ингаляции аэрозоля через спейсер является глубокий медленный вдох или два спокойных глубоких вдоха (до 4-5 вдохов для детей) после высвобождения одной дозы в камеру спейсера, или даже обычное спокойное дыхание для детей.
|
|
Методика изготовления самодельного спейсера:
Для детей до 5 лет спейсер, который охватывает нос и рот ребенка можно изготовить в домашних условиях из пластиковой бутылки:
1. Взять 1 литровую пластиковую бутылку.
2. Отрезать от дна бутылки часть объемом в 250 мл (1/4 часть бутылки).
3. Получится емкость объемом 750 мл.
4. Срезанный край обработать (обклеить) лейкопластырем.
Для детей старше 5 лет спейсер в домашних условиях изготавливается следующим образом:
1. Взять 1 литровую пластиковую бутылку.
2. Сделать отверстие на дне бутылки и вставить аэрозольный ингалятор.
|
|
Бэбихалеры:
|
|
ДПИ (дозирующий порошковый ингалятор):
В настоящее время существуют следующие виды ДПИ: мультидиск, турбухалер, дискхалер, аэролайзер
|
|
Небулайзеры:
Типы небулайзеров:
- компрессорные (воздушные)
- ультразвуковые
Ингаляцию препарата с помощью небулайзера осуществляют в течение 5 мин. При удлинении времени ингаляции от 5 до 10 мин достигается лишь небольшой дополнительный эффект.
Небулайзер применяется преимущественно при обострении тяжёлой БА.
|
|
Техника использования небулайзера:
|
|
Особенности применения небулайзера:
|
|
Не рекомендуется использовать для небулайзеров:
|
Приложение 6
Сравнительные эквипотентные суточные дозы (мкг) ИГКС для базисной терапии БА у взрослых и подростков СТАРШЕ 12 ЛЕТ
Это НЕ таблица эквивалентности. Это предложенные общие суточные дозы для вариантов лечения «низкой», «средней» и «высокой» дозой различными ИГКС.
| Препарат |
Низкие
суточные доза
|
Средние суточные дозы | Высокие суточные дозы |
| Беклометазона дипропионат ДАИ неэкстрамелкодисперсный | 200-500 | >500-1000 | >1000 |
| Беклометазона дипропионат ДАИ экстрамелкодисперсный | 100-200 | >200-400 | >400 |
| Будесонид ДАИ, ДПИ | 200-400 | >400-800 | >800 |
| Циклесонид ДАИ | 80-160 | >160-320 | >320 |
| Флутиказона фуроат, ДПИ | 100 | 200 | |
| Флутиказона пропионат ДАИ, ДПИ | 100-250 | >250-500 | >500 |
| Мометазона фуроат, ДПИ* | 200 | 400 | |
| Мометазон ДПИ* | 110-220 | >220-440 | >440 |
Это НЕ таблица эквивалентности. Это предложенные общие суточные дозы для вариантов лечения «низкой», «средней» и «высокой» дозой различными ИГКС.
* Препарат не зарегистрирован в КР
Сравнительные эквипотентные суточные дозы (мкг) ИГКС для базисной терапии БА у детей 6-11 ЛЕТ
| Препарат |
Низкие
суточные доза
|
Средние суточные дозы | Высокие суточные дозы |
| Беклометазона дипропионат ДАИ неэкстрамелкодисперсный | 100-200 | >200-400 | >400 |
| Беклометазона дипропионат ДАИ экстрамелкодисперсный | 50-100 | >100-200 | >200 |
| Будесонид, ДПИ | 100-200 | >200-400 | >400 |
| Будесонид суспензия для ингаляции через небулайзер | 250-500 | >500-1000 | >1000 |
| Циклесонид, ДАИ | 80 | >80-160 | >160 |
| Флутиказона фуроат, ДПИ | 50 | Не применяется | |
| Флутиказона пропионат ДПИ | 50-100 | >100-200 | >200 |
| Флутиказона пропионат ДАИ | 50-100 | >100-200 | >200 |
| Мометазона фуроат, ДАИ | 100 | 200 | |
Это НЕ таблица эквивалентности. Это предложенные общие суточные дозы для вариантов лечения «низкой», «средней» и «высокой» дозой различными ИГКС.
* Препарат не зарегистрирован в КР
Сравнительные эквипотентные суточные дозы (мкг) ИГКС для базисной терапии БА у детей 5 ЛЕТ И МЛАДШЕ
| Препарат | Низкая общая суточная доза (мкг) (возрастная группа в соответствии адекватными данными о безопасности и эффективности в данной |
| Беклометазона дипропионат ДАИ неэкстрамелкодисперсный | 100 (возраста 5 лет и старше) |
| Беклометазона дипропионат ДАИ экстрамелкодисперсный | 50 (возраст 5 лет и старше) |
| Будесонид суспензия для ингаляции через небулайзер | 500 (возраст 1 год и старше) |
| Флутиказона пропионат ДПИ | 50 (возраст 4 года и старше) |
| Флутиказона фуроат, ДПИ | Не изучено у детей 5 лет и младше |
| Мометазона фуроат, ДАИ | 100 (возраст 5 лет и старше) |
| Циклесонид, ДАИ | Не изучено у детей 5 лет и младше |
Это НЕ таблица эквивалентности. Это предложенные общие суточные дозы для вариантов лечения «низкой», «средней» и «высокой» дозой различными ИГКС.
* Препарат не зарегистрирован в КР
Приложение 7
ПЕРЕЧЕНЬ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ И МЕДИЦИНСКОГО ОБОРУДОВАНИЯ
Приложение 8
Носовые канюли установите неглубоко в просвет ноздрей и закрепите с помощью клейкой ленты на щеках (см. рисунок). Следите за тем, чтобы ноздри были свободны от слизи, которая может заблокировать поток кислорода.
 Носоглоточный катетер. Катетер калибра 6 или 8 (по шкале Шарьера), введите в глотку прямо под уровнем язычка мягкого нёба. Вводите катетер на глубину, равную расстоянию от края ноздри до козелка ушной раковины (см. рисунок). Если ввести катетер слишком глубоко, это может вызвать рвотные позывы с рвотой и, редко, вздутие желудка.
Носоглоточный катетер. Катетер калибра 6 или 8 (по шкале Шарьера), введите в глотку прямо под уровнем язычка мягкого нёба. Вводите катетер на глубину, равную расстоянию от края ноздри до козелка ушной раковины (см. рисунок). Если ввести катетер слишком глубоко, это может вызвать рвотные позывы с рвотой и, редко, вздутие желудка.
Наблюдение
Проверяйте состояние ребенка по крайней мере каждые 3 часа:
|
Первичный уровень
здравоохранения
|
Вторичный, третичный уровень здравоохранения |
| Лекарственные препараты | |
|
- КДБА (ДАИ, небулы и раствор для небулайзерной терапии)
- преднизолон (табл.) - преднизолон (амп.) - дексаметазон (амп.)
- ИГКС (беклометазон)
- комбинированные ИГКС + ДДБА
- антилейкотриеновые препараты
|
- КДБА (ДАИ, небулы и раствор для небулайзерной терапии)
- комбинированные бронходилятаторы – беродуал (раствор для ингаляций, небулы)
- преднизолон (табл.) - преднизолон (амп.)
- дексаметазон (амп.)
- ИГКС (беклометазон - ДАИ, будесонид - небулы)
- комбинированные ИГКС + ДДБА
- антилейкотриеновые препараты
- аминофиллин (амп.)
- эпинефрин (адреналин)
- магния сульфат 25% (амп.)
- кислород
|
| Медицинское оборудование | |
|
- спейсеры, бэбихалер
- мешки Амбу с детскими масками
- пикфлоуметр
- небулайзер
- часы с секундомером
- пульсоксиметр
- кислородный концентратор
- спирометр по доступности
- весы
- ростомер
- фонендоскопы
|
- небулайзеры
- спейсеры, бэбихалер
- весы
- ростомер
- таймеры
- электрокардиограф
- рентген
- кислородный концентратор
- носовые канюли
- пульсоксиметр
- спирометр
- НИВЛ аппарат (СРАР, ВРАР)
- ИВЛ аппарат
- прикроватный монитор
- мешки Амбу с детскими масками - электроотсос
- газовый анализатор
- фонендоскопы
|
Приложение 8
КИСЛОРОДОТЕРАПИЯ

Носовые канюли установите неглубоко в просвет ноздрей и закрепите с помощью клейкой ленты на щеках (см. рисунок). Следите за тем, чтобы ноздри были свободны от слизи, которая может заблокировать поток кислорода.
Установите скорость подачи кислорода 1–2 л/мин (0,5 л/мин для младенцев раннего возраста), обеспечьте концентрацию кислорода на вдохе максимально до 40%. При использовании носовых канюль увлажнения кислорода не требуется.
Носовой катетер. Катетер калибра 6 или 8 (по шкале Шарьера), введите в заднюю часть носовой полости. Вводите катетер на глубину, равную расстоянию от края ноздри до внутренней границы брови. Установите скорость подачи кислорода 1–2 л/мин. При использовании носового катетера увлажнения кислорода не требуется.
 Носоглоточный катетер. Катетер калибра 6 или 8 (по шкале Шарьера), введите в глотку прямо под уровнем язычка мягкого нёба. Вводите катетер на глубину, равную расстоянию от края ноздри до козелка ушной раковины (см. рисунок). Если ввести катетер слишком глубоко, это может вызвать рвотные позывы с рвотой и, редко, вздутие желудка.
Носоглоточный катетер. Катетер калибра 6 или 8 (по шкале Шарьера), введите в глотку прямо под уровнем язычка мягкого нёба. Вводите катетер на глубину, равную расстоянию от края ноздри до козелка ушной раковины (см. рисунок). Если ввести катетер слишком глубоко, это может вызвать рвотные позывы с рвотой и, редко, вздутие желудка.
Установите скорость подачи кислорода 1–2 л/мин, чтобы избежать вздутия желудка. Требуется увлажнение кислорода.
Наблюдение
| Регулярно проверяйте правильность функционирования оборудования и вынимайте и мойте канюли по крайней мере 2 раза в день. |
Проверяйте состояние ребенка по крайней мере каждые 3 часа:
| Уровень насыщения крови кислородом с помощью пульсоксиметрии. |
| Проверить не сместились ли носовые канюли. |
| Проверьте герметичность системы подачи кислорода. |
| Проверить правильность скорости подачи кислорода. |
| Проверить нет ли закупоривания дыхательных путей слизью (прочистите нос с помощью влажной марлевой турунды или осторожным отсасыванием). |
|
Пульсоксиметрия - нормальный уровень насыщения артериальной крови кислородом (SaO2) в местности, расположенной на уровне моря, у ребенка составляет 95–100%.
Кислород назначить при уровне SaO2 < 90% (измеряется при комнатной температуре).
На основании показаний пульсоксиметра дозировать поток кислорода до достижения стабильного уровня SaO2 > 90% без расходования излишнего объема кислорода.
|
Продолжительность кислородотерапии
| Продолжайте постоянно давать кислород до тех пор, пока у ребенка не будет поддерживаться уровень SaO2 > 90% при комнатной температуре. |
| Если состояние ребенка стабильное и улучшается, прервите подачу кислорода на несколько минут. |
| Если уровень SaO2 остается выше 90%, отключите кислород. |
| Проверьте уровень SaO2 через 30 минут. |
| Проверяйте уровень SaO2 каждые 3 часа в течение первых суток после отмены кислородотерапии и убедитесь, что состояние ребенка остается стабильным. |
Если у вас нет пульсоксиметра, необходимую продолжительность кислородотерапии определить по клиническим признакам*:
|
* в диагностическом плане менее надежны.
Приложение 9
ДНЕВНИК САМОНТРОЛЯ
ПЛАН ЛЕЧЕНИЯ| Ф.И.О. пациента | |
| Врач | |
| Дата | |
| Телефон врача |
| Дата составления | План рассчитан до |
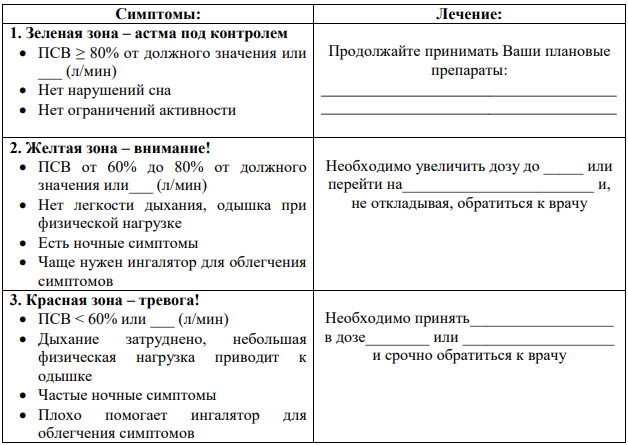
| Врач | Телефон |
|
Правила пользования пикфлоуметром:
|
ГРАФИК ПИКФЛОУМЕТРИИ
(пример заполнения)
Дата октябрь 2022 г. (месяц, год)
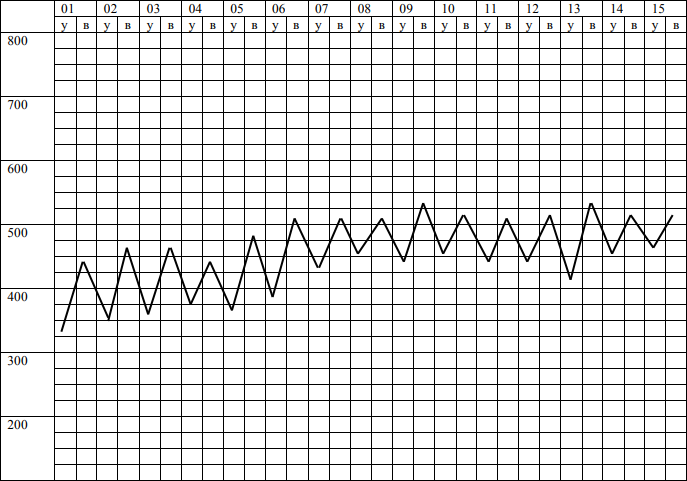
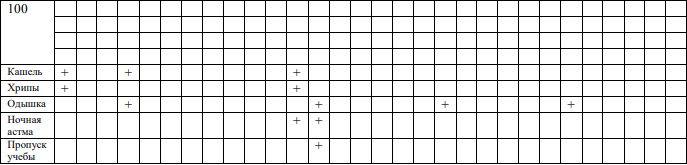
Приложение 10


| Препарат | Доза в сутки | Когда | |
| Облегчающее лекарство | Сальбутамол | 100 мкг в сутки | При удушье |
|
Базовое
лекарство
|
Серетид | 25/125 мкг по 2 вдоха 2 раза в сутки | Постоянно |
| Для заметок |
Приложение 10
ПРОТОКОЛ ПЕРВИЧНОГО ОСМОТРА ВРАЧА ДЛЯ ПОСТУПАЮЩИХ
В СТАЦИОНАР
(ЧЕК-ЛИСТ)
| ФИО пациента | |
| Дата и время осмотра |
ПРИЗНАКИ ХАРАКТЕРНЫЕ ДЛЯ ПОСТАНОВКИ ДИАГНОЗА «БРОНХИАЛЬНАЯ АСТМА»:
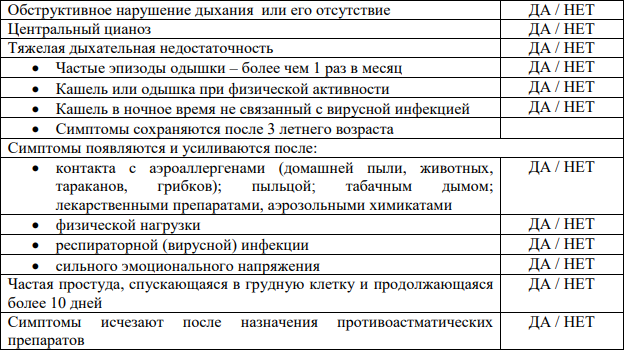
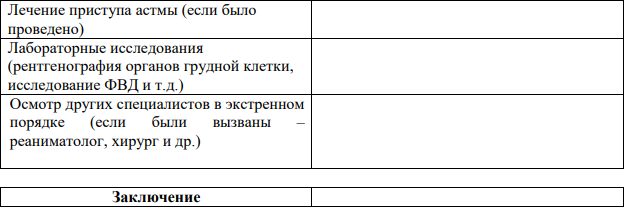
Приложение 11
АЛГОРИТМ ДИАГНОСТИКИ, ЛЕЧЕНИЯ И ВЕДЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ НА АМБУЛАТОРНОМ УРОВНЕ ЗДРАВООХРАНЕНИЯ
АЛГОРИТМ ЛЕЧЕНИЯ
ОБОСТРЕНИЯ АСТМЫ В АМБУЛАТОРНЫХ УСЛОВИЯХ
У ДЕТЕЙ 6-11 ЛЕТ
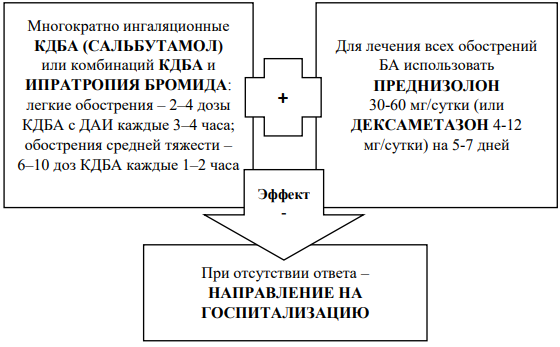
АЛГОРИТМ ЛЕЧЕНИЯ
ОБОСТРЕНИЯ АСТМЫ В АМБУЛАТОРНЫХ УСЛОВИЯХ
У ДЕТЕЙ 5 ЛЕТ И МЛАДШЕ
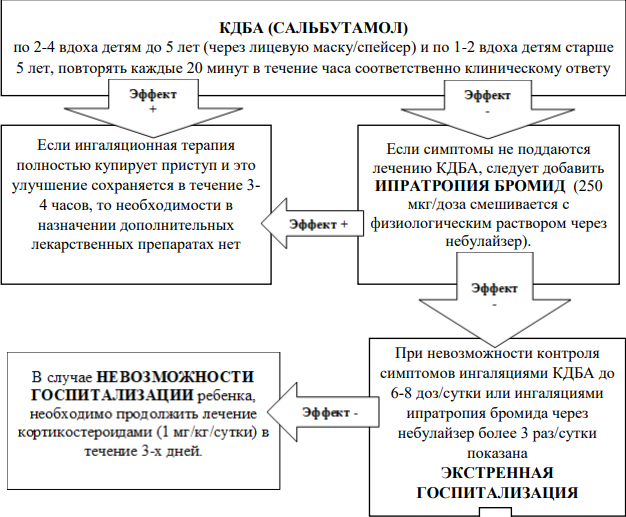

Приложение 12
АЛГОРИТМ ДИАГНОСТИКИ, ЛЕЧЕНИЯ И ВЕДЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ НА СТАЦИОНАРНОМ УРОВНЕ ЗДРАВООХРАНЕНИЯ
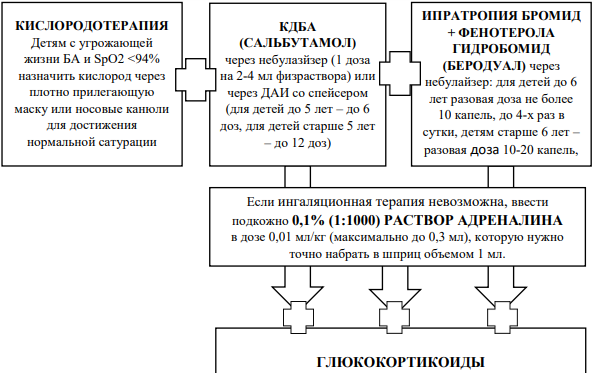
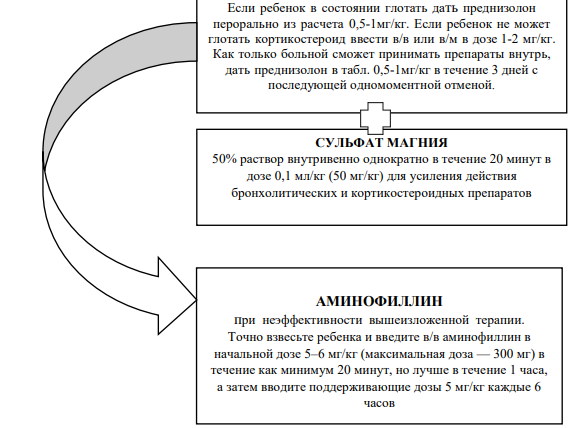


СТАЦИОНАРНЫЙ УРОВЕНЬ




БИБЛИОГРАФИЯ
Дополнительная литература


Приложение 13
СТАНДАРТЫ И ИНДИКАТОРЫ ДЛЯ МОНИТОРИНГА И АУДИТА
ВНЕДРЕНИЯ КЛИНИЧЕСКОГО РУКОВОДСТВА ПО БРОНХИАЛЬНОЙ АСТМЕ
АМБУЛАТОРНЫЙ УРОВЕНЬ


СТАЦИОНАРНЫЙ УРОВЕНЬ




БИБЛИОГРАФИЯ
Базисная литература
1. Британские рекомендации по диагностике и медикаментозному лечению астмы у детей, SIGN, 2019.
2. Астма: диагностика, мониторинг и лечение хронической астмы, NICE, 2021
3. Бронхиальная астма. Клинические рекомендации. Сокращенный вариант. МЗ Российской федерации. МОО Российское респираторное общество. Российская Ассоциация Аллергологов и Клинических иммунологов Союз педиатров России. Москва. 2021.
4. Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention, 2022.
Дополнительная литература
5. Карманный справочник «Оказание стационарной помощи детям. Руководство по ведению наиболее распространенных болезней детского возраста». Всемирная организация здравоохранения. Второе издание. Бишкек. 2017.
6. Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention for adults and children older than 5 years. A Pocket Guide For Health Professionals. Updated May 2022.
7. icd.who.int/browse10/2019/en (официальный сайт МКБ-10 на сайте Всемирной организации здравоохранения).
8. Akenroye AT, Wood R, Keet C. Asthma, biologics, corticosteroids, and coronavirus disease 2019. Ann Allergy Asthma Immunol 2020; 125:12. 9. Crimi C, Impellizzeri P, Campisi R, et al. Practical considerations for spirometry during the COVID-19 outbreak: Literature review and insights. Pulmonology 2021; 27:438.
10. Hussein MH, Elshazli RM, Attia AS, et al. Asthma and COVID-19; different entities, same outcome: a meta-analysis of 107,983 patients. J Asthma 2021; :1.
11. Rosenthal JA, Awan SF, Fintzi J, et al. Asthma is associated with increased risk of intubation but not hospitalization or death in coronavirus disease 2019. Ann Allergy Asthma Immunol 2021; 126:93.
12. Yang JM, Koh HY, Moon SY, et al. Allergic disorders and susceptibility to and severity of COVID-19: A nationwide cohort study. J Allergy Clin Immunol 2020; 146:790.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.