Атипическая гиперплазия эндометрия
гиперплазия с атипией, простая атипическая эндометриальная гиперплазия, комплексная атипическая эндометриальная гиперплазия, эндометриальная интраэпителиальная неоплазия (карцинома in situ эндометрия)
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Карцинома in situ эндометрия (D07.0)
Акушерство и гинекология, Онкология
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «17» марта 2026 года
Протокол №248
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
АТИПИЧЕСКАЯ ГИПЕРПЛАЗИЯ ЭНДОМЕТРИЯ
Синонимы атипической гиперплазия эндометрия: гиперплазия с атипией, простая атипическая эндометриальная гиперплазия, комплексная атипическая эндометриальная гиперплазия, эндометриальная интраэпителиальная неоплазия (карцинома in situ эндометрия) [1-5].
Предраковые заболевания матки имеют риск трансформации в злокачественную опухоль.
К предраковым заболеваниям относят атипическую гиперплазию эндометрия.
Атипическая гиперплазия эндометрия – процесс, который характеризуется избыточным разрастанием желез внутреннего слоя матки, причём клетки, формирующие эти железы, являются аномальными. Атипическая гиперплазия эндометрия развивается из гиперплазии эндометрия (избыточного образования желез нормального гистологического строения во внутренней оболочке матки) или из полипов эндометрия. Существует риск сопутствующего рака эндометрия у тех, у кого диагностирована атипическая гиперплазия при биопсии эндометрия [1-5].
Атипическая гиперплазия эндометрия – процесс, который характеризуется избыточным разрастанием желез внутреннего слоя матки, причём клетки, формирующие эти железы, являются аномальными. Атипическая гиперплазия эндометрия развивается из гиперплазии эндометрия (избыточного образования желез нормального гистологического строения во внутренней оболочке матки) или из полипов эндометрия. Существует риск сопутствующего рака эндометрия у тех, у кого диагностирована атипическая гиперплазия при биопсии эндометрия [1-5].
Синонимы атипической гиперплазия эндометрия: гиперплазия с атипией, простая атипическая эндометриальная гиперплазия, комплексная атипическая эндометриальная гиперплазия, эндометриальная интраэпителиальная неоплазия (карцинома in situ эндометрия) [1-5].
ВВОДНАЯ ЧАСТЬ
Код(ы) Международной классификации болезней 10-го пересмотра (далее – МКБ-10) / Международной классификации болезней 11-го пересмотра (далее – МКБ-11):
|
Код
|
Название |
| МКБ-10 | |
| D07.0 |
Карцинома in situ эндометрия
|
| МКБ-11 | |
| 2E67.0 |
Карцинома in situ эндометрия
|
Дата разработки/пересмотра протокола: 2023 год.
Пользователи протокола: акушер-гинекологи, врачи общей практики, онкогинекологи.
Категория пациентов: взрослые.
Сокращения, используемые в протоколе:
|
АГЭ
|
атипическая гиперплазия эндометрия |
|
АМК
|
аномальное маточное кровотечение |
|
аГн-РГ
|
агонисты гонадотропин-рилизинг-гормона |
|
ВМК
|
Внутриматочный комплекс |
|
ВОЗ
|
Всемирная организация здравоохранения |
|
ГС
|
гистероскопия |
|
ГЭ
|
гиперплазия эндометрия |
|
ЛНГ-ВМС
|
левоноргестрел-высвобождающая внутриматочная система |
|
МА
|
Мегестрола ацетат |
|
МПА
|
Медроскипрогестерона ацетат |
|
МРТ
|
магнитно-резонансная томография |
|
РЭ
|
рак эндометрия |
|
СПЯ
|
синдром поликистозных яичников |
|
УЗИ
|
ультразвуковое исследование |
|
ЭА
|
эндометриоидная аденокарцинома |
|
ЭИН (EIN)
|
эндометриальная интраэпителиальная неоплазия |
|
CIS
|
Карцинома in situ |
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты, которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
Классификация
Классификация:
В клинической практике используется бинарная классификация ВОЗ 2014 года (оставленная без изменений в редакции 2020 года). Согласно данной классификации выделяют две формы [1]:
1) гиперплазия эндометрия без атипии
2) гиперплазия эндометрия с атипией (атипическая гиперплазия эндометрия) или или эндометриальную интраэпителиальную неоплазию (ЭИН).
Классификация ЭИН (эндометриальная интраэпителиальная неоплазия, EIN), где вместо термина «атипическая гиперплазия эндометрия» используется термин «эндометриальная интраэпителиальная неоплазия» [13].
Градация дисплазии эндометриального эпителия включает три степени:
I степень – нарушение нормальной базальной ориентации ядер, которые становятся гиперхромными, немного увеличиваются в размерах, округляются. Клеточный полиморфизм выражен слабо, митозы редкие.
II степень – умеренный ядерный полиморфизм, более выраженное округление ядер, появление заметных ядрышек, неравномерное распределение хроматина, имеется умеренное нарушение рядности эпителиального пласта.
III степень – клетки полиморфны, хаотически расположены в эпителиальном пласте, выраженные гиперхромия и полиморфизм ядер с наличием ядрышек округлой и полглональной формы, встречаются патологические митозы.
Карцинома in situ (CIS) – выраженная ядерная атипия, наличие патологических митозов, т.е. имеются изменения, характерные для аденокарциномы, однако отсутствует инвазия в окружающую цитогенную строму. CIS рассматривается в рамках атипической гиперплазии при выборе способа лечения.
Американская коллегия акушеров и гинекологов (2023), рекомендует клиническое применение классификации ЭИН, как более объективной, основанной на морфометрических параметрах [4]. С 2014 г. термин «EIN» введен в классификационную систему ВОЗ, которая рекомендует его использование наравне с термином АГЭ, с единым гистологическим кодом (8380/2) [1], [4].
Клиническая картина
Cимптомы, течение
Клиническая картина состояния:
проявляется аномальными маточными кровотечениями (АМК) в виде обильных менструаций или межменструальных маточных кровотечений при регулярном менструальном цикле или олигоменореи.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Жалобы:
• на ациклические кровянистые, водянистые из половых путей;
• кровотечения из половых путей на фоне менопаузы.
Анамнез:
Рекомендуется всем пациенткам проведение анализа анамнестических данных с целью выявления факторов риска развития АГЭ. Уровень доказательности С.
АГЭ проявляется аномальными маточными кровотечениями (АМК) в виде обильных или межменструальных маточных кровотечений при регулярном менструальном цикле или олигоменореи [16]. Характер АМК не позволяет предположить тип ГЭ. ГЭ формируется, как правило, на фоне прогестерон-дефицитного состояния и может быть причиной ановуляторного бесплодия [6], [7]. Для женщин с избыточной массой тела, ожирением, имеющих длительные ановуляторные менструальные циклы и увеличение конверсии андрогенов в эстрогены в жировой ткани, характерно повышение риска развития ГЭ и РЭ [3].
Физикальные обследования
Гинекологический осмотр:
• состояние наружных половых органов;
• осмотр влагалища и шейки матки на зеркала;
• наличие патологических выделений.
Ожидаемые результаты: при гинекологическом осмотре могут быть кровянистые выделения разной интенсивности.
Лабораторные диагностические исследования
Основные лабораторные исследования:
Дополнительные инструментальные исследования:
Бимануальный осмотр:
• размеры и форма матки;
• состояние придатков.
Ожидаемые результаты: отклонений от нормы может и не быть. При наличии сопутствующей маточной патологии (миоме матки, аденомиозе) – матка может быть увеличена. Придатки матки при наличии СПЯ могут быть увеличены.
Лабораторные диагностические исследования
Основные лабораторные исследования:
• общий анализ крови;
• общий анализ мочи;
• биохимический анализ крови (общий белок, глюкоза, креатинин, мочевина, АЛТ, АСТ, общий и прямой билирубин);
• коауглограмма (фибриноген, МНО, протромбиновое время, ПТИ, АЧТВ);
• микроскопическое исследование влагалищных мазков у пациенток с подозрением на ГЭ для исключения воспалительных заболеваний органов малого таза.
• цитологическое исследование цервикального мазка (с целью выявления цервикальной интраэпителиальной неоплазии (уровень доказательности С);
• гистологическое исследование биоптата/соскоба эндометрия и цервикального канала [1], [9], [10] (уровень доказательности рекомендаций В).
Ожидаемые результаты: может быть снижение гемоглобина, повышение тромбоцитов, повышение глюкозы крови, в некоторых случаях имеет место гиперкоагуляция.
Инструментальные диагностические исследования
Дополнительные лабораторные исследования:
• исследование уровня ФСГ в сыворотке крови, исследование уровня ЛГ в сыворотке крови, исследование уровня прогестерона в крови, исследование уровня свободного тестостерона, андростендиона, дегидроэпиандростерона сульфата в крови, исследование уровня пролактина в крови, определение уровня ХГЧ в крови (оценка гормонов сыворотки крови для диагностики и выявления причин ановуляции и олигоменореи);
• тиреоидные гормоны ТТГ и Т4 свободный (диагностики и выявления гипотиреоза).
• проведение скрининга на ИППП (Chlamydia trachomatis, Neisseria gonorrhoeae, Trichomonas vaginalis, Mycoplasma genitalium) методом ПЦР (при подозрении на инфекции).
Ожидаемые результаты: может быть повышение эстрогена, снижение прогестерона.
Инструментальные диагностические исследования
Основные инструментальные исследования:
• УЗИ органов малого таза (трансвагинальное). Уровень доказательности В.
• Гистероскопия с прицельной биопсией эндометрия и/или раздельное диагностическое выскабливание цервикального канала и полости матки. Уровень доказательности В.
Дополнительные инструментальные исследования:
• МРТ органов малого таза с контрастированием.
Ожидаемые результаты. На УЗИ органов малого таза, проводимое при возможности в 1-ую фазу цикла или на фоне АМК, будет М-эхо более 10 мм, эндометрий утолщенный и неоднородный [8].
Гистероскопическая картина при атипической гиперплазии эндометрия характеризуется очаговым или диффузным утолщением эндометрия с выраженным сосудистым рисунком, образующим складки различной величины с выраженными железистыми структурами, иногда полость матки заполнена тусклыми полиповидными разрастаниями желтоватого или сероватого цвета.
При выскабливании полости матки может быть получен обильный, пышный соскоб эндометрия. Окончательный диагноз ГЭ у пациенток c рецидивирующей ГЭ, наличием факторов риска развития РЭ в перименопаузе и постменопаузе ставить на основании результатов гистологического исследования эндометрия, полученного при диагностическом выскабливании полости матки (при отсутствии условий выполнения гистероскопии) [1].
На МРТ органов малого таза могут наблюдаться изменения в структуре эндометрия (утолщение, неоднородность, наличие полипов или разрастаний. Визуализация патологических участков позволяет провести более точную биопсию для дальнейшего гистологического исследования. Не рекомендуется рутинно использовать МРТ органов малого таза в качестве метода диагностики ГЭ. Однако этот метод рассматривается как перспективный в дифференциальной диагностике АГЭ и РЭ. Поскольку МРТ с использованием диффузно-взвешенных последовательностей позволяет выявить начальные признаки инвазии ткани эндометрия в миометрий, характерные для ранней стадии РЭ.
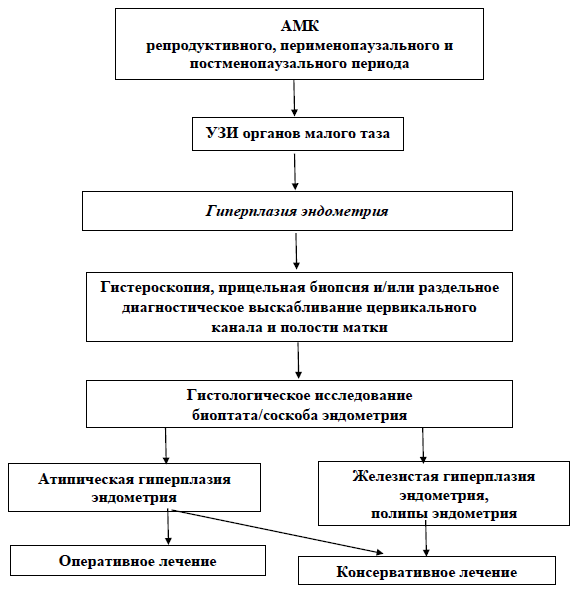
Диагностический алгоритм:
Схема -1. Диагностический алгоритм атипической гиперплазии эндометрия
Показания для консультации узких специалистов:
• консультация репродуктолога. Цель: если пациентки хотят сохранить свою репродуктивную функцию в связи с высоким риском рецидивирования и развития бесплодия. Варианты сохранения фертильности включают криоконсервацию ооцитов или эмбрионов до гистерэктомии с билатеральной сальпингоовариоэктомией;
• консультация маммолога. Цель: выявление патологии молочных желез;
• консультация кардиолога. Цель: при наличии сопутствующей патологии ССС для оценки сердечно-сосудистой системы, выявления и минимизации рисков осложнений, а также для определения оптимального плана подготовки к вмешательству;
• консультация невропатолога. Цель: при сосудистых мозговых нарушениях, в том числе инсультах, травмах головного и спинного мозга, эпилепсии, миастении, нейроинфекционных заболеваниях, а также во всех случаях потери сознания для выявления и минимизации рисков осложнений, а также для определения оптимального плана подготовки к вмешательству;
• консультация гастроэнтеролога (при наличии сопутствующей патологии органов ЖКТ для выявления и минимизации рисков осложнений, а также для определения оптимального плана подготовки к вмешательству);
• консультация эндокринолога (при наличии сопутствующей патологии эндокринных органов для выявления и минимизации рисков осложнений, а также для определения оптимального плана подготовки к вмешательству);
NB! Консультация других узких специалистов по показаниям.
Диагностический алгоритм:
Схема -1. Диагностический алгоритм атипической гиперплазии эндометрия

Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований
Основные заболевания для дифференциальной диагностики представлены в таблице
|
Диагноз
|
Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Гиперплазия эндометрия |
АМК
репродуктивного, перименопаузального и постменопаузального возраста
|
УЗИ органов малого таза;
Гистероскопия или выскабливание полости матки
|
Заключение гистологического исследования биоптата из полости матки – железистая гиперплазия эндометрия без атипии |
| Полип эндометрия |
АМК
репродуктивного, перименопаузального и постменопаузального возраста
|
УЗИ органов малого таза;
гистероскопия, полипэктомия
|
Гистероскопическая картина – полип эндометрия.
Заключение гистологического исследования – полип эндометрия.
|
| Субмукозная миома матки |
АМК
репродуктивного, перименопаузального и постменопаузального возраста
|
УЗИ органов малого таза;
МРТ органов малого таза;
гистероскопия, резекция субмукозного узла
|
УЗ-картина узлового образования полости матки;
гистероскопическая картина – деформация полости матки за счет субмукозного образования белесоватого цвета, плотной консистенции;
заключение гистологического исследования – фибролейомиома.
|
| Аденомиоз |
АМК
репродуктивного, перименопаузального и постменопаузального возраста
|
УЗИ органов малого таза;
МРТ органов малого таза;
гистероскопия
|
УЗ-признаки аденомиоза;
МРТ-признаки аденомиоза;
гистероскопическая картина – эндометриоидные ходы, грубый рельеф стенок в виде хребтов и крипт, ригидность стенок матки.
|
| Рак эндометрия |
АМК
репродуктивного, перименопаузального и постменопаузального возраста
|
УЗИ органов малого таза;
МРТ органов малого таза;
раздельное диагностическое выскабливание цервикального канала и полости матки;
|
УЗ-признаки ГЭ с локусами кровотока;
МРТ-признаки рака эндометрия;
заключение гистологического исследования биоптата из полости матки – эндометриоидная аденокарцинома или другая гистологическая форма рака эндометрия
|
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
Немедикаментозное лечение: нет.
Медикаментозное лечение
Рекомендуется при выявлении АГЭ у пациенток репродуктивного возраста с настойчивым желанием сохранить детородную функцию и отказе от гистерэктомии, определить возможность консервативного лечения путем локального введения ВМК с левоноргестрелом или прогестагенами в непрерывном режиме с обязательным гистологическим исследованием биопсийоного (операционного) материала эндометрия каждые 3-6 месяцев [14], [15], [16], [17] (уровень доказательности В).
Рекомендуется после морфологической верификации диагноза АГЭ в случае противопоказаний к ЛНГ-ВМС или отказа от ее введения терапия прогестагенами в непрерывном или пролонгированном циклическом режимах [13]. Часто используемые пероральные прогестины – ацетат медроксипрогестерона ацетат (МПА) или мегестрола ацетат (МА). Обычно используемая дозировка составляет 250–500 мг МПА и 160–320 мг МПА ежедневно. Уровень доказательности – B.
При оценке результатов применения ЛНГ-ВМС и оральных прогестагенов выявлено, что регрессия ГЭ, индуцированная ЛНГ-ВМС, происходит достоверно чаще. При АГЭ вероятность сопутствующего РЭ диагностируется в 40-60% случаев, что свидетельствует о целесообразности гистерэктомии при АГЭ [14], [15].
В случае противопоказаний к ЛНГ-ВМС или отказа от ее введения при АГЭ возможно назначение в непрерывном или пролонгированном циклическом режимах прогестагенов. Прогестагены в циклическом режиме менее эффективны для регрессии АГЭ в сравнении с непрерывным режимом приема и ЛНГ-ВМС [11], [13],
Пациентам, получающим консервативную терапию, необходимо проверить биопсия эндометрия каждые 3 месяца. Хирургическое лечение должно быть рассматривается, если поражения сохраняются в течение 9–12 месяцев с момента первоначального лечения. Длительность прогестиновой терапии варьируется от 3 до 36 месяцев, что опубликовано во многих исследованиях, хотя в большинстве случаев может наблюдаться атрофия эндометрия через 3–6 месяцев приема препарата.
Рекомендуется применение агонистов гонадотропин-рилизинг-гормона (аГн-РГ) при сочетании ГЭ с миомой матки и эндометриозом [13]. Уровень доказательности С.
Применение аГн-РГ целесообразно при сочетании ГЭ с миомой матки или эндометриозом. При выраженных симптомах эстрогендефицита и необходимости проведении терапии более 6 месяцев целесообразно назначение возвратной терапии препаратами для непрерывного режима менопаузальной гормонотерапии.
Рекомендуется при морфологически верифицированной АГЭ проводить терапию ВМК с левоноргестрелом или прогестагенами в течение 6 месяцев с последующим гистологическим исследованием биопсийоного (операционного) материала эндометрия (при наличии внутриматочной системы – без ее удаления) для определения дальнейшей тактики ведения [12], [13] (уровень доказательности В).
Для контроля эффективности лечения АГЭ забор ткани эндометрия для гистологического исследования как при биопсии, так и при ГС и диагностическом выскабливании слизистой полости матки. Проведение 6 месячного курса терапии ЛНГ-ВМС (в сравнении с 3-х месячным) увеличивает эффективность регресса ГЭ. Если нет побочных эффектов, и пациентка не заинтересована в беременности, целесообразно продлить терапию ВМК с левоноргестрелом на срок до 5 лет, для снижения риска рецидивов АГЭ, проводя ежегодный УЗИ-мониторинг за состоянием эндометрия и биопсию эндометрия.
Рекомендуется информировать пациентку о возможности рецидива ГЭ после завершения курса терапии [13]. Уровень доказательности В.
Несмотря на значительно более высокую эффективность ЛНГ-ВМС в сравнении с непрерывным или циклическим режимами прогестагенов, после отмены 6-месячного курса терапии могут быть рецидивы. Рецидивы значительно чаще возникают у пациенток с ИМТ≥35 кг/м2.
В случае успешной реализации репродуктивной функции пациентке должно быть рекомендовано хирургическое лечение [14].
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
| Фармако-терапевтическая группа | МНН | Способ применения | УД |
|
Гестаген (1 линии)
|
Левоноргестрел
|
Внутриматочное введение комплекса от 6 мес. до 5 лет | В |
|
Гестаген (1 линии)
|
Медроксипрогестерона ацетат (МПА) * | 250-500 мг внутрь ежедневно 3-6 мес. | В |
|
Гестаген (1 линии)
|
Мегестрола ацетат* |
160-320 мг внутрь ежедневно
3-6 мес.
|
В |
Перечень дополнительных лекарственных средств (менее 100% вероятности применения):
|
Фармако-терапевтическая группа
|
МНН | Способ применения | УД |
| Агонисты гонадотропин-рилизинг гормона | Трипторелин | 3,75 г в/м 1 раз в 28 дней 3-6 мес. | С |
| Агонисты гонадотропин-рилизинг гормона | Гозерелин | 3,6 мг п/к 1 раз в 28 дней 3-6 мес. | С |
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЕ НА СТАЦИОНАРНОМ УРОВНЕ
Немедикаментозное лечение: нет.
Медикаментозное лечение: нет.
Хирургическое лечение
При верификации АГЭ или ИЭН вероятность развития инвазивного РЭ достигает 60%. В связи с этим пангистерэктомия наиболее предпочтительна в данной категории пациенток [59]. Однако в случае желания пациентки сохранить свою репродуктивную функцию следует рассматривать консервативное лечение.
Рекомендуется контрольная гистероскопия с прицельной биопсией эндометрия и/или раздельное диагностическое выскабливание цервикального канала и полости матки 1 раз в 3 месяца на фоне лечения, далее 1 раз в 6 месяцев последующие два года после окончания лечения. Уровень доказательности В.
Вид анестезии: тотальная внутривенная анестезия.
Противопоказания: беременность, рак шейки матки, острые инфекционные заболевания (ОРВИ, пневмония и др.), острые воспалительные заболевания половых органов, сопутствующие заболевания внутренних органов (сердца, печени, почек) в стадии декомпенсации, полная атрезия цервикального канала, недавняя перфорация матки.
Риски операции: перфорация матки, кровотечение, инфекции, внутриматочные синехии, гематометра.
Показания к хирургическому лечению:
Рекомендуется при АГЭ проведение пангистерэктомии, по возможности, лапароскопическим доступом [14], [15], [16] (уровень убедительности рекомендаций С)
Необходимо проведение тотальной гистерэктомии ввиду высокой вероятности сопутствующего РЭ (по некоторым данным диагностируется в 40-60% случаев).
Показания к хирургическому лечению:
• Верифицированная АГЭ;
• Отсутствие эффекта от консервативной терапии в течение 6-12 месяцев;
• Если пациентка не соблюдает рекомендации врачей, отказывается от лечения и последующего наблюдения либо объективно не может его применять.
Противопоказания: острые инфекционные заболевания (ОРВИ, пневмония и др.), острые воспалительные заболевания половых органов, сопутствующие заболевания внутренних органов (сердца, печени, почек) в стадии декомпенсации, нарушения гемостаза, большие размеры матки (более 12 недель).
Риски операции: кровотечение во время операции, кровотечение после операции, гематомы в малом тазу, травма мочевого пузыря, мочеточника или кишечника, инфекции, перикультит, инфекции раны, перитонит или сепсис, тромбоз вен нижних конечностей или тромбоэмболия легочных артерий, осложнения, связанные с анестезией: реакции на препараты для анестезии, риски сердечно-сосудистых осложнений, нарушения мочеиспускания, грыжи.
Радикальный объем операции – тотальная гистерэктомия с билатеральной сальпингоовариоэктомией, а в ряде случаев – тотальная гистерэктомия с билатеральной сальпингэктомией, решается в зависимости от возраста пациента, наличия сопутствующей патологии [14], [15], [16].
Вид анестезии: эндотрахеальный наркоз.
Противопоказания: острые инфекционные заболевания (ОРВИ, пневмония и др.), острые воспалительные заболевания половых органов, сопутствующие заболевания внутренних органов (сердца, печени, почек) в стадии декомпенсации, нарушения гемостаза, большие размеры матки (более 12 недель).
Риски операции: кровотечение во время операции, кровотечение после операции, гематомы в малом тазу, травма мочевого пузыря, мочеточника или кишечника, инфекции, перикультит, инфекции раны, перитонит или сепсис, тромбоз вен нижних конечностей или тромбоэмболия легочных артерий, осложнения, связанные с анестезией: реакции на препараты для анестезии, риски сердечно-сосудистых осложнений, нарушения мочеиспускания, грыжи.
Морцелляция матки при гистерэктомии, выполняемой лапароскопическим доступом, также не рекомендована, в связи с высоким риском диссеминации и малигнизации.
Пациенткам, страдающим АГЭ, абляция эндометрия и супрацервикальная гистерэктомия не рекомендуются, так как данные вмешательства не гарантируют полного излечения, а образование внутриматочных синехий после аблации может затруднить последующую диагностику и мониторинг за состоянием эндометрия.
Дальнейшее ведение:
Для предупреждения развития рецидива и с целью исключения рисков малигнизации, при АГЭ необходимо проводить УЗИ органов малого таза и прицельную биопсию эндометрия под гистероскопическим контролем каждые 3 месяцев на фоне терапии, и каждые 6 месяцев в течение 2-х лет после окончания лечения до достижения морфологического регресса, а затем 1 раз в год до тех пор, пока не будут исключены факторы риска, или до момента проведения гистерэктомии с двусторонней сальпингоовариоэктомией. Уровень убедительности рекомендаций С.
Факторами риска развития РЭ являются: избыточная масса тела и ожирение, СПЯ и др. [6]. При ожирении снижается эффективность терапии и вероятность последующей ремиссии АГЭ. Необходима модификация факторов риска, лечение ожирения, сахарного диабета, артериальной гипертензии, СПЯ и нормализации массы тела. Комплекс мер должен включать физические нагрузки и рациональное сбалансированное питание, снижение каллоража на 30% для достижения и поддержания нормальной массы тела. Физическая активность должна составлять минимум 150 минут в неделю, включая упражнения на укрепление мышц в течение 2 дней в неделю. График и интенсивность тренировок подбирается индивидуально. Показано, что длительный прием прогестагенов снижает риск АГЭ.
Индикаторы эффективности лечения:
• состояние после тотальной гистерэктомии;
• гормональный патоморфоз биоптатов эндометрия по результатам гистологического исследования в течение двух лет после окончания гормонотерапии.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для экстренной госпитализации: аномальное маточное кровотечение (АМК).
Показания для плановой госпитализации: верификация АГЭ, оперативное лечение.
Терапия АГЭ включает консервативное (гормональное) и оперативное лечение. Выбор тактики ведения АГЭ зависит от возраста пациентки, ее репродуктивных планов, наличия факторов риска РЭ и сопутствующей гинекологической и экстрагенитальной патологии. Цель терапии АГЭ состоит в купировании АМК, профилактике рецидивов АГЭ и развитии РЭ.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- 1. Cree IA, White VA, Indave BI, Lokuhetty D. Revising the WHO classification: female genital tract tumours. Histopathology. 2020 Jan;76(1):151-156. doi: 10.1111/his.13977. 2. Hutt S, Tailor A, Ellis P, Michael A, Butler-Manuel S, Chatterjee J. The role of biomarkers in endometrial cancer and hyperplasia: a literature review. Acta Oncol. 2019 Mar;58(3):342-352. doi: 10.1080/0284186X.2018.1540886. 3. Russo M, Newell JM, Budurlean L, Houser KR, Sheldon K, Kesterson J et al. Mutational profile of endometrial hyperplasia and risk of progression to endometrioid adenocarcinoma. Cancer. 2020 Jun 15;126(12):2775-2783. doi: 10.1002/cncr.32822. 4. ACOG, Clinical Consensus. Management of Endometrial Intraepithelial Neoplasia or Atypical Endometrial Hyperplasia. Number 5, September 2023. 5. Raffone A, Travaglino A, Saccone G, Insabato L, Mollo A, De Placido G et al. Endometrial hyperplasia and progression to cancer: which classification system stratifies the risk better? A systematic review and meta-analysis. Arch Gynecol Obstet. 2019. 6. Walker K, Decherney AH, Saunders R. Menstrual Dysfunction in PCOS. Clin Obstet Gynecol. 2021 Mar 1;64(1):119-125. doi: 10.1097/GRF.0000000000000596. PMID: 33481414. 7. Tian Y, Liu Y, Wang G, Lv Y, Zhang J, Bai X et al. Endometrial hyperplasia in infertile women undergoing IVF/ICSI: A retrospective cross-sectional study. J Gynecol Obstet Hum Reprod. 2020 Apr 29:101780. doi: 10.1016/j.jogoh.2020.101780. 8. Natarajan P, Vinturache A, Hutson R, Nugent D, Broadhead T. The value of MRI in management of endometrial hyperplasia with atypia. World J Surg Oncol. 2020 Feb 10;18(1):34. doi: 10.1186/s12957-020-1811-5. 9. Hwang WY, Suh DH, Kim K, No JH, Kim YB. Aspiration biopsy versus dilatation and curettage for endometrial hyperplasia prior to hysterectomy. Diagn Pathol. 2021 Jan 14;16(1):7. doi: 10.1186/s13000-020-01065-0. PMID: 33441173; PMCID: PMC7807457. 10. Lee N, Lee KB, Kim K, Hong JH, Yim GW, Seong SJ, Lee B, Lee JM, Cho J, Lim S, Ouh YT, Kim YB. Risk of occult atypical hyperplasia or cancer in women with nonatypical endometrial hyperplasia. J Obstet Gynaecol Res. 2020 Sep 17. doi: 10.1111/jog.14474. 11. Jiao Yu, Yangyang Zhang, Huixia Yang, Yang Xu. Reproductive advance of fertility preservation in patients with early endometrial carcinoma or endometrial atypical hyperplasia: a review article. Gynecology and Obstetrics Clinical Medicine 2 (2022) 186–190 12. Mittermeier T, Farrant C, Wise MR. Levonorgestrel-releasing intrauterine system for endometrial hyperplasia. Cochrane Database Syst Rev. 2020 Sep 6;9:CD012658. doi: 10.1002/14651858.CD012658. 13. Terzic M, Norton M, Terzic S, et al. Fertility preservation in endometrial cancer patients: options, challenges and perspectives. Ecancermedical. sci. 2020; 14:1030.43. 14. Vetter MH, Smith B, Benedict J, Hade EM, Bixel K, Copeland LJ et al. Preoperative predictors of endometrial cancer at time of hysterectomy for endometrial intraepithelial neoplasia or complex atypical hyperplasia. Am J Obstet Gynecol. 2020 Jan;222(1): 15. Doherty MT, Sanni OB, Coleman HG, Cardwell CR, McCluggage WG, Quinn D et al. Concurrent and future risk of endometrial cancer in women with endometrial hyperplasia: A systematic review and meta-analysis. PLoS One. 2020 Apr 28;15(4): e0232231. doi: 10.1371. 16. Garzon S, Uccella S, Zorzato PC, Bosco M, Franchi MP, Student V, Mariani A. Fertilitysparing management for endometrial cancer: review of the literature. Minerva Med. 2021 Feb;112(1):55-69. doi: 10.23736/S0026-4806.20.07072-X. Epub 2020 Nov 18. 17. Fernandez-Montoli ME, Sabadell J, Contreras-Perez NA. Fertility-Sparing Treatment for Atypical Endometrial Hyperplasia and Endometrial Cancer: A Cochrane Systematic Review Protocol. Adv Ther. 2021 Apr 8. doi: 10.1007/s12325-021-01693-y. 18. Karlsson T, Johansson T, Höglund J, Ek WE, Johansson Å. Time-Dependent Effects of Oral Contraceptive Use on Breast, Ovarian, and Endometrial Cancers. Cancer Res. 2021 Feb 15;81(4):1153-1162. doi: 10.1158/0008-5472.CAN-20-2476. Epub 2020 Dec 17.
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1) Шакирова Аида Фазыловна – кандидат медицинских наук, врач высшей квалификационной категории, ТОО «Национальный научный онкологический центр», старший ординатор онкогинеколог Центра многопрофильной хирургии.
2) Имендинова Динара Уйсимбаевна – кандидат медицинских наук, врач высшей квалификационной категории, ГКП на ПХВ «Многопрофильная больница №3 г. Караганды» Управление здравоохранения Карагандинской области, врач онкогинеколог отделения онкогинекологии.
3) Козгамбаева Ляззат Таласпаевна – кандидат медицинских наук, врач высшей квалификационной категории, ГКП на ПХВ «Многопрофильный медицинский центр» Управление общественного здравоохранения города Астаны, заместитель директора по менеджменту качества медицинской помощи.
4) Игембаева Гульмира Исмаиловна – магистр медицины, врач первой квалификационной категории, ТОО «Национальный научный онкологический центр», онкогинеколог сектора онкогинекологии Центра многопрофильной хирургии.
5) Рахимбекова Жанар Турсыновна – магистр MBA, ТОО «Национальный научный онкологический центр», клинический фармаколог Центра лекарственного обеспечения.
Указание на отсутствие конфликта интересов: нет.
Рецензент: Укыбасова Талшын Мухадесовна – доктор медицинских наук, профессор, старший консультант департамента женского здоровья Корпоративного фонда «University Medical Center» «Национальный научный центр материнства и детства», акушер-гинеколог высшей категории.
Условие для пересмотра протокола: пересмотр не реже 1 раза в 5 лет и не чаще 1 раза в 3 года при наличии новых методов диагностики и лечения с уровнем доказательности.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.