Алкогольная болезнь печени у взрослых
Alcoholic liver disease, ALD, АБП
 Версия: Клинические рекомендации РФ 2024 (Россия)
Версия: Клинические рекомендации РФ 2024 (Россия)
Алкогольная болезнь печени (K70)
Гастроэнтерология
Общая информация
Краткое описание
Разработчик клинической рекомендации
- Российское общество по изучению печени
- Российская Гастроэнтерологическая Ассоциация
- Общероссийская общественная организация "Российское научное медицинское общество терапевтов"
- Российское общество профилактики неинфекционных заболеваний
- Ассоциация психиатров и психологов за научно-обоснованную практику
Одобрено Научно-практическим Советом Минздрава РФ
В соответствии с Правилами поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 –9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», утвержденных постановлением Правительства Российской Федерации от 19.11.2021 № 1968 с изменения, клинические рекомендации применяются следующим образом:
– размещенные в Рубрикаторе после 1 января 2024 года – с 1 января 2025 года.
Клинические рекомендации
Алкогольная болезнь печени
Год утверждения (частота пересмотра): 2024
Возрастная категория: Взрослые
Пересмотр не позднее: 2026
ID: 711
Определение заболевания или состояния (группы заболеваний или состояний)
Алкогольная болезнь печени (АБП) – это клинико-морфологическое понятие, отражающее поражение печени в результате злоупотребления алкоголем. АБП включает в себя следующие клинико-морфологические формы: алкогольный стеатоз (АлС), алкогольный гепатит (АлГ) и алкогольный цирроз печени (АЦП).
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
К00-К93 Класс XI. Болезни органов пищеварения
К70-К77 Болезни печени
K70.0 – Алкогольная жировая дистрофия печени;
K70.1 – Алкогольный гепатит;
K70.2 – Алкогольный фиброз и склероз печени;
K70.3 – Алкогольный цирроз печени;
K70.4 – Алкогольная печеночная недостаточность;
K70.9 – Алкогольная болезнь печени неуточненная
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Основываясь на клинических и морфологических критериях, выделяют три основные формы алкогольной болезни печени: стеатоз, гепатит и цирроз.
Считается, что алкогольный стеатоз в 90% случаев развивается у лиц, употребляющих этанол в опасных дозах. К этому приводят три основных метаболических процесса в печени, связанных с систематическим поступлением алкоголя:
1) образование избыточного ацетил-КоА в цитоплазме гепатоцитов, что стимулирует синтез жирных кислот; высокая концентрация НАДН, который восстанавливает дигидроксиацетонфосфат до глицерол-3-фосфата (используется вместе с жирными кислотами для синтеза жира);
2) замедление скорости β-окисления жирных кислот, вследствие избытка НАДН и АТФ, что смещает процесс использования поступающих жирных кислот на синтез жира;
3) нарушение синтеза липопротеинов очень низкой плотности (ЛПОНП) и транспортировки жиров из печени в ткани. В результате происходит накопление жира в ткани печени, что морфологически проявляется чаще макровезикулярным стеатозом, локализованном, в основном, в 3-й и 2-й зонах ацинуса. При соблюдении абстиненции эти изменения разрешаются в течение 4-6 недель. Однако продолжение приема алкоголя в опасных дозах приводит в 10-20% случаев к прогрессированию заболевания в следующую стадию – алкогольного стеатогепатита [26]. На этом этапе заболевание может проявляться умеренным повышением печеночных аминотрансфераз, гамма-глутамилтранспептидазы (ГГТ) и общего билирубина.
Алкогольный гепатит делят на две формы согласно тяжести повреждения печени и жизненному прогнозу: стеатогепатит и тяжелый алкогольный гепатит. Последний манифестирует быстрым прогрессированием печеночной недостаточности, развитием желтухи, асцита, нарушением свертываемости крови и характеризуется высокой краткосрочной летальностью (30–50%).
Таким образом, определение тяжести алкогольного гепатита не является формальностью, так как с этим связан прогноз и, соответственно, тактика лечения пациента. В большинстве случаев тяжелый алкогольный гепатит развивается на фоне алкогольного цирроза печени, что делает жизненный прогноз пациента еще хуже.
Алкогольный цирроз печени развивается у менее 10 % пациентов и классифицируется по степени тяжести ЦП от А до С класса по шкале Child-Pugh. Подробно классификация степени тяжести цирроза печени описана в клинических рекомендациях по данному заболеванию [27].
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Этиология алкогольной болезни печени связана с длительным злоупотреблением алкогольных напитков в опасных дозах, которые оказывают повреждающее действие на печень.
Согласно рекомендациям Всемирной организации здравоохранения (ВОЗ), различают «опасную», «вредную» модели употребления алкоголя, эпизодическое употребление алкоголя в больших количествах и алкогольную зависимость.
Опасное употребление алкоголя – модель употребления алкоголя, включающая дозы и режим употребления, которая увеличивает риск причинения вреда здоровью при условии постоянного употребления алкоголя [1].
Вредным считается употребление алкоголя, способное наносить ущерб здоровью как физическому, так и психическому [1]. При этом больной может и не подозревать о наличии у себя заболевания (как часто и происходит при АБП ввиду отсутствия выраженных симптомов на ранних стадиях заболевания). Эпизодическим употреблением алкоголя в больших количествах считается более 60 г чистого спирта, употреблённого за сутки.
Алкогольную зависимость диагностирует врач-нарколог при формировании психической и физической зависимости. АБП диагностируется практически у всех пациентов с алкогольной зависимостью.
В международном сообществе, чтобы дать объективную оценку уровню употребления алкоголя конкретного человека, вне зависимости от крепости алкогольного напитка, экспертами было принято решение ввести термин «стандартная доза алкоголя». Рассчитывать количество принятых индивидуумом стандартных доз (СтД – «standart drink») принято в граммах. Одна СтД = 10 г этанола (или 12,7 мл спирта), что соответствует 30 мл крепких напитков (водка, коньяк и т. п.), 100 мл 12% вина, 250 мл 5% пива.
Рассчитать количество миллилитров (СтД) этанола в напитке можно с помощью формулы:
Количество СтД алкоголя = Объем (мл) × ABV (%) × 8/10000, где ABV(%) = Alcohol by volume (%), что означает процент алкоголя в напитке.
СтД = (крепость (%об) х объем (мл) х n (раз в неделю)) / 1275 (для расчета суточной дозы n=1).
Употребление более одной стандартной порции алкоголя в день увеличивает вероятность неблагоприятного прогноза для здоровья пациента. Основываясь на данных исследований, согласно рекомендациям Российского общества по изучению печени (РОПИП), Европейской ассоциации по изучению болезней печени (EASL), опасной дозой принято считать приём алкогольных напитков в количестве 30 г чистого этанола (3 СтД) в сутки для мужчин и 20 г чистого этанола (2 СтД) в сутки для женщин [2,3]. Так, например, в 0,5 л водки содержится 16 СтД (160 г чистого этанола), а в 0,5 л пива (крепость 5 %о) – 2 СтД. Опасные и угрожающие для здоровья дозы алкоголя для мужчин 30 г/сут в пересчете на чистый этанол, что составляет 75 мл водки (крепость 40 %о), 300 мл сухого вина (крепость 10%о), 600 мл пива (крепость 5 %о). Употребление более 7 СтД для женщин и более 14 СтД для мужчин в неделю приводит к повышенному риску развития АБП [2].
Среди факторов, определяющих характер повреждения печени, наиболее значимы следующие: пол, генетический полиморфизм (этническая принадлежность), трофологический статус, прием некоторых ксенобиотиков, количество и длительность употребления алкоголя, тип употребляемых спиртных напитков, курение.
Пол. Женщины более чувствительны к действию опасных доз алкоголя, что в определенной степени можно объяснить меньшей активностью алкогольдегидрогеназы слизистой оболочки желудка, что приводит к более высокой концентрации этанола в плазме крови и более активному метаболизму этанола в печени. Факторами риска АБП может быть распределение жировой ткани по женскому типу, с избыточной продукцией этой тканью провосполительных цитокинов. Интересна роль эстрогенов, которые способствуют усилению экспрессии рецептора для бактериального липополисахарида (ЛПС) (CD14) на мононуклеарных фагоцитах. Это может приводить к повышенной проницаемости кишечника и к более выраженному фиброгенезу [4]. Длительное воздействие ЛПС приводит к избыточной продукции провоспалительных цитокинов (например ФНО-а), играющих важную роль в патогенезе АБП [5].
Генетический полиморфизм метаболизирующих этанол ферментов. Известно 7 изоферментов АДГ. Изоферменты сгруппированы в классы на основании их аминокислотной последовательности и ферментативной активности. У человека установлены три основных гена, кодирующих АДГ (алкогольдегидрогеназа): АДГ1, АДГ2, АДГ3. Они имеют разные полиморфные варианты. Так АДГ1 имеет 1 вариант, АДГ2 – 3 варианта, АДГ3 – 2 варианта. Известно, что вариант АДГ2*1 с различной частотой обнаруживается во всех популяциях, в то время как АДГ2*2 выявлен в большем проценте случаев у азиатов и в меньшей – у европейцев. Вариант АДГ2*3 встречается в 15-20 % случаев только у афроамериканцев. Носители АДГ2*2 нередко употребляют меньше алкоголя, кроме того, у них повышен риск возникновения побочных эффектов, обусловленных приемом алкоголя [6].
Классификация АлДГ (альдегиддегидрогеназа) основана на ее электрофоретической подвижности. Основную роль в метаболизме этанола играют цитозольная АлДГ1 и митохондриальная АлДГ2. Экспрессия этих ферментов наблюдается не только в печени, но и в почках, мышцах, сердце, поджелудочной железе. Около 40% активности печеночной АлДГ приходится на АлДГ2. Существует мутантая изоформа АлДГ обозначающаяся АлДГ2*2, нормальный вариант – АлДГ2*1 [6].
АлДГ2*2 обладает низкой ферментативной активностью и считается атипичным вариантом. Низкая активность данного фермента клинически может проявляться флеш-синдромом (от англ. Alcohol flush reaction) – покраснением кожи лица, тахикардией и иногда коллапсом.
Такой полиморфизм, вероятнее всего, приводит к значительным различиям в метаболизме этанола и определяет его переносимость как среди отдельных лиц (индивидуумов), так и среди различных популяций (рас). Риск токсического действия алкоголя повышен у лиц с высокой активностью АДГ и низкой активностью АлДГ [6]. Таким образом, увеличивается скорость образования и снижается скорость распада токсичного ацетальдегида.
Питание. Этанол нарушает кишечную абсорбцию и депонирование питательных веществ, а также вызывает снижение аппетита вследствие собственной высокой калорийности. В результате возникает хронический дефицит белка, витаминов и минералов. Дефицит питания способствует прогрессированию АБП, однако полноценное питание не предотвращает алкогольное повреждение печени [5]. По результатам исследования «Dionysos», проведенном в северной Италии, обнаружено, что употребление алкоголя без еды и употребление более 1 типа алкогольных напитков, повышает риск развития цирроза печени (ЦП) [7].
Ожирение также фактор риска прогрессирования фиброза печени, особенно у лиц, злоупотребляющих алкоголем. По данным одного исследования, употребление более 15 СтД алкоголя в неделю лицами с ожирением, приводит к увеличению риска смерти от заболеваний печени почти в 19 раз (ОШ = 18,9; 95% ДИ 6,84–52,4) по сравнению с худыми (ОШ = 3.16; 95% ДИ 1,28-7,8) [8].
Интересные данные получены в отношении риска формирования ЦП и употребления кофе. По данным мета-анализа, употребление более 2 чашек кофе в день, при прочих равных условиях, снижает риск развития алкогольного цирроза печени (АЦП) в 2 раза (ОР = 0,62; 95% ДИ 0,51-0,73) [9].
Инфекция, обусловленная гепатотропными вирусами. Инфицирование вирусами гепатитов В и С, нередко наблюдающееся у лиц, злоупотребляющих алкоголем, увеличивает скорость прогрессирования поражения печени. Так, например, при сочетанном патогенном действии алкоголя и гепатита С риск развития гепатоцеллюлярной карциномы (ГЦК) увеличивается в два раза [5].
Повышение токсичности ксенобиотиков. Злоупотребление алкоголем ведет к усилению гепатотоксического действия различных лекарственных препаратов: группы нестероидных противовоспалительных препаратов (ацетилсалициловой кислоты, индометацина, ибупрофена, парацетамола и др.), антибиотиков (например, тетрациклинового ряда), амиодарона, метотрексата, кортикостероидов, эстрогенов, противогрибковых препаратов системного действия, противотуберкулезных препаратов (например, изониазид), а также слабительных средств, тамоксифена, противосудорожных средств, психотропных, анестетиков, антидепрессантов [10].
Количество и длительность употребления алкоголя. Частота употребления алкоголя также оказывает значимое влияние на риск прогрессирования АБП. В проспективном когортном исследовании Sandahl T.D и соавт., риск развития АЦП был повышен у ежедневно употребляющих алкоголь людей (ОШ 3,65; 95% ДИ 2,39-5,55) по сравнению с теми, кто употреблял алкоголь 2-3 раза в неделю [11].
Можно выделить несколько опасных стилей употребления алкоголя:
а) Тяжелое эпизодическое употребление алкоголя (прием более 60 г этанола за один алкогольный эпизод [12].
б) Компульсивное употребление алкоголя (в англоязычной версии «binge drinking»), (прием более 4 СтД для женщин и более 5 СтД для мужчин менее чем за 2 часа.
В исследовании, проведенном Askgaard G. и соавт. было показано, что ежедневное употребление алкоголя является самым мощным индуктором формирования АЦП [13]. В то же время в исследовании Aberg F. и соавт. показано, что компульсивное употребление алкоголя является ведущим фактором риска АБП вне зависимости от среднего употребления алкоголя [14]. При компульсивном употреблении алкоголя риск формирования АЦП повышается [13].
Тип употребляемых спиртных напитков. Было доказано, что при употреблении красного вина, риск развития АЦП ниже, чем при употреблении других видов алкоголя (ОР = 0,3) [15].
Курение. Популяционное исследование, проводимое в течение двадцати лет, показало, что курение более 1 пачки сигарет в день приводило к увеличению риска прогрессирования АБП в 3 раза, по сравнению с некурящими, при условии равного количества и характера употребления алкоголя [16].
В патогенезе алкогольной болезни печени выделяют три основных звена: прямое повреждающее действие алкоголя и его метаболитов, активация иннатной иммунной системы, изменение состава кишечной микробиоты. Остановимся подробнее на каждом из них (рисунок 1).
Рисунок 1. Патогенез алкогольной болезни печени
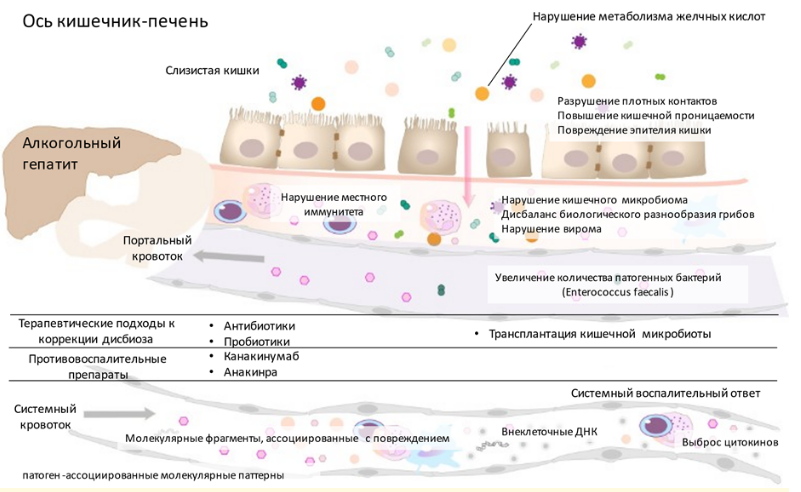
Действие алкоголя и его метаболитов. До 95% этанола окисляется в печени. Для этой цели существует три метаболических пути, которые могут функционировать параллельно или смещаться в ту или иную сторону, в зависимости от количества и длительности употребления этанола. Это пути с использованием: алкогольдегидрогеназы (АДГ), системы микросомального этанолового окисления и каталаз пероксисом.
В результате окисления этанола под действием вышеуказанных ферментов образуется ацетальдегид – высокотоксичное соединение, оказывающее основное повреждающее действие на клетки печени.
При длительном, хроническом употреблении алкоголя его метаболизм преимущественно протекает при участии цитохрома Р450 – микросомальной этанолокисляющей системы (МЭОС). В отличие от алкогольдегидрогеназы МЭОС (CYP2E1-редуктазы) индуцируемый фермент. Кроме того, через эту ферментативную систему осуществляется метаболизм ксенобиотиков, к которым относится и ряд медикаментов. Именно с индукцией CYP2E1 связанна повышенная чувствительность злоупотребляющих алкоголем лиц к некоторым лекарственным препаратам (например, нестероидным противовоспалительным средствам, анальгезирующим препаратам, в частности к парацетамолу). Данный факт необходимо учитывать при подборе терапии и дозы лекарственных препаратов пациентам, злоупотребляющим алкоголем.
Прямое токсическое действие накопленного (избыточного) ацетальдегида способствует перекисному окислению липидов, нарушению работы цепи переноса электронов и митохондриальной дисфункции, подавлению репарации ДНК, что приводит к накоплению мутаций; истощению глутатионпероксидазной защитной системы; повышению синтеза коллагена, что активирует фиброгенез. Отдавая электрон молекуле кислорода, ацетальдегид инициирует образование свободных радикалов, повреждающих белки и фосфолипиды мембран.
В исследованиях была продемонстрирована важная роль иннатной иммунной системы в развитии и прогрессировании АБП, особенно, алкогольного гепатита. Поврежденные гепатоциты выделяют широкий спектр цитокинов, привлекающих в паренхиму печени воспалительные клетки, преимущественно нейтрофилы. Активированные нейтрофилы сами служат источником свободных радикалов. Цитокины вызывают активацию клеток Ито, которые начинают интенсивно синтезировать коллаген I типа, что приводит к фиброзу печени. Ацетальдегид может непосредственно активировать клетки Ито. Таким образом, именно ацетальдегид ответственен за деструктивные, воспалительные и фибротические процессы в печени.
Известно, что под действием этанола происходит изменение состава кишечной микробиоты. Систематическое поступление этанола приводит к избыточному бактериальному росту в кишечнике преимущественно за счет грам-негативной флоры, повышению проницаемости кишечной стенки, в результате чего в систему воротной вены поступает значительное количество липополисахаридов (ЛПС). В печени они запускают сложный каскад реакций, приводящий к секреции большого количества провоспалительных цитокинов, в частности ФНО-α. Вместе с активными формами кислорода ЛПС оказывают повреждающее действие на клетку, запуская механизмы некроза и апоптоза, а также стимулируя синтез белков внеклеточного матрикса, приводя к активации процессов фиброза и цирроза печени [17].
Одной из основных молекул, нейтрализующих свободные радикалы, служит глутатион. Для его синтеза необходим цистеин, образующийся при участии S-аденозилметионина (адеметионина, SAM), который, в свою очередь, образуется из поступающего с пищей метионина посредством фермента метионинаденозилтрансферазы. Также метионин ресинтезируется в организме и его регенерация тесно связана с обменом серина и глицина и взаимопревращениями производных Н4-фолата и витамина В12. SAM не только способствует увеличению концентрации глутатиона, но также снижает образование фактора некроза опухоли альфа (ФНОα) в ответ на стимуляцию липополисахаридом (ЛПС) и увеличивает образование макрофагами противовоспалительного цитокина интерлейкина-10 (ИЛ-10) [18-21]. Алкоголь уменьшает образование SAM.
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Ежегодно употребление алкоголя в опасных дозах приводит к 3,3 миллионам смертей в год (5,9 % от общего числа смертей от всех причин), а также инвалидизации и ухудшению здоровья миллионов людей во всем мире. По данным ВОЗ на опасное и вредное употребление алкоголя приходится 5,1 % глобального «бремени болезней» и травм, что соответствует около 139 млн. лет потерянной трудоспособности, согласно оценкам в показателях DALY («Disability-adjusted life year») [22]. Алкоголь служит ведущей причиной преждевременной смерти у лиц молодого и трудоспособного возраста и составляет 10%.
Среднее употребление алкоголя в мире составляет 6,2 литра чистого этанола на человека в год, а в европейском регионе – 10,9 л/год [22]. Существуют географические различия в характере, стиле и количестве употребляемого алкоголя, что влияет на показатели заболеваемости и смертности от данной причины. По данным Росстата Министерства Здравоохранения РФ заболеваемость алкоголизмом населения России в 2020 г составило 1102,8 тысяч человек. И это только официальная статистика лиц, состоящих на учете в лечебно-профилактических организациях. Точные цифры распространённости АБП, алкоголизма, а тем более злоупотребления алкоголем, практически невозможно подсчитать.
Анализ популяционного исследования, выполненного в г. Москве в 2012 г., в которое были включены 5000 участников, показал, что злоупотребляют алкоголем 12,5% из обследованных лиц, а зависимость наблюдается у 5% согласно ответам на вопросы валидизированных опросников CAGE и AUDIT (Приложение Г). Употребление алкогольных напитков в дозе, наносящей вред здоровью (более 2 баллов в опроснике CAGE, более 16 баллов в опроснике AUDIT; p=0,04), – независимый фактор риска повреждения печени [18]. При анализе причин смертности от заболеваний печени установлено, что 41% составляют тяжелые формы АБП [23].
По данным исследования, проведенного в 2016 г распространенность лиц, злоупотребляющих алкоголем, среди пациентов гастроэнтерологического профиля составила 49,8% (AUDIT-С > 12 баллов), лиц с возможной алкогольной зависимостью (CAGE > 2 баллов) – 45,3% [24].
Столь тревожная ситуация послужила поводом для выработки как международной, так и государственной концепций по снижению вреда, наносимого населению вследствие злоупотребления алкоголем. В январе 2022 г ВОЗ в качестве приоритетного проекта здравоохранения на 2022-2030 гг разработал концепцию для эффективного осуществления глобальной стратегии по сокращению вредного употребления алкоголя. В Российской Федерации, благодаря принятым правительством мерам, направленным на уменьшение потребления алкоголя населением, удалось добиться снижения показателей употребления алкоголя на душу населения с 15,8 л (в пересчёте на чистый этанол) в 2010 году до 9,1 л в 2020 году [25]. Хотя данный показатель имеет динамику к снижению, в структуре употребляемого алкоголя преобладают крепкие алкогольные напитки и пиво (по 39%), в то время как на употребление вина приходится только 13% (по данным ВОЗ на 2018 год).
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Клинические проявления АБП зависят от стадии заболевания.
Стеатоз печени (жировая инфильтрация печени) обычно протекает бессимптомно, некоторые пациенты могут жаловаться на снижение аппетита, диспепсические расстройства, ощущение дискомфорта в верхних отделах живота после еды, тупую боль в правом подреберье. В биохимических тестах крови отклонений от нормы, как правило, не наблюдается, функция печени сохранена. Стеатоз печени часто обнаруживается совершенно случайно (диагностическая находка) при обследовании по другому поводу методом УЗИ органов брюшной полости.
Алкогольный гепатит (АлГ) представляет собой прогрессирующее воспалительно-дистрофическое поражение печени, которое может развиться на любом этапе АБП при длительном систематическом употреблении опасных доз этанола. Так как обычно гепатит развивается на фоне стеатоза печени, признаки последнего (гепатомегалия, гиперэхогенность паренхимы печени) также присутствуют, поэтому иногда используется термин «алкогольный стеатогепатит». Алкогольный гепатит проявляется реакциями острой фазы, к которым относят: лихорадку, общую слабость, артралгии, миалглии. Воспалительный отек и инфильтрация печени может приводить к увеличению ее размеров, растяжению глиссоновой капсулы, что проявляется болью в правом подреберье. На стадии АлГ иногда наблюдаются отеки и увеличение объема живота за счет асцита разной степени выраженности.
При массивном отеке печени может наблюдаться сдавление вен печени и развитие обратимой портальной гипертензии с асцитом и спленомегалией. Сдавление мельчайших желчных протоков может приводить к развитию внутрипеченочного холестаза, характеризующегося повышением активности щелочной фосфатазы (ЩФ) и ГГТ, клиническое проявление – кожный зуд, который может усиливаться в ночное время. Больные могут предъявлять жалобы на желтушное окрашивание кожи и склер.
Алкогольный цирроз печени представляет собой терминальную стадию АБП. Риск развития цирротической трансформации печени повышается пропорционально увеличению дозы алкоголя, начиная от количества более 40-60 г чистого этанола в сутки. Наиболее высокий риск развития АЦП у лиц, употребляющих более 120 г этанола в день. Формирование цирроза может происходить без стадии выраженного воспаления. При развитии АЦП в течение 5 лет умирает 60-85% больных [28], в течение 15 лет – 90% [29]. Если осложнения цирроза не развились, то в течение первого года умирает 10-20% больных, если у больного было кровотечение из варикозно-расширенных вен пищевода (ВРВП) – 20%, асцит – 30%, сочетание асцита и кровотечения из ВРВП – 50%, печеночная энцефалопатия – 60% [28].
В случае сохраненной функции печени самочувствие больных может оставаться относительно удовлетворительным. Компенсированный АЦП в 30-40% случаев протекает бессимптомно или с некоторыми неспецифическими жалобами: общая слабость, снижение или отсутствие аппетита, утомляемость, снижение работоспособности, диспепсические расстройства, снижение массы тела и потеря мышечной массы (саркопения). При декомпенсации функции печени вышеуказанные жалобы усиливаются, появляются клинические признаки печеночной недостаточности. Заболевание может манифестировать появлением отёчно-асцитического синдрома с увеличением живота в объеме/асцит, отеками нижних конечностей; желтухи, развитием печеночной энцефалопатии, кровотечением из варикозно-расширенных вен пищевода и/или желудка, прямой кишки, геморрагический синдром (кровоточивость десен и/или носовые кровотечения, спонтанное появление петехий и экхимозов и др.), инверсия сна (бессонница ночью и сонливость днем). При напряженном асците и/или гидротораксе может появиться одышка при нагрузках, а также кашель в положении лежа. У женщин детородного возраста проявлением АЦП может быть нарушение менструального цикла, вплоть до аменореи, а у мужчин – эректильная дисфункция и снижение либидо [27].
Таким образом, клиническая картина ЦП не зависит от этиологии заболевания и ее подробное описание можно найти в клинических рекомендациях Минздрава РФ 2021 г [27].
При объективном осмотре обнаруживаются стигмы длительного злоупотребления алкоголем (раздел 2.2).
У пациентов с АБП могут наблюдаться различные проявления авитаминоза. Так недостаток тиамина (поступает в организм с пищей и частично синтезируются микрофлорой кишечника) вследствие хронического употребления алкоголя служит одним из факторов повреждения головного мозга. Тиамин – предшественник кофактора (тиаминдифосфата – ТДФ), представляющий собой активную часть ТДФ-зависимых ферментов (пируватдегидрогеназный и альфа-кетоглутаратдегидрогеназный комплексы и транскетолазы), катализирующих обменные процессы, связанные с получением энергии. Данный процесс имеет особое значение в нервной ткани. ТДФ участвует в метаболизме углеводов, его дефицит влияет на многочисленные клеточные функции, в частности снижается утилизация глюкозы нейронами. Накопление глутамата в результате снижения активности альфа-кетоглутаратдегидрогеназного комплекса на фоне дефицита энергии оказывает нейротоксическое действие. Вследствие этого происходят уменьшение числа нейронов, демиелинизация и глиоз области перивентрикулярного серого вещества. Хроническое употребление алкоголя приводит к снижению потребления тиамина с продуктами питания, уменьшению его абсорбции из желудочно-кишечного тракта, и снижению тиамин-зависимых реакций в клетках. Более того, существуют различия в индивидуальной восприимчивости к дефициту тиамина.
При хронической алкогольной интоксикации на фоне дефицита тиамина развивается синдром Вернике–Корсакова, включающий в себя энцефалопатию Вернике (острая фаза) и корсаковский психоз (хроническая фаза).
Классические симптомы энцефалопатии Вернике – офтальмоплегия, нистагм, помрачение сознания и атаксия – в большинстве случаев отсутствует, расстройство остается нераспознанным, и пациенты не получают необходимого лечения.
Частота смертельного исхода в отсутствие терапии составляет 15%, а вероятность перехода в корсаковский психоз, практически не поддающийся обратному развитию, достигает 60% [2].
Для предупреждения неблагоприятных исходов энцефалопатии Вернике при отсутствии ее типичных проявлений следует принимать во внимание возможные дополнительные симптомы, включая тошноту, рвоту, артериальную гипотензию, гипотермию и кому.
Своевременное интенсивное терапевтическое вмешательство (парентеральное ведение высоких доз тиамина**) позволяет предупредить смертельный исход и развитие корсаковского психоза (раздел 3).
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Диагноз алкогольной болезни печени устанавливается при подтвержденном заболевании печени вследствие систематического употребления этанола в опасных дозах. Установление факта длительного употребления алкоголя имеет важное значение для эффективного ведения и своевременного лечения пациента. Рекомендовано использовать опросники и скрининговые тесты для выявления лиц с высоким риском АБП. Постановка диагноза и ведение пациентов с АБП должны осуществляться мультидисциплинарной командой.
Диагноз АБП можно заподозрить на основании анамнестических, клинических, лабораторно-инструментальных признаков. В сложных диагностических случаях, для исключения сопутствующей патологии по показаниям может быть проведена морфологическая верификация.
Диагноз алкогольной болезни печени может быть заподозрен при:
- Анамнестических данных (употребление >20 г этанола в сутки для женщин и >30 г для мужчин при наличии клинических и/или лабораторных признаков поражения печени)
- Скрининговых тестов (тест AUDIT (Alcohol Use Disorders Inventory Test) > 8 баллов – высокий риск алкогольного поражения печени)
- Физикального обследования (обнаружение стигм алкогольной болезни печени (см. раздел 2.2)
- Инструментального обследования (повышение уровня гаммаглутамил-транспептидазы, коэффициент де Ритиса > 1 (АСТ/АЛТ)).
- Применение опросников с целью выявления алкогольного генеза поражения печени рекомендовано для всех пациентов с предполагаемым диагнозом алкогольной болезни печени для определения групп высокого риска по развитию данного заболевания [2,23,30,34]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарии: Важно своевременно и как можно раньше выявлять пациентов с АБП до развития терминальных стадий заболеваний печени. При сборе анамнеза необходимо учитывать, что пациенты с АБП, потребляющие алкоголь в опасных дозах, склонны преуменьшать количество выпиваемого алкоголя или вовсе отрицать сам факт употребления алкоголя. Общение с родственниками пациентов играет значимую роль для выявления факта злоупотребления алкоголем.
Сбор алкогольного анамнеза (скрининг) должен быть стандартизован. Для этого существуют валидизированные опросники, «золотым стандартом» остается опросник AUDIT (Alcohol Use Disorders Inventory Test), разработанный ВОЗ в 1982 г., который демонстрирует высокую чувствительность и специфичность в разных странах [23,31]. Вопросник AUDIT включает 10 вопросов, которые можно условно разделить на секции: вопросы № 1–3 дают возможность получить от пациента информацию о количестве принимаемого алкоголя, вопросы № 4–6 направлены на выявление зависимости, вопросы № 7–10 позволяют получить информацию о проблемах, которые ассоциированы с приемом алкоголя (Приложение Г). Каждый пункт оценивают путем выбора варианта ответа пациентом с последующим подсчетом баллов. В зависимости от количества набранных баллов производят интерпретацию теста [32].
Согласно результатам скрининга, необходимо информировать пациента о том, что злоупотребление алкоголем сопряжено с риском развития более 200 заболеваний, в том числе злокачественных опухолей.
- Рекомендовано пациентам с подозрением на злоупотребление алкоголем на первичном приеме выполнить скрининг посредством вопросника AUDIT-C для уточнения стиля употребления алкоголя, с решением вопроса о использовании полной версии AUDIT [32].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Для ежедневного использования в условиях дефицита времени на первичном приеме можно использовать сокращенную версию вопросника AUDIT – AUDIT-С, которая включает только первые три вопроса. Максимальное количество баллов – 12 (Приложение Г). Чем больше баллов, тем больше вероятность того, что стиль употребления алкоголя оказывает негативное влияние на организм человека. При положительном результате сокращенной версии рекомендовано использовать полную версию вопросника AUDIT.
Также в качестве старта скрининга можно начать с вопроса № 3 из вопросника AUDIT: Как часто вы выпиваете 6 доз и более в течение 1 дня (т. е. ~180 мл водки или других крепких напитков либо ~600 мл вина и т. п.)? В случае ответа «1 раз в неделю» либо «ежедневно или почти ежедневно» рекомендуется далее заполнить весь вопросник AUDIT.
- Рекомендовано пациентам с подозрением на злоупотребление алкоголем проводить скрининг при помощи вопросника CAGE для уточнения наличия алкогольной зависимости [2,3,33,34].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Вопросник CAGE – один из хорошо апробированных и информативных тестов в мире (Приложение Г). Вопросник прост для заполнения, врач легко и быстро оценивает ответы больных [34].
Скрининг на АБП следует проводить в группах высокого риска, у всех лиц, злоупотребляющих алкоголем, выявленных лечащим врачом на первичном приеме, у пациентов, находящихся на лечении в наркологических клиниках по поводу алкогольной зависимости, в клиниках реабилитации от алкоголизма. Важно обращать внимание на стигмы употребления алкоголя (раздел 2.2.), а также на изменения лабораторных методов исследования (раздел 2.3), характерных для пациентов с АБП.
- Для контроля абстиненции пациентам с АБП рекомендовано количественное определение уровня этилглюкуронида (EtG) в моче или обнаружение этиленклюкуронида в волосах [3]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Существуют прямые биомаркеры употребления алкоголя, к ним относятся этилглюкуронид (EtG), этилсульфат (EtS), фосфатидилэтанол (PEth) и этиловые эфиры жирных кислот. Это прямые продукты неокислительного метаболизма этанола, обладающие большей специфичностью, по сравнению с непрямыми маркерами. Среди перечисленных биомаркеров следует выделить определение этилглюкуронида в моче. Этот биомаркер используется во многих странах для контроля абстиненции у лиц, находящихся в листе ожидания трансплантации печени. Этилглюкуронид мочи определяется в течение 80 часов после употребления алкоголя. Для скрининга рекомендуется использовать иммунологический метод определения, а в случае положительного результата проводить повторное исследование с помощью хроматографии и спектрометрии [3]. Важным преимуществом этого биомаркера служит отсутствие диагностических погрешностей у пациентов с ЦП. Чувствительность и специфичность этого метода у пациентов, находящихся в листе ожидания трансплантации печени, составляет 89% и 99%, соответственно [3]. Однако в широкой клинической практике перечисленные методы диагностики не используются.
1. Жалобы и анамнез
Не существует специфических для АБП жалоб. На разных стадиях (от алкогольного стеатоза до цирроза печени) жалобы могут варьировать – см. раздел 1.6.
Алкогольный анамнез – см. раздел 2. Помимо алкогольного анамнеза, у пациентов с АБП важно тщательно собирать историю употребления лекарственных препаратов, с выяснением всех используемых медикаментов по назначению врачей (наличие полипрагмазии), так и без назначения. Необходимо выявлять препараты, которые могут оказывать дозозависимый, токсический эффект и прямое повреждающее действие на печень, а также проводить активный опрос пациента об употреблении биологически активных добавок (БАД), витаминов и препаратов растительного происхождения, которые пациенты часто назначают себе самостоятельно и не считают нужным рассказать о них врачу.
Важно выявлять наличие сопутствующих и сочетанных заболеваний или отдельных симптомов, которые могут быть связаны с повреждением печени и усугублять развитие и течение АБП. Быстрое прогрессирование АБП чаще наблюдается у лиц с сопутствующими (сахарный диабет, ожирение и метаболический синдром, ВИЧ-инфекция, артериальная гипертензия, гиперлипидемия и т.д.) и сочетанными (вирусные гепатиты В и С, перегрузка железом, дефицит альфа-1-антитрипсина и др.) заболеваниями. Вирусные гепатиты и алкоголь обладают синергетическим эффектом в отношении прогрессирования фиброза печени.
Следует уточнить наличие аутоиммунных заболеваний (например, аутоиммунный тиреоидит, воспалительные заболевания кишечника, синдром Шегрена и т.д.), которые могут быть ассоциированы с повреждением печени и усиливать повреждающее действие на ткани печени этанола с прогрессированием АБП.
Обязательно выявление других вредных привычек, в том числе курение, прием наркотических препаратов.
2. Физикальное обследование
Характерные для пациентов с АБП данные физикального обследования зависят от стадии АБП. Они могут варьировать от незначительной астении и диспепсии до симптомов, характерных для острой печёночной недостаточности.
При стеатозе печени, как правило, проявления либо отсутствуют, либо очень скудные. У пациентов с АлС с прогрессированием заболевания может наблюдаться дефицит массы тела, вплоть до истощения и саркопении на стадии цирроза. При пальпации печень может быть увеличена, с гладкой поверхностью и закругленным краем.
На любой стадии АБП при осмотре пациента нередко обнаруживают стигмы длительного злоупотребления алкоголем: «facies alcoholica», яркие телеангиэктазии, гинекомастию, контрактуру Дюпюитрена, пальмарную эритему, увеличение околоушных слюнных желез, ринофиму, расширение сосудов носа и склер, атрофию мышц плечевого пояса, атрофию яичек, тремор пальцев рук, гипергидроз кожи лица и ладоней, различные степени проявления полинейропатии.
У пациентов с алкогольным гепатитом могут отмечаться признаки печеночной энцефалопатии разной степени выраженности и геморрагического синдрома (синяки, кровоточивость слизистых оболочек, желудочно-кишечные кровотечения) в рамках клинических проявлений печеночной недостаточности. При общем осмотре чаще всего на этой стадии можно отметить пониженное питание или даже дефицит ИМТ за счет саркопении. При осмотре живота можно обнаружить расширение вен передней брюшной стенки, отеки, асцит, увеличенную, иногда болезненную при пальпации печень. При массивном воспалительном отеке печени возможно развитие обратимой портальной гипертензии с асцитом и спленомегалией. Иногда формируется внутрипеченочный холестаз с клиническим проявлением в виде кожного зуда и следов расчесов по всему телу.
На стадии АЦП признаки печеночной недостаточности нарастают, клинические проявления становятся выраженными. Могут появиться и усилиться отеки разной локализации, вследствие гипоальбуминемии; телеангиэктазии на коже лица, груди и спины, пальмарная эритема, гинекомастия из-за гиперэстрогении вследствие нарушения обезвреживания активных форм эстрогенов в печени; желтушность кожных покровов и склер, вследствие гипербилирубинемии из-за снижения глюкуронилтрансферазной реакции и детоксицирующей функции печени. Признаки портальной гипертензии: асцит, гепато- и спленомегалия, венозные коллатерали на передней брюшной стенке («голова медузы») и расширение геморроидальных вен. Часто на стадии декомпенсации АЦП у пациентов можно обнаружить тахикардию в покое и гипотонию (гипердинамическое кровообращение) [27]. АЦП с синдром избыточного бактериального роста в кишечнике может проявляться повышением температуры тела (без очевидного источника инфекции), вздутием, урчанием в животе, болезненностью при пальпации живота, ослаблением кишечной перистальтики при аускультации (преходящий парез кишечника), расстройством стула, чаще наблюдается диарея [27].
При наличии выраженного асцита перкуторно над местом скопления свободной жидкости в брюшной полости можно определить тупой звук вместо тимпанита. При напряженном асците пальпация внутренних органов затруднена.
При АЦП может отмечаться полиорганность поражения: алкогольная полинейропатия, панкреатит, кардиомиопатия и т.д., что требует своевременного и тщательного физикального осмотра и обследования таких пациентов у профильных специалистов.
У пациентов с АЦП высока вероятность развития печеночной энцефалопатии (ПЭ), главным проявлением которой служит изменение сознания. ПЭ может проявляться от клинически бессимптомных форм (минимальная ПЭ) до коматозного состояния. Печеночная энцефалопатия требует дифференциальной диагностики с другими заболеваниями неврологического характера (нарушение мозгового кровообращения, неврологические и психические заболевания). При любых подозрениях на ПЭ необходимо оценить сознание, поведение, интеллект, неврологический статус (тремор, изменение почерка, психометрические тесты).
3. Лабораторные диагностические исследования
- Рекомендовано проведение общего (клинического) анализа крови пациентам с АБП для исследования уровня эритроцитов, общего гемоглобина, лейкоцитов, тромбоцитов в крови [2,3,5,23,35].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: В общем анализе крови может отмечаться макроцитоз (увеличение среднего объёма эритроцита – MCV), повышение значения цветового показателя (гиперхромия), а также снижение уровня гемоглобина (анемия). Анемия может быть различной природы и выраженности, чаще всего вследствие дефицита витаминов (фолиевой кислоты и В12), кроме того, вклад могут вносить оккультные кровотечения и постгеморрагическая анемия, а также анемия хронических заболеваний.
У пациентов с АЦП в анализах может быть выявлена трехростковая цитопения. Возможно наличие лейко- и тромбоцитопении, что отражает синдром гиперспленизма. Однако, у пациентов с АЦП спленомегалия и гиперспленизм могут быть выражены минимально или отсутствовать вовсе, что не исключает стадию цирроза. В случае впервые выявленной тромбоцитопении обязательно проведение ручного подсчета форменных элементов крови (дифференциальный диагноз с агрегацией тромбоцитов).
В то же время, при выраженном некровоспалительном процессе в печени в анализах крови может наблюдаться нейтрофильный лейкоцитоз, ускорение СОЭ.
- Рекомендовано проведение анализа крови биохимического общетерапевтического, включая такие показатели как общий белок, альбумин, общий билирубин, прямой билирубин, креатинин, аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (АСТ), щелочная фосфатаза, гамма-глутамилтранспептидаза (ГГТ), лактатдегидрогеназа (ЛДГ), глюкоза, пациентам с АБП для оценки синтетической и некровоспалительной активности, холестаза, функции печени и почек [2,3,5,23,35,36,37].
Уровень убедительности рекомендаций С (Уровень достоверности доказательств – 5).
Комментарии: В результате некроза гепатоцитов в биохимическом анализе крови отмечается повышение уровней печёночных АЛТ, АСТ (более чем в два раза превышает норму, но редко бывает более 300 ед/мл), ЛДГ. Как правило, уровень АСТ выше, чем АЛТ (индекс де Ритиса – АСТ/АЛТ > 1.) [2,3,35].
Повышение активности аминотрансфераз по мере прогрессирования хронического заболевания печени теряет клиническое значение – при декомпенсированном АЦП активность аминотрансфераз может быть в норме или повышена незначительно.
Алкоголь стимулирует экспрессию гена ГГТ. Активность сывороточной ГГТ повышена примерно у 75% лиц, злоупотребляющих алкоголем (чувствительность 60-90%, специфичность 50-72%). При скрининговом исследовании повышение активности ГГТ выявляют у 20% мужчин и 15% женщин, принимающих около 40 г алкоголя в день, и у 40-50% мужчин и 30% женщин, выпивающих более 60 г алкоголя в день. Период полураспада ГГТ составляет 14-26 дней, поэтому активность фермента в крови нормализуется в течение 4-5 недель после прекращения приема алкоголя [2,37]. В связи с этим, оценка активности ГГТ должна проводиться у всех пациентов с предполагаемым диагнозом АБП. Однако нельзя забывать, что уровень ГГТ может отражать и метаболические нарушения (коррелирует с повышением ИМТ).
Несмотря на то, что указанные выше показатели чаще всего используются для ранней диагностики алкогольного поражения печени, их чувствительность и специфичность невысоки.
Обязательно исследование уровня альбумина для оценки белковосинтетической функции печени. В рамках печеночной недостаточности отмечается изолированное снижение уровня альбумина при нормальном/пограничном уровне общего белка.
Исследование концентрации креатинина позволяет оценить функцию почек, в том числе рекомендовано пациентам, планирующим проведение компьютерной томографии (КТ) с введением контрастных веществ. Повышение уровня креатинина может быть признаком самостоятельного заболевания гепато-ренальной системы или быть признаком острого поражения почек при АЦП. В клинической практике обращают внимание на динамику этого показателя за определенные отрезки времени. Быстрый прирост креатинина может соответствовать критериям острого повреждения почек даже в рамках нормальных значений показателя.
Снижение уровня креатинина служит неблагоприятным прогностическим маркером и отражает дефицит мышечной ткани. Помимо трансфузий раствора альбумина человека** таким пациентам показано назначение соответствующей высокобелковой диеты и/или энтерального питания для коррекции нутритивного статуса.
При выраженном поражении печени может развиваться печёночная недостаточность, которая манифестирует следующими симптомами: гипербилирубинемией с преобладанием как прямой фракции билирубина (нарушение транспорта в желчные канальцы; выраженный отёк паренхимы печени, приводящий к сдавлению желчных канальцев), так и непрямой (недостаточность глюкуронилтрансферазной активности; нарушение захвата непрямого билирубина на базолатеральной мембране гепатоцита); гипокоагуляцией; гипоальбуминемией. Последние 2 состояния связаны со снижением белково-синтетической функции печени.
- Рекомендовано выполнение коагулограммы (ориентировочного исследования системы гемостаза), включая определение таких показателей как международное нормализованное отношение (МНО), протромбиновый индекс %, фибриноген, протромбин, протромбиновое (тромбопластиновое) время в крови пациентам с АБП, особенно при подозрении на АЦП для оценки коагуляционного статуса, функции печени и при подозрении на тяжелый АлГ[ 5,38,39,40,77].
Уровень убедительности рекомендаций С (Уровень достоверности доказательств – 4).
Комментарии: при печеночной недостаточности отмечается снижение синтеза всех плазменных факторов коагуляции – как про-, так и антикоагулянтных звеньев гемостаза. В большей степени при использовании стандартных тестов выявляют признаки гипокоагуляции: повышение МНО, снижение протромбинового индекса и уровня фибриногена. Оценка протромбинового времени необходима для подсчета индекса Маддрея и оценки степени тяжести АлГ.
- Рекомендовано исследование общего (клинического) анализа мочи пациентам с АБП для исключения мочевой инфекции, а также пациентам с АЦП с повышением уровня креатинина для исключения протеинурии, цилиндрурии как признака самостоятельного заболевания почек и дифференциальной диагностики с острым повреждением почек [2,3,5,40,83,87,88].
Уровень убедительности рекомендаций С (Уровень достоверности доказательств – 4).
Комментарии: Изменения в анализе мочи (лейкоцитурия, эритроцитурия, протеинурия) позволяют исключить гепаторенальный синдром у пациентов с АЦП и указывают на наличие самостоятельного заболевания почек или инфекции. Следует помнить, что даже латентная мочевая инфекция может провоцировать печеночную энцефалопатию и острую печеночную недостаточность на фоне хронической (и декомпенсацию АЦП).
- Рекомендовано исследование маркеров вирусных гепатитов (определение антител класса M к вирусу гепатита A (anti-HАV IgM), определение антигена (HbsAg) вируса гепатита B (Hepatitis B virus) в крови, определение суммарных антител классов M и G (anti-HCV IgG и anti-HCV IgM) к вирусу гепатита C (Hepatitis C virus) в крови, определение антител к вирусу гепатита D (Hepatitis D virus) в крови, определение антител класса M (anti-HEV IgM) к вирусу гепатита Е (Hepatitis E virus) в крови); а также исследование насыщения трансферрина железом (при подозрении нарушений обмена железа – гематохроматоз или вторичные перегрузки железом), церулоплазмина пациентам с АБП для уточнения этиологии заболеваний и исключения сочетанных заболеваний [2,3,5,6,83].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств – 5)
- Рекомендовано исследование иммуноглобулинов (Ig) А, M, G пациентам с АБП для уточнения этиологии заболевания и исключения сочетанных заболеваний [5,83,89].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств – 5).
Комментарии: Участие гуморальных механизмов в развитии АБП проявляется повышением сывороточных иммуноглобулинов, преимущественно IgA. Исследования концентрации иммуноглобулинов M и G в плазме крови необходимо для проведения дифференциальной диагностики с аутоиммунными заболеваниями печени.
4. Инструментальные диагностические исследования
Методы визуализации, такие как ультразвуковое исследование, магнитно-резонансная и компьютерная томография, позволяют количественно оценить степень стеатоза печени, а также помогают исключить другие причины хронического заболевания печени и способствуют оценке прогрессирующего заболевания печени и его осложнений независимо от этиологии.
- Рекомендовано проведение ультразвукового исследования (УЗИ) органов брюшной полости пациентам с АБП с целью определения размеров и ультразвуковых характеристик печени, диагностики портальной гипертензии (обнаружение асцита, измерение диаметра воротной и селезеночной вен, размеров селезенки), исключения очаговых образований печени, при возможности использовать ультразвуковую доплерографию для оценки проходимости печеночных и воротных вен, с целью обнаружения тромбоза сосудов портальной системы [2,3,5,23].
Уровень убедительности рекомендаций С (Уровень достоверности доказательств – 5).
Комментарии: Проведение УЗИ органов брюшной полости показано всем пациентам с АБП с целью скрининга портальной гипертензии, оценки состояния паренхимы печени, определения ее размеров, расположения, контуров, звукопроводимости, эхогенности, определения функциональных показателей. При проведении ультразвукового исследования обращают особое внимание на степень затухания (аттенюации) УЗ-сигнала, гиперэхогенность печени, размеры воротной и селезеночной вен. При УЗИ обнаруживают характерную гиперэхогенную структуру печени. Однако, УЗИ обладает низкой чувствительностью и специфичностью в диагностике степень стеатоз печени (особенно при пороговом значении ниже 20-30% стеатоза) [3].
При УЗИ признаками портальной гипертензии служат расширение воротной вены до 13 мм и более, снижение в ней скорости кровотока либо ретроградный кровоток, появление портокавальных коллатералей (параумбиликальная вена, расширение селезеночной вены и др.), спленомегалия [27].
- Рекомендовано проведение эзофагогастродуоденоскопии (ЭГДС) пациентам с АБП с целью оценки размеров вен пищевода и желудка и исключения пятен васкулопатии как стигм высокого риска кровотечения, особенно у пациентов с АЦП [2,3,5,27].
Уровень убедительности рекомендаций С (Уровень достоверности доказательств – 5).
Комментарии: Эзофагогастродуоденоскопия (ЭГДС) необходима пациентам с подозрением на наличие портальной гипертензии для исключения варикозного расширения вен пищевода. Пациентам, продолжающим употребление алкоголя, с высоким риском цирротической трансформации печени или с подтвержденным диагнозом АЦП для определения наличия и степени варикозно-расширенных вен пищевода и желудка проведение ЭГДС обязательно.
- Рекомендовано пациентам с АБП проведение регистрации электрокардиограммы (ЭКГ) для исключения нарушений ритма сердца, косвенных признаков алкогольной кардиомиопатии и других сочетанных и сопутствующих заболеваний сердца [5,84-86].
Уровень убедительности рекомендаций С (Уровень достоверности доказательств – 4).
При наличии показаний и отсутствии противопоказаний (не всем пациентам с АБП):
- Рекомендовано проведение компьютерной томографии (КТ) брюшной полости с внутривенным контрастированием (в отсутствии противопоказаний для введения контраста) пациентам с АБП и подозрением на тромбоз в венах портальной системы или с очаговыми изменениями печени на ультразвуковом исследовании с целью исключения тромбоза и уточнения генеза очагов [2,3,5].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств – 5).
- Рекомендовано проведение магнитно-резонансной томографии (МРТ) брюшной полости с внутривенным контрастированием гепатоспецифичным контрастным агентом (в отсутствии противопоказаний для введения контраста) пациентам с АБП и очаговыми изменениями печени на ультразвуковом исследовании (при невозможности проведения компьютерной томографии или сохраняющихся сомнениях о генезе очагов после ее проведения) с целью определения этиологии образований печени, позволяет уточнить характер неясных изменений печени [2,3,5].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств – 5).
Комментарии: Международное агентство по исследованию рака (International Agency for Research into Cancer (IARC) ВОЗ с 1988 года относит алкоголь к канцерогенам 1 группы – к веществам с самой высокой способностью вызывать онкологические заболевания у человека. Пациенты с АБП находятся в группе риска развития гепатоцеллюлярной карциномы.
- Рекомендовано пациентам с АБП проведение пункционной биопсии печени и патолого-анатомического исследования биопсийного материала ткани печени, когда диагноз вызывает сомнения и требует исключения других возможных причин поражения печени при отсутствии абсолютных противопоказаний к ее проведению (см.ниже) [3].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств – 5).
Комментарии: Примерно у 20% пациентов с установленным диагнозом АБП выявляется сочетанное заболевание печени. Биопсия печени может быть проведена для подтверждения диагноза АБП, оценки стадии заболевания, а также для исключения других причин поражения печени [2,3,5]. Для проведения биопсии печени необходимо иметь строгие показания, предварительно оценить результаты общего анализа крови и коагулограммы. Тяжелые осложнения при выполнении биопсии печени, такие как внутрипеченочное кровотечение, пневмоторакс и другие, возникают примерно у 2% пациентов.
- Рекомендовано пациентам с АБП и наличием показаний и отсутствии абсолютных противопоказаний (см. ниже) к проведению биопсии печени при выявлении в анализах тромбоцитопении и увеличенном протромбиновом времени (ПВ) проводить трансъюгулярный, а не привычный чрескожный доступ [49].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Абсолютные противопоказания к биопсии печени:
- Нарушение гемостаза; склонность к кровотечениям с выраженным нарушением протромбинового времени (тромбопластиновое время < 70%, АЧТВ > 1,5 верхних границ норм ; тромбиновое время > 1,5 верхних границ норм, тромбоцитопения < 80 х 109/л)
- Тяжелое, коматозное состояние пациента
- Перитонит, сепсис
- Выраженная портальная, билиарная гипертензия
- Недееспособность пациента (ПЭ 3-4 стадии, психическое заболевание), невозможность подписать добровольное информированное согласие.
Морфологические признаки алкогольной болезни печени.
Морфологический спектр проявлений АБП состоит из четырех основных групп изменений:
- стеатоз, преимущественно макровезикулярный, реже – микро-, макровезикулярный;
- повреждение гепатоцитов, часто описываемое как баллонная дистрофия;
- воспалительный инфильтрат преимущественно лобулярной локализации;
- фиброз различной степени, вплоть до выраженного, с нарушением долькового строения печеночной ткани и формированием стадии ЦП.
У одного пациента возможно сочетание различных видов морфологических изменений либо присутствие какого-либо одного из них, например стеатоза. Частота выявления отдельных морфологических изменений печени среди лиц, злоупотребляющих алкоголем, неизвестна. Согласно результатам отдельных исследований с проведением биопсии печени, частота обнаружения стеатоза составляет 28%, фиброза (в сочетании со стеатозом и без него) – 20%, алкогольного гепатита – 8,5%, ЦП – 29% [49]. Наиболее часто и рано выявляемый гистологический признак АБП – макровезикулярный стеатоз, который традиционно считали доброкачественным и обратимым состоянием в случае абстиненции. Получены данные об ассоциации стеатоза с риском быстрой прогрессии в фиброз, развитии ЦП в течение 10,5 лет у 10% больных [49].
При алкогольном гепатите (стеатогепатите) наблюдается сочетание стеатоза, баллонной дистрофии и воспаления, которое представлено полиморфно-клеточным нейтрофильным инфильтратом. Наличие телец Мэллори и гигантских митохондрий нехарактерно для АБП, тем не менее встречается достаточно часто и ассоциируется с активным употреблением алкоголя [49]. Развитие фиброза лежит в основе формирования ЦП при АБП, что наблюдается у 40% больных алкогольным гепатитом. ЦП, как правило, бывает микронодулярным, иногда – макро-, микронодулярным [2,49].
Прогноз пациентов с АЦП во многом зависит от наличия осложнений. К наиболее серьезным из них относятся печеночная энцефалопатия, кровотечения из варикозно-расширенных вен пищевода и/или желудка, асцит и спонтанный бактериальный перитонит, гепаторенальный синдром, гипонатриемия разведения. Диагностика указанных состояний должны проводиться в обязательном соответствии с разработанными алгоритмами и клиническими рекомендациями [27].
5. Иные диагностические исследования
В круг дифференциального диагноза должны быть включены следующие заболевания: неалкогольный стеатогепатит, лекарственное поражение печени, острые вирусные гепатиты, болезнь Вильсона, нарушение обмена железа, аутоиммунные болезни печени, недостаточность α1-антитрипсина. Для исключения указанных заболеваний необходим тщательный сбор анамнеза, рациональное использование лабораторных тестов, инструментальных методов, в ряде случаев – выполнение биопсии печени (рис.2).
1. Неинвазивная диагностика фиброза печени.
С целью определения стадии заболевания (выраженности фиброза) при АБП доступны сывороточные тесты. Изначально их разрабатывали для пациентов с вирусными гепатитами, а потом стали применять при АБП. Необходимо учитывать, что пороговые значения для разграничения стадий фиброза различаются в зависимости от этиологии поражения печени.
Неинвазивные диагностические методы оценки стадии заболевания печени у пациентов с АБП могут быть использованы в случаях, когда рутинные методы обследования не позволяют получить достоверные результаты, а также в случаях, когда проведение биопсии печени нецелесообразно или невозможно.
- Рекомендовано пациентам с АБП в качестве предпочтительного неинвазивного диагностического индекса для определения степени фиброза печени использовать ФиброТест [2,3,44].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: ФиброТест рассчитывается по результатам анализа крови, включает оценку следующих показателей: уровни α2-макроглобулина, гаптоглобина, ГГТ, аполипопротеина (АроА1) и билирубина, а также пол и возраст пациента. В исследовании с участием 221 пациента с гистологически доказанной АБП среднее значение ФиброТеста составило 0,29 для тех, у кого не было фиброза, и 0,88 у пациентов с ЦП, AUROC для пациентов с ЦП 0,95 [3,44].
Пациентам с АБП при отсутствии возможности проведения ФиброТеста, а также в сложных диагностических ситуациях для уточнения степени прогрессирующего фиброза и АЦП могут быть дополнительно рассчитаны один или несколько индексов из числа нижеперечисленных:
- Рекомендовано пациентам с АБП в качестве дополнительного неинвазивного индекса для определения степени фиброза печени использовать ФиброМетр [2,44].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Фиброметр – сывороточный маркер фиброза, который включает протромбиновое время, уровни α2-макроглобулина и гиалуроновой кислоты, возраст пациента. Его диагностическая точность при АБП подобна таковой ФиброТеста, AUROC для фиброза 0,80, для ЦП – 0,90.
- Рекомендовано пациентам с АБП в качестве дополнительного неинвазивного индекса для определения степени фиброза печени использовать Hepascore [44].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Hepascore – сывороточный маркер фиброза, который включает уровни билирубина, ГГТ, гиалуроновой кислоты, α2-макроглобулина, возраст и пол пациента. Диагностическую точность ФиброТеста, Фиброметра и Hepascore оценивали при АБП. Диагностические показатели Фиброметра и Hepascore не отличались от таковых ФиброТеста при выраженном фиброзе (AUROC около 0,80) и ЦП (AUROC около 0,90), но были статистически значимо выше, чем результаты исследования фиброза посредством непатентованных методов (APRI, Forns – включает количество тромбоцитов, уровни ГГТ и холестерина, возраст пациента; FIB4 – включает количество тромбоцитов, активность АЛТ и АСТ, возраст пациента). Использование комбинаций каких-либо из этих тестов не повышает диагностическую точность, и не рекомендуются для применения в клинической практике [28,45].
- Рекомендовано пациентам с АБП в качестве дополнительного диагностического индекса для определения степени фиброза использовать PGAA [2,3,44].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Для подсчета индекса PGAA исследуют следующие биомаркеры – протромбиновый индекс, ГГТ, ApoA1 и альфа-2-макроглобулин.
- Не рекомендовано пациентам с АБП в качестве дополнительного метода исследования степени фиброза рассчитывать Индекс APRI [3].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Индекс APRI (отношение значения АСТ к уровню тромбоцитов) оценивали у 1308 пациентов с АБП, при этом чувствительность составила 13,2%, специфичность – 77,6%. Диагностическую точность индекса в диагностике фиброза при АБП не изучали [28].
- Рекомендовано пациентам с АБП для определения стадии фиброза печени использовать эластометрию печени (транзиентную эластографию (ТЭ)) печени [2,3,35,41,42,43,44].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 1).
Комментарии: По данным ряда исследований применение ТЭ печени может быть эффективно использовано для определения стадии фиброза у пациентов с АБП [2,3,35,41,42,43]. Показатели плотности печени у пациентов с АЦП значительно превосходят таковые у пациентов с вирусными циррозами печени [3]. Результаты других исследований свидетельствуют о том, что наличие активного алкогольного гепатита, сопровождающегося повышением АСТ >100 ЕД/л, приводит к значительному завышению показателя плотности печени при использовании ТЭ [3]. Это необходимо учитывать при проведении исследования. Кроме того, воспаление, холестаз и застойные явления в печени могут увеличивать показатели плотности печени независимо от стадии фиброза. Употребление алкоголя также может увеличивать значение плотности печени, в то время как отказ от алкоголя может снижать значение данного показателя.
Недавний систематический обзор, основанный на пяти ретроспективных и девяти проспективных когортных исследованиях с участием в общей сложности 834 пациентов, продемонстрировал высокую диагностическую точность ТЭ печени в качестве метода для исключения тяжелого фиброза или ЦП у пациентов с АБП с использованием пороговых значений 9,5 и 12,5 кПа, соответственно [44]. Тяжелый фиброз может быть исключен у пациентов с показателями ТЭ печени менее 8-10 кПа, тяжелый фиброз должен быть заподозрен у пациентов со значениями ТЭ 12-15 кПа (после исключения причин, которые способны дать ложноположительный результат). [45].
Тем не менее, в настоящее время пороговые значения плотности печени у пациентов с АБП недостаточно валидизированы, поскольку существует риск завышения значений плотности печени у пациентов, злоупотребляющих алкоголем.
2. Оценка тяжести алкогольного гепатита
В отличие от МКБ-10 в клинической классификации АБП алкогольный гепатит разделен на стеатогепатит и острый (тяжелый) алкогольный гепатит. Последний манифестирует быстрым прогрессированием печеночной недостаточности, развитием желтухи, асцита, нарушением свертываемости крови и характеризуется высокой краткосрочной летальностью (30-50%). Таким образом, определение тяжести алкогольного гепатита не является формальностью, так как с этим связан прогноз и, соответственно, тактика лечения пациента.
- Рекомендовано применение индекса Маддрея для оценки тяжести алкогольного гепатита у всех пациентов с АБП при наличии желтухи и печёночной недостаточности [2,3,5,23,45].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: Для диагностики и лечения алкогольного гепатита тяжелого течения разработаны оценочные показатели, позволяющие выявлять пациентов с высоким риском летального исхода. Наиболее распространенный из них – индекс Маддрея (дискриминантная функция, DF). Приложение Г. Результат, превышающий 32 балла, свидетельствует о тяжелом алкогольном гепатите и служит показанием к назначению преднизолона в дозе 40 мг/сутки [2,3]. Преимуществом данного показателя служит простота использования и длительный опыт применения в клинике. К недостаткам можно отнести применение протромбинового времени для расчета индекса. Данный показатель может варьировать в зависимости от чувствительности реагента на тромбопластин, использующийся в лабораторном тесте.
- Рекомендовано применение индекса MELD для оценки тяжести алкогольного гепатита у всех пациентов с АБП при наличии желтухи и печёночной недостаточности [2,3,5,23,45].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: Индекс MELD (Приложение Г) был разработан для оценки тяжести поражения печени и используется для стратификации пациентов в листе ожидания трансплантации печени. При тяжелом алкогольном гепатите согласно рекомендациям Американской ассоциации по изучению болезней печени глюкокортикостероиды (ГКС) должны назначаться при MELD > 18 баллов. В то же время в других исследованиях рекомендуется использовать порог MELD ≥ 20 баллов [3]. Индекс GAHS (Glasgow Alcoholic Hepatitis Score – оценивает смертность при алкогольном гепатите (Приложение Г), но широкого применения в клинической практике индекс не нашел. Однако его использование позволяет проводить альтернативную оценку прогноза пациента.
- Рекомендовано применение индекса Лилль у всех пациентов с установленным алкогольным гепатитом тяжёлого течения для оценки эффективности терапии ГКС [2,3].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: Индекс Лилль (Приложение Г) предложен французскими гепатологами из города Лилль, служит для оценки ответа на терапию ГКС через 7 дней после начала лечения. Если пациент набирает более 0,45 баллов, использование кортикостероидов считается неэффективным, а летальность в течение 6 месяцев составляет 75% [3,47].
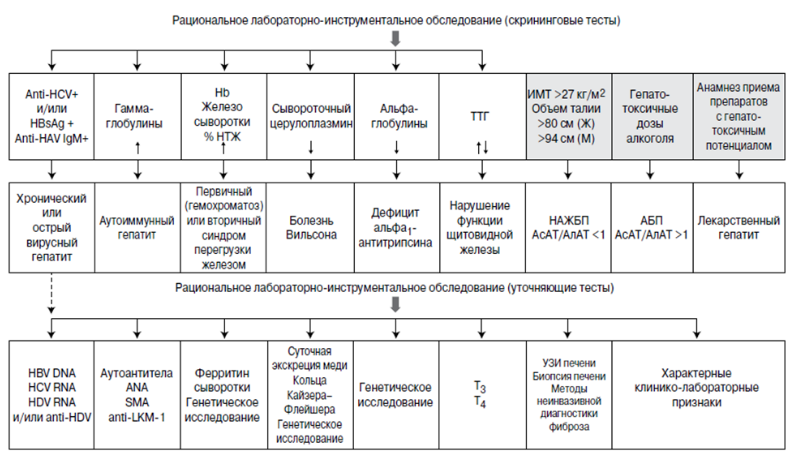

Рисунок 2. Дифференциальный диагноз алкогольной болезни печени
Особую сложность в ведении пациентов с АБП представляет дифференциальный диагноз измененного сознания. Спутанность сознания может возникать не только по причине гипераммониемии (печеночная энцефалопатия), но и в результате нейротоксического действия алкоголя, при развитии энцефалопатии Вернике, корсаковском психозе, синдроме отмены. На стадии ЦП причинами измененного сознания могут быть внепеченочные состояния, которые вызывают или усугубляют симптомы ПЭ – так называемые провоцирующие факторы [90]. К ним относятся хорошо известные факторы: инфекции (пневмония, мочевая инфекция, спонтанный бактериальный перитонит, сепсис, острый гастроэнтерит и другие), желудочнокишечные кровотечения, запор, избыточное расщепление глутамина глутаминазами тонкой кишки, дегидратация, гипонатриемия, гипокалиемия, неконтролируемое использование диуретиков, прием бензодиазепинов, избыточное употребление белка и факторы, роль которых в развитии ПЭ активно обсуждается в последние годы: потеря скелетной мышечной массы (саркопения) и наложение трансъюгулярного внутрипеченочного портосистемного шунта. Мероприятия, направленные на устранение/коррекцию этих факторов, в комбинации с гипоаммониемической терапией сопровождаются клиническим улучшением ПЭ.
- Пациентам с АБП с признаками энцефалопатии с целью дифференциального диагноза, когда генез энцефалопатии вызывает сомнения, рекомендовано проведение пробы с назначением гипоаммониемической терапии [50].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: Нормальный уровень аммиака подвергает сомнению диагноз печеночной энцефалопатии. Однако его измерение не относится к рутинным лабораторным тестам и в большинстве стационаров недоступно. По этой причине при наличии спутанности сознания у пациента с АБП рекомендуется применение препаратов, снижающих уровень аммиака (Орнитин**) [51]. Алгоритм введения орнитина** подробно описан в клинических рекомендациях Минздрава РФ по ведению пациентов с циррозом печени [27]. В случае положительной динамики уровня сознания диагноз рассматривается как печеночная энцефалопатия.
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
1. Общие меры
Достижение и поддержание абстиненции – единственный этиотропный вариант терапии алкогольной болезни печени.
- Рекомендовано пациентам с АБП независимо от ее стадии отказаться от употребления алкоголя для улучшения жизненного прогноза, предотвращения осложнений как со стороны печени, так и со стороны других органов и систем [2,3,5,52,53,78].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарии: Абстиненция (воздержание от алкоголя) – первоочередная и одна из основных терапевтических мер при любой форме и стадии АБП. Продолжение приема алкоголя значительно ухудшает жизненный прогноз пациента: существует риск прогрессирования заболевания печени, развития выраженного фиброза и цирроза, осложнений портальной гипертензии, гепатоцеллюлярной карциномы и рака других локализаций (колоректального, верхних отделов желудочно-кишечного тракта, поджелудочной железы и т. д.) [2]. При полном отказе от приема алкоголя возможны нормализация гистологической картины ткани печени, снижение давления в воротной вене, прекращение прогрессирования цирроза, предотвращение осложнений и улучшение жизненного прогноза пациента. Долгосрочный жизненный прогноз зависит прежде всего от приверженности пациента абстиненции [2]. В этот период основные задачи: сокращение или полное воздержание от употребления алкоголя, предотвращение или снижение частоты срывов абстиненции, лечении алкогольной зависимости. Мета-анализ Yan-Di Xie и соавт., посвященный изучению влияния абстиненции на выживаемость пациентов с АЦП, показал, что статистически значимое увеличение выживаемости появляется через 1,5 года отказа от алкоголя (ОР: 0,51, [95% ДИ 0,33–0,81], p=0,004) и сохраняется в течение 5 лет [54].
- Рекомендовано всем пациентам с АБП для выявления алкогольной зависимости использовать специальные опросники CAGE и AUDIT. [2,3,5]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: При наличии CAGE более 1 и/или AUDIT более 19 баллов показана консультация врача-нарколога.
Достижение и поддержание абстиненции – это комплексная задача, которая стоит перед системой здравоохранения и государством в целом. Таким образом, помимо лечения зависимости, осуществляемой врачами-психиатрами и врачами-наркологами, в задачи здравоохранения должны входить скрининг на злоупотребление алкоголем, информирование о последствиях злоупотребления алкоголем и проведение коротких профилактических консультирований (КПК). Данные меры не только профилактические в аспекте развития алкоголь-индуцированных заболеваний, но и единственный вариант этиотропного лечения для многих из них.
Таким образом, самыми эффективными инструментами в борьбе с пагубными последствиями злоупотребления алкоголем: деятельность врачебного сообщества, в первую очередь врачей первичного звена, которые могут корректировать явную или потенциальную алкогольную зависимость с помощью методики КПК, а также мотиваций пациентов к обращению в наркологическую службу; ограничительные меры государства для уменьшения вреда, оказываемым алкоголем (раздел 5).
- Рекомендовано пациентов с АБП при подозрении на алкогольную зависимость направить к врачу-психиатру-наркологу для совместного ведения и лечения [2,3,5].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
2. Нутритивная поддержка
У подавляющего большинства лиц, злоупотребляющих алкоголем, выявляют алиментарные нарушения. Наиболее часто наблюдаются выраженная белковая недостаточность, дефицит тиамина (витамин В1), фолиевой кислоты, пиридоксина (витамин В6), цинка, витаминов А и D. Тяжесть нутритивных нарушений коррелирует с тяжестью течения заболевания печени и жизненным прогнозом [3]. Пациентам с АБП показано полноценное энтеральное питание.
- Рекомендовано пациентам с АБП назначать калорийный пищевой рацион (35-40 ккал/кг массы тела) с высоким содержанием белка (1,2-1,5 г на 1 кг массы тела в сутки) [2,3,5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Белок в рационе пациента с АБП должен быть представлен преимущественно протеинами растительного происхождения и лактальбумином ввиду их лучшей переносимости. Калорийность пищи обеспечивается адекватным поступлением жиров и углеводов. При невозможности получения необходимого количества питательных веществ из пищи необходимо использовать специальное энтеральное питание.
- Рекомендовано пациентам с АБП и наличием признаков печеночной энцефалопатии ежедневное потребление белка от 1,2 до 1,5 г/кг с целью снижения выраженности гипераммониемии и профилактики ПЭ [2,3,5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Необходимо помнить, что при наличии признаков печеночной энцефалопатии количество белка в рационе следует ограничивать только в индивидуальных случаях белковой интолерантности. Для предотвращения процессов катаболизма количество поступающего белка должно быть не менее 60 г/сут (на 2-3 стадиях ПЭ), в основном за счет белков растительного и животного происхождения. После ликвидации признаков ПЭ суточное количество белка должно быть увеличено до 80-100 г/сут (до 1,5 г/кг). Необходимо учитывать, что у каждого больного АЦП свой порог переносимости пищевого белка, и при белковой интолерантности его дефицит нужно восполнять парентеральными инфузиями.
- Рекомендовано пациентам с АБП и печеночной энцефалопатией ежедневное потребление пищи калорийностью 35-40 ккал/кг идеальной массы тела (около 1800-2500 ккал/сут) для обеспечения достаточной энергетической ценности пищи [2,3,5,27].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Углеводы способствуют уменьшению концентрации аммиака и триптофана в плазме, однако следует помнить, что больным циррозом свойственно развитие нарушения толерантности к глюкозе, что иногда требует назначения инсулина.
Кроме того, метаболизм углеводов требует повышенного расхода тиамина, что может приводить к возникновению его острого дефицита и провокации энцефалопатии Вернике, и поэтому любое введение углеводов требует превентивного назначения тиамина.
Применение фруктозы, сорбитола и ксилитола нецелесообразно вследствие повышенного риска лактоацидоза. Учитывая способность пищевых волокон стимулировать рост бифидо- и лактобактерий, снижать проницаемость кишечной стенки, адсорбировать токсические субстанции, возможно их использование для уменьшения степени бактериальной транслокации у больных АЦП, осложненным асцитом и, соответственно, профилактики спонтанного бактериального перитонита. Пища больного АБП должна также содержать адекватные количества витаминов и микроэлементов. При нарушении всасывания витаминов показано их парентеральное введение.
- Пациентам с АБП и энцефалопатией Вернике (либо подозрением на ее развитие) рекомендовано незамедлительно назначать терапию #тиамином** [2,5].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: Пациентам с острой алкогольной энцефалопатией Вернике проводится терапия по следующей схеме: #тиамин** в дозе 500 мг 3 раза в сутки внутривенно капельно в течение 2-3 дней, далее – по 250 мг/сут внутривенно капельно столь длительно, сколь это необходимо в зависимости от динамики клинических симптомов в каждом конкретном случае, затем – 50-100 мг #тиамина** внутрь длительно [2].
#Тиамин**, наряду с предотвращением и устранением симптомов энцефалопатии Вернике, обладает терапевтическим эффектом при алкогольной полинейропатии, развитие которого также связывают с нехваткой этого витамина.
- По показаниям пациентам с дефицитом питания и АБП может быть рекомендована дополнительная терапия с коррекцией электролитных нарушений: введение препаратов калия, магния; а также введение по показаниям (при развитии авитаминоза): пиридоксина** (витамин В6), цианокобаламина** (витамин В12), никотиновой кислоты (витамин В3 или РР), аскорбиновой кислоты** (витамин С) и фолиевой кислоты**. Возможно назначение поливитаминных смесей внутрь [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
3. Медикаментозная терапия
- При отсутствии активной инфекции рекомендовано пациентам с алкогольным гепатитом тяжелого ечения (индекс Маддрея ≥ 32, MELD ≥ 20) начинать терапию с ГКС (преднизолон** 40 мг/сут или #метилпреднизолон** 32 мг/сут) для снижения краткосрочной смертности. Однако следует помнить, что ГКС не влияют убедительно на долгосрочную выживаемость [2,3,55,56].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: Преднизолон** назначают внутрь в дозе 40 мг/сут на 28 дней, #метилпреднизолон** – в дозе 32 мг. Оценку эффективности терапии проводят на 7-й день от ее начала с помощью индекса Лилль (Lille model – Приложение Г). Если индекс Лилль < 0,45, то лечение преднизолоном** в указанной дозе продолжают в течение 28 дней с последующей полной отменой препарата. Преднизолон отменяют по 1 таблетке 1 раз в 3 дня.
Согласно опубликованным в 2015 г. результатам исследования, проведенного M.R. Thursz и соавт. [23], преднизолон** в указанной дозе приводит к недостоверному уменьшению краткосрочной смертности (в течение 28 дней) и не оказывает влияния на исход заболевания через 90 дней или 1 год после его манифестации. По данным этого же исследования, в группе пациентов, получавших лечение преднизолоном**, в сравнении с группой плацебо достоверно чаще выявляли тяжелые инфекции. До начала лечения преднизолоном пациенты должны быть обследованы на наличие инфекций и желудочно-кишечных кровотечений. В случае выявления указанных осложнений целесообразно их купировать до назначения терапии преднизолоном. Эффективность #метилпреднизолона** 32 мг/сут сопоставима с преднизолоном 40 мг/сут [3].
Недавнее когортное исследование, включающее 3380 пациентов, определило подходящее значения шкалы MELD для назначения ГКС. Применение ГКС достоверно увеличивает 30-дневную выживаемость среди пациентов со шкалой MELD > 20, с максимальной эффективностью (выживаемость > 20%) при шкале MELD в диапазоне от 25 до 39 [57].
- Пациентам с АлГ тяжелого течения, не ответившим на лечение ГКС на 7 день (индекс Лилль ≥ 0,45), рекомендовано прекратить терапию преднизолоном** ввиду ее неэффективности [2,3].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
- С целью повышения эффективности ГКС, а также с целью снижения частоты гепаторенального синдрома пациентам с критериями тяжелого алкогольного гепатита, рекомендовано комбинировать терапию преднизолоном** в дозе 40 мг/сут с #адеметионином** (800 мг/сут внутривенно) [18-21, 58].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарии: При лечении 40 пациентов с алкогольным гепатитом тяжелого течения данная схема лечения (преднизолон** + #адеметионин**) не продемонстрировала различий в сравнении с эффективностью стандартной терапии преднизолоном в дозе 40 мг/сут. Достоверных различий в показателе краткосрочной выживаемости (28 дней) в обеих группах не выявлено (р=0,151). Тем не менее ответ на терапию у пациентов, получавших комбинированную терапию преднизолоном и #адеметионином**, согласно индексу Лилль, был достоверно лучше (р=0,044), а частота развития гепаторенального синдрома – достоверно ниже (р=0,035) [58].
- Рекомендовано пациентам с АБП на стадии цирроза класса А и В по Чайлд–Пью назначать адеметионин** с целью улучшения клинико-биохимических показателей крови и снижения летальности [20,59].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарии: Рандомизированное контролированное исследование, проведенное группой J. Mato [59], продемонстрировало, что применение адеметионина** при АЦП классов А и В по Чайлд–Пью в дозе 1200 мг/сут внутрь в течение 2 лет обусловливает достоверно более низкую летальность или потребность в трансплантации печени в сравнении с этими показателями в группе плацебо (12 и 29% соответственно). В ходе опытов in vitro и in vivo показано, что истощение запасов глутатиона – основного антиоксиданта печени, приводило к повреждению и некрозу гепатоцитов. В связи с этим, использование антиоксидантов, а также препаратов, восстанавливающих запасы глутатиона, представляется перспективным направлением лечения тяжелого алкогольного гепатита. Основываясь на полученных данных, можно предположить, что благоприятное влияние адеметионина** на течение АЦП обусловлено его мембранопротективным и антиоксидантным действием, а также подавлением продукции провоспалительных цитокинов (ФНОα) [17].
- Рекомендовано пациентам с АБП, в том числе на стадии цирроза, в случае развития ПЭ, а также для ее профилактики и коррекции гипераммониемии включать в комплексную терапию #Орнитин** [60-63].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарии: Аммиак играет центральную роль в развитии ПЭ. При этом повышение уровня аммиака коррелирует с тяжестью ПЭ. Таким образом, патогенетически обоснованно в терапии ПЭ включать препараты для коррекции гипераммониемии. L-орнитин-L-аспартат, входящие в состав препарата #Орнитина**, играют основную роль в превращении аммиака в мочевину. Они включаются в этот цикл в качестве субстратов и активируют цикл синтеза мочевины, ускоряя обезвреживание аммиака. Применение препарата #Орнитина** у пациентов с циррозом печени, в том числе в исходе АБП, связано со снижением риска прогрессирования минимальной ПЭ. Также отмечена эффективность #Орнитина** в профилактике развития ПЭ [60]. Согласно данным мета – анализа, применение данного препарата приводило к снижению уровня аммиака в крови и улучшало психическое состояния у пациентов с циррозом печени на любой стадии ПЭ [61]. В недавнем исследовании было показано, что комбинация орнитина** с двумя другими противоаммониемическими средствами (рифаксимин и лактулоза**) сопровождалась более значимыми положительными результатами в сравнении с двукомпонентной комбинацией. Такая трехкомпонентная терапия приводила к более выраженному снижению уровня аммиака в крови, уменьшению степени тяжести ПЭ и смертности у пациентов, в том числе с АЦП [62].
Рекомендуемая суточная доза #Орнитина** может варьировать в зависимости от тяжести АБП. Пероральная доза: от 9 до 18 г/день в виде гранулята, предварительно растворенного в 200 мл жидкости; внутривенная доза – от 20 до 30 г/день в течение 3-8 дней, предварительно разведенного препарата в 500 мл инфузионного раствора, максимальная скорость инфузии – 5 г/ч [64]. Возможный режим дозирования 5 г 3 раза перорально в день в течение 60 дней не оказывает влияния на когнитивные функции, но статистически предотвращает будущие эпизоды явной печеночной энцефалопатии через 6 месяцев (при ЦП) [64].
- Рекомендовано пациентам с АБП и холестатическим синдромом, в том числе на стадии АЦП, назначать урсодезоксихолевую кислоту** (УДХК) с целью улучшения клинико-биохимических показателей крови и гистологической картины печени [65,66].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
Комментарии: Отдельные исследования продемонстрировали эффективность УДХК** в аспекте улучшения клинико-биохимических показателей крови и гистологической картины печени, что может быть обусловлено не только антихолестатическим действием, но и влиянием на выделение провоспалительных цитокинов.
- Рекомендовано пациентам с АБП (в том числе на стадии АЦП) с признаками внутрипеченочного холестаза включать в комплексную терапию адеметионин с целью снижения биохимических показателей холестаза [67].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: Назначение адеметионина пациентам с АБП и внутрипеченочным холестазом может снизить уровень биохимических маркеров холестаза (ЩФ, ГГТ, билирубина). Терапия может быть пероральной или комбинированной (внутривенной/пероральной). Для расчета в/в дозы адеметионина можно исходить из следующего правила: пациентам с массой тела < 70 кг назначать 500 мг/сут , в случае ≥ 70 кг – 800 мг/сут. Рекомендованная доза пероральной формы адеметионина 10-25 мг/кг массы тела в сутки.
Пациентам с исходно высоким уровнем билирубина первоначально может быть назначен адеметионин внутривенно в течение двух недель (500-800 мг ежедневно), с последующим переходом на пероральную форму адеметионин в дозе 1500 мг ежедневно в течение следующих шести недель. Пациенты с исходно нормальными показателями уровня билирубина в сыворотке крови могут получать сразу пероральную форму адеметионина 1500 мг/сутки в течение восьми недель. Желательно основную дозу препарата назначать в первой половине дня (2 таблетки утром, 1 таблетка вечером) [67].
- Рекомендовано пациентам с АБП (в том числе на стадии АЦП) включать в комплексную терапию препарат инозин + меглюмин + метионин + никотинамид + янтарная кислота с целью снижения активности сывороточных трансаминаз, маркеров холестаза, а также для улучшения белково-синтетической функции печени [68].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: в контрольно-сравнительном рандомизированном исследовании препарат инозин + меглюмин + метионин + никотинамид + янтарная кислота в дозе 400 мл/сут продемонстрировал более выраженное уменьшение холестатического и цитолитического синдромов (p<0,05) по сравнению с Адеметионином в дозе 800 мг/сут для парентерального введения у пациентов с АБП. Установлено улучшение белково-синтетической функции печени (увеличение синтеза альбумина гепатоцитами) в группе Ремаксола (p<0,05). Включение препарата инозин + меглюмин +метионин + никотинамид + янтарная кислота в комплексное лечение пациентов с АБП на цирротической стадии способствовало улучшению компенсаторных возможностей печени и краткосрочного жизненного прогноза: в 2,3 раза уменьшилось количество больных со значением расчетного индекса MELD > 11 в основной группе, по сравнению с 1,4 раза в группе сравнения [68].
Прогноз пациентов с АЦП во многом зависит от наличия осложнений. К наиболее серьезным из них относятся печеночная энцефалопатия, кровотечения из варикозно-расширенных вен пищевода и/или желудка, асцит и спонтанный бактериальный перитонит, гепаторенальный синдром, гипонатриемия разведения. Диагностика и лечение указанных состояний должны проводиться в обязательном соответствии с разработанными алгоритмами. Лечение осложнений ЦП не зависит от этиологии заболеваний, его необходимо проводить согласно современным клиническим рекомендациям Минздрава РФ 2021 г [27].
4. Терапия синдрома отмены алкоголя
Более чем у половины пациентов с расстройством употребления алкоголя развивается состояние отмены алкоголя при прекращении его приема либо значительном уменьшении дозы.
Состояние отмены алкоголя может быть неосложненным и осложненным.
Осложнения отмены алкоголя включают алкогольную эпилепсию (алкогольные судороги) и алкогольный делирий (белую горячку).
Наиболее часто алкогольная эпилепсия и алкогольный делирий развиваются на 2-4 дни прекращения употребления либо резкого снижения дозы алкоголя.
- Рекомендовано совместное наблюдение и ведение пациентов с синдромом отмены алкоголя с врачом-психиатром-наркологом с подбором адекватной терапии для предотвращения прогрессирования или купирования алкогольного абстинетного синдрома и алкогольного психоза [2,3].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
- Рекомендовано пациентам с АБП и синдромом отмены алкоголя в комплексной терапии назначать препараты на основе Инозина + Меглюмина + Метионина + Никотинамида + Янтарной кислоты с целью улучшения эффективности лечения [69].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: янтарная кислота (сукцинат) – субстрат для цикла Кребса, который улучшает энергообмен и функционирование клеток, в том числе гепатоцитов. В клинической практике широко используются инфузии комбинированного лекарственного препарата Инозин + Меглюмин + Метионин + Никотинамид + Янтарная кислота.
5. Трансплантация печени
Трансплантация печени показана пациентам в финальной стадии АБП, а также пациентам с АлГ тяжёлого течения, не поддающихся лечению ГКС [3]. Основным принципом определения показаний для ортотопической трансплантации печени служит прогнозирование того, что выживаемость больного после трансплантации превысит его продолжительность жизни без нее.
- Рекомендовано пациентам с декомпенсированным АЦП, а также пациентам с алкогольным гепатитом тяжёлого течения, не ответивших на терапию ГКС, проведение трансплантации печени с целью повышения выживаемости [79,80,81,82].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: в качестве условия для выполнения трансплантации печени большинством центров рассматривается не менее чем 6-месячная абстиненция, хотя, по последним сведениям, достоверные различия по выживаемости в посттрансплантационном периоде между пациентами, продолжающими и прекратившими прием алкоголя, отсутствуют.
Основные противопоказания для трансплантации печени:
- Внепечёночные злокачественные заболевания
- Метастатические поражения
- Активная ВИЧ инфекция
- Тяжёлые сопутствующие заболевания, не коррегирующиеся трансплантацией
- Активный алкоголизм, наркомания
- Внепеченочный сепсис
- Тяжелые заболевания сердечно-сосудистой системы
- Психологическая и социальная несостоятельность больного
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Медицинская реабилитация больных с АБП зависит от стадии заболевания.
Медицинская реабилитация в основном требуется больным АЦП и АлГ тяжелого течения. На стадии компенсации АЦП реабилитация подразумевает под собой раннее выявление признаков начинающейся декомпенсации цирроза печени, присоединения новых осложнений, определение показателей нутритивной недостаточности.
- Рекомендовано пациентам с АБП проводить восстановительное лечение в амбулаторных условиях и оно должно включать прекращение приема алкоголя, исключение воздействия гепатотропных и гепатотоксичных веществ, исключения приема лекарственных средств без назначения врача, умеренную физическую активность с ограничением выраженных и чрезмерных физических нагрузок, прогулки на свежем воздухе, избегая длительной и чрезмерной инсоляции, энтеральное и парентеральное питание растворами белков при снижении синтетической функции печени, коррекцию билиарной и первичной/вторичной панкреатической недостаточности (по показаниям), ограничение приема натрия с пищей (включая минеральные воды с высоким содержанием натрия) у пациентов с асцитом.
Уровень убедительности рекомендаций С (Уровень достоверности доказательств – 4)
Общие принципы питания больных АБП без ее недостаточности: полноценное, сбалансированное по белкам, жирам и углеводам. Полноценное питание с поступлением в достаточном количестве макро- и микронутриентов, витаминов помогает предотвратить потерю веса и как следствие саркопению, снижает риск развития авитаминозов.
Госпитализация
Организация оказания медицинской помощи
Пациенты с АБП должны находиться под совместным наблюдением врача-гастроэнтеролога/гепатолога, врача-психиатра, врача-психиатра-нарколога.
Показания к госпитализации: желтуха, клинически выраженная энцефалопатия (2 стадии и выше), впервые возникший или медикаментозно неконтролируемый/напряжённый асцит, отёчный синдром, подозрение на кровотечение, появление/усиление астенического синдрома, олигурия/анурия, подозрение на развитие инфекционного осложнения, появление/усиление одышки. Госпитализация при АБП может быть плановой и экстренной, в терапевтический или хирургический блок в зависимости от стадии заболевания, по показаниям – в отделение интенсивной терапии и реанимации.
Показания к выписке пациента: Уменьшение выраженности клинических симптомов, отсутствие необходимости хирургического лечения, необходимости проведения интенсивной терапии, стабилизация функции жизненно важных органов: сердечно-сосудистая (гемодинамика) и дыхательная система, почки, ЦНС.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Основные задачи системы национального здравоохранения – это профилактика злоупотребления алкоголем и лечение развившейся алкогольной зависимости. Для реализации поставленных задач наиболее эффективными мерами служат КПК и комбинация когнитивно-поведенческой терапии с медикаментозным лечением (в случае развития зависимости от алкоголя).
- Рекомендовано для профилактики развития АБП ограничить употребление алкоголя в опасных дозах [1,2,3,23].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: Достижение этой цели требует проведения мероприятий, направленных на уменьшение доступности алкоголя, таких как повышение его стоимости, в том числе путем высокого налогообложения, ограничение или полный запрет демонстрации алкогольных напитков в средствах массовой информации (в том числе и косвенная реклама), ограничение времени продажи алкоголя, возрастные ограничения по приобретению алкогольной продукции, а также просветительская работа среди населения о вреде злоупотребления алкоголем и активное продвижение здорового образа жизни, особенно, среди молодежи. Значительный вклад может внести внедрение методики КПК в практику врача-интерниста, медикаментозная терапия алкогольной зависимости и психосоциальная поддержка.
Достижение абстиненции представляется наиболее эффективным средством профилактики прогрессирования АБП. Наступление алкогольной зависимости у пациента в значительной степени увеличивает возможность отказа от абстиненции и продолжительность приёма алкоголя в опасных для здоровья дозах. В связи с этим, наблюдение пациентов с АБП и алкогольной зависимостью должно осуществляться совместно с врачом-психиатром-наркологом, врачом-психиатром.
- Рекомендовано пациентам с выявленным опасным стилем употребления алкоголя провести КПК для снижения риска развития заболеваний, ассоциированных с его злоупотреблением [2,3,70].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: До возникновения зависимости и ассоциированных с употреблением алкоголя заболеваний существует период опасного употребления алкоголя. Длительность этого периода индивидуальна и может варьировать в зависимости от многих факторов, как модифицируемых (количество и частота употребляемого алкоголя), так и немодифицируемых (гендерные различия, генетический полиморфизм белков, сопутствующие заболевания и пр.). Чаще всего для формирования алкогольной зависимости необходимы годы, для некоторых десятилетия. Эффективное вмешательство на ранних стадиях до развития зависимости от алкоголя позволяет замедлить или предотвратить формирование АБП. Скрининг на опасное употребление алкоголя должен проводиться врачами первичного звена, врачами общей практики и в отделениях неотложной помощи. Для этого врач/медицинский работник должны обладать соответствующими навыками проведения КПК.
- Рекомендовано пациентам с высоким риском злоупотребления алкоголем и развитием АБП, выявленным с помощью скрининга, пройти краткое профилактическое консультирование (мотивированное интервьюирование) с целью профилактики развития заболеваний, ассоциированных с употреблением алкоголя [2,3,70-73].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
- Рекомендовано пациентам с установленным диагнозом АБП пройти краткое профилактическое консультирование для прекращения прогрессирования заболевания печени, предотвращения осложнений и улучшение жизненного прогноза пациента. [2,3,70-73].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарии: Врачам-гастроэнтерологам/гепатологам, врачам-терапевтам и другим специалистам, не имеющим специального сертификата для оказания наркологической/психиатрической помощи, рекомендуется в своей клинической практике использовать методику кратких профилактических консультирований (КПК) – «brief interventions». Суть КПК заключается в мотивации пациента к изменению поведения, связанного с употреблением алкоголя, например, уменьшению частоты употребления и объема спиртных напитков, более безопасному поведению, обращению за специализированным наркологическим лечением и т.д.
Ключевым принципом КПК служит пациенто-ориентированное общение. Задача специалиста помочь пациенту найти собственные доводы против употребления алкоголя и усилить его уверенность в собственных силах и возможности полного отказа от алкоголя.
КПК включает три ключевых положения:
1) это особый вид беседы об изменениях (консультирование, лечение, способ коммуникации);
2) беседа всегда совместная и личностно-ориентированная, предполагающая партнерство, а не взаимоотношения эксперта и получателя;
3) она побуждает к воспоминаниям, ее цель – вызвать у пациента желание изменить обстоятельства, себя, свою жизнь и т. д.
Овладеть техникой КПК может каждый желающий работник здравоохранения, для этого не нужно какой-либо особой специализации.
Эффективность КПК в снижении употребления алкоголя была доказана в Кохрановском мета-анализе (2018 г), который включил 69 исследований. Мета-анализ показал, что пациенты, которым проводилась КПК через 12 месяцев употребляли на 20 г/нед алкоголя меньше, чем пациенты, которым не проводилось КПК или чем те участники, с которым проводились более короткие вмешательства (быстрый совет продолжительность менее 5 минут) или не проводилось вмешательства совсем [74]. Было отмечено снижение частоты и интенсивности выпивки в течение недели. При этом продолжительные психологические консультации (более 5 встреч общей продолжительностью более 60 минут) не приводили к усилению эффективности [74]. Несмотря на то, что клинические исследования, включенные в данный мета-анализ, были основаны на выборке больных без АБП, результаты мета-анализа наиболее полно отражают эффект мотивационного интервью на популяционном уровне.
По данным систематического обзора Khan и соавт., показано, что только комбинация мотивирующей и поведенческой терапии с поддерживающей терапией соматического заболевания в течение 2-х лет, приводит к статистически значимому повышению частоты достижения и поддержания абстиненции (74% в группе комбинированной терапии против 48% в группе контроля, р=0,02) [75]. Абстиненция – ведущий фактор улучшения функции печени у пациентов в АБП в долгосрочном периоде.
Кроме снижения доли пациентов, злоупотребляющих алкоголем и зависимых от алкоголя, важным показателем эффективности противоалкогольных мер служит снижение количества лет нетрудоспособности, приобретенных по причине злоупотребления алкоголем (disability-adjusted life year – DALY). Наибольшее положительное влияние на данный показатель оказывало проведение КПК. Введение процедуры тотального скрининга позволит выделить группу часто госпитализируемых пациентов и оказать им квалифицированную медицинскую помощь.
- Рекомендовано пациентам с АБП проводить диспансерное наблюдение для динамического обследования и раннего выявления осложнений [76].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: режим диспансерного наблюдения определяется лечащим врачом индивидуально в зависимости от течения заболевания и наличия осложнений. Впервые выявленные пациенты в первый год наблюдаются каждые 3 месяца, во 2-й год – каждые 6 месяцев, в последующие годы в случае стабилизации процесса – 1 раз в год. Диспансерное наблюдение включает проведение лабораторного обследования (общий анализ крови, биохимический анализ крови, коагулограмма - при наличии показаний). Вопрос о назначении УЗИ органов брюшной полости и других визуализирующих методах исследования, а также ЭГДС решается индивидуально в каждом случае. Диспансерное наблюдение не исключает активных визитов пациента при ухудшении состояния или развитии нежелательных явлений при проведении лечения [76].
Информация
Источники и литература
-
Клинические рекомендации Научного общества гастроэнтерологов России
- Клинические рекомендации Научного общества гастроэнтерологов России - 1. http://www.euro.who.int/ru/health-topics/disease-prevention/alcohol-use/publications/2017/who-alcohol-brief-intervention-training-manual-for-primary-care-2017 2. В.Т. Ивашкин, М.В. Маевская, Ч.С. Павлов, Ю.П. Сиволап, В.Д. Луньков, М.С. Жаркова, Р.В. Масленников. Клинические рекомендации Российского общества по изучению печени по ведению взрослых пациентов с алкогольной болезнью печени. Рос журн гастроэнтерол гепатол колопроктол 2017;27(6):20-40 3. EASL Clinical Practical Guidelines: Management of Alcoholic Liver Disease // J. Hepatol. 2018; 69:154-181. 4. Kim D.K., Kim Y.H., Jang H.H. Estrogen-related receptor γ controls hepatic CB1 receptor-mediated CYP2E1 expression and oxidative liver injury by alcohol // Gut. 2013. No62(7). Р. 1044-1054. doi:10.1136/gutjnl-2012-303347. 5. Болезни печени и желчевыводящих путей: Руководство для врачей / Под ред. В.Т. Ивашкина – 2-е изд. ООО «Издат. Дом «М-Вести», 2005. – 536 с. 6. Алкогольно-вирусные заболевания печени / Ивашкин В.Т., Маевская М.В. – М.: Литтерра, 2007 – 160 с.]. Болезни печени и желчевыводящих путей: Руководство для врачей / Под ред. В.Т. Ивашкина – 2-е изд. ООО «Издат. Дом «М-Вести», 2005. – 536 с. 7. Bellentani S., Saccoccio G., Costa G., Tiribelli C., Manenti F., Sodde M., et al. Drinking habits as cofactors of risk for alcohol induced liver damage. The Dionysos Study Group. // Gut. – 1997. – Vol.41. - No6. – P. 845–850. 8. Hart C.L., Morrison D.S., Batty G.D., Mitchell R.J., Davey Smith G. Effect of body mass index and alcohol consumption on liver disease: analysis of data from two prospective cohort studies. // BMJ. – 2010. – Vol.340. – P. 1240. 9. Kennedy O.J., Roderick P., Buchanan R., Fallowfield J.A., Hayes P.C., Parkes J. Systematic review with meta-analysis: coffee consumption and the risk of cirrhosis. // Alimentary Pharmacology & Therapeutics. – 2016. – Vol.43. – P.562–574. 10. Chan L.N., Anderson G.D. Pharmacokinetic and pharmacodynamic drug interactions with ethanol (alcohol)//Clin Pharmacokinet. 2014. N 53(12). P. 1115 – 36. doi: 10.1007/s40262-014-0190-x. 11. Sandahl T.D., Jepsen P., Thomsen K.L., Vilstrup H. Incidence and mortality of alcoholic hepatitis in Denmark 1999–2008: a nationwide population based cohort study. // Journal of Hepatology. – 2011. – Vol.54. – P. 760–764 12. Rehm J., Gmel Sr G.E., Gmel G., Hasan O.S.M., Imtiaz S., Popova S., et al. The relationship between different dimensions of alcohol use and the burden of disease-an update. // Addiction. – 2017. – Vol.112. – P. 968–1001. 13. Askgaard G., Gronbaek M., Kjaer M.S., Tjonneland A., Tolstrup J.S. Alcohol drinking pattern and risk of alcoholic liver cirrhosis: a prospective cohortstudy. // Journal of Hepatology. - 2015. – Vol.62. - No5. – P.1061–1067. 14. Aberg F., Helenius-Hietala J., Puukka P., Jula A. Binge drinking and the risk of liver events: A population-based cohort study. // Liver International. – 2017. - No37. – P. 1373–1381. 15. Askgaard G., Leon D.A., Kjaer M.S., Deleuran T., Gerds T.A., Tolstrup J.S. Risk for alcoholic liver cirrhosis after an initial hospital contact with alcohol problems: A nationwide prospective cohort study. // Hepatology. – 2017. – Vol. 65. – No3. - P. 929–937. 16. Dam M.K., Flensborg-Madsen T., Eliasen M., Becker U., Tolstrup J.S. Smoking and risk of liver cirrhosis: a population-based cohort study. // Scandinavian Journal of Gastroenterology. – 2013. – Vol.48. – No5. - P. 585–591. 17. Tilg H. Cytokines in alcoholic and nonalcoholic steatohepatitis / Tilg H, Diehl AM. // N Engl J Med. – 2000. – Vol. 343. – p. 1467–1476. 18. McClain C, Hill D, Song Z, et al. S-adenosylmethionine, cytokines, and alcoholic liver disease. Alcohol 2002; 27:185-92. 19. Lu SC, Mato JM. S-adenosylmethionine in liver health, injury, and cancer. Physiol Rev 2012; 92:1515-42. 20. Purohit V, Abdelmalek M, Barve S, et al. Role of S-adenosylmethionine, folate, and betaine in the treatment of alcoholic liver disease: Summary of a symposium. Am J Clin Nutr 2007; 86:14-24. 21. Colell A, Garcia-Ruiz C, Miranda M, et al. Selective glutathione depletion of mitochondria by ethanol sensitizes hepatocytes to tumor necrosis factor. Gastroenterology 1998; 115:1541-51. 22. WHO Global status report on noncommunicable diseases 2014. // WHO Library Cataloguing-in-Publication Data. - 2014. 23. Thursz, Mark et al., EASL Clinical Practice Guidelines: Management of alcohol-related liver disease. // Journal of Hepatology. – 2018 – Vol.69., No1., P.154 – 181. 24. Маевская М.В., Бакулин И.Г., Чирков А.А., Люсина Е.О, Луньков В.Д. Злоупотребление алкоголем среди пациентов гастроэнтерологического профиля. // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. – 2016 – Т.26 - No4. – С. 24-35. 25. https://mednet.ru/images/news/docs/Потребление и продажи алкоголя в 2018-2020 гг.pdf 26. Маевская М.В. Алкогольная болезнь печени / М. В. Маевская // Клинические перспективы в гастроэнтерологии, гепатологии. – 2001. –№1. – с. 4-8. 27. Ивашкин В.Т., Маевская М.В., Жаркова М.С., Жигалова С.Б., Киценко Е.А., Манукьян Г.В., Трухманов А.С., Маев И.В., Тихонов И.Н., Деева Т.А. Клинические рекомендации Российского общества по изучению печени и Российской гастроэнтерологической ассоциации по диагностике и лечению фиброза и цирроза печени и их осложнений. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2021;31(6):56-102. 28. Jepsen P, Ott P, Andersen PK, et al. Clinical course of alcoholic liver cirrhosis: A Danish population-based cohort study. Hepatology 2010; 51:1675-82. 29. Bell H, Jahnsen J, Kittang E, et al. Long-term prognosis of patients with alcoholic liver cirrhosis: A 15-year follow-up study of 100 Norwegian patients admitted to one unit. Scand J Gastroenterol 2004; 39:858-63. 30. Saunders J.B., Aasland O.G., Babor T.F., de la Fuente J.R., Grant M. Development of the alcohol use disorders identification test (AUDIT): WHO collaborative project on early detection of persons with harmful alcohol consumption–II. // Addiction. – 1993. – Vol.88. – P. 791–804. 31. Babor T.F., Higgins-Biddle J.C., Saunders J.B., Monterio M.G. The Alcohol Use Disorders Identification Test, Guidelines for Use in Primary Care, second edition. // World Health Organization Department of Mental Health and Substance Dependence. 2nd edition. Geneva – 2001. 32. Spithoff S., Kahan M. Primary care management of alcohol use disorder and at-risk drinking: Part 1: screening and assessment. // Canadian Family Physician. – 2015. – Vol.61. - No6. – P. 509-514. 33. Adams W.L., Barry K.L., Fleming M.F. Screening for problem drinking in older primary care patients. // JAMA. – 1996. - No276. – P. 1964–1967. 34. Bradley K.A., Bush K.R., Epler A.J., et al. Two brief alcohol- creening tests from the Alcohol Use Disorders Identification Test (AUDIT): Validation in a female veterans affairs patient population. // Archive of Internal Medicine. – 2003. - Vol.163. - No6., P. 821-829. 35. Cara Torruellas, Samuel W. French, Valentina Medici. Diagnosis of alcoholic liver disease//World J Gastroenterol. 2014. N 20(33). P. 11684-11699. doi: 10.3748/wjg.v20.i33.11684. 36. Lee H. A. et al. Direct bilirubin is more valuable than total bilirubin for predicting prognosis in patients with liver cirrhosis //Gut and Liver. – 2021. – Т. 15. – №. 4. – С. 599. 37. Кишкун А.А. Лабораторные маркеры алкоголизма (обзор литературы). Клин лабор диагн 2008;11:3-8 [Kishkun A.A. Laboratory markers of addiction to alcohol (review of literature). Klin labor diagn 2008; 11:3-8. 38. Mammen E. F. Coagulation abnormalities in liver disease //Hematology/oncology clinics of North America. – 1992. – Т. 6. – №. 6. – С. 1247-1257. 39. Violi F. et al. Association between low-grade disseminated intravascular coagulation and endotoxemia in patients with liver cirrhosis //Gastroenterology. – 1995. – Т. 109. – №. 2. – С. 531-539. 40. Khwaja A. KDIGO clinical practice guidelines for acute kidney injury. NephronClinPract 2012;120:c179–c184. 41. Willmann. Ultrasound Elastography: Review of Techniques and Clinical Applications//Theranostics. 2017. N 7(5). P. 1303-1329. doi: 10.7150/thno.18650. 42. Nguyen-Khac E, Thiele M, Voican C, Nahon P, Moreno C, Boursier J, Mueller S, de Ledinghen V,Stärkel P, Gyune Kim S, Fernandez M, Madsen B, Naveau S, Krag A, Perlemuter G, Ziol M, Chatelain D, Diouf M. Non-invasive diagnosis of liver fibrosis in patients with alcohol-related liver disease by transient elastography: an individual patient data meta-analysis. Lancet Gastroenterol Hepatol. 2018 Sep; 3(9): 614-625. doi: 10.1016/S2468-1253(18)30124-9. 43. Grace Lai-Hung Wong. Update of liver fibrosis and steatosis with transient elastography (Fibroscan)//Gastroenterol Rep (Oxf). 2013. N 1(1). P. 19-26. doi: 10.1093/gastro/got007. 44. EASL-ALEH Clinical Practice Guidelines: Non-invasive tests for evaluation of liver disease severity and prognosis. Journal of Hepatology 2015 vol. 63 j 237–264. 45. EASL CPG: Non-invasive tests for evaluation of liver disease severity and prognosis. J Hepatol 2021; 73(3): 659-689. 46. Maddrey W.C., Boitnott J.K., Bedine M.S., et al. Corticosteroid therapy of alcoholic hepatitis. // Gastroenterology. – 1978. – Vol.75. – No2. - P. 193–199.]. Dunn W., Jamil L.H., Brown L.S., et al. MELD accurately predicts mortality in patients with alcoholic hepatitis. // Hepatology. – 2005. – Vol.41. – No2. - P. 353. 47. Mathurin P., Abdelnour M., Ramond M.J., Carbonell N., Fartoux L., Serfaty L., etal. Early change in bilirubin levels is an important prognostic factor in severe alcoholic hepatitis treated with prednisolone. // Hepatology. – 2003. – Vol.38. – P.1363–1369. 48. Gong A., Leitold S., Uhanova J. et al. Predicting Pre-transplant Abstinence in Patients with Alcohol-Induced Liver Disease // Clin. Invest. Med. 2018. No41(2). Р. E37-E42. doi: 10.25011/cim.v41i2.29913. 49. EASL Clinical Practical Guidelines: Management of Alcoholic Liver Disease. J Hepatol 2012; 57:399-420. 50. EASL Clinical Practice Guidelines on the management of hepatic encephalopathy, J of Hepatology, 2022. 51. Amodio P. Hepatic encephalopathy: diagnosis and management. Liver Int 2018;38:966–975. 52. Alvarez M.A., Cirera I., Solà R., et al. Long-term clinical course of decompensated alcoholic cirrhosis: a prospective study of 165 patients. // Journal of Clinical Gastroenterology. – 2011. – Vol.45. - No10. – P. 906. 53. Borowsky S.A., Strome S., Lott E. Continued heavy drinking and survival in alcoholic cirrhotics. // Gastroenterology. – 1981. – Vol.80. – P.1405. 54. Xie Y., Feng B., Gao Y. and Wei L. Alcohol abstinence and survival. // Hepatology Research. - 2014. – Vol.44. – P. 436-449. 55. Chrostek L, Panasiuk A. Liver fibrosis markers in alcoholic liver disease. World J Gastroenterol. 2014; 20(25): 8018 – 23. doi: 10.3748/wjg.v20.i25.8018. 56. Mathurin P, O’Grady J, Carithers RL, Phillips M, Louvet A, Mendenhall CL, et al. Corticosteroids improve short-term survival in patients with severe alcoholic hepatitis: meta-analysis of individual patient data. Gut 2011;60:255–260. doi: 10.1136/gut.2010.224097. 57. Arab JP, Díaz LA, Baeza N, et al. Identification of optimal therapeutic window for steroid use in severe alcohol-associated hepatitis: a worldwide study. J Hepatol 2021;75:1026-33. 58. Tkachenko P., Maevskaya M., Pavlov A. Prednisolone plus S-adenosil-L-methionine in severe alcoholic hepatitis. Hepatol Int 2016 June; DOI 10.1007/s12072-016-9751-4. 59. Mato J.M., Camara J., Fernandez de Paz J. et al. S-adenosylmethionine in alcoholic liver cirrhosis: a randomized, placebo-controlled, double-blind, multicenter clinical trial. J Hepatol 1999; 30:1081-9. 60. Butterworth R. F. Beneficial effects of L-ornithine L-aspartate for prevention of overt hepatic encephalopathy in patients with cirrhosis: a systematic review with meta-analysis //Metabolic brain disease. – 2020. – Т. 35. – №. 1. – С. 75-81. 61. Butterworth R. F. et al. Efficacy of l-ornithine l-aspartate for the treatment of hepatic encephalopathy and hyperammonemia in cirrhosis: systematic review and meta-analysis of randomized controlled trials //Journal of clinical and experimental hepatology. – 2018. – Т. 8. – №. 3. – С. 301-313. 62. Jain A. et al. L‐ornithine L‐aspartate in acute treatment of severe hepatic encephalopathy: A double‐blind randomized controlled trial //Hepatology. – 2022. – Т. 75. – №. 5. – С. 1194-1203. 63. Уваров И. А. РОЛЬ ПРЕПАРАТА ГЕПА-МЕРЦ (L-ОРНИТИНА-L-АСПАРТАТА) В КОМПЛЕКСНОМ ЛЕЧЕНИИ АЛКОГОЛЬНОГО ДЕЛИРИЯ //Вопросы наркологии. – 2009. – №. 3. – С. 35-43. 64. Mahpour NY, Pioppo-Phelan L, Reja M, Tawadros A, Rustgi VK. Pharmacologic Management of Hepatic Encephalopathy. Clin Liver Dis. 2020 May; 24(2): 231-242. doi: 10.1016/j.cld.2020.01.005. 65. Минушкин О.Н., Фролова А.А., Шиндина Т.С. и др. Урсодезоксихолевая кислота в гастроэнтерологической практике. РМЖ. Медицинское обозрение. 2018;26(1(I)):18-22. 66. Gilles Pelletier, Dominique Roulot, Thierry Davion et al. A Randomized Controlled Trial of Ursodeoxycholic Acid in Patients With Alcohol-Induced Cirrhosis and Jaundice. HEPATOLOGY, 2003, 887-892. 67. Ivashkin, Vladimir T., et al. "Open-label Study of Ademetionine for the Treatment of Intrahepatic Cholestasis Associated With Alcoholic Liver Disease." Minerva Gastroenterologica E Dietologica, vol. 64, no. 3, 2018, pp. 208-219. 68. В.В. Стельмах, И.Г. Бакулин, А.Л. Коваленко, В.К. Козлов. Эффективность Ремаксола у пациентов с алкогольной болезнью печени. Экспериментальная и клиническая фармакология. 2022 6(85): 25-31. doi: 10.52420/2071-5943-2022-85-6-25-31. 69. Винникова М.А., Уткин С.И., Ненастьева А.Ю., Захаров М.В. Эффективность включения ремаксола в терапию алкогольного абстинентного синдрома. Журнал неврологии и психиатрии им. С.С. Корсакова. 2016;116(1):40 46. 70. Луньков В.Д. диссертация на соискание к.м.н. Оптимизация прогноза пациента с алкогольной болезнью печени. Москва, 2021. https://www.sechenov.ru/upload/iblock/31c/Dissertatsiya-Lunkova-V.D..pdf?ysclid=ldoatrm1jl41789332. 71. Sassi F., et al., Tackling Harmful Alcohol Use: Economics and Public Health Policy. // OECD report. -2015. 72. Jonas DE, Garbutt JC, Amick HR, Brown JM, Brownley KA, Council CL, et al. Behavioral counseling after screening for alcohol misuse in primary care: a systematic review and meta-analysis for the U.S. Preventive Services Task Force. Ann Intern Med 2012;157:645–654. 73. O’Donnell A, Anderson P, Newbury-Birch D, Schulte B, Schmidt C, Reimer J, et al. The impact of brief alcohol interventions in primary healthcare: a systematic review of reviews. Alcohol Alcohol 2014;49:66–78 http://www.talkingalcohol.com/files/pdfs/WHO_audit.pdf. 74. Kaner E.F.S., Beyer F.R., Muirhead C., Campbell F., Pienaar E.D., Bertholet N.,Daeppen J.B., Saunders J.B., Burnand B. Effectiveness of brief alcohol interventions in primary care populations. // Cochrane Database of Systematic Reviews. – 2018. – Vol.2. - NoCD004148. 75. Khan A., Tansel A., White D.L., et al. Efficacy of psychosocial interventions in inducing and maintaining alcohol abstinence in patients with chronic liver disease – a systematic review. //Clinical Gastroenterology and Hepatology. – 2016. – Vol.14. – P. 4
Информация
Список сокращений
MCV – Средний объем эритроцита
SAM – S-аденозилметионин
TLR4 – Toll-подобный рецептор 4
АБП – Алкогольная болезнь печени
АЛД – Алкогольдегидрогеназа
АлГ – Алкогольный гепатит
АлДГ – Альдегиддегидрогеназа
АЛТ – Аланинаминотрансфераза
АСТ – Аспартатаминотрансфераза
АлС – Алкогольный стеатоз
АЦП – Алкогольный цирроз печени
ВРВП – Варикозно-расширенные вены пищевода
ГГТ – Гамма-глутамилтранспептидаза
ГКС – Глюкокортикостероиды
ЖКТ – Желудочно-кишечный тракт
ИЛ – Интерлейкин
ИМТ – Индекс массы тела
КПК – Короткие профилактические консультирования
КоА – Коэнзим А
ЛДГ – Лактатдегидрогеназа
ЛПС – Липополисахарид
МЭОС – Микросомальная этанолокислительная система
НАДН – Никотинамидадениндинуклеотид, восстановленная форма
ПВ – Протромбиновое время
ПОЛ – Перекисное окисление липидов
ПЭ – печеночная энцефалопатия
РКИ – Рандомизированное клиническое исследование
ФНОα – Фактор некроза опухолей альфа
ЦП – Цирроз печени
ЩФ – Щелочная фосфатаза
Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Критерии оценки качества медицинской помощи
|
№
|
Критерии качества
|
Оценка выполнения
|
|---|---|---|
|
1.
|
Выполнен общий (клинический) анализ крови
|
Да/нет
|
|
2.
|
Выполнен анализ крови биохимический общетерапевтический (общий белок, альбумин, билирубин общий, билирубин связанный (конъюгированный), креатинин, аланинаминотрансфераза, аспартатаминотрансфераза, щелочная фосфатаза, гаммаглутамилтрансфераза, глюкоза)
|
Да/нет
|
|
3.
|
Выполнена коагулограмма (ориентировочное исследование системы гемостаза) (МНО, протромбиновый индекс %, фибриноген, протромбин, протромбиновое (тромбопластиновое) время) пациентам с АБП при подозрении на АЦП и при алкогольном гепатите тяжелого течения
|
Да/нет
|
|
4.
|
Выполнено ультразвуковое исследование органов брюшной полости (комплексное)
|
Да/нет
|
|
5.
|
Выполнена эзофагогастродуоденоскопия
|
Да/нет
|
|
6.
|
Выполнена чрескожная биопсия печени или биопсия печени под контролем ультразвукового исследования (при подозрении на сопутствующую патологию печени и очаговые изменения печени при отсутствии медицинских противопоказаний)
|
Да/нет
|
|
7.
|
Выполнено назначение диетического питания при заболеваниях печени и желчевыводящих путей (при выявленном белковом дефиците содержание белка в дозе не менее 1-1,5 грамма на килограмм идеальной массы тела)
|
Да/нет
|
|
8.
|
Проведено лечение кортикостероидами системного действия (при тяжёлом алкогольном гепатите в острый период коротким курсом и при отсутствии медицинских противопоказаний)
|
Да/нет
|
|
9.
|
Проведено лечение орнитином (при печеночной энцефалопатии и при выраженном эндотоксикозе, при отсутствии медицинских противопоказаний)
|
Да/нет
|
|
10.
|
Проведено лечение адеметионином или инозин+Меглюмин+Метионин+Никотинамид+Янтарная кислота и/или урсодезоксихолевой кислотой (при отсутствии медицинских противопоказаний)
|
Да/нет
|
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Ивашкин Владимир Трофимович – доктор медицинских наук, профессор, академик РАН, лауреат премии Правительства РФ в области науки и техники в 2007 г., в области образования – в 2013 г., Заслуженный врач РФ, Заслуженный деятель науки РФ, Президент Российской гастроэнтерологической ассоциации и Российского общества по изучению печени. Конфликт интересов отсутствует.
Лазебник Леонид Борисович – вице-президент РНМОТ, Президент НОГР, член президиума Общества врачей России, член президиума Национальной медицинской палаты, д.м.н., профессор, профессор кафедры поликлинической терапии ФГБОУ ВО «Московский государственный медицинский стоматологический университет им. А.И. Евдокимова» Минздрава России. Конфликт интересов отсутствует.
Голованова Елена Владимировна – Профессор кафедры поликлинической терапии лечебного факультета ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России, д.м.н. Конфликт интересов отсутствует.
Деева Татьяна Андреевна – кандидат медицинских наук, член Российского общества по изучению печени. Конфликт интересов отсутствует.
Драпкина Оксана Михайловна – доктор медицинских наук, академик РАН, Президент Российского общества профилактики неинфекционных заболеваний. Конфликт интересов отсутствует.
Еремина Елена Юрьевна − Зав. кафедрой пропедевтики внутренних болезней Национального исследовательского мордовского государственного университета имени Н.П. Огарева, д.м.н., профессор, главный внештатный гастроэнтеролог Минздрава Республики Мордовия. Конфликт интересов отсутствует.
Жаркова Мария Сергеевна – кандидат медицинских наук, лауреат премии Правительства РФ в области науки и техники в 2017 г., член Российского общества по изучению печени. Конфликт интересов отсутствует.
Кривошеев Александр Борисович − Профессор кафедры факультетской терапии ГОУ ВПО «Новосибирский государственный медицинский университет Росздрава», д.м.н. Конфликт интересов отсутствует.
Маев Игорь Вениаминович – доктор медицинских наук, академик РАН. Конфликт интересов отсутствует.
Маевская Марина Викторовна – доктор медицинских наук, профессор, лауреат премии Правительства РФ в области науки и техники в 2017 г., вице-президент Российского общества по изучению печени. Конфликт интересов отсутствует.
Мартынов Анатолий Иванович – доктор медицинских наук, академик РАН, Президент Общероссийской общественной организации "Российское научное медицинское общество терапевтов". Конфликт интересов отсутствует.
Некрасова Татьяна Петровна – кандидат медицинских наук, врач-патологоанатом, доцент Института клинической морфологии и цифровой патологии. Конфликт интересов отсутствует.
Сас Евгений Иванович − Профессор второй кафедры терапии (усовершенствования врачей) ФГБВОУ ВО «Военно-медицинская академия им. С.М. Кирова» Министерства обороны Российской Федерации, д.м.н. Конфликт интересов отсутствует.
Сиволап Юрий Павлович – доктор медицинских наук. Конфликт интересов отсутствует.
Тарасова Лариса Владимировна – Заведующая кафедрой факультетской и госпитальной терапии ФГБОУ ВО Чувашский государственный университет им. И.Н. Ульянова» д.м.н., главный внештатный специалист терапевт, гастроэнтеролог Министерства здравоохранения Чувашской Республики, руководитель Республиканского гастроэнтерологического центра Министерства здравоохранения Чувашской Республики, член президиума РНМОТ. Конфликт интересов отсутствует.
Ткаченко Пётр Евгеньевич – кандидат медицинских наук, член Российского общества по изучению печени. Конфликт интересов отсутствует.
Трухан Дмитрий Иванович – Профессор кафедры внутренних болезней и поликлинической терапии лечебного факультета ФГБОУ ВО «Омский государственный медицинский университет», д.м.н. Конфликт интересов отсутствует.
Хлынова Ольга Витальевна – Проректор по науке, зав. кафедрой госпитальной терапии ФГБОУ ВО «Пермский государственный медицинский университет им. академика Е.А. Вагнера» Минздрава России, д.м.н., профессор, член-корр. РАН. Конфликт интересов отсутствует.
Цыганова Юлия Вадимовна – Старший преподаватель кафедры факультетской и госпитальной терапии ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова». Конфликт интересов отсутствует.
Приложение А2. Методология разработки клинических рекомендаций
Предлагаемые рекомендации имеют своей целью довести до практических врачей современные представления об этиологии и патогенезе АБП, познакомить с применяющимся в настоящее время алгоритмами оценки тяжести заболевания, прогноза и лечения.
Целевая аудитория данных клинических рекомендации:
-
Врачи-гастроэнтерологи
-
Врачи общей практики (семейные врачи)
-
Врачи-терапевты
-
Врачи-наркологи
-
Врачи-психиатры
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД
|
Расшифровка
|
|---|---|
|
1
|
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа
|
|
2
|
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа
|
|
3
|
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая
|
|
5
|
Имеется лишь обоснование механизма действия или мнение экспертов
|
Таблица 2. Уровни достоверности доказательств с указанием использованной классификации уровней достоверности доказательств (УДД)
|
УДД
|
Расшифровка
|
|---|---|
|
1
|
Систематический обзор рандомизированных клинических исследований с применением мета-анализа
|
|
2
|
Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа
|
|
3
|
Нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая или серии случаев, исследование «случай-контроль»
|
|
5
|
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение эксперта
|
Таблица 3. Уровни убедительности рекомендаций (УУР) с указанием использованной классификации уровней убедительности рекомендаций
|
УУР
|
Расшифровка
|
|---|---|
|
А
|
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
|
|
В
|
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
|
|
С
|
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
|
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учетом следующих нормативно-правовых документов:
-
Приказ Минздрава России от 28.02.2019 № 103н "Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации" (Зарегистрировано в Минюсте России 08.05.2019 № 54588)
-
Приказ Министерства здравоохранения Российской Федерации от 12 ноября 2012 г. № 906н "Об утверждении порядка оказания медицинской помощи населению по профилю "Гастроэнтерология" (Зарегистрировано в Минюсте России 21 января 2013 г. № 2664)
-
Приказ Министерства здравоохранения Российской Федерации от 10 мая 2017 г. № 203н "Об утверждении критериев оценки качества медицинской помощи».
-
Приказ Министерства здравоохранения РФ от 30 декабря 2015 г. № 1034н "Об утверждении Порядка оказания медицинской помощи по профилю "психиатрия-наркология" и Порядка диспансерного наблюдения за лицами с психическими расстройствами и (или) расстройствами поведения, связанными с употреблением психоактивных веществ" (с изменениями и дополнениями) .
-
Приказ Минздрава России от 18.12.2015 № 933н (ред. от 25.03.2019) О порядке проведения медицинского освидетельствования на состояние опьянения (алкогольного, наркотического или иного токсического).
-
Приказ Министерства здравоохранения РФ от 24 декабря 2012 г. № 1392н "Об утверждении стандарта скорой медицинской помощи при отравлениях алкоголем, органическими растворителями, галогенпроизводными алифатических и ароматических углеводородов".
-
Приказ Министерства здравоохранения Российской Федерации от 28.12.2022 № 810н "Об утверждении стандарта медицинской помощи взрослым при циррозе и фиброзе печени (диагностика и лечение)"
Приложение Б. Алгоритмы действий врача
Алгоритм ведения больных с алкогольным гепатитом.
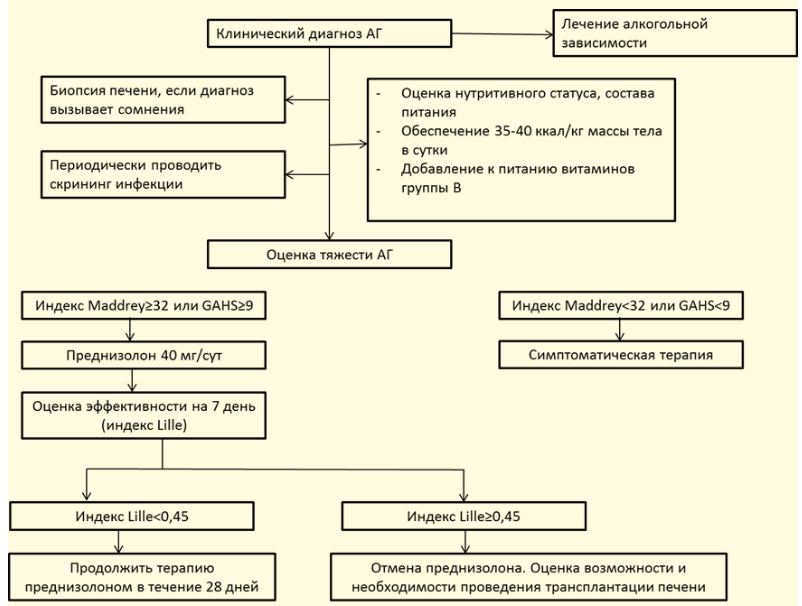

Приложение В. Информация для пациента
Уважаемый пациент! При употреблении опасных доз алкоголя у вас может развиться поражение печени, которое на ранней стадии может не иметь клинических проявлений. Опасной дозой принято считать приём алкогольных напитков в количестве 30 г чистого этанола (3 СтД) в сутки для мужчин и 20 г чистого этанола (2 СтД) в сутки для женщин. Так, например, в 0,5 л водки содержится 16 СтД (160 г чистого этанола), а в 0,5 л пива (крепость 5 %о) – 2 СтД. Опасные и угрожающие для здоровья дозы алкоголя для мужчин 30 г/сут в пересчете на чистый этанол, что составляет 75 мл водки (крепость 40 %о), 300 мл сухого вина (крепость 10%о), 600 мл пива (крепость 5 %о). Употребление более 7 СтД для женщин и более 14 СтД для мужчин в неделю приводит к повышенному риску развития поражения печени.
В случае продолжения злоупотребления алкоголем могут появиться психические нарушения, развиться тяжелый гепатит с желтухой и высоким риском смерти, в последующем может развиться цирроз печени. Симптомы, которые могут свидетельствовать об ухудшении состояния печени: прогрессирующая слабость, нарушения сна, снижение внимания и памяти, появление подкожных гематом («синяков») без каких либо физических воздействий, геморрагические высыпания на коже, носовые и десневые кровотечения, желтушность кожных покровов, рвота кровью или «кофейной гущей», стул черного цвета дегтеобразной консистенции («мелена»), появление или усиление болей в верхних отделах живота, правом и/или левом подреберьях. Во всех этих случаях необходимо посетить лечащего врача.
Уважаемый пациент! Первым и обязательным условием профилактики развития алкогольной болезни печени и ее лечения является прекращение употребления алкоголя!
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Тест «AUDIT»
Название на русском языке: Тест на выявление нарушений, связанных с употреблением алкоголя «AUDIT»
Оригинальное название (если есть): AUDIT – Alcohol Use Disorders Inventory Test
Источник (официальный сайт разработчиков, публикация с валидацией): Babor T.F., Higgins-Biddle J.C., Saunders J.B., Monterio M.G. The Alcohol Use Disorders Identification Test, Guidelines for Use in Primary Care, second edition. // World Health Organization Department of Mental Health and Substance Dependence. 2nd edition. Geneva – 2001.
Тип (подчеркнуть): вопросник
Назначение: Вопросник позволяет определить лиц, злоупотребляющих алкоголем с последствиями для здоровья (определен порог ≥ 8 баллов, обладающий 92% чувствительностью и 94% специфичностью).
Содержание (шаблон):
|
Вопросы
|
Количество баллов
|
||||
|
|
0
|
1
|
2
|
3
|
4
|
|
1. Как часто Вы употребляете спиртные напитки?
|
Никогда
|
Один раз в месяц и реже
|
2-4 раза в месяц
|
2-3 раза в неделю
|
4 и более раз в неделю
|
|
2. Сколько Вы обычно выпиваете в день?
|
30-60 мл. 40% водки,
или
75-150 мл. 17-20% крепленого вина,
или
75-150 мл. 11-13% сухого вина,
или
250 мл. – 1 бутылка 5% пива.
|
90-120 мл. 40% водки,
или
225-300 мл. 17-20% крепленого вина,
или
300-400 мл. 11-13% сухого вина,
или
1.5-2 бутылки 5% пива.
|
150-180 мл. 40% водки,
или
375-450 мл. 17-20% крепленого вина,
или
500-600 мл. 11-13% сухого вина,
или
2.5-3 бутылки 5% пива.
|
210-240 мл. 40% водки,
или
525-600 мл. 17-20% крепленого вина,
или
700-1000 мл. 11-13% сухого вина,
или
3.5-4 бутылки 5% пива.
|
более 300 мл. 40% водки,
или
более 750 мл. 17-20% крепленого вина,
или
более 1000 мл. 11-13% сухого вина,
или
более 5 бутылок 5% пива.
|
|
3. Как часто Вы выпиваете более 180 мл водки (450 мл вина) в течение одного дня?
|
Никогда
|
Менее 1 раза в месяц
|
1 раз в месяц
|
1 раз в неделю
|
Ежедневно или почти ежедневно
|
|
4. Как часто за последний год Вы находили, что не способны остановиться, начав пить?
|
Никогда
|
Менее 1 раза в месяц
|
1 раз в месяц
|
1 раз в неделю
|
Ежедневно или почти ежедневно
|
|
5. Как часто за последний год Вы из-за выпивки не сделали то, что от Вас обычно ожидают?
|
Никогда
|
Менее 1 раза в месяц
|
1 раз в месяц
|
1 раз в неделю
|
Ежедневно или почти ежедневно
|
|
6. Как часто за последний год Вам необходимо было выпить утром для устранения похмелья
|
Никогда
|
Менее 1 раза в месяц
|
1 раз в месяц
|
1 раз в неделю
|
Ежедневно или почти ежедневно
|
|
7. Как часто за последний год у Вас возникало чувство вины на следующий день после употребления алкоголя?
|
Никогда
|
Менее 1 раза в месяц
|
1 раз в месяц
|
1 раз в неделю
|
Ежедневно или почти ежедневно
|
|
8. Как часто за последний год Вы были не способны вспомнить, что было накануне, из-за того что Вы выпивали?
|
Никогда
|
Менее 1 раза в месяц
|
1 раз в месяц
|
1 раз в неделю
|
Ежедневно или почти ежедневно
|
|
9. Являлось ли когда-либо употребление Вами алкоголя причиной телесных повреждений у Вас или других людей?
|
Никогда
|
|
Да, но это было более, чем год назад
|
|
Да, в течение этого года
|
|
10. Случалось ли, что Ваш родственник, знакомый или доктор проявлял озабоченность по поводу употребления Вами алкоголя либо предлагал прекратить выпивать?
|
никогда
|
|
Да, но это было более, чем год назад
|
|
Да, в течение этого года
|
Интерпретация результатов (ключ):
|
Количество баллов
|
Интерпретация
|
Действие врача
|
|
0-7
|
Относительно безопасное употребление алкоголя
|
Рекомендовать не увеличивать объем потребляемого алкоголя
|
|
8 -15
|
Избыточное потребление алкоголя
|
Рекомендовать снизить объем потребляемого алкоголя
|
|
16-19
|
Потребление алкоголя в опасных объемах
|
Строго рекомендовать снизить объем потребляемого алкоголя, проводить мониторинг потребления алкоголя и зависимых от алкоголя поражений
|
|
20-40
|
Зависимость от алкоголя высоко вероятна
|
Направить к наркологу
|
Приложение Г2. Тест «AUDIT-С»
Название на русском языке: Тест на выявление нарушений, связанных с употреблением алкоголя, сокращенный вариант «AUDIT-С»
Оригинальное название (если есть): AUDIT-С – Alcohol Use Disorders Inventory Test – С
Источник (официальный сайт разработчиков, публикация с валидацией): https://www.calculators.tech/audit-c-calculator
Тип (подчеркнуть): вопросник
Назначение: для ежедневного использования в условиях дефицита времени на первичном приеме можно использовать сокращенную версию вопросника AUDIT, состоящего из 3 вопросов, для выявления лиц с высоким риском опасного употребления алкоголя.
Содержание (шаблон):
|
1. Как часто Вы употребляете спиртные напитки?
|
никогда
|
Один раз в месяц и реже
|
2-4 раза в месяц
|
2-3 раза в неделю
|
4 и более раз в неделю
|
|
2. Сколько Вы обычно выпиваете в день?
|
30-60 мл. 40% водки,
или
75-150 мл. 17-20% крепленого вина,
или
75-150 мл. 11-13% сухого вина,
или
250 мл. – 1 бутылка 5% пива.
|
90-120 мл. 40% водки,
или
225-300 мл. 17-20% крепленого вина,
или
300-400 мл. 11-13% сухого вина,
или
1.5-2 бутылки 5% пива.
|
150-180 мл. 40% водки,
или
375-450 мл. 17-20% крепленого вина,
или
500-600 мл. 11-13% сухого вина,
или
2.5-3 бутылки 5% пива.
|
210-240 мл. 40% водки,
или
525-600 мл. 17-20% крепленого вина,
или
700-1000 мл. 11-13% сухого вина,
или
3.5-4 бутылки 5% пива.
|
более 300 мл. 40% водки,
или
более 750 мл. 17-20% крепленого вина,
или
более 1000 мл. 11-13% сухого вина,
или
более 5 бутылок 5% пива.
|
|
3. Как часто Вы выпиваете более 180 мл водки (450 мл вина) в течение одного дня?
|
Никогда
|
Менее 1 раза в месяц
|
1 раз в месяц
|
1 раз в неделю
|
Ежедневно или почти ежедневно
|
Интерпретация результатов (ключ): тест считают положительным, если у мужчины насчитывается 4 балла и более, а у женщины – 3 балла и более. Максимальное количество баллов, которое можно набрать по данному опроснику – 12. Как правило, чем больше баллов, тем больше вероятность того, что стиль употребления алкоголя оказывает негативное влияние на организм человека. При положительном результате сокращенной версии рекомендовано использовать полную версию вопросника AUDIT.
Приложение Г3. Анкета-опросник «CAGE»
Название на русском языке: Анкета-опросник «CAGE»
Оригинальное название (если есть): The CAGE (Cut, Annoyed, Guilty, Eye-opener) questionnaire
Источник (официальный сайт разработчиков, публикация с валидацией): Dhalla S., Kopec J. A. The CAGE questionnaire for alcohol misuse: a review of reliability and validity studies //Clinical and Investigative Medicine. – 2007. – С. 33-41.
Тип (подчеркнуть): вопросник
Назначение: Предназначен для выявления пациентов с алкогольной зависимостью.
Содержание (шаблон):
Ответьте «да» или «нет» на каждый из предложенных вопросов.
1. У Вас когда-нибудь возникало чувство, что вы должны постараться уменьшить употребление алкоголя?
а) да б) нет
2. У Вас когда-нибудь люди вызывали раздражение своими упреками в отношении Вашего употребления алкоголя?
а) да б) нет
3. Испытывали ли Вы когда-нибудь чувство вины по поводу своего употребления алкоголя?
а) да б) нет
4. Вы когда-нибудь опохмелялись, чтобы успокоить свои нервы, или избавиться от плохого самочувствия, или чтобы обрести способность что-нибудь делать?
а) да б) нет
Интерпретация результатов (ключ):
-
положительный ответ на один из четырех вопросов (даже если таковым является последний, четвертый) не дает оснований для конкретных выводов; • положительные ответы на два вопроса свидетельствуют об эпизодическом употреблении спиртных напитков (эпизодическое пьянство);
-
положительные ответы на три вопроса позволяют предполагать систематическое употребление алкоголя;
-
положительные ответы на все четыре вопроса почти наверняка указывают на систематическое употребление алкоголя, приближающееся к состоянию алкогольной зависимости или уже сформировавшейся зависимости. В этом случае необходимо предпринять меры для коррекции сложившейся ситуации или, возможно, обратиться к специалисту. Тест считают положительным при наличии двух положительных ответов и более.
Чувствительность теста ‒ 66%, специфичность ‒ 91,4% [24].
Приложение Г4. Индекс Maddrey (Маддрея).
Название на русском языке: Дискриминантная функция (по Maddrey)
Оригинальное название (если есть): Maddrey score
Источник (официальный сайт разработчиков, публикация с валидацией): Maddrey W.C., Boitnott J.K., Bedine M.S., et al. Corticosteroid therapy of alcoholic hepatitis. // Gastroenterology. – 1978. – Vol.75. – No2. - P. 193–199.
Тип: шкала оценки
Назначение: оценка тяжести алкогольного гепатита и решение вопроса о назначении ГКС.
Содержание (шаблон):
DF = 4,6 х (ПВ (сек) – ПВ контроля (сек)) + билирубин (мг/дл)
Интерпретация результатов (ключ): Сумма баллов по шкале Maddrey ≥ 32 ассоциирована с летальностью 25% – 45% в течение ближайших 28 дней, в то время как нетяжелый гепатит (Maddrey < 32 баллов) приводит к летальному исходу в течение 3-х месяцев менее чем у 10% пациентов. Чувствительность и специфичность шкалы Maddrey в определении летального исхода в течение месяца составляет 86% и 48%, соответственно.
Приложение Г5. Индекс MELD.
Название на русском языке: Оценка тяжести состояния пациентов с циррозом печени по шкале MELD.
Оригинальное название (если есть): Model for End-Stage Liver Disease.
Источник (официальный сайт разработчиков, публикация с валидацией): https://www.uptodate.com/contents/calculator-model-of-endstage-liver-disease-meld-score-not-for-liver-transplantation-listing-purposes-not-appropriate-for-patients-under-age-12-years?source=see_link
Тип: шкала оценки.
Назначение: данная числовая шкала принята для определения летального исхода (смертности) больных АБП в течение 3 месяцев, а также используется для определения очередности трансплантации печени в листе ожидания (в связи с ограниченным количеством донорских органов).
Содержание (шаблон):
MELD = 9,6Ln (уровень креатинина) + 3,8Ln (уровень общего билирубина) + 11,2Ln (МНО) + 6,4.
MELD калькулятор, где Ln – натуральный логарифм, МНО – международное нормализованное отношение.
Интерпретация результатов (ключ):
Смертность больных в течение 3 мес. в зависимости от значения MELD составляет:
40 и более – 71.3%
30–39 – 52.6%
20–29 – 19.6%
10–19 – 6.0%
<9 – 1.9%
Минимальное значение для любой из трех переменных – 1 мг/дл, максимальный возможный уровень креатинина – 4 мг/дл, максимальное значение для индекса MELD – 40. Неблагоприятный жизненный прогноз ассоциирован со значением МELD > 18. Чем выше значение индекса, тем тяжелее протекает заболевание печени. При использовании классификации MELD было выявлено, что она обладает большой достоверностью при прогнозировании летального исхода в течение трех месяцев у пациентов с декомпенсированным ЦП. Так, при MELD > 35 баллов летальный исход прогнозируется в 80% случаев, при MELD от 20 до 34 баллов – в 10-60%, при MELD < 8 баллов – пациент является амбулаторным и требует активного наблюдения. Также используется для оценки тяжести алкогольного гепатита (> 21 балла – тяжелый).
Приложение Г6. Индекс Lille (Лилль).
Название на русском языке: Оценка выживаемости пациентов с алкогольным гепатитом по шкале Lille.
Оригинальное название (если есть): Lille model (score) for alcoholic hepatitis
Источник (официальный сайт разработчиков, публикация с валидацией): https://www.mdcalc.com/calc/2024/lille-model-alcoholic-hepatitis.
Тип: шкала оценки.
Назначение: предназначена для оценки эффективности терапии тяжелого алкогольного гепатита ГКС с решением вопроса о продолжительности лечения этими препаратами.
Содержание (шаблон):
R = 3,19 – 0,101х (возраст в годах) + 0,147 х (альбумин в день поступления в г/л) + 0,0165 х (общий билирубин в мкмоль/л на 8ой день терапии) + 0,206 х (наличие почечной недостаточности – 0 или 1) + 0,0065 х (общий билирубин в день поступления в мкмоль) + 0,0096 х (протромбиновое время в секундах)
Интерпретация результатов: При значении показателя менее 0,45 можно прогнозировать, что в течение 6 месяцев выживаемость больных составит в среднем 25%.
Приложение Г7. Шкала Глазго (GAHS)
Название на русском языке: Шкала Глазго ля определения степени тяжести алкогольного гепатита (GAHS)
Оригинальное название (если есть): the Glasgow Alcoholic Hepatitis Score
Источник (официальный сайт разработчиков, публикация с валидацией): https://www.mdcalc.com/calc/680/glasgow-alcoholic-hepatitis-score
Тип (подчеркнуть): шкала оценки
Назначение: оценка краткосрочной выживаемости и тяжести алкогольного гепатита с учетом возраста пациента, количества лейкоцитов в крови, МНО, уровня в сыворотке крови общего билирубина и мочевины. Если сравнить ее с предыдущими шкалами, то она более дискретна, что снижает ее точность, но улучшает формализованность, креатинин заменен на мочевину и добавлены такие важные факторы, как возраст больных (у пожилых смертность выше) и выраженность воспалительной реакции, которую оценивают по лейкоцитозу.
Содержание (шаблон):
|
Показатели
|
Баллы
|
||
|---|---|---|---|
|
|
1
|
2
|
3
|
|
Возраст, лет
|
<50
|
≥50
|
-
|
|
Лейкоциты, 109 /л
|
<15
|
≥15
|
-
|
|
Мочевина, ммоль/л
|
<5
|
≥5
|
-
|
|
МНО
|
<1,5
|
1,5-2,0
|
>2
|
|
Билирубин, мг/дл (мкмоль/л)
|
<7,3 (125)
|
7,3-14,6 (125-250)
|
>14,6 (250)
|
Интерпретация результатов: При значениях более 8 баллов (критерий тяжелого АлГ) к 28-му дню выживает 52% больных, к 84-му дню – 38%, при назначении таким больным глюкокортикостероидов выживаемость увеличивается – 78% и 59% соответственно.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.