Акушерский сепсис
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Общая информация
Краткое описание
Одобрено
Объединенной комиссией по качеству медицинских услуг
от «26» мая 2023 года
Протокол №181
Определение ВОЗ: Материнский сепсис – опасная для жизни дисфункция органов, вызванная инфекцией во время беременности, родов, послеродового периода или после аборта.
Код(ы) МКБ-10:

Сокращения, используемые в протоколе:
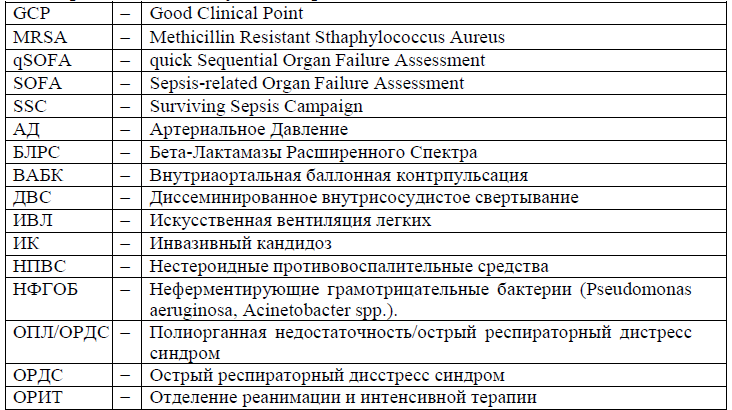
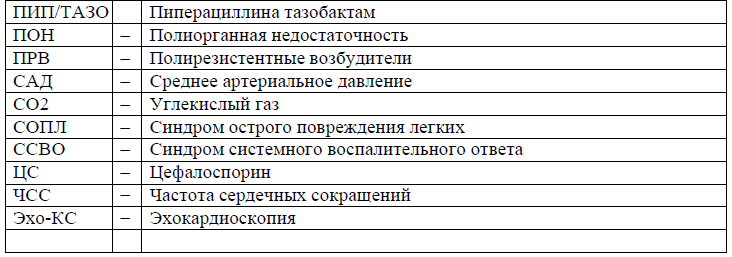
Категория пациентов: беременные, роженицы, родильницы.
Шкала уровня доказательности:

Классификация
Классификация: [4]
- сепсис;
- септический шок – это сепсис, в сочетании с необходимостью проведения терапии возопрессорами для подъема АД ср 65 мм рт. ст. и с уровнем лактата более 2 ммоль/л на фоне адекватной инфузионной терапии.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии (The Third International Consensus Definitions for Sepsis and Septic Shock - Sepsis-3). Обязательным критериями для диагноза сепсиса являются: очаг инфекции и признаки полиорганной недостаточности [1].
Жалобы и анамнез:
Физикальное обследование [4]:
Таблица 1. Диагностические критерии уровня прокальцитонина

Измерение уровней ПСП возможно оперативно проводить непосредственно при поступлении пациента в ОНТ, ОИТ, ОРИТ и в операционном блоке (тестирование Point-of-Care), что обеспечит своевременное принятие обоснованных клинических решений.
Таблица 2. Диагностические уровни пресепсина, пг/мл

Правила забора крови на микробиологический посев, грибы и анаэробы
: Кровь для исследования необходимо забирать до назначения антибиотиков. Необходимым минимумом забора являются 2 пробы, взятые из вен разных верхних конечностей с интервалом 30 мин. Оптимальным считается забор 3-х проб крови. Забор крови на высоте лихорадки не повышает чувствительности метода (УД – С). Кровь для исследования необходимо забирать только из периферической вены. Оптимальным является использование стандартных коммерческих флаконов с готовыми питательными средами. Забор крови из периферической вены следует проводить с тщательным соблюдением асептики. Кожу в месте венепункции обрабатывают раствором йода или повидон-йода концентрическими движениями от центра к периферии в течение как минимум минуты. Непосредственно перед забором кожу обрабатывают 70% спиртом. При проведении венепункции используют стерильные перчатки. Крышку флакона со средой обрабатывают спиртом. Для каждой пробы забирают 10 мл крови.
Показание для консультации специалистов:
Шкала qSOFA – упрощенная шкала SOFA для быстрой оценки на догоспитальном этапе и вне палаты интенсивной терапии (таблица 3).
Таблица 3. Шкала qSOFA.


NB!
Количество баллов по шкале qSOFA 2 и более – сильный предиктор неблагоприятного исхода и пациентка требует перевода в отделение реанимации и интенсивной терапии.
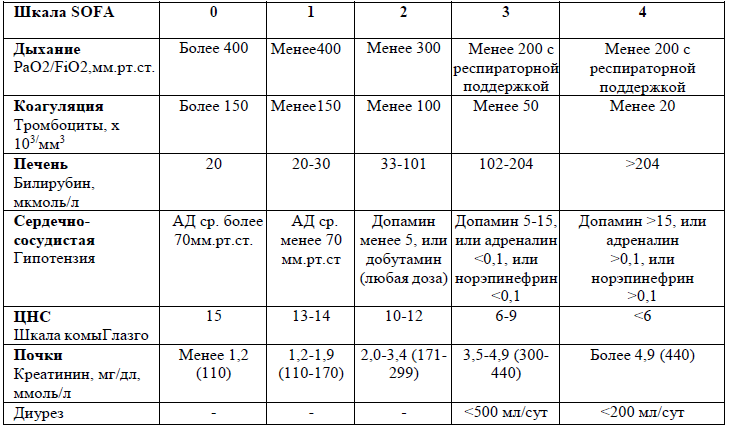
Таблица 4. Шкала SOFA
Диагностический алгоритм (Рисунок 1)
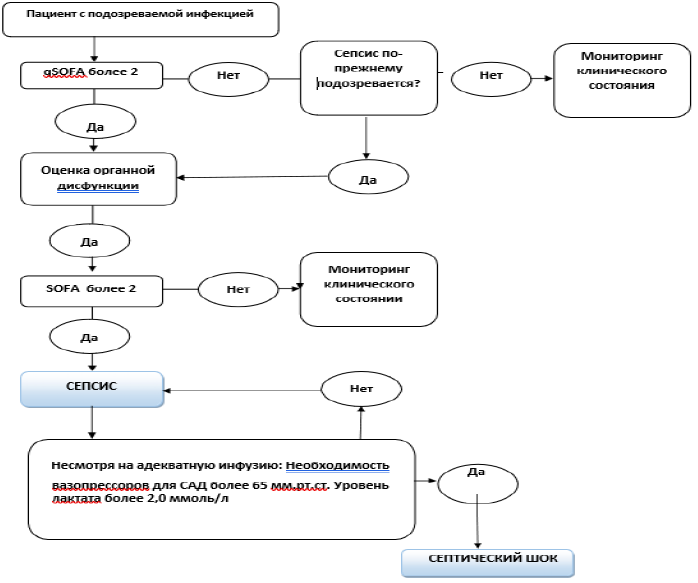
Идентификация и лечение артериальной гипотонии. У пациентов, у которых есть инфекция и артериальная гипотония или уровень лактата, более чем или равно 2 ммоль/л, необходимо начать инфузию кристаллоидов 30 мл/кг с переоценкой ответа на объем и перфузии ткани. Шестичасовые мероприятия и цели лечения должны быть выполнены. Сепсис 3 вводит qSOFA как инструмент для идентификации пациентов из-за опасности сепсиса с более высоким риском стационарной смерти или продленного нахождения в ОРИТ.
NB! У пациенток с инфекционным очагом необходимо оценивать признаки полиорганной недостаточности, а у пациенток с признаками полиорганной недостаточности необходимо оценивать явную или подозреваемую инфекцию. Это служит основой ранней диагностики и максимального раннего начала лечения сепсиса врачами всех специальностей.
Диагностика и оценка степени тяжести полиорганной недостаточности при сепсисе и септическом шоке должна проводится по шкале SOFA (УД-В) [2,18].
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований
Таблица 4.
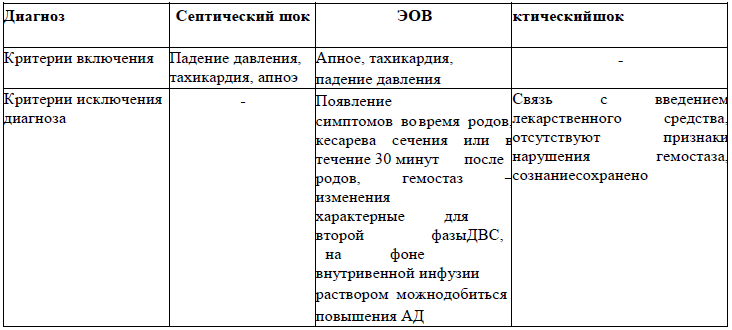
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ: нет.
Лечение (стационар)
карта наблюдения пациента, маршрутизация пациента: нет.
Немедикаментозное лечение:
Диета у пациентов с тяжелым сепсисом и септическим шоком суточный каллораж в первые 7 дней с момента постановки диагноза не должен превышать 500 ккал/сут (УД В). При этом предпочтение отдается комбинации энтерального питания и внутривенного введения глюкозы, нежели только парентеральному (УД В).
Рисунок 2. Начальная терапия сепсиса, септического шока
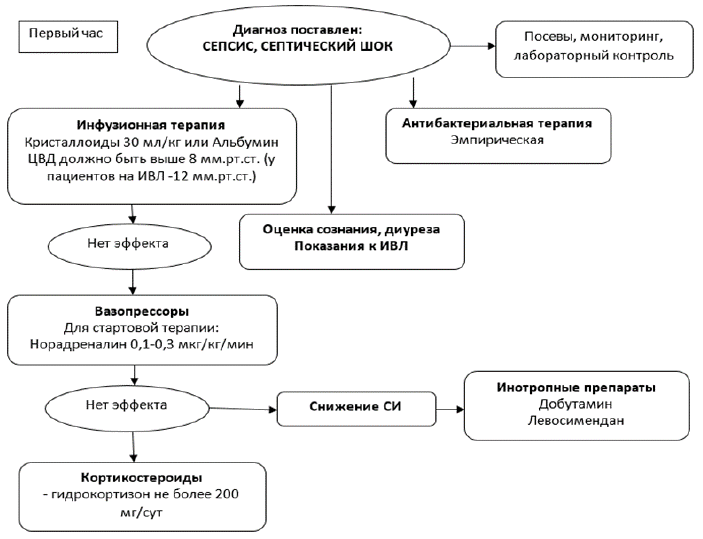
NB! Санация очага инфекции должна быть проведена в первые 6-12 ч после диагностики сепсиса и септического шока.
NB! Необходимость в положительном гидробалансе более 3-х суток с момента диагностики сепсиса ассоциируется с неблагоприятным исходом.
Таблица 5. Клинические действия при септическом шоке:
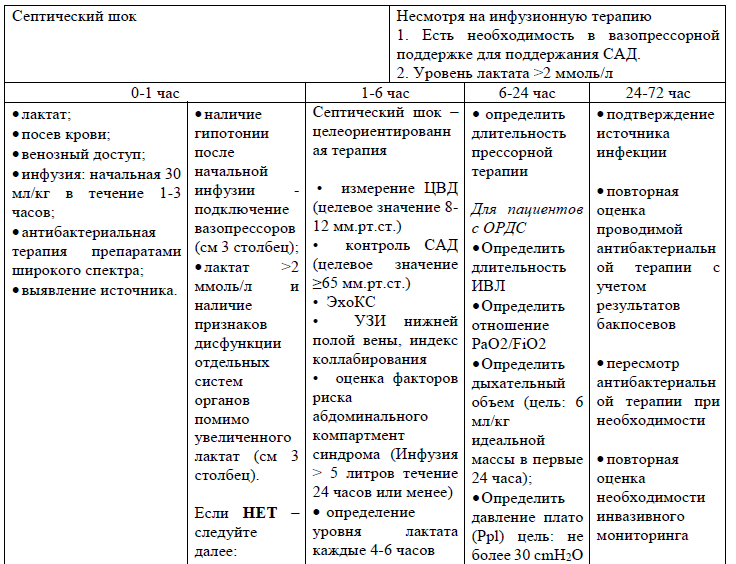


Инфузионная терапия
NB! Ограничение объема инфузии требуется, когда ЦВД увеличивается без гемодинамической стабилизации (АД, ЧСС), а также при поражении легких (пневмония, ОРДС).
Таблица 6. Дозы вазопрессоров и инотропных препаратов
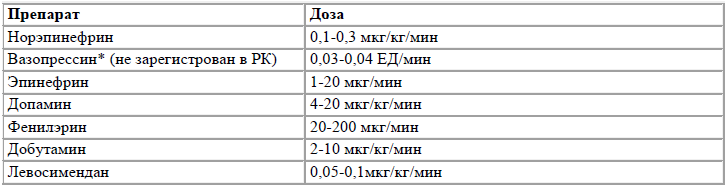
Рисунок 3. Эмпирический выбор антимикробной терапии у пациентов с абдоминальной инфекцией с учетом стратификации риска полирезистентных возбудителей.
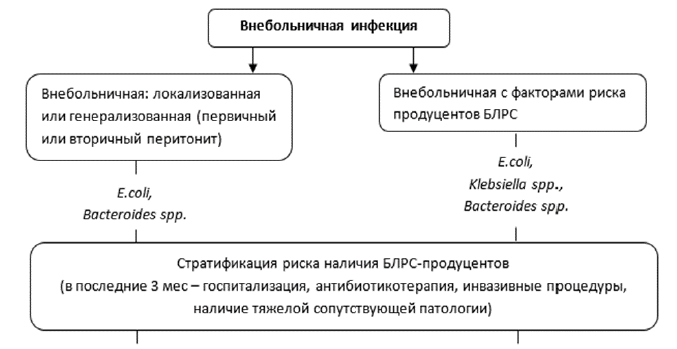
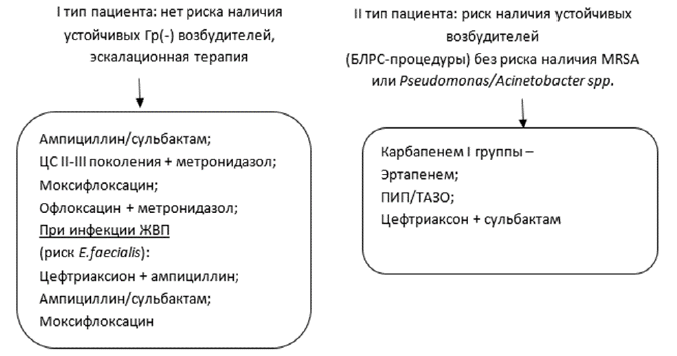
Рисунок 4. Эмпирический выбор антимикробной терапии у пациентов с абдоминальной инфекцией с учетом стратификации риска полирезистентных возбудителей и инвазивного кандидоза.
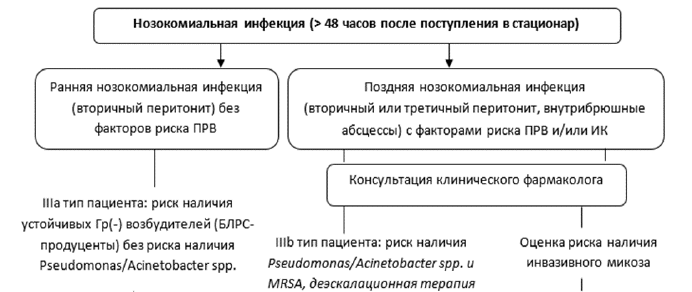
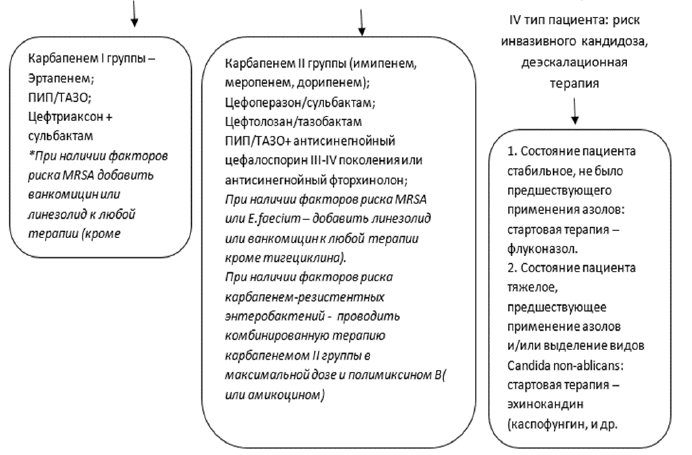
При сепсисе или септическом шоке парентерально [3-6,8,18-21,32,33,35]:
NB! С учетом персонифицированных подходов и индивидуальных особенностей пациентки возможно изменение дозировок и сроков антибактериальной терапии [46].
Абсолютные:
Таблица 9. Критерии острой почечной недостаточности – RIFLE

Таблица 10. Стадии острой почечной недостаточности

Таблица 11. Стадии острого почечного повреждения (KDIGO, 2012)


NB! Карнитин, глютамин, аргинин, иммунное питание, селен, омега-3 ЖК – не рекомендуются для ПП при сепсисе (SSC 2021)
взрослым с сепсисом или септическим шоком рекомендуется начинать инсулинотерапию при уровне глюкозы ≥ 10 ммоль/л.;
Таблица 12. Дозы препаратов для тромбопрофилактики [47]:
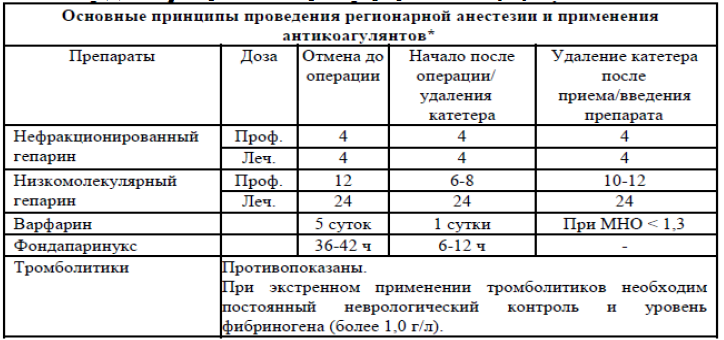
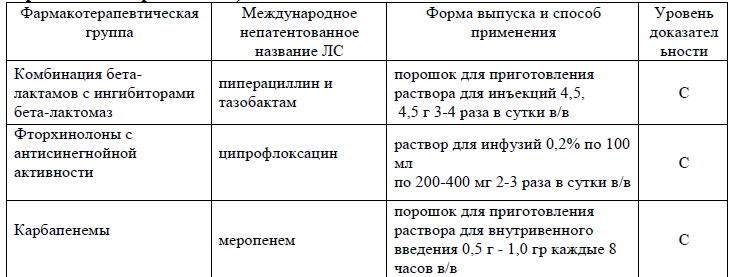
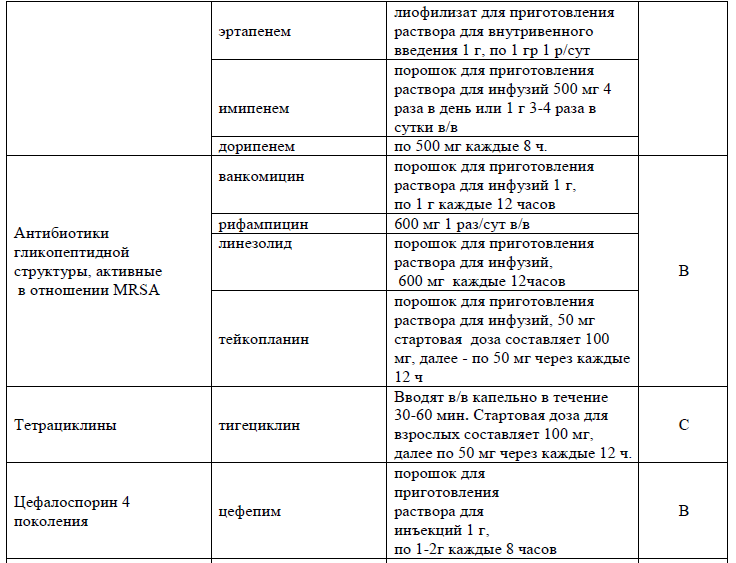
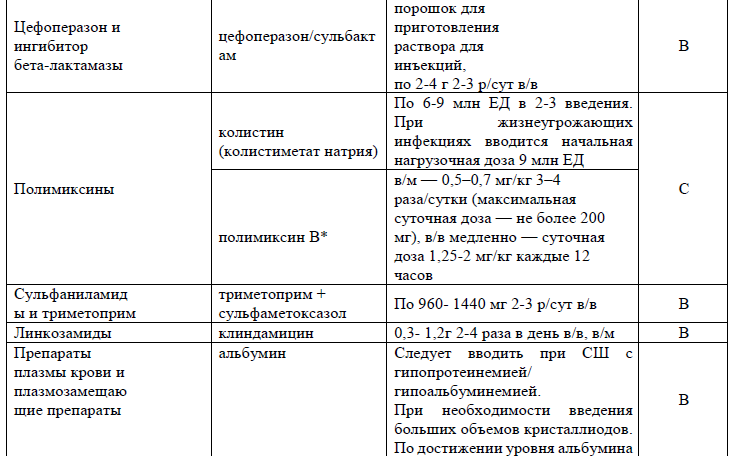
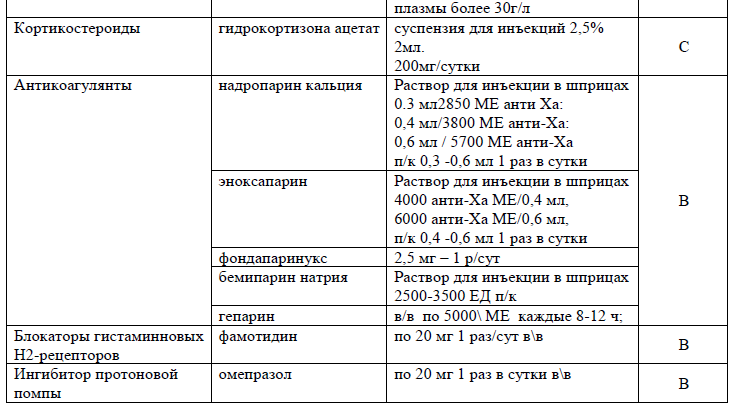
Таблица 13. Перечень основных лекарственных средств (имеющих 100% вероятность применения)
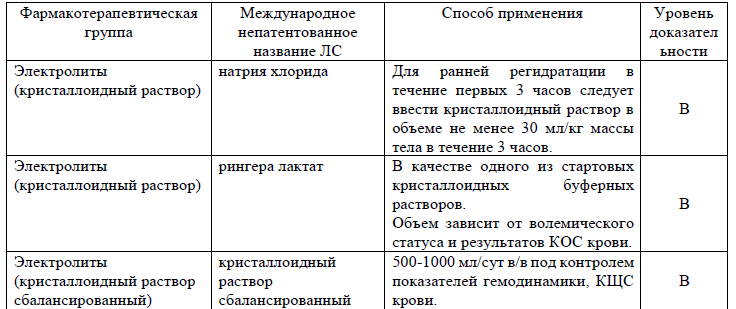
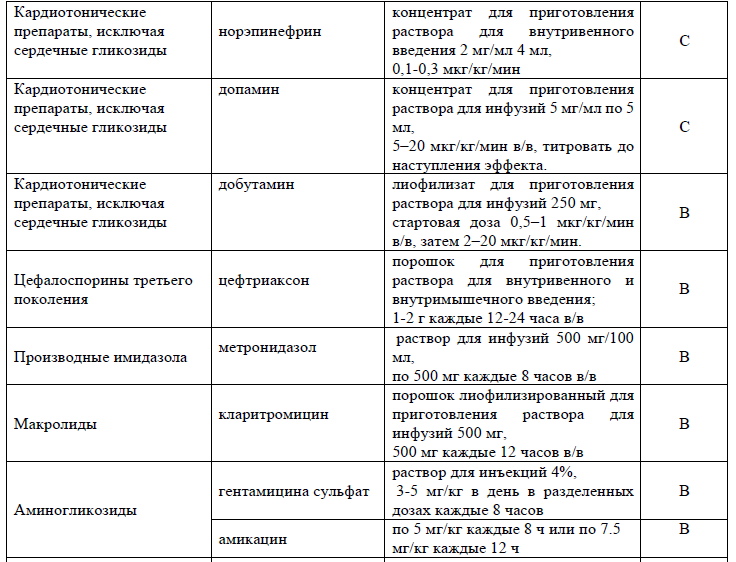

Таблица 14. Перечень дополнительных лекарственных средств (менее 100% вероятности применения)
NB! Раннее выявление признаков системного поражения и манифестации полиорганной недостаточности является ключевым моментом для решения вопроса об оперативном вмешательстве и радикальной санации очага инфекции в акушерстве и гинекологии.
Рисунок 5. Алгоритм определения тактики санации очага (гистерэктомия) [36]
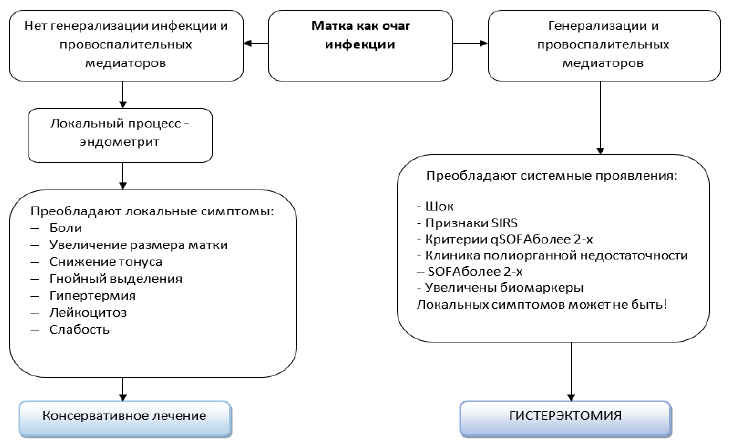
NB! Решение вопроса о гистерэктомии должно проводиться коллегиально в рамках мультидисциплинарного консилиума.
Дальнейшее ведение:
Госпитализация
Показания для плановой госпитализации: нет.
Показания для экстренной госпитализации: подозрение на сепсис.
NB! Явные признаки сепсиса, при наличии которых требуется госпитализация [9].
Скорость распространения симптомов ухудшения состояния очень важна. Раннее лечение антибиотиками, пероральными или парентеральными является решающим в определении исхода. Абдоминальная боль, лихорадка более 38.0С, тахикардия более 90 ударов в минуту являются показаниями для госпитализации и внутривенного назначения антибиотиков.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- 1) Albright CM, Mehta ND, Rouse DJ, Hughes BL. Sepsis in Pregnancy: Identification and Management. J Perinat Neonatal Nurs. 2016 Apr-Jun;30(2):95-105. 2) Singer M, Deutschman CS, Seymour CW, Shankar-Hari M, Annane D et al. The Third International Consensus Definitions for Sepsis Shock (Sepsis-3). JAMA. 2016 Feb 23;315(8):801-10. 3) SOGC Clinical Practice Guideline. The Prevention of Early-Onset Neonatal Group B Streptococcal Disease No. 298, October 2013. 10 p (Replaces #149, September 2004) 4) Kaukonen KM, Bailey M, Pilcher D, et al. Systemic inflammatory response syndrome criteria in defining severe sepsis. N Engl J Med 2015;372:1629-38 5) Bacterial Sepsis in Pregnancy NICE Green-top Guideline No. 64a 1st edition April 2012 6) Canadian Association of Emergency Physicians Sepsis Guidelines: the optimal management of severe sepsis in Canadian emergency departments 2008 7) Morocho JP, Martínez AF, Cevallos MM, Vasconez-Gonzalez J, et al.. Prolonged Capillary Refilling as a Predictor of Mortality in Patients With Septic Shock. J Intensive Care Med. 2022 Mar;37(3):423-429. ttp://doi:10.1177/08850666211003507 8) Royal College of Obstetricians and Gynaecologists. Bacterial Sepsis in Pregnancy / Green-top Guideline No. 64a April 2012.- 14 p. 9) Levy MM, Evans LE, Rhodes A. The Surviving Sepsis Campaign Bundle: 2018 Update. Crit Care Med. 2018 Jun;46(6):997-1000. http://doi.org/10.1097/CCM.0000000000003119 37 10) Dockree S, O'Sullivan J, Shine B, James T, Vatish M. How should we interpret lactate in labour? A reference study. BJOG. 2022 Dec;129(13):2150-2156. doi: 10.1111/1471-0528.17264. 11) Vardon-Bounes F, Ruiz S, Gratacap MP, Garcia C, et al. Platelets Are Critical Key Players in Sepsis. Int J Mol Sci. 2019 Jul 16;20(14). pii: E3494. http://doi.org/10.3390/ijms20143494 12) Assinger A, Schrottmaier WC, Salzmann M, Rayes J. Platelets in Sepsis: An Update on Experimental Models and Clinical Data. Front Immunol. 2019 Jul 17;10:1687. http://doi.org/10.3389/fimmu.2019.016 13) Jonsson AB, Rygård SL, Hildebrandt T, Perner A. et al. Thrombocytopenia in intensive care unit patients: A scoping review. Acta Anaesthesiol Scand. 2021 Jan;65(1):2-14. http://doi: 10.1111/aas.13699. 14) Mervak BM, Altun E, McGinty KA, Hyslop WB, et al. MRI in pregnancy: Indications and practical considerations. J Magn Reson Imaging. 2019 Mar;49(3):621-631. http://http://doi: 10.1002/jmri.26317. 15) Ray JG, Vermeulen MJ, Bharatha A, Montanera WJ, et al. Association Between MRI Exposure During Pregnancy and Fetal and Childhood Outcomes. JAMA. 2016 Sep 6;316(9):952-61. http://doi: 10.1001/jama.2016.12126. 16) Chartier AL, Bouvier MJ, McPherson DR, Stepenosky JE, et al. The Safety of Maternal and Fetal MRI at 3 T. AJR Am J Roentgenol. 2019 Nov;213(5):1170-1173. http://doi: 10.2214/AJR.19.21400. 17) Puac P, Rodríguez A, Vallejo C, Zamora CA, et al. Safety of Contrast Material Use During Pregnancy and Lactation. Magn Reson Imaging Clin N Am. 2017 Nov;25(4):787-797. http://doi: 10.1016/j.mric.2017.06.010. 18) Netto CM, Whitten M, Shetty N. Postpartum sepsis. Br J Hosp Med (Lond). 2015 Aug; 76(8):C118-21 19) Сепсис: классификация, клинико-диагностическая концепция и лечение: Практическое руководство/под ред. В.С. Савельева, Б.Р. Гельфанда. 23-е изд. доп. и перер.-М.: ООО «Медицинское информационное агенство», 2011.-352 с. 20) Oud L. Pregnancy-assiciated severe sepsis. Curr Opin Obstet Gynecol. 2016 Apr; 28(2):73-8 21) Evans L, Rhodes A, Alhazzani W, Antonelli M, Coopersmith CM et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021. Intensive Care Med. 2021 Nov;47(11):1181-1247. doi: 10.1007/s00134-021-06506-y. 22) Cecconi M, De Backer D, Antonelli M, Beale R, Bakker J, Hofer C, Jaeschke R, Mebazaa A, Pinsky MR, Teboul JL, Vincent JL, Rhodes A. Consensus on circulatory shok and hemodynamic monitoring. Task force of the European Society of Intensive Care Medicine. Intensive Care Med. 2014 Dec; 40(12):1795-815 23) Avni T, Lador A, Lev S, Leibovici L, Paul M, Grossman A. Vasopressors for the Treatment of Septic Shock: Systematic Review and Meta-Analysis. PLoS One. 2015;10(8):e0129305. 24) Annane D. The Role of ACTH and Corticosteroids for Sepsis and Septic Shock: An Update. Front Endocrinol (Lausanne). 2016 Jun 20; 7: 70 25) Pisano A, Monti G, Landoni G. Levosimendan: new indications and evidence for reduction in perioperative mortality? Curr Opin Anaesthesiol. 2016 Aug;29(4):454-61 26) Kakihana Y, Ito T, Nakahara M, Yamaguchi K, Yasuda T. Sepsis-induced myocardial dysfunction: pathophysiology and management. J Intensive Care. 2016 Mar 23;4:22 27) Kanter J, DeBlieux P. Pressors and inotropes. Emerg Med Clin North Am. 2014 Nov;32(4):823-34. doi: 10.1016/j.emc.2014.07.006.Epub 2014 Aug 28. 28) Gelinas JP, Russell JA. Vasopressors During Sepsis: Selection and Targets. Clin Chest Med. 2016 Jun;37(2):251-62. doi: 10.1016/j.ccm.2016.01.008 29) Jiang LB, Zhang M, Jiang SY, Ma YF. Early goal-directed resuscitation for patients with severe sepsis and septic shock: a meta-analysis and trial sequential analysis. Scand J Trauma Resusc Emerg Med. 2016 Mar 5;24:23 30) Zangrillo A, Putzu A, Monaco F, Oriani A, Frau G et al. Levosimendan reduces mortality in patients with severe sepsis and septic shock: A meta-analysis of randomized trials. J Crit Care. 2015 Oct;30(5):908-13 31) ARISE Investigators; ANZICS Clinical Trials Group, Peake SL, Delaney A, Bailey M, Bellomo R et al. Goal-directed resuscitation for patients with early septic shock. N Engl J Med. 2014 Oct 16;371(16):1496-506. 32) Стратегия и тактика применения антимикробных средств в лечебных учреждениях Росии. Российские национальные рекомендации/ под ред. В.С. Савельева, Б.Р.Гельфанда, С.В.Яковлева. – Москва, 2012 – 94с. 33) Sartelli M, Weber DG, Ruppe E, Bassetti M, Wright BJ et al. Antimicrobials: a global alliance for optimizing their rational use in intra-abdominal infections (AGORA). World J Emerg Surg. 2016 Jul 15;11:33. 34) Источник: VolbedaМ et al. Glucocorticosteroids for sepsis: systematic review with meta-analysis and trial sequential analysis. Intensive Care Medicine volume 41, P.1220–1234(2015) 35) Jiang LB, Zhang M, Jiang SY, Ma YF. Early goal-directed resuscitation for patients with severe sepsis and septic shock: insights and comparisons to ProCESS, ProMISe, and ARISE. Crit Care. 2016 Jul 1;20(1):160 36) Rivers E, Nguyen B, Havstad S, Ressler J et al. Early goal-directed therapy in the treatment of severe sepsis and septic shock. N Engl J Med. 2001 Nov 8;345(19):1368-77. 37) Zampieri FG, Mazza B. Mechanical Ventilation in Sepsis: A Reappraisal. Shock. 2016 Jul 21. 38) Gonzales JN, Lucas R, Verin AD. The Acute Respiratory Distress Syndrome: Mechanisms and Perspective Therapeutic Approaches. Austin J Vasc Med. 2015 Jun 4;2(1). 39) Goligher EC, Doufle G, Fan E. Update in Mechanical Ventilation, Sedation, and Outcomes 2014. Am J Respir Crit Care Med. 2015 Jun 15;191(12):1367-73. 40) Kim WY, Hong SB. Sepsis and Acute Respiratory Distress Syndrome: Recent Update. Tuberc Respir Dis (Seoul). 2016 Apr;79(2):53-7. 41) Takeuchi M, Tachibana K. Mechanical ventilation for ARDS patients-for a better understanding of the 2012 Surviving Sepsis Campaign Guidelines. Cardiovasc Hematol Disord Drug Targets. 2015;15(1):41-5. 42) Martensson J, Bellomo R. Sepsis-Induced Acute Kidney Injury. Crit Care Clin. 2015 Oct;31(4):649-60. 43) Swaminathan S, Rosner MH, Okusa MD. Emerging therapeutic targets of sepsis- associated acute kidney injury. Semin Nephrol. 2015 Jan;35(1):38-54. 44) Alobaidi R, Basu RK, Goldstein SL, Bagshaw SM. Sepsis-associated acute kidney injury. Semin Nephrol. 2015 Jan;35(1):2-11. 45) National Clinical Guideline Centre (UK). Acute Kidney Injury: Prevention, Detection and Management Up to the Point of Renal Replacement Therapy [Internet]. London: Royal College of Physicians (UK); 2013 Aug. 46) Источник: American Diabetes Association. Diabetes Care 2018 Jan; 41(Supplement 1): S144-S151 47) Клинический протокол от 13.01.2023 г., «Тромбоэмболическое осложнения в акушерстве», протокол №177.
Информация
Список разработчиков протокола с указание квалификационных данных:
Указание на отсутствие конфликта интересов: нет.
Рецензент: Искаков Серик Саятович – кандидат медицинских наук, PhD, НАО «Медицинский университет Астана» заведующий кафедрой акушерства и гинекологии №2, акушер-гинеколог высшей категории.
Условие для пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или наличии новых методов с уровнем доказательности.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.