Хронический вирусный гепатит С у взрослых
 Версия: Клинические рекомендации РФ 2025 (Россия)
Версия: Клинические рекомендации РФ 2025 (Россия)
Общая информация
Краткое описание
Разработчик клинической рекомендации
Российская Гастроэнтерологическая Ассоциация,
Российское общество по изучению печени,
Национальная ассоциация специалистов по инфекционным болезням имени академика В. И. Покровского (НАСИБ)
Одобрено Научно-практическим Советом Минздрава России
Клинические рекомендации
Хронический вирусный гепатит С
Год утверждения (частота пересмотра): 2025
Пересмотр не позднее: 2027
ID:516_3
Возрастная категория: Взрослые
Определение заболевания или состояния (группы заболеваний или состояний)
Хронический вирусный гепатит С (ХВГС) – хроническое воспалительное заболевание в течение более 6 месяцев с преимущественным поражением ткани печени вследствие инфицирования вирусом гепатита С (ВГС), которое может привести к тяжелым последствиям – циррозу, раку печени (гепатоцеллюлярной карциноме, ГЦК) и летальному исходу [1].
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
B18.2 – хронический вирусный гепатит С.
Применявшийся ранее код Z22.5 для носителей вирусного гепатита был исключен из последнего пересмотра МКБ 10.
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Заболевание классифицируют в зависимости от ГТ ВГС, а также наличия ЦП и внепеченочных проявлений.
По стадиям:
0 – без фиброза;
1 – слабовыраженный фиброз;
2 – умеренный фиброз;
3 – выраженный фиброз;
4 – тяжелый фиброз.
По генотипу ВГС:
-
– генотип 1
-
Генотип 1а
-
Генотип 1b
-
-
– генотип 2 (в том числе 2k1b)
-
– генотип 3
-
– генотип 4
-
– генотип 5
-
– генотип 6
-
– генотип 7
-
– генотип 8
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Возбудителем ХВГС является ВГС, который представляет собой небольшой гепатотропный РНК-вирус из семейства Flaviviridae. Вирус состоит из нуклеокапсида, состоящего из сердцевинного (ядерного) белка (HCVcAg) и одноцепочечной (+) РНК, и белково-липидной оболочки, содержащей аполипопротеин Е (апоЕ) человека и вирусные белки Е1 и Е2. Вирусный геном кодирует 10 различных белков, среди которых 3 описанных выше структурных и 7 неструктурных (p7, NS2, NS3, NS4A, NS4B, NS5A и NS5B) [2].
Выделяют 8 генотипов (ГТ) [3], которые обозначаются арабскими цифрами от 1 до 8, и несколько десятков субтипов ВГС, которые обозначаются латинскими буквами. Наибольшее клиническое значение имеют субтипы ГТ 1: а и b. Генотипы и субтипы различаются в последовательностях приблизительно на 30% и 20% соответственно. Вариабельность генома вируса обусловливает изменения в строении антигенных детерминант, которые определяют выработку специфических антител. Это препятствует элиминации вируса из организма и созданию эффективной вакцины против ВГС [4,5].
Инфицирование ВГС в большей доле случаев (55-85%) приводит к хроническому течению заболевания и примерно у четверти больных приводит в течение последующих десятилетий к развитию ЦП, что, в свою очередь, может служить основой для формирования ГЦК [6]. Довольно часто ввиду преимущественного бессимптомного течения инфекции заболевание впервые проявляется осложнениями ЦП.
Ведущим патогенетическим механизмом при ХВГС является нарушение взаимодействия иммунных клеток с инфицированными ВГС гепатоцитами. Повреждение печеночной ткани в большей степени является результатом реализации иммунного ответа в очаге воспаления, а не цитопатического действия вируса [7]. В печени накапливаются иммунокомпетентные клетки, часть из которых (NK-клетки, цитотоксические T-лимфоциты) обладают высокой цитотоксичностью и способностью повреждать гепатоциты [8]. В результате контактаинфицированных гепатоцитов с CTL-лимфоцитами (компонента адаптивного иммунного ответа) происходит запуск апоптоза. Отмечается дефицит Т-системы, депрессия макрофагов, ослабление системы интерфероногенеза, отсутствие специфического антителогенеза в отношении антигенов вирусов, что в конечном итоге нарушает адекватное распознавание и элиминацию иммунной системой антигенов вирусов на поверхности гепатоцитов [8-11].
У больных с выраженным Т-клеточным ответом происходит полная элиминация ВГС после перенесенного острого гепатита С. Вследствие взаимодействия вируса и иммунной системы происходит угнетение активности CTL-лимфоцитов белками вируса. В результате этого при ХВГС формируется иммунологическая толерантность к вирусу [12].
Действие вируса при ХВГС и вызванные им иммунологические реакции обусловливают не только повреждение печени, но и других органов и тканей. Концепция системных поражений при ХВГС заключается в возможности репликации вируса вне печени, а именно в тканях лимфоидного и нелимфоидного происхождения [13]. Размножение вируса в иммунокомпетентных клетках (лимфоцитах) приводит к нарушению их иммунологической функции. Сохранение ВГС в моноцитах является основной причиной реинфекции после трансплантации печени у больных тяжелыми формами ХВГС [10].
Среди факторов хозяина, влияющих на исход и течение ХВГС, имеет значение возраст на момент инфицирования, злоупотребление алкоголем, коинфицирование гепатотропными вирусами, нарушения липидного обмена и др. [14,15].
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
По оценочным данным в мире у 1% населения (порядка 71 млн человек) выявляются антитела к ВГС (anti-HCV), среди которых 2/3 хронически инфицированы, и 1/3 выздоровели самостоятельно или вследствие излечения. Заболевание шире распространено в Африке и Азии (почти 3% населения), в то время как в Америке и Европе оно выявляется у 1,5-2,0% [17]. Достоверная распространённость ХВГС в РФ остаётся неизвестной, расчетное число пациентов может достигать 4,9 млн [16]. По данным Роспотребнадзора в субъектах РФ по состоянию на 01.01.2017 на диспансерном учёте состояло 591 830 пациентов с ХВГС [16].
В России самым распространенными являются ГТ 1 (52,6%, из них 3,7% приходятся на субтип 1а и 48,9% – на субтип 1b) и ГТ 3 (39,6%), гораздо реже встречается ГТ 2 (7,8%). Генотипы 4-6 встречаются менее чем в 0,01% случаев, ГТ 7 и 8 – крайне редко [16]. С появлением пангенотипных схем противовирусного лечения ХВГС клиническое значение ГТ ВГС постепенно утрачивается, однако остается еще ряд генотип-специфичных препаратов, перед применением которых необходимо уточнять ГТ ВГС.
Источником инфекции является больной человек. Наиболее значимым является парентеральный путь передачи (при употреблении внутривенных наркотических препаратов, медицинских манипуляциях, травмирующих косметических процедурах, включая маникюр и педикюр, нанесение татуировок и установку пирсинга), существенно реже – половой и вертикальный пути передачи [18].
Риск профессионального заражения медицинских работников при случайном уколе игрой, контаминированной инфицированной кровью, составляет около 1,8%. При попадании крови пациента на поврежденную кожу или неповрежденные слизистые медицинского работника риск инфицирования значительно меньше, а попадание ее на неповреждённую кожу безопасно. В связи с этим риск заражения для медицинского персонала мал. Риск инфицирования пациента от заражённого медицинского работника крайне мал [18]. Риск перинатальной передачи инфекции составляет 5-10% и мало зависит от способа родоразрешения, однако возрастает при наличии коинфекции ВИЧ у матери до 14-16% [18]. Низкая концентрация вируса в секретах половых желез и органах определяют низкий риск его передачи половым путем: около 0,5% в год при незащищенном половом контакте в моногамной гетеросексуальной паре, около 0,4-1,8% в год среди лиц, оказывающих сексуальные услуги [19], около 0,8% в год среди мужчин, практикующих секс с мужчинами с моноинфекцией ВГС (при коинфекции ВИЧ он выше в 4 раза) [20].
ВГС обладает сравнительно невысокой устойчивостью к воздействию факторов окружающей среды. Известно, что вирус устойчив к нагреванию до 50°С, полная его инактивация наступает через 30 минут при температуре 60°С и через 2 минуты при температуре 100°С. Вирус чувствителен к ультрафиолетовому облучению и воздействию растворителей липидов [21].
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
У большинства пациентов заболевание протекает бессимптомно и выявляется при обследовании в рамках диспансеризации, догоспитальной подготовки, при посещении гастроэнтеролога по поводу диспепсических явлений (как правило, не связанных прямо с наличием ХВГС) и других специалистов (гинекологов, урологов, стоматологов и т.д.). От времени инфицирования до установления диагноза может пройти несколько лет. В ряде случаев первым проявлением заболевания являются В-клеточные лимфопролиферативные или иммунологически обусловленные внепеченочные заболевания (криоглобулинемический васкулит, в том числе с синдромом Рейно; интерстициальные заболевания легких; гломерулонефрит; синдром Шегрена; артрит и др.). У достаточного числа пациентов диагноз устанавливается только после манифестации осложнений ЦП: кровотечение из варикозно расширенных вен (ВРВ) пищевода и желудка и развития асцита [22,23].
При физикальном осмотре в отсутствии ЦП патологических проявлений, как правило, нет [22].
Активность трансаминаз может быть как повышенной, так и в пределах референсных значений. В некоторых случаях отмечается периодическое повышение активности АЛТ. В крови обнаруживаются anti-HCV и РНК ВГС. Активность АЛТ в пределах нормальных значений не свидетельствует об отсутствии изменений в печени, и пациенты не могут рассматриваться как «здоровые носители». Было показано, что 30-50% случаев у таких больных может быть диагностирован ЦП [24,25]. Часто в начальной стадии компенсированного ЦП отмечаются лишь похудание, астенизация, снижение работоспособности. При осмотре выявляют увеличение печени с ее уплотнением и спленомегалию. Однако у 20% больных в начальной стадии ЦП протекает бессимптомно, и его обнаруживают, как правило, случайно во время профилактического осмотра или обследования по поводу другого заболевания.
Цирроз печени развивается, как правило, в 25-35% случаев ХВГС. Вероятность его развития составляет 7,3% в год (5,1-9,5%). У многих пациентов ЦП в исходе ХВГС впервые диагностируется по данным гистологического исследования биоптата печени. Темпы декомпенсации ЦП составляют 5,5% в год. Вероятность развития в течение года синдрома портальной гипертензии у больных с компенсированным ЦП составляет 3,6%, печеночной энцефалопатии – 0,4%, ГЦК – 1,5% [24,26,27].
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии диагноза ХВГС:
Диагноз ХВГС устанавливается на основании наличия антител к вирусу гепатита С (Определение суммарных антител классов M и G (anti-HCV IgG и anti-HCV IgM) к вирусу гепатита C (Hepatitis C virus) в крови, далее везде в тексте – anti-HCV) и РНК вируса гепатита С (Определение РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР, качественное исследование, далее везде в тексте – РНК ВГС) или ядерного антигена ВГС (Определение Core-антигена вируса гепатита C (Hepatitis C virus) в крови, далее везде в тексте – HCVcAg) на протяжении более 6 месяцев [1].
1. Жалобы и анамнез
Специфических жалоб, характерных для ХВГС, нет. Заболевание, как правило, протекает бессимптомно, и довольно часто манифестирует осложнениями ЦП (асцит, кровотечение из ВРВ пищевода и желудка, печеночная энцефалопатия) [28]. В ряде случаев первыми проявлениями заболевания выступают иммунологически обусловленные внепеченочные проявления [23].
2. Физикальное обследование
При физикальном осмотре, как правило, никаких изменений не выявляется. Возможно наличие признаков ЦП (асцит, «печеночные ладони», ВРВ брюшной стенки, отеки, спленомегалия). При развитии иммунологически обусловленных внепеченочных проявлений имеют место соответствующие изменения [23].
3. Лабораторные диагностические исследования
На этапе скрининга
Скрининг на наличие ХВГС основан на выявлении anti-HCV. Если обнаружены anti-HCV, следует обязательно провести анализ на РНК ВГС. В случае если анализ на РНК ВГС недоступен, допустимо провести тест на HCVcAg. Этот антиген в сыворотке или плазме крови также является маркером репликации ВГС. Анализ HCVcAg менее чувствителен, чем РНК ВГС (нижний предел обнаружения эквивалентен приблизительно 500-3000 МЕ/мл РНК ВГС, в зависимости от ГТ ВГС [28,29]). В редких случаях HCVcAg не обнаруживается при определяемой РНК ВГС [30].
-
Рекомендуется определение суммарных антител классов M и G (anti-HCV IgG и anti-HCV IgM) к вирусу гепатита C (Hepatitis C virus) в крови у лиц из группы повышенного риска для выявления потенциально инфицированных [1].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарии: отношение к группе повышенного риска устанавливается, как правило, на основании слов пациента (место работы, реципиент в анамнезе, введение инъекционных наркотиков, половые партнеры, семейный анамнез и т.д.).
К группе повышенного риска относятся:
-
Беременные;
-
Реципиенты крови и ее компонентов, органов и тканей;
-
Персонал медицинских организаций;
-
Пациенты центров и отделений гемодиализа, пересадки почки, сердечно-сосудистой и лёгочной хирургии, гематологии;
-
Пациенты наркологических и кожно-венерологических кабинетов;
-
Опекаемые и персонал учреждений с круглосуточным пребыванием детей или взрослых;
-
Контактные лица в очагах острого и хронического гепатита С;
-
Потребители инъекционных наркотиков и их половые партнеры;
-
Лица, оказывающие услуги сексуального характера, и их половые партнеры;
-
Мужчины, практикующие секс с мужчинами;
-
Лица с большим количеством случайных половых партнеров;
-
Лица, сделавшие татуаж;
-
Лица, находящиеся в местах лишения свободы;
-
Доноры крови (ее компонентов), органов и тканей, спермы;
-
Пациенты с иммунодефицитом (пациенты с онкологическими заболеваниями, пациенты на гемодиализе, пациенты на лечении иммунодепрессантами и др.);
-
Пациенты с заболеваниями печени неясной этиологии (в процессе первичного клинико-лабораторного обследования).
Cанитарными правилами (СП 3.3686-21, приложение 18) определены контингенты, подлежащие обязательному одновременному обследованию на наличие anti-HCV и РНК ВГС [234]: (см. Приложение А3 таблица 1)
-
Всем пациентам с выявленными антителами к вирусу гепатиту C (Hepatitis C virus) в крови (anti-HCV) рекомендуется провести определение РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР, качественное исследование или определение Core-антигена вируса гепатита C (Hepatitis C virus) в крови (HCVcAg) (в случае недоступности первого) для подтверждения наличия текущей инфекции [1].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
-
Всем пациентам с выявленными антителами к вирусу гепатиту C (Hepatitis C virus) в крови (anti-HCV) и отрицательной РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР (или отрицательным Core-антигеном вируса гепатита C (Hepatitis C virus) в крови (HCVcAg) в случае недоступности первого), рекомендуется провести повторно определение РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР, качественное исследование через 12 и 24 недели, с тем чтобы подтвердить или опровергнуть наличие ХВГС [1].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарии: наличие anti-HCV в сочетании с РНК ВГС (или HCVcAg) характерно как для пациентов с ХВГС, так и пациентов с острым гепатитом С. Концентрация РНК ВГС (или HCVcAg) у больных с острым гепатитом С может значительно колебаться, вплоть до неопределяемого уровня. Таким образом, пациентам с неопределяемой РНК ВГС (или HCVcAg), необходимо повторно провести анализ РНК ВГС (или HCVcAg) через 12 и 24 недели после отрицательного результата, с тем чтобы убедиться в клиренсе ВГС (самостоятельное выздоровление от острого гепатита С) или подтвердить формирование ХВГС.
На этапе постановки диагноза:
-
Определение генотипа вируса гепатита С (определение генотипа вируса гепатита C (Hepatitis C virus), далее везде в тексте – ГТ ВГС) рекомендуется только пациентам с ХВГС для планирования генотип-специфичной схемы противовирусной терапии (ПВТ) [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: ГТ ВГС имеет значение только при планировании генотип-специфичных противовирусных препаратов. При доступности пангенотипных препаратов это обследование не требуется.
-
Всем пациентам с ХВГС с исходом в ЦП и/или признаками внепеченочных проявлений (лимфопролиферативные заболевания) рекомендуется проведение общего (клинического) анализа крови развернутого [23,36-38].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: течение ХВГС может влиять на клеточный состав крови, однако убедительных доказательств таких изменений в отсутствии ЦП и лимфопролиферативных заболеваний, индуцированных ВГС, нет. В случае формирования ЦП чаще всего наблюдается тромбоцитопения различной степени выраженности, реже другие варианты цитопений.
-
Всем пациентам с ХВГС рекомендуется проведение анализа крови биохимического общетерапевтического (определение активности аланинаминотрансферазы, аспартатаминотрансферазы, исследование уровня общего билирубина, исследование уровня креатинина в крови) для оценки тяжести повреждения гепатоцитов, функции печени и почек [39-41].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: в отсутствии признаков ЦП клиническое значение активности трансаминаз и других показателей функции печени (билирубин, альбумин) невелико. Оно приобретает большее значение, если имеет место сочетанная патология печени. У пациентов с ЦП в исходе ХВГС тяжесть поражения гепатоцитов и признаки декомпенсации имеют решающее значение в выборе тактики ведения пациента, препаратов ПВТ, прогнозе течения заболевания [39]. Кроме того, АЛТ и АСТ могут использоваться для самостоятельной оценки выраженности фиброза печени (например, индексы APRI, FIB-4) в отсутствии возможности выполнить инструментальное обследование [42] (см. Приложение Г). Оценка функции почек (исследование уровня креатинина в крови) необходима при планировании схем ПВТ, содержащих софосбувир** [40,41].
-
Всем пациентам с ХВГС с исходом в ЦП рекомендуется определение протромбинового (тромбопластинового) времени в крови или в плазме для оценки функции печени [46].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
-
Рекомендуется исследование уровня альфа-фетопротеина (АФП) в сыворотке крови пациентам с ХВГС с выраженным и тяжелым фиброзом печени (F3-F4 по METAVIR) для своевременной диагностики ГЦК [44,45].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Комментарии: риск развития ГЦК на стадии ЦП составляет приблизительно 1-5% в год. Вероятность летального исхода в течение первого года после постановки диагноза у пациентов с ГЦК составляет 33%.
-
Рекомендуется определение содержания ревматоидного фактора в крови (РФ) для всех пациентов с ХВГС с целью исключения синдрома смешанной криоглобулинемии [231, 232, 233].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Хроническая ВГС-инфекция ассоциирована с высоким риском развития синдрома смешанной криоглобулинемии. [231,232] Всем пациентам с ХВГС и клиническими проявлениями синдрома смешанной криоглобулинемии необходимо безотлагательное проведение ПВТ [233]
На этапе ПВТ:
-
Лабораторный мониторинг не рекомендуется пациентам с ХВГС без ЦП во время ПВТ без применения #рибавирина** [205,206].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Комментарий: препараты современной ПВТ обладают высокой безопасностью и эффективностью, в связи с чем необходимости в лабораторном мониторинге во время ПВТ без применения #рибавирина** нет.
-
При применении #РБВ** рекомендуется раз в 2-4 недели исследовать общий (клинический) анализ крови развернутый, с тем чтобы исключить вероятность частого побочного эффекта препарата – анемии [117].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Не рекомендуется определение РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР качественное исследование во время ПВТ для оценки ее эффективности [46-48] (см. Приложение Б).
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: закономерности между скоростью элиминации ВГС во время ПВТ и вероятностью УВО нет, в связи с чем необходимости в контроле РНК ВГС во время лечения нет [48].
4. Инструментальные диагностические исследования
На этапе постановки диагноза:
-
Всем пациентам с ХВГС рекомендуется выполнить УЗИ органов брюшной полости (комплексное) и забрюшинного пространства для выявления признаков ЦП и ГЦК [52,53].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарии: УЗИ органов брюшной полости (комплексное) и забрюшинного пространства проводится для диагностики ГЦК, признаков портальной гипертензии (увеличения селезенки, расширения вен портальной системы), асцита, исключения сопутствующей патологии желудочно-кишечного тракта, что в некоторых случаях может иметь решающее значение в определении стадии заболевания и тактики лечения. ЦП и ГЦК в исходе ХВГС могут протекать бессимптомно и выявляться только по данным УЗИ. При обнаружении в печени образования, подозрительного на ГЦК, следует продолжить исследования согласно клиническим рекомендациям по диагностике и лечению ГЦК.
-
Всем пациентам с ХВГС рекомендуется выполнение неинвазивной диагностики фиброза, с тем чтобы определить тактику ПВТ и дальнейшее ведение пациента (в случае ЦП) [54-58].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: неинвазивная диагностика позволяет с высокой точностью определить стадию фиброза. Она может быть выполнена с помощью эластометрии печени (должна быть выполнена на валидизированном аппарате), либо с помощью сывороточных тестов. При недоступности эластометрии могут использоваться некоммерческие расчетные показатели, основанные на результатах лабораторного обследования (например, расчет индексов APRI, FIB-4, см. Приложения Г).
-
При получении противоречивых данных неинвазивной диагностики рекомендуется рассмотреть вопрос о проведении чрескожной биопсии печени, с тем чтобы определить тактику ПВТ и дальнейшее ведение пациента (в случае ЦП) [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Биопсия печени является инвазивной процедурой с риском развития осложнений, поэтому ее следует проводить только в случае, если не удается получить результат с помощью применения неинвазивных методов [1].
-
Рекомендовано выполнение эзофагогастродуоденоскопии (ЭГДС) пациентам с ХВГС с исходом в ЦП для оценки наличия и степени ВРВ пищевода и желудка [59-61].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Эндоскопический осмотр выполняется для диагностики степени ВРВ пищевода и желудка, а также при наложении клипс и лигатур при кровотечении или его профилактики из вен пищевода у пациентов с ЦП. Возможно проведение процедуры в условиях седации, что требует предварительной консультации и сопровождения анестезиолога.
-
Компьютерную томографию органов брюшной полости с внутривенным болюсным контрастированием или магнитно-резонансную томографию органов брюшной полости с внутривенным контрастированием рекомендуется провести пациентам с ХВГС при обнаружении в печени образования по результатам УЗИ органов брюшной полости (комплексное) для уточнения его природы [62-65].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
5. Иные диагностические исследования
Не применяется.
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Цель лечения ХВГС – элиминация ВГС для профилактики осложнений ХВГС (включая ЦП, ГЦК, смерть), улучшение качества жизни и предотвращение дальнейшей передачи ВГС в популяции. Вирус гепатита С не образует высокостабильных внутриклеточных форм генетического материала, поэтому может быть элиминирован из организма полностью [1]. Показателем элиминации вируса из организма является стойкое достижение неопределяемого уровня РНК вируса в крови, которое оценивают через 12 недель после окончания терапии (УВО12) [29,30].
На выбор тактики лечения оказывают влияние следующие факторы [68]:
-
стадия фиброза печени, наличие ЦП и его класс;
-
ГТ ВГС;
-
наличие некоторых сопутствующих заболеваний;
-
опыт предыдущей ПВТ (если есть);
-
прием лекарственных средств по поводу сопутствующей патологии.
1. Показания к началу противовирусной терапии
-
Противовирусное лечение рекомендуется проводить всем пациентам с ХВГС, независимо от наличия ЦП, с целью излечения от инфекции (эрадикации ВГС) [1,69] (см. также Приложение А3).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: лечение ХВГС показано всем больным, так как в настоящее время применяются высокоэффективные и безопасные препараты, которые позволяют добиться УВО в подавляющем большинстве случаев.
-
Безотлагательно терапию рекомендуется рассмотреть в первую очередь у пациентов:
-
с ХВГС с исходом в ЦП (включая декомпенсированный ЦП);
-
с выраженным фиброзом (F3 по METAVIR);
-
с клинически значимыми внепеченочными проявлениями;
-
с рецидивом ХВГС после трансплантации печени;
-
с риском быстрого развития заболевания печени по причине сопутствующих заболеваний (хронический вирусный гепатит В, ВИЧ-инфекция, сахарный диабет и др., после трансплантации других органов кроме печени);
-
женщин детородного возраста, желающих забеременеть;
-
с высоким риском передачи инфекции, включая лиц, пребывающих в местах лишения свободы, пациентов с сексуальным поведением высокого риска, потребителей инъекционных наркотиков и др. [1,69].
-
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
-
Перед применением ПППД рекомендуется проверить сочетаемость назначенной схемы с уже принимаемыми пациентом препаратами, используя любой специальный ресурс (например, https://www.hep-druginteractions.org). При выявлении значимого взаимодействия рекомендуется заменить схему или препарат, который пациент принимает при лечении сопутствующего заболевания. Если это невозможно, решение следует принимать в индивидуальном порядке, оценивая соотношение пользы и риска от данной комбинации и возможных последствий от ее применения [70].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Большинство ПППД безопасно, но особенности их фармакокинетики могут приводить к значимому взаимодействию с другими препаратами, принимаемыми пациентом.
2. Лечение пациентов без цирроза печени и с компенсированным циррозом печени
-
Рекомендовано пациентов с ХВГС разделять на несколько групп, учитывая наличие опыта предшествующей терапии и ЦП, что влияет на эффективность ПВТ, а ее состав и длительность различается в зависимости от наличия этих факторов:
-
Пациенты без опыта ПВТ и без ЦП;
-
Пациенты без опыта ПВТ с компенсированным ЦП;
-
Пациенты, не ответившие на предшествующую ПВТ (ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**) без ЦП;
-
Пациенты, не ответившие на предшествующую ПВТ (ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**) с компенсированным ЦП. [1,69]:
-
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
-
Лечение пациентов с ХВГС без ЦП, без опыта ПВТ и без трансплантации печени в анамнезе рекомендуется проводить по одной из альтернативных схем согласно таблице 2 Приложения А3
- Велпатасвир+Софосбувир** [76,79]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
- Глекапревир+Пибрентасвир** [85]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
- Даклатасвир** + Софосбувир** [105,107,208,218-220]
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 3)
- Гразопревир+Элбасвир** или Гразопревир+Элбасвир** + #Рибавирин** (ГРА+ЭЛБ** 100/50 мг 1 таб. 1р/д + #РБВ** 1000 мг/сут, если масса тела <75 кг и 1200 мг/сут, если масса тела ≥75 кг. Курс лечения 16 нед) или Гразопревир+Элбасвир** + Софосбувир** при генотипе 3 [93,207, 221-224, 237-240, 244]
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
- Даклатасвир** + Нарлапревир** + #Ритонавир** (ДАК** 60 мг 1р/д + НРВ** 200 мг 1 р/д (2 таб. одновременно, по 100 мг каждая) + #р** 100 мг 1р/д. Курс лечения 12 нед) [109]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
- Ледипасвир+Софосбувир [90, 225]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
- Нарлапревир** + Софосбувир** + #Ритонавир** (НОВ** 200 мг 1 р/д (2 таб. одновременно, по 100 мг каждая) + #р** 100 мг 1р/д + СОФ** 400 мг 1 таб. 1р/д. Курс лечения 12 нед; у пациентов со слабовыраженным фиброзом (F0-2) и ВН менее 1 000 000 МЕ/мл можно рассмотреть длительность 8 недель по решению врачебной комиссии) [110,209]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
-
Лечение пациентов с ХВГС с компенсированным ЦП без опыта ПВТ рекомендуется проводить по одной из альтернативных схем согласно таблице 3 Приложения А3
- Велпатасвир+Софосбувир** или Велпатасвир+Софосбувир** + #Рибавирин** (ВЕЛ+СОФ** (100/400 мг) 1 таб. 1р/д + #РБВ** 400-1000 мг/сут при массе <75 кг, 1200 мг/сут при ≥75 кг; у Child-Pugh B/C старт 600 мг/сут. Курс лечения 12 нед.) [76, 79, 237, 245, 254, 260]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
- Глекапревир+Пибрентасвир** [83-85,229]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 4)
- Даклатасвир** + Софосбувир** при генотипе 1, 2 и 4 [106,107,218]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
- Даклатасвир** + Софосбувир** + #Рибавирин** (ДАК** 60 мг 1 таб. 1р/д + СОФ** 400 мг 1 таб. 1р/д + #РБВ** РБВ 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг. Курс лечения 24 нед) [237, 246, 247, 254, 263-266]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
- Гразопревир+Элбасвир** или Гразопревир+Элбасвир** + #Рибавирин** (ГРА+ЭЛБ** 100/50 мг 1 таб. 1р/д + #РБВ** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг. Курс лечения 16 нед.) [93,207, 223, 226, 237, 254, 255]
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
- Гразопревир+Элбасвир** + Софосбувир** + #Рибавирин** при генотипе 3 (ГРА+ЭЛБ** 100/50 мг 1 таб. 1р/д + #РБВ** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг + CОФ** 400 мг 1 таб. 1р/д. Курс лечения 12 нед).[93,207, 223, 226, 237, 254, 256, 257]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
- Ледипасвир+Софосбувир или Ледипасвир+Софосбувир + #Рибавирин** (ЛЕД+СОФ 90/400 мг 1 таб. 1р/д + #РБВ** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг. Курс лечения при генотипе 1 и 4 – 12 нед, при генотипе 3 – 24 нед). [89-92,213- 217, 248, 254, 260, 261]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
-
Лечение пациентов с ХВГС, не ответивших на предшествующую терапию ПегИФН** + #РБВ** ± СОФ** или СОФ** + #РБВ**, без ЦП рекомендуется проводить по одной из альтернативных схем согласно таблице 4 Приложения А3
- Велпатасвир+Софосбувир** [76, 79]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
- Глекапревир+Пибрентасвир** [83-85]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
- Даклатасвир** + Софосбувир** или Даклатасвир** + Софосбувир** + #Рибавирин** (ДАК** 60 мг 1 таб. 1р/д + СОФ** 400 мг 1 таб. 1р/д + #РБВ 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг. Курс лечения 12 недель) [106,107,210,211,218, 237,249,250, 254, 263-266]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
- Гразопревир+Элбасвир** или Гразопревир+Элбасвир + #Рибавирин** (ГРА+ЭЛБ ** 100/50 мг 1 таб. 1р/д + #РБВ** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг. Курс лечения 16 нед.) [93,207, 223, 226, 237, 254, 255]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
- Ледипасвир+Софосбувир или Ледипасвир+Софосбувир + #Рибавирин** (ЛЕД+СОФ 90/400 мг 1 таб. 1р/д + #РБВ** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг. Курс лечения 24 нед). [89-92,213- 217, 251, 252, 254, 261, 262]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
-
Лечение пациентов с ХВГС, не ответивших на предшествующую терапию ПегИФН** + #РБВ** ± СОФ** или СОФ** + #РБВ**, с компенсированным ЦП рекомендуется проводить по одной из альтернативных схем согласно таблице 5 Приложения А3
- Велпатасвир + Софосбувир** [76, 79]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
- Глекапревир+Пибрентасвир** [84,85]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
- Даклатасвир** + Софосбувир** [106,107, 218, 227]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
- Даклатасвир** + Софосбувир** + #Рибавирин** (ДАК** 60 мг 1 таб. 1р/д + СОФ** 400 мг 1 таб. 1р/д + #РБВ** 1000 мг/сут при массе тела <75 кг и 1200 мг/сут при массе тела ≥75 кг. Курс лечения 24 нед) [108,210,211, 218, 237, 253, 254]
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
- Гразопревир+Элбасвир** [93,207,223,226]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
- Гразопревир+Элбасвир** + #Рибавирин** ( ГРА+ЭЛБ** 100/50 мг 1 таб. 1р/д + #РБВ** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг. Курс лечения 16 нед). [93,207,223,226, 237, 244, 254, 258, 259]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
- Ледипасвир+Софосбувир или Ледипасвир+Софосбувир + #Рибавирин** ЛЕД+СОФ 90/400 мг 1 таб. 1р/д + #РБВ** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг. Курс лечения при генотипе 1 и 4 – 12 нед, при генотипе 3 – 24нед.) [90-92,213- 217, 251, 252, 254, 261, 262]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
Все вышеперечисленные препараты для лечения пациентов с ХВГС (всех ГТ ВГС) с ЦП (в т.ч. декомпенсированным) или без него, с опытом предшествующей ПВТ или без него суммированы в таблице 6 Приложения А3
Лечение пациентов с декомпенсированным ЦП описано разделе 3.11 и 3.12.
Принципы перелечивания после неуспешного курса ПППД (ингибирующими NS3/4А и/или ингибирующими NS5A) рассматриваются в разделе 3.4.
3. Контроль терапии
-
Всем пациентам, получившим ПВТ ХВГС, рекомендуется провести качественное определение РНК ВГС через 12 недель после окончания лечения, с тем чтобы оценить эффективность проведенной ПВТ. Рекомендуется использовать методы с высокой чувствительностью (≤15 МЕ/мл) [46-48,111]. Отсутствие РНК ВГС через 12 недель после окончания ПВТ означает излечение от ХВГС. Напротив, положительный результат РНК ВГС в эти сроки указывает на неудачу проведенного лечения.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
-
При применении РБВ** рекомендуется раз в 2-4 недели исследовать общий (клинический) анализ крови развернутый, и при снижении гемоглобина на 10 г/л от исходного и более уменьшить дозу препарата на 200 мг/сут, а при концентрации гемоглобина менее 85 г/л отменить терапию РБВ** [112-117].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Большинство современных препаратов ПВТ ХВГС хорошо переносятся, однако в ряде случаев необходимо добавлять РБВ** (для некоторых схем, особенно для пациентов с ЦП) – препарат, одним из основных побочных эффектов которого является не иммунный гемолиз. При применении РБВ** следует контролировать общий (клинический) анализ крови развернутый и при необходимости проводить коррекцию терапии.
-
По решению лечащего врача, независимо от условий оказания медицинской помощи, для контроля ПВТ (в т.ч. оценки эффективности и безопасности) взрослых пациентов с ХВГС рекомендуется рассмотреть применение телемедицинских технологий [228,230].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3)
4. Перелечивание
В большинстве случаев (95-100%) применение ПППД приводит к УВО, однако в редких случаях достичь УВО не удается.
-
При неэффективности терапии ПППД рекомендуется использовать схему с другими препаратами, а также комбинацию из трех препаратов различного механизма действия (препаратом, ингибирующим NS3/NS4A + препаратом, ингибирующим NS5A + препаратом, ингибирующим NS5B) без РБВ** или с добавлением его. Если доступно исследование мутаций резистентности ВГС к различным ПППД, рекомендуется выполнить его для рационального подбора новой схемы [71-76,167,212].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
-
Рекомендовано пациентам с ХВГС (ГТ 1-6) с декомпенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS3/4А+/-NS5В: для перелечивания пангенотипная схема велпатасвир+софосбувир** 100/400 мг в комбинации с #РБВ** (в дозе 1000 мг для пациентов весом <75 кг и 1200 мг для пациентов весом ≥75 кг) в течение 12 недель [167]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
-
Рекомендовано пациентам с ХВГС (ГТ 1-6) без ЦП или с ЦП (компенсированным и декомпенсированным) после неэффективной ПВТ препаратами, ингибирующими NS5А, для перелечивания пангенотипная схема велпатасвир+софосбувир** 100/400 мг в комбинации с #РБВ** (в дозе 1000 мг для пациентов весом <75 кг и 1200 мг для пациентов весом ≥75 кг) в течение 24 недель [167]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
-
Рекомендовано пациентам с ХВГС (ГТ 1) без ЦП или с компенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS3/4А без препаратов, ингибирующих NS5A, для перелечивания схема глекапревир+пибрентасвир** (300/120 мг) в течение 12 недель [71-76, 83-85, 167,212,229].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
-
Рекомендовано пациентам с ХВГС (ГТ 1) без ЦП или с компенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS5A, без препаратов, ингибирующих NS3/4А для перелечивания схема глекапревир+пибрентасвир** (300/120 мг) в течение 16 недель [71-76, 83-85, 167,212,229].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
-
Рекомендовано пациентам с ХВГС (ГТ 1-6) без ЦП или с компенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS3/4А и NS5А: по решению врачебной комиссии для перелечивания #глекапревир+пибрентасвир** (300/120 мг 1р/д) в сочетании с #софосбувиром** (400 мг 1 р/д) внутрь в течение 12 недель. Длительность курса определяется индивидуально и зависит, в том числе, от стадии фиброза печени и наличия резистентных к ПППД вариантов ВГС [71-76, 83-85, 167,212,229].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
5. Патогенетическая терапия
Патогенетическая терапии ХГВС неспецифична, она проводится в случае необходимости с учетом особенностей течения заболевания у конкретного пациента.
6. Симптоматическая терапия
Симптоматическая терапия ХВГС неспецифична, она проводится в случае необходимости с учетом особенностей течения заболевания у конкретного пациента
7. Хирургическое лечение
-
Рекомендуется проведение трансплантации печени при наличии стойких признаков декомпенсации функции печени пациентам с ЦП для сохранения жизни [118-120].
Уровень достоверности рекомендации С (уровень убедительности доказательств – 4)
Комментарий: дообследование проводится в соответствии с протоколом ведения пациентов из листа ожидания в трансплантологическом центре.
-
Пациентам с ЦП рекомендуется выполнение эндоскопического лигирования или склерозирования ВРВ пищевода и желудка для профилактики кровотечения или его купирования [121-125].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
-
Рекомендуется выполнение парацентеза пациентам с ЦП при наличии рефрактерного асцита для его купирования [126].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендуется выполнение трансъюгулярного внутрипеченочного порто-системного шунтирования пациентам при наличии выраженной портальной гипертензии [126].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
8. Внепеченочные проявления хронического вирусного гепатита С
-
Пациентам с внепеченочными иммунологически обусловленными проявлениями ХВГС рекомендуется назначить ПППД по описанным выше схемам [23,127-129].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: ХВГС может проявиться внепеченочными иммунологически обусловленными состояниями (криоглобулинемический васкулит, в том числе с синдромом Рейно, интерстициальные заболевания легких, гломерулонефрит, синдром Шегрена, артрит и другие), а также неходжкинскими В-клеточными лимфомами. Во всех случаях следует назначить ПППД по описанным выше схемам. Раннее начало ПВТ значительно снижает риск развития внепеченочных проявлений
9. Коинфекция
9.1 Коинфекция ВГС/ВИЧ
Пациенты с ХВГС и коинфекцией ВИЧ относятся к группе, требующей безотлагательной ПВТ ХВГС [1,69]. Течение ХВГС у ВИЧ-инфицированных зависит от степени выраженности иммунодефицита, обусловленного ВИЧ. Вероятность развития тяжелого поражения печени особенно высока при снижении CD4 лимфоцитов менее 200/мкл. Прогрессирование, связанное с поражением печени, обусловлено повышением концентрации вируса в крови (в 2-8 раз) на фоне выраженного иммунодефицита. Коинфекция ВИЧ и ВГС приводит к увеличению частоты развития осложнений, а также связанной с этими заболеваниями смертности. Антиретровирусная терапия коинфицированных ВГС/ВИЧ больных ассоциирована с возможным риском нарушения функций печени вследствие ее гепатотоксичности [130,131].
-
Для лечения ХВГС у больных, коинфицированных ВИЧ, рекомендуется использовать те же схемы ПВТ, что и для лечения моноинфекции ВГС, с целью эрадикации ВГС [132-137].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: все схемы ПВТ на основе ПППД требуют учета межлекарственных взаимодействий. Одним из удобных способов оценки межлекарственных взаимодействий является использование Ливерпульской таблицы лекарственных взаимодействий в Интернет ресурсе (http://www.hep-druginteractions.org).
9.2 Коинфекция ВГС/ВГВ
Пациенты с ХВГС и коинфекцией вирусом гепатита В (ВГВ) относятся к группе, требующей безотлагательной ПВТ ХВГС [1,69]. Коинфекция ВГС/ВГВ ускоряет прогрессирование заболевания и увеличивает риск развития ГЦК [138,139].
-
Всем больным ХВГС рекомендуется провести тестирование на наличие перенесенной или текущей инфекции, вызванной ВГВ: определение антигена (HBsAg) вируса гепатита B (Hepatitis B virus) в крови, качественное исследование, определение антител классов к ядерному антигену (HBcAg) вируса гепатита B (Hepatitis B virus) в крови, определение антител к поверхностному антигену (HBsAg) вируса гепатита B (Hepatitis B virus) в крови [140-143].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
-
Пациентам с коинфекцией ВГС/ВГВ рекомендуется назначить ПВТ нуклеозидами и нуклеотидами, кроме ингибиторов обратной транскриптазы, для профилактики реактивации инфекции, вызванной ВГВ. ПВТ нуклеозидами и нуклеотидами, кроме ингибиторов обратной транскриптазы, рекомендуется назначить на весь срок терапии ХВГС, а также на 12 недель после ее успешного завершения [142].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарии: поскольку ВГС, как правило, подавляет репликацию ВГВ, устранение первого вируса может привести к реактивации второго. Поэтому при лечении ХВГС следует тщательно контролировать маркеры активности ВГВ, и при их увеличении назначить ПВТ инфекции, вызванной ВГВ. Эту терапию также можно назначить с профилактической целью на срок лечение ХВГС и далее в течение 12 недель после ее успешного завершения.
-
Пациентам с ХВГС и anti-HBc (в отсутствии HBsAg и anti-HBs) во время ПВТ ХВГС рекомендуется ежемесячное определение активности аланинаминотрансферазы в крови для исключения реактивации ВГВ [142].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
-
При коинфекции ВГС/ВГВ для лечения ХВГС рекомендуется использовать стандартные схемы, описанные выше [1,138,142-145].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
10. Пациенты с хронической болезнью почек
-
Для ПВТ ХВГС у пациентов с ХБП (включая тяжелую, с СКФ <30 мл/мин/1,73 м2) рекомендуется использование ПППД в соответствии с общими рекомендациями ПВТ ХВГС пациентов без ХБП [146-155] (см. подраздел 3.2 и Приложение А3).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: на сегодня накоплено достаточно клинического опыта применения софосбувира** у пациентов с тяжелой ХБП [153-155], что позволяет назначать софосбувир**-содержащие схемы ПВТ всем таким пациентам без коррекции доз ПППД.
-
Для ПВТ ХВГС у пациентов с тяжелой ХБП (с СКФ <30 мл/мин/1,73 м2), тем не менее, рекомендуется по возможности отдавать предпочтение схемам, не содержащим софосбувир** [146-152]:
-
Глекапревир+пибрентасвир** для всех ГТ ВГС;
-
Гразопревир+элбасвир** для ГТ 1, 4;
-
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-
Пациентам с декомпенсированным ЦП (класс В или С по Child-Pugh) и тяжелой ХБП (с СКФ <30 мл/мин/1,73 м2) рекомендуется назначать следующие схемы ПВТ ХВГС в течение 24 недель [153,154,156,157]:
-
#Велпатасвир+софосбувир** (100/400 мг) 1 таб. 1р/д (для ГТ 1-6) [76,77,78,79,154, 247, 254]:
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Даклатасвир** 1 таб. (60 мг) 1 р/д + софосбувир** 1 таб. (400 мг) 1 р/д (для ГТ 1-4)
-
Ледипасвир+cофосбувир (для ГТ 1 и 4).
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
11. Пациенты с декомпенсированным циррозом печени
-
Лечение пациентов с ХВГС с декомпенсированным циррозом печени (Child-Pugh В или С) или эпизодами декомпенсации в анамнезе рекомендуется проводить по одной из альтернативных схем (согласно таблице 7 Приложения А3):
- Велпатасвир+Софосбувир** (100/400 мг) 1 таб. 1р/д + #Рибаверин** (все ГТ) 400-1000 мг/сут при массе <75 кг, 1200 мг/сут при ≥75 кг; у Child-Pugh B/C старт 600 мг/сут 12 недель [76,78,79, 254, 260];
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
- Даклатасвир** 60 мг 1 таб. 1р/д + Софосбувир** 400 мг 1 таб. 1р/д + #Рибаверин**(для ГТ 1,2,3,4) 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг 12-24 недели. [105,107,208,218-220, 254];
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 3)
- Ледипасвир+Софосбувир (для ГТ 1,4,5,6) -24 недели [89-92,213- 217,251, 252, 254];
- Ледипасвир+Софосбувир 90/400 мг 1 таб. 1р/д + #Рибаверин** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) (для ГТ 1,4,5,6) -12 недель [89-92,213- 217, 251, 252, 254];
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
12. Трансплантация печени
12.1 Противовирусная терапия ХВГС у больных с декомпенсированным циррозом печени, находящихся в Листе ожидания трансплантации печени
Целями ПВТ ХВГС у больных с декомпенсированным ЦП, находящихся в Листе ожидания ортотопической трансплантации печени (ОТП), являются:
-
Предотвращение инфицирования трансплантата печени;
-
Улучшение функции печени перед трансплантацией;
-
Выведение пациента из Листа ожидания ОТП.
Улучшение функции печени оценивается по клиническим показателям, а также по шкалам Child-Pugh (см. Приложение Г) и MELD (для подсчета этого индекса можно использовать любой интернет-ресурс, например, https://www.mdcalc.com/meldna-meld-na-score- liver-cirrhosis). Улучшение оценки MELD наблюдается у 60% больных с декомпенсированным ЦП, завершивших курс ПВТ. Это улучшение тем более вероятно и тем сильнее выражено, чем ниже оценка MELD до начала терапии.
До 25-30% больных с декомпенсированным ЦП могут иметь стойкое улучшение (компенсацию) ЦП, что позволяет вывести их из Листа ожидания ОТП. Выживаемость таких пациентов на протяжении 3-х лет не ниже, чем в группе реципиентов печени, которым была проведена ОТП, сопоставимых по исходной MELD [118,119,158-162].
-
Больным с декомпенсированным циррозом в исходе ХВГС (Child-Pugh В или С) без ГЦК, ожидающим ОТП, рекомендуется назначать ПВТ, если MELD <20. ПВТ рекомендуется начинать как можно быстрее, чтобы завершить курс и оценить ответ до трансплантации [165,166].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Комментарии: для ПВТ пациентов с декомпенсированным ЦП строго противопоказано использование препаратов, ингибирующих NS3/4.
-
Больным с декомпенсированным ЦП в исходе ХВГС (Child-Pugh В или С) без ГЦК, ожидающим трансплантацию печени, с MELD ≥20 рекомендуется провести ОТП, не назначая ПВТ. ПВТ ХВГС рекомендуется провести после трансплантации [165,166].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
-
Больным с декомпенсированным ЦП в исходе ХВГС (Child-Pugh В или С) без ГЦК, ожидающие ОТП, с MELD ≥20 могут начать лечение до ОТП, если предполагаемое время ожидания органа превышает 6 месяцев [165,166].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
12.2 Противовирусная терапия инфекции, вызванной вирусом гепатита С, у реципиентов печени
-
ПВТ инфекции трансплантата, вызванной ВГС, рекомендуется проводить всем реципиентам, у которых выявляется РНК ВГС в крови, насколько это возможно по состоянию пациента [176,177].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: частота УВО у реципиентов печени с компенсированной болезнью трансплантата, получивших запланированный курс ПВТ, составляет более 95%. УВО ассоциируется с замедлением прогрессирования фиброза и улучшением выживаемости трансплантата и реципиентов.
12.3 Противовирусная терапия ХВГС у реципиентов печени и других солидных органов от донора с антителами к вирусу гепатита С
В настоящее время в Российской Федерации Трансплантация органов от анти-HCV-позитивных доноров не разрешена. Международные клинические рекомендации подразумевают ведение пациентов в случае трансплантации солидных органов от доноров с ВГС-виремией [1,46].
13. Беременные
Беременность, по-видимому, не оказывает негативного влияния на течение ХВГС. Активность АЛТ в сыворотке крови снижается в течение I и III триместров беременности и повышаются после родов. Уровень РНК ВГС повышается в течение I и III триместров, достигая пика в течение III триместра, и снижается после родоразрешения. Эти события, вероятно, обусловлены иммуносупрессивными эффектами беременности и увеличением объема материнской плазмы [191,192]. Передача ВГС от матери ребенку встречается с общей частотой от 5% до 15% [193,194]. Убедительных данных о негативном влиянии ВГС на развитие плода и исход беременности нет. Есть отдельные сообщения о влиянии ЦП на течение беременности и ее исход. Так, беременные женщины с ЦП подвергаются повышенному риску неблагоприятных исходов для матери (например, преэклампсия, геморрагические осложнения и смерть) и для плода (например, преждевременные роды, низкая масса тела при рождении и неонатальная смерть). Женщины с ЦП в исходе ХВГС должны быть проинформированы об этих возможных осложнениях [195,196].
-
Женщинам репродуктивного возраста рекомендуется ПВТ ХВГС до планирования беременности, с тем чтобы снизить риск передачи ВГС будущему ребенку [197].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
-
Для выявления ХВГС рекомендуется проводить обследование беременных на anti-HCV крови (Определение суммарных антител классов M и G (anti-HCV IgG и anti-HCV IgM) к вирусу гепатита C (Hepatitis C virus) в крови) в I (при постановке на учет по беременности) и в III триместрах беременности [198].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Не рекомендуется проводить ПВТ ПППД во время беременности из-за отсутствия в настоящее время достаточных данных о безопасности и эффективности ПППД [199, 200].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: на сегодня не существует крупномасштабных клинических испытаний, оценивающих безопасность ПППД при беременности. Специальные исследования ПВТ СОФ** и ЛЕД+СОФ во время беременности продемонстрировали хорошую безопасность для плода. Данных об использовании пангенотипных схем во время беременности в настоящее время нет.
-
Женщинам детородного возраста, получающим ПВТ ХВГС с РБВ**, не рекомендуется беременность во время приема ПВТ и в течение не менее 6 месяцев после прекращения ПВТ [201,202].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
-
Мужчинам, получающим ПВТ ХВГС с РБВ**, не рекомендуется беременность их половых партнерш во время приема ПВТ и в течение не менее 6 месяцев после прекращения ПВТ [201,202].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: РБВ** обладает тератогенным свойством, то есть может вызвать аномалии развития и гибель плода. Его не следует назначать беременным женщинам или женщинам детородного возраста, которые могут забеременеть во время лечения РБВ** или в течение 6 месяцев после прекращения РБВ**. Кроме того, следует помнить, что РБВ** аналогичным образом может вызывать врожденные дефекты у плода, в случае если мужчина получал РБВ**, когда женщина забеременела от него. Таким образом, для избегания беременности во время лечения РБВ** и в течение не менее 6 месяцев после этого лицам с детородным потенциалом крайне важно использовать по крайней мере 2 формы эффективной контрацепции. Консультирующему врачу необходимо задокументировать обсуждение потенциальных тератогенных эффектов РБВ** в медицинской карте пациента.
-
Женщинам с ХВГС не рекомендуется отмена грудного вскармливания, за исключением случаев повреждения сосков и кровотечения из этих повреждений [203,204].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии: грудное вскармливание не представляет риска для передачи ВГС от матери ребенку, поскольку частота инфицирования детей по результатам исследований сопоставима в группах на грудном вскармливании и на искусственном вскармливании. Однако в случае повреждения сосков и кровотечения из этих повреждений возникает риск инфицирования ребенка от матери с ХВГС вследствие передачи ВГС через кровь.
14. Пациенты с сопутствующими онкологическими заболеваниями
Известно, что лечение онкологических заболеваний может негативно влиять состояние печени у пациентов с ВГС-инфекцией. Противовирусная терапия может способствовать формированию более благоприятных условий для начала или продолжения химиотерапии, благодаря снижению риска прогрессирования заболевания печени [235].
-
Пациентам с ВГС и сопутствующими онкологическими заболеваниями, также может быть рекомендовано противовирусное лечение с применением ПППД в соответствии с общими рекомендациями, в том числе в сочетании (одновременно) со специфической химиотерапией, с учетом возможных межлекарственных взаимодействий [236]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Для пациентов с ХВГС специализированные реабилитационные мероприятия не разработаны.
Госпитализация
Организация оказания медицинской помощи
Медицинская помощь оказывается в форме:
-
экстренной медицинской помощи;
-
неотложной медицинской помощи;
-
плановой медицинской помощи.
1. Условия оказания медицинских услуг
Медицинская помощь оказывается в виде:
-
первичной медико-санитарной помощи;
-
скорой, в том числе скорой специализированной, медицинской помощи;
-
специализированной, в том числе высокотехнологичной, медицинской помощи.
Медицинская помощь взрослым больным с ХВГС может оказываться в следующих условиях:
-
амбулаторно (в условиях, не предусматривающих круглосуточное медицинское наблюдение и лечение);
-
в дневном стационаре (в условиях, предусматривающих медицинское наблюдение и лечение в дневное время, не требующих круглосуточного медицинского наблюдения и лечения);
-
стационарно (в условиях, обеспечивающих круглосуточное медицинское наблюдение и лечение).
Первичная медико-санитарная помощь пациентам оказывается в амбулаторных условиях и в условиях дневного стационара.
Первичная доврачебная медико-санитарная помощь в амбулаторных условиях осуществляется в фельдшерско-акушерских пунктах.
Первичная врачебная медико-санитарная помощь осуществляется врачом-терапевтом участковым, врачом общей практики (семейным врачом) в амбулаторных условиях.
Первичная специализированная медико-санитарная помощь осуществляется врачом- инфекционистом или врачом-гастроэнтерологом медицинской организации, оказывающим медицинскую помощь пациентам в амбулаторных условиях.
Специализированная, в том числе высокотехнологичная, медицинская помощь оказывается в условиях стационара врачами-инфекционистами и другими врачами- специалистами и включает в себя профилактику, диагностику, лечение заболеваний и состояний, требующих использования специальных методов и сложных медицинских технологий, а также медицинскую реабилитацию.
Лечение пациентов осуществляется в условиях круглосуточного или дневного стационара по направлению врача-терапевта участкового, врача общей практики (семейного врача), врача-инфекциониста, врача-гастроэнтеролога, медицинских работников, выявивших ХВГС.
Больные ХВГС должны находиться под наблюдением до достижения УВО12, а при наличии фиброза печени F3-4 по METAVIR пожизненно.
Показанием к экстренной госпитализации служит развитие острой печеночной недостаточности, в том числе печеночной энцефалопатии и острой печеночной недостаточности на фоне хронической.
Медицинская помощь пациентам ХВГС оказывается в соответствии с утвержденным стандартом специализированной медицинской помощи.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
1. Специфическая профилактика
Специфическая профилактика ХВГС в настоящее время не разработана.
-
Пациентам с ХВГС рекомендуется вакцинация против гепатита А и В для предотвращения инфицирования этими вирусами [1,183-186].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
2. Неспецифическая профилактика
-
Рекомендуется активное выявление источников инфекции (обследование лиц, подверженных повышенному риску инфицирования и/или имеющих особую эпидемиологическую значимость) для своевременного проведения ПВТ [31,32].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендуется профилактика искусственного механизма передачи (переливание крови только по жизненным показаниям, обоснованность инвазивных методов обследования, использование одноразового инструментария, строгое соблюдение режимов обработки медицинского инструментария и оборудования, использование защитных средств медработниками) для снижения риска распространения инфекции, вызванной ВГС [187-189].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
-
Рекомендуется ПВТ больных, инфицированных ВГС, направленная на полную эрадикацию возбудителя, для профилактики распространения инфекции [17,32,190].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
3. Диспансерное наблюдение
-
Пациентам с ХВГС, которым отложено проведение ПВТ, рекомендуется диспансерное наблюдение один раз в год с проведением комплексного клинико-лабораторного и инструментального обследования для динамического наблюдения [54,55,57,59-61,66,67] (см. также подразделы 2.3, 2.4):
-
Всем пациентам с ХВГС – анализ крови биохимический общетерапевтический, УЗИ органов брюшной полости (комплексное) и забрюшинного пространства, эластометрия печени (при ее недоступности могут использоваться некоммерческие расчетные показатели, основанные на результатах лабораторного обследования, например, расчет индексов APRI, FIB-4 (см. Приложение Г))
-
Всем пациентам с ХВГС с исходом в ЦП в дополнение к вышеперечисленному – общий (клинический) анализ крови развернутый, определение протромбинового (тромбопластинового) времени в крови или в плазме, ЭГДС.
-
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
-
Не рекомендуется диспансерное наблюдение пациентам с показаниями к безотлагательному началу ПВТ ХВГС [1,69] (см. подраздел 3.1).
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
-
Рекомендуется диспансерное наблюдение пациентам с выраженным и тяжелым фиброзом печени (F3-F4 по METAVIR), получившим ПВТ ХВГС, даже после достижения УВО12 в связи с продолжающимся риском развития ГЦК (контроль АФП крови и УЗИ органов брюшной полости (комплексное) каждые полгода) специалистами неинфекционного профиля (врачами-гастроэнтерологами, врачами общей практики (семейными врачами), врачами-терапевтами) [44,45,53] (см. подразделы 2.3, 2.4).
Уровень убедительности рекомендации B (уровень достоверности доказательств – 2)
-
Не рекомендуется диспансерное наблюдение пациентам без фиброза печени, со слабовыраженным и умеренным фиброзом печени (F0-F2 по METAVIR) после достижения УВО12 при отсутствии установленных факторов риска дальнейшего прогрессирования фиброза [46-48] (см. подраздел 2.3).
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: пациенты с anti-HCV, у которых отсутствует РНК ВГС после проведенной ПВТ ХВГС в течение 12 недель, считаются излечившимися от ХВГС и при отсутствии установленных факторов риска дальнейшего прогрессирования фиброза печени подлежат подлежат снятию с диспансерного наблюдения.
-
Рекомендуется выполнение неинвазивной диагностики стадии фиброза печени (эластометрия печени, при ее недоступности – сывороточные расчетные некоммерческие тесты APRI, FIB-4 (см. Приложение Г)) пациентам с ХВГС 1 раз в год для динамического наблюдения [54,55,57,66].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
-
Рекомендуется выполнение ЭГДС пациентам с ХВГС с исходом в ЦП для динамического наблюдения 1 раз в год [59-61,67].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
-
После излечения от ХВГС пациентам с ЦП или выраженным фиброзом печени (F3 по METAVIR) рекомендуется пожизненно проводить скрининговое обследование для раннего выявления ГЦК (УЗИ органов брюшной полости (комплексное) каждые 6 месяцев) [53].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: у данных пациентов сохраняется риск развития ГЦК, несмотря на элиминацию вируса из организма, поэтому им необходимо проведение профилактического обследования для ее раннего выявления.
На этапе диспансерного наблюдения:
-
Не рекомендуется использовать анализ anti-HCV пациентам, выздоровевшим от ХВГС вследствие ПВТ, для контроля реинфицирования ВГС [49-51].
Уровень убедительности рекомендаций С (уровень достоверности доказательств –5)
Комментарий: после успешной ПВТ anti-HCV сохраняются длительно в подавляющем большинстве случаев, поэтому этот анализ не может использоваться для определения реинфицирования у пациентов с опытом элиминации ВГС. Доля пациентов, у которых anti- HCV постепенно исчезают, очень мала, и срок этого исчезновения неизвестен.
-
Всем пациентам, получившим курс ПВТ ХВГС, рекомендуется определение РНК ВГС через 12 недель после окончания ПВТ для оценки ее эффективности (УВО12) [46-48] (см. Приложение Б).
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: отсутствие РНК ВГС через 12 недель после завершения ПВТ соответствует излечению от ХВГС, так как поздний рецидив возникает менее чем в 0,2% случаев [48].
-
После излечения от ХВГС пациентам с ЦП или выраженным фиброзом печени (F3 по METAVIR) рекомендуется пожизненное определение уровня АФП пациентам 1 раз в полгода для диагностики ГЦК [44,45].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарий: риск развития ГЦК на стадии ЦП составляет около 1-5% в год. Вероятность летального исхода в течение первого года после постановки диагноза у пациентов с ГЦК составляет 33%.
Информация
Источники и литература
-
Клинические рекомендации Национальной ассоциации специалистов по инфекционным болезням имени академика В. И. Покровского (НАСИБ)
- 1. EASL recommendations on treatment of hepatitis C: Final update of the series. J Hepatol 2020 Nov;73(5):1170-1218. 2. Dubuisson J, Cosset FL. Virology and cell biology of the hepatitis C virus life cycle: an update. J Hepatol. 2014;61(1 Suppl):3-13. 3. Sergio M Borgia, et al. Identification of a novel hepatitis c virus genotype from punjab, india: expanding classification of hepatitis c virus into 8 genotypes. J Infect Dis. 2018 Oct 20;218(11):1722-1729. 4. Дунаева, Н. В. Структурно-функциональная организация генома вируса гепатита С. Вопросы вирусологии. – 2006. – № 51 (2). – С. 10 – 14. 5. Irshad M, Gupta P, Irshad K. Immunopathogenesis of liver injury during hepatitis c virus infection. Viral Immunol. 2019;32(3):112-205. 6. Lingala S, Ghany MG. Natural history of hepatitis C. Gastroenterol Clin North Am. 2015;44(4):717-34. 7. Yamane, D. Liver injury and disease рathogenesis in chronic hepatitis C. Curr Top Microbiology Immunology 2013;369:263-288. 8. Семенов, А. В. Особенности популяционного состава CXCRS-положительных лимфоцитов периферической крови больных хроническим гепатитом С. Журнал микробиологии, эпидемиологии и иммунобиологии. – 2013. –№ 6. – С. 69 – 76. 9. Елезов, Д. С. Анализ популяций Т-хелперных клеток памяти, экспрессирующих хемокиновые рецепторы CXCR3 и CCR6, в периферической крови больных хроническим вирусным гепатитом С. Бюллетень экспериментальной биологии и медицины. – 2015. – № 160 10. (8). – С. 204 – 208.Lohr, H. F. HCV replication in mononuclear cells simulates anti-HCV-secreting B cells and reflects nonresponsiveness to interferon-alfa. J. Med. Virol. 1995;46(4):314-21. 11. Арсентьева, Н. А. Хемокиновые рецепторы CXCR3 и CCR6 и их лиганды в печени и крови больных хроническим вирусным гепатитом С. Бюллетень экспериментальной биологии и медицины. – 2015. – № 8. – С. 218 – 222. 12. Давидович, Н. В. Иммунный ответ при вирусном гепатите С: ведущая роль натуральных киллеров. Ж. «Вестник Северного (Арктического) федерального университета». – 2015. – №4. – C. 68 – 78. 13. Хронический вирусный гепатит. Под ред. В. В. Серова, З. Г. Апросиной. – М: Медицина. – 2002. – 384 с. 14. Дудина, К. Р. Факторы прогрессирующего течения хронического гепатита С. Ж. Лечащий врач. – 2013. – №10. – С. 36. 15. Сухорук, А. А. Цирроз печени как исход хронического гепатита С. Журнал инфектологии. – 2014. –№ 6(1). – С. 67 – 71. 16. Пименов Н.Н., Комарова С.В., Карандашова И.В., Цапкова Н.Н., Волчкова Е.В., Чуланов В.П. Гепатит С и его исходы в России: анализ заболеваемости, распространенности и смертности до начала программы элиминации инфекции. Инфекционные болезни, 2018, т.16, №3, с. 37-45 17. WHO Global hepatitis report, 2018 https://www.who.int/news-room/fact- sheets/detail/hepatitis-c Обращение к сайту в мае 2021. 18. Alter MJ. Epidemiology of hepatitis C virus infection. World J Gastroenterol. 2007;13(17):2436-41. 19. Terrault NA. Sexual activity as a risk factor for hepatitis C. Hepatology. 2002;36(5 Suppl 1):99-105. 20. Chan DP, Sun HY, Wong HT, Lee SS, Hung CC. Sexually acquired hepatitis C virus infection: a review. Int J Infect Dis. 2016;49:47-58. 21. Жданов, К. В. Вирусные гепатиты. СПб.: Фолиант. – 2011. – 304 с. 22. Wang LS, D'souza LS, Jacobson IM. Hepatitis C – a clinical review. J Med Virol. 2016;88(11):1844-55. 23. Kuna L, Jakab J, Smolic R, Wu GY, Smolic M. HCV Extrahepatic Manifestations. J Clin Transl Hepatol. 2019;7(2):172-182. 24. Ющук, Н. Д. Инфекционные болезни: национальное руководство – 2-е изд., переработанное и доп. М.: ГЭОТАР-Медиа, 2019. – 1104 с. 25. Майер, К. П. Гепатит и последствия гепатита. Практич. рук. Пер. с нем. – 2-е изд.// М: ГЭОТАР- МЕД, 2004. – С. 265, 467 – 479; 491 – 503. 26. Сухорук, А. А. Цирроз печени как исход хронического гепатита С. Журнал инфектологии. – 2014. – Т. 6, № 1. – С. 67 – 71. 27. Билалова, А. Р. Клинико-лабораторная характеристика хронических гепатитов и циррозов печени различной этиологии. Архивъ внутренней медицины. – 2015. – № 2(22). – С. 8 – 14. 28. Chevaliez S, Soulier A, Poiteau L, Bouvier-Alias M, Pawlotsky JM. Clinical utility of hepatitis C virus core antigen quantification in patients with chronic hepatitis C. J Clin Virol 2014;61:145–148. 29. Heidrich B, Pischke S, Helfritz FA, Mederacke I, Kirschner J, Schneider J, et al. Hepatitis C virus core antigen testing in liver and kidney transplant recipients. J Viral Hepat 2014;21:769–779. 30. Freiman JM, Tran TM, Schumacher SG, White LF, Ongarello S, Cohn J,et al. Hepatitis C core antigen testing for diagnosis of hepatitis C virusinfection: a systematic review and meta- analysis. Ann Intern Med 2016;165:345–355. 31. Håvard Midgard, Amanda Weir, et al. HCV epidemiology in high-risk groups and the risk of reinfection. J Hepatology 2016;65:33-45. 32. WHO. Global health sector strategy on viral hepatitis, 2016–2021. Available from: http://www.who.int/hepatitis/strategy2016-2021. 33. Arase Y, Ikeda K, Chayama K, Murashima N, Tsubota A, Suzuki Y, et al. Fluctuation patterns of HCV-RNA serum level in patients with chronic hepatitis C. J Gastroenterol 2000;35:221– 225. 34. Cividini A, Cerino A, Muzzi A, Furione M, Rebucci C, Segagni L, et al. Kinetics and significance of serum hepatitis C virus core antigen in patients with acute hepatitis C. J Clin Microbiol 2003;41:2144-46 35. Michael J. Zoratti, et al. Pangenotypic direct acting antivirals for the treatment of chronic hepatitis C virus infection: A systematic literature review and meta-analysis. E Clinical Medicine. 2020 Jan; 18: 100237. 36. Amir A. Qamar, Norman D. Grace, et al. Incidence, prevalence, and clinical significance of abnormal hematologic indices in compensated cirrhosis. Clinical gastroenterology and hepatology 2009;7:689-695. 37. Sheehan, Vivien A., et al. Hepatitis C and neutropenia. Current Opinion in Hematology 2014;21:58-63. 38. Weksler B B. Review article: the pathophysiology of thrombocytopenia in hepatitis C virus infection and chronic liver disease. Aliment Pharmacol Ther 2007: Nov;26 (Suppl 1):13-9. 39. Zohair Ahmed, Umair, et al. Liver function tests in identifying patients with liver disease. Clin Exp Gastroenterol. 2018;11:301-307. 40. Saxena, V. Safety and efficacy of sofosbuvir-containing regimens in hepatitis C- infected patients with impaired renal function. Liver Int. 2016;36:807-816. 41. Bhamidimarri, K. R. Safety, efficacy and tolerability of half-dose sofosbuvir plus simeprevir in treatment of hepatitis C in patients with end stage renal disease. J. Hepatol. 2015;63: 763- 765. 42. Uroš Karić, et al. FIB-4 and APRI scores for predicting severe fibrosis in chronic hepatitis C - a developing country's perspective in DAA era. J Infect Dev Ctries 2018; 12(3):178-182. 43. Michael F. Harrison. The Misunderstood Coagulopathy of Liver Disease: A Review for the Acute Setting. West J Emerg Med. 2018 Sep; 19(5): 863-871. 44. Gupta, S. Test characteristics of alpha-fetoprotein for detecting hepatocellular carcinoma in patients with hepatitis C. A systemic review and critical analysis. Med. 2003;139:46-50. 45. Di Bisceglie, A. M. Serum alpha-fetoprotein levels in patients with advanced hepatitis C: results from the HALT-C Trial. J. Hepatol. 2005;43:434- 441. 46. Deblka Bhattacharya, Andrew Aronsohn, Jennifer Price, Vincent Lo Re, the American Association for the Study of Liver Diseases-lnfectious Diseases Society of America HCV Guidance Panel, Hepatitis С Guidance 2023 Update: American Association for the Study of Liver Diseases - lnfectious Diseases Society of America Recommendations for Testing, Managing, and Treating Hepatitis С Virus lnfection, Clinical lnfectious Diseases, 2023; ciad319, https://doi.org/10.1093/cid/ciad319. 47. Treatment optimisation for hepatitis C in the era of combination direct-acting antiviral therapy: a systematic review and meta-analysis. Wellcome Open Research 2019, 4:132 Last updated: 13 Nov 2019. 48. Sarrazin C, Isakov V, Svarovskaia ES, Hedskog C, Martin R, Chodavarapu K, et al. Late relapse versus hepatitis C virus reinfection in patients with sustained virologic response after sofosbuvir-based therapies. Clin Infect Dis 2017;64:44-52. 49. Chevaliez S, Pawlotsky JM. Diagnosis and management of chronic viral hepatitis: antigens, antibodies and viral genomes. Best Pract Res Clin Gastroenterol 2008;22:1031–1048. 50. Kamili S, Drobeniuc J, Araujo AC, Hayden TM. Laboratory diagnostics for hepatitis C virus infection. Clin Infect Dis 2012;55:43-48.
Информация
Список сокращений
** – указывается в конце названия лекарственного препарата или комбинации лекарственных препаратов, означает их принадлежность к списку ЖНВЛП
# – указывается в начале названия лекарственного препарата или схемы лекарственных препаратов, применяющихся не по медицинской инструкции (off-label)
Anti-HCV – антитела к вирусу гепатита С
Anti-HBc – антитела к ядерному антигену вируса гепатита В
HBcAg – hepatitis B core antigen, ядерный антиген вируса гепатита В
HBsAg – hepatitis B surface antigen, поверхностный антиген вируса гепатита
ВHBV – hepatitis B virus, вирус гепатита В
HCVcAg – hepatitis C virus core antigen, ядерный антиген вируса гепатита
СHCV hepatitis C virus, вирус гепатита С
HIV – human immunogenicity virus, вирус иммунодефицита человека
MELD – model of end liver disease, расчетный индекс, характеристика тяжести терминальной стадии болезни печени
NS3/4A ингибиторы – противовирусные средства для лечения гепатита C, блокируют неструктурные белки NS3 и NS4A вируса гепатита С (J05AЕ Ингибиторы ВИЧ-протеаз)
NS5A ингибиторы – противовирусные средства для лечения гепатита C, блокируют неструктурный белок NS5A вируса гепатита С (J05AХ Другие противовирусные препараты)
АЛТ – аланинаминотрансфераза
АСТ – аспартатаминотрансфераза
АФП – альфа-фетопротеин
ВГВ – вирус гепатита В
ВГС – вирус гепатита С
ВЕЛ+СОФ** – велпатасвир+софосбувир**
ВН – вирусная нагрузка
ВИЧ – вирус иммунодефицита человека
ВРВ – варикозно расширенные вены
ГГТ – гамма-глутамилтрансфераза
ГЛЕ+ПИБ** – глекапревир+пибрентасвир**
ГРА+ЭЛБ** – гразопревир+элбасвир**
ГТ – генотип
ГЦК – гепатоцеллюлярная карцинома
ДАК** – даклатасвир**
ДНК – дезоксирибонуклеиновая кислота
ЖНВЛП – жизненно необходимые и важнейшие лекарственные препараты
ЛЕД+СОФ – ледипасвир+софосбувир
МЕ – международная единица
МКБ 10 – Международная классификация болезней 10-го пересмотра
НРВ** – нарлапревир**
НРВ**/р**– нарлапревир**, бустированный ритонавиром**
ОТП – ортотопическая трансплантация печени
ПегИФН** – Пэгинтерферон альфа 2b **
ПППД – противовирусные препараты прямого действия
ПТИ – протромбиновый индекс
РБВ** – рибавирин**
РНК – рибонуклеиновая кислота
р/д – раз в день
СКФ – скорость клубочковой фильтрации
СОФ** – софосбувир**
таб. – таблетка
УЗИ – ультразвуковое исследование
УВО – устойчивый вирусологический ответ
УВО12 – устойчивый вирусологический ответ через 12 недель после окончания терапии
ХБП – хроническая болезнь почек
ХВГС – хронический вирусный гепатит
ЦП – цирроз печени
Термины и определения
Вирусная нагрузка (ВН) – количество вирусной РНК в крови, измеряется в МЕ/мл.
Генотипы вируса гепатита С – варианты вируса гепатита С, разделяются на основании различий в нуклеотидной последовательности определенных областей генома вируса. В клинической практике имеют большое значение для подбора схемы противовирусного лечения, в случае если применяются генотип-специфические препараты.
Гепатит – воспаление в ткани печени, характеризуется наличием некровоспалительных изменений в биоптате печени.
Гепатоцеллюлярная карцинома – злокачественное образование печени, является одним из возможных неблагоприятных исходов хронического вирусного гепатита С, возникает, как правило, на фоне сформированного цирроза печени.
Коинфекция – инфицирование двумя и более инфекционными агентами. В случае хронического вирусного гепатита С обычно применяется в отношении сочетания с вирусами гепатита В, Д и ВИЧ.
Пангенотипный – характеристика лекарственного средства или группы средств, эффективных в отношении всех наиболее распространенных генотипов вируса гепатита С.
Устойчивый вирусологический ответ (УВО) – отсутствие в крови РНК вируса гепатита С через 12 после окончания терапии.
Фиброз печени – процесс замещения паренхиматозной ткани печени соединительной тканью, является универсальной реакцией организма на хроническое повреждение.
Цирроз печени – терминальная стадия хронического заболевания печени, характеризуется замещением паренхимы соединительной тканью и нарушением архитектуры органа. На ранних этапах при сохраненной функции печени называется компенсированным, при потере функции – декомпенсированным.
APRI – некоммерческий расчетный индекс фиброза печени, метод неинвазивной диагностики. Может использоваться в качестве альтернативного при недоступности эластометрии печени.
FIB-4 – некоммерческий расчетный индекс фиброза печени, метод неинвазивной диагностики. Может использоваться в качестве альтернативного при недоступности эластометрии печени.
METAVIR – популярная система оценки степени воспаления (от А0 до А3) и фиброза (от F0 по F4) в ткани печени. Применяется как для характеристики биоптата печени, так и для оценки фиброза печени неинвазивными методами (например, при эластометрии печени или расчете индекса фиброза) (см. Приложение Г).
Критерии оценки качества медицинской помощи
|
|
Критерии качества |
Оценка выполнения (да/нет) |
|
Этап скрининга |
||
|
1. |
Выполнено определение суммарных антител классов M и G (anti-HCV IgG и anti-HCV IgM) к вирусу гепатита C (Hepatitis C virus) в крови |
Да/нет |
|
2. |
Выполнено определение РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР, качественное исследование или определение Core-антигена вируса гепатита C (Hepatitis C virus) в крови |
Да/нет |
|
Этап постановки диагноза |
||
|
3. |
Выполнено определение генотипа вируса гепатита C (Hepatitis C virus), пациентам с ХВГС для планирования генотип-специфичной схемы противовирусной терапии |
Да/нет |
|
4. |
Выполнен общий (клинический) анализ крови развернутый |
Да/нет |
|
5. |
Выполнен анализ крови биохимический общетерапевтический (определение активности аланинаминотрансферазы, аспартатаминотрансферазы, исследование уровня общего билирубина, исследование уровня креатинина в крови) |
Да/нет |
|
6. |
Пациентам с ЦП выполнено определение протромбинового (тромбопластинового) времени в крови или в плазме |
Да/нет |
|
7. |
Пациентам с выраженным и тяжелым фиброзом печени (F3-F4 по METAVIR) определен уровень АФП в сыворотке крови |
Да/нет |
|
8. |
Выполнено УЗИ органов брюшной полости (комплексное) и забрюшинного пространства |
Да/нет |
|
9. |
Выполнена неинвазивная диагностика фиброза оценка фиброза печени |
Да/нет |
|
10. |
Выполнена эзофагогастродуоденоскопия (пациентам с ЦП) |
Да/нет |
|
11. |
Выполнен определение содержания ревматоидного фактора в крови |
Да/нет |
|
Этап ПВТ |
||
|
1. |
В случае применения РБВ** выполнен общий (клинический) анализ крови развернутый каждые 2-4 недели ПВТ |
Да/нет |
|
Этап диспансерного наблюдения |
||
|
1. |
Выполнено определение РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР, качественное исследование исходно и через 12 недель после окончания терапии |
Да/нет |
|
2. |
Пациентам с выраженным и тяжелым фиброзом печени (F3-F4 по METAVIR) определен уровень АФП 1 раз в полгода |
Да/нет |
|
3. |
Выполнена неинвазивная диагностика стадии фиброза печени (эластометрия печени, при ее недоступности – сывороточные расчетные некоммерческие тесты APRI, FIB-4) 1 раз в год |
Да/нет |
|
4. |
Пациентам с выраженным и тяжелым фиброзом печени (F3-F4 по METAVIR) выполнено УЗИ органов брюшной полости (комплексное) 1 раз в полгода |
Да/нет |
|
5. |
Пациентам с ЦП выполнена эзофагогастродуоденоскопия 1 раз в год |
Да/нет |
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
-
Богомолов Павел Олегович – к.м.н., руководитель отделения гепатологии ГБУЗ МО МОНИКИ им. М.Ф. Владимирского.
-
Волчкова Елена Васильевна – д.м.н., профессор, заведующая кафедрой инфекционных болезней Института клинической медицины им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет).
-
Гусев Денис Александрович – д.м.н., профессор, главный врач СПб ГБУЗ «Клиническая инфекционная больница имени С.П. Боткина», заведующий кафедрой инфекционных болезней Института медицинского образования НМИЦ им В.А. Алмазова
-
Дмитриев Александр Сергеевич – к.м.н., руководитель Центра эпидемически значимых инфекционных болезней ФГБУ "НМИЦ ФПИ" Минздрава России, врач- инфекционист.
-
Жаркова Мария Сергеевна – к.м.н., заведующая отделением гепатологии Клиники пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В.Х. Василенко ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет).
-
Жданов Константин Валерьевич – д.м.н., профессор, член-корр. РАН, директор научно-клинического центра ФГБУ «Федеральный научно-клинический центр инфекционных болезней Федерального медико-биологического агентства».
-
Ивашкин Владимир Трофимович – д.м.н., профессор, академик РАН, Президент Российской гастроэнтерологической ассоциации и Российского общества по изучению печени, заведующий кафедрой пропедевтики внутренних болезней, гастроэнтерологии и гепатологии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), заслуженный врач РФ, заслуженный деятель науки РФ.
-
Козлов Константин Вадимович – д.м.н., начальник кафедры инфекционных болезней (с курсом медицинской паразитологии и тропических заболеваний) ФГБВОУ ВО «Военно-медицинская академия им. С. М. Кирова» Минобороны России
-
Кравченко Ирина Эдуардовна – д.м.н., профессор кафедры инфекционных болезней ФГБОУ ВО Казанский ГМУ Минздрава России.
-
Маевская Марина Викторовна – д.м.н., профессор ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), консультант ЛДО3 УКБ 2.
-
Мамонова Нина Алексеевна – научный сотрудник лаборатории генетических технологий и трансляционных исследований ФГБУ «НМИЦ ФПИ» Минздрава России.
-
Масленников Роман Вячеславович – к.м.н., ассистент кафедры пропедевтики внутренних болезней, гастроэнтерологии и гепатологии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет).
-
Михайлов Михаил Иванович – профессор, академик РАН, главный научный сотрудник лаборатории молекулярной эпидемиологии вирусных гепатитов ФБУН ЦНИИ Эпидемиологии Роспотребнадзор
-
Новак Ксения Егоровна – к.м.н., доцент, доцент кафедры инфекционных болезней взрослых и эпидемиологии ФГБОУ ВО СПбГПМУ Минздрава России.
-
Никитин Игорь Геннадиевич – д.м.н., профессор, заведующий кафедрой госпитальной терапии №2 лечебного факультета ФГАУ ВО «Российский национальный исследовательский университет им. Н.И. Пирогова» Минздрава России
-
Сюткин Владимир Евгеньевич – д.м.н., ведущий научный сотрудник отделения трансплантации печени ГБУЗ «НИИ скорой помощи им. Н.В. Склифосовского ДЗМ», профессор кафедры хирургии с курсами онкохирургии, эндоскопии, хирургической патологии, клинической трансплантологии и органного донорства ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России.
-
Тихонов Игорь Николаевич – ассистент кафедры пропедевтики, гастроэнтерологии и гепатологии ИКМ Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), врач-гастроэнтеролог отделения гепатологии УКБ 2.
-
Чуланов Владимир Петрович – д.м.н., профессор, главный внештатный специалист по инфекционным болезням Минздрава России, заместитель директора по научной работе и инновационному развитию ФГБУ «НМИЦ ФПИ» Минздрава России.
-
Шептулин Аркадий Александрович – д.м.н., профессор кафедры пропедевтики внутренних болезней гастроэнтерологии и гепатологии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет).
-
Широкова Елена Николаевна – д.м.н., профессор кафедры пропедевтики внутренних болезней ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет).
-
Эсауленко Елена Владимировна – д.м.н., профессор, заведующая кафедрой инфекционных болезней взрослых и эпидемиологии ФГБОУ ВО СПбГПМУ Минздрава России.
Приложение А2. Методология разработки клинических рекомендаций
Предлагаемые рекомендации имеют своей целью довести до практических врачей современные представления об этиологии и патогенезе ХВГС, а также ознакомить их с применяющимся в настоящее время алгоритмами ее диагностики и лечения.
Целевая аудитория данных клинических рекомендации:
-
Врачи-инфекционисты;
-
Врачи-гастроэнтерологи;
-
Врачи общей практики (семейные врачи);
-
Врачи-терапевты.
Табл. П1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД |
Расшифровка |
|
1 |
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2 |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3 |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4 |
Не сравнительные исследования, описание клинического случая |
|
5 |
Имеется лишь обоснование механизма действия или мнение экспертов |
Табл. П2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
|
УДД |
Расшифровка |
|
1. |
Систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2. |
Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3. |
Нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4. |
Несравнительные исследования, описание клинического случая или серии случаев, исследование «случай-контроль» |
|
5. |
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение эксперта |
Табл. П3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР |
Расшифровка |
|
А |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
|
В |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
|
С |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений и/или замечаний к ранее утверждённым клиническим рекомендациям, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учетом следующих нормативно-правовых документов:
-
Федеральный закон от 17 сентября 1998г. № 157-ФЗ «Об иммунопрофилактике инфекционных болезней».
-
Федеральный закон Российской Федерации от 29 ноября 2010г. № 326-ФЗ «Об обязательном медицинском страховании в Российской Федерации».
-
Федеральный закон от 21 ноября 2011г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации».
-
Приказ Минздравсоцразвития РФ от 9 августа 2005г. № 494 «О порядке применения лекарственных средств у больных по жизненным показаниям».
-
Приказ Минздрава России от 13.10.2017 № 804н. «Об утверждении номенклатуры медицинских услуг».
-
Приказ Минздрава России от 02.05.2023 № 205н «Об утверждении Номенклатуры должностей медицинских работников и фармацевтических работников»
-
Приказ Минздрава России от 07 октября 2015г. № 700н «О номенклатуре специальностей специалистов, имеющих высшее медицинское и фармацевтическое образование».
-
Приказ Минтруда России от 26.07.2024 № 374н «Об утверждении классификаций и критериев, используемых при осуществлении медико-социальной экспертизы граждан федеральными учреждениями медико-социальной экспертизы».
-
Федеральный закон от 30.03.1999 52-ФЗ «О санитарно-эпидемиологическом благополучии населения»
-
Постановление Главного государственного санитарного врача РФ от 25.06.2025 № 12 «О внесении изменений в санитарные правила и нормы СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней", утвержденные постановлением Главного государственного санитарного врача Российской Федерации от 28.01.2021 N 4»
-
Приказ Министерства здравоохранения Российской Федерации от 5 августа 2003г № 330 «О мерах по совершенствованию лечебного питания в лечебно-профилактических учреждениях Российской Федерации».
-
Приказ Министерства здравоохранения Российской Федерации от 21 июня 2013 г. № 395н «Об утверждении норм лечебного питания».
-
Приказ Министерства здравоохранения Российской Федерации от 23 сентября 2020г. № 1008н «Об утверждении порядка обеспечения пациентов лечебным питанием».
Примеры формулировки диагноза
Пример 1
Перенесенный вирусный гепатит С (ВГС): реконвалесценция в результате самоизлечения (РНК ВГС отрицательная от [дата], anti-ВГС положительные от [дата]) Снят/не снят с учёта (выбрать вариант) [дата].
Пример 2
Перенесенный вирусный гепатит С (ВГС): реконвалесценция в результате противовирусной терапии в период [указать сроки начала и окончания противовирусной терапии], достигнут устойчивый вирусологический ответ (РНК ВГС отрицательная от [дата]), anti-ВГС положительные от [дата]) Снят/не снят с учёта (выбрать вариант) [дата].
Контингенты, подлежащие обязательному одновременному обследованию на наличие anti-HCV и РНК ВГС
Таблица 1
|
N |
Контингенты населения |
Период обследования |
|
1 |
Доноры крови (ее компонентов), органов и тканей, спермы |
При каждой донации или каждом взятии донорского материала |
|
2 |
Дети в возрасте до 12 месяцев, рожденные от инфицированных вирусом гепатита С матерей |
В возрасте 4-6 месяцев |
|
3 |
Дети, рожденные от ВИЧ-инфицированных матерей |
В возрасте 4-6 месяцев |
|
4 |
Лица с иммунодефицитом (больные онкологическими заболеваниями, пациенты на гемодиализе, пациенты, находящиеся на лечении иммунодепрессантами, и другие) |
Согласно приложению 17 к Санитарным правилам СП 3.3686-21 |
|
5 |
Лица, имеющие заболевание печени неясной этиологии |
В процессе первичного клинико-лабораторного обследования |
|
6 |
Пациенты отделений гемодиализа, гематологии и трансплантации, пребывающие в медицинской организации более 1 месяца |
Не реже 1 раза в 3 месяца |
|
7 |
Контактные в очагах ОГС |
При выявлении очага и далее однократно через 30 календарных дней |
|
8 |
Контактные в очагах ХГС |
При выявлении очага |
|
* альтернативным тестом РНК ВГС может быть тест ВГС core антиген. Также допустимо для этой категории пациентов выполнять скрининговый тест, одновременно выявляющим core ВГС антиген и антитела к ВГС. |
||
Схемы ПВТ ХВГС для пациентов без предшествующего опыта ПВТ и без цирроза печени в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).
Таблица 2.
|
|
Пангенотипные схемы лечения |
Генотип-специфичные схемы лечения |
|||||
|
ГТ |
ВЕЛ+СОФ** |
ГЛЕ+ПИБ**
|
ДАК** + СОФ** |
ГРА+ЭЛБ** |
ДАК** + НРВ** + #р** |
ЛЕД+СОФ |
НРВ** + #р** + СОФ** |
|
1а |
12 нед. |
8 нед. |
12 нед. |
12/16 нед.а |
- |
8 нед. |
12 нед. #8 нед.в |
|
1b |
8/12 нед.б |
12 нед. |
|||||
|
2 |
- |
- |
- |
- |
|||
|
3 |
12 нед + СОФ** |
- |
- |
- |
|||
|
4 |
12/16 нед.а |
- |
12 нед. |
- |
|||
Примечания:
ВЕЛ+СОФ** – велпатасвир+софосбувир** (100/400 мг) 1 таб. 1р/д или;
ГЛЕ+ПИБ** – глекапревир+пибрентасвир** (3 таб. одновременно, по 100/40 мг каждая) 1р/д;
ДАК** + СОФ** – даклатасвир** 60 мг 1 таб. 1р/д + софосбувир** 400 мг 1 таб. 1р/д;
ГРА+ЭЛБ** – гразопревир+элбасвир** 100/50 мг 1 таб. 1р/д или ГРА+ЭЛБ** 100/50 мг 1 таб. 1р/д + #РБВ**[93,207, 223, 226, 237, 244, 254];
ДАК** + НРВ** + #р** – даклатасвир** 60 мг 1р/д + нарлапревир** 200 мг 1 р/д (2 таб. одновременно, по 100 мг каждая) + #ритонавир** 100 мг 1р/д;
ЛЕД+СОФ – ледипасвир+софосбувир 90/400 мг 1 таб. 1р/д;
НРВ** + #р** + СОФ** – нарлапревир** 200 мг 1 р/д (2 таб. одновременно, по 100 мг каждая) + #ритонавир** 100 мг 1р/д + софосбувир** 400 мг 1 таб. 1р/д;
Комментарии ко всем схемам:
а - при ВН не более 800 000 МЕ/мл срок лечения 12 недель; при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A следует рассмотреть 16-недельный курс совместно с #РБВ**(в дозе 1000 мг для пациентов весом <75 кг и 1200 мг для пациентов весом ≥75 кг) [167];
б - у пациентов со слабовыраженным фиброзом (F0-2) #8 недель, с фиброзом F3-F4 по METAVIR – 12 недель.
в - у пациентов со слабовыраженным фиброзом (F0-2) и ВН менее 1 000 000 МЕ/мл можно рассмотреть длительность 8 недель по решению врачебной комиссии.
Схемы ПВТ ХВГС для пациентов с компенсированным циррозом печени без предшествующего опыта ПВТ в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).
Таблица 3.
|
|
Пангенотипные схемы лечения |
Генотип-специфичные схемы лечения |
|||
|
ГТ |
ВЕЛ+СОФ** |
ГЛЕ+ПИБ** |
ДАК** + СОФ** |
ГРА+ЭЛБ** |
ЛЕД+СОФ |
|
1а |
12 нед.б |
8 нед. |
12 нед. |
12/16 нед.а |
12 нед + #РБВ** 24 нед. без РБВ** |
|
1b |
12 нед. |
||||
|
2 |
- |
- |
|||
|
3 |
24 нед +/- #РБВ** |
12 нед + CОФ**б |
24 нед + #РБВв |
||
|
4 |
12 нед. |
12/16 нед.а |
12 нед + #РБВ** 24 нед. без РБВ** |
||
Примечания:
ВЕЛ+СОФ** – велпатасвир+софосбувир** (100/400 мг) 1 таб. 1р/д или ВЕЛ+СОФ** (100/400 мг) 1 таб. 1р/д + #РБВ** 1000 мг/сут, если масса тела <75 кг и 1200 мг/сут, если масса тела ≥75 кг [76,78,79, 237, 247, 254, 260] ;
ГЛЕ+ПИБ** – глекапревир+пибрентасвир** (3 таб. одновременно, по 100/40 мг каждая) 1р/д [85];
ДАК**+СОФ** – даклатасвир** 60 мг 1 таб. 1р/д + софосбувир** 400 мг 1 таб. 1р/д или ДАК**+СОФ** даклатасвир** 60 мг 1 таб. 1р/д + софосбувир** 400 мг 1 таб. 1р/д + #РБВ**1000 мг/сут, если масса тела <75 кг и 1200 мг/сут, если масса тела ≥75 кг [105,107,208,218-220, 237, 246, 247, 254];
ГРА+ЭЛБ** – гразопревир+элбасвир** 100/50 мг 1 таб. 1р/д или ГРА+ЭЛБ**100/50 мг 1 таб. 1р/д + #РБВ** 1000 мг/сут, если масса тела <75 кг и 1200 мг/сут, если масса тела ≥75 кг и ГРА+ЭЛБ** 100/50 мг 1 таб. 1р/д + #РБВ** 1000 мг/сут, если масса тела <75 кг и 1200 мг/сут, если масса тела ≥75 кг + CОФ**400 мг 1 таб. 1р/д [93,207, 221-224, 237-240, 244, 254, 255]
ЛЕД+СОФ – ледипасвир+софосбувир 90/400 мг 1 таб. 1р/д или ЛЕД+СОФ 90/400 мг 1 таб. 1р/д + #РБВ** 1000 мг/сут, если масса тела <75 кг и 1200 мг/сут, если масса тела ≥75 кг [89-92,213- 217, 248, 254, 260, 261]
а - при ВН не более 800 000 МЕ/мл срок лечения 12 недель; 16-недельный курс совместно с #РБВ** следует рассмотреть при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A;
б - для ГТ 3 можно рассмотреть добавление #РБВ**;
в - в случае недоступности иных схем лечения.
Схемы ПВТ ХВГС для пациентов, не ответивших на предшествующую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**, без цирроза печени в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).
Таблица 4.
|
|
Пангенотипные схемы лечения |
Генотип-специфичные схемы лечения |
|||
|
ГТ |
ВЕЛ+СОФ** |
ГЛЕ+ПИБ** |
ДАК** + СОФ** |
ГРА+ЭЛБ** |
ЛЕД+СОФ |
|
1а |
12 нед. |
8 нед. |
12 нед. |
12/16 нед.а |
12 недель |
|
1b |
12 нед. |
||||
|
2 |
|
8 нед. |
- |
- |
|
|
3 |
16 нед. |
24 нед. +/- #РБВ** |
- |
24 нед + #РБВ** |
|
|
4 |
8 нед. |
12 нед. |
12/16 нед.а |
12 недель |
|
Примечания:
ВЕЛ+СОФ** – велпатасвир+софосбувир** (100/400 мг) 1 таб. 1р/д;
ГЛЕ+ПИБ** – глекапревир+пибрентасвир** (3 таб. одновременно, по 100/40 мг каждая) 1р/д;
ДАК** + СОФ** – даклатасвир** 60 мг 1 таб. 1р/д + софосбувир** 400 мг 1 таб. 1р/д;
ДАК** 60 мг 1 таб. 1р/д + СОФ** 400 мг 1 таб. 1р/д + #РБВ 1000 мг/сут, если масса тела <75 кг и 1200 мг/сут, если масса тела ≥75 кг [106,107,210,211,218, 237,249,250, 254]
ГРА+ЭЛБ** – гразопревир+элбасвир** 100/50 мг 1 таб. 1р/д или ГРА+ЭЛБ** 100/50 мг 1 таб. 1р/д + #РБВ** 1000 мг/сут, если масса тела <75 кг и 1200 мг/сут, если масса тела ≥75 кг [93,207, 223, 226, 237, 254, 255]
ЛЕД+СОФ – ледипасвир+софосбувир 90/400 мг 1 таб. 1р/д или ЛЕД+СОФ100/50 мг 1 таб. 1р/д + #РБВ**1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг). Курс лечения 24 нед. [89-92,213- 217, 251, 252, 254, 261, 262]
Комментарии ко всем схемам:
а - при ВН не более 800 000 МЕ/мл срок лечения 12 недель; при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A следует рассмотреть 16-недельный курс совместно с #РБВ**(в дозе 1000 мг для пациентов весом <75 кг и 1200 мг для пациентов весом ≥75 кг) [167];;
Схемы ПВТ ХВГС для пациентов, не ответивших на предшествующую терапию, ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**, с компенсированным циррозом печени в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).
Таблица 5
|
|
Пангенотипные схемы лечения |
Генотип-специфичные схемы лечения |
|||
|
|
ВЕЛ+СОФ** |
ГЛЕ+ПИБ** |
ДАК** + СОФ** |
ГРА+ЭЛБ** |
ЛЕД+СОФ |
|
1а |
12 нед.б |
12 нед. |
12 нед. |
12/16 нед.а |
12 нед + #РБВ** 24 нед. без РБВ** |
|
1b |
12 нед. |
||||
|
2 |
- |
- |
|||
|
3 |
16 нед. |
24 нед. +/- #РБВ** |
- |
24 нед + #РБВ**в |
|
|
4 |
12 нед. |
12 нед. |
12/16 неда |
12 нед + #РБВ** 24 нед. без РБВ** |
|
Примечания:
ВЕЛ+СОФ** – велпатасвир+софосбувир** (100/400 мг) 1 таб. 1р/д или ВЕЛ+СОФ** (100/400 мг) 1 таб. 1р/д + #РБВ** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг [167];
ГЛЕ+ПИБ** – глекапревир+пибрентасвир** (3 таб. одновременно, по 100/40 мг каждая) 1р/д [85];
ДАК** + СОФ** – даклатасвир** 60 мг 1 таб. 1р/д + софосбувир** 400 мг 1 таб. 1р/д или ДАК** 60 мг 1 таб. 1р/д + СОФ** 400 мг 1 таб. 1р/д + #РБВ** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг [105,107,208,218-220];
ГРА+ЭЛБ** – гразопревир+элбасвир** 100/50 мг 1 таб. 1р/д или ГРА+ЭЛБ** 100/50 мг 1 таб. 1р/д + #РБВ** 1000 мг/сут, если масса тела <75 кг и 1200 мг/сут, если масса тела ≥75 кг [93,207,223,226, 237, 244, 254, 258, 259]
ЛЕД+СОФ – ледипасвир+софосбувир 90/400 мг 1 таб. 1р/д или ЛЕД+СОФ 90/400 мг 1 таб. 1р/д + #РБВ****1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг. Курс лечения при генотипе 1 и 4 – 12 нед, при генотипе 3 – 24нед. [90-92,213- 217, 251, 252, 254, 261, 262]
Комментарии:
а - при ВН не более 800 000 МЕ/мл срок лечения 12 недель; при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A следует рассмотреть 16-недельный курс совместно с #РБВ**( 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) [167];
б - для ГТ 3 можно рассмотреть добавление #РБВ**;
Схемы противовирусной терапии хронического вирусного гепатита С с учетом генотипа, опыта предшествующей терапии, наличия цирроза печени (названия лекарственных средств указаны в алфавитном порядке)
Таблица 6
|
Пациентам, инфицированным ВГС ГТ 1 |
|
Схема 1 Велпатасвир+софосбувир** ВЕЛ+СОФ** 1 таб. (100/400 мг) 1 р/д. 12 недель – для пациентов без ЦП или с компенсированным ЦП, в том числе ранее получавших лечение ПегИФН** + РБВ** ± СОФ** и/или препаратами, ингибирующими NS3/4А, и пациентов с рецидивом ХГС после трансплантации печени и солидных органов. 24 недели – с добавлением #РБВ** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг для пациентов без ЦП или с компенсированным ЦП печени, ранее получавшим лечение режимом, включающим препараты, ингибирующие NS5A, в том числе с рецидивом ХГС после трансплантации печени и солидных органов [76,78,79,167]. Схема 2 Глекапревир+пибрентасвир** ГЛЕ+ПИБ** (100/40 мг) 3 таб. одновременно 1 р/д. 8 недель – для пациентов без ЦП или с ЦП, ранее не получавших лечение; для пациентов без ЦП, не ответивших на предыдущую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**; 12 недель – для пациентов с ЦП, не ответивших на предыдущую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**; для пациентов без ЦП или с ЦП с предшествующим опытом терапии препаратами, ингибирующими NS3/4A, без предшествующей терапии препаратами, ингибирующими NS5A; для пациентов с рецидивом ХГС после трансплантации печени или почки; 16 недель – для пациентов без ЦП или с ЦП с предшествующим опытом терапии препаратами, ингибирующими NS5A, без предшествующей терапии препаратами, ингибирующими NS3/4A, включая пациентов с рецидивом ХГС после трансплантации печени или почки. Схема 3 Гразопревир+элбасвир** ГРА+ЭЛБ** (100/50 мг) 1 таб. 1 р/д. 8 недель – для пациентов, ранее не получавших лечение, инфицированных субтипом 1b, без выраженного фиброза печени (F0-F2); 12 недель – для пациентов с субтипами 1а (с исходной концентрацией РНК ВГС менее 800 000 МЕ/мл) или 1b без ЦП или компенсированным ЦП; 16 недель – с добавлением #РБВ** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг для пациентов, инфицированных субтипом 1а, при исходной концентрации РНК ВГС более 800 000 МЕ/мл и/или при наличии полиморфизма NS5A.[93,207, 221-224] Схема 4 Даклатасвир** + нарлапревир** + #ритонавир** 12 недель ДАК** 1 таб. (60 мг) 1 р/д + НРВ** 2 таб. (по 100 мг каждая) 1 р/д +#р** 2 таб. (по 50 мг каждая) 1 р/д [109]. Для пациентов с субтипом 1b без ЦП без опыта ПВТ. Схема 5 Даклатасвир** + софосбувир** 12 недель ДАК** 1 таб. (60 мг) 1 р/д + СОФ** 1 таб. (400 мг) 1 р/д. 12 недель – для пациентов без ЦП и с компенсированным ЦП, как ранее не получавшим лечение, так и с предшествующей неэффективностью терапии ПегИФН** + РБВ** и/или препаратами, ингибирующими NS3/4А+/- СОФ**; 12 недель – с добавлением #РБВ** для пациентов с рецидивом инфекции (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) после трансплантации печени.[106, 107, 210, 211, 227] Схема 6 Ледипасвир+софосбувир ЛЕД+СОФ 1 таб. (90/400 мг) 1 р/д. 8 недель – для пациентов без ЦП, ранее не получавших лечение; 12 недель – для пациентов без ЦП, ранее получавших лечение ПегИФН** + #РБВ** +/- СОФ** и/или препаратами, ингибирующими NS3/4А, в том числе с рецидивом ХГС после трансплантации печени и солидных органов; 12 недель – с добавлением #РБВ** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) [90,91,92,225]; Для пациентов с компенсированным ЦП, ранее не получавших лечение или получавших лечение ПегИФН**+#РБВ**+/- СОФ** и/или препаратами, ингибирующими NS3/4А, в том числе рецидивом ХГС после трансплантации печени и солидных органов; 24 недели – для пациентов с ЦП (в т.ч. после трансплантации – с добавлением #РБВ** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг), ранее не получавших лечение или получавших лечение ПегИФН**+#РБВ** и/или препаратами, ингибирующими NS3/4А, в том числе с рецидивом ХГС после трансплантации печени и солидных органов [91,92,225];. Схема 7 Нарлапревир** + софосбувир** + #ритонавир** НРВ** 2 таб. (по 100 мг каждая) 1 р/д + #р** 2 таб. (по 50 мг каждая) 1 р/д + СОФ** 1 таб. (400 мг) 1 р/д [110,209]. #8 недель – для пациентов со слабовыраженным фиброзом и ВН менее 1 000 000 МЕ/мл можно рассмотреть 8 недель (по решению врачебной комиссии). 12 недель – для пациентов без ЦП (F0-F3), не получавших ПВТ. |
|
Пациентам, инфицированным ВГС ГТ 2 |
|
Схема 1 Велпатасвир+софосбувир** ВЕЛ+СОФ** 1 таб. (100/400 мг) 1 р/д. 12 недель – для пациентов без ЦП или с компенсированным ЦП, в том числе ранее получавших лечение ПегИФН** + РБВ** ± СОФ** и/или препаратами, ингибирующими NS3/4А, и пациентов с рецидивом ХГС после трансплантации печени и солидных органов. 24 недели – с добавлением #РБВ** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) для пациентов без ЦП или с компенсированным ЦП печени, ранее получавшим лечение режимом, включающим препараты, ингибирующие NS5A [76, 78,79, 237, 245, 254, 260, 267]. Схема 2 Глекапревир+пибрентасвир** ГЛЕ+ПИБ (100/40 мг) 3 таб. одновременно 1 р/д. 8 недель – для пациентов без ЦП или с ЦП, ранее не получавших лечение; для пациентов без ЦП, не ответивших на предыдущую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**; 12 недель – для пациентов с ЦП, не ответивших на предыдущую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**; для пациентов с рецидивом ХГС после трансплантации печени или почки. Схема 3 Даклатасвир** + софосбувир** 12 недель ДАК** 1 таб. (60 мг) 1 р/д + СОФ** 1 таб. (400 мг) 1 р/д. 12 недель – для пациентов без ЦП и с компенсированным ЦП, как ранее не получавшим лечение, так и с предшествующей неэффективностью терапии ПегИФН** + РБВ** и/или препаратами, ингибирующими NS3/4А+/- СОФ**; 12 недель – с добавлением #РБВ** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) для пациентов для пациентов с рецидивом инфекции после трансплантации печени [106,107,210,211,218, 227, 237,249,250, 254, 263-266] . |
|
Пациентам, инфицированным ВГС ГТ 3 |
|
Схема 1 Велпатасвир+софосбувир** ВЕЛ+СОФ** 1 таб. (100/400 мг) 1 р/д. 12 недель – для пациентов без ЦП, в том числе ранее получавших лечение ПегИФН** + РБВ** ± СОФ** и/или препаратами, ингибирующими NS3/4А, и пациентов с рецидивом ХГС после трансплантации печени и солидных органов; 24 недели – с добавлением #РБВ** 1000 или 1200 мг при весе <75 кг или ≥75 кг соответственно для пациентов без ЦП или с компенсированным ЦП печени, ранее получавшим лечение режимом, включающим препараты, ингибирующие NS5A, в том числе с рецидивом ХГС после трансплантации печени и солидных органов [76,78,79]. Схема 2 Глекапревир+пибрентасвир** ГЛЕ+ПИБ (100/40 мг) 3 таб. одновременно 1 р/д. 8 недель – для пациентов без ЦП или с ЦП, ранее не получавших лечение; |
|
16 недель – для пациентов без ЦП или с ЦП, ранее получавших ПегИФН** + РБВ** ± СОФ**, СОФ **+ РБВ**; для пациентов с рецидивом ХГС после пересадки печени или почки. Схема 3 Гразопревир+элбасвир** + софосбувир** 12 недель ГРА+ЭЛБ** (100/50 мг) 1 таб. 1 р/д + СОФ** 1 таб. (400 мг) 1 р/д. Для пациентов без ЦП и с компенсированным ЦП, ранее не получавшим ПВТ. Схема 4 Даклатасвир** + софосбувир** ДАК** 1 таб. (60 мг) 1 р/д + СОФ** 1 таб. (400 мг) 1 р/д. 12 недель – для пациентов без ЦП, как ранее не получавшим лечение, так и с предшествующей неэффективностью терапии ПегИФН** + РБВ** и/или препаратами, ингибирующими NS3/4А+/- СОФ**; 12 недель – с добавлением #РБВ** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) [106,107,210,211,218, 227, 237,249,250, 254, 263-266] . для пациентов с рецидивом инфекции после трансплантации печени; 12-24 недели – с добавлением #РБВ**(1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) или без него для пациентов с компенсированным циррозом как ранее не получавших лечение, так и с предшествующей неэффективностью терапии ПегИФН** + РБВ** +/- СОФ** и/или препаратов, ингибирующих NS3/4А [106,107,210,211,218, 227, 237,249,250, 254, 263-266] . Схема 5 Ледипасвир+софосбувир + #рибавирин** 24 недели ЛЕД+СОФ 1 таб. (90/400 мг) 1 р/д + #РБВ** 1000 или 1200 мг при весе <75 кг или ≥75 кг соответственно [89-92,113,213- 217]. Для пациентов с компенсированным ЦП и/или ранее получавших лечение ПегИФН** + РБВ** +/- СОФ** и/или препаратами, ингибирующими NS3/4А. |
|
Пациентам, инфицированным ВГС ГТ 4 |
|
Схема 1 Велпатасвир+софосбувир** ВЕЛ+СОФ** 1 таб. (100/400 мг) 1 р/д. 12 недель – для пациентов без ЦП или с компенсированным ЦП, в том числе ранее получавших лечение ПегИФН** + РБВ** ± СОФ** и/или препаратами, ингибирующими NS3/4А, и пациентов с рецидивом ХГС после трансплантации печени и солидных органов; 24 недели – с добавлением #РБВ** 1000 или 1200 мг при весе <75 кг или ≥75 кг, соответственно, для пациентов без ЦП или с компенсированным ЦП печени, ранее получавшим лечение режимом, включающим препараты, ингибирующие NS5A, в том числе с рецидивом ХГС после трансплантации печени и солидных органов [76,79,167]. Схема 2 Глекапревир+пибрентасвир** ГЛЕ+ПИБ** (100/40 мг) 3 таб. одновременно 1 р/д. 8 недель – для пациентов без ЦП или с ЦП, ранее не получавших лечение; для пациентов без ЦП, не ответивших на предыдущую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**; 12 недель – для пациентов с ЦП, не ответивших на предыдущую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг); для пациентов с рецидивом ХГС после трансплантации печени или почки [83-85]. Схема 3 Гразопревир+элбасвир** ГРА+ЭЛБ** (100/50 мг) 1 таб. 1 р/д. 12 недель – для пациентов с исходной концентрацией РНК ВГС менее 800 000 МЕ/мл. 16 недель – в комбинации с #РБВ** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг), инфицированных субтипом 4 при исходной концентрации РНК ВГС более 800 000 МЕ/мл [93,207, 221-224]. Схема 4 Даклатасвир** + софосбувир** ДАК** 1 таб. (60 мг) 1 р/д + СОФ** 1 таб. (400 мг) 1 р/д. 12 недель – для пациентов без ЦП и с компенсированным ЦП, как ранее не получавшим лечение, так и с предшествующей неэффективностью терапии ПегИФН** + РБВ** и/или препаратами, ингибирующими NS3/4А+/- СОФ**; 12 недель – с добавлением #РБВ** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) для пациентов с рецидивом инфекции после трансплантации печени [106,211,218,227]. Схема 5 Ледипасвир+софосбувир ЛЕД+СОФ 1 таб. (90/400 мг) 1 р/д. 12 недель – для пациентов без ЦП, в том числе ранее получавших лечение ПегИФН** + РБВ** и/или препаратами, ингибирующими NS3/4А; 12 недель – с добавлением #РБВ** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) [89-92,213- 217,225]; Для пациентов с компенсированным ЦП, ранее получавших лечение и ранее не получавших лечение ПегИФН** + РБВ** +/- СОФ** и/или препаратами, ингибирующими NS3/4А; 24 недели – для пациентов с компенсированным ЦП, ранее не получавших лечение или ранее получавших лечение ПегИФН** + РБВ** +/- СОФ** и/или препаратами, ингибирующими NS3/4А. |
|
Пациентам с декомпенсированным ЦП |
|
Схема 1 (все ГТ) Велпатасвир+софосбувир** + #рибавирин** 12 недель ВЕЛ+СОФ** 1 таб. (100/400 мг) 1 р/д + #РБВ** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) [76,78,79, 247, 254]. Для пациентов с декомпенсированным ЦП (класс В или класс С), в том числе у пациентов с предшествующей неудачей ПегИФН** + РБВ** ± СОФ** и/или препаратами, ингибирующими NS3/4А, и пациентов с рецидивом ХГС после пересадки печени и солидных органов. Для пациентов с ЦП класса С по классификации Child-Pugh до трансплантации следует начинать с дозы #РБВ** (1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) при хорошей переносимости [167] Для пациентов с опытом лечения препаратами, ингибирующими NS5A, длительность лечения следует увеличить до 24 недель. |
|
Схема 2 (для ГТ 1,2,3,4) Даклатасвир** + софосбувир** + #рибавирин** ДАК** 1 таб. (60 мг) 1 р/д + СОФ* 1 таб. (400 мг) 1 р/д + #РБВ**(1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг) [108,210,211, 218,227, 246 247, 254]. 12 недель – для пациентов с циррозом класса В по Child-Pugh как ранее не получавшим лечение, так и с предшествующей неэффективностью терапии ПегИФН** + РБВ** +/- СОФ** и/или препаратами, ингибирующими NS3/4А; 24 недели – для пациентов с циррозом класса С по Child-Pugh как ранее не получавшим лечение, так и с предшествующей неэффективностью терапии ПегИФН** + РБВ** +/- СОФ** и/или препаратами, ингибирующими NS3/4А. Для пациентов с непереносимостью РБВ** может рассматриваться режим без РБВ**. Схема 3 (для ГТ 1,4-6) Ледипасвир+софосбувир + #рибавирин** 12 недель ЛЕД+СОФ 1 таб. (90/400 мг) 1 р/д + #РБВ** 1000 или 1200 мг при весе <75 кг или ≥75 кг соответственно [90-92,213- 217, 247, 254]. Для пациентов с декомпенсированным ЦП, ранее получавших лечение и ранее не получавших лечение ПегИФН** + РБВ** +/- СОФ** и/или препаратами, ингибирующими NS3/4А. Для пациентов с ЦП класса С по классификации Child-Pugh до трансплантации следует начинать с начальной дозы #РБВ** 600 мг, которую можно титровать до максимума в 1000/1200 мг (800 мг при массе пациента менее 65 кг, 1000 мг при массе 65-80 кг, 1200 мг при массе 81-105 кг) при хорошей переносимости [90-92,113,167,213- 217,241,242]. Если наблюдается непереносимость РБВ**, можно рассмотреть применение ЛЕД+СОФ без РБВ** в течение 24 недель. |
Схемы ПВТ ХВГС для пациентов с декомпенсированным циррозом печени (Child-Pugh В или С) или эпизодами декомпенсации в анамнезе
Таблица 7
|
Схема |
ГТ |
Длительность |
|
ВЕЛ+СОФ** + #РБВ** |
1-6 |
12 неделя |
|
ДАК** + СОФ** + #РБВ** |
1-4 |
12-24 неделиб |
|
ЛЕД+СОФ + #РБВ** |
1,4,5,6 |
12 недель |
|
ЛЕД+СОФ |
1,4,5,6 |
24 недели |
Примечания:
ВЕЛ+СОФ** + #РБВ** – велпатасвир+софосбувир** (100/400 мг) 1 таб. 1р/д + #рибавирина** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг [76,78, 79, 247, 254]);
ДАК** + СОФ** + #РБВ** – даклатасвир** 60 мг 1 таб. 1р/д + софосбувир** 400 мг 1 таб. 1р/д + #рибавирина** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг 12 -24 недели. [105,107,208,218-220, 254];
ЛЕД+СОФ + #РБВ** – ледипасвир+софосбувир 90/400 мг 1 таб. 1р/д+ #рибавирина** 1000 мг при весе менее 75 кг или 1200 мг при весе не менее 75 кг (для ГТ 1,4,5,6) -12 недель [89-92,213- 217, 251, 252, 254];
а - Международные клинические рекомендации по гепатиту С подразумевают возможность использования схемы #ВЕЛ+СОФ** велпатасвир+софосбувир** (100/400 мг) 1 таб. 1р/д 24 недели при непереносимости РБВ** по решению врачебной комиссии [1,46,76,78, 79].
б - Длительность 12 недель для пациентов с циррозом печени (Child-Pugh А или В). Для генотипа 3 возможно продление терапии до 24 недель, с применением #РБВ** или без. Длительность 24 недели для пациентов с циррозом печени Child-Pugh С. Для пациентов с непереносимостью РБВ** может рассматриваться терапия ДАК**+ СОФ** без РБВ** 24 недели.
Активность ингибиторов NS5A в отношении распространенных исходных мутаций ВГС
Источник: Клинические рекомендации Американской Ассоциации по Изучению Болезней Печени (AASLD and IDSA HCV Guidance: Recommendations for Testing, Managing, and Treating Hepatitis C. https://www.hcvguidelines.org/evaluate/resistance, обращение в феврале 2025) [254].
Наиболее распространённые клинически-значимые мутации, связанные с резистентностью (RAS) с распределением по генотипам, ПППД и кратности изменения чувствительности
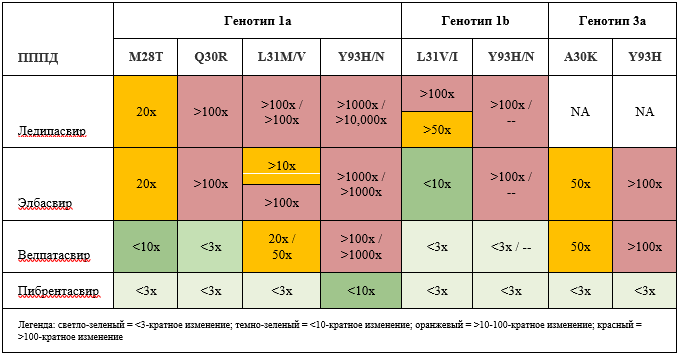
Рекомендации в случае пропуска приема пангенотипных комбинаций ПППД
Источник: Клинические рекомендации Американской Ассоциации по Изучению Болезней Печени (AASLD and IDSA HCV Guidance: Recommendations for Testing, Managing, and Treating Hepatitis C. https://www.hcvguidelines.org/evaluate/monitoring#incomplete-adherence, обращение в феврале 2025) [254].
Рекомендации в случае пропуска приема СОФ/ВЕЛ или ГЛЕ/ПИБ для первичных пациентов с компенсированной стадией заболевания печени
|
Прерывание в течение первых 28 дней терапии |
Прерывание после первых 28 дней терапии |
|
Пропуск ≤7 дней
|
Пропуск ≤7 дней
|
|
Пропуск ≥8 дней
|
Пропуск 8-20 дней подряд
|
|
|
Пропуск ≥21 дня
|
Приложение Б. Алгоритмы действий врача
Диагностика, лечение ХВГС
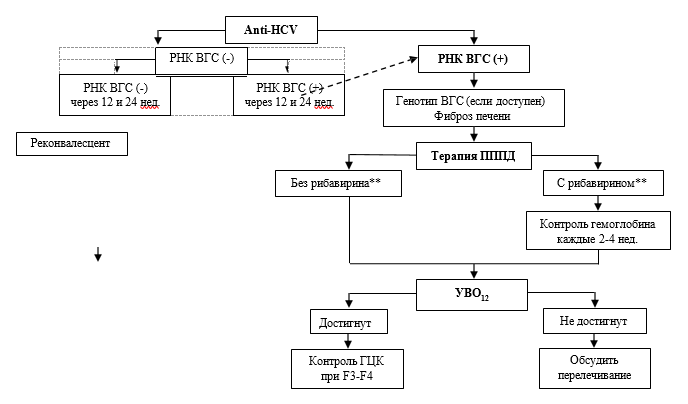
Приложение В. Информация для пациента
Уважаемый пациент! У Вас гепатит С. Современными лекарствами возможно полностью излечиться от данного заболевания. Это позволит не допустить развитие таких осложнений, как цирроз и рак печени. Обычно болезнь протекает без симптомов и выявляется при случайном обследовании. Однако это не значит, что ее не следует лечить. Объем терапии определит Ваш лечащий врач. Он же определит перечень необходимых исследований и их периодичность. Вам не следует самостоятельно отменять или заменять препараты, даже если Вы чувствуете себя лучше или считаете себя здоровым человеком. По всем появляющимся вопросам обращайтесь к лечащему врачу.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Оценка степени тяжести цирроза печени по шкале Child-Pugh
Название на русском языке: Оценка степени тяжести цирроза печени по шкале Child- Pugh
Источник: Durand F., Valla D. Assessment of the prognosis of cirrhosis: Child–Pugh versus MELD //Journal of hepatology. – 2005. – Т. 42. – №. 1. – С. S100-S107
Тип: шкала оценки
Назначение: оценка степени тяжести цирроза печени
Содержание:
|
Оцениваемые параметры |
Число баллов в зависимости от значения параметра |
||
|---|---|---|---|
|
|
1 балл |
2 балла |
3 балла |
|
Асцит |
Отсутствует |
Мягкий(легко поддаётся лечению) |
Напряжённый(плохо контролируемый) |
|
Общий билирубин, мкмоль/л (мг/дл) |
<34 (<2) |
34-50 (2-3) |
>50 (>3) |
|
Альбумин крови, г/л |
>3,5 |
2,8-3,5 |
<2,8 |
|
Печеночная энцефалопатия |
Отсутствует |
I-II ст.(лёгкая, терапевтически контролируемая) |
III-IV ст.(тяжёлая, плохо контролируемая) |
|
ПТИ, % или ПТВ, сек или МНО |
>60 или 1-4 или <1,70 |
40-60 или 4-6 или 1,71-2,20 |
<40 или >6 или >2,20 |
Ключ (интерпретация):
Баллы выставляются в зависимости от значения каждого из параметров от 1 до 3, после чего суммируются. Оценка выживаемости больных ЦП в зависимости от полученных баллов:
|
Класс по Child-Pugh |
Баллы |
Годичная выживаемость, % |
Двухлетняя выживаемость, % |
|
A |
5-6 |
100 |
85 |
|
B |
7-9 |
81 |
57 |
|
C |
10-15 |
45 |
35 |
Приложение Г2. Расчет индекса фиброза APRI
Название: Расчет индекса фиброза APRI
Источник: Yen Y. H. et al. APRI and FIB-4 in the evaluation of liver fibrosis in chronic hepatitis C patients stratified by AST level //PloS one. – 2018. – Т. 13. – №. 6. – С. e0199760.Тип: индекс
Содержание: Расчетная формула:
APRI = (АСТ/(ВГН АСТ)) * 100 / тромбоциты (109/л)
АСТ – значение аспарагиновой аминотрансферазы пациента ВГН АСТ – верхняя граница нормы АСТ
Тромбоциты (109/л) – число тромбоцитов пациента в 1 л крови
Ключ (интерпретация):
|
Значение APRI |
Вывод |
Шкала оценки |
|
>2,0 |
F4 |
METAVIR |
|
≥1,5 |
F3-F4 |
METAVIR |
|
0,5-1,5 |
Сомнительный результат |
|
|
<0,5 |
F0-F2 |
METAVIR |
Приложение Г3. Расчет индекса фиброза FIB-4
Название: Расчет индекса фиброза FIB-4
Источник: Yen Y. H. et al. APRI and FIB-4 in the evaluation of liver fibrosis in chronic hepatitis C patients stratified by AST level //PloS one. – 2018. – Т. 13. – №. 6. – С. e0199760.
Тип: индекс
Содержание: Расчетная формула:
FIB-4 = Возраст (лет)) * АСТ / тромбоциты (109/л) * √АЛТ
Возраст – возраст пациента (лет)
АСТ – значение аспарагиновой аминотрансферазы пациента Тромбоциты (109/л) – число тромбоцитов пациента в 1 л крови
√АЛТ – квадратный корень значения АЛТ пациента
Ключ (интерпретация):
|
Значение FIB-4 |
Вывод |
Шкала оценки |
|
>3,25 |
F3-F4 |
METAVIR |
|
<1,45 |
F0-F2 |
METAVIR |
|
1,45-3,25 |
Сомнительный результат |
|
Приложение Г4. Стадии фиброза печени по шкале METAVIR
Название: Шкала METAVIR
Источник: Shiha G., Zalata K. Ishak versus METAVIR: terminology, convertibility and correlation with laboratory changes in chronic hepatitis C //Liver biopsy. – 2011. – Т. 10. – С. 155- 170.
Тип: шкала
Содержание и ключ (интерпретация):
|
F0 |
Фиброз отсутствует |
|
F1 |
Звездчатое расширение портальных трактов без образования септ |
|
F2 |
Расширение портальных трактов с единичными портопортальными септами |
|
F3 |
Многочисленные портоцентральные септы без цирроза |
|
F4 |
Цирроз |
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.