Хроническая болезнь почек стадии 4-5D и принципы нутриционной поддержки
 Версия: Клинические протоколы КР 2024 (Кыргызстан)
Версия: Клинические протоколы КР 2024 (Кыргызстан)
Общая информация
Краткое описание
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ КЫРГЫЗСКОЙ РЕСПУБЛИКИ
Приложение 1 к приказу МЗ КР № 468 от 07.05. 2024 г.
Название документа
Этапы оказания помощи
Первичный, вторичный и третичный уровни здравоохранения, отделений «Искусственной почки»
Цель создания Клинического руководства
Целевые группы
Семейные врачи, врачи вторичного, третичного уровня здравоохранения, врачи отделения «Искусственной почки», реаниматологи, врачи других специальностей; организаторы здравоохранения; специалисты, контролирующие качество оказания медицинской помощи (ФОМС).
Дата создания: обновлено в мае 2023 г. Клиническое руководство, 1-я версия была утверждена приказом МЗ КР №785 от 21.11.2018г.
ТЕРМИНАЛЬНАЯ ХРОНИЧЕСКАЯ ПОЧЕЧНАЯ НЕДОСТАТОЧНОСТЬ (ТХПН) – состояние, связанное с необратимой утратой функции почек, т.е. снижение СКФ менее 15 мл/мин/1,73м2, соответствующее 5 стадии ХБП, анатомической основой которого является процесс замещения нормальных анатомических структур органа фиброзом, приводящий к его дисфункции [1- 4].
Классификация по МКБ-10:
Классификация
Пример 1
|
Основное заболевание: N 18.0. ХБП С5 как исход хронического гломерулонефрита неуточненной морфологией.
Осложнение заболевания: D 63.8 - Ренальная анемия
|
Таблица 1. Стратификация стадий ХБП по уровню СКФ (KDIGO) 2002
|
Обозначение
|
Характеристика функций почек | Уровень СКФ, мл/мин |
| С1 | Высокая и оптимальная | > 90 |
| С2 | Незначительно сниженная | 60-80 |
| С3а | Умеренно сниженная | 45-59 |
| С3б | Существенно сниженная | 30-44 |
| С4 | Резко сниженная | 15-29 |
| С5 | Терминальная почечная недостаточность (не диализная) | < 15 |
| С5d | Терминальная почечная недостаточность (диализная) |
|
Категории ХБП
|
Определение |
| ХБП | ХБП 1-5 стадии без или с почечным трансплантатом, включая диализ-независимую ХБП (ХБП НД 1-5) и диализ-зависимую ХБП (ХБП Д 5) |
| ХБП НД | Диализ-независимая ХБП любой стадии, без или с почечным трансплантатом (т.е. ХБП не включая ХБП Д5) |
| ХБП Т | Диализ-независимая ХБП любой стадии, с почечным трансплантатом |
| ХБП 5D | Диализ-зависимая ХБП 5 стадии |
Этиология и патогенез
Основные механизмы патогенеза хронической болезни почек.
Функционально-адаптивные механизмы
Метаболические и эндокринные механизмы
Врожденные и генетические факторы
Педиатрические аспекты
Многие факторы, ассоциирующиеся с развитием дисфункции почек, одновременно являются и «традиционными» сердечно-сосудистыми факторами риска. В патогенезе ХБП существенное значение имеют кардиоваскулярные изменения, которые являеются доминирующей причиной смертности в этой популяции пациентов. Риск смерти у пациентов на ЗПТ вследствие сердечно-сосудистых заболеваний в десятки раз выше, чем в общей популяции, что связано с резким ускорением процессов сосудистого повреждения. Проблема поражения сердечно-сосудистой системы касается и пациентов с начальным и умеренными снижением скорости клубочковой фильтрации (СКФ), когда уровень креатинина в сыворотке крови «нормален» или только незначительно повышен. Данные ранних обсервационных исследований, продемонстрировавших значительное увеличение частоты встречаемости АГ и других традиционных факторов риска развития кардиоваскулярной патологии, ее распространенности и заболеваемости при снижении СКФ или увеличении уровня сывороточного креатинина [11-13]. Таким образом, взаимоотношения дисфункции почек и изменений сердечнососудистой системы носят многогранный характер и выстраиваются по типу обратной связи. В этом контексте, с одной стороны, почка может выступать как орган-мишень для действия большинства известных факторов, связанных с сердечно-сосудистыми изменениями; с другой – активно вмешиваться в формирование системных метаболических и сосудистых патологических процессов, являясь активным генератором, и традиционных, и нетрадиционных факторов риска, тем самым, замыкая сложный патогенетический круг, определяющий судьбу таких пациентов.
Эпидемиология
ЭПИДЕМИОЛОГИЯ
Распространенность ХБП сопоставима с такими социально значимыми заболеваниями, как гипертоническая болезнь и СД, а также с ожирением и метаболическим синдромом. Признаки повреждения почек и/или снижение СКФ выявляют, как минимум, у каждого десятого представителя общей популяции.
Глобальная распространенность ХБП в общей популяции по результатам крупных когортных исследований составила, в среднем, 13,4% [5]. По оценкам Всемирной организации здравоохранения, 850 миллионов людей по всему миру страдают различными заболеваниями почек. Опасность заболеваний почек, как и многих других, заключается в том, что пациенты долго игнорируют опасные симптомы и обращаются за помощью уже на поздних стадиях [5].
По данным Европейского регистра ХБП, распространенность предиализной стадии ХБП у взрослых составляет 55 на миллион общего населения. В то же время у детей ХБП регистрируется около 12 на миллион детского населения [6].
Согласно данным Японского национального реестра и реестра Австралии и Новой Зеландии по диализу и трансплантации (ANZDATA), ежегодная заболеваемость тХБП равна 22 на 1 млн. населения [7].
Факторы и группы риска
ФАКТОРЫ РИСКА РАЗВИТИЯ ХБП
| С |
Немодифицируемые (которые не поддаются изменениям)
• Пожилой возраст
• Исходно низкое число нефронов (низкая масса тела при рождении)
• Расовые и этнические особенности(негроидная раса)
• Наследственные факторы (в том числе семейный анамнез по ХБП)
• Перенесенное острое повреждение почек
|
| С |
Модифицируемые (поддаются изменениям)
• Сахарный диабет
• Артериальная гипертензия
• Дислипопротеидемия
• Табакокурение
• Ожирение/метаболический синдром
• Неалкогольная жировая болезнь печени
• Гиперурикемия
• Аутоиммунные болезни
• Хроническое воспаление/cистемные инфекции
• Инфекции и конкременты мочевых путей
• Обструкция нижних мочевых путей
• Лекарственная токсичность
• Высокое потребление белка
• Беременность
|
Диагностика
КРИТЕРИИ ДИАГНОЗА ХБП:
Для вычисления величины СКФ по плазменной концентрации креатинина в 4 – 5 стадиях ХБП не рекомендуются формулы Кокрофта – Голта и MDRD ввиду их меньшей информативности по сравнению с CKD-EPI [2, 3, 6].
Таблица 3. Диагностика ХБП по уровню СКФ и альбуминурии проводится с учетом данных креатинина и альбуминурии, на основании чего оценивается риск прогрессирования ХБП.
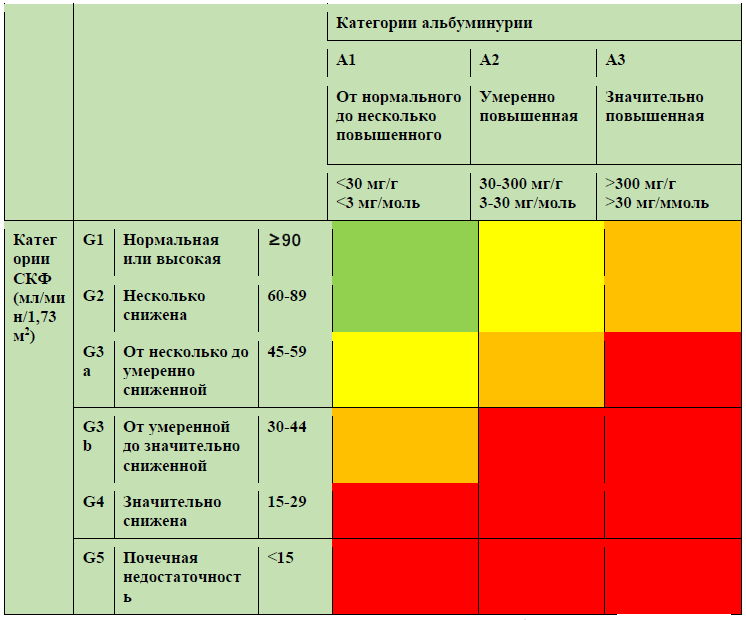
Обозначения:


| А | Пациентам с ХБП С4-5 рекомендуется проведение клинической диагностики системных осложнений дисфункции почек (анемии, АГ, минеральных и костных нарушений (МКН-ХБП), дисэлектролитемии, метаболических нарушений, гиперурикемии, дислипопротеидемии). |
| А | С целью раннего выявления ХБП врачам всех специальностей в клинической практике рекомендуется регулярно, но не реже 1 раза в 2 года проводить диагностику на основе исследования альбуминурии/протеинурии и рСКФ у лиц с факторами риска ХБП. |
| А | В тех клинических случаях, когда точность расчета СКФ по формуле CKD-EPI на основании концентрации креатинина в сыворотке крови может быть существенно снижена, для скрининговой оценки и подтверждающей диагностики рекомендуется использовать расчет СКФ с использованием концентрации цистатина С по формуле CKD-EPI «Цистатин С» (2012) |
Клинические признаки заболевания
|
Маркеры
|
Примечание |
| Жалобы | изменения цвета мочи, изменения объема диуреза (олигурия, полиурия), никтурия |
| Данные анамнеза | данные за выявленные ранее изменения мочи или изменения почек при любых видах визиализирующей диагностики |
| Физикальное обследования | уменьшение размера почек, симптомы уремии, шум в проекции почечных артерий, периферические и полостные отеки, изменение цвета и объема мочи, АГ |
| Лабораторные данные |
• повышенная альбуминурия/протеинурия,
• стойкое снижение скорости клубочковой фильтрации менее 60 мл/мин/1,73 м2,
• стойкие изменения в клеточном осадке мочи: эритроцитурия (гематурия), тубулярные клетки, лейкоцитурия (пиурия), лейкоцитарные цилиндры, эритроцитарные цилиндры.
|
| Изменения состава крови и мочи: | азотемия, уремия, изменения сывороточной и мочевой концентрации, нарушения кислотно-щелочного равновесия и электролитов |
| Изменения почек по данным лучевых методов исследования | аномалии развития почек, кисты, гидронефроз, изменение размеров почек, нарушение интраренальной гемодинамики и др |
| Изменения в ткани почек, выявленные при прижизненном морфологическом исследовании: | признаки активного необратимого повреждения почечных структур, и универсальные маркеры фиброза компартментов органа, указывающие на «хронизацию» патологического процесса, при этом исследования органа специфические для каждого хронического заболевания почек. |
При наличии «красных флагов» направить к нефрологу для решения вопроса об экстренном начале ЗПТ.
При отсутствии «красных флагов» пациенту с ХБП С4-5 и/или его родственникам должна быть предоставлена достаточная информация для осознанного выбора ЗПТ (Рис.1):
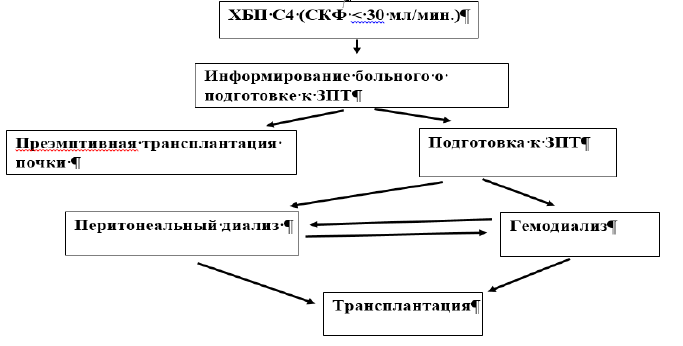
Специфическая диагностика
| А | Для диагностики, подтверждения и определения прогноза у пациентов с ХБП рекомендуется определение альбумина в моче и количества белка в суточной моче либо определение альбумина в моче с исследованием уровня креатинина в моче и расчетом отношения альбумин/креатинин |
РУТИННЫЕ ИССЛЕДОВАНИЯ БОЛЬНЫХ С ХБП С5D
|
Параметры
|
Единицы измерения | Кратность выполнения исследования для пациентов, получающих ГД | |
|
Гематологические исследования
Клинический анализ крови
|
|||
| 1 |
Гемоглобин
|
г/л | 12 раз/год |
| 2 |
Гематокрит
|
% | 12 раз/год |
| 3 |
Эритроциты
|
х 10^12/л | 12 раз/год |
| 4 |
Лейкоциты
|
х 10^9/л | 12 раз/год |
| 5 | Лейкоцитарная формула | 12 раз/год | |
| 6 |
Тромбоциты
|
х 10^9/л | 12 раз/год |
| 7 | Ретикулоциты | 12 раз/год | |
|
Иммуногематологические исследования
|
|||
| 1 | Группа крови | однократно, при поступлении | |
| 2 | Резус фактор | однократно, при поступлении | |
|
Коагулогические исследования
|
|||
| 1 |
Фибриноген
|
г/л | 2 раз/год |
| 2 |
АЧТВ
|
Сек | 2 раз/год |
|
Биохимические исследования крови
|
|||
| 1 |
Глюкоза
|
ммоль/л | 1 раз в год (по специальным показаниям и при наличии СД - чаще) |
| 2 |
Альбумин
|
г/л | 4 раз/год (по специальным показаниям – чаще) |
| 3 |
Креатинин
|
мкмоль/л | 12 раз/год; |
| 4 | Мочевина | ммоль/л | 24 раза/год (при прямом измерении Kt/V 4 раза/год) |
| 5 | Мочевая кислота | мкмоль/л | 1 раз/год |
| 6 | Липопротеин низкой плотности | ммоль/л | 2 раза/год |
| 7 | Аланинаминотрансфераза (АлТ) | ед/л | 2 раз/год |
| 8 | Аспартатаминотрансфераза (АсТ) | ед/л | 2 раз/год |
| 9 | Гамма- глутамилтранспептидаза (ГГТП) | ед/л | 2 раз/год |
| 10 | Щелочная фосфатаза (ЩФ) | ед/л | 2 раз/год |
| 11 | Калий | ммоль/л | 12 раз/год |
| 12 | Натрий | ммоль/л | 12 раз/год |
| 13 | Общий кальций или Кальций ионизированный |
ммоль/л
ммоль/л
|
12 раз/год
12 раз/год
|
| 14 | Магний | ммоль/л | 2 раз/год |
| 15 | Фосфор | ммоль/л | 12 раз/год |
| 16 |
Сывороточное железо
|
мкмоль/л | 4 раза/год |
| 17 | Бикарбонат | ммоль/л | 4 раза/год |
| 18 | Трансферрин | мкг/л | 4 раза/год |
| 19 | Ферритин | мкг/л | 4 раза/год |
|
Иммунологические исследования
|
|||
| 1 | С-реактивный белок | мг/л | 4 раза/год |
| 2 | Бета-2-микроглобулин | мг/л | 1 раз/год |
| Гормональные | |||
| 1 |
Паратиреоидный гормон
(ПТГ)
|
пг/мл | 4 раза/год |
|
Вирусологические исследования
|
|||
| 1 | Антитела к ВИЧ (Anti-HIV) | качественное значение | 1 раз/год (при положительном результате больше не выполнять) |
| 2 | HBs-антиген (HBsAg) | качественное значение | 2 раза/год |
| 3 | анти-HBsAg | ME/л | 1 раз/год |
| 4 |
Антитела классов IgG и IgM
к HBcoreAg
|
качественное значение | при наличии показаний |
| 5 |
Антитела класса IgM к
HBcoreAg
|
качественное значение | при наличии показаний |
| 6 | ПЦР гепатита С (качественный) | качественное значение | при наличии показаний |
| 7 | Антитела к антигенам вируса гепатита С (Anti-HСV total) | качественное значение | 2 раза/год |
|
Специфические исследования крови
|
|||
| 1 | Сифилис ELA (ИФА) IgGIgM | качественное значение | 1 раз/год |
| Инструментальные исследования | |||
| 1 | Рентгенография легких | 1 раз/год | |
| 2 | Рентгенография костей | по показаниям | |
| 3 | Денситометрия костей | по показаниям | |
| 4 | ЭГДС | по показаниям | |
| 5 | ЭКГ | по показаниям | |
| 6 | Холтеровское мониторирование | по показаниям | |
| 7 | УЗИ органов брюшной полости | по показаниям | |
| 8 | УЗИ паращитовидных желез | по показаниям | |
| 9 | ЭХО-КГ | 2 (по специальным показаниям – чаще) | |
| 10 | УЗДГ сосудистого доступа | по показаниям | |
| Консультации специалистов | |||
| 1 | Эндокринолог для больных СД | по показаниям | |
| 2 | Кардиолог | 1 раз в год | |
| 3 | Офтальмолог | по показаниям | |
| 4 | Невропатолог | по показаниям | |
| 5 | Диетолог | по показаниям | |
| 6 | Психолог | по показаниям | |
Диагностика (амбулатория)
Лабораторные исследования на амбулаторном уровне
| А | На амбулаторном уровне рекомендуется проводить лабораторные исследования пациентам с ХБП С4-5 без осложнений. |
Прогрессирование почечной недостаточности у больных ХБП С4 можно предупредить или существенно замедлить при помощи следующих мер:
Детям с ХБП подготовка к ЗПТ необходима при снижении скорости СКФ <30 мл/мин на 1,73 м2 (ХБП С4). Необходимо информирование больного и его семьи/опекунов о вариантах ЗПТ (превентивная трансплантация почки, перитонеальный диализ и гемодиализ).
Перечень исследований
ЛАБОРАТОРНЫЕ КРИТЕРИИ ДИАГНОСТИКИ ОСЛОЖНЕНИЙ ХБП С4-5
| А |
Анемия: Общий (клинический) анализ крови с дифференцированным подсчетом лейкоцитов; железо сыворотки крови; ферритин в крови; насыщение трансферрина железом; исследование кала на скрытую кровь, определение СРБ
|
| А | Дизэлектролитемия: Исследование уровня натрия, калия, хлоридов, общего кальция, неорганического фосфора в крови; |
| А |
Ацидоз: Исследование кислотно-основного состояния и газов крови
pH<7,1, HCO3 < 16 – тяжелый метаболический ацидоз
|
| А | Нарушение питания: Исследование уровня альбумина в крови |
| В | Дислипидемия: Исследование уровня холестерина липопротеинов низкой плотности; |
| А | Гиперурикемия Исследование уровня мочевой кислоты в крови |
| А | МКН-ХБП Исследование уровня неорганического фосфора, паратиреоидного гормона, 25-ОН витамина Д в крови; определение активности щелочной фосфатазы в крови; |
| В | Для оценки прогноза и выбора лечения, направленного на предупреждение сердечно-сосудистых осложнений, а также снижения риска неблагоприятных исходов рекомендуется оценка нарушений липидного обмена: липопротеины низкой плотности (ЛПНП) |
| А | Рекомендуется выполнять исследование уровня СРБ в сыворотке крови для выявления воспалительной реакции, оценки ассоциированных рисков и терапии |
Оценка содержания газов артериальной крови
• рН: 7,35-7,45 (если pH>7,45 – алкалоз, если pH<7,35 – ацидоз);
• Парциальное давление кислорода (РаО2): от 75 до 100 мм рт. ст.;
• Парциальное давление углекислого газа (РаСО2): 35-45 мм рт.ст.;
• Бикарбонат (HCO3): 22-26 мг-экв/л;
Обязательные инструментальные исследования
|
Перечень инструментальных исследований
|
Результаты | Кратность проведения |
| УЗИ почек | Определение размера почек, толщины паренхимы, дополнительных изменений (наличие кист, МКБ и.т.д.) | 1-2 раза в год |
| УЗДГ сосудов почек | Определение индекса резистентности почечных сосудов | 1-2 раза в год |
| ЭХОКГ | Для выявления и оценки структурных изменений и дисфункции миокарда | 1-2 раза в год |
| ЭКГ | Выявление нарушений ритма и проводимости сердца, острого коронарного синдрома | при госпитализации, дополнительно по показаниям |
| А | Рекомендуется выполнение динамического УЗИ почек пациентам с ХБП для выявления и оценки макроскопических изменений органа |
| А | Рекомендуется пациентам с ХБП выполнение дуплексного сканирования артерий почек. При сомнительных результатах или явных ограничениях метода следует дополнить магнитно-резонансной томографией (МРТ) или компьютерной томографией (КТ) с контрастированием |
МРТ или КТ с контрастированием имеют высокую диагностическую ценность в сравнении с ангиографией. Типичное ограничение дуплексного сканирования связано с затрудненной визуализацией сосудов почек. При применении контраста рекомендуется тщательно оценить риск развития ОПП на фоне существующей ХБП. Решение об использовании рентгеноконтрастных препаратов для диагностики должно быть принято на индивидуальной основе с учетом пользы результатов исследования для пациента и потенциальных почечных рисков.
| В | У пациентов с ХБП С4-5 рекомендуется использовать контрастные препараты из групп макроциклических хелатов (гадобутрол, гадотеровая кислота, гадотеридол) и гадобеновой кислоты для снижения риска развития нефрогенного системного склероза. |
| А | У пациентов с ХБП С4-5 рекомендуется проводить инструментальную диагностику кальцификации периферических артерий и аорты для выявления, оценки связанных с ней рисков и выбора терапии |
| В | У пациентов с ХБП С4-5 рекомендуется эхокардиография для выявления и оценки структурных изменений и дисфункции миокарда с целью определения ассоциированных рисков и выбора терапии |
Осложнения
АНЕМИЯ
Анемия диагностируется у детей с ХБП, если концентрация гемоглобина ниже 110 г/л у детей от полугода до 5 лет, ниже 115 г/л у детей 5–12 лет и ниже 120 г/л у детей 12–15 лет.
Уровень Нв, который трактуется как анемия и служит основанием для начала выявления ее причин, зависит от возраста и пола. Необходимо проводить коррекцию нормальных величин для детей и взрослых, живущих в местности, расположенной на больших высотах.
При выявлении низкого гемоглобина следует, не основываясь в выводах на единственном определении, повторить его перед началом диагностического поиска.
| С | Всем пациентам с ХБП рекомендуется выполнение общего (клинического) анализа крови, оценка гематокрита (Hct), исследование уровня эритроцитов в крови и исследование уровня ретикулоцитов с целью диагностики и дифференциальной диагностики анемии [1–3]. |
| С | Пациентам с ХБП и анемией рекомендуется исследование уровня железа сыворотки крови, исследование насыщения трансферрина железом, исследование уровня ферритина в крови с целью уточнения характера анемии и дифференциальной диагностики с железодефицитной анемией [1–3]. |
Алгоритм коррекции анемии у больных на гемодиализе
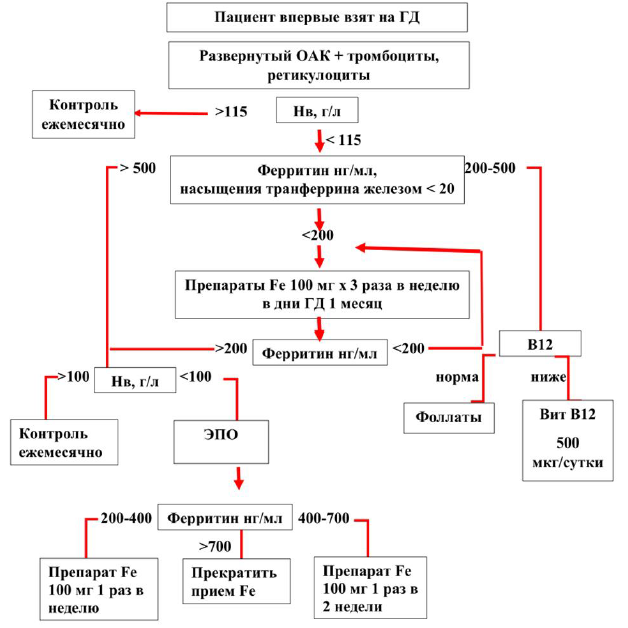
Более частый мониторинг насыщения трансферрина и концентрации ферритина показан:
5. при любых ситуациях, когда можно предположить дефицит железа.
| С | Пациентам с анемией на фоне ХБП рекомендуется определение уровня витамина В12 (цианокобаламина) в крови и исследование уровня фолиевой кислоты в сыворотке крови с целью исключения B12-дефицитной или фолиеводефицитной анемии [89-91]. |
Лечение пациентов с ХБП и анемией
У детей целевой уровень гемоглобина составляет от 110 до 120 г/л. Следует избегать повышения уровня гемоглобина выше 120 г/л. Более высокая концентрация гемоглобина может ассоциироваться с ухудшением почечного и кардиоваскулярного прогноза.
Препараты железа
| С | Пациентам с ХБП и анемией при насыщении трансферрина ниже 20% и уровне ферритина ниже 100 нг/мл рекомендуется назначение препаратов железа для поддержания уровня насыщении трансферрина выше 20% и ферритина выше 100 нг/мл [89-93]. |
|
Параметр
|
Оптимально |
|
Ферритин мкг/л
|
≤500 |
|
TSAT %
|
30% |
|
Число гипохромных эритроцитов %
|
<2,5 |
Большинство пациентов с ХБП при уровне ферритина выше 100 мкг/л имеют достаточные запасы железа в костном мозге [94–99]. Тем не менее, у многих из этих пациентов возрастет гемоглобин и/или снизится доза ЭПО, если провести терапию железом [16, 23, 30, 31, 40]. Существенная доля пациентов с TSAT выше 20% отвечают на терапию железом увеличением гемоглобина и/или снижением дозы ЭПО. Безопасность дополнительной терапии железом для намеренного поддержания TSAT выше 30% и ферритина выше 500 мкг/л исследована у очень небольшого числа пациентов. Не рекомендуется терапия железом у пациентов с TSAT выше 30% и ферритином выше 500 мкг/л, поскольку, преимущества и риски такой тактики недостаточно исследованы. У всех пациентов, получающих железо, важно оценивать как краткосрочную, так и острую токсичность терапии и исключать наличие активной инфекции перед началом внутривенного курса железа.
| С | ЭПО рекомендуется назначать всем пациентам с ХБП, имеющим Нв <100 г/л, после исключения других возможных причин анемии и нормализации показателей железа [87, 88]. |
| А | При диагностировании анемии у пациентов на гемодиализе ранее получавших ЭПО, но не получавших препараты железа, рекомендуется лечение препаратами железа, предпочтительнее для внутривенного введения, с целью повышение Hb и уменьшения дозы ЭПО, при условии, что ферритин <500 мкг/л, TSAT <30% [87, 88]. |
| В | С осторожностью ЭПО назначаются пациентам с высоким риском инсульта (в том числе с ОНМК в анамнезе) и больным со злокачественными новообразованиями в активной стадии или в анамнезе [34, 35]. |
| А | У всех детей с ХБП, получающих ЭПО, целевая концентрация гемоглобина находится в диапазоне 110–120 г/л. |
| А | Выбор типа ЭПО должен основываться на балансе показателей фармакодинамики, безопасности, клинических исходах, стоимости и доступности. Предпочтение следует отдавать препаратам, прошедшим полный цикл клинических испытаний |
Выбор целевого значения гемоглобина и параметра, при котором начинается терапия ЭПО, у каждого пациента является индивидуальным и определяется многими клиническими факторами.
| В | Терапию ЭПО можно начинать при показателях Нв >100 г/л, но не >120 г/л, у пациентов, у которых при этом улучшается качество жизни, но при этом не желательно намеренно превышать показатели Нв >130 г/л. |
| А | Путь введения ЭПО у пациентов на гемодиализе либо в/в либо п/к, в зависимости от дозы до 2-3 р в неделю |
Уровни Нв крови должны регулярно проверяться: каждые 2-4 недели при инициации терапии препаратами железа и ЭПО, ежемесячно после стабилизации показателей, каждые 2-4 недели при изменении дозировок препаратов [87, 88].
|
Фаза лечения
|
Дозы ЭПО | Кратность контроля Нв |
| Фаза коррекции | 50-100 Ед/кг в неделю (в среднем 6000 Ед/нед на пациента) | Каждые 2- 4 недели |
| Поддерживающая фаза | Поддерживать скорость повышения гемоглобина на 10-20 г/л/мес, при достижении целевых уровней гемоглобина снижать дозы ЭПО на 30% от дозы в фазу коррекции; изменение гемоглобина менее 10 г/л/мес или более 20 г/л/мес, требует повышения/снижения дозы ЭПО на 25% | Ежемесячно |
| А | Если после стабилизации уровня гемоглобина, пациентам требуется двукратное увеличение дозы ЭПО более 50% от стартовой для поддержания стабильных уровней гемоглобина, этих больных необходимо классифицировать, как пациентов с приобретенной низкой чувствительностью к ЭПО. |
| А | У пациентов с первичной и приобретенной низкой чувствительностью к терапии ЭПО не рекомендуется превышать вдвое и выше дозы ЭПО для достижения целевых уровней гемоглобина |
| А | Рекомендуется, не использовать ЭПО при концентрации гемоглобина выше 130 г/л |
Резистентность к препаратам ЭПО
| А | Резистентность к ЭПО определяется как невозможность достичь целевого уровня гемоглобина при дозах ЭПО, превышающих 300 Ме/кг при п/к введении или 450Ме/кг при в/в введении. |
У пациентов с приобретенной пониженной чувствительностью к ЭПО мы предлагаем избегать повторных увеличений доз более чем в два раза по сравнению с той, на которой был достигнут стабильный эффект.
|
Необходимо заподозрить развитие Антиген-опосредованной истинной красноклеточной аплазии костного мозга (PRCA) у пациентов, получающих ССЭ 8 недель и более при следующих состояниях:
• резкое снижение концентрации уровня гемоглобина крови более чем на 5
• 10 г/нед ИЛИ необходимость в гемотрансфузиях от 1 до 2 раз в неделю (В)
• нормальные уровни тромбоцитов и лейкоцитов (В)
• абсолютное количество ретикулоцитов менее 10 000 ‰
|
| А | При подтверждении диагноза PRCA (тяжелая анемия, низкий уровень ретикулоцитов, отсутствие эритробластов, резистентность к ЭПО, нейтрализующие антитела к ЭПО, нормальные уровни тромбоцитов и лейкоцитов) терапию ЭПО следует прекратить [34, 102] |
После установления диагноза опосредованной антителами PRCA следует немедленно прекратить лечение ЭПО, с которым связывается аплазия, и не возобновлять терапию тем же или другим основанным на эритропоэтине средством. Иммуносупресивная терапия может ускорить исчезновение антител у пациентов с индуцированной ЭПО PRCA, и позволить эндогенному эритропоэтину восстановиться до исходных уровней. Возобновление терапии ЭПО или дарбэпоэтином-альфа может привести к повторной индукции образования антител. Появление опосредованной антителами PRCA у пациентов, леченых рекомбинантными эпоэтинами, подчеркивает необходимость полного клинического документирования и постмаркетингового наблюдения за всеми новыми ЭСС и биоаналогами, равно как и за всеми находящимися в терапевтическом использовании рекомбинантными белками [103].
Если принимается решение лечить пациента пегинесатидом, его можно начать в дозе 0,05-0,075 мг/кг массы тела подкожными инъекциями один раз в четыре недели. В последующем доза требует коррекции для достижения целевого уровня гемоглобина.
| А | Гемотрансфузия пациентам на гемодиализе применяется только в случае прямых показаний: снижении уровня Нв ниже 70 г/л или 80 г/л после хирургических операций, при кровопотере при наличии четких симптомов, связанных с анемией, при резистентности к терапии ЭПО или высоких рисках терапии ЭПО |
МИНЕРАЛЬНЫЕ И КОСТНЫЕ НАРУШЕНИЯ (МКН) ПРИ ХБП С4-5D
| А | Рекомендуется проводить мониторинг сывороточных уровней кальция, фосфата, паратиреоидного гормона (ПТГ) и активности щелочной фосфатазы (ЩФ), начиная с ХБП С3. |
| В | У детей предлагается начинать такое мониторирование с ХБП С2. |
|
Показатель
|
ХБП С4-5D (СКФ мл/мин/1,73 м2) |
|
Фосфор
|
0,87-1,49 ммоль/л |
|
Кальций общий
|
2,1-2,5 ммоль/л |
|
Кальций ионизированный
|
1,1-1,3 ммоль/л |
|
ПТГ
|
150-300 пг/мл |
|
ЩФ
|
М – 53-128 Ед/л; Ж – 42-98 Ед/л |
Костная система
Традиционно используется метод биопсии подвздошной кости с двойной тетрациклиновой маркировкой с последующей гистоморфометрией. Однако данных об эффективности и безопасности ее проведения у пациентов на ГД недостаточно [3, 18, 41, 42].
У пациентов с ХБП С3-5D, целесообразно выполнять биопсию кости при:
| А | У детей до 2 лет с ХБП С2-5D рекомендуется измерять рост ежеквартально. У детей более старшего возраста с ХБП С2-5 D линейный рост оценивается, ежегодно. |
| А | У пациентов с высоким риском остеопороза и симптомами МКН, рекомендуется проведение остеоденситометрии для выявления риска развития переломов и коррекции лечения |
| В | У пациентов с ХБП С3а-5, целесообразно выполнить биопсию кости, если известный тип почечной остеодистрофии будет влиять на решения в отношении лечения. |
| А | У пациентов на ГД решение о начале лечения антирезорбтивными препаратами принимается индивидуально. Обучение пациентов методам безопасной ходьбы также может способствовать снижению частоты переломов. |
Золотым стандартом лечения остеопороза являются препараты группы бифосфонатов. Однако, данных об эффективности и безопасности применения бифосфонатов (аледронат, ризедронат) у пациентов на ГД недостаточно.
Сосудистая кальцификация
| В | У пациентов с ХБП С3-5D рекомендуется использовать латеральную абдоминальную рентгенографию для обнаружения наличия или отсутствия сосудистой кальцификации, и эхокардиографии - для определения наличия или отсутствия клапанной кальцификации [3, 18, 36-41]. |
Паратиреоидный гормон
| В |
У пациентов с ХБП С3-5D, рекомендуется контроль ПТГ сыворотки или костно-специфичной щелочной фосфатазы для оценки заболевания
кости
|
| В | Не рекомендуется рутинно использовать кальцитриол и аналоги витамина D у взрослых пациентов с ХБП С3а-5 не находящихся на диализе. Необходимо, препараты кальцитриола и аналогов витамина D использовать при тяжелом и прогрессирующем гиперпаратиреозе у больных с ХБП С5D. |
| А | У пациентов с ХБП С3-5 медикаментозная коррекция ВГПТ включает пероральный прием неселективных ВДРА (кальцитриол, альфакальцидол) или селективных ВДРА (парикальцитол) при уровне Р и Са в целевом диапазоне или при гипокальциемии. |
| А | Кальцитриол, альфакальцидол не следует назначать пациентам с додиализной ХБП с гиперкальциемией и/или гиперфосфатемией |
| В | У пациентов с тяжелым гиперпаратиреозом с отсутствием ответа на медикаментозное лечение рекомендуется проведение паратиреоидэктомии. |
| А | У пациентов на ГД рекомендуется поддержание уровней ПТГ в пределах от 2-х до 9-ти кратного превышения верхней границы нормы. |
Кальцимиметик является эффективным препаратом коррекции ВГПТ:
| А | Сочетанная терапия кальцимиметиком с витамином D (альфакальцидол) позволяет снизить дозы принимаемых препаратов, уменьшить частоту дозозависимых побочных эффектов цинакальцета (гипокальциемия, тошнота), увеличить эффективность и безопасность терапии. |
Паратиреоидэктомия
ПТЭ рекомендуется у пациентов при;
| А | Перед выполнением ПТЭ обязательно проведение дооперационной ультразвуковой визуализации ПЩЖ, которую при необходимости можно дополнить однофотонно эмиссионной компьютерной томографией или магнитнорезонансной томографией, радиоизотопной сцинтиграфией. |
Выбор способа ПТЭ и объем оперативного вмешательства (субтотальная, тотальная с аутотрансплантацией фрагмента ПЩЖ под кожу/мышцу предплечья, тотальная ПТЭ без аутотрансплантации фрагмента ПЩЖ, ревизия вилочковой железы и удаление её верхних полюсов, резекция/удаление доли щитовидной железы) остается за хирургом и определяется индивидуально в каждом конкретном случае. Во всех возможных случаях следует рекомендовать субтотальную или тотальную ПТЭ с аутотрансплантацией паратиреоидной ткани.
При снижении сывороточного Са менее 1,8 ммоль/л или появлении клинических симптомов гипокальциемии (парестезии, бронхоспазм, ларингоспазм, симптомы Хвостека и Труссо, тетания и/или судороги) рекомендуется инфузия 10% раствора глюконата или хлорида кальция, увеличение концентрации Ca в диализирующем растворе.
Симптом Хвостека – это непроизвольное подергивание лицевых мышц при легком постукивании в области лицевого нерва (перед наружным слуховым проходом). Он присутствует у ≤ 10% здоровых людей и у большинства людей с острой гипокальциемией, но часто отсутствует при хронической гипокальциемии.
Симптом Труссо – это кистевой спазм, возникающий из-за уменьшения кровоснабжения руки с помощью жгута или манжеты тонометра, накачанной до 20 мм рт. ст. выше систолического артериального давления; манжету держат на предплечье в течение 3 минут. Этот симптом выявляется у пациентов с пониженным содержанием кальция.
При отсутствии эффекта или непереносимости терапии индивидуально решить вопрос о проведении повторной операции.
Факторами, влияющими на уровень сывороточного фосфора при ХБП, являются:
Целевой уровень Р достигается:
Основным источником фосфатов является белок. При превышении целевого диапазона сывороточного фосфора, потребление фосфора с пищей следует ограничивать до 800–1000 мг/день с коррекцией на пищевую потребность в белке. Рекомендуется потребление продуктов питания с отношением фосфаты (мг)/белок (г) менее 12 мг/г, с большим количеством растительных белков, отсутствием или самым низким содержанием неорганических фосфатов в пищевых добавках (A).
| А | У пациентов с додиализными стадиями ХБП в условиях нормофосфатемии (с целью снижения секреции FGF 23) не рекомендуется превентивное назначение любых ФСП вследствие возможного ускорения сосудистой кальцификации. |
| А | Учитывая высокий риск осложнений фосфат снижающими препаратами на основе кальция (гиперкальциемия, адинамическая болезнь кости, кальцификация сосудов) и алюминия (алюминиевая токсичность) у пациентов на ГД, рекомендуется применять фосфат снижающие препараты, не содержащие кальция алюминий. |
Гели алюминия – одна из наиболее эффективных форм фосфат-связывающих препаратов. Однако их широкое применение было ограничено из-за токсичности алюминия, проявляющейся так называемой «диализной» деменцией, нейропатией, микроцитарной анемией и остеомаляцией (из-за блокирующего включения алюминия во фронт минерализации остеоида). Алюминиевая интоксикации была широко распространена в 70–80-е года прошлого века, когда из-за несовершенства систем водоочистки основным источником алюминия, поступающего в организм пациента гемодиализа, была вода, используемая для приготовления диализирующего раствора. Применение же гелей алюминия в качестве ФСП имело лишь второстепенное значение.
| А | Фосфат-связывающие препараты на основе кальция (ацетат кальция, карбонат кальция) могут использоваться в качестве стартовой терапии гиперфосфатемии у пациентов с гипокальциемией или уровнем сывороточного Са в пределах целевого диапазона и при повышенном уровне ПТГ. |
| В | У детей с ХБП С3a-5D рекомендуется поддерживать Са сыворотки в соответствующем возрасту нормальном диапазоне. |
| В |
Максимальной суточной дозой Са-содержащих ФСП следует считать 1,5 г
элементарного Са, а суммарное потребление элементарного Са (включая потребление с пищей) не должно превышать 2,0 г/сутки. После назначения Са-содержащих ФСП требуется более частый (ежемесячный) контроль уровня Са в крови для исключения эпизодов гиперкальциемии.
|
У пациентов с ХБП 4-5D стадий с гиперфосфатемией рекомендуется отказаться от применения Са-содержащих ФСП при:
1. постоянной или рецидивирующей гиперкальциемии;
2. уровне ПТГ ниже целевых значений;
3. кальцинозе сосудов/кальцификации мягких тканей;
4. адинамической болезни кости;
| А | Терапия ФСП, не содержащими Са (севеламера гидрохлорид), приводит к снижению уровня холестерина, замедлению сердечно-сосудистой кальцификации, снижению сердечно-сосудистой и общей летальности у пациентов ХБП 5D стадии |
Исключить использование алюминий-содержащих ФСП при:
1. низком уровне иПТГ (B);
2. адинамической болезни кости (B);
3. гиперкальциемии (НГ);
4. одновременном назначении с препаратами витамина D (А).
Увеличение длительности сеансов гемодиализа на 0,5-1 час при трех процедурах в неделю, увеличение площади и проницаемости диализатора имеют ограниченные возможности в увеличении клиренса фосфатов из-за преимущественно внутриклеточного их содержания и медленного перемещения между секторами тела, приводящего к выраженному «эффекту рикошета».
В ходе короткого (4 часа) сеанса диализа существенно увеличить удаление фосфатов едва ли возможно. Известно, что фосфаты из «ближних пулов» организма (кровь, межклеточная жидкость) удаляются быстро, но их уровень так же быстро восстанавливается после окончания сеанса из-за перемещения из внутриклеточного пространства. Кроме того, эти вещества имеют склонность к агрегации нескольких молекул, что превращает их в довольно крупные соединения. Поэтому не следует рассчитывать на существенное увеличение удаления фосфатов при использовании более высокопоточных диализаторов или гемодиафильтрации (в сравнении с применяющимися в настоящее время типичными режимами высокоэффективного диализа). Наиболее доказанным способом повышения элиминации фосфатов можно считать увеличение длительности процедуры гемодиализа до 6–8 часов. За это время фосфаты успевают перейти во внутрисосудистый сектор и выводятся через мембрану диализатора. Другим направлением является увеличение кратности процедур, что позволяет чаще выводить фосфаты из внутрисосудистого сектора.
1. удлинением времени диализной сессии до 6-8 часов (исключить дефекты питания);
2. применением гемодиафильтрации on-line;
3. применением автоматического перитонеального диализа.
Контроль уровня сывороточного кальция
| А | При превышении верхней границы целевого уровня корректированного общего Са сыворотки, следует модифицировать терапию, которая может вызывать гиперкальциемию |
С целью коррекции гиперкальциемии у больных ХБП 3-5D стадии рекомендуется:
1. уменьшить дозу или отказаться от применения ФСП на основе кальция (А);
2. у пациентов с ВГПТ уменьшить дозу или отказаться от применения ВДРА до возвращения уровня корректированного общего Са сыворотки к целевым значениям;
3. при высоконормальном уровне Са (2,45-2,5 ммоль/л) на додиализных стадиях ХБП возможно назначение селективного ВДРА (парикальцитол) (А);
4. при сохранении гиперкальциемии, несмотря на модификацию терапии витамином D и/или прекращение приема Са-содержащих ФСП, больным с ХБП 5D назначить кальцимиметик (цинакальцет) (А);
5. провести дополнительный диагностический поиск других возможных причин повышения уровня сывороточного Са (множественная миелома, метастатическое поражение скелета, адинамическая болезнь кости и др. (А).
| В | При длительно существующей гиперкальциемии или гипокальциемии рекомендуется изменить концентрацию Са в диализате, поскольку гипокальциемия приводит к ускорению прогрессирования ВГПТ, а гиперкальциемия – к усилению сосудистой кальцификации. |
| А | У пациентов с гиперкальциемией рекомендуется понизить концентрацию Са в диализирующем растворе до 1,25 ммоль/л. |
Низкокальциевый диализат (1,25 ммоль/л и менее) может препятствовать дальнейшему снижению продукции ПТГ, прогрессированию адинамической болезни кости и внекостной кальцификации, способствовать коррекции гиперкальциемии и повысить эффективность препаратов витамина D (B).
При развитии гипокальциемии с клиническими симптомами, превышении целевых значений иПТГ рекомендуется терапия, направленная на повышение уровня Са:
1. назначение солей кальция (например, карбоната кальция) и/или
2. назначение или увеличение дозы препаратов витамина D при отсутствии значимой гиперфосфатемии и/или
3. снижение дозы или отмена кальцимиметика (В).
Адинамическая болезнь кости
Факторами риска низкообменной /адинамической болезни кости (АБК) являются:
1. возраст старше 65 лет;
2. сахарный диабет;
3. перитонеальный диализ;
4. увеличение нагрузки Са (высокое содержание Са в диализате, дополнительный прием препаратов Са, длительное применение больших доз Са-содержащих ФСП);
5. избыточно высокие дозы препаратов витамина D;
6. низкий уровень ПТГ;
7. ПТЭ в анамнезе;
8. перегрузка алюминием;
9. длительное предшествующее применение бифосфонатов.
Диагноз АБК можно предположить (при невозможности проведения костной биопсии) у пациентов с перечисленными факторами риска при:
1. стабильно низком или нормальном уровне ПТГ без терапии антипаратиреоидными средствами;
2. нормальном уровне ЩФ;
3. гиперкальциемии.
При АБК, имеющей высокие риски сосудистой кальцификации и переломов, рекомендуется предпринять все усилия для исключения гиперкальциемии и гиперфосфатемии (B), активации косного обмена и стимуляции секреции ПТГ (B):
1. отказ от применения Са-содержащих ФСП;
2. отказ от алюминий-содержащих ФСП;
3. применение диализирующего раствора с низкой концентрацией Са в диализате;
4. строгая диета с пониженным содержанием фосфатов и исключением неорганических фосфатов;
5. коррекция ацидоза;
6. исключить применение бифосфонатов и других антирезорбтивных агентов.
Кальцифилаксия
Кальцифилаксия – редкое тяжелое осложнение МКН-ХБП, характеризующееся прогрессирующей медианной кальцификацией сосудов кожи малого калибра (~100μм), сопровождающееся некрозами кожи и мягких тканей с выраженным болевым синдромом.
Кальцифилаксия резко снижает качество жизни и повышает смертность больных с ХБП 5Д стадией. Кальцифилаксия развивается преимущественно у больных на гемодиализе и в посттрансплантационном периоде, значительно реже у пациентов на перитонеальном диализе и никогда – на додиализных стадиях.
Вероятными факторами риска кальцифилаксии являются:
1. декомпенсированный ВГПТ;
2. гиперкальциемия и гиперфосфатемия;
3. гипоальбуминемия;
4. предшествующая терапия антагонистами витамина К (варфарин, синкумар);
5. ожирение, женский пол, терапия кортикостероидами;
6. длительная терапия метаболитами витамина D в высоких дозах;
7. заболевания печени;
Диагностика кальцифилаксии основывается в первую очередь на клинических признаках и данных рентгенографии (наиболее чувствительный вариант – маммографии), позволяющих выявить кальцификацию сосудов кожи. При возможности следует проводить радиоизотопное сканирование с технецием-99, повышенное накопление которого под кожей свидетельствует о кальцификации мелких сосудов.
Биопсия кожи повышает риск образования язвенных дефектов с последующим инфицированием.
Лечение кальцифилаксии
При возникновении кальцифилаксии рекомендуется направить усилия на коррекцию существующих факторов риска (А):
1. оптимизировать терапию ВГПТ (снизить дозу или отменить терапию метаболитами витамина D;
2. назначить или увеличить дозу кальцимиметиков (цинакальцет) (В);
3. при неэффективности медикаментозной терапии произвести ПТЭ (В);
4. нормализовать уровень альбумина плазмы;
5. назначить севеламера гидрохлорид в качестве ФСП;
6. использовать низкокальциевый диализат (1,25 ммоль/л);
7. увеличить продолжительность или частоту сеансов гемодиализа;
8. отказ от терапии варфарином с переходом на альтернативные антикоагулянты (гепарин или клопидогрель);
В качестве дополнительной терапии рекомендуется (А):
1. антисептическая обработка некротических очагов без хирургического удаления некротизированных тканей;
2. системная терапия инфекций (НГ);
3. назначение бифосфонатов в качестве антирезорбтивного (снижение уровня Са) и антицитокинового (противовоспалительного и обезболивающего) агента (В); 4. 25% раствор тиосульфата натрия внутривенно или внутрь
5. улучшение оксигенации тканей (гипербарическая оксигенация) (НГ)
6. терапия витамином К
7. ампутация конечности в неконтролируемой ситуации (НГ).
КОЖНЫЙ ЗУД
Клиника. Уремический зуд чаще всего поражает спину, но может также поражать руки, голову и живот [7,104]. У значительного числа больных отмечается генерализованный зуд. Он может длиться несколько минут каждый день или беспокоить постоянно [104].
Лабораторные исследования при уремическом зуде
Лечение устойчивого зуда
Пероральные антигистаминные препараты.
Гипертензия, развивающаяся непосредственно после начала, либо в течение процедуры диализа, при нормальном преддиализном уровне АД, называется интрадиализной гипертензией [108-110].
Лечение АГ у больных с ХБП С5D
| В | В большинстве случаев целесообразно начинать терапию препаратами, снижающими АД, при стойком повышении САД ≥ 140 или ДАД ≥ 90 мм рт. ст. и добиваться при хорошей переносимости достижения уровня САД < 140, но не ниже 120 и ДАД < 90, но не ниже 70 мм рт. ст. [3, 112]. |
Для пациентов, получающих лечение гемодиализом, характерна высокая лабильность АД, в связи с чем на фоне мощной антигипертензивной терапии возможны эпизоды гипотензии, связанные с риском ишемического поражения сердца и головного мозга, а также с гиперактивацией вазопрессорных гормональных систем, приводящих к дальнейшему резкому повышению АД [3, 36-41]. ЗПТ является основным средством снижения АД у пациентов с ТПН, исходя из этого развитие или нарастание тяжести АГ может быть одним из проявлений неадекватности диализа. [4] Имеются данные, что эффективный в отношении достижения «сухого веса» гемодиализ позволяет добиться нормализации АД у большинства пациентов с ХБП С5D [3, 36-41].
| А | Целевые уровни АД до диализа <140/80 мм рт. ст., после диализа <130/80 мм рт. ст. |
При каузальных измерениях АД для оценки эффективности антигипертензивной терапии следует ориентироваться на уровень АД непосредственно перед очередным сеансом гемодиализа. Для ответа на вопрос, насколько антигипертензивная терапия безопасна, следует учитывать измерения АД, выполненные в течение процедуры диализа. У пациентов с ХБП С5D при врачебных осмотрах также рекомендуется чаще выполнять тест на наличие постуральной (ортостатической) гипотензии [3, 18, 36-41].
ИАПФ и БРА, а также АК занимают важное место в лечении пациентов, получающих лечение диализом, благодаря их кардио и вазопротективным свойствам.
При назначении препаратов пролонгированного действия нужно учитывать, что многие из них подвергаются диализу. Рутинная отмена антигипертензивных препаратов перед началом ГД должна пересматриваться в пользу приема. Необходимо соблюдение кратности и длительности процедур, адекватных данным анализов пациента и режиму дозирования натрия (в соответствии с преддиализным уровнем), кальция (не превышать 1,5-1,75 ммоль/л) и калия (2 ммоль/л) диализата [36-41].
Препараты для купирования интрадиализной гипертензии: иАПФ короткого действия (каптоприл), производные дигидропиридина (нифедипин).
| А | При инициации ГД всем пациентам, независимо от наличия/отсутствия симптомов, рекомендуется оценка на риски развития кардиоваскулярных заболеваний, скрининг на традиционные и нетрадиционные риски кардиоваскулярных осложнений [3, 18, 36, 41]. |
| А | Эхо КГ должно проводиться сразу по достижении «сухого» веса (первые 1-3 месяца начала ГД) и повторяться регулярно с кратностью 1 раз в год или чаще по показаниям |
| А | Рекомендуется полное прекращение курения на ГД, рекомендуется регулярное проведение просветительных занятий на тему пользы прекращения курения на ГД с пациентами |
| А | Все пациенты на ГД с симптомами ОКС, кардиомиопатией должны получать лечение такое же, как в основной популяции, с учетом клиренса препаратов |
| А | Пациенты на ГД с аритмиями должны получать лечение как в основной популяции, искусственные водители ритма рекомендуется использовать с осторожностью (отсутствуют данные о безопасности использования в группе диализных больных, необходимость инвазивного введения, потенциальное взаимодействие с диализным катетером) |
| А | Пациенты на ГД с ОНМК должны получать лечение как в основной популяции, учитывая высокий риск геморрагических осложнений тромболитическая терапия должна применяться с осторожностью. |
Контроль АД и сохранение его в пределах 140/80 mm Hg достоверно снижает частоту гипертрофии левого желудочка и смертность. Причем, как снижение, так и повышение АД имеют неблагоприятное влияние на выживаемость и смертность больных на ГД [5, 18].
Пациенты с сахарным дибетом и ХБП С5 с автономной нейропатией, с CCЗ (CН, ГЛЖ с диастолической дисфункцией, заболеваниями клапанов сердца, перикардитом), с БЭН и гипоальбуминурией, с автономной дисфункцией МП, с тяжелой анемией, высокой междиализной прибавкой в весе, преддиализным САД менее 100 мм рт.ст., старше 65 л находятся в группе высокого риска развития интрадиализной гипотензии [5, 18].
| В | У пациентов на ГД с устойчивой гипотензией, симптомами сердечной недостаточности, сохраняющихся при достижении «сухого» веса, невозможность достижения «сухого» веса из-за частых эпизодов диализной гипотензии, рекомендуется проведение обследования на наличие коронарной болезни сердца. |
При необходимости проведения инвазивных процедур для диагностики и лечения КБС рекомендуется избегать использования внутренней яремной вены, брахиальной и радиальной артерии, т.к. они в дальнейшем могут использоваться для создания сосудистого доступа. С целью минимизации риска осложнений рекомендуется использование изо-осмолярных контрастов при проведении ангиографии.
| А | При проведении инвазивных процедур для диагностики и лечения КБС рекомендуется предварительная оценка риска геморрагических осложнений, наличие/степень анемии. |
| В | Индивидуализированное автоматическое управление ультрафильтрацией на основании показателей относительного объема крови позволяет снизить частоту интрадиализной гипотензии |
| В | Профилирование скорости ультрафильтрации позволяет снизить частоту интрадиализной гипотензии. Пульсирующие профили ультрафильтрации нежелательны |
| А | При использовании профилирования концентрации натрия в диализате или при создании высокого градиента по натрию между диализатом и плазмой необходимо учитывать возможность перегрузки организма пациента натрием, чреватой артериальной гипертензией, развитием жажды и увеличением междиализной гидратации |
| А | При неэффективности мероприятий, направленных на профилактику интрадиализной гипотензии, необходимо рассмотреть модификацию программы лечения в сторону увеличения частоты и/или продолжительности сеансов лечения, а также возможность перевода на лечение перитонеальным диализом. |
| А | Лечение КБС у пациентов на ГД по таким же принципам, как в основной популяции с учетом некоторых особенностей: необходимость достижения/поддержания «сухого» веса, необходимость достижения/поддержания целевого Нв крови, модификация режима дозирования препаратов с учетом проведения ГД/ГДФ (возможность ночного приема препаратов), у пациентов с сохранной остаточной функции почек назначение петлевых диуретиков может улучшить объем выделяемой мочи. |
| А | Снижение температуры диализата позволяет уменьшить частоту интрадиализной гипотензии. Избыточное снижение температуры может привести к относительной централизации кровообращения и увеличению «эффекта рикошета» после сеанса с общим снижением эффективности диализа. |
Факторы риска МС, ГС:
Пути решения: при возникновении МС рекомендовано введение гипертонического раствора натрия хлорида или декстрозы 40% (с осторожностью при АГ), болюсное введение изотонического раствора натрия хлорида 100-200 мл, снижение скорости УФ и местное применение тепла и легкого массажа для улучшения притока крови [5, 18].
Причины тошноты и рвоты на гемодиализе:
Пути решения: Необходима нормализация АД. Если тошнота продолжается, применяют противорвотные препараты (метоклопрамид). При рвоте нужно придать пациенту положение со слегка повышенным головным концом, повернуть голову в сторону, противоположенную АВФ, подать емкость (таз, лоток). Параллельно снизить скорость кровотока, пересмотреть уровень достигнутой и целевой УФ [5, 18].
Лечение
Профилактика
Причины:
Лечение:
Профилактика
Причины:
Алгоритм действия при болях в груди
Профилактика
Причины:
1. Бактериемия
2. Инфекция в области сосудистого доступа
3. Пирогенная реакция
4. Загрязнение аппарата для гемодиализа или раствора
5. Использование высокопроницаемого диализатора с бикарбонатным диализатом и повторное использование диализатора связаны с увеличенной частотой пирогенных реакций
Признаки и симптомы:
1. У пациентов с лихорадкой, связанной с пирогенами, перед диализом температура тела обычно бывает нормальной, но во время диализа она повышается.
2. У пациентов с бактериемией, связанной с сосудистым доступом, температура тела может быть повышенной как перед, так и во время и после диализа.
3. Краснота, болезненность или выделения в месте сосудистого доступа (см. раздел катетер-ассоциированная инфекция).
Тактика ведения
1. Взять анализ крови на бактериальный посев и чувствительность к антибиотикам.
2. Взять культуру экссудата на бактериальный посев, если он присутствует.
3. Собрать культуру диализата и воды.
4. Дать жаропонижающие препараты (аспирин или ацетаминофен).
5. Ввести антибиотики (согласно протоколу).
Профилактика
1. Правильная обработка воды.
2. Правильные техники подготовки оборудования и материалов и для начала процедуры диализа.
3. Не готовить диализатор или материалы заранее, т.е. раньше, чем за 2 часа до начала диализа.
4. Защитить пациента от известных инфекционных агентов (лечение ран и перевязка хирургической раны) во время диализа.
5. Правильный уход за концентратом жидкого бикарбоната (для избежания роста бактерий).
6. Правильный уход и чистка системы обработки воды и системы распределения воды.
7. Правильная чистка и уход за всеми контейнерами концентрата.
8. Использование диализного фильтра, особенно при использовании высокопоточного диализатора.
КРОВОПОТЕРЯ
1. Разрыв или отсоединение кровопроводящих магистралей 2. Отсоединение крышки от катетера или катетера от кровеносного сосуда. 3. Выход диализной иглы из места сосудистого доступа. 4. Мониторы кровопроводящих магистралей (артериальные и/или венозные) неправильно установлены, и пределы тревоги не активированы. 5. Отказ (неисправность) детектора кровотечения. 6. Разрыв аневризмы или анастомоза фистулы. 7. Избыточная гепаринизация (внутреннее кровотечение).
Признаки и симптомы
1. Источник кровотечения обычно явно виден. (см клиническое руководство МЗ КР «ЖКТ кровотечения»)
2. Судороги, рвота и шок могут привести к смерти
Тактика ведения
1. Закрепить кровопроводящие магистрали.
2. Остановить кровяной насос.
3. При возможности сдавить место кровотечения.
4. Оценить возможность возврата крови больному
5. При значительной потере крови подключить кислород.
6. Перезапустить процедуру, если это необходимо.
7. Провести гемотрансфузию, ввести инфузионные жидкости по необходимости (восполнить ОЦК).
Профилактика
1. Закрепить все кровопроводящие магистрали и соединения сосудистого доступа к коже.
2. Если соединения не являются «Луер-лок», необходимо использовать ленту
3. Закрепить место введения игл лентой, чтобы избежать их движения и выпадения
4. Непрерывно наблюдать за экстракорпоральной цепью и сосудистым доступом пациента.
5. В комнате, где проводится диализ, должен быть включен свет.
6. Не допускать, чтобы пациент закрывал место сосудистого доступа.
7. Правильно заправить кровопроводящие магистрали к насосному сегменту.
8. Верхний предел артериального давления не должен превышать -20 мм рт. ст. (до насоса).
Дифференциальный диагноз:
Технические проблемы: массивная воздушная эмболия, острый гемолиз, массивная кровопотеря, анафилактическая реакция на диализатор, дезинфицирующее средство или инъекционный лекарственный препарат, небезопасный состав диализата.
Режим диализа
Медикаментозные методы
Привлечение консультантов
СИНДРОМ ДИСЭКВИЛИБРИУМА
Комплекс системных и неврологических симптомов, связанных с характерными ЭЭГ-изменениями, которые могут происходить во время или после диализа. Состояние может быть легким или тяжелым. Ранние проявления включают тошноту, рвоту, беспокойство и головную боль. Более серьезные проявления включают судороги, помрачение сознания и кому. Синдром часто наблюдается при инициации гемодиализа у пациентов с высоким уровнем мочевины.
Причины:
2. Острое изменение pH цереброспинальной жидкости во время диализа.
3. Больные с выраженной уремией и очень высокими значениями уровня азота мочевины в сыворотке крови часто подвержены продолжительному диализу.
Тактика ведения
1. Снижение скорости кровотока для уменьшения удаления растворенных веществ и изменений pH.
2. Введение гипертонического раствора хлорида натрия, 40% глюкозы или маннитола.
3. Лечение неукротимой тошноты и рвоты.
4. Прекращение диализа, если возникают судороги, помрачение сознания или кома.
5. Лечение судорог противосудорожными препаратами (расписать прием препаратов магния)
Профилактика
1. У новых пациентов с тяжелой уремией и очень высоким уровнем мочевины сыворотки крови следует проводить короткие и частые сеансы диализа (два часа дневного диализа в течение 3 дней). Возможно развитие отека мозга. Это приведет к более медленному удалению мочевины.
2. Использование менее эффективного диализатора при очень высоком уровне мочевины сыворотки крови.
3. Использование более низкой скорости кровотока при очень высоком уровне мочевины сыворотки крови.
4. Дать кислород больным без задержки СО2.
5. Использование более высокой концентрации натрия для противодействия или замедления падения осмотического давления плазмы
6. Целевое снижение уровня мочевины сыворотки крови вначале следует ограничивать примерно до 40%.
Проявления:
1. Одышка
2. Чувство грозящей опасности
3. Чувство тепла на месте фистулы или по всему телу
4. Может произойти остановка сердца и даже смерть.
Более легкие формы могут проявляться:
1. Зуд
2. Крапивница
3. Кашель
4. Боли в животе или диарея
5. Чихание
6. Насморк
7. Слезотечение
Пациенты с атопией и/или эозинофилией в анамнезе склонны к развитию этих реакций. Симптомы обычно появляются в течение первых нескольких минут диализа, но иногда их появление может задерживаться на 30 минут или более.
1. В конце 1970-х годов окись этилена использовалась для стерилизации почти всех диализных мембран. Гиперчувствительность к окиси этилена наблюдалась исключительно при первом использовании диализаторов, часто после недостаточного промывания.
2. Зараженный диализный раствор бактериями и эндотоксинами; такие реакции возникают в течение 2 минут после начала диализа (реакции, связанные с комплементом, проявляются с позже (15-30 минут)).
3. Недостаточная промывка диализаторов при подготовке АИП к процедуре ГД.
4. Повторное использование диализаторов
5. Гепарин иногда ассоциируется с аллергическими реакциями, включая крапивницу, насморк, свистящее дыхание и даже анафилаксию.
6. Эозинофилия. У пациентов с очень высоким количеством эозинофилов возникают тяжелые реакции на диализ, которые связывают с внезапной дегрануляцией эозинофилов с выделением бронхоспастических и других медиаторов.
Тактика ведения
1. Немедленно остановить диализ.
2. Зажать кровопроводящие магистрали.
3. Утилизировать диализатор и магистрали.
4. Не возвращать содержащуюся кровь пациенту.
5. В зависимости от тяжести реакции могут быть назначены внутривенные антигистаминные препараты, стероиды и эпинефрин.
1. Использование синтетической полисульфоновой мембраны
2. Правильное промывание диализаторов перед использованием для устранения остаточного этиленоксида и других аллергенов
3. У пациентов с реакцией типа A на диализатор, подвергшийся стерилизации этиленоксидом в анамнезе, использовать диализаторы со стерилизацией гамма-излучением или паром.
4. Предварительное введение антигистаминных препаратов перед диализом тем пациентам, у которых после перехода на оборудование без этиленоксида продолжаются легкие симптомы типа A.
НЕСПЕЦИФИЧЕСКАЯ РЕАКЦИЯ НА ДИАЛИЗАТОР ТИПА В
Симптомы:
2. Симптомы обычно возникают через 20-40 минут после начала диализа.
3. Реакции типа B гораздо менее тяжелые, чем реакции типа A.
Этиология: Причина неизвестна, но предполагается активация комплемента.
Лечение:
1. Симптоматическое лечение
2. Назальный кислород
3. Если подозревается ишемическая болезнь сердца, лечить соответствующим образом.
4. Продолжать диализ, как только симптомы уменьшатся после первого часа.
Профилактика: Попробуйте использовать синтетическую полисульфонную мембрану.
ВНУТРИЧЕРЕПНОЕ КРОВОИЗЛИЯНИЕ
Имеющееся основное сосудистое заболевание и гипертония, в совокупности с применением гепарина, иногда могут осложниться внутричерепными, субарахноидальными или субдуральными кровоизлияниями. Оценка сознания по Шкале Глазго (см клиническое руководство МЗ КР «Инсульты»)
Нейрохирург должен немедленно оценить состояние пациента.
Острый гемолиз во время диализа является экстренной ситуацией.
Симптомы
1. Боль в спине
2. Боль в груди и одышка
3. Чувство жара.
Признаки
1. Ярко-красный цвет крови в венозном контуре магистрали
2. Розоватая окраска плазмы в центрифугированной крови
3. Значительное падение гематокрита
4. Гипотония
Последствия:
1. Гиперкалиемия вследствие высвобождения калия из гемолизированных эритроцитов
2. Мышечная слабость
3. Изменения на ЭКГ вследствие гиперкалиемии
4. Остановка сердца
Острый гемолиз был зафиксирован в двух основных случаях:
1. Обструкция или стеноз в кровопроводящих магистралях, катетере или игле.
2. Проблемы с диализным раствором, включая:
1) перегретый раствор для диализа
2) гипотонический раствор для диализа
3) раствор для диализа, загрязненный формальдегидом, хлорамином, медью (из медных труб), фторидами, нитратами, цинком и перекисью водорода.
Тактика
1. Немедленно пережать венозную магистраль кровотока. Не возвращать гемолизированную кровь.
2. Прекратить процедуру диализа, но оставить одну иглу на месте.
3. Следить за показателями жизненных функций и наблюдать за появлением аритмий, гипотензии и одышки.
4. Дать кислород. 5. Немедленно проверить уровень калия и гемоглобина.
6. Внутривенное ведение дексаметазона 8-16 мг, антигистаминных препаратов и физиологического раствора 500-1000 мл.
7. Незамедлительно вызвать реанимационную бригаду СМП и госпитализировать больного в стационар под наблюдением в течение 24 часов.
1. Проверять проводимость и температуру диализата непосредственно перед началом диализа.
2. Перед началом процедуры диализа проверять на отсутствие дезинфицирующих химических веществ в системе водоочистки и системе приготовления диализата, и документировать это.
3. Проводить регулярное плановое техническое обслуживание мониторов, сигнализации и байпас механизмов.
4. Перед началом диализа проверять, что байпас клапан диализата функционирует.
5. Устанавливать более низкий предел для монитора артериального давления, чтобы уменьшить повреждение клеток, вызванное насосом (меньшее отрицательное давление).
6. Устанавливать лимиты в 20 мм рт.ст. от показаний давления.
7. Лимиты не должны превышать –250 мм рт.ст. (для монитора артериального давления).
8. Не использовать медные трубы в системе очистки воды для диализа, в системе распределения воды и/или системе приготовления диализата.
9. Включать использование угольной фильтрации в системе водоочистки для удаления хлораминов, вызывающих гемолиз.
ВОЗДУШНАЯ ЭМБОЛИЯ
Симптомы
Они отчасти зависят от положения пациента.
• У пациентов, находящихся в положении сидя, попавший в кровоток воздух склонен мигрировать в венозное русло мозга, вызывая потерю сознания, судороги и даже смерть.
• У пациентов, находящихся в положении лежа, воздух склонен попадать в сердце и образовывать пену в легких, вызывая одышку, кашель, стеснение в груди и аритмии. Дальнейшее прохождение воздуха через капилляры легких в левый желудочек может привести к воздушной эмболии артерий мозга и сердца, с острой неврологической и сердечной дисфункцией.
• Пена может быть видна в венозной магистрали. Если воздух попал в сердце, при аускультации выслушивается особый шум, напоминающий бульканье.
Этиология
Наиболее распространенными местами, откуда происходит попадание воздуха являются:
1. Артериальная игла
2. Артериальный сегмент перед насосом
3. Непреднамеренно открытый конец центрального венозного катетера
1. Немедленно прекратить введение воздуха.
2. Положить пациента на левый бок в положение Тренделенбурга (голова вниз, ноги вверх).
1) Удерживать воздух в вершине правого желудочка.
2) Предотвратить попадание воздуха в легочную вену.
3) Предотвратить блокировку воздухом в легочной вене.
4) Предотвратить перемещение воздушных пузырей в другие органы.
3. Дать кислород. Пациенту может потребоваться интубация.
Профилактика
1. Использовать только растворы для внутривенного введения, которые не имеют вентиляционных отверстий и не могут впускать воздух, в гибких мешках, которые могут изменять свою форму и объем при вытеснении жидкости или газа изнутри. Не использовать бутылки; если вынуждены это делать, то не оставлять их без присмотра.
2. Не использовать вентилируемые кровопроводящие магистрали.
3. Не использовать растворы для инъекций в вентилируемых стеклянных или пластиковых бутылках.
4. Не вводить растворы для инъекций медленно (капельно) в кровопроводящую магистраль. Использовать раствор для инъекций в виде болюса, а не медленной инфузии.
5. Не использовать воздух для возвращения крови в конце гемодиализа. Верните кровь пациента с помощью инфузионного солевого раствора.
6. Корректно использовать детектор воздуха/пены на протяжении всей процедуры. Детектор воздуха/пены должен использоваться в начале процедуры, во время процедуры и в конце процедуры.
7. Все соединения должны быть надежно закручены. Закрепить лентой все соединения, которые не имеют дизайна Луер-лок.
8. Не игнорировать звуковой сигнал детектора, внимательно осматривать венозную магистраль на наличие воздуха/пены.
Лечение
РЕКОМЕНДАЦИИ ПО ЛЕЧЕНИЮ ХБП С4-5
Лечение в основном зависит от тяжести заболевания и фокусируется на следующих принципах:
• ЗПТ (гемодиализ, перитонеальный диализ, трансплантация)
• нефропротективная терапия
• кардиопротективная терапия
• коррекция анемии
• коррекция минерально-костных нарушений
• коррекция нарушений липидного обмена
• коррекция метаболического ацидоза
• коррекция электролитных нарушений
• коррекция гиперурикемии.
НЕ НАЗНАЧАТЬ НЕДОКАЗАННЫЕ ПРЕПАРАТЫ – травы, препараты для снижения креатинина (L – аргинин, сорбенты и др.).
Утвержденные в КР стандарты диализного лечения больных с ХБП 4-5D стадий определяют требования к процессу оказания медицинской помощи населению в амбулаторных и стационарных условиях районных, городских, областных и республиканских муниципальных организаций здравоохранения. “Клиническое руководство по диагностике и лечению хронической болезни почек 4-5 D и принципы диетотерапии”. Приказ МЗ КР №785 от 21.11.2018г.
Пациенты с тяжелой уремией, находящиеся в отделениях реанимации всех уровней организации здравоохранения МЗ КР, где имеется специальная аппаратура для проведения гемодиализа, по жизненым показаниям в экстренном порядке должны получать ЗПТ до стабилизации состояния по месту нахождения.
Вопрос о превентивной трансплантации почки от живого донора у взрослых следует рассматривать при СКФ <20 мл/мин/1,73 м2 и доказанной прогрессирующей и необратимой ХБП в течение предшествующих 6 - 12 месяцев [7,17].
Метод детоксикации и гемокоррекции организма перитонеальным диализом проводится с использованием в качестве диализатора собственно брюшную полость пациента. А роль мембраны выполняет перитонеальная мембрана (брюшина). Около двух литров диализной жидкости медленно вливаются в брюшную полость с помощью гибкой силиконовой трубки – катетера. Вода и растворенные вещества из крови перемещаются в диализат, проходя через брюшину, которая представляет собой тончайший слой, покрывающий кишечник и печень. Диализат в брюшной полости находится до 2х часов. За это время метаболические отходы и избыточная жидкость из организма (сосудистого русла, пронизывающего и оплетающего брюшину) стремятся в диализат под действием градиента концентрации, до тех пор, пока концентрации веществ, растворенных в крови и в диализате не сравняются [15, 16]. Перемещение жидкости и метаболических отходов происходит в процессе так называемого «обмена». Спустя определенное количество времени, которое занимает процедура обмена, диализат вновь сливается посредством катетера. Затем диализирующую жидкость заменяют свежей, после чего процедура перитонеального диализа может продолжаться. Процесс замены старой диализной жидкости свежей и называется обменом. Обмен повторяют несколько раз в день (как правило, 4-5 раз). Чтобы повысить эффективность метода, интенсифицируют кратность ручного обмена жидкости или применяют аппаратный обмен [15, 16].
Показание: Решение о начале диализа должно основываться на клинических данных и не опираться только на расчет СКФ.
НАЧАЛО: У пациентов с ХБП С5 экстренный гемодиализ должен быть начат при наличии одного и, тем более, сочетании следующих симптомов [3-5, 13,14, 18]:
Концепция раннего или своевременного начала гемодиализа
| С | Больным с ХБП С5 рекомендуется более раннее начало ЗПТ [5, 13, 14, 18]. |
Традиционные показания к ЗПТ, разработанные для пациентов с ХБП, не всегда применимы к больным с ОПП на фоне существующей ХБП. Например, тяжелая гипергидратация, возникающая в результате восполнения объема жидкости, может быть показанием к началу ЗПТ даже при отсутствии значительного повышения уровней азота мочевины или креатинина в крови у пациентов, исходя из этого данный метод необходимо рассматривать как вид «поддерживающей», а не «заместительной» почечной терапии [5, 13, 14, 18].
Выбор метода ЗПТ
Относительные показания к началу диализа включают:
| В | Рекомендуется стандартный центральный венозный двухпросветный катетер (предпочтительней, чем использование в качестве первого доступа туннельного манжеточного катетера) [2]. |
| А | Применение двухпросветного «острого, временного» нетуннельного катетера нежелательно, но допустимо при острой необходимости срочного формирования доступа и невозможности иных вариантов. Такой катетер насколько возможно быстро должен быть заменен на АВФ, протез или туннельный катетер [5, 13, 14]. |
| В | При имплантации диализного катетера во внутреннюю яремную или подключичную вену рекомендуется проводить диагностическую рентгенографию органов грудной клетки сразу после установки катетера и перед первым его использованием |
| А | Рекомендуется устанавливать центральный венозный катетер при помощи ультразвукового наведения. |
Золотым стандартом является высококачественная нативная АВФ, которая доступна для большинства пациентов. АВФ долговечна, отличается самым низким уровнем осложнений, не требует значимых дополнительных вмешательств, экономична [5, 13, 14, 25].
Правила проверки состояния фистулы
|
Осмотреть руку с установленной фистулой
|
Визуально оценить наличие:
- покраснений
- припухлостей
|
| Проверить кровоток через фистулу |
С помощью стетоскопа прослушать наличие «шума»
Прикоснуться к фистуле рукой
Оценить наличие ритмической вибрации (дрожания)
|
| Проверить наличие осложнений |
Прикосновением проверить повышение температуры в области фистулы
Оценить наличие болезненности при прикосновении
|
Правила ухода за артерио-венозной фистулой (Приложение 2).
Порядок выбора точек для имплантации диализного катетера у детей:
|
Вес ребенка (кг)
|
Калибр катетера (Fr) | Длина катетера (см) |
| Двойной просвет | ||
|
от 3 до 10
|
7 или 8 | от 7 до 15 |
|
>10 до 20
|
9 или 10 | от 10 до 20 |
|
>20 до 30
|
от 10 до 11,5 | от 12 до 24 |
|
>30 до 40
|
от 11,5 до 12,5 | от 20 до 30 |
|
>40 до 50
|
от 12,5 до 14 | от 30 до 40 |
|
>50
|
от 14 до 16 | 40 |
| Однопросветный | ||
|
<5
|
6,5 | 29 или 32 |
|
>10
|
10 | 36 или 40 |
Инфекционные осложнения. Нельзя пунктировать фистулу, если есть признаки ее инфицирования. Поверхностно инфицированная фистула может вызывать распространение инфекции в кровоток. Это приводит к сепсису, а это одна из главных причин смерти гемодиализных больных. Пациенты должны быть обучены уходу за фистулой, в случае появления признаков инфекции немедленно обращаться к нефрологу относительно возможности пункции и назначения антибиотикотерапии.
Экссангвинация (серьѐзная потеря крови) может произойти при выпадении иглы, разъединении кровяной линии или разрыва фистулы. Чтобы не допускать возможности выхода иглы из сосуда, еѐ следует надежно фиксировать липкой лентой. Кровяные линии должны быть безупречно соединены, а лимиты артериального и венозного давления на мониторе установлены так, чтобы можно было тотчас распознать утечку крови. Детектор воздух/пена и мониторы артериального и венозного давления могут помочь избежать кровопотери, если они исправно работают. Но иногда кровопотерю может вызвать смещение иглы во время гемодиализа. При этом подтекание крови будет недостаточным, чтобы упало венозное давление и сработал сигнал тревоги. В результате персонал может не заметить подтекание крови, если рука пациента закрыта одеялом.
Воздушная эмболия. Воздух, попавший в циркуляцию крови пациента, может остановить кровоток, как настоящий тромб. Если в циркуляцию попало много воздуха, сердце начинает перекачивать пену вместо жидкой крови. Эффективность работы сердца падает, иногда вплоть до остановки. Кровяная пена в легких вызывает расстройство дыхания. Кровяная пена в сосудах мозга может привести к инсульту. Клиническая картина воздушной эмболии зависит от того, куда попал воздух: может быть возбуждение больного, затруднение дыхания, цианоз, расстройства зрения, снижение артериального давления, нарушения сознания, параличи. Следует обучить пациента наблюдению за своими кровяными линиями, чтобы была уверенность в том, что воздух в кровяную линию не попал. Не должно быть воздуха на участке кровяной линии от детектора воздух/пена (ниже венозной ловушки) до пациента. Если воздух попадает в артериальную линию перед диализатором, он ловится в артериальной ловушке, которая находится перед входом в диализатор. Детектор воздух/пена должен остановить насос крови, если в венозной ловушке появился воздух.
Инфильтрация/гематома. Инфильтрация возникает, когда игла проходит вену насквозь, выходя с другой стороны сосуда, или делает надрыв, позволяющий крови вытекать в окружающие ткани. Инфильтрация - самое частое осложнение пункции фистулы.. Инфильтрация вредит доступу и может привести к его недостаточности. У пациента инфильтрация вызывает боль, чувство жжения, возникает необходимость дополнительной пункции, пациент теряет доверие к персоналу. Кровь, попавшая в ткани вокруг сосуда, вызывает в этой области выбухание, уплотнение и иногда покраснение.
Кровотечение во время гемодиализа. Кровотечение во время гемодиализа может быть незначительной проблемой (просачивание крови из-под иглы) или угрожающим (если игла выскочила, а насос крови работает). Частая, даже незначительная потеря крови во время гемодиализа способствует развитию диализной анемии.
Рециркуляция. Рециркуляция возникает, когда очищенная венозная кровь частично смешивается с кровью, поступающей в артериальную иглу. Это смешение означает, что уже очищенная кровь вновь поступает в диализатор для новой очистки, в то время как оставшаяся кровь очищается недостаточно. Таким образом, рециркуляция делает гемодиализ менее эффективным. Со временем «плохой» диализ приводит к появлению симптомов уремии. Рециркуляция возникает в следующих случаях: кровоток по фистуле ниже, чем в диализаторе (< 300-500 мл/мин); иглы расположены слишком близко друг от друга; обратное подсоединение кровяных линий; имеется стеноз фистулы.
Синдром обкрадывания. Его возникновение связано с уменьшением кровотока в конечности из-за сброса по фистуле части артериальной крови в венозный кровоток. Синдром обкрадывания состоит из симптомов, обусловленных гипоксией тканей конечности, на которой расположен доступ: боли в конечности с доступом; покалывание или пощипывание в конечности с доступом; ощущение холода в конечности с доступом; изменение моторных навыков руки; ногтевые ложа становятся голубого цвета; некротические (омертвевшие, черные) пятна на коже; потеря чувствительности конечности с доступом
Аневризма. Пункция фистулы в одно и тоже место через некоторое время приводит к образованию аневризмы. Шаблонная пункция приводит к слабости мышечной стенки фистулы, образованию выпячиваний и «надутому» виду фистулы. Со временем поток крови в изначально нормальной фистуле продолжает расти и фистульная вена расширяется. Аневризма чаще образуется «вверх» по течению крови, ретроградно от венозного стеноза, особенно в местах повторных пункций. Эти места легко определяются на взгляд. Для предотвращения образования аневризм необходимо использовать метод ротации мест пункции или пункцию по методу «петлицы». Аневризмы существенно сокращают наличие мест для пункции. Если на коже появились признаки угрожающего разрыва, такие как истончение, изъязвление или кровотечение, необходимо хирургическое вмешательство.
Существует три области, где наиболее часто образуется стеноз: приток – наиболее частый вид стеноза в области анастомоза артерии и вены. Его часто называют юкста-анастомозный стеноз (ЮАС). Он образуется в вене тотчас после анастомоза. ЮАС не дает фистуле созреть, так как не пропускает достаточно крови в фистулу. ЮАС возникает вследствие растяжения, перекрута или другой травмы при наложении фистулы. При пальпации ЮАС определяется как уплощение тотчас за анастомозом; отток – стеноз может располагаться где угодно по ходу оттекающей вены. Например, в месте, где ранее больному пунктировали вену. Вена после стеноза имеет небольшой диаметр, что делает пункцию трудной и повышает вероятность инфильтрации; центральная вена - стеноз центральных вен возникает в крупных венах руки, часто в области плеча. Если подозревается стеноз, необходимо проверить всю венозную систему от анастомоза до сердца. Только так можно выявить центральный стеноз. Эти стенозы чаще всего возникают вследствие катетеризации центральных вен в прошлом.
Тромбоз (образование тромба или сгустка крови) возникает во всех типах сосудистого доступа, но фистулы тромбируются в 6 раз реже, чем протезы. Ранний тромбоз чаще всего связан с хирургическими проблемами или с перекрутом сосудов. Тромбоз возникает также вследствие стеноза, сниженного кровотока при гипотензии на диализе, остановки сердца или компрессии сосудов. Сдавление сосудов может произойти после операции, если кровь вытекает в ткани с образованием гематомы. Гематома может образовываться в результате инфильтрации при пункции, или при слишком раннем использовании фистулы после операции для доступа к циркуляции. Длительное прижатие фистулы под давлением после пункции также может вызвать тромбоз. Не следует прижимать место пункции более 20 минут. Если кровотечение продолжается более 20 минут, медсестра должна проверить дозу введенного гепарина и осмотреть доступ на предмет возможного стеноза или других проблем. Поздние тромбозы могут возникать и в работающих фистулах. Их вызывает турбуленция в области стеноза. Нелеченый тромбоз может погубить фистулу. Тромбоз чаще всего возникает вследствие стеноза или низкой скорости кровотока.
Мониторинг сосудистого доступа позволяет выявить пациентов с риском развития тромбоза. KDOQI (Clinical Practice Guidelines for Vascular Access) рекомендует программу мониторинга доступа. Мониторинг АВФ состоит из измерения статического и динамического венозного давления, измерения скорости кровотока и дуплексного ультразвука. Программа мониторинга доступа помогает повысить уровень выживаемости доступа за счет раннего выявления проблем. Тромбоэктомия доступа может быть выполнена хирургически, механически и химически (применение препаратов, которые растворяют тромб). Более чем в 90% случаев причиной тромбоза является стеноз. Стеноз можно исправить хирургически или с помощью ангиопластики после удаления тромба.
Пациенты с сердечной недостаточностью вследствие высокого выброса имеют учащенный пульс, так как их сердце должно перекачивать дополнительный объем крови, поступающий из доступа (20 % и более). У пациентов может быть одышка, отеки на фистульной руке или ноге вследствие плохого оттока крови к сердцу, со временем может развиться полная декомпенсация сердечной деятельности с гидротораксом, асцитом, нарушением сердечного ритма. Сердечная недостаточность с высоким выбросом также возникает при анемии или вследствие заболеваний сердца, которые были у пациента до установки доступа к циркуляции. Поэтому лучшим способом профилактики сердечной недостаточности с высоким выбросом является коррекция анемии и создание доступа, гемодинамически наименее значимого для сердца. Если сердечная недостаточность с высоким выбросом уже имеется, следует ограничить междиализную прибавку веса, что может существенно снизить нагрузку на сердце. Решению проблемы может помочь более длительный или более частый диализ, медикаментозное лечение сердечной недостаточности, постоянный контроль общего самочувствия и уровня активности пациентов. Иногда может потребоваться хирургическое вмешательство для снижения сброса крови по доступу в виде стяжки анастомоза или полной перевязки фистулы.
| А | Гемодиализ/Гемодиафильтрацию следует проводить не менее 3-х раз в неделю, и общее эффективное диализное время должно быть не менее 720 минут в неделю, за исключением случаев значительной остаточной почечной функции. Двухразовый в неделю диализ неприемлем [5, 13, 14, 25]. |
| А |
При необходимости, например, при невозможности достичь требуемой эффективности за 4 часа или при выраженной гемодинамической нестабильности в ходе сеанса гемодиализа, при неконтролируемой фосфатемии, выраженном нарушении статуса питания число и/или продолжительность сеансов лечения могут быть увеличены, по решению консилиума [5, 13, 14, 25].
При необходимости, по решению консилиума, число и/или продолжительность сеансов лечения могут быть увеличены в следующих случаях: при невозможности достичь требуемой эффективности за 4 часа, выраженной гемодинамической нестабильности в ходе сеанса гемодиализа, неконтролируемой фосфатемии, выраженном нарушении статуса питания.
|
Экстракорпоральный диализ (прерывистый, продолжительный, продленный) специализированный полуселективный мембранный метод диализа с использованием аппаратов «искусственная почка» (АИП), основанный на принципе переноса через полупроницаемую мембрану, изготовленную из естественных или синтетических материалов, воды и растворенных в ней молекул за счет градиента концентрации и градиента давления [9, 14].
Забираемая из сосудистого доступа кровь циркулирует через экстракорпоральный контур, состоящий из магистралей и фильтра. Во время процедуры в фильтре происходит эффективное удаление из крови воды и низкомолекулярных компонентов крови, токсических веществ и продуктов метаболизма, нормализация нарушений водного и электролитного баланса [9, 10]. Белки, форменные элементы крови, бактерии и вещества с молекулярной массой более 30000 через мембрану не проходят. Очищенная кровь затем возвращается в организм больного через сформированный сосудистый доступ.
Гемодиализ прерывистый (интермитирующий) – специализированный полуселективный мембранный метод экстракорпорального диализа с использованием АИП, основанный на принципе диффузионного и фильтрационного переноса через полупроницаемую мембрану, изготовленную из естественных или синтетических материалов. Забираемая из сосудистого доступа кровь пропускается через гемодиализатор и находится с одной стороны от полупроницаемой мембраны Low Flux, в то время как раствор, по своему электролитному составу близкий к циркулирующей крови, прокачивается с другой стороны от нее. В большинстве случаев скорость кровотока составляет более 200 мл/мин, диализата более 300 мл/мин, длительность процедуры до 6 часов, поэтому требуется проведение болюсной или непрерывной антикоагуляции. Для выполнения процедур требуется сложная инфраструктура (вода, электричество), комплекс оборудования (водоподготовка; при отсутствии готового концентрата, оборудование для его подготовки и, при необходимости, раздачи концентрата) и высококвалифицированный медицинский персонал. Процедура проводится в условиях стационара, дневного стационара, амбулаторно, в домашних условиях пациентам ХБП С5D.
Интермитирующий гемодиализ может проводиться помимо стандартного в вариантах короткого ежедневного или ночного гемодиализа. В связи с высокой частотой и/или длительностью диализной сессии данные варианты гемодиализа чаще проводятся амбулаторно в домашних условиях, где стационарно устанавливаются система водоподготовки и АИП. Пациент и /или «помощник» - обычно родственник, проходят специальную подготовку, подключение и отключения больного проводит приезжающая медицинская сестра.
Гемодиализ ночной (еженощный) проводится 3-6 раз в неделю в ночное время с длительностью каждой сессии от 6 до 8 часов с целью повышения дозы и переносимости диализного лечения за счет улучшения выведения токсинов низкой и средней молекулярной массы, уменьшения колебаний уровней токсемии и гидратации [5].
Гемодиализ интермиттирующий, низкопоточный - специализированный полуселективный мембранный метод экстракорпорального диализа с использованием АИП, основанный на принципе диффузионного и фильтрационного переноса через низкопоточную мембрану, изготовленную из естественных или синтетических материалов. Забираемая из сосудистого доступа кровь пропускается через гемодиализатор и находится с одной стороны от полупроницаемой мембраны Low Flux, в то время как раствор, по своему электролитному составу близкий циркулирующей крови, прокачивается с другой стороны от нее. Проводится в условиях стационара, дневного стационара, амбулаторно в домашних условиях пациентам ХБП С5D [5].
Гемодиализ интермиттирующий высокопоточный – специализированный полуселективный мембранный метод экстракорпорального диализа с использованием АИП, основанный на принципе диффузионного и фильтрационного переноса через высокопоточную мембрану, изготовленную из модифицированных естественных или синтетических материалов. Забираемая из сосудистого доступа кровь пропускается через гемодиализатор и находится с одной стороны от полупроницаемой мембраны High Flux, в то время как раствор повышенной очистки (ультрачистый), по своему электролитному составу близкий циркулирующей крови, прокачивается с другой стороны от нее. Проводится в условиях стационара, дневного стационара, амбулаторно, в домашних условиях пациентам ХБП С5D [5].
Гемодиафильтрация, (гемодиафильтрация интермиттирующая) – специализированный полуселективный мембранный метод экстракорпорального диализа с использованием модифицированных АИП. Метод основан на принципе диффузионного, фильтрационного и конвекционного переноса через высокопроницаемую, высокопоточную мембрану High Flux воды и растворенных в ней молекул за счет градиента концентрации и давления, обеспечивающий эффективное удаление из крови воды и низко- и средне молекулярных субстанций плазмы крови. В большинстве случаев для проведения прерывистой (интермиттирующей) гемодиафильтрации требуются скорость кровотока более 300 мл/мин., диализата – более 350 мл/мин., длительность процедуры до 6 часов, массивная УФ с одновременным замещением сбалансированным раствором, либо заранее приготовленным, либо приготовляемым непосредственно аппаратом (on line) из диализирующего раствора повышенной очистки (ультрачистого) в процессе проведения процедуры. Требуется проведение болюсной или непрерывной антикоагуляции. Для выполнения процедур требуется высококвалифицированный персонал, сложная инфраструктура (вода, электричество), комплекс оборудования (водоподготовка; при отсутствие готового концентрата, оборудование для его подготовки и, при необходимости, раздачи концентрата). Проводится в условиях стационара, дневного стационара, амбулаторно, в домашних условиях пациентам ХБП С5D [5].
Ультрафильтрация крови, ультрафильтрация изолированная – специализированный полуселективный мембранный метод экстракорпорального диализа с использованием АИП, основанный на принципе переноса через полупроницаемую низкопоточную мембрану Low Flux воды и растворенных в ней молекул за счет градиента давления, обеспечивающий эффективное дозированное удаление из крови воды. Производится путем создания трансмембранного давления в экстракорпоральном контуре при циркуляции крови со скоростью более 200 мл/мин в течение менее 6 часов, без потока диализата. Скорость ультрафильтрации 5-15 мл/мин. От величины трансмембранного давления (не более 500 мм рт. ст.) и коэффициента проницаемости мембраны для ультрафильтрата зависит скорость ультрафильтрации. В большинстве случаев требуется проведение болюсной или непрерывной антикоагуляции. Проводится в условиях стационара как способ дозированной дегидратации пациентам ХБП С5D в дополнение к другим методам диализа [5].
Гемодиализ интермиттирующий продленный - специализированный полуселективный мембранный метод экстракорпорального диализа с использованием АИП, основанный на принципе диффузионного и фильтрационного переноса через полупроницаемую высокопоточную мембрану High Flux воды и растворенных в ней молекул за счет градиента концентрации и градиента давления, обеспечивающий эффективное удаление из крови воды и низкомолекулярных компонентов крови. Характерными особенностями является: длительность от 8 до 12 часов в сутки, снижение интенсивности выведения метаболитов, скорость кровотока менее 200 мл/мин., диализата менее 200 мл/мин., проведение непрерывной антикоагуляции. Проводится пациентам ХБП С5D при госпитализации их в отделение реанимации стационара и пациентам с ОПП [5].
Гемофильтрация крови – специализированный полуселективный мембранный метод экстракорпорального диализа, основанный на принципе фильтрационного и конвекционного переноса через высоко проницаемую, высокопоточную мембрану High Flux воды и растворенных в ней молекул за счет градиента давления, обеспечивающий эффективное удаление из крови воды и низко - и средне молекулярных субстанций плазмы крови. Процедура может быть интермитирующей до 6 часов или продлена во времени до 8 – 12 часов. При необходимости, может использоваться АИП. Характерной особенностью ГФ являются: массивная УФ с одновременным замещением специальным заранее приготовленным сбалансированным раствором в процессе проведения процедуры, в большинстве случаев требуется проведение непрерывной антикоагуляции. Проводится пациентам ХБП С5D при госпитализации их в отделение реанимации стационара и пациентам с ОПП [5].
Гемодиафильтрация продленная – специализированный полуселективный мембранный метод экстракорпорального диализа с использованием модифицированных АИП. Метод основан на принципе диффузионного, фильтрационного и конвекционного переноса через высокопроницаемую, высокопоточную мембрану High Flux воды и растворенных в ней молекул за счет градиента концентрации и давления, обеспечивающий эффективное удаление из крови воды и низко- и средне молекулярных субстанций плазмы крови. Характерными особенностями являются: использование низких скоростей кровотока (100-200 мл/мин), потока диализата (12-18 л/ч) массивная УФ с одновременным замещением сбалансированным раствором приготовляемым непосредственно аппаратом (on line) из диализирующего раствора повышенной очистки (ультрачистого) в процессе проведения процедуры. В большинстве случаев требуется проведение болюсной или непрерывной антикоагуляции. Процедура продлена во времени до 8 – 12 часов в сутки. Проводится пациентам ХБП С5D при госпитализации их в отделение реанимации стационара и пациентам с ОПП [5].
Гемодиализ продолжительный - специализированный полуселективный мембранный метод экстракорпорального диализа с использованием аппаратов для продолжительных методов диализа, основанный на принципе диффузионного и фильтрационного переноса через полупроницаемую высокопоточную High Flux мембрану воды и растворенных в ней молекул за счет градиента концентрации и давления, обеспечивающий эффективное удаление из крови воды и низкомолекулярных компонентов крови. Характерными особенностями являются: продолжительность около 24 часов в сутки, сниженная скорость перфузии крови (100-200 мл/мин.), поток диализата (16-34 мл/мин.), проведение непрерывной антикоагуляции. Проводится пациентам ХБП С5D при госпитализации их в отделение реанимации стационара и пациентам с ОПП [5].
Гемофильтрация крови продолжительная – специализированный полуселективный мембранный метод экстракорпорального диализа, основанный на принципе фильтрационного и конвекционного переноса через высокопоточную, высокопроницаемую мембрану High Flux воды и растворенных в ней молекул за счет градиента давления, обеспечивающий эффективное удаление из крови воды и низко - и средне молекулярных субстанций плазмы крови. Характерными особенностями являются: продолжительность около 24 часов в сутки, скорость перфузии крови (100-300 мл/мин.), отсутствие потока диализата, проведение непрерывной антикоагуляции, скоростью удаления субституата (24-96 л/сут.), с одновременным замещением сбалансированным заранее приготовленным раствором (22-90 л/сут.) в процессе проведения процедуры. При необходимости, может использоваться аппарат для продолжительных методов диализа. Проводится пациентам ХБП С5D при госпитализации их в отделение реанимации стационара и пациентам с ОПП [5].
Гемодиафильтрация продолжительная – специализированный полуселективный мембранный метод экстракорпорального диализа с использованием аппаратов для продолжительных методов диализа. Основан на принципе диффузионного, фильтрационного и конвекционного переноса через высоко проницаемую высоко поточную биосовместимую мембрану High Flux воды и растворенных в ней субстанций за счет градиента давления и градиента концентрации, обеспечивающий эффективное удаление из крови воды, низко- и средне молекулярных компонентов плазмы крови. Характерными особенностями являются: использование низких скоростей кровотока (100-200 мл/мин), поток диализата (16-34 мл/мин.) массивная УФ (24 - 48 л/сут.) с одновременным замещением сбалансированным раствором приготовляемым непосредственно аппаратом (on line) из диализирующего раствора повышенной очистки (ультрачистого) в процессе проведения процедуры), требуется проведение болюсной или непрерывной антикоагуляции. Процедура продлена во времени до 8 – 12 часов в сутки на аппарате для продолжительных методов диализа. Проводится пациентам ХБП С5D, ОПП [5].
Таблица 5. Теоретические преимущества и недостатки ПЗПТ, ИГД, ПНПГД и ПД [2, 5, 18]
|
Метод
|
Возможная клиническая ситуация | Преимущества | Недостатки |
| ИГД | Стабильная гемодинамика | Быстрое удаление токсинов и низкомолекулярных веществ. Освобождает время для диагностики и лечебных мероприятий. Уменьшает продолжительность антикоагуляции. Дешевле, чем ПЗПТ. | Развитие гипотензии при быстром удалении жидкости. Развитие дизэквилибриум синдрома с риском отека мозга. Более сложен и трудоемок технически. |
| ПЗПТ | Нестабильность гемодинамики. Больные с риском повышения внутричерепного давления. | Продолжительное удаление токсинов. Стабильность гемодинамики. Простой контроль водного баланса. Не вызывает повышения внутричерепного давления. Аппарат прост в применении. | Медленный клиренс токсинов. Необходимость длительной антикоагуляции. Иммобилизация пациента. Гипотермия. Высокая стоимость. |
| ПНПГД | Нестабильность гемодинамики | Более медленное удаление жидкости и растворенных веществ. Стабильность гемодинамики. Освобождает время для диагностики и лечебных мероприятий. Уменьшает продолжительность антикоагуляции. | Медленный клиренс токсинов. Более сложен и трудоемок технически. |
| ПД | Нестабильность гемодинамики. Нарушения коагуляции. Проблемы с сосудистым доступом. Больные с риском повышения внутричерепного давления. Регион с недостаточным финансированием. | Не сложен технически Стабильность гемодинамики Не требуется антикоагуляция Не требуется сосудистый доступ Низкая стоимость Постепенное удаление токсинов | Недостаточный клиренс у больных с гиперкатаболизмом. Потеря белка. Невозможно контролировать скорость удаления жидкости. Риск перитонита. Гипергликемия. Не должно быть повреждений в брюшной полости. Нарушает подвижность диафрагмы, возможны респираторные нарушения |
|
ПЗПТ – продленная заместительная почечная терапия;
ИГД – итермиттирующий гемодиализ;
ПД – перитонеальный диализ;
ПНПГД – продленный низкопоточный гемодиализ
|
|||
| В | У пациентов с нестабильной гемодинамикой рекомендуется отдавать предпочтение продленной ЗПТ, а не стандартным интермиттирующим методикам ЗПТ [2] |
| А | Для предотвращения тромбообразования в экстракорпоральном контуре в ходе процедуры используются антикоагулянты или антитромботические агенты. |
Для больных без высокого риска кровотечения или нарушений коагуляции и не получающих эффективную системную антикоагуляционную терапию предлагается следующее [2, 5]:
| А | Для антикоагуляции при проведении интермиттирующей ЗПТ рекомендуется использовать нефракционированный или низкомолекулярный гепарин (предпочтительней), чем другие антикоагулянты [2, 18 - 20]. |
Для пациентов с повышенным риском кровотечения, не получающим антикоагуляцию, для проведения антикоагуляции при ЗПТ, предлагается следующее [2, 5]:
| В |
Использовать регионарную цитратную антикоагуляцию (предпочтительней,
проводить продленную ЗПТ без антикоагуляции) для тех больных, кто не имеет противопоказаний для введения цитрата [2, 18-20]. Предлагается избегать применения регионарной гепаринизации при проведении ПЗПТ у пациентов с повышенным риском кровотечения
|
У пациентов с гепарин-индуцированной тромбоцитопенией любое введение гепарина должно быть прекращено.
| А | При гепарин индуцированной тромбоцитопении предпочтительней использовать прямые ингибиторы тромбина (аргатробан) или ингибиторы фактора Xa (данапароид или фондапаринукс), чем применение других антикоагулянтов или ЗПТ без антикоагуляции [2, 18-20]. |
6. Погрешности при заполнении магистралей (воздух, пережатия, турбулентный ток)
Визуальный контроль:
Тесты на время свертывания
Время свертывания по Ли-Уайту
Таблица 6. Схемы дозирования нефракционированного гепарина
| Стандартная доза |
Исходная: 25 МЕ/кг Поддерживающая: 1000 МЕ/час, остановить за 30-60 минут до окончания |
При повышенной кровоточивости или тромбообразовании изменить дозу соответственно на 500 МЕ/час |
| Низкая доза |
Исходная: 10 МЕ/кг Поддерживающая: 10 МЕ/кг/час, остановить за 30-60 минут до окончания |
При повышенной кровоточивости исключить нагрузочную дозу. При персистирующей кровоточивости или тромбообразовании изменить дозу инфузии соответственно на 500 МЕ/час |
Таблица 7. Схемы применения препаратов фракционированного (низкомолекулярного) гепарина
| Далтепарин | Низкий риск кровотечения | 85 анти-Ха-МЕ/кг как болюс (ГД до 5 час) или исходный болюс 30-35 МЕ/кг, поддерживающая доза 10-15 МЕ/кг/час (целевой анти-Ха 0.5 ≥ МЕ/мл |
| Высокий риск кровотечения | 85 анти-Ха-МЕ/кг как болюс (ГД до 5 час) или исходный болюс 30-35 МЕ/кг, поддерживающая доза 10-15 МЕ/кг/час (целевой анти-Ха 0.5 ≥ МЕ/мл) | |
| Эноксапарин | Низкий риск кровотечения | 100 анти-Ха-МЕ/кг как болюс, при образовании сгустков повторить 50-100 анти-Ха-МЕ/кг |
| Высокий риск кровотечения | 50 анти-Ха-МЕ/кг при использовании двухпросветного катетера, 75 анти-Ха-МЕ/кг при использовании однопросветного катетера | |
| Надропарин | Обычный риск кровотечения | ГД до 4 час. Болюсно: при весе больного < 50 кг 2850 анти-Ха-МЕ, 50-69 кг – 3800 анти-Ха-МЕ, > 70 кг – 5700 анти-Ха-МЕ |
| Тинзапарин | 4500 анти-Ха-МЕ болюсно в артериальную линию, на следующем ГД: увеличить на 500 МЕ при видимых сгустках, уменьшить на 500 МЕ при длительном кровотечении из фистулы |
| А | При повышенном риске кровотечения необходимо редуцировать антикоагулянтную терапию |
Техника введения гепарина:
| В диализных центрах очень важно определять свертываемость крови (АЧВ, время свертывания по Ли Уайту, АВС). |
После диализа в диализаторе имеется несколько тромбированных волокон и в концах диализатора содержатся небольшие сгустки крови или депозиты. Более значительное тромбообразование должно быть документировано персоналом и служит сигналом для увеличения дозы гепарина [5, 13, 19-21]. При коротком диализе (2 часа) доза гепарина не должна доводится до 4000 ЕД.
Средняя скорость, составляющая 1200 ед/час, вызывает дальнейшее удлинение ЧТВ на 60 с., скорость введения 1800 ЕД /час вызывает удлинение ЧТВ до 90 с., а скорость 600 ЕД/час вызывает удлинение ЧТВ до 30 с. При режиме легкой гепаринизации скорость составляет 600 ЕД /час [5, 13, 19-21].
3) Периодическое промывание диализатора физиологическим раствором. Каждые 30 мин быстро промывают диализатор физиологическом раствором 100-200 мл, закрывая линию подачи крови. Частота промывание увеличивается или уменьшается по мере необходимости [5, 13, 19-21].
Немаловажным является также и то, что с использованием кинетики мочевины у диализных больных к настоящему времени накоплен огромный статистический материал, позволяющий делать достоверные выводы. Многочисленные исследования показали минимальный предел дозы диализа за сеанс при трехкратном в неделю диализе – при расчете однопулового spKt/V – не менее 1,4; что соответствует сбалансированному eKt/V – не менее 1,2 [5, 18]. При проведении более частых процедур доза за один сеанс может быть меньше, в связи с этим удобнее пользоваться расчетом недельного Kt/V по Gotch – не менее 2,2 [5, 13, 14, 18].
Продолжительность сеансов лечения является независимым фактором, определяющим результаты лечения. Поэтому недопустимо сокращение времени лечения на том основании, что формальная эффективность сеанса по показателю Kt/V достигнута раньше, чем за 4 часа [5, 13, 14, 18].
|
Адекватность диализа определяется по следующим параметрам
URR – Доля снижения мочевины
spKt/V – однопуловый
eKt/V – эквилибрированный фракционный клиренс Ur
stKt/V – стандартный Kt/V (не зависящий от кратности ГД в неделю)
on-line
по диализансу натрия (кондуктометрически)
по клиренсу мочевой кислоты (спектрометрически)
|
Урежение кратности диализных процедур
Поскольку такое определение чрезвычайно трудоемко и затратно, учитывать остаточную функцию почек при оценке эффективности диализа рекомендуется лишь в отдельных случаях, а в общей практике ориентироваться на приведенные величины продолжительности диализа и показателя Kt/V [5, 18, 25].
| А | Доза диализа должна выражаться коэффициентом очищения Kt/V по мочевине, представленного в виде эквилибрированного показателя (eKt/V) и рассчитанного на основании двухпуловой кинетической модели с изменяемым объемом. |
| А | Маркером оценки качества выведения веществ с низкой молекулярной массой является мочевина. |
| А | В рутинной практике эквилибрированный показатель рассчитывается по величине spKt/V – показателя, рассчитанного по формуле, основанной на однопуловой модели с изменяемым объемом, с учетом ожидаемого влияния перераспределения мочевины |
Для определения spKt/V в клинической практике используется формула с натуральным логарифмом, основанная на однокамерной модели с изменяемым объемом распределения мочевины [5]:
Формула для расчета стандартизованного недельного Kt/V (stdKt/V)

| А | При трехразовом в неделю проведении гемодиализа/ гемодиафильтрации минимальная доза одного сеанса должна составлять по эквилибрированному показателю eKt/V – 1,2, что соответствует spKt/V – 1,4. Стандартизованный недельный показатель stKt/V (по Gotch) должен быть ≥ 2.2. |
| А | Показатель Kt/V по пробам крови должен определяться ежемесячно, если не производится постоянный мониторинг Kt/V в течение каждого сеанса диализа валидизированными аппаратными методами (ионный диализанс, фотометрическое исследовании, уреазный метод и др.) с расчетом средней величины за месяц. |
Для учета остаточной функции почек у пациентов на гемодиализе при оценке суммарной дозы очищения необходимо проводить ее лабораторное определение со сбором мочи за весь междиализный интервал и исследованием клиренсов мочевины и креатинина. Среднее арифметическое значение данных клиренсов может быть приплюсовано к эффективности гемодиализного лечения. Для пересчета СКФ в эквивалент Kt/V используется метод Касино – Лопеса. Поскольку на фоне диализной терапии отмечается прогрессивная утрата остаточной функции почек, при оценке суммарной дозы очищения должны использоваться актуальные величины СКФ с давностью не более 2 месяцев [5, 18].
| А | Продолжительность каждого сеанса при трехразовом в неделю лечении должна быть не менее 4-х часов, вне зависимости от формального достижения эффективности процедуры по показателю Kt/V на более ранних ее стадиях |
Выведение веществ средней молекулярной массы.
| В | Оценка выведения среднемолекулярных веществ может осуществляться по додиализному уровню β2микроглобулина [5, 18]. |
Специальные показания к применению высокопоточных синтетических мембран включают [5, 18]:
| А | Для увеличения выведения средне- и высокомолекулярных веществ наиболее эффективны конвективные методики (ГДФ), осуществляемые на высокопоточных диализаторах – гемодиафильтрах (коэффициент ультрафильтрации более 20 мл/час/мм рт. ст., коэффициент просеивания для β2-микроглобулина свыше 0,6). |
| А | При использовании гемодиафильтраци on-line критерием эффективности конвективного переноса является объем замещения за процедуру |
| В | Высокообъемной считается процедура с конвекционным объемом свыше 24-х литров. |
Наиболее частым методом замещения конвекционного объема при гемодиафильтрации on-line является постдилюция.
| А | Показаниями к предилюции или смешанной дилюции являются трудности достижения целевого конвекционного объема или опасность "тромбирования" диализатора вследствие избыточной гемоконцентрации или по другим причинам. При предилюционном способе (компоненте) замещения объем ультрафильтрации должен рассчитываться с учетом разведения крови в экстракорпоральном контуре. |
БИОСОВМЕСТИМОСТЬ И ЭКСТРАКОРПОРАЛЬНЫЙ КОНТУР
| А | Следует избегать использования диализных мембран, в значительной степени активирующих систему комплемента и клеточные элементы крови |
| А | Оптимальным способом стерилизации диализаторов следует считать паровую стерилизацию (чистый маркетинг!). Лучевая стерилизация может вызывать деградацию некоторых материалов диализатора. Следует избегать использования диализаторов и других компонентов экстракорпорального контура, стерилизованных окисью этилена. |
| А | При подготовке экстракорпорального контура необходимо обеспечивать заявленный производителем объем промывки. При отсутствии информации минимальным объемом является 2 литра раствора |
| А | Многократное использование компонентов системы экстракорпорального контура настоятельно не рекомендуется |
| А | При использовании мембран, выполненных из материалов, способных активировать брадикининовую систему (полиакрилонитрил), не показано назначение ингибиторов ангиотензинконвертазы. |
Таблица 8. Рекомендуемый размер игл в зависимости от предписанной скорости кровотока
|
Скорость кровотока (мл/мин)
|
Размер игл | Внутренний диаметр (мм) |
|
≤ 200
|
17G | 1,5 |
|
200 - 280
|
16G | 1,6 |
|
280 - 400
|
15G | 1,8 |
|
≥ 400
|
14G | 2,0 |
| А | При проведении сеансов лечения должна использоваться вода, по химической и бактериологической чистоте удовлетворяющая требования соответствующего стандарта |
Для обеспечения показателей качества воды и диализирующей жидкости в центре диализа должна иметься рабочая программа мониторинга, определяющая спектр и частоту исследований [5, 18].
| А | При использовании высокопоточных диализных мембран необходимо использовать сверхчистую диализирующую жидкость |
| В | Для снижения выраженности хронического воспаления применение сверхчистого диализата показано во всех случаях |
Такие свойства диализирующей жидкости обеспечиваются инкорпорированием дополнительных ультрафильтров в систему подачи диализата [5, 18].
| А | При проведении конвективных процедур с приготовлением замещающей жидкости из диализата (гемодиафильтрации on-line) должна использоваться аппаратура, сертифицированная для данного вида лечения |
| В | При использовании жидкого бикарбонатного концентрата открытая канистра должна использоваться в течение 1 дня |
| А | Предписанная производителем стерилизация системы гидравлики диализного аппарата (тепловая, химическая или комбинированная) должна проводиться после каждой процедуры лечения |
| А | Для исключения бактериального загрязнения концентрата диализирующей жидкости желательно использование бикарбоната в сухом виде |
| А | В качестве основного буфера диализирующей жидкости должен использоваться бикарбонат натрия |
|
Параметр
|
Диализирующая жидкость* | Сверхчистая диализирующая жидкость** (субституат) |
| Число колонииформирующих единиц/мл | менее 100 | менее 0,1 |
| Концентрация бактериального эндотоксина ЭЕ/мл | менее 0,25 | менее 0,03 |
СОСТАВ ДИАЛИЗИРУЮЩЕЙ ЖИДКОСТИ
| А | Применение ацетата в качестве основного буфера диализирующей жидкости не показано во всех случаях и противопоказано пациентам с сахарным диабетом и патологией печени |
Кислый компонент бикарбонатного концентрата традиционно содержит уксусную кислоту или ее соли, что результируется содержанием ацетатного иона в бикарбонатном диализате 3,0 – 6,0 ммоль/л [5, 18].
Правильная, индивидуализированная отработка состава диализата и других параметров процедуры позволяет в большинстве случаев обеспечить неосложненное ее течение с адекватной коррекцией уремии, статуса гидратации, кислотно-основного состояния и электролитных отклонений [5, 18].
| А | Применение диализата с содержанием глюкозы 5,0 – 5,5 ммоль/л для профилактики гипогликемии и повышения гемодинамической стабильности целесообразно у всех больных и обязательно у пациентов с сахарным диабетом, у которых может применяться диализат с содержанием глюкозы до 11 ммоль/л |
| В | Применение диализата с содержанием Са 1,75 ммоль/л у больных на программном гемодиализе нецелесообразно. Уровень Са 1,5 ммоль/л показан при гиперпаратиреозе, целевых значениях Са и отсутствии признаков сосудистой кальцификации. Уровень Са 1,25 ммоль/л и ниже показан при гипопаратиреозе, гиперкальциемии и сосудистой кальцификации |
| В | Увеличенное до 3,0 – 3,5 ммоль/л содержание калия в диализате показано пациентам с сахарным диабетом, пациентам, находящимся на лечении расширенной диализной программой, а также склонным к гипокалиемии в связи с особенностями диеты и сопутствующей патологии |
| В | Преддиализный уровень бикарбоната сыворотки должен находиться в пределах 21 – 24 ммоль/л; последиализный не должен превышать 29 ммоль/л. При установке уровня бикарбоната диализирующей жидкости необходимо учитывать влияние ацетатного иона или цитратного иона в зависимости от типа кислого компонента бикарбонатного концентрата. |
| Бикарбонат | 30-35 мэкв/л | Подбирается индивидуально для каждого больного в зависимости от преддиализного уровня. У пациентов с ацидозом рекомендуется использование стандартной концентрации. При алкалозе (преддиализный бикарбонат 28 ммоль/л и выше) нужно использовать более низкие концентрации (20-28 ммоль/л) |
| Натрий | 135-145 ммоль/л | Необходимо корректировать с натрием пациентов и устанавливать более близким к нему. Можно использовать более высокие концентрации (от уровня натрия пациента) или профилирование натрия при частых диализных гипотензиях. |
| Калий | 3-3,5 ммоль/л | У пациентов с СД и склонным к гипокалиемии рекомендуются более высокие концентрации. Использование низких концентраций опасно в связи с развитием последиализной гипокалиемии и высоким риском внезапной сердечной смерти |
| Кальций | 1,25-1,5 ммоль/л | У пациентов с гипопаратиреозом, гиперкальциемией и сосудистой кальцификацией 1,25 ммоль/л и ниже. |
| Глюкоза | 5-5,5 ммоль/л | Может применяться у всех пациентов и обязательно у пациентов с СД |
|
Контаминант
|
Максимальная концентрация по AAMI (Ассоциация усовершенствования медицинского оборудования) | Максимальная концентрация по Европейским стандартам |
|
Алюминий
|
0.0100 | 0.0100 |
|
Мышьяк
|
0.0050 | 0.0050 |
|
Барий
|
0.1000 | 0.1000 |
|
Бериллий
|
0.0004 | 0.0004 |
|
Кадмий
|
0.0010 | 0.0010 |
|
Кальций
|
2 (0.05 mmol/l) | 2 (0.05 mmol/l) |
|
Хлорамин
|
0.1000 | 0.1000 |
|
Медь
|
0.1000 | 0.1000 |
|
Цианиды
|
0.0200 | 0.0200 |
|
Фториды
|
0.2000 | 0.2000 |
|
Хлор
|
0.5000 | 0.5000 |
|
Свинец
|
0.0050 | 0.0050 |
|
Магний
|
4 (0.16 mmol/l) | 2 (0.08 mmol/l) |
|
Ртуть
|
0.0002 | 0.0010 |
|
Нитраты
|
2.0000 | 2.0000 |
|
Калий
|
(0.2 mmol/l) | 2 (0.08 mmol/l) |
|
Селен
|
0.0900 | 0.0900 |
|
Серебро
|
0.0050 | 0.0050 |
|
Натрий
|
70 (3.0 mmol/l) | 50 (2.2 mmol/l) |
|
Сульфаты
|
100 | 100 |
|
Таллий
|
0.0020 | 0.0020 |
|
Цинк
|
0.1000 0.1000 | 0.1000 0.1000 |
Перед началом гемодиализа аппарат должен пройти обязательное автоматическое тестирование по заданной программе, обеспечивающей проверку годности всех блоков аппаратуры. Если аппарат по каким-либо причинам не проходит этап тестирования следует вызвать инженера и не производить подключение пациента до устранения ошибки [5, 8-14, 18].
Диализатор располагается в держателе вертикально так, чтобы надписи на этикетке были доступны для прочтения и диализирующий раствор после подсоединения магистралей АИП двигался снизу-вверх. Желательно располагать диализатор строго по вертикальной линии, чтобы устранить эффект появления «мертвых» волокон, остающихся заполненными воздухом и не участвующих в промывке [5, 18].
Подсоединяются кровопроводящие магистрали. Рекомендуется плотное и правильное присоединение линий магистралей как к аппарату, так и к диализатору, чтобы избежать ошибок при заполнении, повреждении линий магистралей и утечки крови во время процедуры. Расположение кровопроводящих магистралей и манжет диализатора должно обеспечивать противоток диализата и крови пациента по отношению друг другу.
Предварительная подготовка контура кровообращения заключается в заполнении и промывании диализатора и магистралей 0,9% раствором хлорида натрия в строгом соответствии с инструкцией по применению диализатора. Для этого артериальная магистраль подсоединяется к флакону или мешку с 1 л стерильного 0,9% раствора хлорида натрия. Включается перфузионный насос и со скоростью 150-180 мл/мин раствор начинает поступать по артериальной линии в кровопроводящий контур диализатора, вытесняя из него воздух. Для облегчения вытеснения воздуха следует осуществлять краткие пережатия артериальной магистрали. Для удаления возможных остатков стерилизующих веществ первые 300-500 мл необходимо слить. Этим обеспечивается профилактика возможных анафилактоидных реакций [5, 18]. После заполнения магистралей раствором и слива первой порции производится остановка перфузионного насоса и подсоединение конца венозной магистрали к флакону или мешку с 0,9% раствором хлорида натрия. Обеспечивается рециркуляция раствора в системе в течение 10-15 минут с многократным кратковременным пережатием артериальной магистрали до достижения необходимого объема промывки [5, 8-14, 18]. Последующее заполнение магистралей и диализатора кровью пациента осуществляется только после тщательной промывки и вытеснения воздуха из кровопроводящего контура стерильным физиологическим раствором [5, 8-14, 18].
При подключении больного к АИП врач, проводящий гемодиализ, контролирует либо выставляет параметры скорости кровотока (150-350 мл/мин), потока диализирующего раствора (500-800 мл/мин), проводимости и температуры диализирующего раствора (36-38°), времени и объема ультрафильтрации. Объем ультрафильтрации устанавливается исходя из разницы между текущим и сухим весом, которая определяется путем взвешивания пациента до и после процедуры [5, 18]. После того, как АИП полностью готов к работе (пройден первоначальный тест, кровопроводящий контур заполнен и промыт 0,9% раствором хлорида натрия, вытеснен воздух из контура крови и контура диализирующего раствора) в асептических условиях производится подключение пациента [5, 18].
Пункция артерио-венозной фистулы. Перед пункцией следует осмотреть кожу вокруг АВФ на наличие воспалений, повреждений целостности, проверить наличие шума и вибрации. Пункция осуществляется фистульной иглой срезом вверх под углом приблизительно 45 градусов к поверхности кожи. После попадания в просвет фистулы иглу необходимо повернуть по оси на 180 градусов для предотвращения повреждения задней стенки сосуда. Артериальная игла (забор крови) должна располагаться по возможности навстречу току крови, венозная (возврат крови) - наоборот, по току крови. Расстояние между иглами должно составлять не менее 5 см, что предотвращает рециркуляцию и ухудшение качества очищения крови. При использовании двухпросветного диализного катетера забор и возврат крови должен осуществляться в соответствии с маркировкой коннектеров на катетере: красный - артериальный, синий – венозный [5, 8-14, 18]. Болюсное введение антикоагулянта производится сразу после подключения, дозированное введение начинается параллельно заполнению магистралей кровью в автоматическом режиме.
После соединения артериальной магистрали с артериальной иглой включается насос крови и начинается вытеснение 0,9% раствора хлорида натрия из системы магистралей и диализатора кровью пациента при скорости не более 150-180 мл/мин. Раствор хлорида натрия вытесняется до тех пор, пока не определяется окрашивание кровью дистального отдела венозной магистрали, после чего насос крови останавливается, венозная магистраль пережимается и соединяется с венозной иглой. Проверяется надежность и правильность всех соединений, после чего включается насос крови и устанавливается необходимая скорость кровотока в зависимости от возможностей сосудистого доступа и состояния сердечно-сосудистой системы. Типичной является скорость кровотока в пределах 200-300 мл/мин [5, 8-14, 18]. Производится надежная фиксация магистралей клеящимися пластырями или зажимами. Фистулу рекомендуется оставлять открытой, для лучшего визуального обзора за иглами и эффективностью фиксации [5, 8-14, 18].
После извлечения игл места пункций прижимаются свернутыми стерильными салфетками, через 5-10 мин после начала прижатия проверяется остановка кровотечения. Если кровотечение остановлено, накладывается клеящийся пластырь. При его отсутствии или наличии аллергии можно накладывать сухую повязку [5, 18].
«Сухой» вес - это минимальная масса тела пациента после процедуры ГД, при которой не наблюдаются симптомы избыточной УФ (интрадиализная гипотензия, судороги в мышцах).
«Сухой вес» – это вес тела с нормальным объемом внеклеточной жидкости. Это не только отсутствие отеков, но состояние, крайне близкое к гиповолемии, которое должно быть достигнуто в конце сеанса ГД без введения больного в гипотензию.
На практике о достижении «сухого веса» можно говорить, опираясь на ряд клинических симптомов. «Сухой вес» не является постоянной величиной организма − на него влияет характер питания, образ жизни, сопутствующие заболевания. При значительной перегрузке жидкостью невозможно одномоментно достигнуть «сухого веса».
Величина гипергидратации у пациентов, находящихся на лечении программным гемодиализом, слагается из двух компонентов. Первым является междиализная прибавка в весе, практически целиком зависящая от количества потребляемой жидкости – интермиттирующая гипергидратация. Вторым компонентом служит возможная «базовая», персистирующая гипергидратация у пациентов с неправильно отработанным сухим весом. То есть в тех ситуациях, когда избыточный объем сохраняется в организме даже после сеанса лечения с ультрафильтрацией [5].
Исследования, проведенные с использованием биоимпедансного анализа показали, что адекватный последиализный вес, так называемый сухой вес, характеризующий состояние нормогидратации или даже незначительной дегидратации, не достигается у трети пациентов на программном гемодиализе. В таких случаях даже незначительная, укладывающаяся в клинические рекомендации, междиализная прибавка в весе может приводить к гипергидратации, сопряженной с повышением уровня смертности [5].
Учитывая эти данные, можно заключить, что отработка сухого веса в практике программного гемодиализа должна осуществляться на постоянной основе.
| А | Контроль состояния гидратации или верификация величины «сухого веса» у пациентов на программном гемодиализе должны осуществляться на регулярной основе, но не реже 1 раза в месяц |
| А | У пациентов с частыми эпизодами интрадиализной гипотензии, не позволяющими устранить клинические признаки гипергидратации, требуется объективизация уровня волемии |
Оценка статуса гидратации по данным биоимпедансного анализа может рассматриваться как оптимальный метод в практике программного гемодиализа. Частое возникновение интрадиализной гипотензии у пациентов с отработанным сухим весом требует углубленного обследования сердечно-сосудистой системы.
| А | Снижение величины междиализной гидратации и, соответственно, скорости ультрафильтрации в ходе сеанса лечения является мерой первого порядка для профилактики интрадиализных осложнений |
| А | Основным мероприятием, направленным на снижение величины междиализной гидратации, является модификация диеты со строгим ограничением потребления хлорида натрия |
| В | Величина междиализной гидратации не должна превышать 4,5% сухого веса пациента или 15% внеклеточного объема. Скорость не восполняемой ультрафильтрации в ходе сеанса лечения не должна превышать 12 мл/час на 1 кг массы тела пациента. Оценка динамики относительного объема крови в ходе сеанса лечения позволяет объективизировать статус волемии |
Депрессия, деменция, лекарственная и алкогольная зависимость, тревога, расстройства персонализации, отсутствие сотрудничества со стороны пациентов (раздражительность), половая дисфункция.
Воспоминания или сны о том, что больной зависит от аппарата «Искусственной почки» могут посещать его, даже если он этого совсем не хочет. Больного могут посещать тяжелые мысли или чувства, связанные с потенциальным риском для жизни. Настроение также может ухудшиться по причине того, что из-за зависимости от диализа пациенты не могут вернуться к обычному ритму жизни, к которому они так привыкли. В свою очередь, эти тяжелые и сложные чувства могут повлиять на способность заниматься повседневной деятельностью – особенно в случае снижения мотивации в силу большого разрыва между ожиданиями и тем, что реально может быть достигнуто.
Младенцы и дети с ХБП имеют более высокую частоту развития неврологических и психосоциальных нарушений по сравнению с педиатрической популяцией в целом [56, 64, 65]. Чем дольше продолжительность диализа, тем больше вероятность когнитивных нарушений и нарушений обучения [65].
Полноценный сон. Сон больного вероятнее всего был нарушен в состоянии уремии. Чувство стресса также может оказать негативное влияние на продолжительность и качество сна. Нужно рекомендовать пациенту восстановить обычный для него режим сна и бодрствования, например, используя для этой цели напоминающие звуковые сигналы. Пациенту или ухаживающему за ним лицу нужно позаботиться о том, чтобы в окружающей больного обстановке не было факторов, которые могут нарушить его покой, например, слишком много света или шума. Сведение к минимуму поступления в организм никотина (например, от курения), кофеина и алкоголя, а также использование стратегий релаксации помогут ему заснуть и не просыпаться в течение ночи.
Важно сохранять физическую активность, так как физическая активность способствует уменьшению стресса и снижению вероятности развития депрессии. Интенсивность физической активности следует увеличивать постепенно и с соблюдением всех мер безопасности. Физические упражнения, которые не превышают индивидуальных возможностей и проводятся на регулярной основе, позволяют уменьшить проявления депрессии и тревоги у пациентов.
Поддержание социальных связей имеет очень важное значение для психического благополучия пациентов. Беседы с другими людьми могут помочь не только уменьшить стресс, но и найти способы преодоления трудностей и проблем, связанных с восстановлением прежнего уровня здоровья. Если пациент живет один, то поддержание контактов с друзьями или родственниками по телефону или с помощью интернета может помочь ему чувствовать себя менее одиноким. Из-за своего депрессивного настроения больной может испытывать чувство социального отчуждения.
Постепенно, учитывая состояние здоровья, рекомендуется повышать уровень бытовой и трудовой деятельности пациента или увлечения хобби, так как это способствует улучшению настроения.
Оценка физического состояния
| В | У пациентов на программном гемодиализе ИМТ должен быть не менее 23 кг/м2. При меньших значениях можно предполагать недостаточность питания. Если индекс массы тела меньше 18,5 кг/м2 или 25 перцентиля и ниже данного значения, относится к группе риска недостаточности питания |
Недостаточность питания (НП) можно предполагать при потере в весе > 10% за 6 месяцев или более короткий промежуток времени. Изменения, не превышающие 5% массы тела, можно рассматривать как физиологические. Незначительная за промежутки времени, но постоянная в динамике потеря веса также может быть проявлением НП.
| А | Показатель глобальной субъективной оценки (по 7-бальной шкале) ниже 5 предполагает недостаточность питания, ниже 3 – свидетельствует о выраженной недостаточности. |
Таблица 12. Определение степени нарушения нутритивного статуса у больных хронической болезнью почек (по Bilbrey G.L., Cohen T.L.).
|
Показатель
|
Пол | Норма | Степень нарушения нутритивного статуса | ||
|
1 балл
|
2 балла | 3 балла | |||
| КЖСТ, мм | М | 10.5-9.5 |
9.4-8.4
|
8.3-7.4 | <7.4 |
| Ж | 14.5-13.1 |
13.0-11.7
|
11.6-10.1 | <10.1 | |
| ОМП, см | М |
25.7-23.0
|
22.9-20.4 | 20.3-18.0 | <18.0 |
| Ж |
23.4-21.0
|
20.9-18.8 | 18.7-16.4 | <16.4 | |
| Альбумин сыв., г/л | М и Ж | 45-35 |
34-30
|
29-25 | <25 |
| Трансферрин сыв, мг/дл | М и Ж | >180 |
180-160
|
159-140 | <140 |
| Абс. число лимфоцитов | М и Ж | >1800 |
1800-1500
|
1499-900 | <900 |
| В | У взрослых пациентов с ХБП С5D предлагается использовать силу сжатия кисти в качестве индикатора БЭН и функционального статуса при наличии исходных данных (предшествующие измерения) для сравнения. |
Лабораторные показатели оценки питания
К лабораторным показателям, применяющимся для косвенной оценки достаточности питания, относятся сывороточные концентрации альбумина и холестерина, показатель nPNA [26-28].
| С | Сывороточная концентрация альбумина у пациентов на программном гемодиализе должна быть не ниже 38 г/л |
| С | Сывороточная концентрация холестерина должна превышать нижнюю границу нормы (3,6 ммоль/л) |
| С | У пациентов на гемодиализе nPNA должен быть не ниже 1 г на 1 кг идеального веса |
| А | Концентрация бикарбоната перед средним за неделю гемодиализом должна быть 20-22 ммоль/л. |
| В | У пациентов с концентрацией бикарбоната < 20 ммоль/л, следует рассмотреть назначение натрия бикарбоната перорально или повышение концентрации бикарбоната диализата до 40 ммоль/л для коррекции ацидоза. Чрезмерно высокие концентрации – более 29 ммоль/л сопряжены с опасностью развития последиализного алкалоза |
Чтобы уменьшить нагрузку на почки с ослабленной функцией, и избежать нарушения баланса жидкости и электролитов, пациентам с ХБП следует изменять свою диету в соответствии с рекомендациями врача и диетолога. Не существует готовых диет для больных с ХБП. Каждый пациент получает различные диетические рекомендации в зависимости от клинического статуса, стадии почечной недостаточности и других медицинских проблем. Диетические рекомендации могут меняться у одного пациента в разные отрезки времени.
Общие принципы нутриционной поддержки у пациентов с ХБП С4-5 до ЗПТ
Общие принципы нутриционной поддержки у пациентов с ХБП С5 D
| В | Суточное потребление белков с пищей у диализных больных должно быть в пределах 1,2 г/кг ИМТ/сут. Потребление фосфора не должно превышать 1000 – 1200 мг в сутки. |
| В | Рекомендованная энергетическая ценность питания у диализных больных должна быть в пределах 30-40 ккал/кг ИМТ/сут, с учетом возраста, пола и расчётной максимальной физической активности |
Таблица 13. Суточная потребность в различных диетических компонентах у пациентов на ГД
|
Наименование
|
Суточная потребность |
| Водорастворимые витамины | |
|
Тиамин (В1)
|
1,1-1,2 мг |
|
Рибофлавин (В2)
|
1,1-1,3 мг |
|
Пиридоксин (В6)
|
10 мг |
|
Аскорбиновая кислота (С)
|
75-90 мг |
|
Фолиевая кислота (В9)
|
1 мг |
|
Цианокобаламин (В12)
|
2,4 мкг |
|
Никотиновая кислота (В3)
|
14-16 мг |
|
Биотин (В8)
|
30 мкг |
|
Пантотеновая кислота (В5)
|
5 мг |
| Жирорастворимые витамины | |
|
Ретинол (А)
|
700-900 мкг (рутинного назначения не требует) |
| Токоферол (Е) | 400-800 Ме (назначается для предупреждения кардиоваскулярных осложнения и лечения мышечных спазмов) |
| Витамин К | 90-120 мкг (рутинного назначения не требует, но в исключительных случаях (при длительном приеме антибиотиков, нарушении свертываемости возможны короткие курсы по 10 мг/сут) |
| Минералы | |
|
Фосфор
|
800-1000 мг |
|
Кальций
|
2000 мг |
|
Натрия хлорид
|
5-6 г (75 мг/кг массы) |
|
Жидкость
|
Не более 4,5-5% от «сухой» массы тела |
| Калий | 1950-2730 мг (50-70 ммоль или 1 ммоль/кг ИМТ/сут) |
| Рассеянные микроэлементы | |
| Железо | 8 мг – муж., 15 мг – жен. |
| Цинк | 8-12 мг – муж., 10-15 – жен. (рутинного назначения не требует, при БЭН с недостаточностью цинка и таких ее проявлениях как импотенция, периферическая нейропатия, хрупкость кожи может назначатя по 50 мг в день курсами на 3-6 мес) |
| Селен | 55 мкг (рутинного назначения не требует, но может применяться курсами по 3-6 мес при недостаточности, сопровождающейся следующими состояниями: кардиомиопатия, миопатия, гипотиреоз, гемолиз, дерматоз) |
Если диетическими манипуляциями не удается обеспечить белково- энергетический минимум, показано применение пищевых добавок. При этом предпочтительно использование смесей, разработанных специально для диализных пациентов. Многие смеси содержат также и витамины.
| А | При достаточном потреблении калорий и наличии признаков белковой недостаточности показано назначение препаратов аминокислот, в том числе в кетоформе |
| В | Взрослым пациентам с ХБП С 4 - 5D с риском развития или с уже развившейся БЭН, рекомендуется как минимум 3-х месячный пробный курс пероральных питательных смесей для улучшения нутриционного статуса, если только диетические консультации не позволяют достичь достаточного потребления белка и энергии в соответствии с нутритивными потребностями. |
Если применение пищевых добавок не позволяет обеспечить белково-энергетический минимум, необходимо рассмотреть возможность применения зондового введения питательных смесей. При этом предпочтительны формулы, специально разработанные для диализных пациентов. В отдельных случаях применяется наложение чрескожной энтеро-гастростомы. Если зондовое питание неэффективно, необходимо рассмотреть возможность проведения курса парэнтерального питания во время процедуры диализа.
| А | В случае, когда энергетическая ценность обычной диеты не превышает 20 кКал/кг, а потребление белка не превышает 0,8 г/кг массы тела, необходимо рассмотреть возможность ежедневного энтерального или парэнтерального питания |
Диета может отличаться в дни диализа и дни без него. При потере аппетита в дни диализа надо обеспечить увеличение потребления пищи между днями процедур. Целесообразен частый прием пищи малыми порциями.
Диета на неделю представлена в приложении 3.
При лихорадке, жаркой погоде, рвотах, поносах объем принимаемой жидкости может быть увеличен до 1 л в сутки.
ДН развивается у 30–40% больных СД 1-го и 2-го типов, она является ведущей причиной развития ХБП С5 в мире: удельный вес лиц с ДН в структуре больных, получающих лечение с замещением функции почек, достигает 40% [43-45].
У пациентов с диабетом диализ начинается при клиренсе креатинина свыше 15 мл/мин, при отсутствии клиники явной уремии. Тому есть несколько причин: гипертензия, сочетающаяся с быстрым прогрессированием диабетической ретинопатии, во многих случаях трудно поддается контролю при клиренсе ниже 15 мл/мин.
1. Гликолизированный гемоглобин.
|
Причины ложного занижения HbA1с
|
Причины ложного повышения HbA1с |
|
1. Гипогликемия
2. Анемия
3. Лечение эритропоэтином или препаратами железа
4. Дефицит белка
5. Лизис эритроцитов
6. Гемоглобинопатии
|
1. Гипертриглицеридемия
2. Гипербилирубинемия
3. Спленэктомия
4. Метаболический ацидоз
5. Повышенное образование карбоксигемоглобина
6. Дефицит фолатов
8. Спленэктомия
|
В международных рекомендациях (2020 - 2023 гг.) считается, что целевой уровень HbA1c для пациентов, получающих диализную терапию, не установлен. HbA1c менее надежен и не обеспечивает точного гликемического контроля у пациентов, находящихся на гемодиализе [46-50].
| С | Уровень же HbA1c > 9,5%, отражает плохой гликемический контроль, если только нет тяжелого дефицита железа. |
3. Непрерывный мониторинг глюкозы (НМГ).
| С | Всем лицам с СД, находящимся на диализе с использованием инсулина и имеющих рецидивирующую гипогликемию, рекомендуется использование НМГ в реальном времени [49]. |
4. Определение глюкозы в крови
Инсулинотерапия при гемодиализе [49, 75-78]
| С | Инсулинотерапия в базис-болюсном режиме с регулярным контролем уровня глюкозы в крови является самым эффективным методом коррекции гликемии у пациентов с СД на ГД. Они лучше всего подходят при гликемической вариабельности (ВГ), наблюдаемой у лиц с СД на диализе |
3. период после проведения ГД: снижается инсулинорезистентность, потребность в инсулине снижается.
| С | Снижение дозы инсулина на 25% в дни гемодиализа может снизить риск гипогликемии, но оценка с помощью СМГ может лучше контролировать дозу инсулина в дни диализа и без него. |
| С | У лиц с СД, находящихся на диализе, которые не могут справиться с базисно-болюсным режимом, следует рассмотреть режимы один раз в день с инсулином более длительного действия |
| С | У пациентов, страдающих тяжелой гипогликемией на инсулине НПХ, можно рассмотреть переход на аналог инсулина |
Введение инсулина с диализатом может потребовать увеличения дозы до 30% из-за потерь в трубке и разведения. Кроме того, использование диализата на основе декстрозы может потребовать дополнительного введения инсулина для смягчения системного влияния абсорбции декстрозы на уровень гликемии [79].
1. Вариабельность гликемии у пациентов с СД на гемодиализе
Регидратация. Неспособность развить осмотический диурез означает, что гипергликемия, связанная с диализом и кетоз может происходить без особого обезвоживания. Лечение кетоацидоза при этом нельзя начинать с введением больших количеств жидкости. Тем не менее, для тех, у кого имеется гиповолемия, можно вводить по 250 мл (0,9% хлорид натрия или 10% декстроза) с частой клинической оценкой (2D).
Инсулинотерапия. Лицам на диализе, заместительная терапия ДКА инсулином является основой лечения. Его следует вводить как с начальной фиксированной скоростью 0,1 ЕД/кг/ч, но может потребоваться увеличение, если требуемая скорость падения уровня глюкозы не достигается. Тем не менее, нарушение выведения инсулина почками, может повышать риск гипогликемии. Снижение глюкозы у диализных больных обычно такое же, как у людей с сохраненной функцией почек, т. е. 3,0 ммоль/л/час. Если скорость падения выше, или уровень глюкозы падает до <14,0 ммоль/л, настоятельно рекомендуется уменьшить скорость внутривенной инфузии инсулина до 0,05 ЕД/кг/час. Необходим постоянный ежечасный мониторинг глюкозы.
Восстановление электролитных нарушений. Добавление калия лицам с ДКА на гемодиализе обычно не требуется из-за отсутствия осмотического диуреза, так как потери калия значительно меньше, чем у пациентов с сохраненной почечной функция. Однако ацидоз может привести к значительной гиперкалиемии, поэтому необходим мониторинг калия крови и ЭКГ каждые 2-3 час, при необходимости нужна интенсивная терапия, с принятием неотложных мер (гемодиализ/гемофильтрация).
Контроль АД у пациентов с СД на диализе [46]
Анемия у пациентов с СД и ХБП С5 D [46]
Трансплантация почки у пациентов с СД [4]
БЕРЕМЕННОСТЬ У ЖЕНЩИН НА ДИАЛИЗЕ
У женщин, находящихся на диализе, гораздо меньше шансов забеременеть, но больше вероятность осложненной беременности по сравнению с женщинами с нормальной функцией почек. Отсутствуют данные об отдаленном прогнозе
Виды диализа, влияющие на частоту наступления беременности.
Ночной гемодиализ. Пациенты, получающие ночной диализ, имеют более высокие показатели беременности по сравнению с обычным гемодиализом.
Перитонеальный диализ. Частота наступления беременности ниже среди пациентов на перитонеальном диализе по сравнению с гемодиализом [114,115].
Контрацепции
Рекомендуемые контрацепции у женщин с ХБП C5D такие же, как и у населения в целом. Обратимые контрацептивы длительного действия являются предпочтительными методами для женщин с ХБП С5D, которым нужны наиболее эффективные и/или долговременные варианты контрацепции.
Обратимые контрацептивы длительного действия: медные внутриматочные спирали (ВМС), левоноргестрел-высвобождающие ВМС и имплантат этоногестрела. Эстрогенсодержащие пероральные таблетки, трансдермальный пластырь и вагинальные кольца менее предпочтительны из-за высокого сердечно-сосудистого риска у пациентов с ХБП С5D.
Планирование беременности
Рекомендована консультация гинеколога перед зачатием. Пациентки должны быть проинформированы о том, что беременность у диализных пациентов считается высоким риском и требует междисциплинарных усилий с участием как акушера, так и нефролога. Всем диализным пациенткам, которые планируют беременность, рекомендуется мультидисциплинарное обследование, включающее нефролога и акушер-гинеколога, диетолога.
Необходимо изучить анамнез и изучить препараты пациента. Прекратить или заменить препараты, имеющие потенциальные тератогенные или фетотоксические эффекты.
1. Ингибиторы АПФ не следует применять во время беременности, поскольку они связаны с аномалиями развития плода.
2. Мочегонные средства. Беременные женщины почти ежедневно подвергаются диализу и удаление жидкости лучше всего достигается тщательной ультрафильтрацией с диализом.
Контрацепция. Поскольку беременность у женщин, находящихся на диализе, связана с повышенным риском для матери и плода, консультирование по вопросам контрацепции является активной частью помощи до зачатия. Обсуждается контрацепция со всеми женщинами с репродуктивным потенциалом и советуется использовать противозачаточные средства до тех пор, пока активно не планируется беременность.
Решение планировать или отложить зачатие зависит от исходного состояния, сопутствующего заболевания, возраста женщины. У реципиентов трансплантата частота успешных беременностей выше, меньше осложнений и меньше врожденных аномалий, в связи с этим диализным пациенткам, советуется планирование беременности после трансплантации почки [22].
Перед зачатием необходимо обсудить с пациенткой следующие вопросы:
1. Методы контрацепции, которые следует использовать до активной попытки забеременеть
2. Исходы беременности (как матери, так и плода) в условиях диализа
3. Риски для матери
4. Прием лекарств до, во время и после беременности
5. Ведение диализа во время беременности
Акушерские результаты
У пациентов с диализом исторически были плохие исходы беременности, но они улучшились благодаря более качественному оказанию диализной помощи. Небольшие исследования показали, что интенсивный диализ улучшает исход беременности [10]. Диализные пациенты с остаточной функцией почек могут иметь лучшие исходы живорождения. Лучшие исходы связаны с более высокой остаточной функцией почек, которая часто снижается со временем на диализе. Однако, в литературе нет данных о продолжительности жизни детей, рожденных от пациенток, получавших диализ во время беременности.
Материнство. Данные о течении беременности у пациенток с ХБП С5D, ограничены. Первоначальные отчеты указывали на повышенную частоту неконтролируемой гипертензии, преэклампсии и HELLP-синдрома (гемолиз, повышенный уровень ферментов печени и низкий уровень тромбоцитов) [116]. Женщины с ХБП C5D должны быть обследованы на депрессию как во время беременности, так и в послеродовом периоде.
Плод. Имеется высокий уровень неонатальной смертности/мертворождения, риски преждевременных родов и низкий вес при рождении.
Беременность
Во время беременности женщину необходимо перевести на ежедневный диализ с момента подтверждения беременности.
Обследование
1. Контроль мочевины, бикарбоната и электролитов в сыворотке.
2. Оценка адекватности клиренса растворенных веществ (коэффициент восстановления мочевины [URR], Kt/V).
3. Функциональные пробы печени
4. Развернутый анализ крови и исследование железа, процент насыщения трансферрина и ферритин в сыворотке
5. Измерение сывороточного кальция, фосфора и паратиреоидного гормона
6. Измерение сывороточного альбумина и оценка нутритивного статуса.
7. Уровень глюкозы в плазме и, у пациентов с известным или имеющим риск развития прегестационного сахарного диабета, гликозилированный гемоглобин (HbA1C).
8. У пациентов с системной красной волчанкой (СКВ) определение антифосфолипидных антител [волчаночный антикоагулянт (LA), антитела иммуноглобулина G (IgG) и IgM к кардиолипину (aCL) и антитела IgG и IgM к бета2-гликопротеину (GP) I] и антитела, которые могут воздействовать на плод (анти-Ro/SSA, анти-La/SSB)
Диагностика беременности.
Беременность диагностируется с помощью сывороточного бета-хорионического гонадотропина человека (ХГЧ) и ультразвукового исследования.
Одного содержания бета-ХГЧ в сыворотке недостаточно для диагностики у диализных пациентов. Бета-ХГЧ экскретируется почками, и его уровни в сыворотке могут быть повышены у женщин с ХБП C5D в отсутствие беременности, при этом в одном исследовании предлагается использовать более высокое пороговое значение 25 мМЕ/мл для исключения беременности, когда статус фертильности неясен [115]. У женщин с подозрением на беременность из-за повышенного уровня бета-ХГЧ в сыворотке УЗИ подтверждает наличие жизнеспособного плода и оценивает гестационный возраст.
Мониторинг беременной
Беременные женщины с ХБП С5D, должны находиться под совместным наблюдением нефролога, диетолога и акушер-гинеколога.
Наблюдение врачей нефролога, диетолога и акушер-гинеколога
| Наблюдение | Частота |
| Первый триместр | ежемесячно |
| Второй триместр | каждые две недели |
| Третий триместр | еженедельно |
Рекомендации по ведению дневника наблюдения беременных с ХБП C5D
| Данные | |
| Речь | ежедневно |
| Подвижность | ежедневно |
| Температура тела | ежедневно |
| Частота дыхания | ежедневно |
| Частота сердечных сокращений | ежедневно |
| АД при каждом посещении | ежедневно |
| Сатурация (SpO2) | ежедневно |
| Суточное АД мониторирование | ежемесячно |
| Измерение мочевины | еженедельно |
| Измерение мочевая кислота | еженедельно |
| Измерение бикарбонатов | еженедельно |
| Измерение электролитов | еженедельно |
| Измерение глюкозы в сыворотке крови | ежедневно |
| Оценка адекватности клиренса растворенных веществ (коэффициент восстановления мочевины [URR], Kt/V), недельный st Kt/V | ежедневно |
| Полный анализ крови и процентное насыщение трансферрина | раз в неделю* |
| Железо в сыворотке, общая железосвязывающая способность | раз в неделю* |
| Измерение ферритина в сыворотке | раз в неделю* |
| Измерение корректированного кальция | раз в неделю* |
| Измерение фосфора и паратиреоидного гормона | раз в неделю* |
| Витамин Д | раз в неделю* |
| Измерение сывороточного альбумина | раз в неделю* |
| Оценка нутритивного статуса | ежедневно |
| Функциональные пробы печени | раз в неделю* |
Скрининги беременных
Беременным без факторов риска по диабету на сроке от 24 - 28 недель беременности рекомендовано проводить скрининг на нарушение толерантности к глюкозе с целью выявления гестационного диабета.
Женщины, получающие глюкокортикоиды и/или ингибиторы кальциневрина, а также имеющие традиционные факторы риска гестационного диабета, проходят дополнительный ранний скрининг.
Женщины, с остаточной мочой, должны периодически проходить скрининг на наличие бессимптомной бактериурии. Лечение проводится в соответствии с рекомендациями для беременных, не находящихся на диализе.
Мониторинг плода
| Время | Метод оценки |
| Первый триместр | определение толщины воротникового пространства |
| Второй триместр | оценка хромосомных аномалий, включая синдром Дауна |
| Каждые три-четыре недели | рост и вес плода, количество околоплодных вод |
| два раза в неделю | антенатальное тестирование (биофизический профиль с допплеровской оценкой пуповины) |
Питание во время беременности.
Внимание к вопросам питания и правильное увеличение веса необходимы для успешной беременности [26].
Диета:
Белок: ежедневное потребление белка от 1,5 до 1,8 г/кг в день.
Витамины: двойные дозы водорастворимых витаминов и добавки с фолиевой кислотой 5 мг/день. Потребность в фолиевой кислоте выше, чем у людей без диализа, потому что фолиевая кислота выводится при диализе. Прием витаминов группы В ежедневно.
Фосфор: беременные женщины, находящиеся на диализе, не должны подвергаться никаким ограничениям фосфатов и, как правило, не нуждаются в связывающих фосфаты препаратах из-за интенсификации гемодиализа. На самом деле во время диализа может потребоваться добавление фосфатов.
Оценка сухого веса: женщины должны набирать примерно от 0,9 - 1,8 кг в течение первых трех месяцев беременности и по 0,45 кг в неделю после этого, что требует регулярной корректировки сухого веса. Для определения целей ультрафильтрации рекомендуется тщательная клиническая оценка состояния объема тела.
Роды
У большинства женщин, находящихся на диализе, сроки родов запланированы на 37 неделю беременности или сразу после нее, если они еще не были родоразрешены по акушерским или медицинским показаниям. Продление беременности дольше 37 недель может увеличить материнский и/или перинатальный риск. Поскольку эти женщины получают гепарин во время гемодиализа срок родов должен быть запланирован. Кесарево сечение проводится по стандартным акушерским показаниям.
Преждевременные роды могут быть необходимы при тяжелой преэклампсии, задержке роста или при выявлении аномалий развитии плода.
Сульфат магния. Многие женщины получают сульфат магния перед родами либо для предотвращения судорог при преэклампсии, либо для снижения риска церебрального паралича до преждевременных родов младенца <32 недель. Магний выводится, преимущественно, почками. Накопление магния потенциально опасно для жизни из-за угнетения дыхания, аритмии и угнетения центральной нервной системы. Женщинам с ХБП С5D, которым требуется сульфат магния перед родами, наполовину снижается как нагрузочная доза, так и скорость инфузии. Необходимо, следить за концентрацией магния в сыворотке крови и клиническое наблюдение за наличием признаков токсичности магния.
Материнские осложнения
Потенциальные осложнения у беременных женщин на диализе: преэклампсия, инфекция и анемия, HELLP-синдром.
Инфекция. Беременные женщины на диализе подвержены риску инфекций, связанных с диализным доступом, таких как бактериемия, связанная с туннельным гемодиализным катетером, которая может быть опасной для жизни.
Анемия. Анемия является частым осложнением у беременных женщин с ХБП С5D.
Факторы, способствующие развитию анемии у беременных с ХБП C5D
1. относительный дефицит эритропоэтина из-за высокой потребности в выработке эритроцитов для поддержки роста плаценты и плода,
2. потеря железа и эритроцитов при частом и интенсивном диализе
3. резистентность к эритропоэтину из-за продукции воспалительных цитокинов.
Доза диализа и лечение
Дозу диализа необходимо скорректировать как можно скорее после подтверждения беременности. Конкретная доза варьирует в зависимости от остаточной функции почек. Беременным пациенткам без остаточной функции почек рекомендуется диализ не менее 24 часов в неделю.
Интенсивный диализ. Более частый (до 5 или 6 раз в неделю) и/или более длительный диализ снижает риск многоводия, помогает контролировать гипертензию, увеличивает массу тела при рождении и гестационный возраст, улучшает питание матери и увеличивает шансы живорождения [19,29]. Оценка адекватности клиренса растворенных веществ (коэффициент восстановления мочевины [URR], Kt/V). Достигать целевых уровней. Нет необходимости в гемодиафильтрации!
Калий. Рекомендуется использовать диализат с содержанием калия ≥3 мЭкв/л. Это снижает риск гипокалиемии, которой следует избегать. Гиперкалиемия встречается редко из-за интенсивного диализа, и концентрация диализата <3 мЭкв/л требуется редко.
Кальций. Используется концентрацию кальция в диализате 1,5 ммоль/л (6 мг/дл), чтобы избежать риска гипокальциемии.
Бикарбонат. Используется концентрация диализата 30 мЭкв/л, что обычно достаточно для предотвращения метаболического ацидоза у пациентов, находящихся на интенсивном диализе. Если развивается метаболический ацидоз, бикарбонат диализата может быть увеличен до 35 мЭкв/л.
Фосфат. При развитии гипофосфатемии, несмотря на обильное потребление фосфора с пищей (и отсутствие связывающих фосфаты), рекомендуется добавлять фосфат натрия в диализат, чтобы достичь концентрации до 4,5 мг/дл (1,5 ммоль/л). Концентрацию фосфатов в диализате регулируют для поддержания концентраций фосфатов до и после диализа в пределах нормы.
Интрадиализная гипотензия. Беременные пациенты должны находиться под более тщательным наблюдением во время диализа, чтобы избежать интрадиализной гипотензии. Это особенно важно во время последней части сеанса. Гемодинамическая нестабильность матери может нарушить маточно-плацентарное кровообращение и может быть связана с индукцией сокращений матки [ 18 ].
Еженедельная оценка объема жидкости. Врач должен еженедельно проводить тщательное физикальное обследование, включая оценку массы тела пациента, АД жидкость, полученную между сеансами диализа, от жидкости, вызванной увеличением веса, связанным с беременностью. Сухой вес увеличивается на протяжении всей беременности и должен увеличиваться примерно на 0,5 кг в неделю во втором и третьем триместрах. Тем не менее, предполагаемое увеличение сухой массы во время беременности не следует считать фиксированным, и сухую массу следует постоянно переоценивать и корректировать по мере необходимости в зависимости от артериального давления пациентки, объема и состояния питания.
Отсутствует доказательства высокого качества, определяющие оптимальную скорость или цель ультрафильтрации у беременных женщин, находящихся на диализе.
Удаление жидкости во время гемодиализа должно подбираться индивидуально для каждого пациента. Поскольку у беременных проводится ежедневный гемодиализ (т.е. пять-шесть раз в неделю), рекомендуется проводить ультрафильтрацию 1-2 литра за сеанс диализа, что аналогично тому, что используется у пациентов, находящихся на ночном гемодиализе. У пациентов, чье артериальное давление до диализа составляет >120/70 мм рт.ст., скорость ультрафильтрации во время диализа корректируется, чтобы избежать интрадиализую гипотензию.
У беременных женщин ультрафильтрация (УФ) может увеличить число эпизодов интрадиализной гипотензии, что может привести к ишемическому повреждению плаценты и является изменяемым фактором риска для плода, приводящим к выкидышам, преждевременным родам, низкому весу при рождении. Расчет объема и скорости УФ должен быть персонифицированным, проводиться тщательно и осторожно, с использованием наименьшей возможной скорости УФ. Оценка сухого веса беременной пациентки пересматривается и определяется еженедельно в начале недели перед диализом, чтобы избежать излишнего удаления жидкости УФ. С целью мониторинга сухого веса и коррекции объема и скорости ультрафильтрации необходимо оценивать кровоток в плаценте и плоде с помощью акушерской допплеровской ультразвуковой диагностики, проводимой в комнате гемодиализа в начале и конце сеанса, чтобы получить допплеровские велосиметрические параметры (пульсационный индекс и индекс сопротивления) маточных, пупочных и средних мозговых артерий.
Антикоагулянты. Гепарин считается безопасным для использования в качестве антикоагулянта во время беременности.
Артериальная гипертензия. Конкретные целевые значения АД для беременных с ХБП C5D не определены [33]. Постдиализная цель для небеременных диализных пациенток составляет <140/90 мм рт.ст.
При диагностировании резистентной гипертензии рекомендовано решить вопрос о прерывании беременности.
МКН-ХБП. Во время беременности нет необходимости использовать фосфатсвязывающие средства, хотя они и не противопоказаны. Гиперфосфатемия наблюдается редко, так как больные почти ежедневно находятся на диализе. Если необходимы фосфатсвязывающие средства, то предпочтительнее карбонат кальция, поскольку данные о беременности относительно других фосфатсвязывающих средств (например, севеламера, карбоната лантана, ацетата кальция) ограничены. Связывающие фосфаты могут снижать всасывание жирорастворимых витаминов и фолиевой кислоты. Кальцитриол можно применять до и во время беременности, показания такие же, как и для небеременных пациентов с ХБП. Однако, необходимо учесть риски кальцификации.
Цинакальцет не используется во время беременности, поскольку данные о безопасности ограничены.
Лечение анемии. Лечение анемии у беременных на диализе такое же, как и у небеременных, и обычно заключается в поддержании достаточных запасов железа и ЭПО. ЭПО не проникают через плаценту из-за их большой молекулярной массы. Беременным женщинам часто требуются более высокие дозы ЭПО для поддержания адекватной массы эритроцитов, поскольку физиологические изменения и требования беременности могут привести к ухудшению анемии. Показания и цели лечения препаратами железа и ЭПО такие же, как и у небеременных пациентов на диализе. Препараты железа вводятся внутривенно.
Послеродовый уход
Послеродовой уход у женщин ХБП C5D аналогичен уходу у женщин с нормальной функцией почек. Единственным исключением является то, что необходимо избегать приема нестероидных противовоспалительных препаратов (НПВП), особенно у женщин с остаточной функцией почек. Рекомендуется продолжить прием ЭПО и внутривенное введение железа по мере необходимости. Противопоказаний к грудному вскармливанию среди диализных больных нет. Важно избегать агрессивной УФ при диализе, так как уменьшение объема может помешать грудному вскармливанию.
Гипертензию следует лечить препаратами, которые считаются безопасными для грудного вскармливания, такими как лабеталол, нифедипин и иАПФ, которые не попадают в грудное молоко (например, каптоприл , эналаприл или квинаприл) [116,117]. Не используется БРА, так как они недостаточно изучены.
В послеродовом периоде многие женщины возобновляют свои графики диализа три раза в неделю как до беременности, поскольку интенсивные графики, рекомендуемые во время беременности, трудно поддерживать.
Стандартное определение случая КАИК:
| А |
Лечащий врач ежедневно вносит в историю болезни (лист наблюдения)
катетеризированного пациента данные о манипуляциях, проведенных с катетером, замене повязки, изменениях в области установки катетера и др.
|
| Рекомендуемые количественные показатели | Расчет показателя |
| Частота катетер-ассоциированных инфекций кровотока | 1/1000 пациенто/часов |
| Частота ИСМП | 1/1000 госпитализаций |
| Охват персонала вакцинацией против HBV | 100% |
| Охват персонала вакцинацией против гриппа | 100% |
|
Например:
N 18.0. ХБП C5D (2023) как исход хронического гломерулонефрита, неуточненной морфологии. Хронический программный гемодиализ.
R65.1 Катетер-ассоциированная инфекция. Сепсис. Септический шок.
|
Клинические признаки:
Лабораторные признаки:
Лабораторные исследования при подозрении на сепсис:
Препараты гидроксиэтилкрахмала при сепсисе и септическом шоке ПРОТИВОПОКАЗАНЫ
Необходимо оценивать волемический статус и предотвратить возможное развитие гиперволемии.
Рекомендуется сократить объемы вводимых растворов или прекратить инфузию, если состояние пациента в результате болюсной инфузии растворов не улучшается и появляются признаки гиперволемии (т.е. влажные хрипы при аускультации, отек легких по данным рентгенографии грудной клетки) [118-124].
Цели лечения в первые 6 ч:
Не рекомендуется:
Рекомендуется определение возбудителя инфекции с целью перехода от эмпирической к этиотропной эскалационной терапии в течение 3-5 дней:
Рекомендуется при выборе препарата учитывать спектр действия, предполагаемый очаг инфекции и предыдущую антибактериальную терапию до поступления в ОРИТ.
Факторы риска по антибиотикорезистентности:
Септический шок ставится при наличии артериальной гипотонии (см. таблицу) или двух или трех из следующих симптомов:
Нижние границы САД у детей
| Возраст | Показатель |
| Доношенные новорожденные | Менее 60 мм рт. ст. |
| 1 месяц – 12 месяцев | Менее 70 мм рт. ст. |
| 1 – 10 лет | Менее (70 + 2 x возраст, годы) |
| Старше 10 лет | Менее 90 мм рт. ст. |
Кристаллоиды - физиологический раствор и раствор Рингера.
Необходимо сократить объем вводимых растворов или прекратить инфузию при признаках перегрузки объемом, которые могут проявляться как:
Целевые показатели перфузии включают показатели, соответствующие возрастной норме у детей:
Примечание:
Риск смерти от рака. Несмотря на более высокий риск развития определенных опухолей среди пациентов, находящихся на диализе, злокачественные новообразования являются относительно редкой причиной смерти в этой популяции пациентов. Например, в ежегодном отчете United States Renal Data System (USRDS) за 2020 г. указано, что злокачественные новообразования стали причиной приблизительно 3% всех смертей среди пациентов, находящихся на гемодиализе, которые умерли в 2018 г. [136]. Для сравнения, аритмия/остановка сердца, отказ от диализа и инфекция стали причиной 44, 19 и 7 процентов всех смертей, соответственно.
Предоперационная оценка
Оценка доступа
Оценка сопутствующих заболеваний
Кровоточащий диатез. Пациенты с ХБП С5D могут иметь повышенную склонность к кровотечениям во время и/или после хирургического вмешательства.
Гемодиализ
Объемная перегрузка. Оптимальный объемный статус перед операцией частично основан на оценках ожидаемого количества жидкости, которое будет введено и/или потеряно во время операции. Желательно обсудить с хирургом и анестезиологом цели послеоперационного объемного статуса.
Интраоперационная гипотензия - осложнение, обусловленное анестезией, которая способствует системной вазодилатации у пациента с относительно гиповолемией. Последствием гипотензии могут быть тромбоз артериовенозного доступа.
Использование гепарина. Если диализ проводится в день операции, рекомендуется минимизировать или не использовать гепарин во время диализа.
Уремическое кровотечение. Профилактические меры для минимизации или предотвращения клинически значимого кровотечения во время и после операции, включают:
РЕКОМЕНДАЦИИ ПО ВЕДЕНИЮ И ЛЕЧЕНИЮ ВИЧ-ИНФИЦИРОВАННЫХ С ХБП С4-5D
Обучение всех медицинских работников, сотрудников, стажеров и партнеров по оказанию помощи стандартным процедурам инфекционного контроля и протоколам инъекций игл имеет важное значение. Несмотря на редкость задокументированной передачи ВИЧ от пациента к пациенту и от пациента к медицинскому работнику в условиях диализа, необходимо проводить рутинный скрининг на ВИЧ с целью профилактики постконтактных вспышек. Соблюдение мер предосторожности в диализном отделении должно свести к минимуму риск передачи ВИЧ.
Диализная изоляция — Центры по контролю и профилактике заболеваний США (Centers for Disease Control and Prevention - CDC) не рекомендуют рутинную изоляцию или специальные аппараты для больных с ВИЧ, находящихся на гемодиализе, учитывая низкую вероятность передачи инфекции от пациента к пациенту и/или от пациента к персоналу [26]. Пока медицинские работники соблюдают стандартные меры предосторожности в диализных отделениях, считается, что нет необходимости в специальной изоляции для больных с ВИЧ, находящихся на диализе.
Передача иглой. Риск сероконверсии ВИЧ после укола иглой оценивается в 3 на 1000 или 0,3 процента. Для сравнения, предполагаемый риск передачи вирусов HBV и HСV составляет от 6 до 30 процентов и 2 процента, соответственно [143]. Чем крупнее инокулят крови, чем глубже чрескожное повреждение, и чем позже стадия ВИЧ-инфекции у исходного пациента, тем выше риск передачи ВИЧ [144].
Количество вируса в ультрафильтрате. Недостаточно доказательств, касающихся наличия или отсутствия ВИЧ в ультрафильтрате. Вирус ВИЧ, способный к репликации, можно обнаружить из выделений после перитонеального диализа [144-146]. Клиническая значимость репликативно-компетентного ВИЧ в выделениях после перитонеального диализа неизвестна. Хотя не было описано ни одного случая передачи ВИЧ через перитонеальный диализ. Жидкость представляет теоретический биологический риск для работников, занимающихся утилизацией отходов, и медицинского персонала.
Выбор методов диализа. Нет убедительных доказательств того, что для людей с ВИЧ один из методов диализа лучше, чем другой [146].
Сосудистый доступ. Всем пациентам с ВИЧ, находящиеся на подготовке к ЗПТ рекомендуется предварительная установка АВФ [147]. При отсутствии технической возможности установки АВФ, рекомендуется установить артерио-венозный протез. Не рекомендуется перманентный туннельный катетер в связи с высоким риском инфицирования независимо от ВИЧ-статуса.
Пересадка почки у больных с ВИЧ
Лечение туберкулеза у диализных пациентов. Пациенты с туберкулезом не должны прекращать прием противотуберкулезных препаратов. Профилактическое лечение туберкулеза, лечение лекарственно-чувствительного или лекарственно-устойчивого туберкулеза должно продолжаться непрерывно, чтобы сохранить здоровье пациента, снизить передачу и предотвратить развитие лекарственной устойчивости.
Выявление и оценка ВГС при ХБП С 4-5D
| А | Рекомендуется проводить скрининг на инфицирование ВСГ всем пациентам при первом обследовании по поводу ХБП |
| А | Рекомендуется проведение экспресс теста или серологического тестирования методом ИФА для определения анти-ВГС суммарных (IgG и IgМ) или класса IgG |
| А | Рекомендуется, в случае обнаружения антител анти-ВГС, определить РНК ВГС ПЦР-тестированием |
| А | Рекомендуется проводить скрининг на инфицирование ВГС всем пациентам на момент начала гемодиализа в любом диализном центре, а также при переводе пациента из другого диализного центра или переходе на гемиодиализ с другого вида заместительной терапии |
| А | Рекомендуется проводить скрининг на инфицирование ВГС всем пациентам, проходящим обследование перед трансплантацией почки |
| А | Рекомендуется проводить скрининг на инфицирование ВГС каждые 6 месяцев с помощью иммуноферментного анализа или ТНК |
О каждом новом случае инфицирования ВГС у пациентов, получающих лечение гемодиализом, следует сообщать в соответствующие органы здравоохранения.
| А | При выявлении в отделении нового случая инфицирования ВГС рекомендуется обследовать на наличие инфекции ВГС всех пациентов отделения и увеличить частоту последующих обследований на ВГС |
| А | При выявлении в отделении нового случая инфицирования ВГС рекомендуется обследовать на наличие инфекции ВГС всех пациентов отделения и увеличить частоту последующих обследований на ВГС |
| А | После излечения от ВГС рекомендуется обследовать пациентов, получающих лечение гемодиализом, каждые 6 месяцев с помощью ТНК для выявления возможной реинфекции. |
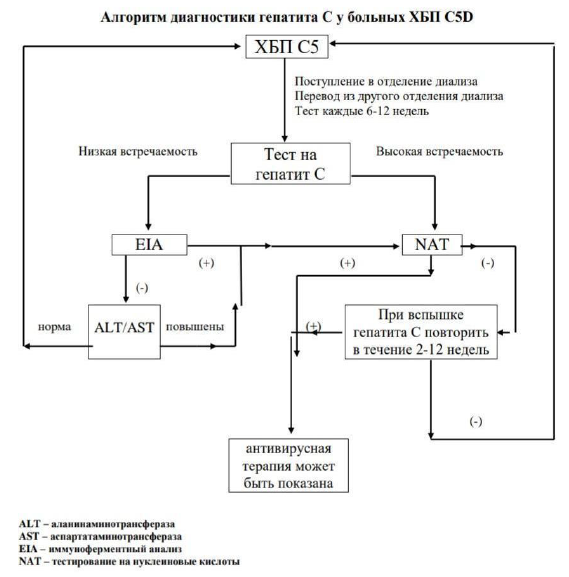
| А | Все пациенты с ВГС (острый и хронический с вирусемией) являются кандидатами для ПВТ, включая с неудачей предыдущей ПВТ [WHO, EASL, AASLD] |
Лечение гепатита С у больных с ХБП С ХБП 4-5D
| А |
РЕКОМЕНДУЕТСЯ назначить пациентам старше 18 лет без цирроза печени следующие ПППД [WHO, AASLD]:
• софосбувир/велпатасвир (12 нед);
• софосбувир/даклатасвир (12 нед);
• глекапревир/пибрентасвир (8 нед).
|
| А | Пациенты с ХБП легкой и средней степени тяжести (СКФ≥30 мл/мин/1,73 м2) должны получать лечение ПППД без коррекции доз в соответствии с общими рекомендациями с тщательным мониторингом побочных явлений [WHO, EASL, AASLD] |
| А | Пациентам с компенсированным заболеванием печени, вызванным любым генотипом ВГС, с тяжелой ХБП (СКФ <30 мл/мин/1,73 м2) или терминальной стадией ХБП, находящимся на гемодиализе, не имеющим показаний к трансплантации почки, может быть назначена фиксированная комбинация Глекапревир/Пибрентасвир продолжительностью 8 или 12 недель, согласно общим рекомендациям |
| А | НЕ РЕКОМЕНДУЕТСЯ использовать комбинации на основе софосбувира в лечении ВГС для пациентов с ХБП 4 и 5 степени (СКФ <30 мл/мин/1,73 м2) [WHO, AASLD] |
| А | Вне зависимости от того, проводилась ли терапия ПППД и каков ее результат, все больные гепатитом С должны быть обследованы на наличие осложнений и сопутствующих гепатиту заболеваний. |
| А | Пациенты с клинически или гистологически подтвержденным циррозом печени должны проходить обследование каждые 6 месяцев. |
Профилактика гепатита С в отделении гемодиализа
| А | Отделение гемодиализа должно соблюдать строгие меры профилактики инфекций, передающихся парентеральным путем, включая гепатит С |
Изоляция пациентов, инфицированных вирусом гепатита С, не замещает строгого соблюдения мер профилактики по предотвращению кровяных инфекций.
| В | Использование диализных машин, предназначенных только для инфицированных HСV пациентов, не рекомендуется |
| А | Меры по предотвращению инфекций должны эффективно предотвращать контакт пациентов с кровью или биологическими жидкостями, содержащими кровь, непосредственно, а также через инфицированное оборудование и другие предметы. |
Можно организовать регулярные проверки диализного отделения по соблюдению мер по предотвращению кровяных инфекций.
Профилактика и ведение больных с гепатитом B (HBV) на программном гемодиализе
Независимые факторы риска инфицирования HBV среди пациентов, находящихся на диализе в неэндемичных районах, включают следующее:
1. Наличие HBsAg-положительных пациентов в одном и том же отделении диализа
2. Отсутствие специализированных аппаратов для гемодиализа для HBsAg-положительных пациентов
3. Уровень вакцинации против HBV ниже 50 процентов среди пациентов, находящихся на диализе в одном и том же отделении.
Внутрибольничная передача является общепризнанным риском инфицирования HBV у пациентов, находящихся на гемодиализе. Приготовление инъекционных препаратов на тележке или на месте в зоне гемодиализа связано с более высоким уровнем инфицирования HBV по сравнению с центрами, которые готовили эти лекарства в специальном кабинете для лечения.
Решающее значение для предотвращения внутрибольничной передачи имеет осуществление и соблюдение:
1. Стандартных или универсальных мер предосторожности
2. Процедур отделения гемодиализа для профилактики инфекций, передающихся через кровь
3. Вакцинация против HBV неиммунных лиц
Вспышки инфекции HBV в отделениях диализа чаще всего связаны с несоблюдением универсальных мер предосторожности, отсутствием первоначального и/или периодического скрининга на HBsAg, совместным использованием многодозовых флаконов или оборудования для контакта с кровью или неадекватной вакцинацией, при этом основным фактором, способствующим этому, является загрязнение HBV поверхностей общего оборудования.
Оценка статуса HBV до начала диализа
Все пациенты, начинающие гемодиализ, должны быть обследованы на инфекцию HBV до начала диализа. Следует проводить следующие серологические тесты: поверхностный антиген HBV (HBsAg), поверхностные антитела к гепатиту В (анти-HBs) и основные антитела к гепатиту В (анти-HBc; общий или иммуноглобулин G [IgG])
Последующее лечение зависит от результатов серологического тестирования:
Пациенты с титром анти-HBs ≥10 миллимеждународных единиц (мМЕ)/мл имеют иммунитет к инфекции HBV либо через вакцинацию (отрицательный анти-HBc), либо через предшествующую инфекцию (анти-HBc-положительный). Пациенты с иммунитетом из-за вакцинации должны проходить мониторинг титров анти-HBs, чтобы проверить ослабление иммунитета. Кроме того, эти пациенты должны регулярно проверяться на HBV во время диализа, поскольку сероконверсия в HBsAg-положительный статус может произойти из-за ослабления иммунитета.
HBsAg отрицательный, анти-HBc отрицательный, анти-HBs отрицательный (без предшествующего воздействия) - Лица, ранее не подвергавшиеся воздействию HBV, подвергаются риску внутрибольничной передачи HBV в отделении диализа и должны пройти вакцинацию как можно скорее. Такие пациенты также должны регулярно проверяться на HBV во время диализа. Тем, кто отказывается от вакцинации, может быть показан дополнительный контроль.
HBsAg-положительный (хронический HBV) - Пациенты с HBsAg-положительным результатом имеют острую или хроническую инфекцию HBV. Такие больные должны получать диализ в зоне, которая отделена от основного отделения диализа и требует специальных мер инфекционного контроля для предотвращения передачи HBV другим пациентам и персоналу. Следует отметить, что не все отделения диализа могут иметь ресурсы для диализа пациентов с хронической инфекцией HBV. Для пациентов, у которых впервые диагностирован хронический HBV, дальнейшее тестирование включает оценку статуса е-антигена HBV (HBeAg), уровня ДНК HBV и наличия или отсутствия цирроза.
Изолированный анти-HBc-положительный - Пациенты, которые отрицательны как на HBsAg, так и на анти-HBs и положительны на анти-HBc, называются изолированными анти-HBc-положительными. У таких пациентов следует измерять уровень циркулирующей ДНК HBV, чтобы лучше оценить статус HBV. Считается, что те, у кого отрицательный результат на HBsAg, но у которых обнаруживается ДНК HBV, имеют скрытую инфекцию HBV, которая часто представляет собой низкое вирусное репликативное состояние. Изолированный анти-HBc-положительный результат также может возникать как преходящее явление при острой инфекции HBV, и в этом случае анти-HBc относится к изотипу иммуноглобулина M (IgM).
Скрытый гепатит В относительно редко встречается среди пациентов, находящихся на гемодиализе, затрагивая менее 3 процентов, и заболеваемость коррелирует с местной распространенностью носителей HBV. Однако скрытая инфекция HBV несет в себе риск внутрибольничной передачи; таким образом, рекомендуется, чтобы HBsAg-отрицательные, HBV-ДНК-положительные пациенты были отделены во время диализа от тех, кто является HBsAg-положительными.
Интерпретация серологической панели HBV
|
Тесты
|
Результаты | Интерпретация |
| HBsAg | Отрицательная | Восприимчивое лицо к HBV |
| анти-HBc | Отрицательная | |
| анти-HBs | Отрицательная | |
| HBsAg | Отрицательная | Предшествующая инфекция (неактивная) |
| анти-HBc | Положительная | |
| анти-HBs | Положительная | |
| HBsAg | Отрицательная | Поствакцинальный иммунитет против HBV* |
| анти-HBc | Отрицательная | |
| анти-HBs | Положительная | |
|
HBsAg
|
Положительная | Острое заражение |
|
анти-HBc IgM
|
Положительная | |
|
анти-HBs
|
Отрицательная | |
| HBsAg | Положительная | Хроническая инфекция |
| анти-HBc IgG | Положительная | |
| анти-HBc IgM | Отрицательная | |
| анти-HBs | Отрицательная | |
|
HBsAg
|
Отрицательная | Четыре интерпретации возможный¶ |
|
анти-HBc IgG
|
Положительная | |
|
анти-HBs
|
Отрицательная |
* Реакция антител (анти-HBs) может быть измерена количественно или качественно. О защитном ответе антител сообщается количественно как 10 или более миллимеждународных единиц (≥10 мМЕ / мл) или качественно как положительный. Поствакцинальное тестирование должно быть завершено через один-два месяца после третьей дозы вакцины, чтобы результаты были значимыми.
Это согласуется с хорошо установленной связью между риском внутрибольничной передачи и распространенностью HBsAg-положительных пациентов в центре гемодиализа.
Пациенты с ТХПН имеют сниженный ответ на вакцинацию против HBV. Для улучшения выработки антител к вакцине против HBV в этой популяции использовались следующие стратегии:
1. Удвоение дозы вакцины (т.е. 40 мкг/доза у пациентов с ТХПН).
2. Введение вакцины против HBV с использованием нового иммуностимулирующего адъюванта.
3. Начало серии вакцинации, как только будет распознана ХБП и у пациента будет известно, что у него отрицательный поверхностный антиген HBV (HBsAg) и антитела. Клиницист не должен ждать, пока пациент станет зависимым от диализа, чтобы начать протокол вакцинации.
4. Введение дополнительной серии вакцин пациентам, находящимся на диализе, которые не ответили на начальную серию, которая определяется как титры антител ≤10 международных единиц / л через один-два месяца после завершения первой серии.
5. Введение однократной бустерной дозы, если титр антител падает до ≤10 международных единиц/л у пациента, у которого первоначально развился ответ антител на вакцинацию или после естественной инфекции.
6. Введение комбинированной вакцины против гепатита А и В.
Рекомендуемые дозы рекомбинантных вакцин против HBV для лиц в возрасте 18 лет лет и старше.
|
Возрастная группа и связанные с ней состояния
|
Объем (мл) | Доза HBsAg (мкг) | Рекомендуемая схема | |
| Одноантигенные вакцины | ||||
| Рекомбивакс НВ | ||||
| Педиатрическая/подростковая формулировка | От 18 до 19 лет |
0.5
|
5 | 0, 1 и 6 месяцев |
|
Взрослая формулировка
|
≥20 лет | 1 | 10 | |
| Препарат для диализа | Взрослые, находящиеся на гемодиализе, и другие взрослые с ослабленным иммунитетом в возрасте ≥20 лет | 1 | 40 | 0, 1 и 6 месяцев |
| Энгерикс-Б | От 18 до 19 лет | 0,5 | 10 | 0, 1 и 6 месяцев |
| ≥20 лет | 1 | 20 | ||
| Взрослые, находящиеся на гемодиализе, и другие взрослые с ослабленным иммунитетом в возрасте ≥20 лет |
2*
|
40 | 0, 1, 2 и 6 месяцев | |
| Геплисав-Б¶Δ | ≥18 лет | 0,5 | 20 | 0 и 1 месяцев |
| ПреХевбрионΔ◊ | ≥18 лет | 1 | 10 | 0, 1 и 6 месяцев |
| Комбинированная вакцина | ||||
| Twinrix (комбинированная вакцина против HBV-Гепа) | ≥18 лет | 1 | 20 |
Стандарт: 0, 1 и 6 месяцев
Ускоренный: 0, 7 и от 21 до 30 дней и 12 месяцев
|
Это двойная доза стандартной формы Engerix-B для пациентов ≥ возрасте 20 лет (Engerix-B не имеет отдельной диализной формулы).
Δ Недостаточно данных для информирования о рисках, связанных с вакцинацией Heplisav-B и PreHevbrio во время беременности. Таким образом, медицинские работники должны вакцинировать беременных женщин, нуждающихся в вакцинации против HBV, препаратами Engerix-B, Recombivax HB или Twinrix. Кроме того, отсутствуют данные для оценки влияния Heplisav-B и PreHevbrio на грудных детей или на выработку и выделение материнского молока.
Госпитализация
Решение принимается на индивидуальной основе, пользуясь следующими общими принципами и маршрутизацией в зависимости от степени тяжести:
Течение ХБП С4-5 без осложнений:
1. коррегируемая артериальная гипертензия и гиперволемия
2. отсутствие тяжелой анемии
3. коррегируемые медикаментозно электролитные нарушения и метаболический ацидоз
4. отсутствие уремии.
Рекомендовано: лечить амбулаторно у нефролога в ОЗ вторичного или третичного уровня. Предварительно подготовить сосудистый доступ.
Течение ХБП С4-5 с осложнениями:
1. некоррегируемая артериальная гипертензия и гиперволемия
2. тяжелая анемия
3. электролитные нарушения
4. метаболический ацидоз
5. белково-энергетическая недостаточность
6. уремия
Рекомендовано: госпитализация в стационар вторичного или третичного уровня. При отстутствии отделения нефрологии в регионах, необходимо госпитализировать в любое терапевтическое отделение для коррекции терапии. В отделении необходимо пациенту создать постоянный сосудистый доступ (артерио-венозная фистула, артерио-венозный протез, перманентный катетер), достичь целевых уровней АД, провести гемотрансфузию, откорректировать нарушения электролитного обмена, кислотно-основного состояния, водно-электролитного баланса, нутритивного статуса и минерально-костных нарушений.
Критическое течение ХБП:
1. Декомпенсация сердечной недостаточности при уремической интоксикации (острая и подострая левожелудочковая недостаточность, анасарка, уремический перикардит, артериальная гипотония);
2. Электролитные нарушения (жизнеугрожающая гипер-и гипокалемия, гипонатриемия, гипокальциемия, дизэквилибриум-синдром);
3. Уремическая интоксикация (кома);
4. Неконтролируемая артериальная гипертензия;
5. Тяжелая прогрессирующая анемия (ренальная и/или постгеморрагическая);
6. Осложнения функционирующей артериовенозной фистулы (АВФ) (инфекции, кровотечения);
7. Метаболический ацидоз и другие осложнения, требующие неотложной терапии.
Рекомендовано: госпитализация в отделение интенсивной терапии. Экстренно начать ЗПТ.
Информация
Источники и литература
-
Клинические протоколы Министерства здравоохранения Кыргызской Республики
- 1. Клиническое руководство по ведению больных с острым почечным повреждением. Калиев Р.Р., Айыпова Д.А., Бейшебаева Н.А. 2019. 2. Клиническое руководство по ведению больных с хронической болезнью почек. Калиев Р.Р., Айыпова Д.А., Бейшебаева Н.А. 2019. 3. National Kidney Foundation. K/DOQI clinical practice guidelines for chronic kidney disease: evaluation, classification, and stratification. Am J Kidney Dis 2002; 39: S1-266. 4. Джон Т. Даугирдас, Питер Дж. Блейк, Тодд С. Руководство по диализу. 2003 г. 5. KDOQI Clinical Practice Guideline for Hemodialysis Adequacy. AJKD 2015: 66 (5); 884–930. 6. KDIGO clinical practice guideline for the care of kidney transplant recipients. Am J. Transplant, 2009. 9 Suppl 3: p. S1-155 7. Daul AE, Schafers RF, Daul K et al. Exercise during hemodialysis. Clin Nephrol 2004; 61 (Suppl 1): S26–30. 8. Deligiannis A. Cardiac adaptations following exercise training in hemodialysis patients. Clin Nephrol 2004; 61 (Suppl 1): S39–45. 9. Liu SH, C. LC, Yeh SH et al. Effect of exercise training on hemodialysis. Journal of the Formosan Medical Association 2002; 6: 129–142. 10. Mustata S, Chan C, Lai V et al. Impact of an exercise program on arterial stiffness and insulin resistance in hemodialysis patients. J Am Soc Nephrol 2004; 15: 2713–2718. 11. Ouzouni S, Kouidi E, Sioulis A et al. Effects of intradialytic exercise training on health-related quality of life indices in haemodialysis patients. Clin Rehabil 2009; 23: 53–63. 12. European Best Practice Guidelines for Haemodialysis (Part 1) Nephrol Dial Transplant (2002) 17 [Suppl 7] 13. European best practice guidelines on haemodialysis (Part 2) Nephrol Dial Transplant (2007) 22 [Suppl 2] 14. Гуревич К.Я. с соавт. Перитонеальный диализ (пособие для врачей). Издание второе, переработанное и дополненное. СПб, 2003 15. Dombros N et al. European Best Practice Guidelines for Peritoneal Dialysis. Nephrol Dial Transplant 2005; 20 [Suppl 9]:1-36. 16. Данович Габриэль М. Трансплантация почки / Пер. с англ. под ред. Я.Г. Мойсюка.– М: ГЭОТАР-Медиа, 2013; с.848 17. Строков А.Г., Гуревич К.Я. Клинические рекомендации. Лечение пациентов с хронической болезнью почек 5 стадии (ХБП 5) методами гемодиализа и гемодиафильтрации. 2016. 18. Davenport A. Optimization of heparin anticoagulation for hemodialysis. Hemodial Int 2011; 15 (suppl 1):43-48 19. Fischer KG. Essentials of anticoagulation in hemodialysis. Hemodial Int 2007; 11: 178-189 20. Go AS, Chertow GM, Fan D et al. Chronic kidney disease and the risks of death, cardiovascular events, and hospitalization. N Engl J Med 2004; 351(13):1296‐305 21. Askenazi DJ, Ambalavanan N, Hamilton K, Cutter G, Laney D. et al. Acute kidney injury and renal replacement therapy independently predict mortality in neonatal and pediatric noncardiac patients on extracorporeal membrane oxygenation. Pediatr Crit Care Med. 2011 Jan;12(1):e1-6. 22. Lopes JA, Fernandes P, Jorge S, Gonçalves S, Alvarez A, Costa e Silva Z, França C, Prata MM. Acute kidney injury in intensive care unit patients: a comparison between the RIFLE and the Acute Kidney Injury Network classifications Critical Care Vol 12 No 4 2008, 12:R110 23. Wizemann V, Wabel P, Chamney P et al. The mortality risk of overhydration in haemodialysis patients. Nephrol Dial Transplant. 2009; 24(5):1574-1579 24. Tattersall J et EUDIAL, Online haemodiafiltration: definition, dose quantification and safety revisited. Nephrol Dial Transplant. 2013 ;28(3): 542-550 25. Chauveau P, Couzi L, Vendrely B et al. Long‐term outcome on renal replacement therapy in patients who previously received a keto acid‐supplemented very‐low‐protein diet. Am J Clin Nutr 2009;90(4):969‐974 26. Fouque D, Pelletier S, Mafra D, Chauveau P. Nutrition and chronic kidney disease. Kidney Int 2011; 80(4): 348‐357 27. Hsu CY, McCulloch CE, Iribarren C, Darbinian J, Go AS. Body mass index and risk for end‐stage renal disease. Ann Intern Med 2006 3;144(1):21‐28 28. de Boer IH, Rue TC, Hall YN, Heagerty PJ, Weiss NS, Himmelfarb J. Temporal trends in the prevalence of diabetic kidney disease in the United States. JAMA. Jun 22 2011;305(24): 2532-2539. 29. Slinin Y, Ishani A, Rector T, et al. Management of hyperglycemia, dyslipidemia, and albuminuria in patients with diabetes and chronic kidney disease: A systematic review for a clinical practice guideline for the National Kidney Foundation. Am J Kidney Dis. 2012; 60(5):747-769. 30. Drechsler C, Krane V, Ritz E, Marz W, Wanner C. Glycemic control and cardiovascular events in diabetic hemodialysis patients. Circulation. Dec 15 2009; 120(24): 2421-2428. 31. Freedman BI, Andries L, Shihabi ZK, et al. Glycated albumin and risk of death and hospitalizations in diabetic dialysis patients. Clin J Am Soc Nephrol. Jul 2011;6(7):1635-1643. 32. Hayashino Y, Fukuhara S, Akiba T, et al. Diabetes, glycaemic control and mortality risk in patients on haemodialysis: the Japan Dialysis Outcomes and Practice Pattern Study. Diabetologia. Jun 2007;50(6):1170-1177 33. Анемия Locatelli F, Aljama P, Canaud B et al. Anaemia Working Group of European Renal Best Practice (ERBP). Target haemoglobin to aim for with erythropoiesis‐stimulating agents: a position statement by ERBP following publication of the Trial to reduce cardiovascular events with Aranesp therapy (TREAT) study. Nephrol Dial Transplant 2010; 25(9): 2846‐2850 34. Locatelli F, Covic A, Eckardt KU et al. ERA–EDTA ERBP Advisory Board. Anaemia management in patients with chronic kidney disease: a position statement by the Anaemia Working Group of European Renal Best Practice (ERBP). Nephrol Dial Transplant 2009; 24:348‐354 35. Joint Speciality Committee on Renal Medicine of the Royal College of Physicians and the Renal Association at RCoGP. Chronic Kidney Disease in adults: UK guidelines for management and referral. Royal College of Physicians, London: 2006 36. Levey AS, Eckardt KU, Tsukamoto Y et al. Definition and classification of chronic kidney disease: a position statement from Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int 2005; 67(6): 2089‐2100. 37. Мухин НА, Моисеев ВС, Кобалава ЖД и др. Кардиоренальные взаимодействия: клиническое значение и роль в патогенезе заболеваний сердечно‐сосудистой системы и почек. Тер арх 2004; (6): 39‐46 38. Kidney Disease Outcome Quality Initiative. K/DOQI clinical practice guidelines on hypertension and antihypertensive agents in chronic kidney disease. Am J Kidney Dis 2004; 43: 1‐290 39. Glynn LG, Reddan D, Newell J et al. Chronic kidney disease and mortality and morbidity among patients with established cardiovascular disease: a West of Ireland community‐based cohort study. Nephrol Dial Transplant 2007; 22(9): 2586‐2594 40. Goodman WG, London G, Amann K et al. Vascular calcification in chronic kidney disease. Am J Kidney Dis 2004;43(3): 572‐579 41. Практические рекомендации KDIGO по диагностие, профилактике и лечению минеральных и костных нарушений при хронической болезни почек (ХБП‐МКН). Краткое изложение рекомендаций. Нефрология 2011; 15(1): 88‐95 42. Hsu CY, McCulloch CE, Iribarren C, Darbinian J, Go AS. Body mass index and risk for end‐stage renal disease. Ann Intern Med 2006 3;144(1):21‐28 43. Дедов И.И., Шестакова М.В., Майоров А.Ю. и др. Сахарный диабет 2 типа у взрослых. Клинические Рекомендации. Сах. диаб 2020;23(S2):36-41. doi: 10.14341/DM23S2 44. Томилина НА. Хроническая болезнь почек. Избранные главы нефрологии. ГЭОТАР-Медиа, М., 2017; 136 c. 45. Gomez LA, Lei Y, Devarapu SK, Anders H-J. The diabetes pandemic suggests unmet needs for «CKD with diabetes» in addition to «diabetic nephropathy»— implications for pre-clinical research and drug testing. Nephrol Dial Transplant 2018;33:1292-1304. doi: 10.1093/ndt/gfx219. 46. Алгоритмы специализированной медицинской помощи больным сахарным диабетом / Под редакцией И.И. Дедова, М.В. Шестаковой, А.Ю. Майорова. – 11-й выпуск. – М.; 2023. 47. Добронравов ВА, Карунная АВ. Прогностическое значение оптимального начала диализа (мета-анализ Рабочей Группы Ассоциации нефрологов). https://rusnephrology.org/wp-content/uploads/2021/04/hd_start_ma.pdf 48. Toward Revision of the ‘Best Practice for Diabetic Patients on Hemodialysis 2012’. Kidney Dial. 2022, 2(4), 495-511; https://doi.org/10.3390/kidneydial2040045 49. Management of adults with diabetes on dialysis: Summary of recommendations of the Joint British Diabetes Societies guidelines 2022. Diabet Med. 2023 Apr;40(4):e15027. doi: 10.1111/dme.15027. Epub 2022 Dec 23. 50. Кidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group. KDIGO 2020 Clinical Practice Guideline for Diabetes Management in Chronic Kidney Disease. Kidney Int. 2020, 98, S1–S115.
Информация
Список сокращений
|
АБК
|
– адинамическая болезнь кости |
| АВП | – артериовенозный протез |
| АВФ | – артериовенозная фистула |
| АГ | – артериальная гипертензия |
| АД | – артериальное давление |
| АК | – антагонисты кальция |
| АПФ | – ангиотензин-превращающий фермент |
|
БЭН
|
– белково-энергетическая недостаточность |
| ВГПТ | – вторичный гиперпаратиреоз |
| ВДРА | – активатор рецепторов витамина D |
| ГД | – гемодиализ |
| ГДФ | – гемодиафильтрация |
| ГЛЖ | – гипертрофия левого желудочка |
| ГПТ | – гиперпаратиреоз |
|
ДАД
|
– диастолическое артериальное давление |
| ДН | – диабетическая нефропатия |
| ДР | – диализный раствор |
| ЖКТ | – желудочно-кишечный тракт |
| ЗПТ | – заместительная почечная терапия |
| ИМТ | – индекс массы тела |
| иПТГ | – интактный паратиреоидный гормон |
| ИЭ | – инфекционный эндокардит |
|
КВЗ
|
– кардиоваскулярные заболевания |
| КЖСТ | – кожно-жировая складка над трехглавой мышцей плеча |
| КИН | – контраст-индуцированная нефропатия |
| КНИ | – ингибитор кальциневрина |
| Кр | – креатинин крови |
|
КТ
|
– компьютерная томография |
| МБД | – малобелковая диета |
| МКН | – минеральные и костные нарушения |
| МПК | – минеральная плотность кости |
| МРТ | – магнитно-резонансная томография |
|
НГ
|
– нет градации |
| НПВС | – нестероидное противовоспалительное средство |
| НФГ | – нефракционированный гепарин |
| ОВЖ | – объем внеклеточной жидкости |
| ОМП | – мышечная масса в области плеча |
| ОПП | – острое повреждение почек |
| ОФП | – остаточная функция почек |
| ОЦК | – объем циркулирующей крови |
|
ПКК
|
– подключичный катетер |
| ПТГ | – паратиреоидный гормон |
| ПТЭ | – паратиреоидэктомия |
| ПЩЖ | – паращитовидные железы |
|
РААС
|
– ренин-ангиотензин-альдостероновая система |
| РВГ | – реноваскулярная артериальная гипертензия |
| РКИ | – рандомизированное клиническое исследование |
| рчЭПО | – рекомбинантный человеческий эритропоэтин |
|
САД
|
– систолическое артериальное давление |
| СД | – сахарный диабет |
| СЗП | – свежезамороженная плазма |
| СКАД | – самостоятельный контроль артериального давления пациентом |
| СКФ | – скорость клубочковой фильтрации |
| СМАД | – суточное мониторирование артериального давления |
| СРБ | – С-реактивный белок |
|
ССО
|
– сердечно-сосудистые осложнения |
| ССЭ | – средства, стимулирующие эритропоэз |
| УЗИ | – ультразвуковое исследование |
| УФ | – ультрафильтрация |
|
ФСП
|
– фосфат-связывающий препарат |
| ХБП | – хроническая болезнь почек |
| ЦВК | – центральный венозный катетер |
| ЩФ | – щелочная фосфатаза |
| ЭхоКГ | – эхокардиография |
|
CKD-EPI
|
- Chronic Kidney Disease Epidemiology Collaboration (Сотрудничество в области эпидемиологии хронических заболеваний почек) |
|
eGFR
|
- Estimated glomerular filtration rate (Расчетная скорость клубочковой фильтрации) |
|
eKt/V
|
- Equilibrated Kt/V (Эквилибрированный Kt/V) |
| Hb | – гемоглобин |
| HBV | – вирус гепатита В |
| HCV | – вирус гепатита С |
|
KDIGO
|
- Kidney Disease: Improving Global Outcomes (Заболевания почек: Улучшение глобальных результатов) |
|
KDOQI
|
- Kidney Disease Outcomes Quality Initiative (Инициатива по обеспечению качества исходов заболеваний почек) |
|
MDRD
|
- Modification of Diet in Renal Disease (Модификация диеты при заболеваниях почек) |
|
NKF
|
- National Kidney Foundation (Национальный почечный фонд) |
| SCr | – сывороточный креатинин |
|
sp
|
- Single-pool (Kt/V) (Единый пул) |
| std | - Standard (Kt/V) (Стандарт) |
| T | – длительность процедуры в часах |
| Vu | – объем мочевины |
Термины и определения
Нефротический синдром - симптомокомплекс, обусловленный нарушением гломерулярно-базального барьера с развитием массивной (нефротической) протеинурии, критериями которого являются: протеинурия >3,5 г/сут/1,73 м*, гипоальбуминемия (альбумин в крови <30 г/л)
Острое повреждение почек - патологическое состояние, развивающееся в результате непосредственного острого воздействия ренальных и/или экстраренальных повреждающих факторов, продолжающееся до 7-ми суток и характеризующееся быстрым (часы-дни) развитием признаков повреждения или дисфункции почек различной степени выраженности. Поскольку острое повреждение почечной паренхимы может быть обусловлено не только реальными (почечными), но также преренальными и постренальными факторами, англоязычному термину «acute kidney injury» соответствует перевод «острое повреждение почек». Термин «острое почечное повреждение», который возник по аналогии с термином «острая почечная недостаточность, не отражает смысла и положений теоретической концепции KDIGO и не рекомендуется к использованию.
Скорость клубочковой (гломерулярной) фильтрации - это количество миллилитров плазмы крови, профильтровавшейся во всех клубочках почек за одну минуту. Величина скорости клубочковой фильтрации выражается в мл/мин, определяется величинами почечного плазмотока, фильтрационного давления, фильтрационной поверхности и зависит от массы действующих нефронов. Используется, как интегральный показатель функционального состояния почек и стандартизуется на площадь поверхности тела.
Терминальная почечная недостаточность - это патологическое состояние, характеризующееся величиной скорости клубочковой фильтрации менее 15 мл/мин/1,73 м3, что соответствует 5-й стадии хронической болезни почек. Хроническая болезнь почек - это персистирующее в течение трех месяцев или более поражение органа вследствие действия различных этиологических факторов, анатомической основой которого является процесс замещения нормальных анатомических структур фиброзом, приводящий к его дисфункции
Адинамическая костная болезнь - форма почеч ной остеопатии, которая характеризуется бедным клеточным составом костных структур (снижение количества остеокластов и остеобластов), уменьше нием скорости резорбции и костеобразования.
Гемодиафильтрация (ГДФ) — это метод заместительной почечной терапии, предусматривающий сочетание диффузии и конвекции для усиления удаления веществ с малой и средней молекулярной массой.
Контраст-индуцированная нефропатия – это ухудшение функции почек после внутривенного введения рентген-контрастного вещества, как правило, временное. Диагноз устанавливается на основании прогрессирующего повышения уровня сывороточного креатинина в течение 24–48 часов после введения контраста.
Ингибиторы кальциневрина – новая группа нестероидных средств с противовоспалительным и иммуносупрессивным действием. Представителями этого класса препаратов являются такролимус и пимекролимус.
Рекомбинантный эритропоэтин человека (очищенный гликопротеин), являющийся гематопоэтическим фактором роста. Получен методом генной инженерии. Увеличивает число эритроцитов, ретикулоцитов, стимулирует синтез гемоглобина в клетках. Не оказывает влияния на лейкопоэз.
Ультрафильтрация — процесс мембранного разделения, а также фракционирования и концентрирования веществ, осуществляемый путем фильтрования жидкости под действием разности давлений до и после мембраны. Размер пор ультрафильтрационных мембран варьируется от 0,01 до 0,1 мкм.
Фосфат-биндеры или фосфат-связывающие препараты (на основе кальция и не содержащие кальций) рекомендуются для снижения сывороточного фосфата и предотвращения гиперфосфатемии у пациентов с ХБП. Кальций связывается с фосфатами в организме и выводит их через почки с мочой.
Хроническая болезнь почек — это медленно прогрессирующее (от нескольких месяцев до нескольких лет) ухудшение способности почек фильтровать метаболические продукты жизнедеятельности, поступающие из крови.
Новая формула креатинина CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration Formula) – это современный метод оценки функции почек( их фильтрационной способности) . Диагностическая точность данной формулы высокая.
eGFR (расчетная скорость клубочковой фильтрации) - показывает в какой степени продукты жизнедеятельности организма выводятся почками из организма.
eKt/v (уравновешенный, двухкамерная модель): Показатель уравновешенного Kt/V (eKt/V) вычисляется по уравнению, основанному на 2х-камерной (двухпуловой) кинетической модели с регионарным кровотоком, которая учитывает последиализный рикошет мочевины.
Организационная работа
Ответственные за клиническое содержание по ведению больных на гемодиализе при сопутствующих заболеваниях
Абылова Назгуль Кубанычбековна ассистент кафедры профессорского курса эндокринологии КГМИПиПК, главный эндокринолог г. Бишкек
Ответственные исполнители проводили систематизацию и обновление ключевых рекомендаций из выбранных международных клинических руководств, включая их адаптацию, предоставили обобщенные данные, а также использовали свой обширный практический опыт для отражения наилучших клинических практик в рекомендациях при формировании содержания обновленного руководства.
Внутренняя рецензия
Декларация конфликта интересов
Перед началом работы по обновлению и формированию 2-й версии клинического руководства на рабочем совещании согласительной комиссии, проведенном 2 июня 2023 г., все члены рабочей группы дали согласие сообщить в письменной форме о наличии финансовых взаимоотношений с фармацевтическими компаниями. Никто из членов авторского коллектива не заявил о наличии коммерческой заинтересованности или другого конфликта интересов с фармацевтическими компаниями или другими организациями, производящими продукцию для диагностики, лечения и профилактики ХБП С4-5 D.
Стратегия поиска информации.
Ключевые поисковые слова и построение запроса
Поиск клинических руководств по ведению больных с ХБП С4-5D осуществлялся в международных доступных электронных базах данных в сети Интернет.
Найденные электронные базы данных по клиническим руководствам и практическим рекомендациям
|
Название ресурса
|
Адрес в сети интернет |
| Российское диализное общество | http://www.nephro.ru/index.php?r=site/main |
| International Society of Nephrology | http://www.theisn.org/ |
| European Renal Association | https://www.era-online.org/ |
| National Kidney Foundation | https://www.kidney.org/ |
| Evidence Based Medicine Guidelines | http://www.ebm-guidelines.com/dtk/ebmg/home |
В итоге поиска было найдено 5 клинических руководств.
Критерии включения/исключения
Характеристика отобранных клинических руководств по ХБП
|
№
|
Название руководства | Качество | Новизна | Применимость | Варианты действий |
| 1 | Российское диализное общество | ++ | +++ | ++ | Обновленные рекомендации по диагностике и ведению хронической болезни почек 2024 |
| 2 | International Society of Nephrology | +++ | +++ | ++ |
Даны рекомендации по лечению и ведению пациентов с ХБП С5d
|
| 3 | European Renal Association | ++ | ++ | + | Обновлены рекомендации о программном гемодиализе |
| 4 | National Kidney Foundation | +++ | +++ | ++ | Обновленные рекомендации по нутритивной поддержке у больных с ХБП |
| 5 | Evidence Based Medicine Guidelines | ++ | ++ | ++ | Даны новые рекомендации по диагностике ХБП |
Дальнейший поиск клинических рекомендаций проводился с использованием англоязычных библиографических ресурсов Medline (через PubMed https://www.ncbi.nlm.nih.gov/pubmed), в базе данных Cochrane Library (http://www.cochranelibrary.com/).
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результата |
| В | Высококачественный (++) систематический обзор когортных исследований или исследований случай-контроль или высококачественное (++) когортное или исследование случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+) |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов |
Цель: Улучшить ведение больных с ХБП С4-5D и сопутствующими состояниями на всех уровнях здравоохранения КР с учетом имеющихся доказательств.
Задачи:
1. Внедрение в практику научно-обоснованных клинико-лабораторных критериев диагностики, принципов и подходов в лечении и ведении больных с ХБП С4-5D и сопутствующих состояний на всех уровнях здравоохранения КР.
Ожидаемые результаты применения клинического руководства:
ИНФЕКЦИОННЫЙ КОНТРОЛЬ В ГЕМОДИАЛИЗНЫХ ЦЕНТРАХ
Предотвращение передачи вирусных и бактериальных инфекций от пациента пациенту, от пациента персоналу и от персонала пациенту.
У больных на хроническом гемодиализе имеется высокий риск инфицирования из-за следующих причин:
1. у больных на гемодиализе нарушен иммунитет из-за их основного заболевания, что повышает их восприимчивость к инфекциям.
2. процесс гемодиализа требует контакта с кровью через сосудистый доступ в течение продолжительного времени.
3. больные на гемодиализе нуждаются в частых госпитализациях и оперативных вмешательствах, что повышает их риск инфицирования нозокомиальными инфекциями.
Отделение гемодиализа — это среда, в которой несколько больных одновременно получают диализ, где существуют повторяющиеся возможности для передачи инфекционных агентов от человека человеку, непосредственно или косвенно через загрязненные устройства, оборудование и расходные материалы, окружающие поверхности или руки медицинского персонала.
Пациенты, получающие диализ, могут столкнуться не только с риском заражения инфекционными заболеваниями, но и с другими неблагоприятными реакциями, которые сложно отличить от инфекций (например, пирогенные и аллергические реакции) или быть такими же опасными для жизни, как инфекции (например, диализная деменция, отравление фтором и воздействие хлораминов).
Инфекции и побочные реакции могут быть результатом системных недостатков в диализном отделении, таких как отсутствие или нарушение правил и процедур контроля инфекции, включая неправильное мытье рук, нарушение правил одевания и снятия перчаток, халатов, масок и т.д.; отсутствие мониторинга известных загрязнителей; или недостаточно обученный персонал.
Медицинский персонал
Все сотрудники диализного отделения (врачи, медсестры, техники, биомедицинские инженеры, диетологи, социальные работники и санитары) должны проходить обследование на гепатит В и гепатит С при приеме на работу.
Все работники диализного отделения, которые подвержены риску заражения вирусным гепатитом В и вирусным гепатитом С, должны ежегодно проходить обследование и, при необходимости, после любого контакта с кровью, серозными жидкостями, мочой.
Всем сотрудникам диализного отделения, которые подвержены риску заражения гепатитом В, должна быть предложена вакцинация против HBV, если у них еще не выработался иммунитет.
Весь вакцинированный персонал должен сдавать анализы на антитела к вирусному гепатиту В для оценки эффекта вакцинации. Всем тем, у кого не получен эффект от первой серии вакцинации, должна быть предложена повторная серия вакцинации против HBV.
После того, как у сотрудника выработались анти- HBsAg антитела, сдавать анализы на антиген или антитела к гепатиту B в будущем не требуется.
Если сотрудник не реагирует на вакцину или подвержен риску заражения, то он должен сдавать анализ на наличие HBsAg и анти-HBsAg антител каждые 6 месяцев. Медицинские работники, устойчивые и неподдающиеся вакцинации против HBV (после 6 доз) НЕ должны работать в зоне, где присутствует риск заражения гепатитом В.
Сотрудники, работающие с больными, у которых обнаружен HBsAg, НЕ должны одновременно ухаживать за пациентами, которые подвержены риску заражения гепатитом В (в течение той же смены или при смене пациентов).
Данные о результатах анализов на гепатит следует хранить в базе данных, чтобы обеспечить быстрый доступ к информации.
Во время всех процедур диализа необходимо соблюдать правила асептики.
Стандартные меры предосторожности должны соблюдаться персоналом при оказании медицинской помощи всем пациентам.
Необходимо мыть руки до и после каждого контакта с пациентом и после снятия перчаток.
Средства индивидуальной защиты (СИЗ) должны одеваться при инициации гемодиализа и при окончании процедуры гемодиализа, а также в любое время, когда есть вероятность контакта с кровью, серозными жидкостями организма и мочой.
Сотрудники диализного центра должны носить чистые защитные халаты, чтобы предотвратить загрязнение одежды при проведении процедур, например, при начале и завершении диализа, а также в процессе работы при чрезвычайных ситуациях (например, когда возникают проблемы с сосудистым доступом и требуется срочное вмешательство во время диализа).
Если одежда запачкается кровью и/или другими биологическими жидкостями, ее следует немедленно сменить. Загрязненный халат должен быть сложен в пластиковый пакет для биологически опасного материала, прежде чем отправить в прачечную.
Халат следует снимать каждый раз при выходе из диализного зала и повесить в специально отведенном месте внутри отделения. В конце рабочей смены использованный халат должен быть брошен в корзину для белья для дальнейшей стирки.
Защитные очки, маска или щиток на лицо, а также стерильные перчатки должны одеваться во время проведения процедуры диализа (например, во время инициации и окончания диализа, установки диализного катетера или в любое время, когда требуется манипулирование сосудистым доступом больного).
Диализный персонал должен вымыть руки, сменить перчатки и избегать касания окружающих предметов непосредственно перед введением инъекций.
Чистые одноразовые перчатки должны использоваться при работе с больным или при прикосновении к оборудованию пациента на диализном месте. Необходимо снимать перчатки и мыть руки после каждого пациента (т.е. между каждым пациентом и диализным местом). Если нет видимого загрязнения рук, то можно использовать безводный антисептический гель для рук (например, спиртовой гель).
Всему вспомогательному персоналу, которые взаимодействуют с пациентами, но не имеют прямой контакт с ними (например, социальные работники, диетологи), следует мыть руки при входе и выходе из диализного зала.
Все порезы и раны должны быть закрыты водонепроницаемым бинтом при уходе за пациентом внутри диализного зала.
Работа с кровью и другим биологическим материалом должна проводиться с применением стандартных мер предосторожности.
Белье должно обрабатываться соответствующим образом.
Все процедуры, при которых может произойти бактериальное или химическое загрязнение, должны контролироваться.
Персоналу НЕ разрешается есть и пить внутри зоны для лечения больных (например, в диализном зале, процедурной комнате, кабинетах).
Только квалифицированному и хорошо подготовленному диализному персоналу, который понимает последствия отклонения от установленных правил, разрешается выполнять процедуры диализа.
Необходимо проводить непрерывное обучение и тренинг персонала правилам и процедурам инфекционного контроля, с постоянным мониторингом и контролем за правильным и адекватным их применением.
Как минимум раз в год необходимо предлагать сотрудникам курс обновленного обучения по инфекционному контролю, а также новым сотрудникам до приема их на работу в диализном центре и это обязательно должно быть задокументировано. Такие курсы также важны для обновления и закрепления знаний уже работающего персонала, чтобы поддерживать высокий уровень инфекционного контроля.
Окружающие предметы
Между каждым сеансом диализа окружающие предметы и поверхности должны быть тщательно почищены, а также должны чиститься каждый раз при попадании крови и других биологических жидкостей.
Санитарный персонал должен периодически опорожнять контейнеры для отходов, когда они заполнены (не переполнены), и помещать в них соответствующие пластиковые пакеты (для биологически опасных или общих отходов).
Оборудование
Химическая дезинфекция системы обратного осмоса (ОО) и аппаратов диализа должна проводиться один раз в неделю с использованием гипохлорита натрия или его эквивалента.
Распределительный контур воды для диализа и аппараты диализа должны подвергаться термической дезинфекции ночью (когда диализ не проводится) и промыты перед началом каждого диализа (за 15 минут до назначенного времени начала диализа).
Забор проб диализата и воды, используемой для его приготовления, на посев и исследование на эндотоксины должен проводиться один раз в месяц (см. контроль качества системы водоочистки).
Должны соблюдаться следующие стандарты для диализата:
Вода, используемая для приготовления диализата, должна содержать микробное количество не более 100 КОЕ/мл и уровень эндотоксинов не должен превышать 0,25 ЕД/мл.
Диализаторы и кровопроводящие магистрали НЕ должны использоваться повторно.
Защитный фильтр - (обычно гидрофобный 0,2 микрон фильтр), расположенный между элементами слежения за давлением экстракорпоральной системы и системы диализной машины. Этот фильтр позволяет воздуху свободно проходить к элементу слежения за давлением системы диализной машины, но препятствует проникновению жидкости. Такая система одновременно предохраняет пациента от микробного загрязнения и машину - от загрязнения кровью. Внешний защитный фильтр расположен у элемента слежения за давлением в кровесодержащей системе. Внутренний фильтр расположен внутри машины. Его замена требует вызова специалиста технической поддержки производителя машины.
Дезинфекция внутреннего контура. Если используются диализные машины “нерециркулирующего” типа, дезинфекция внутреннего контура не требуется в случае, если не случилость попадания крови в контур. В случае, если кровь попала во внутренний контур, необходимо провести дезинфекцию контура и соединения Хэнсена (Hensen) перед лечением следущего пациента. Следует удостовериться, что персонал имеет достаточно времени для внешней дезинфеции машины между пациентами. “Рециркулирующий” тип машин должен быть дезинфицирован каждый раз после процедуры гемодиализа.
Наружная обработка. После каждого сеанса наружная поверхность диализной машины должна быть обработана слабым дезинфицирующим раствором, если нет видимых следов загрязнения. Если есть следы загрязнения кровью, требуется обработка раствором 500 ppi гипохлорита (1:100 разведение 5% отбеливателя). Конкретный дезинфицирующий раствор и его концентрация прилагаются производителем диализной машины. Если кровь или биологическая жидкость со следами крови проникла внутрь машины, аппарат не должен использоваться до тех пор, пока он не разобран и не продезинфицирован.
Кресло для диализа и столик над кроватью должны быть помыты и дезинфицированы раствором гипохлорита натрия, разведенным в пропорции 1:10.
Материалы для ухода за пациентом (например, диализные фильтры, кровопроводящие магистрали, фистульные иглы, шприцы) не должны храниться в диализном зале.
"Коробка для отходов", выделенная для каждого диализного места, должна использоваться для подготовки материалов для каждой процедуры диализа. Она должна быть обработана дезинфицирующим средством (например, 70% раствор спирта) после каждого использования.
Одноразовые предметы, принесенные на диализное место, должны быть использованы только на одного пациента, а неиспользованные лекарства или материалы (например, шприцы, марлевые тампоны, спиртовые салфетки), принесенные на диализное место, НЕ должны возвращаться в общую чистую зону или использоваться для других больных. Неиспользованные предметы должны быть либо утилизированы, либо отправлены на повторную стерилизацию.
Многоразовые предметы НЕ должны использоваться несколькими пациентами, так как любой предмет, взятый на диализное место, может быть загрязнен кровью или другими биологическими жидкостями и служить переносчиком инфекции для других больных напрямую или опосредованно через загрязнение рук медсестер.
Повторно используемое медицинское оборудование
Стетоскопы и термометры: почистить и обработать дезинфицирующим средством (например, 70% спиртом).
Манжеты для измерения артериального давления и жгуты: опрыскивать 70% спиртом и дать высохнуть. Если они загрязнены кровью, биологическими жидкостями и/или другими загрязнителями, удалить и вымыть моющим средством, затем выдержать в готовом растворе гипохлорита натрия 0,5% в течение не менее 10 минут и дать высохнуть.
Все флаконы для многоразового применения должны оставаться в отдельно выделенном месте для хранения медикаментов.
Остатки лекарств (в флаконе или шприце) никогда не должны смешиваться с лекарствами из другого флакона или шприца. Если пациенту требуется больше лекарства, чем есть в одном шприце, то лекарство из отдельного флакона должно быть взято в отдельный шприц для введения.
Все дозы из данного флакона должны быть взяты и введены в течение часового периода.
Для того, чтобы использовать диализный аппарат, который ранее использовался для пациента с положительным статусом HCV, для лечения "отрицательных" пациентов, необходимо выполнить следующие действия:
1. Тщательно и правильно почистить и дезинфицировать внешние поверхности аппарата, так как передача инфекционных агентов чаще происходит через загрязненные окружающие поверхности, а не через путь потока жидкости аппарата.
2. Дезинфицировать пути потока жидкости в аппарате. Производители гемодиализных аппаратов обычно указывают тип предпочтительного дезинфицирующего средства, которое следует использовать для их аппарата, и дезинфицирующие средства, которые не рекомендуется использовать
3. Если внутренняя трубопроводная система и порт давления загрязнены, их необходимо заменить.
Все пациенты должны пройти скрининг на HBV, HСV и ВИЧ в начале диализа, а также проходить регулярное наблюдение и контроль. Должны быть проведены следующие тесты: HBsAg, анти HCV (EIA III), RIBA III, ПЦР для обнаружения РНК HCV и ВИЧ.
Сдать анализ на анти-HBs через 1-2 месяца после последней дозы. Если анти-HBs отрицательный (<10 мМЕ/мл), рассматривать пациента как восприимчивого, повторно прививать дополнительными тремя дозами и повторно сдать анализ на анти-HBs.
Если анти-HBs положительный (≥10 мМЕ/мл), рассматривать пациента как иммунного и повторно сдавать анализ ежегодно.
В случае отрицательного результата анти-HBs дать бустерную дозу вакцины и продолжать повторно сдавать анализ ежегодно.
Пациенты, инфицированные HBV, должны строго изолироваться в отдельной комнате и лечиться с использованием отдельных диализных аппаратов, оборудования, инструментов и расходных материалов, используемых исключительно для HBV.
Пациенты, инфицированные гепатитом С, должны проводить диализ в общей зоне. Однако, если имеется высокий уровень сероконверсии, недостаточное следование правилам и процедурам и недостаток медицинского персонала, то больным диализ проводится в отдельной зоне/комнате с отдельными диализными аппаратами, оборудованием, инструментами и расходными материалами.
Пациент, который был принят на диализ до получения результатов вирусологических тестов, должен быть лечен, как если бы он был положительным на любой вирусологический анализ, за исключением того, что такие пациенты не должны лечиться в изолированной комнате. Аналогично, обычный пациент на диализе, который путешествовал и проходил несколько диализов за пределами центра и возвращается после долгого отсутствия, должен рассматриваться как новый пациент или пациент с неизвестным вирусологическим статусом.
Для пациентов на регулярном гемодиализе, которые часто путешествуют (например, каждую неделю или каждый месяц), следующие тесты должны проводиться регулярно каждый месяц: HBsAg, анти HCV (EIA III), RIBA III (независимо от результата EIA для анти-HCV) и ВИЧ.
Главная медсестра каждого отделения гемодиализа должна вести запись о поездках пациентов и их диализе вне центра, которая содержит информацию, такую как: имя пациента, дата отъезда и возвращения, район и название центра/отделения диализа, посещенного пациентом, вирусный статус до отъезда и по возвращении, любые хирургические и/или стоматологические процедуры и переливание крови. Планируемая дата повторной сдачи анализов (для преодоления периода окна) должна быть отслежена медсестрой, ответственной за инфекционный контроль.
Больным с положительными результатами RIBA III и первоначально отрицательными результатами RT-PCR должен быть проведен повторный анализ RT-PCR на HCV RNA. Если RIBA III остается положительным, а PCR отрицательным, это может означать предыдущий контакт с гепатитом С, который не обеспечивает иммунитета пациенту.
Гемодиализ пациента с неизвестным вирусологическим статусом:
Всегда придерживаться жестких рекомендаций по инфекционному контролю, рекомендуемых для гемодиализных отделений для всех пациентов (независимо от вирусологического статуса), например, не делиться принадлежностями с другими пациентами.
Пациент, который принимается на гемодиализ до тех пор, пока неизвестны результаты вирусологических тестов, должен проходить лечение, как если бы он был положительным на любой вирусологический тест, за исключением того, что таких пациентов не должны лечить в изолированной комнате.
- Назначить определенную медсестру для проведения гемодиализа у данного пациента, и не позволять ей обслуживать других пациентов в течение той же смены.
- Пациент должен получать гемодиализ предпочтительно в отдельной комнате с выделенным диализным аппаратом и другим оборудованием, предназначенным для использования у пациентов с неизвестным вирусологическим статусом. Если по какой-либо причине это невозможно, тогда следует использовать аппарат в дальнем углу отделения.
Уход за оборудованием, используемым для пациентов с неизвестным вирусным статусом:
● Тщательно почистить и дезинфицировать внешние поверхности аппарата для гемодиализа и всего другого используемого оборудования (процедурный столик, кресло для диализа, ящик для инструментов и т. д.) рекомендуемым дезинфицирующим раствором (70% изопропиловый спирт, раствор гипохлорита в разведении 1:100). Доказано, что передача инфекционных агентов наиболее вероятна с поверхностей окружающих предметов, чем по току жидкости в диализном аппарате.
● Дезинфицировать пути потока жидкости в диализном аппарате термическим и химическим методами дезинфекции. Все производители аппаратов для гемодиализа обычно указывают тип предпочтительного дезинфицирующего средства для использования на их аппаратах и дезинфицирующие средства, которые не рекомендуется использовать.
● Если подозревается, что внутренний набор трубок для подачи жидкости и порт давления в машине загрязнены, следует обратиться к биомедицинскому инженеру для проверки и замены при необходимости.
● Если это возможно, предпочтительнее оставить диализный аппарат (и всё другое используемое оборудование) в режиме ожидания и не использовать его для других больных, пока не будет известен вирусный статус пациента, или использовать после истечения 7-дневного периода, так как самое длительное время жизнеспособности вирусов, передающихся через кровь (HBV), на окружающих поверхностях составляет 7 дней.
ПРАВИЛА И ПРОЦЕДУРЫ ПРИ НАПРАВЛЕНИИ ПАЦИЕНТА НА ГЕМОДИАЛИЗ МЕЖДУ ДИАЛИЗНЫМИ ЦЕНТРАМИ
● Если пациент на диализе хочет путешествовать и/или посетить родственников в другом регионе, направляющий диализный центр должен организовать диализное место для своего пациента на период его пребывания, общаясь напрямую (по телефону/факсу/электронной почте) с принимающим диализным центром.
● Диализные отделения/центры ОБЯЗАНЫ предоставлять принимающему диализному центру отчёт о диализе (направление на диализ) с указанием последнего и датированного серологического статуса/результатов анализов (например, HBV, HCV и ВИЧ). Копия этого отчета также должна быть дана пациенту на руки.
● При возвращении пациента на диализ в его/её диализный центр, ему/ей необходимо предоставить отчет о диализе (направление на диализ) от посещаемого диализного центра, отображающий все хирургические или стоматологические процедуры и/или переливание крови, если такие были, в посещаемом диализном центре, вместе с его/ее серологическими тестами/результатами, если они были повторены.
● По возвращении, скрининг на наличие ВГВ, ВГС и ВИЧ должен быть проведен для всех новых пациентов перед поступлением в диализный центр. Тесты на гепатит С должны включать ПЦР.
● Для пациента, переведенного из другого центра, новые результаты тестов должны быть получены непосредственно перед переводом пациента.
● Если вирусологический статус пациента неизвестен на момент поступления, обследование должно быть проведено немедленно.
● Информация о впервые выявленном пациенте с положительными результатами вирусологических тестов должна быть подана в ДПЗиГСЭН.
● Пациенты на регулярном гемодиализе, которые путешествовали и получали несколько сеансов диализа за пределами центра и возвращаются обратно, должны рассматриваться как новые пациенты или пациенты с неизвестным вирусологическим статусом.
Приложение 1.
Чек-лист по регистрации симптомов и объективных данных у больных с ХБП С4-5.
| Анамнез, симптомы/признаки | ДА | НЕТ | Если «да», то как давно? |
| Изменения цвета мочи, изменения объема диуреза (олигурия, полиурия), никтурия | |||
| Длительность болезни более 3х мес. | |||
| Наличие отеков | |||
| Снижение массы тела | |||
| Артериальная гипертензия | |||
| Наличие зуда и сухости кожных покровов | |||
| Наличие аномалии развития почек, кисты, гидронефроз | |||
| Повышение креатинина, СКФ <30 мл/мин | |||
| Анемия | |||
| Уменьшение размера почек | |||
| Повышение уровня калия, фосфора | |||
| Повышение уровня паратгормона |
| Наличие «красных флагов | ДА | НЕТ |
|
Одышка
|
||
| Ортопноэ | ||
|
Рвота, отвращение к пище
|
||
| Наличие периферических отеков | ||
|
Гидроторакс, гидроперикард
|
||
| Тяжелая анемия | ||
|
Уремия
|
||
| Олигоурия или анурия | ||
|
Судороги
|
||
| Без сознания |
Приложение 2.
ПРАВИЛА УХОДА ЗА АРТЕРИО-ВЕНОЗНОЙ ФИСТУЛОЙ
|
№ п/п
|
Что нужно сделать | Как нужно выполнить | Почему нужно делать именно так |
| 1. |
Подготовиться к сеансу гемодиализа
Перед каждым сеансом
|
Теплой водой с мылом вымыть руку, на которую установлена фистула | Для исключения распространения инфекций |
| 2. | Проконтролировать кровотечение после гемодиализа | Визуально оценить кровотечение | Чтобы избежать излишней потери крови и не допустить кровотечение во время следующего диализа |
| Если кровотечение длится дольше 30 минут, необходимо немедленно обратиться к врачу | |||
| 3. |
Проверить функционирование фистулы
Ежедневно
|
Согласно правилу «Проверка состояния фистулы» | Для исключения нарушения циркуляции крови |
| 4. |
Сохранять область фистулы чистой
Ежедневно
|
Теплой водой с мылом вымыть руку, на которую установлена фистула | Для исключения распространения инфекций и заражения крови |
| Не наносить на руку косметические средства (крема, мази, парфюмерию и др.) | |||
| 5. | Обеспечить спокойствие для руки, на которую установлена фистула |
Не поднимать этой рукой тяжести
|
Чтобы избежать травмы фистулы |
|
Сильно не сгибать руку с фистулой
|
Чтобы не препятствовать свободному кровотоку | ||
| Не спать на этой руке | Чтобы избежать образования временных перегибов фистулы и снижения кровотока | ||
| Не носить одежду или украшения, сдавливающие руку | |||
| Не измерять артериальное давление на этой руке | Чтобы избежать сдавливания кровеносных сосудов из-за надувания манжеты | ||
| Исключить чрезмерное тепло | Чтобы избежать расширения сосудов и снижения кровяного давления и кровотока | ||
| Исключить чрезмерный холод | Чтобы избежать сужения сосудов, приводящего к уменьшению кровотока через конечности, в том числе и в руке с фистулой | ||
| 6. | Соблюдать диету | Согласно памятке «Диета для пациентов, находящихся на хроническом гемодиализе» | Для повышения результативности гемодиализа |
| 7. | Осуществить контроль показателей | Измерять артериальное давление | Резкие скачки артериального давления отрицательно влияют на функционирование фистулы |
| Контролировать междиализную прибавку | Для сохранения результативности гемодиализа | ||
| Примечание: Междиализная прибавка в весе не должна превышать 5% от «сухого веса» | |||
СЕМИДНЕВНОЕ МЕНЮ
| Понедельник | |
|
1-й Завтрак
|
Яйцо всмятку 2 шт. 96 г Салат из сборных овощей 170 г Кисель из варенья 180 г |
|
2-й Завтрак
|
Яблоко печеное 120г |
|
Обед
|
Борщ вегетарианский ½ порции, без соли 250 г Мясо отварное 90 г Свекла, тушеная в сметанном соусе 160 г Желе фруктовое лимонное 125 г |
|
Полдник
|
Отвар шиповника 100 |
|
Ужин
|
Зразы картофельные, фаршированные яйцом и луком, жареные на растительном масле без соли
Сметана 100 г
Чай 200 |
|
На ночь
|
Вишневый кисель 140 г |
|
На весь день
|
Сахар 40 г Сливочное масло 20 г Хлеб белый 150 г Мед или варенье 50 г |
| Содержание веществ в суточном наборе: | Белки 80г, жиры 114,7г, углеводы 410г, калорийность 2902 ккал, выход (нетто) 2200г |
| Вторник | |
| 1-й Завтрак |
Пудинг из обезжиренного творога, паровой 150 г Винегрет с растительным маслом 230 г Чай 200 г |
| 2-й Завтрак | Салат из сырой моркови тертой с сахаром 155г |
| Обед |
Суп перловый с овощами, ½ порции, без соли 250г Мясо отварное 90г Пюре картофельное с маслом, без соли200г Яблоки 200г |
| Полдник | Отвар шиповника 100г |
| Ужин |
Плов с фруктами б/с 180г Сметана 150г Вишневый кисель 100 |
| На ночь | Кисель 180г |
| На весь день |
Сахар 40 г
Сливочное масло 20 г
Хлеб белый 150 г
Мед или варенье 50 г
|
| Содержание веществ в суточном наборе: | Белки 81,8 г, жиры 113,3г, углеводы 473,9г, калорийность 3154 ккал, выход (нетто) 2325г |
| Среда | |
| 1-й Завтрак |
Язык говяжий 100г Салат из сборных овощей с р/м, б/с 170г Чай 200г |
| 2-й Завтрак | Яблоко печеное 100г |
| Обед |
Борщ со сметаной вегет. ½ порции 250г Бефстроганов из отварного мяса 55/100г Картофель отварной без соли 180г Вишневый кисель 140г |
| Полдник | Отвар шиповника 100г |
| Ужин |
Шницель капустный жареный 200г Лапшевник с творогом ½ порц. 110г Кисель из сухой черной смородины |
| На ночь | Яблоки 200г |
| На весь день |
Сахар 40 г
Сливочное масло 20 г
Хлеб белый 150 г
Мед или варенье 50 г
|
| Содержание веществ в суточном наборе: | Белки 86,3г, жиры 99,2г, углеводы 426г, калорийность 2854ккал, выход (нетто) 2600г |
| Четверг | |
| 1-й Завтрак |
Белковый омлет паровой 110г Винегрет с р/м, б/с 230г Чай 200г |
| 2-й Завтрак | Сок сливовый 200г |
| Обед |
Суп вегетарианский из сборных овощей ½ порц., без соли 250г Рагу из отварного мяса без соли 55/260г Вишневый кисель 140г |
| Полдник | Отвар шиповника 100г |
| Ужин |
Кабачки тушеные в сметане без соли 200 Сыр голландский 30г Сметана 150г |
| На ночь | Фрукты 200г |
| На весь день |
Сахар 40 г
Сливочное масло 20 г
Хлеб белый 150 г
Мед или варенье 50 г
|
| Содержание веществ в суточном наборе: | Белки 79,3г, жиры 123,2г, углеводы 400,7г, калорийность 2940 ккал, выход (нетто) 2600г |
| Пятница | |
| 1-й Завтрак |
Яйцо всмятку 2шт. 96г Салат из свежей капусты и яблок со сметаной 200г Чай 200г |
| 2-й Завтрак | Яблоки 100г |
| Обед |
Суп-лапша ½ порц. без соли 250г Куры отварные 75г Картофель отварной 150г Вишневый кисель 140г |
| Полдник | Отвар шиповника 100г |
| Ужин |
Котлеты картофельные запечные 259г Сметана 100г Кисель 180г |
| На ночь | Фрукты 200г |
| На весь день |
Сахар 40 г
Сливочное масло 20 г
Хлеб белый 150 г
Мед или варенье 50 г
|
| Содержание веществ в суточном наборе: | Белки 81,5г, жиры 100,3г, углеводы 465,1г, калорийность 3001ккал, выход (нетто) 2400г |
| Суббота | |
| 1-й Завтрак |
Пудинг из обезжиренного творога паровой 150г Салат из яблок, чернослива и апельсин150г Чай 200г |
| 2-й Завтрак | Сок сливовый 200г |
| Обед |
Борщ вегет. ½ порц. без соли 250г Рагу из отварного мяса без соли 55/260г Кисель вишневый 100 |
| Полдник | Отвар шиповника 100г |
| Ужин |
Плов с фруктами 180г Яйцо всмятку 1шт. 48г Кисель 140г |
| На ночь | Фрукты 200г |
| На весь день |
Сахар 40 г
Сливочное масло 20 г
Хлеб белый 150 г
Мед или варенье 50 г
|
| Содержание веществ в суточном наборе: | Белки 84г, жиры 73,1г, углеводы 419,3г, калорийность 2583ккал, выход 2500 (нетто) 2500г |
| Воскресенье | |
| 1-й Завтрак |
Сыр голландский 60г Салат из сборных овощей на растительном масле без соли 200г Чай 200г |
| 2-й Завтрак | Яблоко печеное 100г |
| Обед |
Щи свежие вегетарианские на растительном масле без соли 250г Плов из отварного мяса 55/180г Вишневый кисель 140г |
| Полдник | Отвар шиповника 100г |
| Ужин |
Пирог с яблоками 150г Голубцы фаршированные овощами с р/м б/c 220/50г Кисель 180г |
| На ночь | Фрукты 240г |
| На весь день |
Сахар 40 г
Сливочное масло 20 г
Хлеб белый 150 г
Мед или варенье 50 г
|
| Содержание веществ в суточном наборе: | Белки 77,5 жиры 106,4, углеводы 375,8г, калорийность 2682 ккал, выход (нетто) 2400г |
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.