Трансплантация гемопоэтических стволовых клеток пациентам с первичными (врожденными) иммунодефицитами (детское население)
 Версия: Клинические протоколы 2025 (Беларусь)
Версия: Клинические протоколы 2025 (Беларусь)
Агранулоцитоз (D70), Дефицит аденозиндезаминазы (D81.3), Дефицит молекул класса I главного комплекса гистосовместимости (D81.6), Дефицит молекул класса II главного комплекса гистосовместимости (D81.7), Другие комбинированные иммунодефициты (D81.8), Другие уточненные апластические анемии (D61.8), Другие уточненные иммунодефицитные нарушения (D84.8), Другие уточненные нарушения с вовлечением иммунного механизма, не классифицированные в других рубриках (D89.8), Другие уточненные синдромы врожденных аномалий, не классифицированные в других рубриках (Q87.8), Иммунодефицит, связанный с другими уточненными значительными дефектами (D82.8), Отдельные болезни, протекающие с вовлечением лимфоретикулярной ткани и ретикулогистиоцитарной системы (D76), Синдром Вискотта-Олдрича (D82.0), Тяжелый комбинированный иммунодефицит с низким или нормальным содержанием В-клеток (D81.2), Тяжелый комбинированный иммунодефицит с низким содержанием Т- и В-клеток (D81.1), Тяжелый комбинированный иммунодефицит с ретикулярным дисгенезом (D81.0)
Гематология детская, Педиатрия, Трансплантология детская
Общая информация
Краткое описание
УТВЕРЖДЕНО
Постановление
Министерства здравоохранения Республики Беларусь
16.10.2025 № 151
КЛИНИЧЕСКИЙ ПРОТОКОЛ
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
ГЛАВА 1
ОБЩИЕ ПОЛОЖЕНИЯ
1. Настоящий клинический протокол устанавливает общие требования к объему оказания медицинской помощи при трансплантации гемопоэтических стволовых клеток (далее – ТГСК) пациентам (детское население) с первичными (врожденными) иммунодефицитами (далее – ПИД).
3. Для целей настоящего клинического протокола используются основные термины и их определения в значениях, установленных Законом Республики Беларусь «О здравоохранении», Законом Республики Беларусь от 30 ноября 2010 г. № 197-З «О донорстве крови и ее компонентов», а также следующие термины и их определения:
4. Оказание высокотехнологичной медицинской помощи осуществляется в государственном учреждении «Республиканский научно-практический центр детской онкологии, гематологии и иммунологии».
5. В зависимости от источника получения ГСК выделяют следующие виды алло-ТГСК:
6. Определение трансплантационных групп:
2. Требования настоящего клинического протокола являются обязательными для государственных организаций здравоохранения.
3. Для целей настоящего клинического протокола используются основные термины и их определения в значениях, установленных Законом Республики Беларусь «О здравоохранении», Законом Республики Беларусь от 30 ноября 2010 г. № 197-З «О донорстве крови и ее компонентов», а также следующие термины и их определения:
- ПИД – гетерогенная группа генетически детерминированных заболеваний иммунной системы, характеризующихся ее дисфункцией и, как следствие, хроническими или рецидивирующими инфекциями, аутоиммунными, аллергическими, неопластическими заболеваниями;
- режим кондиционирования – протокол полихимиотерапии, проводимый непосредственно накануне ТГСК и предусматривающий назначение миелоаблативных или немиелоаблативных доз цитостатических лекарственных препаратов (далее – ЛП) с целью достижения иммуносупрессии и частичной или полной эрадикации кроветворения реципиента перед введением ему гемопоэтических стволовых клеток (далее – ГСК) костного мозга (далее – КМ) или периферических стволовых клеток крови (далее – ПСКК), а также клеток пуповинной крови (далее – ПК). От качества иммуносупрессии реципиента зависят приживление трансплантата или вероятность его отторжения после аллогенной ТГСК (далее – алло-ТГСК);
- ТГСК – трансфузия взвеси ГСК с целью предотвращения фатальной депрессии кроветворения, протезирования (замещения) иммунной системы реципиента. Технология ТГСК заключается в проведении предтрансплантационной иммуносупрессивной полихимиотерапии, а также комплекса сопроводительной терапии, которая сделала бы безопасной течение перитрансплантационного и посттрансплантационного периода;
- HLA – человеческий лейкоцитарный антиген (система тканевой совместимости человека);
- HLA-типирование – определение HLA-антигенов с целью выявления совместимой пары «донор-реципиент». Антигены HLA-системы I класса кодируются 17 генами, которые подразделяются на локусы А, В и С. В состав антигенов HLA-системы II класса входит D-регион, специфичность которого определяют 15 генов, в свою очередь разделенные на субрегионы DR, DQ, DP, DN и DO. Наиболее важным из них при алло-ГСК является субрегион DR. Идентичность донора с реципиентом по HLA-системе I и II классов свидетельствует о наличии полностью совместимого донора. Несовпадение по 1, 2 и 3 антигенам HLA-системы указывает на частичную совместимость.
4. Оказание высокотехнологичной медицинской помощи осуществляется в государственном учреждении «Республиканский научно-практический центр детской онкологии, гематологии и иммунологии».
5. В зависимости от источника получения ГСК выделяют следующие виды алло-ТГСК:
- трансплантация КМ, при которой источником ГСК является КМ;
- трансплантация стволовых клеток периферической крови, при которой источником ГСК являются ПСКК;
- трансплантация ПК, при которой источником ГСК является ПК.
6. Определение трансплантационных групп:
- совместимый родственный донор: геноидентичные (от HLA-идентичных сиблингов), HLA-генотипически идентичный донор или «12 из 12» совпадений при HLA-типировании высокой степени разрешения (4 знака на аллель), если родительские гаплотипы неизвестны;
- совместимый неродственный донор: феноидентичный «12 из 12» или «11 из 12» совпадений при HLA-типировании высокой степени разрешения (4 знака на аллель), «6 из 6» или «5 из 6» совместимых неродственных доноров ПК;
- несовместимый родственный донор: неполностью (частично) совместимый родственный донор «10 из 12» совпадений при HLA-типировании высокой степени разрешения (4 знака на аллель);
7. Фармакотерапия при ТГСК пациентам с ПИД назначается в соответствии с настоящим клиническим протоколом с учетом всех индивидуальных особенностей пациента, индивидуальных медицинских противопоказаний, аллергологического и фармакологического анамнеза, тяжести заболевания, наличия сопутствующей патологии и клинико-фармакологической характеристики ЛП.
- несовместимый неродственный донор: неполностью (частично) совместимый неродственный донор «10 из 12» совпадений при типировании высокой степени разрешения (4 знака на аллель), менее чем «5 из 6» совместимости донора ПК;
- гаплоидентичный родственный донор: неполностью (частично) совместимый родственный донор «6 и более из 12» совпадений при HLA-типировании высокой степени разрешения (4 знака на аллель).
7. Фармакотерапия при ТГСК пациентам с ПИД назначается в соответствии с настоящим клиническим протоколом с учетом всех индивидуальных особенностей пациента, индивидуальных медицинских противопоказаний, аллергологического и фармакологического анамнеза, тяжести заболевания, наличия сопутствующей патологии и клинико-фармакологической характеристики ЛП.
Применение ЛП осуществляется по медицинским показаниям и в режиме дозирования в соответствии с общей характеристикой ЛП и инструкцией по медицинскому применению (листком-вкладышем). Допускается включение в схему лечения ЛП по медицинским показаниям, не предусмотренным в инструкции по медицинскому применению (листке-вкладыше), дополнительно указываются особые условия назначения, способ применения, доза, длительность и кратность приема.
Назначение ЛП, изделий медицинского назначения, не входящих в клинические протоколы, допускается при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача-специалиста или лица, его заменяющего, с оформлением записи в медицинских документах.
ЛП, назначаемые по решению врачебного консилиума (в том числе off-lable) для лечения пациентов с ПИД, установлены согласно приложению 1.
Лечение
ГЛАВА 2
МЕДИЦИНСКИЕ ПОКАЗАНИЯ И МЕДИЦИНСКИЕ ПРОТИВОПОКАЗАНИЯ К ПРОВЕДЕНИЮ ТГСК
8. Абсолютными медицинскими показаниями к ТГСК являются следующие заболевания:
D 76 Другие уточненные заболевания с вовлечением лимфоретикулярной ткани и ретикулогистиоцитарной системы (семейные гемофагоцитарные лимфогистиоцитозы; семейные гемофагоцитарные лимфогистиоцитозы с гипопигментацией: синдром Чедиака–Хигаси, синдром Грисцелли тип 2, синдром Германского–Пудлака типы 2, 10);
D 81.0 Тяжелый комбинированный иммунодефицит с ретикулярным дисгенезом;
D 81.1 Тяжелый комбинированный иммунодефицит с низким содержанием T- и B-клеток;
D 81.2 Тяжелый комбинированный иммунодефицит с низким или нормальным содержанием B-клеток;
D 81.3 Дефицит аденозиндезаминазы (ADA);
D 81.6 Дефицит молекул класса I главного комплекса гистосовместимости;
D 81.7 Дефицит молекул класса II главного комплекса гистосовместимости;
D 84.8 Другие уточненные иммунодефицитные нарушения (дефициты адгезии лейкоцитов I и II типов);
D 82.8 Иммунодефицит, связанный с другими уточненными значительными дефектами (X-сцепленный лимфопролиферативный синдром I и II типов);
D 82.8 Иммунодефицит, связанный с другими уточненными значительными дефектами (Т-клеточная панникулитоподобная подкожная лимфома, ассоциированная с мутацией HAVCR2).
9. Относительными медицинскими показаниями к ТГСК при наличии HLA-совместимого донора являются:
D 89.8 Другие уточненные нарушения с вовлечением иммунного механизма (хроническая гранулематозная болезнь);
10. Решение о наличии/отсутствии медицинских показаний к проведению ТГСК принимается врачебным консилиумом с учетом тяжести течения заболевания, рисков неблагоприятных клинических исходов, текущего и ожидаемого в будущем поражения органа, психологических и социальных факторов.
11. Решение о проведении ТГСК при других редких иммунодефицитах (например, Q 78.2 Остеопетроз, D 80.5 Иммунодефицит с повышенным содержанием иммуноглобулина M [IgM] (гипер-IgM-синдромы); D 82.4 Синдром гипериммуноглобулина E [IgE] (при наличии мутации DOCK8) принимается врачебным консилиумом.
12.1. абсолютными медицинскими противопоказаниями к ТГСК являются:
12.2. относительными медицинскими противопоказаниями к ТГСК являются:
D 70 Агранулоцитоз (тяжелая врожденная нейтропения – ELANE (аутосомно-доминантная); болезнь Костмана–HAX1 (аутосомно-рецессивная); Х-сцепленная нейтропения/миелодисплазия–WAS GOF, синдром Кохен; дефекты рецептора G-CSF; другие врожденные синдромы, ассоциированные с нейтропенией;
D 81.8 Другие комбинированные иммунодефициты;
D 82.0 Синдром Вискотта–Олдрича;
D 82.8 Иммунодефицит, связанный с другими уточненными значительными дефектами (Х-сцепленный синдром иммунодисрегуляции; полиэндокринопатии и энтеропатии (IPEX-синдром);
Q 87.8 Другие уточненные синдромы врожденных аномалий, не классифицированные в других рубриках (синдром Ниймегена; синдром Блума, ICF1, 2, 3, 4);
D 84.8 Другие уточненные иммунодефицитные нарушения (дефицит CD40L, дефицит CTLA4, дефицит LRBA, другие дефекты регуляторных Т-лимфоцитов и иные);
D 61.8 Другие уточненные апластические анемии (анемия Фанкони; синдром атаксии-панцитопении, ассоциированный с SAMD9L; другие моногенные синдромы недостаточности костного мозга).
10. Решение о наличии/отсутствии медицинских показаний к проведению ТГСК принимается врачебным консилиумом с учетом тяжести течения заболевания, рисков неблагоприятных клинических исходов, текущего и ожидаемого в будущем поражения органа, психологических и социальных факторов.
11. Решение о проведении ТГСК при других редких иммунодефицитах (например, Q 78.2 Остеопетроз, D 80.5 Иммунодефицит с повышенным содержанием иммуноглобулина M [IgM] (гипер-IgM-синдромы); D 82.4 Синдром гипериммуноглобулина E [IgE] (при наличии мутации DOCK8) принимается врачебным консилиумом.
12. Медицинскими противопоказаниями к ТГСК являются:
12.1. абсолютными медицинскими противопоказаниями к ТГСК являются:
- индекс Карновского/Ланского менее 70 (60) %;
- шкала оценки соматического состояния пациента, индекс Карновского представлены в приложении 2;
- шкала оценки соматического состояния пациента, индекс Ланского (для детей до 18 лет) представлены в приложении 3;
- неуправляемые тяжелые инфекции (бактериальные, вирусные, грибковые) с дисфункцией органов на фоне адекватной терапии;
- активный гепатит;
- активная цитомегаловирусная (далее – ЦМВ) инфекция;
- тяжелые хронические заболевания или их сочетание (хроническая сердечная недостаточность, тяжелые повреждения легких и иные), при которых проведение ТГСК не приведет к увеличению продолжительности и качества жизни, но может ускорить развитие неблагоприятного исхода;
- тяжелые психические заболевания, глубокая задержка психического развития, необратимое повреждение головного мозга с потерей интеллекта;
- отсутствие окончательного диагноза;
12.2. относительными медицинскими противопоказаниями к ТГСК являются:
- отсутствие стабилизации состояния и основных клинико-лабораторных показателей патологического процесса по основному заболеванию (состоянию);
- аутоиммунные заболевания: воспалительные заболевания кишечника, системная красная волчанка, васкулиты и иные при сохранении высокой степени их активности и другие аутоиммунные процессы;
- хронические неинфекционные заболевания (сердечная недостаточность, аутоиммунные гепатиты и иные) в стадии субкомпенсации;
- хронические инфекционные заболевания не в стадии ремиссии: туберкулез, заболевание, вызванное вирусом иммунодефицита человека (далее – ВИЧ), вирусный гепатит С;
- социальные противопоказания: отсутствие у пациента мотивации к ТГСК, а также отказ от приема ЛП и выполнения других врачебных назначений.
13.1. эксфузия КМ выполняется под общей или перидуральной анестезией в условиях операционной. Положение пациента – лежа на животе. КМ аспирируется иглами большого диаметра путем множественных пункций задних остей тазовых кости с обеих сторон в шприцы, содержащие антикоагулянт (гепарин и электролитная среда в соотношении 100 ЕД/мл), и переносится в коллекционный мешок. Объем аспирируемой костномозговой взвеси определяется в зависимости от количества в ней ядросодержащих клеток (далее – ЯСК), массы тела пациента и необходимости дополнительных манипуляций с полученным трансплантатом (удаление плазмы и (или) эритроцитов), но в тоже время объем не должен превышать 10–15 мл на 1 кг массы тела донора. Общая клеточность в трансплантате КМ должна составлять не менее 2 х 108 на 1 кг массы тела реципиента. Контрольный подсчет ЯСК в коллекционном мешке проводится в процессе забора трансплантата для определения достаточности собранного;
13.2. обработка КМ после эксфузии включает фильтрацию материала для удаления мелких костных обломков, сгустков крови и частично жира, для чего применяется фильтр для костного мозга или лейкоцитарная система;
13.3. в случаях несовместимости по системе АВ0 между донором и реципиентом аллогенный КМ после фильтрации подвергается седиментации с применением 6% раствора гидроксиэтилкрахмала для удаления эритроцитов и плазмоэкстракции для удаления плазмы, содержащей антитела;
13.4. концентрация клеток аллогенного КМ выполняется, используя центрифугирование при 2000 оборотов в минуту в течение 10 минут, с последующим удалением плазмы с помощью плазмоэкстрактора;
13.5. оценка качества трансплантата КМ включает подсчет ЯСК методом микроскопии с помощью камеры Горяева или на анализаторе крови, определение количества CD34+, CD3+, CD19+, CD16+56+ клеток методом проточной цитофлуориметрии с использованием моноклональных антител; определение жизнеспособности клеток; посев на стерильность.
14. При получении гемопоэтических стволовых клеток из ПСКК осуществляются следующие этапы:
14.1. для мобилизации ПСКК у доноров применяется рекомбинантный гранулоцитарный колониестимулирующий фактор, назначаемый в дозе 10 мкг/кг/сут. в течение 4–5–6 дней подкожно (допускается внутривенное использование).
ГЛАВА 3
ПОЛУЧЕНИЕ И ОБРАБОТКА ТРАНСПЛАНТАТА ГСК
13. При получении ГСК из КМ осуществляются следующие этапы:
13.1. эксфузия КМ выполняется под общей или перидуральной анестезией в условиях операционной. Положение пациента – лежа на животе. КМ аспирируется иглами большого диаметра путем множественных пункций задних остей тазовых кости с обеих сторон в шприцы, содержащие антикоагулянт (гепарин и электролитная среда в соотношении 100 ЕД/мл), и переносится в коллекционный мешок. Объем аспирируемой костномозговой взвеси определяется в зависимости от количества в ней ядросодержащих клеток (далее – ЯСК), массы тела пациента и необходимости дополнительных манипуляций с полученным трансплантатом (удаление плазмы и (или) эритроцитов), но в тоже время объем не должен превышать 10–15 мл на 1 кг массы тела донора. Общая клеточность в трансплантате КМ должна составлять не менее 2 х 108 на 1 кг массы тела реципиента. Контрольный подсчет ЯСК в коллекционном мешке проводится в процессе забора трансплантата для определения достаточности собранного;
13.2. обработка КМ после эксфузии включает фильтрацию материала для удаления мелких костных обломков, сгустков крови и частично жира, для чего применяется фильтр для костного мозга или лейкоцитарная система;
13.3. в случаях несовместимости по системе АВ0 между донором и реципиентом аллогенный КМ после фильтрации подвергается седиментации с применением 6% раствора гидроксиэтилкрахмала для удаления эритроцитов и плазмоэкстракции для удаления плазмы, содержащей антитела;
13.4. концентрация клеток аллогенного КМ выполняется, используя центрифугирование при 2000 оборотов в минуту в течение 10 минут, с последующим удалением плазмы с помощью плазмоэкстрактора;
13.5. оценка качества трансплантата КМ включает подсчет ЯСК методом микроскопии с помощью камеры Горяева или на анализаторе крови, определение количества CD34+, CD3+, CD19+, CD16+56+ клеток методом проточной цитофлуориметрии с использованием моноклональных антител; определение жизнеспособности клеток; посев на стерильность.
14. При получении гемопоэтических стволовых клеток из ПСКК осуществляются следующие этапы:
14.1. для мобилизации ПСКК у доноров применяется рекомбинантный гранулоцитарный колониестимулирующий фактор, назначаемый в дозе 10 мкг/кг/сут. в течение 4–5–6 дней подкожно (допускается внутривенное использование).
Аферез ПСКК проводится обычно на 4, 5 и (или) 6 дни стимуляции. В это время наблюдается значительное повышение количества лейкоцитов периферической крови (в 4–10 раз), сопровождающееся увеличением уровня клеток-предшественников различных линий гемопоэза (CD34+ клетки). Критерием адекватности дозы ПСКК для аллогенной ТГСК является количество CD34+ клеток – более 4 х 106/кг массы тела реципиента.
Аферез ПСКК выполняется на сепараторе клеток крови. В качестве антикоагулянта используется цитратный раствор в декстрозе, формула-А.
Для обеспечения адекватного венозного доступа при проведении лейкафереза проводится катетеризация периферических, а при их отсутствии – центральных (подключичной, яремной или бедренной) вен.
15. При получении ГСК из ПК осуществляются следующие этапы:
15.1. забор ПК производится только в случае целостности пуповины и отсутствия видимых повреждений в течение первых 30 секунд после наложения зажима и перерезания пуповины, но не позднее 15 минут после рождения ребенка. Критерием адекватности образца ПК для аллогенной ТГСК является количество ЯСК не менее 3,5 х 107/кг массы тела реципиента, CD34+ клеток более 1,7 х 105/кг массы тела реципиента;
15.2. приготовление концентрата стволовых клеток ПК осуществляется ручным или автоматизированным методом:
15.3. криозамораживание концентрата стволовых клеток ПК проводят на программируемом замораживателе с добавлением раствора криопротектора на основе диметилсульфоксида до достижения 10% концентрации диметилсульфоксида в конечном продукте. Хранение образцов ПК осуществляется в специальных контейнерах при сверхнизкой температуре – 196 °С;
15.4. для оценки качества ПК проводят: подсчет ЯСК методом микроскопии с помощью камеры Горяева или анализатора крови; определение количества CD34+ клеток методом проточной цитофлуориметрии с использованием моноклональных антител; оценку жизнеспособности клеток; посев на стерильность.
23. Выбор комбинации цитостатических ЛП перед ТГСК зависит от нозологической формы (вида иммунодефицита) и соматического статуса пациента.
24. Наиболее распространенными режимами кондиционирования при проведении алло-ТГСК являются:
25. У пациентов с тяжелой комбинированной иммунной недостаточностью допускается отсутствие кондиционирования. В таком случае проводится медицинская профилактика реакции «трансплантат против хозяина» (далее – РТПХ) с использованием антитимоцитарного глобулина (далее – АТГ).
26. В целях медицинской профилактики острой РТПХ применяется комбинация иммуносупрессивных ЛП. Состав комбинаций ЛП определяется нозологической формой заболевания, клиническими проявлениями и коморбидным статусом пациента и включает следующие ЛП:
метотрексат (раствор для инъекций 10 мг/мл 5 мл, порошок лиофилизированный для приготовления раствора для инъекций 10 мг, 50 мг) – внутривенно струйно в дозе 10 мг/м2 на введение, дни +1, +3, +6;
такролимус (концентрат для приготовления раствора для внутривенного введения 5 мг/мл) – внутривенно постоянной инфузией в суточной дозе 0,02 мг/кг со дня –1 (при гапло ТГСК – со дня +5). Затем перорально в суточной дозе 0,02–0,03 мг/кг в день (не более 2 мг) (капсулы 0,5 мг, 1 мг, капсулы пролонгированного действия 0,5 мг, 1 мг); при этом целевая концентрация ЛП в крови должна быть 5–15 нг/мл;
микофенолата мофетил (микофеноловая кислота) (далее – ММФ) (капсулы 250 мг, таблетки, покрытые оболочкой, 500 мг, таблетки, покрытые кишечнорастворимой оболочкой, 180 мг, 360 мг) – перорально в дозе 30–45 мг/кг/сут., разделенной на два приема с +1 дня (при гапло-ТГСК – с дня +5);
АТГ (концентрат для приготовления раствора для инфузий 20 мг/мл 5 мл, лиофилизированный порошок для приготовления раствора для инфузий 25 мг) внутривенно три (четыре) последовательных дня в дозе от 2,5 мг/кг/сут. до 20 мг/кг/сут. в зависимости от нозологии, типа донора, источника ГСК, производителя (бренда) АТГ;
циклофосфамид (порошок для приготовления раствора для внутривенного введения (для инъекций) 200 мг) – внутривенно 1-часовой инфузией в дозе 10–50 мг/кг в дни +3 и +4 (в том числе при гапло-ТГСК);
сиролимус (таблетки 1 мг) – стартовая доза 6 мг в сутки однократно, далее по 2 мг 1 раз в сутки. У детей массой менее 40 кг стартовая доза 3–5 мг/м2, далее 1–2 мг/м2. Коррекция дозы осуществляется индивидуально под контролем концентрации ЛП в сыворотке крови. Целевая концентрация от 4 до 12 нг/мл. Назначают с дня –3 с постепенной отменой при отсутствии РТПХ;
руксолитиниб (таблетки 5 мг, 10 мг, 15 мг) в суточной дозе 4–7,5 мг/м2 (распределение в 2 приема) под контролем гематологических показателей с возможным дальнейшим увеличением дозы;
бортезомиб (лиофилизированный порошок для приготовления раствора для внутривенного введения и подкожного введения 2 мг, 3,5 мг) дозирование 1–1,5 мг/м2 внутривенно в дни +1, +4, +7;
тоцилизумаб (концентрат для приготовления раствора для инфузий 20 мг/мл 4 мл, 10 мл, 20 мл) 8 мг/кг внутривенно каждые 3–4 недели;
ведолизумаб 300 мг (порошок для приготовления концентрата для приготовления раствора для инфузий 300 мг) (100 мг для детей с массой < 10 кг, 150 мг для детей с массой 10–25 кг) на –1, +13 и далее каждые 28 дней, всего до 7 введений.
27. В целях медицинской профилактики судорожного синдрома при приеме высоких доз бусульфана назначается клоназепам (таблетки 0,5 мг, 2 мг) для пациентов младше 6 лет* и пациентов старше 6 лет в дозе 0,01–0,03 мг/кг/сут. с –7 до +1 дня. Клоназепам начинают применять за сутки до назначения бусульфана в дозе 0,125–0,5 мг утром и вечером.
28. В целях медицинской профилактики геморрагического цистита назначается месна (раствор для внутривенного введения 100 мг/мл 4 мл) внутривенно капельно.
29. Гастропротекция включает прием ингибиторов протонной помпы (омепразол, эзомепразол) внутривенно в профилактических дозах с –7 дня до восстановления показателей гемопоэза.
30. Медицинская профилактика вено-окклюзионной болезни проводится гепарином (раствор для внутривенного и подкожного введения (для инъекций) 5 000 МЕ/мл) в дозе 100 ЕД/кг/сут. (5 ЕД/кг/час), внутривенно в виде непрерывной внутривенной инфузии с –1 дня до +30 дня под контролем показателей коагулограммы.
31. Медицинская профилактика цитолитической гиперурикемии включает прием аллопуринола (таблетки 100 мг, 150 мг, 200 мг, 300 мг) в дозе 10 мг/кг/сут. в 2 приема в таблетках с первого дня кондиционирования до дня 0 включительно.
32. Медицинская профилактика рвоты включает прием одного из следующих ЛП (off-lable):
гранисетрон (концентрат для приготовления раствора для инфузий 1 мг/мл 3 мл, раствор для инъекций 1 мг/мл 3 мл) для детей младше 2 лет*, для детей старше 2 лет 1–3 мг в сутки;
трописетрон (раствор для внутривенного введения (для инъекций) 1 мг/мл 5 мл) для детей младше 2 лет*, для детей старше 2 лет – 0,2 мг/кг. Максимальная суточная доза 5 мг;
метоклопрамид (раствор для внутривенного и внутримышечного введения (для инъекций) 5 мг/мл 2 мл) для детей младше 1 года*, для детей старше 1 года – 0,1–0,15 мг/кг. Начинается за 30 минут до первого введения химиопрепарата. При необходимости продолжается 24–48 часов после последнего введения химиопрепаратов.
При недостаточной эффективности противорвотных ЛП их действие может быть усилено введением глюкокортикоидов внутривенно (дексаметазон – 0,1 мг/кг).
33. Медицинская профилактика витаминной недостаточности включает применение поливитаминных ЛП для внутривенного введения: кальция фолинат (порошок лиофилизированный для приготовления раствора для внутривенного и внутримышечного введения (для инъекций) 50 мг 10 мл, раствор для внутривенного и внутримышечного введения 10 мг/мл 3 мл, 5 мл, 10 мл) – 10 мг/м2 внутривенно 1 раз в неделю.
34. Гидратация осуществляется путем внутривенного капельного введения солевых и декстрозных растворов:
Контроль гидратации: измерение веса каждые 12 часов, баланса объема мочеиспускания и поступившей в организм пациента жидкости (инфузии, питье).
35. Заместительная терапия внутривенным иммуноглобулином осуществляется путем введения иммуноглобулина для внутривенного введения капельно 0,2 г/кг со дня – 10 – 1 раз в неделю до дня +100, далее при снижении уровня IgG в сыворотке крови ниже 5 г/л – внутривенно капельно 0,2–0,4 мг/кг 1 раз в 4 недели.
36. В целях стимуляции гемопоэза назначается один из следующих ЛП:
ленограстим (лиофилизат для приготовления раствора для внутривенного и подкожного введения 33,6 млн. МЕ) 5–10 мг/кг подкожно либо внутривенной инфузией 1 раз в день, до восстановления показателей гранулопоэза;
эритропоэтин (раствор для внутривенного и подкожного введения (для инъекций) 2 000 МЕ/мл 1 мл, Раствор для инъекций 4 000 МЕ/мл 1 мл, раствор для инъекций 10 000 МЕ/мл 1 мл, раствор для внутривенного и подкожного введения 40 000 МЕ/1 мл) 100 МЕ/кг внутривенной инфузией 3 раза в неделю до восстановления показателей эритропоэза;
агонисты тромбопоэтиновых рецепторов – ромиплостим (лиофилизированный порошок для приготовления раствора для подкожного введения 250 мкг) 1 мкг/кг подкожно или внутривенной инфузией 1 раз в неделю, до восстановления показателей тромбоцитопоэза.
37.1. организационные мероприятия:
37.2. медицинскую профилактику бактериальной инфекции (по медицинским показаниям) в индивидуальном порядке;
37.3. медицинскую профилактику протозойных инфекций – назначается сульфаметоксазол/триметоприм (ко-тримоксазол) раствор для инфузий (80 мг +16 мг)/мл 5 мл, суспензия для приема внутрь – 5 мг/кг/сут. по триметоприму каждые 12 часов, таблетки 400 мг + 80 мг для детей до 2 лет*, с 2 лет – 5 мг/кг/сут. по триметоприму каждые 12 часов 3 раза в неделю с момента приживления трансплантата (восстановления лейкоцитов) до 6 месяцев после отмены иммуносупрессивной терапии и восстановления иммунной системы;
ганцикловир (порошок лиофилизированный для приготовления раствора для инфузий 500 мг) (получают только ЦМВ-серопозитивные реципиенты) 5 мг/кг/сут. за 1 введение внутривенно со дня +1.
валганцикловир (таблетки, покрытые оболочкой, 450 мг) в позднем посттрансплантационном периоде 16 мг/кг 2 раза в сутки.
У детей до 16 лет доза валганцикловира (мг) = 7 х площадь тела в м2 х клиренс по эндогенному креатинину или 16 мг/кг 2 раза в сутки, но не более 900 мг в сутки, старше 16 лет – 900 мг 2 раза в сутки (за исключением пациентов с тяжелой желудочно-кишечной РТПХ).
Пациентам из группы высокого риска развития EBV-ассоциированного посттрансплантационного лимфопролиферативного заболевания назначается ритуксимаб (концентрат для приготовления раствора для инфузий 10 мг/мл 10 мл, 30 мл, 50 мл) 200–375 мг/м2 внутривенно не менее 1 введения до ТГСК или в день 0;
37.5. медицинскую профилактику грибковой инфекции, при которой осуществляется изоляция пациента в боксе, оборудованном HEPA (High Efficiency Particulate Air) фильтрами – воздушными фильтрами высокой эффективности для очистки воздуха и назначается один из ЛП, применяемых для медицинской профилактики грибковой инфекции, согласно приложению 7;
37.6. медицинскую профилактику катетер-ассоциированных инфекций, которая включает:
37.7. медицинскую профилактику мукозита, которая осуществляется путем полоскания полости рта растворами хлоргексидина, фурациллина со дня госпитализации, раствором повидон-йода 2 г/1000 мл.
38. Подготовка к медицинскому применению крови, ее компонентов:
38.1. с целью снижения иммуногенности, а также с целью медицинской профилактики РТПХ все компоненты крови, переливаемые реципиентам ГСК, подвергаются гамма-облучению, используются лейкоредуцированные компоненты донорской крови (снижение количества лейкоцитов с целью уменьшения риска аллоиммунизации) и патогенредуцированные компоненты крови с целью уменьшения вероятности передачи вирусных инфекций;
38.2. лейкоцитные компоненты крови (гранулоциты) подвергаются только гамма-облучению (25–30 Гр);
38.3. трансплантат ГСК не фильтруется и не облучается. При АВ0-несовместимости донора и реципиента перед миелоинфузией производится очистка трансплантата от донорских эритроцитов > 98%;
38.4. в случае несовпадения крови донора и реципиента по антигенам системы АВ0 и RhD-принадлежности в период от проведения ТГСК до зафиксированного приживления и смены группы крови пациент получает трансфузионную терапию согласно алгоритму выбора трансфузионной среды при несовместимости по системе АВ0, установленному согласно приложению 8.
39. Трансфузиологическая тактика для пациентов, различных с донорами по RhD-принадлежности:
40. Медицинскими показаниями к трансфузии ЭКК массы являются:
14.2. для оценки качества ПСКК проводят подсчет ЯСК методом микроскопии с помощью камеры Горяева или на анализаторе крови; определение количества CD34+, CD3+, CD19+, CD16+56+ клеток методом проточной цитофлуориметрии с использованием моноклональных антител; оценку жизнеспособности клеток; посев на стерильность.
15. При получении ГСК из ПК осуществляются следующие этапы:
15.1. забор ПК производится только в случае целостности пуповины и отсутствия видимых повреждений в течение первых 30 секунд после наложения зажима и перерезания пуповины, но не позднее 15 минут после рождения ребенка. Критерием адекватности образца ПК для аллогенной ТГСК является количество ЯСК не менее 3,5 х 107/кг массы тела реципиента, CD34+ клеток более 1,7 х 105/кг массы тела реципиента;
15.2. приготовление концентрата стволовых клеток ПК осуществляется ручным или автоматизированным методом:
- ручной метод двойного центрифугирования: ПК с добавлением 6% гидроксиэтилкрахмала центрифугируется в коллекционном мешке при 600 оборотов в минуту в течение 5 минут с целью удаления эритроцитов и получения плазмы, обогащенной ЯСК, включающими фракцию стволовых клеток. Отсепарированные ЯСК, переносится в трансферный мешок и цинтрифугируется при 2000 оборотов в минуту с последующим удалением избытка плазмы;
- аппаратный метод с помощью сепаратора с добавлением гидроксиэтилкрахмала.
Этот метод позволяет в автоматизированном режиме сконцентрировать ЯСК ПК до 20 мл в течение 20–30 минут;
15.3. криозамораживание концентрата стволовых клеток ПК проводят на программируемом замораживателе с добавлением раствора криопротектора на основе диметилсульфоксида до достижения 10% концентрации диметилсульфоксида в конечном продукте. Хранение образцов ПК осуществляется в специальных контейнерах при сверхнизкой температуре – 196 °С;
15.4. для оценки качества ПК проводят: подсчет ЯСК методом микроскопии с помощью камеры Горяева или анализатора крови; определение количества CD34+ клеток методом проточной цитофлуориметрии с использованием моноклональных антител; оценку жизнеспособности клеток; посев на стерильность.
ГЛАВА 6
РЕЖИМ КОНДИЦИОНИРОВАНИЯ, МЕДИЦИНСКАЯ ПРОФИЛАКТИКА ОСЛОЖНЕНИЙ
23. Выбор комбинации цитостатических ЛП перед ТГСК зависит от нозологической формы (вида иммунодефицита) и соматического статуса пациента.
24. Наиболее распространенными режимами кондиционирования при проведении алло-ТГСК являются:
- миелоаблативные режимы кондиционирования, установленные согласно приложению 5;
- режимы со сниженной интенсивностью кондиционирования, установленные согласно приложению 6.
25. У пациентов с тяжелой комбинированной иммунной недостаточностью допускается отсутствие кондиционирования. В таком случае проводится медицинская профилактика реакции «трансплантат против хозяина» (далее – РТПХ) с использованием антитимоцитарного глобулина (далее – АТГ).
26. В целях медицинской профилактики острой РТПХ применяется комбинация иммуносупрессивных ЛП. Состав комбинаций ЛП определяется нозологической формой заболевания, клиническими проявлениями и коморбидным статусом пациента и включает следующие ЛП:
циклоспорин (концентрат для инфузий 50 мг/мл, 1 мл; капсулы по 25, 50 и 100 мг; раствор для приема внутрь 100 мг/мл, 50 мл) в начальной суточной дозе 1–3 мг/кг массы тела пациента внутривенно (со дня –1), до момента восстановления основных показателей гемопоэза, под контролем концентрации в крови. Целевая доза для достижения уровня в плазме 100–150 нг/мл. Затем ЛП назначается перорально в суточной дозе в 2 раза больше последней внутривенной, разделенной на два приема. Отмена циклоспорина при отсутствии хронической РТПХ рекомендуется не ранее 6 месяцев после ТГСК. Снижение дозы проводится градуировано, под контролем клинических проявлений РТПХ;
метотрексат (раствор для инъекций 10 мг/мл 5 мл, порошок лиофилизированный для приготовления раствора для инъекций 10 мг, 50 мг) – внутривенно струйно в дозе 10 мг/м2 на введение, дни +1, +3, +6;
метилпреднизолон (стерильный порошок для приготовления раствора для инъекций 40 мг, 125 мг, 250 мг, 500 мг, 1000 мг, суспензия для инъекций 40 мг/мл мл) – внутривенно струйно в стартовой суточной дозе 1 мг/кг в течение 28 дней, начиная со дня +1, с последующим постепенным снижением дозы, возможным переходом на пероральный прием (таблетки 4 мг, 8 мг, 16 мг, 32 мг) и отменой ЛП в течение двух недель;
такролимус (концентрат для приготовления раствора для внутривенного введения 5 мг/мл) – внутривенно постоянной инфузией в суточной дозе 0,02 мг/кг со дня –1 (при гапло ТГСК – со дня +5). Затем перорально в суточной дозе 0,02–0,03 мг/кг в день (не более 2 мг) (капсулы 0,5 мг, 1 мг, капсулы пролонгированного действия 0,5 мг, 1 мг); при этом целевая концентрация ЛП в крови должна быть 5–15 нг/мл;
микофенолата мофетил (микофеноловая кислота) (далее – ММФ) (капсулы 250 мг, таблетки, покрытые оболочкой, 500 мг, таблетки, покрытые кишечнорастворимой оболочкой, 180 мг, 360 мг) – перорально в дозе 30–45 мг/кг/сут., разделенной на два приема с +1 дня (при гапло-ТГСК – с дня +5);
АТГ (концентрат для приготовления раствора для инфузий 20 мг/мл 5 мл, лиофилизированный порошок для приготовления раствора для инфузий 25 мг) внутривенно три (четыре) последовательных дня в дозе от 2,5 мг/кг/сут. до 20 мг/кг/сут. в зависимости от нозологии, типа донора, источника ГСК, производителя (бренда) АТГ;
циклофосфамид (порошок для приготовления раствора для внутривенного введения (для инъекций) 200 мг) – внутривенно 1-часовой инфузией в дозе 10–50 мг/кг в дни +3 и +4 (в том числе при гапло-ТГСК);
сиролимус (таблетки 1 мг) – стартовая доза 6 мг в сутки однократно, далее по 2 мг 1 раз в сутки. У детей массой менее 40 кг стартовая доза 3–5 мг/м2, далее 1–2 мг/м2. Коррекция дозы осуществляется индивидуально под контролем концентрации ЛП в сыворотке крови. Целевая концентрация от 4 до 12 нг/мл. Назначают с дня –3 с постепенной отменой при отсутствии РТПХ;
руксолитиниб (таблетки 5 мг, 10 мг, 15 мг) в суточной дозе 4–7,5 мг/м2 (распределение в 2 приема) под контролем гематологических показателей с возможным дальнейшим увеличением дозы;
бортезомиб (лиофилизированный порошок для приготовления раствора для внутривенного введения и подкожного введения 2 мг, 3,5 мг) дозирование 1–1,5 мг/м2 внутривенно в дни +1, +4, +7;
тоцилизумаб (концентрат для приготовления раствора для инфузий 20 мг/мл 4 мл, 10 мл, 20 мл) 8 мг/кг внутривенно каждые 3–4 недели;
ведолизумаб 300 мг (порошок для приготовления концентрата для приготовления раствора для инфузий 300 мг) (100 мг для детей с массой < 10 кг, 150 мг для детей с массой 10–25 кг) на –1, +13 и далее каждые 28 дней, всего до 7 введений.
27. В целях медицинской профилактики судорожного синдрома при приеме высоких доз бусульфана назначается клоназепам (таблетки 0,5 мг, 2 мг) для пациентов младше 6 лет* и пациентов старше 6 лет в дозе 0,01–0,03 мг/кг/сут. с –7 до +1 дня. Клоназепам начинают применять за сутки до назначения бусульфана в дозе 0,125–0,5 мг утром и вечером.
28. В целях медицинской профилактики геморрагического цистита назначается месна (раствор для внутривенного введения 100 мг/мл 4 мл) внутривенно капельно.
Режим дозирования ЛП: непосредственно перед началом введения циклофосфамида в дозе, составляющей 50 % от дозы циклофосфамида быстрой инфузией, и далее по 50 % от дозы циклофосфамида на 3, 6, 9 и 24 часы от начала инфузии циклофосфамида. Общая доза – 200 % от дозы циклофосфамида.
29. Гастропротекция включает прием ингибиторов протонной помпы (омепразол, эзомепразол) внутривенно в профилактических дозах с –7 дня до восстановления показателей гемопоэза.
30. Медицинская профилактика вено-окклюзионной болезни проводится гепарином (раствор для внутривенного и подкожного введения (для инъекций) 5 000 МЕ/мл) в дозе 100 ЕД/кг/сут. (5 ЕД/кг/час), внутривенно в виде непрерывной внутривенной инфузии с –1 дня до +30 дня под контролем показателей коагулограммы.
31. Медицинская профилактика цитолитической гиперурикемии включает прием аллопуринола (таблетки 100 мг, 150 мг, 200 мг, 300 мг) в дозе 10 мг/кг/сут. в 2 приема в таблетках с первого дня кондиционирования до дня 0 включительно.
32. Медицинская профилактика рвоты включает прием одного из следующих ЛП (off-lable):
ондансетрон (раствор для внутривенного и внутримышечного введения (для инъекций) 2 мг/мл 2 мл, 4 мл) для детей младше 6 месяцев*, для детей старше 6 месяцев при площади тела < 0,6 м2 назначают по 2 мг 3 раза в сутки, от 0,6 м2 до 1,2 м2 по 4 мг, более 1,2 м2 – по 8 мг 3 раза в сутки или 5 мг/м2 (по инструкции к ЛП);
гранисетрон (концентрат для приготовления раствора для инфузий 1 мг/мл 3 мл, раствор для инъекций 1 мг/мл 3 мл) для детей младше 2 лет*, для детей старше 2 лет 1–3 мг в сутки;
трописетрон (раствор для внутривенного введения (для инъекций) 1 мг/мл 5 мл) для детей младше 2 лет*, для детей старше 2 лет – 0,2 мг/кг. Максимальная суточная доза 5 мг;
метоклопрамид (раствор для внутривенного и внутримышечного введения (для инъекций) 5 мг/мл 2 мл) для детей младше 1 года*, для детей старше 1 года – 0,1–0,15 мг/кг. Начинается за 30 минут до первого введения химиопрепарата. При необходимости продолжается 24–48 часов после последнего введения химиопрепаратов.
При недостаточной эффективности противорвотных ЛП их действие может быть усилено введением глюкокортикоидов внутривенно (дексаметазон – 0,1 мг/кг).
33. Медицинская профилактика витаминной недостаточности включает применение поливитаминных ЛП для внутривенного введения: кальция фолинат (порошок лиофилизированный для приготовления раствора для внутривенного и внутримышечного введения (для инъекций) 50 мг 10 мл, раствор для внутривенного и внутримышечного введения 10 мг/мл 3 мл, 5 мл, 10 мл) – 10 мг/м2 внутривенно 1 раз в неделю.
34. Гидратация осуществляется путем внутривенного капельного введения солевых и декстрозных растворов:
- натрия хлорид раствор для инфузий (для инъекций) 9 мг/мл;
- глюкоза раствор для инфузий 50 мг/мл, в объеме от 2 до 4 литров/м2/сут.
Контроль гидратации: измерение веса каждые 12 часов, баланса объема мочеиспускания и поступившей в организм пациента жидкости (инфузии, питье).
При положительном балансе используются мочегонные ЛП (фуросемид (раствор для инъекций (раствор для внутривенного и внутримышечного введения) 10 мг/мл 2 мл) 1 мг/кг/сут. внутривенно разделенная на 2–3 введения или суточным титрованием под контролем артериального давления и суточного диуреза).
35. Заместительная терапия внутривенным иммуноглобулином осуществляется путем введения иммуноглобулина для внутривенного введения капельно 0,2 г/кг со дня – 10 – 1 раз в неделю до дня +100, далее при снижении уровня IgG в сыворотке крови ниже 5 г/л – внутривенно капельно 0,2–0,4 мг/кг 1 раз в 4 недели.
36. В целях стимуляции гемопоэза назначается один из следующих ЛП:
филграстим (раствор для инъекций (для внутривенного и подкожного введения) 300 мкг/мл (30 млн. МЕ/мл)) 5–10 мг/кг подкожно или внутривенной инфузией 1 раз в день, до восстановления показателей гранулопоэза;
ленограстим (лиофилизат для приготовления раствора для внутривенного и подкожного введения 33,6 млн. МЕ) 5–10 мг/кг подкожно либо внутривенной инфузией 1 раз в день, до восстановления показателей гранулопоэза;
эритропоэтин (раствор для внутривенного и подкожного введения (для инъекций) 2 000 МЕ/мл 1 мл, Раствор для инъекций 4 000 МЕ/мл 1 мл, раствор для инъекций 10 000 МЕ/мл 1 мл, раствор для внутривенного и подкожного введения 40 000 МЕ/1 мл) 100 МЕ/кг внутривенной инфузией 3 раза в неделю до восстановления показателей эритропоэза;
агонисты тромбопоэтиновых рецепторов – ромиплостим (лиофилизированный порошок для приготовления раствора для подкожного введения 250 мкг) 1 мкг/кг подкожно или внутривенной инфузией 1 раз в неделю, до восстановления показателей тромбоцитопоэза.
37. Медицинская профилактика инфекционных осложнений включает:
37.1. организационные мероприятия:
- изоляция пациента в боксе с ламинарным потоком воздуха;
- регулярный и тщательный гигиенический и антисептический уход за кожей и слизистыми;
- «стерильный» режим работы персонала – использование стерильной одежды, перчаток, масок, специальной обработки рук, личный микробиологический контроль;
- ограничение посещаемости бокса;
- мониторинг микробиологического статуса пациента 1 раз в неделю (кал, зев);
37.2. медицинскую профилактику бактериальной инфекции (по медицинским показаниям) в индивидуальном порядке;
37.3. медицинскую профилактику протозойных инфекций – назначается сульфаметоксазол/триметоприм (ко-тримоксазол) раствор для инфузий (80 мг +16 мг)/мл 5 мл, суспензия для приема внутрь – 5 мг/кг/сут. по триметоприму каждые 12 часов, таблетки 400 мг + 80 мг для детей до 2 лет*, с 2 лет – 5 мг/кг/сут. по триметоприму каждые 12 часов 3 раза в неделю с момента приживления трансплантата (восстановления лейкоцитов) до 6 месяцев после отмены иммуносупрессивной терапии и восстановления иммунной системы;
______________________________
* Off-lable.
37.4. медицинскую профилактику вирусной инфекции, при которой назначается один из противовирусных ЛП:
ацикловир (порошок лиофилизированный для приготовления раствора для инфузий 250 мг, 500 мг, 100, мг) внутривенно со дня –10 в дозе 250-350 мг/м2 3 раза в сутки в течение периода нейтропении. При восстановлении уровня нейтрофилов периферической крови выше 0,5 х 109/л пациент переводится на пероральный прием при отсутствии нарушения энтерального усвоения. Доза для перорального приема (таблетки (таблетки, покрытые оболочкой) 200 мг, 400 мг) – 250–500 мг/м2 3 раза в сутки до дня +180, далее – 250 мг/м2 2–3 раза в сутки не менее 1 года после алло ТГСК;
ганцикловир (порошок лиофилизированный для приготовления раствора для инфузий 500 мг) (получают только ЦМВ-серопозитивные реципиенты) 5 мг/кг/сут. за 1 введение внутривенно со дня +1.
Назначается при двукратной ПЦР-позитивности в анамнезе, наличии других проявлений инфекции;
валганцикловир (таблетки, покрытые оболочкой, 450 мг) в позднем посттрансплантационном периоде 16 мг/кг 2 раза в сутки.
У детей до 16 лет доза валганцикловира (мг) = 7 х площадь тела в м2 х клиренс по эндогенному креатинину или 16 мг/кг 2 раза в сутки, но не более 900 мг в сутки, старше 16 лет – 900 мг 2 раза в сутки (за исключением пациентов с тяжелой желудочно-кишечной РТПХ).
Пациентам из группы высокого риска развития EBV-ассоциированного посттрансплантационного лимфопролиферативного заболевания назначается ритуксимаб (концентрат для приготовления раствора для инфузий 10 мг/мл 10 мл, 30 мл, 50 мл) 200–375 мг/м2 внутривенно не менее 1 введения до ТГСК или в день 0;
37.5. медицинскую профилактику грибковой инфекции, при которой осуществляется изоляция пациента в боксе, оборудованном HEPA (High Efficiency Particulate Air) фильтрами – воздушными фильтрами высокой эффективности для очистки воздуха и назначается один из ЛП, применяемых для медицинской профилактики грибковой инфекции, согласно приложению 7;
37.6. медицинскую профилактику катетер-ассоциированных инфекций, которая включает:
- соблюдение режима асептики и антисептики;
- обработка кожи вокруг катетеров антисептиками (хлоргексидин, йодсодержащие и спиртосодержащие ЛП);
- использование катетеров, которые снижают риск развития катетер-ассоциированных инфекций;
- своевременная замена пластырной наклейки центрального венозного катетера;
37.7. медицинскую профилактику мукозита, которая осуществляется путем полоскания полости рта растворами хлоргексидина, фурациллина со дня госпитализации, раствором повидон-йода 2 г/1000 мл.
ГЛАВА 7
ТРАНСФУЗИОЛОГИЧЕСКАЯ ТАКТИКА
38. Подготовка к медицинскому применению крови, ее компонентов:
38.1. с целью снижения иммуногенности, а также с целью медицинской профилактики РТПХ все компоненты крови, переливаемые реципиентам ГСК, подвергаются гамма-облучению, используются лейкоредуцированные компоненты донорской крови (снижение количества лейкоцитов с целью уменьшения риска аллоиммунизации) и патогенредуцированные компоненты крови с целью уменьшения вероятности передачи вирусных инфекций;
38.2. лейкоцитные компоненты крови (гранулоциты) подвергаются только гамма-облучению (25–30 Гр);
38.3. трансплантат ГСК не фильтруется и не облучается. При АВ0-несовместимости донора и реципиента перед миелоинфузией производится очистка трансплантата от донорских эритроцитов > 98%;
38.4. в случае несовпадения крови донора и реципиента по антигенам системы АВ0 и RhD-принадлежности в период от проведения ТГСК до зафиксированного приживления и смены группы крови пациент получает трансфузионную терапию согласно алгоритму выбора трансфузионной среды при несовместимости по системе АВ0, установленному согласно приложению 8.
39. Трансфузиологическая тактика для пациентов, различных с донорами по RhD-принадлежности:
если донор является RhD-положительным, а реципиент RhD-отрицательным:
с 1 по 28 дни используются RhD-отрицательные эритроцитные компоненты крови (далее – ЭКК); с 29 дня – RhD-положительные ЭКК;
если донор RhD-отрицательный, используются RhD-отрицательные ЭКК.
40. Медицинскими показаниями к трансфузии ЭКК массы являются:
- снижение уровня гемоглобина < 80 г/л или число эритроцитов менее 2,0 х 1012/л;
- снижение уровня гемоглобина < 100 г/л в условиях активного кровотечения (продолжительное носовое кровотечение, геморрагический цистит, кровотечение из желудочно-кишечного тракта (далее – ЖКТ), легочный геморраж) или при подозрении на внутреннее кровотечение;
- снижение уровня гемоглобина < 100 г/л у клинически нестабильного пациента (полиорганная недостаточность, шок, сепсис, кишечная РТПХ 4 ст.);
- снижение уровня гемоглобина < 100 г/л при сопутствующих сердечных, легочных или цереброваскулярных заболеваниях, которые приводят к значительному снижению доставки О2 в ткани;
- острая потеря крови в объеме > 15% объема циркулирующей крови или снижение уровня гемоглобина на 20 мг/дл и более в течение 24 часов;
ЭКК назначаются в дозировке 10 мл/кг (максимально 15 мл/кг), внутривенно со скоростью 2–5 мл/кг массы тела в час, при продолжающемся кровотечении – до 10–15 мл/кг массы тела в час с обязательным контролем показателей гемодинамики и дыхания.
41. Для трансфузии тромбоцитных компонентов крови (далее – ТКК) предпочтительно использовать тромбоциты, полученные автоматическим аферезом, обедненные лейкоцитами, патогенредуцированные.
Медицинскими показаниями к трансфузии ТКК являются:
42. Для трансфузии компонентов плазмы предпочтительно использовать свежезамороженную плазму крови (далее – СЗП), полученную автоматическим аферезом, обедненную лейкоцитами, карантинизированную, патогенредуцированную.
Медицинскими показаниями к трансфузии СЗП являются:
Трансфузия СЗП назначается в дозе 10–20 мл/кг веса (до 30 мл/кг), скорость введения в зависимости от состояния пациента внутривенно капельно или струйно, при ДВС-синдроме – преимущественно струйно.
43. Медицинскими показаниями к переливанию криопреципитата являются:
44. Медицинскими показаниями к переливанию лейкоцитных компонентов крови (гранулоцитов) являются:
55. Терапия и медицинская профилактика ВОБ:
56. Посттрансплантационный лимфопролиферативный синдром (ассоциированный или не ассоциированный с ВЭБ):
57. Лечение вирусных инфекций:
57.1. лечение активной ЦМВ инфекции:
57.2. лечение ВК-вирусной инфекции:
57.3. лечение JC-вирус инфекции: коррекция (снижение) иммуносупрессивной терапии;
57.4. лечение ВЭБ инфекции: уменьшение иммуносупрессии, при ВЭБ-виремии с концентрацией > 1000 копий ДНК ВЭБ/мл – ритуксимаб 375 мг/м2 один раз в неделю (1–4 дозы) до получения отрицательного результата ПЦР сыворотки крови;
57.5. лечение ВГЧ-6 инфекции – используется один из ЛП:
57.6. лечение ВПГ-1,2 инфекции: ацикловир (порошок лиофилизированный для приготовления раствора для инфузий 250 мг, 500 мг, 1000 мг) внутривенно 10–15 мг/кг каждые 8 часов в виде медленной инфузии в течение 10–14 дней до получения двух последовательных отрицательных результатов ПЦР;
57.7. лечение ВЗВ инфекции:
57.8. лечение парвовирусной В19 инфекции: внутривенный иммуноглобулин в суммарной дозе 1–2 г/кг за 2–3 введения.
58.1. стартовую терапию неосложненных эпизодов фебрильной нейтропении (однократное повышение температуры тела выше 38,5 °С при содержании нейтрофилов крови менее 1 х 109 клеток в литре или двукратное повышение температуры тела выше 38 °С, измеренной с интервалом в 1 час при содержании нейтрофилов крови менее 0,5 х 109 или менее 1 х 109 клеток в литре с тенденцией к дальнейшему снижению их количества) проводят β-лактамным антибиотиком широкого спектра действия с антипсевдомонадной активностью: цефалоспорины 3–4 поколения, карбапенемы (за исключением эртапенема) или защищенные пенициллины с антипсевдомонадной активностью согласно приложению 18;
58.2. дальнейший выбор схемы лечения определяется источником инфекции, предшествующей колонизацией резистентными бактериями (например, метициллин-резистентный золотистый стафилококк, ванкомицин-резистентные энтерококки, микроорганизмы продуценты β-лактамаз расширенного спектра, в том числе карбапенемаза-продуцирующие штаммы Klebsiella pneumoniae), клинической картиной инфекционного эпизода.
59. Лечение грибковых инфекций:
ЛП выбора для терапии мукормикоза является амфотерицин В (липидная форма).
Альтернативными ЛП являются: посаконазол, изавуконазол. При терапии мукормикоза приоритетом является хирургическая санация пораженных тканей.
ЛП выбора для терапии инвазивного кандидоза и кандидемии являются эхинокандины. Альтернативные ЛП – флуконазол или амфотерицин В (липидная форма).
ЛП выбора для терапии фузариоза являются: посаконазол, амфотерицин В (липидная форма). Альтернативными ЛП являются: вориконазол или изавуконазол.
- уровень гемоглобина < 100 г/л при ожидаемой острой потере крови в объеме 15 % объема циркулирующей крови (при подготовке к хирургическому вмешательству).
ЭКК назначаются в дозировке 10 мл/кг (максимально 15 мл/кг), внутривенно со скоростью 2–5 мл/кг массы тела в час, при продолжающемся кровотечении – до 10–15 мл/кг массы тела в час с обязательным контролем показателей гемодинамики и дыхания.
41. Для трансфузии тромбоцитных компонентов крови (далее – ТКК) предпочтительно использовать тромбоциты, полученные автоматическим аферезом, обедненные лейкоцитами, патогенредуцированные.
Медицинскими показаниями к трансфузии ТКК являются:
- снижение уровня тромбоцитов < 20 000/мкл в отсутствие активного кровотечения у клинически стабильного пациента;
- уровень тромбоцитов < 50 000/мкл у пациента с признаками кровотечения, в условиях синдрома диссеминированного внутрисосудистого свертывания (далее – ДВС-синдром), при быстром падении уровня тромбоцитов в ОАК, перед броноальвеолярным лаважем;
- уровень тромбоцитов < 80 000/мкл при подготовке к инвазивным процедурам или после них (фиброгастродуоденоскопия или колоноскопия с биопсией, смена центрального венозного катетера);
- уровень тромбоцитов < 100 000/мкл в условиях активного жизнеугрожающего кровотечения (требующего трансфузии ЭКК, кровотечения во внутреннее пространство, внутричерепное кровоизлияние, или в условиях высокого риска кровотечений), при подготовке к выполнению биопсии печени.
Трансфузия ТКК назначается в дозе: 60 х 109 тромбоцитов на 10 кг веса, внутривенно со скоростью 10/мл/кг массы тела в час.
42. Для трансфузии компонентов плазмы предпочтительно использовать свежезамороженную плазму крови (далее – СЗП), полученную автоматическим аферезом, обедненную лейкоцитами, карантинизированную, патогенредуцированную.
Медицинскими показаниями к трансфузии СЗП являются:
- острая массивная кровопотеря, ДВС-синдром, геморрагический синдром при лабораторно подтвержденном дефиците факторов свертывания крови по данным коагулограммы (удлинение активированного частичного тромбопластинового времени и протромбинового времени менее 1,5 от нормы);
- дефицит факторов свертывания крови;
- дефицит естественных антикоагулянтов (антитромбин-III, протеины C, S).
Трансфузия СЗП назначается в дозе 10–20 мл/кг веса (до 30 мл/кг), скорость введения в зависимости от состояния пациента внутривенно капельно или струйно, при ДВС-синдроме – преимущественно струйно.
43. Медицинскими показаниями к переливанию криопреципитата являются:
приобретенная гипофибриногенемия (критический уровень фибриногена 1,5 г/л, целевой – более 2,0 г/л по Клаусу);
одна доза криопреципитата на 10 кг массы тела реципиента.
Введение криопреципитата осуществляется внутривенно струйно или быстро капельно из расчета 50–60 капель в минуту.
44. Медицинскими показаниями к переливанию лейкоцитных компонентов крови (гранулоцитов) являются:
- абсолютная нейтропения (количество лейкоцитов в крови менее 0,5 x 109/л) в сочетании с тяжелым инфекционным процессом с рефрактерностью к антибактериальной (антимикотической) терапии с прогнозируемой длительностью нейтропении более 10 дней.
Объем лейкоцитного компонента крови для переливания составляет не более 15 мл/кг массы тела.
Время переливания лейкоцитных компонентов крови составляет 2–4 часа при скорости переливания не более 10 мл/кг массы тела в час.
45. В случае первой в жизни трансфузии препарата крови или в случае отягощенного трансфузионного анамнеза (аллергические реакции на кровь, ее компоненты) может быть назначена премедикация одним из следующих ЛП:
- дифенгидрамин внутривенно 1 % раствор 0,5–1 мг/кг (максимально 50 мг) с промежутками между введениями не менее 4 часов;
- клемастин внутривенно 1 % раствор 0,1 мл/год жизни (максимально 2 мг);
- дексаметазон внутривенно 0,15–0,2 мг/кг массы тела.
46. Во время проведения ТГСК (с 10 по 30 день):
ГЛАВА 8
МОНИТОРИНГ СОСТОЯНИЯ ПАЦИЕНТОВ
46. Во время проведения ТГСК (с 10 по 30 день):
- измерение температуры тела, пульса, артериального давления, частоты дыхания – каждые 3 часа (при необходимости – каждый час);
- измерение массы тела пациента – 1–2 раза в сутки;
- баланс жидкости: внутрь + внутривенно – диурез + патологические потери – каждые 3 часа;
- суточный диурез – ежедневно;
- контроль за стулом (объем и кратность в течение суток) – ежедневно;
- ОАК – ежедневно (включая период нейтропении); лейкоцитарная формула, СОЭ, ретикулоциты – 2 раза в неделю;
- анализ мочи общий – 2–3 раза в неделю (включая период нейтропении), по медицинским показаниям – чаще;
- БАК: общий белок, билирубин, мочевина, креатинин, глюкоза, натрий, калий, магний, кальций – ежедневно (включая период нейтропении), по медицинским показаниям – чаще;
- БАК: гемоглобин плазмы, ЛДГ, щелочная фосфатаза, АсАТ, АлАТ, ГГТП, С-реактивный белок, мочевая кислота, амилаза, скорость клубочковой фильтрации – 2 раза в неделю, по медицинским показаниям – чаще; гаптоглобин, железо, ферритин, холестерин, триглицериды – по медицинским показаниям;
- определение клиренса по эндогенному креатинину, определение уровня калия, натрия, мочевины, глюкозы в суточной моче – по медицинским показаниям;
- исследование показателей гемостаза – 2 раза в неделю, по медицинским показаниям – чаще;
- определение альбумина, иммуноглобулинов крови – 1 раз в неделю, по медицинским показаниям – чаще;
- вирусологическое исследование (ДНК ЦМВ, ВЭБ, ВПГ, ВГЧ-6 типа, парвовирус B19, BK-вирус) – 1 раз в неделю до 100 дня, 1 раз в 2 недели до 180 дня, 1 раз в месяц до 365 дня, при наличии медицинских показаний – чаще, далее – по медицинским показаниям;
- вирусологическое исследование в культуре клеток – по медицинским показаниям;
- вирусологическое исследование на респираторные вирусы, кишечные вирусы, легочные инфекции – по медицинским показаниям;
- определение Ag аспергиллы – 1–2 раза в неделю;
- проба Кумбса непрямая – 1 раз в неделю; по медицинским показаниям – чаще;
- определение маркеров гепатитов В, С – при наличии медицинских показаний;
- бактериологическое исследование: посевы из полости рта/зева, посев кала – 1 раз в неделю; по медицинским показаниям – чаще; посевы на флору из других локусов – по медицинским показаниям;
- лекарственный мониторинг: уровень циклоспорина А или такролимуса в крови – 2 раза в неделю;
- лекарственный мониторинг: концентрация вориконазола, бусульфана – по медицинским показаниям;
- ЭКГ, рентгенография органов грудной клетки – по медицинским показаниям;
При наличии клинических признаков или при положительном скрининге на ТА-ТМА:
48. Медицинское наблюдение за пациентами после ТГСК (с +30 дня по +365 день) включает оценку объективного статуса, медицинское наблюдение врачей-специалистов, лабораторную и инструментальную диагностику:
48.1. кратность медицинских осмотров:
48.2. лабораторные методы исследования:
- дополнительные методы обследования (УЗИ органов брюшной полости, сердца, щитовидной железы, КТ придаточных пазух носа, органов грудной клетки, органов брюшной полости), осмотр врачами-специалистами – по медицинским показаниям.
47. Скрининг трансплантат-ассоциированной тромботической микроангиопатии (далее – ТА-ТМА) от дня 0 до разрешения или дня +30:
- ОАК, БАК, измерение артериального давления – ежедневно;
- ЛДГ – 2 раза в неделю;
- шистоциты, rUPCR (индекс соотношения количества белка и креатинина в моче) – еженедельно.
При наличии клинических признаков или при положительном скрининге на ТА-ТМА:
- обзор мазка периферической крови врачом-лаборантом;
- проба Кумбса (прямая и непрямая);
- ДВС-панель;
- гаптоглобин;
- свободный гемоглобин плазмы;
- дополнительно органные функции – по медицинским показаниям.
48. Медицинское наблюдение за пациентами после ТГСК (с +30 дня по +365 день) включает оценку объективного статуса, медицинское наблюдение врачей-специалистов, лабораторную и инструментальную диагностику:
48.1. кратность медицинских осмотров:
- до +100 дней – 1–2 раза в неделю, по медицинским показаниям – чаще (контроль приема иммуносупрессивной и сопроводительной терапии: антибактериальной, противовирусной и противогрибковой);
- до +180 дней – 1 раз в 2 недели, по медицинским показаниям – чаще;
- до 1 года – 1 раз в месяц, по медицинским показаниям – чаще;
- рост, вес, АД на дни: +30, +60, +100, +180, +365;
48.2. лабораторные методы исследования:
- ОАК: лейкоцитарная формула, СОЭ, ретикулоциты – 2 раза в неделю до +100 дня, 1 раз в 2 недели до +180 дня, 1 раз в месяц до +365 дня, по медицинским показаниям – чаще;
- БАК: общий белок, мочевина, креатинин, глюкоза, калий, натрий, кальций, магний, щелочная фосфатаза, АлАТ, АсАТ, ЛДГ, ГГТП, билирубин, гемоглобин плазмы, гаптоглобин) – 2 раза в неделю, 1 раз в 2 недели до +180 дня, 1 раз в месяц до +365 дня, по медицинским показаниям – чаще;
- исследование крови на уровень циклоспорина/такролимуса – 1 раз в неделю;
- коагулограмма – 1 раз в неделю до 100 дней, по медицинским показаниям – чаще; после 100 дней – по медицинским показаниям;
- общий анализ мочи – 1 раз в 2 недели до + 100 дня, далее – по медицинским показаниям;
- протеинограмма – 1 раз в неделю до 100 дней, далее – по медицинским показаниям;
- ПЦР на ЦМВ, ВЭБ, HСV, ВГЧ-6 – 1 раз в месяц до 180 дней, по медицинским показаниям – чаще, после 180 дней – по медицинским показаниям;
- диагностическая костномозговая пункция на дни: +100, +180, +365, далее – по медицинским показаниям;
- диагностическая люмбальная пункция – по медицинским показаниям;
- определение группы крови по системе АВ0 – 1 раз в месяц до смены группы (при несовместимости по АВ0, далее – по медицинским показаниям;
- кровь на химеризм на дни: +30, +45, +60, +80, +100, +140, +180, +245, +365, по медицинским показаниям – чаще:
эритроцитарный химеризм (серологическая лаборатория);
лейкоцитарный химеризм (генетическая лаборатория при HLA-несовместимости пары донор/реципиент);
ПЦР-химеризм (молекулярно-биологическая лаборатория);
48.3. инструментальные методы исследования:
половой химеризм при разнополых ТГСК (цитогенетическая лаборатория);
- иммунограмма на дни: +30, +45, +60, +80, +100, +140, +180, +245, +365, по медицинским показаниям – чаще;
- определение гормонов щитовидной железы: Т3, Т4, ТТГ, половых гормонов (ФСГ, эстрадиол, тестостерон), кортизол, АКТГ на дни: +30, +60, +100, +180, +365;
- проба Кумбса на дни: +30, +60, +100, +180, по медицинским показаниям – чаще; далее по медицинским показаниям;
- вирусологическое исследование: гепатиты В, С, ВПГ, ЦМВ, токсоплазмоз, ВЭБ – 1 раз в месяц до 180 дней, по медицинским показаниям – чаще, после 180 дней – по медицинским показаниям;
48.3. инструментальные методы исследования:
- рентгенограмма органов грудной клетки – по медицинским показаниям;
- КТ органов грудной клетки, придаточных пазух носа на дни: +30, +100, +180, +365; по медицинским показаниям – чаще.
- ЭКГ + УЗИ сердца на дни: +30, +100, +180, +365, по медицинским показаниям – чаще;
- УЗИ органов брюшной полости – 1 раз в месяц до 180 дней, по медицинским показаниям – чаще, после 180 дней – по медицинским показаниям;
- спирометрия на дни: +180; +365; по медицинским показаниям – чаще;
- денситометрия на дни +180, +365; по медицинским показаниям – чаще.
Консультации врачей-специалистов: врача – детского эндокринолога, врача – детского невролога, врача-офтальмолога: дни + 100, +180, +365, консультация других врачей-специалистов – по медицинским показаниям согласно приложению 4.
49. К осложнениям раннего посттрансплантационного периода, возникающим в течение 100 дней после ТГСК, относятся:
49.1. осложнения, связанные с токсичностью режима кондиционирования:
49.2. инфекционные осложнения:
49.3. неприживление трансплантата: проявляется аплазией КМ и периферической панцитопенией (число нейтрофилов менее 0,5 х 109/л к +30 дню/ к +42 дню для ПК).
49.4. смешанный донорский химеризм – уровень химеризма 89% – 5%, равное распределение донорского химеризма во всех ростках кроветворения;
49.5. расщепленный смешанный химеризм – значимое различие уровня донорского химеризма в субпопуляциях клеточных линий реципиента;
49.6. недостаточное функционирование трансплантата – частичная зависимость от трансфузий препаратов крови и (или) факторов роста при отсутствии других причин (например, рецидив заболевания, прием миелотоксических ЛП или инфекции). При этом донорский химеризм находится в пределах желаемого целевого уровня;
49.7. отторжение трансплантата – снижение кроветворной функции (снижение гемоглобина и (или) тромбоцитов и (или) нейтрофилов), требующее поддержки препаратами крови или факторами роста, после приживления трансплантата, донорский химеризм менее 5% после ранее диагностированного полного или смешанного донорского химеризма;
49.8. РТПХ острая.
В зависимости от интенсивности клинических проявлений и количества вовлеченных в поражение органов осуществляется стадирование острой РТПХ. Различают I, II, III и IV стадии острой РТПХ.
В зависимости от времени развития клиники острой РТПХ различают:
Определение категории РТПХ осуществляется в соответствии с классификацией острой и хронической РТПХ, установленной согласно приложению 12.
49.9. ранние эндотелиальные осложнения (синдром перегрузки жидкостью; синдром капилярной утечки; синдром синусоидальной обструкции; синдром приживления; тромботическая микроангиопатия, связанная с ТГСК; синдром сосудистой идиопатической пневмонии, включающий диффузное альвеолярное кровоизлияние, синдром гиперпроницаемости легочных капилляров и респираторный дистресс-синдром на фоне приживления трансплантата, синдром задней обратимой энцефалопатии);
49.10. синдром синусоидальной обструкции/веноокклюзионное заболевание печени (далее – ВОБ) является жизнеугрожающим осложнением после трансплантации ГСК.
49.11. ТА-ТМА – является тяжелым осложнением ТГСК с высоким риском летальности. Критерии для диагностики ТА-ТМА у детей приведены в приложении 14.
50. К осложнениям позднего посттрансплантационного периода относятся:
50.1. хроническая РТПХ, которая может возникнуть самостоятельно (de novo) или быть продолжением острой РТПХ. Стадирование хронической РТПХ возможно также по объему и степени поражения различных органов и систем.
50.2. посттрансплантационный лимфопролиферативный синдром (ассоциированный или не ассоциированный с ВЭБ);
ГЛАВА 9
ОСЛОЖНЕНИЯ ТГСК
49. К осложнениям раннего посттрансплантационного периода, возникающим в течение 100 дней после ТГСК, относятся:
49.1. осложнения, связанные с токсичностью режима кондиционирования:
- панцитопения (количество гранулоцитов в крови менее 0,5 х 109/л, тромбоцитопения, анемия);
- интерстициальный пневмонит, фиброз (связанный с бусульфаном);
- поражение ЖКТ (тошнота, рвота, мукозит, эзофагит, гастродуоденит, диарея);
- поражение сердечно-сосудистой системы: гипертензия, гипотония, нарушения ритма сердца, эндокардит;
- поражение почек и мочеполовой системы: острая почечная недостаточность;
- геморрагический цистит;
- эндотелиальные осложнения;
- поражение кожи, придатков кожи и алопеция;
- поражение глаз;
- нейротоксичность;
- нарушение водно-электролитного баланса;
- кровотечения и тромботические осложнения;
- поражения печени;
49.2. инфекционные осложнения:
- бактериальные инфекции;
- вирусные инфекции;
- грибковые инфекции.
Во всех случаях подозрения на инфекционные осложнения проводится исследование крови на стерильность;
49.3. неприживление трансплантата: проявляется аплазией КМ и периферической панцитопенией (число нейтрофилов менее 0,5 х 109/л к +30 дню/ к +42 дню для ПК).
Донорский химеризм менее 5%. Для снижения вероятности неприживления трансплантата, рекомендуется придерживаться клеточности трансплантата, установленной согласно приложению 9;
49.4. смешанный донорский химеризм – уровень химеризма 89% – 5%, равное распределение донорского химеризма во всех ростках кроветворения;
49.5. расщепленный смешанный химеризм – значимое различие уровня донорского химеризма в субпопуляциях клеточных линий реципиента;
49.6. недостаточное функционирование трансплантата – частичная зависимость от трансфузий препаратов крови и (или) факторов роста при отсутствии других причин (например, рецидив заболевания, прием миелотоксических ЛП или инфекции). При этом донорский химеризм находится в пределах желаемого целевого уровня;
49.7. отторжение трансплантата – снижение кроветворной функции (снижение гемоглобина и (или) тромбоцитов и (или) нейтрофилов), требующее поддержки препаратами крови или факторами роста, после приживления трансплантата, донорский химеризм менее 5% после ранее диагностированного полного или смешанного донорского химеризма;
49.8. РТПХ острая.
Клиническая классификация стадий острой РТПХ установлена согласно приложению 10.
В зависимости от интенсивности клинических проявлений и количества вовлеченных в поражение органов осуществляется стадирование острой РТПХ. Различают I, II, III и IV стадии острой РТПХ.
Система органного стадирования острой РТПХ установлена согласно приложению 11.
В зависимости от времени развития клиники острой РТПХ различают:
- классическую острую РТПХ – возникает в период 0 – +100 день после алло-ТГСК;
- персистирующую позднюю острую РТПХ – признаки острой РТПХ, возникшие до дня +100 и сохраняющиеся после дня +100;
- рецидивирующую острую – РТПХ возникает и разрешается в период 0 – +100 дней, повторно развивается после дня +100;
- de novo острая РТПХ – впервые появление признаков острой РТПХ после +100 дня.
Определение категории РТПХ осуществляется в соответствии с классификацией острой и хронической РТПХ, установленной согласно приложению 12.
Стероид-независимая/стероид-резистентная РТПХ – отсутствие ответа на проводимую стандартную терапию глюкокортикоидами (прогрессирование в течение 3–5 дней от начала терапии или неполный ответ на терапию в течение 7–14 дней) или рецидив после начального снижения дозы гормонов диагностируется, требует назначения второй линии лечения;
49.9. ранние эндотелиальные осложнения (синдром перегрузки жидкостью; синдром капилярной утечки; синдром синусоидальной обструкции; синдром приживления; тромботическая микроангиопатия, связанная с ТГСК; синдром сосудистой идиопатической пневмонии, включающий диффузное альвеолярное кровоизлияние, синдром гиперпроницаемости легочных капилляров и респираторный дистресс-синдром на фоне приживления трансплантата, синдром задней обратимой энцефалопатии);
49.10. синдром синусоидальной обструкции/веноокклюзионное заболевание печени (далее – ВОБ) является жизнеугрожающим осложнением после трансплантации ГСК.
Синдром обусловлен повреждением эндотелиальных клеток печени, синусов и гепатоцитов ЛП.
Факторы риска развития ВОБ печени у детей установлены согласно приложению 13;
49.11. ТА-ТМА – является тяжелым осложнением ТГСК с высоким риском летальности. Критерии для диагностики ТА-ТМА у детей приведены в приложении 14.
Полиорганная дисфункция при ТА-ТМА изложена в приложении 15.
50. К осложнениям позднего посттрансплантационного периода относятся:
50.1. хроническая РТПХ, которая может возникнуть самостоятельно (de novo) или быть продолжением острой РТПХ. Стадирование хронической РТПХ возможно также по объему и степени поражения различных органов и систем.
Оценка органного поражения при хронической РТПХ производится по шкале согласно приложению 16.
Оценка степени тяжести хронической РТПХ установлена согласно приложению 17;
50.2. посттрансплантационный лимфопролиферативный синдром (ассоциированный или не ассоциированный с ВЭБ);
- вторичные онкологические заболевания;
- персистирование смешанного химеризма, расщепленного смешанного химеризма;
- эндокринная дисфункция (нарушение полового созревания, гипотиреоз, нарушение роста);
- поражение легких (хронические обструктивные заболевания, рестриктивные заболевания);
- поражения глаз (ретинопатии, катаракта, синдром сухости);
- патология костной ткани (аваскулярные некрозы, остеопороз).
51. В случае выявления диагностических критериев ТА-ТМА без протеинурии производится отмена ингибиторов кальциневрина, сиролимуса.
52. При наличии критериев тяжелой ТА-ТМА (протеинурия > 30 мг/дл; клинические признаки синдрома полиорганной дисфункции) показано:
52.1. проведение специфической терапии экулизумабом согласно приложению 1.
52.2. терапевтический плазмообмен;
52.3. ритуксимаб, дефибротид согласно приложению 1.
53. Лечение острой РТПХ у пациента осуществляется в зависимости от стадии:
53.1. стадия I:
53.2. стадия II:
53.3. стадия более II:
ГЛАВА 10
ЛЕЧЕНИЕ ОСЛОЖНЕНИЙ ТГСК
51. В случае выявления диагностических критериев ТА-ТМА без протеинурии производится отмена ингибиторов кальциневрина, сиролимуса.
52. При наличии критериев тяжелой ТА-ТМА (протеинурия > 30 мг/дл; клинические признаки синдрома полиорганной дисфункции) показано:
52.1. проведение специфической терапии экулизумабом согласно приложению 1.
Терапия экулизумабом продолжается до разрешения гематологических проявлений ТА-ТМА и улучшения со стороны полиорганной дисфункции или отсутствия ее прогрессирования;
52.2. терапевтический плазмообмен;
52.3. ритуксимаб, дефибротид согласно приложению 1.
53. Лечение острой РТПХ у пациента осуществляется в зависимости от стадии:
53.1. стадия I:
- назначение местной терапии топическими стероидами (бетаметазон (мазь для наружного применения 0,5 мг/г, 1 мг/г), преднизолон (мазь для наружного применения 5 мг/г);
- приведение концентрации ингибиторов кальциневрина (циклоспорина, такролимуса) к целевым показателям 100–150 нг/мл (при его использовании);
53.2. стадия II:
- назначение циклоспорина или такролимуса в случае, если пациент не получал его ранее;
- приведение концентрации ингибиторов кальциневрина к целевым показателям;
- начало терапии метилпреднизолоном (стерильный порошок для приготовления раствора для инъекций 40 мг, 125 мг, 250 мг, 500 мг, 1000 мг, суспензия для инъекций 40 мг/мл 1 мл) в дозе 1–2 мг/кг/сут. внутривенно в течение 7–14 дней с 50 % редукцией дозы каждые 5–7 дней при хорошем ответе.
Пациенты с легкой формой РТПХ верхнего отдела ЖКТ могут начинать с доз метилпреднизолона 0,5–2 мг/кг/сут. внутривенно;
53.3. стадия более II:
при наличии клинически значимой РТПХ назначаются циклоспорин до достижения терапевтического уровня и метилпреднизолон внутривенно в дозе 1 мг/кг (кожная форма II степени) или 2 мг/кг (изолированная кишечная, печеночная форма либо кожная форма III степени и более; во всех случаях II стадии и более) в сутки, терапия продолжается на протяжении 14 дней. При отсутствии новых признаков РТПХ проводится постепенное снижение дозы (на 20 % от инициальной дозы в неделю). Редукция дозы производится на 0,2 мг/кг за 5 дней, далее возможен переход на альтернирующий прием в пероральной форме (таблетки 4 мг, 8 мг, 16 мг, 32 мг).
Назначаются ЛП согласно приложению 1.
возможно произвести замену циклоспорина на такролимус;
метилпреднизолон (стерильный порошок (лиофилизат) для приготовления раствора для инъекций 40 мг, 125 мг, 250 мг, 500 мг; лиофилизат для приготовления раствора для инъекций 1000 мг) 10–30 мг/кг/сут в течение 3–5 дней;
метотрексат (порошок лиофилизированный для приготовления раствора для инъекций 10 мг, 50 мг; порошок лиофилизированный для приготовления раствора для внутривенного введения (для инъекций) 1000 мг) 3–10 мг/м2 в неделю;
мезенхимальные стволовые клетки 1–2 млн/кг веса пациента еженедельно;
АТГ внутривенно в суточной дозе 20 мг/кг;
циклофосфамид (порошок для приготовления раствора для внутривенного введения (для инъекций) 200 мг, 500 мг, 1000 мг) 20 мг/кг в неделю;
экстракорпоральный фотоферез (далее – ЭКФ) – стартовый режим 16 сеансов.
54. К ЛП, применяемым для лечения хронической РТПХ, относятся:
54.1. при лимитированном процессе: топические кортикостероиды, ингибиторы кальциневрина (циклоспорин, такролимус), ЭКФ, при экстенсивном поражении обязательна комбинированная иммуносупрессивная терапия (например, ингибиторы кальциневрина с метилпреднизолоном, с ЭКФ);
54.2. лечение первой линии состоит из стероидов, назначаемых отдельно или в сочетании с ингибиторами кальциневрина. Доза метилпреднизолона не должна превышать 1 мг/кг массы тела в день.
В случае ухудшения состояния, манифестации поражения нового органа, отсутствии клинического улучшения через 1 месяц от начала терапии, невозможности редуцировать дозу преднизолона менее 1 мг/кг через 2 месяца терапии – показано добавление 3 компонента иммуносупрессии:
54.3. во всех случаях комбинированной терапии хронической РТПХ длительность лечения составляет от 3 до 6 месяцев, редукция иммуносупрессии начинается с ухода от стероидов, далее, при отсутствии повторной манифестации РТПХ, проводится постепенная отмена ингибиторов кальциневрина (на 10 % в неделю), последним отменяется третий ЛП через месяц от окончания приема ингибиторов кальциневрина при отсутствии отрицательной динамики;
ММФ (капсулы 250 мг, таблетки, покрытые оболочкой 500 мг, таблетки, покрытые кишечнорастворимой оболочкой 180 мг, 360 мг) перорально в дозе до 45 мг/кг/сут.;
возможно произвести замену циклоспорина на такролимус;
такролимус (концентрат для приготовления раствора для внутривенного введения 5 мг/мл) в суточной дозе 0,05–0,1 мг/кг; терапевтическим уровнем такролимуса, определяемым как 5–12 нг/мл, после эмпирического дозирования в зависимости от веса в размере 0,02 мг/кг в день;
метилпреднизолон (стерильный порошок (лиофилизат) для приготовления раствора для инъекций 40 мг, 125 мг, 250 мг, 500 мг; лиофилизат для приготовления раствора для инъекций 1000 мг) 10–30 мг/кг/сут в течение 3–5 дней;
метотрексат (порошок лиофилизированный для приготовления раствора для инъекций 10 мг, 50 мг; порошок лиофилизированный для приготовления раствора для внутривенного введения (для инъекций) 1000 мг) 3–10 мг/м2 в неделю;
мезенхимальные стволовые клетки 1–2 млн/кг веса пациента еженедельно;
АТГ внутривенно в суточной дозе 20 мг/кг;
циклофосфамид (порошок для приготовления раствора для внутривенного введения (для инъекций) 200 мг, 500 мг, 1000 мг) 20 мг/кг в неделю;
экстракорпоральный фотоферез (далее – ЭКФ) – стартовый режим 16 сеансов.
Используется 2 стандартных режима:
первый режим: 2 недели по 2 сдвоенных сеанса, далее – 2 недели 1 раз в неделю, далее – 1 сдвоенный сеанс в 2 недели, далее – 1 раз в месяц;
второй режим: 4 недели по 2 сдвоенных сеанса, далее – 2 недели 1 раз в неделю, далее – 1 сдвоенный сеанс в 2 недели, далее – 1 раз в месяц.
54. К ЛП, применяемым для лечения хронической РТПХ, относятся:
54.1. при лимитированном процессе: топические кортикостероиды, ингибиторы кальциневрина (циклоспорин, такролимус), ЭКФ, при экстенсивном поражении обязательна комбинированная иммуносупрессивная терапия (например, ингибиторы кальциневрина с метилпреднизолоном, с ЭКФ);
54.2. лечение первой линии состоит из стероидов, назначаемых отдельно или в сочетании с ингибиторами кальциневрина. Доза метилпреднизолона не должна превышать 1 мг/кг массы тела в день.
В случае ухудшения состояния, манифестации поражения нового органа, отсутствии клинического улучшения через 1 месяц от начала терапии, невозможности редуцировать дозу преднизолона менее 1 мг/кг через 2 месяца терапии – показано добавление 3 компонента иммуносупрессии:
ММФ в дозе 30–45 мг/кг/сут.;
циклофосфамид в дозе 200–400 мг/м2 еженедельно – при поражении суставов и (или) легких;
один из следующих ЛП: руксолитиниб, сиролимус, ибрутиниб, бортезомиб, ритуксимаб, иматиниб согласно приложению 1;
замена циклоспорина А на такролимус;
введение мезенхимальных стволовых клеток в дозе 1–2 млн/кг веса пациента (не менее 4 введений с интервалом в 1 неделю);
ЭКФ – при поражении кожи. Стартовый режим 16 сеансов. Первый режим: 2 недели по 2 сдвоенных сеанса, далее – 2 недели 1 раз в неделю, далее – 1 сдвоенный сеанс в 2 недели, далее – 1 раз в месяц. Второй режим: 4 недели по 2 сдвоенных сеанса, далее – 2 недели 1 раз в неделю, далее – 1 сдвоенный сеанс в 2 недели, далее – 1 раз в месяц;
54.3. во всех случаях комбинированной терапии хронической РТПХ длительность лечения составляет от 3 до 6 месяцев, редукция иммуносупрессии начинается с ухода от стероидов, далее, при отсутствии повторной манифестации РТПХ, проводится постепенная отмена ингибиторов кальциневрина (на 10 % в неделю), последним отменяется третий ЛП через месяц от окончания приема ингибиторов кальциневрина при отсутствии отрицательной динамики;
54.4. при присоединении бронхо-облитерирующего поражения легких к комбинированной иммуносупрессии добавляется один из ЛП: инфликсимаб, метотрексат, циклофосфамид и ЭКФ. Обязательно назначается комбинированная терапия: ингаляционные кортикостероиды, бронходилататоры, азитромицин, монтелукаст.
55. Терапия и медицинская профилактика ВОБ:
- для пациентов с легкой степенью ВОБ осуществляется медицинское наблюдение при условии тщательного мониторинга всех критериев диагностики;
- для пациентов с более тяжелой степенью ВОБ незамедлительно назначается терапия ЛП: применяется дефибротид согласно приложению 1.
56. Посттрансплантационный лимфопролиферативный синдром (ассоциированный или не ассоциированный с ВЭБ):
- редукция иммуносупрессивной терапии;
- применение ритуксимаба внутривенно согласно приложению 1 или интратекально (при поражении центральной нервной системы (далее – ЦНС) в дозе 10–30 мг в 3–10 мл физиологического раствора, вводимого еженедельно) до редукции клинической симптоматики.
57. Лечение вирусных инфекций:
57.1. лечение активной ЦМВ инфекции:
- ганцикловир (порошок лиофилизированный для приготовления раствора для инфузий 500 мг) 5 мг/кг 2 раза в сутки внутривенно до получения отрицательного результата количественной ПЦР не менее 21 дня с последующим переходом на поддерживающую дозу;
- в случае ЦМВ-пневмонии и (или) ЦМВ-энтероколита – дополнительно введение анти-ЦМВ человеческого иммуноглобулина в дозе 100 мг/кг до 5 введений с интервалом 3–5 дней;
57.2. лечение ВК-вирусной инфекции:
- снижение иммуносупрессии;
- внутривенное назначение человеческого иммуноглобулина (от 0,3 до 0,6 г/кг/сут., суммарная доза от 0,5 до 2,0 г/кг);
57.3. лечение JC-вирус инфекции: коррекция (снижение) иммуносупрессивной терапии;
57.4. лечение ВЭБ инфекции: уменьшение иммуносупрессии, при ВЭБ-виремии с концентрацией > 1000 копий ДНК ВЭБ/мл – ритуксимаб 375 мг/м2 один раз в неделю (1–4 дозы) до получения отрицательного результата ПЦР сыворотки крови;
57.5. лечение ВГЧ-6 инфекции – используется один из ЛП:
- ганцикловир (порошок лиофилизированный для приготовления раствора для инфузий 500 мг) по 5 мг/кг 2 раза в сутки внутривенно до исчезновения клинических проявлений и получения одного отрицательного результата количественной ПЦР, длительность терапии – не менее 2 недель;
- валганцикловир (таблетки, покрытые оболочкой, 450 мг), у детей до 16 лет доза (мг) = 7 х площадь тела в м2 х клиренс по эндогенному креатинину или 16 мг/кг 2 раза в сутки, но не более 900 мг в сутки, старше 16 лет – 900 мг 2 раза в сутки (за исключением пациентов с тяжелой желудочно-кишечной РТПХ) – 21 день;
57.6. лечение ВПГ-1,2 инфекции: ацикловир (порошок лиофилизированный для приготовления раствора для инфузий 250 мг, 500 мг, 1000 мг) внутривенно 10–15 мг/кг каждые 8 часов в виде медленной инфузии в течение 10–14 дней до получения двух последовательных отрицательных результатов ПЦР;
57.7. лечение ВЗВ инфекции:
ацикловир внутривенно 10–15 мг/кг каждые 8 часов в виде медленной инфузии в течение 7–14 дней до получения отрицательного результата ПЦР сыворотки крови;
57.8. лечение парвовирусной В19 инфекции: внутривенный иммуноглобулин в суммарной дозе 1–2 г/кг за 2–3 введения.
58. Антибактериальная терапия включает стартовую терапию с дальнейшей коррекцией в зависимости от инфекционного статуса пациента и результатов лабораторной диагностики:
58.1. стартовую терапию неосложненных эпизодов фебрильной нейтропении (однократное повышение температуры тела выше 38,5 °С при содержании нейтрофилов крови менее 1 х 109 клеток в литре или двукратное повышение температуры тела выше 38 °С, измеренной с интервалом в 1 час при содержании нейтрофилов крови менее 0,5 х 109 или менее 1 х 109 клеток в литре с тенденцией к дальнейшему снижению их количества) проводят β-лактамным антибиотиком широкого спектра действия с антипсевдомонадной активностью: цефалоспорины 3–4 поколения, карбапенемы (за исключением эртапенема) или защищенные пенициллины с антипсевдомонадной активностью согласно приложению 18;
58.2. дальнейший выбор схемы лечения определяется источником инфекции, предшествующей колонизацией резистентными бактериями (например, метициллин-резистентный золотистый стафилококк, ванкомицин-резистентные энтерококки, микроорганизмы продуценты β-лактамаз расширенного спектра, в том числе карбапенемаза-продуцирующие штаммы Klebsiella pneumoniae), клинической картиной инфекционного эпизода.
Режимы дозирования антимикробных ЛП установлены согласно приложению 18.
59. Лечение грибковых инфекций:
ЛП выбора для терапии инвазивного аспергиллеза являются: вориконазол или изавуконазол (off-lable):
изавуконазол (в форме лиофилизата для приготовления раствора для инфузий 200 мг). Нагрузочная доза составляет 200 мг 3 раза в день в течение 2 дней, затем 200 мг 1 раз в день внутривенно. Альтернативными ЛП для терапии инвазивного аспергиллеза являются: посаконазол, амфотерицин В (липидная форма).
ЛП выбора для терапии мукормикоза является амфотерицин В (липидная форма).
Альтернативными ЛП являются: посаконазол, изавуконазол. При терапии мукормикоза приоритетом является хирургическая санация пораженных тканей.
ЛП выбора для терапии инвазивного кандидоза и кандидемии являются эхинокандины. Альтернативные ЛП – флуконазол или амфотерицин В (липидная форма).
При фунгемии, вызванной дрожжевыми грибами, необходимо удаление и (или) замена всех искусственных устройств (сосудистых катетеров, зондов, дренажей и т.д.).
При инвазивном кандидозе или кандидемии приемлемо назначение эхинокандинов на 10 дней с последующим переходом на терапию флуконазолом в лечебной дозе в случае клинически стабильного состояния пациента.
ЛП выбора для терапии фузариоза являются: посаконазол, амфотерицин В (липидная форма). Альтернативными ЛП являются: вориконазол или изавуконазол.
Упреждающая противогрибковая терапия продолжается до исчезновения очагов и (или) признаков инфекции. Далее на период нейтропении проводится вторичная медицинская профилактика. При неэффективности (ухудшение по данным визуализирующих методов, клинически) отменяется не позднее 14 дней с момента назначения. Режимы дозирования противогрибковых ЛП установлены согласно приложению 19.
60. При неосложненном течении после алло-ТГСК выписка пациента из отделения трансплантации осуществляется на 30–40 сутки после ТГСК, при развитии трансплантат-зависимых осложнений – после их купирования.
61. Медицинские осмотры и диагностические исследования с коррекцией иммуносупрессивной и другой поддерживающей терапии осуществляются в отделении осложнений – в консультативно-поликлиническом отделении государственного учреждения «Республиканский научно-практический центр детской онкологии, гематологии и иммунологии» согласно приложению 20.
62. Для осуществления медицинского наблюдения в амбулаторных условиях необходимо:
63. Вакцинация рекомендуется всем пациентам через 9–18 месяцев после ТГСК при отмене иммуносупрессивной терапии и удовлетворительной иммунореконституции (по данным иммунофенотипирования), при условии отсутствия проявлений острой или хронической РТПХ (при явлениях хронической РТПХ – по решению врачебного консилиума с участием врача-инфекциониста) и при достижении минимальной иммунореконституции (количество В клеток > 50–100/мкл, количество CD4 + > 200/мкл).
64. Медицинскими противопоказаниями к вакцинации являются:
Временным медицинским противопоказанием к вакцинации является острая респираторная вирусная инфекция (через месяц после выздоровления допустима вакцинация). Вакцинация живыми вакцинами противопоказана.
ГЛАВА 11
МЕДИЦИНСКОЕ НАБЛЮДЕНИЕ ПАЦИЕНТА В АМБУЛАТОРНЫХ УСЛОВИЯХ, ВАКЦИНАЦИЯ
60. При неосложненном течении после алло-ТГСК выписка пациента из отделения трансплантации осуществляется на 30–40 сутки после ТГСК, при развитии трансплантат-зависимых осложнений – после их купирования.
61. Медицинские осмотры и диагностические исследования с коррекцией иммуносупрессивной и другой поддерживающей терапии осуществляются в отделении осложнений – в консультативно-поликлиническом отделении государственного учреждения «Республиканский научно-практический центр детской онкологии, гематологии и иммунологии» согласно приложению 20.
62. Для осуществления медицинского наблюдения в амбулаторных условиях необходимо:
- удовлетворительное соматическое состояние пациента;
- стабильный уровень лейкоцитов более 1000/мкл, нейтрофилов более 500/мкл, тромбоцитов более 20 000/мкл;
- отсутствие геморрагического синдрома;
- энтеральный прием ЛП, в том числе иммуносупрессивных, пищи.
63. Вакцинация рекомендуется всем пациентам через 9–18 месяцев после ТГСК при отмене иммуносупрессивной терапии и удовлетворительной иммунореконституции (по данным иммунофенотипирования), при условии отсутствия проявлений острой или хронической РТПХ (при явлениях хронической РТПХ – по решению врачебного консилиума с участием врача-инфекциониста) и при достижении минимальной иммунореконституции (количество В клеток > 50–100/мкл, количество CD4 + > 200/мкл).
64. Медицинскими противопоказаниями к вакцинации являются:
- наличие инфекционных осложнений в течение 14 дней до вакцинации;
- индивидуальная непереносимость вакцины или ее компонентов в анамнезе;
- наличие клинических признаков активации РТПХ.
Временным медицинским противопоказанием к вакцинации является острая респираторная вирусная инфекция (через месяц после выздоровления допустима вакцинация). Вакцинация живыми вакцинами противопоказана.
Информация
Источники и литература
-
Постановления и приказы Министерства здравоохранения Республики Беларусь об утверждении клинических протоколов 2025
-
www.minzdrav.gov.by
Информация
ПОСТАНОВЛЕНИЕ МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ
РЕСПУБЛИКИ БЕЛАРУСЬ
16 октября 2025 г. № 151
Об утверждении клинического протокола
На основании абзаца девятого части первой статьи 1 Закона Республики Беларусь от 18 июня 1993 г. № 2435-XII «О здравоохранении», подпункта 8.3 пункта 8 и подпункта 9.1 пункта 9 Положения о Министерстве здравоохранения Республики Беларусь, утвержденного постановлением Совета Министров Республики Беларусь от 28 октября 2011 г. № 1446, Министерство здравоохранения Республики Беларусь
ПОСТАНОВЛЯЕТ:
1. Утвердить клинический протокол «Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами».
2. Настоящее постановление вступает в силу после его официального опубликования.
Министр А.В.Ходжаев
СОГЛАСОВАНО
Брестский областной исполнительный комитет
Витебский областной исполнительный комитет
Гомельский областной исполнительный комитет
Гродненский областной исполнительный комитет
Могилевский областной исполнительный комитет
Минский областной исполнительный комитет
Минский городской исполнительный комитет
Приложение 1
ЛП, назначаемые по решению врачебного консилиума (в том числе off-lable) для лечения пациентов с ПИД
ШКАЛА
Приложение 1
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
ЛП, назначаемые по решению врачебного консилиума (в том числе off-lable) для лечения пациентов с ПИД
|
№ п/п
|
Название ЛП |
Медицинские показания к назначению пациентам с ПИД
|
Лекарственная форма, способ применения, продолжительность применения
|
| 1 |
Экулизумаб, концентрат
для приготовления раствора для инфузий 10 мг/1 мл 30 мл
|
Лечение ТМА |
Рекомбинантное гуманизированное моноклональное антитело, которое связывается с компонентом С5 комплемента человека.
Нагрузочная доза:
вес пациента менее 10 кг – 300 мг каждые 72 часа не менее 5 доз;
вес пациента от 10 до 39 кг – 600 мг каждые 72 часа не менее 5 доз;
вес пациента более 40 кг – 900 мг каждые 72 часа не менее 5 доз.
Терапия индукции:
вес пациента менее 10 кг – 300 мг – 1 раз в неделю не менее 4 доз;
вес пациента от 10 до 39 кг – 600 мг – 1 раз в неделю не менее 4 доз;
вес пациента более 40 кг – 900 мг – 1 раз в неделю не менее 4 доз.
Поддерживающая терапия:
вес пациента менее 10 кг – 300 мг – 1 раз в 2 недели не менее 2 доз;
вес пациента более 10 кг – 300 мг – 1 раз в неделю не менее 4 доз.
Снижение терапии:
вес пациента от 10 до 20 кг – самая низкая доза 300 мг;
вес пациента > 20 кг – самая низкая доза 600 мг 1 раз в неделю две дозы
|
| 2 |
Дефибротид,
раствор для инъекций, 200 мг/2,5 мл – 2,5 мл
|
Лечение эндотелиальных осложнений
|
25 мг/кг/сут., разделить на 4 введения, внутривенно в течение 2 часов каждые 6 часов в течение 21 дня
|
| 3 |
Инфликсимаб, порошок лиофилизированный для приготовления концентрата,
для приготовления раствора, для внутривенного введения (лиофилизат для приготовления раствора для инфузий), 100 мг
|
Для лечения острой и хронической РТПХ
|
Ингибитор фактора некроза опухоли-альфа (ФНО-альфа).
Разовая доза – 3–10 мг/кг. Частота и длительность применения
устанавливаются индивидуально
|
| 4 |
Сиролимус, таблетки по 1 мг
|
Для лечения острой и хронической РТПХ
|
Ингибиторы mTOR.
Стартовая доза 6 мг 1 раз в сутки, далее – по 2 мг 1 раз в сутки. У детей массой менее 40 кг стартовая доза 3 мг/м2, далее – 1 мг/м2.
Коррекция дозы осуществляется индивидуально под контролем концентрации препарата в сыворотке крови.
Целевая концентрация от 4 нг/мл до 12 нг/мл. Назначают с дня –3 с постепенной отменой при отсутствии РТПХ.
Длительность терапии определяется врачом-специалистом
|
| 5 |
Руксолитиниб, таблетки по 5 мг, 15 мг, 20 мг
|
Для лечения и профилактики острой и хронической РТПХ, стероид-резистентной формы РТПХ
|
Селективный ингибитор JAK-киназ.
Профилактика: в суточной дозе 4–7,5 мг/м2 (распределение в 2 приема) под контролем гематологических показателей с возможным дальнейшим увеличением дозы.
Лечение: 2,5 мг 2 раза в сутки при МТ менее 25 кг, 5 мг 2 раза в сутки при МТ более 25 кг, максимальная доза 10 мг 2 раза в сутки при отсутствии токсического эффекта и для детей старше 12 лет. Или же дозирование в зависимости от поверхности тела (12,6 мг/м2/день)
|
| 6 |
Ритуксимаб, концентрат для приготовления раствора для инфузий 10 мг/мл
|
Для профилактики, лечения острой и хронической РТПХ,
ТМА, посттрансплантационного лимфопролиферативного синдрома
|
Химерные моноклональные антитела.
Приготовленный раствор ритуксимаба вводится внутривенно капельно через отдельный катетер. Раствор нельзя вводить внутривенно струйно или болюсно.
Режим дозирования устанавливается индивидуально.
Рекомендуемая стартовая доза 1 раз в неделю – 375 мг/м2
|
| 7 |
Бортезомиб, лиофилизат для приготовления раствора для внутривенного
и подкожного введения 2 мг, 3.5 мг
|
Для профилактики и лечения острой и хронической РТПХ
|
Высокоселективный обратимый ингибитор активности протеасомы 26S.
Профилактика: дозирование 1–1,5 мг/м2 внутривенно в дни +1, +4, +7
Лечение: 0,2–1,5 мг/м2 еженедельно (максимум 8 введений под контролем неврологического статуса)
|
| 8 |
Тоцилизумаб, концентрат для приготовления раствора для инфузий по 80 мг, 20 мг и 400 мг во флаконе по 4 мл, 10 мл, 20 мл
|
Для профилактики и лечения острой РТПХ
|
Рекомбинантное гуманизированное моноклональное антитело к человеческому рецептору интерлейкина-6 (далее – ИЛ-6) из подкласса иммуноглобулинов IgG1.
Рекомендуемая стартовая доза 8 мг/кг 1 раз в 3–4 недели внутривенно капельно, но не более 800 мг на одну инфузию
|
| 9 |
Ведолизумаб, порошок для приготовления концентрата для приготовления раствора для инфузий 60 мг/мл – 5 мл
|
Для профилактики и лечения острой РТПХ
|
Гуманизированное моноклональное антитело.
100 мг для детей с массой < 10 кг, 150 мг для детей с массой 10–25 кг на –1, +13 и далее каждые 28 дней, всего до 7 введений
|
| 10 |
Иматиниб, таблетки, покрытые пленчатой оболочкой, по 100 мг, 400 мг
|
Для лечения хронической РТПХ
|
Ингибитор тирозинкиназы 100–200–260 мг/м2 в день
|
| 11 |
Базиликсимаб, лиофилизат для приготовления концентрата для приготовления раствора для инфузий 20 мг/мл – 5 мл
|
Для лечения острой РТПХ |
Гуманизированное моноклональное антитело.
20 мг в сутки при массе более 35 кг, 10 мг в сутки при массе менее 35 кг, три последовательных введения (на дни 1, 4, 8), далее при необходимости – повторное введение через 7 дней
|
Приложение 2
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
ШКАЛА
оценки соматического состояния пациента, индекс Карновского, %
ШКАЛА
|
№ п/п
|
Параметры | Проценты | Степень нарушения |
| 1 |
Нормальная физическая активность, пациент не требует специального ухода
|
100 | Нормальная активность, нет симптомов болезни |
| 90 | Нормальная активность, легкие симптомы болезни | ||
| 80 |
Нормальная активность, достигается с напряжением, средние симптомы болезни
|
||
| 2 |
Нормальная физическая активность невозможна, хотя пациент вполне независим
|
70 |
Независимость, но неспособность к нормальной активности или работе
|
| 60 |
Периодически необходима помощь, но, в основном, пациент независим
|
||
| 50 | Часто необходима поддержка и медицинский уход | ||
| 3 |
Независимость невозможна, необходимы длительное лечение и уход
|
40 |
Пациент прикован к постели, нуждается в специальном уходе и лечении
|
| 30 |
Постоянно прикован к постели, показана госпитализация, но терминальный кризис не угрожает
|
||
| 20 |
Тяжело болен, необходима госпитализация и активная поддерживающая терапия
|
||
| 10 |
Терминальная стадия, быстрое прогрессирование заболевания
|
||
| 0 | Смерть |
Приложение 3
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
ШКАЛА
оценки соматического состояния пациента, индекс Ланского (для пациентов до 18 лет)
ПЕРЕЧЕНЬ
|
№ п/п
|
Проценты | Общее состояние |
| 1 | 100 | Нормальная активность, нет симптомов заболевания |
| 2 | 90 | Небольшое ограничение физической активности, требующей усилий |
| 3 | 80 | Активный, но быстро утомляется |
| 4 | 70 | Значительное ограничение физической активности, уменьшение времени активных игр |
| 5 | 60 |
Играет, но участие в активных играх минимальное, продолжает заниматься спокойными играми
|
| 6 | 50 | Не играет в активные игры, но участвует в спокойных играх |
| 7 | 40 | В основном находится в кровати, иногда принимает участие спокойных играх |
| 8 | 30 | Находится только в кровати, необходима помощь даже в спокойных играх |
| 9 | 20 | Часто спит, игры вовсе ограничены очень пассивным участием |
| 10 | 10 | Не играет, не встает с постели |
| 11 | 0 | Не реагирует на внешние раздражители |
Приложение 4
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
ПЕРЕЧЕНЬ
консультаций врачей-специалистов и медицинские показания для их проведения реципиентам ГСК
Миелоаблативные режимы кондиционирования (стандартные)
Приложение 6
РЕЖИМЫ
|
№ п/п
|
Врач-специалист | Медицинские показания | Примечание |
| 1 |
Врач-анестезиолог-реаниматолог детский
|
Установка центрального венозного катетера
|
|
| 2 | Врач-гастроэнтеролог |
При наличии подозрений на ВЗК, энтеропатию
|
|
| 3 | Врач-акушер-гинеколог |
Меноррагии, врачебная консультация при назначении комбинированных оральных контрацептивов
|
|
| 4 | Врач-дерматовенеролог | Кожный синдром | |
| 5 | Врач-инфекционист | ||
| 6 | Врач – детский кардиоревматолог |
Артериальная гипертензия, хроническая сердечная недостаточность, нарушения сердечного ритма и проводимости
|
|
| 7 | Врач – детский невролог |
Менингит, энцефалит, в анамнезе судороги, другие неврологические нарушения
|
|
| 8 | Врач-нефролог | Почечная недостаточность | |
| 9 | Врач-оториноларинголог |
Диагностика и лечение воспалительных заболеваний придаточных пазух носа и среднего уха
|
Всем пациентам |
| 10 | Врач-офтальмолог |
Нарушения зрения, воспалительные заболевания глаза и придатков
|
Всем пациентам |
| 11 | Врач – детский хирург |
Анальная трещина, парапроктит, хирургические осложнения (инфекционные, геморрагические)
|
Всем пациентам |
| 12 | Психолог | Депрессия, анорексия, иное | |
| 13 | Врач-ревматолог | Синдром Свита | |
| 14 | Врач-трансфузиолог |
Для подбора трансфузионных сред при положительном непрямом антиглобулиновом тесте, неэффективности трансфузий, отягощенном трансфузионном анамнезе
|
|
| 15 | Врач-фтизиатр |
Подозрение на туберкулез, осложнение вакцинацией БЦЖ
|
|
| 16 | Врач – челюстно-лицевой хирург |
Инфекционно-воспалительные заболевания зубочелюстной системы
|
Приложение 5
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
Миелоаблативные режимы кондиционирования (стандартные)
|
№ п/п
|
Режим (международная аббревиатура)
|
ЛП | Форма выпуска |
Суточная доза; разовая доза
|
Общая доза |
Способ и кратность введения
|
Сутки до ТГСК |
| 1 | Bu/Flu | Бусульфан |
Концентрат для приготовления раствора для внутривенного введения 50 мг/2 мл
|
4 мг/кг;
1 мг/кг
|
16 мг/кг |
внутривенно за 2 часа 4 раза в сутки, 4 дня (16 введений)
|
8, 7, 6, 5, или 5, 4, 3, 2
|
| Флударабин |
Порошок лиофилизированный для приготовления раствора для инъекций (лиофилизированный порошок для приготовления раствора для внутривенного введения) 50 мг
|
40 мг/м2 | 160 мг/м2 |
4 дня 1 раз в сутки за 30 минут внутривенно
|
6, 5, 4, 3, или день 5, 4, 3, 2
|
||
| 2 | Bu/Flu/Mel | Бусульфан |
Концентрат для приготовления раствора для внутривенного введения 50 мг/2 мл
|
4 мг/кг;
1 мг/кг
|
16 мг/кг |
внутривенно за 2 часа 4 раза в сутки, 4 дня (16 введений)
|
8, 7, 6, 5 |
| Флударабин |
Порошок лиофилизированный для приготовления раствора
для инъекций (лиофилизированный порошок
для приготовления раствора для внутривенного введения)
50 мг
|
30 мг/м2 | 150 мг/м2 |
5 дней 1 раз в сутки за 30 минут внутривенно
|
6, 5, 4, 3 | ||
| Мелфалан |
Лиофилизат для приготовления раствора для внутрисосудистого введения 50 мг
|
140 мг/м2 | 140 мг/м2 |
Однократно за 30 минут внутривенно
|
3 или 2 | ||
| 3 | Bu/Flu/TIT | Бусульфан |
Концентрат для приготовления раствора для внутривенного введения 50 мг/2 мл
|
4 мг/кг;
1 мг/кг
|
16 мг/кг |
внутривенно за 2 часа 4 раза в сутки, 4 дня (16 введений)
|
8, 7, 6, 5 |
| Флударабин |
Порошок лиофилизированный для приготовления раствора для инъекций (лиофилизированный порошок для приготовления раствора для внутривенного введения) 50 мг
|
30 мг/м2 | 150 мг/м2 |
5 дней 1 раз в сутки за 30 минут внутривенно
|
6, 5, 4, 3 | ||
| Тиотепа* | 5–10 мг/кг | 5–10 мг/кг |
2 раза в сутки через 12 часов внутривенно за 1 час
|
3 или 2 | |||
| 4 | Treo/Flu/Mel | Треосульфан | Порошок для приготовления раствора для инфузий 1000 мг | 14 г/м2 или 12 г/м2 |
42 г/м2 или 36 г/м2
|
3 дня 1 раз в сутки за 2 часа
|
7, 6, 5 |
| Флударабин |
Порошок лиофилизированный для приготовления раствора для инъекций (лиофилизированный порошок для приготовления раствора для внутривенного введения) 50 мг
|
30 мг/м2 | 150 мг/м2 |
5 дней 1 раз в сутки за 30 минут внутривенно
|
6, 5, 4, 3 | ||
| Мелфалан |
Лиофилизат для приготовления раствора
для внутрисосудистого введения 50 мг
|
140 мг/м2 | 140 мг/м2 |
Однократно за 30 минут внутривенно
|
3 или 2 | ||
| 5 | Treo/Flu/TIT | Треосульфан | Порошок для приготовления раствора для инфузий 1000 мг | 14 г/м2 или 12 г/м2 |
42 г/м2 или
36 г/м2
|
3 дня 1 раз в сутки за 2 часа
|
7, 6, 5 |
| Флударабин |
Порошок лиофилизированный для приготовления раствора для инъекций (лиофилизированный порошок для приготовления раствора для внутривенного введения) 50 мг
|
30 мг/м2 | 150 мг/м2 |
5 дней 1 раз в сутки за 30 минут внутривенно
|
6, 5, 4, 3 | ||
| Тиотепа* | Порошок для инфузий 15 мг, 100 мг |
5 мг/кг 2 раза в сутки
|
10 мг/кг |
2 раза в сутки через 12 часов внутривенно за 1 час
|
3 или 2 |
______________________________
* Off-lable.
Приложение 6
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
РЕЖИМЫ
со сниженной интенсивностью кондиционирования
|
№ п/п
|
Режим (международная аббревиатура) | ЛП | Форма выпуска |
Суточная доза; разовая доза*
|
Общая доза |
Способ и кратность введения
|
Сутки до ТГСК |
| 1 | Flu/Mel | Флударабин |
Порошок лиофилизированный для приготовления раствора для инъекций (лиофилизированный порошок для приготовления раствора для внутривенного введения) 50 мг
|
30 мг/м2 | 150 мг/м2 |
5 дней 1 раз в сутки за 30 минут внутривенно
|
7, 6, 5, 4, 3 |
| Мелфалан |
Лиофилизат для приготовления раствора для внутрисосудистого введения 50 мг
|
140 мг/м2 | 140 мг/м2 |
Однократно за 30 минут внутривенно
|
2 | ||
| 2 | Treo/Flu | Треосульфан | Порошок для приготовления раствора для инфузий 1000 мг | 14 г/м2 или 12 г/м2 |
42 г/м2 или
36 г/м2
|
3 дня 1 раз в сутки за 2 часа
|
7, 6, 5 |
| Флударабин |
Порошок лиофилизированный для приготовления раствора для инъекций (лиофилизированный порошок для приготовления раствора для внутривенного введения) 50 мг
|
30 мг/м2 | 150 мг/м2 |
5 дней 1 раз в сутки за 30 минут внутривенно
|
7, 6, 5, 4, 3 | ||
| 3 | Bu/Flu | Бусульфан* |
Концентрат для приготовления раствора для внутривенного введения 50 мг/2 мл
|
внутривенно за 2 часа 4 раза в сутки, 4 дня подряд (16 введений)
|
5, 4, 3, 2 | ||
| Флударабин |
Порошок лиофилизированный для приготовления раствора для инъекций (лиофилизированный порошок для приготовления раствора для внутривенного введения) 50 мг
|
45 мг/м2 | 180 мг/м2 |
5 дней 1 раз в сутки за 30 минут внутривенно
|
7, 6, 5, 4 | ||
| 4 | Flu/Cy | Флударабин |
Порошок лиофилизированный для приготовления раствора для инъекций (лиофилизированный порошок для приготовления раствора для внутривенного введения) 50 мг
|
30 мг/м2 | 120–150 мг/м2 |
4–5 дней 1 раз в сутки за 30 минут внутривенно
|
9, 8, 7, 6, 5 |
| Циклофосфан | порошок для внутривенно инъекций | 5–10 мг/кг | 20–40 мг/кг |
4 дня 1 раз в сутки за 1 час
|
5, 4, 3, 2 |
______________________________
* Расчет дозы бусульфана проводится на килограмм веса тела, а не по возрасту.
Расчет дозы Бусульфана (Bu) у пациентов от 0 до 17 лет при немиелоаблативном режиме кондиционирования
Достигнутая доза бусульфана рассчитывается по следующей формуле:
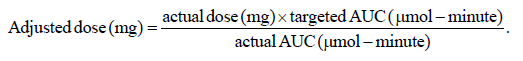
| Фактическая масса тела реципиента (кг) | Разовая доза BU (мг/кг/сут.) |
| 3-15 | 5,1 |
| 15-25 | 4,9 |
| 25-50 | 4,1 |
| 50-75 | 3,3 |
| 75-100 | 2,7 |
Терапевтический диапазон для равновесной концентрации бусульфана составляет 600–1000 нг/мл в случае миелоаблативного режима кондиционирования.
Мониторинг дозы бусульфана внутривенного осуществляется для контроля достижения целевой концентрации.
Достигнутая доза бусульфана рассчитывается по следующей формуле:
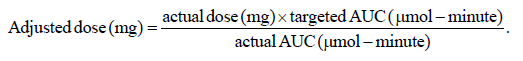
Расчет дозы Бусульфана (Bu) у новорожденных, детей и подростков (от 0 до 17 лет) при немиелоаблативном режиме кондиционирования
ЛП, применяемые для медицинской профилактики грибковых инфекций
АЛГОРИТМ
| Фактическая масса тела реципиента (кг) | Разовая доза BU (мг/кг/сут.) |
| 3-15 | 3,5 |
| 15-25 | 3,2 |
| 25-50 | 2,8 |
| 50-75 | 2,2 |
| 75-100 | 1,8 |
Приложение 7
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
ЛП, применяемые для медицинской профилактики грибковых инфекций
|
№ п/п
|
Медицинские показания | Возраст пациента | Наименование ЛП | Способ применения | Срок назначения |
| 1 |
Алло-ТГСК в фазу нейтропении, без РТПХ/с РТПХ < 2 ст.
|
От 0 до 18 лет | Флуконазол |
5–8 мг/кг 1 раз в сутки внутривенно или внутрь (максимальная доза 400 мг в сутки) ежедневно
|
Весь период нейтропении, до 75 дней после ТГСК
|
| От 2 до 14 лет (весом < 50 кг) | Вориконазол | 8 мг/кг 2 раза в сутки внутривенно | |||
|
От 12 до 18 лет (весом > 50 кг) при кишечной форме РТПХ или невозможности энтерального приема
|
Вориконазол | 4 мг/кг 2 раза в сутки внутривенно | |||
| От 0 до 2 лет | Микафунгин | 1 мг/кг 1 раз в сутки внутривенно | |||
| Каспофунгин |
50 (70) мг/м2 1 раз в сутки внутривенно капельно
|
||||
| От 0 до 18 лет | Амфоморонал | 100 мг/мл 1–5 мл 4 раза в сутки | |||
| 2 | Алло-ТГСК с РТПХ > 2 ст. | От 0 до 2 лет | Микафунгин | 1 мг/кг 1 раз в сутки внутривенно | На период иммуносупрессии |
| От 2 до 14 лет (весом < 50 кг) | Вориконазол | 8 мг/кг 2 раза в сутки внутривенно | |||
|
От 12 до 18 лет (весом > 50 кг) при кишечной форме РТПХ или невозможности энтерального приема
|
Вориконазол | 4 мг/кг 2 раза в сутки внутривенно | |||
|
От 12 до 18 лет без кишечной формы
РТПХ
|
Посаконазол | 200 мг 3 раза в сутки внутрь | |||
| 3 |
Хроническая гранулематозная болезнь (до ТГСК)
|
От 0 до 18 лет | Итраконазол |
2,5 мг/кг 2 раза в сутки (максимальная доза 200 мг в сутки) внутрь
|
Ежедневно |
| 4 |
Хроническая гранулематозная болезнь (после ТГСК)
|
Смотри aлло-ТГСК с РТПХ > 2 ст. |
День 0 и далее весь период нейтропении
|
||
Приложение 8
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
АЛГОРИТМ
выбора трансфузионной среды при несовместимости в системе АВО
Рекомендуемая клеточность трансплантата
Клиническая классификация стадий острой РТПХ
Система органного стадирования острой РТПХ
Классификация острой и хронической РТПХ
ФАКТОРЫ
|
№ п/п
|
Несовместимость пары «донор-реципиент» в системе АВО
|
Группа крови реципиента
|
Группа крови донора
|
Эритроциты |
Тромбоциты и плазма
|
| 1 | Большая | 0 | А | 0 | А, АВ |
| 0 | В | 0 | В, АВ | ||
| 0 | АВ | 0 | АВ | ||
| А | АВ | А, 0 | АВ | ||
| В | АВ | В, 0 | АВ | ||
| 2 | Малая | А | 0 | 0 | А, АВ |
| В | 0 | 0 | В, АВ | ||
| АВ | 0 | 0 | АВ | ||
| АВ | А | А, 0 | АВ | ||
| АВ | В | В, 0 | АВ | ||
| 3 | Большая с малой | А | В | 0 | АВ |
| В | А | 0 | АВ |
Приложение 9
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
Рекомендуемая клеточность трансплантата
|
№ п/п
|
Источник трансплантата | Режим кондиционирования | Клеточность трансплантата |
| 1 | Костный мозг | ЯСК 3 х 108/кг | |
| 2 | ПСКК |
Миелоаблативные режимы кондиционирования
|
CD34+ более 2 х 106/кг |
| CD34+ оптимально более 4 х 106/кг | |||
|
Режимы со сниженной интенсивностью кондиционирования
|
CD34+ более 2 х 106/кг | ||
| CD34+ оптимально 4–8 х 106/кг | |||
| 3 | ПК | HLA 4–6/6 | ЯСК более 2,5–3 х 107/кг |
| CD34+ более 1 х 105/кг |
Приложение 10
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
Клиническая классификация стадий острой РТПХ
|
№ п/п
|
Стадия РТПХ | Степень поражения | ||
| Кожа | Печень | ЖКТ | ||
| 1 | I – легкая | 1-2 | 0 | 0 |
| 2 | II – умеренная | 1-3 | 1 | 1 |
| 3 | III – тяжелая | 2-3 | 2-3 | 2-3 |
| 4 | IV – угрожающая жизни | 2-4 | 2-4 | 2-4 |
Приложение 11
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
Система органного стадирования острой РТПХ
|
№ п/п
|
Степень | Пораженный орган | ||
| Кожа |
Печень (уровень билирубина)
|
ЖКТ | ||
| 1 | 1 |
Макуло-папуллезная сыпь < 25% поверхности тела
|
34–50 ммоль/л | Диарея > 500 мл |
| 2 | 2 |
Макуло-папуллезная сыпь 25–50% поверхности тела
|
51–102 ммоль/л | Диарея > 1000 мл |
| 3 | 3 | Генерализованная эритродермия | 103–255 ммоль/л | Диарея > 1500 мл |
| 4 | 4 |
Генерализованная эритродермия с буллезными образованиями и десквамацией эпителия
|
> 255 ммоль/л |
Сильная боль в животе с или без непроходимости
|
Приложение 12
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
Классификация острой и хронической РТПХ
| № п/п |
Категории РТПХ
|
Манифестация симптомов – срок после ТГСК
|
Наличие признаков острой РТПХ
|
Наличие признаков хронической РТПХ
|
| 1 | Классическая острая РТПХ | < 100 дней или менее | Да | Нет |
| 2 |
Персистирующая, возобновляющаяся или поздняя острая РТПХ
|
> 100 дней | Да | Нет |
| 3 | Хроническая РТПХ |
Нет временных ограничений
|
Нет | Да |
| 4 |
Синдром перекреста острой и хронической РТПХ
|
Нет временных ограничений | Да | Да |
Приложение 13
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
ФАКТОРЫ
риска развития ВОБ печени у детей
ДИАГНОСТИКА ТА-ТМА*
Приложение 15
Полиорганная дисфункция при ТА-ТМА
ШКАЛА
| Критерии | |
| Немодифицируемые | Модифицируемые |
|
Вторая ТГСК
Предшествующая ВОБ
Прогрессирование основного заболевания
Злокачественный инфантильный остеопетроз, врожденные синдромы активации макрофагов, ювенильный миеломоноцитарный лейкоз, нейробластома
Генетические факторы
Дети до 2 лет
Повышение трансаминаз > 2,5 норм до ТГСК
Индекс Карновского менее 90 %
Метаболический синдром
Прием эстрогенов
Предшествующий прием гемтузумаб озогамицина или инотузумаб озогамицина, других моноклональных антител
Прием гепатотоксичных ЛП
Перегрузка железом
Уровень билирубина > 26 ммоль/л до ТГСК
Предшествующее заболевание печени: фиброз, цирроз, активный вирусный гепатит
Облучение брюшной полости или печени
|
Кондиционирование:
миелоаблативные режимы;
использование бусульфана;
высокодозный треосульфан;
тотальное облучение тела.
Донор:
неродственный совместимый;
частично-совместимый.
Медицинская профилактика РТПХ:
сиролимус + метотрексат + такролимус;
метотрексат + циклоспорин или такролимус.
Трансплантат без манипуляций
Нутритивная поддержка: парентеральное питание
|
Приложение 14
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
ДИАГНОСТИКА ТА-ТМА*
|
№ п/п
|
Признаки ТА–ТМА | Симптомы |
| 1 |
Анемия, определяемая как один из симптомов
|
Неспособность достичь трансфузионной независимости, несмотря на приживление нейтрофилов; снижение гемоглобина на 1 г/дл; вновь возникшая трансфузионная зависимость
|
| 2 |
Тромбоцитопения, определяемая как один из симптомов:
|
Неспособность достичь приживления тромбоцитов; более высокая, чем ожидалось, потребность в трансфузии; рефрактерность к переливанию тромбоцитов; снижение количества тромбоцитов на 50 % после полного приживления (восстановления) тромбоцитов
|
| 3 |
Уровень ЛДГ, превышающий верхнюю границу нормы
|
|
| 4 | Шизоциты в ОАК | |
| 5 | Артериальная гипертензия |
(> 99 процентиля для возраста < 18 лет) или систолическое АД > 140 мм рт. ст, или диастолическое АД > 90 мм рт. ст. > 18 лет
|
| 6 |
Растворимый C5b-9 (sC5b-9) превышает верхнюю границу нормы
|
|
| 7 | Протеинурия | Отношение белка к креатинину мочи [rUPCR]) > 1 мг/мг |
______________________________
* Пациенты с любым из следующих признаков имеют повышенный риск безрецидивной смертности и должны быть стратифицированы как ТА-ТМА высокого риска [hrTA-TMA]:
повышенный уровень sC5b-9;
ЛДГ в 2 раза выше верхней границы нормы;
rUPCR > 1 мг/мг;
любая органная дисфункция, развивающаяся в сеттинге TMA, кроме KDIGO Stage I острого почечного повреждения;
сопутствующая острая РТПХ II–IV степени или инфекция (бактериальная или вирусная).
Приложение 15
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
Полиорганная дисфункция при ТА-ТМА
|
№ п/п
|
Нарушение функции органов | Критерии |
| 1 | Почечная |
Снижение СКФ > 50 % по сравнению с предтрансплантационным периодом, рассчитанным по креатинину или цистатину С, или увеличение креатинина более чем в 2 раза от базового уровня
|
| 2 | Легочная |
Любая потребность в вентиляции легких с положительным давлением (неинвазивной или инвазивной) > 24 часов в отсутствии определенной патологии (аденовирусная пневмония, перегрузка жидкостью, тяжелый сепсис), диффузный альвеолярный геморраж
|
| 3 | Сердечно-сосудистая |
Легочная гипертензия, диагностированная кардиологом с помощью катереризации сердца, или с помощью диагностических критериев эхокардиографии
|
| 4 | Серозиты |
Клинически значимые серозиты (плевральный или перикардиальный выпоты или асцит), требующие медикаментозной терапии (диуретики) или дренирования в отсутствии других причин (ВОБ, застойная сердечная недостаточность)
|
| 5 | ЦНС |
Заторможенность, измененный психический статус, судороги с или без доказательств синдрома задней обратимой энцефалопатии (PRES)
|
| 6 | ЖКТ |
ЖКТ кровотечение и (или) кишечные стриктуры, требующие медицинских или хирургических вмешательств
|
Приложение 16
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
ШКАЛА
оценки органного поражения при хронической РТПХ
Степень тяжести хронической РТПХ
РЕЖИМЫ
| Орган | Балл 0 | Балл 1 | Балл 2 | Балл 3 |
|
Кожа
Пятнисто-папулезная сыпь;
лихеноиды;
папуло-сквамозные участки;
ихтиоз;
гиперпигментация;
гипопигментация; кератоз;
эритема; эритродермия;
пойкилодерма;
склеротические изменения;
зуд;
повреждение волос;
нарушение структуры ногтей.
С оценкой % вовлеченной площади
|
Нет симптомов |
Менее 18 % площади поверхности тела с признаками заболевания, но без склеротических изменений
|
19 %–50 % площади поверхности тела или поверхностные склеротические изменения (не глубокие, возможность щипка)
|
> 50 % площади поверхности тела или глубокие склеротические изменения или нарушение мобильности, язвенные поражения или выраженный зуд)
|
| Полость рта | Нет симптомов |
Незначительные симптомы с признаками заболевания, но без значительного ограничения перорального приема пищи
|
Умеренные проявления с признаками заболевания и с частичным ограничением перорального приема
|
Выраженные симптомы с признаками заболевания и выраженным ограничением перорального приема
|
| Глаза | Нет симптомов |
Легкая сухость, без нарушения ежедневной активности (далее – ЕДА) (капли < 3 раз в день) или асимптоматическое течение сухого кератоконъюнктивита
|
Умеренная сухость с частичным нарушением ЕДА (капли > 3 раз)
|
Выраженная сухость со значительным нарушением ЕДА (специальные гели для обезболивания) или неспособность работать вследствие поражения глаз либо
потеря зрения вследствие сухого кератоконъюнктивита
|
| ЖКТ | Нет симптомов |
Дисфагия, анорексия, тошнота, рвота, боли в животе или диарея без значительной потери веса (менее 5 %)
|
Симптомы ассоциированы с незначительной либо умеренной потерей веса (5 %–15 %)
|
Симптомы ассоциированы со значительной потерей веса > 15 %, требуют нутритивной поддержки для обеспечения основных энергетических затрат либо дилатации пищевода
|
| Печень | Нормальная функция |
Повышен билирубин, щелочная фосфатаза, AсАТ или АлАТ менее 2 норм
|
Билирубин более 3 мг/дл или билирубин, ферменты 2–5 норм
|
Билирубин или ферменты более 5 норм |
| Легкие | Нет симптомов |
Незначительные симптомы (одышка при подъеме по лестнице)
|
Умеренные симптомы (одышка при ходьбе по плоскости)
|
Выраженные симптомы (одышка в покое, требующая кислородотерапии)
|
|
Форсированный объем выдоха 1 (ФОВ1)
|
Более 80 % | 60%–79% | 40%–59% | Менее 39% |
| Суставы и фасции | Нет симптомов |
Легкая тугоподвижность рук или ног, нормальная или несколько сниженная активность движений (далее – АД), не влияющая на ЕДА
|
Тугоподвижность рук или ног либо контрактуры суставов, эритема вследствие фасциита, умеренное снижение АД от незначительного до умеренного ограничения ЕДА
|
Контрактуры со значительным снижением АД и выраженным ограничением ЕДА (невозможность обуться, завязать шнурки, застегнуть рубашку, одеться самостоятельно и иное)
|
| Гениталии | Нет симптомов |
Незначительные проявления при осмотре, без влияния на коитус и минимальный дискомфорт при гинекологическом обследовании
|
Умеренные проявления при осмотре, с незначительной диспареунией или дискомфортом при гинекологическом обследовании
|
Выраженные симптомы (стриктуры, лабиаагглютинация с язвенным поражением) и сильная боль при коитусе
либо невозможность влагалищной пенетрации
|
Приложение 17
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
Степень тяжести хронической РТПХ
|
№ п/п
|
Степень | Вовлечение органов и систем |
| 1 | Легкая |
1 или 2 органа или локализации (кроме легких), без клинически значимого функционального нарушения (максимально 1 балл во всех пораженных органах)
|
| 2 | Умеренная |
Вовлечение не менее одного органа или участка с клинически значимой, но не обширной дисфункцией (максимально 2 балла), или 3 и более органов без нарушения клинической функции (максимально 1 балл в каждом органе)
Вовлечение легких максимально 1 балл |
| 3 | Тяжелая |
Значительная дисфункция (3 балла в каждом органе) или поражение легких (2 балла и более)
|
Приложение 18
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
РЕЖИМЫ
дозирования антимикробных ЛП
ЛП для лечения грибковых инфекций
СХЕМА
|
№ п/п
|
Международное непатентованное наименование ЛП
|
Форма выпуска и доза | Режим дозирования |
| 1 | Меропенем |
порошок для приготовления раствора для внутривенного введения
500 и 1000 мг;
100–120 мг/кг/сут.
|
суточную дозу делить на 3 введения каждые 8 часов внутривенно капельно за 1–3 часа. Максимально 6000 мг в сутки
|
| 2 | Имипенем/Циластатин |
порошок для приготовления раствора для инфузий 500 мг/500 мг
60–100 мг/кг/сут. (по имипенему)
|
суточную дозу за 3–4 введения внутривенно капельно за 1–3 часа.
Максимально 4000 мг в сутки
|
| 3 | Дорипенем | порошок для инфузий 500 мг |
по 0,5 мг – 1000 мг каждые 8 часов внутривенно капельно в виде продленных 4-часовых инфузий
|
| 4 | Амикацин |
раствор для внутривенного и внутримышечного введения
250 мг/мл – 2 мл, 4 мл;
15–20 мг/кг/сут.
|
внутривенно капельно путем инфузии за 60–120 минут не более 1500 мг. Длительность терапии не более 7 дней
|
| 5 | Колистин |
порошок для инъекций и ингаляций 2 млн МЕ
детям с массой тела < 40 кг –100 000–150 000 МЕ/кг/сут. после нагрузочной дозы 75 тыс. МЕ/кг за 30 мин;
Режим дозирования у детей с массой тела > 40 кг соответствует режиму дозирования у взрослых:
9–12 млн МЕ/сут.
|
суточную дозу делить на 3 введения внутривенно капельно путем инфузии за 30–60 минут или суточным титрованием
|
| 6 | Цефепим |
порошок для приготовления раствора для внутривенного и внутримышечного введения 500 мг и 1000 мг
100–150 мг/кг/сут.
|
суточную дозу делить на 3 введения внутривенно капельно за 30 минут – 1 час. Максимально 6 г в сутки
|
| 7 | Пиперациллин/тазобактам |
порошок для инъекций внутривенных лиофилизированный 4000 мг/500 мг
|
суточную дозу за 3 введения каждые 8 часов внутривенно капельно за 1 час
|
| 8 |
Зафицефта
(Цетазидим/авибактам)
|
с 1 месяца до 12 лет 30–50 мг/кг каждые 8 часов внутривенно, не более 6 г в сутки (по цефтазидиму)
Старше 12 лет – 1–2 г внутривенно каждые 8 часов
|
внутривенно за 30–60 минут |
| 9 | Цефоперазон/сульбактам |
порошок для приготовления раствора для внутривенного и внутримышечного введения 1,0 г/1,0 г
|
по 4,0 г (2,0/2,0) каждые 12 часов внутривенно капельно в течение 60 минут
|
| 10 | Левофлоксацин |
раствор для инфузий 400 мг/250 мл
Применение у детей (off-lable):
6 мес. – 5 лет:
8–10 мг/кг/доза (не более 250 мг) 2 раза в сутки;
> 5 лет: 10 мг/кг/доза 1 раз в сутки, не более 750 мг в сутки.
|
внутривенно капельно путем инфузии за 60–90 минут.
Разовая доза не более 750 мг
|
| 11 | Ванкомицин |
порошок лиофилизированный для приготовления раствора для инфузий 500 мг и 1000 мг 60 мг/кг/сут.
|
суточную дозу за 3 введения внутривенно капельно за 60 минут и более. Максимально 3 г в сутки
|
| 12 | Тейкопланин |
порошок для приготовления раствора для внутривенного и внутримышечного введения 200 мг и 400 мг
|
3 введения с интервалом 12 часов в дозе 10 мг/кг, далее – 6–10 мг/кг/сут. 1 введение в сутки внутривенно капельно в течение 30–60 минут. Разовая доза не более 400 мг
|
| 13 | Линезолид |
раствор для инфузий
2 мг/мл – 100 мл, 200 мл и 300 мл
детям до 12 лет – 30 мг/кг/сут.
детям старше 12 лет – 600 мг 2 раза в сутки
|
суточную дозу за 3 введения внутривенно капельно за 1–2 часа (дети до 12 лет)
|
| 14 | Даптомицин |
порошок для инфузий лиофилизированный 500 мг
С 1 до 6 лет – 12 мг/кг за 60 минут 1 раз в сутки
С 7 до 11 лет 9 мг/кг внутривенно 1 раз в сутки
12–17 лет 7 мг/кг внутривенно 1 раз в сутки
|
внутривенно капельно за 60 минут для детей до 6 лет;
внутривенно капельно за 30 минут для детей старше 6 лет
|
| 15 | Тигециклин |
лиофилизат для приготовления раствора для инфузий 50 мг
Дети от 8 до 11 лет (off-lable): 2,4 мг/кг 2 раза в день нагрузочная доза, далее 1,2 мг/кг 2 раза в сутки;
дети от 12 до 17 лет – 50 мг 2 раза в сутки
|
внутривенно капельно путем инфузии в течение 30–60 минут каждые 12 часов. Максимальная разовая доза 50 мг (дети до 18 лет)
|
| 16 | Азтреонам |
дети 9 мес. – 2 года: 30 мг/кг внутривенно каждые 6–8 часов (не более 120 мг/кг/сут.)
Дети старше 2 лет: 50 мг/кг
|
внутривенно капельно путем инфузии в течение 30–60 минут 3–4 раза в день
|
Приложение 19
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
ЛП для лечения грибковых инфекций
|
№ п/п
|
Наименование ЛП | Форма выпуска | Возраст | Дозировка | Кратность приема |
| 1 | Микафунгин |
Лиофилизат для приготовления раствора для инфузий 50 мг, 100 мг
|
0–18 лет и старше |
2 мг/кг (максимальная доза: 100 мг в сутки), при очень тяжелой инфекции допустимо увеличение дозы до 12 мг/кг
|
1 раз в сутки, внутривенно капельно путем инфузии
|
| 2 | Каспофунгин |
Лиофилизат для приготовления раствора для инфузий 50 мг, 70 мг
|
3 мес. – 8 лет и старше |
70 мг/м2 в первые сутки, далее – 50 мг/м2 (максимальная доза: 70 мг в сутки)
|
1 раз в сутки, внутривенно капельно путем инфузии
|
| 3 | Анидулафунгин |
Лиофилизат для приготовления раствора для инфузий 100 мг
|
старше 1 мес. |
3 мг/кг/сут. (максимально 200 мг в первые сутки), далее – 1,5 мг/кг/сут (максимально 100 мг в сутки)
|
1 раз в сутки, внутривенно капельно путем инфузии
|
| 4 |
Амфотерицин В
(липидные формы)
|
Концентрат (липидный комплекс) для приготовления раствора для внутривенного введения 5 мг/мл в стеклянных флаконах по 2 мл, 10 мл и 20 мл
|
1 мес. – 18 лет и старше | 3–5 мг/кг |
1 раз в сутки, внутривенно капельно путем инфузии
|
| 5 | Флуконазол |
Раствор для инфузий 2 мг/мл в стеклянных флаконах по 100 мл.
Капсулы по 50 и 150 мг
|
4–18 лет и старше | 10–12 мг/кг |
1 раз в сутки, внутривенно с переходом на прием внутрь (максимально 400 мг в сутки)
|
| 6 | Вориконазол |
Лиофилизат для приготовления раствора для инфузий 200 мг.
Таблетки, покрытые оболочкой по 50 и 200 мг
|
от 2 до 14 лет (весом < 50 кг) | 9 мг/кг в первые сутки, далее – 8 мг/кг |
2 раза в сутки, внутривенно капельно путем инфузии с переходом на прием внутрь 9 мг/кг 2 раза в сутки внутривенно капельно
|
|
от 12 до 14 лет (весом > 50 кг), а также дети старше 14 лет и взрослые
|
6 мг/кг в первые сутки, далее – 4 мг/кг |
2 раза в сутки, внутривенно капельно путем инфузии с переходом на прием внутрь
|
|||
| 7 | Посаконазол | Суспензия для приема внутрь 40 мг/мл 105 мл | от 12 лет и взрослые | 400 мг | 2 раза в сутки, внутрь |
Приложение 20
к клиническому протоколу
«Трансплантация гемопоэтических стволовых клеток пациентам (детское население) с первичными (врожденными) иммунодефицитами»
СХЕМА
медицинского наблюдения пациентов после алло-ТГСК
|
Дни
Параметры
|
Д+30
|
31–59 |
Д+60
|
61–99 |
Д+100
|
101–179 |
Д+180
|
181–364 |
Д+365
|
1 год – 5 лет |
| Медицинский осмотр | + | 2 раза в неделю | + | 1 раз в неделю | + | 2 раза в месяц | + | 1 раз в месяц | + | 2 раза в год |
| Рост | + | 2 раза в неделю | + | 1 раз в неделю | + | 2 раза в месяц | + | 1 раз в месяц | + | 2 раза в год |
| Вес | + | 2 раза в неделю | + | 1 раз в неделю | + | 2 раза в месяц | + | 1 раз в месяц | + | 2 раза в год |
|
Артериальное давление, частота сердечных сокращений, частота дыхания
|
+ | 2 раза в неделю | + | 1 раз в неделю | + | 2 раза в месяц | + | 1 раз в месяц | + | 2 раза в год |
| Индекс Карновского, Ланского, ECOG | + | 2 раза в неделю | + | 1 раз в неделю | + | 2 раза в месяц | + | 1 раз в месяц | + | 2 раза в год |
| ОАК | + | 2 раза в неделю | + | 1 раз в неделю | + | 2 раза в месяц | + | 1 раз в месяц | + | 2 раза в год |
| БАК | + | 2 раза в неделю | + | 1 раз в неделю | + | 2 раза в месяц | + | 1 раз в месяц | + | 2 раза в год |
| Уровень ферритина, сывороточного железа | + | + | + | |||||||
| Ca2+, K+, Na+, Cl2+, P, Mg | + | 2 раза в неделю | + | 1 раз в неделю | + | 2 раза в месяц | + | 1 раз в месяц | + | 2 раза в год |
| Анализ мочи общий | + | 2 раза в неделю | + | 1 раз в неделю | + | 2 раза в месяц | + | 1 раз в месяц | + | 2 раза в год |
| Скорость клубочковой фильтрации | + | 2 раза в неделю | + | 1 раз в неделю | + | 2 раза в месяц | + | 1 раз в месяц | + | 2 раза в год |
| IgM, IgG к ЦМВ, ВПГ, ВЭБ, токсоплазмоз | + | - | + | - | + | - | + | - | + | 1 раз в год |
| HbsAg, а/HСV | + | - | + | - | + | - | + | - | + | |
| ПЦР крови на ЦМВ | + | - | + | - | + | - | + | - | + | |
| Посевы со слизистой зева, рта, посев мочи* | ||||||||||
| Аспергиллезный антиген | + | - | + | - | + | - | + | - | + | |
| Миелограмма | + | - | - | + | - | + | - | + | ||
| Химеризм | + | - | + | - | + | - | + | - | + | 1 раз в год |
| Определение группы крови* | + | + | + | + | + | 1 раз в год | ||||
| Гормональный статус | + | - | + | - | + | - | + | - | + | 1 раз в год |
| Коагулограмма | + | - | + | - | + | - | + | - | + | 1 раз в год |
| Проба Кумбса | + | - | + | - | + | - | + | - | + | 1 раз в год |
| ЭКГ | + | - | + | - | + | - | + | - | + | 1 раз в год |
| ЭхоКГ | + | - | + | - | + | - | + | - | + | 1 раз в год |
| Электроэнцефалограмма | - | - | - | - | ||||||
| УЗИ брюшной полости и забрюшинного пространства | + | - | + | - | + | - | + | - | + | 1 раз в год |
| МРТ головы* | ||||||||||
| КТ грудной клетки | + | - | + | - | + | - | + | - | + | 1 раз в год |
| КТ брюшной полости* | ||||||||||
| КТ придаточных пазух носа* | ||||||||||
| Функция внешнего дыхания | + | - | + | - | + | - | + | - | + | 1 раз в год |
| Консультация врача-стоматолога-терапевта* | ||||||||||
| Консультация врача оториноларинголога | + | - | + | - | + | - | + | - | + | - |
| Консультация врача офтальмолога | + | - | + | - | + | - | + | - | + | 1 раз в год |
| Консультация врача – детского невролога | + | - | + | - | + | - | + | - | + | 1 раз в год |
| Консультация других врачей-специалистов * | ||||||||||
| Консультация врача-психиатра детского* | ||||||||||
| Консультация врача инфекциониста* | ||||||||||
| Вакцинация | - | - | - | - | - | - | - | - | + | + |
______________________________
* Медицинские наблюдения пациентов после алло-ТГСК осуществляется при необходимости.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.