Реанимация новорожденных
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Неуточненная асфиксия при рождении (P21.9), Средняя и умеренная асфиксия при рождении (P21.1), Тяжелая асфиксия при рождении (P21.0)
Неонатология, Реаниматология
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «17» марта 2023 года
Протокол №180
КЛИНИЧЕСКИЙ ПРОТОКОЛ МЕДИЦИНСКОГО ВМЕШАТЕЛЬСТВА
РЕАНИМАЦИЯ НОВОРОЖДЕННЫХ
Реанимация: комплекс неотложных мероприятий при остановке кровообращения или дыхания с целью их восстановления или стабилизации, тем самым обеспечив кровоснабжение и доступ кислорода к таким жизненно важным органам организма, как головной мозг и сердце (Медицинский словарь Pschyrembel; https://www.pschyrembel.de, дата посещения 31.01.2021).
Код(ы) МКБ-10:

Дата разработки: 2014 год (пересмотр 2018 год/2023 год).
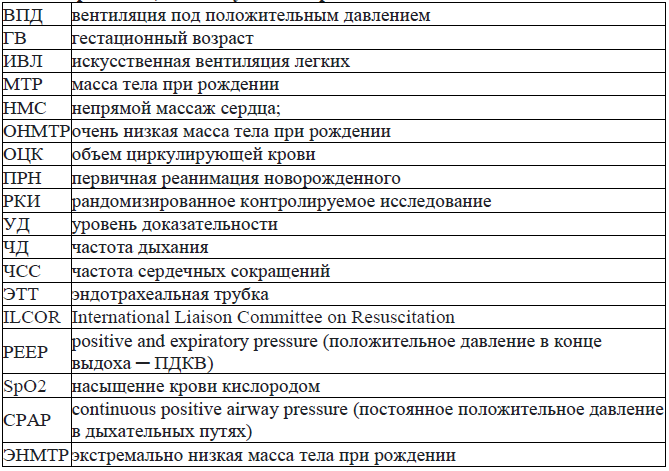
Сокращения, используемые в протоколе:
Категория пациентов: новорожденные дети.
Шкала уровня доказательности:

ВВОДНАЯ ЧАСТЬ
Код(ы) МКБ-10:

Дата разработки: 2014 год (пересмотр 2018 год/2023 год).
Сокращения, используемые в протоколе:

Пользователи протокола: неонатологи, анестезиологи-реаниматологи, акушер-гинекологи, акушерки, медицинские сестры родовспомогательных организаций, педиатры, врачи скорой медицинской помощи.
Категория пациентов: новорожденные дети.
Шкала уровня доказательности:

Классификация
Клиническая классификация:

“2020 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care, Part 5: Neonatal Resuscitation”. ILCOR, 2020.
Лечение
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Цель проведения процедуры/вмешательства: Цель реанимации – полное восстановление жизненно важных функций организма, нарушение которых может быть обусловлено перинатальной гипоксией и асфиксией в родах. [1,2,3].
(2020 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care, Part 5: Neonatal Resuscitation. ILCOR, 2020.)
Показания и противопоказания к процедуре/ вмешательству:
Показания к процедуре/ вмешательству:
- нарушение срочной адаптации дыхания и кровообращения новорожденного к условиям внеутробной жизни.
Противопоказания к процедуре/вмешательству:
- Если гестационный̆ возраст, масса тела при рождении или врожденные аномалии развития ассоциированы с практически неминуемым летальным исходом или неприемлемо тяжелой инвалидизацией у выживших детей; Рождение недоношенного новорожденного с подтвержденным гестационным возрастом менее 22- ой недели и массой тела менее 500 грамм;
- наличие у новорожденного младенца критических врожденных пороков развития, несовместимые с жизнью и хромосомных аномалий, связанных с высоким риском смертности;
- анэнцефалия;
Рекомендации по неоказанию или прекращению реанимационных мероприятий [1,2]:
- Неоказание или прекращение реанимационных мероприятий должны быть этически обоснованы (УД C) [9,10].
- Если, несмотря на все необходимые меры и после исключения всех возможных причин, поддающихся лечению, новорожденному по-прежнему требуется постоянное проведение сердечно-легочной реанимации после родов, через примерно двадцать минут следует обсудить с бригадой и родственниками прекращение реанимационных мероприятий (УД С) [1,2,15].
- При рождении ребенка «На грани жизнеспособности» или при высоком риске того, что состояние ребенка приведет к его ранней смерти или тяжелому заболеванию, представляется целесообразным после консультации со специалистами и с привлечением родителей̆ принять решение о неоказании реанимационных мероприятий или же их оказании в ограниченном объеме (УД C) [9-15].
Перечень основных и дополнительных диагностических мероприятий, определяющих готовность к реанимации:
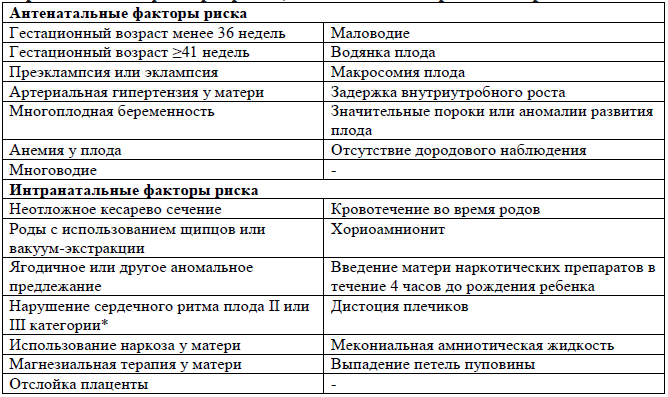
Предвидение потребности в реанимации новорожденного определяется оценкой факторов перинатального риска (Приложение 2) и ответов акушерского персонала на 4 вопроса:
1) гестационный возраст?
2) околоплодные воды чистые?
3) есть ли дополнительные факторы риска? (смотрите приложения 2).
4) план пережатия пуповины?
Оценка факторов риска и ответы акушерского персонала на вышеуказанные вопросы определяют формирование состава команды с предварительным обсуждением клинического сценария, определением лидера команды, распределением обязанностей каждого члена команды, а также стандартизованный подход к проверке наличия и функционирования наиболее важных материалов и оборудования для ПРН (смотрите приложение 3).
Потребность в реанимации новорожденного определяется оценкой ответов на следующие 3 вопроса, задаваемых сразу после рождения ребенка:
- новорожденный доношенный?
- хороший ли у него мышечный тонус?
- ребенок дышит или кричит?
Если на все 3 вопроса ответ «Да», то он может оставаться с матерью и ему следует обеспечить стандартный уход (обсушить, положить на грудь матери, накрыть сухой теплой пеленкой, продолжать наблюдение за дыханием и активностью).
Если ответ на любой из трех вопросов «Нет», младенца следует перенести на реанимационный стол под лучистый обогреватель, чтобы последовательно выполнить одно или несколько действий по алгоритму реанимации новорожденных.
Требования к проведению процедуры/вмешательства:
Требования к оснащению, расходным материалам, используемым при реанимации новорожденного. Готовность к реанимации.
- На подготовительном этапе реанимации новорожденного следует проверить наличие и функционирование оборудования, согласно оперативному контрольному списку-чек, лист (приложение 3).
- На каждых родах должен присутствовать как минимум 1 медработник, владеющий навыками начальной помощи и проведения вентиляции под положительным давлением, единственной обязанностью которого является оказание помощи новорожденному.
- При наличии значимых перинатальных факторов риска, повышающих вероятность расширенной реанимации должен быть немедленно доступен дополнительный персонал с навыками непрямого массажа сердца, интубации трахеи и катетеризации пупочной вены.
- Учитывая, что новорожденный без очевидных факторов риска неожиданно может потребовать реанимационных мероприятий, в каждой родовспомогательной организации должна быть разработана процедура быстрой мобилизации на любые роды команды реаниматологов, владеющих всеми навыками реанимации новорожденного.
- На каждых родах должны быть легко доступны все материалы и оборудование, необходимые для выполнения всех этапов реанимации. Если ожидается рождение ребенка высокого перинатального риска, все соответствующие материалы и оборудование должны быть готовы к немедленному использованию.
Стандартные меры предосторожности:
- При проведении реанимационных мероприятий строго соблюдаются все положения инфекционного контроля по отношению к обработке родильного зала, палат интенсивной терапии, оборудования, материалов, используемых в процессе реанимации, рук персонала и т.д.
- Ситуация при проведении реанимации новорожденных характеризуется высоким риском контакта с биологическими жидкостями человеческого организма (кровь, моча, стул, слюна, рвотные массы), которые следует расценивать как потенциально инфицированные. Поэтому перед началом реанимации новорожденного необходимо надеть стерильные перчатки. При выполнении процедур, связанных с вероятным разбрызгиванием капель крови или других биологических жидкостей, следует надевать маску, защитные приспособления для глаз и лица, халат и фартук.
Классификация по первичной оценке сразу после рождения новорожденного.
На основании первичной оценки состояния новорожденного, проводимой сразу после рождения, его следует отнести в одну из трех групп и провести соответствующие первичной оценке начальные шаги помощи новорожденному:
1. Энергично дышит или кричит, хороший мышечный тонус, ЧСС выше
100 в 1 мин. В этом случае нет необходимости в начальной помощи и немедленном пережатии пуповины. Для новорожденных, которым не требуется реанимация, рекомендуется отсроченное пережатие пуповины по меньшей мере на одну минуту. Аналогичную задержку пережатия пуповины следует применять и у недоношенных новорожденных, не нуждающихся в реанимации сразу после рождения. Это обеспечивает значительное снижение частоты НЭК, ВЖК, потребности в гемотрансфузиях (УД-А2).
Дышащему или кричащему ребенку с хорошим мышечным тонусом не потребуется никаких вмешательств, за исключением обсушивания, контакта кожа-к-коже с матерью, накрывания теплой (предварительно согретых) сухой пеленкой или полотенцем и дальнейшего наблюдения в динамике.
3. Дыхание неадекватно или отсутствует, мышечный тонус низкий, ЧСС низкая или не определяется, часто пониженная перфузия становится причиной бледности.
2. Дыхание не адекватно или отсутствует, мышечный тонус нормальный или сниженный, ЧСС ниже 100 в 1 мин.
Этому ребенку потребуются следующие вмешательства: провести сцеживание пуповины, если ее пульсация, определяемая пальпаторно, менее 100 в минуту и ребенок нуждается в незамедлительном начале реанимационных мероприятий. Следует отметить, что сцеживание пуповины по эффективности сравнимо с отстроченным пережатием пуповины (УД-А2) и является альтернативой ее отсроченному пережатию. Сцеживание проводится по направлению от плаценты к ребёнку.
3. Дыхание неадекватно или отсутствует, мышечный тонус низкий, ЧСС низкая или не определяется, часто пониженная перфузия становится причиной бледности.
Обсушить. Такому ребенку немедленно требуется контроль дыхательных путей и вентиляция под положительным давлением. Как только это успешно выполнено, ребенку может потребоваться непрямой массаж сердца и, возможно, медикаментозная терапия.
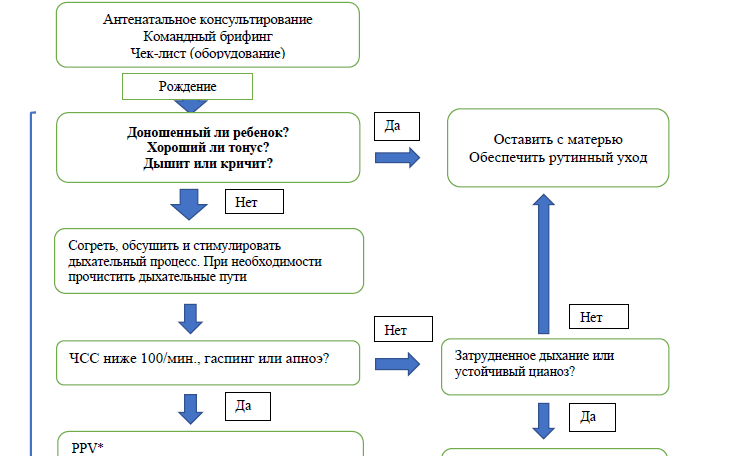
Последовательность основных реанимационных мероприятий представлена в виде алгоритма в Приложении 1 и состоит из следующих этапов:
Реанимационные мероприятия у новорожденных:
Последовательность основных реанимационных мероприятий представлена в виде алгоритма в Приложении 1 и состоит из следующих этапов:
А. Начальные шаги стабилизации состояния новорожденного;
В. Вентилировать и оксигенировать;
С. Начать непрямой массаж сердца;
D. Ввести эпинефрин и/или восполнить объем крови.
- Объем и характер лечения в родильном зале определяются не только исходным состоянием ребенка, но и его реакцией на проводимые реанимационные мероприятия. С самого начала следует проводить непрерывный мониторинг ЧСС, SpО2 и температуры ребенка. В зависимости от показателей ЧСС и SpО2 следует принимать решение о дальнейших действиях при проведении реанимационных мероприятий.
- Действия, проводимые реаниматологом и оценка ответа ребенка на них (проводимые помощником реаниматолога) выполняются одновременно, это определяет необходимость и содержание последующих действий.
- Приблизительно 60 секунд («золотая минута») выделяются для завершения начальных шагов, повторной оценки состояния новорожденного и начальной вентиляции, если это необходимо.
Начальные реанимационные мероприятия.
Начальные мероприятия включают:
- Обеспечение минимальных потерь тепла, согревание.
- Обсушивание.
- Проведение тактильной стимуляции.
- Придание ребенку правильного положения для обеспечения проходимости дыхательных путей.
- Провести санацию по показаниям.
- Оценке дыхания и частоты сердечных сокращений.
Требования к поддержанию температуры тела новорожденного.
- С целью профилактики гипотермии ребенка, нуждающегося в реанимации, следует уложить на реанимационный столик под источник лучистого тепла и обсушить теплой пеленкой, после чего влажная пеленка должна быть удалена с поверхности стола.
- Следует задокументировать температуру тела новорожденного при поступлении (УД В) [1,2,5].
- Недоношенные новорожденные особенно подвержены риску гипотермии, которая может повысить потребление кислорода и препятствовать эффективной реанимации. Такая ситуация наиболее опасна для новорожденных с экстремально низкой (˂ 1000 г) и очень низкой массой тела при рождении (˂ 1500 г). С целью профилактики гипотермии необходимо предпринять дополнительные действия, которые не ограничиваются, как это было описано выше, поднятием температуры воздуха в родильном зале до ≥26°С и в той зоне, где будут проводиться реанимационные мероприятия, дополнительно помещают экзотермический матрас под несколько слоев пеленок, находящихся на реанимационном столе (УД В) [1,2,5].
- Недоношенные новорожденные с гестационным возрастом 29 недель и менее помещаются сразу же после рождения (без обсушивания) в полиэтиленовый пакет или под полиэтиленовую пеленку по шею на заранее подогретые пеленки на реанимационном столе под источник лучистого тепла. Поверхность головы ребенка дополнительно покрывается пленкой или ребенку надевается шапочка. Датчик пульсоксиметра присоединяется к правому запястью ребенка до его помещения в термопакет. Пакет или пеленка не должны убираться во время реанимационных мероприятий.
- При отсроченном пережатии и пересечении пуповины поддержание температуры тела ребенка следует осуществлять сразу после его рождения.
- Температуру тела новорождённых в родильном зале следует поддерживать в диапазоне 36,5-37,50С.
- Температура ребенка должна тщательно мониторироваться, поскольку иногда, использование методов, направленных на предотвращение потери тепла, может приводить к гипертермии.
- Все реанимационные мероприятия, включая интубацию трахеи, непрямой массаж сердца, венозный доступ, должны осуществляться при одновременном обеспечении терморегуляции (УД – С) [1,2,5].
- Обеспечение телесного контакта, не требующих реанимации здоровых новорожденных с матерью может быть эффективным для стимулирования грудного вскармливания, терморегуляции, стабилизации уровня глюкозы вкрови.
Тактильная стимуляция.
Во многих случаях придание голове правильного положения и санация дыхательных путей (при наличии показаний) оказываются достаточным стимулом для начала дыхания. Обсушивание тела и головы новорожденного также обеспечивает стимуляцию дыхания при правильном положении головы. Если у ребенка нет адекватных дыхательных движений, то для стимуляции дыхания можно провести дополнительное тактильное раздражение: нежное поглаживание вдоль спины, туловища или конечностей (1-2 раза), после чего провести оценку эффективности первичных реанимационных мероприятий.
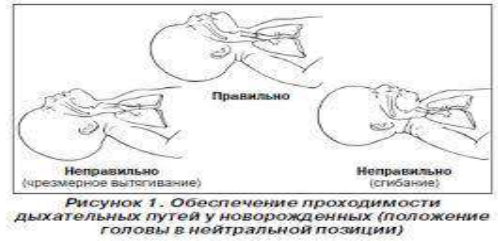
Придание голове новорожденного правильного положения.
Ребенка следует положить на спину с головой в нейтральном (правильном) положении (рисунок ниже) для обеспечения анатомической проходимости дыхательных путей. Под лопатки следует положить полотенце или одеяльце, сложенное до толщины 2 см для сохранения нужного положения головы. Для открытия дыхательных путей у ребенка со сниженным мышечным тонусом может быть полезным выведение нижней челюсти или применение воздуховода соответствующего размера. Как правило, нет необходимости в проведении рутинной санации дыхательных путей. Отсасывание субстрата необходимо только при обструкции дыхательных путей.

Санация дыхательных путей (эвакуация содержимого из ротоглотки).
Доказано, что санация дыхательных путей может спровоцировать брадикардию во время реанимации, поэтому ее рутинное проведение не рекомендуется (УД С) [1,2,4]. Санацию можно рассмотреть в том случае, если у ребенка отсутствуют адекватные дыхательные движения или же если ему требуется проведение вентиляции легких положительным давлением и в дыхательных путях отмечается обструкция (УД С) [4]. Для ослабленных младенцев, рожденных при наличии мекония в амниотической жидкости, может быть целесообразно проведение интубации и аспирация трахеи, если во время вентиляции легких с положительным давлением было обнаружено нарушение проходимости дыхательных путей. (УД С) [4]. Для ослабленных младенцев (с остановкой дыхания или неэффективными дыхательными усилиями), рожденных при наличии мекония в амниотической жидкости, не рекомендуется проводить ларингоскопию с аспирацией или без аспирации трахеи. (УД С) [1,2,4].
Меконий.
Если новорожденный, родившийся после излития мекониальных вод, активен и у него выявляются хорошие дыхательные усилия и мышечный тонус, его оставляют с матерью, чтобы оказать начальную помощь. При необходимости (если рот ребенка заполнен меконием) может быть проведена осторожная санация рта и носа для освобождения от мекония с помощью резиновой груши. Однако, если у младенца, родившегося после излития мекониальных вод, снижен мышечный тонус и неадекватны дыхательные усилия, начальные шаги реанимации должны быть выполнены под лучистым обогревателем. При этом, если рот ребенка заполнен меконием, может быть проведена осторожная санация рта и носа для освобождения от мекония с помощью резиновой груши.
Если после оказания начальной помощи ребенок не дышит или частота сердечных сокращений менее 100 в 1 минуту, следует начать вентиляцию под положительным давлением; рутинная интубация для санации трахеи в этой ситуации не рекомендуется, потому что недостаточно данных, чтобы продолжать рекомендовать такую практику (класс IIb, УД C-LD).
При внесении этого изменения большее значение придавалось предотвращению вреда (т.е. задержкам в обеспечении вентиляции мешком и маской ─ потенциальному вреду процедуры) по сравнению с научно недоказанными преимуществами рутинной интубации и санации трахеи. Поэтому акцент следует делать на начале вентиляции легких у младенцев с отсутствующим или неэффективным дыханием в течение первой минуты их жизни.
Однако, при наличии показаний (у ребенка отсутствует дыхание после осторожного освобождения рта и носа от мекония с помощью груши, указывающее на наличие обструкции дыхательных путей), такому ребенку необходимо инициировать соответствующее вмешательство для поддержки вентиляции и оксигенации. Такое вмешательство может включать интубацию и санацию трахеи, если дыхательные пути непроходимы. Продолжительность санации не должна превышать 5 секунд. Следует избегать глубокой санации глотки из-за возможного провоцирования брадикардии, ларинго- и бронхоспазма.
Если оценка состояния новорожденного после начальных шагов оказанной помощи указывает, что адекватное нормальное регулярное дыхание отсутствует или наблюдается затрудненное дыхание, или ЧСС менее 100 в 1мин, ему следует прикрепить датчик пульсоксиметра на правое предплечье и электроды ЭКГ (при наличии) и начинать реанимационные мероприятия, то есть переходить к вентиляции под положительным давлением (БлокуБ):
Оценка эффективности блока «А».
Принятие решения о переходе к следующему этапу реанимации основывается на оценке двух критериев:
● наличие/отсутствие спонтанного дыхания, его характер (апноэ, дыхание типа «гаспинг», затрудненное/не затрудненное);
● частота сердечных сокращений (ЧСС более 100 уд/мин. или менее 100 уд/мин).
Если оценка состояния новорожденного после начальных шагов оказанной помощи указывает, что адекватное нормальное регулярное дыхание отсутствует или наблюдается затрудненное дыхание, или ЧСС менее 100 в 1мин, ему следует прикрепить датчик пульсоксиметра на правое предплечье и электроды ЭКГ (при наличии) и начинать реанимационные мероприятия, то есть переходить к вентиляции под положительным давлением (БлокуБ):
● Открыть дыхательные пути.
● Принудительная вентиляция легких под положительным давлением.
● Обеспечить мониторинг SpO2, ЧСС.
Блок «Б» ‒ вентилировать и оксигенировать.
Перед выполнением вентиляции легких необходимо сначала и/или одновременно:
● Открыть дыхательные пути. Придание голове новорожденного правильного положения.
● Целесообразно наложить электроды ЭКГ.
Устройства для проведения искусственной вентиляции легких в родильном зале.
Аппарат ИВЛ с Т-коннектором
Вентиляция под положительным давлением:
Устройства для проведения искусственной вентиляции легких в родильном зале.
Для проведения ИВЛ в родильном зале возможно использовать ручной аппарат ИВЛ с Т-коннектором, аппараты ИВЛ или саморасправляющийся мешок.
Аппарат ИВЛ с Т-коннектором
В аппаратах ИВЛ с Т-коннектором газовая смесь поступает в маску или интубационную трубку через контур, подключенный к смесителю сжатого воздуха и кислорода к манометру. Вентиляция обеспечивается благодаря окклюзии пальцем выходной трубки Т-коннектора, осуществляемой с определенной периодичностью. Аппарат позволяет создавать и регулировать необходимое давление как на вдохе, так и при помощи изменения диаметра отверстия выходной трубки на выдохе (СРАР, PEEP). Время вдоха регулируется путем изменения длительности окклюзии пальцем выходной трубки Т-коннектора. Для функционирования устройства требуется подключить его к источнику газовой смеси. По сравнению с саморасправляющимся мешком устройства с Т-коннектором являются наиболее эффективными для проведения ИВЛ у новорожденных детей в родильном зале.
У недоношенных новорожденных с ГВ менее 30 недель начальное использование СРАР имеет преимущества по сравнению с интубацией трахеи и ВПД в плане сокращения продолжительности механической вентиляции с потенциальным снижением смертности и/или частоты бронхолегочной дисплазии, а также не сопровождается значительным увеличением частоты синдромов утечки воздуха и тяжелых ВЖК.
Основываясь на этих доказательствах, для начальной респираторной поддержки самостоятельно дышащих недоношенных новорожденных рекомендуется использовать СРАР.
Саморасправляющийся мешок
У новорожденных следует использовать саморасправляющийся мешок объемом не более 240 мл. Для проведения ИВЛ воздушно-кислородной смесью следует подключить мешок к источнику кислорода и установить скорость потока 10 л/мин. Такая скорость позволяет добиться концентрации в дыхательной смеси около 40%. Для создания более высокой концентрации кислорода (80–90%) к саморасправляющемуся мешку требуется дополнительно подключить кислородный резервуар.
При использовании саморасправляющегося мешка невозможно создать положительное давление в конце выдоха, не подключив дополнительно клапан, создающий давление в конце выдоха. Использование саморасправляющегося мешка не позволяет обеспечить вдох длительностью более 1 с, а также проводить респираторную терапию методом СРАР.
У недоношенных новорожденных с ГВ менее 30 недель начальное использование СРАР имеет преимущества по сравнению с интубацией трахеи и ВПД в плане сокращения продолжительности механической вентиляции с потенциальным снижением смертности и/или частоты бронхолегочной дисплазии, а также не сопровождается значительным увеличением частоты синдромов утечки воздуха и тяжелых ВЖК.
Основываясь на этих доказательствах, для начальной респираторной поддержки самостоятельно дышащих недоношенных новорожденных рекомендуется использовать СРАР.
Независимо от типа используемых устройств ИВЛ может проводиться через маску, назальные канюли, ларингеальную маску или эндотрахеальную трубку.
Для достижения положительного давления необходимо обеспечить герметичность между краями маски и лицом ребенка. Круглая маска более герметично прилегает к лицу недоношенного ребенка с экстремально низкой массой тела (<1000 г), а для новорожденного с большей массой лучше использовать маску анатомической формы- Ее накладывают заостренным краем на нос ребенка.
NB! Основными критериями эффективности вентиляции легких является быстрое увеличение ЧСС и сатурации.
Заблокированы дыхательные пути ребенка:
ИВЛ через лицевую маску:
- Частота ИВЛ должна составлять 40-60 в одну минуту. Для удобства соблюдения правильного отношения времени вдоха к выдоху можно использовать счет: «Вдох, два, три; Вдох, два, три; Вдох, два, три».
- Всем новорожденным рекомендуется начинать ИВЛ с PIP равным 20 см водного столба и менять его в зависимости от клинического эффекта. Однако у доношенных новорожденных может возникнуть необходимость увеличения PIP до ≥ 30 см водн ст. Если отсутствует возможность воспользоваться манометром, следует проводить вентиляцию легких с минимально возможным пиковым давлением, обеспечивающим увеличение ЧСС.
- Положительное давление в конце выдоха (РЕЕР) — 5 см Н2О может быть обеспечено проточно заполняющимся мешком с реанимационной маской, реанимационным устройством с Т-коннектором, но только при наличии у него соответствующего РЕЕР-клапана, присоединенного к источнику сжатого газа).
- Скорость потока газа — 8-10 л/мин (для проточно заполняющегося мешка и Т-системы).
- Для начальной вентиляции легких ребенка с гестационным <35 недель рекомендуется использовать воздух (21% О2).
- Для более незрелых новорожденных (< 32 нед.) начальная концентрация О2 30%.
- Последующую концентрацию О2 изменяют в зависимости от показателей SpO2. Вентиляция легких 100% кислородом показана при проведении непрямого массажа сердца (НМС).
Для достижения положительного давления необходимо обеспечить герметичность между краями маски и лицом ребенка. Круглая маска более герметично прилегает к лицу недоношенного ребенка с экстремально низкой массой тела (<1000 г), а для новорожденного с большей массой лучше использовать маску анатомической формы- Ее накладывают заостренным краем на нос ребенка.
NB! Основными критериями эффективности вентиляции легких является быстрое увеличение ЧСС и сатурации.
- Если эти показатели не возрастают, необходимо оценить данные аускультации легких с обеих сторон, обратить внимание на наличие и амплитуду экскурсий грудной клетки при каждом принудительном вдохе. Эффективной считается ИВЛ, при которой выслушиваются дыхательные шумы над обоими легочными полями и определяется экскурсия грудной клетки.
- Если грудная клетка новорожденного с каждым принудительным вдохом не движется и дыхательные шумы выслушиваются плохо, вентиляция неэффективна.
- Существуют три причины неэффективности вентиляции легких:
Недостаточная герметичность прилегания маски.
- Если слышно, как воздух выходит из-под краев маски, или если клиническое состояние новорожденного не улучшается, необходимо переустановить маску на лице ребенка, чтобы добиться ее более плотного прилегания, выдвинуть нижнюю челюсть немного вперед.
Заблокированы дыхательные пути ребенка:
- исправить положение головы;
- проверить полость рта, ротоглотку и нос на наличие посторонних предметов, провести эвакуацию содержимого, если это необходимо;
- попробовать вентилировать легкие, приоткрыв рот ребенка.
Недостаточное давление:
- Рекомендуется повысить создаваемое положительное давление в дыхательных путях. Использование манометра предотвращает риск создания избыточных объемов и давления в дыхательных путях, позволяет оценить податливость легких и выбрать параметры вентиляции. Для этого рекомендуется:
- Постепенно повышать давление (через каждые несколько принудительных вдохов), пока начнут выслушиваться дыхательные шумы над обоими легкими и появятся экскурсии грудной клетки с каждым принудительным вдохом. Зафиксировать давление, которое потребовалось для улучшения ЧСС, SpO2, выслушивания дыхательных шумов, отчетливых экскурсий грудной клетки.
- Если при использовании само расправляющегося мешка клапан сброса давления срабатывает или выпускает газ при давлении 40 см водн. ст., то можно заблокировать клапан сброса, чтобы создать более высокое давление.
- Если не удается достичь экскурсии грудной клетки и увеличения ЧСС, следует подумать об использовании приспособления для более эффективной проходимости дыхательных путей ─ эндотрахеальной трубки или ларенгиальной маски.
- Проведение принудительной вентиляции легких под положительным давлением мешком и маской в течение нескольких минут требует введения ротожелудочного зонда размером 8F, чтобы предупредить раздувание желудка газом и избежать компрессии диафрагмы, а также возможной регургитации и аспирации желудочного содержимого. Вводить зонд следует на глубину, соответствующую расстоянию от переносицы до мочки уха и от мочки уха до мечевидного отростка. После введения зонда в желудок шприцом отсасывают газ, зонд оставляют открытым и фиксируют лейкопластырем к щеке. ИВЛ немедленно возобновляют, наложив маску поверх зонда.
Оценка эффективности блока «В»
После 30 секунд вентиляции легких под положительным давлением или СРАР оценивают эффективность проведенных мероприятий, которая должна основываться на трех показателях:
● частота сердечных сокращений (ЧСС);
● частота дыхания;
● показатель сатурации.
Дальнейшие действия зависят от полученного результата.
Если определение ЧСС проводится по показанию пульсоксиметра, то вентиляцию в этот момент не прекращают. Если же ЧСС определяют с помощью аускультации, то вентиляцию останавливают на 6 секунд.
Дальнейшие действия зависят от полученного результата.
● Важнейшим признаком эффективного проведения принудительной вентиляции легких под положительным давлением и показанием к ее прекращению является увеличение частоты сердечных сокращений до 100 уд/мин и более, повышение насыщения крови кислородом (SpO2 соответствует целевому показателю в минутах) и появление спонтанного дыхания.
● Если ЧСС менее 100 уд/мин при отсутствии самостоятельного дыхания, продолжают ИВЛ при помощи маски.
● Если ЧСС составляет 60-99 в 1 мин, продолжают ИВЛ и готовят интубацию трахеи.
● Если попытка интубации оказалась безуспешной, отмечается выраженная брадикардия или в результате продолжительной попытки интубации снижается сатурация крови кислородом, рекомендуется начать ИВЛ при помощи маски
● Если ЧСС ˂60 в 1 мин, начинают непрямой массаж сердца, продолжают ИВЛ и предусматривают необходимость интубации трахеи.
Эффективность каждого последующего этапа оценивается по трем выше перечисленным показателям, но наиболее важным из них, определяющим переход к следующему этапу реанимации, является низкая частота сердечных сокращений.
Применяется ларингеальная маска у новорожденных с массой тела более 2000 г и сроком гестации ≥34 недель. При установке ларингеальной маски не требуется использование специальных инструментов для визуализации гортани. Ларингеальную маску устанавливают «Вслепую» и направляют на место пальцем врача.
Техника интубации трахеи:
Когда масочная вентиляция неэффективна и выполнение интубации трахеи затруднено или невозможно, применяют ларингеальную маску.
Такая ситуация может возникнуть при:
● врожденных аномалиях рта, губ или твердого неба, не позволяющих добиться плотного прилегания маски;
● аномалиях рта, языка, глотки или шеи, мешающие хорошему обзору гортани с помощью ларингоскопа;
● очень маленькая нижняя челюсть или относительно большой язык (синдром Робина и трисомия по 21 хромосоме).
Применяется ларингеальная маска у новорожденных с массой тела более 2000 г и сроком гестации ≥34 недель. При установке ларингеальной маски не требуется использование специальных инструментов для визуализации гортани. Ларингеальную маску устанавливают «Вслепую» и направляют на место пальцем врача.
Интубация трахеи.
Интубация трахеи показана:
● при подозрении на диафрагмальную грыжу;
● при атрезии пищевода у ребенка с потребностью в проведении ИВЛ;
● при неэффективной масочной ИВЛ;
● при необходимости проведения непрямого массажа сердца.
Техника интубации трахеи:
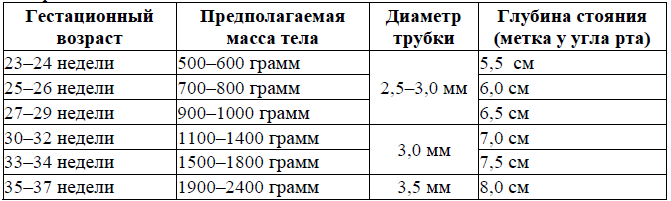
- Размер интубационной трубки следует подбирать на основании предполагаемой массы тела ребенка (таблица 2) [1,2,3].
- Размер голосовой щели ребенка может отличаться от стандартного, и при подготовке к интубации следует позаботиться о наличии трубок всех размеров. Перед интубацией следует убедиться в исправности ларингоскопа, источника кислорода и аппарата (мешка) ИВЛ.
- В родильном зале, как правило, используют технику интубации трахеи через рот. Ларингоскоп держат левой рукой, правой рукой открывают рот ребенка. Клинок ларингоскопа вводят через правый угол рта, продвигая по средней линии и отодвигая язык кверху и влево. При продвижении клинка внутрь находят первый ориентир – язычок мягкого нёба. Продвигая клинок ларингоскопа глубже, ищут второй ориентир – надгортанник. Конструкция клинка предусматривает возможность приподнять надгортанник кончиком ларингоскопа, при этом обнажается голосовая щель – третий ориентир.
- Интубационная трубка вводится через правый угол рта и продвигается в голосовую щель между связками. Через С-образную щель ларингоскопа осуществляют визуальный контроль продвижения трубки. Если использовался стилет, последний удаляют. Интубационную трубку соединяют с мешком или аппаратом ИВЛ, убедившись в правильном положении, фиксируют лейкопластырем.
Кроме указанной ниже таблицы 2, после взвешивания ребенка глубину стояния эндотрахеальной трубки можно перепроверить по формуле:
Таблица 2. Диаметр, глубина стояния интубационной трубки и размер катетера для санации в зависимости от массы тела и гестационного возраста новорожденного.

Метка у угла рта (см) = 6 см + масса тела в кг.
Возможно использование устройств для определения СО2 в выдыхаемом воздухе, что позволяет в 2 раза сократить время принятия решения о переинтубации в сложных случаях. Если трубка введена в трахею, то с самого начала ИВЛ индикатор показывает наличие СО2 в выдыхаемом воздухе. При эзофагальной интубации СО2 не определяется. Вместе с тем следует помнить, что СО2 также не будет определяться при ИВЛ через эндотрахеальную трубку в случае асистолии. При затруднениях интубации трахеи возможно использование ларингеальной маски.
Таблица 2. Диаметр, глубина стояния интубационной трубки и размер катетера для санации в зависимости от массы тела и гестационного возраста новорожденного.


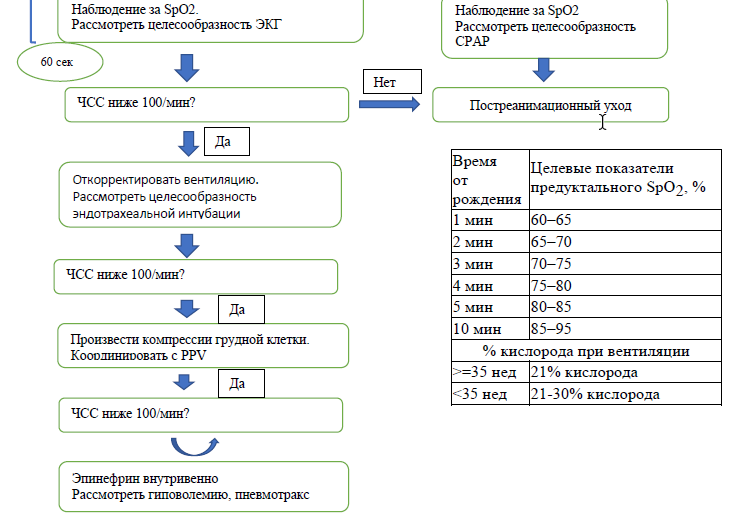
Использование кислорода:
- У детей, родившихся до завершения 28-й недели беременности, респираторную терапию следует начинать с FiО2 0,3. У детей, родившихся на 28–31-й неделе беременности, ИВЛ следует начинать с FiО2 0,21–0,3. У детей, родившихся на 32-й неделе беременности, ИВЛ следует начинать с FiO2 0,21 (В2) [14].
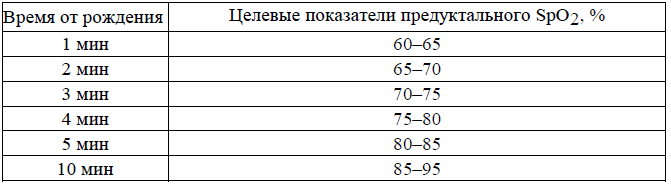
- Далее, с конца 1-й минуты жизни рекомендуется ориентироваться на показатели пульсоксиметра (таблица 3) и следовать описанному ниже алгоритму изменения концентрации кислорода.
- При нахождении показателей, определенных у ребенка, за пределами указанных значений, следует изменять (увеличивать/уменьшать) концентрацию дополнительного FiО2 ступенчато на 10–20% до достижения целевых показателей.
- При начале непрямого массажа сердца концентрацию О2 следует увеличить до 100%.
Таблица 3. Целевые показатели оксигенации крови по данным предуктального SpО2 первые 10 мин жизни (ILCOR, 2015)

Блок «С» ─ Circulation, поддержание кровообращения с помощью непрямого массажа сердца.
Показанием для проведения непрямого массажа сердца является ЧСС менее 60 уд/мин, несмотря на эффективную принудительную вентиляцию легких под положительным давлением в течение 30 секунд.
- Непрямой массаж сердца проводят надавливанием на нижнюю треть грудины.
- Используют две техники непрямого массажа, в соответствии с которыми компрессии грудины производят:
1) подушечками двух больших пальцев - при этом остальные пальцы обеих рук поддерживают спину (метод больших пальцев);
2) кончиками двух пальцев одной руки (второго и третьего или третьего и четвертого) - при этом вторая рука поддерживает спину (метод двух пальцев).
Оценка эффективности блока «С»:
- Глубина компрессий должна составлять одну треть переднезаднего диаметра грудной клетки, а частота - 90 в 1 мин.
- После каждых трех надавливаний на грудину проводят вентиляцию, после чего надавливания повторяют. За 2 сек. необходимо произвести 3 нажатия на грудину (90 в 1 мин) и одну вентиляцию (30 в 1 мин).
- Хорошо скоординированные непрямой массаж сердца и принудительную вентиляцию легких проводят каждые 30 секунд.
- Пульсоксиметр и монитор сердечного ритма помогут определить ЧСС, не прекращая проведение НМС:
Оценка эффективности блока «С»:
- Когда ЧСС достигнет более 60 уд/мин. следует прекратить НМС, но продолжить принудительную вентиляцию легких под положительным давлением с частотой 40-60 принудительных вдохов в минуту.
- Как только ЧСС станет более 100 уд/мин. и ребенок начнет самостоятельно дышать, следует постепенно уменьшать частоту принудительных вдохов и снижать давление вентиляции легких, а затем перенести ребенка в отделение интенсивной терапии для проведения постреанимационных мероприятий (терапевтическая гипотермия – см. ниже).
- Если частота сердечных сокращений остается менее 60 уд/мин, несмотря на продолжающиеся непрямой массаж сердца, скоординированный с принудительной вентиляцией легких под положительным давлением то переходят к блоку «D».
Блок «D» ─ введение медикаментов.
Введение эпинефрина, продолжая вентиляцию легких под положительным давлением и непрямой массаж сердца.
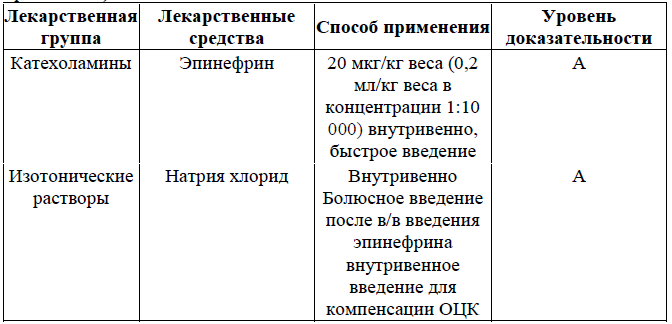
- Рекомендуемая доза эпинефрина при внутривенном введении новорожденным 20 мкг/кг веса (0,2 мл/кг веса в концентрации 1:10 000). Ее следует ввести как можно быстрее.
- Эндотрахеальное введение эпинефрина 0,1 мг/кг (1,0мл/кг).
- Если эпинефрин введен внутривенно через катетер, то вслед за ним надо болюсно ввести 3,0 мл физиологического раствора, чтобы обеспечить попадание всего объема препарата в кровоток.
- Если после введения 1-й дозы эпинефрина ЧСС остается менее 60 уд/мин, следует повторить введение препарата через 5 мин.
Необходимо дополнительно убедиться, что:
- Существует хороший воздухообмен, о чем свидетельствуют адекватная экскурсия грудной клетки и выслушивание дыхательных шумов над обоими легочными полями; если интубация трахеи еще не выполнена, следует ее провести;
- ЭТТ не сместилась при проведении реанимационных мероприятий;
- Компрессии осуществляются на глубину 1/3 переднезаднего диаметра грудной клетки; Они хорошо скоординированы с принудительной вентиляцией легких.
- Если ребенок не реагирует на проводимые реанимационные мероприятия и у него отмечаются признаки гиповолемического шока (бледность, слабый пульс, глухость сердечных тонов, положительный симптом «белого пятна»), или имеются указания на предлежание плаценты, вагинальное кровотечение или кровопотерю из сосудов пуповины, следует подумать о восполнении объема циркулирующей крови.
- Препаратом выбора, нормализующими ОЦК, являются 0,9% раствор натрия хлорида.
- Раствор для восполнения ОЦК вводится в пупочную вену в дозе 10-20 мл/кг струйно медленно в течение около 5-10 минут. Если после введения первой дозы, улучшение состояния ребенка не происходит, может потребоваться введение второй дозы раствора в том же объеме.
- Как только ЧСС станет более 100 уд/мин. и ребенок начнет самостоятельно дышать, следует постепенно уменьшать частоту принудительных вдохов и снижать давление вентиляции легких, а затем перенести ребенка в отделение интенсивной терапии для проведения постреанимационной помощи.
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
Прекращение реанимации:
- Если после выполнения всех реанимационных мероприятий у новорожденного не появятся сердечные сокращения, необходимо обсудить решение о прекращении реанимации с командой медицинских работников и членами семьи. Разумный период такого изменения целей реанимации составляет 20 минут после рождения.
Индикаторы эффективности процедуры:
- Индикатором эффективности реанимации новорожденных является быстрое увеличение ЧСС, улучшение состояния, появление самостоятельного дыхания.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- 1) Perlman JM, Wyllie J, Kattwinkel J, et al. Neonatal resuscitation: 2020 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. 2010. p. e1319–44. 2) 2020 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care, Part 5: Neonatal Resuscitation. 3) Wyckoff MH, Aziz K, Escobedo MB, et al. Part 13: Neonatal resuscitation: 2015. American Heart Association guidelines update for cardiopulmonary resuscitation and emergency cardiovascular care (reprint). Pediatrics. 2015;136(suppl 2): 196– 218. 4) Gungor S., Kurt E. et al. Oronasopharyngeal suction versus no suction in normal and term infants delivered by elective cesarean section: a prospective randomized controlled trial. Gynecpl. Obstet. Invest. 2006; 61:9-14. 5) Singh A, Duckett J, Newton T, Watkinson M. Improving neonatal unit admission temperatures in preterm babies: exothermic mattresses, polythene bags or a traditional approach? J Perinatol. 2010; 30:45-49. 6) Perlman J.M., Volpe J.J. Suctioning in the preterm infant: effects on cerebral blood flow velocity, intracranial pressure and arterial blood pressure. Pediatrics. 1983; 72:329- 334. 7) Wyllie J., Perlman J.M., Kattwinkel J., Wyckoff M.H., Aziz K., Guinsburg R., Kim H.S., Liley H.G., Mildenhall L., Simon W.M., Szyld E., Tamura M., Velaphi S.: Neonatal Resuscitation Chapter Collaborators. Part 7: Neonatal resuscitation: 2015 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Resuscitation. 2015; 95: e169-201. 8) Barber CA, Wyckoff MH. Use and efficacy of endotracheal versus intravenous epinephrine during neonatal cardiopulmonary resuscitation in the delivery room. Pediatrics. 2006 Sep;118(3):1028-34. 9) Jain L., Ferre C., Vidyasagar D., Nath S., Sheftel D. Cardiopulmonary resuscitation of apparently stillborn infants: survival and long-term outcome. J. Pediatr. 1991; 118::778-782. 10) Casalaz DM., Marlow N., Speidel B.D. Outcome of resuscitation following unexpected apparent stillbirth. Arch. Dis. Child Fetal Neonatal Ed. 1998; 78: F 112- F115. 11)Chalak, L. F. (2016). Perinatal asphyxia in the delivery room: Initial management and current cooling guidelines. NeoReviews, 17(8), e463-e470. 12) Sarnat HB, Sarnat MS. Neonatal encephalopathy following fetal distress. A clinical and electroencephalographic study. Arch Neurol 1976; 33(10):696–705 27 13) Shankaran S, Laptook AR, Ehrenkranz RA, et al. Whole-body hypothermia for neonates with hypoxic-ischemic encephalopathy. N Engl J Med 2005; 353(15):1574– 84. 14) Emery JR, Peabody JL. Head position affects intracranial pressure in newborn infants. J Pediatr 1983; 103(6):950–3. 15) Методическое письмо / под ред. проф. Е.Н. Байбариной. М., Реанимация и стабилизация состояния новорожденных детей в родильном зале, 2020г.
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1) Жубанышева Карлыгаш Биржановна – завевающая кафедрой неонатологии НУО «Казахстанско-Российский Медицинский университет», неонатолог-реаниматолог, высшая категория, профессор, Президент ассоциации неонатологов и специалистов детской медицины.
2) Бейсенбаева Зарина Джамбуловна – врач неонатолог-реаниматолог, высшей категории, ассистент кафедры неонатологии Казахстанско-Российского медицинского университета, г. Алматы.
3) Абентаева Ботагоз Абубакировна – UMC КФ «Центр материнства и детства», кандидат медицинских наук, врач неонатолог – реаниматолог, старший ординатор отделения реанимации новорожденных «Центр материнства и детства», г.Астана.
4) Ахмадьяр Нуржамал Садыр-кызы – доктор медицинских наук, профессор, заведующая кафедрой клинической фармакологии НАО «Медицинский университет Астана», врач - клинический фармаколог высшей категории.
Рецензенты:
Джаксалыкова Куляш Каликановна – доктор медицинских наук, врач-неонатолог, заведующая кафедрой неонатологии, профессор НАО «Медицинский университет Астана».
Указание условий пересмотра протокола: пересмотр протокола через 3-5 лет и/или при появлении новых методов диагностики и/или лечения с более высоким уровнем доказательности.
Алгоритм реанимации новорожденных
Перинатальные факторы риска, повышающие вероятность реанимации:
Контрольный список - чек лист оборудования по реанимации новорожденных



Указание на отсутствие конфликта интересов: нет.
Рецензенты:
Джаксалыкова Куляш Каликановна – доктор медицинских наук, врач-неонатолог, заведующая кафедрой неонатологии, профессор НАО «Медицинский университет Астана».
Указание условий пересмотра протокола: пересмотр протокола через 3-5 лет и/или при появлении новых методов диагностики и/или лечения с более высоким уровнем доказательности.
Приложение 1
Алгоритм реанимации новорожденных


Приложение 2
Перинатальные факторы риска, повышающие вероятность реанимации:

Приложение 3
Контрольный список - чек лист оборудования по реанимации новорожденных



Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.