Профилактика, диагностика и лечение инфекции, вызванной Candidozyma auris
 Версия: Клинические протоколы КР 2025 (Кыргызстан)
Версия: Клинические протоколы КР 2025 (Кыргызстан)
Общая информация
Краткое описание
к приказу МЗКР №1293
от 29 декабря 2025 г.
Министерство здравоохранения Кыргызской Республики
Кыргызская государственная медицинская академия им. И.К. Ахунбаева
Международная высшая школа медицины Кыргызско-Российский Славянский универсистет им. Б. Ельцина
Кыргызский государственный медицинский институт переподготовки и повышения квалификации им. С.Б. Даниярова
КЛИНИЧЕСКОЕ РУКОВОДСТВО ПО ПРОФИЛАКТИКЕ, ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ИНФЕКЦИЙ, ВЫЗВАННЫХ CANDIDOZYMA AURIS
Бишкек – 2025
Клиническая проблема: Инфекция, вызванная Candidozyma auris
Этапы оказания помощи: Амбулаторный и стационарный уровни здравоохранения
Цель создания Клинического руководства: Внедрение и организация системы единого подхода к профилактике, диагностике и лечению инфекции, вызванной Candidozyma auris, основанного на международных клинических руководствах высокого методологического качества, адаптированных к местным условиям.
Целевые группы: Инфекционисты, реаниматологи, семейные врачи/ВОП, хирурги, клинические микробиологи, эпидемиологи, врачи и медицинские сестры отделений (особенно ОРИТ, ожоговых, онкологических, отделений для пациентов с травмами), специалисты по инфекционному контролю, администрация организаций здравоохранения, сотрудники ФОМС, МЗ КР.
Дата создания: Данное Клиническое руководство по профилактике, диагностике и лечению инфекции, вызванной Candidozyma auris, разработано на основании данных по наилучшей клинической практике, в дальнейшем будет обновляться по мере появления новых доказательств.
ВВЕДЕНИЕ
Candidozyma auris включена в «группу критического приоритета» списка приоритетных грибковых патогенов Всемирной организации здравоохранения (ВОЗ), созданного для направления исследований, разработки и мер общественного здравоохранения [1].
C. auris – это новый патогенный дрожжевой грибок, впервые описанный в 2009 году у пациента в Японии [2], и впоследствии связанный с инвазивными инфекциями и вспышками в медицинских учреждениях по всему миру [3]. Большинство изолятов C. auris устойчивы к флуконазолу [4]. Эхинокандины являются препаратами выбора для лечения пациентов с инвазивной инфекцией C. auris, однако риск неэффективности терапии и рецидива инфекции после лечения выше при C. auris, чем при других видах Candida [5]. Кроме того, сообщалось о изолятах с множественной лекарственной устойчивостью, демонстрирующих различный уровень резистентности к амфотерицину B и эхинокандинами, а также о пан-резистентных штаммах C. auris [6–8]. Кандидемия, вызванная C. auris, ассоциирована с высокой летальностью, варьирующей от 29% до 62% [9]. Регулярная система надзора за грибковыми патогенами, включая Candidozyma auris, на уровне Европейского Союза в настоящее время отсутствует. Тем не менее, Европейский центр по профилактике и контролю заболеваний (ECDC) с 2018 года проводит периодические опросы, направленные на оценку эпидемиологической ситуации, лабораторных возможностей и уровня готовности государств-членов к выявлению и контролю C. auris. Последний, четвёртый опрос был выполнен в 2024 году и включает данные о случаях заболевания, зарегистрированных до конца 2023 года [10].
Candida auris (C. auris) — это инвазивный, мультирезистентный дрожжевой грибок, представляющий серьезную глобальную угрозу для общественного здоровья. Его ключевые особенности — устойчивость к противогрибковым препаратам, способность к длительной персистенции в условиях больничной среды и вызывание вспышек с высокой летальностью.
Настоящее руководство призвано унифицировать подходы к противодействию C. auris в организациях здравоохранения.
Актуальность проблемы обусловлена быстрым глобальным распространением C. auris, высоким уровнем смертности при инвазивных формах инфекции, а также ограниченными терапевтическими возможностями. Всемирная организация здравоохранения включила C. auris в группу критически важных приоритетных грибковых патогенов (Critical Priority Group), что подчёркивает необходимость разработки национальных и международных мер по раннему выявлению, контролю и лечению инфекции.
Особенности патогена, включая мульти- и панрезистентность, выраженную устойчивость к дезинфицирующим средствам, сложность лабораторной идентификации и высокий потенциал межпациентской передачи, требуют разработки строгих протоколов инфекционного контроля и готовности лечебных организаций к своевременному реагированию.
Данное руководство направлено на систематизацию современных знаний о C. auris и формирование стандартизированных подходов к профилактике, диагностике, лечению и эпидемиологическому надзору.
Этиология и патогенез
Эпидемиология
Глобальное распространение характеризуется несколькими генетическими квазиклонами, возникавшими почти одновременно в разных регионах мира. Это указывает не на один источник происхождения, а на множественные независимые события появления и адаптации патогена.
В Европе эпидемиологическая ситуация отслеживается Европейским центром по профилактике и контролю заболеваний (ECDC). С 2018 по 2024 годы ECDC провёл четыре масштабных опроса стран-членов, направленных на оценку числа случаев, лабораторной готовности и уровня организации инфекционного контроля. Последний опрос (2024 г.) выявил нарастающее количество эпизодов инфекции и колонизации, расширение географии случаев и улучшение, но всё ещё недостаточную готовность лабораторной сети.
В странах СНГ сообщения о выявлении C. auris остаются ограниченными, что может быть связано как с реальным низким уровнем распространения, так и с трудностями лабораторного подтверждения. Ввиду глобального движения населения и межгоспитальных переводов пациентов риск заноса в регион оценивается как умеренный, требующий усиления лабораторной диагностики и эпиднадзора.
К основным факторам распространения C. auris относятся:
• длительная госпитализация и высокая плотность пациентов;
• недостаточные меры инфекционного контроля;
• недостаточная идентификация дрожжей до вида;
• внутрибольничное распространение через загрязнённые поверхности и оборудование;
• международные перемещения пациентов, особенно из регионов с высокой заболеваемостью.
Эти данные подчёркивают необходимость формирования устойчивой системы обнаружения, реагирования и профилактики, особенно в странах, где надзор за грибковыми патогенами находится на начальном этапе развития. Candidozyma auris представляет собой одну из наиболее значимых угроз современной клинической микологии. За последние годы этот дрожжевой патоген стал причиной многочисленных внутрибольничных вспышек, характеризующихся трудностями в диагностике, высокой устойчивостью к противогрибковым препаратам и способностью к длительной персистенции в условиях стационара.
Актуальность проблемы обусловлена быстрым глобальным распространением C. auris, высоким уровнем смертности при инвазивных формах инфекции, а также ограниченными терапевтическими возможностями. Всемирная организация здравоохранения включила C. auris в группу критически важных приоритетных грибковых патогенов (Critical Priority Group), что подчёркивает необходимость разработки национальных и международных мер по раннему выявлению, контролю и лечению инфекции.
Данное руководство направлено на систематизацию современных знаний о C. auris и формирование стандартизированных подходов к профилактике, диагностике, лечению и эпидемиологическому надзору.
Клиническая картина
Cимптомы, течение
РЕКОМЕНДАЦИИ ПО КЛИНИЧЕСКОЙ ДИАГНОСТИКЕ
Клинические проявления
Бессимптомная колонизация
Колонизированные пациенты являются основным резервором внутрибольничной передачи, даже при отсутствии симптомов.
Инвазивные инфекции
Основные клинические формы:
Кандидемия (fungemia) — наиболее частая форма, характеризуется лихорадкой, сепсисом, нарушениями со стороны кровообращения;
Сепсис, ассоциированный с C. auris, нередко рефрактерный к стандартной терапии;
Инфекции кровотока, связанные с катетерами, центральными линиями, порт-системами;
Диссеминированная инфекция с поражением внутренних органов.
Очаговые инфекции и поражения отдельных систем
| Клинические проявления | Особенности поражения |
| Инфекции мочевыводящих путей |
чаще протекают в форме колонизации;
могут переходить в симптоматические формы у ослабленных пациентов;
усугубляются при наличии длительного катетера.
|
| Инфекции дыхательных путей |
характерны для пациентов на искусственной вентиляции лёгких;
могут проявляться как вентилятор-ассоциированные инфекции;
требуют исключения смешанной бактериально-грибковой инфекции.
|
| Инфекции ран и послеоперационных швов |
могут быть причиной хронического инфекционного процесса;
нередко выявляются при вспышках в хирургических отделениях и ожоговых центрах.
|
| Поражения кожи и мягких тканей |
обычно возникают на фоне колонизации кожи;
требуют комплексного лечения, включая тщательную местную обработку
|
| С |
Рекомендуется обратить внимание на следующие группы риска [11-13]:
онкологические пациенты на химиотерапии;
пациенты после трансплантации органов и тканей;
пациенты на длительной кортикостероидной терапии;
пациенты с тяжёлыми формами COVID-19, получающие иммуносупрессивное лечение;
ВИЧ-инфицированные с низким CD4.
|
Диагностика
Цель оценки
Первичная: Экстренно определить тяжесть состояния пациента и необходимость проведения реанимационных мероприятий или перевода в ОРИТ.
Динамическая: Оценить эффективность проводимой терапии, выявить ранние признаки прогрессирования инфекции или развития осложнений, определить ответ на лечение.
РЕКОМЕНДАЦИИ ПО ПЕРВИЧНОЙ ОЦЕНКЕ
| С | Рекомендуется проводить оценку не реже 2 раза в сутки у стабильных пациентов и каждые 1-4 часа у нестабильных [11-13] (см. Приложение 1) |
| С | Рекомендуется провести экстренную оценку по системе ABCDЕ для выявления неотложных состояний в первые часы (30-60 мин) [11-13] |
Экстренная оценка по системе ABCDE:
A (Airway) – Дыхательные пути: Признаки обструкции? Отек? Необходимость интубации?
B (Breathing) – Дыхание:
- Частота дыхательных движений (ЧДД): Тахипноэ (>22 в мин.) — ранний маркер сепсиса.
- Сатурация кислорода (SpO2): <94% на воздухе — признак дыхательной недостаточности.
C (Circulation) – Кровообращение:
- Артериальное давление (АД): Систолическое АД < 100 мм рт. ст. или снижение на >40 мм рт. ст. от обычного.
- Частота сердечных сокращений (ЧСС): Тахикардия > 90 в мин.
- Периферическая перфузия: Холодные конечности, время капиллярного наполнения > 2 сек.
- ЦВД (при наличии доступа): Для оценки волемического статуса.
D (Disability) – Неврологический статус:
- Шкала комы Глазго (ШКГ): Снижение сознания (ШКГ < 15) — грозный признак.
- Спутанность, возбуждение (особенно у пожилых).
E (Exposure/Examination) – Осмотр:
- Поиск очага инфекции: осмотр всех катетерных мест, послеоперационных ран, дренажей.
- Осмотр кожи: высыпания, следы инъекций, целлюлит.
| С |
Рекомендуется провести быструю оценку по шкале qSOFA (Quick SOFA) при подозрении на сепсис [11-13]: ЧДД ≥ 22/мин. Изменение сознания (ШКГ < 15). Систолическое АД ≤ 100 мм рт. ст. ≥2 балла — высокий риск неблагоприятного исхода, требует углубленной оценки |
| С | Рекомендуется провести оценку органной дисфункции в ОРИТ используя шкалу SOFA (Sequential Organ Failure Assessment) [11-13] |
| С | Рекомендуется провести комплексную оценку витальных функций используя шкалу NEWS-2 (National Early Warning Score 2) [11-13] |
| С |
Рекомендуется уточнить наличие специфических факторов риска для C. auris [11-13]: Недавнее пребывание в зарубежном стационаре или ОРИТ. Предшествующая длительная или неадекватная противогрибковая терапия. Наличие множественных дренажей, катетеров, трахеостомы. |
РЕКОМЕНДАЦИИ ПО ДИНАМИЧЕСКОЙ ОЦЕНКЕ (МОНИТОРИНГ ЭФФЕКТИВНОСТИ ТЕРАПИИ)
| С |
Рекомендуется оценивать следующие клинические критерии минимум 2 раза в суткиs [11-13]: Температурная кривая: Стойкая или рецидивирующая лихорадка >38°C после 72-96 часов адекватной терапии — тревожный признак неэффективности. Гемодинамика: Стабилизация АД и ЧСС, снижение потребности в вазопрессорах. Неврологический статус: Улучшение сознания. Состояние очага: Уменьшение гиперемии, отека, отделяемого из ран/катетерных мест. |
| С |
Рекомендуется оценивать следующие лабораторные критерии [11-13]: Посевы крови: Время до первой отрицательной гемокультуры. Персистирование положительных посевов >3-5 дней — показатель неэффективности лечения. Маркеры воспаления: - Прокальцитонин (ПКТ): Наиболее специфичен для бактериальных инфекций, но может повышаться. Динамическое снижение — благоприятный признак. - С-реактивный белок (СРБ): Менее специфичен. Снижение на 25-50% от пикового значения к 3-5 дню терапии — критерий эффективности. - Лактат крови: Нормализация уровня (<2 ммоль/л) — ключевая цель реанимации при септическом шоке. Органные функции: Креатинин, билирубин, диурез, количество тромбоцитов. |
| С |
Рекомендуется провести следующие инструментальные методы исследования (активный скрининг) [11-13]: Эхокардиография (ЭхоКГ): Для исключения инфекционного эндокардита при персистирующей кандидемии (>3-5 дней) или появлении новых шумов. Офтальмологический осмотр: Обязателен всем пациентам с кандидемией для исключения эндофтальмита (осмотр с расширенным зрачком). УЗИ/КТ брюшной полости: При подозрении на абсцессы печени, селезенки (редко). КТ грудной клетки/МРТ головного мозга: При соответствующей симптоматике. |
| С |
Рекомендуется провести следующие лабораторные исследования для оценки состояния пациента [11-13]: Посев крови. Маркеры воспаления: - Прокальцитонин (ПКТ). - С-реактивный белок (СРБ) - Лактат крови Креатинин; Билирубин; ОАК и количество тромбоцитов. |
Лабораторная диагностика Candidozyma auris представляет собой один из наиболее критических элементов системы инфекционного контроля. Ошибки идентификации приводят к задержке диагностики, отсутствию своевременных мер IPC и распространению патогена внутри стационара. Настоящий раздел описывает современные методы обнаружения, типичные проблемы диагностики и рекомендуемые алгоритмы.
Общие принципы
Высокая настороженность: C. auris следует подозревать у пациентов групп риска с клиническими признаками инвазивного кандидоза, особенно при отсутствии ответа на стандартную эхинокандиновую терапию.
Важность видовой идентификации: Рутинные методы лабораторной диагностики кандидозов часто ошибочно идентифицируют C. auris как другие виды (например, C. haemulonii, C. famata, Saccharomyces cerevisiae). Целенаправленная идентификация обязательна.
Двухуровневая диагностика: Скрининг на колонизацию + диагностика инвазивной инфекции.
| С |
Рекомендуется проводить целенаправленное обследование на C. auris следующим группам риска [11-13]: Пациенты с клинической картиной инвазивного кандидоза (кандидемия, диссеминированная инфекция), не отвечающие на первую линию противогрибковой терапии. Пациенты, ранее госпитализированные за пределами региона/страны, особенно в стационары, где регистрировались случаи C. auris. Пациенты, находящиеся в ОРИТ длительное время (более 14 дней). Пациенты с ослабленным иммунитетом (онкогематологические, после трансплантации). Пациенты с обширными ожогами, после обширных операций, с центральными венозными катетерами, на ППП. Контактные пациенты в очаге выявленной инфекции/колонизации C. auris. |
Точность диагностики улучшилась после разработки хромогенных сред специально для C. auris и усовершенствования спектральных баз данных систем матрично-ассоциированной лазерной десорбционной ионизационной масс-спектрометрии с измерением времени пролета (MALDI-TOF MS).
- Материал: Мазки с кожи (композитный мазок с обеих подмышечных впадин и паха). Дополнительно: мазки из ноздрей, прямой кишки, области вокруг стом/трахеостом, места установки дренажей/катетеров.
- Техника: Использование транспортной среды (например, Amies) или немедленная доставка в лабораторию.
Для диагностики инвазивной инфекции:
- Кровь: Забор во флаконы для гемокультур (предпочтительно автоматические системы типа BACTEC, BacT/ALERT). C. auris может давать поздний или слабый рост.
- Другие стерильные жидкости: Ликвор, синовиальная, перитонеальная жидкость, биоптаты тканей – в стерильных контейнерах.
- Моча, мокрота, отделяемое ран: Могут указывать на колонизацию или локальную инфекцию.
Посев на стандартные среды (Сабуро, кровяной агар) и хромогенные селективные среды (например, CHROMagar™ Candida, с дополнительным солением). C. auris растет при 37-42°C, что является диагностическим признаком.
Внешний вид колоний: Часто кремовые, розовато-мероватые, матовые, гладкие, через несколько дней могут становиться розоватыми с вариабельной текстурой.
Морфология не является надёжным критерием, поэтому требуется подтверждение
2. Методы видовой идентификации:
МЕТОД ВЫБОРА: Масс-спектрометрия с лазерной десорбцией и ионизацией (MALDI-TOF MS). Требование: Обязательно использование актуальных коммерческих баз данных (Vitek MS v3.0, Bruker Biotyper с базой, содержащей C. auris). Старые базы не идентифицируют данный вид.
Молекулярные методы (высокоспецифичные и чувствительные):
- ПЦР в реальном времени (RT-PCR) с вид-специфичными праймерами – самый быстрый метод (результат за несколько часов).
- Секвенирование генов рибосомальной ДНК (ITS, D1/D2 регионы 28S рДНК) или других генов-мишеней – "золотой стандарт" для подтверждения.
Традиционные биохимические системы (НЕНАДЕЖНЫ):
| С | Рекомендуется использовать для видовой идентификации метод Масс-спектрометрия с лазерной десорбцией и ионизацией (MALDI-TOF MS) [11-16] |
MALDI-TOF является золотым стандартом для рутинной лабораторной идентификации
Подходы:
Молекулярные методы используют для:
| С | Рекомендуется проводить молекулярное типирование по время вспышки для определения штаммов и путей передачи наиболее точными методами – ПЦР и полногеномное секвенирование [11-16] |
Полногеномное секвенирование позволяет проводить генетический анализ штаммов с высоким разрешением, включая идентификацию механизмов устойчивости к противогрибковым препаратам, филогенетические исследования и поддержку эпидемиологического надзора и управления вспышками заболевания.
Условия для проведения полногеномного секвенирования C. Auris необходимо создать в ДПЗиГСЭН.
Метод: Предпочтение отдается методу бульонного микроразведения согласно стандартам EUCAST или CLSI.
Минимальный набор АФТ для тестирования:
- Азолы: Флуконазол, вориконазол, позаконазол, итраконазол.
- Эхинокандины: Каспофунгин, микафунгин, анидулафунгин.
- Полиены: Амфотерицин В.
Интерпретация: Следовать актуальным клиническим наборам EUCAST/CLSI. Отчет должен включать конкретные значения МПК (минимальной подавляющей концентрации).
Определение MПК (минимальной подавляющей концентрации) обязательно для выбора терапии
Диагностика C. auris требует перехода от рутинных методов к целенаправленному использованию современных технологий (MALDI-TOF MS, ПЦР). Промедление или ошибка в идентификации ведут к катастрофическим последствиям для пациента и риску внутрибольничной вспышки.
Рекомендации по скринингу
| С | Рекомендуется использовать для скрининга колонизации следующие материалы – мазок с кожи подмышечных впадин и паха, ноздрей, прямой кишки, области вокруг стом/трахеостом, мест установки дренажей/катеторов [11-16] |
| С | Рекомендуется проводить скрининг при подтвержденном случае C. auris, подозрении на вспышку и межгоспитальном переводе пациента из учреждения, где C. auris ранее выявлялась [11-16] |
| С |
Рекомендуется проводить скрининг по следующей схеме [11-16]:
Первичный скрининг — день 0.
Повторный скрининг — через 48 часов.
Контрольный скрининг — на 7-й день.
Еженедельный скрининг — в отделениях ОРИТ.
|
Рекомендации по диагностике инвазивной диагностике
| С | Рекомендуется использовать для диагностики инвазивной инфекции следующие материалы – кровь, ликвор, перитонеальная жидкость, биоптаты тканей, моча, мокрота, отделяемое ран, которые необходимо хранить при температуре -800С [11-16] |
| С | Рекомендуется для подтверждения C. auris метод диагностики MALDI-TOF MS [11-16] |
| С | Рекомендуется немедленно направить все подозрительные изоляты в референс-лабораторию с маркировкой «подозрение на C. auris», если MALDI-TOF недоступен [11-13] |
| С | Рекомендуется немедленно направить все подозрительные изоляты в референс-лабораторию с маркировкой «подозрение на C. auris» [11-13] |
| С | Рекомендуется проводить ПЦР/секвенирование при сложных случаях [11-13] |
| С | Рекомендуется определять МПК для всех клинически значимых изолятов [11-13] |
| С | Рекомендуется проводить контроль эрадикации с и интервалом 24-48 часов из разных локализаций (минимум три отрицательных результата) [11-13] |
Рекомендации по алгоритмы ведения в случае выявления Candidozyma auris
| С | Рекомендуется немедленно уведомить лечащего врача и службы инфекционного контроля по телефону при подозрении на C. auris на основе морфологии колоний и роста при 42°C [11-13] |
| С | Рекомендуется срочно оформить официальное заключение с указанием вида и профиля резистентности после идентификации и получения данных АФТ [11-13] |
| С | Рекомендуется проводить маркировку всех образцов и заключения должны иметь пометку «Candida auris – особые меры предосторожности» [11-13] |
| С | Рекомендуется вести обязательный журнал учета с указанием даты выделения, локализации, предварительных результатов и подтвержденных случаев [11-13] |
| С | Рекомендуется проводить обучение всех сотрудников лабораторной службы и специалистов инфекционного контроля [11-13] |
Дифференциальный диагноз
Дифференциальная диагностика
Поражения, вызванные C. auris, необходимо дифференцировать с:
Корректная идентификация вида является критически важной, поскольку тактика лечения C. auris значительно отличается от лечения других дрожжевых инфекций.
Лечение
Общие принципы лечения:
Высокий уровень резистентности: C. auris часто демонстрирует устойчивость к нескольким классам противогрибковых препаратов (азолам, полиенам, эхинокандинам). Эмпирическая терапия без данных о чувствительности недопустима.
Первостепенное значение контроля очага: Удаление или замена инфицированных/колонизированных устройств (центральные венозные катетеры, мочевые катетеры, дренажи) является обязательным и часто более критичным, чем медикаментозная терапия.
Комбинированная терапия: Рассматривается как опция для тяжелых, персистирующих инфекций или при МЛУ (множественной лекарственной устойчивости).
Мониторинг эффективности: Оценка клинического и микробиологического ответа должна проводиться регулярно. Неэффективность начальной схемы требует немедленного пересмотра на основании данных АФТ (антифунгальной чувствительности).
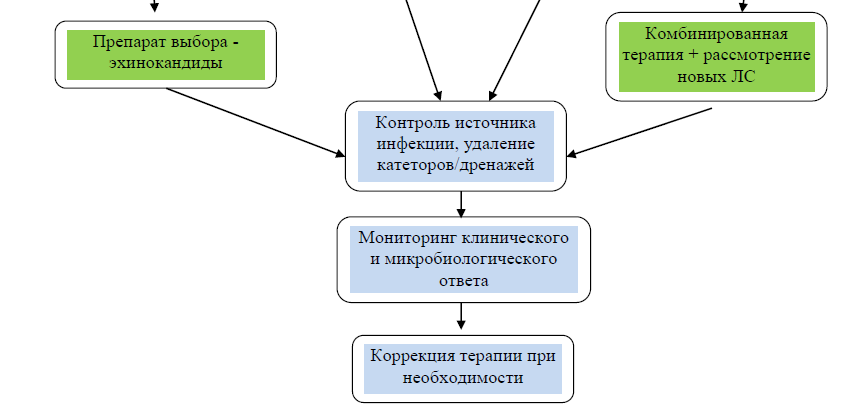
I. При чувствительности к эхинокандинам (предпочтительный сценарий):
Препараты выбора: Анидулафунгин, Каспофунгин, Микафунгин.
Стандартные дозы эхинокандинов
| Препарат выбора | Взрослые | Дети |
| Анидулафунгин | Нагрузочная доза 200 мг в/в, затем 100 мг в/в 1 раз/сут | Нет данных |
| Каспофунгин | Нагрузочная доза 70 мг в/в, затем 50 мг в/в 1 раз/сут | 70 мг/м²/сут (макс. 70 мг/сут) |
| Микафунгин | 100 мг в/в 1 раз/сут | 2–4 мг/кг/сут (до 10 мг/кг/сут при тяжёлых формах) |
Обоснование: Эхинокандины демонстрируют наилучшую активность in vitro и in vivo в большинстве регионов и являются препаратами первой линии.
Основные причины неудач:
II. При резистентности к эхинокандинам, но чувствительности к другим классам
| Альтернативные препараты | Дозировка | Примечание |
| Липосомальный амфотерицин В (л-АмБ) | 3-5 мг/кг в/в 1 раз/сут | Препарат выбора при резистентности к эхинокандинам, но чувствительности к амфотерицину В. Нефротоксичность ниже, чем у классического АмБ |
| Фосфлуконазол (при подтвержденной чувствительности in vitro!) | Нагрузочная доза 800 мг (12 мг/кг) в/в/перорально, затем 400 мг (6 мг/кг) в/в/перорально 1 раз/сут. | Более 90% изолятов C. auris устойчивы к флуконазолу. Использование фосфлуконазола оправдано только при доказанной чувствительности и невозможности применять другие препараты |
III. При множественной лекарственной устойчивости (МЛУ) или отсутствии альтернатив
| Стратегия 1: Комбинация высоких доз эхинокандина + липосомальный АмБ | Стратегия 2: Новые противогрибковые препараты |
| Рациональное: Синергизм in vitro, возможность преодоления умеренно повышенных МПК |
Изавуконазол: Может сохранять активность против некоторых штаммов, устойчивых к другим азолам. Требует подтверждения чувствительности.
Доза: нагрузочная 200 мг в/в/перорально каждые 8 часов (2 дня), затем 200 мг 1 раз/сут
|
| Микафунгин в дозе 150 мг/сут + Л-АмБ в дозе 5 мг/кг/сут |
Манногептулоза (Ibrexafungerp):
Первый представитель нового класса (глюкан-синтазные ингибиторы, тритерпеноиды). Может быть активен против эхинокандин-резистентных штаммов.
Применяется по специальным протоколам
|
Инфекции центральной нервной системы
| С | Рекомендуется назначить комбинацию высоких доз л-АмБ (5 мг/кг/сут) с фосфлуконазолом (если чувствителен) или вориконазолом в течение более, чем 4-6 недель под контролем ликвора и санации источника инфекции [11-13] |
| С | НЕ Рекомендуется назначать монотерапию эхинокандинами, т.к. они плохо проникают через ГЭБ [11-13] |
Инфекции мочевыводящих путей:
| С | Рекомендуется удалить катетер и назначить амфотерицин В или фосфлуконазол (при чувствительности) в связи с высокой концентрацией в моче при отсутствии инвазии паренхимы почек [11-13] |
Кандидемия
| С | Рекомендуется назначить эхинокандин в течении не менее 14 дней после клинического улучшения и устранении источника инфекции [11-13] |
Инфекции ран и мягких тканей
| С | Рекомендуется назначить эхинокандин и провести местную обработку с возможным переходом на амфотерицин В при отсутствии положительной динамики [11-13] |
Деэскалация: При стабилизации состояния и получении данных о чувствительности возможен переход с комбинированной терапии на монотерапию наиболее активным препаратом.
Длительность терапии
| С | Рекомендуется проводить дэслакационную терапию минимум 14 дней после первого отрицательного посева крови и разрешения симптомов при кандидемии [11-13] |
| С | Рекомендуется проводить дэслакационную терапию от 4 до 12 недель и более в зависимости от локализации, контроля очага и клинического ответа при других инвазивных инфекциях (перитонит, эндокардит, остеомиелит) [11-13] |
РЕКОМПЕНДАЦИИ ПО САНАЦИИ (“ДЕКОЛОНИЗАЦИИ”)
| D | НЕ РЕКОМЕНДУЕТСЯ рутинно использовать меры санации (“деколонизации”), т.к. эффективность ограничена [11-13] |
Может рассматриваться в индивидуальном порядке у пациентов с длительной колонизацией кожи для снижения риска передачи.
| D | Рекомендуется применять ежедневно местные антисептики (хлоргекседин для мытья тела, назально мупироциновая мазь) в сочетании с санацией кишечника нистатином или амфотерицином В (перорально) [11-13] |
Успех данного метода санации не гарантирован.
Критерии эффективности и неэффективности терапии
Критерии эффективности:
нормализация температуры в течение 72 часов;
улучшение гемодинамики;
отрицательные повторные посевы крови/материала из очага;
разрешение клинических симптомов
Причины неэффективности: Неадекватный источник-контроль, неверный выбор препарата (резистентность), недостаточная дозировка, глубокая иммуносупрессия.
Критерии неэффективности терапии (требующие срочного пересмотра тактики)
Ухудшение гемодинамики, нарастание потребности в вазопрессорах.
Персистирующая или рецидивирующая лихорадка после 96-120 часов терапии.
Положительные посевы крови на 4-5 день и позже.
Появление новых метастатических очагов инфекции.
Нарастание органной дисфункции (повышение креатинина, билирубина, падение тромбоцитов).
Профилактика
Цель: Полностью предотвратить или максимально ограничить внутрибольничную передачу C. auris в медицинской организации, минимизировав риск вспышек.
Ключевой принцип: C. auris отличается исключительной устойчивостью в окружающей среде и способностью колонизировать кожу. Стандартные меры предосторожности недостаточны.
Требуется строгий, многоуровневый подход.
| D |
Рекомендуется размещать пациента с подозрением/подтвержденной инфекцией C. auris в отдельной палате с отдельным санузлом (душем/туалетом) [11-13]
|
Приоритет — палаты с предвариттельной дезинфекцией. Все средства для ухода тщательно очищаются и дезинфицируются в соответствии с инструкциями производителя, включая соблюдение рекомендуемого времени контакта с дезинфицирующими растворами, а также с Приложением 21 к Инструкции по ИК.
Контактные меры предосторожности
| D |
Рекомендуется обязательно использовать СИЗ для всего персонала и посетителей перед входом в палату [11-13]:
Халат (одноразовый или многоразовый, предназначенный только для этой палаты). Перчатки. Смена перчаток после контакта с потенциально контаминированными поверхностями. Маска (хирургическая или процедурная). При проведении манипуляций, генерирующих аэрозоль (туалет трахеи), — респиратор типа N95. |
Использование средства индивидуальной защиты (СИЗ) C. auris распространяется через прямой контакт с колонизированными или инфицированными пациентами. Рекомендуется соблюдать меры предосторожности, используемые для профилактики контактного пути передачи с использованием следующих СИЗ:
˗ Перчаток в соответствии с гл. 3 п. 36-39 «Инструкции по ИК»;
˗ Халатов в соответствии с гл. 3 п. 42 «Инструкции по ИК». Когда ожидаются мероприятия по уходу за пациентом с высокой степенью риска, которые могут привести к длительному контакту пациента с одеждой медицинского работника или открытой кожей необходимо использовать халаты с длинными рукавами.
˗ Фартуки в случаях, когда проводятся процедуры с предполагаемым разбрызгиванием биологических жидкостей и/или уходе за пациентом с кожными или слизистыми поражениями
СИЗ следует надевать после проведения обработки рук перед контактом с пациентом или перед входом в палату пациента.
Обработка рук
C. auris демонстрирует повышенную устойчивость к спиртсодержащим антисептикам.
| D |
Рекомендуется проводить обязательную обработку рук [11-13]:
Мытье рук с мылом и водой с последующим нанесением спиртсодержащего антисептика;
После снятия перчаток и халата, перед выходом из палаты и перед контактом с другим пациентом
|
Для снижения риска передачи C. auris через руки медперсонал должен соблюдать требования гигиены рук в соответствии с гл.3, п.25-41 «Инструкции по ИК» (уровень доказательности А). При выполнении гигиенической антисептики рук необходимо использовать спиртосодержащий антисептик заводского изготовления.
Обработка окружающей среды и оборудования (приоритетное направление)
C. auris может сохраняться на поверхностях неделями и месяцами, устойчив к многим дезинфектантам.
| D |
Рекомендуется использовать для ежедневной и заключительной дезинфекции средства на основе хлора (например, гипохлорит натрия с концентрацией не менее 1000 ppm, или перекиси водорода) [11-13]
|
Уборка помещений в организациях здравоохранения проводится в соответствии с требованиями гл. 17 Инструкции по ИК.
Кварцевание (УФО) является вспомогательным методом и не заменяет химическую дезинфекцию.
Особое внимание: Обработка всех высококонтактных поверхностей (кнопки, поручни кровати, столики, раковины, туалет), а также пола, стен вокруг кровати и оборудования.
Обработка многоразового медицинского оборудования:
Термометры, манжеты для измерения АД, стетоскопы, глюкометры должны быть индивидуальными для пациента или подвергаться тщательной дезинфекции после каждого использования.
После выписки пациента оборудование (тонометры, мониторы) должно пройти камерную дезинфекцию.
Постельные принадлежности и отходы: Обрабатываются как потенциально инфицированные. Белье помещается в герметичные пакеты в палате.
Обращение с чистым бельем, его обработка, транспортировка и хранение должны осуществляться в соответствии с СанПиН "Санитарно-эпидемиологические требования к лечебно-профилактическим организациям", утвержденные постановлением Правительства КР от 11 апреля 2016 года № 201, обеспечивая постоянное отделение чистого белья от использованного.
Скрининг и наблюдение за контактами
Цель: Определить масштаб бессимптомной колонизации.
| D |
Рекомендуется провести скрининг всех пациентов, находящихся в одной палате/боксе с выявленным случаем, а также пациентов, имевших прямой контакт без средств защиты [11-13]
|
| D |
Рекомендуется использовать метод – взятие соскоба/мазка из обоих подмышечных впадин и паха [11-13]
|
Когортное размещение: При выявлении нескольких случаев возможно размещение колонизированных/инфицированных пациентов в одном отделении (когорте) с выделением отдельного персонала.
Рекомендации по управлению перемещениями пациента
Ограничить перемещения пациента за пределы палаты до минимума.
При необходимости транспортировки (на исследования) заранее уведомить принимающее отделение/кабинет.
Пациент должен быть в чистом халате, накрыт чистой простыней.
После транспортировки маршрут и кабинет должны быть продезинфицированы.
Политика применения антимикробных препаратов
| D |
Рекомендуется провести аудит назначений антибиотиков широкого спектра и противогрибковых препаратов в отделении, где выявлен случай [11-13]
|
| D |
Рекомендуется максимально сузить спектр или отменить необоснованную эмпирическую терапию для снижения селективного давления и риска дальнейшей колонизации [11-13]
|
Критерии для прекращения мер предосторожности
| D |
Рекомендуется соблюдать меры изоляции и контактные меры предосторожности на всем протяжении госпитализации [11-13]
|
Решение о "снятии" с учета принимается редко и индивидуально, обычно только для хронических носителей при переводе в учреждения длительного ухода.
| D |
Рекомендуется принимать решения о «снятии с учета» при следующих обстоятельствах [11-13]:
не менее трех последовательных отрицательных результатов скрининговых мазков (из подмышечных впадин и паха), взятых с интервалом не менее 1 недели, при отсутствии противогрибковой терапии.
отсутствия открытых ран, дренажей, трахеостом.
|
Коммуникация и документация
| D |
Рекомендуется проводить маркировку историй болезней, назначений и палаты [11-13]
|
| D |
Рекомендуется обязательное письменное информирование следующего учреждения/врача о статусе C. auris при переводе или выписке пациента [11-13]
|
| D |
Рекомендуется проведение обязательного эпидемиологического расследования - установление возможного источника, оценка соблюдения протоколов, молекулярное типирование изолятов для подтверждения связи случаев [11-13]
|
| D |
Рекомендуется проведение обязательного инструктажа всего персонала отделения (врачи, медсестры, санитарки) по специфике C. auris, правилам использования СИЗ, обработке рук и поверхностей [11-13]
|
Можно развесить плакаты-напоминалки на входах в палаты.
Меры инфекционного контроля проводятся в соответствии с «Инструкцией по инфекционному контролю в организациях здравоохранения Кыргызской Республики», утвержденное постановлением Кабинета Министров Кыргызской Республики от 12 декабря 2023 года № 663 (далее Инструкция по ИК).
Информация
Источники и литература
-
Клинические протоколы Министерства здравоохранения Кыргызской Республики
- 1. Satoh K, et al. Candida auris, a novel species isolated from the external ear canal of an inpatient in Japan. Microbiol Immunol. 2009. 2. Lockhart SR, et al. Simultaneous emergence of multidrug-resistant Candida auris on three continents. Clin Infect Dis. 2017. 3. Jeffery-Smith A, et al. Candida auris: a review of the literature. Clin Microbiol Rev. 2018. 4. Osei Sekyere J. Candida auris: A systematic review and meta-analysis of current updates. Mycoses. 2021. 5. Arendrup MC, et al. Candida auris: treatment and resistance mechanisms. Curr Opin Infect Dis. 2020. 6. Chow NA, et al. Genomic analysis of emerging Candida auris. N Engl J Med. 2021. 7. Welsh RM, et al. Clinical characteristics and outcomes of patients with Candida auris infection. Emerg Infect Dis. 2019. 8. Horton MV, et al. Antifungal drug resistance in Candida auris. J Fungi. 2022. 9. Kordalewska M, Perlin DS. Molecular mechanisms of resistance in Candida auris. Curr Fungal Infect Rep. 2019. 10. Rhodes J, et al. Environmental persistence of Candida auris. mBio. 2022. 11. WHO. Guidelines for the prevention and control of fungal infections. 2023. 12. Centers for Disease Control and Prevention (CDC). Candida auris clinical update. Atlanta, USA; обновления 2016–2024. 13. European Centre for Disease Prevention and Control (ECDC). Candida auris in healthcare settings – Europe. 2025. 14. CLSI. Reference Method for Broth Dilution Antifungal Susceptibility Testing of Yeasts. CLSI M27, 4th ed. 15. EUCAST. Breakpoint tables for interpretation of MICs. Version 12.0, 2024. 16. Bruker Daltonics. MALDI-TOF MS Library Update for Candida auris Identification. 2023. 17. СанПиН "Санитарно-эпидемиологические требования к лечебно-профилактическим организациям", постановление Правительства КР от 11 апреля 2016 года № 201 18. Порядок обращения с медицинскими отходами», постановление Кабинета Министров Кыргызской Республики от 22 июля 2025 года № 437
Информация
Адрес для переписки с рабочей группой:
Кыргызская Республика,
г. Бишкек, ул. Тоголок Молдо 1, 720040
e-mail: kutmanova@yahoo.com
МУЛЬТИДИСЦИПЛИНАРНАЯ РАБОЧАЯ ГРУППА
Для разработки Клинического руководства по профилактике, диагностике и лечению инфекции, вызванной Candidozyma auris для всех уровней оказания медицинской помощи была создана рабочая группа из специалистов согласно Указанию МЗ КР №1131 от 24.10.2025 г.
Кутманова А.З. д.м.н., проф., заведующая кафедрой инфекционных болезней МВШМ, главный̆ внештатный̆ инфекционист МЗКР руководитель группы
Узакбаева А.З. заместитель главного врача РКИБ
Создание мультидисциплинарной рабочей группы позволило исключить конфликт интересов разработчиков и включить в разработку Клинического руководства все заинтересованные стороны, участвующие в организации медицинской помощи пациентам, представители специальностей, из ведущих организаций здравоохранения (ОЗ) КР, которые в повседневной практике могут столкнуться с данной проблемой.
Декларация конфликта интересов
Перед началом работы по разработке Клинического руководства/протокола по профилактике, диагностике и лечению инфекции, вызванной Candidozyma auris, на рабочем совещании, проведённом 20 октября 2025 г., все члены рабочей группы дали согласие сообщить в письменной форме о наличии финансовых взаимоотношений с фармацевтическими компаниями. Никто из членов авторского коллектива не заявил о наличии коммерческой заинтересованности или другого конфликта интересов с фармацевтическими компаниями или другими организациями, производящими продукцию для диагностики и лечения ботулизма.
Все члены группы подписали декларацию о конфликте интересов.
СТРАТЕГИЯ ПОИСКА ИНФОРМАЦИИ
Нашей рабочей группой было принято решение о разработке клинического руководства по профилактике, диагностике и лечению инфекции, вызванной Candidozyma auris для всех уровней ОЗ КР путем адаптирования уже существующих международных руководств высокого методологического качества, основанных на принципах доказательной медицины. В связи с появлением проблемы по профилактике, диагностике и лечению инфекции, вызванной Candidozyma auris в мире существует небольшое количество разнообразных клинических руководств, консенсусов, стандартов и рекомендаций.
Ответственные исполнители осуществляли систематизацию и поиск ключевых рекомендаций из выбранных международных клинических руководств путем адаптации, предоставили обобщенные данные по ссылкам для формирования клинического содержания руководства.
Критерии включения/исключения публикаций
В связи с тем, что рабочая группа провела четкие ограничения по вопросам, которые необходимо было включать в клиническое руководство в качестве опорных клинических руководств выбраны только те, которые были обновлены с применением подходов доказательной медицины за последние 5 лет и посвящены вопросам профилактики, диагностики и лечению инфекции, вызванной Candidozyma auris для всех уровней здравоохранения.
Были установлены языковые ограничения, так как рабочая группа имела возможность изучать источники литературы только на английском и русском языках.
Описание процесса поиска и оценки существующих клинических руководств и других доказательств по Candidozyma auris
Поиск клинических руководств по диагностике и лечению Candidozyma auris осуществлялся в международных доступных электронных базах данных в сети Интернет – PubMed с использованием стратегии поиска PIPOH, стратегии поиска GLAD на платформах SUMSearch, Google Scholar за последние 5 лет.
Найденные электронные базы данных по клиническим руководствам и практическим рекомендациям
| Страна и название ресурса | Интернет-адрес |
| Международная ассоциация | |
| Всемирная организация здравоохранения (World Health Organization, WHO) | https://www.who.int/publications/i/item/9789240060241 |
| Всемирная организация здравоохранения (World Health Organization, WHO) | https://www.clinicalmicrobiologyandinfection.org/article/S1198-743X(24)00118-6/fulltext |
| Соединенные Штаты Америки | |
| Centers for Disease Control and Prevention | https://www.cdc.gov/candida-auris/index.html |
| FDA | https://www.fda.gov/media/85514/download |
| Европейский центр по профилактике и контролю заболеваний (ECDC) | |
| European Centre for Disease Prevention and Control | https://www.ecdc.europa.eu/sites/default/files/documents/RRA-Candida-auris-European-Union-countries.pdf |
| European Centre for Disease Prevention and Control. | https://www.ecdc.europa.eu/sites/default/files/documents/candidozyma-auris-survey-epidemiological-situation-laboratory-capacity-2024.pdf |
| По лекарственным средствам | |
| The Global Drug Database | www.globaldrugdatabase.com |
| Drugs.com | www.drugs.com |
| Medscape | www.medscape.com |
Оценка найденных клинических рекомендаций и доказательств
В итоге поиска было найдено 7 клинических руководств. Найденные клинические руководства были оценены МДРГ при помощи инструмента AGREE GRS. В результате среди найденных 7 клинических руководств, после проведённой оценки с инструментом AGREE GRS были взяты в качестве опорных 3 клинических руководств, в которых четко отражены вопросы диагностики, лечения и ведения пациентов с Candidozyma auris, которые содержали необходимую информацию, соответствующую задаче рабочей группы (см. табл. Характеристика отобранных клинических руководств).
Характеристика отобранных клинических руководств по ботулизму
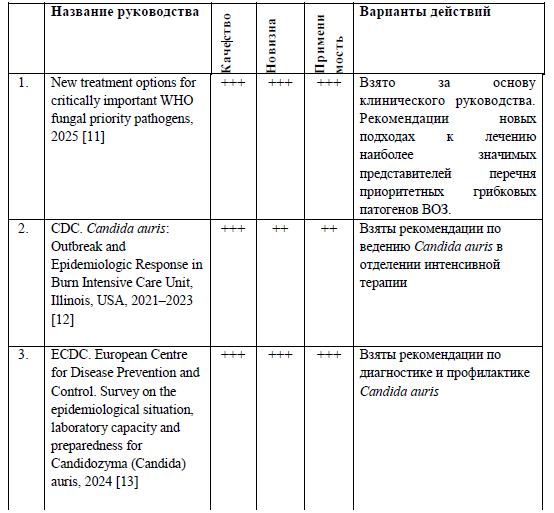
Предпочтение для разработки руководства основывались на вебсайте WHO, CDC, ECDC. По черновому варианту были получены комментарии и замечания специалистов. Обновление данного руководства предполагается по мере появления новых данных.
Так как в найденных клинических руководствах МДРГ были отражены необходимые рекомендации по диагностике и лечению Candidozyma auris, то дополнительный поиск медицинских публикаций по результатам метаанализов, систематических обзоров, РКИ и т.д. в международных базах не проводился.
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+) |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов |
Ответственная за методологическое содержание руководства и формирование клинических рекомендаций по результатам обсуждения
Зурдинова А.А. д.м.н., профессор, главный внештатный клинический фармаколог МЗ КР, специалист по ДМ
Ответственный исполнитель осуществляла систематизированный поиск имеющихся международных клинических руководств, критическую их оценку, методологическую поддержку при формировании МДРГ ключевых рекомендаций и содержания разработанного руководства.
Оценка клинического содержания руководства
| Аалиев Г.К | к.м.н., главный врач Республиканской клинической инфекционной больницы |
| Джузумалиева Г.С. |
к.м.н., доцент, заведующая отделением анестезиологии и реанимации №2 Национального госпиталя при Министерстве здравоохранения
|
Оценка методологического качества клинического руководства
Методологами была проведена оценка методологического содержания и структуры клинического руководства по логическому изложению, отражению наилучшей клинической практики в рекомендациях и применимости в клинической практике на местах согласно инструменту AGREE II.
Процесс разработки клинического руководства
В стране отсутствовало Клиническое руководство по диагностике и лечению Candidozyma auris, в связи с чем было принято решение разработать данный документ для специалистов всех уровней здравоохранения.
ЦЕЛИ И ЗАДАЧИ РУКОВОДСТВА
Главная цель: Снижение заболеваемости, летальности и экономического ущерба, связанных с инфекциями Candida auris, на национальном и уровне отдельных медицинских организаций путем внедрения научно-обоснованных протоколов.
Конкретные цели:
1. Обеспечить раннее выявление и своевременное подтверждение случаев колонизации и инфекции C. auris.
2. Унифицировать и оптимизировать тактику антимикотической терапии на основе данных о локальной и региональной резистентности.
3. Предотвратить внутрибольничную передачу C. auris за счет внедрения строгих и эффективных профилактических и противоэпидемических мероприятий.
4. Обеспечить безопасность пациентов и медицинского персонала при уходе за пациентами с C. auris.
5. Создать алгоритмы управления вспышками для быстрой локализации и ликвидации очагов.
Задачи клинического руководства
Руководство ставит перед медицинскими работниками и администрацией ЛПУ следующие практические задачи:
1.1. В области диагностики и эпидемиологического надзора:
Определить группы пациентов высокого риска для целенаправленного скрининга на колонизацию C. auris (пациенты ОРИТ, переводные из других стационаров, с длительной госпитализацией, получавшие антимикотики/антибиотики широкого спектра).
Установить алгоритм забора, транспортировки и маркировки образцов для микробиологического исследования (с акцентом на мазки из подмышечных/паховых областей, прямой кишки, ноздрей, трахеостомических/катетерных мест).
Определить требования к лабораторной диагностике: методы идентификации (MALDI-TOF MS с расширенными базами данных, молекулярные методы), тестирование чувствительности к противогрибковым препаратам (согласно стандартам EUCAST/CLSI).
Внедрить систему молекулярного типирования штаммов для расследования вспышек и определения путей передачи.
1.2. В области лечения:
Разработать эмпирические и целенаправленные схемы терапии инвазивных инфекций (кандидемия, инфекции ЦНС, раневая инфекция и др.) в зависимости от данных о чувствительности in vitro.
Определить тактику при мультирезистентных штаммах (устойчивых к азолам, полиенам и эхинокандинам).
Четко регламентировать показания, дозировки, длительность терапии и критерии ее эффективности.
Определить подходы к деколонизации (санации) и доказать ее ограниченную эффективность, сделав акцент на мерах изоляции.
1.3. В области профилактики и инфекционного контроля:
Установить строгий режим изоляции (контактные меры предосторожности): размещение в отдельной палате с санузлом, использование средств индивидуальной защиты (СИЗ) – халат, перчатки, маска.
Детализировать протоколы обработки рук (спиртсодержащие антисептики против C. auris менее эффективны, чем мытье с мылом и водой с последующей обработкой антисептиком).
Установить стандарты окончательной и текущей дезинфекции помещений и оборудования с использованием средств, эффективных против C. auris (например, на основе хлора, перекиси водорода, ускоренного перекисного соединения).
Определить порядок обработки многоразового медицинского оборудования (например, термометров, датчиков АД).
Внедрить правила управления контактами и алгоритм действий при выявлении нового случая.
3.4. В области организации и управления:
Определить роли и ответственность Команды по инфекционному контролю (КИК), администрации, лечащих врачей, среднего и младшего персонала, клинических микробиологов.
Разработать формы учета и отчетности о случаях C. auris для внутреннего мониторинга и информирования вышестоящих органов (Министерство здравоохранения).
Внедрить программу обязательного обучения персонала по вопросам C. auris.
Создать план действий при вспышке, включая формирование оперативного штаба, приостановку плановых переводов/госпитализаций и усиление контрольных мероприятий.
Целевая аудитория руководства
Данное руководство предназначено для: инфекционистов, реаниматологов, терапевтов, хирургов, клинических микробиологов, эпидемиологов, врачей и медицинских сестер отделений (особенно ОРИТ, ожоговых, онкологических, отделений для пациентов с травмами), специалистов по инфекционному контролю, администрации организаций здравоохранения, сотрудников ФОМС и МЗ КР.
Ожидаемые результаты внедрения клинического руководства
Внедрение настоящего руководства направлено на достижение конкретных, измеримых результатов на трех уровнях: пациентский, организационный и системный (национальный).
1. Ожидаемые клинические и эпидемиологические результаты (уровень пациента и популяции)
Снижение общей летальности от инвазивных инфекций, вызванных C. auris, за счет более ранней и адекватной эмпирической и целенаправленной терапии.
Сокращение частоты развития осложнений у инфицированных пациентов (например, эндофтальмита, эндокардита, персистирующей кандидемии) благодаря четким протоколам мониторинга и контроля эффективности лечения.
Уменьшение числа внутрибольничных вспышек, связанных с C. auris, и сокращение их длительности и масштаба за счет реализации эффективных профилактических и противоэпидемических мероприятий.
Снижение уровня внутрибольничной передачи и коэффициента вторичной заболеваемости C. auris среди пациентов групп риска.
Своевременное выявление (в течение 24-48 часов) случаев колонизации и инфекции C. auris за счет налаженной системы скрининга и диагностики.
2. Ожидаемые организационно-процессные результаты (уровень медицинской организации)
Стандартизация и унификация подходов ко всем аспектам работы с C. auris: от момента поступления пациента из группы риска до его выписки, что минимизирует человеческий фактор и ошибки.
Формирование эффективной мультидисциплинарной модели управления риском, включающей четкое распределение обязанностей между клиническими, микробиологическими, эпидемиологическими и административными службами.
Оптимизация использования ресурсов:
- Лабораторных: За счет целенаправленного скрининга и рационального использования дорогостоящих методов идентификации.
- Лекарственных: Снижение нерационального расхода широкого спектра противогрибковых препаратов, применение более целенаправленной и эффективной терапии.
- Кадровых и материальных: Сокращение затрат на ликвидацию масштабных вспышек благодаря их предотвращению.
Повышение компетентности и настороженности персонала. Не менее 95% медицинских работников ключевых отделений (ОРИТ, реанимации, хирургических) должны быть обучены и регулярно подтверждать знание ключевых положений руководства.
Создание и поддержание актуальной локальной эпидемиологической базы данных по штаммам C. auris, их чувствительности и случаям инфицирования/колонизации, что является основой для принятия управленческих решений.
3. Ожидаемые результаты в области антимикробной резистентности и безопасности
Сдерживание роста и распространения штаммов C. auris с множественной лекарственной устойчивостью (МЛУ) за счет рационального назначения антимикотиков и предотвращения перекрестной передачи.
Уменьшение селективного давления неправильной эмпирической терапии на микробиом пациента и госпитальную среду.
Повышение биологической безопасности в организации здравоохранения за счет строгого соблюдения протоколов обработки рук, дезинфекции и использования СИЗ.
4. Ожидаемые экономические результаты
Прямая экономия: Снижение прямых затрат на лечение одного случая инвазивной инфекции C. auris за счет сокращения длительности госпитализации, использования менее дорогих, но эффективных схем терапии (при возможности) и предотвращения осложнений.
Косвенная экономия: Избежание колоссальных финансовых потерь, связанных с приостановкой деятельности отделений (особенно ОРИТ), проведением массового скрининга и заключительной дезинфекции в ходе ликвидации крупной вспышки.
Минимизация медико-социальных издержек, связанных с длительной нетрудоспособностью и инвалидизацией пациентов.
5. Ключевые показатели результативности для мониторинга эффективности руководства
Для оценки достижения ожидаемых результатов предлагается отслеживать следующие индикаторы:
1. Показатель летальности при инвазивных инфекциях C. auris (цель: снижение на 20-30% от исходного уровня за 2 года).
2. Частота внутрибольничных вспышек C. auris (цель: отсутствие крупных вспышек >5 связанных случаев).
3. Индекс вторичной заболеваемости (число случаев, вероятно связанных с внутрибольничной передачей, от общего числа).
4. Время от забора материала до постановки окончательного диагноза с идентификацией вида и определением чувствительности.
5. Доля пациентов групп риска, охваченных скринингом на колонизацию C. auris при поступлении (цель: >95%).
6. Соблюдение протоколов изоляции и мер предосторожности (по результатам аудитов, цель: >90%).
7. Структура назначения противогрибковых средств: увеличение доли целенаправленной терапии по сравнению с эмпирической.
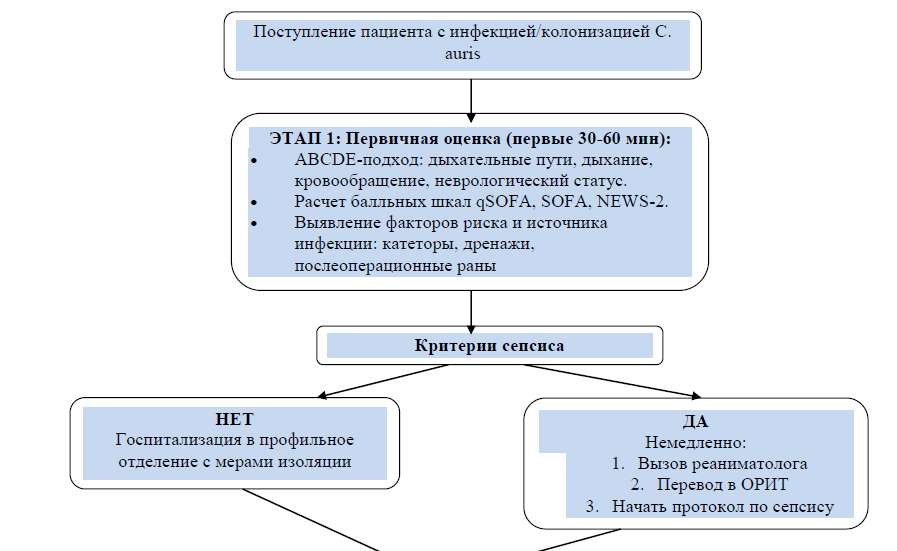
Приложение 1
Алгоритм клинической оценки
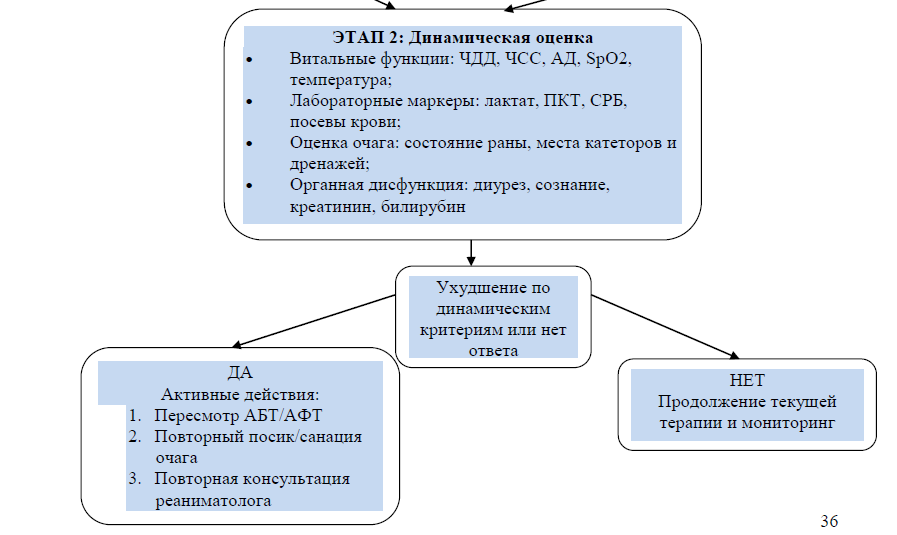
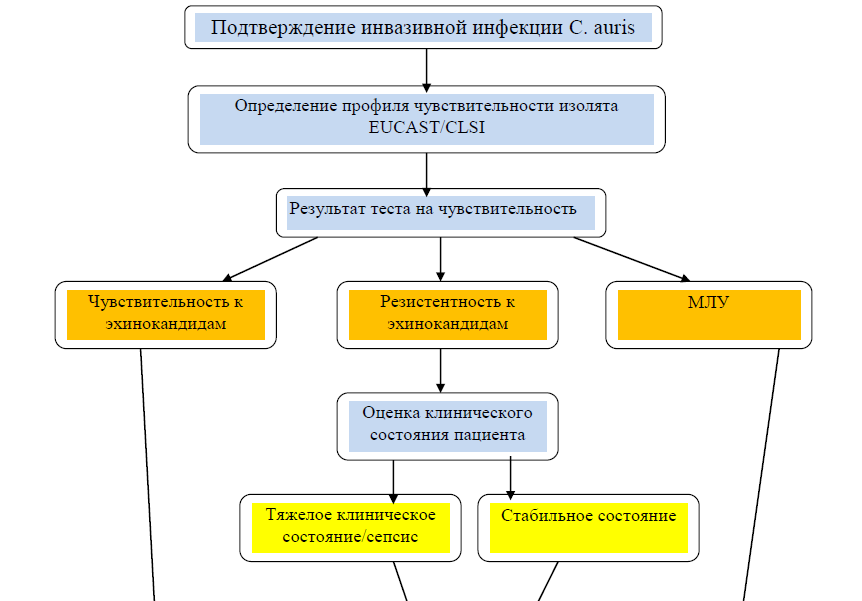
Приложение 2
Алгоритм по определению стратегии лечения
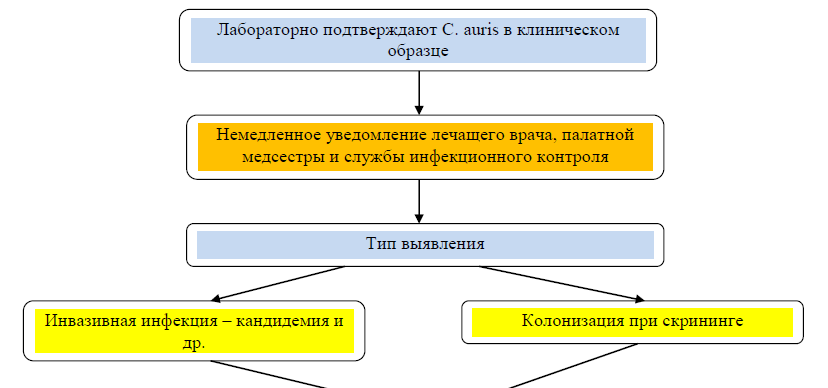
Алгоритм по профилактике распространения инфекции C. auris
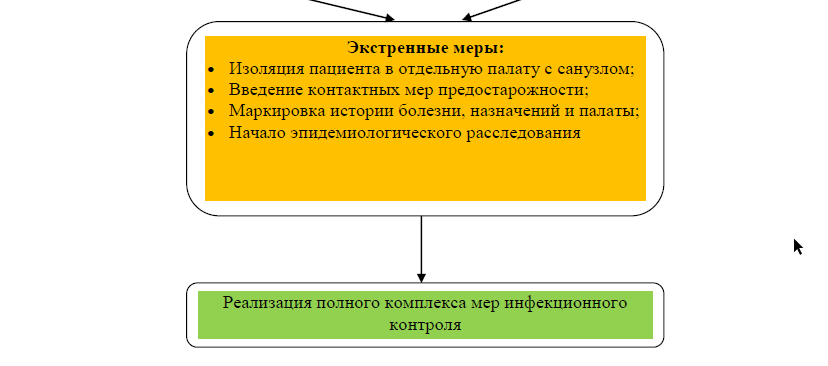
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.