Преждевременный разрыв плодных оболочек. Дородовое излитие околоплодных вод
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
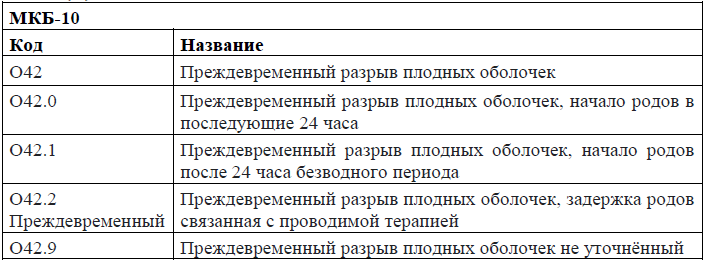
Преждевременный разрыв плодных оболочек (O42), Преждевременный разрыв плодных оболочек неуточненный (O42.9), Преждевременный разрыв плодных оболочек, задержка родов, связанная с проводимой терапией (O42.2), Преждевременный разрыв плодных оболочек, начало родов в последующие 24 ч (O42.0), Преждевременный разрыв плодных оболочек, начало родов после 24-часового безводного периода (O42.1)
Акушерство и гинекология
Общая информация
Краткое описание
Одобрено
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «26» мая 2023 года
Протокол №181
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «26» мая 2023 года
Протокол №181
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
ПРЕЖДЕВРЕМЕННЫЙ РАЗРЫВ ПЛОДНЫХ ОБОЛОЧЕК
ДОРОДОВОЕ ИЗЛИТИЕ ОКОЛОПЛОДНЫХ ВОД
Дородовый разрыв плодных оболочек (ДРПО) – спонтанный разрыв амниотических оболочек до начала регулярных сокращений матки в сроке 37 недель и более.
Преждевременный разрыв плодных оболочек (ПРПО) – спонтанный разрыв амниотических оболочек до начала регулярных сокращений матки в сроке 22 до 37 недель.
Три основные причины неонатальной смертности связаны с ПРПО: недоношенность, сепсис и гипоплазия легких [1, 2]. Риск для матери связан, прежде всего, с хориоамнионитом.
Код(ы) МКБ-10:
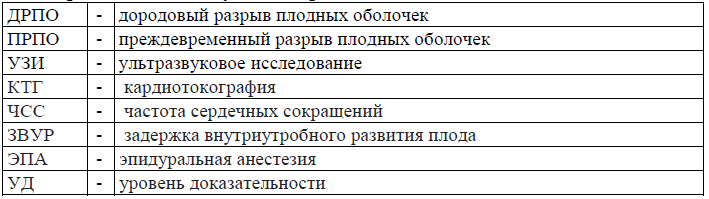
Сокращения, используемые в протоколе:
Категория пациентов: беременные, роженицы.
Шкала уровня доказательности:

Дородовый разрыв плодных оболочек (ДРПО) – спонтанный разрыв амниотических оболочек до начала регулярных сокращений матки в сроке 37 недель и более.
Преждевременный разрыв плодных оболочек (ПРПО) – спонтанный разрыв амниотических оболочек до начала регулярных сокращений матки в сроке 22 до 37 недель.
Три основные причины неонатальной смертности связаны с ПРПО: недоношенность, сепсис и гипоплазия легких [1, 2]. Риск для матери связан, прежде всего, с хориоамнионитом.
ВВОДНАЯ ЧАСТЬ
Код(ы) МКБ-10:

Дата разработки/пересмотра протокола: 2014 год (пересмотрен в 2022 год)
Сокращения, используемые в протоколе:

Пользователи протокола: акушеры-гинекологи, акушерки врачи общей практики, терапевты, инфекционисты.
Категория пациентов: беременные, роженицы.
Шкала уровня доказательности:

Классификация
Классификация: [2]
Преждевременный дородовый разрыв плодных оболочек
происходит в сроке 22 – 37 недель беременности.
Дородовый разрыв плодных оболочек
происходит в сроке 37 недель или больше недель беременности.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Жалобы и анамнез: Диагноз основывается на характерном анамнезе (подтекание жидкости во влагалище) и подтверждающем осмотре в зеркале, при котором видно, что жидкость вытекает из цервикального канала.
Следует избегать пальцевого цервико-влагалищного исследования, так как оно связано с повышенным риском внутриутробной инфекции.
Физикальное обследование:
При подозрении на ПРПО – осмотр в зеркалах (УД-В) [4]. В некоторых случаях дополнительное подтверждение диагноза достигается при проведении УЗИ (УД - С). Если разрыв оболочек произошел достаточно давно, диагностика ПРПО может быть затруднена.
Возможно проведение следующих диагностических тестов после тщательного сбора анамнеза:
предложить пациентке чистую прокладку и оценить характер и количество выделений через 1 час.;
произвести осмотр на гинекологическом кресле стерильными зеркалами жидкость, вытекающая из цервикального канала или находящаяся в заднем своде влагалища, подтверждает диагноз;
может быть предложен тест (при его наличии) на фетальный фибронектин (чувствительность 94%) [5]
Лабораторные исследования:
общий анализ крови (лейкоцитоз является неспецифическим признаком и может быть связан не только с инфекцией, но и с воспалением. Заметное повышение количества лейкоцитов (более 20 000 на мм3) или значительный сдвиг влево предполагают хориоамнионит);
мазок на степень чистоты (вагинальный посев бесполезен, так как вагинальная флора - полимикробная);
оценка состояния плода с помощью нестрессового теста; С-реактивный белок;
Тестирование на Neisseria gonorrhoeae, Chlamydia trachomatis, Trichomonas vaginalis и бактериальный вагиноз (мазок со слизистой влагалища или ПЦР диагностика) [4].
Инструментальные исследования:
УЗИ малого таза и брюшной полости;
ректовагинальный посев на стрептококк группы В (см приложение 5);
ультразвуковое исследование остаточного объема амниотической жидкости: положение и анатомию плода; оценить биофизический профиль;
кардиотокография для мониторинга частоты сердечных сокращений плода (включая нестрессовый тест) и частоты сокращений матки;
выявление признаков инфекции (лихорадка, тахикардия плода, лейкоцитоз у матери);
УЗИ - олигогидрамнион (единственный самый глубокий карман <2 см или индекс амниотической жидкости ≤5 см).
Показания для консультации специалистов:
ректовагинальный посев на стрептококк группы В (см приложение 5);
ультразвуковое исследование остаточного объема амниотической жидкости: положение и анатомию плода; оценить биофизический профиль;
кардиотокография для мониторинга частоты сердечных сокращений плода (включая нестрессовый тест) и частоты сокращений матки;
выявление признаков инфекции (лихорадка, тахикардия плода, лейкоцитоз у матери);
УЗИ - олигогидрамнион (единственный самый глубокий карман <2 см или индекс амниотической жидкости ≤5 см).
Необходим анализ медицинской документации и текущего материнского статуса соматических и акушерских осложнений, влияющих на принятие решения о сроках родов.
Показания для консультации специалистов:
консультация терапевта - при повышении температуры тела;
консультация генетика - при выявлении пороков развития плода.
Диагностический алгоритм: нет.
Проведение следующих диагностических тестов, после тщательного сбора анамнеза:
предложить пациентке чистую прокладку и оценить характер и количество выделений через 1 час;
произвести осмотр на гинекологическом кресле стерильными зеркалами;
жидкость, вытекающая из цервикального канала или находящаяся в заднем своде влагалища, подтверждает диагноз;
экспресс-тесты диагностики околоплодных вод (тест-полоски, тест-прокладки);
при возможности может быть предложен тест на фетальный фибронектин (чувствительность 94%) [5];
если диагноз неясен, то при возможности, провести диагностическое тестирование жидкости, скопившейся в заднем своде, на инсулиноподобный фактор роста-связывающий белок 1 (IGFBP-1), или тест на плацентарный альфа-микроглобулин-1 (PAMG-1) (УД – В) [4].
Диагностический алгоритм: нет.
Дифференциальный диагноз
Дифференциальный диагноз:
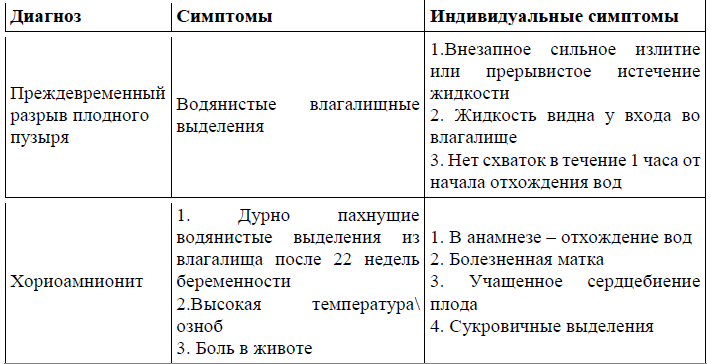

Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ: нет.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Карта наблюдения пациента, маршрутизация пациента: в зависимости от срока гестации беременная должна быть направлена на соответствующий уровень.
Немедикаментозное лечение: нет, не проводится.
Медикаментозное лечение:
При отсутствии осложнений, существует консенсус в отношении того, что пациентки с ПРПО до 34+0 недель должны находиться под пристальным наблюдением и вести выжидательную тактику, по крайней мере, до 34+0 недель беременности [13].
Амниоинфузия (см приложение 1).
Ведение при ПРПО в гестационном сроке от 22-х до 24 недель беременности:
При выборе выжидательной тактике беременная информируется о высоком риске гнойно – септических осложнений, гипо – аплазией легочной тканей у плода и сомнительных исходах у новорожденного.
Выжидательная тактика при преждевременном излитии плодных оболочек на сроке менее 24 недель беременности была связана со значительно повышенным риском материнской заболеваемости по сравнению с прерыванием беременности [6].
При отказе беременной от активной тактики ведения как альтернативный метод может быть предложена амниоинфузия [УД А] [1, 6, 7].
Амниоинфузия (см приложение 1).
Установка порт-системы (см приложение 2).
Активная тактика:
Оценка состояния шейки матки при незрелой шейке матки (оценка по шкале Бишопа <6 баллов) – рекомендуются методы подготовки шейки матки: простагландины Е1 (мизопростол) и Е2 (динопростон) по рекомендуемым схемам. При «зрелой» шейке 7 баллов и более – окситоцин по схеме [1].
Выжидательная тактика проводится при отсутствии противопоказаний к пролонгированию беременности. Наблюдение за пациенткой может осуществляться в палате акушерского отделения (контроль температуры тела, пульса, ЧСС плода, выделений из половых путей, каждые 4-8 часов в первые 48 часов; уровень лейкоцитов крови каждые 12 часов. В дальнейшем контроль температуры тела, пульса, ЧСС плода, выделений из половых путей не реже чем каждые 12 часов, развернутый анализ крови матери не реже чем 1 раз в неделю и по показаниям, с ведением листа наблюдений в истории родов.
Дальнейшее ведение:
Ведение при ПРПО и ВИЧ-инфекции (см приложение 4).
Индикаторы эффективности лечения и безопасности методов диагностики и лечения – рождение жизнеспособного новорожденного.
Ведение при ПРПО в гестационном сроке от 25-х до 34 недель беременности:
Тактика ведения при ПРПО в сроке до 34 недель беременности определяется после предоставления максимальной информации о состоянии матери и плода, преимуществах и недостатках выжидательной и активной тактики, обязательного получения информированного письменного согласия от пациентки на выбранную тактику ведения.
Выжидательная тактика проводится при отсутствии противопоказаний к пролонгированию беременности. Наблюдение за пациенткой может осуществляться в палате акушерского отделения (контроль температуры тела, пульса, ЧСС плода, выделений из половых путей, каждые 4-8 часов в первые 48 часов; уровень лейкоцитов крови каждые 12 часов. В дальнейшем контроль температуры тела, пульса, ЧСС плода, выделений из половых путей не реже чем каждые 12 часов, развернутый анализ крови матери не реже чем 1 раз в неделю и по показаниям, с ведением листа наблюдений в истории родов.
При подозрении на интраамниотическую инфекцию см. клинический протокол МЗ РК «Хориоамнионит».
С началом регулярной родовой деятельности необходим перевод в родильное отделение.
В индивидуальных случаях можно проводить мониторинг вне условий стационара только после тщательного обследования врачом акушером – гинекологом и 48-72 часового наблюдения в условиях стационара. Пациентки должны измерять на дому температуру 2 раза в день и посещать врача согласно точного графика [1, 2].
Проводить обследование (включая анализы крови [количество лейкоцитов и С-реактивный белок], клинические записи и мониторинг сердечного ритма плода), например, в отделении дневного стационара, родильном отделении или дородовое отделение, один или два раза в неделю; если у женщины есть какие-либо опасения, она должна обратиться в больницу немедленно. При этом пациентка должна быть информирована о симптомах хориоамнионита, при выявлении которых необходимо обратиться за медицинской помощью [4, 7].
Токолитики при преждевременных родах показаны на период не более 48 часов для проведения курса кортикостероидов (профилактика дистресс – синдрома). Профилактический токолиз у беременных с ПРПО без наличия активной маточной деятельности не рекомендуется (УД - А). Токолитики не следует назначать пациенткам с раскрытием маточного зева > 5 см, или у которых есть какие-либо признаки, указывающие на хориоамнионит. Другие потенциальные
противопоказания к токолизу включают нереактивный нестрессовый тест [НСТ], отслойку плаценты.
(Обзор пришел к выводу, что недостаточно доказательств в поддержку использования токолиза у женщин с ПРПО, так как отмечается увеличение материнского хориоамнионита без существенного преимущества для новорожденного. Более поздние публикации показали, что по сравнению с отсутствием токолиза, токолиз не связан с улучшение неонатальных исходов!! [4, 7]).
Препаратом выбора для токолитической терапии являются блокаторы кальциевых каналов (нифедипин), поскольку доказаны его преимущества по сравнению с другими препаратами.
Побочные эффекты:
Схема применения нифедипина: начальная доза 20 мг per os, с последующим приемом по 10 мг каждые 6 часов в течение 3-7 дней, по показаниям [10].
Побочные эффекты:
• гипотензия, однако, это крайне редко проявляется у пациенток с нормальным уровнем артериального давления;
• вероятность гипотензии повышается при совместном использовании нифедипина и магния сульфата; • другие побочные эффекты: тахикардия, приливы крови, головные боли, головокружение, тошнота.
После купирования родовой деятельности дальнейший токолиз не рекомендуется из-за недоказанной эффективности и безопасности.
При возникновении побочных эффектов от нифедипина, препаратом выбора является атозибан. Атозибан представляет собой синтетический конкурентный ингибитор вазопрессина и окситоцина. Связываясь с рецепторами окситоцина, атозибан снижает частоту маточных сокращений и тонус миометрия, что приводит к угнетению сократимости матки. Атозибан также связывается с рецепторами вазопрессина, таким образом угнетая эффект последнего. Атозибан – единственный токолитик, разработанный специально для применения при самопроизвольной сократительной деятельности матки. Во многих европейских странах атозибан является препаратом выбора для терапии угрозы преждевременных родов [11, 12].
После купирования родовой деятельности дальнейший токолиз не рекомендуется из-за недоказанной эффективности и безопасности.
При возникновении побочных эффектов от нифедипина, препаратом выбора является атозибан. Атозибан представляет собой синтетический конкурентный ингибитор вазопрессина и окситоцина. Связываясь с рецепторами окситоцина, атозибан снижает частоту маточных сокращений и тонус миометрия, что приводит к угнетению сократимости матки. Атозибан также связывается с рецепторами вазопрессина, таким образом угнетая эффект последнего. Атозибан – единственный токолитик, разработанный специально для применения при самопроизвольной сократительной деятельности матки. Во многих европейских странах атозибан является препаратом выбора для терапии угрозы преждевременных родов [11, 12].
Антибиотикопрофилактика.
Цель - снижение частоты инфицирования матери и плода и, таким образом, отсрочка начала преждевременных родов.
Цель - снижение частоты инфицирования матери и плода и, таким образом, отсрочка начала преждевременных родов.
Начинается сразу после постановки диагноза ПРПО – перорально эритромицин 250 мг каждые 6 часов в течение 10 дней [УД - А].
Азитромицин (например, 1 г однократно) «является подходящей альтернативой» для замены эритромицина, если он недоступен или плохо переносится [2].
Пенициллин можно использовать у женщин, которые не переносят эритромицин [4, 7].
С началом родовой деятельности – стартовая доза пенициллина G – 2,4 млн ЕД, затем каждые 4 часа по 1,2 млн ЕД до рождения, при наличии аллергии на пенициллин назначают цефазолин, начальная доза 2 гр в\в, затем по 1 гр каждые 8 часов до рождения ребенка или клиндамицин 600 мг каждые 8 часов внутривенно до рождения [13].
Ко-амоксиклав следует избегать, так как он связан с повышенным риском неонатального некротизирующий энтероколит [4, 7].
Кортикостероиды для профилактики РДС.
Введение кортикостероидов рекомендовано беременным с ПРПО 23+0 до 33+6 недель беременности. (Данные, подтверждающие эту рекомендацию, были предоставлены систематическими обзорами рандомизированных исследований, которые показали, что неонатальная смертность, респираторный дистресс-синдром, внутрижелудочковое кровоизлияние, некротизирующий энтероколит и продолжительность неонатальной респираторной поддержки значительно сокращались за счет антенатальной терапии кортикостероидами без увеличения материнской или неонатальной инфекции [5,6]. Среднее снижение риска этих нежелательных явлений колебалось от 30 до 60 процентов).
Для профилактики РДС плода используют кортикостероиды (дексаметазон по 6 мг через 12 часов в/м 2 дня, курсовая доза 24 мг или бетаметазон по 12 мг через 24 часа в/м, курсовая доза 24 мг) [УД - А].
Не рекомендуется проводить повторные курсы кортикостероидов.
Кортикостероиды не предлагать рутинно, только в случае вероятности рождение в ближайшие 48 часов (наличие структурных изменений шейки матки, нерегулярная/регулярная сократительная активность матки)!
Курс кортикостероидов может быть рассмотрен для пациенток с ПРПО в сроке от 34+0 до 36+6 недель беременности, которым предстоит выжидательная тактика, которые не получали предыдущий курс стероидов и у которых запланированы роды в >24 часов и <7 дней.
Кортикостероиды не назначают при хориоамнионите [4, 7].
Сульфат магния в нейропротекции ребенка. Использование сульфата магния для нейропротекции при беременностями <32 недель гестации, роженицам с установленными преждевременными родами или с запланированными преждевременными родами в следующем 24 часа, уменьшает церебральный паралич и моторную дисфункцию у потомства (УД - А). (Большинство данных рандомизированных исследований были получены при беременности <32 недель).
Ко-амоксиклав следует избегать, так как он связан с повышенным риском неонатального некротизирующий энтероколит [4, 7].
Кортикостероиды для профилактики РДС.
Введение кортикостероидов рекомендовано беременным с ПРПО 23+0 до 33+6 недель беременности. (Данные, подтверждающие эту рекомендацию, были предоставлены систематическими обзорами рандомизированных исследований, которые показали, что неонатальная смертность, респираторный дистресс-синдром, внутрижелудочковое кровоизлияние, некротизирующий энтероколит и продолжительность неонатальной респираторной поддержки значительно сокращались за счет антенатальной терапии кортикостероидами без увеличения материнской или неонатальной инфекции [5,6]. Среднее снижение риска этих нежелательных явлений колебалось от 30 до 60 процентов).
Для профилактики РДС плода используют кортикостероиды (дексаметазон по 6 мг через 12 часов в/м 2 дня, курсовая доза 24 мг или бетаметазон по 12 мг через 24 часа в/м, курсовая доза 24 мг) [УД - А].
Не рекомендуется проводить повторные курсы кортикостероидов.
Кортикостероиды не предлагать рутинно, только в случае вероятности рождение в ближайшие 48 часов (наличие структурных изменений шейки матки, нерегулярная/регулярная сократительная активность матки)!
Курс кортикостероидов может быть рассмотрен для пациенток с ПРПО в сроке от 34+0 до 36+6 недель беременности, которым предстоит выжидательная тактика, которые не получали предыдущий курс стероидов и у которых запланированы роды в >24 часов и <7 дней.
Кортикостероиды не назначают при хориоамнионите [4, 7].
Сульфат магния в нейропротекции ребенка. Использование сульфата магния для нейропротекции при беременностями <32 недель гестации, роженицам с установленными преждевременными родами или с запланированными преждевременными родами в следующем 24 часа, уменьшает церебральный паралич и моторную дисфункцию у потомства (УД - А). (Большинство данных рандомизированных исследований были получены при беременности <32 недель).
Продолжительность выжидательной тактики зависит от:
• гестационного срока;
• состояния плода;
• наличия инфекции.
Маловодие при поступлении ИАЖ менее 5см, по оценке состояния плода при ультразвуковом исследовании, связано с тяжелой неонатальной респираторной заболеваемостью [8, 9].
Ведение при ПРПО в гестационном сроке с 34 -37 недель беременности.
Возможна активная или выжидательная тактика.
Тактика определяется после предоставления максимальной информации о состоянии матери и плода, преимуществах и недостатках выжидательной и активной тактики, обязательного получения информированного письменного согласия от пациентки на выбранную тактику ведение.
Выжидательная тактика после 34 недель не целесообразна, так как пролонгирование беременности связано с повышенным риском развития хориоамнионита. Существует мало доказательств того, что активное ведение после 34 недель негативно влияет на неонатальные исходы.
Возможно проведение (при отказе пациентки от активной тактики ведения) выжидательной тактики в сроке 34–36+6 недель, при отсутствии явных признаков инфекции или нарушения состояния плода. Необходимо надлежащее наблюдение за состоянием матери и плода [4].
Активная тактика:
Наблюдение в течении 24-х часов без влагалищного исследования, контроль ЧСС плода, температуры тела, пульса матери, выделений из половых путей, сокращений матки каждые 4 часа с ведением специального листа наблюдений в истории родов) с последующей индукцией родов (см. протокол «Индукция родов»).
Антибиотикопрофилактику начинать с началом родовой деятельности – стартовая доза пенициллина G – 2,4 г, затем каждые 4 часа по 1,2 гр до рождения, при наличии аллергии на пенициллин назначают цефазолин, начальная доза 2 гр в/в, затем по 1 гр каждые 8 часов до рождения ребенка или клиндамицин 600 мг каждые 8 часов внутривенно до рождения.
Ведение при ДРПО в гестационном сроке 37 и более недель [4]
Тактика при отсутствии показаний к немедленной индукции: наблюдение в течение 24 – х часов без влагалищного исследования, (контроль ЧСС плода, температуры тела, пульса матери, выделений из половых путей, сокращений матки каждые 4 часа с ведением специального листа наблюдений в истории родов), с последующей индукцией родов (см. протокол «Индукция родов»). Пациенткам, не имеющим противопоказаний к вагинальным родам, предложить индукцию окситоцином без преиндукционного созревания шейки матки. Окситоцин легче титровать, чем простагландины.
Антибиотикопрофилактику начинать при ПРПО при безводном периоде более 18 часов с началом родовой деятельности стартовая доза пенициллина G - 2,4 г, затем каждые 4 часа по 1,2 гр до рождения, при наличии аллергии на пенициллин G назначают цефазолин, начальная доза 2 гр в\в, затем по 1 гр каждые 8 часов до рождения ребенка или клиндамицин 600 мг каждые 8 часов внутривенно до рождения [13].
Антибиотикотерапия показана только при наличии клинических признаков хориоамнионита.
Хориоамнионит – см. протокол МЗ РК «Хориоамнионит».
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
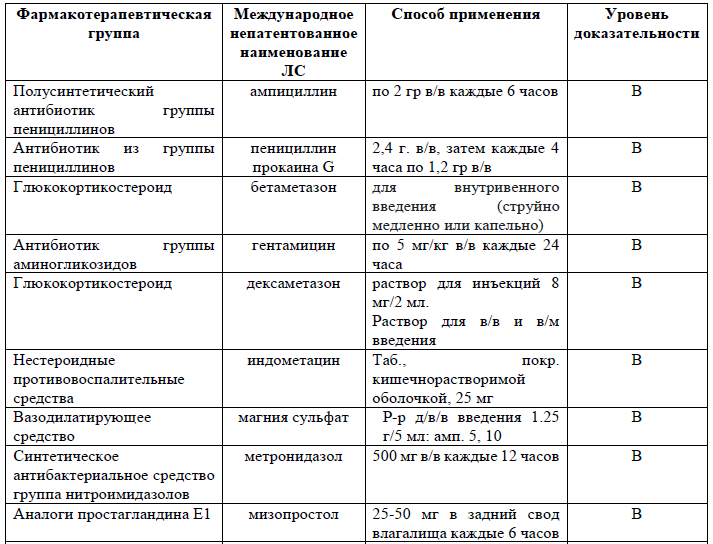
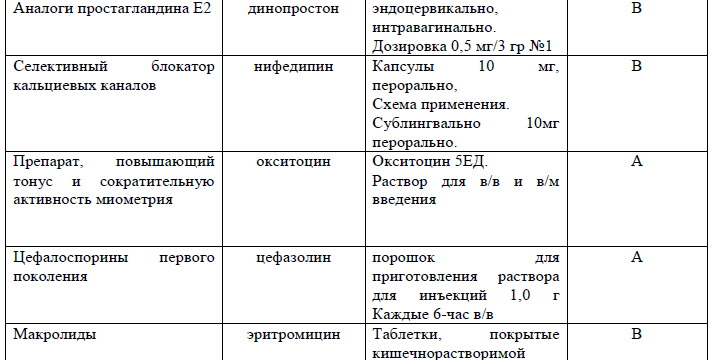

Перечень основных лекарственных средств (имеющих 100% вероятность применения):



Хирургическое вмешательство: нет.
Дальнейшее ведение:
Ведение при ПРПО и инфекция ВПГ (см приложение 3).
Ведение при ПРПО и ВИЧ-инфекции (см приложение 4).
Беременность двойней с ПРПО ведется так же, как и одноплодная беременность с ПРПО. Это положение основано на клиническом опыте и общепринятых практиках. (Некоторые исследования ПРПО включали как одноплодную беременность, так и беременность двойней, но ни одно исследование не оценивало конкретно ведение ПРПО с двойней [2]).
Индикаторы эффективности лечения и безопасности методов диагностики и лечения – рождение жизнеспособного новорожденного.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации: нет.
Показания для экстренной госпитализации:
- беременная должна быть госпитализирована при установленном факте ПРПО.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- 1. Протокол РЦРЗ МЗ РК от «13» января 2023 года №177 «Индукция родов» 2. Обновление руководства ACOG: диагностика и лечение PROM (предродовой разрыв плодных оболочек) American College of Obstetricians and Gynecologists 2022г 3. Thomson AJ, on behalf of the Royal College of Obstetricians and Gynaecologists. Care of Women Presenting with Suspected Preterm Prelabour Rupture of Membranes from 24+0 Weeks of Gestation. BJOG 2019;126:e152–166 4. NICE guideline (NG25), Preterm labour and birth (published November 2015). 5. Michael Tchirikov et al. Mid-trimester preterm premature rupture of membranes (PPROM): etiology, diagnosis, classification, international recommendations of treatment options and outcome. J Perinat Med, 2018 Jul 26;46(5):465-488. doi: 10.1515/jpm-2017-0027. 6. Ariel Sklar , Jeanelle Sheeder. Maternal morbidity after preterm premature rupture of membranes at <24 weeks' gestation. Am J Obstet Gynecol. 2022 Apr;226(4):558.e1-558.e11. doi: 10.1016/j.ajog.2021.10.036. Epub 2021 Nov 2. 7. Thomson AJ, on behalf of the Royal College of Obstetricians and Gynaecologists. Care of Women Presenting with Suspected Preterm Prelabour Rupture of Membranes from 24+0 Weeks of Gestation. BJOG 2019;126:e152–166. 8. E Weiner 1 2, J Barrett 1, A Zaltz 1, M Ram 1 3, A Aviram 1 3, M Kibel 1, H Lipworth 1, E Asztalos 4, N Melamed. «Amniotic fluid volume at presentation with early preterm prelabor rupture of membranes and association with severe neonatal respiratory morbidity». Ultrasound Obstet Gynecol. 2019 Dec;54(6):767-773. doi: 10.1002/uog.20257. 9. Ashraf Sadat Mousavi, Neda Hashemi, Maryam Kashanian, Narges Sheikhansari, Arash Bordbar & Shayesteh Parashi (2018) Comparison between maternal and neonatal outcome of PPROM in the cases of amniotic fluid index (AFI) of more and less than 5 cm, Journal of Obstetrics and Gynaecology, 38:5, 611-615, DOI: 10.1080/01443615.2017.1394280 10. WHO recommendation on tocolytic therapy for improving preterm birth outcomes. Geneva: World Health Organization; 2022. Licence: CC BY-NC-SA 3.0 IGO. 11. Van Vliet E.O.G., Nijman T.A.J., Schuit E., Heida K.Y., Opmeer B.C., Kok M. et al. Nifedipine versus atosiban for threatened preterm birth (APOSTEL III): a multicentre, randomised controlled trial. Lancet. 2016; 387(10033): 2117-24. doi: 10.1016/S0140-6736(16)00548-1. 12. Haram K., Mortensen J.H., Morrison J.C. Tocolysis for acute preterm labor: does anything work. J. Matern. Fetal Neonatal Med. 2015; 28(4): 371-8. doi: 10.3109/14767058.2014.918095. 13. Cochrane Database of Systematic Reviews. Planned early birth versus expectant management for women with preterm prelabour rupture of membranes prior to 37 weeks' gestation for improving pregnancy outcome (Review). Bond DM, Middleton P, Levett KM, van der Ham DP, Crowther CA, Buchanan SL, Morris J. Cochrane Database of Systematic Reviews 2017, Issue 3. Art. No.: CD004735. DOI: 10.1002/14651858.CD004735.pub4. 14. Emma L. Barber, Guomao Zhao, Irina A. Buhimschi, MD. Duration of Intrapartum Prophylaxis and Concentration of Penicillin G in Fetal Serum at Delivery. Obstet Gynecol. 2008 August; 112(2 Pt 1): 265–270. doi:10.1097/AOG.0b013e31817d0246.
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указанием квалификационных данных:
1) Искаков Серик Саятович – кандидат медицинских наук, PhD, НАО «Медицинский университет Астана», заведующий кафедрой акушерства и гинекологии №2, врач акушер-гинеколог высшей квалификационной категории.
2) Рапильбекова Гульмира Курбановна – доктор медицинских наук, заведующая гинекологическим отделением Корпоративного фонда «University Medical Center», врач акушер-гинеколог высшей квалификационной категории.
3) Шегенов Г.А. – PhD, НАО «Медицинский университет Астана», доцент кафедры акушерства и гинекологии №2, врач акушер-гинеколог первой квалификационной категории.
4) Тулетова Айнур Серикпаевна - PhD, ассоциированный профессор, ТОО «Талмас Медикус», руководитель клинико-инновационного центра, врач акушер-гинеколог высшей квалификационной категории.
5) Акылжанова Ж.Е. – кандидат медицинских наук, НАО «Медицинский университет Астана», ассистент кафедры акушерства и гинекологии №2, врач акушер-гинеколог высшей квалификационной категории.
6) Ожмухаметова Э.К. – PhD, КГП на ПХВ «Городская многопрофильная больница №2», Управление общественного здравоохранения города Астаны, врач клинический фармаколог.
Указание на отсутствие конфликта интересов: отсутствует.
Рецензенты:
Омарова Гульжахан Кашкинбаевна – доктор медицинских наук, профессор кафедры акушерства и гинекологии НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова», врач акушер-гинеколог высшей категории.
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Приложение 1.
NB! Не рекомендуется проводить дородовую амниоинфузию у пациентов с ПРПО. В систематическом обзоре и метаанализе 2014 г. сравнивались исходы беременности у пациенток, получивших дородовую трансабдоминальную амниоинфузию, с теми, кто получал обычную помощь для ведения ПРПО в третьем триместре (пять рандомизированных исследований, n = 241 беременность) Трансабдоминальная амниоинфузия привела к статистически значимому снижению неонатальной смертности, сепсиса/инфекции и легочной гипоплазии, но данные по каждому исходу были ограничены одним-двумя очень небольшими испытаниями низкого или среднего качества.
Чтобы более полно понять, полезна ли амниоинфузия при ПРПО, требуется больше и лучше информации о влиянии конкретных протоколов амниоинфузии, отборе пациентов (например, гестационном возрасте на момент разрыва плодных оболочек) и других вмешательствах (тип, доза и продолжительность введения, антибиотики, применение кортикостероидов) на перинатальный исход.
Амниоинфузия – операция по введению раствора, по составу сходного с составом амниотической жидкости в амниотическую полость. Теоретически, плод может выиграть от амниоинфузии, так как это может помешать развитию гипоплазии легких и контрактуры суставов. Однако, преимущество повторяющихся трансабдоминальных амнионифузий для лечения ПРПО видится весьма скромными. Основными проблемами, возникающими при данной манипуляции, были:
- неспособность удержать жидкость внутри полости матки после процедуры amniotransfusion, и, следовательно, минимальная эффективность процедуры,
- потребность в многочисленных пункциях плодных оболочек, которые повышают риск преждевременных родов и внутриутробной инфекции.
Не рекомендуются проводить дородовую амниоинфузию у пациентов с ПРПО [8].
Имплантация порт-системы. Катетер специальной формы (предотвращающей ее изгнание из матки) устанавливается в амниотической полости. Используя эту систему, жидкость может непрерывно вводиться в матку [4]. Основные результаты предыдущих исследований показали, что использование подкожно имплантированной AFR порт – системы для долгосрочной амниоинфузии в лечении ПРПО является эффективным с целью пролонгирования беременности и в предотвращении гипоплазия легких [2, 8]. Подкожная имплантация порта предоставляет врачу возможность введения частых и долгосрочных вливаний, тем самым позволяя врачу заменить потерю жидкости из-за ПРПО и, как следствие, продлить срок гестации [7]. Эффект промывания путем непрерывного внутриамниотического вливания гипотонического солевого раствора также способен защитить пациента от развития синдрома амниотической инфекции.
Со стороны плода
Противопоказания
Данную операцию может проводить только специально обученный медицинский персонал.
Шаг 1: Премедикация. Внутривенное введение магния сульфат в размере 2 г/ч и индометацина в виде ректальных свечей в дозе 100 мг два раза в день, до процедуры, чтобы избежать сокращений матки.
Шаг 2: Амниоинфузия. После ультразвуковой диагностики локализации плаценты и местной анестезии с 20 мл 0,25% раствора новокаина, амниоинфузия 300 мл физиологического раствора осуществляется с иглой 22G под ультразвуковым контролем.
Шаг 4: Введение катетера в амниотическую полость. После пункции амниотической полости с поисковой иглой 19G под контролем УЗИ через подготовленное вместилище и рентгеноконтрастный (1,5 French) резиновый катетер для инфузия со съемным (1,0 French) стилет вводится через иглу в амниотическую полость. Тонкий стилет удаляют, и катетер сокращается. Правильное позиционирование катетера проверяют аспирированием небольшого количества околоплодных вод
Шаг 5: Имплантация капсулы порта. Капсула порта сначала промывается физиологическим раствором с использованием атравматической иглы 25G (длиной 9 мм), чтобы заполнить порт-систему. Капсула порта, связанная с катетером вновь промывается с физиологически раствором. Впоследствии, порт вставляется в подготовленный карман, где он крепится к подкожной жировой клетчатки и закрывается кожей.
NB!! Положительный эффект непрерывной амниоинфузии через подкожно имплантированную перинатальную портовую систему с амниотической жидкостью, такой как гипоосмотический раствор, при «классическом ПРПО» сроком беременности менее 28/0 недель является многообещающим, но должен быть доказан!! в будущих проспективных рандомизированных исследованиях [5].
Ведение при ПРПО и инфекция ВПГ
Рецидивирующий активный ВПГ:
Первичный ВПГ:
Приложение 2.
Имплантация порт-системы. Катетер специальной формы (предотвращающей ее изгнание из матки) устанавливается в амниотической полости. Используя эту систему, жидкость может непрерывно вводиться в матку [4]. Основные результаты предыдущих исследований показали, что использование подкожно имплантированной AFR порт – системы для долгосрочной амниоинфузии в лечении ПРПО является эффективным с целью пролонгирования беременности и в предотвращении гипоплазия легких [2, 8]. Подкожная имплантация порта предоставляет врачу возможность введения частых и долгосрочных вливаний, тем самым позволяя врачу заменить потерю жидкости из-за ПРПО и, как следствие, продлить срок гестации [7]. Эффект промывания путем непрерывного внутриамниотического вливания гипотонического солевого раствора также способен защитить пациента от развития синдрома амниотической инфекции.
Условия для проведения операции амниоинфузии:
Со стороны матери
• письменное информированное согласие;
• одноплодная беременность;
• срок гестации от 22 недель+ 0 дней до 25 недели + 6 дней;
• выраженное маловодие (индекс амниотической жидкости < 5th centile или минимальный амниотический пакет < 2cm) [4].
Со стороны плода
• наличие ПРПО, подтвержденное клиническими и лабораторными исследованиями.
Противопоказания
Пороки развития плода, несовместимые с жизнью;
внутриутробная гибель плода;
хориоамнионит;
роды.
Данную операцию может проводить только специально обученный медицинский персонал.
Техника операции Имплантация порт-системы
Порт имплантация должна быть выполнена в соответствии с определенным протоколом [4].
Шаг 1: Премедикация. Внутривенное введение магния сульфат в размере 2 г/ч и индометацина в виде ректальных свечей в дозе 100 мг два раза в день, до процедуры, чтобы избежать сокращений матки.
Шаг 2: Амниоинфузия. После ультразвуковой диагностики локализации плаценты и местной анестезии с 20 мл 0,25% раствора новокаина, амниоинфузия 300 мл физиологического раствора осуществляется с иглой 22G под ультразвуковым контролем.
Шаг 3: Подготовка ложа для порта. Небольшой разрез кожи производится с помощью скальпеля под местной анестезией с 20 мл 0,25% раствора новокаина, после подготовки подкожного вместилища для капсулы порта с помощью ножниц.
Шаг 4: Введение катетера в амниотическую полость. После пункции амниотической полости с поисковой иглой 19G под контролем УЗИ через подготовленное вместилище и рентгеноконтрастный (1,5 French) резиновый катетер для инфузия со съемным (1,0 French) стилет вводится через иглу в амниотическую полость. Тонкий стилет удаляют, и катетер сокращается. Правильное позиционирование катетера проверяют аспирированием небольшого количества околоплодных вод
Шаг 5: Имплантация капсулы порта. Капсула порта сначала промывается физиологическим раствором с использованием атравматической иглы 25G (длиной 9 мм), чтобы заполнить порт-систему. Капсула порта, связанная с катетером вновь промывается с физиологически раствором. Впоследствии, порт вставляется в подготовленный карман, где он крепится к подкожной жировой клетчатки и закрывается кожей.
Физиологический раствор вводят в порту системы под контролем цветной ультразвуковой допплерографии через 25G атравматическую иглу для проверки правильности расположения катетера. После имплантации порт системы, гипотонический раствор вливают с перерывами со скоростью инфузии от 50 мл / ч до 100 мл/ч при периодическом контролем УЗИ для того, чтобы обеспечить постоянное количество жидкости в амниотической полости [6].
NB!! Положительный эффект непрерывной амниоинфузии через подкожно имплантированную перинатальную портовую систему с амниотической жидкостью, такой как гипоосмотический раствор, при «классическом ПРПО» сроком беременности менее 28/0 недель является многообещающим, но должен быть доказан!! в будущих проспективных рандомизированных исследованиях [5].
Приложение 3
Ведение при ПРПО и инфекция ВПГ
Риск вертикальной передачи при первичном ВПГ составляет 30-50%, рецидиве ВПГ 3%.
Рецидивирующий активный ВПГ:
рекомендуется выжидательная тактика при беременности <34недель 0 дней;
начать терапию ВПГ;
кортикостероиды, антибиотики, сульфат магния - по показаниям;
кесарево сечение показано при наличии активного заболевания или продромальных симптомов во время родов.
Первичный ВПГ:
управление менее ясно из-за высокого риска вертикальной передачи;
рекомендуется терапия ВПГ;
кесарево сечение рекомендуется при наличии активных поражений.
Ведение при ПРПО и ВИЧ-инфекции
Посев на бета-гемолитический стрептококк группы В.
Специальной подготовки к исследованию не требуется. Исследование проводят методом посева на плотные питательные среды. Исследуемый материал: мазок из входа во влагалище или аноректальной области; отделяемое влагалища. Интерпретация: в норме рост стрептококка группы В отсутствует. Обнаружение роста у беременной женщины в любом титре расценивают как клинически значимое.
Приложение 4
Ведение при ПРПО и ВИЧ-инфекции
оптимальное управление не определено из-за опасений вертикальной передачи при ДИВ;
ведение должно включать врача, имеющего опыт лечения ВИЧ-инфекции во время беременности, и следует следовать стандартным рекомендациям по ВИЧ;
самые последние данные свидетельствуют о том, что риск вертикальной передачи не увеличивается, если пациентка находится на высокоактивной антиретровирусной терапии с низкой вирусной нагрузкой и получала зидовудин до и во время родов;
управление должно быть индивидуальным;
если гестационный возраст ранний, но пациентка получает соответствующую терапию с низкой вирусной нагрузкой, может быть целесообразным выжидательная тактика.
Приложение 5
Посев на бета-гемолитический стрептококк группы В.
Специальной подготовки к исследованию не требуется. Исследование проводят методом посева на плотные питательные среды. Исследуемый материал: мазок из входа во влагалище или аноректальной области; отделяемое влагалища. Интерпретация: в норме рост стрептококка группы В отсутствует. Обнаружение роста у беременной женщины в любом титре расценивают как клинически значимое.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.