Папилломавирусная инфекция человека
 Версия: Клинические протоколы КР 2022 (Кыргызстан)
Версия: Клинические протоколы КР 2022 (Кыргызстан)
Аногенитальные (венерические) бородавки (A63.0), Вирусные бородавки (B07), Доброкачественное новообразование кожи века, включая спайку век (D23.1), Доброкачественное новообразование кожи верхней конечности, включая область плечевого сустава (D23.6), Доброкачественное новообразование кожи волосистой части головы и шеи (D23.4), Доброкачественное новообразование кожи губы (D23.0), Доброкачественное новообразование кожи других и неуточненных частей лица (D23.3), Доброкачественное новообразование кожи неуточненной локализации (D23.9), Доброкачественное новообразование кожи нижней конечности, включая область тазобедренного сустава (D23.7), Доброкачественное новообразование кожи туловища (D23.5), Доброкачественное новообразование кожи уха и наружного слухового прохода (D23.2), Доброкачественное новообразование молочной железы (D24), Доброкачественное новообразование ободочной кишки, прямой кишки, заднего прохода [ануса] и анального канала (D12), Доброкачественное новообразование рта и глотки (D10), Доброкачественное новообразование среднего уха и органов дыхания (D14), Доброкачественные новообразования мочевых органов (D30), Другие доброкачественные новообразования матки (D26), Папилломавирусы как причина болезней, классифицированных в других рубриках (B97.7)
Дерматовенерология, Инфекционные болезни у детей, Инфекционные и паразитарные болезни
Общая информация
Краткое описание
Приложение 5
к приказу МЗ КР №1023
от “23” августа 2022 г.
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ КЫРГЫЗСКОЙ РЕСПУБЛИКИ
КЛИНИЧЕСКОЕ РУКОВОДСТВО
по диагностике и лечению папилломавирусной инфекции человека
(для всех уровней организаций здравоохранения)
Папилломавирусная инфекция (ПВИ) - заболевания, вызванные вирусом папилломы человека (ВПЧ), передающиеся преимущественно половым, редко контактным, путем, с латентным началом, хроническим персистирующим течением, и проявляются доброкачественными и злокачественными новообразованиями в зоне входных ворот инфекции. [1, 2]
ПВИ является одной из наиболее распространенных инфекций репродуктивного тракта и причиной ряда заболеваний как у мужчин, так и у женщин, включая предраковые поражения, которые могут развиться в рак. Хотя большинство ВПЧ-инфекций не вызывает симптомов и купируется спонтанно, хроническая инфекция, вызванная ВПЧ, может привести к заболеванию. У женщин хроническая инфекция, вызванная специфическими типами ВПЧ (чаще всего типами ВПЧ-16 и ВПЧ-18), может привести к предраковым поражениям, которые, если их не лечить, могут развиться в рак шейки матки. С ВПЧ также ассоциируют рак ротоглотки и рак аногенитальной области и другие болезни как у мужчин, так и у женщин [3].
Кодирование по МКБ-10
Кодирование по МКБ-10
|
Код
|
Наименование |
| А63.0 | Аногенитальные (венерические) бородавки |
|
B07
|
Вирусные бородавки |
| В97.7 | Папилломавирусы как причина болезней, классифицированных в других рубриках |
|
D10
|
Доброкачественное новообразование рта и глотки / Губы |
| D12 | Доброкачественное новообразование ободочной кишки, прямой кишки, заднего прохода [ануса] и анального канала |
| D14 | Доброкачественное новообразование среднего уха и органов дыхания |
|
D23.0
|
Другие доброкачественные новообразования кожи губ |
| D23.1 | Доброкачественные новообразования кожи века, включая спайку век |
| D23.2 | Доброкачественные новообразования кожи уха и наружного слухового прохода |
|
D23.3
|
Доброкачественные новообразования кожи других и неуточненных частей лица |
| D23.4 | Доброкачественные новообразования кожи волосистой части головы и шеи |
| D23.5 | Доброкачественные новообразования кожи туловища |
|
D23.6
|
Доброкачественные новообразования кожи верхней конечности, включая область плечевого сустава |
|
D23.7
|
Доброкачественные новообразования кожи нижней конечности, включая область тазобедренного сустава |
| D23.9 | Доброкачественные новообразования кожи неуточненной локализации |
|
D24
|
Доброкачественное новообразование молочной железы |
| D26 | Другие доброкачественные новообразования матки |
| D30 | Доброкачественные новообразования мочевых органов |
Классификация
Классификация
Общепринятой классификации папилломавирусной инфекции не существует.
Этиология и патогенез
Этиология и патогенез
Этиология
ВПЧ - это группа чрезвычайно распространенных и генетически разнородных ДНК-содержащих вирусов, поражающих эпителий кожных покровов и слизистых оболочек. В настоящее время идентифицировано более 200 генотипов вирусов папилломы человека, из них около 45 генотипов ВПЧ могут инфицировать урогенитальный тракт [3].
Возбудитель заболевания – вирус папилломы человека (ВПЧ) относится к семейству папилломавирусов (Papillomaviridae), состоящему из 16 родов, представители 5 из которых патогенны для человека 3:
1. Alphapapillomavirus (инфицирует оральный и урогенитальный эпителий): ВПЧ 2, 3, 6, 7, 10, 11, 13, 16, 18, 26-35, 39, 40, 42-45, 51-59, 61, cand62, 66-74, 77, 78, 81-84, cand85-90, 91, 94, PCPV-1, 1С, RhPV-1;
Инфицируют клетки кожи человека:
2. Betapapillomavirus (ВПЧ 5, 8, 9, 12, 14, 15, 17, 19-25, 36-38, 47, 49, 75, 76, 80, cand92, cand96, BPV-1, BPV-2, DPV, OvPV-1, OvPV-2);
3. Gammapapilloma virus (ВПЧ 4, 48, 50, 60, 65, 88, 95);
4. Mupapillomavirus (ВПЧ 1, 63);
5. Nupapillomavirus (вызывает доброкачественные и злокачественные новообразования): ВПЧ-41.
В настоящее время к вирусам высокого онкогенного риска отнесены 15 генотипов ВПЧ (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 73, 82), к вирусам возможно высокого онкогенного риска – 3 генотипа (26, 53, 66) и к вирусам низкого онкогенного риска – 12 генотипов ВПЧ (6, 11, 40, 42, 43, 44, 54, 61, 70, 72, 81 и СР 6108).
Международное Агентство по исследованию рака (The InternationalAgency for Research on Cancer) признало ВПЧ этиологическим агентом широкого спектра онкологических заболеваний, таких как рак шейки матки, вульвы, влагалища, анального канала, пениса, головы и шеи, а также аногенитальных (венерических) бородавок, как у мужчин, так и у женщин, и рецидивирующего респираторного папилломатоза [4-7].
В настоящее время к вирусам высокого онкогенного риска отнесены 15 генотипов ВПЧ (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 73, 82), к вирусам возможно высокого онкогенного риска – 3 генотипа (26, 53, 66) и к вирусам низкого онкогенного риска – 12 генотипов ВПЧ (6, 11, 40, 42, 43, 44, 54, 61, 70, 72, 81 и СР 6108).
Патогенез
ВПЧ обладает тропностью к эпителиальным тканям (кожа, слизистые оболочки) вне зависимости от их локализациии проникает в клетку через микроскопические порезы и потертости (дефекты). Несмотря на то, что большинство людей на протяжении жизни инфицируются этим возбудителем, чаще всего инфицирование заканчивается самопроизвольной элиминацией вируса из организма при полноценной иммунной сопротивляемости организма в течение 2 лет у 90% инфицированных лиц [7].
Факторами, способствующими инфицированию ПВИ и развитию заболеваний, признаются раннее начало половой жизни (увеличивает риск инфицирования в 22 раза), частая смена половых партнеров, частые роды и аборты, сопутствующая урогенитальная инфекция и нарушения биоценоза влагалища, курение, иммунодефицитные состояния, генетическая предрасположенность и гормональные факторы [8-10].
В процессе инфицирования вирус папилломы человека поражает незрелые клетки, чаще базального слоя, которые затем являются постоянным источником инфицирования эпителиальных клеток. Инфицированию способствует наличие микротравм и воспалительных процессов кожи и слизистых оболочек, приводящих к снижению местного иммунитета.
По мере того как делятся инфицированные базальные клетки, осуществляются репликация вирусного генома и его распределение между дочерними клетками, что приводит к увеличению количества инфицированных клеток в данном клеточном слое. Выработка новых вирусных частиц в уже инфицированных клетках подавляется, и процесс становится продуктивным только при перемещении данных клеток в вышерасположенные слои, в первую очередь в супрабазальные. При перемещении инфицированных базальных клеток в восходящем направлении происходит нарушение клеточного цикла нормальных эпителиоцитов. Таким образом, интеграция генома ВПЧ в геном человеческой клетки обеспечивает преимущество роста и постоянной неконтролируемой пролиферации генетически измененных клеток, что в конечном итоге приводит к развитию предраковых поражений и рака некоторых органов [8-10]. Персистенция онкогенных типов ВПЧ - необходимое условие для развития злокачественной опухоли и имеет место у 5-10% пациентов.
Вирус папилломы человека - единственный вирус, который не проникает в кровь, вследствие чего инфекционный процесс протекает без развития воспалительной реакции. Перенесенная ПВИ не защищает от повторного инфицирования, вирус способен персистировать в месте проникновения как угодно долго. Более того, ВПЧ является генетически стабильным и исключительно внутриэпителиальным, проникает в цитоплазму без повреждения кератиноцита, поэтому препятствует активации врожденного иммунитета посредством реryляции продукции противовирусных цитокинов, в частности фактора некроза опухоли и γ-интерферона, обладающих противовирусными и антипролиферативными свойствами.
Онкопротеины вируса Е6 и Е7 способны подавлять противовирусные механизмы в клетке. ВПЧ не экспрессирует антигенные белки (Ll иL2), имеющие основное значение в формировании гуморального (антительного) ответа, пока не образует достаточного количества копий вируса (до фазы позднего репликативного цикла). В результате антитела к ВПЧ обнаруживаются только у 50-70% инфицированных женщин, гyморальный ответ организма человека на естественную ПВИ развивается относительно медленно и является недостаточно эффективным [10-11].
Наиболее характерными типоспецифичными антителами являются антитела, направленные против белка L1 вируса. В среднем с момента инфицирования до сероконверсии проходит приблизительно 8-12 месяцев [11]. Интервал между инфицированием ВПЧ и прогрессированием до инвазивного рака, как правило, составляет более 10 лет. Инвазивному раку предшествуют предраковые поражения или интраэпителиальные неоплазии различной степени тяжести: шейки матки I-III степени (CIN I-III), вульвы (VIN I-III), влагалища (VaIN I-III), анального канала (AIN I-III), полового члена (PIN I-III).
Факторами, способствующими инфицированию ПВИ и развитию заболеваний, признаются раннее начало половой жизни (увеличивает риск инфицирования в 22 раза), частая смена половых партнеров, частые роды и аборты, сопутствующая урогенитальная инфекция и нарушения биоценоза влагалища, курение, иммунодефицитные состояния, генетическая предрасположенность и гормональные факторы [8-10].
В процессе инфицирования вирус папилломы человека поражает незрелые клетки, чаще базального слоя, которые затем являются постоянным источником инфицирования эпителиальных клеток. Инфицированию способствует наличие микротравм и воспалительных процессов кожи и слизистых оболочек, приводящих к снижению местного иммунитета.
По мере того как делятся инфицированные базальные клетки, осуществляются репликация вирусного генома и его распределение между дочерними клетками, что приводит к увеличению количества инфицированных клеток в данном клеточном слое. Выработка новых вирусных частиц в уже инфицированных клетках подавляется, и процесс становится продуктивным только при перемещении данных клеток в вышерасположенные слои, в первую очередь в супрабазальные. При перемещении инфицированных базальных клеток в восходящем направлении происходит нарушение клеточного цикла нормальных эпителиоцитов. Таким образом, интеграция генома ВПЧ в геном человеческой клетки обеспечивает преимущество роста и постоянной неконтролируемой пролиферации генетически измененных клеток, что в конечном итоге приводит к развитию предраковых поражений и рака некоторых органов [8-10]. Персистенция онкогенных типов ВПЧ - необходимое условие для развития злокачественной опухоли и имеет место у 5-10% пациентов.
Вирус папилломы человека - единственный вирус, который не проникает в кровь, вследствие чего инфекционный процесс протекает без развития воспалительной реакции. Перенесенная ПВИ не защищает от повторного инфицирования, вирус способен персистировать в месте проникновения как угодно долго. Более того, ВПЧ является генетически стабильным и исключительно внутриэпителиальным, проникает в цитоплазму без повреждения кератиноцита, поэтому препятствует активации врожденного иммунитета посредством реryляции продукции противовирусных цитокинов, в частности фактора некроза опухоли и γ-интерферона, обладающих противовирусными и антипролиферативными свойствами.
Онкопротеины вируса Е6 и Е7 способны подавлять противовирусные механизмы в клетке. ВПЧ не экспрессирует антигенные белки (Ll иL2), имеющие основное значение в формировании гуморального (антительного) ответа, пока не образует достаточного количества копий вируса (до фазы позднего репликативного цикла). В результате антитела к ВПЧ обнаруживаются только у 50-70% инфицированных женщин, гyморальный ответ организма человека на естественную ПВИ развивается относительно медленно и является недостаточно эффективным [10-11].
Наиболее характерными типоспецифичными антителами являются антитела, направленные против белка L1 вируса. В среднем с момента инфицирования до сероконверсии проходит приблизительно 8-12 месяцев [11]. Интервал между инфицированием ВПЧ и прогрессированием до инвазивного рака, как правило, составляет более 10 лет. Инвазивному раку предшествуют предраковые поражения или интраэпителиальные неоплазии различной степени тяжести: шейки матки I-III степени (CIN I-III), вульвы (VIN I-III), влагалища (VaIN I-III), анального канала (AIN I-III), полового члена (PIN I-III).
Эпидемиология
Эпидемиология
Папилломавирусная инфекция наиболее часто регистрируется у лиц молодого возраста, имеющих большое число половых партнеров. По данным ВОЗ, 50-80% населения инфицировано ВПЧ, но лишь 5-10% инфицированных лиц имеют клинические проявления заболевания [3].
Согласно систематизированному анализу мировых данных, заболеваемость аногенитальными бородавками мужчин и женщин (включая новые случаи и рецидивы заболевания) варьирует от 160 до 289 случаев на 100000 населения, со средним значением 194,5 случаев на 100000 населения, а средний ежегодный уровень выявляемости новых случаев аногенитальных бородавок составляет 137 случаев на 100000 населения среди мужчин и 120,5 случаев на 100000 населения среди женщин.
ВПЧ относится к высококонтагиозным мукозотропным и дерматотропным вирусам, передаваемым от человека к человеку половым путем (вагинальные, анальные, оральные половые контакты), а также контактно-бытовым и вертикальным путями. При однократном половом контакте вероятность инфицирования ВПЧ достигает 80%. К факторам риска относят раннее начало половой жизни, беспорядочные половые связи, незащищенные половые контакты, сопутствующие инфекции и воспалительные процессы, затрагивающие шейку матки.
Инфицирование детей происходит – трансплацентарным (редко), перинатальным и половым путями. Возможность аутоинокуляции и передачи ВПЧ через бытовые предметы остается недостаточно изученной. Медицинский персонал может инфицироваться ВПЧ во время лазерной деструкции аногенитальных бородавок, вдыхая образующийся дым, содержащий вирус.
Клиническая картина
Cимптомы, течение
Клиническая картина [12]
Инкубационный период заболевания может длиться от нескольких месяцев до нескольких лет. Среднее время между инфицированием ВПЧ и развитием аногенитальных бородавок составляет от 3 месяцев у женщин до 11 месяцев у мужчин. Инфицирование человека может происходить как одним, так и несколькими типами ВПЧ [10, 11].
В зависимости от клинической картины, вызванным вирусом папилломы, возможно несколько вариантов течения инфекционного процесса:
1 стадия, ее также именуют латентной. На данном этапе нет никаких внешних проявлений заболевания, в таком состоянии ВПЧ может оставаться много лет и обнаруживаться при случайной диагностике, причем информативны только данные исследования методом ПЦР.
2 стадия, этап развития клинической симптоматики в результате влияния вириона на клетку. Спектр эффективных диагностических анализов расширяются, кроме того, на теле или слизистых оболочках отчетливо заметны специфические признаки ВПЧ.
3 этап дисплазии. Характерна для канцерогенных изменений в структуре клетки.
4 стадия, этап формирования карциномы, иными словами, злокачественного перерождения клетки.
Прогноз заболевания, которое вызвал вирус папилломы, зависит от свойств самого вириона. Если он проникает в клетку и встраивается в ДНК человека, не избежать злокачественного образования. Но в некоторых случаях ВПЧ не затрагивает геном инфицированной клетки, тогда инфекция приобретает рецидивирующее течение.
Заболевание может протекать в нескольких вариантах. Выраженная форма ВПЧ подразумевает наличие определенной клинической симптоматики, субклиническая сопровождается периодическими проявлениями признаков заболевания, латентная протекает скрыто и может вообще не проявиться на протяжении всей жизни человека.
Таблица 1. Типы ВПЧ, ассоциированные с поражениями кожи и слизистых оболочек (Villiers, 1989)
Инфицирование ВПЧ как высокого, так и низкого канцерогенного риска способно привести (как у мужчин, так и у женщин) к развитию генитальных бородавок, а также цервикальной дисплазии легкой степени (L-SIL или CIN I).
Прогноз заболевания, которое вызвал вирус папилломы, зависит от свойств самого вириона. Если он проникает в клетку и встраивается в ДНК человека, не избежать злокачественного образования. Но в некоторых случаях ВПЧ не затрагивает геном инфицированной клетки, тогда инфекция приобретает рецидивирующее течение.
Заболевание может протекать в нескольких вариантах. Выраженная форма ВПЧ подразумевает наличие определенной клинической симптоматики, субклиническая сопровождается периодическими проявлениями признаков заболевания, латентная протекает скрыто и может вообще не проявиться на протяжении всей жизни человека.
Клинические проявления хронической ПВИ многообразны и одинаково актуальны как для женщин, так и для мужчин (табл. 1).
Таблица 1. Типы ВПЧ, ассоциированные с поражениями кожи и слизистых оболочек (Villiers, 1989)
|
Клинические проявления
|
Типы ВПЧ |
| Поражения кожи | |
| Подошвенные бородавки | 1, 2, 4 |
| Обычные бородавки | 2, 4, 26, 27, 29, 57 |
| Плоские бородавки | 3, 10, 28, 49 |
| Бородавки Бютчера | 7 |
| Бородавчатая эпидермодисплазия | 5, 8, 9, 10, 12, 15, 19, 36 |
| Небородавчатые кожные поражения | 37, 38 |
| Поражения слизистых оболочек гениталий | |
| Остроконечные кондиломы | 6, 11, 42–44, 54 |
| Некондиломатозные поражения | 6, 11, 16, 18, 30, 31, 33, 34, 35, 39, 40, 42, 43, 51, 52, 55, 56, 57–59, 61, 64, 67–70 |
| Карцинома | 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 70 |
| Экстрагенитальные поражения слизистых оболочек | |
| Папиллома гортани | 6, 11, 30 |
| Карцинома шеи, языка | 2, 6, 11, 16, 18, 30 |
Инфицирование ВПЧ как высокого, так и низкого канцерогенного риска способно привести (как у мужчин, так и у женщин) к развитию генитальных бородавок, а также цервикальной дисплазии легкой степени (L-SIL или CIN I).
Диагностика
Диагностика
Жалобы и осмотр [12-16]
Поражения кожи
В зависимости от особенностей клинической картины заболевания выделяют следующие виды кожных поражений:
вульгарные бородавки;
ладонно-подошвенные бородавки;
мозаичные бородавки;
кистозные бородавки;
плоские бородавки;
нитевидные бородавки;
бородавки «мясников»;
фокальная эпителиальная гиперплазия;
верруциформная эпидермодисплазия.
Жалобы:
Жалобы:
Наиболее частым симптомом, которым характеризуется папилломавирус человека, служит появление бородавок.
Их локализация может быть различной, но чаще всего они располагаются на участках кожи, подверженной травмам и микротрещинам. Это подошва, кисти рук, ладони.
Субъективные симптомы:
наличие одиночных или множественных образований в виде папул на коже и/или слизистых оболочках;
болезненность при компрессии в местах локализации бородавок;
деформация ногтевых пластинок при формировании разрастаний в зоне околоногтевых валиков;
деформация стопы при массивном поражении кожи подошвы и выраженном болевом синдроме.
Осложнения
ВОЗ и многие международные организации по борьбе с онкологическими заболеваниями рекомендуют использовать молекулярно-генетические исследования — тест на ВПЧ при первичном скрининге у женщин старше 30 лет в сочетании с цитологическим исследованием или в качестве самостоятельного теста в странах, где плохо организованы программы цервикального цитологического скрининга, а также для мониторинга лечения умеренной и тяжелой дисплазии (CIN II и CIN III), карциномы in situ и инвазивного рака. Данный метод весьма полезен и для разрешения сомнительных результатов цитологического исследования, как при первичном выявлении неопластических изменений, так и у пациенток, получающих лечение по поводу дисплазии и рака.
Тест на уксусную кислоту может быть полезен при диагностике остроконечных кондилом. В частности, замачивание уксусной кислоты в подозрительных очагах может повысить степень подозрительности в очагах без классических признаков. Способ включает наложение на предполагаемые поражения полового члена, шейки матки, половых губ или перианальной области марлевого тампона, смоченного 3-5%–ной уксусной кислотой, в течение 5-10 минут. Незаметные, плоские повреждения гениталий, которые трудно оценить, становятся заметными. Диспластические и неопластические ткани белеют (ацетовит). Ложноположительные результаты распространены и могут быть результатом всего, что вызывает паракератоз (например, кандидоз, псориаз, красный плоский лишай, заживление эпителия, сальных желез). Тест на уксусную кислоту можно использовать в сочетании с кольпоскопией для изучения поражений шейки матки. Однако этот тест предназначен только для подозрительных поражений и не должен использоваться для рутинного скрининга.
Существующие методы диагностики в КР
Визуальный осмотр шейки матки.
Кольпоскопия – данный диагностический метод применяется в некоторых государственных клиниках и в частных медицинских центрах.
Цитологический анализ соскоба шейки матки – большинство врачей осуществляют забор соскоба и направляют в лаборатории для проведения цитологического исследования. Цитологический анализ проводится в центре онкологии, в патологоанатомическом бюро и в его филиалах.
Биопсия из патологического участка шейки матки – в клиниках, где проводится кольпоскопия, осуществляется забор материала с помощью конхотома и скальпеля, а также применяется электрохирургические аппараты Сургитрон, Фотек (электропетля).
ПЦР на ВПЧ (ПВЧ скрининг, Квант) – данное исследование осуществляется только в частных медицинских лабораториях.
Клинические анализы для выявления онкогенных типов ВПЧ:
Инструментальная диагностика [12-16]
Объективные симптомы:
вульгарные бородавки: множественные безболезненные папулы диаметром 0,2-0,5 см, покрытые папилломатозными разрастаниями и локализующиеся преимущественно на тыле кистей и стоп;
ладонно-подошвенные бородавки: плотные болезненные округлые папулы и бляшки, локализующиеся на коже подошв стоп и/или ладонной поверхности кистей на одном уровне с неизмененной кожей, имеющие зернистую поверхность, покрытую гиперкератотическими наслоениями; в центре образований нередко наблюдаются черно-коричневых точки затромбированных капилляров, повреждение которых приводит к кровотечению;
мозаичные бородавки: диффузные очаги гиперкератоза, локализующиеся на коже ладоней и подошв, чаще в области переднего отдела стопы, нередко покрытые глубокими трещинами;
кистозные бородавки: образования в виде мягкого узла с гиперкератозом и трещинами на поверхности, при вскрытии которого выделяется бело-желтое творожистое содержимое; локализуются на давящей поверхности подошвы;
плоские бородавки: мелкие множественные папулы цвета нормальной кожи, локализующиеся преимущественно на тыле кистей, предплечий, лице и слизистых оболочках;
нитевидные бородавки: тонкие роговые выросты, локализующиеся, как правило, вокруг рта, носа и глаз;
бородавки «мясников»: гипертрофические бородавчатые разрастания цвета нормальной кожи, напоминающие цветную капусту и локализующиеся на тыле кистей и пальцах у людей, имеющих профессиональный контакт с мясом;
фокальная эпителиальная гиперплазия: множественные светлые или бледно-розовые куполообразные папулы размером 0,1-0,5 см, сливающиеся в бляшки и локализующиеся на красной кайме губ с переходом на слизистую оболочку полости рта, десен и языка; встречаются исключительно у лиц индейского происхождения;
верруциформная эпидермодисплазия — аутосомно-рецессивно наследуемое заболевание, характеризующееся множественными пигментными пятнами и бородавками, главным образом, плоского типа, которые имеют тенденцию к слиянию и распространяются по всей поверхности тыла кисти, предплечий, голени, лица.
Не менее часто встречаются папилломы, которые представляют собой небольшие по размеру наросты, которые прикреплены к коже тоненькой перемычкой. Они могут формироваться на шее, лице, в подмышечных впадинах и т.д.
Выделяют несколько клинических разновидностей аногенитальных бородавок:
Не менее часто встречаются папилломы, которые представляют собой небольшие по размеру наросты, которые прикреплены к коже тоненькой перемычкой. Они могут формироваться на шее, лице, в подмышечных впадинах и т.д.
Поражения слизистых оболочек аногенитальной локализации
Заражение ВПЧ как низкого, так и высокого канцерогенного риска, способно привести к формированию аногенитальных бородавок в области половых губ, слизистой влагалища, шейки матки, кожи вокруг ануса.
Выделяют несколько клинических разновидностей аногенитальных бородавок:
остроконечные кондиломы;
бородавки в виде папул;
поражения в виде пятен;
внутриэпителиальная неоплазия;
бовеноидный папулез и болезнь Боуэна;
гигантская кондилома Бушке-Левенштайна.
Субъективные симптомы: наличие одиночных или множественных образований в виде папул, папиллом, пятен на кожных покровах и слизистых оболочках половых органов; зуд и парестезии в области поражения; болезненность во время половых контактов (диспареуния); при локализации высыпаний в области уретры – зуд, жжение, болезненность при мочеиспускании (дизурия); при обширных поражениях в области уретры – затрудненное мочеиспускание; болезненные трещины и кровоточивость кожных покровов и слизистых оболочек в местах поражения.
Субъективные симптомы: наличие одиночных или множественных образований в виде папул, папиллом, пятен на кожных покровах и слизистых оболочках половых органов; зуд и парестезии в области поражения; болезненность во время половых контактов (диспареуния); при локализации высыпаний в области уретры – зуд, жжение, болезненность при мочеиспускании (дизурия); при обширных поражениях в области уретры – затрудненное мочеиспускание; болезненные трещины и кровоточивость кожных покровов и слизистых оболочек в местах поражения.
Физикальное обследование
Проводится осмотр половых органов, паховых складок, перианальной областей.
Остроконечные кондиломы представляют собой мелкие новообразования, располагающиеся на неизмененном основании в виде тонкой нити или короткой ножки, напоминая маленькую бородавку, малину, цветную капусту или петушиный гребень. Цвет в зависимости от локализации может быть телесным или интенсивно-красным, а при мацерации — снежно-белым. По форме остроконечные кондиломы могут быть плоскими или экзофитными, иногда достигают размеров крупных опухолей; реже приобретают бородавчатую, нитевидную или висячую форму (последняя особенно характерна для кондилом, локализующихся на половом члене). Чаще всего локализуются на местах, которые подвергаются травматизации при половых контактах: у мужчин на уздечке, венечной борозде, головке и крайней плоти полового члена; реже на стволе полового члена и мошонке, где нередко бывают множественными [12].
Экзофитные кондиломы иногда поражают уретру (изолированно или в сочетании с экстрауретральными кондиломами). У женщин остроконечные кондиломы локализуются на наружных половых органах, в мочеиспускательном канале, влагалище, на шейке матки, примерно в 20% случаев вокруг заднего прохода и в промежности. На сводах влагалищной части матки остроконечные кондиломы наблюдаются преимущественно у беременных.
Остроконечные кондиломы, локализующиеся в области ануса и прямой кишки, являются следствием гениторектальных половых контактов, особенно у мужчин. Причиной их обычно является ВПЧ 6-го типа. У 50% мужчин, имеющих остроконечные кондиломы в области заднего прохода, их обнаруживают и на слизистой оболочке прямой кишки (особенно у мужчин, практикующих секс с мужчинами).
Признаками малигнизации остроконечных кондилом является быстрое увеличение за счет периферического роста, уплотнение, появление кровянистых выделений и болезненности. Многочисленными клиническими, цитологическими и гистологическими исследованиями установлено, что одной из причин дисплазий или интраэпидермального рака шейки матки являются ВПЧ 16-го и 18-го типов.
У мужчин подобные образования возникают также около анального отверстия и на половом члене. Кондиломы чем-то напоминают папилломы, но они быстро распространяются и расположены рядом друг с другом. Папиллома человека, которая располагаются в области гениталий и заднего прохода, обычно передается половым путем.
У женщин ВПЧ, локализованный в области половых органов, характеризуется такими проявлениями:
Остроконечные кондиломы представляют собой мелкие новообразования, располагающиеся на неизмененном основании в виде тонкой нити или короткой ножки, напоминая маленькую бородавку, малину, цветную капусту или петушиный гребень. Цвет в зависимости от локализации может быть телесным или интенсивно-красным, а при мацерации — снежно-белым. По форме остроконечные кондиломы могут быть плоскими или экзофитными, иногда достигают размеров крупных опухолей; реже приобретают бородавчатую, нитевидную или висячую форму (последняя особенно характерна для кондилом, локализующихся на половом члене). Чаще всего локализуются на местах, которые подвергаются травматизации при половых контактах: у мужчин на уздечке, венечной борозде, головке и крайней плоти полового члена; реже на стволе полового члена и мошонке, где нередко бывают множественными [12].
Экзофитные кондиломы иногда поражают уретру (изолированно или в сочетании с экстрауретральными кондиломами). У женщин остроконечные кондиломы локализуются на наружных половых органах, в мочеиспускательном канале, влагалище, на шейке матки, примерно в 20% случаев вокруг заднего прохода и в промежности. На сводах влагалищной части матки остроконечные кондиломы наблюдаются преимущественно у беременных.
Остроконечные кондиломы, локализующиеся в области ануса и прямой кишки, являются следствием гениторектальных половых контактов, особенно у мужчин. Причиной их обычно является ВПЧ 6-го типа. У 50% мужчин, имеющих остроконечные кондиломы в области заднего прохода, их обнаруживают и на слизистой оболочке прямой кишки (особенно у мужчин, практикующих секс с мужчинами).
Признаками малигнизации остроконечных кондилом является быстрое увеличение за счет периферического роста, уплотнение, появление кровянистых выделений и болезненности. Многочисленными клиническими, цитологическими и гистологическими исследованиями установлено, что одной из причин дисплазий или интраэпидермального рака шейки матки являются ВПЧ 16-го и 18-го типов.
У мужчин подобные образования возникают также около анального отверстия и на половом члене. Кондиломы чем-то напоминают папилломы, но они быстро распространяются и расположены рядом друг с другом. Папиллома человека, которая располагаются в области гениталий и заднего прохода, обычно передается половым путем.
Уровень убедительности рекомендаций - мнение экспертов
У женщин ВПЧ, локализованный в области половых органов, характеризуется такими проявлениями:
из-за особенностей бактериальной флоры влагалища, под остроконечной кондиломой скапливается слизистый секрет с неприятным специфическим запахом;
беспокоит зуд;
при случайной травме во время гигиенических процедур или сексуального контакта появляется боль, повреждение кондиломы сопровождается небольшим кровотечением.
Кроме того, при нетрадиционных сексуальных контактах возможны болевые ощущения и кровотечение, что повышает риск заражения другими венерическими болезнями, особенно ВИЧ. Инфицирование детей раннего возраста происходит или во время родов, или при использовании общих с зараженными родителями предметов гигиены (полотенец, мочалок и т.д.).
У мужчин папиллома характеризуется образованием сросшихся кондилом на мошонке, под головкой и на уздечке полового члена. Кожные наросты на ощупь не плотные, однако во время сексуального контакта постоянное их трение доставляет сильный дискомфорт. Рост кондиломы вокруг анального отверстия часто сопровождается болью и зудом, так как эта область все время подвержена микротравмам при дефекации и последующих гигиенических процедур.
Кроме того, при нетрадиционных сексуальных контактах возможны болевые ощущения и кровотечение, что повышает риск заражения другими венерическими болезнями, особенно ВИЧ. Инфицирование детей раннего возраста происходит или во время родов, или при использовании общих с зараженными родителями предметов гигиены (полотенец, мочалок и т.д.).
Экстрагенитальные поражения слизистых оболочек
Помимо бородавок и папиллом различной локализации, возможно поражение слизистых оболочек ротовой полости, конъюнктивы и верхних дыхательных путей. В таком случае папилломавирус человека вызывает образование так называемых ларингеальных бородавок. При ослабленном иммунитете, особенно у новорожденных, они распространяются на нижние отделы респираторного тракта, что может даже стать причиной асфиксии.
Особенности ПВИ у детей
У девочек с папилломавирусной инфекцией начиная с возраста 3-4 недель и до 7-8 лет при любых вульвовагинитах и дисбиозах влагалища отмечают тенденцию к ярко выраженному воспалению. При этом область поражения очень обширна и часто переходит на зону промежности, паховые и бедренные складки. Иногда возникают эрозии. Подобные проявления связывают с незрелостью механизмов местного иммунитета, что усугубляется нарушением правил гигиены (слишком частое или, наоборот, недостаточное подмывание, использование для этих целей неподходящих гелей и мыл, плохое выполаскивание нательного белья после стирки, чрезмерное укутывание и т.д.).
Особенности ПВИ у беременных
Как правило, папиллома никак не влияет ни на течение беременности, ни на внутриутробное развитие плода. По крайней мере, на сегодняшний день медики не выявили никакой связи между врожденными патологиями у ребенка и ВПЧ. В соответствии с разработанными в гинекологии протоколами, у любой женщины при постановке на учет в поликлинике берут мазок из влагалища на инфекции, также во время осмотра врач обращает внимание на наличие кондилом.
Папилломавирус человека типа 6 и 11 с локализацией в области половых органов может привести к поражению респираторного тракта у ребенка, поэтому женщины с подобной патологией требуют особого подхода в процессе родоразрешения.
Осложнения
Рак шейки матки (карцинома и аденокарцинома);
Анальный рак;
Рак вульвы и влагалища;
Орофарингеальный рак;
Рак полового члена;
Рецидивирующий респираторный папиллломатоз.
Лабораторная диагностика [1, 2, 12-16]
Рекомендовано исследование молекулярно-биологическими методами с целью подтверждения диагноза, идентификации генотипа ВПЧ, определения степени вирусной нагрузки и прогнозирования течения заболевания: молекулярно-биологическое исследование отделяемого из цервикального канала на вирус папилломы человека (Papilloma virus); молекулярно-биологическое исследование влагалищного отделяемого на вирус папилломы человека (Papilloma virus); молекулярно-биологическое исследование отделяемого из уретры на вирус папилломы человека (Papilloma virus) [1]
Рекомендовано исследование молекулярно-биологическими методами с целью подтверждения диагноза, идентификации генотипа ВПЧ, определения степени вирусной нагрузки и прогнозирования течения заболевания: молекулярно-биологическое исследование отделяемого из цервикального канала на вирус папилломы человека (Papilloma virus); молекулярно-биологическое исследование влагалищного отделяемого на вирус папилломы человека (Papilloma virus); молекулярно-биологическое исследование отделяемого из уретры на вирус папилломы человека (Papilloma virus) [1]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: показаниями для обследования на ВПЧ высокого онкогенного риска являются: наличие аногенитальных бородавок, других инфекций, передаваемых половым путем, у лиц женского пола – патологии шейки матки и/или изменений при кольпоскопическом и/или цитологическом исследовании, половые контакты с партнерами, у которых выявлены аногенитальные бородавки и/или положительные результаты ПЦР на ВПЧ.
Рекомендовано цитологическое исследование цервикальных мазков пациенткам для исключения цервикальной итраэпителиальной неоплазии [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств –4)
Рекомендовано прижизненное патолого-анатомическое исследование при подозрении на малигнизацию [2].
Рекомендовано прижизненное патолого-анатомическое исследование при подозрении на малигнизацию [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств –4)
Комментарии: патолого-анатомическое исследование при необходимости проводится с применением иммуногистохимического типирования.
Рекомендовано в связи с применением в терапии аногенитальных бородавок методов физической деструкции и хирургического иссечения дополнительно проводить серологическое исследование на сифилис, ВИЧ, гепатиты В и С [30].
Рекомендовано в связи с применением в терапии аногенитальных бородавок методов физической деструкции и хирургического иссечения дополнительно проводить серологическое исследование на сифилис, ВИЧ, гепатиты В и С [30].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Методы культивирования ВПЧ не разработаны. Лабораторная диагностика папилломавирусной инфекции основана на использовании молекулярно-генетических методов обнаружения фрагментов генома ВПЧ непосредственно в цервикальных соскобах или биоптатах ткани.
Цервикальная ВПЧ-инфекция может диагностироваться с использованием тестов, основанных на идентификации ДНК ВПЧ на цервикальных или вагинальных мазках. Индуцированные ВПЧ изменения эпителия шейки матки могут быть выявлены при микроскопии отторгнувшихся клеток методом, известным как тест Папаниколау (Рар). Тестирование на ДНК ВПЧ, цитология и, особенно в условиях ограниченных ресурсов, визуальный осмотр с применением уксусной кислоты используются для идентификации поражений и скрининга в отношении рака шейки матки.
Информативность цитологического метода определяется качеством взятия и обработки материала для исследования и уровнем подготовки врача-цитолога. Материал для цитологического исследования следует брать с экзоцервикса, с участка на границе многослойного плоского и цилиндрического эпителия цервикального канала и из нижней трети эндоцервикса с помощью щетки-эндобраша до проведения гинекологического осмотра или кольпоскопии при условии отсутствия воспалительных заболеваний. Мазки Папаниколау должны содержать образцы клеток из эктоцервикса, зоны трансформации и эндоцервикального канала. Тест выполняется, когда у пациентки нет менструации, чтобы цитологический образец не был закупорен кровью. Кроме того, если у пациентки имеется цервиковагинальная инфекция со слизисто-гнойными выделениями из влагалища, рассматривается возможность выполнения теста после того, как бактериальная инфекция разрешилась. Если тест должен быть выполнен, выделения должны быть аккуратно очищены смоченным физиологическим раствором ватным тампоном. Материал наносят тонким слоем на специально обработанное обезжиренное стекло. Для получения адекватного результата мазок должен быть немедленно обработан во избежание высыхания клеток, поскольку их структура может необратимо деформироваться, и трактовка такого материала будет неправильной. Фиксированные препараты окрашивают разными способами, но классической является окраска по методу Папаниколау. При микроскопии препаратов, окрашенных этим методом (Pap-smear test), учитывают специфический комплекс признаков, характеризующих ядро и цитоплазму клеток, а также их расположение (разрозненное, в виде пластов и др.).
Существует несколько методов диагностики инфекции:
Визуальный осмотр шейки матки в сочетании с проведением специфического теста с 3-5% уксусной кислотой и раствором Люголя.
Цитологическое обследование с оценкой результатов по классификации Папаниколау, по которой выделяют 5 классов. Первые два свидетельствуют об отсутствии ВПЧ, изменения, соответствующие третьему классу, требуют проведения повторной диагностики или использование дополнительных методов обследования, четвертый класс характеризуется наличием отдельных клеток с признаками злокачественной трансформации, пятый класс подразумевает присутствие в анализируемом образце большого количества атипических клеток. В таком случае диагноз злокачественной опухоли практически не вызывает сомнений.
Кольпоскопия и биопсия тканей шейки матки и цервикального канала необходимы для уточнения цитологической картины.
Полимеразно-цепная реакция (ПЦР) является наиболее достоверным способом диагностики даже если папилломавирус человека протекает латентно, так как в ходе анализа определяют наличие ДНК вириона. Кровь для этого исследования не берут, так как локализация симптомов инфекции вне генитальной зоны обычно свидетельствует о доброкачественном течении заболевания. Поэтому в качестве материала для проведения ПЦР используют ткань, полученную при урогенитальном соскобе.
Как правило, при положительном результате на папилломавирус проводят дополнительные тесты для определения причины заболевания, так как клинические проявление инфекции обычно свидетельствуют об иммунодефиците
Методы культивирования ВПЧ не разработаны. Лабораторная диагностика папилломавирусной инфекции основана на использовании молекулярно-генетических методов обнаружения фрагментов генома ВПЧ непосредственно в цервикальных соскобах или биоптатах ткани.
Цервикальная ВПЧ-инфекция может диагностироваться с использованием тестов, основанных на идентификации ДНК ВПЧ на цервикальных или вагинальных мазках. Индуцированные ВПЧ изменения эпителия шейки матки могут быть выявлены при микроскопии отторгнувшихся клеток методом, известным как тест Папаниколау (Рар). Тестирование на ДНК ВПЧ, цитология и, особенно в условиях ограниченных ресурсов, визуальный осмотр с применением уксусной кислоты используются для идентификации поражений и скрининга в отношении рака шейки матки.
Информативность цитологического метода определяется качеством взятия и обработки материала для исследования и уровнем подготовки врача-цитолога. Материал для цитологического исследования следует брать с экзоцервикса, с участка на границе многослойного плоского и цилиндрического эпителия цервикального канала и из нижней трети эндоцервикса с помощью щетки-эндобраша до проведения гинекологического осмотра или кольпоскопии при условии отсутствия воспалительных заболеваний. Мазки Папаниколау должны содержать образцы клеток из эктоцервикса, зоны трансформации и эндоцервикального канала. Тест выполняется, когда у пациентки нет менструации, чтобы цитологический образец не был закупорен кровью. Кроме того, если у пациентки имеется цервиковагинальная инфекция со слизисто-гнойными выделениями из влагалища, рассматривается возможность выполнения теста после того, как бактериальная инфекция разрешилась. Если тест должен быть выполнен, выделения должны быть аккуратно очищены смоченным физиологическим раствором ватным тампоном. Материал наносят тонким слоем на специально обработанное обезжиренное стекло. Для получения адекватного результата мазок должен быть немедленно обработан во избежание высыхания клеток, поскольку их структура может необратимо деформироваться, и трактовка такого материала будет неправильной. Фиксированные препараты окрашивают разными способами, но классической является окраска по методу Папаниколау. При микроскопии препаратов, окрашенных этим методом (Pap-smear test), учитывают специфический комплекс признаков, характеризующих ядро и цитоплазму клеток, а также их расположение (разрозненное, в виде пластов и др.).
Самой распространенной классификацией при оценке результатов цитологического исследования является классификация Папаниколау:
1-й класс — атипические клетки отсутствуют, нормальная цитологическая картина;
2-й класс — незначительное изменение клеточных элементов (небольшое увеличение ядра, появление клеток метаплазированного эпителия), обусловленное воспалительным процессом во влагалище и (или) шейке матки;
3-й класс — единичные клетки с изменениями соотношения ядра и цитоплазмы, дискариоз (требуется повторение цитологического исследования или гистологическое исследование биоптата);
4-й класс — отдельные клетки с явными признаками озлокачествления (увеличение ядер, базофильная цитоплазма, неравномерное распределение хроматина);
5-й класс — большое число атипических (раковых) клеток. Диагноз злокачественного новообразования не вызывает сомнений.
ВОЗ и многие международные организации по борьбе с онкологическими заболеваниями рекомендуют использовать молекулярно-генетические исследования — тест на ВПЧ при первичном скрининге у женщин старше 30 лет в сочетании с цитологическим исследованием или в качестве самостоятельного теста в странах, где плохо организованы программы цервикального цитологического скрининга, а также для мониторинга лечения умеренной и тяжелой дисплазии (CIN II и CIN III), карциномы in situ и инвазивного рака. Данный метод весьма полезен и для разрешения сомнительных результатов цитологического исследования, как при первичном выявлении неопластических изменений, так и у пациенток, получающих лечение по поводу дисплазии и рака.
Тест на уксусную кислоту может быть полезен при диагностике остроконечных кондилом. В частности, замачивание уксусной кислоты в подозрительных очагах может повысить степень подозрительности в очагах без классических признаков. Способ включает наложение на предполагаемые поражения полового члена, шейки матки, половых губ или перианальной области марлевого тампона, смоченного 3-5%–ной уксусной кислотой, в течение 5-10 минут. Незаметные, плоские повреждения гениталий, которые трудно оценить, становятся заметными. Диспластические и неопластические ткани белеют (ацетовит). Ложноположительные результаты распространены и могут быть результатом всего, что вызывает паракератоз (например, кандидоз, псориаз, красный плоский лишай, заживление эпителия, сальных желез). Тест на уксусную кислоту можно использовать в сочетании с кольпоскопией для изучения поражений шейки матки. Однако этот тест предназначен только для подозрительных поражений и не должен использоваться для рутинного скрининга.
Существующие методы диагностики в КР
Визуальный осмотр шейки матки.
Кольпоскопия – данный диагностический метод применяется в некоторых государственных клиниках и в частных медицинских центрах.
Цитологический анализ соскоба шейки матки – большинство врачей осуществляют забор соскоба и направляют в лаборатории для проведения цитологического исследования. Цитологический анализ проводится в центре онкологии, в патологоанатомическом бюро и в его филиалах.
Биопсия из патологического участка шейки матки – в клиниках, где проводится кольпоскопия, осуществляется забор материала с помощью конхотома и скальпеля, а также применяется электрохирургические аппараты Сургитрон, Фотек (электропетля).
ПЦР на ВПЧ (ПВЧ скрининг, Квант) – данное исследование осуществляется только в частных медицинских лабораториях.
Существует возможность забора материала медицинскими работниками на уровне ПМСП с последующим анализом в частной мед. лаборатории.
Клинические анализы для выявления онкогенных типов ВПЧ:
1. Скрининг на рак шейки матки с проведением теста Папаниколау;
2. Сортировка результатов аномальной цитологии шейки матки;
3. Последующее наблюдение после лечения по поводу предраковых состояний шейки матки.
Инструментальная диагностика [12-16]
Не применяется.
Иные диагностические исследования [16]
Рекомендована консультация:
врача-акушера-гинеколога с целью диагностики фоновых и диспластических процессов шейки матки, вульвы и влагалища; при ведении беременных, больных аногенитальными бородавками. Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
врача-уролога – при внутриуретральной локализации аногенитальных бородавок. Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
врача–колопроктолога – при наличии обширного процесса в анальной области. Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
врача-хирурга, врача-онколога – при ведении больных гигантской кондиломой Бушке-Левенштайна. Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
врача аллерголога-иммунолога – при наличии иммунодефицитных состояний и рецидивировании заболевания. Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Лечение
Лечение [1, 2, 12-16]
Консервативное лечение
Консервативное лечение
Специфического антивирусного лечения ВПЧ-инфекции нет.
Хирургическое лечение
Ведущим направлением в лечении вирусных бородавок является деструктивная терапия. Данная методика является приоритетной, несмотря на то, что ее эффективность составляет 50-80%, а вероятность развития рецидива после регенерации тканей остается весьма высокой. Высокий риск рецидивирования отмечается при распространенных бородавках (площадью более 2 см2), при подошвенных бородавках, при бородавках с околоногтевой локализацией.
При выборе метода терапии необходимо учитывать локализацию и площадь очагов поражения.
Методы деструкции вирусных бородавок
Физические методы
1. Электрокоагуляция (В) [1-2] Вирусные бородавки методом электрокоагуляции удаляют послойно. Воздействие электротоком проводят под местной инфильтрационной анестезией путем легкого контакта игольчатого наконечника электрода с поверхностью образования. Деструкцию проводят под местной инфильтрационной анестезией 2% раствором лидокаина.
2. Криодеструкция (В) [3-6] Замораживание патологического образования производится с помощью жидкого азота, закиси азота, двуокиси углерода. С целью деструкции используют насадки круглой формы с гладкой контактной поверхностью. Охлажденный криозонд помещают перпендикулярно поверхности кожи и плотно прижимают к ней. Экспозиция составляет 1-5 мин. При деструкции плоских и вульгарных бородавок применяется одноцикловой метод, подошвенных бородавок - метод «олимпийских колец» и двухцикловой метод. Повторное криовоздействие проводят через 7-10 дней.
3. Лазерная деструкция (В) [7-14]. Бородавки удаляют послойно. Воздействие осуществляют контактным способом, сканирующими движениями световода, в непрерывном режиме работы аппарата, с экспозицией от 2-5 секунд до 2-3 минут в зависимости от размера бородавки. Образовавшийся в процессе лазерной абляции струп иссекают ножницами, затем дно раны вторично облучают лазером. После облучения разрушенные ткани удаляют марлевым тампоном, смоченным спиртовым раствором или раствором перекиси водорода. Пациенту рекомендуется обрабатывать раневую поверхность растворами анилиновых красителей (бриллиантового зеленого, фукорцина) 2-4 раза в сутки, избегать травмирования раны и контакта с водой, а также самостоятельного удаления струпа до окончания процесса заживления. Деструкцию проводят под местной инфильтрационной анестезией 2% раствором лидокаина.
4. Радиохирургическая деструкция (С) [15, 16] Метод основан на генерации электромагнитной волны различных частот в диапазоне от 100 кГц до 105 МГц. Радиоволна большой мощности проходит от рабочего электрода через ткань, вызывая незначительный разогрев в месте касания рабочего электрода, при этом происходит разрыв или рассечение ткани без механического усилия или коагуляции. Деструкцию проводят под местной инфильтрационной анестезией 2% раствором лидокаина.
Химические методы
1. 1,5% раствор цинка хлорпропионата в 50% 2-хлорпропионовой кислоте (С) [17-19]. Раствор для наружного применения наносится на бородавки с помощью деревянного шпателя с заостренным наконечником (для новообразований с диаметром от 0,1 до 0,5 см) или с помощью стеклянного капилляра (для новообразований с диаметром свыше 0,5 см). Перед нанесением препарата обрабатываемую поверхность предварительно обезжиривают 70% спиртовым раствором для лучшего проникновения раствора. Нанесение раствора проводят до изменения окраски тканей: плоские бородавки изменяют цвет на серовато-белый спустя 1-3 мин после однократного нанесения, вульгарные бородавки - на серовато-желтый в течение 2-5 мин после 2-3-кратного нанесения препарата. При подошвенных бородавках цвет образований практически не меняется, однако в течение 5-7 мин после 3-5 последовательных аппликаций наблюдается их выраженная инфильтрация. Для получения клинического эффекта при плоских и вульгарных бородавках достаточно 1-2 последовательных обработок кратностью 1 раз в 7-14 дней, при подошвенных бородавках — 1-3 обработок кратностью 1 раз в 14-21 день. Перед каждой обработкой рекомендуется механически удалять мумифицированные ткани. Обработку комбинированным препаратом на основе 2-хлорпропионовой кислоты и хлорпропионата цинка рекомендуется проводить в условиях процедурного кабинета медицинским персоналом. После деструкции бородавок рекомендуется ограничение водных процедур и обработка мумифицирующихся образований неспиртовыми растворами антисептиков (хлоргекседин, мирамистин, перекись водорода).
2. Комбинация азотной, уксусной, щавелевой, молочной кислот и тригидрата нитрата меди (В) [20, 21]. Раствор для наружного применения наносится специальным пластиковым шпателем или с помощью стеклянного капилляра на предварительно обезжиренную спиртовым раствором поверхность очага. Обработку бородавок проводят до появления желтого окрашивания очагов, расположенных на коже, или белого окрашивания очагов, расположенных на слизистых оболочках, не затрагивая здоровых тканей. Появление равномерной желтой или белой окраски свидетельствует о достаточном уровне обработки и является гарантией последующей мумификации образования. Контрольный осмотр больных проводится через 3-5 дней после первичной обработки, в случае необходимости проводят повторную обработку очагов (перерыв между процедурами составляет 1-4 недели). Не рекомендуется обрабатывать поверхность, превышающую 4-5 см2.
Реабилитация [16]
Хирургическое лечение
Ведущим направлением в лечении вирусных бородавок является деструктивная терапия. Данная методика является приоритетной, несмотря на то, что ее эффективность составляет 50-80%, а вероятность развития рецидива после регенерации тканей остается весьма высокой. Высокий риск рецидивирования отмечается при распространенных бородавках (площадью более 2 см2), при подошвенных бородавках, при бородавках с околоногтевой локализацией.
При выборе метода терапии необходимо учитывать локализацию и площадь очагов поражения.
Методы деструкции вирусных бородавок
Физические методы
1. Электрокоагуляция (В) [1-2] Вирусные бородавки методом электрокоагуляции удаляют послойно. Воздействие электротоком проводят под местной инфильтрационной анестезией путем легкого контакта игольчатого наконечника электрода с поверхностью образования. Деструкцию проводят под местной инфильтрационной анестезией 2% раствором лидокаина.
2. Криодеструкция (В) [3-6] Замораживание патологического образования производится с помощью жидкого азота, закиси азота, двуокиси углерода. С целью деструкции используют насадки круглой формы с гладкой контактной поверхностью. Охлажденный криозонд помещают перпендикулярно поверхности кожи и плотно прижимают к ней. Экспозиция составляет 1-5 мин. При деструкции плоских и вульгарных бородавок применяется одноцикловой метод, подошвенных бородавок - метод «олимпийских колец» и двухцикловой метод. Повторное криовоздействие проводят через 7-10 дней.
3. Лазерная деструкция (В) [7-14]. Бородавки удаляют послойно. Воздействие осуществляют контактным способом, сканирующими движениями световода, в непрерывном режиме работы аппарата, с экспозицией от 2-5 секунд до 2-3 минут в зависимости от размера бородавки. Образовавшийся в процессе лазерной абляции струп иссекают ножницами, затем дно раны вторично облучают лазером. После облучения разрушенные ткани удаляют марлевым тампоном, смоченным спиртовым раствором или раствором перекиси водорода. Пациенту рекомендуется обрабатывать раневую поверхность растворами анилиновых красителей (бриллиантового зеленого, фукорцина) 2-4 раза в сутки, избегать травмирования раны и контакта с водой, а также самостоятельного удаления струпа до окончания процесса заживления. Деструкцию проводят под местной инфильтрационной анестезией 2% раствором лидокаина.
4. Радиохирургическая деструкция (С) [15, 16] Метод основан на генерации электромагнитной волны различных частот в диапазоне от 100 кГц до 105 МГц. Радиоволна большой мощности проходит от рабочего электрода через ткань, вызывая незначительный разогрев в месте касания рабочего электрода, при этом происходит разрыв или рассечение ткани без механического усилия или коагуляции. Деструкцию проводят под местной инфильтрационной анестезией 2% раствором лидокаина.
Химические методы
1. 1,5% раствор цинка хлорпропионата в 50% 2-хлорпропионовой кислоте (С) [17-19]. Раствор для наружного применения наносится на бородавки с помощью деревянного шпателя с заостренным наконечником (для новообразований с диаметром от 0,1 до 0,5 см) или с помощью стеклянного капилляра (для новообразований с диаметром свыше 0,5 см). Перед нанесением препарата обрабатываемую поверхность предварительно обезжиривают 70% спиртовым раствором для лучшего проникновения раствора. Нанесение раствора проводят до изменения окраски тканей: плоские бородавки изменяют цвет на серовато-белый спустя 1-3 мин после однократного нанесения, вульгарные бородавки - на серовато-желтый в течение 2-5 мин после 2-3-кратного нанесения препарата. При подошвенных бородавках цвет образований практически не меняется, однако в течение 5-7 мин после 3-5 последовательных аппликаций наблюдается их выраженная инфильтрация. Для получения клинического эффекта при плоских и вульгарных бородавках достаточно 1-2 последовательных обработок кратностью 1 раз в 7-14 дней, при подошвенных бородавках — 1-3 обработок кратностью 1 раз в 14-21 день. Перед каждой обработкой рекомендуется механически удалять мумифицированные ткани. Обработку комбинированным препаратом на основе 2-хлорпропионовой кислоты и хлорпропионата цинка рекомендуется проводить в условиях процедурного кабинета медицинским персоналом. После деструкции бородавок рекомендуется ограничение водных процедур и обработка мумифицирующихся образований неспиртовыми растворами антисептиков (хлоргекседин, мирамистин, перекись водорода).
2. Комбинация азотной, уксусной, щавелевой, молочной кислот и тригидрата нитрата меди (В) [20, 21]. Раствор для наружного применения наносится специальным пластиковым шпателем или с помощью стеклянного капилляра на предварительно обезжиренную спиртовым раствором поверхность очага. Обработку бородавок проводят до появления желтого окрашивания очагов, расположенных на коже, или белого окрашивания очагов, расположенных на слизистых оболочках, не затрагивая здоровых тканей. Появление равномерной желтой или белой окраски свидетельствует о достаточном уровне обработки и является гарантией последующей мумификации образования. Контрольный осмотр больных проводится через 3-5 дней после первичной обработки, в случае необходимости проводят повторную обработку очагов (перерыв между процедурами составляет 1-4 недели). Не рекомендуется обрабатывать поверхность, превышающую 4-5 см2.
Реабилитация [16]
Реабилитация показана после хирургического вмешательства.
1-й этап – ранняя реабилитация, со 4-6 по 7-10 сутки после хирургического вмешательства. В данный период пациент находится на реабилитационном стационарном лечении в течение 3-5 дней, после чего дальнейшая реабилитация происходит в течение 7-14 дней в амбулаторных условиях.
Наиболее важными задачами 1 этапа реабилитации является нормализация работы желудочно-кишечного тракта с формированием нормальной консистенции и частоты стула. Кроме того, на данном этапе осуществляется контроль гемостаза, раневого процесса и купирование послеоперационного болевого синдрома.
Критерием окончания реабилитации является полное заживление послеоперационных ран промежности и анального канала.
На всем протяжении послеоперационного периода пациентам необходимо соблюдать диету с потреблением адекватного количества жидкости и пищевых волокон. и приема препаратов, способствующих регулярной и полноценной дефекации (наиболее часто применяются средства на основе оболочки семян подорожника, лактулозы, макрогола) с исключением необходимости натуживаний для опорожнения прямой кишки, ограничение физических нагрузок, связанных с повышением внутрибрюшного давления и напряжением мышц тазового дна [46, 50, 23].
2-й этап с 15 по 45 сутки после операции, направлен на ускорение репаративных процессов и заживление послеоперационных ран, контроль деятельности желудочно-кишечного тракта.
Критерием окончания реабилитации является полное заживление послеоперационных ран промежности и анального канала.
На всем протяжении послеоперационного периода пациентам необходимо соблюдать диету с потреблением адекватного количества жидкости и пищевых волокон. и приема препаратов, способствующих регулярной и полноценной дефекации (наиболее часто применяются средства на основе оболочки семян подорожника, лактулозы, макрогола) с исключением необходимости натуживаний для опорожнения прямой кишки, ограничение физических нагрузок, связанных с повышением внутрибрюшного давления и напряжением мышц тазового дна [46, 50, 23].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
При отсутствии полной эпителизации, на 45 день после операции, раны можно считать длительно незаживающей. В этих случаях необходимым является проведение: микробиологического посева раневого отделяемого, консультация и наблюдение врачом-физиотерапевтом [46,50].
После выписки из стационара, на период заживления раны пациентам рекомендовано находиться под наблюдением врача-колопроктолога или хирурга поликлиники [46, 50].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
При отсутствии полной эпителизации, на 45 день после операции, раны можно считать длительно незаживающей. В этих случаях необходимым является проведение: микробиологического посева раневого отделяемого, консультация и наблюдение врачом-физиотерапевтом [46,50].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Госпитализация
Организация медицинской помощи [16]
Лечение проводится амбулаторно в условиях медицинского учреждения дерматовенерологического профиля.
При локализации аногенитальных (венерических) бородавок на слизистой оболочке прямой кишки лечение проводится в условиях медицинского учреждения гинекологического/проктологического профиля.
Показания для госпитализации в медицинскую организацию: обширные поражения кожи и слизистых оболочек с целью хирургического иссечения и последующего гистологического исследования.
Профилактика
Профилактика [1, 2, 17-20]
Первичная профилактика РШМ предполагает проведение мероприятий в отношении лиц, не имеющих признаков заболевания, с целью предотвращения его развития в дальнейшем. Классическим примером первичной профилактики любого заболевания является вакцинация.
Вторичная профилактика развития РШМ предполагает раннее выявление и лечение лиц, имеющих фоновые и предраковые заболевания шейки матки, с целью предупредить в последующем развитие инвазивного рака.
Третичная профилактика этого заболевания представляет собой комплексное или комбинированное лечение, включающее оперативное вмешательство в сочетании с лучевой и химиотерапией.
Иммунизация четырёхвалентной вакциной против ВПЧ включена в национальный календарь профилактических прививок (Приказ МЗ КР №1131 от 23.12.2019г. «Об утверждении Национального календаря профилактических прививок и сертификата профилактических прививок КР»).
Вакцина против ВПЧ была признана эффективной в профилактике онкогенных генотипов ВПЧ. В настоящее время существует три ВПЧ-вакцины, направленные на типы ВПЧ высокого риска, которые имеются на рынке во многих странах мира для профилактики заболеваний, обусловленных ВПЧ: четырехвалентная вакцина была впервые лицензирована в 2006 году, бивалентная вакцина – в 2007 году и девятивалентная вакцина – в 2014 году. Все эти вакцины желательно применять, если возможно, до начала сексуальной активности, т.е. до того, когда реципиенты могут подвергнуться воздействию ВПЧ. Все три вакцины получены с использованием рекомбинантной ДНК-технологии из очищенного L1 структурного белка, который самостоятельно формирует типоспецифические пустые оболочки ВПЧ, называемые вирусоподобными частицами (VLP). Ни одна из вакцин не содержит живого биологического продукта или вирусной ДНК и поэтому не является контагиозной; вакцины не содержат ни антибиотиков, ни консервантов.
На 31 марта 2017 года 71 страна (37%) включила ВПЧ-вакцину в свои национальные программы иммунизации для девочек, а 11 стран (6%) также и для мальчиков.
Четырехвалентная вакцина
Эта вакцина представляет собой суспензию для внутримышечного введения и содержит очищенный L1 белок типов ВПЧ 6, 11, 16 и 18. Она существует в однодозовой расфасовке или в виде готового к использованию шприца с вакциной. Вакцина производится с использованием дрожжевого субстрата и включает в качестве адъюванта аморфный гидроксифосфат алюминия (AAHS). Каждая доза (0.5 мл) этой вакцины содержит 20 мкг белка L1 ВПЧ-6, 40 мкг белка L1 ВПЧ-11, 40 мкг белка L1 ВПЧ-16 и 20 мкг белка L1 ВПЧ-18, адсорбированных на 225 мкг адъюванта. Эта вакцина предназначена для использования среди женщин и мужчин в возрасте 9 лет и старше для предотвращения предраковых поражений и рака шейки матки, влагалища и ануса, вызываемых типами ВПЧ высокого риска, а также аногенитальных бородавок, появление которых связано со специфическими типами ВПЧ.
Календари прививок ВПЧ-вакциной, рекомендуемые производителями, зависят от возраста реципиента. Вакцины должны вводиться внутримышечно в область дельтовидной мышцы.
Четырехвалентная ВПЧ-вакцина. Для девочек и мальчиков в возрасте 9-13 лет эта вакцина может вводиться в соответствии с двухдозовым календарем (0.5 мл в 0 и 6 месяцев). Если вторая доза вакцины вводится ранее чем через 6 месяцев после первой дозы, необходимо введение третьей дозы. С другой стороны, вакцина может вводиться в соответствии с трехдозовым календарем (0.5 мл в 0, 2, 6 месяцев). Вторая доза должна вводиться, по крайней мере, через 1 месяц после первой дозы, а третья доза должна вводиться, по крайней мере, через 3 месяца после второй дозы. В возрасте 14 лет девочкам и мальчикам вакцина должна вводиться в соответствии с трехдозовым календарем (0.5 мл в 0, 2, 6 месяцев). Вторая доза должна вводиться, по крайней мере, через месяц после первой дозы, а третья – не ранее, чем через 3 месяца после второй дозы. В отношении бустерной дозы позиция не определена.
Вакцинопрофилактика
В КР вакцинация против ВПЧ в масштабе всей страны внедрена начиная 2022 года в рамках Программы «Иммунопрофилактика» на 2019-2023гг в соответствии с текущим комплексном многолетним планом по иммунизации на 2019-2023 годы.
Иммунизация четырёхвалентной вакциной против ВПЧ включена в национальный календарь профилактических прививок (Приказ МЗ КР №1131 от 23.12.2019г. «Об утверждении Национального календаря профилактических прививок и сертификата профилактических прививок КР»).
Вакцина против ВПЧ была признана эффективной в профилактике онкогенных генотипов ВПЧ. В настоящее время существует три ВПЧ-вакцины, направленные на типы ВПЧ высокого риска, которые имеются на рынке во многих странах мира для профилактики заболеваний, обусловленных ВПЧ: четырехвалентная вакцина была впервые лицензирована в 2006 году, бивалентная вакцина – в 2007 году и девятивалентная вакцина – в 2014 году. Все эти вакцины желательно применять, если возможно, до начала сексуальной активности, т.е. до того, когда реципиенты могут подвергнуться воздействию ВПЧ. Все три вакцины получены с использованием рекомбинантной ДНК-технологии из очищенного L1 структурного белка, который самостоятельно формирует типоспецифические пустые оболочки ВПЧ, называемые вирусоподобными частицами (VLP). Ни одна из вакцин не содержит живого биологического продукта или вирусной ДНК и поэтому не является контагиозной; вакцины не содержат ни антибиотиков, ни консервантов.
На 31 марта 2017 года 71 страна (37%) включила ВПЧ-вакцину в свои национальные программы иммунизации для девочек, а 11 стран (6%) также и для мальчиков.
Четырехвалентная вакцина
Эта вакцина представляет собой суспензию для внутримышечного введения и содержит очищенный L1 белок типов ВПЧ 6, 11, 16 и 18. Она существует в однодозовой расфасовке или в виде готового к использованию шприца с вакциной. Вакцина производится с использованием дрожжевого субстрата и включает в качестве адъюванта аморфный гидроксифосфат алюминия (AAHS). Каждая доза (0.5 мл) этой вакцины содержит 20 мкг белка L1 ВПЧ-6, 40 мкг белка L1 ВПЧ-11, 40 мкг белка L1 ВПЧ-16 и 20 мкг белка L1 ВПЧ-18, адсорбированных на 225 мкг адъюванта. Эта вакцина предназначена для использования среди женщин и мужчин в возрасте 9 лет и старше для предотвращения предраковых поражений и рака шейки матки, влагалища и ануса, вызываемых типами ВПЧ высокого риска, а также аногенитальных бородавок, появление которых связано со специфическими типами ВПЧ.
Календари прививок ВПЧ-вакциной, рекомендуемые производителями, зависят от возраста реципиента. Вакцины должны вводиться внутримышечно в область дельтовидной мышцы.
Четырехвалентная ВПЧ-вакцина. Для девочек и мальчиков в возрасте 9-13 лет эта вакцина может вводиться в соответствии с двухдозовым календарем (0.5 мл в 0 и 6 месяцев). Если вторая доза вакцины вводится ранее чем через 6 месяцев после первой дозы, необходимо введение третьей дозы. С другой стороны, вакцина может вводиться в соответствии с трехдозовым календарем (0.5 мл в 0, 2, 6 месяцев). Вторая доза должна вводиться, по крайней мере, через 1 месяц после первой дозы, а третья доза должна вводиться, по крайней мере, через 3 месяца после второй дозы. В возрасте 14 лет девочкам и мальчикам вакцина должна вводиться в соответствии с трехдозовым календарем (0.5 мл в 0, 2, 6 месяцев). Вторая доза должна вводиться, по крайней мере, через месяц после первой дозы, а третья – не ранее, чем через 3 месяца после второй дозы. В отношении бустерной дозы позиция не определена.
Иммуногенность. Предполагается, что механизм защиты, вызываемой ВПЧ-вакцинами, основанный на данных исследований на экспериментальных моделях животных, связан с нейтрализацией антител против основного белка вирусной оболочки L1. ВПЧ вакцины также индуцируют B-клетки памяти, которые участвуют в созревании гуморального иммунного ответа и синтезе высокоаффинных антител.
Вакцинные антитела достигают очага инфекции путем активной транссудации в женские половые пути [2, 3].
В клинических испытаниях, проведенных среди здоровых мужчин и женщин в возрасте 9 – 45 лет, у 95-99% вакцинированных развивались нейтрализующие антитела к каждому типу ВПЧ вакцины после рекомендованных серий [2, 3]. Серологический ответ на вакцину достигает пикового уровня через 4 недели после последней дозы вакцины в первичной серии, а затем сокращается и стабилизируется на постоянном уровне через 18 месяцев. В 3-дозовой серии пик гуморальной иммунной реакции вначале выше у девочек 9 – 14 лет, чем у молодых взрослых или более старших женщин. После 3-дозовой серии иммунизации титры антител оставались высокими в течение более 10 лет при использовании бивалентной и четырехвалентной вакцин и более 5 лет после введения 9-валентной вакцины. У мужчин и женщин титры антител, достигнутые в ответ на вакцинацию, значительно выше (в 1-4 раза), чем ответ на естественную инфекцию. Причины этого явления неясны, но могут быть связаны с лучшей активизацией/нацеленностью клеток лимфатических узлов введенных внутримышечно вакцинами, чем инфекцией слизистой оболочки и, возможно, с использованием адъювантов в существующих вакцинах. Долговечные плазмоциты отвечают за длительное существование ВПЧ-специфических антител.
Хранение ВПЧ-вакцин: ВПЧ-вакцины должны храниться при температуре 2-8оС и не подвергаться замораживанию. ВПЧ-вакцины должны использоваться как можно раньше после того, как они извлечены из холодильника. Изучение термостабильности в отношении четырехвалентной вакцины показала, что вакцина сохраняет свою активность в течение 3-х дней при ее хранении при температуре от 8 до 42оС.
ВПЧ-вакцины были лицензированы на основании продемонстрированной их клинической действенности среди молодых взрослых женщин, а в отношении четырехвалентной и девятивалентной вакцин – также и среди взрослых мужчин.
Таким образом, рекомендация по иммунизации женщин против ПВИ имеет на сегодняшний день уровень доказательности 1А; рекомендация вакцинации мужчин против ПВИ обладает уровнем доказательности 1В.
Вакцинация групп риска
Вакцинация пациентов с нарушениями иммунной системы
У лиц с нарушенной реактивностью иммунной системы вследствие иммунодепрессантной терапии (системные кортикостероиды, цитотоксичные препараты, антиметаболиты, алкилирующие препараты), генетического дефекта или других причин защитный эффект может быть снижен.
Вакцинация ВИЧ-инфицированных лиц
Озабоченность относительно безопасности или сниженной эффективности вакцинации у ВИЧ-инфицированных женщин не должна быть причиной отсрочки начала вакцинации против ПВИ. Тестирование на ВИЧ не должно быть условием проведения плановой вакцинации против ВПЧ.
Вакцинация пациентов с хроническими заболеваниями
Хронические заболевания вне обострения не должны служить противопоказанием к вакцинации пациентов.
Возможность одновременной вакцинации с другими вакцинами
Четырехвалентную вакцину против ПВИ можно вводить в один день (в другой рекомендованный участок тела) с рекомбинантной вакциной против гепатита В, с менингококковой конъюгированной вакциной, с инактивированной вакциной против полиомиелита и бесклеточной вакциной против дифтерии, столбняка, коклюша.
Двухвалентная вакцина против ВПЧ может применяться одновременно с такими вакцинами, как инактивированная вакцина против полиомиелита, вакцина против гепатита А, рекомбинантная вакцина против гепатита В, с условием введения в разные участки тела и разными шприцами.
В отчете ВОЗ, посвященном вакцинам против ПВИ, указывается на возможность одновременного их введения с любыми живыми и инактивированными вакцинами с условием введения разными шприцами в разные участки тела [17].
Поствакцинальные реакции
Нежелательные реакции, которые наблюдались в связи с введением четырехвалентной вакцины были легкой степени тяжести. Встречались покраснение, боль и припухлость - очень часто; боль в конечностях, пирексия, зуд, гематома - часто; бронхоспазм - очень редко.
За период пострегистрационного применения накопились данные о развитии таких явлений, как флегмона, бронхоспазм и крапивница, лимфаденопатия, идиопатическая тромбоцитопеническая пурпура, головная боль, тошнота, рвота, артралгия, миалгия, астения, усталость, озноб, дискомфорт, головокружение, острый первичный идиопатический полирадикулоневрит, головная боль, синдром Гийена-Барре, острый рассеянный энцефаломиелит, обморок (иногда сопровождаемый тонико-клоническими судорогами); реакции гиперчувствительности, включая анафилактические/анафилактоидные, бронхоспазм и крапивница. Однако, достоверно оценить частоту перечисленных нежелательных явлений и связь с прививкой не представляется возможным.
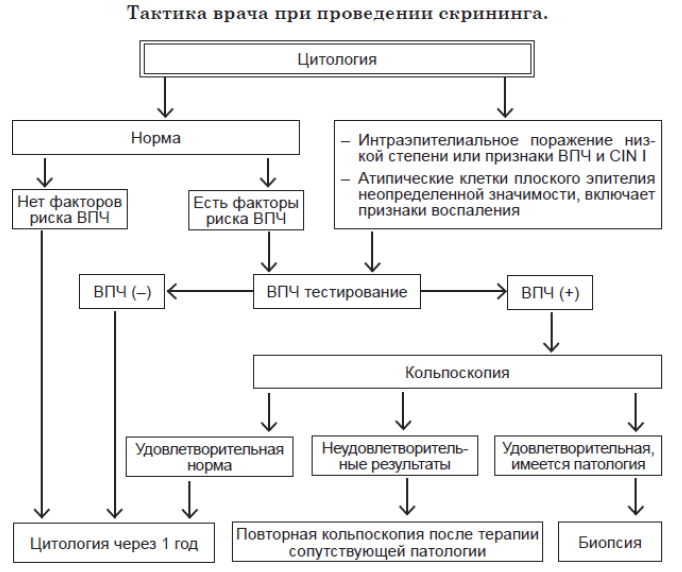
Скрининг [15]
В случае, если факт наличия ВПЧ был установлен, для минимизации прогрессирования вируса следует: определить подтипы ВПЧ для исключения их онкогенности; проводить регулярные (каждые 2 года) тестирования на онкоцитологию; провести онкотестирование; выполнить ДНК ВПЧ мониторинг в случае необходимости.
В клинических испытаниях, проведенных среди здоровых мужчин и женщин в возрасте 9 – 45 лет, у 95-99% вакцинированных развивались нейтрализующие антитела к каждому типу ВПЧ вакцины после рекомендованных серий [2, 3]. Серологический ответ на вакцину достигает пикового уровня через 4 недели после последней дозы вакцины в первичной серии, а затем сокращается и стабилизируется на постоянном уровне через 18 месяцев. В 3-дозовой серии пик гуморальной иммунной реакции вначале выше у девочек 9 – 14 лет, чем у молодых взрослых или более старших женщин. После 3-дозовой серии иммунизации титры антител оставались высокими в течение более 10 лет при использовании бивалентной и четырехвалентной вакцин и более 5 лет после введения 9-валентной вакцины. У мужчин и женщин титры антител, достигнутые в ответ на вакцинацию, значительно выше (в 1-4 раза), чем ответ на естественную инфекцию. Причины этого явления неясны, но могут быть связаны с лучшей активизацией/нацеленностью клеток лимфатических узлов введенных внутримышечно вакцинами, чем инфекцией слизистой оболочки и, возможно, с использованием адъювантов в существующих вакцинах. Долговечные плазмоциты отвечают за длительное существование ВПЧ-специфических антител.
Хранение ВПЧ-вакцин: ВПЧ-вакцины должны храниться при температуре 2-8оС и не подвергаться замораживанию. ВПЧ-вакцины должны использоваться как можно раньше после того, как они извлечены из холодильника. Изучение термостабильности в отношении четырехвалентной вакцины показала, что вакцина сохраняет свою активность в течение 3-х дней при ее хранении при температуре от 8 до 42оС.
ВПЧ-вакцины были лицензированы на основании продемонстрированной их клинической действенности среди молодых взрослых женщин, а в отношении четырехвалентной и девятивалентной вакцин – также и среди взрослых мужчин.
Таким образом, рекомендация по иммунизации женщин против ПВИ имеет на сегодняшний день уровень доказательности 1А; рекомендация вакцинации мужчин против ПВИ обладает уровнем доказательности 1В.
Вакцинация групп риска
Вакцинация пациентов с нарушениями иммунной системы
У лиц с нарушенной реактивностью иммунной системы вследствие иммунодепрессантной терапии (системные кортикостероиды, цитотоксичные препараты, антиметаболиты, алкилирующие препараты), генетического дефекта или других причин защитный эффект может быть снижен.
Вакцинация ВИЧ-инфицированных лиц
Озабоченность относительно безопасности или сниженной эффективности вакцинации у ВИЧ-инфицированных женщин не должна быть причиной отсрочки начала вакцинации против ПВИ. Тестирование на ВИЧ не должно быть условием проведения плановой вакцинации против ВПЧ.
Вакцинация пациентов с хроническими заболеваниями
Хронические заболевания вне обострения не должны служить противопоказанием к вакцинации пациентов.
Возможность одновременной вакцинации с другими вакцинами
Четырехвалентную вакцину против ПВИ можно вводить в один день (в другой рекомендованный участок тела) с рекомбинантной вакциной против гепатита В, с менингококковой конъюгированной вакциной, с инактивированной вакциной против полиомиелита и бесклеточной вакциной против дифтерии, столбняка, коклюша.
Двухвалентная вакцина против ВПЧ может применяться одновременно с такими вакцинами, как инактивированная вакцина против полиомиелита, вакцина против гепатита А, рекомбинантная вакцина против гепатита В, с условием введения в разные участки тела и разными шприцами.
В отчете ВОЗ, посвященном вакцинам против ПВИ, указывается на возможность одновременного их введения с любыми живыми и инактивированными вакцинами с условием введения разными шприцами в разные участки тела [17].
Поствакцинальные реакции
Нежелательные реакции, которые наблюдались в связи с введением четырехвалентной вакцины были легкой степени тяжести. Встречались покраснение, боль и припухлость - очень часто; боль в конечностях, пирексия, зуд, гематома - часто; бронхоспазм - очень редко.
За период пострегистрационного применения накопились данные о развитии таких явлений, как флегмона, бронхоспазм и крапивница, лимфаденопатия, идиопатическая тромбоцитопеническая пурпура, головная боль, тошнота, рвота, артралгия, миалгия, астения, усталость, озноб, дискомфорт, головокружение, острый первичный идиопатический полирадикулоневрит, головная боль, синдром Гийена-Барре, острый рассеянный энцефаломиелит, обморок (иногда сопровождаемый тонико-клоническими судорогами); реакции гиперчувствительности, включая анафилактические/анафилактоидные, бронхоспазм и крапивница. Однако, достоверно оценить частоту перечисленных нежелательных явлений и связь с прививкой не представляется возможным.
В поствакцинальный период после введения двухвалентной вакцины отмечались: головная боль, миалгия, артралгия, зуд, сыпь, крапивница, астения, лихорадка > 38°С, тошнота, рвота, диарея, боли в области живота - часто; лимфаденопатия, головокружение, уплотнение в месте введения вакцины - нечасто; синкопе, вегетососудистые реакции, иногда сопровождаемые тонико-клоническими движениями, аллергические реакции, включая отек Квинке и анафилаксию - редко.
Никакой связи вакцинации против ВПЧ с влиянием на фертильность, развитием аутоиммунных заболеваний или смерти не установлено.
Следует напоминать женщинам о том, что вакцинация не отменяет необходимость проведения регулярных гинекологических осмотров для проведения вторичной профилактики, поскольку вакцина не защищает от всех заболеваний, вызванных разными типами ВПЧ.
Никакой связи вакцинации против ВПЧ с влиянием на фертильность, развитием аутоиммунных заболеваний или смерти не установлено.
Следует напоминать женщинам о том, что вакцинация не отменяет необходимость проведения регулярных гинекологических осмотров для проведения вторичной профилактики, поскольку вакцина не защищает от всех заболеваний, вызванных разными типами ВПЧ.
Скрининг [15]
В случае, если факт наличия ВПЧ был установлен, для минимизации прогрессирования вируса следует: определить подтипы ВПЧ для исключения их онкогенности; проводить регулярные (каждые 2 года) тестирования на онкоцитологию; провести онкотестирование; выполнить ДНК ВПЧ мониторинг в случае необходимости.

Информация
Источники и литература
-
Клинические протоколы Министерства здравоохранения Кыргызской Республики
- 1. Вакцинопрофилактика заболеваний, вызванных вирусом папилломы человека. Федеральные клинические рекомендации. Москва, Педиатр, 2016. – 41 с. 2. ВОЗ. Папилломавирусная инфекция человека. Стандарты эпиднадзора за управляемыми инфекциями последнее обновление 5 сентября 2018. 3. WHO. Human papillomavirus vaccines: WHO position paper, May 2017. Wkly Epidemiol Rec. 2017; 92(19):241–68. 4. Раrkin DM, Вrау F. Chapter 2: Тhе burdеn of НРV-rеlаtеd саnсеrs. Vассinе. 2006;24(Suppl 3) :S3/ 1 1 -25. 5. Parkin DM. Тhе global health Burdеn of infection associated саnсеrs in the уеаr 2002. Int J Сапсеr. 2006; 1 1В( 12):30З0-4а. 6. Garland SM, Steben М, Sings HL et al. Natural history of genital warts: analysis of the placebo аrm of 2 randomized phase III trials of а quadrivalent human papillomavirus (types 6, 11, 16, and 18) vaccine. J Infесt Dis. 2009;199(6):В05-14. 7. Lacey CJ, Lowndes СМ, Shah КV. Сhарtеr 4: Burden and management of non-саnсеrоus HPV-related conditions: НРV-6/ 1 1 disease. Vассinе. 2006;24( Suppl 3): S3/35-a 1. 8. Bosch FХ, Lorincz А, Mufroz N, Meijer CJ, Shаh КV. Тhе causal геlаtiоn between human papillomavirus and сеrviсаl саnсеr. J Clin Pathol. 2002;55(4):244 265. 9. Meyer T, Arndt R, Christophers E, et al. Association of rare human papillomavirus types with genital premalignant and malignant lesions. J Infec Dis. 1998;178:252-255. 10. Walboomers JL et al. Human papillomavirus is a necessary cause of invasive cervical cancer worldwide. J. Pathol, 1999;189:12–19. 11. Ключарева С.В., Сыдиков А.А., Чупров И.Н., Касаткин Е.В., Гивировский С.Е., Эсавулова Л.Т., Бафталовская О.А., Ахалая М.Р. Папилломавирусная инфекция: современные представления о патогенезе и лечении. //Клиническая дерматология и венерология, 1, 2018, С. 94-103. https://doi.org/10.17116/klinderma201817194-103 12. Федеральные клинические рекомендации по ведению больных вирусными бородавками. Российское общество дерматовенерологов и косметологов. 2015. 13 с. 13. Рахматулина М. Р., Большенко Н. В. Особенности клинического течения папилломавирусной инфекции в зависимости от генотипа и количественных показателей вирусов папилломы человека высокого онкогенного риска. Вестник дерматологии и венерологии, 2014; №3: С.95-105. 14. Хрянин А.А., Тапильская Н.И., Кнорринг Г.Ю. Современные представления о папилломавирусной инфекции: эпидемиология и тактика ведения пациентов с аногенитальными бородавками. //Клиническая дерматология и венерология. 2020, Т. 19, № 5, с. 719-728. https://doi.org/10.17116/klinderma202019051719 15. Папилломавирусная инфекция урогенитального тракта женщин (эпидемиология, клинико-патогенетические особенности, методы диагностики, лечение, профилактика): информационно-методическое пособие / Е.В. Фоляк, Т.М. Соколова, К.Ю. Макаров, А.В. Якимова, В.Р. Мухамедшина, А.В. Усова. – Новосибирск : Вектор-Бест, 2010. – 88 с. 16. Аногенитальные (венерические) бородавки. / Клинические рекомендации. Российская ассоциация колопроктологов Общероссийская общественная организация «Российское общество дерматовенерологов и косметологов», 2021, 38 с. 17. WHO. The Immunological Basis for Immunization Series Module 19: Human papillomavirus infection. Printed in May 2011; 18. HPV vaccine background document. Available at http://www.who.int/immunization/sage/meetings/2016/october/1_HPV_vaccine_background_document_27Sept2016.pdf?ua=1 , accessed February 2017. 19. Рахматулина М. Р., Кицак В. Я., Большенко Н. В. Современные методы профилактики развития онкологических заболеваний шейки матки у больных папилломавирусной инфекцией. Вестник дерматологии и венерологии, 2013; №6: С.40- 49. 20. Профилактика рака шейки матки. Руководство для врачей. Под ред. ГТ Сухих и ВН Прилепской. 3-е изд. М.: МЕDпресс-информ,2012. 192 с. Дополнительная литература 1. WHO. Annex 4. Recommendations to assure the quality, safety and efficacy of recombinant human papillomavirus virus-like particle vaccines. In: WHO Expert Committee on Biological Standardization. Sixty-sixth report. WHO Technical Report Series, No. 999. Geneva: WHO; 2016; 2. WHO. Monitoring the coverage and impact of human papillomavirus vaccine – report of WHO meeting, November 2009. Wkly Epidemiol Rec. 2010; 85(25): 237–43. 3. WHO. Human papillomavirus laboratory manual, first edition. Geneva: WHO; 2010. 4. WHO. HPV vaccine introduction clearinghouse. In: Immunization, vaccines and biologicals [website]. Geneva:2018.
Информация
Ключевые слова:
вируса папилломы человека, папилломавирусная инфекция человека, аногенитальные остроконечные кондиломы, венерические бородавки, рак шейки матки, эпидемиология, этиология, патогенез, вакциноуправляемая инфекция, заболеваемость, смертность, вакцинация, вакцинопрофилактика, диагностика, лечение, терапия, реабилитация, профилактика.
Список использованных сокращений
ВОЗ Всемирная организация здравоохранения
ВПЧ вирус папилломы человека
КГМА Кыргызская государственная медицинская академия
КР Кыргызская Республика
МЗ КР Министерство здравоохранения Кыргызской Республики
МКБ –10 Международная классификация болезней 10-го пересмотра
ПВИ папилломавирусная инфекция
ПЦР полимеразно-цепная реакция
РЦИ Республиканский центр иммунопрофилактики
УОМПиЛП Управление организации медицинской помощи и лекарственной политики
ЦРЗиМТ Центр развития здравоохранения и медицинских технологий
CIN цервикальная интраэпителиальная неоплазия
Pap-smear test
тест Папаниколау
Состав рабочей группы
Адреса для переписки с рабочей группой:
Методы, использованные для формулирования рекомендаций: консенсус экспертов.
Рейтинговая схема для оценки силы рекомендаций
Алгоритм ведения пациента
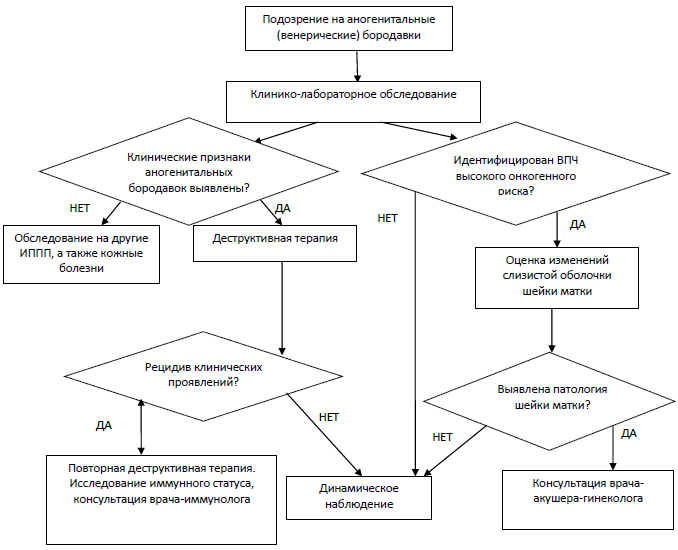
Приложение В
Информация для пациента
Приложение А1
Состав рабочей группы
- Шукурова В.К. - к.м.н., заведующая кафедрой детских болезней КГМИПиПК им. С.Б. Даниярова, руководитель группы;
- Ишенапысова Г.С.- директор РЦИ МЗ КР;
- Джолбунова З.К. – д.м.н, заведующая кафедрой детских инфекционных болезней КГМА им. И.К. Ахунбаева;
- Кадырова Р.М. - д.м.н., профессор, кафедра детских инфекционных болезней КГМА им.И.К. Ахунбаева;
- Чечетова С.В. – к.м.н, доцент кафедры детских инфекционных болезней КГМА им. И.К. Ахунбаева;
- Ырысова М.Б. - к.м.н., доцент кафедры общей и клинической эпидемиологии КГМА им. И.К. Ахунбаева;
- Искакова Д.Т. - заместитель директора по ОЗМиД ОЦСМ Первомайского района г. Бишкек;
- Жумагулова Г.Ж. - заместитель директора РЦИ МЗ КР;
- Малышева М.А. - врач эпидемиолог РЦИ МЗ КР.
Адреса для переписки с рабочей группой:
720040, Кыргызская Республика, Бишкек, ул. Фрунзе, 535
Республиканский центр иммунопрофилактики
тел: (996-312) 32 30 11
Данное клиническое руководство рассмотрено и рекомендовано: на заседании.
Мониторинг внедрения клинического руководства (анализ использования, сбор информации по недостаткам и замечаниям), внесение дополнений и изменений осуществляет ЦРЗ и МТ. Обновление версии руководства осуществляется по мере необходимости, по мере появления новых ключевых доказательств по диагностике и лечению столбняка, но не реже 1 раза в 5 лет.
Методология разработки клинических рекомендаций
Цель разработки данного клинического руководства
Целевые группы: врачи скорой неотложной помощи, врачи общей практики, терапевты, инфекционисты, невропатологи, анестезиологи, реаниматологи, хирурги, травматологи, организаторы здравоохранения.
Методологическая экспертная поддержка
Методы, использованные для сбора/селекции доказательств
Конфликт интересов
Перед началом работы по созданию данного клинического протокола все члены рабочей группы дали согласие сообщить в письменной форме о наличии финансовых взаимоотношений с фармацевтическими компаниями. Никто из членов авторского коллектива не имел коммерческой заинтересованности или другого конфликта интересов с фармацевтическими компаниями или другими организациями.
Данное клиническое руководство рассмотрено и рекомендовано: на заседании.
Все поправки, к представленным рекомендациям, будут опубликованы в соответствующих журналах. Любые комментарии и пожелания по содержанию руководства приветствуются.
Мониторинг внедрения клинического руководства (анализ использования, сбор информации по недостаткам и замечаниям), внесение дополнений и изменений осуществляет ЦРЗ и МТ. Обновление версии руководства осуществляется по мере необходимости, по мере появления новых ключевых доказательств по диагностике и лечению столбняка, но не реже 1 раза в 5 лет.
Приложение А2
Методология разработки клинических рекомендаций
Цель разработки данного клинического руководства
Представить обновленные и объективно обоснованные рекомендации по профилактике, диагностике и лечению паротитной инфекции.
При этом в документ включены рекомендации Всемирной организации здравоохранения (ВОЗ) стандарты эпиднадзора за вакциноуправляемыми инфекциями (2017).
Целевые группы: врачи скорой неотложной помощи, врачи общей практики, терапевты, инфекционисты, невропатологи, анестезиологи, реаниматологи, хирурги, травматологи, организаторы здравоохранения.
Методологическая экспертная поддержка
- Джакубекова А.У. – главный специалист УОМП и ЛП МЗ КР, к.м.н., доцент;
- Матоморова А.А. – зав. отделом доказательной медицины и медицинских технологий ЦРЗ и МТ при МЗ КР
Методы, использованные для сбора/селекции доказательств
Поиск в электронных базах данных. Описание методов, использованных для сбора/селекции доказательств. Доказательной базой для публикации являются публикации, вошедшие в Кокрановскую библиотеку, базы данных EMBASE и MEDLINE. Глубина поиска составляла 5 лет.
Шкала уровней доказательности и градации рекомендаций SIGN (Scottish Intercollegiate Guidelines Network)
Методы, использованные для оценки качества и силы доказательств
Шкала уровней доказательности и градации рекомендаций SIGN (Scottish Intercollegiate Guidelines Network)
| 1++ |
Высококачественные мета-анализы, систематические обзоры РКИ
или РКИ с очень низким риском ошибки
|
| 1+ |
Хорошо выполненные мета-анализы, систематические обзоры РКИ
или РКИ с очень низким риском ошибки
|
| 1 |
Мета-анализы, систематические обзоры РКИ или РКИ с высоким
риском ошибки
|
| 2++ | Высококачественные систематические обзоры исследований типа случай-контроль или когортных исследований, либо высококачественные исследования типа случай-контроль, либо когортные исследования с очень низким риском ошибки, предвзятости и с высокой вероятностью выявления связи с причиной |
| 2+ | Правильно проведенные исследования типа случай-контроль или когортные исследования с низким риском ошибки, предвзятости и с умеренной вероятностью выявления связи с причиной |
| 2 |
Исследования типа случай-контроль или когортные исследования с высоким риском ошибки, предвзятости и со значительным риском отсутствия связи с причиной
|
| 3 | Неаналитические исследования, например, сообщение о случае, серии случаев |
| 4 | Мнения экспертов |
Критерии оценки диагностических, лечебных, профилактических, реабилитационных медицинских технологий
При включении в клиническое руководство медицинских технологий разработчики в соответствующих разделах протокола должны учитывать показатели, характеризующие:
для методов диагностики:
чувствительность метода — частоту положительных результатов диагностики при наличии заболевания;
- специфичность метода — частоту отрицательных результатов диагностики при отсутствии заболевания;
- прогностическую ценность метода — вероятность наличия заболевания при положительном результате и вероятность отсутствия при отрицательном результате диагностики;
- отношение правдоподобия
- отношение вероятности события при наличии некоего условия к вероятности события без этого условия (например, отношение частоты симптома при наличии болезни к частоте симптома в отсутствие болезни):
для методов профилактики, лечения и реабилитации:
- действенность метода — частоту доказанных положительных результатов профилактики, лечения и реабилитации в искусственно созданных экспериментальных условиях;
- эффективность метода — частоту доказанных положительных результатов профилактики, лечения и реабилитации в условиях клинической практики.
Методы, использованные для формулирования рекомендаций: консенсус экспертов.
Рейтинговая схема для оценки силы рекомендаций
|
Сила
|
Описание |
| А | По меньшей мере, один мета-анализ, систематический обзор, или РКИ, оцененные, как 1++ , напрямую применимые к целевой популяции и демонстрирующие устойчивость результатов или группа доказательств, включающая результаты исследований, оцененные, как 1+, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов |
| В | группа доказательств, включающая результаты исследовании, оцененные, как 2++, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов или экстраполированные доказательства из исследований, оцененных, как 1++ или 1+ |
| С | группа доказательств, включающая результаты исследований оцененные, как 2+, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов; или экстраполированные доказательства из исследований, оцененных, как 2++ |
| D | Доказательства уровня 3 или 4; или экстраполированные доказательства, из исследований, оцененных, как 2+ |
Приложение Б
Алгоритм ведения пациента

Приложение В
Информация для пациента
1. В период лечения необходимо воздержаться от половых контактов или использовать барьерные методы контрацепции до установления излеченности.
2. Рекомендуется обследование и лечение половых партнеров.
3. С целью установления излеченности необходима повторная явка к врачу через 7 дней после проведения деструкции.
4. Рекомендуется обследование на другие инфекции, передаваемые половым путем.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.