Оказание медицинской помощи пациентам с ВИЧ-инфекцией
 Версия: Клинические протоколы 2022 (Беларусь)
Версия: Клинические протоколы 2022 (Беларусь)
Бессимптомный инфекционный статус, вызванный вирусом иммунодефицита человека [ВИЧ] (Z21), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде других состояний (B23), Болезнь, вызванная вирусом иммунодефицита человека [вич] (B20-B24), Болезнь, вызванная вирусом иммунодефицита человека [вич], неуточненная (B24), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде других уточненных болезней (B22), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде злокачественных новообразований (B21), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде инфекционных и паразитарных болезней (B20), В личном анамнезе другие уточненные факторы риска, не классифицированные в других рубриках (Z91.8), Другое уточненное специальное обследование (Z01.8), Другой уточненный вид медицинской помощи (Z51.8), Использование наркотиков (Z72.2), Консультирование по вопросам, связанным с вирусом иммунодефицита человека [ВИЧ] (Z71.7), Контакт с больным и возможность заражения вирусом иммунодефицита человека [ВИЧ] (Z20.6), Обследование и наблюдение после другого несчастного случая (Z04.3), Обследование и наблюдение после несчастного случая на производстве (Z04.2), Последующее обследование после другого вида лечения по поводу других состояний (Z09.8), Сексуальное поведение с высокой степенью риска (Z72.5), Специальное скрининговое обследование с целью выявления инфицирования вирусом иммунодефицита человека [ВИЧ] (Z11.4)
Инфекционные болезни у детей, Инфекционные и паразитарные болезни
Общая информация
Краткое описание
ПОСТАНОВЛЕНИЕ
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ
РЕСПУБЛИКИ БЕЛАРУСЬ
25 июля 2022 г. № 73
Об утверждении клинического протокола
На основании абзаца девятого части первой статьи 1 Закона Республики Беларусь от 18 июня 1993 г. № 2435-XII «О здравоохранении», подпункта 8.3 пункта 8, подпункта 9.1 пункта 9 Положения о Министерстве здравоохранения Республики Беларусь, утвержденного постановлением Совета Министров Республики Беларусь от 28 октября 2011 г. № 1446, Министерство здравоохранения Республики Беларусь
ПОСТАНОВЛЯЕТ:
1. Утвердить клинический протокол «Оказание медицинской помощи пациентам с ВИЧ-инфекцией» (прилагается).
2. Признать утратившим силу постановление Министерства здравоохранения Республики Беларусь от 1 июня 2017 г. № 41 «Об утверждении клинического протокола «Диагностика и лечение пациентов с ВИЧ-инфекцией».
3. Настоящее постановление вступает в силу после его официального опубликования.
Министр Д.Л.Пиневич
СОГЛАСОВАНО
Брестский областной исполнительный комитет
Витебский областной исполнительный комитет
Гомельский областной исполнительный комитет
Гродненский областной исполнительный комитет
Могилевский областной исполнительный комитет
Минский областной исполнительный комитет
Минский городской исполнительный комитет
Министерство внутренних дел Республики Беларусь
Управление делами Президента Республики Беларусь
Государственный пограничный комитет Республики Беларусь
Министерство обороны Республики Беларусь
УТВЕРЖДЕНО
Постановление
Министерства здравоохранения
Республики Беларусь
25.07.2022 № 73
КЛИНИЧЕСКИЙ ПРОТОКОЛ «Оказание медицинской помощи пациентам с ВИЧ-инфекцией»
ГЛАВА 1
ОБЩИЕ ПОЛОЖЕНИЯ
1. Настоящий клинический протокол устанавливает общие требования к объему оказания медицинской помощи пациентам с инфекцией, вызванной вирусом
иммунодефицита человека (далее – ВИЧ) (шифр по Международной статистической классификации болезней и проблем, связанных со здоровьем, десятого
пересмотра (далее – МКБ-10) – B20–B24 Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ]; Z01.8 Другое уточненное специальное обследование; Z04.2 Обследование и наблюдение после несчастного случая на производстве; Z04.3 Обследование и наблюдение после другого несчастного случая; Z09.8 Последующее обследование после другого вида лечения по поводу других состояний; Z11.4 Специальное скрининговое обследование с целью выявления инфицирования вирусом иммунодефицита человека [ВИЧ]; Z20.6 Контакт с больным и возможность заражения вирусом иммунодефицита человека [ВИЧ]; Z21 Бессимптомный инфекционный статус, вызванный вирусом иммунодефицита человека [ВИЧ]; Z51.8 Другой уточненный вид медицинской помощи; Z71.7 Консультирование по вопросам, связанным с вирусом иммунодефицита человека [ВИЧ]; Z72.2 Использование наркотиков; Z72.5 Сексуальное поведение с высокой степенью риска; Z91.8 В личном анамнезе другие уточненные факторы риска, не классифицированные в других рубриках).
2. Требования настоящего клинического протокола являются обязательными для юридических лиц и индивидуальных предпринимателей, осуществляющих медицинскую деятельность в порядке, установленном законодательством о здравоохранении.
3. Для целей настоящего клинического протокола используются термины и их определения в значениях, установленных Законом Республики Беларусь «О здравоохранении», Законом Республики Беларусь от 19 ноября 1993 г. № 2570-XII «О правах ребенка», а также следующие термины и их определения:
антиретровирусная терапия (далее – АРТ) – лечение с использованием антиретровирусных лекарственных средств (далее – АРВ-ЛС) не менее чем двух различных классов, позволяющее подавить репликацию ВИЧ;
АРВ-ЛС – лекарственное средство (далее – ЛС), подавляющее репликацию ВИЧ. Выделяются следующие основные классы АРВ-ЛС: нуклеозидные ингибиторы обратной транскриптазы (далее – НИОТ), ненуклеозидные ингибиторы обратной транскриптазы (далее – ННИОТ), ингибиторы протеазы (далее – ИП) с фармакологическим усилителем (бустером) (далее – ИП/б) и ингибиторы интегразы (далее – ИИ);
вирусная супрессия – подавление репликации ВИЧ в результате АРТ, при котором концентрация рибонуклеиновой кислоты (далее – РНК) ВИЧ в плазме крови (вирусная нагрузка (далее – ВН)) становится ниже уровня 50 копий ВИЧ в 1 мл исследуемого образца плазмы; у подавляющего большинства пациентов вирусная супрессия достигается в течение 6 месяцев эффективной АРТ;
вирусологическая неудача лечения – невозможность достичь и поддерживать вирусную супрессию, определяется как постоянно определяемая ВН ВИЧ более 200 копий/мл в двух последовательных исследованиях с интервалом 3 месяца и более у пациента, получающего текущую схему АРТ не менее 6 месяцев;
ВИЧ-положительный статус пациента – статус пациента, определяемый фактом получения положительных результатов лабораторных тестов в ходе диагностического тестирования на ВИЧ-инфекцию;
ВИЧ-сервисные негосударственные некоммерческие организации (далее – ВИЧ-сервисные НКО) – негосударственные некоммерческие организации, предоставляющие услуги по профилактике, уходу и поддержке в связи с ВИЧ-инфекцией;
диагностика ВИЧ-инфекции – комплекс медицинских услуг, направленных на установление диагноза ВИЧ-инфекция, включающих в том числе скрининговое и диагностическое тестирование на ВИЧ-инфекцию;
диагностическое тестирование на ВИЧ-инфекцию – применение лабораторных методов исследования биологических образцов с определением РНК ВИЧ, антител, антигена или антигенов к ВИЧ, антител к антигенам ВИЧ;
ключевые группы населения – группы населения с наибольшим риском инфицирования ВИЧ: люди, употребляющие инъекционные наркотики; мужчины, практикующие секс с мужчинами; трансгендерные люди; секс работники; лица, находящиеся в местах лишения свободы;
люди, живущие с ВИЧ (далее, если не указано иное, – ЛЖВ) – пациенты, у которых были получены положительные результаты диагностического тестирования на ВИЧ-инфекцию;
неопределяемая ВН – подавление репликации ВИЧ в результате АРТ, при котором концентрация РНК ВИЧ в плазме крови становится ниже порога чувствительности используемой тест–системы (который должен быть не выше 50 копий ВИЧ в 1 мл);
оппортунистические заболевания – оппортунистические инфекции (далее – ОИ), новообразования и обусловленные воздействием ВИЧ нарушения функций отдельных органов, возникающие в результате дефицита активности T-лимфоцитов хелперов (CD4+ лимфоцитов) и (или) прямого цитопатического действия ВИЧ;
отрыв от лечения – прекращение АРТ на срок более одного месяца, в том числе по инициативе ЛЖВ;
первичная ВИЧ-инфекция – состояние, характеризующееся наличием риска инфицирования ВИЧ в последние 6 недель, детекцией p24 антигена или РНК ВИЧ в крови и (или) сероконверсией – динамикой антител к ВИЧ от отрицательных к положительным, включая изменения реактивности иммунного блоттинга (далее – ИБ); первичная ВИЧ- инфекция может проявляться острым ретровирусным синдромом или протекать малосимптомно;
постэкспозиционная (постконтактная) профилактика ВИЧ-инфекции (далее – ПЭП) – метод медицинской профилактики с использованием короткого курса АРТ после контакта, способного привести к заражению ВИЧ;
предэкспозиционная (доконтактная) профилактика ВИЧ-инфекции (далее – ПрЭП) – метод медицинской профилактики заражения ВИЧ с использованием АРВ-ЛС у лиц с высоким риском инфицирования ВИЧ;
приверженность АРТ – поведение пациента, проявляющееся строгим соблюдением рекомендаций врача-специалиста по приему АРВ-ЛС. Приблизительно оценивается на основании отношения количества принятых доз к назначенным за определенный промежуток времени, выражается в процентах. Приверженность АРТ выше 90 % считают высокой;
продвинутая ВИЧ-инфекция – состояние, характеризующееся снижением CD4+ лимфоцитов менее 200 кл/мкл до начала АРТ или на АРТ при определяемой ВН, или развитием любого из состояний и заболеваний, характерных для 3 и 4 стадий ВИЧ-инфекции; при этом все дети в возрасте 2–5 лет, живущие с ВИЧ, относятся к категории пациентов с продвинутой ВИЧ-инфекцией, если не получают эффективную АРТ, и все дети младше 2 лет, вне зависимости от лечения и лабораторных показателей, относятся к категории пациентов с продвинутой ВИЧ-инфекцией;
скрининговое тестирование на ВИЧ-инфекцию – первичный этап обследования на ВИЧ-инфекцию, включающий определение антител к ВИЧ или антител, антигена или антигенов ВИЧ с применением экспресс-тестов или серологических методов исследования; при получении реактивного результата скринингового тестирования на ВИЧ-инфекцию проводится диагностическое тестирование на ВИЧ-инфекцию;
терапевтическая ремиссия – состояние пациента, отвечающее следующим критериям: стабильная вирусная супрессия (подтвержденная двумя измерениями ВН ВИЧ с интервалом 6 месяцев и более); восстановление иммунитета, достаточное для защиты от появления новых и прогрессирования имевшихся оппортунистических заболеваний;
тест на резистентность ВИЧ – молекулярно-генетическое исследование на наличие мутаций в геноме ВИЧ-1, определяющих устойчивость к АРВ-ЛС;
трансгендерные люди – лица, заявившие о необходимости изменения половой принадлежности или прошедшие коррекцию (гормональную и (или) хирургическую) половой принадлежности: с мужской при рождении на женскую (далее – трансгендерные женщины) или с женской при рождении на мужскую (далее – трансгендерные мужчины).
4. Диагностика ВИЧ-инфекции осуществляется по алгоритму согласно приложению 1.
Обязательному направлению на скрининговое тестирование на ВИЧ-инфекцию по эпидемическим и клиническим показаниям подлежат контингенты населения при наличии клинических показаний, указанных в пункте 9 приложения 1, а также контингенты населения, указанные в пункте 5 приложения 2 к постановлению
Министерства здравоохранения Республики Беларусь от 12 июля 2012 г. № 97 «Об установлении клинических показаний и категорий лиц, подлежащих обязательному медицинскому освидетельствованию».
Каждое обследование на выявление ВИЧ-инфекции сопровождается дотестовым и послетестовым консультированием с оказанием психологической помощи.
Перед проведением скринингового и диагностического тестирования на ВИЧ-инфекцию заполняется направление на исследование крови на вирусные инфекции и сифилис по форме, установленной Министерством здравоохранения. В случае анонимного скринингового тестирования на ВИЧ-инфекцию вместо персональных данных в направлении указывается код, который сообщается пациенту. Проведение анонимного диагностического тестирования на ВИЧ-инфекцию не допускается.
5. В случае подтверждения ВИЧ-положительного статуса по результатам диагностического тестирования на ВИЧ-инфекцию проводится послетестовое консультирование пациента и эпидемиологическое расследование случая ВИЧ-инфекции врачом-эпидемиологом государственного учреждения «Республиканский центр гигиены, эпидемиологии и общественного здоровья», государственного учреждения «Республиканский центр гигиены и эпидемиологии Департамента финансов и тыла Министерства внутренних дел Республики Беларусь», областного центра гигиены, эпидемиологии и общественного здоровья, государственного учреждения «Минский городской центр гигиены и эпидемиологии», городского, районного, зонального центра гигиены и эпидемиологии.
6. Диагноз ВИЧ-инфекции устанавливает врач-инфекционист на основании эпидемиологических, клинических и лабораторных данных.
В диагнозе указываются:
стадия заболевания, а также заболевание и (или) состояние, характеризующее стадию, которые устанавливаются в соответствии с классификацией ВИЧ-инфекции у пациентов в возрасте 15 лет и старше и классификацией ВИЧ-инфекции у детей в возрасте до 15 лет согласно приложениям 2 и 3 соответственно, а также в соответствии с классификацией ВИЧ-ассоциированного иммунодефицита согласно приложению 4;
количество CD4+ лимфоцитов и ВН ВИЧ с датой их последнего определения;
терапевтическая ремиссия или вирусологическая неудача лечения, а также указание на отрыв от лечения (при наличии этих состояний).
количество CD4+ лимфоцитов и ВН ВИЧ с датой их последнего определения;
терапевтическая ремиссия или вирусологическая неудача лечения, а также указание на отрыв от лечения (при наличии этих состояний).
Примерами диагноза ВИЧ-инфекции являются:
ВИЧ-инфекция, 1 клиническая стадия (CD4 678 кл/мкл, ВН ВИЧ <300 копий/мл 03.04.2022 г.), терапевтическая ремиссия;
ВИЧ-инфекция, 2 клиническая стадия, умеренное снижение массы тела (CD4 237 кл/мкл, ВН ВИЧ 10 000 копий/мл 31.03.2022 г.), отрыв от лечения;
ВИЧ-инфекция, 3 клиническая стадия, тромбоцитопения, (CD4 178 кл/мкл, ВН ВИЧ 2589 копий/мл 28.03.2022 г.), вирусологическая неудача лечения;
ВИЧ-инфекция, 4 клиническая стадия, криптококковый менингит, синдром восстановления иммунной системы (CD4 8 кл/мкл (1,2 %), ВН ВИЧ 258 000 копий/мл 01.03.2022 г.);
ВИЧ-инфекция, 4 клиническая стадия (пневмоцистная пневмония, 2014 г.), (CD4 388 кл/мкл, ВН ВИЧ <50 копий/мл 03.03.2022 г.), терапевтическая ремиссия.
Для целей статистического учета используется шифр диагноза по МКБ-10 (В.20–В.24).
7. Пациенты с ВИЧ-положительным статусом, относящиеся к ключевым группам населения, при наличии возможности направляются в ближайший кабинет профилактики ВИЧ-инфекции среди потребителей инъекционных наркотиков или анонимно-консультативные пункты на базе ВИЧ-сервисных НКО для получения консультационной, информационной, психологической, юридической помощи, выполнения мероприятий по поддержанию высокой приверженности медицинскому наблюдению и лечению, перенаправления и (или) сопровождения в специализированные организации для решения медицинских и социально-бытовых проблем, ухудшающих качество жизни и негативно влияющих на состояние здоровья.
8. Оказание медицинской помощи лицам, инфицированным ВИЧ, осуществляется в соответствии с Инструкцией о порядке организации оказания медицинской помощи лицам, инфицированным вирусом иммунодефицита человека, утвержденной постановлением Министерства здравоохранения Республики Беларусь от 8 ноября 2017 г. № 93.
Алгоритм клинического и лабораторного мониторинга состояния здоровья пациентов с ВИЧ-инфекцией приведен в приложении 5.
9. АРТ и другое противомикробное лечение назначается пациентам с ВИЧ-инфекцией с учетом индивидуальных особенностей, тяжести заболевания, наличия сопутствующей патологии, аллергологического анамнеза, клинико-фармакологических характеристик ЛС и потенциальных лекарственных взаимодействий.
10. АРВ-ЛС с целью медицинской профилактики используются для профилактики передачи ВИЧ-инфекции от матери ребенку и по эпидемическим показаниям лицам, имеющим высокий риск заражения ВИЧ-инфекцией (используется ПрЭП) либо подвергшимся риску заражения ВИЧ-инфекцией (используется ПЭП). Проведение медицинской профилактики передачи ВИЧ-инфекции от матери ребенку осуществляется в соответствии с клиническим протоколом «Профилактика передачи ВИЧ-инфекции от матери ребенку», утвержденным постановлением Министерства здравоохранения Республики Беларусь от 28 июня 2018 г. № 59.
Диагностика
ГЛАВА 2
ДИАГНОСТИКА ВИЧ-ИНФЕКЦИИ
11. Скрининговое тестирование на ВИЧ-инфекцию с применением экспресс-тестов проводится медицинскими работниками в организациях здравоохранения, работниками ВИЧ-сервисных НКО, а также путем самотестирования населения экспресс-тестами на ВИЧ-инфекцию.
Скрининговое тестирование на ВИЧ-инфекцию с применением лабораторных методов (далее – лабораторное скрининговое тестирование на ВИЧ-инфекцию) проводится медицинскими работниками в организациях здравоохранения и основано на выявлении антител к ВИЧ 1, 2 или антител, антигена и (или) антигенов ВИЧ 1, 2 методом иммуноферментного анализа (далее – ИФА) или иммунохемилюминесцентного анализа (далее – ИХА), в том числе с использованием экспресс-тестов по крови.
12. Для скринингового тестирования на ВИЧ-инфекцию применяются экспресс-тесты на ВИЧ-инфекцию, медицинское применение которых разрешено на территории Республики Беларусь. Тестирование с применением экспресс-тестов проводится в соответствии с инструкцией по медицинскому применению (листком-вкладышем).
13. При получении нереактивного (отрицательного) результата скринингового тестирования на ВИЧ-инфекцию и при отсутствии данных о первичной ВИЧ-инфекции результат скринингового тестирования на ВИЧ-инфекцию регистрируется как отрицательный, дальнейшие исследования не проводятся.
Подозрение на первичную ВИЧ-инфекцию при нереактивном (отрицательном) результате скринингового тестирования возникает при наличии эпидемиологических данных в виде контакта с высоким риском заражения в течение менее чем 6 недель назад и (или) при наличии клинических проявлений острого ретровирусного синдрома.
При получении реактивного (положительного) результата лабораторного скринингового тестирования на ВИЧ-инфекцию фамилия, собственное имя, отчество (если таковое имеется), дата рождения пациента (исключение составляют анонимные пробы) проверяются по базе данных Республиканского регистра пациентов с ВИЧ-инфекцией (далее – Регистр). При наличии информации о пациенте в Регистре в результат исследования вносится пометка «состоит на статистическом учете», дальнейшее диагностическое тестирование на ВИЧ-инфекцию не назначается и не проводится.
Положительные результаты лабораторного скринингового тестирования на ВИЧ-инфекцию в течение 24 часов направляются в организацию здравоохранения, направившую биологический образец на исследование, сведения о положительном результате передаются в государственное учреждение «Республиканский центр гигиены и эпидемиологии Департамента финансов и тыла Министерства внутренних дел Республики Беларусь», государственное учреждение «Минский городской центр гигиены и эпидемиологии», городские, районные, или зональные центры гигиены и эпидемиологии по месту жительства (месту пребывания) пациента.
14. В случае получения реактивного (положительного) результата скринингового тестирования на ВИЧ-инфекцию, медицинский работник, инициировавший тестирование, назначает пациенту диагностическое тестирование на ВИЧ-инфекцию (работник ВИЧ-сервисной НКО – предлагает клиенту ВИЧ-сервисной НКО пройти диагностическое тестирование).
15. Диагностическое тестирование на ВИЧ-инфекцию проводится медицинскими работниками в лабораториях государственных организаций здравоохранения с применением лабораторных методов исследования образцов крови. Доставка образцов для проведения лабораторных исследований осуществляется не позднее 48 часов с момента забора. Забор биологического образца крови осуществляется в пробирки с этилендиаминтетрауксусной кислотой (далее – ЭДТА).
Диагностическое тестирование на ВИЧ-инфекцию назначается врачом-инфекционистом, иным врачом-специалистом по результатам скринингового тестирования на ВИЧ-инфекцию или при наличии клинических показаний (вероятная первичная ВИЧ-инфекция с или без проявлений острого ретровирусного синдрома, наличие клинических проявлений, схожих с 3 или 4 клинической стадией ВИЧ-инфекции). Забранная проба крови направляется в лабораторию на повторное тестирование.
Забор крови для диагностического тестирования на ВИЧ-инфекцию может быть проведен медицинским работником на базе ВИЧ-сервисных НКО с последующей доставкой в лабораторию государственной организации здравоохранения.
16. Диагностическое тестирование на ВИЧ-инфекцию проводится в два этапа.
На первом этапе проводится тестирование биологического материала на выявление антител к ВИЧ 1, 2 или антител, антигена и (или) антигенов ВИЧ 1, 2 методом ИФА или ИХА, в том числе с использованием двух экспресс-тестов по крови с разным набором антигенных, антительных детерминант и высокой чувствительностью (по меньшей мере, 99 %) и специфичностью (по меньшей мере, 99 %).
В случае получения нереактивного (отрицательного) результата на первом этапе диагностического тестирования на ВИЧ-инфекцию (отрицательный ИФА или ИХА или два отрицательных экспресс-теста) результат регистрируется как отрицательный, дальнейшее исследование не проводится. В течение 24 часов результат исследования направляется в организацию здравоохранения, направившую биологический образец на исследование, и в государственное учреждение «Республиканский центр гигиены и эпидемиологии Департамента финансов и тыла Министерства внутренних дел Республики Беларусь», областные центры гигиены, эпидемиологии и общественного здоровья, государственное учреждение «Минский городской центр гигиены и эпидемиологии», городские, районные или зональные центры гигиены и эпидемиологии по месту жительства (месту пребывания) пациента.
В случае получения реактивного (положительного) результата на первом этапе диагностического тестирования на ВИЧ-инфекцию (положительный ИФА или ИХА или положительный один из двух или оба выполненных экспресс-тестов) фамилия, собственное имя, отчество (если таковое имеется), дата рождения пациента проверяются по базе данных Регистра:
при наличии информации о пациенте в Регистре дальнейшее диагностическое тестирование на ВИЧ-инфекцию не проводится, в результат исследования вносится пометка «состоит на статистическом учете», в течение 24 часов результат исследования направляется в организацию здравоохранения, направившую биологический образец на исследование, и в государственное учреждение «Республиканский центр гигиены и эпидемиологии Департамента финансов и тыла Министерства внутренних дел Республики Беларусь», областные центры гигиены, эпидемиологии и общественного здоровья, государственное учреждение «Минский городской центр гигиены и эпидемиологии», городские, районные или зональные центры гигиены и эпидемиологии по месту жительства (месту пребывания) пациента;
при отсутствии информации о пациенте в Регистре, образец биологического материала, из которого получен положительный результат на первом этапе, направляется на второй этап диагностического тестирования на ВИЧ-инфекцию.
На втором этапе проводится тестирование биологического материала на выявление РНК ВИЧ.
Реактивным (положительным) результатом исследования на выявление РНК ВИЧ считается результат, превышающий порог чувствительности используемой тест-системы. В случае реактивного (положительного) результата лабораторных исследований на втором этапе диагностического тестирования на ВИЧ-инфекцию фиксируется ВИЧ-положительный статус пациента, в течение 24 часов результат направляется в организацию здравоохранения, направившую биологический образец на исследование, и в государственное учреждение «Республиканский центр гигиены и эпидемиологии Департамента финансов и тыла Министерства внутренних дел Республики Беларусь», областные центры гигиены, эпидемиологии и общественного здоровья, государственное учреждение «Минский городской центр гигиены и эпидемиологии», городские, районные или зональные центры гигиены и эпидемиологии по месту жительства (месту пребывания) пациента.
В случае нереактивного (отрицательного) результата на выявление РНК ВИЧ (ниже порога чувствительности используемой тест-системы) на втором этапе диагностического тестирования на ВИЧ-инфекцию, проводится повторный забор биологического образца крови в пробирки с ЭДТА и повторное лабораторное исследование с использованием метода ИБ для определения наличия антител к антигенам ВИЧ 1, 2 (при наличии возможности исследование методом ИБ проводится с использованием той же пробы).
В случае получения реактивного (положительного) результата ИБ фиксируется ВИЧ-положительный статус пациента, в течение 24 часов результат направляется в организацию здравоохранения, направившую биологический образец на исследование, и в государственное учреждение «Республиканский центр гигиены и эпидемиологии Департамента финансов и тыла Министерства внутренних дел Республики Беларусь», областные центры гигиены, эпидемиологии и общественного здоровья, государственное учреждение «Минский городской центр гигиены и эпидемиологии», городские, районные или зональные центры гигиены и эпидемиологии по месту жительства (месту пребывания) пациента.
В случае получения нереактивного (отрицательного) результата исследования, проведенного методом ИБ, статус пациента регистрируется как отрицательный, в течение 24 часов результат направляется в организацию здравоохранения, направившую биологический образец на исследование, и в государственное учреждение «Республиканский центр гигиены и эпидемиологии Департамента финансов и тыла Министерства внутренних дел Республики Беларусь», областные центры гигиены, эпидемиологии и общественного здоровья, государственное учреждение «Минский городской центр гигиены и эпидемиологии», городские, районные или зональные центры гигиены и эпидемиологии по месту жительства (месту пребывания) пациента.
17. Пациенты с неопределенными результатами диагностического тестирования на ВИЧ-инфекцию, проводимого с использованием метода ИБ, направляются на повторное диагностическое тестирование на ВИЧ-инфекцию через 3 месяца с целью окончательного определения ВИЧ-статуса. Если через 3 месяца после первого тестирования результаты ИБ являются неопределенными, у пациента не выявляются факторы риска заражения и клинические симптомы ВИЧ-инфекции, результат тестирования расценивается как ложноположительный. Если через 3 месяца после первого тестирования результаты ИБ являются неопределенными, у пациента выявляются факторы риска заражения и (или) клинические симптомы ВИЧ-инфекции, решение о ВИЧ-статусе пациента принимается врачебным консилиумом.
18. При получении реактивных (положительных) результатов лабораторных исследований на всех этапах диагностического тестирования на ВИЧ-инфекцию информация о результатах обследования пациента вносится в Регистр.
19. Алгоритм диагностики ВИЧ-инфекции имеет особенности в следующих группах:
ВИЧ-экспонированные дети в возрасте до 18 месяцев;
беременные;
пациенты с вероятной первичной ВИЧ-инфекцией с или без проявлений острого ретровирусного синдрома.
Диагностика ВИЧ-инфекции у ВИЧ-экспонированных детей в возрасте до 18 месяцев проводится с учетом следующих особенностей:
выявление и подтверждение ВИЧ-инфекции у экспонированных детей в возрасте до 18 месяцев проводится с помощью качественных генетических молекулярных тестов полимеразная цепная реакция – дезоксирибонуклеиновая кислота–ВИЧ (далее – ПЦР-ДНК-ВИЧ);
выявление и подтверждение ВИЧ-инфекции у экспонированных детей в возрасте до 18 месяцев проводится с помощью качественных генетических молекулярных тестов полимеразная цепная реакция – дезоксирибонуклеиновая кислота–ВИЧ (далее – ПЦР-ДНК-ВИЧ);
для экспонированных детей первый качественный генетический молекулярный тест ПЦР-ДНК-ВИЧ выполняется в возрасте 2–5 дней. В случае получения реактивного (положительного) результата забирается второй образец крови для подтверждения, тестирование проводится с помощью качественных генетических молекулярных тестов ПЦР-ДНК-ВИЧ. Если повторное тестирование дает положительный результат, подтверждается ВИЧ-положительный статус ребенка. В случае нереактивного (отрицательного) результата повторное тестирование проводится в возрасте 8–10 недель и 4 месяца. В случае получения реактивного (положительного) результата теста при проведении тестирования в возрасте 8–10 недель и (или) 4 месяца, забирается второй образец крови для подтверждения, тестирование проводится с помощью качественных генетических молекулярных тестов ПЦР-ДНК-ВИЧ. Если и повторное тестирование дает положительный результат, тогда подтверждается ВИЧ-положительный статус ребенка. По достижении экспонированным ребенком возраста 18 месяцев лабораторные исследования проводятся по алгоритму диагностики ВИЧ-инфекции согласно приложению 1;
при наличии медицинских и эпидемиологических показаний у детей в возрасте до 18 месяцев, являющихся неэкспонированными, их обследование проводится согласно алгоритму диагностики ВИЧ-инфекции согласно приложению 1.
при наличии медицинских и эпидемиологических показаний у детей в возрасте до 18 месяцев, являющихся неэкспонированными, их обследование проводится согласно алгоритму диагностики ВИЧ-инфекции согласно приложению 1.
Диагностика ВИЧ-инфекции у беременных женщин проводится с учетом следующих особенностей:
при постановке на учет по беременности до 20 недель беременные женщины в обязательном порядке направляются на лабораторное скрининговое тестирование на ВИЧ-инфекцию на выявление антител, антигена и (или) антигенов ВИЧ 1, 2 методом ИФА или ИХА. Повторное лабораторное скрининговое тестирование на ВИЧ-инфекцию беременных женщин с отрицательным результатом при первом тестировании проводится в случаях, определяемых Министерством здравоохранения;
в случаях постановки на учет по беременности в сроке свыше 20 недель, а также беременной с неизвестным ВИЧ-статусом при родовспоможении проводится
дополнительное скрининговое тестирование на ВИЧ-инфекцию с применением экспресс-тестов до получения результатов тестирования на выявление антител, антигена и (или) антигенов ВИЧ 1, 2 методом ИФА или ИХА.
Подозрение на вероятную первичную ВИЧ-инфекцию может возникать при наличии эпидемиологических данных (контакт с высоким риском заражения в течение менее чем 6 недель назад) или клинических проявлений острого ретровирусного синдрома. В этом случае при отрицательном или сомнительном результате выявления антител к ВИЧ при скрининговом тестировании на ВИЧ-инфекцию выполняется также тест на выявление РНК ВИЧ или антител, антигена и (или) антигенов ВИЧ 1, 2 методом ИФА или ИХА.
Лечение
ГЛАВА 3
АРТ
20. АРТ показана ЛЖВ с момента установления диагноза ВИЧ-инфекции.
21. АРТ осуществляется с применением схем, сочетающих несколько АРВ-ЛС.
Основные характеристики и режимы дозирования АРВ-ЛС, режимы дозирования жидких пероральных форм АРВ-ЛС у детей в возрасте младше 4 недель, упрощенные режимы дозирования твердых пероральных форм АРВ-ЛС для приема один раз в день у детей в возрасте 4 недель и старше, упрощенные режимы дозирования твердых и жидких пероральных форм АРВ-ЛС для приема два раза в день у детей в возрасте 4 недель и старше устанавливаются согласно приложениям 6–9 соответственно.
Схема АРТ состоит из сочетания основания схемы, представленного двумя НИОТ, и третьего ЛС одного из трех классов: ННИОТ, ИП или ИИ. Нестандартные схемы АРТ назначаются пациентам с вирусологическими неудачами лечения по результатам теста на резистентность ВИЧ, а также пациентам с вирусной супрессией и невозможностью использовать определенные ЛС в схеме (индивидуальная непереносимость, взаимодействия с другими ЛС).
22. Схемы АРТ первого и второго рядов назначаются согласно приложениям 10 и 11 соответственно врачом-специалистом, прошедшим обучение по назначению АРТ.
Схемы АРТ третьего ряда назначаются согласно приложению 12. АРТ третьего ряда, нестандартные схемы АРТ назначаются врачебным консилиумом с привлечением заведующих консультативно-диспансерных отделений по ВИЧ-инфекции организаций здравоохранения областного уровня и (или) специалистов профильных кафедр учреждений образования, осуществляющих подготовку, повышение квалификации и (или) переподготовку специалистов с высшим медицинским, фармацевтическим образованием.
23. При начале АРТ учитываются следующие факторы:
оптимальным является немедленное (в день первого обращения после установления ВИЧ-положительного статуса) или быстрое (в течение 7 дней после первого обращения) начало АРТ, что способствует повышению эффективности лечения у большинства пациентов;
пациентам без признаков продвинутой ВИЧ-инфекции АРТ начинается в кратчайшие сроки после оценки результатов лабораторных исследований, необходимых
для безопасного назначения выбранных АРВ-ЛС, при необходимости схема АРТ может быть модифицирована после получения некоторых результатов обследования;
пациентам с продвинутой ВИЧ-инфекцией АРТ начинается после исключения туберкулезного менингита, токсоплазмоза головного мозга и криптококкового менингита;
при наличии перечисленных ОИ АРВ-ЛС назначаются после начала этиотропного лечения этих ОИ;
пациентам с первичной ВИЧ-инфекцией с проявлениями менингита (менингоэнцефалита) АРТ начинается по экстренным медицинским показаниям при
получении положительного результата скринингового этапа обследования до получения результата диагностического этапа; в схему АРТ при этом включается ЛС класса ИИ;
девушки и женщины детородного возраста, а также беременные при назначении им долутегравира (далее – DTG) информируются о пользе и потенциальных рисках, связанных с приемом DTG;
беременным АРТ начинается в кратчайшие сроки с учетом пользы и потенциальных рисков для плода, связанных с приемом отдельных АРВ-ЛС.
24. Перед началом АРТ с пациентом или одним из родителей, усыновителей (удочерителей) несовершеннолетнего, опекунов, попечителей проводится беседа с целью информирования о предстоящем лечении и оценки готовности его начать. У пациентов, готовых начать АРТ и не имеющих медицинских противопоказаний к немедленному или быстрому началу, лечение начинается сразу, оптимально в течение первых 7 дней после установления ВИЧ-положительного статуса. Приоритетными для первоочередного медицинского обследования, назначения АРТ и обеспечения приверженности являются пациенты с продвинутой ВИЧ-инфекцией, беременные и женщины с детьми младше трех лет.
При начале АРТ пациент получает от медицинского работника необходимую информацию о режиме приема ЛС, возможных нежелательных реакциях на них и последующем медицинском наблюдении. В случае отказа пациента от начала АРТ при каждом последующем визите для медицинского наблюдения или госпитализации пациенту рекомендуется начать прием АРТ.
25. АРТ начинается со схемы первого ряда. Правильный выбор схемы первого ряда и обеспечение высокой приверженности АРТ у ЛЖВ являются залогом долговременной эффективной АРТ с наименьшими неблагоприятными воздействиями. При выборе схемы АРТ предпочтение отдается назначению комбинированных ЛС в фиксированных дозировках с однократным приемом в течение суток, что улучшает приверженность АРТ. Для немедленного или быстрого начала АРТ назначаются предпочтительные схемы первого ряда.
26. Медицинские работники, оказывающие помощь ЛЖВ, помогают пациенту поддерживать высокую приверженность АРТ. При каждом обращении для врачебной консультации (медицинского осмотра) или получения АРВ-ЛС производится анализ приверженности АРТ, выявляются и фиксируются в медицинских документах факторы, определяющие недостаточную приверженность АРТ. При наличии зависимости от алкоголя или других психоактивных веществ, признаков депрессии, когнитивных проблем пациент направляется к профильному врачу-специалисту, в том числе с возможностью получения анонимного лечения. В случае необходимости пациент направляется в кабинет профилактики ВИЧ-инфекции среди потребителей инъекционных наркотиков или анонимно-консультативные пункты на базе ВИЧ-сервисных НКО.
27. Модификация схемы АРТ в пределах ряда осуществляется при непереносимости определенного АРВ-ЛС или наличии медицинских противопоказаний к его применению, в том числе неблагоприятных лекарственных взаимодействий с одним или несколькими другими жизненно важными ЛС. Схема АРТ модифицируется при развитии тяжелых или длительно сохраняющихся умеренных нежелательных реакций на любой из ее компонентов. Легкие или умеренные нежелательные реакции на ЛС могут быть преодолены или со временем проходят самостоятельно.
28. Модификация удовлетворительно переносимой схемы АРТ с целью оптимизации производится для повышения ее эффективности и безопасности: уменьшения кратности приема, использования комбинированных ЛС или ЛС с меньшими метаболическими последствиями долговременного использования.
Оптимизация АРТ в виде перехода на DTG-содержащие схемы первого ряда проводится в соответствии с алгоритмом перехода на схему тенофовир дизопроксил (далее – TDF) + ламивудин (далее – 3TC) + DTG у взрослых и детей 10 лет и старше согласно приложению 13.
Алгоритм оптимизации схем АРТ у детей при достижении ими соответствующей массы тела приведен в приложении 14.
Избегаются модификации схемы, приводящие к снижению ее генетического порога резистентности.
Допускается сохранение текущей эффективной схемы АРТ, которая хорошо переносится пациентом, если для смены этой схемы АРТ нет других причин, кроме появления новых рекомендованных АРВ-ЛС. Исключение составляют ситуации, связанные с прекращением производства или поставок АРВ-ЛС, и использование схем, состоящих из трех НИОТ.
В первые шесть месяцев после начала или возобновления АРТ модификация схемы с заменой одного или двух компонентов допустима при определяемой ВН ВИЧ. В последующем модификация схемы лечения производится только при неопределяемой ВН ВИЧ, по результатам исследования, проведенного в течение последних 3 месяцев.
У пациентов без предшествующих неудач лечения модификация схемы АРТ, как правило, не приводит к снижению ее эффективности.
29. Оптимизация АРТ с переходом на DTG или биктегравир (далее – BIC) содержащие схемы проводится с учетом достижения вирусной супрессии и потенциальных лекарственных взаимодействий.
Наличие потенциальных лекарственных взаимодействий может потребовать коррекции дозы DTG.
При неопределяемой ВН ВИЧ в течение последних трех месяцев у взрослых и детей старше 10 лет переход осуществляется без замены НИОТ-основания. При определении ВН ВИЧ в диапазоне 50–1000 копий/мл проводится работа по оптимизации приверженности АРТ, исследование повторяется через 3 месяца. При сохраняющейся ВН ВИЧ >200 копий/мл производится переход на следующий ряд АРТ. Тенофовир сохраняется в НИОТ-основании схемы, использующей ИИ, при наличии медицинских противопоказаний к использованию зидовудина (далее – AZT). Тенофовир используется в виде TDF или тенофовира алафенамида (далее – TAF).
Исследование на ВН ВИЧ у детей младше 10 лет для перехода на DTG-содержащую схему является желательным. В обязательном порядке исследование на ВН ВИЧ у детей младше 10 лет проводится при переходе со схемы, содержащей ралтегравир (далее – RAL), где переход осуществляется только в случае неопределяемой ВН ВИЧ.
30. Переход на схемы второго и последующего рядов осуществляется при развитии вирусологической неудачи лечения на фоне используемого лечения. При этом в схеме производится замена не менее чем двух АРВ-ЛС. Замена одного АРВ-ЛС допустима при наличии результатов молекулярно-генетического теста на резистентность ВИЧ с доказанной резистентностью только к данному ЛС (исключая резистентность к 3TC или эмтрицитабину (далее – FTC), обусловленную изолированной мутацией M184V, которая не требует замены этих ЛС в схеме). В новой схеме АРТ назначается не менее двух полностью активных АРВ-ЛС, одно из которых ИИ или ИП. При вирусологической неудаче лечения до назначения новой схемы перерыв в АРТ не допускается. В случае невозможности достижения вирусной супрессии по причине резистентности ВИЧ и (или) медицинских противопоказаний к использованию имеющихся АРВ-ЛС пациенту назначается наиболее эффективная схема из доступных и продолжается ее использование до появления новых терапевтических возможностей. АРТ при этом не прекращается.
В случае развития вирусологической неудачи лечения определяются вероятные причины ее возникновения (недостаточная приверженность АРТ, лекарственные
взаимодействия, первичная резистентность, иное) для предотвращения неудач лечения в будущем.
У пациентов с ВН ВИЧ 50–200 копий/мл анализируются приверженность лечению и лекарственные взаимодействия. При отсутствии указанных проблем АРТ не меняются. При повторном определении с интервалом 3 и более месяцев ВН ВИЧ более 200 копий/мл производится замена на одну из рекомендованных схем следующего ряда, при необходимости после теста на резистентность ВИЧ.
31. Схемы третьего ряда подбираются на основании результатов теста на резистентность ВИЧ, всего анамнеза АРТ и истории вирусологических неудач лечения, а также предшествовавших тестов на резистентность ВИЧ. Эти схемы назначаются врачебным консилиумом. В случае развития оппортунистического заболевания переход на схему третьего ряда производится в кратчайшие сроки с модификацией ее при необходимости после получения результата исследования лекарственной устойчивости ВИЧ.
В схеме третьего ряда назначается не менее двух активных АРВ-ЛС, одно из которых представлено ИИ или ИП/б. Бустерами для ИП выступают ритонавир (далее – RTV или/r) либо кобицистат (далее – COB или/с). В схеме третьего ряда из ИП/б предпочтение отдается бустированному дарунавиру (далее – DRV). Только у пациентов, никогда ранее не принимавших ИП, допустимо назначение в третьем ряду бустированного атазанавира (далее – ATV) или лопинавира/ритонавира (далее – LPV/r). У всех пациентов, принимавших ранее другие ИП, назначение DRV/RTV проводится в дозе 600 мг/100 мг 2 раза в день.
При отсутствии выбора у пациентов с CD4 менее 100 кл/мкл и риском значительного ухудшения состояния допустимо использовать схему АРТ с одним полностью активным ЛС с целью улучшения иммунного статуса из-за снижения ВН ВИЧ.
У пациентов с множественными вирусологическими неудачами лечения, вероятнее всего, НИОТ-основание схемы не содержит ни одного полностью активного АРВ-ЛС. В этом случае рассматривается схема из 4–5 АРВ-ЛС, включающая в себя ИИ. Если у пациента в анамнезе есть вирусологическая неудача лечения в период приема схемы с DTG, он назначается по 50 мг 2 раза в день, если результаты теста на резистентность ВИЧ не определяют другую тактику (обычная доза или полный отказ от использования).
32. При возобновлении АРТ после отрыва от лечения определяется причина, по которой было прекращено лечение. Если отрыв произошел у пациента по причинам, связанным с непереносимостью АРВ-ЛС в схеме, то это ЛС заменяется на другое в соответствии с рекомендованными компонентами среди схем соответствующего ряда. Чаще всего производится замена на АРВ-ЛС того же, при невозможности – другого класса без понижения генетического порога резистентности. Если отрыв от АРТ произошел по причинам, не связанным с переносимостью АРВ-ЛС, то назначается последняя схема, которую принимал пациент, при невозможности – схема из АРВ-ЛС тех же классов, учитывая вирусологическую эффективность и переносимость предшествующей АРТ. Дальнейшая тактика лечения определяется после оценки эффективности АРТ.
33. Приостановка АРТ по медицинским показаниям происходит в следующих случаях:
тяжелые нежелательные реакции на ЛС (тяжелая гепатотоксичность, тяжелые реакции гиперчувствительности);
острое психотическое расстройство у пациента, не связанное с оппортунистическим заболеванием центральной нервной системы (далее – ЦНС), до выработки совместной тактики лечения врачами-специалистами (врачом-психиатром-наркологом, врачом-психиатром детским и врачом-инфекционистом);
в периоперационном периоде (на 1–2 дня);
при развитии острой недостаточности органов и систем, не обусловленной ВИЧ-инфекцией.
при развитии острой недостаточности органов и систем, не обусловленной ВИЧ-инфекцией.
При приостановке АРТ по медицинским показаниям или отказе от нее пациента для схем, содержащих ННИОТ (эфавиренц (далее – EFV), невирапин (далее – NVP)), по возможности продлевается прием НИОТ-основания на 7–14 дней. В случае использования схем, содержащих ИП или ИИ, прием всех АРВ-ЛС в схеме прекращается одновременно.
34. Алгоритм лабораторного мониторинга ВИЧ-инфекции и эффективности АРТ у пациентов с ВИЧ-инфекцией приведен в приложении 15.
Лабораторный мониторинг эффективности АРТ осуществляется путем определения ВН ВИЧ. Через 3 месяца эффективной АРТ у большинства пациентов ВН ВИЧ составляет <500 копий/мл, через 6 месяцев – <50 копий/мл. При начальной ВН ВИЧ более 106 копий/мл описанный ответ на терапию может запаздывать на несколько недель. Отсутствие ответа на терапию по динамике ВН ВИЧ на АРТ требует анализа приверженности и принятия мер по ее восстановлению, а сохранение через 3 месяца ВН ВИЧ более 200 копий/мл ведет к констатации вирусологической неудачи лечения и быстрому переходу на следующий ряд АРТ.
Результаты определения количества CD4+ лимфоцитов необходимы для установления степени ВИЧ-ассоциированного иммунодефицита, назначения или прекращения профилактического лечения ОИ.
35. Тест на резистентность ВИЧ выполняется по следующим медицинским показаниям:
вирусологическая неудача лечения схемой АРТ первого ряда при невозможности использовать рекомендованные схемы второго ряда;
вирусологическая неудача лечения схемой второго или третьего ряда;
начало АРТ, если есть сведения, указывающие на возможность инфицирования в результате контакта с ЛЖВ с неэффективной АРТ;
начало АРТ, если заражение произошло на фоне приема ПрЭП;
вирусологическая неудача лечения на схеме АРТ любого ряда у пациента с ко-инфекцией вирусом гепатита В (далее – ВГВ), получающего тенофовир;
беременность с впервые выявленной ВИЧ-инфекцией;
перинатальное заражение ВИЧ у детей.
Необходимыми условиями выполнения теста на резистентность ВИЧ являются:
наличие ВН ВИЧ не менее 1000 копий/мл;
продолжающийся прием АРВ-ЛС или не позднее чем через 4 недели после отмены всей схемы АРТ или ее компонентов.
Тест на резистентность ВИЧ, как правило, включает определение мутаций к АРВ-ЛС классов НИОТ, ННИОТ и ИП. При необходимости определения мутаций резистентности к ИИ в случае вирусологической неудачи лечения на фоне использования ЛС этого класса делается соответствующая отметка в направлении.
Не допускается отсрочка начала АРТ в ожидании результатов теста на резистентность ВИЧ у пациентов с продвинутой ВИЧ-инфекцией, туберкулезом (далее – ТБ), беременных, детей в возрасте до 1 года. Лечение начинается эмпирически подобранной или рекомендованной настоящим клиническим протоколом схемой
с последующей модификацией после получения результата исследования. При выборе схемы отдается предпочтение АРВ-ЛС с высоким генетическим барьером резистентности (ИИ или ИП).
До получения результатов теста на резистентность ВИЧ пациенту продолжается лечение прежней схемой или назначается новая схема АРТ, которая затем при необходимости модифицируется с учетом результатов исследования.
ГЛАВА 4
АРТ У БЕРЕМЕННЫХ
36. При наступлении беременности у женщины, получающей эффективную АРТ, терапия продолжается, кроме случаев, когда в отношении используемых в схеме АРВ-ЛС нет достаточных данных об эффективности во время беременности (BIC, доравирин (далее – DOR), схемы из двух АРВ-ЛС). В этом случае проводится анализ истории АРТ и с пациентом обсуждаются потенциальные риски и польза от использования текущей схемы.
Если в схеме используются АРВ-ЛС, концентрация которых во время беременности не достигает терапевтического уровня (DRV/с, рилпивирин (далее – RPV), DRV/r 800 мг/100 мг 1 раз в день), схема АРТ заменяется на рекомендованную на время беременности.
Использование EFV у беременных не повышает риск возникновения отклонений развития плода и неблагоприятных исходов беременности.
DTG может быть назначен женщинам детородного возраста, если они были проинформированы о возможном, но не доказанном повышении риска дефектов нервной трубки (при зачатии и до конца первого триместра на уровне 0,19 %, что не является статистически значимым). Если у женщины выявляется беременность после первого триместра, следует начать или продолжить прием DTG на протяжении всей беременности.
37. У женщин, не получавших АРТ ко времени наступления беременности, АРТ начинается в кратчайшие сроки с использованием одной из рекомендованных схем. Схемы АРТ, рекомендованные для использования у беременных, установлены в приложении 16.
Если АРТ начинается во втором или третьем триместре, DTG входит в схему.
При получении ВН ВИЧ более 200 копий/мл при обследовании перед родами DTG присоединяется к схеме, если он в нее еще не входит. При этом забирается кровь для последующего исследования теста на резистентность ВИЧ.
38. Если ко времени наступления или во время беременности фиксируется вирусологическая неудача лечения, в кратчайшие сроки производится переход на схему следующего ряда из числа рекомендованных во время беременности.
39. Медицинское наблюдение и лабораторное обследование беременных с ВИЧ-инфекцией, а также лечебно-профилактические мероприятия в родах и послеродовом периоде осуществляется в соответствии с клиническим протоколом «Профилактика передачи ВИЧ-инфекции от матери ребенку».
ГЛАВА 5
АРТ У ДЕТЕЙ
40. АРТ показана всем ВИЧ-положительным детям независимо от возраста, клинической и иммунологической стадии ВИЧ-инфекции.
Дети, рожденные ВИЧ-положительными матерями, обследуются, и в случае выявления ВИЧ-положительного статуса в кратчайшие сроки начинается АРТ.
41. Предпочтительной схемой АРТ первого ряда для детей в возрасте >4 недель с массой тела >3 кг является схема, включающая DTG. Альтернативным ИИ для детей в возрасте >6 лет и массой тела >25 кг является BIC (в виде фиксированной комбинации TAF/FTC/BIC).
У новорожденных для начала АРТ используются схемы, включающие:
RAL (дети в возрасте <4 недель с массой тела >2 кг),
или
LPV/r (дети в возрасте >14 дней <4 недель),
или
NVP (дети в возрасте <14 дней).
Перед началом АРТ у ребенка проводится забор крови для выполнения теста на резистентность ВИЧ к АРВ-ЛС. АРТ начинается до получения результатов теста на резистентность ВИЧ, при выборе схемы АРТ учитывается возможность переданной резистентности (анамнез лечения человека, от которого произошло заражение) и резистентности, связанной с неудачей проведения профилактики передачи ВИЧ-инфекции от матери ребенку. Если во время беременности использовались EFV или NVP, то в случае произошедшей вертикальной передачи используется схема, основанная не на ННИОТ: используется RAL, LPV/r или DTG.
42. При достижении детьми соответствующих возраста и (или) массы тела проводится модификация схем АРТ с переходом на более эффективные, безопасные и удобные в приеме ЛС.
43. Высокая приверженность АРТ является критически важной при лечении детей. Для поддержки приверженности АРТ медицинская помощь оказывается мультидисциплинарными командами, включающими врача-педиатра, психолога, педагога-дефектолога, социального работника. Для детей, живущих половой жизнью, мотивацией к приему АРТ может служить обеспечение безопасности полового партнера (Н=Н, наличие неопределяемой ВН <200 копий/мл на протяжении >6 месяцев сопряжено с отсутствием риска половой передачи ВИЧ).
44. При ведении ВИЧ-положительных детей врачу-педиатру необходимо консультироваться с врачом-специалистом по инфекционным болезням у детей.
ГЛАВА 8
СОПУТСТВУЮЩИЕ СОМАТИЧЕСКИЕ ЗАБОЛЕВАНИЯ И СОСТОЯНИЯ У ЛЖВ
62. Риски развития сопутствующих соматических заболеваний и состояний (атеросклероз, остеопороз, некоторые виды рака, сахарный диабет второго типа, стеатоз и стеатогепатит, заболевания почек, тревога, депрессия) у ЛЖВ сохраняются выше общепопуляционных, несмотря на своевременно начатую эффективную АРТ. Врач-специалист предоставляет рекомендации по воздействию на модифицируемые факторы риска: коррекция веса (включая диету и двигательный режим), отказ от курения, сокращение употребления алкоголя.
63. Лекарственная терапия сопутствующих заболеваний у ЛЖВ сопровождается анализом потенциальных лекарственных взаимодействий с АРВ-ЛС.
64. Коррекции доз АРВ-ЛС у пациентов с нарушением функции печени и с нарушением функции почек осуществляются согласно приложениям 27 и 28 соответственно.
65. Тревожные расстройства, депрессия, а также расстройства, обусловленные употреблением алкоголя, негативно сказываются на результатах АРТ. Первичная
диагностика этих состояний проводится по медицинским показаниям врачом-специалистом, предоставляющим АРТ, при обращении пациента за медицинской
помощью.
Тестирование для выявления расстройств, обусловленных употреблением алкоголя (AUDIT), проводится на основании опросника по форме согласно приложению 29.
Тестирование для выявления генерализованного тревожного расстройства (далее – ГТР) проводится на основании опросника по форме согласно приложению 30. К факторам риска тревожных расстройств относятся наследственность, употребление алкоголя и других психоактивных веществ, когнитивные расстройства, социальное неблагополучие. У пациентов с возможным ГТР проводится оценка суицидального риска.
Тестирование для выявления депрессии и определения степени ее тяжести проводится на основании опросника здоровья пациента PHQ-2, PHQ-9 для выявления депрессии по форме согласно приложению 31.
66. Пациенты с вероятным ГТР направляются к врачу-специалисту для дальнейшей диагностики и получения помощи, в том числе медицинской. До этого исключаются другие причины, связанные с воздействием ЛС или других веществ (избыточное употребление кофеина, употребление психостимуляторов), а также сопутствующие заболевания и состояния (гипертиреоидизм, гипогликемия и гиперадренокортицизм).
При наличии умеренно-тяжелого, тяжелого депрессивного расстройства, а также при выявлении суицидального риска пациенты направляются к врачу-психиатру-наркологу или врачу-психиатру детскому.
ГЛАВА 9
ПРЭП ВИЧ-ИНФЕКЦИИ С ПРИМЕНЕНИЕМ АРВ-ЛС
67. ПрЭП назначается по эпидемическим показаниям лицам с высоким риском инфицирования ВИЧ (при отсутствии медицинских противопоказаний) из числа
следующих контингентов населения: люди, употребляющие наркотики; мужчины, практикующие секс с мужчинами; секс работники; трансгендерные люди; половые партнеры ЛЖВ, не достигшие вирусной супрессии (неопределяемой ВН).
При проведении врачебной консультации перед назначением ПрЭП разъясняется, что ЛЖВ с неопределяемой ВН в результате эффективной АРТ не являются источниками ВИЧ-инфекции при сексуальных отношениях без использования презерватива.
68. К медицинским противопоказаниям для назначения ПрЭП относятся:
ВИЧ-положительный статус обратившегося лица (по данным Регистра);
реакция гиперчувствительности на TDF/FTC или TAF/FTC, или любой компонент данного ЛС в анамнезе;
нарушение функции почек (согласно медицинским документам или по результатам медицинского обследования), подтверждаемое расчетным клиренсом креатинина (далее – КК) <60 мл/мин. (по формуле Кокрофта-Голта) при планируемом использовании TDF и <30 мл/мин. при планируемом использовании TAF.
69. ПрЭП может предоставляться в амбулаторных условиях при строгом соблюдении рекомендаций по приему ЛС и с лабораторным мониторингом, включая периодическое тестирование на ВИЧ-инфекцию.
70. ПрЭП используется в периоды значительного риска заражения ВИЧ-инфекцией и может быть прекращена в периоды низкого риска или отсутствия риска.
71. Для ПрЭП назначается TDF/FTC 300/200 мг таблетки, покрытые оболочкой, или TAF/FTC 25 г/200 мг, таблетки.
72. Для использования TDF/FTC с целью ПрЭП может применяться один из двух режимов – постоянный или интермиттирующий (по требованию). Выбор режима определяется гендерной принадлежностью, частотой и типом сексуальных контактов, а также личными предпочтениями пациента. Ежедневный прием ПрЭП обладает большей эффективностью, так как при его использовании легче формируется высокая приверженность АРТ без развития более значимых токсических и метаболических последствий. При этом при правильном приеме интермиттирующий режим (режим приема по требованию) обладает сравнимой эффективностью, но имеет гендерные и поведенческие ограничения использования и не защищает от заражения ВИЧ парентеральным путем.
73. При использовании TAF/FTC с целью ПрЭП может применяться только постоянный режим приема ЛС.
74. Определение медицинских показаний к применению ПрЭП проводится путем интервьюирования по признаку наличия любого из факторов высокого риска инфицирования ВИЧ на протяжении последних 6 месяцев:
анальный или вагинальный секс без презерватива с партнером с неизвестным или ВИЧ-положительным статусом;
новый эпизод заболевания инфекцией, передающейся половым путем (далее – ИППП) (сифилис, гонорея, хламидиоз);
получение ПЭП заражения ВИЧ.
75. Перед назначением ПрЭП проводятся следующие диагностические мероприятия:
осмотр врачом-специалистом;
тестирование на ВИЧ путем определения антител к ВИЧ или антител, антигена или антигенов ВИЧ в сроки не более 7 дней до начала приема;
определение HBsAg. Положительный результат определения не является медицинским противопоказанием к ПрЭП, но требует дополнительного медицинского
обследования для решения вопроса о необходимости противовирусной терапии инфекции, вызванной ВГВ;
определение креатинина крови;
при отсутствии возможности быстрого определения креатинина крови: у лиц младше 30 лет без заболеваний почек в анамнезе, сопутствующих артериальной гипертензии и (или) сахарного диабета ПрЭП может быть назначена до получения результата определения креатинина крови и затем отменена при выявлении медицинских противопоказаний; у лиц в возрасте 30–50 лет без сопутствующих артериальной гипертензии и (или) сахарного диабета может быть использовано определение протеинурии; при отсутствии белка в моче креатинин в крови в плановом порядке определяется через 3 месяца после начала приема TDF/FTC.
76. Ограничениями к немедленному назначению ПрЭП являются:
незавершенное тестирование на ВИЧ-инфекцию (положительный результат скринингового тестирования на ВИЧ-инфекцию) до подтверждения ВИЧ-негативного статуса;
вероятная острая ВИЧ-инфекция (отрицательный результат теста на ВИЧ при наличии симптомов острого ретровирусного синдрома) – до подтверждения ВИЧ-негативного статуса;
незащищенный сексуальный контакт с известным ВИЧ-положительным статусом в последние 72 часа (в этом случае предлагается ПЭП);
парентеральное употребление психоактивных веществ с использованием общих приспособлений (шприц, игла, иное) совместно с лицом с неизвестным или ВИЧ-положительным статусом в последние 72 часа (в этом случае предлагается ПЭП);
прием АРВ-ЛС с целью ПЭП во время обращения за ПрЭП (ПрЭП может быть назначена сразу после завершения ПЭП).
77. Постоянный режим ПрЭП заключается в ежедневном приеме 1 таблетки TDF/FTC или TAF/FTC приблизительно в одно и то же время (±2 часа) 1 раз в сутки. Постоянный режим приема TDF/FTC может быть использован у представителей любых групп риска, включая цисгендерных и трансгендерных людей, практикующих секс с мужчинами или женщинами. TAF/FTC может быть использован только у мужчин и трансгендерных женщин.
Для начала постоянного режима ПрЭП у трансгендерных женщин, не получающих лечение половыми гормонами, используется прием 2 таблеток TDF/FTC за 2–24 часа до сексуального контакта (как при интермиттирующем режиме). Всем остальным категориям лиц в первые 7 дней после начала постоянного режима ПрЭП рекомендуется практиковать секс с использованием презерватива и (или) использовать другие способы профилактики.
При прекращении постоянного режима ПрЭП прием TDF/FTC продолжают в течение 7 дней: после последнего рискованного сексуального контакта - трансгендерные мужчины или получающие гормональную терапию трансгендерные женщины, после последнего парентерального контакта – все лица вне зависимости от половой принадлежности и идентичности.
ПрЭП с использованием ежедневного приема TDF/FTC эффективна и безопасна у женщин, планирующих беременность, беременных и кормящих, имеющих половых партнеров из числа ЛЖВ с неизвестной ВН или с недостигнутой вирусной супрессией.
78. Интермиттирующий режим ПрЭП (режим приема по требованию) заключается в приеме 2 таблеток TDF/FTC за 2–24 часа до сексуального контакта, затем одной таблетки TDF/FTC через 24 часа после первых двух и затем еще 1 таблетки TDF/FTC через 24 часа после второго приема (или через 48 часов после приема первых двух таблеток). Таким образом, схема приема описывается как 2+1+1 и занимает 48 часов.
Интермиттирующий режим ПрЭП может быть использован для предотвращения половой передачи ВИЧ у трансгендерных женщин, не получающих лечение половыми гормонами. Интермиттирующий режим ПрЭП назначается после информирования о доступности использования постоянного режима ПрЭП, в случае если пациент считает более приемлемым использование интермиттирующего режима. Эффективность интермиттирующего приема ПрЭП для других ключевых групп в настоящее время не доказана, но может использоваться при появлении научно обоснованных рекомендаций.
79. Если пациент, получающий ПрЭП, решает перейти с интермиттирующего на постоянный режим, он продолжает ежедневный прием одной таблетки TDF/FTC
приблизительно в одно и то же время суток.
Если пациентом принято решение о переходе с постоянного на интермиттирующий режим, он может прекратить ежедневное использование TDF/FTC, приняв последнюю таблетку через 48 часов после последнего сексуального контакта.
80. При прохождении ПрЭП осуществляется обязательный мониторинг безопасности и эффективности, включая:
осмотр врачом-специалистом через 1 месяц после начала и в дальнейшем каждые три месяца;
тестирование на ВИЧ-инфекцию путем определения антител к ВИЧ или антител, антигена и (или) антигенов ВИЧ через 1 месяц после начала и затем каждые 3 месяца;
тестирование на ВИЧ-инфекцию по медицинским показаниям (признаки острого ретровирусного синдрома, перерывы в ПрЭП более 7 дней при постоянном режиме приема);
определение содержания креатинина крови и расчет КК каждые 6–12 месяцев у лиц в возрасте 50 лет и старше или при наличии хронического заболевания почек, а также у пациентов с КК<90 мл/мин., определенном в первые 3 месяца прохождения ПрЭП или перед ее началом; при определении КК <60 мл/мин анализ повторяется, в случае повторного результата КК <60 мл/мин ПрЭП прекращается до выяснения причины нарушения функции почек;
при необходимости по медицинским показаниям проводятся определение анти-HBs, определение антител к ВГС (далее – анти-HCV), обследование на ИППП.
81. При получении реактивного результата экспресс-теста на ВИЧ-инфекцию перед назначением или в ходе мониторинга эффективности ПрЭП обеспечивается забор венозной крови для диагностического тестирования на ВИЧ-инфекцию.
82. В случае обнаружения анти-HCV или при положительных результатах тестирования на возбудителей ИППП, ПрЭП может быть назначена, при этом даются рекомендации по дальнейшему медицинскому обследованию у профильного врача- специалиста, до завершения которого необходимо избегать незащищенных сексуальных контактов.
ГЛАВА 10
ПЭП ВИЧ-ИНФЕКЦИИ С ПРИМЕНЕНИЕМ АРВ-ЛС
83. ПЭП назначается по эпидемическим показаниям лицам, подвергшимся риску инфицирования ВИЧ (экспонированным) в следующих случаях:
ранение острым инструментом при выполнении манипуляций при оказании медицинской помощи пациенту с положительным ВИЧ-статусом или пациенту с неизвестным ВИЧ-статусом, но принадлежащим к ключевой группе населения (подкожный или внутримышечный укол полой иглой, постановка внутрисосудистого катетера, повреждение кожи скальпелем, полой или шовной иглой в ходе хирургического вмешательства);
контакт длительностью более 15 минут слизистых или поврежденной кожи с кровью пациента с положительным ВИЧ-статусом;
сексуальный контакт (вагинальный или анальный секс, рецептивный оральный секс с эякуляцией) экспонированного лица, не получающего или не приверженного ПрЭП, с партнером с положительным ВИЧ-статусом без вирусной супрессии или с партнером с неизвестным ВИЧ-статусом, но принадлежащим к ключевой группе населения;
парентеральное употребление психоактивных веществ с использованием общих приспособлений (шприц, игла, иное) совместно с лицом с ВИЧ-положительным статусом;
контакт с другими биологическими жидкостями, содержащими ВИЧ (цереброспинальной, плевральной, синовиальной, перитонеальной, амниотической), с учетом обстоятельств повреждения кожи, длительности экспозиции и наличия видимой примеси крови.
84. Перед началом ПЭП или в течение первых 48 часов экспонированных лиц обследуют на ВИЧ, ВГС и ВГВ. При невозможности использования экспресс-тестов в эти сроки забирается кровь для последующего проведения серологических исследований в лаборатории. При сексуальном контакте предлагается медицинское обследование на ИППП, женщинам фертильного возраста в случае необходимости предлагается пройти тест на беременность. Такой же комплекс обследований назначается лицу, с которым произошел контакт, если его можно установить. Если ВИЧ-положительный статус известен, проводится медицинское обследование на ВН ВИЧ. При определяемой ВН ВИЧ назначается тест на резистентность ВИЧ.
85. ПЭП начинается как можно быстрее, желательно в первые 4 часа после контакта, но не позднее 72 часов.
86. ПЭП назначает врач-специалист при наличии медицинских показаний. Первую дозу АРВ-ЛС пациент может получить в приемных отделениях инфекционных больниц при круглосуточном обращении. В последующем пациент обращается в ближайшее консультативно-диспансерное отделение (кабинет) по ВИЧ-инфекции либо в кабинет инфекционных заболеваний, осуществляющий выдачу АРТ, где врач-специалист, назначающий АРТ, определяет целесообразность продолжения ПЭП и при необходимости модифицирует схему по результатам медицинского обследования экспонированного лица и того, с кем произошел контакт. В рабочее время пациент может обращаться непосредственно в консультативно-диспансерное отделение (кабинет) по ВИЧ-инфекции либо в кабинет инфекционных заболеваний, осуществляющий выдачу АРТ. Контроль переносимости АРВ-ЛС, лекарственных взаимодействий с другими ЛС производит врач- инфекционист или врач-специалист, прошедший обучение по АРТ.
87. Медицинскими противопоказаниями к ПЭП являются:
ВИЧ-инфекция у экспонированного лица;
отрицательный результат скринингового тестирования на ВИЧ-инфекцию лица, с которым произошел контакт, при отсутствии у него признаков острой ВИЧ-инфекции и информации о принадлежности к ключевой группе населения;
контакт с биологическими жидкостями без содержания крови, не представляющими угрозу инфицирования ВИЧ (слезы, моча, пот, слюна), или не сопровождавшийся значимым нарушением целости кожи и слизистых.
88. Экспонированное лицо, которому назначается ПЭП, информируется о процедуре ПЭП, режиме использования АРВ-ЛС, потенциальных рисках и пользе от приема некоторых АРВ-ЛС и лабораторном мониторинге после завершения. Также всем экспонированным лицам рекомендуется практиковать защищенный секс до подтверждения ВИЧ-отрицательного статуса после завершения ПЭП.
89. Схемы АРВ-ЛС, используемые для ПЭП ВИЧ-инфекции, приведены в приложении 32, состоят из НИОТ-основания и третьего АРВ-ЛС.
90. Тенофовир-содержащие схемы ПЭП назначаются лицам вне зависимости от ко-инфекции ВГВ. У лиц с ко-инфекцией ВГВ после завершения ПЭП контролируется функция печени, проводится биохимическое исследование крови через 1 и 4 месяца после завершения ПЭП. У лиц с неизвестным статусом в отношении ВГВ-инфекции при назначении ПЭП выполняется исследование на наличие HBsAg в крови и затем в случае получения положительного результата проводится комплекс дополнительных медицинских обследований.
91. Продолжительность ПЭП составляет 28 дней. При получении отрицательного результата скринингового тестирования на ВИЧ лица, с которым произошел контакт, ПЭП может быть прекращена досрочно, если нет информации о принадлежности этого лица к ключевой группе риска. ПЭП также может быть прекращена, если имелся сексуальный контакт с лицом с положительным ВИЧ-статусом, у которого получен результат обследования на ВН ВИЧ менее 200 копий/мл.
92. После завершения ПЭП через 3 и 6 месяцев проводится тестирование на ВИЧ с применением лабораторных методов ИФА на тест-системах четвертого поколения.
93. Если лицо, с которым произошел контакт, имело инфекцию, вызванную ВГС, экспонированное лицо дополнительно обследуется на анти-HCV через 3 и 6 месяцев после контакта.
94. При сохранении высокого риска инфицирования ВИЧ после завершения ПЭП экспонированному лицу предлагается ПрЭП.
Профилактика
ГЛАВА 6
ОППОРТУНИСТИЧЕСКИЕ ЗАБОЛЕВАНИЯ. КО-ИНФЕКЦИИ ВИРУСАМИ ГЕПАТИТА
45. Оппортунистические заболевания являются проявлениями прогрессирования ВИЧ-инфекции, приводящей к снижению иммунитета, в результате отсутствия АРТ или ее неэффективности.
46. Для предотвращения развития оппортунистических заболеваний назначается противомикробное профилактическое лечение. Первичное профилактическое лечение оппортунистических заболеваний назначается для его предупреждения, до наступления эпизода заболевания (по результатам исследования количества CD4+ лимфоцитов). Вторичное профилактическое лечение назначается после завершения основного курса лечения для предотвращения рецидива оппортунистических заболеваний.
Алгоритмы профилактического лечения ОИ у пациентов с ВИЧ-инфекцией старше 18 лет и профилактического лечения ОИ у пациентов с ВИЧ-инфекцией младше 18 лет и у ВИЧ-экспонированных детей приведены в приложениях 17 и 18 соответственно.
47. При развитии оппортунистических заболеваний проводятся диагностические обследования и назначается лечение.
Объем медицинской помощи, оказываемой пациентам с ВИЧ-инфекцией при оппортунистических заболеваниях (взрослое население) в стационарных условиях, устанавливается согласно приложению 19.
Объем медицинской помощи, оказываемой пациентам с ВИЧ-инфекцией при оппортунистических заболеваниях (детское население) в стационарных условиях, устанавливается согласно приложению 20.
При развитии оппортунистических заболеваний у пациента, получающего АРТ, оценивается ее эффективность и при вирусологической неудаче лечения используются схемы следующего ряда.
В случае медикаментозной аллергии к сульфаметоксазолу/триметоприму назначаются альтернативные ЛС или проводится десенсибилизация. Схемы десенсибилизации к сульфаметоксазолу/триметоприму устанавливаются согласно приложению 21.
48. Часть пациентов с оппортунистическими заболеваниями испытывают затруднения в проглатывании таблеток или капсул из-за тяжести состояния или поражения слизистой ротоглотки и (или) пищевода. В такой ситуации могут быть использованы лекарственные формы для детей (растворы для приема внутрь, диспергируемые таблетки) или некоторые твердые лекарственные формы для взрослых. Допускается дробить таблетки или вскрывать капсулы следующих АРВ-ЛС: абакавир (далее – ABC), 3TC (но не комбинированная форма ABC/3TC), TDF и TAF (в том числе в комбинации с FTC), AZT, EFV, NVP, DRV (но не RTV), DRV/c, DTG, RAL. Допускается дробить таблетки следующих ЛС для лечения и медицинской профилактики оппортунистических заболеваний: сульфаметоксазол/триметоприм (дробится с большим усилием), флуконазол, все ЛС для лечения лекарственно-чувствительного ТБ.
49. ТБ является одним из важнейших оппортунистических заболеваний при ВИЧ-инфекции. Своевременная диагностика ТБ улучшает исход заболевания у ЛЖВ и предотвращает дальнейшее распространение ТБ среди населения.
При каждом медицинском осмотре или обращении ЛЖВ за медицинской помощью осуществляется клинико-анамнестический скрининг на активный ТБ у ЛЖВ в соответствии с алгоритмом согласно приложению 22. При положительном результате скрининга в приоритетном порядке проводятся исследование мокроты методом GeneXpert MBT RIF и рентгенологическое обследование органов грудной клетки. При получении результатов, свидетельствующих против активного ТБ, АРТ назначается не позднее 7 дней после начала обследования.
У пациентов с продвинутой ВИЧ-инфекцией для диагностики ТБ может быть использовано определение антигена липоарабиноманнана микобактерии ТБ в моче с помощью быстрых ИХА-тестов. Исследование показано пациентам с количеством CD4+ лимфоцитов менее 100 кл/мкл до начала АРТ в амбулаторных условиях, пациентам с количеством CD4+ лимфоцитов 101–200 кл/мкл в стационарных условиях при наличии симптомов (лихорадка, потливость, снижение массы тела, головная боль и иное). Положительный результат теста требует дальнейшего обследования пациента для подтверждения диагноза ТБ.
50. У взрослых и детей с активным ТБ АРТ начинается в кратчайшие сроки в течение первых 2 недель противотуберкулезного лечения вне зависимости от количества CD4+ лимфоцитов и профиля чувствительности микобактерии ТБ. В случае неудовлетворительной переносимости противотуберкулезных ЛС, в особенности при лечении лекарственно-устойчивого ТБ, начало АРТ может быть отсрочено до устранения нежелательных явлений от приема этих ЛС, максимально – до 8 недель.
У пациентов с туберкулезным менингитом АРТ начинается после 4 недель противотуберкулезного лечения, но не позднее 8 недель со времени его начала.
Схемы АРТ у пациентов, получающих лечение ТБ с использованием рифампицина, а также у пациентов, получающих лечение лекарственно-устойчивого ТБ, установлены в приложениях 23 и 24 соответственно.
В схемах АРТ у пациентов, получающих профилактическое лечение ТБ с применением схемы рифапентин1 900 мг + изониазид 900 мг один раз в неделю, используются АРВ-ЛС согласно приложению 25.
Если у пациента, принимающего АРТ, выявляется ТБ, противотуберкулезное лечение начинается в кратчайшие сроки в течение 7 дней после подтверждения диагноза.
51. У пациентов с криптококковой антигенемией при отсутствии признаков менингита АРТ начинается через 2 недели после начала первичного профилактического лечения флуконазолом. При исключении криптококкового менингита по результатам люмбальной пункции АРТ начинается немедленно.
У пациентов с криптококковым менингитом переход на схему второго и последующего рядов производится через 4–6 недель в зависимости от режима противогрибкового лечения (не ранее 2 недель после завершения индукционной фазы лечения). У пациентов с туберкулезным менингитом переход на схему второго и последующего рядов производится через 8 недель противотуберкулезного лечения.
52. Начало АРТ у пациентов с низким уровнем CD4 может сопровождаться развитием воспалительного синдрома восстановления иммунитета (далее – ВСВИ). При парадоксальном ВСВИ симптомы оппортунистических заболеваний, вирусного гепатита или некоторых других заболеваний (например, псориаза) усиливаются, несмотря на проводимое лечение. Демаскирующий ВСВИ после начала АРТ предполагает появление симптомов оппортунистических заболеваний, которые не были диагностированы до начала АРТ.
Развитие ВСВИ ухудшает общее состояние пациента и при некоторых оппортунистических заболеваниях может привести к смертельному исходу (криптококковый и туберкулезный менингиты, прогрессирующая мультифокальная лейкоэнцефалопатия, иное). Сроки возникновения ВСВИ – от 2 недель до 12 месяцев после начала АРТ, чаще – первые 3 месяца. Медицинской профилактикой демаскирующего ВСВИ является тщательное медицинское обследование пациента с продвинутой ВИЧ-инфекцией. При средней тяжести парадоксального ВСВИ используются нестероидные противовоспалительные средства (принимается во внимание высокая вероятность сопутствующего поражения почек, в том числе ассоциированного с ВИЧ, и необходимость использования TDF). При тяжелом парадоксальном ВСВИ допускается использование короткого курса глюкокортикоидных гормонов (до 1 месяца). Исключение составляют криптококковый менингит и саркома Капоши, при лечении которых использование глюкокортикоидных гормонов нежелательно.
53. Ко-инфекция ВИЧ и вирусом гепатита С (далее – ВГС) является показанием к лечению хронической инфекции, вызванной ВГС, с помощью ЛС прямого противовирусного действия (далее – ЛС ППД), вне зависимости от степени выраженности фиброза печени.
Лечение начинается после достижения супрессии ВИЧ или в любые сроки в случае, если активность инфекции, вызванной ВГС, в том числе с проявлениями цирроза печени, препятствует использованию жизненно важных ЛС, например, для лечения микобактериоза.
Медицинское обследование и противовирусное лечение взрослых пациентов с ко-инфекцией ВИЧ и ВГС проводятся в соответствии с клиническим протоколом «Диагностика и лечение пациентов (взрослое население) с хроническими вирусными гепатитами B и C», утвержденным постановлением Министерства здравоохранения Республики Беларусь от 19 марта 2019 г. № 19.
С учетом лекарственных взаимодействий ЛС ППД для лечения инфекции, вызванной ВГС, и АРВ-ЛС согласно приложению 26 производится модификация схемы АРТ.
54. При ко-инфекции ВИЧ и ВГВ пациенты получают схему АРТ, включающую тенофовир (кроме случаев непереносимости тенофовира). Прекращение использования тенофовира в схеме АРТ может привести к тяжелому обострению гепатита. У пациентов с циррозом печени в течение полугода после начала, возобновления или перехода на следующий ряд АРТ проводится более частый мониторинг функции печени из-за возможного развития печеночной недостаточности в результате ВСВИ.
Если ко-инфицированный ВИЧ и ВГВ пациент нуждается в отмене TDF или TAF, его прием может быть прекращен при наступлении сероконверсии, то есть при появлении антител к поверхностному антигену ВГВ (далее – анти-HBs). У пациентов с сероклиренсом, то есть при исчезновении поверхностного антигена ВГВ (далее – HBsAg) без появления анти-HBs, определяющимся на протяжении не менее 3 лет, использование тенофовира может быть прекращено, но под тщательным биохимическим контролем функции печени. У пациентов с циррозом печени противовирусное лечение в отношении ВГВ не прекращается; при крайней необходимости тенофовир может быть заменен на энтекавир.
55. Все HBsAg-позитивные пациенты обследуются на инфекцию, вызванную вирусом гепатита D (далее – ВГД).
56. Всем ЛЖВ с отрицательным результатом обследования на анти-HBs проводится вакцинация от гепатита В. Исключение составляют пациенты с изолированными положительным результатом определения антител к сердцевинному антигену ВГВ (HBcAg) при отрицательном результате исследования на другие маркеры ВГВ (HBsAg, анти-HBs). Вакцинация должна проводиться у пациентов с достигнутой вирусной супрессией на АРТ при количестве CD4+ лимфоцитов более 200 кл/мкл (или при более низком количестве у пациентов, не демонстрирующих иммунологический ответ на АРТ).
ГЛАВА 7
ПЕРВИЧНАЯ МЕДИЦИНСКАЯ ПРОФИЛАКТИКА ВАКЦИНОКОНТРОЛИРУЕМЫХ ИНФЕКЦИЙ У ПАЦИЕНТОВ С ВИЧ-ИНФЕКЦИЕЙ МЛАДШЕ 18 ЛЕТ
57. Вакцинация ВИЧ-экспонированных детей, а также ВИЧ-положительных детей с незначительным или умеренным иммунодефицитом проводится в соответствии с постановлением Министерства здравоохранения Республики Беларусь от 17 мая 2018 г. № 42 «О профилактических прививках».
58. ВИЧ-экспонированным детям на 3–5 сутки жизни вводится вакцина против ТБ без предварительного определения уровня CD4+ лимфоцитов.
59. Особенностями вакцинации ВИЧ-положительных детей с тяжелым иммунодефицитом (по количеству CD4+ лимфоцитов у детей в возрасте 1–6 лет <15 %, в возрасте старше 6 лет – <15 % или <200 кл/мкл) являются:
введение живых вакцин (от кори, эпидемического паротита, краснухи, ветряной оспы, желтой лихорадки, живые вакцины от гриппа) противопоказано;
в первичной серии вакцинации от COVID-19 используется дополнительная доза вакцины, так как иммунный ответ на стандартную первичную серию может быть субоптимальным.
60. ВИЧ-положительные дети, не привитые в календарные сроки (в том числе от пневмококковой и гемофильной инфекций), прививаются в любом возрасте по схеме, рекомендуемой инструкцией по медицинскому применению (листком-вкладышем) соответствующей вакцины.
61. Дополнительно рекомендуется использовать у ВИЧ-положительных детей следующие вакцины:
вакцина от ветряной оспы в возрасте 1 год и 6 лет (возможно совместное введение с вакциной от кори, эпидемического паротита и краснухи). Ранее непривитым детям старше 6 лет вакцина вводится двукратно с интервалом >1 месяца. С целью постконтактной профилактики вакцина вводится детям старше 12 месяцев, не имеющим иммунитета к ветряной оспе, однократно не позже 5-х суток после контакта с больным ветряной оспой;
конъюгированная вакцина от менингококковой инфекции серогрупп ACWY вводится в возрасте 2 лет и старше по схеме 2 дозы с интервалом >8 недель, но не ранее чем через 4 недели после завершения серии вакцинации конъюгированной пневмококковой вакциной. Детям с иммунодефицитом возможно введение бустеров каждые 5 лет;
вакцина от вируса папилломы человека вводится в возрасте 9 лет и старше по трехдозовой схеме независимо от возраста ребенка и степени иммунодефицита.
______________________________
1 Назначается за счет собственных средств, средств юридических лиц и иных источников, не запрещенных законодательством, при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача или лица, его заменяющего, с оформлением записи в медицинских документах.
Информация
Источники и литература
-
Постановления и приказы Министерства здравоохранения Республики Беларусь об утверждении клинических протоколов 2022
- Постановления и приказы Министерства здравоохранения Республики Беларусь об утверждении клинических протоколов 2022 -
-
www.minzdrav.gov.by
- www.minzdrav.gov.by -
Информация
Приложение 1
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Алгоритм диагностики ВИЧ-инфекции2
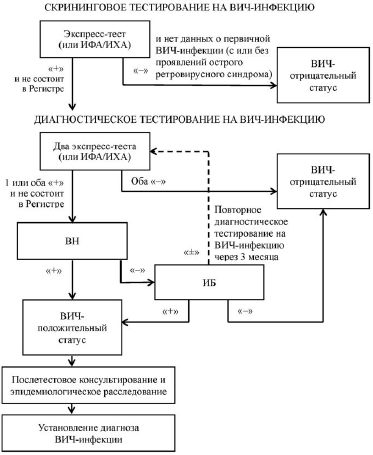
Примечания:

______________________________
2 За исключением ВИЧ-экспонированных детей в возрасте до 18 месяцев, беременных, пациентов с вероятной первичной ВИЧ-инфекцией с проявлениями или без проявлений острого ретровирусного синдрома.
Примечания:
«+» Положительный (реактивный) результат теста.
«–» Отрицательный (нереактивный) результат теста.
«±» Сомнительный (неопределенный) результат теста.
Приложение 2
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Классификация ВИЧ-инфекции у пациентов в возрасте 15 лет и старше
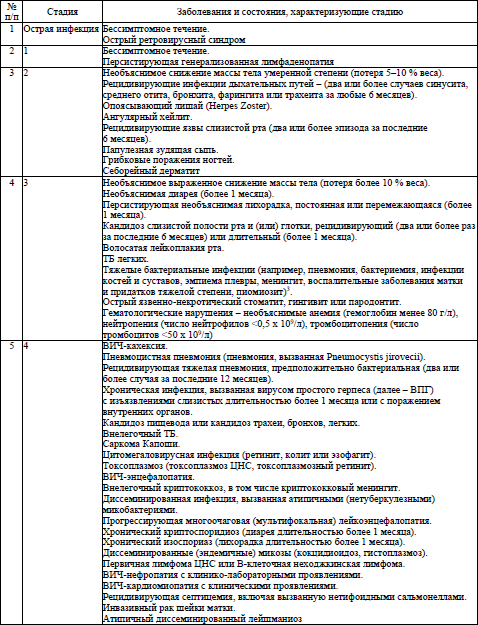
______________________________

______________________________
3 Локальная или системная бактериальная инфекция (абсцесс, флегмона, пиомиозит, сепсис, бактериальный эндокардит), не может быть единственным критерием установления 3 стадии, если любое из перечисленных инфекционных осложнений ассоциировано с внутривенным введением наркотиков.
Приложение 3
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Классификация ВИЧ-инфекции у детей в возрасте до 15 лет

______________________________

______________________________
4 Умеренная недостаточность питания у детей в возрасте до 5 лет устанавливается при соотношении массы тела и роста по шкале Z <2 и (или) при окружности середины плеча от 115 мм до 125 мм. Оценку проводят с использованием программы Anthro, оценка дефицита роста и массы тела возможна также по центильным таблицам.
5 Тяжелая белково-энергетическая недостаточность у детей в возрасте до 5 лет устанавливается при соотношении массы тела и роста по шкале Z <3 и (или) при окружности середины плеча <115 мм, и (или) при наличии отечности. Оценку проводят с использованием программы Anthro, оценка дефицита роста и массы тела возможна также по центильным таблицам.
Приложение 4
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Классификация ВИЧ-ассоциированного иммунодефицита
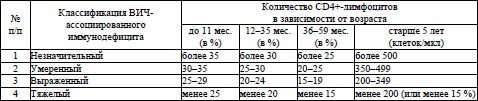
Алгоритм клинического и лабораторного мониторинга состояния здоровья пациентов с ВИЧ-инфекцией
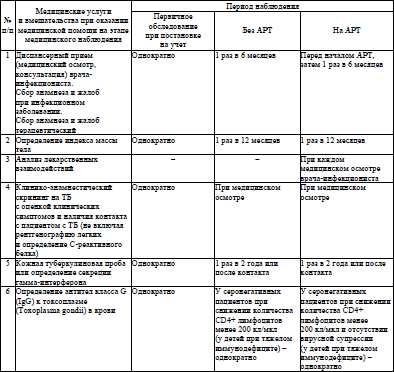
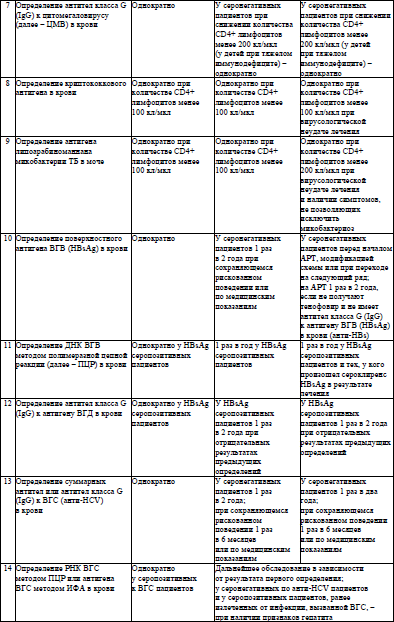
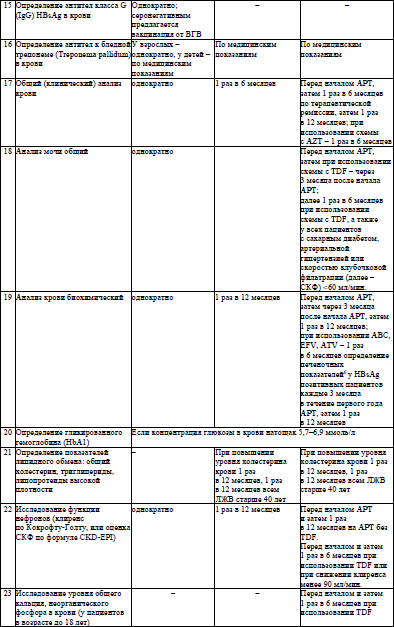
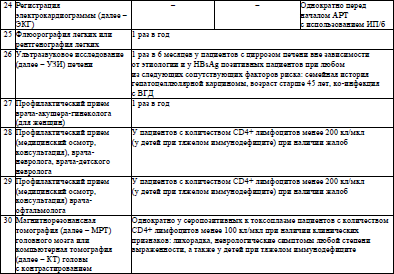
Приложение 6
Основные характеристики и режимы дозирования АРВ-ЛС
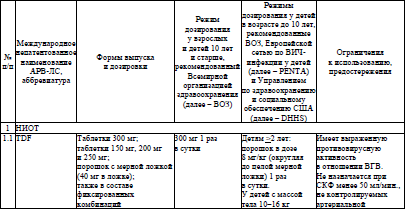
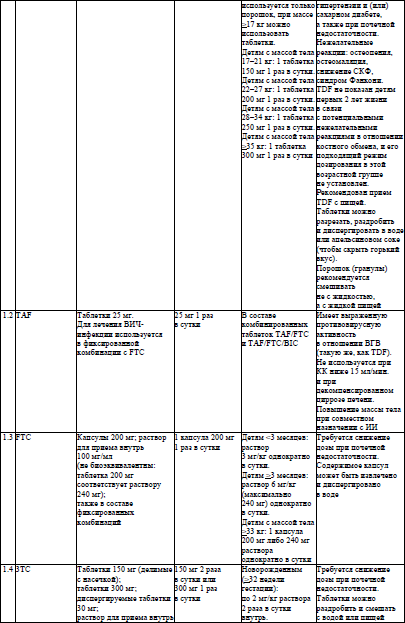
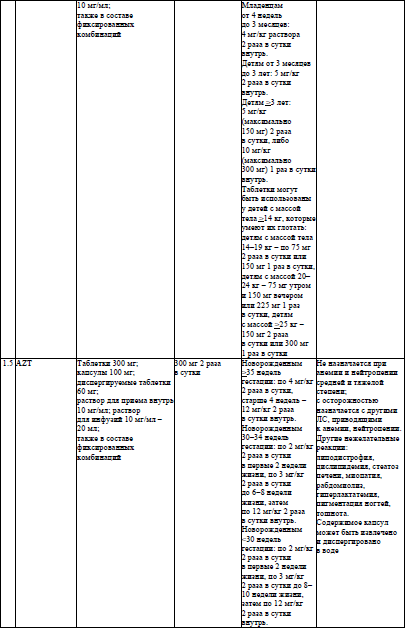
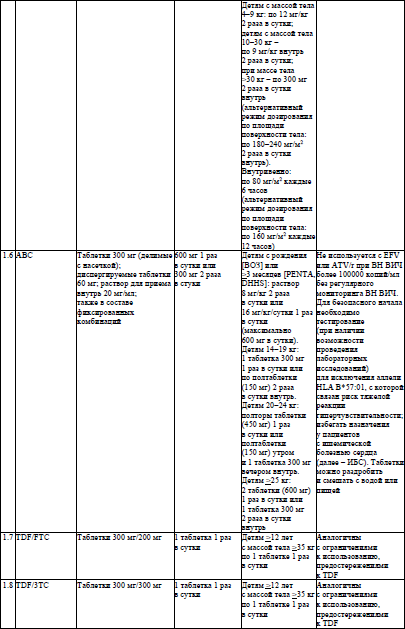
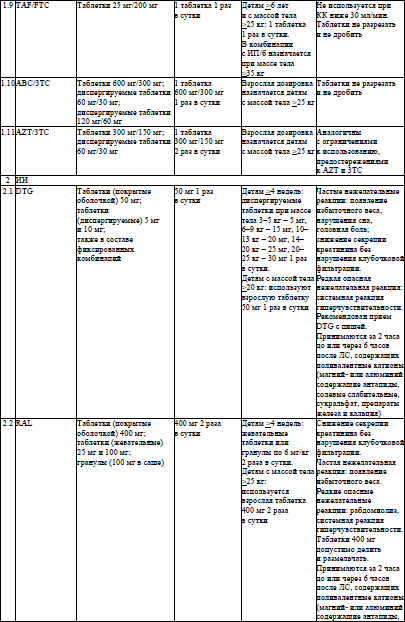
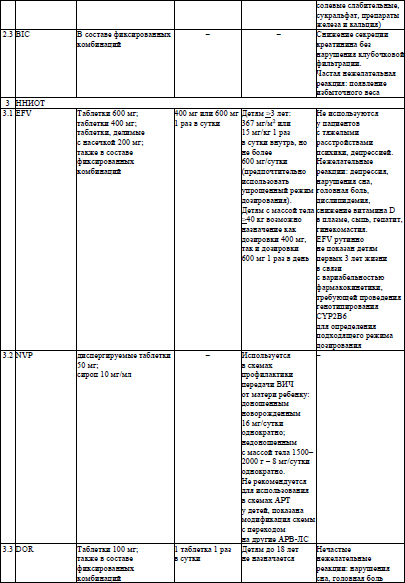
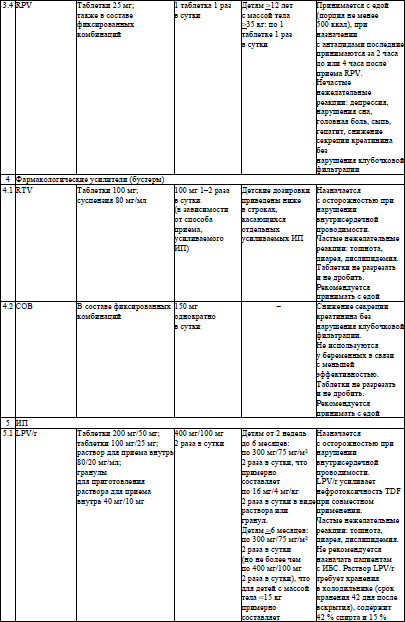
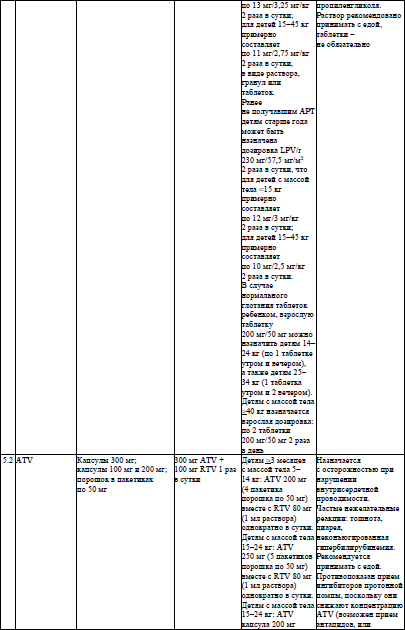
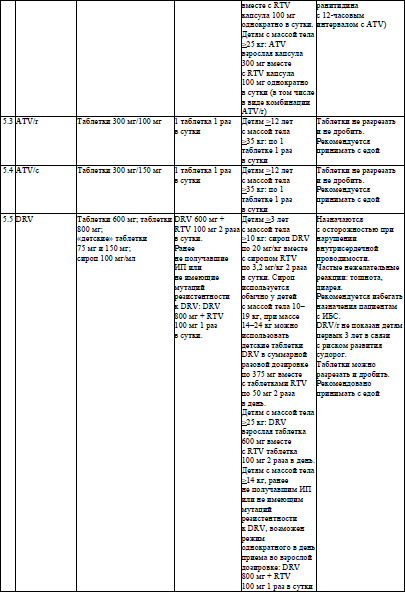
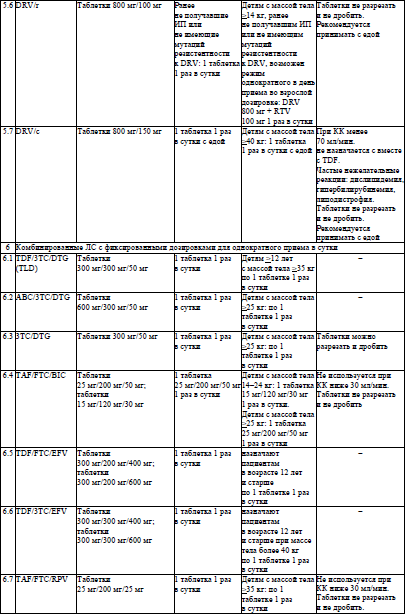

Примечание. TAF, RAL, BIC, DOR, RPV, COB и (или) комбинации с ними назначаются за счет собственных средств, средств юридических лиц и иных источников, не запрещенных законодательством, при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача или лица, его заменяющего, с оформлением записи в медицинских документах.
Приложение 7
Режимы дозирования жидких пероральных форм АРВ-ЛС у детей в возрасте младше 4 недель7
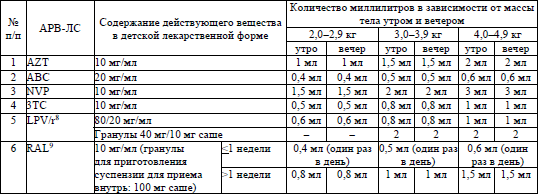
Упрощенные режимы дозирования твердых пероральных форм АРВ-ЛС для приема один раз в день у детей в возрасте 4 недель и старше
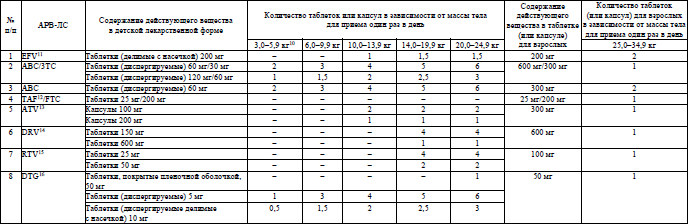
Приложение 9
Упрощенные режимы дозирования твердых и жидких пероральных форм АРВ-ЛС для приема два раза в день у детей в возрасте 4 недель и старше
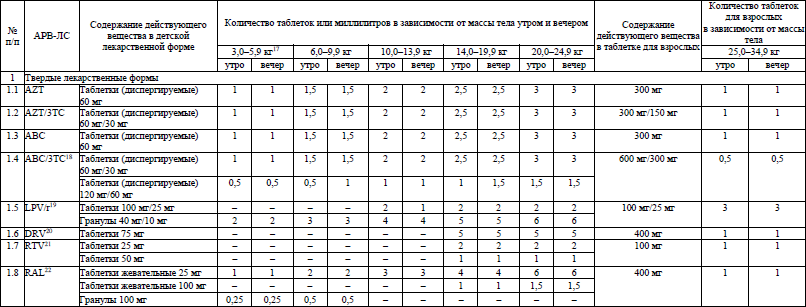
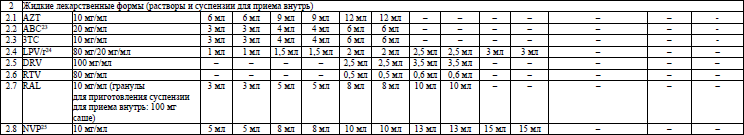

Приложение 5
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Алгоритм клинического и лабораторного мониторинга состояния здоровья пациентов с ВИЧ-инфекцией




______________________________
6 Определение общего и связанного билирубина, аланиновой аминотрансферазы (далее – АЛТ), аспарагиновой аминотрансферазы (далее – АСТ), гаммаглютамилтранспептидазы (далее – ГГТП), щелочной фосфатазы (далее – ЩФ), С-реактивного белка.
Приложение 6
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Основные характеристики и режимы дозирования АРВ-ЛС











Примечание. TAF, RAL, BIC, DOR, RPV, COB и (или) комбинации с ними назначаются за счет собственных средств, средств юридических лиц и иных источников, не запрещенных законодательством, при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача или лица, его заменяющего, с оформлением записи в медицинских документах.
Приложение 7
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Режимы дозирования жидких пероральных форм АРВ-ЛС у детей в возрасте младше 4 недель7

______________________________
7 Данные о фармакокинетике большинства АРВ-ЛС (кроме AZT) у новорожденных ограничены; тем не менее, указанные стандартизованные дозировки для детей первого месяца жизни используются с высокой степенью уверенности, хотя некоторая неопределенность и сохраняется у недоношенных детей и детей с низкой массой при рождении.
8 Раствор LPV/r не назначается новорожденным младше 2 недель, а также недоношенным детям до достижения ими гестационного возраста 42 недель из-за риска метаболических и сердечных нежелательных реакций.
9 Гранулы для приготовления суспензии для приема внутрь RAL используются у новорожденных с массой тела не менее 2 кг, режим приема – один раз в день в течение первой недели жизни и два раза в день после.
Приложение 8
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Упрощенные режимы дозирования твердых пероральных форм АРВ-ЛС для приема один раз в день у детей в возрасте 4 недель и старше

______________________________
10 Указанные дозировки с высокой степенью уверенности используются у детей старше 4 недель жизни с массой тела <3,0 кг, хотя некоторая неопределенность и сохраняется у недоношенных детей и детей с низкой массой при рождении.
11 EFV не рекомендован для детей младше 3 лет и массой тела <10 кг.
12 TAF может быть использован у детей >6 лет с массой тела >25 кг в составе комбинаций с фиксированными дозами TAF/FTC 25 мг/200 мг и TAF/FTC/DTG 25 мг/200 мг/50 мг. Детям с массой тела >35 кг TAF можно назначать в составе комбинации TAF/FTC/RPV и при сочетании TAF/FTC с бустированными ИП.
13 ATV используется у детей в возрасте >3 месяцев в форме порошка, >6 лет – в виде капсул. ATV следует бустировать RTV: детям с массой тела >5 кг, получающим ATV в виде порошка – доза RTV составляет 80 мг (1 мл раствора) однократно в сутки, детям с массой тела >10 кг, получающим ATV в виде капсул – доза RTV составляет стандартную капсулу 100 мг.
14 DRV, бустированный RTV, используется у детей >3 лет; в случае если ранее ИП не использовались – предпочтителен режим однократного в сутки приема.
15 RTV используется в качестве бустера для ATV или DRV или как дополнительный бустер для LPV/r при его одновременном применении с рифампицином.
16 Диспергируемые таблетки DTG и таблетки DTG, покрытые пленочной оболочкой, не являются биоэквивалентными: 30 мг диспергируемой таблетки DTG соответствует 50 мг таблетки, покрытой пленочной оболочкой. Таблетки DTG 50 мг, покрытые пленочной оболочкой, предпочтительны для детей, достигших массы 20 кг (за исключением случаев, когда они не могут проглотить таблетки). Для детей с массой тела >30 кг может быть использовано и является предпочтительным комбинированное ЛС TLD (TDF/3TC/DTG в дозировках 300 мг/300 мг/50 мг). Предпочтительно принимать DTG с пищей, следует избегать приема антацидов/минеральных добавок, содержащих поливалентные катионы, за 6 часов до и через 2 часа после приема.
Приложение 9
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Упрощенные режимы дозирования твердых и жидких пероральных форм АРВ-ЛС для приема два раза в день у детей в возрасте 4 недель и старше


______________________________
17 Указанные дозировки с высокой степенью уверенности используются также у детей старше 4 недель жизни с массой тела <3,0 кг, некоторая неопределенность сохраняется у недоношенных детей и детей с низкой массой тела при рождении.
18 Рекомендуемая дозировка раствора ABC для детей старше 4 недель значимо выше, чем для новорожденных для обеспечения сопоставимости дозы жидкой лекарственной формы и диспергируемых таблеток, и не ведет к повышению токсичности.
19 Термостабильные таблетки LPV/r следует проглатывать целиком, их нельзя делить, дробить или жевать (при том, что таблетка 100 мг/25 мг является достаточно крупной по размеру, и некоторые дети могут иметь затруднения в ее проглатывании). В случае нормального глотания таблеток ребенком, взрослую таблетку 200 мг/50 мг можно назначить уже детям 14–24 кг (по 1 таблетке утром и вечером), а также детям 25–34 кг (1 таблетка утром и 2 вечером).
20 DRV используется у детей >3 лет; назначается вместе с RTV, дозировка RTV для детей с массой тела <15 кг составляет 0,5 мл суспензии 80 мг/мл, для детей с массой тела 15–30 кг составляет 50 мг (таблетки 25 или 50 мг), либо в случае их недоступности – возможно использование взрослой дозировки 100 мг (такое превышение дозировки безопасное и хорошо переносимое).
21 RTV используется только в качестве фармакологического усилителя (бустера) в сочетании с ATV или DRV.
22 У детей в возрасте >4 недель может быть использован RAL как в гранулах, так и размельченные жевательные таблетки: исследования фармакокинетики у младенцев показывают их биоэквивалентность.
23 Рекомендуемая дозировка раствора ABC для детей старше 4 недель значимо выше, чем для новорожденных: это сделано чтобы обеспечить сопоставимость дозы жидкой лекарственной формы и диспергируемых таблеток, и не ведет к повышению токсичности.
24 Раствор LPV/r требует соблюдения холодовой цепи во время транспортировки и хранения. Раствор LPV/r содержит 42,4 % спирта и 15,3 % пропиленгликоля, что может быть значимо при применении у новорожденных и младенцев.
25 NVP не используется в схемах АРТ у детей; ранее NVP назначался детям в разовых дозировках в первые 2 недели приема однократно в сутки, затем переходили на поддерживающий прием 2 раза в день; детям >25 кг назначался NVP во взрослой разовой дозе 200 мг.
Приложение 10
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Схемы АРТ первого ряда
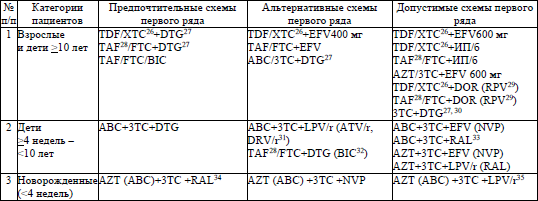
Приложение 11
Схемы АРТ второго ряда

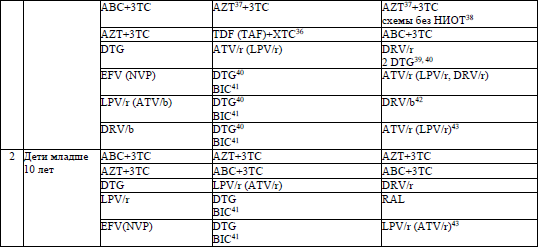
______________________________
Приложение 12
Схемы АРТ третьего ряда
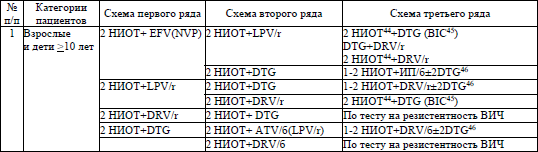

______________________________
Приложение 13
Алгоритм оптимизации схем АРТ у детей при достижении ими соответствующей массы тела
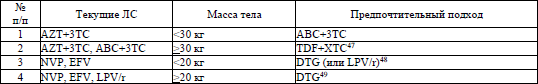
Приложение 15
Алгоритм лабораторного мониторинга ВИЧ-инфекции и эффективности АРТ у пациентов с ВИЧ-инфекцией
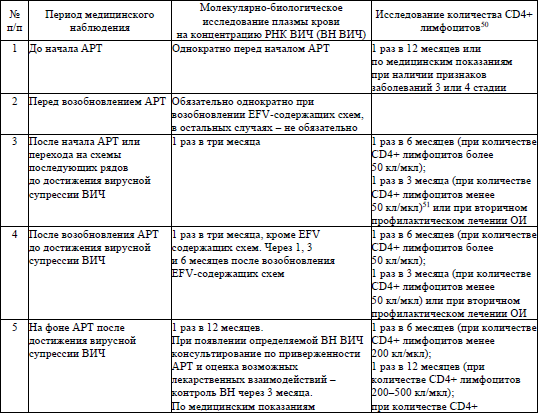

Приложение 16
Схемы АРТ, рекомендованные для использования у беременных

Приложение 17

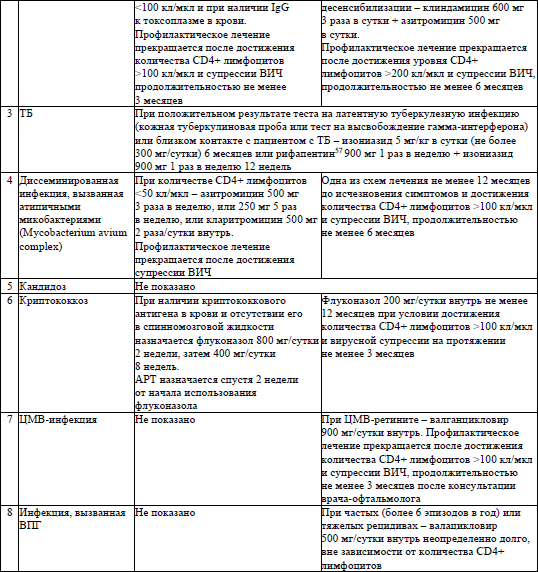
Алгоритм профилактического лечения ОИ у пациентов с ВИЧ-инфекцией младше 18 лет и у ВИЧ-экспонированных детей58
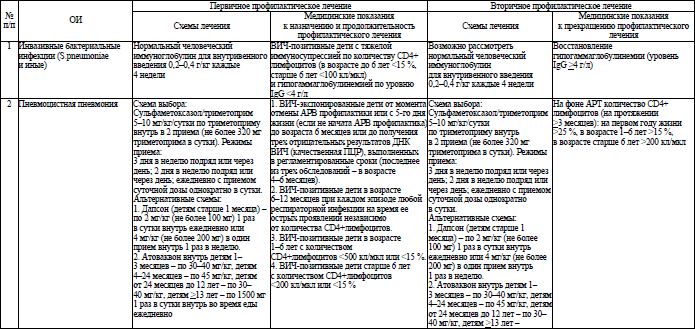
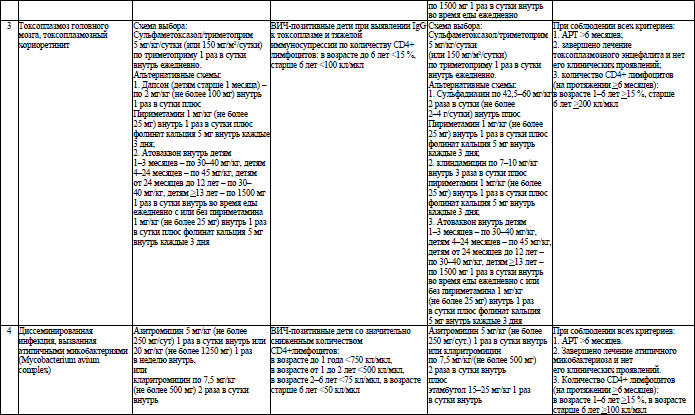
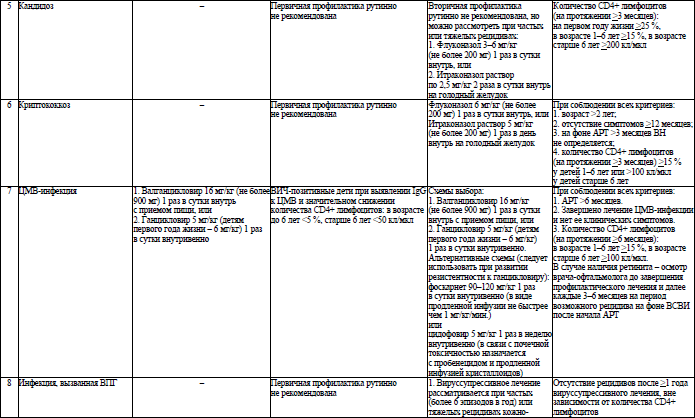
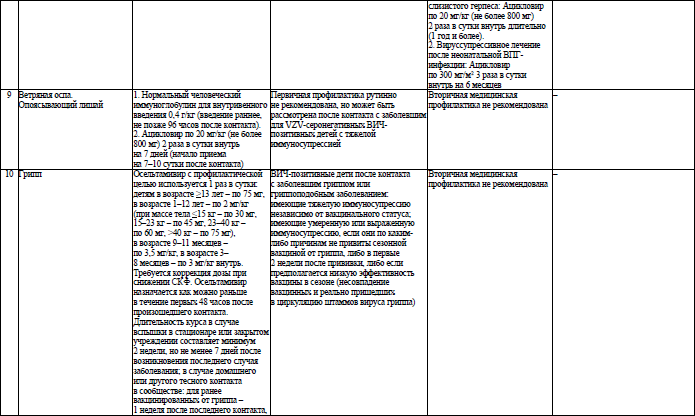

Примечание. Атоваквон, пириметамин, сульфадиазин, фоскарнет, цидофовир, пробенецид назначаются за счет собственных средств, средств юридических лиц и иных источников, не запрещенных законодательством, при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача или лица, его заменяющего, с оформлением записи в медицинских документах.
Приложение 19
Объем медицинской помощи, оказываемой пациентам с ВИЧ-инфекцией при оппортунистических заболеваниях (взрослое население)

______________________________
26 3TC или FTC.
27 DTG может быть назначен женщинам детородного возраста, которые хотят забеременеть или не используют средства контрацепции, если они были проинформированы о возможном, но не доказанном повышении риска дефектов нервной трубки (при зачатии и до конца первого триместра на уровне 0,19 %, что не является статистически значимым). Если у женщины выявляется беременность после первого триместра, следует начать или продолжить прием DTG на протяжении всей беременности.
28 TAF рекомендуется назначать пациентам с установленным остеопорозом, остеопенией и (или) нарушением функции почек, а также при совместном использовании нефротоксичных ЛС. В режимах АРТ без бустера у TDF и TAF в краткосрочной перспективе сравнимое негативное влияние на функцию почек и плотность костной ткани. Использование TAF в схемах с ИИ намного чаще приводит к набору избыточного веса по сравнению с TDF.
29 RPV может быть использован при CD4>200 кл/мкл и ВН ВИЧ <100 000 копий/мл, противопоказан при совместном использовании с антацидами, принимается с калорийной пищей.
30 Схема 3TC+DTG может быть использована у HBsAg-негативных пациентов, при ВН ВИЧ<500 000 копий/мл; не может быть назначена после неудачи ПрЭП, кроме случаев, когда тест на резистентность указывает на сохранение активности 3TC.
31 DRV/r может быть назначен ребенку >3 лет.
32 BIC может быть назначен ребенку >6 лет и веса >25 кг.
33 RAL используются в составе альтернативной схемы, только если твердые лекарственные формы ИП/б (LPV/r, ATV/r или DRV/r) недоступны.
34 Новорожденные, начинающие АРТ по схеме на основе RAL, в кратчайшие сроки переводятся на DTG при наличии соответствующей возрасту лекарственной формы. Для новорожденных с массой тела <2 кг предпочтительная схема включает не RAL, а NVP.
35 Сироп или гранулы LPV/r можно применять с возраста >14 дней.
Приложение 11
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Схемы АРТ второго ряда


______________________________
36 3TC или FTC.
37 При наличии медицинских противопоказаний к использованию AZT и использовании во втором ряду ИИ можно сохранить TDF в НИОТ-основании или перейти на ABC; при использовании ННИОТ, ИП/б а также при длительности использования схемы в условиях вирусологической неудачи лечения >6 месяцев выполняется тест на резистентность ВИЧ для обоснования приемлемости отказа от использования AZT.
38 У пациентов, получавших в схеме первого ряда ННИОТ во втором ряду, может быть использована схема, состоящая из DTG и ИП/б, или DTG+RPV.
39 Удвоенная суточная доза DTG: по таблетке 50 мг (при массе тела <20 кг – в соответствующей разовой дозе) 2 раза в сутки может быть назначен по результатам теста на резистентность ВИЧ у пациентов, не получающих рифампицин или другие ЛС, при совместном использовании с которыми суточную дозу DTG рекомендуется удваивать.
40 DTG может быть назначен взрослым женщинам детородного возраста, которые хотят забеременеть или не используют средства контрацепции, если они были проинформированы о возможном, но не доказанном повышении риска дефектов нервной трубки (при зачатии и до конца первого триместра на уровне 0,19 %, что не является статистически значимым). Если у женщины выявляется беременность после первого триместра, следует начать или продолжить прием DTG на протяжении всей беременности.
41 При условии того, что другие АРВ-ЛС, входящие в комбинированную лекарственную форму с BIC, соответствуют требованиям к замене НИОТ-основания. BIC-содержащие комбинированные схемы доступны для взрослых и для детей с массой тела >14 кг.
42 DRV/b используется только в режиме двукратного приема в сутки (взрослым и детям с массой тела >25 кг – в дозе 600/100 мг 2 раза в сутки).
43 LPV/r или ATV/b может использоваться если они сохранили активность по результатам теста на резистентность ВИЧ.
Приложение 12
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Схемы АРТ третьего ряда


______________________________
44 Из 2 НИОТ в схемах третьего ряда один должен обладать максимальной остаточной активностью по тесту на резистентность ВИЧ (оптимально – быть полностью активным).
45 При условии того, что другие АРВ-ЛС, входящие в комбинированную лекарственную форму с BIC, соответствуют требованиям к замене НИОТ-основания. BIC-содержащие комбинированные схемы доступны для взрослых и для детей с массой тела >14 кг.
46 Удвоенная суточная доза DTG: по таблетке 50 мг (при массе тела <20 кг – в соответствующей разовой дозе) 2 раза в сутки присоединяется к схемам АРТ третьего ряда у пациентов, ранее получавших либо DTG в стандартной дозировке, либо LPV/r (ATV/r) в 1–2 рядах при отсутствии сведений о резистентности ВИЧ.
Приложение 13
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Алгоритм перехода на схему TDF+3TC+DTG у взрослых и детей 10 лет и старше
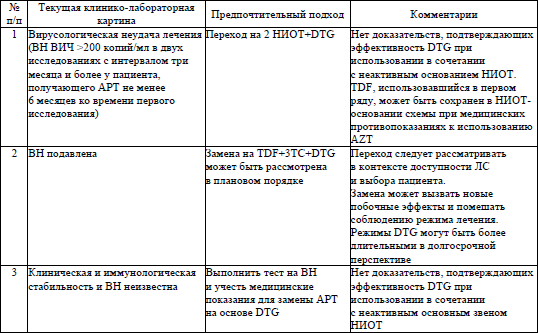
Приложение 14

Приложение 14
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Алгоритм оптимизации схем АРТ у детей при достижении ими соответствующей массы тела

______________________________
47 3TC или FTC.
48 DTG может быть использован у детей в возрасте >4 недель с массой тела >3 кг; в случае недоступности детских лекарственных форм DTG возможен переход на LPV/r.
49 При достижении массы тела 20 кг возможно использование «взрослой» таблетки DTG 50 мг однократно в сутки.
Приложение 15
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Алгоритм лабораторного мониторинга ВИЧ-инфекции и эффективности АРТ у пациентов с ВИЧ-инфекцией


______________________________
50 Включая проведенное при диагностическом тестировании на ВИЧ–инфекцию.
51 У пациентов со стойким отсутствием иммунологического ответа при вирусной супрессии на протяжении более 12 месяцев допустимо осуществлять мониторинг количества CD4+ лимфоцитов 1 раз в 12 месяцев.
Приложение 16
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Схемы АРТ, рекомендованные для использования у беременных

______________________________
52 3TC или FTC.
53 DTG может быть назначен взрослым женщинам детородного возраста, которые хотят забеременеть или не используют средства контрацепции, если они были проинформированы о возможном, но не доказанном повышении риска дефектов нервной трубки (при зачатии и до конца первого триместра на уровне 0,19 %, что не является статистически значимым). Если у женщины выявляется беременность после первого триместра, следует начать или продолжить прием DTG на протяжении всей беременности.
54 TAF не используется у беременных в сроке до 14 недели беременности из-за недостаточности данных о безопасности и эффективности.
55 EFV может быть использован в дозе 600 или 400 мг в любом сроке беременности.
Приложение 17
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Алгоритм профилактического лечения ОИ у пациентов с ВИЧ-инфекцией старше 18 лет


______________________________
56 Снижение количества CD4+лимфоцитов ниже уровня, указанного в таблице, является медицинским показанием для возобновления профилактического лечения у пациентов без вирусной супрессии.
57 Назначается за счет собственных средств, средств юридических лиц и иных источников, не запрещенных законодательством, при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача или лица, его заменяющего, с оформлением записи в медицинских документах.
Приложение 18
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Алгоритм профилактического лечения ОИ у пациентов с ВИЧ-инфекцией младше 18 лет и у ВИЧ-экспонированных детей58





______________________________
58 Лечение ТБ различной локализации у детей, в том числе профилактическое лечение, назначает врач-фтизиатр.
Примечание. Атоваквон, пириметамин, сульфадиазин, фоскарнет, цидофовир, пробенецид назначаются за счет собственных средств, средств юридических лиц и иных источников, не запрещенных законодательством, при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача или лица, его заменяющего, с оформлением записи в медицинских документах.
Приложение 19
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Объем медицинской помощи, оказываемой пациентам с ВИЧ-инфекцией при оппортунистических заболеваниях (взрослое население)
в стационарных условиях
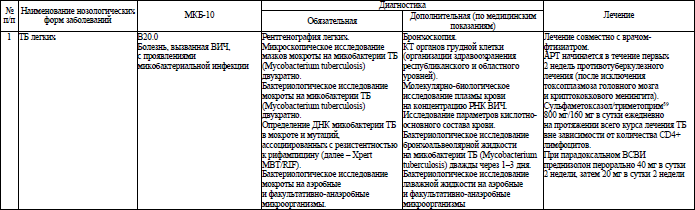
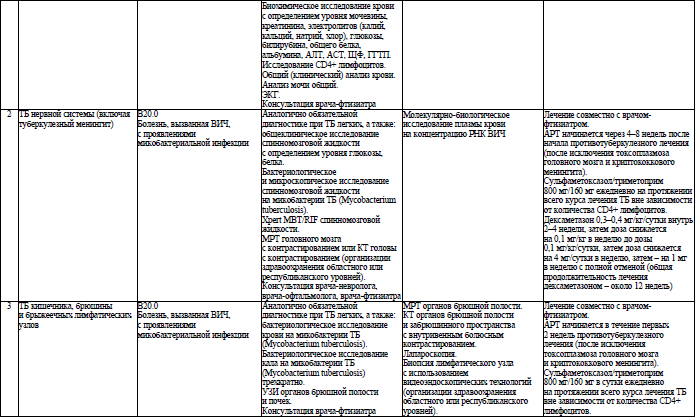
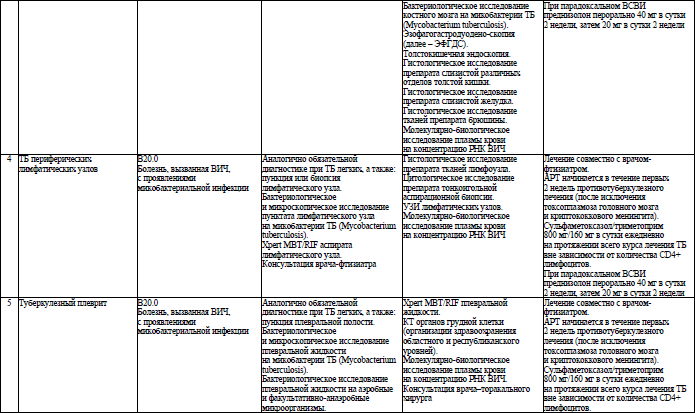
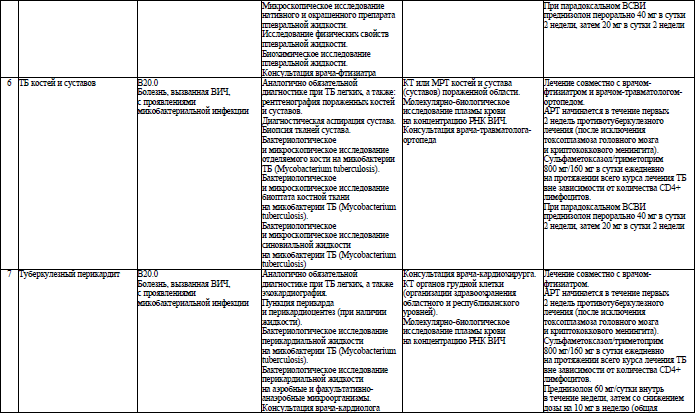
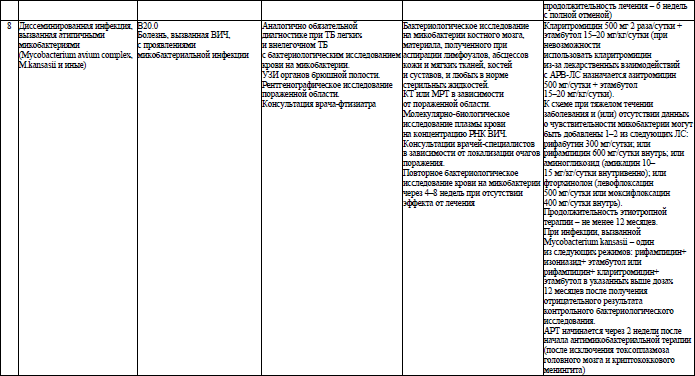
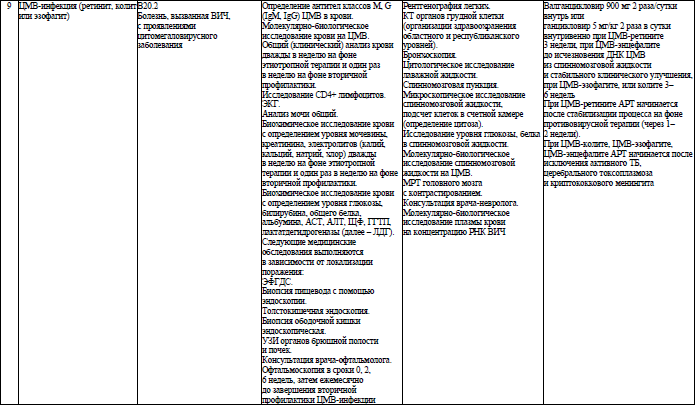
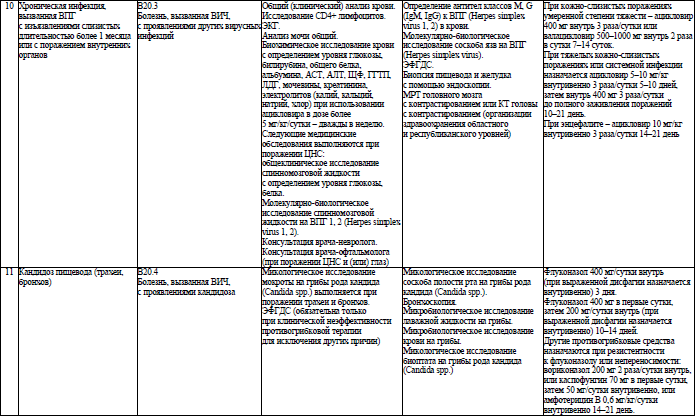
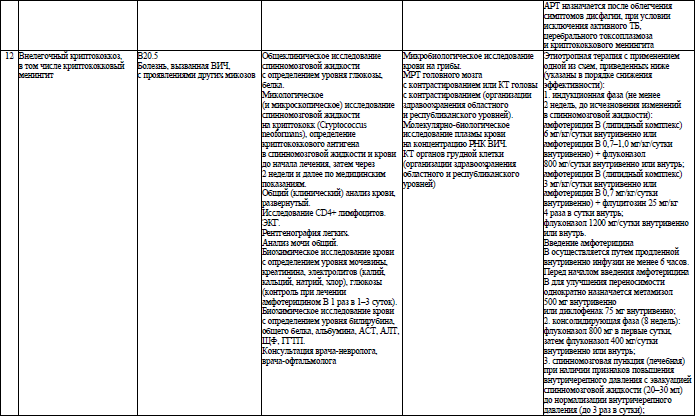
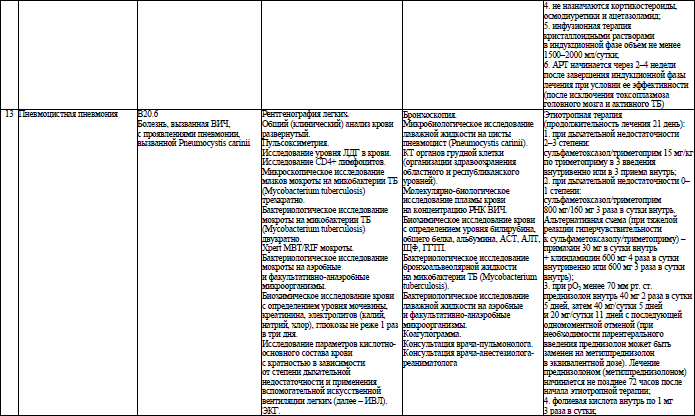
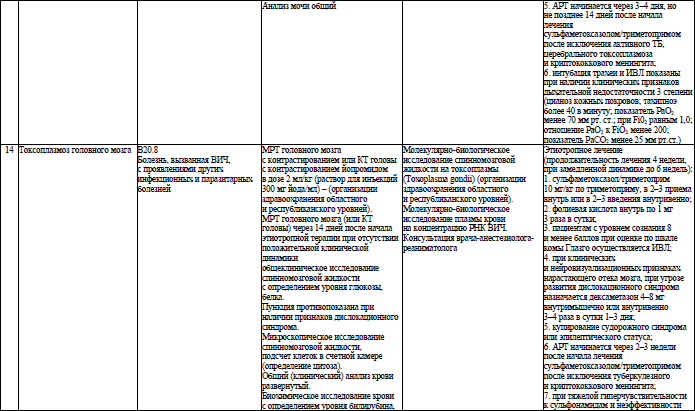
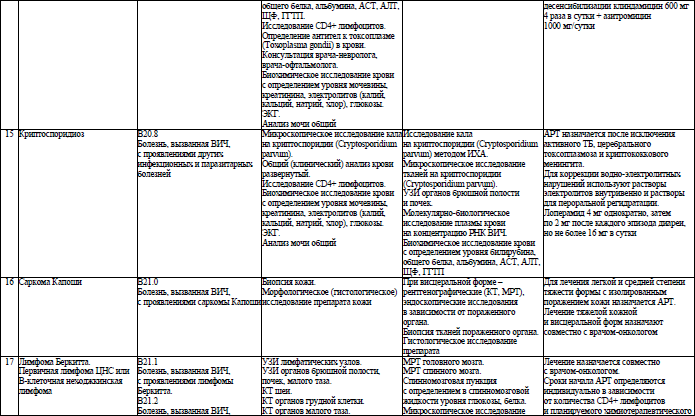
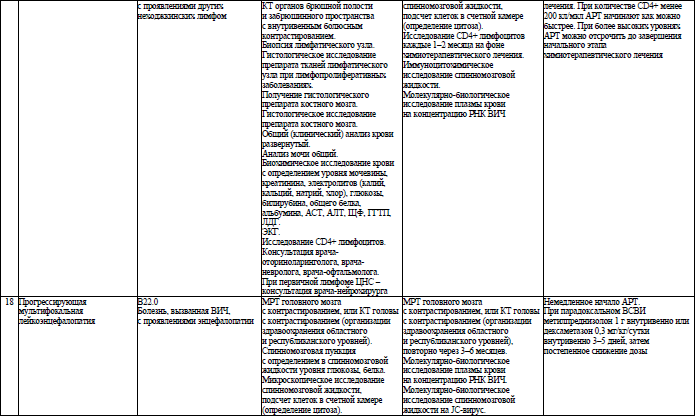
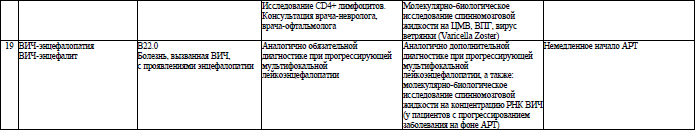
Примечание. Рифабутин, флуцитозин, примахин назначаются за счет собственных средств, средств юридических лиц и иных источников, не запрещенных законодательством, при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача или лица, его заменяющего, с оформлением записи в медицинских документах.
Приложение 20
Объем медицинской помощи, оказываемой пациентам с ВИЧ-инфекцией при оппортунистических заболеваниях (детское население)













______________________________
59 При развитии реакции гиперчувствительности легкой и умеренной степени выраженности к сульфаметоксазолу/триметоприму проводится десенсибилизация.
Примечание. Рифабутин, флуцитозин, примахин назначаются за счет собственных средств, средств юридических лиц и иных источников, не запрещенных законодательством, при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача или лица, его заменяющего, с оформлением записи в медицинских документах.
Приложение 20
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Объем медицинской помощи, оказываемой пациентам с ВИЧ-инфекцией при оппортунистических заболеваниях (детское население)
в стационарных условиях

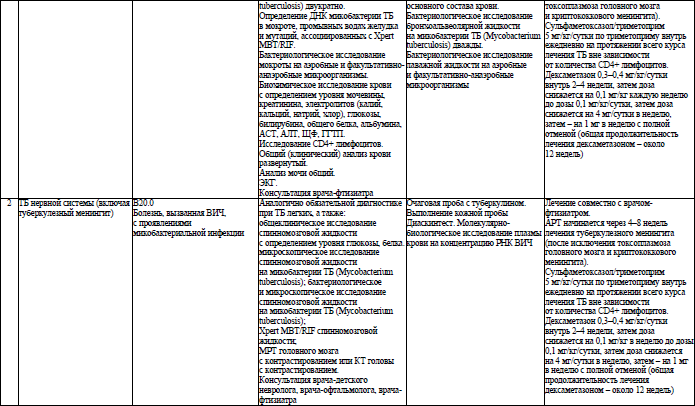
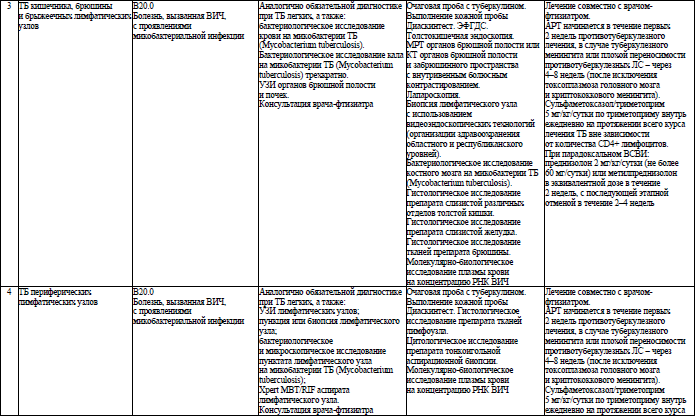
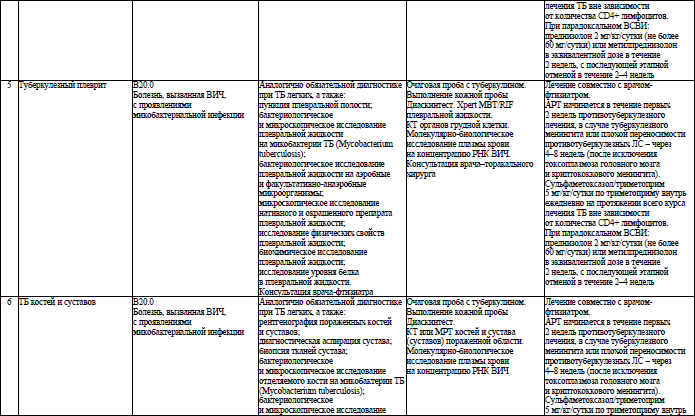
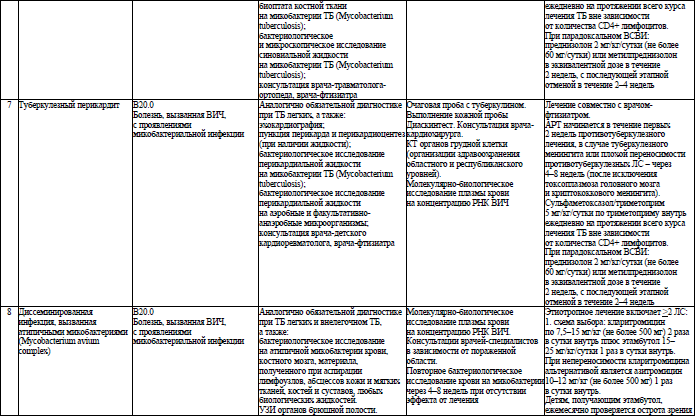
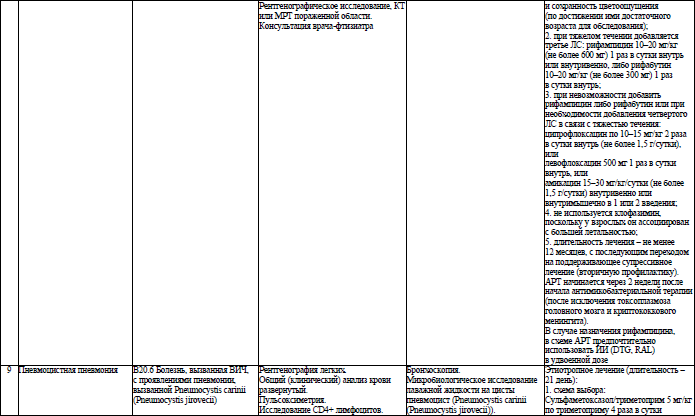
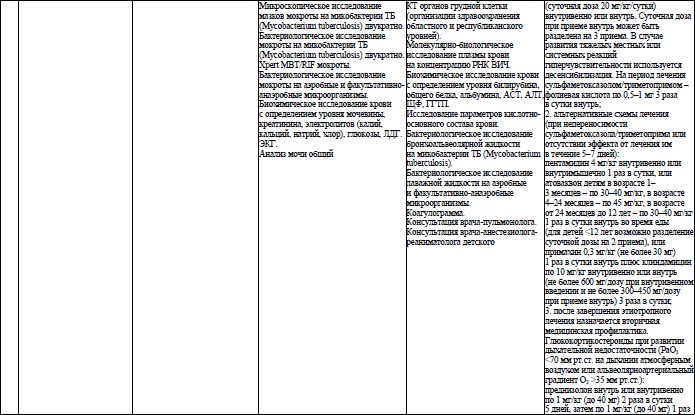
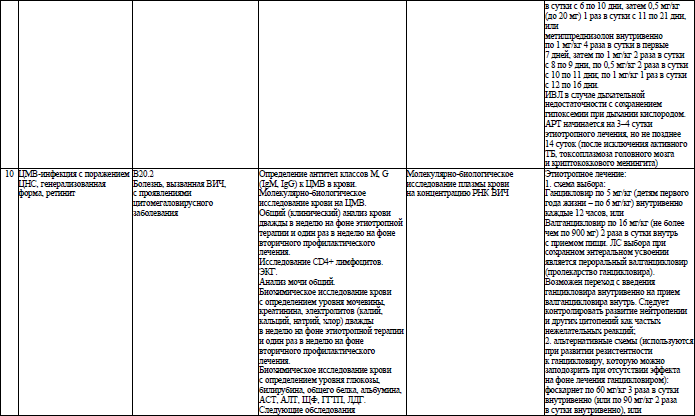
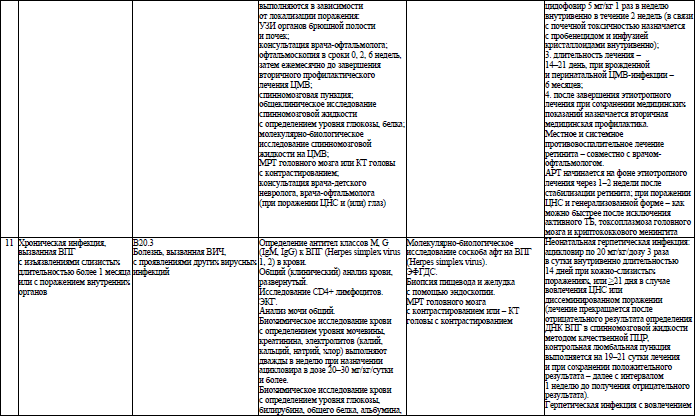

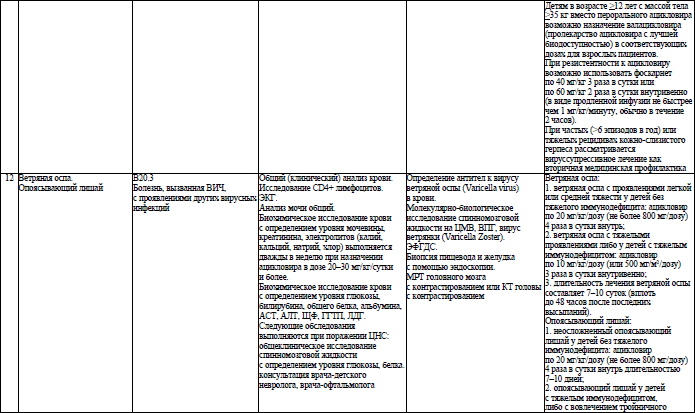
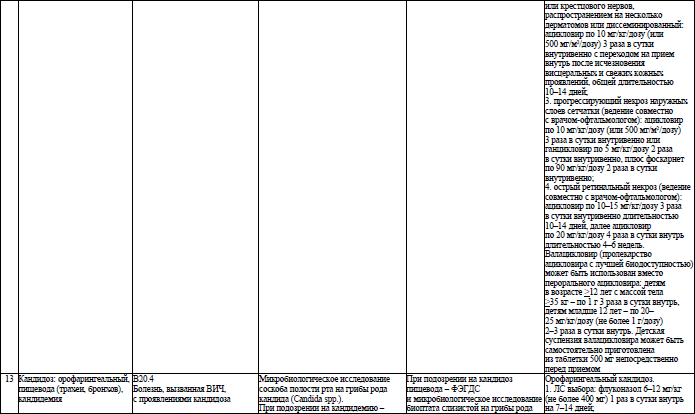
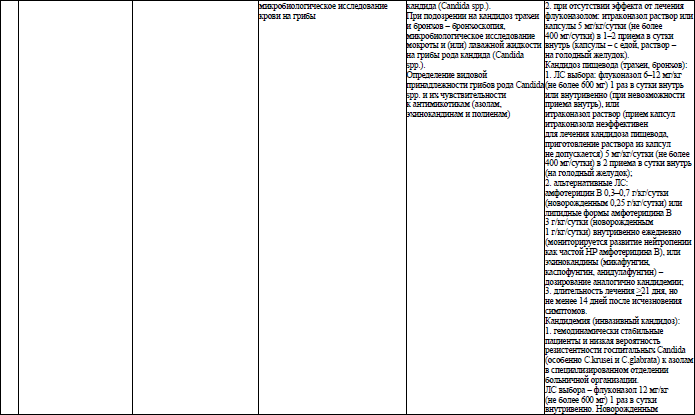


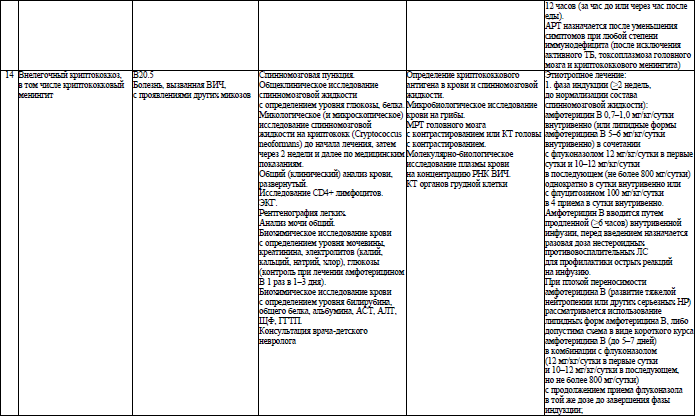
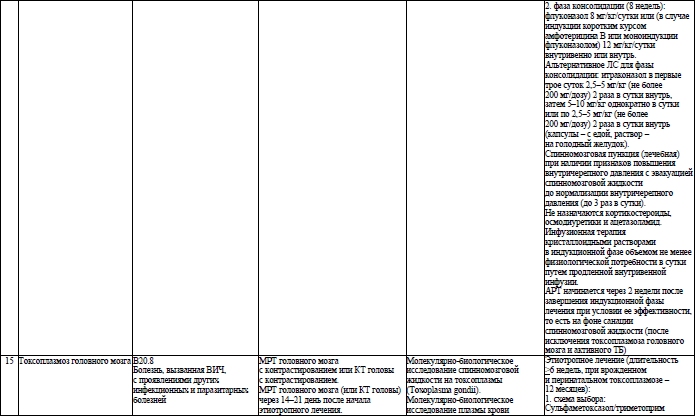
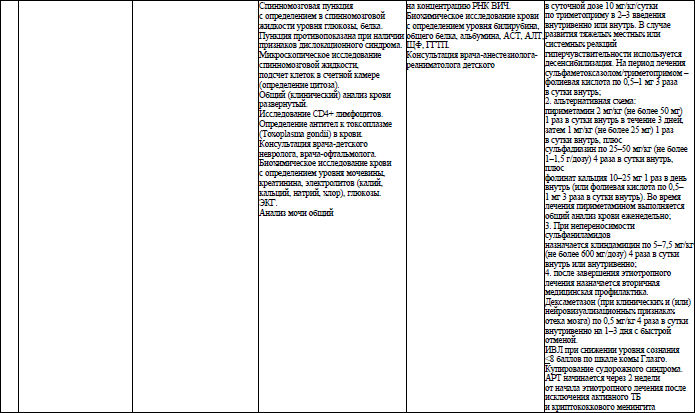
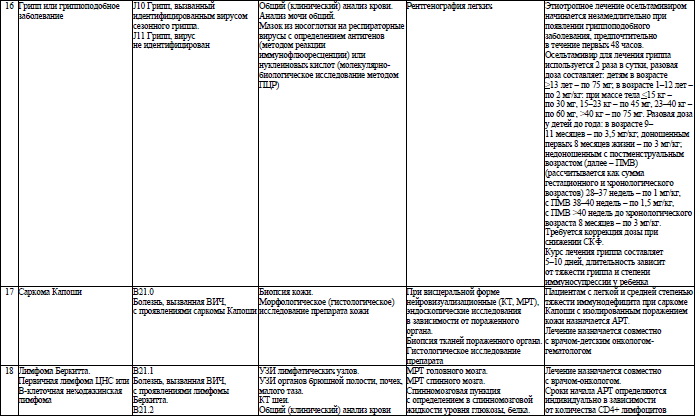
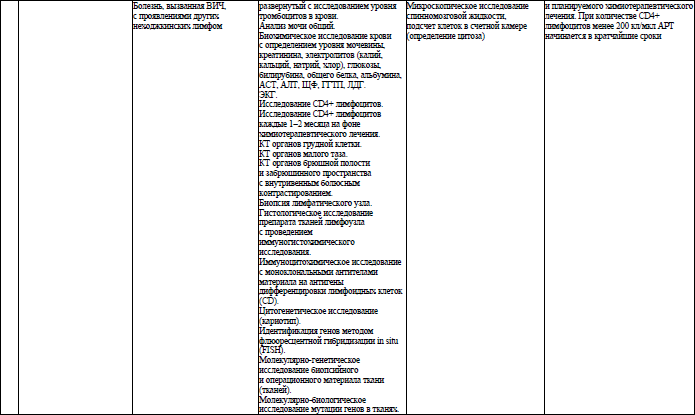

Примечание. Рифабутин, пентамидин, атоваквон, примахин, фоскарнет, цидофовир, пробенецид, флуцитозин, пириметамин, сульфадиазин назначаются за счет собственных средств, средств юридических лиц и иных источников, не запрещенных законодательством, при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача или лица, его заменяющего, с оформлением записи в медицинских документах.
Схемы десенсибилизации к сульфаметоксазолу/триметоприму60
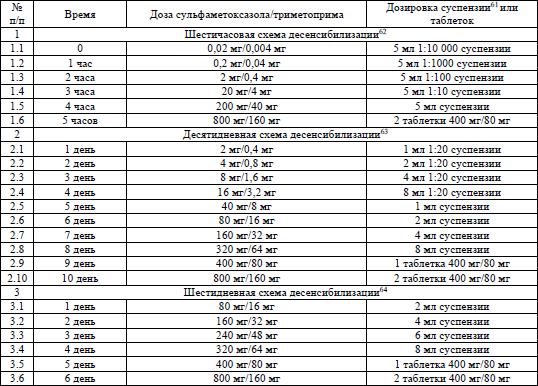
Выбор продолжительности схемы десенсибилизации проводится в зависимости от остроты клинической ситуации.
Во всех случаях десенсибилизация проводится путем приема сульфаметоксазола/триметоприма внутрь.
61 Суспензия сульфаметоксазола/триметоприма содержит в 5 мл 200 мг сульфаметоксазола и 40 мг триметоприма. Разведение суспензии проводится с помощью добавления соответствующего количества воды.
62 Быстрая шестичасовая схема десенсибилизации показана при развитии реакций гиперчувствительности в период проведения основного курса лечения пневмоцистной пневмонии или токсоплазмоза мозга, или при необходимости начать этот курс у пациентов с аллергией на сульфонамиды в анамнезе.
63 Десятидневная схема используется на этапе проведения профилактического лечения (первичного или вторичного).
64 Шестидневная схема является сокращенным вариантом десятидневной схемы.





















Примечание. Рифабутин, пентамидин, атоваквон, примахин, фоскарнет, цидофовир, пробенецид, флуцитозин, пириметамин, сульфадиазин назначаются за счет собственных средств, средств юридических лиц и иных источников, не запрещенных законодательством, при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача или лица, его заменяющего, с оформлением записи в медицинских документах.
Приложение 21
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Схемы десенсибилизации к сульфаметоксазолу/триметоприму60

______________________________
60 Тактика использования сульфаметоксазола/триметоприма при развитии реакций гиперчувствительности зависит от тяжести клинических проявлений:
при легких проявлениях в виде эритематозной сыпи и зудом, но без мокнутия и лихорадки, прием сульфаметоксазола/триметоприма продолжается под наблюдением врача-специалиста, и назначаются антигистаминные ЛС;
при появлении везикулезной сыпи, изъязвлении слизистых и (или) присоединении лихорадки прием сульфаметоксазола/триметоприма прекращается до исчезновения всех проявлений реакции гиперчувствительности (обычно до 2 недель) и затем возобновляется под наблюдением врача-специалиста, или проводится десенсибилизация к ЛС;
при развитии эксфолиативного дерматита, синдрома Стивенса-Джонсона, многоформной экссудативной эритемы сульфаметоксазол/триметоприм отменяется без последующего возобновления его приема.
Выбор продолжительности схемы десенсибилизации проводится в зависимости от остроты клинической ситуации.
Во всех случаях десенсибилизация проводится путем приема сульфаметоксазола/триметоприма внутрь.
61 Суспензия сульфаметоксазола/триметоприма содержит в 5 мл 200 мг сульфаметоксазола и 40 мг триметоприма. Разведение суспензии проводится с помощью добавления соответствующего количества воды.
62 Быстрая шестичасовая схема десенсибилизации показана при развитии реакций гиперчувствительности в период проведения основного курса лечения пневмоцистной пневмонии или токсоплазмоза мозга, или при необходимости начать этот курс у пациентов с аллергией на сульфонамиды в анамнезе.
63 Десятидневная схема используется на этапе проведения профилактического лечения (первичного или вторичного).
64 Шестидневная схема является сокращенным вариантом десятидневной схемы.
Приложение 22
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Алгоритм скрининга на активный ТБ у ЛЖВ
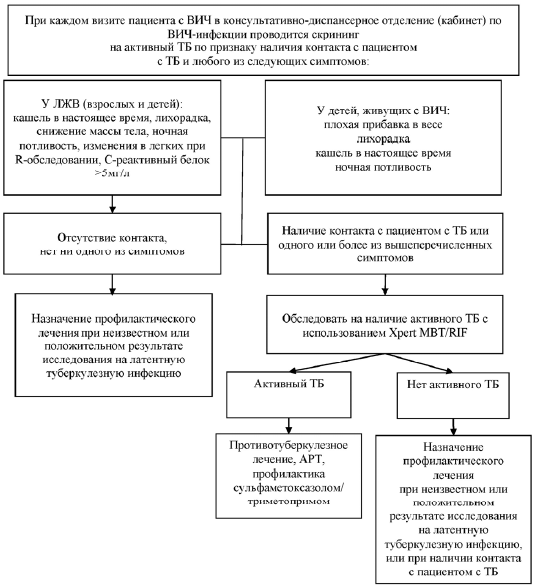

Приложение 23
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Схемы АРТ у пациентов, получающих лечение ТБ с использованием рифампицина

Приложение 24

______________________________
65 TDF может быть заменен на TAF у детей 12 лет и старше.
66 3TC или FTC.
67 Удвоенная суточная доза DTG: по таблетке 50 мг (при массе тела <20 кг – в соответствующей разовой дозе) 2 раза в сутки, использование DTG в этой дозе продолжается еще две недели после отмены рифампицина.
68 EFV используется в дозе 400 или 600 мг 1 раз в день.
69 RAL используется в удвоенной дозе – 12 мг/кг два раза в день – у детей в возрасте от 4 недель до 12 лет, использование RAL в этой дозе продолжается еще две недели после отмены рифампицина.
70 LPV/r используется в удвоенной дозе. LPV/r может быть выбран в качестве альтернативы только у детей, имевших неудачу лечения с использованием DTG или в качестве предпочтительного ЛС у детей <4 недель или с массой тела <3 кг. Другие ИП/б совместно с рифампицином не используются.
Приложение 24
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Схемы АРТ у пациентов, получающих лечение лекарственно-устойчивого ТБ
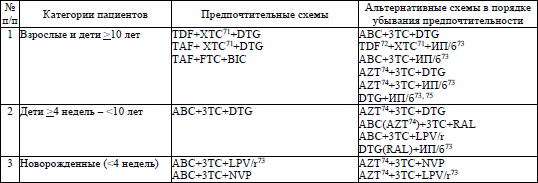
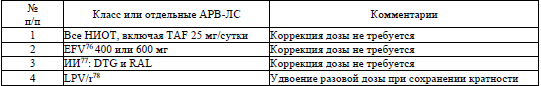
Приложение 26
Лекарственные взаимодействия ЛС ППД для лечения инфекции, вызванной ВГС, и АРВ-ЛС
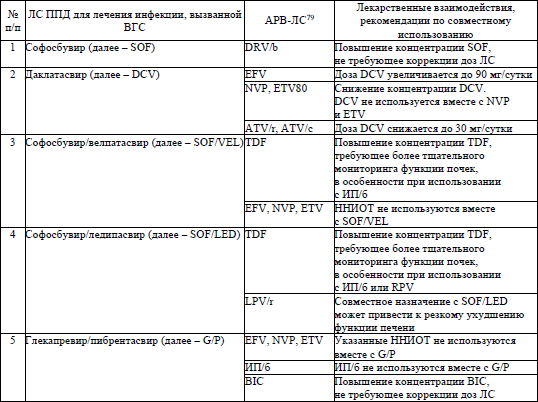

Приложение 27
Коррекция дозы АРВ-ЛС у пациентов с нарушением функции печени
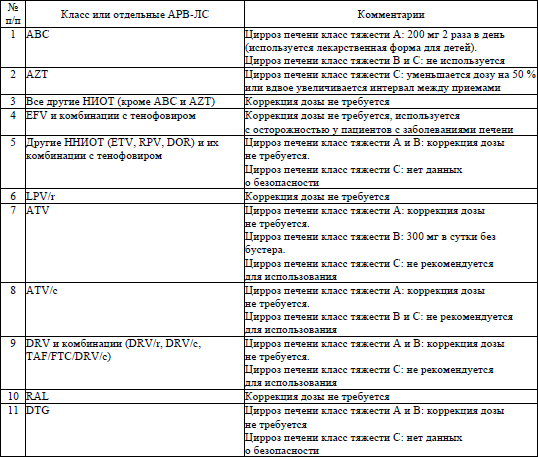

Коррекция дозы АРВ-ЛС у пациентов с нарушением функции почек
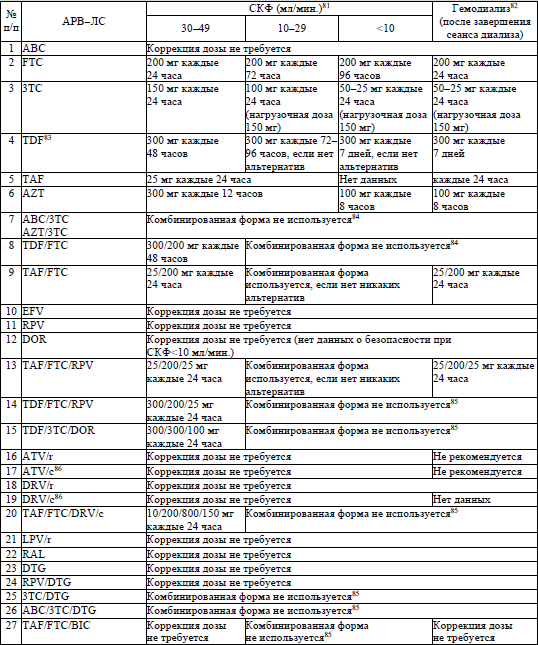
Приложение 29
Форма
Опросник для выявления расстройств, обусловленных употреблением алкоголя (AUDIT)
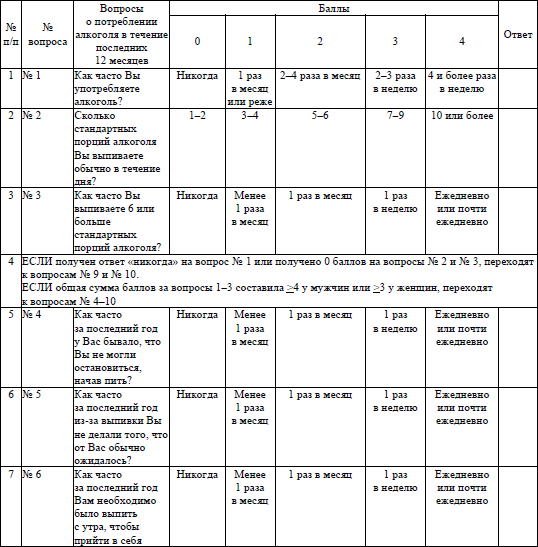
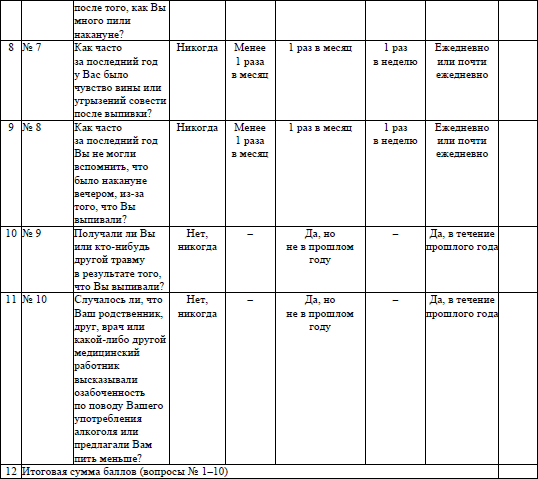
Форма
Опросник для выявления ГТР (ГТР-2, ГТР-7)
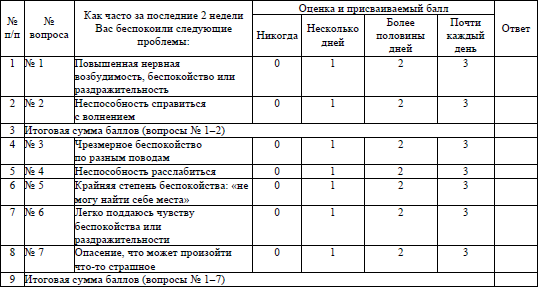
Примечания:
Приложение 31
Форма
Опросник здоровья пациента (PHQ-2, PHQ-9) для выявления депрессии
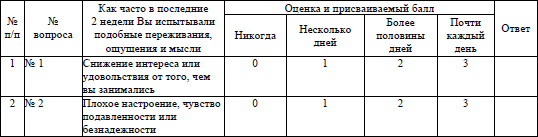
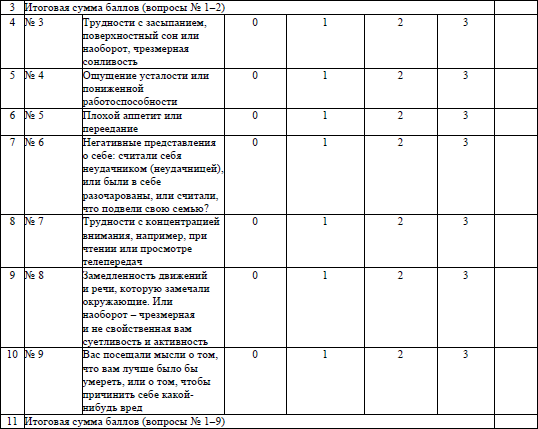

______________________________
71 3TC или FTC.
72 TDF может быть заменен на TAF у детей 12 лет и старше.
73 Все ИП/б, включая LPV/r, повышают концентрации бедаквилина и деламанида, что может привести к кумулятивному эффекту в отношении удлинения интервала QT на ЭКГ; пациенты, получающие это сочетание ЛС, должны находиться под строгим медицинским наблюдением.
74 AZT используется в сочетании с линезолидом только при отсутствии других вариантов лечения и под строгим контролем уровня гемоглобина и эритроцитов.
75 Комбинация ИИ и ИП/б используется только при невозможности подобрать эффективное НИОТ-основание.
Приложение 25
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
АРВ-ЛС, используемые в схемах АРТ у пациентов, получающих профилактическое лечение ТБ с применением схемы рифапентин 900 мг + изониазид 900 мг один раз в неделю

______________________________
76 Другие ННИОТ (NVP, RPV, DOR, этравирин (далее – ETV)) не используются с рифапентином.
77 BIC не используется с рифапентином, RAL возможно использовать с профилактическим еженедельным приемом рифапентина.
78 Другие ИП/б не используются с рифапентином.
Приложение 26
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Лекарственные взаимодействия ЛС ППД для лечения инфекции, вызванной ВГС, и АРВ-ЛС


______________________________
79 АРВ-ЛС ABC, 3TC, FTC, AZT не имеют значимых лекарственных взаимодействий.
80 Назначается за счет собственных средств, средств юридических лиц и иных источников, не запрещенных законодательством, при наличии медицинских показаний (по жизненным показаниям, с учетом индивидуальной непереносимости) по решению врачебного консилиума, а при невозможности его проведения – лечащего врача или лица, его заменяющего, с оформлением записи в медицинских документах.
Приложение 27
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Коррекция дозы АРВ-ЛС у пациентов с нарушением функции печени


Приложение 28
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Коррекция дозы АРВ-ЛС у пациентов с нарушением функции почек

______________________________
81 Для определения СКФ предпочтительно использовать формулу CKD-EPI, в качестве альтернативы могут быть использованы формулы Кокрофта-Голта или aMDRD.
82 Для продленного амбулаторного перитонеального диализа могут быть использованы те же дозы АРВ-ЛС, что и для гемодиализа.
83 TDF при совместном использовании с ИП, в особенности бустированными, проявляет более выраженную нефротоксичность, необходимо избегать этой комбинации у пациентов с хронической болезнью почек, риском хронической болезни почек и (или) снижением СКФ.
84 Там, где не используется комбинированная форма, возможно использование индивидуальных ЛС, входящих в ее состав с соответствующей коррекцией дозы.
85 Там, где не используется комбинированная форма, возможно использование индивидуальных ЛС, входящих в ее состав с соответствующей коррекцией дозы.
86 ATV/c и DRV/c не назначают с вместе с TDF при СКФ <70 мл/мин.
Приложение 29
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Форма
Опросник для выявления расстройств, обусловленных употреблением алкоголя (AUDIT)


Примечания:
1. Стандартная порция алкоголя – это 10 граммов чистого спирта; ориентировочные значения для разных алкогольных напитков с учетом крепости и тары: банка пива 0,5 л 5 % – 2 стандартных порции, бутылка сухого вина 750 мл 12 % – 7 стандартных порций, бутылка крепкого алкоголя (водка, виски, коньяк) 500 мл 40 % – 16 стандартных порций.
2. Интерпретация результатов теста AUDIT:
>8 баллов у мужчин или >7 баллов у женщин указывает на высокую вероятность опасного или вредоносного употребления алкоголя;
>8 баллов у мужчин или >7 баллов у женщин указывает на высокую вероятность опасного или вредоносного употребления алкоголя;
>20 баллов указывает на возможную алкогольную зависимость и необходимость специализированного лечения.
Приложение 30
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Форма
Опросник для выявления ГТР (ГТР-2, ГТР-7)

Примечания:
1. Интерпретация результатов теста ГТР-2 по ответам на первые два вопроса: сумма >3 баллов позволяет считать ГТР вероятным и требует дальнейшего обследования.
2. Интерпретация результатов теста ГТР-7:
сумма >8 баллов позволяет считать ГТР возможным;
0–4 балла соответствует минимальному уровню тревожности;
5–9 баллов – умеренному уровню тревожности;
10–14 баллов – среднему уровню тревожности;
15–21 балл – высокому уровню тревожности.
Приложение 31
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Форма
Опросник здоровья пациента (PHQ-2, PHQ-9) для выявления депрессии


Примечания:
1. Интерпретация результатов теста на выявление наличия депрессии PHQ-2 по ответам на первые два вопроса:
сумма >3 баллов позволяет считать наличие депрессии вероятным, требует дальнейшего обследования с продолжением выполнения теста PHQ-9.
2. Интерпретация результатов теста на наличие депрессии PHQ-9:
при сумме баллов 5–9 речь идет о легкой депрессии, необходимо проведение консультации, ориентированной на выявлении существующих проблем, рекомендаций по увеличению физической активности и сбалансированному питанию, повторное тестирование PHQ-9 при следующем медицинском осмотре;
сумма >10 баллов указывают на возможность большого депрессивного расстройства, рекомендована замена EFV в схеме АРТ;
10–14 баллов говорят об умеренной депрессии и предполагают возможности использования антидепрессантов любым врачом-специалистом с учетом потенциальных лекарственных взаимодействий;
15–19 баллов говорят об умеренно тяжелом, а 20–27 – о тяжелом депрессивном расстройстве и требуют привлечения специалиста по психическому здоровью с назначением лечения;
пациент, ответивший утвердительно на девятый вопрос, нуждается в дальнейшей оценке суицидального риска.
Приложение 32
к клиническому протоколу
«Оказание медицинской помощи
пациентам с ВИЧ-инфекцией»
Схемы АРВ-ЛС, используемые для ПЭП ВИЧ-инфекции
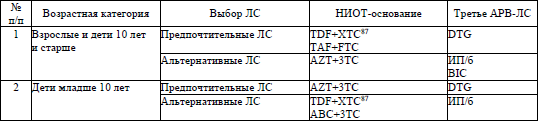

______________________________
87 3TC или FTC.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.