Некротизирующий энтероколит новорожденных
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Некротизирующий энтероколит у плода и новорожденного (P77)
Неонатология, Педиатрия
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «28» июля 2023 года
Протокол №185
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
НЕКРОТИЗИРУЮЩИЙ ЭНТЕРОКОЛИТ НОВОРОЖДЕННЫХ
Некротизирующий энтероколит – неспецифическое воспалительное заболевание неустановленной этиологии с мультифакторным патогенезом, объясняющим развитие НЭК как результат гипоперфузии незрелой слизистой кишечника новорожденного, перенесшего перинатальную гипоксию и, как следствие, изменение кровотока в системе мезентериальных сосудов [1].
Частота выявления в среднем 1 – 5 : 1000 живорожденных детей, среди них 80-90% составляют недоношенные дети и дети с низкой массой тела при рождении (менее 2500 г) [2]. До 7% пациентов с массой тела при рождении от 500 до 1500 г и менее 32 недель гестации переносят НЭК [2,3]. Хирургические стадии НЭК встречаются в среднем у 50% заболевших детей [2,4]. Уровень смертности широко варьирует от 20 до 30%, в группе детей, перенесших хирургическое вмешательство - до 50% [5,6].
ВВОДНАЯ ЧАСТЬ
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «28» июля 2023 года
Протокол №185
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
НЕКРОТИЗИРУЮЩИЙ ЭНТЕРОКОЛИТ НОВОРОЖДЕННЫХ
Некротизирующий энтероколит – неспецифическое воспалительное заболевание неустановленной этиологии с мультифакторным патогенезом, объясняющим развитие НЭК как результат гипоперфузии незрелой слизистой кишечника новорожденного, перенесшего перинатальную гипоксию и, как следствие, изменение кровотока в системе мезентериальных сосудов [1].
Частота выявления в среднем 1 – 5 : 1000 живорожденных детей, среди них 80-90% составляют недоношенные дети и дети с низкой массой тела при рождении (менее 2500 г) [2]. До 7% пациентов с массой тела при рождении от 500 до 1500 г и менее 32 недель гестации переносят НЭК [2,3]. Хирургические стадии НЭК встречаются в среднем у 50% заболевших детей [2,4]. Уровень смертности широко варьирует от 20 до 30%, в группе детей, перенесших хирургическое вмешательство - до 50% [5,6].
ВВОДНАЯ ЧАСТЬ
Код(ы) МКБ-10:

Дата разработки/пересмотра протокола: 2014 год (пересмотр 2021 г./2023 г.).
Пользователи протокола: неонатологи, детские анестезиологи-реаниматологи, детские хирурги.
Категория пациентов: новорожденные.
Категория пациентов: новорожденные.
Шкала уровня доказательности:

Классификация
Клиническая классификация:
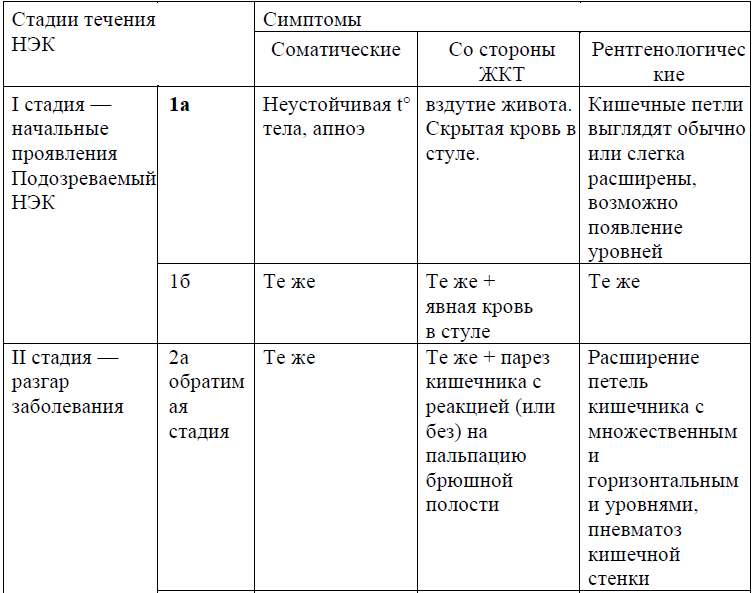
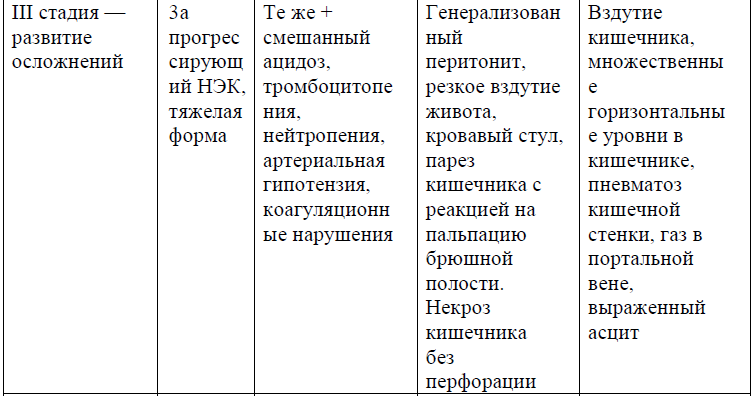
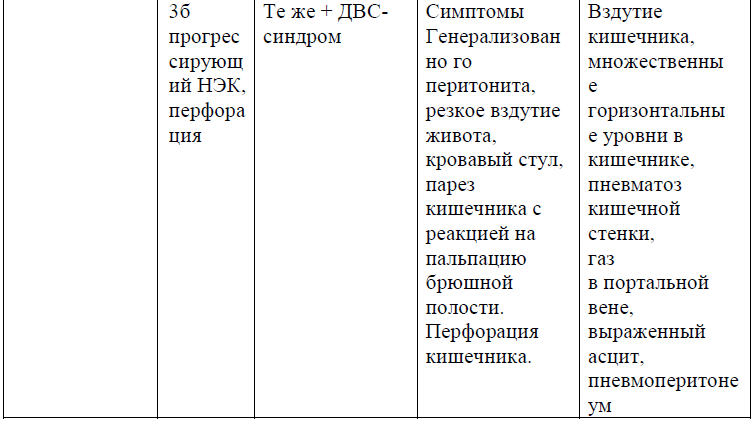
Клинико - рентгенологическая классификация в модификации.
В настоящее время активно применяется классификация НЭК по стадиям течения, предложенная J.M. Bell и соавт. (1978) [7], в модификации М. С. Walsh and R.M. Kliegman (1987) [8].

Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ.
Диагностические критерии: клиническая картина варьирует в широких пределах, состояние ребенка может ухудшиться внезапно или же клиническая картина некротизирующего энтероколита может нарастать в течение нескольких дней. Необходимо рассмотреть вероятность развития некротизирующего энтероколита при наличии следующих симптомов и признаков [9-14].
Жалобы:
• отказ и непереносимость энтерального питания;
• вздутие живота;
• наличие крови в стуле;
• отсутствие стула;
• срыгивание (с примесью или без желчи).
Анамнез (наличие факторов риска) [15-19]:
• гестационный возраст: недоношенность;
• новорожденные <30 недель: некротизирующий энтероколит часто происходит при отсутствии явных нарушений кровообращений кишечника;
• нарушение кровотока: антенатально диагностированный обратный кровоток в пупочной артерии или отсутствие этого кровотока;
• энтеральное питание - молочными смесями;
• врожденные пороки сердца;
• интранатальная асфиксия тяжелая и средней тяжести;
• клинико-анамнестические данные, свидетельствующие о повышенном риске развития бактериальной инфекции у плода и новорожденного []:
Специфичные:
• вздутие живота, сопровождающееся болезненностью;
• отек передней стенки живота;
• отсутствие или снижение перистальтики;
• аспират из желудка с желчью;
• наличие крови в стуле.
• вздутие живота, сопровождающееся болезненностью;
• отек передней стенки живота;
• отсутствие или снижение перистальтики;
• аспират из желудка с желчью;
• наличие крови в стуле.
Неспецифичные:
• непереносимость кормления;
• вздутие живота;
• наличие слизи, «скрытой» крови.
Системные:
• нестабильная температура;
• апноэ;
• стойкий ацидоз, тромбоцитопения, анемия, нейтропения;
• нарушения со стороны кардиоваскулярной системы: артериальная гипотензия;
• олигоурия, шок, симптом «белого пятна»> 3 сек и т.д.
• непереносимость кормления;
• вздутие живота;
• наличие слизи, «скрытой» крови.
Системные:
• нестабильная температура;
• апноэ;
• стойкий ацидоз, тромбоцитопения, анемия, нейтропения;
• нарушения со стороны кардиоваскулярной системы: артериальная гипотензия;
• олигоурия, шок, симптом «белого пятна»> 3 сек и т.д.
Физикальное обследование:
- ІА стадия: мраморность кожных покровов, склонность к брадикардии, единичные приступы апноэ, срыгивания, незначительное вздутие живота, слизистый стул без примесей крови (определяется по анализу кала на скрытую кровь);
- ІБ стадия: эпизоды брадикардии, единичные приступы апноэ, рвота желчью, потеря массы тела, лабильное АД, вздутие живота, стул урежается, слизистый с примесью крови (определяется визуально);
- ІІА стадия: прогрессирующее нарастание симптомов интоксикации, частые апноэ, брадикардия, мышечная гипотония, живот вздут, слабая перистальтика, стул малыми порциями, кровянисто-слизистый;
- ІІБ стадия: тяжелое состояние, апное, брадикардия, растянутая брюшная стенка, при пальпации диффузная болезненность живота. При осмотре - гепатоспленомегалия, стул кровянисто-слизистый, задержка стула;
- ІІІ стадия: состояние ребенка крайне тяжелое, летаргичный, гипотермия, олигоурия, дыхательная и сердечно-сосудистая недостаточность, выраженные симптомы токсикоза и дегидратации. Проявления ДВС-синдрома Рвота кишечным содержимым, «кофейной гущей», инфекционно-токсическая желтуха-нет, живот локально болезнен и резко увеличен в объеме за счет нарастающего асцита, отмечается отек и гиперемия передней брюшной стенки, стул отсутствует или скудный с примесью алой крови, анус сомкнут, легкая ранимость слизистой кишки. При перфорации полого органа определяются выбухание в эпигастрии, исчезновение печеночной тупости при перкуссии и отсутствие перистальтики при аускультации. Поведенческая шкала оценки боли NIPS (для новорожденных и детей до года). Ребенок, набравший по шкале NIPS больше 3 баллов, испытывает боль. 0 – нет боли, 3–5 баллов – умеренно выраженная боль; >5 баллов – сильная боль.
Поведенческая шкала оценки боли NIPS (для новорожденных и детей до года).
Ребенок, набравший по шкале NIPS больше 3 баллов, испытывает боль.
0 – нет боли, 3–5 баллов – умеренно выраженная боль; >5 баллов – сильная боль.
|
№
|
Критерий | 0 | 1 | 2 |
| 1 | Выражение лица | Спокойное/Расслабленное | Гримаса | - |
| 2 | Плач | Отсутствует | Периодически | Постоянный |
| 3 | Дыхание | Спокойное | Измененное | - |
| 4 | Верхние конечности | Расслаблены | Флексия/экстензия | - |
| 5 | Нижние конечности | Расслаблены | Флексия/экстензия | - |
| 6 | Сон | Спит, спокойный | Беспокойный | - |
| 7 | ЧСС | Вариабельность в пределах 10% от исходного уровня | Вариабельность 11–20% от исходного уровня | - |
| 8 | SpO2 | Не требуется дополнительный О2 | Требуется дополнительный О2 | - |
NB! Возможны ограничения использования шкалы: ложно низкие значения могут наблюдаться у новорожденных, состояние которых расценивается как тяжелое либо критическое, когда ответная реакция на боль может быть изменена, либо у детей, получающих препараты седативного, релаксирующего действия [20-21].
Лабораторные исследования [9, 10,22]:
• общий анализ крови – анемия, нейтропения и тромбоцитопения;
• Биохимический анализ крови: гипоальбуминемия, повышение уровня СРБ, повышение мочевины, остаточного азота, повышение прокальцитонина >2 нг/мл;
• Газовый состав крови: смешанный или метаболический ацидоз, гипоксия и гипокарбонатемия, лактатемия;
• Электролиты сыворотки крови: гипонатриемия, гипокальциемия, гипокалиемия;
• Коагулограмма: увеличение АЧТВ, тромбинового времени, снижение уровня фибриногена;
• Бактериологическое исследование крови и стула с чувствительностью к антибиотикам: результат положительный
• Анализ кала на скрытую кровь: положительный
Инструментальные исследования: рентгенография подробно описана в классификации 1.8 соответственно стадии течения НЭК.
УЗИ органов брюшной полости:
• І стадия: гепатомегалия, деформация желчного пузыря, утолщение его стенок с перифокальным отеком, застойная желчь, метеоризм, вялая перистальтика кишечника;
• ІІ стадия: снижение перистальтики в пораженных сегментах, неравномерная, умеренная дилатация петель кишечника, возможно минимальное количество жидкостного компонента между кишечными петлями по типу реактивного выпота;
• ІІІ стадия: выраженное локальное утолщение кишечной стенки, лоцируются инфильтраты симптом «мишени», между петлями кишечника и в полости малого таза нарастает количество жидкости в виде мелкодисперсной взвеси, фрагментарная дилатация кишечных петель, симптом «маятника», перистальтика отсутствует, пневматоз стенки кишки, распространение газа по системе воротной вены;
• ІV стадия (перфорация): эхографически визуализируется значительное количество гетерогенного жидкостного компонента в брюшной полости, что характерно для гнойно-калового выпота. Перистальтических волн не отмечается. Определяются косвенные признаки пневмоперитонеума, так как сложно объективно дифференцировать газы в брюшной полости особенно в аперистальтических кишечных петлях.
Показания для консультации узких специалистов:
• осмотр детского хирурга для своевременного определения показаний к переводу в детское хирургическое отделение;
• осмотр невропатолога при наличии пороков развития ЦНС, двигательных нарушений, судорог, сопорозного состояния;
• осмотр кардиолога для исключения ВПС, признаков сердечно-сосудистой недостаточности.
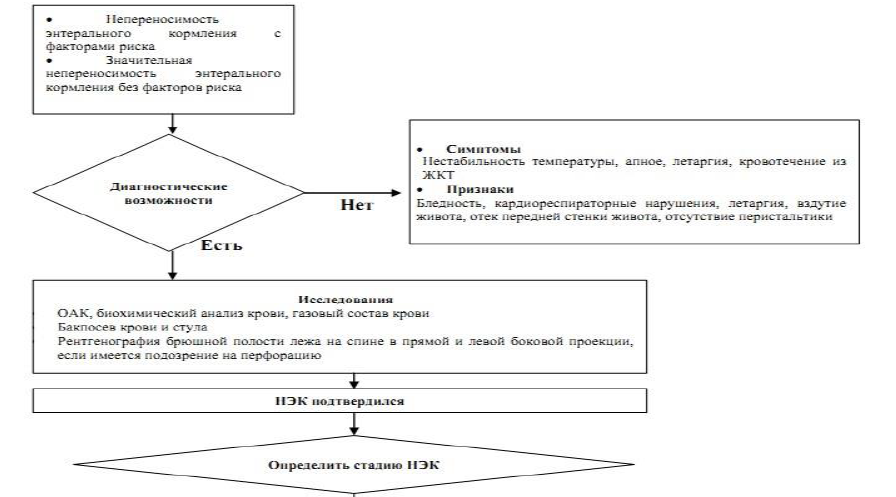
Диагностический алгоритм [21-24]:
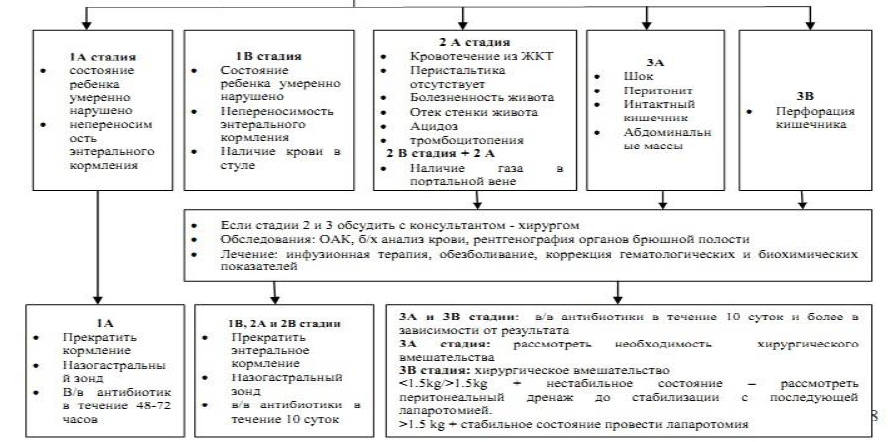
Дифференциальный диагноз
Дифференциальный диагноз:
|
Диагноз
|
Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Мекониальный илеус | Снижения моторики кишечника |
1.Неонатальный скрининг на муковисцедоз:
иммунореактивный трипсин> 40 нг/мл;
2. Потовый тест: хлориды пота> 60 ммоль/л;
3. ДНК-тест мутации гена;
4. На R – ОБП: резко расширенные кишечные петли + участки кишечных петель обычного диаметра. В газовых скоплениях в нижних отделах живота видны гранулярные уплотнения
|
С первых суток жизни отсутствие или скудное отхождение «плотного» мекония. На 2-е сутки появляется рвота, становится неукротимой с примесью желчи, затем «каловая»; характерен вздутый живот, видимая кишечная перистальтика. Возможны осложнения: заворот кишечника, перфорация с развитием мекониевого перитонита. |
|
ВПР желудочно-кишечного тракта.
Высокая кишечная непроходимость
(атрезия, стеноз 12 – перстной кишки.
|
Снижения моторики желудка и непроходимость тонкого кишечника. | R – Органы брюшной полости в вертикальном положении: два газовых пузыря и два уровня жидкости – в желудке и в расширенном нисходящем отделе 12 – перстной кишки выше места стеноза. На боковых рентгенограммах 2 горизонтальных уровня, расположенных на разной высоте. При полной непроходимости кишечника в нижележащих отделах газ не определяется. |
С первых часов жизни обильная рвота с желчью.
Быстрое развитие токсикоза. Вздутие живота в эпигастральной области и западение в остальных отделах. Меконий
«скудный», отходит малыми порциями первые 2-3 дня, в последующие дни стула нет.
|
| ВПР. Врожденное нарушение фиксации кишечника. Синдром Ледда, изолированный заворот среднего отдела кишечника, острая форма болезни Гиршпрунга. | Непроходимость кишечного тракта. | На обзорной R – органов брюшной полости: наличие множества уровней жидкости в верхних отделах. Затемнение в нижних отделах живота (симптом «немой зоны»). Ирригография- при синдроме Ледда- очень высокое стояние слепой кишки, сигмовидная кишка лежит медиально, поперечная ободочная кишка укорочена, ниже обычного положения | С первых суток жизни ребенок беспокойный, рвота с примесью желчи. Прогрессивно нарастает токсикоз. Стул содержит много слизистых пробок, при синдроме Ледда отсутствие мекониевого стула. Живот равномерно вздут, усиленная перистальтика кишечника. |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ: нет.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ [21-25]:
Тактика ведения ребенка при подтвержденном диагнозе некротизирующего энтероколита при I стадии:
• исключение любой энтеральной нагрузки до восстановления функции пассажа по желудочно-кишечному тракту кишечника;
• декомпрессия желудка продолжить (диаметр зонда максимально допустимый у пациента данного веса), канюлю зонда расположить ниже уровня тела ребенка, проводить учет характера и количества отделяемого без активной аспирации содержимого;
• обеспечить венозный доступ;
• при дыхательной недостаточности - респираторная терапия (кислород терапия, СДППД, ИВЛ);
• полное парентеральное питание из расчета физиологической потребности ребенка данного веса и срока гестации согласно протоколу парентерального питания;
• коррекция анемии, тромбоцитопении и дотация факторов свертывания крови по показаниям;
• динамический контроль метаболического и электролитного статуса по показаниям;
• динамический контроль лабораторных показателей не реже 1 раза в неделю;
• УЗИ органов брюшной полости не реже 2 раз в неделю (контроль), обязательно в случае клинического ухудшения состояния;
• обзорная рентгенография грудной и брюшной полостей, в вертикальном положении или латеропозиции, повтор в динамике по показаниям (в случае ухудшения состояния).
Тактика ведения ребенка при подтвержденном диагнозе некротизирующего энтероколита при II стадии:
• исключение любой энтеральной нагрузки на 7 суток;
• декомпрессия желудка продолжить (диаметр зонда максимально допустимый у пациента данного веса), канюлю зонда расположить ниже уровня тела ребенка, проводить учет характера и количества отделяемого без активной аспирации содержимогообеспечить венозный доступ (центральный венозный катетер);
• при дыхательной недостаточности – респираторная терапия (кислород терапия, СРАР, ИВЛ) для нормализации парциального напряжения кислорода и углекислого газа в крови;
• кардиотропная и/или вазопрессорная терапия при нарушениях центральной гемодинамики;
• обезболивание наркотическими аналгетиками при болевом синдроме;
• полное парентеральное питание из расчета физиологической потребности ребенка данного веса и срока гестации с увеличением объема для коррекции патологических потерь;
• коррекция анемии, тромбоцитопении и дотация факторов свертывания крови по показаниям;
• динамический контроль метаболического и электролитного статуса в сутки 1 раз (по показаниям повтор);
• динамический контроль лабораторных показателей не реже 2 раз в неделю;
• УЗИ органов брюшной полости не реже 2 раз в неделю (контроль), обязательно в случае клинического ухудшения состояния;
• обзорная рентгенография грудной и брюшной полостей через 48 часов после установленного диагноза, затем 1 раз в неделю (допустимо в горизонтальном положении при клинически спокойном течении), обязательно в вертикальном положении или латеропозиции в случае клинического ухудшения состояния.
Карта наблюдения пациента, маршрутизация пациента:
- При I а, б и II а стадиях некротизирующего энтероколита показано консервативное лечение. Лечение некротизирующего энтероколита зависит от стадии заболевания и степени выраженности симптомов. Терапия складывается из консервативного и хирургического этапов;
- В случае выявления больного ребенка с НЭК 1-2а степени в родовспомогательном учреждении первого уровня– обеспечить экстренный перевод в родовспомогательную организацию 3-го уровня;
- В случае выявления больного ребенка с НЭК 1-2а степени в родовспомогательном учреждении 2 уровня – обеспечить консультацию хирурга;
- При 2а, б и 3 степени - перевод в экстренное хирургическое отделение (неонатальные хирургические койки) детских медицинских организаций.
Немедикаментозное лечение.
Соблюдение строгого лечебно-охранительного режима. При подозрении на НЭК немедленно:
• прекратить энтеральное кормление;
• установить назогастральный зонд (F6-10) для обеспечения свободного оттока содержимого желудка – декомпрессия кишечника;
• удалить пупочный венозный и артериальный катетер;
• термоконтроль,
• не допускать шума, громких разговоров, яркого света в палате.
• респираторная терапия − поддержание оптимальной оксигенации рО2 (в пределах 90-95%).
Энтеральное питание в терапии некротизирующего энтероколита:
• энтеральную нагрузку начинают НЭК I на 5 день, НЭК II - на 7 день, при достижении клинико-лабораторного улучшения;
• признаки улучшения - нет вздутия и болезненности живота, отсутствие патологического отделяемого из желудка, разрешение пареза кишечника, появление самостоятельного стула, нормализация лабораторных показателей, отсутствие УЗИ-признаков активного воспаления кишечной стенки, асцита, восстановление перистальтики кишечника;
• энтеральное питание начать с объема минимального трофического питания 5-10 мл/кг/сут материнского или пастеризованного грудного молока;
• энтеральное кормление прекращают при двукратном и более превышении полученного за контрольный период объема, или появлении патологических примесей (застойное отделяемое, кровь);
• у недоношенных детей (до 32 недель гестации) без сосательного рефлекса питание предпочтительно вводить в желудок через зонд;
• сроки расширения питания и перехода к периодическому болюсному режиму также индивидуальны, зависят от усвоения объема;
• расширение объема энтерального кормления проводится на 5 мл/кг/сутки.
Медикаментозное лечение.
Инфузионная терапия и поддержание гемодинамики:
• у недоношенных новорожденных начинать внутривенное введение жидкости по 70-80 мл/кг в день с поддержанием в инкубаторе повышенной влажности (60-80%) для снижения неощутимых потерь жидкости и развития гиповолемии;
• прием натрия должен быть ограничен в первые несколько дней жизни и начать после начала диуреза с внимательным мониторингом баланса жидкости, уровней электролитов и массы тела;
• при снижении уровня электролитов в сыворотке крови внутривенно вводится натрий 1-2 мэкв/кг/сутки, калий 1-3 ммоль/кг/сутки, кальций 2 ммоль/кг/сутки;
• объем инфузионной терапии определяется признаками гиповолемии и сниженного сердечного выброса: снижение артериального давления, симптом белого пятна (более 3-х секунд), холодные конечности, тахикардия/брадикардия, олигоурия, нарастание ацидоза и гипернатриемия;
• наличие отеков не является противопоказанием к ограничению объема инфузии, так как они обусловлены повышенной проницаемостью сосудов, потери жидкости в третье пространство и в ЖКТ, вследствие чего ОЦК может оставаться сниженным;
• парентеральное питание следует начинать с первого дня заболевания согласно протоколу парентерального питания;
• при снижении диуреза менее 1 мл/кг/час назначается фуросемид в дозе 1 мг/кг под контролем диуреза;
• в течение суток проводится постоянный мониторинг АД, ЧСС, ЧД, сатурации крови, диуреза, массы тела, желудочного содержимого, стула;
• с целью поддержания гемодинамики назначаются кардиотонические препараты: допамин, добутамин.
Антибактериальная терапия [24-25]:
Антибактериальные препараты подбирают индивидуально в каждом случае при участии клинического фармаколога в соответствии со следующими принципами:
• комбинация препаратов должна охватывать весь спектр микроорганизмов, поскольку в развитии НЭК чаще всего участвует их ассоциация – антимикробные средства с преимущественным действием против грамотрицательных, грамположительных бактерий и анаэробных микроорганизмов;
• с целью усиления антианаэробного звена в терапию должен быть введен метронидазол;
• при назначении препаратов следует учитывать результаты микробиологических посевов, а также типичную для отделения госпитальную микрофлору;
• контроль эффективности подобранной комбинации антибактериальных препаратов проводят через 48-72 часа после начала терапии с последующим продолжением или сменой;
• антибактериальные препараты применяют до устойчивой стабилизации клинико-лабораторного статуса и восстановления функций ЖКТ, НЭК I в течение 5 дней, НЭК II не менее 10 дней;
NB! При назначении антибиотиков учитывать спектр их действий и побочные эффекты [26-30]:
• со стороны пищеварительной системы: повышение активности печеночных трансаминаз, гипербилирубинемия;
• со стороны системы кроветворения: анемия, лейкопения, гранулоцитопения, тромбоцитопения;
• со стороны мочевыделительной системы: олигурия, протеинурия, микрогематурия, почечная недостаточность, тубулярный некроз;
• со стороны нервной системы: подергивания мышц, парестезии;
• со стороны органов чувств: шум в ушах, снижение слуха, вестибулярные и лабиринтные расстройства, необратимая глухота;
• аллергические реакции: кожная сыпь, зуд, крапивница, лихорадка; редко - отек Квинке;
• эффекты, обусловленные химиотерапевтическим действием: кандидоз полости рта.
Коррекция гемостаза:
• при ДВС – синдроме проводится переливание свежезамороженной плазмы 10-15 мл/кг;
• при тромбоцитопении <30×10 /л назначается тромбоцитарная масса 10-15 мл/кг;
• при коагулопатии, связанной с дефицитом витамина К1 - введение витамина К1 внутримышечно недоношенным детям в дозе 0,5 мг, доношенным – 1 мг.
Болевой синдром:
• лечение болевого синдрома проводится наркотическими анальгетиками. Контроль болевого синдрома проводится по адаптированной шкале оценки боли у новорожденного;
• контроль болевого синдрома проводится по адаптированной поведенческой шкале оценки боли NIPS (для новорожденных и детей до года).
Перечень основных лекарственных средств (имеющих 100% вероятность применения)
|
Лекарственная группа
|
Международное непатентованное наименование ЛС | Способ применения | Уровень доказательности |
| Антибактериальная терапия | |||
| Антибиотик группы полусинтетических пенициллинов широкого спектра действия – ампициллин | Ампициллин | в\в в суточной дозе 50-100 мг/кг массы тела 2 раза в сутки | А |
| Антибиотик широкого спектра действия - аминогликозид | Гентамицин | раствор для в/в и в/м введения. 2,5 – 4 мг/кг/сут , 1 раз в 36 часов | А |
| Антимикробный препарат широкого спектра действия для системного лечения инфекций, вызванных облигатными анаэробными бактериями | Метронидазол | в/в 7,5 мг/кг в/в, 2 раза в сутки | А |
Хирургическое вмешательство [31-35].
Показания к хирургическому лечению:
• прогрессивное ухудшение общего состояния;
• наличие опухолевидного образования в брюшной полости;
• воспалительные изменения брюшной стенки;
• лабораторные показатели: остро возникшая тромбоцитопения, нарушения в коагулограмме, тяжелая гипонатриемия, стойкий метаболический ацидоз;
• рентгенологические признаки в виде статичной петли кишки, асцит, газ в портальной вене, пневмоперитонеум.
Хирургическое вмешательство:
• дренирование брюшной полости;
• локальная резекция измененного участка кишки с созданием двойной энтеро/колостомы.
Выбор вида операции зависит от состояния ребенка и массы тела:
• если масса тела ребенка <1500 гр. или состояние ребенка не стабильное – необходимо рассмотреть временное использование перитонеального дренажа;
• если масса тела ребенка> 1500 гр. или состояние ребенка стабильное – необходимо рассмотреть проведения лапаротомии.
NB! При выполнении этой процедуры необходимо обеспечить адекватное обезболивание.
Дальнейшее ведение.
После выписки из стационара:
• осмотр педиатра, в течение первого месяца 1 раз в неделю, далее до 6 месяцев 1 раз в 2 недели, в 6-12 месяцев - 1 раз в месяц;
• осмотр детского хирурга в первый месяц 1 раз в неделю, далее до 6 месяцев 1 раз в месяц, в 6-12 месяцев 1 раз в квартал;
• другие специалисты по показаниям и в декретированные сроки.
ИНДИКАТОРЫ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ И БЕЗОПАСНОСТИ МЕТОДОВ ДИАГНОСТИКИ И ЛЕЧЕНИЯ, ОПИСАННЫХ В ПРОТОКОЛЕ:
• усвоение энтерального питания;
• активное сосание;
• нормальная температура тела;
• прибавка массы тела (15-20 г/кг в сутки);
• мягкий живот, безболезненный при пальпации;
• стул без патологических примесей и изменений.
ИНДИКАТОРЫ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ И БЕЗОПАСНОСТИ МЕТОДОВ ДИАГНОСТИКИ И ЛЕЧЕНИЯ, ОПИСАННЫХ В ПРОТОКОЛЕ:
• усвоение энтерального питания;
• активное сосание;
• нормальная температура тела;
• прибавка массы тела (15-20 г/кг в сутки);
• мягкий живот, безболезненный при пальпации;
• стул без патологических примесей и изменений.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ:
Показания для плановой госпитализации: нет.
Показания для экстренной госпитализации: развитие некротизиующего энтероколита при наличии неспецифичных, специфичных и системных симптомов.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023 - 1) Stoll BJ. Epidemiology of necrotising enterocolitis. Clin Perinatol 1994;21: 205218. 2) Holman RC, Stoll BJ, Curns AT et al. Necrotising enterocolitis hospitalisations among neonates in the United States. Pediatr Perinat Epidemiol. 2006;20;498-506. 3) Fitzgibbons SC, Ching Y, Yu D et al. Mortality of necrotizing enterocolitis expressed by birth weight categories. J Pediatr Surg. 2009;44:1072-1076. 4) Guillet R, Stoll SJ, Curns AT et al. Association of H2-blocker therapy and higher incidence of necrotizing enterocolitis in very low birth weight infants. Pediatrics. 2006;117:e137-42. 5) Blakely ML, Lally KP, McDonald S et. al. Postoperative outcomes of extremely low birth-weight infants with necrotizing enterocolitis or isolated intestinal perforation^ a prospective cohort study by the NICHD Neonatal Research Network. Ann Surg 2005;241:984-9; discussion 989-94. 6) Luig M, Lui K and the NSW & ACT NICUS Group. Epidemiology of necrotizing enterocolitis – Part I: Changing regional trends in extremely preterm infants over 14 years. J Paediatr Child Health. 2005; 41:169-173. 7) Bell JM, Ternberg JL, Feigin RD et al. Neonatal necrotizing enterocolitis: therapeutic decision based upon clinical staging. Ann Surg 1978; 187:1-7. 8) Walsh MC, Kleigman RM. Necrotising enterocolitis: treatment based on staging criteria. Pediatr Clin North Am 1986; 33: 179-201. 9) Gastroenterology and nutrition/ed.by Josef Neu: Neonatology Questions and Controversies. Elsevier Saunders. 2012, 217-225. 10) Neonatology: A Practical Approach to Neonatal Diseases/ ed. by G.Buonocore, R.Bracci, M.Weindling – Springer-Verlag Italia. – 2012, 1348 p. 11) Lambert DK, Christensen RD, Baer VL et al. Fulminant necrotizing enterocolitis in a multihospital healthcare system. J Perinatol 2012; 32:194-198. 12) Cuna AC, Reddy N, Robinson AL, Chan SS. Bowel ultrasound for predicting surgical management of necrotizing enterocolitis: a systematic review and meta-analysis. Pediatr Radiol 2018; 48:658. 13) Munaco AJ, Veenstra MA, Brownie E, et al. Timing of optimal surgical intervention for neonates with necrotizing enterocolitis. Am Surg 2015; 81:438. 14) Khalak R, D'Angio C, Mathew B, et al. Physical examination score predicts need for surgery in neonates with necrotizing enterocolitis. J Perinatol 2018; 38:1644. 15) Rose AT, Patel RM: A critical analysis of risk factors for necrotizing enterocolitis. Semin Fetal Neonatal Med. 2018;23(6):374–9. 10.1016/j.siny.2018.07.005. 16) Samuels N, van de Graaf RA, de Jonge RCJ, et al.: Risk factors for necrotizing enterocolitis in neonates: a systematic review of prognostic studies. BMC Pediatr. 2017;17(1):105. 10.1186/s12887-017-0847-3. 17) Travers CP, Clark RH, Spitzer AR, et al.: Exposure to any antenatal corticosteroids and outcomes in preterm infants by gestational age: prospective cohort study. BMJ. 2017;356;j1039. 10.1136/bmj.j1039. 18) Been JV, Lievense S, Zimmermann LJ, et al.: Chorioamnionitis as a risk factor for necrotizing enterocolitis: a systematic review and meta-analysis. J Pediatr. 2013;162(2):236–42.e2. 10.1016/j.jpeds.2012.07.012. 19) Lu Q, Cheng S, Zhou M, et al.: Risk Factors for Necrotizing Enterocolitis in Neonates: A Retrospective Case-Control Study. Pediatr Neonatol. 2017;58(2):165–70. 10.1016/j.pedneo.2016.04.002. 20) Проблемы клинической оценки боли у новорожденных , Российский вестник перинатологии и педиатрии, 2020; 65. 21) Committee on Fetus and Newborn and Section on Anesthesiology and Pain Medicine Prevention and management of procedural pain in the neonate: an update. Pediatrics 2016; 137(2): e20154271. DOI: https://doi.org/10.1542/peds.2015-4271. 22) Puri P., Höllwarth M. Pediatric Surgery. Springer, Berlin, Heidelberg, 2006. 23) Luig M, Lui K and the NSW & ACT NICUS Group. Epidemiology of necrotizing enterocolitis – Part I: Changing regional trends in extremely preterm infants over 14 years. J Paediatr Child Health. 2005; 41:169-173. 24) Autmizguine J, Hornik CP, Benjamin DK Jr, et al. Anaerobic antimicrobial therapy after necrotizing enterocolitis in VLBW infants. Pediatrics 2015; 135:e117. 25) Shah D, Sinn JK. Antibiotic regimens for the empirical treatment of newborn infants with necrotising enterocolitis. Cochrane Database Syst Rev 2012; :CD007448. 26) Grace M Musiime, Anna C Seale , Sarah G Moxon , Joy E Lawn, Risk of gentamicin toxicity in neonates treated for possible severe bacterial infection in low- and middle-income countries: Systematic Review, Trop Med Int Health 2015 Dec;20(12):1593-606. doi: 10.1111/tmi.12608. Epub 2015 Oct 23. 27) https://www.vidal.ru/drugs/gentamicin__17716#indication 28) Longombe AL, Ayede AI, Marete I, Mir F, Ejembi CL, Shahidullah M, Adejuyigbe EA, Wammanda RD, Tshefu A, Esamai F, Zaidi AK, Baqui AH, Cousens S. Oral amoxicillin plus gentamicin regimens may be superior to the procaine-penicillin plus gentamicin regimens for treatment of young infants with possible serious bacterial infection when referral is not feasible: Pooled analysis from three trials in Africa and Asia. 29) https://www.vidal.ru/drugs/metronidazole__5309#side_effects,https://www.vidal.ru/drugs/ampicillin__3124#side_effects 30) IBM Micromedex NeoFax and Pediatric Drug , 5/9/2020 NeoFax® https://www.micromedexsolutions.com/micromedex2/librarian/CS/A7C3EC/ND_PR/evidencexpert/ND_P/evidencexpert/DUPLICATIONSHIELDSY 31) Караваева С.А. Хирургическое лечение некротического энтероколита: Дис. д-ра мед. наук / С.А. Караваева. – СПб.; 2002. 32) Подкаменев А.В. Патогенез и лечение язвенно-некротического энтероколита и перфораций желудочно-кишечного тракта у новорожденных: Дис. д-ра мед. наук / А.В. Подкаменев. – Иркутск; 2008. 33) Katheleen M., Moss L. Necrotizing enterocolitis. Clinics in perinatology 2012; 387—401. 34) Marko T., Dickerson M.L. Clinical handbook of neonatal pain management for nurses. New York, 2017; 219.
Информация
Сокращения, используемые в протоколе:
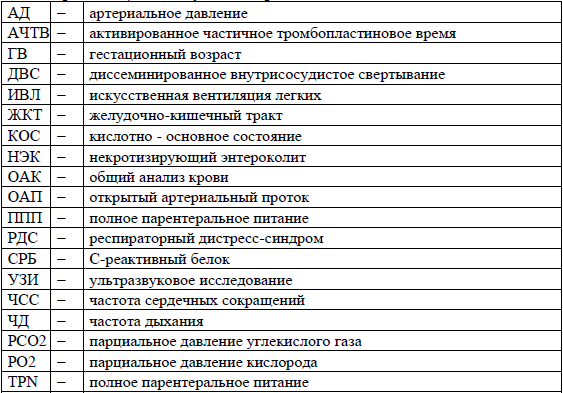
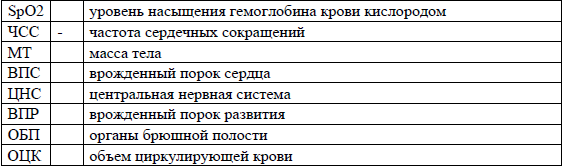
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА.
Список разработчиков протокола с указанием квалификационных данных:
1) Байгазиева Гульжан Жолдасхановна – кандидат медицинских наук, доцент кафедры неонатологии НАО «Казахский Национальный медицинский университет имени С.Асфендиярова», неонатолог.
2) Божбанбаева Нишангуль Сейтбековна – доктор медицинских наук, профессор, заведующая кафедрой неонатологии НАО «Казахский Национальный медицинский университет имени С.Асфендиярова», неонатолог.
3) Жубанышева Карлыгаш Биржановна – PhD, профессор, заведующая курса неонатологии НАО «Казахстанско-Российский Медицинский Университет», неонатолог.
4) Ерекешов Асылжан Абубакирович - кандидат медицинских наук, заместитель директора по клинической работе АО «Научный центр педиатрии и детской хирургии», главный внештатный неонатальный хирург МЗ РК.
5) Ералиева Бибихан Абдилиевна – кандидат медицинских наук, доцент кафедры клинической фармакологии НАО «Казахский Национальный медицинский университет имени С. Асфендиярова», главный внештатный клинический фармаколог МЗ РК.
Указание на отсутствие конфликта интересов: нет.
Рецензент:
Джаксалыкова Куляш Каликановна - доктор медицинских наук, зав.кафедрой неонатологии НАО «Медицинский университет Астана», неонатолог.
Условия пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.