Мигрень у детей
 Версия: Клинические рекомендации РФ 2024 (Россия)
Версия: Клинические рекомендации РФ 2024 (Россия)
Головная боль, вызванная применением лекарственных средств, не классифицированная в других рубриках (G44.4), Мигрень (G43), Синдром гистаминовой головной боли (G44.0), Сосудистая головная боль, не классифицированная в других рубриках (G44.1)
Неврология детская, Педиатрия
Общая информация
Краткое описание
Разработчик клинической рекомендации
- Всероссийское общество неврологов
- Российское межрегиональное общество по изучению боли (РОИБ)
- Ассоциация Здоровье детей
Одобрено Научно-практическим Советом Минздрава РФ
В соответствии с Правилами поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 –9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», утвержденных постановлением Правительства Российской Федерации от 19.11.2021 № 1968 с изменения, клинические рекомендации применяются следующим образом:
– размещенные в Рубрикаторе после 1 января 2024 года – с 1 января 2025 года.
Клинические рекомендации
Мигрень
Год утверждения (частота пересмотра): 2024
Возрастная категория: Дети
Пересмотр не позднее: 2026
ID: 169
Определение заболевания или состояния (группы заболеваний или состояний)
Мигрень (М) представляет собой одну из наиболее распространенных форм первичной головной боли и проявляется повторяющимися приступами головной боли, которые часто сопровождаются сопутствующими симптомами (тошнотой, рвотой, фото- и фонофобией) [1].
Головная боль (ГБ) чаще локализуется в одной половине головы по типу гемикрании, сторонность боли может меняться от приступа к приступу, также может отмечаться двухсторонний характер боли, что часто отмечается в детском возрасте. Головные боли при мигрени отличаются значительной интенсивностью, усиливаются при легкой физической нагрузке, что существенно ограничивает повседневную активность пациента. Продолжительность приступа варьирует от 1 (у детей до 6 лет) - 2 часов (у детей старше 7 лет) до нескольких суток. Обычно приступ прекращается с наступлением сна.
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
G43 – Мигрень
G43.0 – Мигрень без ауры [простая мигрень]
G43.1 – Мигрень с аурой [классическая мигрень]
G43.2 – Мигренозный статус
G43.3 – Осложненная (в том числе, хроническая) мигрень
G43.8 – Другая мигрень (офтальмоплегическая, ретинальная)
G43.9 – Мигрень неуточненная
G44.0 Синдром "гистаминовой" головной боли
G44.1 Сосудистая головная боль, не классифицированная в других рубриках
G44.4 Головная боль, вызванная применением лекарственных средств, не классифицированная в других рубриках
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
В настоящее время для классификации разных форм мигрени пользуются Международной классификацией головных болей третьего пересмотра (МКГБ III) 2018 г.
Согласно МКГБ-III (2018), в зависимости от клинических проявлений и течения приступа, у детей различают мигрень без ауры, мигрень с аурой, хроническую мигрень, осложнения мигрени, возможную мигрень и эпизодические синдромы, которые могут сочетаться с мигренью (таб. 2).
Диагноз разных форм мигрени ставят исключительно на основании клинической картины, для чего применяют диагностические критерии Международной классификации головных болей третьего пересмотра, опубликованные в 2018 г. Дополнительные методы исследования можно применять для дифференциальной диагностики или для выявления вторичных форм головных болей.
Таблица 2. Классификация мигрени согласно МКГБ – III (2018)
|
Классификация мигрени
1. Мигрень 1.1. Мигрень без ауры 1.2. Мигрень с аурой 1.2.1. Мигрень с типичной аурой 1.2.1.1. Типичная аура с ГБ 1.2.1.2. Типичная аура без ГБ 1.2.2. Мигрень со стволовой аурой 1.2.3. Гемиплегическая мигрень 1.2.3.1. Семейная гемиплегическая мигрень 1.2.3.1.1 Семейная гемиплегическая мигрень 1 типа 1.2.3.1.2 Семейная гемиплегическая мигрень 2 типа 1.2.3.1.3 Семейная гемиплегическая мигрень 3 типа 1.2.3.1.4 Семейная гемиплегическая мигрень (с мутациями в других локусах) 1.2.3.2. Спорадическая гемиплегическая мигрень 1.2.4. Ретинальная мигрень 1.3. Хроническая мигрень 1.4. Осложнения мигрени 1.4.1. Мигренозный статус 1.4.2. Персистирующая аура без инфаркта 1.4.3. Мигренозный инфаркт 1.4.4. Мигренозная аура- триггер эпилептического припадка 1.5. Возможная мигрень 1.5.1. Возможная мигрень без ауры 1.5.2. Возможная мигрень с аурой 1.6. Эпизодические синдромы, которые могут сочетаться с мигренью 1.6.1. Повторяющиеся желудочно-кишечные нарушения 1.6.1.1. Синдром циклических рвот 1.6.1.2. Абдоминальная мигрень 1.6.2. Доброкачественное пароксизмальное головокружение 1.6.3. Доброкачественный пароксизмальный тортиколис |
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Большое значение в возникновении мигрени имеют наследственные факторы. Известны три наследственные формы мигрени с установленным моногенным типом наследования: семейная гемиплегическая мигрень I (ген CACNA1A), II (ген ATP1A2) и III (ген SCN1A) типов. Но распространенность семейной гемиплегической мигрени в популяции крайне мала и составляет 0,01%, в большинстве других случаев мигрени преобладает полигенный тип наследования, и наследуется, по-видимому, не сама болезнь, а предрасположенность к определенному типу реагирования центральной нервной и сосудистой систем на различные типы раздражителей.
Для многих пациентов характерно наличие триггерных факторов, которые могут провоцировать приступы мигрени (таб. 1). Часть этих факторов можно определить как модифицируемые (возможно контролировать), а часть факторов являются не поддающимися для изменений (например, гормональные факторы или метеофакторы). Выявление триггерных факторов с помощью ведения дневника головной боли может помочь ребенку и его родителям значительно уменьшать частоту приступов мигрени путем изменения образа жизни при избегании или устранении наиболее важных и частых триггеров. Однако у некоторых пациентов триггерной является совокупность факторов, провоцирующих приступы мигрени в каждом конкретном случае.
Таблица 1. Триггеры приступа мигрени [1, 2, 3]
| Психологические |
Стрессы.
Позитивные и негативные эмоции.
Изменения настроения.
|
|---|---|
| Гормональные факторы |
Менструация.
Овуляция.
|
| Факторы окружающей среды |
Яркий свет.
Громкий шум.
Сильные или резкие запахи (духи, курение, моющие средства).
Погодные условия (ветер, изменения погоды, сильная жара/холод).
|
| Диета, продукты питания, напитки |
Горький шоколад.
Твердые сыры.
Помидоры.
Киви.
Орехи.
Лук.
Чеснок.
Алкоголь (особенно красные вина).
Продукты, содержащие глютамат, нитриты и нитраты.
Сладкие газированные напитки.
|
| Лекарственные препараты |
Резерпин (C02LA51).
Нитроглицерин**.
Эстрогены.
|
| Другие факторы |
Недосыпание/пересыпание.
Голод и нерегулярный прием пищи.
Гипогликемия.
Гипертермия.
Усталость.
Авиаперелеты.
|
Мигрень относится к первичным головным болям и считается формой нейроваскулярной ГБ, при которой первичные изменения в нервной системе приводят к вторичному периваскулярному воспалению, вторичному расширению преимущественно дуральных артерий и, соответственно, к боли и дополнительной тригеминальной активации [3]. Патофизиология боли при мигрени имеет нейрогенную основу, а не первичные сосудистые нарушения [4]. Таким образом имеет место первичная нейрональная инициация каскада нейрохимических процессов, завершающихся широкой волной кортикальной деполяризации и региональной олигемии [5]. Эти изменения лежат в основе возникновения мигренозной ауры.
Известно, что первичные головные боли могут проявляться типичными эпизодическими приступами, возможны хронические ежедневные или почти ежедневные ГБ. Описаны ремиссии — как при эпизодических, так и при хронических ГБ.
Первоначальные исследования механизмов мигрени были сфокусированы на краниальной вазодилятации как источнике боли [3]. Механизмы периферической тригеминальной активации, значимая роль CGRP (кальцитонин ген родственный пептид), активация вторых тригеминоваскулярных нейронов и механизм кортикальной распространяющейся депрессии являются другими интенсивно изучаемыми областями при мигрени.
Исследования с использованием ПЭТ показывают, что ростральные отделы ствола мозга, особенно контралатеральное околоводопроводное серое вещество (ОСВ) среднего мозга — структуры активно вовлеченные в патофизиологии мигрени. Эти данные подтверждают, что области ствола мозга играют важную роль в инициации или завершении приступа мигрени. Мигрень, вероятно, является результатом дисфункции ствола мозга и/ или диэнцефальных ядер, которые вовлечены в сенсорную модуляцию краниоваскулярных афферентов [3].
Пусковым механизмом, активизирующим тригеминоваскулярную систему, является распространяющаяся волна корковой депрессии. Активация тригеминальной системы сопровождается выбросом в периваскулярных окончаниях тройничного нерва воспалительных нейропептидов, в первую очередь CGRP. Развивающееся периваскулярное нейрогенное воспаление приводит к активации тригеминальных ноцицепторов и возникновению боли.
Приступы ГБ при мигрени могут различаться у разных людей, изменяться от атаки к атаке [6]. Такая вариабельность может частично объясняться дисфункцией ионных каналов в аминергических ядрах ствола мозга, которые в норме модулируют сенсорный поток и обеспечивают нейрональный контроль краниальных сосудов. Высвобождение кальцитонин-ген-родственного пептида (CGRP) вызывается периферической тригеминальной активацией. Возникающая в результате боль может рассматриваться как нарушение перцепции обычно безболезненных афферентных стимулов от краниоваскулярных структур, что, возможно, вызвано развитием периферической или центральной сенситизации [7].
Сенсорные нейроны менингеальной оболочки имеют сходство с ноцицептивными нейронами других областей нервной системы, обладают хемосенситивностью и сенситизацией.
Сенситизация — это состояние, при котором постепенно снижается сила стимула, необходимая для получения ответа, а амплитуда ответа повышается [8].
Выделяют периферическую и центральную сенситизацию. Клинически сенситизация проявляется в виде гипералгезии и аллодинии.
При мигрени развитие периферической сенситизации (интракраниальных ноцицепторов менингеальных оболочек и кровеносных сосудов, а также первичных болевых нейронов в узле тройничного нерва) в приступе ГБ связано с выделением провоспалительных медиаторов, экстравазацией белков плазмы при дилатации церебральных и менингеальных сосудов. Интракраниальная механическая стимуляция также способствует развитию периферической сенситизации. Этим объясняется усиление ГБ в приступе мигрени при кашле, наклонах и рутинной физической активности, что связано с небольшим повышением внутричерепного давления и легкой механической стимуляцией интракраниальных ноцицепторов [8].
Считается, что пульсирующая боль является следствием в основном периферической сенситизиции, а аллодиния и повышенная чувствительность кожи головы — в основном центральной сенситизации.
Периферическая сенситизация приводит к развитию центральной сенситизации тригеминальных нейронов второго порядка. Экспериментальными данными показано, что сенситизация этих центральных нейронов может продолжаться до 10 часов [9]. При центральной сенситизации структуры, вовлеченные в периферическую сенситизацию, уже обладают спонтанной активностью даже в отсутствии периферической стимуляции.
При длительном возбуждении тригеминальные нейроны второго порядка начинают отвечать на подпороговые стимулы болевой импульсацией. В результате активируются и сенситизируются нейроны третьего порядка (таламические нейроны).
При длительности приступа мигрени более 4 часов аллодиния развивается у 80% пациентов, зона распространения аллодинии превышает болевые зоны и может захватывать противоположную половину головы и верхние конечности [10]. Предполагается, что этот феномен отражает сенситизацию нейронов третьего порядка, к которым стекаются импульсы от тригеминальных нейронов второго порядка.
Кожная аллодиния определяется как ощущение боли при нанесении неболевых стимулов на неповрежденную кожу. В 60—75% случаев у людей, страдающих мигренью, развивается центральная сенситизация (второго тригеминального нейрона), которая проявляется кожной аллодинией во время приступа [9]. В основе возникновения феномен аллодинии предполагается механизм центральной сенситизации, т.е. сенситизация вторых тригеминальных нейронов в хвостатых ядрах [11].
Центральная сенситизация, вероятно, играет роль в снижении ответа на лечение триптанами и в прогрессировании мигрени [12].
Повторяющиеся эпизоды центральной сенситизации могут лежать в основе перманентного нейронального повреждения ОСВ, что приводит к нарушению процессов модуляции боли, к снижению эффективности профилактического лечения и прогрессированию мигрени.
Частота аллодинии, выявляемой во время приступа ГБ, значительно выше у пациентов с ХМ (66%) и при мигрени с аурой (65%), чем при мигрени без ауры (41%) [13].
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Эпидемиологические исследования головной боли у детей раннего возраста значительно затруднены из-за невозможности для детей четко описать свою боль и вспомнить особенности ассоциированных симптомов.
При использовании критериев мигрени у детей по Vahlquist и Hackzell [14] оказалось, что в возрасте 7 лет распространенность мигрени колеблется от 1,2 до 3,2% (у мальчиков чаще, чем у девочек). В возрастной группе от 7 до 11 лет распространенность мигрени выше и колеблется от 4 до 11 % с одинаковой частотой у мальчиков и девочек. У детей старше 11 лет и подростков распространенность мигрени находится в пределах от 8 до 23% (у девочек чаще, чем у мальчиков) [15, 16,17].
Применение критериев Международной классификации головных болей первого пересмотра (1988) на примере 2165 детей в возрасте от 5 до 15 лет показало, что распространенность мигрени имеет место в 10,6% случаев, причем в 7,8% случаев дети имели мигрень без ауры и 2,8% случаев — мигрень с аурой [18].
Дополнительные исследования с использованием этих же критериев обнаружили, что распространенность мигрени у детей составляет от 6,1 до 10,6% [19, 20, 21].
У подростков в возрасте 15—19 лет распространенность мигрени оказалась намного выше — 28%, причем 19% пациентов имели мигрень без ауры и 9% — мигрень с аурой [22].
При использовании критериев Международной классификации головных болей второго пересмотра (2004) у детей и подростков в возрасте от 12 до 17 лет установлено, что распространенность мигрени составила 14,5% [23]
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Согласно диагностическим критериям мигрени по Международной классификации головной боли 3-го пересмотра выделяют две основные формы мигрени:
1. Мигрень без ауры (MбА) – клинический синдром, характеризующийся приступами головной боли со специфическими сопровождающими симптомами. Для МбА характерно: повторяющиеся головные боли, проявляющиеся приступами (атаками) цефалгии продолжительностью 4–72 часа (у детей от 2часов). К типичным проявлениям относятся: односторонняя локализация боли (у детей чаще двухсторонняя), пульсирующий характер (у детей чаще ноющая или тянущая), средняя или значительная интенсивность, ухудшение головной боли от обычной физической активности, наличие таких сопровождающих симптомов, как тошнота, рвота, фоно- и фотофобия. Данная форма мигрени протекает без ауры и характеризуется только головной болью. Она наблюдается примерно у половины всех больных мигренью.
Диагностические критерии (МКГБ-3):
A. Не менее 5 приступов, которые отвечают следующим критериям (B–D).
B. Приступы головной боли продолжаются от 4 до 72 часов (у детей до 15 лет 2–48 часов) в отсутствие лечения или при его неэффективности.
C. Головной боли присущи не менее двух из следующих признаков:
- односторонняя локализация,
- пульсирующий характер,
-интенсивность боли от средней до значительной (затрудняет или делает невозможной повседневную активность),
- головная боль ухудшается от обычной физической активности или требует прекращения обычной физической активности (на пример, ходьба, подъем по лестнице).
D. Головная боль сопровождается как минимум одним из следующих симптомов:
тошнота и/или рвота,
фотофобия и одновременно фонофобия.
2. Мигрень с аурой (МА) – характеризуется локальными неврологическими симптомами, которые обычно предшествуют или сопровождают головную боль.
Мигрень с аурой – расстройство, проявляющееся повторяющимися эпизодами обратимых локальных неврологических симптомов (аурой), обычно нарастающих в течение 5–20 минут и продолжающихся не более 60 минут. Головная боль с характеристиками мигрени без ауры, как правило, следует, за симптомами ауры. В редких случаях головная боль может отсутствовать совсем или не иметь мигренозных черт.
Диагностические критерии (МКГБ-3):
A. Наличие не менее 2-х приступов, которые отвечают следующим критериям (B–D).
B. Аура включает по меньшей мере один из следующих симптомов и не включает двигательную слабость:
- полностью обратимые зрительные симптомы, в том числе позитивные (мерцающие пятна и полосы) и/или негативные (нарушения зрения);
- полностью обратимые чувствительные симптомы, в том числе позитивные (ощущения покалывания) и/или негативные (онемения);
- полностью обратимые нарушения речи.
C. По меньшей мере два из ниже перечисленных:
- гомонимные зрительные нарушения и/или односторонние чувствительные симптомы;
- как минимум один симптом ауры постепенно развивается на протяжении не менее 5 минут и/или различные симптомы ауры возникают последовательно на протяжении не менее 5 минут;
- каждый симптом ауры имеет продолжительность не менее 5 минут, но не более 60 минут.
D. Наличие головной боли, соответствующей критериям диагностики мигрени без ауры, начинающейся во время ауры или в течение 60 минут после ее начала.
У некоторых пациентов за несколько часов или даже суток до приступа могут возникать предвестники головной боли (продромальная фаза), а также симптомы после приступа (послеприступная фаза). Продромальные и послеприступные симптомы включают гиперактивность или, напротив, снижение активности, депрессию, желание есть определенные продукты, повторную зевоту и другие.
Ретинальная мигрень - повторяющиеся приступы монокулярного расстройства зрения, включающие сцинтилляции (мерцание), скотому или слепоту и сочетающиеся с мигренозной головной болью. Необходимо исключить другие причины преходящей монокулярной слепоты, особенно если это впервые возникшее состояние, такие как невропатия зрительного нерва, расслоение сонной артерии или патология центральной артерии сетчатки и ее ветвей.
Гемиплегическая форма мигрени характеризуется помимо клиники классической мигрени с аурой (обратимые зрительные, сенсорные, речевые нарушения) еще появлением специфической клинической картиной ауры в виде полностью обратимой мышечной слабости.
Мигрень со стволовой аурой характеризуется возникновением хотя бы двух из следующих симптомов: дизартрия, головокружение, шум в ушах, гипакузия, диплопия, атаксия, нарушение уровня сознания.
Хроническая мигрень характеризуется частыми приступами головной боли, возникающими как минимум 15 дней в месяц на протяжении не менее 3 месяцев. При этом у ребенка должны быть в анамнезе эпизодические приступы мигрени.
Мигренозный статус диагностируют в том случае, когда приступ интенсивной головной боли (или несколько следующих друг за другом приступов) продолжается более 72 часов (исключая время сна). Мигренозный статус, как правило, является показанием для госпитализации.
Персистирующая аура без инфаркта характеризуется сохранением симптомов ауры более 7 дней в отсутствие инфаркта по данным нейровизуализации.
Мигренозный инфаркт головного мозга характеризуется возникновением на фоне приступа мигрени с аурой стойкой неврологической симптоматики, соответствующей обычным проявлениям ауры. Критериями такого диагноза являются, сохранение симптомов ауры более 60 минут; многомесячный (многолетний) анамнез характерных приступов мигрени с аналогичной (но более кратковременной) аурой; подтверждение инфаркта мозга методами нейровизуализации; отсутствие других заболеваний, способных вызвать аналогичные симптомы.
Мигрень рассматривается как триггер эпилептического припадка, если эпилептические припадки, вызываемые (запускаемые) мигренью, возникают во время или в течение часа после мигренозной ауры.
В детском возрасте относительно часто отмечаются эпизодические синдромы, которые могут сочетаться с мигренью, или в большинстве случаев являющиеся так называемыми предшественниками развития классической картины мигрени в более старшем возрасте. Два из них связаны с приступами функциональных нарушений желудочно-кишечного тракта (синдром циклических рвот и абдоминальная форма мигрени), другие состояния так же носят пароксизмальный доброкачественный характер (доброкачественные пароксизмальные головокружение и тортиколиз).
Синдром циклических рвот – повторяющиеся эпизодические приступы интенсивной тошноты и рвоты, обычно стереотипные для данного пациента и возникающие с предсказуемой периодичностью. Приступы могут сопровождаться бледностью и вялостью. Между ними какие-либо симптомы нарушений со стороны желудочно-кишечного тракта (ЖКТ) отсутствуют.
Диагностические критерии (МКГБ-3):
A. Не менее 5 приступов интенсивной тошноты и рвоты, соответствующих критериям B и C.
B. Стереотипные у отдельного пациента и повторяющиеся с предсказуемой периодичностью.
C. Все следующее:
– тошнота и рвота происходят не реже 4 раз в час;
– приступ длится ≥ 1 ч и до 10 дней;
– межприступный интервал – ≥ 1 нед.
D. Между приступами каких-либо симптомов нарушений со стороны ЖКТ не отмечается.
E. Анамнез, результаты обследований не выявляют другого заболевания ЖКТ.
Абдоминальная форма мигрени – идиопатическое расстройство, наблюдаемое главным образом у детей, в виде повторяющихся приступов боли в животе по средней линии, умеренной или выраженной интенсивности, сопровождающееся вазомоторными симптомами, тошнотой и рвотой длительностью 2–72 ч и нормальным состоянием в межприступный период. Появление ГБ во время этих эпизодов не характерно. Диагностические критерии (МКГБ-3):
A. Не менее 5 приступов боли в животе, соответствующих критериям B–D.
B. Боль имеет по меньшей мере 2 из следующих 3-х характеристик:
– положение по средней линии, параумбиликально или без четкой локализации;
– боль тупая или носит неопределенный характер;
– умеренная или сильная интенсивность.
C. Во время приступа наличие по крайней мере 2-х из следующих симптомов:
– анорексия;
– тошнота;
– рвота;
– бледность.
D. Продолжительность приступа – 2–72 ч при отсутствии лечения или безуспешном лечении.
E. Между приступами каких-либо симптомов ЖК-нарушений не отмечается.
F. Анамнез, результаты обследований не выявляют другого заболевания ЖКТ.
Доброкачественное пароксизмальное головокружение характеризуется повторяющимися кратковременными приступами головокружения, возникающими спонтанно и проходящими самостоятельно, развивающимися у здоровых детей.
Диагностические критерии (МКГБ-3):
A. Не менее 5 приступов, соответствующих критериям B и C.
B. Головокружение возникает спонтанно, максимально выражено в начале приступа и проходит самостоятельно через минуты или часы и не сопровождается потерей сознания.
C. По меньшей мере 1 из следующих связанных симптомов или признаков:
– нистагм;
– атаксия;
– рвота;
– бледность;
– ощущение боязни.
D. В межприступный промежуток отсутствие патологии в неврологическом статусе, при аудиометрии и исследовании вестибулярной функции.
E. Анамнез, результаты обследований не выявляют другого заболевания, способного вызывать схожую клиническую картину.
Примечания: 1. Маленькие дети не могут описать состояние головокружения. У маленьких детей эпизодические периоды нарушения равновесия и неустойчивости, замечаемые родителями, могут быть истолкованы как эпизоды головокружений. 2. Должны быть исключены опухоли задней черепной ямки, эпилептические пароксизмы, заболевания вестибулярной системы.
Доброкачественный пароксизмальный тортиколиз – повторяющиеся эпизоды наклона головы в одну сторону, возможно, с небольшим поворотом, которые проходят спонтанно. Возникают у младенцев и маленьких детей на первом году жизни. Диагностические критерии (МКГБ-3):
A. Периодические приступы, возникающие у маленького ребенка, соответствующие критериям B и C.
B. Наклонение головы в любую сторону, с небольшим поворотом или без него, самопроизвольно исчезающее через несколько минут или несколько дней.
C. По меньшей мере 1 из следующих связанных симптомов или признаков:
– бледность;
– повышенная возбудимость, раздражительность;
– недомогание;
– рвота;
– атаксия.
D. Отсутствие неврологической патологии между приступами.
E. Отсутствие заболевания, вызывающего схожую клиническую картину.
Примечания: 1. Приступы, как правило, повторяются ежемесячно. 2. Атаксия более вероятна у детей старшего возраста в затрагиваемой возрастной группе.
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии постановки диагноза. Диагностика мигрени у детей и подростков показана всем пациентам при подозрении на её наличие. Диагноз основан на сборе жалоб пациента и его родителей/законных представителей, анамнеза заболевания, результатов неврологического осмотра и обследований, проводимых для исключения других специфических причин головной боли, требующих направления к специалисту соответствующего профиля для дальнейшего обследования и лечения. Для постановки диагноза мигрени необходимо соответствие клинической картины заболевания диагностическим критериям МКГБ-3, приведенных в разделе 1.6 КР.
1. Жалобы и анамнез
- Рекомендуется у детей с ГБ тщательный сбор анамнеза, детальное общеклиническое и неврологическое тестирование [1,3,13,18, 24].
Уровень убедительности рекомендаций С, уровень достоверности доказательств 5.
Комментарии: Приступу мигрени без ауры могут предшествовать предвестники (продромальные явления) в виде эмоциональных нарушений (немотивированная раздражительность, депрессия, апатия), нарушение сна, изменения аппетита (абулия или чувство неутолимого голода), жажды и задержки жидкости (пастозность, отечность). Предвестники возникают за несколько часов (или дней) до приступа [24].
У большинства детей с мигренью без ауры частота приступов составляет 1 раз в месяц или 1 раз в 2 месяца. При мигрени с аурой частота приступов несколько реже, у детей с гемиплегической мигренью еще реже - 1 раз в 4-6 месяцев.
Приступы мигрени могут начинаться в любое время суток, но чаще начало приступа отмечается днем или вечером. Головная боль при мигрени у взрослых пациентов характерно пульсирующая. Однако у детей бывает давящая, распирающая или ломящая. Боль при мигрени локализуется в лобно, лобно-височных, периорбитальной областях, реже — в теменной области. У детей дошкольного возраста наблюдается, как правило, двусторонняя головная боль. Для старших детей характерна односторонняя головная боль, которая может менять сторону от приступа к приступу. Гемикранический характер боли в период приступа отмечают около 30% детей с мигренью без ауры, и половина детей с мигренью с аурой. Как правило, только к 10-12 годам жизни ребенка характеристики головной боли при мигрени соответствуют таковым у взрослых. Во время приступа мигрени характерен внешний вид больных: бледность кожных покровов лица, скудная мимика, иногда страдальческое выражение лица. Помимо головной боли для приступа мигрени характерны тошнота и, реже, рвота. После рвоты, как правило, отмечается облегчение общего состояния, и ребенок обычно засыпает. После сна продолжительностью от 30 минут до 2-3 часов приступ полностью купируется, и головная боль не возобновляется. Средняя продолжительность приступов у большинства детей с мигренью без ауры составляет 2-3 часа, у большинства детей с мигренью с аурой приступы значительно короче, до 1 часа. В межприступном периоде дети с мигренью практически здоровы.
2. Физикальное обследование
- Рекомендуется пациентам с 7 лет использование визуально-аналоговой шкалы (ВАШ) для оценки интенсивности головной боли в приступе мигрени [1,9,72].
Уровень убедительности рекомендаций C, уровень достоверности доказательств 3.
Комментарии: Обычно головная боль в приступе мигрени имеет высокую интенсивность, достигая 7—9 баллов по ВАШ, может быть мучительной, трудно переносимой. Нередко во время болевого приступа отмечается общая гиперестезия, непереносимость яркого света (фотофобия), громких звуков (фонофобия), а также особенная чувствительность к обонятельным и тактильным раздражителям. Обычная физическая нагрузка, движения головой, поездка на транспорте могут усиливать интенсивность головной боли. У пациентов более младшего возраста оценить интенсивность головной боли в цифровой / бальной оценке достаточно затруднительно, у таких пациентов применяют шкалу оценки с изображением лиц или цветовых шкал, отражающих степень болевых ощущений.
3. Лабораторные диагностические исследования
- Не рекомендуются лабораторные методы исследования для диагностики М [25,26,31,73].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
4. Инструментальные диагностические исследования
- Не рекомендуются инструментальные исследования при выполнении диагностических критериев М и нормальных данных неврологического осмотра у пациентов с МбА и МА [25,26,31,73].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарии: у большинства пациентов с М инструментальные методы исследования не выявляют никаких специфических изменений. У ряда пациентов при проведении стандартной МРТ головного мозга в Т2 режиме могут обнаруживаться единичные субклинические гиперинтенсивные очаги в субкортикальном белом веществе полушарий мозга, реже в стволовых структурах [29]. Предполагают, что эти очаговые изменения являются следствием преходящих нарушений церебральной перфузии, которые по данным магнитно-резонансной томографии регистрируются во время повторных приступов М. Показано, что М может являться независимым фактором риска развития субклинического очагового ишемического поражения головного мозга [12]. Поскольку эти очаги не имеют специфических морфологических признаков, они не могут считаться нейровизуализационными маркерами М.
- Не рекомендуется проведение ЭЭГ (электроэнцефалографии с нагрузочными пробами) у пациентов с типичной картиной мигрени и отсутствием подозрений на эпилептический генез головной боли [25,26,31,44].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарии: При подозрении на эпилептический генез головной боли (головная боль как проявление эпилептического приступа или послеприступная головная боль) необходимо проведение электроэнцефалография с видеомониторингом, т.к. это исследование проводится более длительно, захватывает состояние бодрствования и сна и имеет более высокую информативность для выявления эпилептиформной активности. Особенно показано данное исследование при возникновении непродолжительного приступа головной боли после сна, сопровождающегося тошнотой и однократной рвотой, другими кратковременными вегетативными или зрительными нарушениями.
- Рекомендуются инструментальные обследования (магнитно-резонансная томография головного мозга, магнитно-резонансная ангиография интракарниальных сосудов) при редких формах МА и осложнениях М с целью подтверждения диагноза или исключения органических причин для возникновения очаговой неврологической симптоматики [13,27,28,31]
Уровень убедительности рекомендаций – С(уровень достоверности доказательств – 5).
Комментарий: при редких формах МА (например, ретинальная и мигрень с пролонгированной аурой, а так же М со стволовой аурой) показано проведение МРТ головного мозга и магнитно-резонансной ангиографии интракарниальных сосудов с целю исключения аномалий развития сосудов головного мозга (артерио-венозные мальформации, аневризмы, гипоплазии, стенотические процессы и патологические извитости артерий), которые могут быть причиной схожей клинической картины.
- Рекомендуются проведение нейровизуализационных методов исследования (магнитно-резонансная томография головного мозга, магнитно-резонансная ангиография интракарниальных сосудов, момпьютерная томография головного мозга) у детей и подростков с мигренеподобной головной болью при подозрении на симптоматический характер головной боли, то есть при нетипичном течении М или при обнаружении одного или более «сигналов опасности» [2,11,21,27-29,31].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5).
Комментарий: Перечень настораживающих симптомов - «сигналов опасности» у пациентов с головной болью:
- ГБ, изменившая свое течение
- «Громоподобная ГБ» или ГБ, нарастающая до 10 баллов по ВАШ за 1-2 секунды
- Строго односторонняя ГБ
- Прогрессивно ухудшающаяся ГБ без ремиссий
- Внезапно возникшая, необычная для пациента ГБ
- Атипичная мигренозная аура (с необычными зрительными, сенсорными или двигательными нарушениями и/или продолжительностью > 1 часа)
- Изменения в сфере сознания (оглушенность, спутанность или потеря памяти) или психические нарушения
- Очаговые неврологические симптомы и симптомы системного заболевания (повышение температуры тела, кожная сыпь, ригидность шейных мышц, артралгии или миалгии) при первично возникшей головной боли
- Признаки внутричерепной гипертензии (усиление ГБ при кашле, натуживании, физическом напряжении)
- Отек диска зрительного нерва при офтальмоскопии
- ВИЧ-инфекция, онкологическое, эндокринное и другое системное заболевание или травма головы в анамнезе
- Неэффективность адекватного проводимого лечения
- Очаговая симптоматика в неврологическом статусе
- Особенности клинической картины в виде нарастающей во времени ГБ с тошнотой или рвотой, усиливающейся при изменении положения головы в пространстве
Нейровизуализационные исследования могут выявить значительные изменения в ЦНС, особенно при очаговых неврологических симптомах и/или судорожных приступах в анамнезе. Иногда на магнитно-резонансной томографии головного мозга, магнитно-резонансной ангиографии интракарниальных сосудов и компьютерной томографии головного мозга обнаруживают негрубые сосудистые аномалии, небольшие изменения в белом веществе мозга, арахноидальные и/или эпифизарные кисты, которые не имеют клинического значения у детей с ГБ, но вызывают большую обеспокоенность у семьи такого ребенка и требуют дополнительных разъяснений со стороны врача. В случае если родители связывают начало ГБ с травмой шеи, необходима магнитно-резонансная ангиография интракарниальных сосудов и сосудов шеи для исключения возможной диссекции сонной артерии. Когда имеются признаки идиопатической внутричерепной гипертензии, необходимо провести дифференциальный диагноз с тромбозом венозных синусов, который может быть причиной повышения внутричерепного давления. Для этого используют МРТ головного мозга во флебографическом режиме [28].
- Рекомендуется проведение офтальмоскопии для исключения застойных явлений на глазном дне при ГБ у детей [2, 3, 24, 31].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: Исследование глазного дна важно для исключения признаков повышения внутричерепного давления. Подтверждение наличия застойных явлений на глазном дне является показанием к проведению магнитно-резонансной томографии головного мозга или компьютерной томографии головного мозга.
(1) Достоверный диагноз: Особенности клинической картины соответствуют всем диагностическим критериям мигрени с аурой или мигрени без ауры
(2) Вероятный диагноз: Отмечается несоответствие по одному диагностическому критерию
(3) Возможный диагноз: несоответствие по нескольким диагностическим критериям
5. Иные диагностические исследования
- Рекомендуется ведение дневника головной боли (приложение А3.1) с отражением в нем длительности и интенсивности головной боли, наличия сопутствующих симптомов, триггерных факторов, приема лекарственных средств [1, 25, 29].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Одна из главных целей лечащего врача детей и подростков с головной болью — разграничение первичных головных болей от вторичных. Следует обращать внимание на размер и форму головы, поскольку субкомпенсированная гидроцефалия сопровождается частыми ГБ и это является показанием для проведения дополнительным методов обследования. Острое начало ГБ нередко бывает связано с системными инфекциями (ОРВИ, грипп, менингиты и др.), органическим поражением мозга и другими вторичными причинами. Если приступы ГБ повторяются часто или даже эпизодически, но не имеют тенденции к нарастанию интенсивности и изменению клинической картины при отсутствии изменений в неврологическом статусе, следует предполагать наличие первичных ГБ, в том числе мигрени.
Дифференциальная диагностика с другими первичными головными болями (в основном с головными болями напряжения) основывается на отчетливых различиях в клинической картине приступа. Основными отличиями ГБН от мигрени без ауры являются: при ГБН легкая или умеренная интенсивность ГБ, давящий двухсторонний характер, не усиливается при повседневной физической нагрузке, не сопровождается тошнотой и рвотой.
Важно помнить, что односторонние или двусторонние затылочные боли у детей наблюдаются редко и требуют диагностической настороженности, поскольку во многих случаях являются следствием структурных повреждений.
При подозрении на симптоматический генез мигренеподобной головной боли обусловленной наличием аневризмы или артериовенозной мальформации сосудов головного мозга проводят МРТ головного мозга (режим МР-ангиографии), КТ-ангиографию или рентгеноконтрастную ангиографию.
Для исключения мигренеподобных головных болей при метаболических расстройствах проводят анализы на уровень гомоцистеина, витамина B12, фолиевоей кислоты в крови, лакатат/пируват сыворотки крови.
При возникновении непродолжительной мигренеподобной головной боли с тошнотой и рвотой, возникающей ночью или при пробуждении, сопровождающейся постприступной вялостью или сонливостью необходимо исключить эпилептический генез головной боли. Показано проведение ЭЭГ мониторинга в состоянии сна.
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
В терапии мигрени выделяют два основных направления: лечение приступа и профилактическое лечение [29].
Для детей часто бывает трудно определить начало приступа мигрени, что обусловлено тем, что:
- в силу большой эмоциональности, увлечения играми, быстрого переключения внимания дети часто пропускают начало приступа головной боли и замечают ее только в том момент, когда боль имеет уже высокую интенсивность и появляется тошнота, а иногда и рвота;
- многие дети по опыту знают, что головная боль может нарастать очень быстро и поэтому любую головную боль воспринимают как приступ мигрени.
Поэтому следует обучать детей и их родителей раннему определению приступа мигрени и его лечению.
1. Консервативное лечение
- Рекомендуется для приступов умеренной и высокой интенсивности использовать ибупрофен** в разовой дозе 10 мг/кг массы тела [31,32,33,40].
Уровень убедительности рекомендаций А, уровень достоверности доказательств 2.
Комментарии: Назначается в самом начале приступа. В некоторых исследованиях у детей более старшего возраста для эффективного лечения приступов мигрени у детей применялась доза 7,5 мг/кг [32,33]. Ибупрофен** по своим обезболивающему и жаропонижающему эффектам, а также по воздействию на желудочно-кишечный тракт и почки сопоставим с парацетамолом**, но не оказывает токсического действия на печень [41].
- Рекомендуется применение парацетамола** в разовой дозе 10—15 мг/кг [32].
Уровень убедительности рекомендаций В, уровень достоверности доказательств 2.
Комментарии: Назначается в самом начале приступа. Возможно повторное применение препарата через 6—8 часов [32].
- Не рекомендуется при частых приступах мигрени у детей применение обезболивающих препаратов (N02 анальгетиков) более двух (максимум трех) раз в неделю в виду высокого риска формирования лекарственного абузуса [30,31,40,41].
Уровень убедительности рекомендаций C, уровень достоверности доказательств 3.
- Рекомендуется у детей и подростков для купирования эпизодических приступов мигрени умеренной интенсивности назначать НПВП (например, ибупрофен**, парацетамол**), а при тяжелых приступах головной боли и неэффективности НПВП - триптаны (N02CC селективные агонисты серотониновых 5HT1-рецепторов) или эрготамин в комбинации с другими средствами, исключая психолептики (N02CA52) [2, 35, 78].
Уровень убедительности рекомендаций В, уровень достоверности доказательств 2.
Комментарии: Такой подход особенно оправдан у детей и подростков, у которых периодически отмечаются длительные и очень тяжелые приступы головной боли (более 8 баллов по 10-балльной ВАШ).
В международных публикациях возможно у подростков для купирования тяжелых приступов мигрени, помимо анальгетиков, использовать специфические противомигренозные препараты (N02C препараты для лечения мигрени): триптаны (N02CC селективные агонисты серотониновых 5HT1-рецепторов) (#суматриптана, #золмитриптана и др.) [28]. Необходимо учитывать, что в России применение препаратов группы триптанов (N02CC селективные агонисты серотониновых 5HT1-рецепторов) разрешено с 18лет.
Селективные агонисты 5-НТ-1-рецепторов - #суматриптан и другие триптаны (#золмитриптан, #ризатриптан), несмотря на имеющиеся зарубежные публикации по эффективному применению в купировании приступов мигрени у детей [34, 35, 38, 37], применяют до 18 лет с осторожностью в случае неэффективности других препаратов и по решению врачебной комиссии с подписанием представителем ребенка информированного согласия.
В настоящее время нет однозначных данных о доказанной эффективности пероральных триптанов (N02CC селективные агонисты серотониновых 5HT1-рецепторов) для терапии острого приступа мигрени у детей [40]. Назальные формы введения селективных агонистов серотониновых 5HT1-рецепторов в исследованиях показывают более высокую эффективность у детей и подростков с мигренью (38,43). На данный момент зарегистрирован спрей назальный дозированный Золмитриптан (N02CC03).
#Суматриптан в таблетках в дозировке 12,5-25мг (разовый прием) при массе тела меньше 40кг, 50-100мг (разовый прием) при массе тела больше 40кг [79]. У детей пероральный прием #Суматриптана в таблетках в двойном слепом плацебо-контролируемом исследовании не показал эффективности по сравнению с плацебо (34).
#Золмитриптан таблетки 2,5мг, назальный спрей дозированный 2.5мг/доза: 2,5мг (разовый прием) при массе тела меньше 40кг, 5мг (разовый прием) при массе тела больше 40кг [79]. В сравнительном исследовании #Золмитриптан в таблетках 2,5мг с ибупрофеном** (200 и 400мг) у детей и подростков показал схожую эффективность [74].
#Ризатриптан в таблетках в дозировке 5мг (разовый прием) для детей с массой тела меньше 40кг и 10мг (разовый прием) для детей массой тела больше 40кг (разовый прием)[79]. Пероральный прием в указанных дозировках показал в исследовании пациентов 12-17лет с мигренью более высокую эффективность по купированию мигрени по сравнению с плацебо. В исследовании пациентов 6-11лет статистически значимых отличий от плацебо не наблюдалось [36,75]. Важным является то, что применение НПВП (нестероидные противовоспалительные и противоревматические препараты (М01А) должно быть ограничено числом приемов не более 14 раз в месяц, триптанов (N02CC селективные агонисты серотониновых 5HT1-рецепторов) - 9 раз в месяц и комбинации триптанов, НПВП так же до 9 раз в месяц на протяжении не более 3 месяцев для предотвращения развития ЛИГБ [43]. Триптаны (N02CC селективные агонисты серотониновых 5HT1-рецепторов) противопоказаны при сопутствующей патологии сердечно-сосудистой системы (ИБС, инфаркт миокарда, нарушение мозгового кровообращения, в том числе в анамнезе, заболевания периферических сосудов), базилярной и гемиплегической формах мигрени, ограничено применение при эпилепсии, артериальной гипертензии.
- Рекомендуется пациентам при выраженной тошноте и многократной рвоте в условиях стационара применять #метоклопрамид**внутривенное введение терапевтическая доза составляет 0.1 (0.13-0.15) мг/кг массы тела, максимальная доза составляет 10 мг. [80,82] В зарубежных рекомендациях дозировки #метоклопрамида** доходят до 1-2мг/кг [76].
Уровень убедительности рекомендаций С, уровень достоверности доказательств 5.
2. Немедикаментозные методы лечения
- Рекомендуется всем пациентам с мигренью применение немедикаментозных методов лечения, таких как соблюдение режима сна, регулярная оздоровительная спортивная нагрузка, соблюдение режима питания, достаточный объем выпиваемой жидкости и исключение пищевых провокаторов. Применяют поведенческую терапию и психотерапевтическую коррекцию: когнитивно-поведенческая терапия, методики биологической обратной связи, релаксационные методы [44].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5.
1. Когнитивно-поведенческая терапия
- Рекомендуется применение когнитивно-поведенческой терапии, включающей психологическое консультирование и проведение релаксационных тренингов, управление образом жизни и соблюдение приверженности медикаментозной терапии [31,44].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5.
2. Метод биологической обратной связи
- Рекомендуется всем пациентам с мигренью применение из дополнительных, нефармакологических, методов лечения мигрени в детском возрасте биологической обратной связи (БОС) по электромиографическому или электроэнцефалографическому сигналу, общего массажа, иглорефлексотерапии и других форм акупунктуры [44, 45, 46, 47].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5.
Комментарии: Эффективность БОС-терапии показана у взрослых и детей и обусловлена, по-видимому, изменением уровня бета-эндорфина в плазме крови [45]. При обучении расслаблению на курсовых занятиях доказана эффективность БОС- релаксационной терапии для прерывания и предотвращения возвратных головных болей у детей с мигренью [46]. БОС-терапия практически не дает побочных эффектов. У подростков с мигренью прибегают к поведенческой терапии, психотерапевтической помощи и/или консультации психиатра, необходимость и выбор которых определяется типом коморбидных (в основном депрессивных и тревожных) психических расстройств [47].
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- Рекомендуется пациентам с частыми приступами и тяжелым течением мигрени санаторно-курортное лечение 1-2 раза в год [1, 2, 31, 40, 81].
Уровень убедительности рекомендаций В, уровень достоверности доказательств 2.
Комментарии: В санаторно-курортных условиях применяют грязевые аппликации на воротниковую область невысокой температуры (36—38°, 10—15 минут, 10—12 процедур). Иногда грязелечение проводится в чередовании с радоновыми ваннами (100—200 ед. Махе, 36°, 10—12 минут), реже с общими сероводородными ваннами (50—100 мг/л сероводорода 10 процедур). Наряду с грязевыми аппликациями или ваннами применяются лечебная физкультура, массаж воротниковой зоны и головы. Применение воротниковой терапии в чередовании с общими радоновыми или сероводородными ваннами имеет целью воздействовать на шейный вегетативный аппарат и на нарушенное при этом периферическое кровообращение. В местных санаториях целесообразно использовать электрофорез новокаина, папаверина в комплексе с хвойными ваннами. При плохой переносимости жары не следует направлять таких больных на южные курорты в жаркий период года.
Госпитализация
Организация оказания медицинской помощи
Показания для экстренной госпитализации пациента в неврологическое отделение:
1) Головная боль, сопровождающаяся изменением сознания;
2) Головная боль, сопровождающаяся лихорадкой и менингеальными симптомами;
3) Головная боль с нарастающей очаговой неврологической симптоматикой;
4) Головная боль с нарастающей общемозговой симптоматикой;
5) Мигренозный статус.
Показания для плановой госпитализации пациента в неврологическое отделение:
1) Прогрессирующая головная боль;
2) Некупируемая головная боль;
3) Головная боль с аурой.
Показания к выписке пациентов из неврологического отделения:
1) Купирование головной боли;
2) Уменьшение головной боли до 3-4 баллов по визуальной аналоговой шкале;
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
1. Профилактика
Показания к профилактическому лечению должны рассматриваться в следующих случаях:
- два и более приступа мигрени в месяц;
- тяжелые и длительные приступы мигрени;
- низкая эффективность терапии, купирующей приступ мигрени;
- противопоказания или плохая переносимость препаратов, купирующих приступ мигрени;
- наличие необычной ауры, которая пугает ребенка и родителей.
- Рекомендуется всем пациентам с мигренью проведение мероприятий по изменению режима дня [13,18, 23, 29, 44].
Уровень убедительности рекомендаций C, уровень достоверности доказательств 5.
Комментарии: Не менее важны в лечении мигрени у детей мероприятия по модификации привычного образа жизни: устранение или избегание так называемых триггеров мигрени - факторов, провоцирующих мигренозный приступ; проведение релаксационной терапии (мышечной релаксации, аутогенной тренировки, гипноза и др.), более значимой у подростков; соблюдение гигиены сна; изменение диеты для устранения провоцирующих приступ продуктов (шоколад, определенные сыры, острые приправы, некоторые орехи и т.д.) и уменьшение потребления кофеинсодержащих продуктов (пепси, кола, кофе и др.). Если ребенок посещает спортивные секции, необходимо соблюдать разумный контроль над физическими упражнениями и тренировками. Оптимальна регулярная физическая нагрузка составляет 20—30 минут в день. Во время приступа мигрени у ребенка рекомендуется отдых в затемненной комнате в спокойной обстановке. Часто сон может купировать приступ, и после пробуждения ребенка приступ мигрени не возобновляется.
- Рекомендуется выявление триггерных факторов, которые могут провоцировать приступы мигрени, в соответствии с ними проводить мероприятия по модификации образа жизни [1, 2, 8, 44].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5.
- Рекомендуется всем пациентам динамическое наблюдение врача-невролога (профилактический прием (осмотр, консультация) врача-невролога) по месту жительства [1, 2].
Уровень убедительности рекомендаций С, уровень достоверности доказательств 5.
- Рекомендуется для профилактического лечения мигрени у детей и подростков использование противоэпилептических препаратов [51].
Уровень убедительности рекомендаций А, уровень достоверности доказательств 3.
Комментарии: Среди противоэпилептических препаратов наибольшее число исследований проведено для топирамата** и вальпроевой кислоты**.
- Рекомендуется в профилактическом лечении использование #топирамата** перорально в стартовой дозе 25мг/сутки с постепенным повышением дозы до 2-3мг/кг в день с медленной титрацией в течении 8-10 недель до максимальной дозы 100-200мг/сут, минимальная продолжительность курса терапии 3мес [48, 49, 50, 51,76].
Уровень убедительности рекомендаций В, уровень достоверности доказательств 2.
Комментарий: Эффективность #топирамата** в профилактическом лечении мигрени показана в двойных-слепых плацебо контролируемых исследованиях для детей в возрасте от 6 до 15 лет [49, 50] и для подростков 12—17 лет [48]. Если необходимо, доза увеличивается каждые две недели до достижения максимального значения 2-3мг/кг массы тела в сутки. Необходимо помнить что при повышении дозировки нарастает риск нежелательных побочных явлений в виде снижения аппетита, снижении массы тела, парастезий, замедления когнитивных процессов, повышения образования солей в моче.
- Рекомендуется в профилактическом лечении использование #вальпроевой кислоты**, пероральный прием, 15-45мг/кг/сут, эффективная доза составляет 500—1000 мг/сут, минимальная продолжительность курса терапии 3мес. Необходима медленная титрация дозы под контролем биохимических маркеров состояния печени и почек [51, 52-56].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 4.
Комментарии: Доказательства эффективности #вальпроевой кислоты** в профилактическом лечении мигрени у детей основаны на результатах открытых клинических исследований [52, 53], а также сравнительных исследований с #пропранололом**[54] и #топираматом**[55]. Показано эффективное использование препарата #вальпроевой кислоты** в профилактическом лечении циклических рвот [56]. Необходимо учитывать возможное развитие нежелательных побочных эффектов со стороны эндокринной системы и тератогенное действие при применение вальпроевой кислоты** у девочек в пре- и пубертатном периоде [76].
- Рекомендуется в профилактическом лечении мигрени использование #леветирацетама**, перорально по 50мг/кг/сут, минимальная продолжительность курса терапии 3 мес. Необходима постепенная титрация дозы [77].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5.
Комментарии: В настоящее время в немногочисленных исследованиях имеются доказательства эффективности #леветирацетам** в профилактическом лечении мигрени у детей. Так в сравнительном исследовании эффективности с #пропранололом** и #вальпроевой кислоты**. #Леветирацетам** значительно уменьшал тяжесть головной боли (Р=0,026), частоту (Р=0,024) и показатель тяжести влияния мигрени на качество жизни ( PedMIDAS) (Р=0,001) у детей с мигренью. Однако между этими тремя группами не было обнаружено существенной разницы. Процент пациентов, испытавших облегчение боли, составил 69,24%, 92,31% и 30,76% в группах #пропранолола, #вальпроевой кислоты и #леветирацетама соответственно. [77] Для пациентов с массой до 50кг лечение следует начинать с суточной дозы 20 мг/кг, разделенной на 2 введения (по 10 мг/кг 2 раза в сутки). Изменение дозы на 10 мг/кг может осуществляться каждые 2 нед до достижения рекомендуемой суточной дозы — 50 мг/кг. Пациентам с массой тела больше 50мг - лечение следует начинать с суточной дозы 1000 мг, разделенной на 2 введения (по 500 мг 2 раза в сутки). Изменение дозы на 500 мг 2 раза в сутки может осуществляться каждые 2–4 нед.
- Рекомендуется применение для профилактики мигрени у детей #пропранолол** пероральный прием, начальная суточная доза 1 мг/кг, разделенная на три приема, с постепенным повышением дозировки в зависимости от эффективности и побочных явлений (контроль частоты сердечных сокращений и артериального давление), но не более 4 мг/кг в сутки, минимальная продолжительность курса 3мес. [80, 31].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5.
Комментарии: Для профилактического лечения мигрени у взрослых применяют бета-адреноблокаторы (#пропранолол**, #метопролол**). Механизм действия бета-адреноблокаторов при мигрени неизвестен. Исследования, проведенные у детей, содержат неоднозначные данные по эффективности #пропранолола** в профилактическом лечении мигрени перорально в дозе 60мг/сут для пациентов массой тела менее 35кг и в дозе до 120мг для детей массой тела выше 35мг [57, 58]. Некоторые авторы подчеркивают, что #пропранолол** в дозе 1—4 мг/кг/сут. при курсовом лечении не менее 3 месяцев может быть эффективен у детей с мигренью [31]. Необходимо, однако, учитывать, что #пропранолол** противопоказан у детей с бронхиальной астмой, и следует применять с осторожностью у пациентов с сахарным диабетом, ортостатической гипотензией и депрессией [82]. Пролонгированные препараты #пропранолола** можно принимать один раз в сутки. При назначении #пропранолола** необходимо медленное повышение дозы с контролем состояния артериального давления и сердечной деятельности.
- Рекомендуется использование для профилактического лечения у детей при мигрени #циннаризин (N07CA - препараты для устранения головокружения), перорально, в дозировке 1,5 мг/кг/сутки у детей с массой тела менее 30 кг и 50 мг/сутки у детей с массой тела более 30 кг. Минимальный курс терапии 3 мес. [63, 51, 80].
Уровень убедительности рекомендаций В, уровень достоверности доказательств - 3.
Комментарии: Двойное слепое плацебо-контролируемое рандомизированное исследование показало эффективность #циннаризина в профилактическом лечении мигрени у детей в дозировке детям с массой до 30 кг - 1,5мг/кг/сутки, с массой больше 30кг - 50мг/сут, минимальный курс терапии 3 мес. Лучше начинать с меньшей дозы с постепенным увеличением. В исследовании отмечалось минимальное проявление побочных эффектов в виде увеличения массы тела и экстрапирамидных нарушений [63,51,82]. #Циннаризин является блокатором кальциевых каналов L-типа. Противопоказаниями для применения #циннаризин (N07CA- препараты для устранения головокружения) являются синдром слабости синусового узла, атриовентрикулярная блокада 2—3 степени, сердечная недостаточность. Побочные эффекты проявляются в виде отеков, артериальной гипотензии, утомляемости, головокружения, головной боли, запоры, атриовентрикулярной блокады, при превышении рекомендованных дозировок возможны экстрапирамидные нарушения, увеличение массы тела. Меньшее количество исследований эффективности #циннаризина для профилактики мигрени у детей и подростков объясняется отсутствием указанного препарата в США и Канаде.
- Рекомендуется использование для профилактического применения у детей при мигрени из группы антидепрессантов – #амитриптилина** [51, 59, 62].
Уровень убедительности рекомендаций В, уровень достоверности доказательств - 3.
Комментарий: Действие #амитриптилина** при мигрени связывают с его серотонинергическим эффектом; оптимальная доза этого препарата при мигрени у детей составляет 1 мг/кг/сут. Показано медленное повышение дозировки каждые 2 недели начиная с 0,25мг/кг в сутки (на ночь), для снижения выраженности побочных явлений в виде вялости и сонливости. Пероральный прием, минимальный курс терапии 3мес [59, 62].
Перед назначением показано проведение регистрации электрокардиограммы с физической нагрузкой для исключения нарушения сердечной проводимости. В последнее время из-за возможных побочных явлений преимущественно применяется при тяжелом течении и хронической форме мигрени.
В таблице 3 приведены препараты и их дозировки, применяемые для профилактической терапии мигрени у детей и подростков (таб.3).
Таблица 3. Препараты для профилактического лечения мигрени у детей.
| Препарат | Доза, путь введения | Ссылки |
|---|---|---|
|
Бета-адреноблокаторы:
|
Перорально
1-4 мг/кг/сутки
|
31, 37 |
|
Неселективные ингибиторы обратного захвата моноаминов:
|
Перорально
Детям в возрасте от 6 лет - 0,25-1,0 мг/кг/сутки
|
59,62 |
|
Перорально
Детям с массой до 30кг - 1,5мг/кг/сутки, с массой больше 30кг - 50мг/сут.
|
63,51,80
|
|
Противоэпилептические препараты:
#вальпроевая кислота**
|
Перорально
15-45 мг/кг/сутки
(500-1000 мг/сутки)
Перорально
1-2 мг/кг/сутки
(12,5-25 мг/сутки)
Перорально
50мг/кг/сутки
|
51, 52-56
48-51,76
77
|
- Рекомендуется для профилактического лечения мигрени применение витаминов (A11HA другие витаминные препараты) (#рибофлавин** 400мг в день курс 2 мес [66, 80], (C01EB другие препараты для лечения заболеваний сердца ) #Убидекаренон -150-300мг в день, курс 2мес [67, 80].
Уровень убедительности рекомендаций C, уровень достоверности доказательств - 5.
Комментарии: Данные лекарственные средства применяются с целью профилактики мигрени у взрослых и детей (формы выпуска, разрешенные к применению у детей). Для большинства этих средств не проводились исследования по эффективности использования у детей или подростков с мигренью, однако их применение оправдано, видимо, в качестве дополнительного лечения при низкой эффективности фармакологического лечения.
- Рекомендуется комбинация разных видов фармакологического и нефармакологического лечения [25, 26, 47].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5.
Комментарий: При профилактическом лечении тяжелых приступов мигрени у детей и подростков наиболее эффективной оказывается часто комбинация разных видов фармакологического и нефармакологического лечения. Так, например, в одном из исследований показано повышение эффективности применения #амитриптилина** в сочетании с когнитивно-поведенческой терапией в лечении пациентов 10-17лет с хронической мигренью [71].
- Рекомендуется при планировании профилактического лечения учитывать коморбидные расстройства [51].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5.
Комментарий: У подростков с мигренью, особенно при частых приступах или хронической форме, выше чем в популяции встречаются тревожные и депрессивные расстройства, что необходимо учитывать при диагностике коморбидной патологии и выборе методов лечения [51]. Своевременное лечение коморбидной патологии повышает эффективность терапии мигрени и препятствует переходу в хроническую форму.
- Рекомендуется при проведении профилактического лечения учитывать наличие у ребенка ЛИГБ [51].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5
Комментарий: Для предотвращения развития ЛИГБ необходимо ограничивать применение простых анальгетиков и НПВП не более 14 раз в месяц, триптанов (селективных агонистов серотониновых 5HT1-рецепторов), и сочетаний триптанов (селективных агонистов серотониновых 5HT1-рецепторов) и НПВП до 9 раз в месяц [51].
Информация
Источники и литература
-
Клинические рекомендации Всероссийского общества неврологов
- Клинические рекомендации Всероссийского общества неврологов - 1. Азимова Ю.Э., Амелин А.В., Алферова В.В., Артеменко А.Р., Ахмадеева Л.Р., Головачева В.А., Данилов А.Б., Екушева Е.В., Исагулян Э.Д., Корешкина М.И., Курушина О.В., Латышева Н.В., Лебедева Е.Р., Наприенко М.В., Осипова В.В., Павлов Н.А., Парфенов В.А., Рачин А.П., Сергеев А.В., Скоробогатых К.В., Табеева Г.Р., Филатова Е.Г. Клинические рекомендации «Мигрень». Журнал неврологии и психиатрии им. С.С. Корсакова. 2022;122(1 3):4 36. 2. Kelman L. The triggers or precipitants of the acute migraine attack. Cephalalgia. 2007; 27(5): 394–402 doi: 10.1111/j.1468-2982.2007.01303.x 3. Goadsby, P.J. Migraine-current understanding and treatment / P.J. Goadsby, R.B. Lipton, M.D. Ferrari // N. Engl. J. Med. - 2002. - Vol. 346 (4). - P. 257-270. 4. Aurora, S.K. Spectrum of illness: understanding biological patterns and relationships in chronic migraine / S.K. Aurora // Neurology. — 2009. — Vol. 72, Suppl. 5. — P. 8-13. 5. Hershey AD. Pediatric headache: update on recent research. Headache: The Journal of Head and Face Pain. 2012; 52(2): 327–332. https://doi.org/10.1111/j.1526-4610.2011.02085.x 6. Silberstein, S.D. Practice parameter: evidence-based guidelines for migraine headache (an evidence-based review): report of the Quality Standards Subcommittee of the American Academy of Neurology / S.D. Silberstein // Neurology. — 2000. — Vol. 55. — P. 754-762. 7. Welch, K.M. Periaqueductal gray matter dysfunction in migraine: cause or the burden of illness? / K.M. Welch, V. Nagesh, S.K. Aurora, N. Gelman // Headache. — 2001. — Vol. 41 (7). - P. 6629-37. 8. Dodick, D. Central sensitization theory of migraine: clinical impli¬cations / D. Dodick, S. Silberstein // Headache. - 2006. - Vol. 46, Suppl. 4. - P. 182-191. 9. Burstein, R. An association between migraine and cutaneous allodynia / R. Burstein, D. Yarnitsky, I. Goor-Aryeh [et al.] // Ann. Neurol. — 2000. — Vol. 47 (5). - P. 614-624. 10. Burstein, R. Managing migraine associated with sensitization / R. Burstein, M. Jakubowski //Handb. Clin. Neurol. - 2010. - Vol. 97. - P. 207-15. 11. Ashkenazi, A. Identifying cutaneous allodynia in chronic migraine using a practical clinical method / A. Ashkenazi, M. Sholtzow, J.W. Shaw [et al.] // Cephalalgia. — 2007. — Vol. 27 (2). — P. 111-7. 12. Bigal, M.E. When migraine progresses: transformed or chronic migraine / M.E. Bigal, R.B. Lipton // Expert Rev. Neurother. — 2006. — № 6 (3). — P. 297-306. 13. Lovati, С. Allodynia in different forms of migraine / C. Lovati, D. D"Amico, S. Rosa [et al.] // Neurol. Sci. - 2007. - Vol. 28. - P. 220-221. 14. Vahlquist, В. Migraine of early onset. A study of thirty one cases in which the disease first appeared between one and four years of age / B. Vahlquist, G.Hackzell// ActaPaediatr. — 1949. — Vol. 38. - P. 622-636. 15. Mortimer, M.J. Epidemiology of headache and childhood migraine in an urban general practice using Ad Hoc, Vahlquist and IHS criteria / M.J. Mortimer, J. Kay, A. Jaron // Dev. Med. ChildNeurol. - 1992. - Vol. 34 (12). - P. 1095-1101. 16. Bille, B.S. Migraine in school children. A study of the incidence and short-term prognosis, and a clinical, psychological and electroencephalographic comparison between children with migraine and matched controls / B.S. Bille // ActaPaediatr. Suppl. — 1962. — Vol. 136. - P. 1-151. 17. Sillan, M. Prevalence of migraine and other headache in Finnish children starting school / M. Sillanpää// Headache. - 1976. -Vol. 15 (4). - P. 288-290. 18. Abu-Arafeh, L. Prevalence of headache and migraine in school children / L. Abu-Arafeh, G. Russell // British Medical Journal. - 1994. - Vol. 309. - P. 765-769. 19. Barea, L.M. An epidemiologic study of headache among children and adolescents of southern Brazil / L.M. Barea, M. Tannhauser, N.T. Rotta // Cephalalgia. — 1996. — Vol. 16(8). — P. 545-549. 20. Lu, S.R. Migraine prevalence in adolescents aged 13—15: a student population-based study in Taiwan / S.R. Lu, J.L. Fuh, K.D. Juang, S.J. Wang // Cephalalgia. — 2000. — Vol. 20 (5). - P. 479-485. 21. Zwart, J.A. The prevalence of migraine and tension-type headaches among adolescents in Norway. The Nord-Trmndelag Health Study (Head-HUNT-Youth), a large population-based epidemiological study / J.A. Zwart, G. Dyb, T.L. Holmen [et al.] // Cephalalgia. - 2004. - Vol. 24 (5). - P. 373-379. 22. Split, W. Epidemiology of migraine among students from randomly selected secondary schools in Lodz / W. Split, W. Neuman // Headache. — 1999. — Vol. 39(7). — P. 494-501. 23. Karli, N. Headache prevalence in adolescents aged 12 to 17: a student-based epidemiological study in Bursa / N. Karli, N. Аkis, M. Zarifoplu[ et al.] // Headache. — 2006. — Vol. 46 (4). — P. 649-655. 24. Табеева Г.Р. Головные боли в общеврачебной практике. Терапевтический архив. 2022. Т. 94. № 1. С. 114-121. 25. Осипова В.В., Филатова Е.Г., Артеменко А.Р. с соавт. Диагностика и лечение мигрени: рекомендации российских экспертов. Журнал неврологии и психиатрии им. C.C. Корсакова 2017; 2: 28-42. 26. Mitsikostas D., Ashina M., Craven A. et al. EHF committee. European headache federation consensus on technical investigation for primary headache disorders. J. Headache Pain. 2015; 17: 5. 27. Осипова В.В., Филатова Е.Г., Артеменко А.Р., Лебедева Е.Р., Азимова Ю.Э., Латышева Н.В., Сергеев А.В., Амелин А.В., Корешкина М.И., Скоробогатых К.В., Екушева Е.В., Наприенко М.В., Исагулян Э.Д., Рачин А.П., Данилов А.Б., Курушина О.В., Парфенов В.А., Табеева Г.Р., Гехт А.Б., Яхно Н.Н. и др. Краткие рекомендации российских экспертов по диагностике и лечению мигрени. РМЖ. 2017. Т. 25. № 9. С. 556-562 28. Gelfand A.A. Pediatric and Adolescent Headache. Continuum (Minneap Minn). 2018; 24(4):1108-1136. doi: 10.1212/CON.0000000000000638 29. Steiner T.J., Jensen R., Katsarava Z., Linde M., MacGregor E.A., Osipova V., et al. Aids to management of headache disorders in primary care (2nd edition) on behalf of the European Headache Federation and lifting the burden: the global campaign against headache. J. Headache Pain. 2019; 20(1): 57. https://doi.org/10.1186/s10194-018-0899-2 30. Mack KJ, Gladstein J. Management of chronic daily headache in children and adolescents. Paediatr Drugs. 2008;10(1):23-9. doi: 10.2165/00148581-200810010-00003. PMID: 18162005. 31. Klein J., Koch T. Headache in Children. Pediatrics in Review 2020; 41(4): 159-171 doi: 10.1542/pir.2017-0012 32. HamalainenM.L. Ibuprofen or acetaminophen for the acute treatment of migraine in children: a double-blind, randomized, placebo-controlled, crossover study / M.L. Hamalainen, K. Hoppu, E. Valkeila [et al // Neurology. — 1997. — Vol. 48. — P. 102-107. 33. Lewis, D.W. Children"s ibuprofen suspension for pediatric migraine / D.W. Lewis, B.Kellstein, G. Dahl [et al.] // Ann. Neurol. — 2001. — Vol. 50 (3), Suppl. 1. — P.93. 34. Hamalainen, M.L. Sumatriptan for migraine attacks in children: a randomized placebo-controlled study. Do children with migraine respond to oral sumatriptan differently than adults? / M.L. Hamalainen, K. Hoppu, P. Santavuori// Neurology. — 1997. - Vol. 48. — P. 1100-1103. 35. Smith, T.R. Sumatriptan and naproxen sodium for the acute treatment of migraine / T.R. Smith, A. Sunshine, S.R. Stark [et al.] // Headache. — 2005. — Vol. 45 (8). — P. 983-991. 36. Ahonen, K. A randomized trial of rizatriptan in migraine attacks in children / К. Ahonen, М. L. Hdmdldinen, М. Eerola, К. Hoppu // Neurology. — 2006. — Vol. 67(7). — P. 1135—40. 37. Linder, S.L. Zolmitriptan provides effective migraine relief in ado¬lescents / S.L. Linder, A.J. Dowson // Int. J. Clin. Pract. — 2000. — Vol. 54. — P. 466-469. 38. Ueberall, М.А. Intranasal sumatriptan for the acute treatment of migraine in children / M.A. Ueberall // Neurology. - 1999. - Vol. 52. - P.1507-1510. 39. Winner, P. Rizatriptan Adolescent Study Group. Rizatriptan 5 mg for the acute treatment of migraine in adolescents: a randomized, double-blind, placebo-controlled study / P. Winner, D. Lewis, W.H. Visser [et al.] // Headache. — 2002. — Vol. 42 (1). — P. 49-55. 40. Lewis, D.W. Practice parameter: pharmacological treatment of migraine headache in children and adolescents: report of the American Academy of Neurology Quality Standards Subcommittee and the Practice Committee of the Child Neurology Society / D.W.Lewis, S.Ashwal, A. Hershey [et al.] // Neurology. - 2004. - Vol. 63 (12). - P. 2215-2224. 41. Нестеровский, Ю.Е. Принципы лечения головных болей у де¬тей и подростков / Ю.Е. Нестеровский, Н.Н. Заваденко // Фарматека. — 2013. — №1. — С. 106—111. 42. Kabbouche, M.A. Tolerability and effectiveness of prochlorperazine for intractable migraine in children / M.A. Kabbouche, A.L. Vockell, S.L. LeCates[etal.] // Pediatrics. — 2001. — Vol. 107 (4). - P. 62. 43. Oskoui M, Pringsheim T, Holler-Managan Y,et al. Practice guideline update summary: Acute treatment of migraine in children and adolescents: Report of the Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of Neurology and the American Headache Society. Neurology. 2019 Sep 10;93(11):487-499. 44. Нестеровский Ю.Е., Заваденко Н.Н., Шипилова Е.М. Первичные головные боли у детей: диагностика и принципы лечения. Consilium Medicum. 2019; 21(9): 74–80. doi: 10.26442/20751753.2019.9.190464 45. Baumann, R.J. Behavioral treatment of migraine in children and adolescents / R.J. Baumann // Paediatr. Drugs. - 2002. - № 4 (9). - P. 555-561. 46. Blume HK, Brockman LN, Breuner CC. Biofeedback therapy for pediatric headache: factors associated with response. Headache. 2012; 52(9):1377-1386. doi: 10.1111/j.1526-4610.2012.02215.x. 47. Powers, S.W., Andrasik F. Biobehavioral treatment, disability, and psychological effects of pediatric headache. Pediatr. Arm. 2005; 34 (6): 461-465. 48. Lewis, D.W. Randomized, double-blind, placebo-controlled study to evaluate the efficacy and safety of topiramate for migraine prevention in pediatric subjects 12 to 17 years of age / D.W. Lewis, P. Winner, J. Saper [et al.] // Pediatrics. — 2009. — Vol. 123 (3). — P. 924-34. 49. Winner, P.Topiramate Pediatric Migraine Study Investigators. Topiramate for migraine prevention in children: a randomized, double-blind, placebo-controlled trial / P. Winner, E.M. Pearlman, S.L. Linder [ et al.] // Headache. — 2005. — Vol. 45 (10). — P. 1304-12. 50. Lakshmi, C.V.Topiramate in the prophylaxis of pediatric migraine: a double-blind placebo-controlled trial / C.V. Lakshmi, P. Singhi, P. Malhi, M. Ray // J. Child. Neurol. — 2007. — Vol. 22 (7). - P. 829-35. 51. Oskoui M, Pringsheim T, Billinghurst L, et al. Practice guideline update summary: pharmacologic treatment for pediatric migraine prevention: report of the Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of Neurology and the American Headache Society. Neurology 2019;93:500–509. 52. Caruso, J.M.The efficacy of divalproex sodium in the prophylactic treatment of children with migraine / J.M. Caruso, W.D. Brown, G. Exil, G.G. Gascon// Headache. — 2000. — Vol. 40. — P. 672-676. 53. Serdaroglu, G. Sodium valproate prophylaxis in childhood migraine / G. Serdaroglu, E. Erhan E., H. Tekgul [et al.] // Headache. — 2002. — Vol. 42. — P. 819-822. 54. Bidabadi, E. A randomized trial of propranolol versus sodium valproate for the prophylaxis of migraine in pediatric patients / E. Bidabadi, M. Mashouf// Paediatr. Drugs. — 2010. — № 12 (4). - P. 269-75. 55. Nalp, A.Comparison of the effectiveness of topiramate and sodium valproate in pediatric migraine / A. Nnalp, N. Uran, A. Oztürk — J. Child. Neurol. — 2008. — Vol. 23 (12). — P. 1377-81. 56. Hikita, T. Effective prophylactic therapy for cyclic vomiting syndrome in children using valproate / T. Hikita, H. Kodama, N. Nakamoto [ et al.] // Brain. Dev. — 2009. — Vol. 31(6). — P. 411-3. 57. Forsythe, W.I. Propranolol (Inderal) in the treatment of childhood migraine / W.I. Forsythe, D. Gillies, M.A. Sills // Dev. Med. Child. Neurol. - 1984. - Vol. 26. - P. 737-741. 58. Ludvigsson, J.Propranolol used in prophylaxis of migraine in children / J. Ludvigsson // Acta Neurol. - 1974. - Vol. 50. - P. 109-115. 59. Hershey, A.D.Effectiveness of amitriptyline in the prophylactic management of childhood headaches / A.D. Hershey, S.W. Powers, A.L. Bentti, T.J. deGrauw // Headache. — 2000. — Vol. 40. - P. 539-549. 60. Guidetti, V. Flunarizine and migraine in childhood: an evaluation of endocrine function / V. Guidetti, B. Moscato, S. Ottaviano [et al.] // Cephalalgia. — 1987. — № 7. — P. 263—266. 61. Sorge, F.Flunarizine in prophylaxis of childhood migraine. A double-blind, placebo-controlled crossover study / F. Sorge, R. DeSimone, E. Marano [et al.] // Cephalalgia. — 1988. — № 8. - P. 1-6. 62. Lewis, D.W. Prophylactic treatment of pediatric migraine / D.W. Lewis, S. Diamond, D. Scott [et al.] // Headache. - 2004. - Vol. 44. - P. 230-237. 63. Ashrafi MR, Salehi S, Malamiri RA, et al. Efficacy and safety of cinnarizine in the prophylaxis of migraine in children: a double-blind placebo-controlled randomized trial. Pediatr Neurol 2014;51:503–508. 64. Gillies, D.Pizotifen (Sanomigran) in childhood migraine. A double-blind controlled trial / D. Gillies, M. Sills, W.I. Forsythe // Eur. Neurol. - 1986. - Vol. 25 (1). - P. 32-5. 65. Symon, D.N.Double blind placebo controlled trial of pizotifen syrup in the treatment of abdominal migraine / D.N. Symon, G. Russell // Arch. Dis. Child. — 1995. — Vol. 72 (1). — P. 48-50. 66. Schoenen, J.Effectiveness of high-dose riboflavin in migraine prophylaxis. A randomized controlled trial / J. Schoenen, J. Jacquy, M. Lenaerts // Neurology. — 1998. — Vol. 50 (2). — P. 466-470. 67. Sándor, P.S.Efficacy of coenzyme Q10 in migraine prophylaxis: a randomized controlled trial / P.S. Sándor, L. Di Clemente, G. Coppola [et al.] // Neurology. — 2005. — Vol. 64 (4). — P. 713-715. 68. Pfaffenrath, V.Magnesium in the prophylaxis of migraine-a--double-blind placebo-controlled study / V. Pfaffenrath, P. Wessely, C. Meyer [et al.] // Cephalalgia. — 1996. —Vol. 16 (6). — P. 436-440. 69. Lipton, R.B. Petasiteshybridus root (butterbur) is an effective preventive treatment for migraine / R.B. Lipton, H. Göbel H, K.M. Einhäupl [ et al.] // Neurology. — 2004. — Vol. 63 (12). — P. 2240-2244.
Информация
Список сокращений
БОС - биологическая обратная связь
ВАШ - визуально-аналоговая шкала
ГБ - головная боль
ДПГДВ - доброкачественное пароксизмальное головокружение детского возраста
ЛИГБ - Лекарственно-индуцированная головная боль
М - мигрень
МА - мигрень с аурой
МбА - мигрень без ауры
МКБ-10 - международная классификация болезней 10-го пересмотра
МКГБ-3 - Международная классификация головных болей 3-го пересмотра
МРТ - магнитно-резонанстная томография
НПВП - нестероидные противовоспалительные и противоревматические препараты (М01А)
ОСВ - околоводопроводное серое вещество
5-НТ-1 - 5-гидрокситриптамин-1
ХЕГБ - хроническая ежедневная головная боль
ХМ - хроническая мигрень
ЭЭГ - электроэнцефалография
CGRP - (англ. Calcitonin Gene-Related Peptide - кальцитонин-ген-родственный пептид (КГРП)
Термины и определения
Мигрень (М) - одна из наиболее распространенных форм первичной головной боли и проявляется повторяющимися приступами головной боли, которые часто сопровождаются сопутствующими симптомами (тошнотой, рвотой, фото- и фонофобией).
Головная боль (ГБ) — это мучительное и лишающее возможностей нормально функционировать состояние, возникающее в случае немногочисленных типов первичной головной боли, таких как мигрень, головная боль напряжения и кластерная головная боль.
Триггерные факторы могут вызвать приступ головной боли. С английского языка trigger переводится как «пуск», «запуск». Триггерные факторы часто путают с причинами ГБ.
Сенситизация — повышенный ответ возбужденных ноцицептивных нейронов на обычную и/или подпороговую стимуляцию.
Аллодиния — это боль вследствие воздействия раздражений, обычно её не вызывающих. Термические или механические повреждения часто приводят к аллодинии в месте повреждения. Аллодинию следует отличать от гипералгезии, то есть повышенной болевой чувствительности на раздражители, обычно вызывающие боль.
Аура — комплекс транзиторных очаговых неврологических симптомов, возникающих непосредственно перед или в самом начале мигренозной головной боли.
Гомонимные зрительные нарушения – это патологическое состояние, при котором человек воспринимает только одну половину (левую или правую) поля зрения, а граница, разделяющая видимую и выпавшую половины, проходит через центральный вертикальный меридиан.
Дизартрия (из др.-греч. — приставка, означающая затруднённость, расстройство — «сочленяю, соединяю») — нарушение произношения вследствие нарушения иннервации речевого аппарата, возникающее в результате поражения нервной системы.
Гипоакузия – снижение остроты слуха.
Атаксия – это нервно-мышечное расстройство моторики, которое характеризуется нарушением координации движений, а также утратой равновесия как в покое, так и при ходьбе.
Парестезия – это специфический вид нарушения чувствительности, который сопровождается субъективными ощущениями покалывания, жжения, ползания мурашек. Является следствием раздражения чувствительных нервных волокон.
Пароксизмальное состояние — это обобщенное понятие, которое включает в себя судорожные и бессудорожные пароксизмы эпилептического и неэпилептического характера. Пароксизмальное состояние — это припадок (приступ) церебрального происхождения, проявляющийся на фоне видимого здоровья или при внезапном ухудшении хронического патологического состояния, характеризующийся кратковременностью, обратимостью возникающих расстройств, наклонностью к повторениям, стереотипностью.
Хроническая мигрень - форма мигрени, которая возникает 15 и более дней в месяц в течение 3 и более месяцев, при этом приступы головной боли имеют мигренозные признаки не менее 8 дней в месяц.
Мигренозный статус - это состояние диагностируют в том случае, когда приступ мигрени (или несколько следующих друг за другом приступов) продолжается более 72 часов (исключая время сна). Мигренозный статус, как правило, является показанием для госпитализации.
Лекарственно-индуцированная головная боль (ЛИГБ) – клиническая разновидность вторичной хронической ГБ, развивающаяся у пациентов с первичными цефалгиями при избыточном применении препаратов для купирования ГБ.
Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
1. Оценка эффекта проводимой терапии
-
Рекомендуется проводить оценку эффекта проводимой терапии по данным дневника головной боли (приложение А3). Снижение частоты приступов на 50% от исходного уровня считается положительным эффектов проводимой профилактической терапии[25, 44].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5.
2. Исходы и прогноз
-
Рекомендуется при лечении приступа применять адекватные дозы рекомендованных препаратов [1, 2, 8, 40, 44].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5.
-
Рекомендуется своевременная госпитализация в случае возникновения мигренозного статуса [1, 2, 24, 31, 40, 42].
Уровень убедительности рекомендаций С, уровень достоверности доказательств - 5.
Критерии оценки качества медицинской помощи
|
№ п/п
|
Критерий качества
|
Оценка выполнения
|
|---|---|---|
|
1.
|
Выполнена клиническая и дифференциальная диагностика формы мигрени
|
Да/Нет
|
|
2.
|
Выполнено МРТ головного мозга (только при наличии подозрений на вторичный характер головной боли) для исключения вторичной причины головной боли
|
Да/Нет
|
|
3.
|
Выполнена терапия мигрени нестероидными противовоспалительными и противоревматическими препаратами и анальгетиками (во время приступа)
|
Да/Нет
|
|
4.
|
При наличии частых или тяжелых приступов мигрени выполнен подбор профилактической терапии с динамическим наблюдением ее эффективности.
|
Да/Нет
|
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Авторы подтверждают отсутствие финансовой поддержки/конфликта интересов, который необходимо обнародовать.
Артеменко Ада Равильевна, д.м.н., профессор кафедры нервных болезней Института Профессионального Образования, ФГАОУ ВО Первый Московский государственный медицинский университет им. И.М. Сеченова Минздрава России (Сеченовский университет)
Бурсагова Бэлла Ибрагимовна, к.м.н., врач-невролог отделения психоневрологии и психосоматической патологии, ст.н.сотр. лаборатории нервных болезней Центра детской психоневрологии, ФГАУ «Национальный медицинский исследовательский центр здоровья детей» Минздрава России
Гузева Валентина Ивановна, д.м.н., профессор, заведующая кафедрой неврологии, нейрохирургии и медицинской генетики ФГБОУ ВО СПбГПМУ, Главный внештатный детский специалист невролог МЗ РФ
Гузева Виктория Валентиновна, д.м.н., профессор кафедры неврологии, нейрохирургии и медицинской генетики ФГБОУ ВО СПбГПМУ
Гузева Оксана Валентиновна, д.м.н., профессор кафедры неврологии, нейрохирургии и медицинской генетики ФГБОУ ВО СПбГПМУ
Заваденко Николай Николаевич, д.м.н. профессор, заведующий кафедрой неврологии, нейрохирургии и медицинской генетики имени академика Л.О. Бадаляна педиатрического факультета Института нейронаук и нейротехнологий ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России. Член международной ассоциации детских неврологов
Кузенкова Людмила Михайловна, д.м.н., профессор, начальник центра детской психоневрологии и психосоматической патологии, ФГАУ «Национальный медицинский исследовательский центр здоровья детей» Минздрава России
Куренков Алексей Львович, д.м.н., заведующий лабораторией нервных болезней Центра детской психоневрологии, ФГАУ «Национальный медицинский исследовательский центр здоровья детей» Минздрава России
Нестеровский Юрий Евгеньевич, к.м.н., доцент кафедры неврологии, нейрохирургии и медицинской генетики имени академика Л.О. Бадаляна педиатрического факультета Института нейронаук и нейротехнологий ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России. Член международной ассоциации детских неврологов
Охрим Инна Владимировна, к.м.н., доцент кафедры неврологии, нейрохирургии и медицинской генетики ФГБОУ ВО СПбГПМУ
Петрова Наталия Валерьевна, к.м.н., врач-клинический фармаколог, заведующая отделением клинической фармакологии ФГАУ «Национальный медицинский исследовательский центр здоровья детей» Минздрава России
Рачин Андрей Петрович – д.м.н., профессор, заместитель директора по научной работе, зав. отделом нейрореабилитации и клинической психологии ФГБУ «Национальный медицинский исследовательский центр реабилитации и курортологии» Министерства здравоохранения Российской Федерации
Сергеев Алексей Владимирович, к.м.н. доцент кафедры нервных болезней и нейрохирургии лечебного факультета ФГАОУ ВО Первый МГМУ им. Сеченова МЗ РФ (Сеченовский Университет). Член общероссийской общественной организации «Российское общество по изучению головной боли». Член европейской общественной организации «Европейская федерация головной боли». Представитель России в международной общественной организации «Международное общество головной боли»
Холин Алексей Александрович, д.м.н., профессор кафедры неврологии, нейрохирургии и медицинской генетики имени академика Л.О. Бадаляна Института нейронаук и нейротехнологий ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России. Член международной ассоциации детских неврологов
Шипилова Елена Михайловна, к.м.н., доцент кафедры неврологии, нейрохирургии и медицинской генетики имени академика Л.О. Бадаляна Института нейронаук и нейротехнологий ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России. Член международной ассоциации детских неврологов
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
-
Врачи-педиатры;
-
Врачи-неврологи;
-
Врачи-психиатры;
-
Психологи;
-
Врачи-неонатологи;
-
Врачи общей практики (семейные врачи);
-
Врачи-рентгенологи
-
Студенты медицинских ВУЗов;
-
Обучающиеся в ординатуре и аспирантуре;
-
Врачи-инфекционисты
-
Врачи функциональной диагностики
Методы, используемые для сбора/селекции доказательств: поиск в электронных базах данных.
Описание методов, использованных для оценки качества и силы доказательств: доказательной базой для рекомендаций являются публикации, вошедшие в Кохрейновскую библиотеку, базы данных EMBASE, MEDLINE и PubMed. Глубина поиска – 10 лет.
Методы, использованные для оценки качества и силы доказательств:
-
консенсус экспертов;
-
оценка значимости в соответствии с рейтинговой схемой.
Методы, использованные для анализа доказательств:
-
обзоры опубликованных мета-анализов;
-
систематические обзоры с таблицами доказательств.
Описание методов, использованных для анализа доказательств
При отборе публикаций, как потенциальных источников доказательств, использованная в каждом исследовании методология изучается для того, чтобы убедиться в ее валидности. Результат изучения влияет на уровень доказательств, присваиваемый публикации, что в свою очередь, влияет на силу рекомендаций.
Для минимизации потенциальных ошибок каждое исследование оценивалось независимо. Любые различия в оценках обсуждались всей группой авторов в полном составе. При невозможности достижения консенсуса привлекался независимый эксперт.
Методы, использованные для формулирования рекомендаций: консенсус экспертов.
Индикаторы доброкачественной практики (Good Practice Points – GPPs)
Рекомендуемая доброкачественная практика базируется на клиническом опыте авторов разработанных рекомендаций.
Экономический анализ
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидации рекомендаций
-
Внешняя экспертная оценка.
-
Внутренняя экспертная оценка.
Описание метода валидации рекомендаций
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых, прежде всего, попросили прокомментировать, насколько доступна для понимания интерпретация доказательств, лежащая в основе рекомендаций.
От врачей первичного звена (педиатров, гастроэнтерологов) получены комментарии в отношении доходчивости изложения данных рекомендаций, а также их оценка важности предлагаемых рекомендаций, как инструмента повседневной практики.
Все комментарии, полученные от экспертов, тщательно систематизировались и обсуждались членами рабочей группы (авторами рекомендаций). Каждый пункт обсуждался в отдельности.
Консультация и экспертная оценка
Проект рекомендаций был рецензирован независимыми экспертами, которых, прежде всего, попросили прокомментировать доходчивость и точность интерпретации доказательной базы, лежащей в основе рекомендаций.
Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД
|
Расшифровка
|
|---|---|
|
1
|
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа
|
|
2
|
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа
|
|
3
|
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая
|
|
5
|
Имеется лишь обоснование механизма действия или мнение экспертов
|
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
|
УДД
|
Расшифровка
|
|---|---|
|
1
|
Систематический обзор РКИ с применением мета-анализа
|
|
2
|
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа
|
|
3
|
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль»
|
|
5
|
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
|
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР
|
Расшифровка
|
|---|---|
|
A
|
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
|
|
B
|
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
|
|
C
|
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
|
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
-
Приказ Министерства здравоохранения и социального развития РФ от 16 апреля 2012 г. N 366н "Об утверждении Порядка оказания педиатрической помощи"
-
Приказ Министерства здравоохранения РФ "Об утверждении Порядка оказания медицинской помощи больным с врожденными и (или) наследственными заболеваниями" от 15 ноября 2012 г. N 917н).
-
Информация о лекарственных препаратах: Государственный реестр лекарственных средств: https://grls.rosminzdrav.ru
-
Федеральный закон от 21 ноября 2011 г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» (Собрание законодательства Российской Федерации, 2011 г., № 48, ст. 6724);
-
Международная классификация болезней, травм и состояний, влияющих на здоровье (МКБ – 10);
-
Приказ МЗ РФ от 23 июля 2010 г. № 541н. Единый квалификационный справочник должностей руководителей, специалистов и служащих, раздел Квалификационные характеристики должностей работников в сфере здравоохранения.
-
Федеральный закон от 25.12.2018 № 489 489-ФЗ «О внесении изменений в статью 40 Федерального закона "Об обязательном медицинском страховании в Российской Федерации" и Федеральный закон "Об основах охраны здоровья граждан в Российской Федерации" по вопросам клинических рекомендаций».
-
Приказ Минздрава России № 103н от 28.02.2019 г. «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации».
-
Приказ Минздрава России от 13.10.2017 N 804н "Об утверждении номенклатуры медицинских услуг".
-
Приказ Министерства труда и социальной защиты РФ от 27 августа 2019 г. 585н «О классификациях и критериях, используемых при осуществлении медико-социальной экспертизы граждан федеральными государственными учреждениями медико-социальной экспертизы»;
-
Приказ Министерство здравоохранения и социального развития Российской Федерации «О порядке применения лекарственных средств у больных по жизненным показаниям» от 9 августа 2005 г. № 494
-
Информационное письмо Минздрава России по возможности закупки лекарственного препарата по торговому наименованию (https://www.rosminzdrav.ru/news/2019/12/18/13043-minzdrav-podgotovil-informatsionnoe-pismo-po-vozmozhnosti-zakupki-lekarstvennogo-preparata-po-torgovomu-naimenovaniyu).
Примеры диагнозов
Мигрень без ауры
Мигрень с аурой
Хроническая мигрень
Хроническая мигрень. ЛИГБ
Дневник головной боли
Дневник головной боли не является общепринятым валидизированным методом, но при этом ведение Дневника головной боли позволяет улучшить контроль за самочувствием пациента, помогает лечащему врачу определить частоту, время возникновения, продолжительность приступов, факторы, вызывающие головную боль, а также влияние проводимой терапии на ГБ.
С помощью родителей в дневнике отмечаются:
-
дата, день недели, когда возникла ГБ
-
время начала и продолжительность ГБ (как долго длился приступ)
-
факторы, которые могли спровоцировать ГБ
-
тяжесть ГБ (насколько сильным был приступ). ГБ может быть легкой, умеренной или сильной в зависимости от влияния на повседневную активность пациента. Либо ГБ оценивается по ВАШ от 1 до 10 баллов, где 10 – это самая сильная боль, которую можно себе представить
-
любые другие симптомы, если они отмечаются наряду с ГБ (например, тошнота, рвота головокружение, чувствительность к свету, звуку, запахам, изменения зрения, сенсорных нарушений и др.).
-
прием лекарств для купирования ГБ (название, время приема, доза) и их эффективность.
Здесь представлен шаблон ежемесячного Дневника головной боли, который может быть использован.

Приложение Б. Алгоритмы действий врача
Алгоритм диагностики и ведения пациента с мигренью
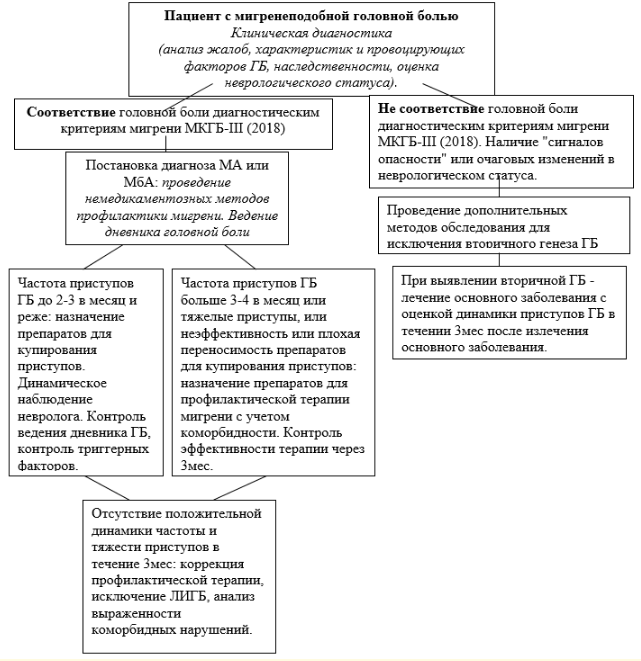

Приложение В. Информация для пациента
Мигрень является хроническим заболеванием центральной нервной системы и в настоящее время нет медикаментозных препаратов способных полностью избавить пациента от приступов ГБ. Но особенностью течения мигрени у детей является высокая вероятность исчезновения приступов мигрени до 18 летнего возраста, что подтверждается в ряде проспективных исследований. Своевременная диагностика, соблюдение здорового образа жизни и исключение наиболее частых провоцирующих факторов позволяют существенно снизить частоту приступов. А обучение правильному купированию приступов и при необходимости назначение медикаментозной профилактической терапии позволяют избежать перехода в хроническую форму мигрень, что определяет более благоприятный прогноз мигрени в детском возрасте по сравнению со взрослыми пациентами. Раннее обращение к врачу позволяет исключить симптоматический характер головной боли, определить лечебную тактику и не допустить хронизации заболевания. Эффект от проводимой терапии может наступить не сразу и требует динамического наблюдения за состояние пациента в течении минимум 3 месяцев. Своевременное выявление и терапия коморбидных заболеваний у пациентов с мигренью позволяют значительно улучшить прогноз течения заболевания.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Не используются.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.