Лимфангиолейомиоматоз
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Другие уточненные интерстициальные легочные болезни (J84.8)
Пульмонология
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «26» ноября 2024 год
Протокол №219
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
ЛИМФАНГИОЛЕЙОМИОМАТОЗ
Лимфангиолейомиоматоз (ЛАМ) - редкое заболевание легких, характеризующееся патологическим разрастанием атипичных гладкомышечных клеток по ходу кровеносных и лимфатических сосудов с разрастанием кистозных образований в легких, ангиолипом почек, лимфангиолейомиом и лимфаденопатии, поражающее в основном женщин детородного возраста.
Код(ы) МКБ-10:
Сокращения, используемые в протоколе:
Лимфангиолейомиоматоз (ЛАМ) - редкое заболевание легких, характеризующееся патологическим разрастанием атипичных гладкомышечных клеток по ходу кровеносных и лимфатических сосудов с разрастанием кистозных образований в легких, ангиолипом почек, лимфангиолейомиом и лимфаденопатии, поражающее в основном женщин детородного возраста.
ВВОДНАЯ ЧАСТЬ
Код(ы) МКБ-10:
| Код | Название |
| J84.81 | Лимфангиолейомиоматоз |
Дата разработки протокола: 2023 год.
Категория пациентов: взрослые.
Пользователи протокола: врачи общей практики, терапевты, пульмонологи, аллергологи, врачи лучевой диагностики, врачи функциональной диагностики, патоморфологи, торакальные хирурги, эндоскописты.
Категория пациентов: взрослые.
Сокращения, используемые в протоколе:
АМЛ – ангиомиолипома
АСТ - аспартатаминотрасфераза
АЛТ - аланинаминотрансфераза
АЧТВ - активированное частичное тромбопластиновое время
АФП – альфа-фетопротеин
БАЛ – бронхо-альвеолярный лаваж
ВАТС – видео ассистированная торакоскопия
ДКТ – длительная кислородотерапия
ЖЕЛ – жизненная емкость легких
КТВР – компьютерная томография высокого разрешения
ЛАМ – лимфангиолейомиоматоз
ЛИП - лимфоидная интерстициальная пневмония
ЛПВП – липопротеиды высокой плотности
ЛПНП – липопротеиды низкой плотности
МДО – мультидисциплинарное обсуждение
МРТ – магнитно-резонансная томография
НЯ – нежелательные явления
ОАК - общий анализ крови
ОБП – органы брюшной полости
ОГК - органы грудной клетки
ОАМ – общий анализ мочи
ОЕЛ - общая емкость легких
ООЛ - общий объем легких
ОФВ1 – объем форсированного выдоха за 1 секунду
ОФВ1/ФЖЕЛ – объем форсированного выдоха за 1 секунду/форсированная жизненная емкость легких
ПТИ - протромбиновый индекс
РО - резервный объем
РКИ – рандомизированные клинические исследования
РсрДЛА – среднее давление в легочной артерии
PaO2 – парциальное давление кислорода
РЭА - раково-эмбриональный антиген
ТББЛ – трансбронхиальная биопсия легкого
ТС - туберозный склероз
ТЭЛА – тромбоэмболия легочной артерии
УЗИ – ультразвуковое исследование
ФВД – функция внешнего дыхания
ФЖЕЛ – форсированная жизненная емкость легких
ХБЛ – хирургическая биопсия легких
CA – cancer antigen
COVID 19 – CoronaVirusDisease 19
CPAP - Continious Positive Airway Pressure
DLco – диффузионная способность легких по монооксиду углерода
FLCN - folliculin
HMB 45 - Human Melanoma Black 45
NYHA - New York Heart Association
mTOR - mammalian target of rapamycin
SpO2 – сатурация крови по пульсоксиметру
TSC2 - TSC complex subunit 2, tuberin
VEGF-D - Vascular Endothelial Growth Factor-D
6MWT – 6 Minute Walk Test
Шкала уровня доказательности:
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты, которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С |
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+).
Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию.
|
| D |
Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
Классификация
Классификация [1-4]:
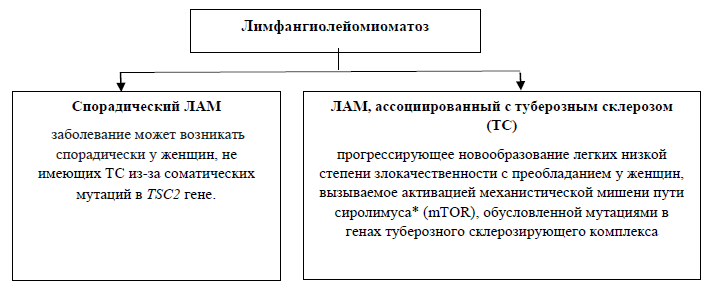
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ [1-10]
Диагностические критерии:
Критерии установления диагноза/состояния:
Критерии диагноза ЛАМ [1-4]
| Достоверный диагноз | Вероятный диагноз | Сомнительный диагноз |
|
Характерная картина КТВР ОГК + морфологическое подтверждение
ИЛИ
Характерные для ЛАМ КТВР паттерн в сочетании с любым из следующих признаков
- ангиолипома почки
- хилезный выпот в грудной или брюшной полости
- лимфангиолейомиома или поражение лимфоузлов характерное для ЛАМ
- верифицированный или подозреваемый туберозный склероз
|
Характерные для ЛАМ КТВР-паттерн и клиническая картина
ИЛИ
Возможные при ЛАМ изменения по КТВР в сочетании с любым из следующих признаков
- ангиолипома почки
- хилоторакс или хилезный асцит
|
Характерные или возможные радиологический признак |
Жалобы:
• прогрессирующая одышка при нагрузке
• кашель, непродуктивный, на поздних стадиях болезни присоединение выделения мокроты
• боль в грудной клетке
• кровохарканье
Анамнез:
• женщины фертильного возраста
• рецидивирующие пневмотораксы
• рецидивирующие хилотораксы
• повторные респираторные инфекции
Физикальное обследование:
• ослабление дыхания при развитии пневмоторакса, хилоторакса
• неспецифические симптомы:
- наличие пальпируемых образований в брюшной полости и малом тазу
- парестезии
- синдромы сдавливания внутренних органов
• признаки дыхательной недостаточности
• признаки легочной гипертензии при прогрессировании заболевания:
- диффузный серо-пепельный цианоз
- усиление II тона над легочной артерией
- тахикардия
- периферические отеки
Основные лабораторные исследования:
Дополнительные лабораторные исследования:
Характерное количество кист 10 и более [11], но КТВР совместима с легочным ЛАМ, когда имеется даже небольшое количество (>2 и <10) [13]. Окружающая кисты легочная паренхима содержит мелкие эмфизематозные изменения, не связанные с курением.
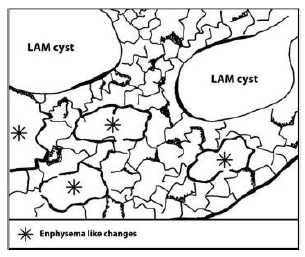
Рисунок 3. Приближенная к кистам паренхима имеет мелкие эмфизематозные изменения, отмеченные звездочками [11-12].

• многочисленные легочные кисты (А)
• Матовость в правой верхней доле (нарушение лимфооттока) (А).
2. Паренхиматозные узелки.
3. Плевральные изменения.
4. Грудная лимфаденопатия.
5. Хилезный выпот, пневмоторакс.
6. Уплотнение по типу матового стекла не часто, указывает на застой лимфы [15].
7. Диффузные очаги (не часто) [15].
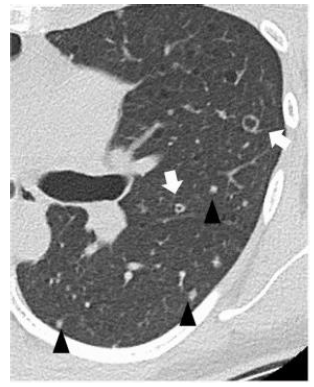
Рисунок 7. Диффузные узелки отмечены черными стрелками. Единичные кисты белыми стрелками.
Пульсоксиметрия:
Тест с 6-минутной ходьбой (6MWT) для оценки:
• степени утраты физической активности и трудоспособности
• прогрессирования заболевания
• ответа на лечение
УЗИ брюшной полости и органов малого таза:
• выявление ангиомиолипом/лимфангиолейомиом или лимфаденопатии
Исследование диффузионной способности легких по моноооксиду углерода (Dlco):
• DLсо <60% от д.в - более чувствительный, чем спирометрия, индикатор ранней стадии заболевания
ЭхоКГ с определением РсрЛА
Показания:
Лабораторные исследования:
Основные лабораторные исследования:
• общий анализ крови (эритроцитоз, может быть лимфопения).
• биохимические анализы – билирубин общий, билирубин прямой, общий белок, АЛТ, АСТ, креатинин, мочевина (гипопротеинемия).
• липидограмма (гиперхолестеринемия).
• коагулограмма – фибриноген, АЧТВ, ПТИ, тромбиновое время.
• Д-димер.
• общий анализ мочи (может быть, гематурия при крупных ангиолипомах).
Дополнительные лабораторные исследования:
• Сывороточный VEGF-D ≥800 пг/мл.
Тестирование необходимо для установления диагноза ЛАМ до рассмотрения вопроса о диагностической биопсии легких.
• Исследование газов артериальной крови (гипоксемия, нормогиперкапния).
• Цитология биологических сред (плевральная жидкость, БАЛ, асцитическая жидкость, лимфатический узел, лимфангиолейомиома) (высокое содержание лимфоцитов, триглицеридов, общего количества клеточных элементов).
Основные инструментальные исследования:
Инструментальные исследования
Основные инструментальные исследования:
Компьютераная томография высокого разрешения (КТВР) является обязательным методом обследования для всех пациентов с предполагаемым ЛАМ [20].
Характерные особенности ЛАМ на КТВР (рис.2-7)
1. Кисты являются отличительным признаком ЛАМ и присутствуют у всех пациентов (рис. 2). Их внешний вид, размер и контур значительно различаются, обычно от 2–5 мм в диаметре, но иногда и до 25-30 мм [13], обычно округлые, чаще с верхним и центральным преобладанием [11]. Толщина стенки кисты колеблется от едва заметной до 2 мм в большинстве серий, есть наблюдаения – до 4 мм [13], [16].
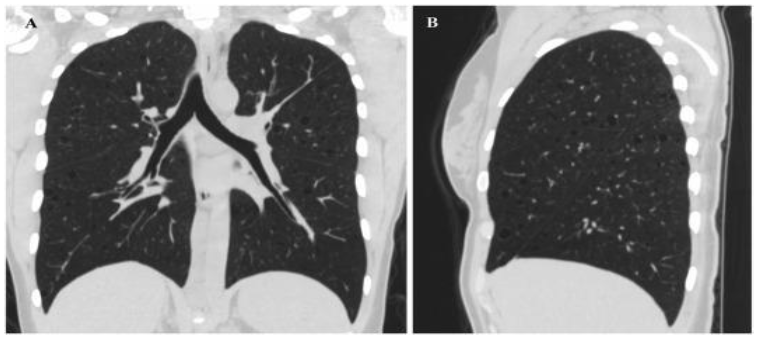
Рисунок 2. Множественные кисты при ЛАМ. А - коронарная реконструкция, В - сагиттальная реконструкция [11].

Рисунок 2. Множественные кисты при ЛАМ. А - коронарная реконструкция, В - сагиттальная реконструкция [11].
Характерное количество кист 10 и более [11], но КТВР совместима с легочным ЛАМ, когда имеется даже небольшое количество (>2 и <10) [13]. Окружающая кисты легочная паренхима содержит мелкие эмфизематозные изменения, не связанные с курением.

Рисунок 3. Приближенная к кистам паренхима имеет мелкие эмфизематозные изменения, отмеченные звездочками [11-12].


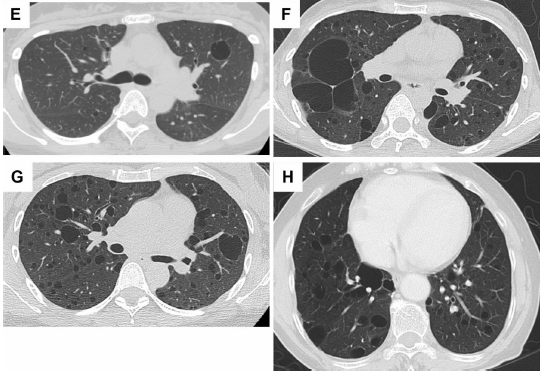
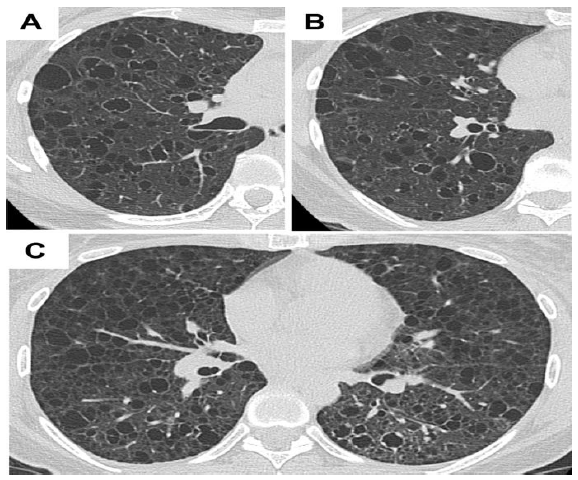
Рисунок 4. Обычные кистозные проявления в отдельности или с сосуществованием крупных кист [15]:
• многочисленные легочные кисты (А)
• кисты от умеренной до тяжелой степени (B)
• не выраженные кисты (C, D)
• немногочисленные кисты (E)
• большие кисты с типичными характеристиками (F)
• несколько крупных кист(G)
• большие кисты преобладают правом легком (H)
Некоторые из кист с неравномерно утолщенными стенками, имеющие «точечный вид» (A,B).
Плотность паренхимы легких вокруг кист с неравномерно утолщенными стенками в левом легком увеличилась по сравнению с правым легким, что указывает на застой лимфы в левом легком (C).
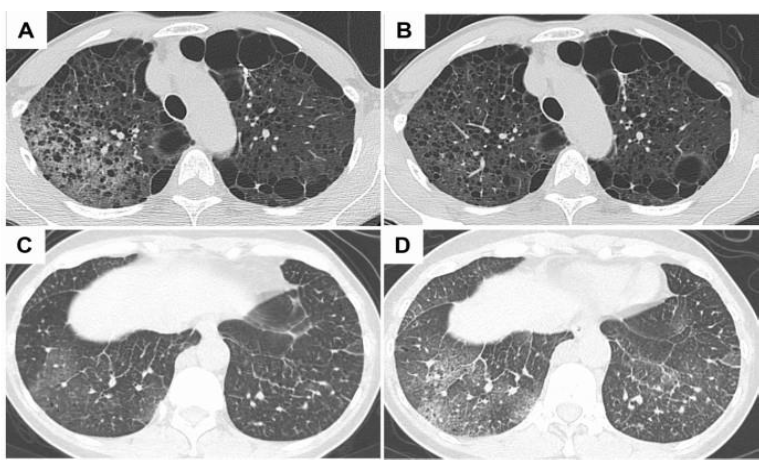

Рисунок 5. Кисты с толстыми стенками.
Некоторые из кист с неравномерно утолщенными стенками, имеющие «точечный вид» (A,B).
Плотность паренхимы легких вокруг кист с неравномерно утолщенными стенками в левом легком увеличилась по сравнению с правым легким, что указывает на застой лимфы в левом легком (C).

Рисунок 6. Симптом матового стекла.
• Матовость в правой верхней доле (нарушение лимфооттока) (А).
• Уменьшение матовости в динамике (В).
• Матовость с утолщением междолькового интерстиция (нарушение лимфооттока) (С).
• Нарастание матовости в динамике (D).
2. Паренхиматозные узелки.
Чаще наблюдаются у пациентов с ЛАМ, асоциированным с туберозным склерозом, реже при спорадической форме. Размер узелков варьирует от 1 до 10 мм, обычно преобладает в верхних долях и по периферии.
3. Плевральные изменения.
Пневмоторакс встречается примерно в 40–70% случаев. У трети пациентов может возникнуть односторонний или двусторонний хилоторакс.
4. Грудная лимфаденопатия.
Расширение грудного протока и увеличение размеров медиастинальных лимфоузлов (1 см и более по короткой оси и 1,5 см и более по длинной оси) являются типичными проявлениями ЛАМ. Ретрокруральная лимфаденопатия встречается у 26% больных.
5. Хилезный выпот, пневмоторакс.
6. Уплотнение по типу матового стекла не часто, указывает на застой лимфы [15].
7. Диффузные очаги (не часто) [15].

Рисунок 7. Диффузные узелки отмечены черными стрелками. Единичные кисты белыми стрелками.
Спирометрия
Функциональные тесты легких следует повторять каждые 3–6 месяцев у пациентов с прогрессирующим заболеванием и каждые 6–12 месяцев у пациентов со стабильным течением болезни.
Обструктивные вентиляционные нарушения:
ОФВ1/ФЖЕЛ <70%
ОФВ1 <80%
Пульсоксиметрия:
• прогрессирующая десатурация крови < 95%.
Тест с 6-минутной ходьбой (6MWT) для оценки:
• степени утраты физической активности и трудоспособности
• прогрессирования заболевания
• ответа на лечение
УЗИ брюшной полости и органов малого таза:
• выявление ангиомиолипом/лимфангиолейомиом или лимфаденопатии
Дополнительные инструментальные исследования:
Обзорная рентгенография грудной клетки - с подозрением на ЛАМ для верификации диагноза не рекомендуется в связи с ее низкой информативностью. В 50% информативна при выявлении спонтанного пневмоторакса.
Исследование диффузионной способности легких по моноооксиду углерода (Dlco):
• DLсо <60% от д.в - более чувствительный, чем спирометрия, индикатор ранней стадии заболевания
Бодиплетизмография
• снижение ОЕЛ<81-85%, ЖЕЛ<81-85% и /или ОЕЛ<81-85%
• снижение ООЛ <85%
• снижение РО выдоха <80% должной величины
ЭхоКГ с определением РсрЛА
Показания:
• тяжелое течение заболевания
• на фоне длительной кислородной терапии
• при планировании трансплантации легких
Биопсии:
КТ брюшной полости и малого таза
Показания:
• выявление ангиомиолипом/лимфангиолейомиом или лимфаденопатии
• уточнение локализации ангиолипом
• оценка динамики размеров ангиолипом
Более чувствительный и специфичный метод, чем ультразвуковое исследование, и может обнаруживать опухоли <1 см в диаметре.
Магнитно-резонансная томография (МРТ) брюшной полости и малого таза:
• диагностика жиросодержащих опухолей, при противопоказании применения йодсодержащего контраста. МРТ головного мозга:
• выявление менингиом при наличии симптомов
• в случаях терапии прогестероном.
Показания:
• выявление ангиомиолипом/лимфангиолейомиом или лимфаденопатии
• уточнение локализации ангиолипом
• оценка динамики размеров ангиолипом
Более чувствительный и специфичный метод, чем ультразвуковое исследование, и может обнаруживать опухоли <1 см в диаметре.
Магнитно-резонансная томография (МРТ) брюшной полости и малого таза:
• диагностика жиросодержащих опухолей, при противопоказании применения йодсодержащего контраста. МРТ головного мозга:
• выявление менингиом при наличии симптомов
• в случаях терапии прогестероном.
Биопсии:
Показания:
На КТВР - кистозные аномалии в легких, характерные для ЛАМ при отсутствии подтверждающих клинических или внелегочных рентгенологических признаков (комплекс туберозного склероза, ангиомиолипомы, хилезный плевральный выпот или асцит, кистозные лимфангиолейомиомы) и/или недоступности проведения исследования VEGF-D.
Видеоторакоскопическая биопсия легких
Морфологическое исследование ткани легкого:
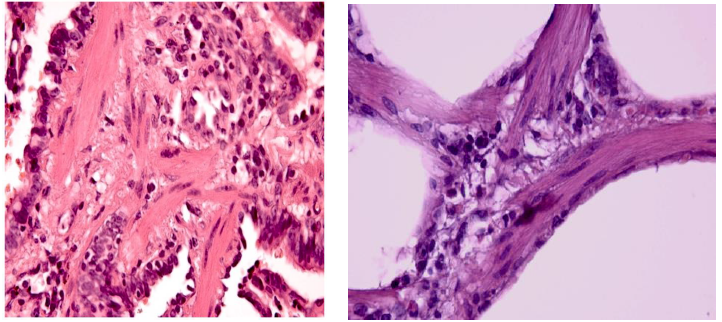
Рисунок 8. Морфологическая картина ЛАМ - хаотическое расположение пучков гладкомышечных клеток в стенке альвеол и строме.
Трансбронхиальная биопсия легких
Малоинвазивный, безопасный и эффективный метод установления диагноза ЛАМ, исключающий необходимость хирургической биопсии легких более чем у 50% пациентов.
Осложнения (риск 2 - 14%):
кровотечения
пневмоторакс
Видеоторакоскопическая биопсия легких
Осложнения (риск 10-19%):
• кровотечения
• пневмоторакс
Смертность от осложнений 1,5-4,5%.
Морфологическое исследование ткани легкого:
• Макроскопически: легочная ткань плотная, множественные мелкие кисты с субплевральным расположением от 0,5-1,5 см в диаметре, белесоватые, заполненные жидкостью.
• Микроскопическая картина: одновременное присутствие множественных
мелких воздушных кист и наличие мультифокальной узловой пролиферации 2 основных видов ЛАМ-клеток - незрелых гладкомышечных и периваскулярных эпителиоидных клеток.
При неспецифической морфологической картине, особенно на ранних стадиях заболевания, целесообразно проведение иммуногистохимического исследования для выявления экспрессии α-гладкомышечного актина и НМВ-45. (рис.8)

Остеоденситометрия
Показания:
Всем пациенткам с ЛАМ, особенно в постменопаузе. Выявляется снижение минеральной плотности костной ткани.
Показания для консультации специалистов:
• эндоскопист - для решения вопроса о возможности проведения ТББЛ
• торакальный хирург – для решения вопроса о возможности проведения хирургической биопсии легких
• мультидисциплинарное обсуждение (МДО) - врач-пульмонолог, врач-рентгенолог, эндоскопист и врач-патоморфолог с опытом диагностики ЛАМ с целью постановки диагноза, определения лечебно-диагностической тактики.
Диагностический алгоритм:
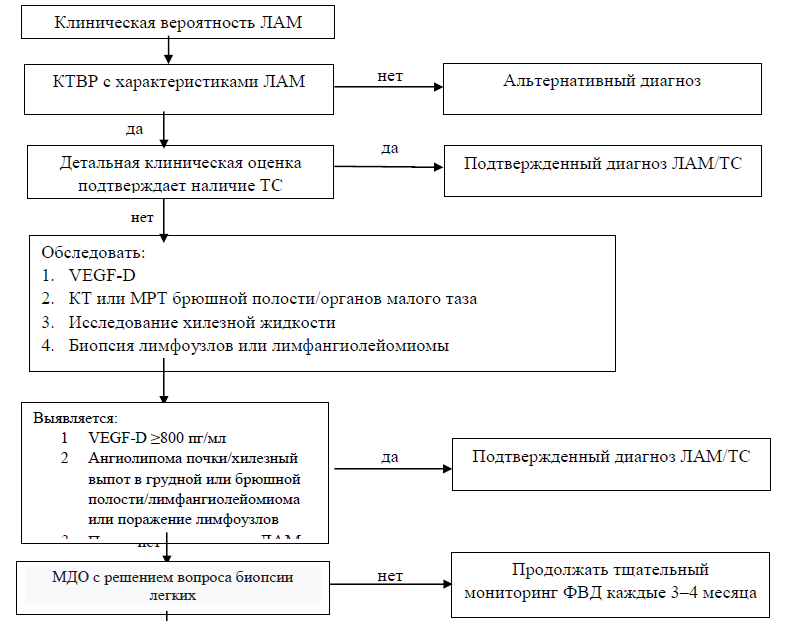

Рисунок 9. Диагностический алгоритм при ЛАМ
Диагностический алгоритм:


Рисунок 9. Диагностический алгоритм при ЛАМ
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований [2,4,14,17-18,19,21]:
| Диагноз | Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Гистиоцитоз Х |
Непродуктивный кашель, одышка, боль и припухлость мягких тканей, кожная сыпь, полидипсия, полиурия.
Факторы риска - курение
|
ВРКТ ОГК
Биопсия
Радиологическое исследование скелета (череп, лицевая кость, позвоночник)
МРТ головного мозга
УЗИ ОБП
|
Чаще встречается у мужчин.
Мелкие тонко- и толстостенные деформированные кисты до 10 мм., преимущественно в верхних долях, интерстициальные очажки 1-5 мм, бронхоцентрические кавитирующие узелки, ветвящиеся или нерегулярные кисты; непораженные реберно-диафрагмальные углы.
Рентген костей (череп, лицевая кость, позвоночник) выявляет очаги деструкции, в челюсти при выраженной альвеолярной резорбции эффект «парящих зубов».
МРТ головного мозга в гипоталамо-гипофизаной области визуализируется новообразование как едва заметное утолщение ножки и в виде крупной опухоли.
УЗИ ОБП – гепатомегалия, холангит и спленомегалия.
Гистологически – деструктивный бронхиолит с формированием бронхоцентричес-ких и перибронхиоляр-ных макрофагов, клетки Лангерганса (дендритные клетки –один из вариантов клеток мононуклеарного ряда)
|
| Лимфоцитарная интерстициальная пневмония | Одышка, с развитием заболевания прогрессирует, малопродуктивный кашель. |
ВРКТ ОГК
ТББЛ
DLco
|
Крупные единичные кисты, преимущественно в базальных отделах, некоторые с внутренними мягкими тканями могут сосуществовать с узелками; помутнение по типу «матовое стекло» и «дерева в почках», лимфомой; утолщение междольковых перегородок, зоны консолидации. У женщин фертильного возраста ЛИП сочетается с заболеваниями соединительной ткани, особенно с синдромом Шегрена.
Гистология: лимфоцитарная интерстициальная инфильтрация, перибронхиальная лимфоидная пролиферация
Снижение DLco
|
| Буллезная эмфизема легких | Одышка, кашель не продуктивный. |
ВРКТ ОГК
Бодиплетизмография
Альфа-1-антитрипсин
|
Крупные размеры кист, субплевральное расположение, утолщение стенок бронхов, парасептальная, центриацинарная и панацинарная эмфизема. Эмфизема на поздних стадиях может выглядеть аналогично запущенной кистозной болезни легких при ЛАМ; фиброз может имитировать стенкикисты; распространение эмфиземы от этиологии; при ЛАМ типичные кисты, разделенные нормальной паренхимой в наименее пораженных участках.
Снижение уровня альфа-1-антитрипсина в сыворотке крови.
Бодиплетизмография: снижение ОЕЛ
|
| Кистозные метастазы в легкие | Одышка, кашель с прожилками крови, похудание |
ВРКТ ОГК
Биопсия
Онкомаркеры
УЗИ брюшной полости, почек, молочной железы, матки.
|
Единичные тонкостенные кисты разных размеров, солидные и кистозные узелки хаотичного распределения.
На УЗИ брюшной полости, почек, молочной железы и матки визуализируются образования различных размеров.
Гистология: аденокарцинома, хориокарцинома, плоскоклеточный.
Повышение уровня СА 125, СА 15-3, РЭА, АФП
|
| Синдром Берта-Хогга-Дюбе | Одышка, папулезная сыпь на лице |
ВРКТ
Бодиплетизмография
УЗИ почек
Онкомаркеры
|
Меньше кист с характерным субплевральным расположением и характерной формой кист; аутосомно-доминантное наследование.
Отягощенная наследственность, наличие рака почек.
Мутация в гене FLCN.
Снижение ОЕЛ на бодиплетизмографии.
УЗИ почек визуализирует образования в почках, гистологических различных типов.
|
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
1. Немедикаментозное лечение [1,38,40]:
Длительная кислородотерапия (ДКТ) пациентам с ЛАМ с клинически значимой гипоксемией в покое (SрO2 <88% при дыхании комнатным воздухом).
Легочная реабилитация (включающие аэробные и силовые тренировки).
Вакцинация против гриппа и пневмококковой инфекции, COVID-19.
2. Медикаментозное лечение [1,2,17-18,38-41]:
Сиролимус* – иммунодепрессант, ингибитор mTOR и киназ.
До начало терапии сиролимусом* определить:
ОАК
липидный профиль (холестерин, триглицериды, холестерин-ЛПВП, холестерин-ЛПНП)
ОАМ
Показания к назначению сиролимуса*:
ОФВ1<70% от должного значения;
При ОФВ1>70% от должного значения:
- повышенный остаточный объем (>120% от должного);
- уменьшение диффузионной способности (DLco<80% от должного);
- десатурация, индуцированная физической нагрузкой (SaO2<90% от должного при 6MWT);
- гипоксемия покоя (РаО2 < 70 мм рт. ст.);
- прогрессирование заболевания (годовая потеря ОФВ1>90 мл/год).
рефрактерные хилезные выпоты, ангиомиолипомы ≥4 см
Перечень основных лекарственных средств [1,17,18,29,30,31,39].
| Фармакотерапевтическая группа | МНН ЛС | Способ применения | УД |
| Иммунодепрессант, ингибитор mTOR и киназ | Сиролимус* | 1-2 мг/сутки внутрь. Через 14 дней лечения измерить минимальный уровень сиролимуса* в сыворотке. Уровень сиролимуса* в крови должен быть 5-15 нг/мл. При медленном прогрессировании болезни начальная доза сиролимуса* 1 мг/сутки. При быстром прогрессировании начинать с 2 мг/сутки и постепенно снижать дозу, до достижения ответа. В случаях крупных ангиомиолипом почек до 6 мг/сутки. | В |
Перечень дополнительных лекарственных средств (менее 100% вероятность назначения) [27-32,35].
| Фармакотерапевтическая группа | МНН ЛС | Способ применения | УД |
| Статины | Симвастатин | 10 или 20 мг 1 раз в сутки вечером, внутрь, не разжевывая и не измельчая таблетку, проглатывать целиком, запивая достаточным количеством воды. | А |
| М-холинолитик/β2 –агонист | Фенотерола гидробромид/ипратропия бромида моногидрат | Ингаляционно по 10-20 капель + 0,9% раствор натрия хлорида 4-5 мл через небулайзер 2-3 раза в сутки. | А |
При развитии осложнений ЛАМ требуется дополнительная терапия, в соответствии с КП развившихся патологических состояний – тяжелая ДН, пневмоторакс, присоединение вторичных инфекций, бронхообструктивный синдром [20-29].
Статины (симвастатин) назначается при ЛАМ пациентам с хилотораксом, гиперлипидемией. Комбинация сиролимуса* и симвастатина обладают синергическим эффектом: ингибирует рост опухоли ксенотрансплантата, повышают регуляцию VEGF-D в условиях нормоксии (высокие уровни VEGF-D усиливает лимфангиогенез в узлах ЛАМ, выравнивают кисты легких, влияя на DLCO), предотвращает развитие кистозных поражений легких, блокирует активацию матриксной металлопротеиназы и предотвращает разрушение альвеол [30-32,35].
Бронхолитическая терапия небулизированной комбинацией М-холинолитика с β2 –агонистом - фенотерола гидробромид 500 мкг / ипратропия бромида моногидрат 261 мкг - показана пациентам с ЛАМ в случае развития бронхиальной обструкции на фоне прогрессирования [27-29].
Антибактериальная терапия показана пациентам с ЛАМ в случаях присоединения вторичной бактериальной пневмонии в соответствии с КП МЗ РК «Внебольничная пневмония». При развитии госпитальной инфекции у пациентов с ЛАМ антибактериальная терапия проводится в соответствии с международными клиническими рекомендациями [33,34].
3. Хирургическое вмешательство: нет.
4. Дальнейшее ведение [1,40,41]:
1. 1 раз в месяц в течение первых 3 месяцев, затем через каждые 3 месяца контроль:
уровня сиролимуса* в крови
общий анализ крови
липидный профиль (холестерин, триглицериды, холестерин-ЛПВП, холестерин-ЛПНП)
общий анализ мочи
2. Спирометрия каждые три месяца для пациентов с прогрессированием заболевания, 1 раз в год для стабильных пациентов
3. Контроль веса, отказ от курения
4. Легочная реабилитация,
5. Вакцинация от гриппа и пневмококковой инфекции, избегать применения живых вакцин во время приема сиролимуса*.
6. Отказ от приема комбинированных пероральных контрацептивов (содержащих эстроген, прогестерон), планирование беременности после консультации со специалистом, запрещение приема заместительной гормональной терапии в период постменопаузы.
Индикаторы эффективности лечения и безопасности: см. Стационарный уровень.
Индикаторы эффективности лечения и безопасности: см. Стационарный уровень.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ [1,29-32]
1. Карта наблюдения пациента, маршрутизация пациента (рисунок 10):
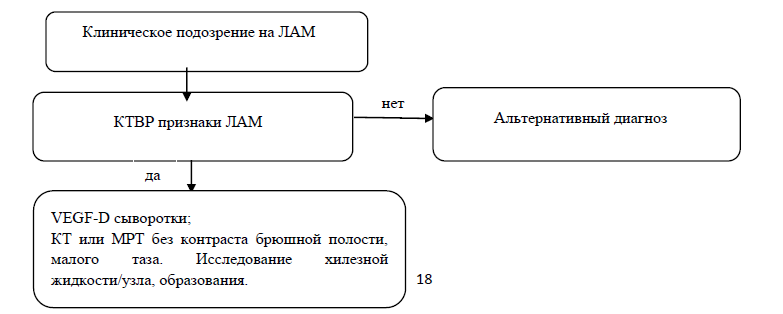
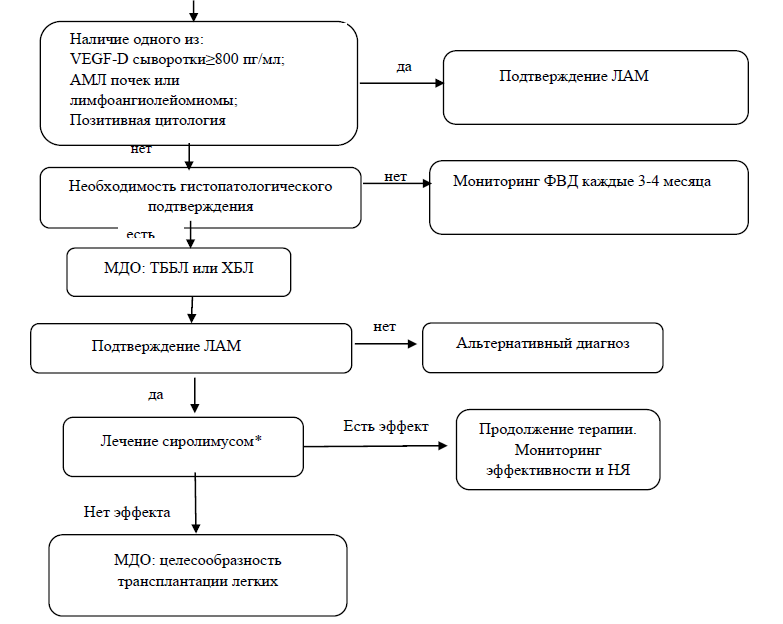
Рисунок 10. Карта наблюдения пациента с ЛАМ
2. Немедикаментозное лечение:
Длительная кислородотерапия (ДКТ) пациентам с ЛАМ с клинически значимой гипоксемией в покое (при SрO2 менее 88% при дыхании комнатным воздухом).
Легочная реабилитация (включающие аэробные и силовые тренировки).
3. Медикаментозное лечение
При госпитализации, независимо от ее причин, показано назначение или продолжение терапии сиролимусом*, при отсутствии клинически значимых побочных эффектов.
Перечень основных лекарственных средств [1,17,18,39-41].
| Фармакотерапевтическая группа | МНН ЛС | Способ применения | УД |
| Иммунодепрессант, ингибитор mTOR и киназ | Сиролимус* | 1-2 мг/сутки внутрь. Через 14 дней лечения измерить минимальный уровень сиролимуса* в сыворотке. Уровень в крови должен быть 5-15 нг/мл. При медленном прогрессировании болезни начальная доза сиролимуса* 1 мг/сутки. При быстром прогрессировании - начинать с 2 мг/сутки постепенно снижая дозу до достижения ответа. В случаях крупных ангиомиолипом почек - до 6 мг/сутки. | В |
*В соответствии с правилами применения ЛС незарегистрированных на территории РК.
Перечень дополнительных лекарственных средств (менее 100% вероятность назначения) [27-32,35].
| Фармакотерапевтическая группа | МНН ЛС | Способ применения и дозировка | УД |
| Статины | Симвастатин | 10 - 20 мг 1 раз в сутки вечером, внутрь | А |
| М-холинолитик/ β2 –агонист |
Фенотерола гидробромид/
ипратропия
бромида моногидрат
|
Ингаляционно по 10-20 капель + 0,9% раствор натрия хлорида 4-5 мл через небулайзер 2-3 раза в сутки. | А |
При развитии осложнений ЛАМ требуется дополнительная терапия, в соответствии с КП МЗ РК развившихся патологических состояний – тяжелая ДН, ТЭЛА, пневмоторакс, присоединение вторичных инфекций, бронхообструктивный синдром, гиперлипидемии [20-29].
Симвастатин назначается при ЛАМ пациентам с хилотораксом, гиперлипидемией. Комбинация сиролимуса* и симвастатина обладают синергическим эффектом: ингибирует рост опухоли ксенотрансплантата, повышают регуляцию VEGF-D в условиях нормоксии (высокие уровни VEGF-D усиливает лимфангиогенез в узлах ЛАМ, выравнивают кисты легких, влияя на DLCO), предотвращает развитие кистозных поражений легких, блокирует активацию матриксной металлопротеиназы и предотвращает разрушение альвеол [30-32,35].
Антикоагулянты рекомендуется использовать у пациентов при развитии тромбоэмболических осложнений в соответствии с КП МЗ РК «Тромбоэмболия легочной артерии» [23-26].
Бронхолитическая терапия небулизированной комбинацией М-холинолитика с β2–агонистом - фенотерола гидробромид 500 мкг/ипратропия бромида моногидрат 261 мкг - показана пациентам с ЛАМ в случае развития бронхиальной обструкции на фоне прогрессирования ЛАМ [27-29].
Антибактериальная терапия показана пациентам с ЛАМ в случаях присоединения вторичной бактериальной пневмонии в соответствии с КП МЗ РК «Внебольничная пневмония». При развитии госпитальной инфекции у пациентов с ЛАМ антибактериальная пневмония проводится в соответствии с международными клиническими рекомендациями [33,34].
4. Хирургическое вмешательство [19,36,37]:
Трансплантация легких
Показания к трансплантации легких:
1. Функциональный класс III или IV по NYHA (Нью-Йоркская кардиологическая ассоциация)
2. Тяжелые нарушения функции легких:
ОФВ1 ≤ 25% от должного значения
DLсо ≤ 27% от должного значения
гипоксемия в покое
Выживаемость после трансплантации 76, 56 и 51% через 1, 3 и 5 лет соответственно.
5. Дальнейшее ведение [1,40,41]:
1. 1 раз в месяц в течение первых 3 месяцев, затем через каждые 3 месяца контроль:
уровня сиролимуса* в крови
общий анализ крови
липидный профиль (холестерин, триглицериды, холестерин-ЛПВП, холестерин-ЛПНП)
общий анализ мочи
3. Спирометрия каждые 3 месяца для пациентов с прогрессированием заболевания, 1 раз в год - для стабильных пациентов
4. Контроль веса, отказ от курения
5. Легочная реабилитация,
6. Вакцинация от гриппа и пневмококковой инфекции, избегать применения живых вакцин во время приема сиролимуса*.
7. Отказ от приема комбинированных пероральных контрацептивов (содержащих эстроген, прогестерон), планирование беременности после консультации со специалистом, запрещение приема заместительной гормональной терапии в период постменопаузы.
6. Индикаторы эффективности лечения [40-41]:
Клиническое улучшение: наличие не менее двух следующих критериев в течение двух последовательных визитов в период от 3 до 6 месяцев лечения:
1.Уменьшение степени одышки.
2.Снижение уровня VEGF-D в сыворотке.
3.Уменьшение объема ангиомиолипом, лимфангиолейомиом и хилезных скоплений.
4.Функциональное улучшение (наличие не менее 2-х критериев):
увеличение ФЖЕЛ ≥ 10 % (минимум 200 мл)
увеличение DLco ≥ 15% (минимум 3 мл/мин/мм Hg)
повышение SaO2 или PaO2 при проведении 6MWT (≥ 4% единиц, ≥ 4 мм Hg)
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации
• проведение биопсии легких
• подготовка к трансплантации легких
• трансплантация легких
Показания для экстренной госпитализации:
• обострении ЛАМ (нарастание одышки, ухудшение оксигенации)
• развитие осложнений ЛАМ (тромбоэмболия легочной артерии, пневмоторакс, острая инфекция нижних дыхательных путей).
Показания к выписке пациента из стационара:
• стабилизация клинического состояния;
• SpO2 не ниже 93% в покое при дыхании комнатным воздухом или на фоне кислородотерапии.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- 1. Francis X. McCormack et al. Official American Thoracic Society/Japanese Respiratory Society Clinical Practice Guidelines: Lymphangioleiomyomatosis Diagnosis and Management. Am J Respir Crit Care Med Vol 194, Iss 6, pp 748–761. 2017. 2. Gupta N, Finlay GA, Kotloff RM, Strange C, Wilson KC, Young LR, Taveira-DaSilva AM, Johnson SR, Cottin V, Sahn SA, Ryu JH, Seyama K, Inoue Y, Downey GP, Han MK, Colby TV, Wikenheiser-Brokamp KA, Meyer CA, Smith K, Moss J, McCormack FX; ATS Assembly on Clinical Problems. Lymphangioleiomyomatosis Diagnosis and Management: High-Resolution Chest Computed Tomography, Transbronchial Lung Biopsy, and Pleural Disease Management. An Official American Thoracic Society/Japanese Respiratory Society Clinical Practice Guideline. Am J Respir Crit Care Med. 2017 Nov 15;196(10):1337-1348. doi: 10.1164/rccm.201709-1965ST. PMID: 29140122; PMCID: PMC5694834. 3. Johnson SR, Cordier JF, Lazor R, Cottin V, Costabel U, Harari S, Reynaud-Gaubert M, Boehler A, Brauner M, Popper H, Bonetti F, Kingswood C; Review Panel of the ERS LAM Task Force. European Respiratory Society guidelines for the diagnosis and management of lymphangioleiomyomatosis. Eur Respir J. 2010 Jan; 35(1):14-26. doi: 10.1183/09031936.00076209. PMID: 20044458. 4. C McCarthy, N Gupta, SR Johnson, JJ Yu, FX. McCormack Lymphangioleiomyomatosis: pathogenesis, clinical features, diagnosis, and management Lancet Respir Med, 9 (11) (2021), pp. 1313-1327 5. Young LR, Vandyke R, Gulleman PM, Inoue Y, Brown KK, Schmidt LS, Linehan WM, Hajjar F, Kinder BW, Trapnell BC, Bissler JJ, Franz DN, McCormack FX. Serum vascular endothelial growth factor-D prospectively distinguishes lymphangioleiomyomatosis from other diseases. Chest. 2010 Sep;138(3):674-81. doi: 10.1378/chest.10-0573. Epub 2010 Apr 9. PMID: 20382711; PMCID: PMC2940071. 6. Hirose M, Matsumuro A, Arai T, Sugimoto C, Akira M, Kitaichi M, Young LR, McCormack FX, Inoue Y. Serum vascular endothelial growth factor-D as a diagnostic and therapeutic biomarker for lymphangioleiomyomatosis. PLoS One. 2019 Feb 28;14(2):e0212776. doi: 10.1371/journal.pone.0212776. PMID: 30818375; PMCID: PMC6395035. 7. Li M, Zhu WY, Wang J, Yang XD, Li WM, Wang G. Diagnostic performance of VEGF-D for lymphangioleiomyomatosis: a meta-analysis. J Bras Pneumol. 2022 Mar 14;48(1):e20210337. doi: 10.36416/1806-3756/e20210337. PMID: 35293487; PMCID: PMC8964149. 8. Cottin V, Harari S, Humbert M, Mal H, Dorfmüller P, Jaïs X, Reynaud-Gaubert M, Prevot G, Lazor R, Taillé C, Lacronique J, Zeghmar S, Simonneau G, Cordier JF; Groupe d'Etudes et de Recherche sur les Maladies "Orphelines" Pulmonaires (GERM"O"P). Pulmonary hypertension in lymphangioleiomyomatosis: characteristics in 20 patients. Eur Respir J. 2012 Sep; 40(3):630-40. doi: 10.1183/09031936.00093111. Epub 2012 Feb 23. PMID: 22362861. 9. Koba T, Arai T, Kitaichi M, Kasai T, Hirose M, Tachibana K, Sugimoto C, Akira M, Hayashi S, Inoue Y. Efficacy and safety of transbronchial lung biopsy for the diagnosis of lymphangioleiomyomatosis: A report of 24 consecutive patients. Respirology. 2018 Mar; 23(3):331-338. doi: 10.1111/resp.13190. Epub 2017 Sep 28. PMID: 28960664. 10. Xu W, Cui H, Liu H, Feng R, Tian X, Yang Y, Xu KF. The value of transbronchial lung biopsy in the diagnosis of lymphangioleiomyomatosis. BMC Pulm Med. 2021 May 3;21(1):146. doi: 10.1186/s12890-021-01518-2. PMID: 33941134; PMCID: PMC8091759.17. Eva Revilla López et al. Multidisciplinary Cystic Lung Disease Group. Long term results of sirolimus treatment in lymphangioleiomyomatosis: a single referral centre experience. Scientifc Reports. (2021) 11:10171. 11. Paola Crivelli, Roberta Eufrasia Ledda, Silvia Terraneo, Maurizio Conti, Gianluca Imeri, Elena Lesma, Fabiano Di Marco. Role of thoracic imaging in the management of lymphangioleiomyomatosis. Respiratory Medicine Volume 157, October 2019, Pages 14-20. 12. J. Yao, A.M. Taveira-DaSilva, T.V. Colby, J. Moss. CT grading of lung disease in lymphangioleiomyomatosis. AJR Am. J. Roentgenol., 199 (2012), pp. 787-793. 13. S. R. Johnson, J. F. Cordier, R. Lazor, V. Cottin, U. Costabel, S. Harari, M. Reynaud-Gaubert, A. Boehler, M. Brauner, H. Popper, F. Bonetti, C. Kingswood, the Review Panel of the ERS LAM Task Force. European Respiratory Society guidelines for the diagnosis and management of lymphangioleiomyomatosis. 2017. 14. https://radiopaedia.org/articles/7334. Last revised by Rania Adel Anan on 16 Aug 2023. Acknowledgement: Professor Deborah Yates. 15. Yasuhito Sekimoto, Kazuhiro Suzuki, Makiko Okura, Takuo Hayashi, Hiroki Ebana, Toshio Kumasaka, Keiko Mitani, Koichi Nishino, Shouichi Okamoto, Etsuko Kobayashi, Kazuhisa Takahashi & Kuniaki Seyama. Uncommon radiologic computed tomography appearances of the chest in patients with lymphangioleiomyomatosis. Scientific Reports volume 11, Article number: 7170 (2021) Cite this article. 16. Gupta, N. et al. Accuracy of chest high-resolution computed tomography in diagnosing diffuse cystic lung diseases. Eur. Respir. J. 46, 1196–1199 (2015). 17. Eva Revilla-López et al. Multidisciplinary Cystic Lung Disease Group. Long-term results of sirolimus treatment in lymphangioleiomyomatosis: a single referral centre experience. Scientifc Reports. (2021) 11:10171. 18. Ando K, Kurihara M, Kataoka H, Ueyama M, Togo S, Sato T, Doi T, Iwakami S, Takahashi K, Seyama K, et al. Efficacy and safety of low dose sirolimus for treatment of lymphangioleiomyomatosis. Respir Investig 2013;51:175–183 19. Krishnan Warrior, Daniel F. Dilling. Lung transplantation for lymphangioleiomyomatosis. Heart and Lung transplantation. https://doi.org/10.1016/j.healun.2022.09.02. 20. КП МЗ РК Спонтанный пневмоторакс. https://diseases.medelement.com/disease/спонтанный-пневмоторакс-2018/16089. 21. Mihir Odak, Kajol Anandani, Patrick J. Rogers. Lymphangioleiomyomatosis Presenting as Recurrent Pneumothorax. Cureus. 2020 Oct; 12(10): e11102. doi: 10.7759/cureus.11102 22. S. R. Johnson, J. F. Cordier, R. Lazor, V. Cottin et al. European Respiratory Society guidelines for the diagnosis and management of lymphangioleiomyomatosis. European Respiratory Journal 2010 35: 14-26; DOI: 10.1183/09031936.00076209 23. КП МЗ РК Тромбоэмболия легочной артерии. https://diseases.medelement.com/disease/тромбоэмболия -легочной-артерии -2019/16466. 24. Junshik Hong, Seo-Yeon Ahn, Yoo Jin Lee et al. Updated recommendations for the treatment of venous thromboembolism. Blood Res. 2021, 31; 56(1): 6-16. doi: 10.5045/br.2021.2020083 25. Olga Baranova, Lubov Novikova, Marina Kameneva et al. Difficulties of diagnosis of pulmonary embolism (PE) in patients with lymphangioleiomyomatosis (LAM). European Respiratory Journal 2013 42: P414 26. Günther A, Mosavi P, Ruppert C, Heinemann S, Temmesfeld B, Velcovsky HG, et al. Enhanced tissue factor pathway activity and fibrin turnover in the alveolar compartment of patients with interstitial lung disease. Thromb Haemost. 2000; 83:853–860. doi: 10.1055/s-0037-1613933 27. Stijn E. Verleden, Arno Vanstapel, Laurens De Sadeleer et al. Quantitative analysis of airway obstruction in lymphangioleiomyomatosis. European Respiratory Journal 2020 56: 1901965; DOI: 10.1183/13993003.01965-2019 28. Julie Ng, Gustavo Pacheco-Rodriguez, Lesa Begley et al. The lung microbiome in end-stage Lymphangioleiomyomatosis Respir Res (2021) 22:277 https://doi.org/10.1186/s12931-021-01873-y 29. КП МЗ РК Хроническая обструктивная болезнь легких. https://diseases.medelement.com/disease/хроническая-обструктивная болезнь-легких -2019/17354 30. V. P. Krymskaya et al. A phase II clinical trial of the Safety of Simvastatin (SOS) in patients with pulmonary lymphangioleiomyomatosis and with tuberous sclerosis complex. Respiratory Medicine, Volume 163; 2020:doi.org/10.1016/j.rmed.2020.105898 31. Angelo M. Taveira-DaSilva, Amanda M. Jones, Patricia A. Julien-Williams et al. Retrospective Review of Combined Sirolimus and Simvastatin Therapy in Lymphangioleiomyomatosis. Chest. 2015 Jan; 147(1): 180–187. doi: 10.1378/chest.14-0758. 32. Loboda A, Jazwa A, Jozkowicz A, et al. Angiogenic transcriptome of human microvascular endothelial cells: effect of hypoxia, modulation by atorvastatin. Vascul Pharmacol 2006;44:206–214. 33. Rafael Zaragoza et al. Update of the treatment of nosocomial pneumonia in the ICU. Critical care 2020; 24:383 https://doi.org/10.1186/s13054-020-03091-2 34. КП МЗ РК Внебольничная пневмония у взрослых. https://diseases.medelement.com/disease -2019/1735 35. The Task Force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS). Russian Journal of Cardiology. 2020;25(5):3826 doi:10.15829/1560-4071-2020-3826 36. Joohyung S, Changwon Sh. Indications for Lung Transplantation and Patient Selection. J Chest Surg 2022; 55(4): 255-264. 37. Ji Zhang, Dong Liu et al. Retrospective study of lung transplantation in patients with lympangioleiomyomatosis. Sec Pulmonary Medicine. 2021:V8. https//doi.org/10.3389/fmed.2021.584826 38. Victoria Maria Garcia de Medeiros, Jéssica Gonçalves de Lima, Claudia Rosa et al. Physiotherapy in lymphangioleiomyomatosis: a systematic review. Ann Med. 2022; 54(1): 2744–2751. doi: 10.1080/07853890.2022.2128401. 39. Hu et al. Long-term efficacy and safety of sirolimus therapy in patients with lymphangioleiomyomatosis. Orphanet Journal of Rare Diseases (2019) 14:206 https://doi.org/10.1186/s13023-019-1178-2 40. Vincent Cottin. Treatment of lymphangioleiomyomatosis: building evidence in orphan diseases. European Respiratory Journal 2014 43: 966 969; DOI: 10.1183/09031936.00025314 41. Nishant Gupta, Hye-Seung Lee, Lisa R. Young et al for the NIH Rare Lung Disease Consortium. Analysis of the MILES cohort reveals determinants of disease progression and treatment response in lymphangioleiomyomatosis. European Respiratory Journal 2019. 53: 1802066; DOI:10.1183/13993003.02066-2018.
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола:
1) Бакенова Роза Агубаевна – доктор медицинских наук, ассоциированный профессор, главный терапевт/пульмонолог РГП «Больница Медицинского Центра Управления Делами Президента Республики Казахстан» на ПХВ.
2) Жумагалиева Ардак Назиловна – PhD, врач-пульмонолог, ведущий научный сотрудник отдела науки РГП «Больница Медицинского Центра Управления Делами Президента Республики Казахстан» на ПХВ.
3) Есенгельдинова Мадина Айтпековна - магистр медицины, врач-пульмонолог РГП «Больница Медицинского Центра Управления Делами Президента Республики Казахстан» на ПХВ, главный внештатный пульмонолог Управление общественного здравоохранения города Астана.
4) Бакиева Кымбат Манаткызы – магистр медицины, врач-пульмонолог РГП «Больница Медицинского Центра Управления Делами Президента Республики Казахстан» на ПХВ.
5) Дунь Александр Павлович – врач-радиолог РГП «Больница Медицинского Центра Управления Делами Президента Республики Казахстан» на ПХВ.
6) Нурпеисова Алтын Алданышовна – клинический фармаколог, начальник клинико-фармакологического отдела РГП «Больница Медицинского центра Управления делами Президента Республики Казахстан» на ПХВ;
7) Гаркалов Константин Анатольевич – кандидат медицинских наук, доцент НАО «Медицинский университет Астана», председатель «Республиканской междисциплинарной пульмонологической комиссии» Министерство здравоохранения Республики Казахстан.
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
1) Латыпова Наталья Александровна – доктор медицинских наук, пульмонолог, заведующая кафедрой семейной и доказательной медицины НАО «Медицинский университет Астана», главный внештатный пульмонолог Министерства здравоохранения Республики Казахстан.
2) Пак Алексей Михайлович – кандидат медицинских наук, директор института внутренней медицины АО «Национальный научный медицинский центр», председатель Национального общества респираторной медицины.
Указание условий пересмотра протокола: пересмотр не реже 1 раза в 5 лет и не чаще 1 раза в 3 года при наличии новых методов диагностики и лечения с уровнем доказательности.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.