Коронавирусная инфекция CОVID-19 у взрослых (7 редакция пересмотр 2024 год)
 Версия: Клинические протоколы МЗ РК - 2024 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2024 (Казахстан)
Общая информация
Краткое описание
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
| Решение по установлению МВС- В принимается консилиумом. |
Код(ы) МКБ-10:
| Код | МКБ-10 |
| U07.1 | Коронавирусная инфекция CОVID-19 (Вирус идентифицирован) |
| U07.2 | Коронавирусная инфекция CОVID-19 (Вирус не идентифицирован) |
| U08.9 |
Личный анамнез COVID-19 неуточненный
Этот необязательный код используется для записи более раннего эпизода подтвержденого или вероятного COVID-19, который влияет на состояние здоровья человека, и человек больше не болеет COVID-19. Этот код не следует использовать для составления первичных таблиц смертности.
|
| U10.9 |
Мультисистемный воспалительный синдром, связанный с COVID-19, неуточненный
Имеющий связь по времени с COVID-19:
цитокиновый шторм;
синдром Кавасаки;
мультисистемный воспалительный синдром у детей (Multisystem Inflammatory Syndrome in Children, MIS-C);
детский воспалительный мультисистемный синдром (Paediatric Inflammatory Multisystem Syndrome, PIMS);
Исключено: слизисто-кожный лимфонодулярный синдром [Кавасаки] (M30.3).
|
Код U07.1 соответствует стандартному определению подтвержденного случая,
7 редакция – пересмотр 2024 год.
Категория пациентов: взрослые.
Шкала уровня доказательности:
| А |
Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которой могут быть распространены на соответствующую популяцию.
|
| В |
Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которой могут быть распространены на соответствующую популяцию.
|
| С |
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которой могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которой не могут быть непосредственно распространены на соответствующую популяцию
|
| D |
Описание серии случаев или неконтролируемое исследование, или мнение экспертов.
|
Методология GRADE (Grading of Recommendations Assessment, Development and Evaluation)
|
a. Настоятельная рекомендация в пользу применения
|
Эта рекомендация указывает на сильное рекомендованное использование определенного медицинского вмешательства. Она говорит о том, что польза от применения данного вмешательства превышает возможные риски или негативные последствия. Медицинские профессионалы и пациенты должны уделять особое внимание этой рекомендации.
|
|
b. Условная рекомендация в пользу применения
|
Эта рекомендация указывает на то, что есть некоторые преимущества в использовании определенного медицинского вмешательства, но также есть значимые факторы, которые могут влиять на решение применять его или нет. Принятие решения об использовании данной рекомендации должно основываться на индивидуальных предпочтениях пациента и клиническом контексте.
|
|
c. Условная рекомендация не применять
|
Эта рекомендация указывает на то, что, хотя есть некоторые доказательства в пользу использования медицинского вмешательства, имеются также значительные факторы, которые могут отрицательно повлиять на его применение. Принятие решения об использовании данной рекомендации должно основываться на индивидуальных предпочтениях пациента и клиническом контексте.
|
|
d. Настоятельная рекомендация не использовать
|
Эта рекомендация указывает на то, что польза от применения определенного медицинского вмешательства недостаточна или неоправдана, и его применение не рекомендуется. Это ясное руководство о том, что данное вмешательство следует избегать.
|
|
e. Заявление о надлежащей практике:
|
Это заявление указывает на то, что определенное медицинское вмешательство является общепринятой нормой практики и следует применять в соответствии с этими нормами. Это неявная рекомендация, которая подчеркивает, что данное вмешательство является стандартом и должно использоваться в клинической практике.
|
|
Методология GRADE (Grading of Recommendations Assessment, Development and Evaluation) предоставляет систему классификации и оценки рекомендаций по основным клиническим вопросам. Эти рекомендации помогают медицинским профессионалам и пациентам принимать информированные решения о лечении и здравоохранении на основе научных данных и клинического контекста.
|
|
Классификация
Классификация
|
Без клинических проявлений
|
Бессимптомная форма (положительный результат ПЦР РНК SARSCoV-2, отсутствие жалоб, клинических симптомов).
|
|
Клинические варианты
|
Поражения верхних дыхательных путей (ринит, фарингит)
Поражения нижних дыхательных путей (COVID-ассоциированная пневмония)
Внелегочные COVID-ассоциированные поражения (гастроэнтерит, нефрит, гепатит, миокардит, неврит, менингит, энцефалит, энцефалопатия, полинейропатия и др.)
|
|
По степени тяжести
|
-легкая степень
-среднетяжелая степень
-тяжелая степень
-крайне тяжелая/критическая степень (ОРДС, ОДН, шок, СПОН и др.)
|
|
По распространенности процесса по данным КТ
(при наличии)
|
КТ-1 (<25% объема)
КТ-2 (25-50% объема)
КТ-3 (50-75% объема)
КТ-4 (>75% объема)
|
|
Рентген/признаки (при отсутствии КТ)
|
Односторонний/Двухсторонний процесс (с указанием доли)
Двухсторонний субтотальный/тотальный процесс
|
| По течению |
- сверхострое (ОРДС, шок) (до 10 дней)
- острое (до 1 мес.)
- подострое (от 4 до12 недель)
- постковидный синдром (свыше 12 нед)
|
| Осложнения |
- ОРДС
- ОДН
- Сепсис
- Септический шок
- СПОН
- ТЭЛА
- ОНМК
- ОИМ
- ОСН
- Нарушения ритма сердца
- Миокардиты, перикардиты
- Инфаркт миокарда при отсутствии обструктивного поражения коронарных артерий
- Синдром Такацуба [92]
|
|
По срокам развития
|
- первичное заболевание
- повторное заболевание
|
Нетяжелое течение COVID-19 — определяется как отсутствие каких‑либо признаков тяжелого или крайне тяжелого течения COVID‑19.
U07.1 Коронавирусная инфекция COVID-19 тяжелой степени тяжести. Подтвержденный случай (ПЦР РНК SARS CoV-2 назофарингиального мазка положительный, дата), подострое течение. COVID-19 ассоциированная пневмония. КТ-2. Осложнение: ОРДС 1 ст. ДН 2 ст.
U07.2 Коронавирусная инфекция CОVID-19 тяжелой степени тяжести (Вирус не идентифицирован). COVID-19 ассоциированная пневмония. КТ-2. Осложнение: ДН 2 ст.
Диагностика
1) Диагностические критерии:
Жалобы и анамнез:
Инкубационный период - 2-14 дней (в среднем до 2-4 дней при инфицировании штаммом «Омикрон»)
|
Симптомы COVID-19 у пожилых могут быть легкими и не соответствовать тяжести заболевания, КТ-картине и серьезности прогноза.
|
Новые рекомендации по эпидемиологическому надзору за COVID-19 от 22 июля 2022 г.):
| 1. |
Предполагаемый случай инфекции вирусом SARS-CoV-2 (3 варианта)
|
A) Лицо, соответствующее следующим клиническим ИЛИ эпидемиологическим критериям:
клинические критерии:
• резкое повышение температуры И кашель (ГПЗ)
ИЛИ
• резкое возникновение ЛЮБЫХ ТРЕХ ИЛИ БОЛЕЕ из следующих признаков и симптомов: лихорадка, кашель, общая слабость/утомляемость1, головные боли, миалгия, боль в горле, ринит, одышка, тошнота/диарея/анорексия
ИЛИ
эпидемиологические критерии2:
• наличие контактов с лицом с вероятной или подтвержденной инфекцией или эпидемиологическим кластером случаев COVID-193.
В) Лицо с тяжелым острым респираторным заболеванием (ТОРЗ: острая респираторная инфекция с лихорадкой в анамнезе или с измеренной температурой тела ≥38°C; кашель; начало симптомов в течение последних 10 дней; показания к госпитализации)
С) Лицо, не имеющее клинических признаков или симптомов ИЛИ НЕ соответствующее эпидемиологическим критериям, с положительным результатом профессионального или самостоятельного антигенного экспресс-тестирования на SARSCoV-24.
|
| 2. |
Вероятный случай инфекции вирусом SARS-CoV-2 (2 варианта)
|
А) Лицо, соответствующее клиническим критериям И, имевшее контакты с лицом с вероятной или подтвержденной инфекцией или эпидемиологическим кластером случаев COVID-193.
В) Летальный исход с неустановленной причиной у взрослого пациента с предшествовавшим респираторным дистресс-синдромом И с контактами с лицом с вероятной или подтвержденной инфекцией или связью с эпидемиологическим кластером случаев COVID-193 |
| 3. |
Подтвержденный случай инфекции вирусом SARS-CoV-2 (2 варианта)
|
А) Лицо с положительным результатом лабораторного исследования методом амплификации нуклеиновых кислот, независимо от клинических ИЛИ эпидемиологических критериев
В) Лицо, соответствующее клиническим И/ИЛИ эпидемиологическим критериям (см. предполагаемый случай инфекции A) с положительным результатом профессионального или самостоятельного антигенного экспресс-тестирования на SARS-CoV-24. |
|
1 Признаки, указанные через косую черту (/), следует рассматривать как один признак.
2 В свете повышенной трансмиссивности новых вариантов и высокой вероятности того, что любой тесный контакт может привести к инфицированию, включены только эпидемиологические критерии для направления на тестирование бессимптомных контактных лиц, когда это возможно, в случае стран, имеющих возможности адаптировать более гибкие стратегии тестирования; это особенно актуально для групп населения и условий повышенного риска.
3 Группа лиц с симптомами инфекции, между которыми установлена эпидемиологическая связь по времени, месту или источнику заражения, в которую входит хотя бы один пациент с инфекцией, подтвержденной методом амплификации нуклеиновых кислот, или не менее двух эпидемиологически связанных между собой симптоматичных лиц (соответствующих клиническим критериям А или В предполагаемого случая) с положительным результатом выполненного специалистом или самостоятельного антигенного экспресс-тестирования (со специфичностью теста ≥97% и вероятностью истинности хотя бы одного положительного результата >99,9%).
4 Антигенные тесты для экспресс-диагностики (Ag-RDT) могут использоваться как обученными специалистами, так и в рамках самотестирования:
- профессиональные антигенные экспресс-тесты на SARS-CoV-2: антигенные экспресс-тесты, одобренные ВОЗ для применения в условиях чрезвычайной ситуации, при использовании которых отбор проб, выполнение тестирования и интерпретация результатов выполняется обученным оператором;
- антигенные экспресс-тесты на SARS-CoV-2 для самотестирования: антигенные экспресс-тесты, одобренные ВОЗ для применения в условиях чрезвычайной ситуации, при использовании которых отбор проб, выполнение тестирования и интерпретация результатов выполняется самим тестируемым.
|
||
|
Примечание: при определении необходимости дальнейшего обследования пациентов, не в полной мере отвечающих указанным клиническим или эпидемиологическим критериям, следует руководствоваться клинической картиной и санитарно-эпидемиологическими соображениями. Данные определения случая разработаны для целей эпидемиологического надзора и не должны использоваться в качестве единственного руководства к принятию решений в клинической практике.
|
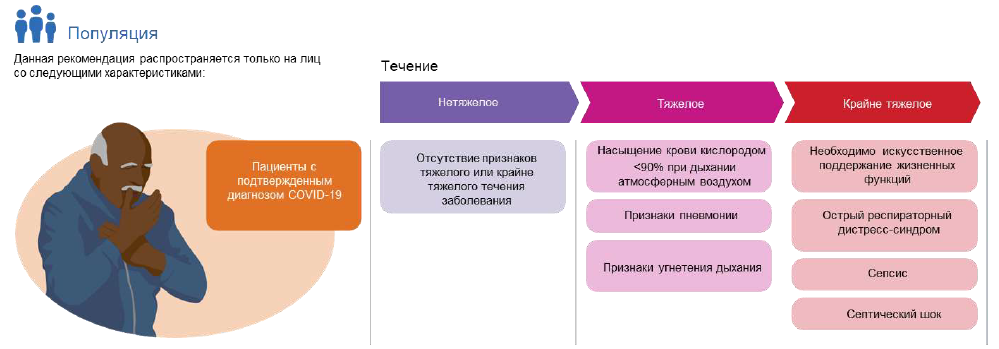
| Легкая форма заболевания |
Наличие клинических проявлений, соответствующих определению случая COVID-19, без признаков вирусной пневмонии или гипоксии.
|
|
|
Среднетяжелое течение заболевания
|
Пневмония |
Подросток или взрослый с клиническими признаками пневмонии (лихорадка, кашель, затрудненное и учащенное дыхание), но без признаков тяжелой пневмонии, включая SpO2 ≥ 90% при дыхании атмосферным воздухом.
Внимание
Порог насыщения кислородом в 90% для определения тяжелого течения COVID-19 является произвольным, и этот показатель следует интерпретировать с осторожностью. Например, принимая решение о том, является ли низкое насыщение крови кислородом признаком тяжести заболевания либо нормой для определенного пациента, страдающего хроническим заболеванием легких, клиницист должен опираться на собственное профессиональное суждение.
Аналогичным образом насыщение крови кислородом в диапазоне 90–94% при дыхании атмосферным воздухом может являться признаком патологии (у пациента со здоровыми легкими) и служить ранним признаком тяжелого течения заболевания в случае, если состояние пациента ухудшается. В качестве общего правила экспертная группа предложила при возникновении каких-либо сомнений трактовать все спорные наблюдения в пользу более тяжелого течения заболевания.
|
| Тяжелое течение заболевания |
Тяжелая пневмония
|
Подросток или взрослый с клиническими проявлениями пневмонии (лихорадка, кашель, затрудненное дыхание) и хотя бы один из следующих признаков: частота дыхания> 30 дыхательных движений/мин, выраженная дыхательная недостаточность или SpO2 <90% при дыхании атмосферным воздухом.
Диагноз может быть поставлен на основании клинических признаков, однако может быть полезным применение методов визуализации, таких как рентгенография, КТ или УЗИ грудной клетки, которые помогут в постановке диагноза и выявлении или исключении легочных осложнений.
|
| Крайне тяжелое течение |
Острый респираторный дистресс-синдром (ОРДС)
|
Начало: в течение 1 недели с момента выявления клинической патологии (пневмонии) или возникновения новых либо усугубления имевшихся ранее респираторных симптомов.
Исследование органов грудной клетки с помощью методов визуализации: рентгенография, КТ или УЗИ легких: двусторонние затенения, которые не могут быть полностью объяснены наличием объемной перегрузки, ателектаза всего легкого или его доли либо узелковых образований.
Происхождение легочных инфильтратов: дыхательная недостаточность, которую нельзя полностью объяснить сердечной недостаточностью или гиперволемией. При отсутствии факторов риска требуется объективная оценка (например, эхокардиография), чтобы исключить гидростатическую причину инфильтратов/отека. Нарушение оксигенации у взрослых.
Анализ газов артериальной крови (ГАК) доступен
• ОРДС легкой степени: 200 мм рт.ст. < PaO2/FiO2
≤ 300 мм рт.ст. (с PEEP или CPAP ≥ 5 cм H2O)
• ОРДС средней степени: 100 мм рт.ст. < PaO2/FiO2
≤ 200 мм рт.ст. (с PEEP или CPAP ≥ 5 cм H2O)
• ОРДС тяжелой степени: PaO2/FiO2 ≤ 100 мм рт. ст. (PEEP ≥ 5 см вод. ст.).
ГАК недоступен (Кигалийская модификация)
• отношение SpO2/FiO2 ≤ 315 указывает на наличие ОРДС (в том числе у пациентов, не находящихся на ИВЛ)
|
| Сепсис |
Взрослые: острая жизнеугрожающая органная дисфункция, вызванная неуправляемым ответом организма на подозреваемую или подтвержденную инфекцию. К признакам дисфункции органов относятся: изменение психического состояния (делирий), затрудненное или учащенное дыхание, недостаточное насыщение крови кислородом, снижение диуреза, учащенное сердцебиение, слабый пульс, холодные конечности или низкое артериальное давление, кожная сыпь, лабораторные признаки коагулопатии, тромбоцитопении, ацидоза, а также высокий уровень лактата в крови или гипербилирубинемия.
Дети: подозреваемая или подтвержденная инфекция и не менее 2 возрастных критериев синдрома системного воспалительного ответа (ССВО), b наряду с этим обязательно отмечается патологическая температура тела либо лейкоцитарная формула.
Критерии ССВО: патологическая температура тела (> 38,5°C или < 36°C); тахикардия с учетом возрастной нормы или брадикардия с учетом возрастной нормы для детей < 1 года; тахипноэ с учетом возрастной нормы или потребность в ИВЛ; аномальная лейкоцитарная формула с учетом возрастной нормы или > 10% палочкоядерных форм.
|
|
|
Септический шок
|
Взрослые: стойкая гипотония, сохраняющаяся несмотря на восполнение объема циркулирующей крови и требующая применения вазопрессорных препаратов для поддержания СрАД на уровне ≥ 65 мм рт. ст. и сывороточного лактата > 2 ммоль/л.
Дети: любая гипотония (САД < 5-го центиля или > 2 СО ниже нормы для возраста) либо два или три из следующих симптомов: изменение психического состояния; брадикардия или тахикардия (ЧСС < 90 или > 160 уд./мин у младенцев либо ЧСС < 70 или > 150 уд./мин у детей старшего возраста); увеличенное время капиллярного наполнения (> 2 сек.) или слабый пульс; тахипноэ; макулярная сыпь или холодные кожные покровы, или петехиальная сыпь, или пурпура; высокий уровень лактата; пониженный диурез; гипертермия или гипотермия.
|
|
|
Острый тромбоз
|
Острая венозная тромбоэмболия (тромбоэмболия легочной артерии), острый коронарный синдром, острый инсульт.
|
|
| MIS-C |
Синдром мультисистемного воспаления у детей.
Предварительное определение случая: наличие у ребенка или подростка (0–19 лет) следующих нарушений: лихорадка дольше 3 дней, А ТАКЖЕ двух из следующих признаков: сыпь или двусторонний негнойный конъюнктивит или признаки воспаления кожи и слизистых оболочек (полость рта, кисти или стопы); гипотония или шок; признаки дисфункции миокарда, перикардит, вальвулит или коронарные аномалии (включая данные эхокардиографии или повышение индекса тропонин/NT-proBNP); признаки коагулопатии (протромбиновое время, частичное тромбопластиновое время, повышение уровня D-димера); острые нарушения функции желудочно-кишечного тракта (диарея, рвота или абдоминальная боль); И повышение уровня маркеров воспаления, таких как СОЭ, С-реактивный белок или прокальцитонин, И не имеется иной очевидной микробной этиологии шокового синдрома, И данных за COVID-19 (положительного результата ОТ-ПЦР, теста на антиген или серологического теста) либо вероятного контакта с пациентами с COVID-19.
|
Основные лабораторные исследования
Специфические методы исследования [13,14]:
2. Относительно высокая вирусная нагрузка в образцах из верхних дыхательных путей (ВДП) обычно выявляется в первую неделю после появления симптомов. При отборе проб из ВДП рекомендуется взятие мазков из носоглотки и зева. При сборе образцов из ВДП следует применять специальные вирусные зонд-тампоны (стерильные лавсановые или вискозные, не хлопчатобумажные), для мазков из носоглотки следует применять специальные тупферы с длинным гибким стержнем. В отсутствие иных указаний принимающей лаборатории образцы необходимо транспортировать с использованием вирусной транспортной среды.
3. После первой недели заболевания результаты исследования материала из НДП (в отличие от материала из ВДП) с большей вероятностью будут положительными. Таким образом, если тестирование образца из ВДП дало отрицательный результат, однако сохраняется клиническое подозрение, следует взять образцы материала из НДП в подходящей ситуации (отхаркивание мокроты или эндотрахеальный аспират/ бронхоальвеолярный лаваж у вентилируемого пациента). Клиницисты могут принять решение брать образцы только из НДП, если это легко осуществимо (например, у пациентов на ИВЛ). Следует избегать искусственной стимуляции отхаркивания мокроты из-за риска аэрозольной передачи инфекции. У пациента с подозрением на COVID-19, особенно с пневмонией или находящегося в тяжелом состоянии, нельзя исключить наличие инфекции на основе лишь одного образца из ВДП: рекомендуется собрать дополнительные образцы из ВДП и НДП. У госпитализированных пациентов с подтвержденным диагнозом COVID-19 при наличии клинических показаний можно осуществлять повторное взятие образцов из ВДП и НДП, однако это более не является обязательным условием для отмены мер профилактики COVID-19.
4. Для подтверждения диагноза COVID-19 рекомендуется использовать тестирование методом МАНК. Однако в тех случаях, когда такое тестирование недоступно или, когда длительные сроки до получения результата приводят к нулевой клинической пользе, в определенных обстоятельствах в диагностический алгоритм может быть включено тестирование на антиген. Если используется тестирование на антиген, следует удостовериться в том, что сбор проб и лабораторные процедуры проводятся в соответствии с инструкциями по применению антигенных тестов, персонал соответствующим образом обучен, а качество тестирования контролируется в рамках всеобщей национальной программы лабораторного тестирования. Кроме того, допускается самотестирование на COVID-19 при помощи АГ-ДЭТ (также «самодиагностика COVID-19»). При проведении самодиагностики лицом с подозрением на COVID-19 положительный результат указывает на наличие активной инфекции, тогда как отрицательный результат не позволяет исключить COVID-19 полностью.
5. В случае, если имеются веские основания подозревать инфекцию COVID-19 у пациента с повторным отрицательным результатом МАНК/ ОТ-ПЦР, допускается взятие парных образцов сыворотки. Первый образец берут в острой фазе, второй – на этапе выздоровления, через 2–4 недели. Это полезно лишь в случае, если в принимающей лаборатории имеются валидированные (полу)количественные серологические тест-системы и обученный персонал для интерпретации результатов тестирования. С помощью парных образцов может быть ретроспективно выявлена сероконверсия или повышение титров антител, что дополнительно подтверждает подозрение на недавно перенесенное заболевание COVID-19, несмотря на отрицательные результаты тестов МАНК.
Биохимические методы исследования (по показаниям):
|
Кратность лабораторных исследований – по показаниям, в зависимости от клинической ситуации
|
Основные инструментальные исследования
Мониторинг SрO2 в стационаре (рекомендации ВОЗ):
| Параметры SрO2 |
Рекомендуемая частота исследования SрO2 в стационаре
|
Действия персонала |
|
>93% (без O2-терапии)
|
Измерение не реже 2-х раз в сутки утром и вечером (по возможности)
|
Оценка по ABCDE*
Продолжить наблюдение
|
|
93-90% (без O2-терапии)
|
Измерение не реже 4-х раз в сутки |
Оценка по ABCDE*
Восстановление проходимости дыхательных путей.
Назначить кислородотерапию при снижении <93%.
|
|
<90% без О2 или
< 93% при кислородотерапии
|
Рекомендуется использование прикроватного монитора с регулярным измерением сатурации
|
Назначить кислородотерапию.
Провести исследование КЩС.
Оценка по ABCDE
Восстановление проходимости дыхательных путей.
НИВЛ по показаниям
|

|
Кратность инструментальных исследований – по показаниям, в зависимости от клинической ситуации
|
2) Диагностический алгоритм: (схема)
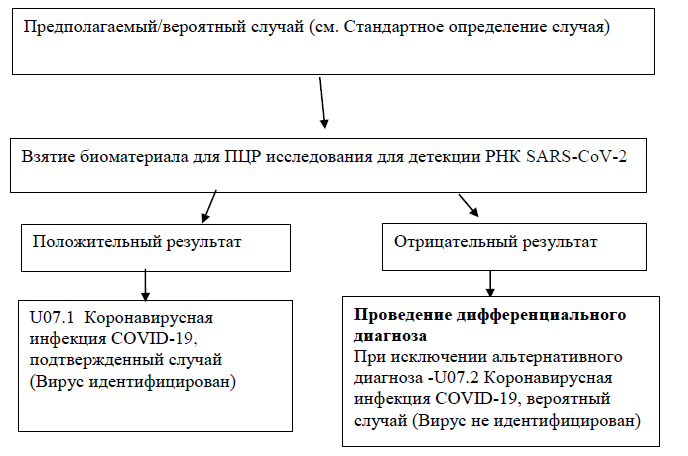
Диагностический поиск
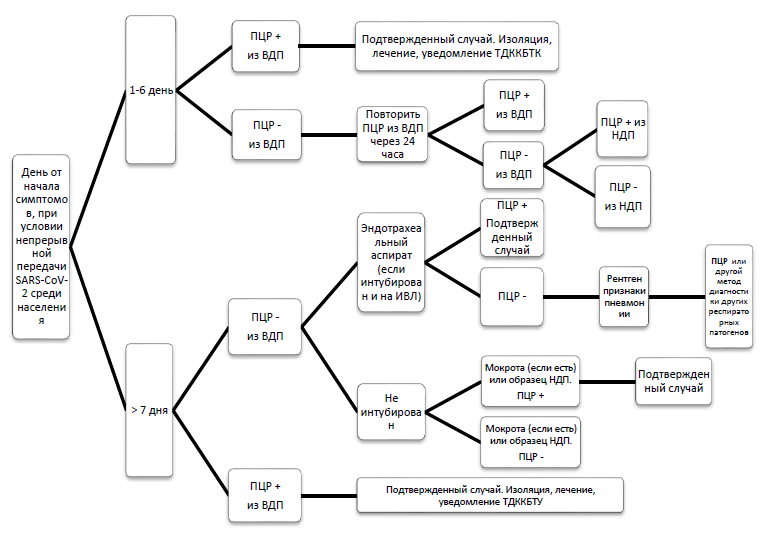
Дифференциальный диагноз
Критерии дифференциальной диагностики COVID-19:
|
Диагноз
|
Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Грипп |
Острое начало, лихорадка, миалгии, артралгии, катаральный синдром, диарея (до 25 %), геморрагический синдром (при тяжелом течении), вирусное поражение легких,
Осложнение: ДН, ОРДС
|
Обнаружение РНК вируса гриппа в ПЦР (мазок из носоглотки, мокрота, бронхоальвеолярный лаваж, если пациент на ИВЛ)
|
Отсутствие выраженного катарального синдрома, склерита, ринореи, трахеита, относительный лимфоцитоз.
Отрицательный результат ПЦР РНК вируса гриппа (в диагностически сложных случаях).
Положительный результат ПЦР РНК SARS Cov-2
|
|
Метапневмовирусная инфекция
|
Острое начало, лихорадка
Пневмония
Осложнение: ДН, ОРДС
|
Обнаружение РНК метапневмовируса в ПЦР (мазок из носоглотки, бронхоальвеолярный лаваж, если пациент на ИВЛ)
|
Отсутствие ринита бронхита, бронхиолита.
Отрицательный результат ПЦР РНК метапневмовируса в ПЦР (в диагностически сложных случаях).
Положительный результат ПЦР РНК SARS Cov-2
|
|
Бокавирусная инфекция
|
Острое начало, лихорадка
Фарингит
Пневмония
Осложнение: ДН, ОРДС
|
Обнаружение РНК бокавируса в ПЦР (мазок из носоглотки, бронхоальвелярный лаваж, если пациент на ИВЛ)
|
Отсутствие бронхиолита
Отрицательный результат ПЦР РНК бокавируса (в диагностически сложных случаях).
Положительный результат ПЦР РНК SARS Cov-2
|
|
Корь, катаральный период
|
Острое начало,
Лихорадка
Катаральный синдром
|
Обнаружение специфических антител IgM в ИФА
|
Отсутствие выраженного катарального синдрома, склерита, коньюнктивита, с последущим этапным высыпанием, пятен Бельского-Филатова-Коплика.
Отрицательный результат в ИФА на обнаружение специфических антител IgM против вируса кори.
Положительный результат ПЦР РНК SARS Cov-2
|
|
Атипичная пневмония (микоплазменна, хламидийная, легионеллезная)
|
Лихорадка
Катаральный синдром
|
Обнаружение специфических антител IgM в ИФА
|
Острое начало, Отрицательный результат в ИФА на обнаружение специфических антител IgM против антигенов микоплазм, хламидий, легионелл.
Положительный результат ПЦР РНК SARS Cov-2
|
|
Острые кишечные инфекции (новые штаммы COVID-19)
|
Лихорадка, тошнота, рвота, боли в животе, жидкий стул
|
Бак.посев кала на сальмонеллез
Экспресс-тест ПЦР кала на этеровирусы, ротавирусы и др. кишечные вирусы
|
Отсутствие эпиданамнеза ОКИ;
Отрицательные результаты лаб. исследований на ОКИ.
Положительный результат ПЦР РНК SARS Cov-2
|
|
Бактериальный сепсис
|
лихорадка, СПОН, шок |
Бак.посев крови, мокроты, мочи, кала, бронхоальвеолярного лаважа, ОАК, ПКТ
|
Отрицателные результаты бакпосевов, отсутствие повышения ПКТ
|
| ТЭЛА |
Нарастающая одышка, тахикардия, десатурация, снижения уровня АД, ОРДС, острая сердечная недостаточность
|
Диагностированный тромбоз глубоких вен нижних и верхних конечностей по данным УЗДГ, наличие катетерных тромбозов, высокий уровень Д-димера, Косвенные признаки ТЭЛА на эхокардиографии
|
Отсутствия признаков тромбоза глубоких вен, нормальные показатели Д-димера (возможно у больных с дефицитом XIII-фактора), отсутствия косвенных признаков ТЭЛА на ЭхоКГ, а также на мультидетекторной КТ легочной ангиографии и вентиляцонно-перфузионной сцинтиграфии легких
|
| ОКС |
Признаки острой сердечной
недостаточности, ОРДС, наличие характерного или выраженного болевого синдрома (больше 20 минут) в грудной клетке у пациента с факторами риска (АГ, ИБС, сахарный диабет, ожирение), подозрение на ИМ, тампонаду сердца
|
ЭКГ в 12 стандартных отведениях (наличие элевации или депрессии сегмента ST, с формированием патологического зубца Q, определение высокочувствительных тропонинов, выявления зон локальной сократимости, механического повреждения структуры сердца) | Нормальная картина ЭКГ в 12 стандартных отведениях, отсутствие повышения уровня высокочувствительного тропонина, отсутствия зон локальной сократимости сердца. |
|
ОНМК – острое нарушение мозгового кровообращения
|
Острое начало, с внезапным появлением общемозговых симптомов и острой очаговой неврологической симптоматики.
Общемозговые симптомы:
головная боль; тошнота/рвота; головокружение; боль в глазных яблоках, усиливающаяся при движении глаз; чувство жара, повышенная потливость; ощущение сердцебиения; сухость во рту; нарушения сознания (оглушённость, сонливость/возбуждение, возможна потеря сознания).
Очаговая неврологическая симптоматика:
невнятность речи (дизартрия, моторная афазия); онемение и/или перекос половины лица; гемианопсия; диплопия; гемипарез/гемиплегия; одностороннее/двусторонние чувствительные расстройства.
|
- КТ и/или МРТ головного мозга,
- МСКТА или МР-ангиография для диагностики окклюзии или стеноза экстра- и (или) интракраниальных артерий головы и решения вопроса о проведении механической тромбоэкстракции;
- КТ венография и/или МР- венография по показаниям, при наличии подозрений инсульта в венозной системе головного мозга.
|
Отсутствие признаков ОНМК на КТ и/или МРТ головного мозга
|
|
Болезнь Кавасаки (для МВС)
|
Лихорадка, сыпь, артралгия, миалгия, СПОН
|
Положительный результат ПЦР РНК SARS Cov-2, ИФА, ИХЛ
|
Отрицательный результат ПЦР РНК SARS Cov-2, ИФА, ИХЛ
|
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ В АМБУЛАТОРНЫХ УСЛОВИЯХ [4-5, 11-16, 19-21, 35, 36, 39, 40, 43-54, 57-69, 81-92, 94, 96]:
На амбулаторном уровне ведется наблюдение и лечение следующих категорий пациентов:
Лица могут получать медицинскую помощь на дому при условии соблюдения двух нижеследующих требований:
Основные лекарственные средства
Ведение пациентов с легкой степенью тяжести COVID-19.
Ведение пациентов со средней степенью тяжести COVID-19
Основные лекарственные средства
Режим дозирования: взрослые с массой тела 40 кг и более:
5) При наличии сопутствующих заболеваний (онкологические заболевания в активной стадии, перенесенные тромбозы глубоких вен и ТЭЛА, тромбофилия, недавно перенесенные инфаркт миокарда, ишемический инсульт и большие оперативные вмешательства, пожилой возраст ≥ 70 лет, ХСН) следует определить риск венозных тромбоэмболий по шкале PADUА или по модели оценки риска IMPROVE, затем оценить риск кровотечений согласно шкале IMPROVE-BLEED. [75-77, 89].
| Фактор риска | Балл |
|
Активное злокачественное новообразование (метастазы и/или химиотерапия/радиотерапия <6 месяцев назад)
|
3 |
| ТГВ/ТЭЛА в анамнезе (за исключением тромбоза поверхностных вен) | 3 |
| Ограниченная подвижность (постельный режим с выходом в туалет) ≥3 дней | 3 |
|
Известная тромбофилия (дефекты антитромбина, протеина С или S, фактор V Лейден, G20210A мутация протромбина, антифосфолипидный синдром)
|
3 |
| Травма и/или операция ≤1 месяца назад | 2 |
| Возраст ≥70 лет | 1 |
| Сердечная и/или дыхательная недостаточность | 1 |
| Инфаркт миокарда или ишемический инсульт | 1 |
| Острая инфекция и/или ревматологическое заболевание | 1 |
| Ожирение (ИМТ >30 кг/м2) | 1 |
|
Продолжение использования гормональной заместительной терапии или пероральных контрацептивов
|
1 |
Модель оценки риска IMPROVEDD VTE
| Факторы риска | Баллы |
| ВТЭ в анамнезе | 3 |
| Уровень Д-димера ≥ 2 раза от верхней границы нормы | 2 |
| Паралич н/к в настоящее время | 2 |
| Рак в настоящее время | 2 |
| Иммобилизация ≥ 1 дня | 1 |
| Госпитализация в ОРИТ или кардио-интенсивный блок | 1 |
| Возраст ≥ 60 лет | 1 |
Модель оценки риска кровотечения IMPROVE-BLEED
| Факторы риска | Баллы |
| Активная язва желудка и 12-перстной кишки | 4,5 |
| Кровотечение <3 мес до госпитализации* (ЖК, ИИ, прим НОАК) | 4 |
| Тромбоциты <50 000** (прим. АСК и P2Y12) | 4 |
| Возраст> 85 лет | 3,5 |
| Печеночная недостаточность с уровнем ПВ> 1,5 ВГН | 2,5 |
| Тяжелая почечная недостаточность с рСКФ <30 мл/мин | 2,5 |
| Госпитализация в ОРИТ | 2,5 |
| Наличие центрального катетера | 2 |
| Наличие ревматического или аутоиммунного заболевания | 2 |
| Рак активный | 2 |
| Возраст: 40-84 года | 1 |
| Мужчины | 1 |
| рСКФ 30-59 мл/мин | 1 |
7) настоятельная рекомендация против использования Апиксабана, Дабигатрана этексилат, Ривароксабана у пациентов с нетяжелым течением COVID-19 (ВОЗ, впервые опубликовано 03.12.2020 г., продолжено 12.03. 2021г., 1.04. 2021 г., 05.08.2021 г..19.11. 2021 г., 28.01.2022г.,25.07.2022г.);
4. Дальнейшее ведение:
|
При обострении сопутствующих хронических неинфекционных заболеваний, при развитии постковидных состояний врач ПМСП направляет реконвалесцента на консультацию к профильному специалисту. Ведение и лечение осуществляется в соответсивии с клиническим протоколом диагностики и лечения по сопутствующему заболеванию.
|
Лечение (стационар)
Немедикаментозное лечение:
|
Необходимо вести пациентов на нулевом гидробалансе, при отсутствии противопоказаний
|
| Раннее начало респираторной поддержки снижает риск развития гипоксии мозга. |
|
N.B.!!! При использовании НИВЛ и HFNO в условиях, не соответствующих требованиям, описанным выше, необходимо помнить о высоком риске образования аэрозолей, что может привести к инфицированию персонала ОРИТ и распространению инфицирующего агента в помещении ОРИТ. Если эти вмешательства осуществляются за пределами одноместных палат в ОРИТ, оснащенных ненадлежащими системами вентиляции, то в целях защиты от воздушной передачи инфекции целесообразно группировать пациентов, которым показаны эти методы лечения, в специально отведенных помещениях с адекватной вентиляцией, куда персонал может входить, только надев надлежащие СИЗ.
|
Оценку тяжести пациентов рекомендуется проводить по шкале NEWS [16,44]
|
При проведении НИВЛ (СРАР) следует оценивать состояние пациента. При неэффективности СРАР в течение 30-60 минут от момента начала терапии (сохраняющаяся гипоксия – SpO2 <90%, признаки ухудшения газообмена, значимое участие дыхательной мускулатуры в акте дыхания), при прогрессирующем ухудшении оксигенации пациента, или если пациент не толерирует устройство СРАР – рассмотреть интубацию трахеи и перевод на ИВЛ. СРАР не должна задерживать интубацию у пациента с показаниями для интубации и ИВЛ.
|
В руководствах по НИВЛ не содержится рекомендаций по применению этого метода при гипоксемической ДН (за исключением кардиогенного отека легких, послеоперационной дыхательной недостаточности и раннего применения НИВЛ у пациентов с иммуносупрессией) или при пандемических вирусных заболеваниях (по имеющимся исследованиям ТОРС и пандемического гриппа). Риски включают задержку интубации, большие ДО и травмирующее транспульмональное давление.
АКТ для профилактики у тяжелых и критических пациентов
| Название препарата | Дозы | Примечание |
|
Надропарин кальция раствор для инъекций в шприцах –
0.3 мл2850 МЕ анти Ха:
0,4 мл/3800 ME анти-Ха:
0,6 мл / 5700 ME анти-Ха
|
Профилактическая доза п/к0,3 -0,4 мл 1 раз в сутки
|
Пациентам с рСКФ < 30 мл/мин назначать не следует.
Противопоказан при кровотечении
|
|
Эноксапарин раствор для инъекций в шприцах
4000 анти-Ха МЕ/0,4 мл,
6000 анти-Ха МЕ/0,6 мл,
|
Профилактическая доза п/к 0,4 мл 1 раз в сутки
|
Пациентам с рСКФ < 30 мл/мин назначать не следует.
Противопоказан при кровотечении
|
|
Фондапаринукс раствор для инъекций в шприцах по 2,5 мг препарат выбора при тромбоцитопении
|
Профилактическая доза п/к 2,5 мг 1 раз в сутки
|
Пациентам с рСКФ < 25-30 мл/мин назначать не следует
Назначается при снижении тромбоцитов <100 000х109/л
|
| Гепарин 1 мл-5000МЕ |
Профилактическая доза
Подкожно 5000 МЕ 3 раза в сутки
|
Биодоступность при п/к составляет до 30%
Препарат выбора при рСКФ <30 мл мин
|
|
Только в случае диагностики ТГВ и ТЭЛА пациента следует перевести на терапевтическую дозу нефракционированного гепарина, НМГ, фондапаринукса (согласно инструкции, см. клинический протокол диагностики и лечения «Тромбоэмболия легочной артерии»).
|
|
Пациентам с тяжелой степенью тяжести, но относительно стабильной гемодинамикой можно продолжить НМГ. В случае нестабильности гемодинамики, или ухудшения функции почек (при уровне КК ниже 30 мл/мин) перевести на НФГ).
|
|
Пациентам в ОРИТ с ВТЭ с нестабильной гемодинамикой предпочтительно применения НФГ под контролем АЧТВ.
|
|
Важно помнить риски развития ГИТ на фоне использования терапевтических доз НФГ, которая проявляется тромбоцитопенией> 30- 50% от исходного уровня после 5 дней применения НФГ и развитием симметричных тяжелых венозных и артериальных тромбозов с высокой смертностью 50% и выше. Частота ГИТ составляет до 5% на фоне использования НФГ, на фоне НМГ значительно реже.
|
Схемы терапии ГКС
| ГКС | Основная схема [39,40] |
|
Дексаметазон
ИЛИ
|
6 мг перорально/внутривенно 1 раз в день, 7-10 дней
|
|
Метилпреднизолон*
ИЛИ
|
32 мг внутривенно (по 8 мг кажде 2 часов или 16 мг каждые 12 часов), 7-10 дней
|
|
Преднизолон ИЛИ |
40 мг в день перорально, 7-10 дней |
|
Гидрокортизон
|
150 мг (по 50 мг каждые 8 часов) |
Примечание: Метилпреднизолон* - после регистрации в РК
|
NB!!! В зависимости от клинической ситуации по показаниям может меняться доза, кратность и продолжительность ГКС на основе решения врачебного консилиума.
Высокие дозы ГКС и длительность терапии коррелируют с повышенным риском присоединения бактериальных и других осложнений.
|
Для пациентов с тяжелым и крайне тяжелым течением COVID-19 рекомендуется (настоятельная рекомендация в пользу применения) применение блокаторов к IL-6 (тоцилизумаб).
В настоящее время ингибитор JAK барицитиниб рекомендуется для лечения пациентов с тяжелым и крайне тяжелым течением COVID-19. Допускается совместное назначение блокаторов рецепторов к IL-6 и барицитиниба.
Рекомендуемая доза тоцилизумаба в зависимости от массы тела:
| Вес пациента | доза препарата - курсовая |
| > 90 кг | 800 мг |
| > 65 и ≤90 кг | 600 мг |
| > 40 и ≤65 кг | 400 мг |
| ≤40 кг | 8 мг / кг |
Продолжительность одномоментно назначаемого курса кортикостероидов обычно составляет до 10 дней, однако может варьировать в диапазоне от 5 до 14 дней.
Пути введения, дозировка и продолжительность применения у взрослых:
Барицитиниб может вызывать увеличение количества тромбоцитов (тромбоцитоз) [114-117].
Антибактериальная терапия при COVID-19
|
Вирусная этиология поражения легких при COVID-19 НЕ ЯВЛЯЕТСЯ показанием для стартовой эмпирической антибактериальной терапии. Назначение АБТ показано только при присоединении вторичной бактериальной инфекции (появление гнойной мокроты, сепсис, повышение прокальцитонина, СРБ), при обострении хронических очагов инфекции, на фоне приема ГКС, присоединении бактериальных осложнений любой локализации, при проведении инвазивных мероприятий катетеризация вен, ИВЛ, ЭКМО и др. (эмпирически/и/или с учетом чувствительности выделенного штамма)
|
НПВС: пациенты с COVID-19, которые принимают НПВС для лечения сопутствующего заболевания, должны продолжать ранее назначенную терапию [53, 54].
Ингаляционные кортикостероиды: пациентам с ХОБЛ, астмой, аллергическим ринитом рекомендуется продолжать предписанные ингаляционные кортикостероиды. Применение небулайзерной терапии при необходимости должно проводиться в отдельной комнате с отрицательным давлением [53, 54].
|
Диагностика и лечение неотложных состояний при COVID-19 и проведение ЭКМО представлены в Приложениях 1 и 2.
|
Нирматрелвир и ритонавир не рекомендуется для пациентов с нетяжелым (легким) течением COVID-19 с низким риском госпитализации (условная рекомендация не применять).
Комбинация казиривимаба и имдевимаба не рекомендуется для всех пациентов с COVID-19 (настоятельная рекомендация не использовать).
Сотровимаб не рекомендуется пациентам с нетяжелым течением COVID-19 (настоятельная рекомендация не использовать).
VV116 - не рекомендуется использовать новый противовирусный препарат для лечения пациентов, только в рамках клинических испытаний.
Ивермектин не рекомендуется пациентам с нетяжелым течением COVID-19 (настоятельная рекомендация не использовать).
Перечень основных лекарственных средств:
|
Фармакотерапевтическая группа
|
Международное непатентованное наименование ЛС | Способ применения | Уровень доказательности |
|
НПВС. Анальгетики-антипиретики другие.
Анилиды.
|
Парацетамол |
Взрослые:
Таблетки: 500 мг каждые 4–6 ч при необходимости. Интервал между приемами – не менее 4 ч.
Максимальная суточная доза парацетамола не должна превышать 4 г.
Р-р для инфузий: Максимальная
суточная доза
> 33 кг до ≤ 50 кг - 60 мг/кг не более 3 г
> 50 кг – 100 мл - 3 г
|
В |
|
НПВС. Производные пропионовой кислоты
|
Ибупрофен |
Взрослые, пожилые в таблетках по 200 мг 3-4 раза в сутки; в таблетках по 400 мг 2-3 раза в сутки.
Суточная доза составляет 1200 мг (не принимать больше 6 таблеток по 200 мг (или 3 таблеток по 400 мг) в течение 24 ч.
Р-р для внутривенного введения:
после введения 400 мг препарата возможен прием еще по 400 мг каждые 4-6 часов или по 100-200 мг каждые 4 часа.
Продолжительность внутривенного введения должна быть не менее 30 минут.
|
В |
|
Антикоагулянт прямого действия
|
Гепарин |
Только в стационаре.
Подкожно 5000 – 2-3 раза МЕ/сут, при непрерывной внутривенной инфузии 1000-2000 МЕ/ч
|
С |
|
Низкомолекулярный гепарин
|
Надропарин |
Только в стационаре.
Взрослые – для профилактики ВТЭ подкожно 0,3-0,6 мл 1 раз в сутки
Для лечения ТГВ и ТЭЛА из расчета 0,1 мл на кг массы тела н/р, если вес пациента составляет 60 кг, то ему 0,6 2 раза в сутки и далее
|
С |
|
Эноксапарин натрия
|
Взрослые - Подкожно 0,2-0,4 мл 1 раз в сутки для профилактики ВТЭ.
Для лечения ТГВ и ТЭЛА из расчета 1 мг/кг массы тела 2 раза/сут.
|
С | |
| Фондапаринукс |
Только в стационаре.
Не применять внутримышечно!
Взрослым для профилактики ТЭ 2,5 мг 1 раз в сутки в виде подкожной инъекции. Для лечения ТГВ и ТЭЛА для пациентов с массой тела менее 50 кг - 5 мг; для пациентов с массой тела 50-100 кг – 7.5 мг; для пациентов с массой тела более 100 кг - 10 мг.
Пациентам с КК менее 30 мл/мин назначать не следует.
|
С | |
| Глюкокортикостероиды | Преднизолон | 40 мг в день перорально, 7-10 дней | В |
| Дексаметазон |
6 мг перорально/внутривенно 1 раз в день, 7-10 дней
|
В | |
| Метилпреднизолон |
32 мг внутривенно (по 8 мг каждые 2 часов или 16 мг каждые 12 часов), 7-10 дней
|
С | |
| Гидрокортизон | 150 мг (по 50 мг каждые 8 часов) | С |
| ГКС | Основная схема [39,40] |
|
Дексаметазон
ИЛИ
|
6 мг перорально/внутривенно 1 раз в день, 7-10 дней
|
|
Метилпреднизолон*
ИЛИ
|
32 мг внутривенно (по 8 мг кажде 2 часов или 16 мг каждые 12 часов), 7-10 дней
|
| Преднизолон | 40 мг в день перорально, 7-10 дней |
|
ИЛИ
*
|
Перечень дополнительных лекарственных средств:
|
Фармакотерапевтическая группа
|
Международное непатентованное наименование ЛС | Способ применения | Уровень доказательности |
|
Экспериментальные лекарственные средства с противовирусным механизмом действия
|
Ремдесивир |
200 мг в/в в 1-й день, затем 100 мг в/в ежедневно, 5 – 10 дней
|
В |
|
Нирматрелвир/ритонавир*
|
Режим дозирования: взрослые с массой тела 40 кг и более:
- 300 мг нирматрелвира (две таблетки по 150 мг) и 100 мг ритонавира (одна таблетка по 100 мг) - все 3 таблетки принимают внутрь два раза в день в течение 5 дней.
Для пациентов с умеренной почечной недостаточностью разрешенная доза (рСКФ от 30 до 59 мл/мин) составляет 150 мг нирматрелвира и 100 мг ритонавира два раза в сутки.
Таблетки можно принимать независимо от приема пищи.
Пропущенная доза: если доза пропущена в течение 8 часов после того, как она обычно принимается, необходимо принять ее как можно скорее и возобновить обычный режим дозирования; если доза пропущена более чем на 8 часов, не принимать пропущенную дозу, а вместо этого необходимо принять следующую дозу в обычное время. Не удваивать дозу, чтобы компенсировать пропущенную дозу.
|
В | |
|
Противовирусный препарат системного действия
|
Молнупиравир* |
Внутрь по 800 мг 2 раза/сут.
Суточная доза составляет 1600 мг. Курс лечения - 5 сут.
|
В |
|
Препарат на основе моноклональных антител, ингибирует рецепторы ИЛ-6.
|
Тоцилизумаб |
Концентрат для приготовления раствора для инфузий 400 мг внутривенно капельно медленно (в течение не менее 1 часа), при недостаточном эффекте повторить введение через 12 ч.
Максимальная курсовая доза – 800 мг
|
В |
| Барицитиниб |
Режим дозирование у взрослых:
4 мг перорально один раз в день в течение 14 дней.
Доза зависит от расчетной скорости клубочковой фильтрации (рСКФ).
- 4 мг один раз в день у пациентов с рСКФ ≥ 60 мл/мин/1,73 м2
- 2 мг один раз в день у пациентов с рСКФ от ≥ 30 мл/мин до < 60 мл/мин/1,73 м2
- 1 мг один раз в день для пациентов с рСКФ от 15 мл/мин до < 30 мл/мин/1,73 м2
- не рекомендуется у пациентов с рСКФ < 15 мл/мин).
|
В | |
|
Регуляторы водно-электролитного баланса и КЩС
|
Натрий хлорид |
Стартовая инфузия 0,9% раствора натрия хлорида из расчета 10-20 мл/кг в течение 30 мин в/в (под контролем гемодинамики).
в/в капельно
|
С |
|
Регуляторы водно-электролитного баланса и КЩС
|
Гидрокарбонат натрия
|
Раствор 100 мл, 200 мл, 400 мл | С |
| Альфа-адреномиметик | Норэпинефрин |
Раствор норэпинефрина 0,05-0,3 мкг/кг/мин – введение только при наличии центрального доступа;
в случае отсутствия норэпинефрина либо центрального доступа вводится допамин 4% 5-10-15 мкг/кг/мин и/или добутамин 5-10 мкг/кг/мин
|
С |
|
Агонист допаминовых рецепторов
|
Допамин | С | |
| Бета1-адреномиметик | Добутамин | С | |
| Диуретик | Фуросемид | Начальная доза 1 мг/кг. | С |
| Антиагреганты |
Ацетилсалициловая кислота
|
по 75 мг х 1 раз/ по 100 мг х 1 раз | С |
| Клопидогрел | по 75 мг х 1 раз | С |
Хирургическое вмешательство: нет.
Выписка пациентов из стационара [19,61]:
Госпитализация
Показания для экстренной госпитализации:
|
На уровне скорой помощи и приемного покоя стационара рекомендуется проводить сортировку согласно Алгоритма межведомственного комплексного инструмента сортировки (Приложение 3).
|
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2024
- 1. Уртаева К.К., Сучков В.Н. Случай новой коронавирусной инфекции COVID-19 у пациента, находящегося на лечении программным гемодиализом. Журнал инфектологии. 2020;12(3):94-98. https://doi.org/10.22625/2072-6732-2020-12-3-94-98 2. Zou X, Chen K, Zou J, et al. Single-cell RNA-seq data analysis on the receptor ACE2 expression reveals the potential risk of different human organs vulnerable to 2019-nCoV infection. Front Med. 2020 Apr; 14(2):185-92. 3. Национальная комиссия здравоохранения и Национальная администрация народной китайской медицины Китайской Народной Республики. Протоколы диагностики и лечения COVID-19 (7-я пробная версия) [ЕВ/OL]. (2020-03-04) [2020- 03-15]. http://www.nhc.gov.cn/yzygj/s7653p/202003/46c9294a7dfe4cef80dc7f5912ebl989.shtml (на китайском языке) 4. Китайский Центр по контролю и профилактике заболеваний. Руководство по эпидемиологическому исследованию COVID-19 [ЕВ/OL], (на китайском языке) (2020-03-09) (2020-03-15]. http://www.chinacdc.cn/jkzt/crb/zl/5zkb_n803/j5zl_n815/202003/t20200309_214241.ht 5. Тромбо-воспалительный синдром при COVID-19. Место и роль антикоагулянтной терапии в лечении COVID-19/Сугралиев А.Б., Plinio Cirillo//Ж.Медицина (Алматы)-№3 (213) 2020 г. 6. Case Series of Multisystem Inflammatory Syndrome in Adults Associated with SARSCoV- 2 Infection — United Kingdom and United States, March–August 2020 https://www.cdc.gov/mmwr/volumes/69/wr/mm6940e1.htm 7. Gupta A, Madhavan MV, Sehgal K, et al. Extrapulmonary manifestations of COVID- 19. Nat Med 2020;26:1017–32.https://doi.org/10.1038/s41591-020-0968-3 8. Undiagnosed pneumonia - China (HU) (01): wildlife sales, market closed, RFI Archive Number: 20200102.6866757. Pro MED mail. International Society for Infectious Diseases. Датаобращения 13 января 2020. 9. Zhonghua Jie, He He, Hu Xi, ZaZhi. Clinical features of 2019 novel coronavirus pneumonia in the early stage from a fever clinic in Beijing. Article in Chinese; Abstract available in Chinese from the publisher. 10. Jonas F Ludvigsson. Systematic review of COVID-19 in children show milder cases and a better prognosis than adults. Actapediatrica. First published: 23 March 2020 https://doi.org/10.1111/apa.15270. 11. Временные методические рекомендации. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 12 (29.09.2021г) МЗ РФ, с.226 12. https://apps.who.int/iris/bitstream/handle/10665/337834/WHO-2019-nCoVSurveillance_ Case_Definition-2020.2-rus.pdf?sequence=10&isAllowed=y 13. Справочник по профилактикеилечениюCOVID-19. Первая клиническая больница Медицинского факультета Университета Чжэцзян. Справочник составлен на основании клинических данных и опыта. Главный редактор: ЛИАН Тинбо (LIANGTingbo), 2020, 49С 14. Laboratory testing for 2019 novel coronavirus (2019-nCoV) in suspected human cases Interim guidance 17 January 2020. 15. Bernheim A, Mei X, Huang M et al (2020) Chest CT findings in coronavirus Disease- 19 (COVID-19): relationship to duration of infection. Radiology. https://doi.org/10.1148/radiol.2020200463 16. Методическое пособие «Клиническое ведение тяжелой острой респираторной инфекции». https://apps.who.int/iris/bitstream/handle/10665/333080/WHO-2019-nCoVSARI- toolkit-2020.1-rus.pdf?sequence=1&isAllowed=y 17. Morris SB, Schwartz NG, Patel P, et al. Case series of multisystem inflammatory syndrome in adults associated with SARS-CoV-2 infection: United Kingdom and United States, March–August 2020. MMWR Morb Mortal Wkly Rep. 2020 Oct 9 [Epub ahead of print]. 18. Консенсусное заявление РАСУДМ об ультразвуковом исследовании легких в условиях COVID-19 (версия 1) / Митьков В.В. соавт // Ультразвуковая и функциональная диагностика. 2020. № 1. С. 24–45. DOI: 10.24835/1607-0771-2020-1- 24-45. http://www.rasudm.org/files/RASUDM-Consensus-Statement-COVID-2.pdf 19. Руководство по профилактике и лечению новой коронавирусной инфекции COVID-19. Первая академическая клиника Университетской школы медицины провинции Чжэцзян. Составлено на основе клинической практики. 2020. С96https://ria.ru/ips/op/COVID_19_Book.pdf 20. EMA gives advice on the use of non-steroidal antiinflammatories for COVID-19. 18 March 2020 EMA/136850/2020. https://www.ema.europa.eu/en/documents/pressrelease/ ema-gives-advice-use-non-steroidal-anti-inflammatories-covid-19_en.pdf 21. Coronavirus disease 2019 (COVID-19). Treatment algorithm. https://bestpractice.bmj.com/topics/en-gb/3000168/treatment-algorithm#patientGroup-0- 1у 22. Mach F et al 2019 ESC/EAS Guidelines for themanagement of dyslipidaemias: lipid modification to reduce cardiovascular risk European Heart Journal (2019) 00, 178doi:10.1093/eurheartj/ehz455 23. Pulmonary embolismin COVID-19 patients: a French multicentre cohort study European Heart Journal (2020) 0, 1–11doi:10.1093/eurheartj/ehaa500. 24. Schulman S. et. al. ISTH guidelines for antithrombotic treatment in COVID-19 J Thromb Haemost. 2022 Oct; 20(10):2214-2225. doi: 10.1111/jth.15808. Epub 2022 Jul 29. 25. Giancarlo Agnelli, Buller HR, Cohen A, Apixaban for Extended Treatment of Venous Thromboembolism N Engl J Med 2013; 368:699-708, DOI: 10.1056/NEJMoa1207541. 26. Spyropoulos AC, Ageno Walter, Alber GW Post-Discharge Prophylaxis With Rivaroxaban Reduces Fatal and Major Thromboembolic Events in Medically Ill Patients Journal of the American College of Cardiology Volume 75, Issue 25, June 2020 DOI: 10.1016/j.jacc.2020.04.071 27. Weitz JI,. Lensing A, Prins MH Rivaroxaban or Aspirin for Extended Treatment of Venous thromboembolism N Engl J Med 2017; 376:1211-1222 DOI: 10.1056/NEJMoa1700518. 28. Schulman S, Kearon C, Kakkar AK Extended Use of Dabigatran, Warfarin, or Placebo in Venous Thromboembolism N Engl J Med 2013; 368:709-718 DOI: 10.1056/NEJMoa1113697 Connolly SJ, Ezekowitz MD et al. Dabigatran versus Warfarin in Patients with Atrial Fibrillation (RE-LY). N Engl J Med 2009; 361:1139-1151 DOI: 10.1056/NEJMoa0905561. 29. CDC.gov 2Du L et al Biochem Biophys Res Commun 2007; 359:174-9 30. Пособие по реабилитации после COVID-19 для пациентов https://apps.who.int/iris/bitstream/handle/10665/333288/WHO-EURO-2020-855-40590- 54572-rus.pdf 31. Второй этап (продолженный) медицинской реабилитации. "Внебольничная пневмония, в том числе COVID-19-пневмония" (взрослые) Одобрен Объединенной комиссией по качеству медицинских услуг Министерства здравоохранения Республики Казахстан от «10» сентября 2020 года Протокол №115 32. Третий этап (поздний) медицинской реабилитации. "Внебольничная пневмония, в том числе COVID-19 пневмония" (взрослые) Одобрен Объединенной комиссией по качеству медицинских услуг Министерства здравоохранения Республики Казахстан от «10» сентября 2020 года Протокол №115 33. Marietta М et al COVID-19 and haemostasis: a position paper from Italian Society on Thrombosis and Haemostasis (SISET). Blood Transfus. 2020:18 (3); 167-169. DOI 10.2450/2020.0083-20; 34. Donders F. ISIDOG Recommendations Concerning COVID-19 and Pregnancy Diagnostics 2020, 10, 243; doi: 10.3390/diagnostics10040243 35. Ramacciotti E, Barile Agati L, Calderaro D, et al. Rivaroxaban versus no anticoagulation for postdischargethromboprophylaxis after hospitalisation for COVID-19 (MICHELLE): an open-label,multicentre, randomised, controlled trial. Lancet. 2022; 399: 50-9. 36. Technical Report. Novel coronavirus (SARS-CoV-2).Discharge criteria for confirmed COVID-19 cases –When is it safe to discharge COVID-19 cases from the hospital or end home isolation? /European Centre for disease prevention and control// www.ecdc.europa.eu 37. Luo L, Liu D, Liao X, et al. Contact settings and risk for transmission in 3410 close contacts of patients with COVID-19 in Guangzhou, China: a prospective cohort study. Ann Intern Med. 2020 Aug 13 [Epub ahead of print]. 38. Koh WC, Naing L, Chaw L, et al. What do we know about SARS-CoV-2 transmission? A systematic review and meta-analysis of the secondary attack rate and associated risk factors. PLoS One. 2020 Oct 8; 15(10):e0240205. 39. Burke RM, Midgley CM, Dratch A, et al. Active monitoring of persons exposed to patients with confirmed COVID-19 - United States, January-February 2020. MMWR Morb Mortal Wkly Rep. 2020 Mar 6; 69(9):245-6. 40. Cheng HY, Jian SW, Liu DP, et al. Contact tracing assessment of COVID-19 transmission dynamics in Taiwan and risk at different exposure periods before and after symptom onset. JAMA Intern Med. 2020 May 1 [Epub ahead of print]. 41. Zhang W, Cheng W, Luo L, et al. Secondary transmission of coronavirus disease from presymptomatic persons, China. Emerg Infect Dis. 2020 May 26; 26(8). 42. Критерии для отмены режима изоляции в отношении пациентов с COVID-19 Научная справка ВОЗ - 17 июня 2020 г. 43. «Клинический протокол диагностики и лечения тромбоэмболия легочной артерий», одобренный Объединенной комиссией по качеству медицинских услуг Министерства здравоохранения и социального развития Республики Казахстан от «23» июня 2016 года Протокол № 5. 44. National Early Warning Score (NEWS) 2. https://www.rcplondon.ac.uk/projects/outputs/national-early-warning-score-news-2 45. Cruz AF, Ruiz-Antoran B, and Gomez AM et al. Impact of glucocorticoid treatment in SARS-CoV-2 infection mortality: A retrospective controlled cohort study. MedRxiv 2020. 46. Villar J, Confalonieri M, Pastores SM et al. Rationale for prolonged corticosteroid tratment in the acute respiratory distress syndrome (ARDS) caused by COVID-19. Crit Care Expl 2020; 2:e0111. 47. Fadel R, Morrison AR, Vahia A et al. Early course corticosteroids in hospitalized patients with COVID-19. MedRxiv 2020. 48. Chroboczek T, Lacoste M, Wackenheim C et al. Beneficial effect of corticosteroids in severe COVID-19 pneumonia: a propensity score matching analysis. MedRxiv 2020. 49. Liu J, Zheng X, Huang Y et al. Successful use of methylprednisolone for treating severe COVID-19. J Allergy Clin Immunol 2020. 50. Medicines and Healthcare products Regulatory Agency. Dexamethasone in the treatment of COVID-19: implementation and management of supply for treatment in hospitals. 2020 [internet publication].
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указанием квалификационных данных:
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
Указание условий пересмотра протокола: пересмотр не реже 1 раза в 5 лет и не чаще 1 раза в 3 года при наличии новых методов диагностики и лечения с уровнем доказательности.
Сокращения, используемые в протоколе:
|
АЛТ
|
аланинаминотрансфераза |
| АСК | ацетилсалициловая кислота |
| АСТ | аспартатаминотрансфераза |
| АЧТВ | активированное частичное тромбопластиновое время |
|
БА
|
бронхиальная астма |
| БСК | болезни системы кровообращения |
| ВДП | верхние дыхательные пути |
| ВГН | верхняя граница нормы |
|
ГЛП
|
гиперлипидемия |
| ГИТ | гепарин-индуцированная тромбоцитопения |
| ДВС | диссеминированное внутрисосудистое свертывание |
| ИБС | ишемическая болезнь сердца |
| ИВЛ | искусственная вентиляция легких |
|
КТ
|
компьютерная томография |
| КУЗИ | компрессионное УЗИ |
| КЩР | кислотно-щелочное равновесие |
| МВС | мультисистемный воспалительный синдром |
| МНО | международное нормализованное отношение |
|
НПВС
|
нестероидные противовоспалительные средства |
| НИВЛ | неинвазивная искусственная вентиляция легких |
| НЛИ | нейтрофильно-лимфоцитарный индекс |
| НМГ | низкомолекулярный гепарин |
| НФГ | нефракционированный гепарин |
|
ОДН
|
острая дыхательная недостаточность |
| ОКС | острый коронарный синдром |
| ОПП | острое повреждение почек |
| ОРВИ | острая респираторная вирусная инфекция |
| ОРЗ/ОРИ | острое респираторное заболевание/инфекция |
| ОРДС | острый респираторный дистресс синдром |
| ОСН | острая сердечная недостаточность |
|
ПИИК
|
профилактика инфекций и инфекционный контроль |
| ПГГСВ | Постановление Главного государственного санитарного врача |
| ПМСП | Первичная медико-санитарная помощь |
| ПЦР | полимеразная цепная реакция |
| РНК | рибонуклеиновая кислота |
|
СД
|
сахарный диабет |
| САД | систолическое артериальное давление |
| СрАД | среднее артериальное давление |
| СОЭ | скорость оседания эритроцитов |
| СПОН | синдром полиорганной недостаточности |
| СИЗ | средства индивидуальной защиты |
|
ССС
|
сердечно-сосудистая система |
| ТВ | тромбиновое время |
| ТОРИ | тяжелая острая респираторная инфекция |
| ТЭЛА | тромбоэмболия легочной артерии |
| ХСН | хроническая сердечная недостаточность |
| ХБП | хоническая болезнь почек |
| ЭКМО | экстракорпоральная мембранная оксигенация |
| COVID-19 | коронавирусная инфекция, впервые выявленная в 2019 г. |
|
ТОРС
короновирус/
SARS CoV
|
ТОРС-коронавирус, вызывающий тяжелый острый респираторный синдром/Severe acute respiratory syndrome coronavirus
|
|
SARS CoV-2
|
коронавирус-2, вызывающий COVID-19 (тяжелый острый респираторный синдром / Severe acute respiratory syndrome coronavirus)
|
|
ЧКВ
|
чрезкожное коронарное вмешательство |
| СPAP | постоянное положительное давление в дыхательных путях |
| FiO2 | фракция вдыхаемого кислорода |
| OI | индекс оксигенации |
| OSI | индекс оксигенации с использованием SpO2 |
|
PaO2
|
парциальное давление кислорода |
| PEEP | положительное давление конца выдоха |
| SpO2 | сатурация кислородом |
| HFNO |
high-flow nasal oxygenation - высокопоточная назальная
оксигенация
|
| IL-6 | интерлейкин-6 |
Приложения к клиническому протоколу "Коронавирусная инфекция COVID-19 у взрослых"
При COVID-19 от 4% до 5% всех инфицированных могут быть в критическом состоянии и нуждаться в наблюдении и лечении в отделении реанимации/интенсивной терапии (ОРИТ), и у двух третей из них, как правило, развивается COVID-19 специфическое поражение лёгких [6] и/или острый респираторный дистресс-синдром (ОРДС), при котором необходима искусственная вентиляция легких (ИВЛ).
Использование соответствующих средств индивидуальной защиты (СИЗ), их правильное надевание, снятие, утилизация, надлежащая гигиена рук, маршрутизация потоков в ОРИТ имеют первостепенное значение для предотвращения передачи респираторной инфекции COVID-19 пациентам и медицинским работникам.
Поэтому стандартизированные протоколы и меры защиты должны быть приняты, чтобы свести к минимуму риск контаминации и уменьшить количество осложнений [1,5,12]:
• выполнять процедуры в хорошо проветриваемом помещении
• использовать соответствующие СИЗ:
Основные принципы терапии неотложных состояний при коронавирусной инфекции COVID-19:
Наблюдение за клиническим состоянием пациента осуществляется непрерывно, с почасовым отражением витальных показателей, врачебных назначений в карте менеджмента, согласно Приложению 2 (пациент без ЭКМО) и Приложению 3 (пациент на ЭКМО).
Противовирусная, антибактериальная и противогрибковая терапия осуществляются согласно текущему Клиническому протоколу (раздел 5.3 Медикаментозное лечение).
Идеальная масса тела (ИМТ):
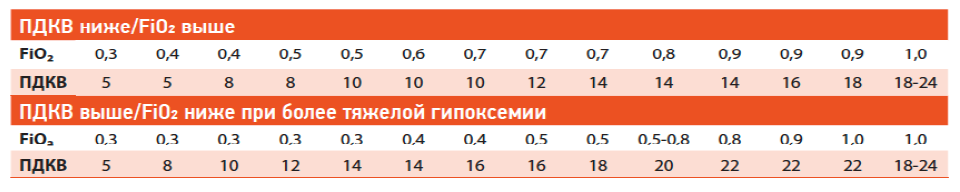
Неинвазивная вентиляция легких и высокопоточная назальная оксигенация (HFNO):
Примечание. У взрослых пациентов с острой гипоксемической дыхательной недостаточностью на кислороде, рекомендуется поддерживать SpO2 на уровне 90-96%
ВАЖНО соблюдать следующие алгоритмы:
Слив конденсата из влагосборника дыхательного контура:
Противопоказания [8]:
Снижение частоты развития стрессовых язв и желудочно-кишечных кровотечений.
Алгоритм отлучения пациента от ИВЛ [10]
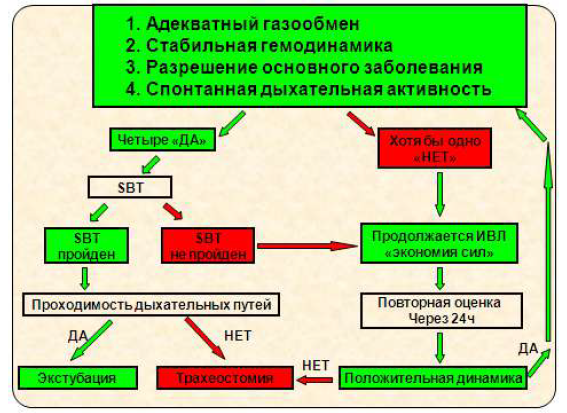
Варианты седации пациента на ИВЛ:
Ренальные:
Показаниями к проведению «почечной поддержки» методами ЗПТ являются: обеспечение полноценного питания и инфузионной терапии при олигоанурии, удаление жидкости при застойной сердечной недостаточности, и поддержание адекватного гидробаланса у пациента с полиорганной недостаточностью.
Кроме того, показанием к срочному началу экстракорпорального лечения являются:
Относительные противопоказания к проведению процедур ЗПТ:
• уменьшение признаков гипергидратации (при наличии).
4. Комбинация методов экстракорпоральной гемокоррекции и комбинированные методики:
|
NB!!! В зависимости от клинической ситуации по показаниям может меняться доза, кратность и продолжительность АКТ на основе решения врачебного консилиума.
|
| АЧТВ | Дозирование |
| ˂35с (˂1,2*контроль) | 80 МЕ/кг болюсно, увеличение в инфузии на 4 ME/кг/ч |
| 35-45с (1,2-1,5*контроль) | 40 МЕ/кг болюсно, увеличение в инфузии на 2 ME/кг/ч |
| 46-70с (1,5-2,3*контроль) | Не меняется |
| 71-90с (2,3-3,0*контроль) | Уменьшение в инфузии на 2 ME/кг/ч |
| ˃90с (˃3,0*контроль) |
Остановить инфузию на 1 час, затем снизить в инфузии
на 3 МЕ/кг/ч
|
|
Терапевтические дозы антикоагулянтов назначаются только в случае подтвержденного диагноза ТГВ и ТЭЛА. Возможно применение терапевтических доз АКТ при особых случаях COVID-19 при отсутствии диагноза ТГВ и ТЭЛА (например, при тяжелой форме ОРДС) решением консилиума, однако пока доказательств не получено.
Пациентам с ВТЭ с нестабильной гемодинамикой предпочтительно применение НФГ под контролем АЧТВ. Пациентам с тяжелой формой, но относительно стабильной гемодинамикой могут продолжить НМГ. В случае нестабильности гемодинамики или ухудшения функции почек (при уровне КК ниже 30 мл/мин) показан перевод на НФГ решением консилиума.
|
Терапевтические дозы антикоагулянтов*
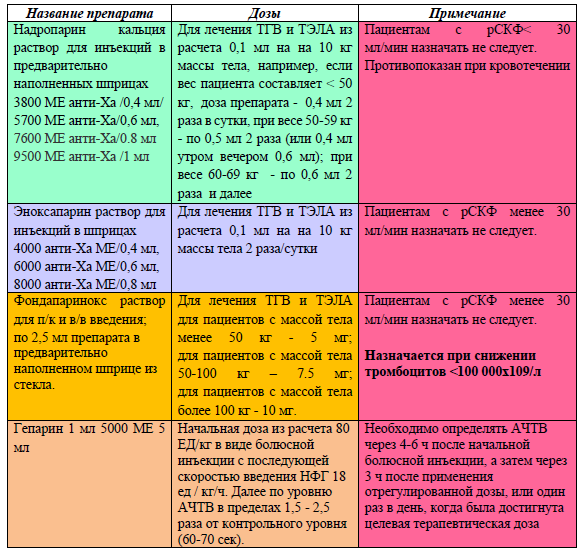
Контроль гипергликемии:
Определение нутритивной недостаточности.
| Степени | Легкая | Средняя | Тяжелая |
| Общий белок, г\л | 60-55 | 55-50 | Менее 50 |
| Альбумин, г\л | 35-30 | 30-25 | < 25 |
| Трансферрин г\л | 2,0-1,8 | 1,8-1,6 | < 1,6 |
|
Лимфоциты, абсолютное количество
|
1800-1500 | 1500-800 | < 800 |
|
Дефицит массы тела в % от идеально массы
|
11-10% | 21-30% | более 30% |
| Индекс масса-рост, кг\м2 | 19-17,5 | 17.5-15,5 | <15,5 |
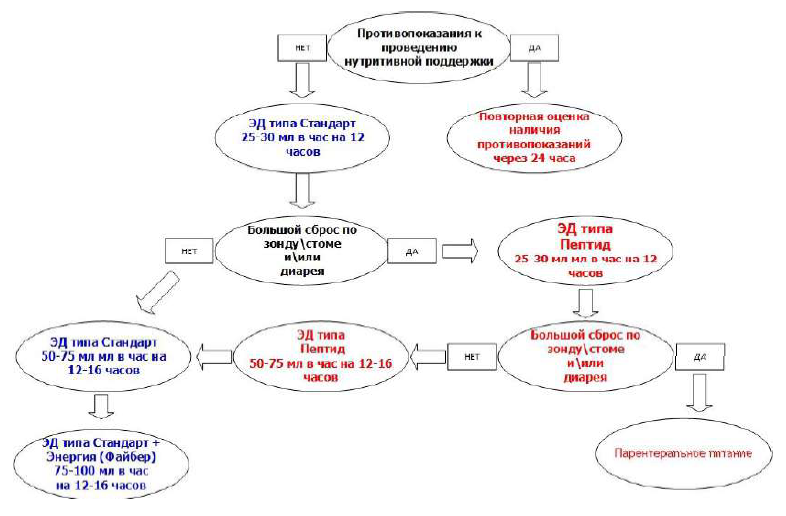
Физиотерапия
Список медицинских изделий реанимационного отделения инфекционного стационара
| № | Наименование | Количество | Примечание |
| 1 |
Аппарат искусственой вентиляции легких
|
1 единица на 1 койку |
параметры аппарата должны быть предусмотрены для длительной вентиляции, желательно аппарат экспертного класса
|
| 2 |
Монитор с гемодинамическим модулем и пульсоксиметром
|
1 единица на 1 койку |
обязательное наличие гемодинамического модуля для оценки параметров дыхания
|
| 3 | Перфузоры |
не менее 5 единиц на 1 койку
|
|
| 4 | Инфузомат | 2 единицы на 1 койку | |
| 5 |
Ультразвуковой аппарат экспертного класса
|
1 единица на 1 реанимационное отделение
|
|
| 6 |
Аппарат для определения кислотно-щелочного состояния (КЩС)
|
1 единица на 1 реанимационное отделение
|
|
| 7 |
Аппарат для определения ACT (активированное время свертывания)
|
1 единица на 1 реанимационное отделение
|
|
| 8 | ЭКГ аппарат |
1 единица на 1 реанимационное отделение
|
|
| 9 |
Передвижной рентгенаппарат (мобильный)
|
1 единица на 1 реанимационное отделение
|
|
| 10 |
Видеобронхоскоп с эндоскопической стойкой
|
1 единица на 1 реанимационное отделение | |
| 11 |
Моечная машинка для обработки эндоскопа
|
1 единица на 1 реанимационное отделение | |
| 12 |
Противопролежневый матрац многофункциональный
|
1 единица на 1 койку | |
| 13 |
Тепловая пушка с обдувным одеялом
|
1 единица на 1 койку | |
| 14 | Электронный термометр | 1 единица на 1 койку | |
| 15 |
Аппарат продленной заместительной почечной терапии
|
по мере необходимости
|
|
| 16 |
Оборудование для проведения бифокальной резонансной виброакустической терапии
|
количество зависит от числа коек в отделении
|
|
| 17 |
Аппарат для проведения высокопоточной оксигенотерапии
|
по мере необходимости |
Список расходных компонентов на одного пациента на ИВЛ в сутки
| № | Наименование | Количество | Примечание |
| 1 | Контур ИВЛ | 1 шт | замена 1 раз в 3 дня |
| 2 | Фильтр ИВЛ (антибактериальный противовирусный, влагозащищенный) | 10 шт | Замена каждые 4 часа |
| 3 | Закрытая аспирационная система (размер 14-16) | 1 шт | замена 1 раз в 3 дня |
| 4 | Аспирационный катетер (размер 14-16-18) | 5 шт | |
| 5 | Трубка интубационная (размер 8,0, 7,0, 7,5) | 2 шт | |
| 6 | Фиксатор интубационной трубки | 3 шт | |
| 7 | Набор для пункционной трахеостомии | 1 шт | |
| 8 | Набор для пункционной гастростомии | 1 шт | |
| 9 | Набор для гигиены пациента KimberlyClark | по мере необходимости | |
| 10 | Подгузники для взрослых | по мере необходимости | |
| 11 | Небулайзер контура ИВЛ | 2 шт | |
| 12 | Фартук одноразовый | по мере необходимости | |
| 13 | Гофрированный переходник контура ИВЛ | 5 шт | |
| 14 | Вода дистиллированная стерильная | 1 литр | |
| 15 | Перчатки не стерильные (размер L, М) | 100 шт | |
| 16 | Перчатки стерильные (размер 7,5 - 8,0) | 10 шт | |
| 17 | Колпак (шапочка-берет) | 10 шт | |
| 18 | Халат стерильный | 5 шт | |
| 19 | Маска – респиратор | 3 шт | |
| 20 | ЦВК катетер (центральный венозный катетер) | 1 шт | обязательно должен быть трех- или четырехпортовый |
| 21 | Периферический катетер (размер 20 G; 22G;) | 5 шт | |
| 22 | Мочевой катетер | 1 шт | |
| 23 | Мочеприёмник для контроля почасового диуреза | 1 шт | |
| 24 | Лейкопластырь | 2 шт | |
| 25 | Бинт стерильный | 1 шт | |
| 26 | Адгезивная повязка размер |
10*35 – 2 шт, 10*25 – 2 шт, 7*8,5 – 3 шт |
|
| 27 | Антисептик для рук | 1 шт | |
| 28 | Антисептик водный для слизистых | 1 литр | |
| 29 | Спиртовый антисептик для распыления (Хлоргексидин) | по мере необходимости | |
| 30 | Электроды ЭКГ – | 30 шт | |
| 31 | Зонд желудочный | 1-2 шт. | |
| 32 | Шприц: 2,0 | 20 шт | |
| 33 | Шприц: 5,0 | 30 шт | |
| 34 | Шприц: 10,0 | 30 шт | |
| 35 | Шприц: 20,0 | 30 шт | |
| 36 | Шприц: Жане | 2 шт | |
| 37 | Шприц: 50,0 | 10 шт | |
| 38 | Шприц: инсулиновый | 10 шт | |
| 39 | Шприц гепаринизирванный | 10 шт | |
| 40 | Система для переливания крови и компонентов | 5 шт | |
| 41 | Система для переливания растворов | 5 шт | |
| 42 | Система для введения энтерального питания | 2 шт | |
| 43 | Система (удлинитель для дозаторов) | 15 шт | |
| 44 | Система для инвазивного давления (АД, ЦВД) | 1 шт | |
| 45 | Катетер для измерения инвазивного АД | по мере необходимости | |
| 46 | Стоп кок (краник 3х ходовой) | 10 шт | |
| 47 | Мини спайк | ||
| 48 | Пробирки для анализов: биохимический анализ | 3 шт | |
| 49 | Пробирки для анализов: Общий анализ крови | 3 шт | |
| 50 | Пробирки для анализов: Коагулограмма | 3 шт | |
| 51 | Пробирки для анализов: Обший анализ мочи | 2 шт | |
| 52 | Пробирки для сбора образцов бронхо-альвеолярного лаважа | по мере необходимости | |
| 53 | Шовный материал с иглой (шёлк) | 2 шт | |
| 54 | Скальпель | 2 шт | |
| 55 | Жесткий наконечник для санации ротовой полости | 5 шт | |
| 56 | Кружка Эсмарха | 2 шт | |
| 57 | Глицерин Стерильный | 1 фл. | |
| 58 | Перевязочный набор (перевязочный материал (салфетки, шарики), пинцет, иглодержатель) | 2 шт | |
| 59 | Повидон-йод | 1 фл | |
| 60 | Бумажные полотенца/салфетки | по мере необходимости | |
| 61 | Контейнер КБСУ | по мере необходимости | |
| 62 | Емкость для взятия промывных вод | 3 шт | при проведении бронхоскопии |
| 63 | Набор для заместительной терапии | 1 комплект по мере необходимости | |
| 64 | Раствор для гемо/диафильтрации 5л | 5 мешков в сутки | |
| 65 | Набор для катетеризации центральных вен двухпросветный для проведения заместительной почечной терапии | 1 комплект | |
| 66 | Набор для проведения высокопоточной кислородотерапии | по мере необходимости |
Лекарственные средства на 1 пациента 1 день на ИВЛ
| № | Направление | Наименование ЛС | Количество |
| 1 | Антибактериальная терапия | Амоксициллин+Клавулановая кислота875/125 | 2 |
| 2 | |||
| 4 | Линезолид 600 мг | 2 | |
| 5 | Цефтриаксон 1 г | 2 | |
| 6 | Цефтазидим 2 г | 4 | |
| 7 | Цефепим 1 г | 2 | |
| 8 | Левофлоксацин 500 мг | 1 | |
| 9 | Ципрофлоксацин 200 мг | 2 | |
| 10 | Моксифлоксацин 400 мг | 1 | |
| 11 | Пиперациллин/Тазобактам 4,5 г | 3 | |
| 12 | Меропенем 1 г | 3-4 | |
| 13 | Ванкомицин 1 г | 2 | |
| 14 | Амикацин 500 мг | 1-3 | |
| 15 | Гентамицин 80 мг | 4 | |
| 16 | Метронидазол 500 мг | 3 | |
| 17 | Цефоперазон/Сульбактам 2 г | 2 | |
| 18 | Имипенем/Циластатин 500 мг/500 мг | 3 | |
| 19 | Колистиметат натрия | 2 | |
| 20 | Противогрибковые препараты |
Флуконазол 200 мг |
1 |
| 21 | |||
| Вориконазол 200 мг | 1 | ||
| 22 | Гастропротекторы | Эзомепразол 40 мг | 1 |
| 23 | Фамотидин 40 мг | 2 | |
| 24 | Омепразол 20 мг | 2 | |
| 25 | Стимуляция ЖКТ | Метоклопрамид 0,5%, 2 мл | 3 |
| 26 | Неостигмин 0,5 мг/мл | 3 | |
| 27 | Муколитики | Ацетилцистеин 100 мг/мл; 600 мг | 2 |
| 28 | Инсулин | Инсулин короткого действия Ед | 10-20 |
| 29 | Электролиты | Калия хлорид, раствор для в/в введения 4%-10 мл | 1-20 |
| 30 | Кальция хлорид, раствор для в/в введения 10%-5 мл | 1-10 | |
| 31 | Магния сульфат, раствор для в/в введения 25%-5 мл | 1-10 | |
| 32 | Седативные препараты, аналгетики, миорелаксанты | Пропофол 10 мг/мл по 50 мл, 20 мл, 10 мл | 1-10 |
| 33 | Дексмедетомидин 100 мкг/мл по 4 мл, 2 мл | 1-6 | |
| 34 | Фентанил 0,005% | 10 | |
| 35 | Морфин 1% по 1 мл | 1-3 | |
| 36 | Диазепам 5 мг/мл по 2 мл | 6 | |
| 37 | Трамадол 5% по 1 мл | 1-4 | |
| 38 | Рокурония Бромид 10 мг/мл, 10 мл; 5 мл. | 1-10 | |
| 39 | Атракурия Безилат 25 мг/2,5 мл | 1-5 | |
| 40 | Пипекурония Бромид 4 мг | 1-5 | |
| 41 | Анилиды | Парацетамол, таб 500 мг | 1-8 |
| 42 | Парацетамол, раствор для инфузий 1000 мг/ 100 мл | 1-4 | |
| Парацетамол суспензия 120 мг/5 мл | 1 | ||
| 43 | НПВС | Ибупрофен, 200 мг, 400 мг. | 1-2 |
| 44 | Ибупрофен, 400 мг/4 мл; 800мг/8 мл | 1-3 | |
| Ибупрофен, суспензия 100 мг/5 мл | 1 | ||
| 45 | Антигистаминные средства | Хлоропирамин 2% по 1 мл | 1-2 |
| 46 | |||
| 47 | Кортикостероиды | Преднизолон 30мг | 1-12 |
| 48 | Дексаметазон 4 мг | 1-5 | |
| 49 | Метилпреднизолон 250 мг | 1-4 | |
| 50 | Гидрокортизон 2,5% 2 мл | 2-10 | |
| 51 | Инфузионная терапия | Сбалансированнй электролитный раствор для инфузий (калия хлорид, кальция хлорида дигидрат, магния хлорида гексагидрат, натрия ацетата тригидрат, натрия хлорид, яблочная кислота) 1000 мл, 500 мл | 1-3 |
| 52 | Сукцинилированный желатин раствор для инфузий 500 мл | 1-3 | |
| 53 | Натрия хлорид, раствор для инфузий 0,9%-500 мл, 400 мл, 250 мл, 200 мл, 100 мл, 10 мл, 5 мл | 1-3 | |
| 54 | Декстроза раствор для инфузий 5%-500 мл, 400 мл, 200 мл, 250 мл, 100 мл | 1-3 | |
| 55 | Натрия Гидрокарбонат раствор для инфузий 4% - 200 мл | 1-6 | |
|
56 |
Парентеральное питание | Аминокислоты для парентерального питания + Прочие препараты (Жировые эмульсии для парентерального питания + Декстроза + Минералы) Эмульсия для инфузий | 1-2 |
| Аминокислоты для парентерального питания + Прочие препараты (Декстроза + Минералы) | 1-2 | ||
| 57 | Энтеральное зондовое питание | Специализированные продукты для энтерального питания. Полноценные, сбалансированные по всем нутриентам, готовые к использованию жидкие смеси для перорального или зондового питания. | 1-5 |
| 63 | Ингаляционная терапия | Ипратропия бромид + Фенотерол 1 мл-2,5 мл (10-20 кап) | 3 |
| 64 | Будесонид 0,5 мг/мл | 3 | |
| 63 | Петлевые диуретики | Фуросемид, 20 мг | 1-20 |
| 64 | Торасемид, 5 мг | 1-10 | |
| 65 | Вазопрессоры | Норэпинефрин 2 мг/мл, 4 мл | 1-10 |
| 66 | Эпинефрин 0,18 % 1 мл | 1-10 | |
| 67 | Вазопрессин 40Ед | 1-3 | |
| 68 | Инотропные препараты | Добутамин 250 мг | 1-5 |
| 69 | Допамин 4% по 5 мл | 1-3 | |
| 70 | Холинолитики | Атропин 1 мг/мл | 1-5 |
| 71 | Антикоагулянты | Нефракционированный гепарин 25000 Ед | 1-2 |
| 72 | Эноксапарин 4000 анти-Ха МЕ/0,4 мл; | 1-2 | |
| Эноксапарин 6000 анти-Ха МЕ/0,6 мл | 1-2 | ||
| 73 | Надропарин кальция 3800 МЕ анти-Ха/0,4мл | 1-2 | |
| Надропарин кальций 5700 МЕ анти-Ха/0,6мл | 1-2 | ||
| 74 | Фондапаринукс натрия 2,5 мг/0,5 мл | 1 | |
| 75 | Антиаритмические препараты | Амиодарон 150 мг/3 мл | 1-8 |
| 76 | Метопролол 1 мг/мл 5 мл | 1-5 | |
| 77 | Бисопролол 5 мг | 1-3 | |
| 78 | Дигоксин 0,25 мг | 1 | |
| 79 | Верапамил 5 мг | 1-10 | |
| 80 | Препараты крови | Альбумин раствор для инфузий10%; 20% 100;200 мл | 1-3 |
| 81 | Концентат протромбинового комплекса 500 МЕ | 2-6 | |
| 82 | |||
| 83 | Ксантины | Аминофиллин раствор для инъекций 2,4% | 1-2 |
| 84 | Антисептики и дезинфицирующие средства | Хлоргексидин, водный раствор д/местн. и наружн. прим. 0.05% | 1-20 |
| 85 | Хлоргексидин, спиртовой раствор д/местн. и наружн. прим. 2% | 1-20 | |
| 86 | Повидон-йод , раствор д/наружн. прим. 10% | 1-30 |
Приложение 2.
Карта менеджмента пациента в палате интенсивной терапии (предоставлена автором Вахрушевым И.А.)
(карта приложена отдельно в формате Word в разделе "Прикрепленные файлы")
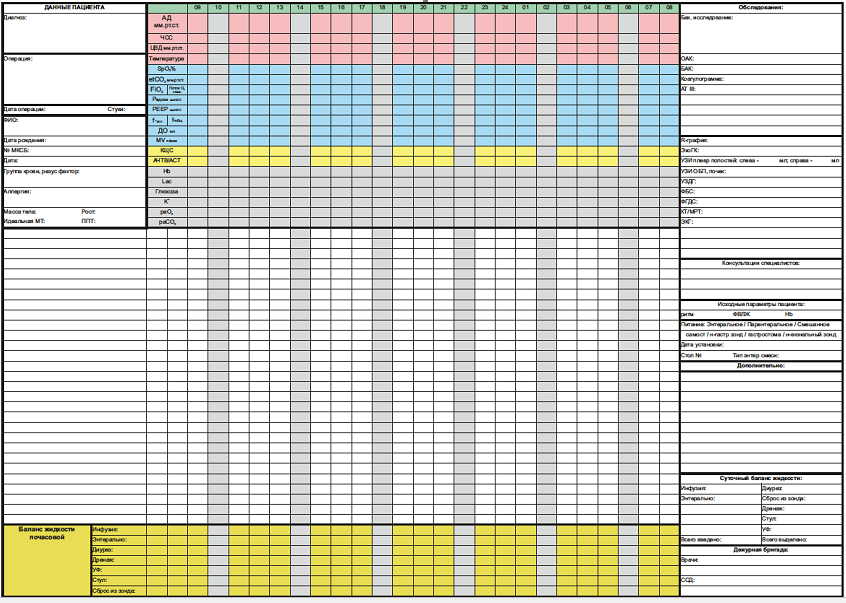
Приложение 3. Карта менеджмента пациента на ЭКМО в палате интенсивной терапии (предоставлена автором Вахрушевым И.А.)
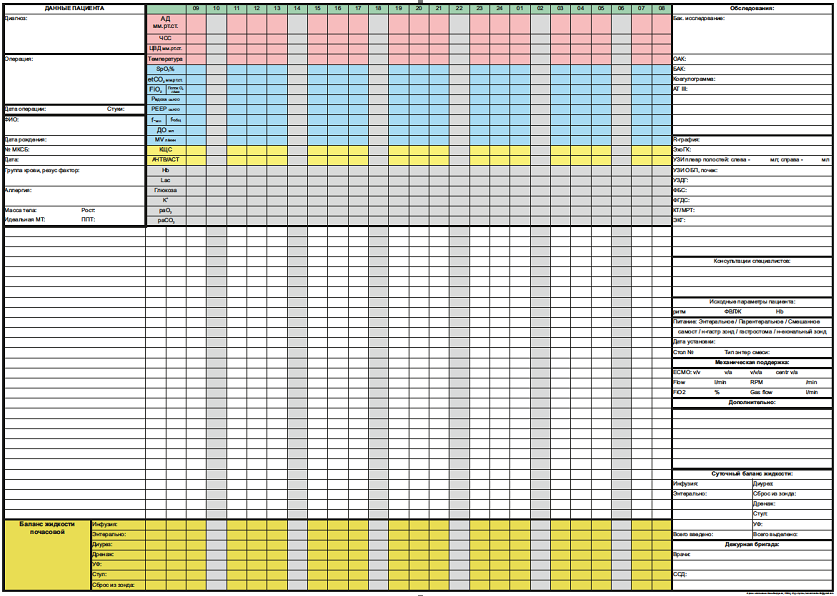
Таблица расчета дозы кардиотоников и вазопрессоров (использовать при отсутствии перфузоров с функцией расчета вводимой дозировки препарата).
Ссылка предоставлена автором Логвиненко И.А.
! Действующий калькулятор для расчета приложен отдельно в формате Excel в разделе "Прикрепленные файлы"
Основным показанием для проведения ЭКМО является тяжёлая дыхательная недостаточность, обуславливающая высокий риск смерти (вследствие ОРДС тяжелого течения или COVID-19 специфического тяжёлого повреждения лёгких) не поддающаяся максимальной терапии (включающей протективную ИВЛ, перевороты в prone позицию, маневры рекрутмента, миорелаксацию и седацию) с длительностью ИВЛ не более 5 суток. При присоединении сердечной (например, при миокардите) и/или сердечно-сосудистой (например, при развитии сепсиса) недостаточности следует рассматривать ЭКМО как циркуляторную и дыхательную поддержку. Роль ЭКМО в менеджменте пациентов с COVID-19 в натоящее время не донца изучена (1,2,3).
Целевые параметры производительности ЭКМО.
Вено-венозное ЭКМО.
FiO2 100%
Поток газа в соотношении 1:1 (1 литр производительности ЭКМО к 1 литру сжатого воздуха, подаваемого в газовый смеситель)
Производительность ЭКМО (LPM) для взрослых: 80 мл/кг/мин.
Вено-артериальное ЭКМО.
FiO2 100%
Поток газа в соотношении 1:1 (1 литр производительности ЭКМО к 1 литру сжатого воздуха, подаваемого в газовый смеситель)
Производительность ЭКМО (LPM) для взрослых: 80 мл/кг/мин (максимально 80% от расчётного минутного объёма кровообращения пациента)
Таблица взята из NIHNHLBIARDSClinical Network Mechanical Ventilation Protocol Summary.
| FiO2 | Low PEEP | High PEEP |
| 0.3 | 5 | 5-14 |
| 0.4 | 5-8 | 14-16 |
| 0.5 | 8-10 | 16-20 |
| 0.6 | 10 | 20 |
| 0.7 | 10-14 | 20 |
| 0.8 | 14 | 20-22 |
| 0.9 | 14-18 | 22 |
Рисунок 1. Фемо-яугулярная конфигурация ВВ ЭКМО.
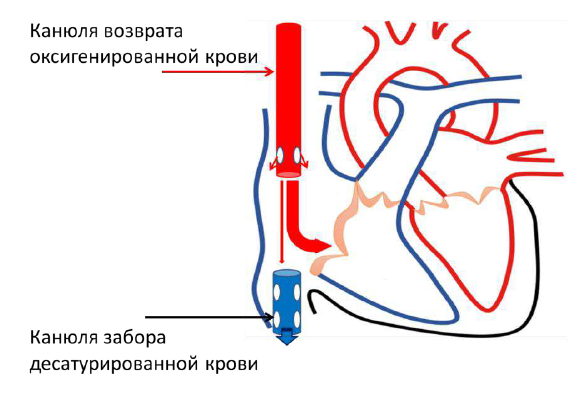
Рисунок 2.Двухпросветная канюля ВВ ЭКМО.
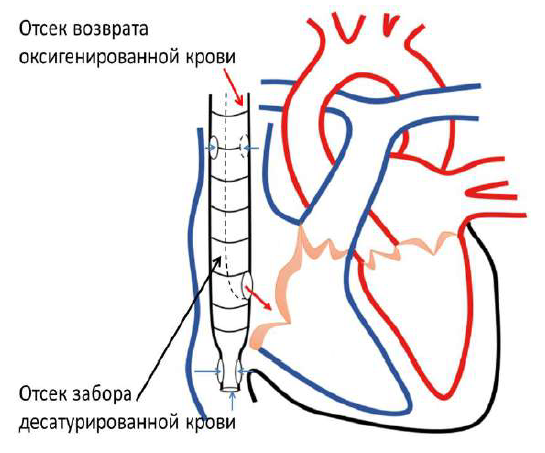
Рисунок 3. фемо-феморальная конфигурация ВВ ЭКМО.
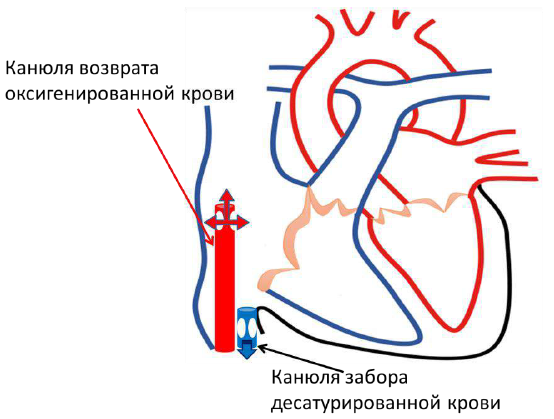
Рисунок 4. Синдром Арлекино.
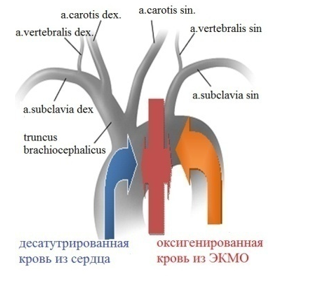
Для своевременного распознавания данного осложнения необходимо мониторировать SаO2 и/или газовый состав артериальной крови из ПРАВОЙ лучевой артерии.
Бифеморально-яугулярная конфигурация - забор десатурированной крови из системы нижней полой вены, возврат оксигенированной крови в артериальную систему (через общую бедренную артерию, при этом кончик канюли достигает общей подвздошной артерии или нисходящей части аорты) и в правое предсердие через v. Jugularis interna dex.
Рисунок. Бифеморально-яугулярная конфигурация периферической вено-артериальной ЭКМО.
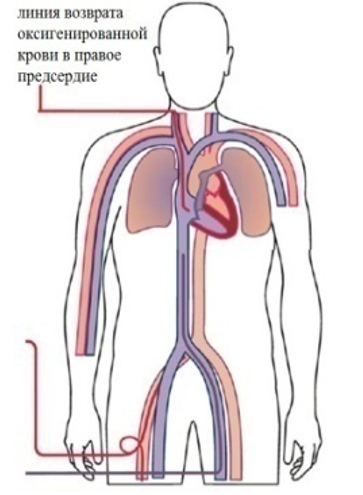
Экстренное отлучение - процесс снижения производительности ЭКМО с последующим отключением, несмотря на потребность в ней. Причинами, побуждающими к этому, являются грозные осложнения, такие как массивное кровотечение, выраженный гемолиз, канюли ассоциированная инфекция и др.
Отключение – временная остановка ЭКМО, перед деканюляцией, для демонстрации того, что пациент способен находиться без ЭКМО. Отключение выполняется только после успешного процесса отлучения, когда 70% - 80% нагрузки могут быть толерированы сердцем и лёгкими. Последнее должно быть документировано исследованием гемодинамических параметров, газового и метаболического статуса пациента.
Деканюляция – процедура извлечения канюль контура ЭКМО из крупных сосудов или из камер сердца после успешного процесса отлучения и отключения.
Отлучение от вено-венозного ЭКМО.
Карта отлучения от ЭКМО (4).
______день на ЭКМО. Дата ___(ч)/___(м)/20___(г). Начало ___:___ Окончание ___:___
Кардио/хирург/и ________________ _____________________
Анестезиолог/Реаниматолог ________________ _____________________
Перфузиолог ________________ _____________________
Кардиолог/Специалист ЭХОКГ ________________ _____________________
Анестезист(ка) ________________ _____________________
Операционная м/с / м/б ________________ _____________________
АСТ до начала отлучения _____ секунд.Болюс Гепарина ______тысяч МЕ перед началом процедуры. АСТ _____ секунд.
| Время |
Начало __:__ |
__:__ |
__:__ |
__:__ |
| КЩС/газы крови | ||||
| Hb г/л | ||||
| Ph | ||||
| PO2 mmHg | ||||
| PCO2 mmHg | ||||
| SaO2% | ||||
| Lac mmol/l | ||||
| Base mmol/l | ||||
| HCO3 mmol/l | ||||
| FShunt % | ||||
| SaO2 % (вен/смеш.вен) |
| Время |
Начало ___:___ |
___:___ |
___:___ |
___:___ |
| Поток ЭКМО л/мин | ||||
| Параметры гемодинамики | ||||
| Ритм | ||||
| ЧСС | ||||
| АД(сист/диаст)mmHg | ||||
| СрАДmmHg | ||||
| ЦВД mmHg | ||||
| ДЛА mmHg | ||||
| ДЗЛК mmHg | ||||
| СВл/мин | ||||
| ОПСС | ||||
| ЛСС | ||||
| Поддержка гемодинамики | ||||
| Норэпинефринµg/кг/мин | ||||
| Эпинефринµg/кг/мин | ||||
| Милринон µg/кг/мин | ||||
| Добутамин µg/кг/мин | ||||
| Левосимендан µg/кг/мин | ||||
| ВАБК (соотношение) | ||||
| NO (ppm) | ||||
| Параметры ИВЛ | ||||
| Режим | ||||
| ПДКВ | ||||
| FiO2 % | ||||
| ЧД/МОВ | ||||
| P insp | ||||
| P peak | ||||
| Compliance mbar/L/s | ||||
| Resistance ml/mbar |
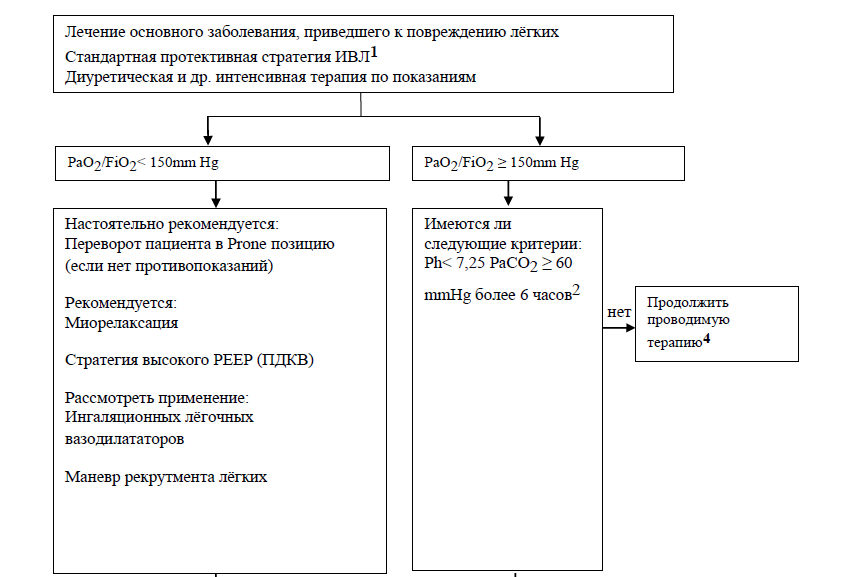
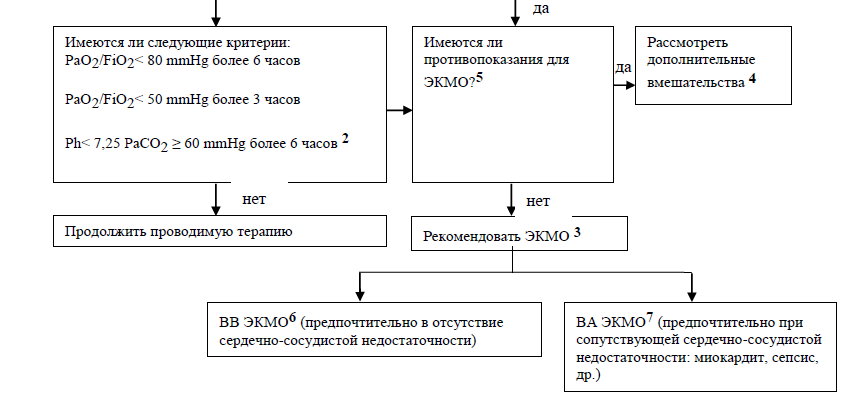
Приложение 5
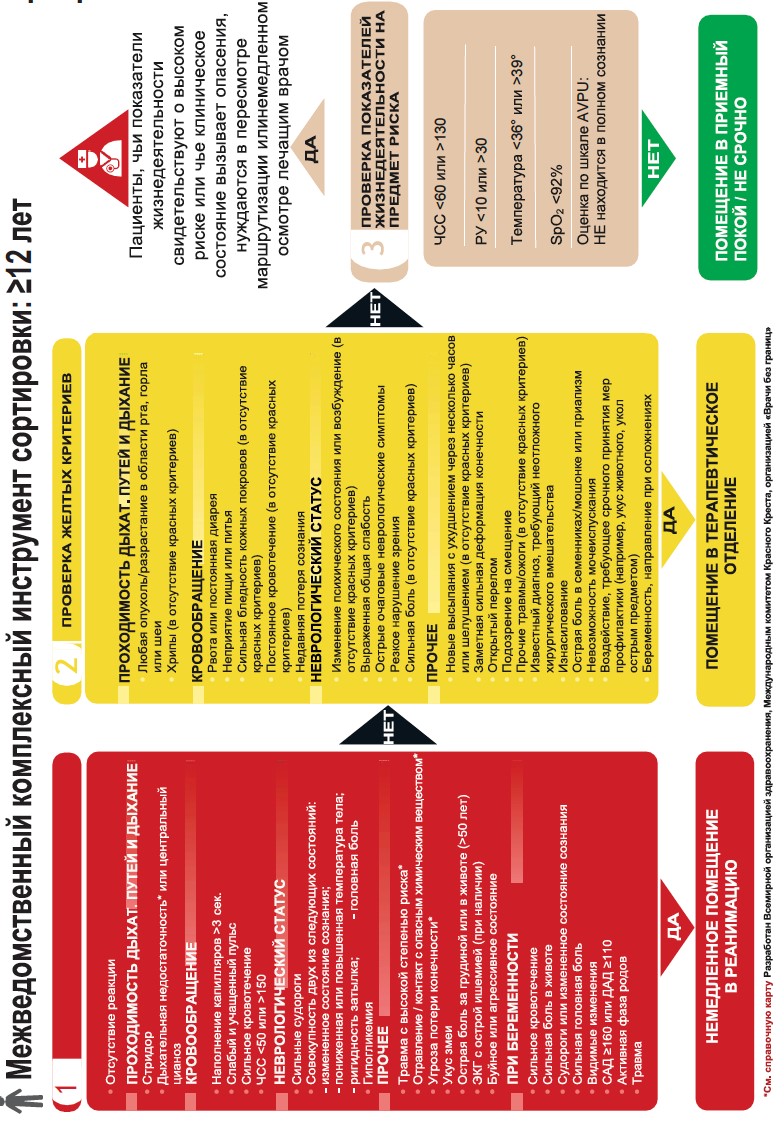
ИНФОРМИРОВАННОЕ СОГЛАСИЕ
Я, ___________________________________________________________/________/_________,
(Ф.И.О. пациента полностью, число, месяц, год рождения пациента)
адрес _____________________________________________________________________________
Родитель: мать / отец ______________________________________________________________,
(ФИО полностью, дата рождения родителя)
адрес_________________________________________________________________________
Опекун/законный представитель пациента _____________________________________________________________________________,
(ФИО полностью, дата рождения опекуна или представителя пациента)
адрес _____________________________________________________________________________
Заявляю о добровольном согласии на применение этиопатогенетических лекарственных средств или других видов лечения COVID-19 _____________________________________________________________________________________________________________________________
(указать название лекарственного средств, форма выпуска, доза, путь введения или вид лечения при оказании мне/моему подопечному медицинских услуг при лечении COVID-19)
1.Я, получил(а) от лечащего врача полную информацию о коронавирусной инфекции, прогнозе заболевания, течении и возможных исходах, и осложнениях.
2. Я понимаю, что в настоящее время нет четких и достаточных данных, подтверждающих либо опровергающих эффективность иммунной плазмы реконвалесцентов, ремдесивира и тоцилизумаба. Основанием для их применения являются результаты небольших открытых исследований, либо положительный опыт применения в других странах и клиниках у пациентов с коронавирусной инфекцией.
3. Я понимаю, что существует альтернативный подход в лечении коронавирусной инфекции – это стандартная поддерживающая терапия без применения экспериментальных препаратов.
4. Я получил от лечащего врача информацию о возможных нежелательных эффектах и вероятности их появления при применении иммунной плазмы реконвалесцентов, ремдесивира и тоцилизумаба. Я понимаю и осознаю риски и возможную пользу от него.
5. Я заявляю, что получил ответы на все интересующие меня вопросы, которые были мною заданы, все полученные ответы и разъяснения врача мною поняты, возможные риски от применения иммунной плазмы реконвалесцентов и других видов лечении я понимаю.
6. Я знаю, что в моих интересах сообщить врачу обо всех имеющихся у меня (подопечного) и известных мне проблемах со здоровьем, аллергических реакциях/осложнениях от вводимых раньше препаратов, непереносимости, побочных эффектах лекарств, о наличии в прошлом или в настоящее время инфекционного гепатита, туберкулеза, венерических заболеваний (в том числе сифилиса), ВИЧ-инфекции, а также о злоупотреблении алкоголем и/или пристрастии к наркотическим препаратам или иных зависимостях.
7. Я понимаю, что нарушение врачебных рекомендаций, а также сокрытие информации о состоянии здоровья может привести к осложнениям терапии и другим неблагоприятным последствиям.
8. Я уведомлен (а) о том, что ухаживающим лицам запрещено самостоятельно вмешиваться в назначение врача, самостоятельно без уведомления врача принимать собственные медикаменты и БАДы.
9. Информацию о состоянии моего здоровья, результатах обследования и лечения я разрешаю сообщать следующим лицам:
_____________________________________________________________________________
(ФИО лица, которому разрешается сообщать о ходе лечения, родство /отношение к пациенту (друг, доверенное лицо, опекун, представитель интересов)
Контакты лиц, которым разрешаю передавать информацию о моём здоровье
_____________________________________________________________________________
(телефоны, адреса электронной почты)
10. Сведения обо мне (моем ребенке или подопечном) могут быть использованы в целях проведения статистических, эпидемиологических и/или клинических исследований, и должны быть обезличены.
11. Я полностью ознакомлен(а) со всеми пунктами настоящего документа и подтверждаю
_____________________________________________________________________________
(ФИО и подпись пациента; или ФИО, дата рождения и подпись законного представителя пациента, его отношение к пациенту)
Дата: «___» __________ 20____года Время: _______
Врач: __________________________Подпись______________Дата: ____________Время: __
Лекарственное взаимодействие Нирматрелвир/ Ритонавир
|
Противопоказано назначение в комбинации со следующими препаратами
|
Значимое взаимодействие | Умеренное взаимодействие |
|
Альфузозин
Амиодарон
Апалутамид
Астемизол
Аторвастатин
Бепридил
Бромокриптин
Карбамазепин
Цизаприд
Клозапин
Колхицин
Кониваптан
Кризотиниб
Дигидроэрготамин
Дронедарон
Эфавиренц
Эльбасвир
Элетриптан
Элиглустат
Энкаинид
Эплеренон
Эрголоидные мезилаты
Эргоновин
Эрготамин
Эстетрол
Этинилэстрадиол
Эверолимус
Финеренон
флекаинид
Флибансерин
Флуконазол
Фосфенитоин
Гразопревир
Изавуконазония сульфат
ивабрадин
Лисуриде
Ломитапид
Ловастатин
Луразидон
Маравирок
Меперидин
Мезоридазин
Метерголин
Метилэргоновин
Метисергид
Мидазолам
Налоксегол
Нелфинавир
Ницерголин
Нимодипин
Фенобарбитал
Фенитоин
Пимозид
Пиперахин
Пироксикам
Примидон
Пропафенон
Пропоксифен
Хинидин
Ранолазин
Рифампин
Риосигуат
Ромидепсин
Силденафил
силодозин
Симвастатин
Сиролимус
Спарфлоксацин
Зверобой
Такролимус
Терфенадин
тиоридазин
Толваптан
Триазолам
Уброгепант
Венетоклакс
Воклоспорин
Вориконазол
Зипразидон
|
Абемациклиб
Акалабрутиниб
Адотрастузумаб эмтансин
Афатиниб
Альфентанил
Алпразолам
Амисульприд
Амлодипин
Амфетамин
Анагрелид
Апиксабан
Апоморфин
Апрепитант
Арипипразол
Арипипразол
Лауроксил
Триоксид мышьяка
Артеметер
Атогепант
Атоваквон
Авакопан
Аванафил
Авапритиниб
Акситиниб
Бедаквилин
Бензгидрокодон
Бензфетамин
Беротральстат
Бетаметазон
Бетриксабан
Боцепревир
Босентан
бозутиниб
Брекспипразол
Бригатиниб
Будесонид
бупренорфин
бупропион
бусерелин
Кабазитаксел
Каботегравир
Кабозантиниб
кальцифедиол
Карипразин
Церитиниб
Хлорохин
Циклесонид
Цилостазол
Кларитромицин клофазимин
Кобицистат
Кобиметиниб
Кодеин
Копанлисиб
Циклофосфамид
Циклоспорин
Дабигатран этексилат
Дабрафениб
Даклатасвир
Даридорексант
Дазатиниб
Деферазирокс
Дефлазакорт
Дегареликс
Деламанид
Дезлорелин
Дезогестрел
Дейтетрабеназин
Дексаметазон
Декстроамфетамин
Диеногест
Дигоксин
Дигидрокодеин
доцетаксел
Домперидон
Донепезил
Доксорубицин
Липосомы доксорубицина
гидрохлорида
Дроспиренон
Дувелисиб
Элаголикс
Элексакафтор
Элуксадолин
Энкорафениб
Энтректиниб
Энзалутамид
Эрлотиниб
Эритромицин
Эсциталопрам
Эстрадиол
Эзопиклон
Этинодиол
Этоногестрел
Этравирин
федратиниб
фентанил
Фезотеродин
Фексинидазол
Финголимод
Флуоксетин
Флутиказон
Формотерол
Фосапрепитант
Фоскарнет
Фостемсавир
Фузидовая кислота
Чеснок
Гестоден
Глаздегиб
Глекапревир
гонадорелин
Госерелин
Хемин
Хистрелин
Гидрокодон
Гидроксихлорохин
Гидроксизин
Ибрексафунгерп
Ибрутиниб
Иделалисиб
Ифосфамид
Илоперидон
Инфигратиниб
Инотузумаб Озогамицин
Иринотекан
Иринотекан липосома
Истрадефиллин
Ивакафтор
Ивосидениб
Иксабепилон
Кетоконазол
Лакосамид
Лапатиниб
Ларотректиниб
Лефамулин
Лемборексант
Ленватиниб
Левофлоксацин
Левомилнаципран
Левоноргестрел
Лисдексамфетамин
Лофексидин
Лорлатиниб
Луматепероне
Лурбинектин
Макиморелин
Маситентан
Манидипин
Медроксипрогестерон
Местранол
Метадон
Метамфетамин
Метилендиоксиметамфетамин
Метилпреднизолон
Метронидазол
Мидостаурин
Мифепристон
Миртазапин
Мобоцертиниб
Мометазон
Морфий
Липосомы сульфата морфина
Моксифлоксацин
Нафарелин
Нератиниб
Нифедипин
Нилотиниб
Номегестрол
Норелгестромин
Норэтиндрон
Норгестимат
Норгестрел
Олапариб
Омепразол
Ондансетрон
Орлистат
Осилодростат
Осимертиниб
Оксалиплатин
Оксикодон
Озанимод
Палбоциклиб
Панобиностат
Пасиреотид
Пазопаниб
Пемигатиниб
Пентазоцин
пексидартиниб
Пибрентасвир
Пимавансерин
Питолизант
Пиксантрон
Понатиниб
Понесимод
Позаконазол
Пралсетиниб
правастатин
Преднизолон
Кветиапин
Хинин
Ребоксетин
Регорафениб
Релуголикс
Ретапамулин
Рибоциклиб
Рифабутин
рифапентин
Римегепант
Ривароксабан
Розувастатин
руксолитиниб
Салметерол
Сегестерон
селперкатиниб
Селуметиниб
Сертралин
Севофлуран
Симепревир
Сипонимод
Сиролимус, связанный с белками
Сонидегиб
Соталол
Суфентанил
Сульпирид
Сунитиниб
Суворексант
Тадалафил
Тамсулозин
Таземетостат
Темсиролимус
Тезакафтор
Тиотепа
Тикагрелор
Топотекан
Торемифен
трабектин
Трамадол
Тразодон
Триамцинолон
Триклабендазол
Трипторелин
Валбеназин
Вандетаниб
Вемурафениб
Венлафаксин
Вилантерол
Вилазодон
Винбластин
Винкристин
Липосомы винкристина сульфата
Винфлунин
Ворапаксар
Занубрутиниб
Золпидем
Зуклопентиксол
|
Аценокумарол
Амитриптилин
Ампренавир
Церивастатин
Клоназепам
Дальфопристин
Делавирдин
Дезипрамин
Диданозин
Дизопирамид
Дутастерид
Фосампренавир
Имипрамин
Индинавир
Итраконазол
Ламотриджин
Левотироксин
мексилетин
Нефазодон
Оланзапин
пароксетин
Прасугрель
Хинупристин
Рисперидон
Тенофовира дизопроксила
фумарат
Теофиллин
Вальпроевая кислота
Варфарин
|
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.