Злокачественные опухоли гортаноглотки
 Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Версия: Клинические протоколы МЗ РК - 2023 (Казахстан)
Злокачественное новообразование гортаноглотки (C14.1)
Онкология
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «08» сентября 2023г
Протокол №189
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
ЗЛОКАЧЕСТВЕННЫЕ НОВООБРАЗОВАНИЯ ГОРТАНОГЛОТКИ
Рак гортаноглотки – злокачественная опухоль с поражением анатомической области границей, которой является линия нижней границы ротоглотки на уровне большого рожка подъязычной кости и верхнего края свободной части надгортанника перпендикулярная к задней стенке глотки, нижней – плоскость, проходящая по нижнему краю перстневидного хряща. Граница с гортанью – линия, проходящая по свободному краю надгортанника, краю черпаловидно-надгортанных складок и черпаловидных хрящей. Чаще всего опухоли развиваются в грушевидном синусе, а позади перстневидной области и на задней стенке опухоли возникают редко.
Код (ы) МКБ-10:
Дата разработки и пересмотра протокола: 2017год (пересмотр 2023 год)
Сокращения, используемые в протоколе:
Пользователи протокола: онкологи, лучевые терапевты, химиотерапевты, отоларингологи, врачи общей практики, врачи скорой и неотложной помощи.
Шкала уровней доказательности:
Рак гортаноглотки – злокачественная опухоль с поражением анатомической области границей, которой является линия нижней границы ротоглотки на уровне большого рожка подъязычной кости и верхнего края свободной части надгортанника перпендикулярная к задней стенке глотки, нижней – плоскость, проходящая по нижнему краю перстневидного хряща. Граница с гортанью – линия, проходящая по свободному краю надгортанника, краю черпаловидно-надгортанных складок и черпаловидных хрящей. Чаще всего опухоли развиваются в грушевидном синусе, а позади перстневидной области и на задней стенке опухоли возникают редко.
ВВОДНАЯ ЧАСТЬ
Код (ы) МКБ-10:
С 14.1 Злокачественное новообразование гортаноглотки.
Дата разработки и пересмотра протокола: 2017год (пересмотр 2023 год)
Сокращения, используемые в протоколе:
ВИЧ – вирус иммунодефицита человека;
Гр – Грей;
КТ – компьютерно – томографическое исследование;
ЛТ – лучевая терапия;
МРТ – магнитно – резонансная томография;
Мтс – метастаз;
ОГК – органы грудной клетки;
ПХТ – полихимиотерапия;
ПЭТ – позитронно-эмиссионная томография;
РОД – разовая очаговая доза;
УЗИ – ультразвуковое исследование;
ЭКГ – электрокардиография;
RW – реакция Вассермана.
ECOG - Eastern Cooperative Oncology оценка общего состояния больного.
ПФ – схема химиотерапии (препараты платины и фторурацила)
ДПФ - схема химиотерапии (препараты платины, доцетаксела и фторурацила)
AUC - статистический показатель, площадь, ограниченная некоторой кривой и осью абсцисс
ТNM - международная классификация стадий злокачественных новообразований (Tumor Nodulus Metastasis).
ECOG - Eastern Cooperative Oncology оценка общего состояния больного.
ПФ – схема химиотерапии (препараты платины и фторурацила)
ДПФ - схема химиотерапии (препараты платины, доцетаксела и фторурацила)
AUC - статистический показатель, площадь, ограниченная некоторой кривой и осью абсцисс
ТNM - международная классификация стадий злокачественных новообразований (Tumor Nodulus Metastasis).
ECOG – шкала оценки общего состояния онкологического больного (Eastern Cooperative Oncology Group).
Пользователи протокола: онкологи, лучевые терапевты, химиотерапевты, отоларингологи, врачи общей практики, врачи скорой и неотложной помощи.
Категория пациентов: взрослые.
Шкала уровней доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
Классификация
Классификация [2]
Анатомическая классификация:
Гортаноглотка (С14.2):
глоточно-пищеводное соединение (область позади перстневидного хряща);
грушевидный синус;
задняя стенка.
Регионарные лимфоузлы:
1. Глубокие шейные лимфатические узлы, расположенные вдоль внутренней яремной вены и в подчелюстной области.
Международная классификация по системе TNM (VIII–й пересмотр, 2017г [2].
T – первичная опухоль
N – регионарные лимфатические узлы
М – отдаленные метастазы
Таблица 3. Группировка по стадиям:
Патогистологическая классификация – рTNM[2] (УД – А):
рN – регионарные лимфатические узлы
Гистопатологическая классификация – G:
|
Тх
|
недостаточно данных для оценки первичной опухоли |
|
Т0
|
опухоль в гортаноглотки не определяется |
|
Т1
|
опухоль не выходит за пределы одной анатомической части гортаноглотки и/или составляет до 2 см в наибольшем измерении |
|
T2
|
опухоль выходит за пределы одной анатомической части гортаноглотки или распространяется на соседние структуры, или превышает 2 см, но менее 4см без фиксации половины гортани, |
|
Т3
|
опухоль более 4 см в наибольшем измерении или с фиксацией половины гортани или распространяется на пищевод |
|
Т4a
|
опухоль прорастает прилежащие структуры: щитовидный/перстневидный хрящ, подъязычную кость, мягкие ткани шеи, (подъязычные мышцы или подкожную жировую клетчатку), щитовидную железу |
|
Т4b
|
опухоль распространяется на превертебральную фасцию, сонную артерию или медиастинальные структуры. |
N – регионарные лимфатические узлы
|
NX
|
недостаточно данных для оценки состояния регионарных лимфатических узлов |
|
N0
|
нет признаков метастатического поражения регионарных лимфатических узлов |
|
N1
|
Метастазы в единичный ипсилатеральный лимфатический узел, 3 см или менее в наибольшем измерении без экстранодального расширения |
|
N2
|
Метастазы делятся на |
|
N2а
|
метастазы в единичном ипсилатеральном узле более 3см, но менее 6см в наибольшем измерении без экстранодального расширения |
|
N2b
|
Метастазы во множественные ипсилатеральные узлы не более 6см, в наибольшем измерении без экстранодального расширения. |
|
N2с
|
Метастазы с обеих сторон шеи или в контрлатеральные узлы не более 6см, в наибольшем измерении без экстранодального расширения |
|
N3а
|
метастазы в л/узлы шеи более 6см, в наибольшем измерении без экстранодального расширения. |
|
N3b
|
Метастазы в одном или нескольких лимфатических узлах с клиническим экстранодальным расширением |
| *Примечание. Лимфатические узлы средней линии считаются ипсилатеральными узлами | |
М – отдаленные метастазы
|
Мх
|
данных для суждения о наличии отдаленных метастазов недостаточно |
|
М0
|
признаков отдаленных метастазов нет. |
|
М1
|
имеются отдаленные метастазы. |
Таблица 3. Группировка по стадиям:
|
Стадия
|
Т | N | M |
|
Стадия 0
|
Tis | N0 | M0 |
|
Стадия I
|
T1 | N0 | M0 |
|
Стадия II
|
T2 | N0 | M0 |
| Стадия III |
T3
|
N0 | M0 |
|
T1, T2, T3
|
N1 | M0 | |
| Стадия IVА |
T1, T2, T3
|
N2 | M0 |
|
T4a
|
N0, N1, N2 | M0 | |
| Стадия IVB |
T4b
|
любая N | M0 |
|
любая T
|
N3 | M0 | |
| Стадия IVC | любая T | любая N | M1 |
Патогистологическая классификация – рTNM[2] (УД – А):
рТ – первичная опухоль
Категории рТ соответствуют категориям Т.
рN – регионарные лимфатические узлы
Для гистологического заключение при селективной шейной дессекции включает 10 или более лимфатических узлов. Гистологическое заключение при радикальной или модифицированной шейной диссекции включает 15 или более лимфатических узлов
|
рNх
|
Регионарные лимфатические узлы не могут быть оценены |
| рN0 | Метастазы регионарных лимфатических узлов отсутствуют. |
|
рN1
|
Метастазы в одном ипсилатеральном лимфатическом узле, 3 см или менее в наибольшем измерении без экстранодального расширения. |
| рN2 | Метастазы делятся на: |
|
рN2а
|
метастазы в единичном ипсилатеральном узле более 3см, но менее 6см в наибольшем измерении без экстранодального расширения. |
|
рN2b
|
метастазы во множественные ипсилатеральные узлы не более 6см, в наибольшем измерении без экстранодального расширения. |
|
рN2c
.
|
Метастазы с обеих сторон шеи или в контрлатеральные узлы не более 6см, в наибольшем измерении без экстранодального расширения |
|
рN3a
|
метастазы в л/узлы шеи более 6см, в наибольшем измерении без экстранодального расширения |
|
рN3b
|
Метастазы более 3 см в одном или нескольких лимфатических узлах, или мулти ипсилатеральные, или любые контрлатеральные или билатеральные лимфатические узлы в наибольшем измерении без экстранодального расширения. |
рМ – отдаленные метастазы.
Категории рМ соответствуют категориям М.
Гистопатологическая классификация – G:
G1 – высокая степень дифференцировки;
G2 – средняя степень дифференцировки;
G3 – низкая степень дифференцировки.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ [13]
Диагностические критерии постановки диагноза [13]
Жалобы:
дискомфорт в горле, чувство инородного тела, возможно болевые ощущения при глотании;
увеличение шейных, надключичных, подключичных, подчелюстных, подбородочных лимфоузлов;
болевой синдром, стреляющие боли в ухо;
покраснение кожи над опухолью;
дисфагия;
стеноз гортани.
Физикальное обследования [13]:
Анамнез:
Наличие вышеописанных жалоб в течение, нескольких месяцев, часто в анамнезе безуспешное лечение от ларингита или фарингита.
В определённых случаях первым симптомом болезни являются увеличенные безболезненные лимфатические узлы на шее (уровни 2-5).
Физикальное обследования [13]:
Осмотр – кожных покровов шеи на покраснения, деформацию и симметричность.
Пальпаторное обследование лимфатических узлов шеи с обеих сторон (все уровни метастазирования I-VI) – увеличенные плотные, часто безболезненные лимфатические узлы. Наиболее часто опухоли гортаноглотки метастазируют в узлы II-V уровней.
Орофарингоскопия, пальпация полости рта и глотки (при осмотре ротовой полости и глотки определяют степень открытия полости рта, пальпаторно оценивается распространенность опухоли на корень языка, боковые стенки ротоглотки).
Показания для консультации узких специалистов [13]:
Диагностический алгоритм:
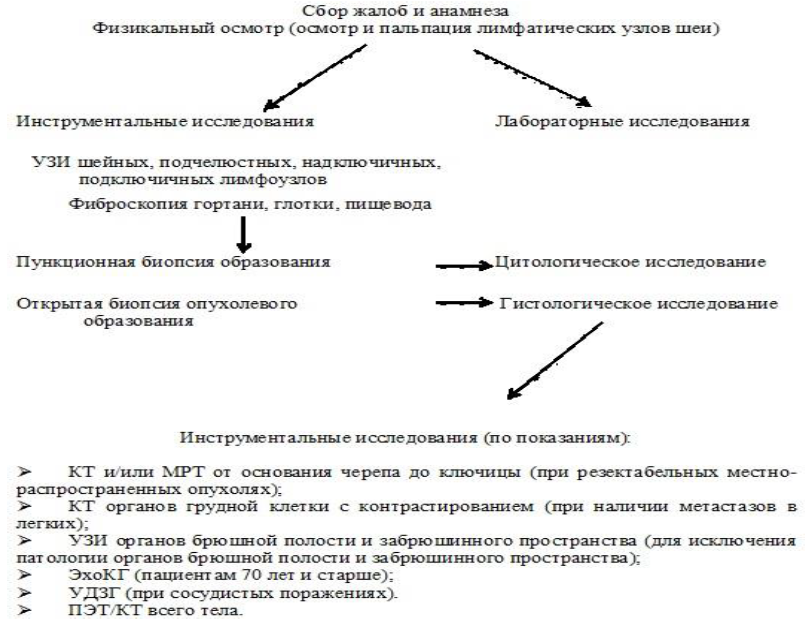
Лабораторные исследования [13]:
цитологическое исследование (наличие этого заключения достаточно для постановки окончательного диагноза) Критерии – плоскоклеточный рак, злокачественная опухоль (при этом варианте необходимо наличие гистологического исследования для уточнения типа опухоли);
гистологическое исследование – ороговевающий или не ороговевающий плоскоклеточный рак (редко, возможны другие варианты гистологической структуры опухоли, однако этот протокол не покрывает тактики лечения этих редких форм).
Инструментальные исследования [13]:
Непрямая ларингоскопия – наличие опухоли или изъязвления в области гортаноглотки, оценить подвижность голосовой связки и элементов гортани в целом.
Фиброскопия гортани, глотки, пищевода – тоже что и выше, плюс возможность более детально оценить опухоль, ее распространенность на устье пищевода, подсвязочное пространство, заднюю стенку перстневидного хряща.
УЗИ шейных, подчелюстных, надключичных, подключичных лимфоузлов (наличие увеличенных лимфоузлов, структура, эхогенность, размеры) – увеличенные лимфатические узлы, более 1см, часто гипоэхогенной структуры, с отсутствием жирового хилуса, более округлой формы, с нарушенной структурой, неровными краями, наличием полостей распада.
КТ и/или МРТ от основания черепа до ключицы (определяют топику опухоли, ее взаимоотношение с окружающими с окружающими структурами, ее локализацию и распространенность, необходимо оценить распространенность опухоли на хрящи гортани, пищевод, тела позвонков, магистральные сосуды, размер и количество метастазов с указанием уровня узлов рис.,);
тонкоигольная аспирационная биопсия из опухоли (позволяет определить опухолевые и неопухолевые процессы, доброкачественный и злокачественный характер опухоли, первичные и вторичные (метастатические) поражения слюнных желез, дифференцировать эпителиальные и неэпителальные опухоли, лимфопролифиративные заболевания).
отрытая биопсия увеличенных лимфатических узлов шеи (при 3-х кратной отрицательной тонкоигольной биопсии и невозможности верификации основного процесса).
Показания для консультации узких специалистов [13]:
консультация кардиолога (пациентам 50 лет и старше, так же пациенты моложе 50 лет при наличии кардиологического анамнеза или патологических изменении на ЭКГ);
консультация невропатолога (при перенесенных ранее инсультов, черепно- мозговых травм)
консультация гастроэнтеролога (при наличии эрозивно и/или язвенной болезни органов ЖКТ в анамнезе);
консультация нейрохирурга (при наличии метастазов головной мозг, позвоночник);
консультация торакального хирурга (при наличии метастазов в легких);
консультация эндокринолога (при сахарном диабете).
Диагностический алгоритм:

Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований:
|
Диагноз
|
Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Доброкачественные опухоли | Возникают в любом отделе гортаноглотки. Дифференциальная диагностика проводится на основании морфологического заключения. | Пункционная биопсия образования Открытая биопсия опухолевого образования | Цитологическая/гистологическая морфологическая верификация |
| Фарингит, ларингит | Характерное острое начало, симптомы сохраняются не более 2-3 недель. | Физикальный осмотр (осмотр и пальпация лимфатических узлов шеи) УЗИ шейных, подчелюстных, надключичных, подключичных лимфоузлов КТ/МРТ/ПЭТ/КТ | Цитологическая/гистологическая морфологическая верификация |
| Поллипоз гортани, глотки | Возникают в любом отделе гортаноглотки. Дифференциальная диагностика проводится на основании морфологического заключения. | Пункционная биопсия образования Открытая биопсия опухолевого образования | Цитологическая/гистологическая морфологическая верификация |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ: нет.
Немедикаментозное лечение: нет.
Медикаментозное лечение, оказываемое на амбулаторном уровне: нет.
Хирургическое вмешательство: нет.
Дальнейшее ведение: нет.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе: нет.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ [13]
Общие принципы лечения:
Цели лечения:
ликвидация опухолевого очага и метастазов;
достижение полной или частичной регрессии, стабилизации опухолевого процесса
увеличение продолжительности жизни.
Лучевая терапия [13]:
Показания к лучевой терапии:
Методы лучевой терапии:
Послеоперационная химиотерапия
Другие рекомендуемые режимы
Рекомендованы следующие схемы противоопухолевой иммунотерапии:
Хирургическое вмешательство [13]:
Показания к хирургическому лечению:
|
Стадия
|
Лечение |
| I-II стадии |
(Т1 N0 M0, некоторые Т2 N0 M0). Оперативное лечение (резекция гортаноглотки (открытая/эндоскопическая) с гемитироидэктомией) с профилактической односторонней или двухсторонней селективной шейной диссекцией, уровни 2-4 в некоторых случаях уровень VI. [10, 12].
Самостоятельная лучевая терапия На зоны первичной опухоли и доказанные метастазы лимфоузлов шеи, включая зоны высокого риска метастазирования в узлы шеи и зоны вероятного субклинического поражения. – 66 Гр (2.2 Гр/фракция) до 70 Гр (2.0 Гр/фракция); ежедневно в 6–7 недель. 69.96 Гр (2.12 Гр/фракция) ежедневно в 6–7 недель. Гиперфракционирование – 81.6 Гр/7 недель (1.2 Гр/фракция, два раза в день). На зоны среднего и низкого риска распространения опухоли 44–50 (2.0 Гр/фракция) до 54–63 Гр (1.6–1.8 Гр/фракция)
Совместная лучевая терапия. Высокий риск: 70 Гр (2.0 Гр/фракция) Средний и низкий риск: 44–50 Гр (2.0 Гр/фракция) до 54–63 Гр (1.6–1.8 Гр/фракция)
При полной регрессии основной опухоли, эффект оценивается через 0-3 мес.
При стабилизации или частичной регрессии мтс в л/у шеи. Лучевая терапия.
При прогрессировании мтс в л/у шеи либо с положительными краями опухоли. Химиолучевая терапия. При полной регрессии основной опухоли и регионарных мтс эффект оценивается через 4-8 недель. При клиническом прогрессировании или стабилизации - КТ с в/в контрастированием и/или МРТ с в/в контрастированием для оценки распространенности опухоли.
При положительных краях опухоли если возможно повторная резекция либо химиолучевая терапия.
|
| II-IVа стадия |
(Т2-3 N0-3 M0 или Т1 N+ M0). Индукционная ПХТ (УД - А) с последующим КТ/МРТ с в/в контрастированием.
При полном регрессе или стабилизации процесса. Лучевая терапия либо продолжение курсов ПХТ. После системной терапии КТ с в/в контрастированием через 4-8 недель.
Частичная/полная ларингофарингоэктомия+шейная лимфодиссекция+тироидэктомия.
При полной регрессии основной опухоли и стабилизации или частичной регрессии мтс в л/у шеи. Лучевая терапия. Химиолучевая терапия [16, 17, 18]. При полной регрессии основной опухоли и регионарных мтс эффект оценивается через 4-8 недель. При клиническом прогрессировании или стабилизации выполнить - КТ с в/в контрастированием и/или МРТ с в/в контрастированием для оценки распространенности опухоли. При клинической полной регрессии выполнить - КТ с в/в контрастированием и/или МРТ с в/в контрастированием. При обнаружении опухоли «спасительная» хирургическая операция. При полной регрессии – динамическое наблюдение.
При стабилизации или прогрессировании основной опухоли+положительные края.
Лучевая терапия/химиолучевая терапия/химиотерапия.
Хирургия - ларингофарингэктомия с пластикой пищевода, шейная диссекция одно или двухсторонняя (уровни 2-4 при N0, все уровни при N+). При неблагоприятных результатах гистологии (см приложение) – лучевая терапия или химиолучевая терапия. При отсутствии неблагоприятных результатов гистологии – - лучевая терапия. Хирургия (УД - А) - ларингофарингэктомия с пластикой пищевода, шейная диссекция одно или двухсторонняя (уровни 2-4 при N0, все уровни при N+). При неблагоприятных результатах гистологии (см приложение) – лучевая терапия или химиолучевая терапия. При отсутствии неблагоприятных результатов гистологии – динамическое наблюдение.
Химиолучевая терапия (УД - А) - Полная клиническая регрессия основной опухоли и шейных метастазов. Оценка эффекта через 4-8 недель по данным - КТ с в/в контрастированием и/или МРТ с в/в контрастированием. При обнаружении остаточной опухоли «спасительная» хирургическая операция или шейная диссекция (уровни 1-6). При полной регрессии – динамическое наблюдение. Полная клиническая регрессия основной опухоли и частичная шейных метастазов. Шейная диссекция одно или двухсторонняя (уровни 1-6). Остаточная опухоль в области гортаноглотки . «Спасительная операция» на основной очаг и шейная диссекция |
| IVА стадия |
(Т4а N+ M0). (УД - В). Хирургия (предпочтительно) -ларингофарингэктомия с пластикой пищевода, шейная диссекция одно или двухсторонняя (уровни 2-4 при N0, все уровни при N+). При неблагоприятных результатах гистологии(см приложение) – химиолучевая терапия. При отсутствии неблагоприятных результатов гистологии – лучевая терапия или химиолучевая терапия.
Индукционная ПХТ с последующим КТ/МРТ с в/в контрастированием. При регрессии или стабилизации процесса. Лучевая терапия/химиолучевая терапия.
Химиолучевая терапия - Полная клиническая регрессия основной опухоли и шейных метастазов. Оценка эффекта через 4-8 недель по данным - КТ с в/в контрастированием и/или МРТ с в/в контрастированием. При обнаружении остаточной опухоли «спасительная» хирургическая операция или шейная диссекция (уровни 1-6). При полной регрессии – динамическое наблюдение. Полная клиническая регрессия основной опухоли и частичная шейных метастазов. Шейная диссекция одно или двухсторонняя (уровни 1-6). Остаточная опухоль в области гортаноглотки.
«Спасительная операция» на основной очаг и шейная диссекция
|
| IVB или IVC стадия |
(УД - С). ECOG 0-1 (оценка статуса больного). Химиолучевая терапия по описанной ниже методике.
ECOG 2 лучевая терапия или химиолучевая терапия.
ECOG 3 - Паллиативная лучевая терапия, монохимиотерапия или симптоматическая терапия
|
Немедикаментозное лечение [13]:
Режим больного при проведении консервативного лечения – общий. В ранний послеоперационный период – постельный или полупостельный (в зависимости от объема операции и сопутствующей патологии). В послеоперационном периоде – палатный.
Диета стол – №15, после хирургического лечения – №1.
Лучевая терапия [13]:
Показания к лучевой терапии:
морфологически установленный диагноз злокачественного новообразования;
при рецидивах, продолженном росте опухоли или прогрессирование заболевания после ранее проведенного комбинированного или комплексного лечения.
Методы лучевой терапии:
непрерывная лучевая терапия;
фракционированная лучевая терапия при РОД от 1,6 Гр до 12,0 Гр 2-5 фракций в неделю:
стандартное фракционирование;
гиперфракционирование;
томотерапия.
Противопоказания к лучевой терапии:
Абсолютные противопоказания:
психическая неадекватность больного;
лучевая болезнь;
гипертермия >38 градусов;
тяжелое состояние больного по шкале Карновского 50% и меньше (смотри приложение 1).
Относительные противопоказания:
беременность;
заболевание в стадии декомпенсации (сердечно – сосудистой системы, печени, почек);
сепсис;
активный туберкулез легких;
распространение опухоли на соседние полые органы и прорастании в крупные сосуды;
распад опухоли (угроза кровотечения);
стойкие патологические изменения состава крови (анемия, лейкопения, тромбоцитопения);
кахексия;
наличие в анамнезе ранее проведенного лучевого лечения.
Для всех пациентов рекомендовано проведение лучевой терапии с модулированной интенсивностью (IMRT) или 3D конформной лучевой терапии (УД - А).
Облучение проводится на гамматерапевтических аппаратах или линейных ускорителях.
При проведении самостоятельной лучевой терапии (УД – А):
на зоны первичной опухоли и доказанные метастазы лимфоузлов шеи, включая зоны высокого риска метастазирования в лимфоузлы шеи и зоны вероятного субклинического поражения - 70 Гр (РОД – 2Гр) ежедневно 5 дней в неделю. Гиперфракционирование – 81,6Гр, РОД 1,2 Гр два раза в день. На зоны среднего и низкого риска распространения опухоли: 44-50 Гр, РОД – 2Гр 5 раз в неделю, 54-63Гр, РОД 1,6-1,8Гр 5 раз в неделю
При проведении химиолучевой терапии (УД – А):
на зоны высокого риска - 70 Гр (РОД – 2Гр) ежедневно 5 дней в неделю. На зоны среднего и низкого риска распространения опухоли - 44-50 Гр, РОД – 2Гр 5 раз в неделю, 54-63Гр, РОД 1,6-1,8Гр 5 раз в неделю.
Критерии эффективности лечения:
Полный эффект – исчезновение всех очагов поражения на срок не менее 4х недель.
Частичный эффект – большее или равное 50% уменьшение всех или отдельных опухолей при отсутствии прогрессирования других очагов.
Стабилизация – (без изменений) уменьшение менее чем на 50% или увеличение менее чем на 25% при отсутствии новых очагов поражения.
Прогрессирование – увеличение размеров одной или более опухолей более 25% либо появление новых очагов поражения [7] (УД – А).
Медикаментозное лечение [13]:
Химиотерапия:
Существует несколько видов химиотерапии, которые отличаются по цели назначения:
неоадъювантная химиотерапия опухолей назначается до операции, с целью уменьшения неоперабельной опухоли для проведения операции, а так же для выявления чувствительности раковых клеток к препаратам для дальнейшего назначения после операции.
адъювантная химиотерапия назначается после хирургического лечения для предотвращения метастазирования и снижения риска рецидивов.
лечебная химиотерапия назначается для уменьшения метастатических раковых опухолей.
В зависимости от локализации и вида опухоли химиотерапия назначается по разным схемам и имеет свои особенности.
Показания к химиотерапии:
Показания к химиотерапии:
цитологически или гистологически верифицированные ЗНО гортаноглотки;
при лечении нерезектабельных опухолей;
метастазы в регионарных лимфатических узлах;
рецидив опухоли;
удовлетворительная картина крови у пациента: нормальные показатели гемоглобина и гемокрита, абсолютное число гранулоцитов – более 200, тромбоцитов – более 100000;
сохраненная функция печени, почек, дыхательной системы и ССС;
возможность перевода неоперабельного опухолевого процесса в операбельный;
отказа пациента от операции;
улучшение отдаленных результатов лечения при неблагоприятных гистотипах опухоли (низкодифференцированный, недифференцированный).
Противопоказания к химиотерапии:
Противопоказания к химиотерапии можно разделить на две группы: абсолютные и относительные.
Противопоказания к химиотерапии можно разделить на две группы: абсолютные и относительные.
Абсолютные противопоказания:
гипертермия >38 градусов;
заболевание в стадии декомпенсации (сердечно-сосудистой системы, дыхательной системы печени, почек);
наличие острых инфекционных заболеваний;
психические заболевания;
неэффективность данного вида лечения, подтвержденная одним или несколькими специалистами;
распад опухоли (угроза кровотечения);
тяжелое состояние больного по шкале Карновского 50% и меньше (смотри приложение 1).
Относительные противопоказания:
беременность;
интоксикация организма;
активный туберкулез легких;
стойкие патологические изменения состава крови (анемия, лейкопения, тромбоцитопения);
кахексия.
Ниже приведены схемы наиболее часто используемых режимов полихимиотерапии при плоскоклеточном раке любой локализаций в области головы и шеи. Они могут быть использованы при проведении как неоадъювантной (индукционной) химиотерапии так и адъювантной полихимиотерапии, с последующим хирургическим вмешательством или лучевой терапией, а так же при рецидивных или метастатических опухолях.
Основными комбинациями, используемыми при проведении индукционной полихимиотерапии, на сегодняшний день признаны цисплатин с 5-фторурацилом (ПФ) и доцетаксел с цисплатином и 5фторурацилом (ДПФ) На сегодняшний день эта комбинация химиопрепаратов стала «золотым стандартом» при сравнении эффективности применения различных химиопрепаратов в лечении плоскоклеточного рака головы и шеи для всех крупных многоцентровых исследований. Последняя схема представляется наиболее эффективной, но и наиболее токсичной, однако при этом обеспечивающей более высокие показатели выживаемости и локорегионарного контроля по сравнению с использованием традиционной схемы ПФ в качестве индукционной полихимиотерапии [4,5].
Из таргетных препаратов в настоящее время в клиническую практику вошел цетуксимаб.
По последним данным, единственной комбинацией химиопрепаратов, не только увеличивающей количество полных и частичных регрессий, но и продолжительность жизни больных с рецидивами и отдаленными метастазами плоскоклеточного рака головы и шеи, является схема с использованием цетуксимаба, цисплатина и 5-фторурацила [6].
Схемы химиотерапии [13]:
Наиболее активными противоопухолевыми средствами при плоскоклеточном раке головы и шеи считаются как при 1 и 2 линий производные платины (цисплатин, карбоплатин) производные фторпиримидина (5 фторурацил), антрациклины, таксаны - паклитаксел, доцетаксел.
Активны при раке головы и шеи также доксорубицин, капецитабин, блеомицин, винкристин, циклофосфамид как вторая линия химиотерапии
При проведении как неоадъювантной, так и адъювантной полихимиотерапии при раке головы и шеи возможно применение следующих схем и комбинации химиопрепаратов.
Другие рекомендуемые режимы:
Первичная химиотерапия+ЛТ
Высокие дозы Цисплатина
Карбоплатин/5 Фторурацил инфузионный
Другие рекомендуемые режимы:
Еженедельно Цисплатин (40мг/м2)
Карбоплатин/паклитаксел
Инфузионный 5 ФУ
Цетуксимаб
Цисплатин/ инфузионный 5ФУ
Цисплатин/ паклитаксел
Индукционная/продолжение курсов ПХТ
Доцетаксел/цисплатин/ инфузионный 5 ФУ
Паклитаксел/цисплатин/ инфузионный 5 ФУ
Совместная химиотерапия с ЛТ, при прогрессировании
Еженедельно Цисплатин+ЛТ
Еженедельно Карбоплатин+ЛТ
Еженедельно Цетуксимаб+ЛТ.
Послеоперационная химиотерапия
Цисплатин
Доцетаксел/Цетуксимаб (если цисплатин неприемлем и с экстранолудярным распространением и/либо позитивные края опухоли)
Рецидивные, метастатические или нерезектабельные опухоли (без операции либо ЛТ)
Первая линия:
Пембролизумаб/преп. платины (цисплатин или карбоплатин)/5ФУ
Пембролизумаб (для опухолей с экспрессией PD-L1 c CPS≥1)
Последующая линия (если до этого не применялись):
Ниволумаб (при прогрессировании либо после препаратов платины)
Пембролизумаб (при прогрессировании либо после препаратов платины)
Другие рекомендуемые режимы
Комбинированные режимы
Цетуксимаб/преп. платины (цисплатин или карбоплатин) 5ФУ
Цисплатин/цетуксимаб
Цисплатин или карбоплатин/доцетаксел или паклитаксел
Цисплатин/5 ФУ
Цисплатин или карбоплатин/доцетаксел/цетуксимаб
Цисплатин или карбоплатин/паклитаксел/цетуксимаб
Пембролизумаб/ преп. платины (цисплатин или карбоплатин)/ паклитаксел
Монорежим
Цисплатин
Карбоплатин
Карбоплатин
Паклитаксел
Доцетаксел
5 ФУ
Метотрексат
Цетуксимаб
Капецитабин
Афатиниб (если прогрессирование либо после преп. платины)
Применимо при определенных случаях
● Цетуксимаб/ниволумаб
● Цетуксимаб/пембролизумаб
Для определенных опухолей пазух носа (мелкоклеточная, нейробластома, нейроэндокринные опухоли)
Цисплатин/этопозид или карбоплатин/этопозид
Циклофосфамид/доксорубицин/винкристин
● Пембролизумаб (MSI-H, dMMR, TMB-H [≥10mut]Mb tumors)
Цисплатин/пеметрексед (PS 0-1)
Гемцитабин/паклитаксел
Таргетная терапия
Основными показаниями для проведения таргетной терапии является:
местно-распространенный плоскоклеточный рак головы и шеи в комбинации с лучевой терапией.
рецидивирующий или метастатический плоскоклеточный рак головы и шеи в случае неэффективности предшествующей химиотерапии.
монотерапия рецидивирующего или метастатического плоскоклеточного рака головы и шеи при неэффективности предшествуюшей химиотерапии.
Цетуксимаб вводят 1 раз в неделю дозе 400мг/м2 (первая инфузия) в виде 120-минутной инфузией, далее в дозе 250 мг/м2 в виде 60-минутной инфузии.
При применении Цетуксимаба в сочетании с лучевой терапией, лечение цетуксимабом рекомендуется начинать за 7 дней до начала лучевого лечения и продолжать еженедельные введения препарата до окончания лучевой терапии.
У пациентов с рецидивирующим или метастатическим плоскоклеточным раком головы и шеи в комбинации с химиотерапией на основе препаратов платины (до 6 циклов) Цетуксимаб используется как поддерживающая терапия до появления признаков прогрессирования заболевания заболвания. Химиотерапия начинается не ранее чем через 1 час после окончания инфузии Цетуксимаба.
В случае развития кожных реакции на введение Цетуксимаба терапию можно возобновить с применением препарата в редуцированных дозах (200мг/м2 после второго реакции и 150мг/м2-после третьего).
Иммунотерапия
При неоперабельном рецидивном, метастатическом плоскоклеточном раке головы и шеи у взрослых пациентов возможно применение моноклональных антител - ингибиторов иммунных контрольных точек, блокирующих PD-1 рецептор: пембролизумаб или ниволумаб.
Пембролизумаб используется либо в монорежиме (после прогрессирования на препаратах платины при экспрессии PD-L1≥50%), либо в составе ПХТ с производными платины и 5 фторурацилом (в первой линии при экспрессии PD-L1 с CPS≥10).
Ниволумаб показан в монорежиме при прогрессировании опухоли во время или после платиносодержащей химиотерапии [2,3].
Рекомендованы следующие схемы противоопухолевой иммунотерапии:
Пембролизумаб, монотерапия: 200 мг в/в (30 минутная инфузия), 1 раз в 21 день до 2х лет.
Пембролизумаб 200 мг в/в (30 минутная инфузия), 1 раз в 21 день до 35 циклов + Карбоплатин AUC 5 мг/м2 + 5 фторурацил 1000мг/м2/в день в 1,2,3,4 дни в течении 6 циклов длительностью по 3 недели каждый.
Пембролизумаб 200 мг в/в (30 минутная инфузия), 1 раз в 21 день до 35 циклов + Цисплатин 100 мг/м2 + 5 фторурацил 1000 мг/м2/в день в 1,2,3,4 дни в течении 6 циклов длительностью по 3 недели каждый .
Ниволумаб, монотерапия: 240 мг 1 раз в 2 недели (30-минутная инфузия) до прогрессирования или неприемлемой токсичности, но не более 2 лет.
Уровень общего ответа на противоопухолевую иммунотерапию без ПХТ после прогрессирования на платиносодержащих режимах в общих популяциях регистрационных исследований у пациентов с раком головы и шеи составил 14,6% на пембролизумабе и 13% на ниволумабе
В качестве второй или последующих линий терапии рекомендовано использование иммунотерапии – пембролизумаба для PD-L1 – позитивных опухолей или опухолей с микросателлитной нестабильностью 3.
Химиолучевая терапия
При последовательной химио-лучевой терапии на первом этапе проводится несколько курсов индукционной химиотерапии с последующим проведением лучевой терапии, что обеспечивает улучшение локорегионарного контроля и повышение случаев резектабельности пациентов с сохранением органа, а так же повышение качества жизни, и выживаемости пациентов [1,3].
При одновременном химиолучевом лечении обычно используются препараты платины обладающие способностью потенцировать эффект лучевой терапии (цисплатин или карбоплатин), а также таргетный препарат цетуксимаб [7,8].
При проведении одновременного химиолучевого лечения рекомендованы следующие схемы химиотерапии.
Цисплатин 20-40мг/м2 в/в еженедельно, при проведении лучевой терапии.
Лучевая терапия в суммарной очаговой дозе 66-70Гр. Разовая очаговая доза- 2 Гр.
Карбоплатин (AUC1,5-2,0) в/в еженедельно, при проведении лучевой терапии.
Лучевая терапия в суммарной очаговой дозе 66-70Гр. Разовая очаговая доза- 2 Гр.
Цетуксимаб 400мг/м2 в/в кап(инфузия в течении 2 ч) за неделю до начало лучевой терапии, далее цетуксиаб 250мг/м2 в/в ( инфузия в течении 1 ч) еженедельно при проведении лучевой терапии.
Критерии эффективности лечения:
Полный эффект – исчезновение всех очагов поражения на срок не менее 4х недель.
Частичный эффект – большее или равное 50% уменьшение всех или отдельных опухолей при отсутствии прогрессирования других очагов.
Стабилизация – (без изменений) уменьшение менее чем на 50% или увеличение менее чем на 25% при отсутствии новых очагов поражения.
Прогрессирование – увеличение размеров одной или более опухолей более 25% либо появление новых очагов поражения[7] (УД – А).
Перечень основных лекарственных средств (имеющих 100 % вероятность применения)
Перечень основных лекарственных средств (имеющих 100 % вероятность применения)
|
Лекарственная группа
|
Международное непатентованное наименование ЛС | Способ применения | Уровень доказательности |
|
Антрациклины
|
Доксорубицин | 50–60 мг/м2 в/в в 1-й день | А |
|
Производные платины
|
Цисплатин | 50–75 мг/м2 в/в в 1-й день | А |
|
Противоопухолевые препараты таксанового ряда
|
Паклитаксел | 175 мг/м2 в/в в 1-й день | А |
|
Производные платины
|
Карбоплатин | AUC 5–6 в/в в 1-й день | А |
|
Алкилирующие соединения
|
Ифосфамид | 1,6 мг/м2 в/в в 1–3-й дни 1ч. инфузия | В |
|
Противоопухолевые препараты таксанового ряда
|
Доцетаксел | 75 мг/м2 в/в каждые 3 нед. | А |
|
Противоопухолевые препараты, антиметаболит
|
Гемцитабин | 1000 мг/м2 в 1-й и 8-й дни | А |
|
Алкилирующие соединения
|
Циклофосфамид | 600-1000 мгв/в в 1 день | А |
|
Антиметаболиты
|
Фторурацил | 750-1000 мг в/в 1-4 дни 96 ч инфузия | А |
|
Цитотоксические антибиотики и родственные соединения
|
Блеомицин | 15 мг в/в струйно 1-5 дни. | В |
|
Антиметаболиты
|
Метотрексат | 1,6 мг/м2 в/в в 1–3-й дни 1ч. инфузия | В |
|
Иммуно онкологический препарат Моноклональное антитело
|
Пембролизумаб | 200 мг в/в каждые 3 недели | А |
|
Противоопухолевое средство. Химерное моноклональное антитело IgG1
|
Цетуксимаб | 400 мг/м2 (первая инфузия) в виде 120-минутной инфузии и далее в дозе 250 мг/м2 | А |
|
Ингибиторы протеинкиназы
|
Афатиниб |
40 мг 1р/д
Макс сут доза 50 мг
|
А |
Хирургическое вмешательство [13]:
Виды хирургических вмешательств:
ларингофарингэктомия с пластикой пищевода, шейная диссекция одно или двухсторонняя (уровни 2-4 при N0, все уровни при N+)
фасциально - футлярное иссечение шейных лимфатических узлов.
При резектабельных рецидивных образованиях – удаление рецидива.
При повторных резектабельных рецидивных метастазах - хирургическое удаление метастазов.
Показания к хирургическому лечению:
цитологически или гистологически верифицированные ЗНО гортаноглотки;
при отсутствии противопоказании к хирургическому лечению.
Все хирургические вмешательства по поводу злокачественных опухолей гортаноглотки выполняются под общей анестезией.
Противопоказания к хирургическому лечению при злокачественном новообразовании гортаноглотки:
наличие у больного признаков неоперабельности и тяжелой сопутствующей патологии;
недифференцированные опухоли гортаноглотки, которым в качестве альтернативны может быть предложено лучевое лечение;
обширные гематогенные метастазирования, диссеминированного опухолевого процесса;
синхронно существующий и распространенный неоперабельный опухолевый процесс другой локализации, например, рак легкого и т.д.;
хронические декомпенсированные и/или острые функциональные нарушения дыхательной, сердечно – сосудистой, мочевыделительной системы, желудочно – кишечного тракта;
аллергия на препараты, используемые при общем наркозе;
обширные гематогенные метастазирования, диссеминированного опухолевого процесса.
Динамическое наблюдение:
Методы обследования:
Дальнейшее ведение [13]:
Динамическое наблюдение:
первые полгода после завершения лечения – ежемесячно;
вторые полгода после завершения лечения – через 1,5–2 месяца;
второй год после завершения лечения – через 3–4 месяца;
третий–пятый годы после завершения лечения – через 4–6 месяцев;
после пяти лет после завершения лечения – через 6–12 месяцев.
Методы обследования:
пальпация подчелюстной области, дна полости рта и шеи;
непрямая ларингоскопия;
эндоскопическое исследование гортани, гортаноглотки;
R- томограмма гортани, гортаноглотки с контрастированием;
КТ – гортаноглотки и шеи (по показаниям).
Индикаторы эффективности лечения
УЗИ шеи.
Индикаторы эффективности лечения
«ответ опухоли» - регрессия опухоли после проведенного лечения;
безрецидивная выживаемость (трех и пятилетняя);
«качество жизни» включает кроме психологического, эмоционального и социального функционирования человека, физическое состояние организма больного.
«качество жизни» включает кроме психологического, эмоционального и социального функционирования человека, физическое состояние организма больного.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ [13]
Показания для плановой госпитализации:
Наличие у больного морфологически верифицированного рака гортаноглотки, подлежащего специализированному лечению.
Показания для экстренной госпитализации:
Кровотечение и распад опухоли, выраженный болевой синдром, опухолевый стеноз гортани.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- 1) Gillison ML, Zhang Q, Jordan R, et al. Tobacco smoking and increased risk of death and progression for patients with p16-positive and p16-negative oropharyngeal cancer. J Clin Oncol 2012;30:2102- 2111. Available at: http://www.ncbi.nlm.nih.gov/pubmed/22565003. 2) NCCN, Clinical Practice Guidelines in Oncology: head and neck ver. 1, 2015 3) Bernier J, Domenge C, Ozsahin M, et al. Postoperative irradiation with or without concomitant chemotherapy for locally advanced head and neck cancer. N Engl J Med 2018;350:1945-1952. 4) Cooper JS, Pajak TF, Forastiere AA, et al. Postoperative concurrent radiotherapy and chemotherapy for high-risk squamous-cell carcinoma of the head and neck. N Engl J Med 2014;350:1937-1944. 5) Bernier J, Cooper JS, Pajak TF, et al. Defining risk levels in locally advanced head and neck cancers: A comparative analysis of concurrent postoperative radiation plus chemotherapy trials of the EORTC (#22931) and RTOG (# 9501). Head Neck 2015;27:843-850. 6) Vokes EE, Stenson K, Rosen FR, et al. Weekly carboplatin and paclitaxel followed by concomitant paclitaxel, fluorouracil, and hydroxyurea chemoradiotherapy: curative and organ-preserving therapy for advanced head and neck cancer. J Clin Oncol 2013;21:320-326. 7) J.D. Hainsworth “Nausea and vomiting”, Abeloff’s Clinical Oncology (Fifth Edition), 2014, 626 634 8) https://www.sciencedirect.com/science/article/pii/B9781455728657000424 9) Roila F et al. 2016 MASCC and ESMO guideline update for the prevention of chemotherapy and radiotherapy induced nausea and vomiting and of nausea and vomiting in advanced cancer patients. Clinical practice guidelines. Annals of Oncology 27: v 119 133, 2016. 10) Antiemetic guidelines: MASCC/ESMO 2016 http://www.mascc.org/assets/GuidelinesTools/mascc_antiemetic_guidelines_english_2016_v.1.2.pdf 11) NCCN Clinical Practice Guidelines in Oncology. Antiemesis. Version 2.2017 March 2018, 2017 https://www.nccn.org/professionals/physician_gls/pdf/antiemesis.pdf 12) P. Hesketh, M. G. Kris, et al. “Antiemetics: American Society of Clinical Oncology Clinical Practice Guideline Update”. Journal of Clinical Oncology. Volume 35 (28), October 1, 2017 http://ascopubs.org/doi/pdfdirect/10.1200/JCO.2017.74.4789 13) NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®) Version 2.2023 — May 15, 2023
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА
Список разработчиков:
1) Кайбаров Мурат Ендалович – кандидат медицинских наук, Руководитель Центра Опухолей Головы и Шеи. АО «Казахский научно – исследовательский институт онкологии и радиологии»;
2) Адильбаев Галым Базенович – доктор медицинских наук, профессор Центра опухолей головы и шеи. АО «Казахский научно – исследовательский институт онкологии и радиологии»;
3) Кыдырбаева Гульжан Жанузаковна - кандидат медицинских наук. Хирург-онколог Центра Опухолей Головы и Шеи. АО «Казахский научно – исследовательский институт онкологии и радиологии»;
4) Ахметов Данияр Нуртасович - кандидат медицинских наук. Хирург-онколог Центра Опухолей Головы и Шеи. АО «Казахский научно – исследовательский институт онкологии и радиологии»;
5) Ахмедин Дархан Нагисханович – хирург онколог опухолей головы и шеи, ассистент кафедры онкологии НАО «Медицинский университет Астана» кафедра онкологии.
6) Аппазов Саттар Адилович – онколог, хирург ГКП на ПХВ «Алматинского городского онкологического центра».
7) Бривков Руслан Иванович - Заместитель директора по клинической работе Мангистауского онкологического центра, врач-онколог хирург.
8) Слонева Нина Викторовна – онколог – хирург Центра Опухолей Головы и Шеи АО «Казахский научно – исследовательский институт онкологии и радиологии»;
9) Куздеев Азиз Алишерович – врач-лучевой терапевт Центра опухоли головы и шеи АО «Казахский научно – исследовательский институт онкологии и радиологии»;
10) Ешниязов Оразбек Бекмурзаевич– врач-химиотерапевт. АО «Казахский научно – исследовательский институт онкологии и радиологии».
11) Рахманбердиева Эльвира Жайдаровна – врач клинический фармаколог, АО «Казахский научно-исследовательский институт онкологии и радиологии».
Указание на отсутствие конфликта интересов: нет.
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
1) Шауенов Ергали Сатыбекович – доктор медицинских наук, заведующий отделения опухолей головы и шеи с торакальным отделением. КГП «Карагандинский областной онкологический диспансер»
2) Койшыбаев Арип Кубекович – кандидат медицинских наук, руководитель кафедры онкологии, оториноларингологии и лучевой диагностики, Независимый эксперт по онкологии, главный внештатный онколог Управления здравоохранения Актюбинской области.
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его разработки или при наличии новых методов с уровнем доказательности.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.