Диагностика и лечение лекарственно-устойчивого туберкулеза
 Версия: Клинические протоколы КР 2023 (Кыргызстан)
Версия: Клинические протоколы КР 2023 (Кыргызстан)
Общая информация
Краткое описание
КЛИНИЧЕСКОЕ РУКОВОДСТВО ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ
Клиническая проблема:
Название документа:
Целевые группы:
Цель клинического руководства
Дата создания
Проведение следующего пересмотра планируется по мере появления новых ключевых доказательств или в 2025 году.
Классификация
КЛАССИФИКАЦИЯ СЛУЧАЕВ ЛУ-ТБ
Классификация случаев ЛУ-ТБ основана на истории предшествующего лечения и показана в таблице 1.
Таблица 1. Классификация случаев
| Случай | Определение | |
| Новый случай | Пациент никогда ранее не лечился от ТБ или принимал противотуберкулезные препараты в течение менее 1 месяца | |
| Рецидив | Пациент, который ранее получал лечение от ТБ и по завершении последнего курса терапии был признан излеченным или завершившим лечение, но в настоящее время у него диагностирован повторный эпизод ТБ | |
| Ранее леченные (исключая рецидивы) |
|
Пациент, который ранее лечился от туберкулеза и был оценен как «потерян для дальнейшего врачебного наблюдения» в конце последнего курса лечения |
|
Пациент, получивший курс повторного лечения и результат оказался неэффективным | |
|
Пациент, лечившийся от ТБ ранее, но результат лечения по окончании последнего курса терапии неизвестен или не подтвержден документально | |
| История предыдущего лечения неизвестна | Пациент не подпадает ни под одну из вышеперечисленных категорий | |
Локализация туберкулезного процесса
По локализации процесса туберкулез подразделяется на легочный и внелегочный.
Легочный ТБ: в патологический процесс вовлечена паренхима легких и туберкулезное поражение внутригрудных лимфатических узлов (средостения или корня легкого).
Внелегочный ТБ: ТБ любого органа, кроме легких, например: ТБ плевры, лимфатических узлов (кроме ТБВГЛУ) брюшины, мочеполовых органов, кожи, костей и суставов, мозговых оболочек. Диагноз ВЛ-ТБ должен быть основан хотя бы на одном положительном результате посева на M.tuberculosis и/или при наличии у больного явных клинико-рентгенологических проявлений, типичных для активного ВЛ-ТБ.
Сочетанная локализация легочного и внелегочного ТБ классифицируют как легочный ТБ.
Этиология и патогенез
ЭТИОЛОГИЯ, ПАТОГЕНЕЗ
Этиология
Эпидемиология
Диагностика
ДИАГНОСТИКА ТБ
СКРИНИНГ на симптомы ТБ:
A. Выясните, нет ли у пациента симптомов легочного ТБ, включая:
Общие симптомы:
Локальные симптомы зависят от того, какой орган поражен, например:
II. Если при скрининге на ТБ были обнаружены один или несколько симптомов ТБ, в таком случае данному пациенту с предполагаемым ТБ следует провести обследование на АКТИВНЫЙ ТБ:
1. Необходимо тщательно собрать жалобы и анамнез:
Риск развития лекарственной устойчивости наиболее высок, если в прошлом проводили неадекватное лечение или пациент не соблюдал рекомендованный режим лечения.
2. Провести физикальное исследование пациента.
3. Провести диагностический алгоритм.
АЛГОРИТМ ДИАГНОСТИКИ ТБ / ЛУ-ТБ
LF-LAM5 поможет по анализу собранного материала (мочи) диагностировать активный ТБ среди взрослых, подростков и детей, живущих с ВИЧ, которые имеют признаки туберкулеза (легочного, внелегочного или и того, и другого) и имеют количество клеток CD4 ≤100 клеток/мм или серьезно больны, независимо от количества клеток CD4.
В случае отрицательного результата исследования мокроты на Xpert, на уровне ЦСМ проводится посев мокроты на неспецифическую флору и ТЛЧ к АБП широкого спектра действия.
В случае подтверждения устойчивости к рифампицину (при наличии или отсутствии устойчивости к изониазиду) следует провести молекулярный тест (Хайн) к препаратам первого ряда GenoType MTBDRplus и к препаратам второго ряда GenoType MTBDRsl.
5 Lateral flow urine lipoarabinomannan assay (LF-LAM) for the diagnosis of active tuberculosis in people living with HIV, 2019
При получении результата устойчивости M. tuberculosis к рифампицину с использованием Xpert MTB/RIF или Xpert MTB/RIF Ultra и/или фТЛЧ - проводится (полногеномное) секвенирование штаммов выросшей культуры (при наличии ресурсов).
Рис 1. Диагностический алгоритм ведения лиц с предполагаемым ТБ
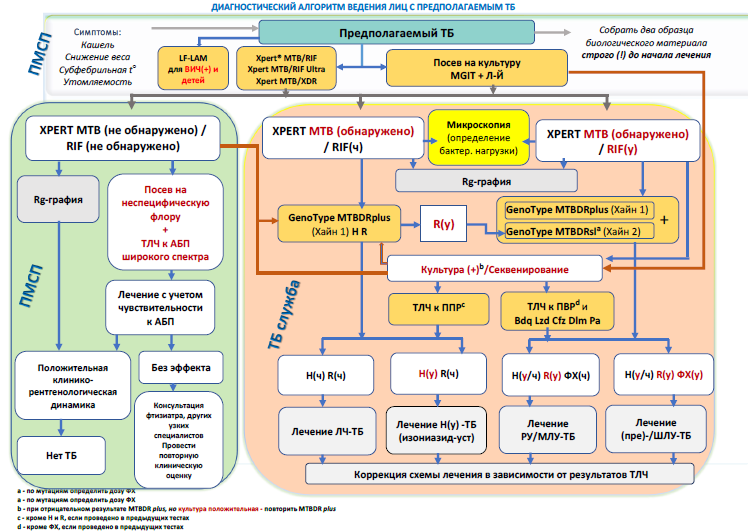
Алгоритм диагностики проводится перед началом повторного эпизода лечения, в случаях после потери пациента для врачебного наблюдения на 2 месяца и более, и после неэффективного лечения (Рис 2).
Проводится GenoType MTBDRplus (Хайн) к препаратам первого ряда, и GenoType MTBDRsl (Хайн) к препаратам второго ряда в случае, если результат предыдущего исследования не известен или чувствительность к ПТП была сохранена.
Вне зависимости от результатов GenoType MTBDRsl, при получении положительного результата культуры проводится фТЛЧ к ППР (кроме препаратов H и R, если результат уже имеется), и фТЛЧ к ПВР (кроме ФХ, если результат уже имеется) и фТЛЧ к бедаквилину, линезолиду, клофазимину, деламаниду и претоманиду.
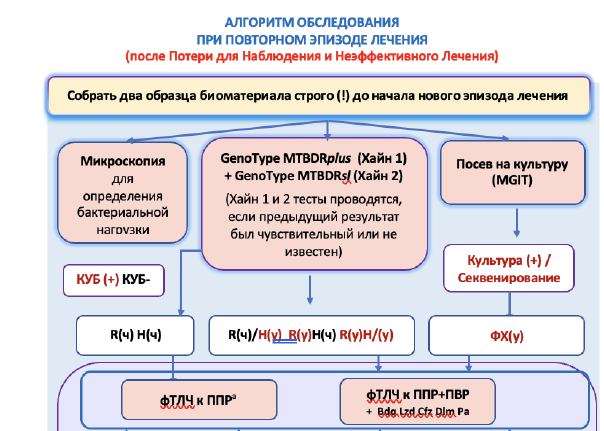
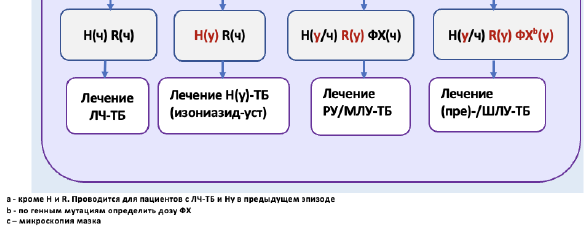
Лечение
ЛЕЧЕНИЕ
7 Frequently asked questions on the WHO treatment guidelines for isoniazid-resistant tuberculosis Version: 24 April 2018, р 6
При выявленной устойчивости к изониазиду следует начать лечение по схеме для пациентов с Ну-ТБ (Табл 2).
- если нельзя исключить устойчивость к рифампицину (т. е. неизвестная чувствительность к рифампицину; результат теста GeneXpert MTB/RIF не определен/ либо выдал ошибку «error»;
- известная или предполагаемая устойчивость к левофлоксацину;
- известная непереносимость фторхинолонов;
- известный или предполагаемый риск удлинения интервала QT;
При невозможности применения фторхинолонов, пациент получает лечение по схеме 6(Н)REZ.
При монорезистентности к Z, можно назначить лечение по режиму 6(9) HRE.
При монорезистентности к Е, можно назначить лечение по режиму 6(9) HRZ.
Дозы ПТП назначаются в соответствии с весовой категорией, и корректируются в случае прибавки веса в ходе лечения (Приложение C).
При положительном результате посева на культуру и микроскопии мокроты после 2 месяцев лечения необходимо провести Xpert MTB/RIF и исключить приобретение дополнительной устойчивости к рифампицину, а также ТЛЧ для исключения устойчивости к фторхинолонам и пиразинамиду.
Пациенты с распространенным поражением. Продления 6-месячного режима (H)REZ с левофлоксацином до 9 месяцев возможно на индивидуальной основе у пациентов с распространенным поражением, определяемым наличием полостей распада, а также стабильно положительным бактериологическим статусом мокроты по истечении 3 месяцев (путем посева культуры и микроскопии)9.
При большинстве форм полирезистентности, таких как H+E или H+Z, лечение можно продолжать с помощью 6(H)RZ-Lfx и 6(H)RЕ-Lfx (Таблица 2).
В случаях резистентности к H+Lfx назначается лечение 6(H)REZ.
Таблица 2. Схемы лечения для пациентов с Нy-ТБ и ПЛУ-ТБ10
| Устойчивость МБТ | Схема ПТП | |
| Ограниченный процесс | Распространенный процесс | |
|
Н
H+E
H+Z
|
6 (Н)REZ-Lfx
6 (Н)RZ-Lfx
6 (Н)RE-Lfx
|
|
| Z | 6 HRE | |
| Е | 6 HRZ | |
| H+Lfx | 6 (H)REZ | |
| H+Z+Lfx | Индивидуальный режим, включающий другие препараты на основе данных ТЛЧ, за исключением бедаквилина, претоманида и деламанида. | |
Лечение РУ-ТБ туберкулеза
- профиль лекарственной устойчивости,
- предшествующее лечение противотуберкулезными препаратами и историю болезни,
- профиль лекарственной устойчивости у близких контактов,
- возраст пациента,
- локализацию внелегочного туберкулеза и
- степень распространенности легочного туберкулеза.
Краткосрочные режимы для пациентов с МЛУ ТБ:
- 6 BPaLM (Bdq-Pa-Lzd-Mfx)
- 4-6 Bdq(6 м)-Lfx(Mfx)-Cfz-Z-E- Pto- Hhd (4 м) / 5-6 Lfx (Mfx)-Cfz-Z-E-Pto
- 4-6 Bdq(6 м)-Lfx/Mfx-Cfz-Z-E-Hh(4м)- Lzd(2 м) / 5 Lfx/Mfx Cfz-Z-E
- Модифицированный краткосрочный режим лечения ТБ (мКРЛ) – в рамках операционного исследования.
Схемы лечения для пациентов 6 лет и старше:
Схема лечения для детей младше 6 лет:
Краткосрочный режим для пациентов с МЛУ-ТБ с устойчивостью к фторхинолонам:
-
6(9) BPaL (Bdq-Pa-Lzd)
Критерии исключения с лечения краткосрочными режимами
Пациенты с подтвержденным МЛУ/РУ-ТБ, у которых:
- Пациенты с МЛУ/РУ-ТБ с сохраненной чувствительностью к Mfx,
- Пациенты, ранее принимавшие бедаквилин, линезолид, претоманид или деламанид и фторхинолоны (Mfx) менее чем 1 месяц.
- Пациенты с пре-ШЛУ-ТБ, т.е. МЛУ/РУ-ТБ с дополнительной устойчивостью к фторхинолонам,
- Пациенты, ранее принимавшие бедаквилин, линезолид, претоманид или деламанид менее чем 1 месяц.
- более 2 недель происходит прерывание последовательного приема всех препаратов в схеме; или
- в совокупности более 4 недель происходит прерывания непоследовательного приема всех препаратов в схеме;
- сохраняется положительный результат посева на 4-м и 5-м месяце лечения и положительный результат микроскопии на 5-м и 6-м месяце.
При возникновении нежелательных явлений следует определить «виновный» препарат и последующую тактику ведения пациентов проводить на основе таблицы 3.
Таблица 3. Тактика ведения пациентов при возникновении НЯ на режиме BPaLM/BPaL
| Препарат | Нежелательное явление | Предпринятые меры | Действие |
| Бедаквилин | непереносимость | отмена препарата | перевод на ИР |
| Претоманид | непереносимость | отмена препарата | перевод на ИР |
| Линезолид | периферическая невропатии 1 или 2 степени или миелосупрессия |
1-9 неделя лечения
• снижение дозы до 300 мг
|
перевод на ИР |
|
9-16 неделя лечения
• приостановка приема препарата на 1–2 нед перед снижением дозы
• снижение дозы до 300 мг
|
продолжение лечения по BPaL/BPaL M | ||
|
17-26 неделя лечения
• снижение дозы до 300 мг
• возможна полная отмена препарата
|
продолжение лечения по BPaL/BPaL M | ||
| периферическая невропатии 3 или 4 степени | полная отмена приема линезолида; | перевод на ИР | |
| неврит зрительного нерва, любой степени тяжести | полная отмена линезолида | перевод на ИР |
4-6 Bdq(6 м)-Lfx-Cfz-Z-E- Eto- Hhd (4 м) / 5-6 Lfx (Mfx)-Cfz-Z-E-Eto
4-6 Bdq(6 м)-Lfx/Mfx-Cfz-Z-E-Hh(4м)- Lzd(2 м) / 5 Lfx/Mfx Cfz-Z-E
- - женщинам, которые беременны или кормят грудью;
- - при возникновении НЯ на Eto;
ВНЕДРЕНИЕ РЕЖИМОВ ЛЕЧЕНИЯ В РАМКАХ ОПЕРАЦИОННЫХ ИССЛЕДОВАНИЙ
- протокол исследования, который должен включать наблюдение после окончания лечения;
- одобрение национального совета по этике;
- обеспечение доступа к базовому пакету исследований для исключения НЯ.
- краткий исследовательский пакет содержит дополнительные рекомендации по разработке протокола, инструментов сбора данных и других вспомогательных документов, которые облегчают операционные исследования.
В 2022 года, в условиях операционного исследования, в Кыргызстане начато внедрение нового модифицированного короткого режима лечения РУ/МЛУ-ТБ, на основании рекомендаций ВОЗ.
Модифицированные полностью пероральные укороченные схемы лечения МЛУ-ТБ включает препараты из группы А, группы В и деламанид из группы С.
Продолжительность лечения составляет 39 недель.
Схемы лечения для пациентов 6 лет и старше:
Схема лечения для детей младше 6 лет:
Дозировки лекарственных препаратов соответствуют общепринятым и представлены в Приложении D.
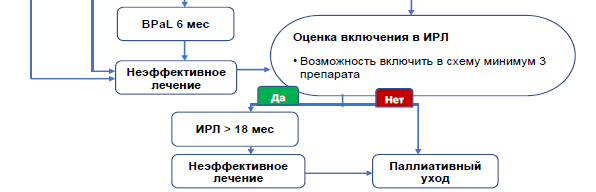
ИНДИВИДУАЛЬНЫЙ (ДЛИТЕЛЬНЫЙ) РЕЖИМ ЛЕЧЕНИЯ ТБ (ИРЛ)
Принципы лечения
Дизайн более длительных схем (18–20 месяцев) основан на выборе лекарственных средств из групп А, В и С (Таблица 4), на основе профиля лекарственной устойчивости.
| Группа | Препараты | Сокращения |
| Группа А: Включите в режим лечения все 3 препарата, за исключением случаев когда они не могут быть использованы |
Левофлоксацин или Моксифлоксацин Бедаквилин Линезолид |
Lfx Mfx Bdq Lzd |
| Группа В: Добавьте оба препарата за исключением случаев, когда они не могут быть использованы |
Клофазимин Циклосерин |
Cfz Cs |
| Группа С : Включите для формирования полного режима химиотерапиии, в тех случаях, когда препараты из группы А и В не могут быть использованы |
Этамбутол Деламанид Пиразинамид Имипенем-циластатин или Меропенем Амикацин или Стрептомицин Этионамид или Протионамид Пара-аминосалициловая кислота |
E Dlm Z Ipm/Cln Mpm Am или St Eto / Pto PAS |
Предварительная клиническая оценка
Предварительная клиническая оценка включает:
Составление индивидуального/длительного режима лечения для ЛУ-ТБ пациентов
- Препараты следует выбирать на основе иерархии, приведенной в таблице 4, с учетом самых последних результатов ТЛЧ пациента.
- В схему лечения пациента с МЛУ /ШЛУ ТБ при назначении индивидуального режима должны быть включены все три препарата группы А и, по крайней мере, один препарат группы В, чтобы гарантировать, что лечение начинается, по крайней мере, с 4-х препаратов, которые могут быть эффективными, и что, как минимум, три эффективных препарата останутся в режиме после того, как лечение c бедаквилином будет прекращено через 24-36 недель.
- Если используются только один или два препарата группы A, оба препарата группы B должны быть включены.
- Если режим не может быть составлен только препаратами из групп A и B, для его завершения добавляются препараты группы C.
- Дозы ПТП назначаются в соответствии с весовой категорией, и корректируются в случае прибавки веса в ходе лечения (Приложение D).
- Нет возрастных ограничений среди детей для назначения бедаквилина и деламанида.
- Для предотвращения развития НЯ (нейротоксических эффектов и / или миелосупрессии) с профилактической целью назначается пиридоксин (витамин B6) из расчёта 50 мг на каждый препарат (линезолид и изониазид). При приеме циклосерина – пиридоксин назначается из расчета 50 мг на 1 капсулу (250 мг) препарата. Максимальная суточная профилактическая доза пиридоксина составляет не более 150 мг.
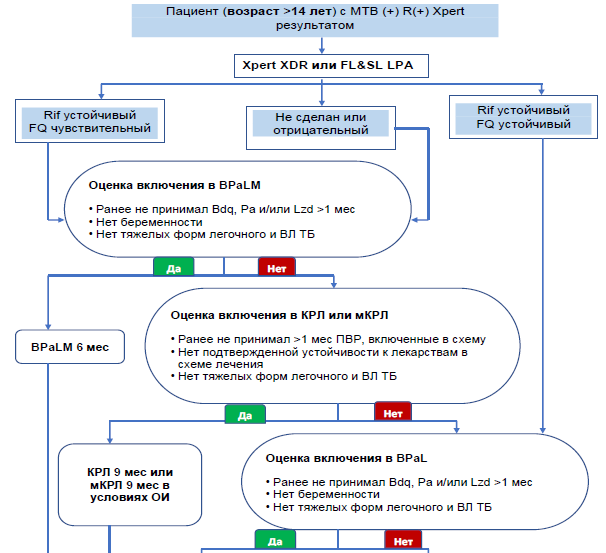
МОНИТОРИНГ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ ТБ, Ну-ТБ И РУ/МЛУ-ТБ
Чтобы ограничить риск приобретения дополнительной лекарственной устойчивости, следует избегать добавления одного противотуберкулезного препарата у пациентов, у которых остаются положительные результаты мазка или посева после 2-го месяца лечения, у которых не наблюдается благоприятного клинического ответа.
Кроме того, для предотвращения и лечения возможных токсических эффектов этамбутола у детей (например, ретробульбарный неврит) необходимо:
Мониторинг лечения РУ/МЛУ-ТБ
- Мониторинг лечения РУ/МЛУ-ТБ проводится ежемесячно и включает направление двух образцов мокроты (один из которых должен быть утренним) на микроскопию и посев на MGIT до 6-го месяца, затем посев на среду Левенштейн-Йенсена до конца лечения (Рис 4).
- Микроскопия мазка и посев проводятся ежемесячно на протяжении полного курса лечения;
- Если в конце 4-го месяца лечения или позже получен положительный результат посева, следует провести фТЛЧ с целью своевременной коррекции режима лечения.
- Клиницист указывает в направлении на исследование – «Вероятность неэффективного лечения».
- Нет необходимости повторять исходные тесты (GeneXpert MTB/RIF) на чувствительность к рифампицину, поскольку устойчивость к этому препарату сохраняется.
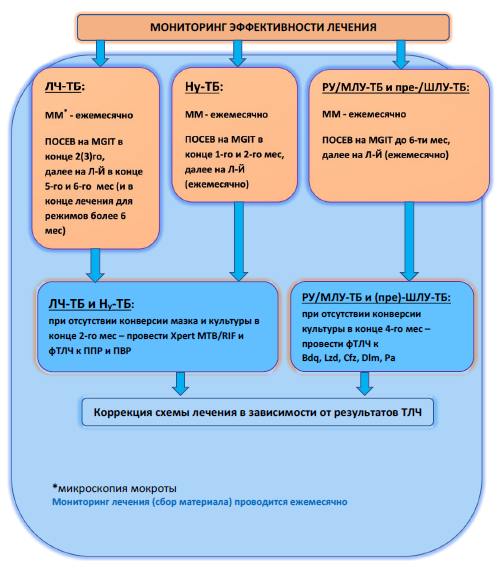
a - кроме H и R. Проводится для пациентов с ЛЧ-ТБ и Hу в предыдущем эпизоде
b - по генным мутациям определить дозу ФХ
с – микроскопия мазка
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ЛЕГОЧНОГО ТБ
Лечение после хирургического вмешательства
Оперативное лечение является дополнением к химиотерапии и может принести пользу пациенту в случае, если операция проведена высококвалифицированным хирургом и завершена отличным послеоперационным уходом.
Таблица 5. Определения результатов лечения ЛУ -ТБ
| Результат* | Формулировка |
| Вылечен |
Курс терапии закончен при отсутствии свидетельств неэффективного лечения и имеется:
- 3 и более отрицательных посева мокроты, с промежутком в 30 дней к концу курса лечения (включая последний месяц) - для краткосрочных режимов лечения, и
- 5 и более отрицательных посева мокроты, с промежутком в 30 дней к концу курса лечения (включая последний месяц) - для длительных режимов лечения.
|
| Лечение завершено |
Курс терапии закончен при отсутствии свидетельств неэффективного лечения, но нет доказательств, что имеется:
- 3 и более отрицательных посева мокроты, с промежутком в 30 дней к концу курса лечения (включая последний месяц) - для краткосрочных режимов лечения, и
- 5 и более отрицательных посева мокроты, с промежутком в 30 дней к концу курса лечения (включая последний месяц) - для длительных режимов лечения.
|
| Неэффективное лечение |
Пациент, режим лечения которого нужно было прекратить или полностью изменить на новый режим лечения.
К причинам изменения относятся:
|
| Умер | Пациент умер до начала лечения или в процессе химиотерапии, причина смерти может быть любой. |
| Потерян для наблюдения | Пациент, который не начал лечение или прервал лечение на 2 месяца и более. |
| Успешное лечение | Сумма показателей «Излечен» и «Лечение завершено». |
| Не оценен | В эту подгруппу входят случаи, «переведенные» в другое лечебное учреждение, результат лечения которых неизвестен; однако она исключает тех, кто потерян для последующего наблюдения. |
| Дополнительное определение для оценки режимов лечения | |
| Устойчивый успех лечения | Пациент, оцененный через 6 месяцев (для лекарственно-чувствительного и лекарственно-устойчивого туберкулеза) и через 12 месяцев (только для лекарственно-устойчивого туберкулеза) после успешного завершения лечения и не имеет активного туберкулеза. |
Термины
Конверсия: 2 отрицательных результата исследований культуры, проведенных последовательно, с интервалом в 30 дней. Датой конверсии считается дата сбора мокроты от первого полученного отрицательного результата культуры.
- выяснить наличие сопутствующих состояний,
- назначить консультацию соответствующего специалиста,
- назначить необходимый комплекс обследования.
БЕРЕМЕННОСТЬ
Существует 5 классов безопасности противотуберкулёзных препаратов для беременных женщин по классификации FDA:
| Безопасность класса | Описание | Препарат |
| A | Препарат безопасен | --- |
| B | Предположительно безопасен | Bdq*, E |
| C | Ожидаемая польза от препарата оправдывает возможный риск для плода | H, R, Z, Cm, Fq, Cs, PAS, Cfz, Clr, Lzd |
| D | Препарат небезопасен, есть риск для плода | Am, Eto, Pto, Dlm |
| X | Риск от препарата превышает любую возможную пользу | --- |
Во время беременности следует избегать назначения амикацина, который обладает особенно выраженным токсическим действием на плод, а также – тиоамидов, которые усиливают побочные эффекты и обладают выраженным тератогенным свойством.
САХАРНЫЙ ДИАБЕТ
ПОЧЕЧНАЯ НЕДОСТАТОЧНОСТЬ

Для пациентов с клиренсом креатинина менее 30 мл/мин или находящихся на гемодиализе назначение ПТП проводится соответственно предлагаемой таблице 6.
Таблица 6. Рекомендуемые дозы и частота приема ПТП при почечной недостаточности
| Препарат | Изменять ли частоту приёма? | Рекомендуемые дозы и частота приема ПТП Клиренс креатинина менее 30 мл/мин. или на гемодиализе |
| Изониазид | нет | 300 мг однократно ежедневно |
| Рифампицин | нет | 600 мг однократно ежедневно или 600 мг 3 раза в неделю |
| Пиразинамид | да | 25-35 мг/кг 3 раза в неделю |
| Этамбутол | да | 15-25 мг/кг 3 раза в неделю |
| Левофлоксацин | да | 750-1000 мг 3 раза в неделю |
| Моксифлоксацин | нет | 400 мг 1 раз день |
| Циклосерин | да | 250 мг 1 раз в день или 500 мг 3раза в неделю |
| Протионамид | нет | 250-500 мг ежедневно |
| Этионамид | нет | 250-500 мг ежедневно |
| Амикацин | да | 12-15 мг/кг 2-3 раза в неделю |
| Клофазимин | нет | 100 мг ежедневно |
| Амоксицилин/ Клавуланат | да | 1000 мг ежедневно из расчета на амоксициллин |
| Бедаквилин | нет |
У пациентов с легкой и средней степенью тяжести коррекции дозы не требуется.
При тяжелой почечной недостаточности прием с осторожностью
|
| Деламанид | нет |
У пациентов с легкой и средней степенью тяжести коррекции дозы не требуется.
При тяжелой почечной недостаточности прием с осторожностью
|
| Линезолид | нет | Возможен приём при проведении мониторинга лабораторных исследований |
| Имипинем /Циластатин | нет |
Клиренс креатинина 20-40 мл / мин: доза 500 мг каждые 8 ч
клиренс креатинина <20 мл / мин: доза 500 мг каждые 12 ч
|
СУДОРОЖНЫЕ СОСТОЯНИЯ
ПСИХИЧЕСКИЕ ЗАБОЛЕВАНИЯ
АКТИВНЫЙ МОНИТОРИНГ И МЕНЕДЖМЕНТ БЕЗОПАСНОСТИ ЛЕЧЕНИЯ
Нежелательное явление (НЯ) - это любое неблагоприятное медицинское явление, которое может наблюдаться у ТБ пациента в ходе лечения фармацевтическими препаратами, но которое не обязательно имеет причинно-следственную связь с данным лечением.
Степень тяжести НЯ отражает интенсивность нежелательного явления и оценивается по шкале СТСАЕ (Criteria for Adverse Events), подробно показывающей признаки и симптомы и/или лабораторные значения (Таблица 7).
Таблица 7. Степень тяжести проявлений нежелательных явлений
| Степень 1 (легкая) | Степень 2 (умеренная) | Степень 3 (тяжелая) | Степень 4 (угрожающая жизни) | Степень 5 (смерть) |
|
Легкий дискомфорт (<48 часов);
Не требуется медицинское вмешательство
|
Умеренные ограничения деятельности.
Может потребоваться минимальное медицинское вмешательство
|
Заметное ограничение деятельности. Необходимо медицинское вмешательство, возможна госпитализация | Чрезмерное ограничение деятельности. Необходимо серьезное медицинское вмешательство, госпитализация и больничный уход | Смерть |
Серьезные нежелательные явления и Нежелательные явления, представляющие особый клинический интерес включают:
| НЯ, представляющие особый клинический интерес (часто встречаемые) | Серьезные НЯ |
|
• Переферическая невропатия
• Психические расстройства и нарушения со стороны центральной нервной системы (например: депрессия, психоз, суицидальные попытки, судороги)
• Неврит зрительного нерва или ретинопатия
• Ототоксичность (нарушение слуха, потеря слуха)
• Миелосупрессия (проявляется как анемия, тромбоцитопения, нейтропения или лейкопения)
• Удлинение интервала QT*
• Гипотиреоз
• Гипокалиемия
• Панкреатит
• Острая почечная недостаточность
• Гепатит определяется как увеличение уровня аланинаминотрансферазы (АЛАТ) или аспартатаминотрансферазы (АСАТ):
|
• Смерть пациента по любой причине
• Состояние, угрожающее жизни (которое может привести к летальному исходу)
• Состояние, требующее госпитализации или продления срока текущей госпитализации
• Состояние, приводящее к стойкой или значительной утрате трудоспособности
• Не вынашивание плода, дефект развития плода
• Другое значимое, с медицинской точки зрения, событие, которое не попадает под перечисленные выше критерии, однако, заслуживает особого внимания |
Общие принципы
НАБЛЮДЕНИЕ ПАЦИЕНТОВ
Для пациентов, завершивших лечение по коротким режимам лечения РУ ТБ. Необходимо исследование мокроты методом бактериоскопии и посева 1 раз в 3 месяца. Проведение рентген обследования – 1 раз в 6 месяцев в течение 12 месяцев после окончания лечения. Затем эти же исследования повторяются 1 раз в 6 месяцев в течении следующих 12 месяцев. Если у пациента в течении первых 12 месяцев после окончания лечения возобновилось бактериовыделение и установлен активный туберкулёз, то успешный исход лечения меняется на исход «неэффективное лечение». При возобновлении бактериовыделения на 2 году наблюдения, исход не меняется, случай расценивается как «рецидив процесса».
Для пациентов, отказавшихся от лечения.
Для пациентов в процессе лечения.
Для пациентов, прервавших лечение/отказ.
ДОПУСК К РАБОТЕ И УЧЕБЕ
Для пациентов с ПЛУ-ТБ
Для пациентов с пре-ШЛУ и ШЛУ-ТБ
Если пациенту проведена операция на легком
Госпитализация
ОРГАНИЗАЦИЯ МЕДИЦИНСКОЙ ПОМОЩИ
- Рассмотрение случаев ТБ пациентов, находящихся на лечении в НЦФ, в том числе случаев для подтверждения клинически установленного ТБ, назначение режима химиотерапии, контроль мониторинга лечения и определения исходов лечения согласно действующим в стране руководствам и протоколам по ТБ.
- Общая координация работы консилиумов страны. Осуществление мониторинга выполнения функций врачебного консилиума и поддержка в работе региональных консилиумов.
- Принятие окончательного решения в спорных диагностических и клинических случаях ведения пациентов.
Задачи областного консилиума
В процессе лечения, каждые 3 месяца все пациенты с ЛУ ТБ должны быть представлены на консилиум. В следующих случаях предоставляются чаще:
Критерии госпитализации
- выраженные симптомы интоксикации (лихорадка, потеря массы тела, истощение),
- дыхательная недостаточность,
- нарушение сердечной деятельности,
- осложнения туберкулёзного процесса,
- тяжёлые сопутствующие заболевания, осложняющие течение ТБ.
Условия перевода на амбулаторное лечение
Этот комплекс мероприятий по организации ведения каждого случая туберкулёза с учётом пациент-ориентированного подхода, включает социальное и психологическое сопровождение. Лечение под непосредственным наблюдением (ЛНН) может проводиться в условиях ГСВ, ФАП, ПТК, на дому, под контролем медицинских работников или специально обученных общественных помощников. Этот способ более предпочтителен, по сравнению с лечением под контролем родственников или самостоятельным лечением (СЛ). Лечение под видеонаблюдением (ЛВН) может заменить ЛНН при наличии видеосвязи. ЛВН повышает автономию пациента (сокращение транспортных расходов пациента, гибкий график), удобен для пациента и медицинского работника, снижает вероятность стигматизации, сокращает число посещений в медицинское учреждение. Также снижает риск передачи ТБ инфекции в случаях бактериовыделения. Потенциально может обеспечить повышение приверженности пациента и улучшить эффективность лечения.
Профилактика
ПРОФИЛАКТИКА ЛУ-ТБ
Информация
Источники и литература
-
Клинические протоколы Министерства здравоохранения Кыргызской Республики
- Клинические протоколы Министерства здравоохранения Кыргызской Республики - 1. WHO consolidated guidelines on tuberculosis. Module 4: treatment - drug-resistant tuberculosis treatment, Dec 2022 update 2. WHO operational handbook on tuberculosis. Module 4: treatment - drug-resistant tuberculosis treatment, Dec 2022 update 3. Оперативное сообщение: ключевые изменения в лечении туберкулеза с лекарственной устойчивостью, май 2022 4. Практический справочник ВОЗ по туберкулезу. Модуль 4. Лечение. Лечение лекарственно-устойчивого туберкулеза (2021) https://www.euro.who.int/tuberculosis/ publications. 5. Rapid communication on updated guidance on the management of tuberculosis in children and adolescents, WHO guideline, August 2021 6. WHO consolidated guidelines on tuberculosis. Module 3: Diagnosis - Rapid diagnostics for tuberculosis detection 2021 update 7. WHO consolidated guidelines on tuberculosis. Module 4: treatment - drug-resistant tuberculosis treatment. Geneva: World Health Organization; 2020. Licence: CC BY-NC-SA 3.0IGO. http://apps.who.int/iris. 8. Сводное руководство ВОЗ по лечению лекарственно-устойчивого туберкулеза. Женева: Всемирная организация здравоохранения; 2020. Лицензия: CCBY-NC-SA 3.0 IGO. 9. Meeting report of the WHO expert consultation on drug-resistant tuberculosis treatment outcome definitions 17-19 November 2020 10. Global tuberculosis report 2019. Geneva: World Health Organization; 2019, http://apps.who.int/iris. 11. WHO TB country profile Kyrgyzstan: http://www.who.int/tb/country/data/profiles/en/ Last accessed 22.04.2017. 12. Treatment guidelines for multidrug – and rifampicin - resistant tuberculosis, WHO. 2018 update 13. Определения и система отчетности по туберкулезу, WHO. 2013 14. Companion handbook to the WHO Guidelines for the programmatic management of drug-resistant tuberculosis, WHO. 2014 15. Guidelines for Clinical and Operation Management of Drug-Resistant Tuberculosis, IUATLD. 2013 16. Commercial products for preserving clinical specimens for the diagnosis of tuberculosis, 2017. WHO 17. Алгоритм для лабораторной диагностики и мониторинга лечения туберкулёза лёгких и туберкулёза с лекарственной устойчивостью, применяя современные быстрые молекулярные методы, ВОЗ. 2017 18. Line probe assays for drug-resistant tuberculosis detection, interpretation and reporting guide for laboratory staff and clinicians, GLI. 2018 19. Guidelines for the treatment of drug-susceptible tuberculosis and patient care. (WHO/HTM/TB/2017.05) [Internet]. Geneva, World Health Organization. 2017. 20. Nunn AJ, Rusen ID, Van Deun A, Torrea G, Phillips PPJ, Chiang C-Y, et al. Evaluation of a standardized treatment regimen of anti-tuberculosis drugs for patients with multi-drug-resistant tuberculosis (STREAM): study protocol for a randomized controlled trial. Trials. 2014; 15:353. 21. Preliminary results from STREAM trial provide insight into shorter treatment for multidrug-resistant tuberculosis [Internet]. [cited 2017 Oct 17]. 22. Kuaban C, Noeske J, Rieder HL, Aït-Khaled N, Abena Foe JL, Trébucq A. High effectiveness of a 12-month regimen for MDR-TB patients in Cameroon. Int J Tuberc Lung Dis. 2015 May;19(5):517–24. 23. Consolidated guidelines on the use of antiretroviral drugs for treating and preventing HIV infection, recommendations for a public health approach - Second edition,2016 24. The role of surgery in the treatment of pulmonary TB and multidrug-and extensively drug-resistant TB, WHO,2014
Информация
Ключевые слова: лекарственно-устойчивый туберкулез (drug-resistant tuberculosis), монорезистентный туберкулез (monodrug-resistant tuberculosis), полирезистентный туберкулез (polydrug-resistant tuberculosis), туберкулез с множественной лекарственной устойчивостью (multidrug-resistant tuberculosis), туберкулез с широкой лекарственной устойчивостью (extensively-drug-resistant tuberculosis), случаи лекарственно-устойчивого туберкулеза (DR-TB cases), диагностика (diagnosis), тест на лекарственную чувствительность (drug susceptibility test), лечение (treatment), химиотерапия (chemotherapy), противотуберкулезные препараты второго ряда (anti-tuberculosis drugs of the second line), нежелательные явления (adverse events), регистрация (notification).
СПИСОК СОКРАЩЕНИЙ
1 Risk factors for types of recurrent tuberculosis (reactivation versus reinfection): A global systematic review and meta-analysis, International Journal of Infectious Diseases, March 2022, Pages 14-20
2 Фторхинолоны включают левофлоксацин и моксифлоксацин, рекомендованные в настоящее время ВОЗ для включения в короткие и длительные схемы лечения.
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
Что такое туберкулез?
Туберкулез распространяется по воздуху в виде маленьких капелек (которые не видны невооруженным глазом). Эти капельки вылетают изо рта и носа больного человека, когда он говорит, кашляет или чихает. В некоторых из этих капелек могут быть микобактерии туберкулеза. Когда другой человек вдыхает этот воздух, некоторые капельки с микобактериями туберкулеза могут попасть в его организм и достичь легких.
Могут ли окружающие заразиться от тебя туберкулезом?
Что такое внелегочный туберкулез?
Почему мне нужно пить так много разных таблеток?
Могу ли я воспользоваться услугами целителя или использовать средства народной медицины?
Приложение А2. Методология разработки клинических рекомендаций
Клиническая проблема:
Название документа:
Целевые группы:
Цель клинического руководства
Дата создания
Адрес для переписки с рабочей группой
Декларация конфликта интересов
| Найденные электронные базы данных по клиническим руководствам и практическим рекомендациям | Интернет-адрес |
| Страна и название ресурса | |
| Международная ассоциация | |
| Всемирная организация здравоохранения (World Health Organization, WHO) | www.who.int |
| Ahmad N., et al. Treatment correlates of successful outcomes in pulmonary multidrug-resistant tuberculosis: An individual patient data meta-analysis. | Lancet. 2018; 392:821–834. doi: 10.1016/S0140-6736(18)31644-1. |
| WHO consolidated guidelines on tuberculosis. Module 4: Treatment Drug-resistant tuberculosis treatment, 2020. | www.who.int |
| WHO operational handbook on tuberculosis. Module 4: Treatment Drug-resistant tuberculosis treatment, 2020. | www.who.int |
| The Lancet Respiratory Medicine Commission: 2019 update: epidemiology, pathogenesis, transmission, diagnosis, and management of multidrug-resistant and incurable tuberculosis. | Lancet Respir Med 2019; 7: 820– 26. |
| Van Deun, A., et al., Short, highly effective, and inexpensive standardized treatment of multidrug-resistanttuberculosis. | American Journal of Respiratory and Critical Care Medicine, 2010. 182(5): p. 684-692. |
| Trebucq A., et al. Short-Course Regimen for Multidrug-Resistant Tuberculosis: A Decade o fEvidence. | J Clin Med. 2020 Jan; 9(1): 55. doi: 10.3390/jcm9010055 |
| Kuaban, C., et al., High effectiveness of a 12-month regimen for MDR-TB patients in Cameroon. | International Journal of Tuberculosis and Lung Disease, 2015. 19(5): p. 517-524. |
| Piubello A, H.S., Souleymane MB, Boukary I, Morou S, Daouda M, et al., High cure rate with standardised short-course multidrug-resistant tuberculosis treatment in Niger: no relapses | Int J Tuberc Lung Dis Off J Int Union Tuberc Lung Dis. , 2014. 18(10): p. 1188–94 |
| FDA approves new drug for treatment-resistant forms of tuberculosis that affects the lungs. August 14, 2019 | https://www.fda.gov/newsevents/press-announcements/fdaapproves-new-drug-treatmentresistant-forms-tuberculosisaffects-lungs |
| Aung, K.J.M., et al., Successful ‘9-month Bangladesh regimen’ for multidrug resistant tuberculosis among over 500 consecutive patients. | Int J Tuberc Lung Dis, 2014. 18(10): p. 1180-1187. |
| Rapid Communication: Key changes to the treatment of drug-resistant tuberculosis, | https://www.who.int/tb/publications/2019/rapid_communications_MDR/en/ |
Классы рекомендаций и уровни доказательности
| Классы рекомендаций | Определения | Предлагаемая формулировка |
| Класс I | Данные и/или всеобщее согласие, что конкретный метод лечения или вмешательство полезны, эффективны, имеют преимущества | Рекомендуется/ показан |
| Класс II | Противоречивые данные и/или расхождение мнений о пользе/эффективности конкретного метода лечения или процедуры | |
| Класс II a | Большинство данных/мнений говорит о пользе/эффективности | Целесообразно применять |
| Класс II b | Данные/мнения не столь убедительно говорят о пользе/эффективности | Можно применять |
| Класс III | Данные и/или всеобщее согласие, что конкретный метод лечения или вмешательство не являются полезной или эффективной, а в некоторых случаях могут приносить вред |
Не
рекомендуется
|
Уровни доказательности
| Уровень доказательности | Определения |
| Уровень доказательности А | Данные многочисленных рандомизированных клинических исследований или мета-анализов |
| Уровень доказательности В | Данные одного рандомизированного клинического исследования или крупных не рандомизированных исследований |
| Уровень доказательности С | Согласованное мнение экспертов и/или небольшие исследования, ретроспективные исследования, регистры |
Приложение В. Исследование участка определения устойчивости к хинолонам гена gyrA и gyrВ тестом GenoType MTBDRsl13
| Участок-мишень | MTBDRsl зонд | Исследуемая мутация | Клиническая интерпретация |
| gyrA WT1 | gyrA WT1 не выражен | Кодон(ы) 85-89 |
Lfx не эффективен
Mfx (высокие дозы) можно использовать
Схему следует пересмотреть на основе результатов фТЛЧ
|
| gyrA WT2 | gyrA МУТ1 выражен | A90V |
Lfx не эффективен
Mfx (высокие дозы) можно использовать
Схему следует пересмотреть на основе результатов фТЛЧ
|
| gyrA МУТ2 выражен | S91P |
Lfx не эффективен
Mfx (высокие дозы) можно использовать
Схему следует пересмотреть на основе результатов фТЛЧ
|
|
|
gyrA
МУТ1 и МУТ2
не выражены
|
Кодон(ы) 89-93 |
Lfx не эффективен
Mfx (высокие дозы) можно использовать
Схему следует пересмотреть на основе результатов фТЛЧ
|
|
| gyrA WT3 | gyrA МУТ3A выражен | D94 |
Lfx не эффективен
Mfx (высокие дозы) можно использовать
Схему следует пересмотреть на основе результатов фТЛЧ
|
| gyrA МУТ3B выражен | D94N или D94Y |
Lfx не эффективен
Mfx не эффективен
|
|
| gyrA WT3 | gyrA МУТ3С выражен | D94G |
Lfx не эффективен
Mfx не эффективен
|
| gyrA МУТ3D выражен | D94H |
Lfx не эффективен
Mfx не эффективен
|
|
| gyrA МУТ3A МУТ3В, МУТ3С, МУТ3D не выражены | Кодон(ы) 92-96 |
Lfx не эффективен
Mfx (высокие дозы) можно использовать
Схему следует пересмотреть на основе результатов фТЛЧ
|
8 Line probe assays for drug-resistant tuberculosis detection, interpretation and reporting guide for laboratory staff and clinicians, GLI. 2018
Приложение С. Суточные пероральные дозировки противотуберкулезных препаратов для взрослых с учетом веса (для пациентов с весом ≥30 кг)
|
ПРЕПАРАТЫ
|
Суточная доза
|
30–35 кг
|
36–45 кг
|
46–55 кг
|
56–70 кг | >70 кг |
|
Рифампицин
|
10 (8-12) мг/кг - 1 раз в день
|
300мг
|
450мг
|
450мг
|
600мг |
600мг
|
|
Изониазид
|
5 (4-6) мг/кг - 1 раз в день
|
150мг
|
200мг
|
300мг
|
300мг |
300мг
|
|
Пиразинамид
|
20–30 мг/кг - 1 раз в день
|
800мг
|
1000мг
|
1200-1600* мг
|
1600мг | 2000мг |
|
Этамбутол
|
15–25 мг/кг - 1 раз в день
|
600мг
|
800мг
|
1000мг
|
1200мг |
1200мг
|
|
Левофлоксацин
|
750–1000 мг - 1 раз в день
|
750мг
|
750мг
|
1000мг
|
1000мг |
1000мг
|
|
Моксифлоксацин
|
400 мг -1 раз в день
|
400мг
|
400мг
|
400мг
|
400мг |
400мг
|
|
Моксифлоксацин высокая доза
|
400-800 мг -1 раз в день
|
400мг
|
400-600мг
|
400-600мг
|
800мг |
800мг
|
|
Протионамид
|
500–750 мг/в день двумя раздельными дозами
|
500мг
|
500мг
|
750мг
|
750мг |
1000мг
|
|
Циклосерин
|
500–750 мг/в день двумя раздельными дозами
|
500мг
|
500мг
|
500-750 *мг
|
750мг |
750мг
|
|
Парааминосалициловая кислота
|
8 гр/в день двумя раздельными дозами
|
8 гр
|
8 гр
|
8 гр
|
8 гр |
8-12 гр
|
|
Бедаквилин
|
400 мг один раз в день в течение 2 недель, затем по 200 мг 3 раза в неделю
|
|||||
|
Деламанид
|
100 мг два раза в день (общая ежедневная доза = 200 мг)
|
|||||
|
Клофазимин
|
100 мг ежедневно
|
|||||
|
Линезолид
|
600 мг один раз в день
|
600мг
|
600мг
|
600мг
|
600мг |
600мг
|
|
Высокая доза Изониазида
|
10 мг/кг в день, максим. сут доза 600 мг
|
300мг
|
400мг
|
500мг
|
600мг |
600мг
|
|
Имипенем/ Циластатин
|
1000 имипенем/1000 мг циластатина два раза в день
|
|||||
|
Меропенем
|
1000 мг три раза в день (альтернативная доза по 2000 мг два раза в день)
|
|||||
|
Амоксициллин/ клавулановая кислота
|
875 мг амоксициллин/125 мг клавулоновая кислота 80 мг/кг в день двумя дозами
|
2000мг
|
2000мг
|
2000мг
|
2000мг |
2000мг
|
*Дозы рекомендованы ВОЗ 2019 г.
Приложение D. КЛИНИЧЕСКИЙ МОНИТОРИНГ ЛЕЧЕНИЯ МЛУ/ШЛУ-ТБ (заполняется лечащим врачом в карте ТБ 01 У)
Фамилия и имя пациента ________________________________________________ Дата начала лечения _____/______/_______
| Основные исследования | Норма | До леч-я | Месяц лечения | ||||||||||||
| 0 мес | 1 | 2 | 3 | 4 | 5 | 6 | ..мес | ..мес | ..мес | ..мес | ..мес | ..мес | |||
| Дата | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | ||
| 1 | Вес / Рост | ||||||||||||||
| 2 | Гемоглобин (г/л) | ||||||||||||||
| 3 | Эритроциты (1012) | ||||||||||||||
| 4 | Лейкоциты (109) | ||||||||||||||
| 5 | Тромбоциты (109) | ||||||||||||||
| 6 | СОЭ мм/час | ||||||||||||||
| 7 | АЛТ (ммоль/л) | ||||||||||||||
| 8 | ACT(ммоль/л) | ||||||||||||||
| 9 | Глюкоза (ммоль/л) | ||||||||||||||
| 10 | Креатинин (мкмоль/л) | ||||||||||||||
| 11 | Скорость клубочк фильтрации (СКФ) | ||||||||||||||
| 12 | Альбумин (г/л) | ||||||||||||||
| 13 | 'К (ммоль/л) | ||||||||||||||
| 14 | Са (ммоль/л) | ||||||||||||||
| 15 | Mg (ммоль/л) |
N>10 сек П-N |
|||||||||||||
| 16 |
Ощущение вибрации
камертона*
|
||||||||||||||
| 17 | Тест на остроту зрения** | ||||||||||||||
| Л-N | |||||||||||||||
| 18 | Тест Ишихара*** | ||||||||||||||
* N- норма (ощущается >10 сек); 1- легкая ст. (ощущается 6–10 сек); 2 – умеренная ст. (ощущается <5 сек); 3 – сильное снижение (не ощущается)
Данные ЭКГ
| 1 | ЭКГ/ QTc Дата_____ Результат | Норма <430 (м) <450 (ж) | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг |
Исследования по показаниям
| Норма | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | дд/мм/гг | ||
| 2 | Тиреотропный гормон (ТТГ) | |||||||||||||||
| 2 | Липаза | |||||||||||||||
| 2 | Амилаза | |||||||||||||||
| 2 | Тест на беременность | |||||||||||||||
| 2 | Другое | |||||||||||||||
| 2 | ||||||||||||||||
| 2 |
Примечание: частота и показания для проведения исследований по вышеперечисленным пунктам:
1. Ежемесячно
2. Ежемесячно до 6 мес. лечения; после 6 мес - минимум 1 раз в квартал
3, 4. См п.2
5. При лечении Lzd и при ВИЧ позитивном статусе: в 1-й месяц еженедельно, далее см п.2.
6. См п.2
7, 8. При вирусном гепатите: в 1-й месяц еженедельно, далее см п.2.
9. До начала лечения, далее по показаниям
10. При лечении инъекционными препаратами – ежемесячно
12. При лечении Dlm - 1 раз в 2 мес до 6 мес лечения; после 6 мес – по показаниям
13. При лечении инъекционными ПВР и при назначении Bdq, Dlm – ежемесячно
14, 15. При назначении Bdq, Dlm – ежемесячно
16. При лечении инъекционными препаратами – ежемесячно
17, 18. При лечении Lzd и E – ежемесячно
19. При лечении Bdq, Dlm, Cfz, Mfx или с низким уровнем альбумина (<3,4g/dl) - в 1-й месяц еженедельно, далее ежемесячно
20. При лечении Pto и Pas – 1 раз в три месяца; при лечении одним из них (Pto или Pas) – 1 раз в 6 мес
21, 22. По показаниям
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.