Диагностика и лечение злокачественных новообразований: Лимфома Ходжкина
 Версия: Клинические протоколы 2006-2019 (Беларусь)
Версия: Клинические протоколы 2006-2019 (Беларусь)
Болезнь Ходжкина [лимфогранулематоз] (C81)
Онкология
Общая информация
Краткое описание
ПОСТАНОВЛЕНИЕ
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ
РЕСПУБЛИКИ БЕЛАРУСЬ
6 июля 2018 г. № 60
Об утверждении клинического протокола «Алгоритмы диагностики и лечения злокачественных новообразований»
На основании подпункта 8.3 пункта 8 Положения о Министерстве здравоохранения Республики Беларусь, утвержденного постановлением Совета Министров Республики Беларусь от 28 октября 2011 г. № 1446 «О некоторых вопросах Министерства здравоохранения и мерах по реализации Указа Президента Республики Беларусь от 11 августа 2011 г. № 360», Министерство здравоохранения Республики Беларусь
ПОСТАНОВЛЯЕТ:
1. Утвердить прилагаемый клинический протокол «Алгоритмы диагностики и лечения злокачественных новообразований».
2. Начальникам главных управлений по здравоохранению областных исполнительных комитетов, председателю комитета по здравоохранению Минского городского исполнительного комитета, руководителям государственных организаций, подчиненных Министерству здравоохранения Республики Беларусь, обеспечить проведение диагностики, лечение и профилактику заболеваний в соответствии с клиническим протоколом.
3. Настоящее постановление вступает в силу после его официального опубликования.
Министр В.А.Малашко
УТВЕРЖДЕНО
Постановление
Министерства здравоохранения
Республики Беларусь
06.07.2018 № 60
КЛИНИЧЕСКИЙ ПРОТОКОЛ «Алгоритмы диагностики и лечения злокачественных новообразований»
ГЛАВА 39
ЛИМФОМА ХОДЖКИНА (С81)
Классификация
ГЛАВА 1
ОБЩИЕ СВЕДЕНИЯ О TNM КЛАССИФИКАЦИИ
Система TNM для классификации злокачественных опухолей была разработана французом Р. Denoix в 1943–1952 гг. В 1953 г. Комитет по номенклатуре опухолей и статистике, организованный UICC, и Международная комиссия по стадированию рака достигли соглашения по классификации анатомической распространенности опухолей на основе системы TNM. В 1954 г. Международный противораковый союз (UICC) создает Комитет по клинической классификации и прикладной статистике, который в 1958 г. публикует первые рекомендации по клинической классификации рака молочной железы и гортани.
В результате многолетней деятельности Комитета в 1968 г. издается первая редакция TNM классификация злокачественных опухолей. По мере разработки классификации для новых локализаций опухолей и уточнения более ранних рекомендаций в 1974, 1978, 1987, 1997, 2002 и 2009 гг. публикуются 2-я, 3-я, 4-я, 5-я, 6-я и 7-я редакции.
Настоящая (8-я) редакция правил классификации и стадирования полностью соответствуют 8-й редакции руководства по стадированию рака и одобрена всеми национальными TNM комитетами.
В данном руководстве используются морфологические формы злокачественных новообразований в соответствии с классификацией МКБ-О-3, адаптированной под МКБ-10 (проставление кодов врачом-патологом в морфологическом заключении обязательно).
UICC признает необходимость постоянства TNM классификации в течение определенного периода времени, необходимого для накопления данных. Поэтому классификация не должна изменяться до тех пор, пока не будут сделаны крупные достижения в диагностике и лечении злокачественных опухолей, требующие пересмотра настоящей классификации.
Общие правила системы TNM.
TNM система для описания анатомической распространенности болезни основывается на оценке 3 компонентов:
Т – распространение первичной опухоли;
N – отсутствие или наличие метастазов в регионарных лимфатических узлах и степень их поражения;
М – отсутствие или наличие отдаленных метастазов.
К этим трем компонентам добавляются цифры, указывающие на распространенность злокачественного процесса:
Т0, Т1, Т2, Т3, Т4; N0, N1, N2, N3; M0, M1.
В действительности система является «стенографическим» описанием распространенности злокачественной опухоли.
Общие правила классификации, применяемые для опухолей всех локализаций, следующие:
Для каждой локализации имеются две классификации:
Клиническая классификация, обозначаемая TNM (или cTNM). Она основывается на результатах обследования до лечения. Эти данные получают при врачебном осмотре, лучевой диагностике, эндоскопии, биопсии, хирургическом диагностическом вмешательстве и других методах обследования.
Патологическая классификация, обозначаемая pTNM. Она основана на данных обследования до лечения, дополненных или измененных в результате хирургического вмешательства и морфологического исследования. Гистологическая оценка первичной опухоли включает резецированную опухоль или биопсию, позволяющую оценить наивысшую Т категорию. Гистологическая оценка регионарных лимфатических узлов включает исследование удаленных узлов в количестве, адекватном для установления отсутствия метастазов в регионарных лимфатических узлах (pN0) и достаточном для оценки наиболее высокой pN категории. Отдаленные метастазы должны быть подтверждены при микроскопическом исследовании (рМ).
После обозначения Т, N, М и/или рТ, pN и рМ категорий они могут группироваться по стадиям. TNM классификация и стадии, установленные однажды, должны оставаться неизменными в медицинских документах. Клиническая стадия служит основой для выбора лечения, тогда как патологическая стадия обеспечивает наиболее точные данные для оценки прогноза и расчета конечных результатов.
При сомнении в правильности оценки Т, N или М категории должно быть выбрано меньшее значение категории, (т.е. меньшее распространение опухоли).
В случае множественных опухолевых очагов в органе должна классифицироваться опухоль с более высокой Т категорией, а в скобках указываться множественность (т) или количество опухолей, например: Т2(т) или Т1(5). При одновременном поражении парных органов каждая опухоль должна классифицироваться отдельно. При опухолях печени, яичников и фаллопиевой трубы множественные очаги поражения являются критерием Т классификации.
Выявление второй опухоли в одном органе в течение 2 месяцев с момента выявления первой нужно расценивать как синхронное поражение.
TNM категории и стадия могут подразделяться или объединяться для клинических и научных целей (например, любые Т, N или М могут быть разбиты на подгруппы). Однако рекомендованные основные обозначения не должны изменяться.
Анатомические области и локализации.
Локализации в этой классификации обозначаются кодовым номером Международной классификации онкологических болезней.
TNM/pTNM классификация.
Используются следующие общие определения:
Т/рТ – первичная опухоль:
TX/рTX – первичная опухоль не может быть оценена;
Т0/рТ0 – нет доказательств первичной опухоли;
Tis/pTis – рак «in situ»;
Т1/рТ1, Т2/рТ2, ТЗ/рТЗ, Т4/рТ4 – размер или местное распространение опухоли в порядке увеличения.
N/pN – регионарные лимфатические узлы:
Nx/pNx – регионарные лимфатические узлы не могут быть оценены;
N0/pN0 – отсутствуют метастазы в регионарных лимфоузлах;
Nl/pNl, N2/pN2, N3/pN3 – возрастающее поражение регионарных лимфатических узлов.
Непосредственное распространение первичной опухоли на лимфатические узлы классифицируется как метастазы в лимфатических узлах. Метастаз в любом лимфоузле, не относящемся к регионарному, расценивается как отдаленный метастаз.
Опухолевый узел в области регионарных лимфатических узлов, не имеющий гистологических признаков лимфоузла, классифицируется как метастаз в регионарном лимфатическом узле, если имеет форму и ровный контур лимфатического узла. Опухолевый узел с неровным контуром классифицируется в рТ категории.
Когда размер является критерием pN классификации, производится измерение метастатического очага, а не всего лимфатического узла.
Случаи с микрометастазами, когда размеры метастазов не превышают 0,2 см, могут обозначаться добавлением «(mi)», например: pNl(mi) или pN2(mi).
М/рМ – отдаленные метастазы:
МХ/рМХ – отдаленные метастазы не могут быть оценены;
М0/рМ0 – нет отдаленных метастазов;
М1/рМ1 – имеются отдаленные метастазы;
Категория М может быть в дальнейшем специфицирована в соответствии со следующими обозначениями (таблица 1.1):
Таблица 1.1
| Легкие | PUL | Костный мозг | MAR |
| Кости | OSS | Плевра | PLE |
| Печень | HEP | Брюшина | PER |
| Головной мозг | BRA | Надпочечники | ADR |
| Лимфоузлы | LYM | Кожа | SKI |
| Другие | ОТН |
Подразделения TNM
Главные категории в классификации могут иметь подразделения, придающие критерию большую специфичность (например; Tla, lb или N2a, 2b).
Сигнальный лимфоузел
Это первый лимфоузел, получающий лимфу из первичной опухоли. Если в нем имеется метастаз, то и другие лимфоузлы могут быть поражены. Если этот лимфоузел не поражен, то и наличие метастазов в других узлах маловероятно. Иногда встречаются более одного сигнальных лимфоузлов.
При оценке сигнального лимфоузла применяются следующие определения:
Главные категории в классификации могут иметь подразделения, придающие критерию большую специфичность (например; Tla, lb или N2a, 2b).
Сигнальный лимфоузел
Это первый лимфоузел, получающий лимфу из первичной опухоли. Если в нем имеется метастаз, то и другие лимфоузлы могут быть поражены. Если этот лимфоузел не поражен, то и наличие метастазов в других узлах маловероятно. Иногда встречаются более одного сигнальных лимфоузлов.
При оценке сигнального лимфоузла применяются следующие определения:
- pNX(sn) – сигнальный узел не может быть оценен; pN0(sn) – нет поражения сигнального узла;
- pN1(sn) – есть поражение сигнального узла.
Отдельные опухолевые клетки
Отдельные опухолевые клетки (ITC) представляют собой единичные опухолевые клетки или маленькие кластеры клеток не более 0,2 мм в наибольшем измерении. ITC обычно не демонстрируют метастатической активности (пролиферацию или реакцию стромы) или инвазии стенок сосудистого или лимфатического синуса. Случаи с ITC в лимфатических узлах или отдаленных органах и тканях должны классифицироваться как N0 или М0 соответственно.
Это же применимо и к случаям, когда наличие опухолевых клеток или их компонентов подтверждается неморфологическими исследованиями, такими как проточная морфометрия или анализ ДНК.
Случаи с ITC должны анализироваться отдельно.
Классификация ITC:
- pN0 – гистологически не выявляются метастазы в регионарных лимфатических узлах, не проводились исследования по выявлению ITC;
- pN0(i-) – гистологически нет метастазов в регионарных лимфатических узлах, негативные морфологические данные по выявлению ITC;
- pN0(i+) – гистологически нет метастазов в регионарных лимфатических узлах, позитивные морфологические данные по выявлению ITC;
- pN0(mol-) – гистологически нет метастазов в регионарных лимфатических узлах, негативные неморфологические данные по выявлению ITC;
- pN0 (mol+) – гистологически нет метастазов в регионарных лимфатических узлах, неморфологическими методами выявляются ITC.
При исследовании ITC в сигнальном лимфоузле к обозначениям выше приведенной классификации в скобках указывается «(sn)», например: pN0(i+) (sn).
Отдельные опухолевые клетки, выявленные в костном мозгу морфологическими методами, классифицируются аналогично схеме для N, например: pM0(i+), а неморфологическими – pM0(mol+).
Гистопатологическая дифференцировка.
Это стадирование позволяет оценить степень агрессивности опухолей некоторых гистологических типов и может влиять на прогноз и выбор лечения.
Для большинства локализаций выделяется 4 степени дифференцировки опухолей:
- G1 – хорошо дифференцированные;
- G2 – умеренно дифференцированные;
- G3 – низко дифференцированные;
- G4 – недифференцированные.
При наличии различных степеней дифференцировки в опухоли указывается наименее благоприятная степень.
Саркомы костей и мягких тканей классифицируется также с использованием градаций «высокая степень» и «низкая степень» дифференцировки.
Для некоторых форм рака (молочной железы, тела матки, печени) рекомендуются специальные системы стадирования по степеням.
Дополнительные дескрипторы.
Для идентификации особых случаев в TNM/pTNM используются символы m, у, r, а.
Хотя они не влияют на группировку по стадиям, но указывают опухоли, которые должны анализироваться отдельно:
- m – используется для обозначения множественных опухолей одной локализации;
- у – в тех случаях, когда классификация приводится в течение или после проведения комбинированного (многокомпонентного) лечения, cTNM или pTNM категория обозначается префиксом «у», например: ycTNM или ypTNM. При оценке распространения опухоли до начала комбинированного лечения символ «у» не исключается;
- r – рецидив опухоли после радикального лечения при классификации обозначается префиксом «r» (rcTNM или rpTNM);
- а – применяется для обозначения классификации опухолей, впервые выявленных при аутопсии.
Необязательные дескрипторы.
L – инвазия лимфатических сосудов
Классифицируется как LX, L0 и L1.
V – инвазия вен
Классифицируется как VX, VO, VI (микроскопическая инвазия) и V2 (макроскопическая инвазия). Макроскопическое вовлечение стенки вены при отсутствии опухоли в просвете сосуда классифицируется как V2.
С-фактор
С-фактор или «фактор надежности» отражает достоверность классификации с учетом использованных методов диагностики. Его использование не является обязательным.
Определения С-фактора:
- С1 – данные стандартных диагностических методов (осмотр, пальпация, рентгенологическое исследование, эндоскопическое исследование),
- С2 – данные, полученные при использовании специальных диагностических методов (рентгенологическое исследование в специальных проекциях, томография, компьютерная томография, ультразвуковое исследование, лимфография, ангиография, сцинтиграфия, магнитно-резонансная томография, ПЭТ/КТ, эндоскопия, биопсия, цитологическое исследование);
- С3 – данные хирургического диагностического вмешательства, включая биопсию и цитологическое исследование;
- С4 – данные, полученные после радикальной операции и гистологического исследования удаленного препарата;
- С5 – данные патологоанатомического вскрытия.
Степени С-фактора могут использоваться при описании категорий Т, N и М (например: Т3С2, N2C1, М0С2).
Клиническая классификация TNM соответствует CI, С2 и С3 степеням, тогда как pTNM эквивалентна С4.
Классификация остаточных опухолей (R)
TNM/pTNM классификация описывает анатомическую распространенность опухоли без рассмотрения вопросов лечения. R-классификация описывает статус опухоли после лечения. Она отражает эффект лечения и является прогностическим фактором. При R- классификации оценивается не только первичная опухоль, но и остающиеся отдаленные метастазы.
Эта классификация может применяться после хирургического лечения, лучевой или химиотерапии, а также после комбинированного лечения. После консервативного лечения остаточная опухоль оценивается клиническими методами. После хирургического лечения R-классификация требует тесного сотрудничества хирурга и морфолога.
Случаи с макроскопически определяемой остаточной опухолью (R2) могут подразделяться на R2a (без микроскопического подтверждения) и R2b (микроскопически подтвержденные).
R0 группа может включать пациентов как с М0, так и с Ml. В последнем случае отдаленные метастазы, как и первичная опухоль, должны быть полностью удалены. Трудности с R-классификацией могут возникнуть при удалении опухоли по частям, а не «en blok». В таких случаях уместна категория RX.
Наличие микроскопически определяемой инвазивной опухоли по линии резекции классифицируется как R1, а в случае неинвазивной карциномы – R1 (is).
Группировка по стадиям.
Комбинация всех значений дескрипторов TNM позволяет получить 24 категории TNM, описывающие распространенность опухоли. Для табличного представления данных и анализа эти категории объединяются в ограниченное количество групп – стадий. Каждая стадия более или менее однородна по прогнозу и критерию выживаемости относящихся к ней пациентов.
Карцинома «in situ» относится к стадии 0, а опухоли с отдаленными метастазами – к стадии IV (за исключением некоторых локализаций, например, папиллярного и фолликулярного рака щитовидной железы).
Для патологической стадии необходимо морфологическое исследование достаточного количества тканей, позволяющее оценить наибольшее значение Т и N. Если же имеется морфологическое подтверждение отдаленных метастазов, то и классификация (рМ1) и стадия являются патологическими.
Термин «стадия» употребляется только для комбинаций Т, N, М или рТ, pN или рМ категорий. Необходимо избегать выражений типа «Т стадия» или «N стадия»
ЛИМФОМА ХОДЖКИНА (С81)
39.2. Гистологическая классификация
Диагноз должен быть установлен гистологически. Только конкретное описание диагностических клеток Березовского–Рид–Штернберга и клеток сопровождения позволяет считать диагноз бесспорным и окончательным. Не являются основанием для установления диагноза ни наличие характерной клинической картины, ни типичные данные рентгенологического исследования, ни предположительное гистологическое или цитологическое заключение. Первичная диагностика классической лимфомы Ходжкина предусматривает применение иммуногистохимической панели, включающей антитела к CD30, CD15, PAX5, CD20, EBV LMP1.
При необходимости дифференциальной диагностики классической лимфомы Ходжкина и опухолей с выраженным сходством гистологического строения, включая нодулярный тип лимфоидного преобладания лимфомы Ходжкина, анапластическую крупноклеточную неходжскинскую лимфому, лимфоматоидный Гранулематоз, медиастинальную В-крупноклеточную диффузную лимфому и В-крупноклеточную диффузную лимфому с обилием гистиоцитов и Т-лимфоцитов, основная панель может дополняться антителами к антигенам CD45, CD23, CD10, ОСТ-2, ВОВ-1, ЕМА, bcl-6, ALK, CD79a, CD3, MUM1, CD68, CD57 и т.д.
Выделяют следующие морфологические варианты лимфогранулематоза (классификация опухолей лимфоидной ткани ВОЗ, 2016 г.):
39.2.1. Лимфома Ходжкина, нодулярный тип лимфоидного преобладания [9659/3].
39.2.2. Классическая лимфома Ходжкина [9650/3]:
классическая лимфома Ходжкина, лимфоидное преобладание [9651/3];
классическая лимфома Ходжкина, нодулярный склероз [9663/3];
классическая лимфома Ходжкина, смешанно-клеточная [9652/3];
классическая лимфома Ходжкина, лимфоидное истощение [9653/3].
39.3. Клиническое стадирование
Цель стадирования – распределение пациентов на Группы, требующие различной интенсивности лечения.
Клиническое стадирование основано на данных анамнеза, клинического обследования, биопсии и результатов обследования, полученных с помощью методов визуализации.
Для правильного стадирования необходимо различать лимфатическое (нодальное) и экстралимфатическое (экстранодальное) проявление болезни.
39.3.1. К лимфатическим структурам относятся:
лимфатические узлы;
Вальдейерово кольцо;
селезенка;
аппендикс;
вилочковая железа;
Пейеровы бляшки.
39.3.2. Экстралимфатическое (экстранодальное) проявление – поражение нелимфатических структур и тканей, обозначается символом Е.
39.3.3. Классификация по стадиям (TNM-классификация, 8-е издание) (таблица 39.2)
Таблица 39.2. Классификация по стадиям
|
Стадия I
|
Поражение одной лимфатической зоны или лимфатической структуры (I)
Локализованное поражение одного экстралимфатического органа (IE).
|
|
Стадия II
Стадия II Bulky |
Поражение двух и более лимфатических зон по одну сторону диафрагмы (II).
Локализованное поражение одного экстралимфатического органа и его регионарных лимфатических узлов с или без поражения других лимфатических зон по ту же сторону диафрагмы (IIE). Стадия II с наличием одного опухолевого образования размером более 10 см в наибольшем измерении или размером более трети поперечника Грудной клетки на уровне Th 5-6 по данным КТ. |
|
Стадия III
|
Поражение лимфатических узлов по обе стороны диафрагмы (III), которое может сочетаться с поражением селезенки (IIIS).
|
|
Стадия IV
|
Диссеминированное (многофокусное) поражение одного или нескольких экстралимфатических органов с или без поражения лимфатических узлов. Изолированное поражение экстралимфатического органа с поражением лимфатических узлов по одну или обе стороны диафрагмы.
|
Симптомы А и Б.
Каждая стадия должна быть разделена на А и Б в зависимости от отсутствия (А) или наличия (Б) общих симптомов. К ним относятся:
- Необъяснимая потеря массы тела более чем на 10 % за последние 6 месяцев.
- Необъяснимые подъемы температуры выше 38°С в течение 3 дней.
- Профузные ночные поты.
Эпидемиология
39.1. Основные статистические показатели (таблица 39.1)
Таблица 39.1. Основные статистические показатели
|
Показатель
|
Число
|
|
|
2011
|
2016
|
|
|
Число вновь выявленных случаев заболевания
|
274 | 254 |
|
Заболеваемость на 100 000 населения (грубый интенсивный показатель)
|
2,9 | 2,7 |
|
Диагноз установлен в I стадии заболевания (% к вновь выявленным случаям)
|
7,7 | 7,5 |
|
Диагноз установлен в II стадии заболевания (% к вновь выявленным случаям)
|
55,5 | 44,1 |
|
Диагноз установлен в III стадии заболевания (% к вновь выявленным случаям)
|
23 | 22 |
|
Диагноз установлен в IV стадии заболевания (% к вновь выявленным случаям)
|
6,6 | 16,1 |
|
Прожили менее года с момента установления диагноза из числа заболевших в предыдущем году (одногодичная летальность в %)
|
9,8 | 7,2 |
|
Умерло от злокачественных новообразований
|
81 | 61 |
|
Смертность на 100 000 населения Грубый интенсивный показатель
|
0,9
|
0,6 |
|
Отношение смертности к заболеваемости в % (интенсивные показатели)
|
31 | 22,2 |
|
Число пациентов, состоящих на учете на конец года
|
4283 | 4530 |
|
Из них состоящих на учете 5 и более лет, %
|
72,6 | 75,8 |
Диагностика
39.4. Диагностические мероприятия
Обычно необходимы следующие диагностические мероприятия:
- детальный сбор анамнеза с особым вниманием к наличию симптомов интоксикации, «алкогольных» болей (появление болей в зонах поражения после приема даже небольшого количества алкоголя) и темпу роста лимфатических узлов.
- тщательное пальпаторное обследование всех Групп периферических лимфатических узлов (подчелюстных, шейно-надключичных, подключичных, подмышечных, подвздошных, паховых, подколенных, бедренных, локтевых, затылочных), печени, селезенки.
- осмотр ЛОР-врача (небные миндалины, носоглотка).
- эксцизионная биопсия. Для исследования берется самый ранний из появившихся лимфатических узлов, который удаляется полностью. При удалении узел не должен быть поврежден механически. Нежелательно для гистологического исследования использовать паховые лимфатические узлы, если имеются вовлеченные в процесс другие Группы лимфатических узлов. Пункционная биопсия для начальной диагностики недостаточна.
- УЗИ: всех Групп периферических лимфатических узлов, включая шейные, над- и подключичные, подмышечные, паховые, бедренные; брюшной полости и таза с исследованием печени, селезенки, парааортальных, подвздошных лимфатических узлов.
- компьютерная томография шеи, Грудной клетки, брюшной полости и таза с болюсным внутривенным контрастным усилением.
- ПЭТ/КТ шеи, Грудной клетки, брюшной полости и таза и/или МРТ с диффузионно-взвешенным исследованием (МРТ-ДВИ) шеи, Грудной клетки, брюшной полости и таза.
- группа крови и резус-фактор.
- общий анализ крови, включая содержание эритроцитов, гемоглобина, тромбоцитов, лейкоцитарную формулу, СОЭ.
- биохимическое исследование крови (креатинин, мочевина, билирубин, общий белок, АСТ, АЛТ, ЛДГ, щелочная фосфатаза).
- анализ крови на наличие ВИЧ-инфекции, гепатита В и С.
- функция внешнего дыхания (если предполагается применение блеоцина).
- уровень гормонов щитовидной железы при поражении шейных лимфатических узлов и планировании облучения области шеи.
- УЗИ сердца (определение фракции выброса левого желудочка)
- тест на наличие беременности, если женщина находится в детородном возрасте.
При формулировке окончательного диагноза обязательно указываются стадия, морфологический вариант опухоли, перечисляются все зоны лимфатического поражения, зона массивного поражения (bulky disease), наличие или отсутствие В-симптомов, вовлечение селезенки и экстранодальных областей.
С женщинами детородного возраста следует обсуждать вопрос о необходимости гормональной контрацепции, а так же о методах возможной гормональной защиты яичников при проведении интенсивных программ лечения (введение агонистов гонадотропин-рилизинг гормона).Так как химиотерапия и лучевая терапия потенциально могут привести к необратимой стерильности пациента, необходимо обсуждать вопрос о возможной криоконсервации спермы/яйцеклеток и хирургической транспозиции яичников из зоны планируемого облучения.
39.4.1. Факторы риска
Наиболее значимыми факторами риска, определяющими прогноз болезни, являются:
1. СОЭ≥50 мм/ч при отсутствии симптомов интоксикации (А); ≥30 мм/ч при наличии симптомов интоксикации (Б);
2. поражение 3 и более лимфатических областей (рисунок 39.1.).
3. массивное поражение средостения (МТИ≥0,33, определяемый как отношение максимальной ширины средостения к максимальной ширине Грудной клетки на уровне 5– 6-го Грудных позвонков) или наличие увеличенных лимфатических узлов >10 см (bulky disease) при любой локализации.
4. экстранодальное поражение;
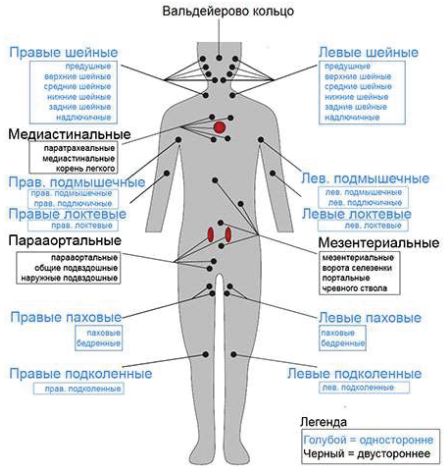
Рисунок 39.1 – Зоны (мелким шрифтом) для определения стадии лимфомы и области (крупным шрифтом) для определения прогностической Группы
Лечение
39.5. Общие принципы лечения пациентов с лимфомой Ходжкина
Лечение проводится с учетом стадии заболевания и факторов риска. Программы лечения классической лимфомы Ходжкина и варианта нодулярного типа лимфоидного преобладания отличаются.
Общие принципы лечения классической лимфомы Ходжкина
Лечение пациентов классической лимфомой Ходжкина всегда начинается с химиотерапии. После 2 курсов с целью оценки эффекта и определения дальнейшей терапевтической практики выполняется ПЭТ/КТ.
Стандартным режимом химиотерапии для первичного лечения классической лимфомы Ходжкина является схема ABVD, при ее неэффективности – схема BEACOPPesc.
39.5.1. Схема ABVD:
Доксорубицин 25 мг/м2 внутривенно в течение 20–30 мин, дни 1-й и 15-й.
Блеомицин 10 мг/м2 внутривенно в течение 10 мин, дни 1-й и 15-й.
Винбластин 6 мг/м2 внутривенно струйно, дни 1-й и 15-й.
Дакарбазин 375 мг/м2 внутривенно в течение 15–30 мин, дни 1-й и 15-й.
Начало следующего курса на 29-й день после начала предшествующего курса лечения.
39.5.2. Схема BEACOPP-escalated:
Циклофосфамид 1250 мг/м2 внутривенно в течение 60 мин, день 1-й.
Доксорубицин 35 мг/м2 внутривенно в течение 20–30 мин, день 1-й.
Этопозид 200 мг/м2 внутривенно в течение 60 мин, дни 1-й, 2-й и 3-й.
Прокарбазин 100 мг/м2 внутрь, дни 1–7-й.
Преднизолон 40 мг/м2 внутрь, дни 1–14-й.
Винкристин 1,4 мг/м2 внутривенно струйно, день 8-й (максимально 2 мг).
Блеомицин 10 мг/м2 внутривенно в течение 10–15 мин, день 8-й.
Гранулоцитарный колониестимулирующий фактор (G-CSF) подкожно в 8–14-й день.
Начало очередного курса через 7 дней после окончания приема преднизолона или на 22-й день от начала предыдущего курса.
Применение Гранулоцитарного колониестимулирующего фактора при использовании BEACOPP-esc. является обязательным, при использовании схемы ABVD – при необходимости. Применение эритропоэтина не показано. С целью коррекции анемии необходимо проводить гемотрасфузии.
После завершения химиотерапии у пациентов с ранними стадиями без факторов риска проводится облучение зон исходного поражения. У пациентов с распространенными стадиями и ранними стадиями с неблагоприятным прогнозом облучаются либо зоны массивного исходного поражения, либо ПЭТ – позитивные зоны.
При необходимости применения лучевой терапии используются РОД в диапазоне 1,8–2,0 Гр, облучение проводится 5 раз в неделю, при определении объемов облучения используется концепция IFRT (involved fild radiation therapy – лучевая терапия исходно пораженных зон) либо ISRT (involved site radiation therapy – лучевая терапия исходно пораженных мест (очагов): лимфатических узлов и/или внутренних органов).
ISRT следует использовать только в том случае, когда при постановке диагноза и определении степени распространенности опухоли использовалась ПЭТ/КТ. При описании очагов опухолевого поражения должна быть четко указана анатомическая локализация очагов поражения, их количество и максимальные размеры в 3-х измерениях, а при необходимости – соотношение очагов поражения с близлежащими анатомическими структурами (например, с костями).
Объемы облучения при использовании ISRT:
GTV (gross tumor volume) – определяемый на основании клинических данных и данных инструментального исследования (ПЭТ/КТ, МРТ, УЗИ и т.д.) объем очагов опухолевого поражения, диагностированный как до, так и после (при прогрессировании после ПХТ либо хирургического лечения) проведения ПХТ либо хирургического лечения.
CTV (clinical target volume)
a. При поражении лимфоузлов – GTV + 1 см в осевом направлении и 1–4 см в кранио-каудальном направлении вдоль путей лимфооттока. В случае расстояния между пораженными лимфоузлами <5 см их можно включать в 1 объем, если расстояние между пораженными лимфоузлами ≥5 см – следует использовать разные объемы облучения. При облучении медиастинальных лимфоузлов после окончания ПХТ Границы CTV не должны превышать боковые Границы средостения. Лимфоузлы корней легких при отсутствии их поражения в CTV не включаются.
b. При экстранодальном поражении – в большинстве случаев в CTV включается весь пораженный орган (например желудок, слюнная железа, щитовидная железа и т.д.). Для орбиты, молочной железы, мягких тканей, костей и локализованного облучения кожи после проведения ПХТ возможно включение в CTV части пораженного органа.
PTV (planning target volume) – CTV + 0,5 см, однако при поражении средостения или верхних отделов брюшной полости PTV может быть увеличен до 1,5–2 см в зависимости от смещения опухоли при дыхании.
При использовании IFRT в клинический объем облучения (CTV) включаются все исходно пораженные зоны.
Оценка эффекта лечения
Оценку эффекта проводят по данным ПЭТ/КТ с использованием критериев Довиль. Эта пятибалльная шкала учитывает различия в накоплении радиоактивного фтора в различных участках тела: 1-нет накопления в ранее определяемых зонах поражения, 2-накопление в ранее определяемых зонах поражения < чем накопление в просвете дуги аорты, 3-накопление в ранее определяемой зоне поражения > чем накопление в просвете дуги аорты, но < чем накопление в печени, 4 – накопление в ранее определяемой зоне поражения > чем накопление в печени, 5-существенное увеличение накопления в ранее определяемых зонах поражения или появление ранее неопределяемых очагов гиперметаболизма.
39.6. Лечение пациентов с лимфомой Ходжкина в зависимости от стадии и факторов риска.
39.6.1. Лечение пациентов с ранними стадиями (I–II) без факторов риска.
Программа лечения.
Лечение начинают с химиотерапии по схеме ABVD. После проведения 2 курсов через 2 недели выполняется ПЭТ/КТ:
- при критерии Довиль 1–2 проводится еще 1 курс ABVD (суммарно до 3), затем лучевая терапия.
- при критерии Довиль 3–4 проводится еще 2 курса ABVD (суммарно до 4) и лучевая терапия.
- при критерии Довиль 5 выполняется биопсия. При позитивном результате – мультидисциплинарный консилиум и решение вопроса о дальнейшей терапевтической тактике. При негативном – подход, аналогичный критерию Довиль 3–4 (рисунок 39.2.).
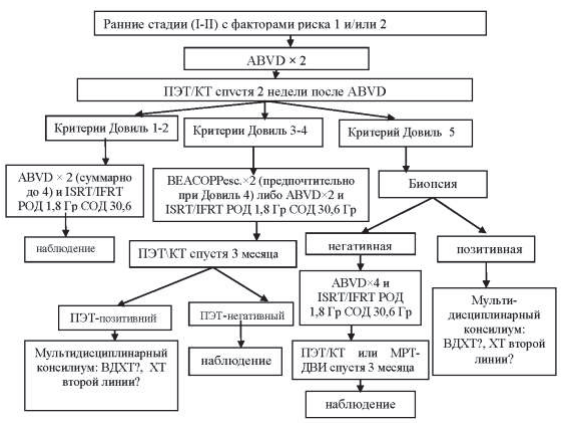
Рисунок 39.2 – Алгоритм лечения пациентов с ранними стадиями (I–II) без факторов риска
39.6.2. Лечение пациентов с ранними стадиями (I–II) и факторами риска 1 и/или 2 (СОЭ≥50 мм/ч при отсутствии симптомов интоксикации (А); ≥30 мм/ч при наличии симптомов интоксикации (Б) и/или поражение 3 и более лимфатических областей).
Программа лечения.
Лечение начинают с химиотерапии по схеме ABVD. После проведения 2 курсов через 2 недели выполняется ПЭТ/КТ:
- при критерии Довиль 1–2 проводится еще 2 курса ABVD (суммарно до 4), затем лучевая терапия.
- при критерии Довиль 3–4 проводится еще 2 курса ABVD (суммарно до 4) или 2 курса BEACOPP esc и лучевая терапия.
-
при критерии Довиль 5 выполняется биопсия. При позитивном результате – мультидисциплинарный консилиум и решение вопроса о дальнейшей терапевтической тактике. При негативном – 4 курса ABVD (суммарно до 6), затем лучевая терапия.
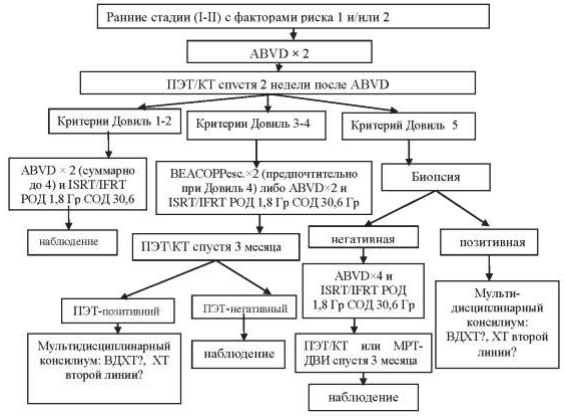
Рисунок 39.3 – Алгоритм лечения пациентов с ранними стадиями (I–II) и факторами риска 1 и/или 2
39.6.3. Лечение пациентов с ранними стадиями (I–II) и факторами риска 3 и/или 4 (массивное поражение либо экстранодальное поражение).
Программа лечения
Лечение начинают с химиотерапии по схеме ABVD. После проведения 2 курсов через 2 недели выполняется ПЭТ/КТ:
- при критерии Довиль 1–2 проводится еще 2 курса ABVD (суммарно до 4), затем лучевая терапия.
- при критерии Довиль 3–4 пациентам проводится 2 курса BEACOPP esc,
- или 2 курса ABVD (суммарно до 4) и лучевая терапия. Спустя 3 месяца выполняется ПЭТ/КТ. При негативном результате пациенты далее наблюдаются, при позитивном – мультидисциплинарным консилиумом решается вопрос о дальнейшей терапевтической тактике.
- при критерии Довиль 5 выполняется биопсия. При позитивном результате – мультидисциплинарный консилиум и решение вопроса о дальнейшей терапевтической тактике.
При негативном – подход, аналогичный критерию Довиль 3–4 (рисунок 39.4).
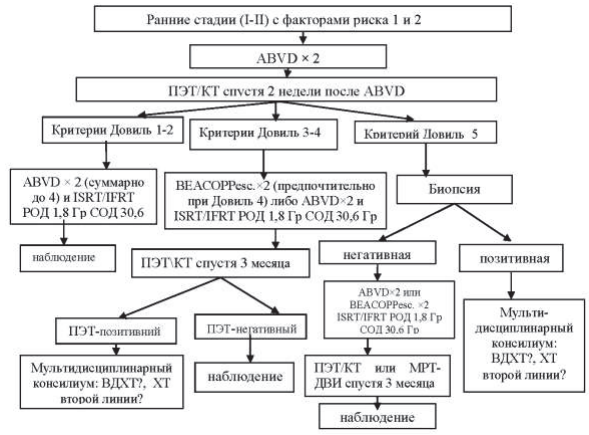

Рисунок 39.4 – Алгоритм лечения пациентов с ранними стадиями (I–II) и факторами риска 3 и 4
39.6.4. Лечение пациентов с распространенными стадиями (III–IV).
Программа лечения.
Лечение начинают с химиотерапии по схеме ABVD. После проведения 2 курсов через 2 недели выполняется ПЭТ/КТ:
- при критерии Довиль 1–3 проводится 4 курса ABVD (суммарно до 6). Далее проводится лучевая терапия на зоны (IFRT) или очаги (ISRT) исходного массивного поражения.
- при критерии Довиль 4–5 проводится либо еще 2 курса ABVD (суммарно до 4) с ПЭТ/КТ рестадированием через 2 недели, либо переходят на режим BEACOPP esc. 4 курса также с ПЭТ/КТ рестадированием через 2 недели.
В первом случае (продолжение лечения по схеме ABVD):
- если достигнут критерии Довиль 1–3, пациенты получают еще 2 таких курса (суммарно до 6) и лучевую терапию на зоны (IFRT) или очаги (ISRT) исходного массивного поражения.
- если сохраняется критерии Довиль 4–5, пациентам выполняется биопсия. При позитивном результате – мультидисциплинарный консилиум. При негативном результате биопсии – 2 курса ABVD (суммарно до 6) затем проводится лучевая терапия на зоны (IFRT) или очаги (ISRT) исходного массивного поражения.
Во втором случае (переход на режим BEACOPP esc.):
- если достигнут критерии Довиль 1–3, пациенты получают лучевую терапию на зоны (IFRT) или очаги (ISRT) исходного массивного поражения.
- если сохраняется критерии Довиль 4–5, пациентам выполняется биопсия. При позитивном результате – мультидисциплинарный консилиум (рисунок 39.5.). При негативном результате биопсии – лучевая терапия на зоны (IFRT) или очаги (ISRT) исходного массивного поражения (или на ПЭТ-позитивные области). Лучшие результаты лечения у данной категории пациентов наблюдаются при использовании режима BEACOPP esc. Однако при выборе режима химиотерапии необходимо учитывать общее состояние пациента и риск возможных осложнений, т.е. провести точную оценку соотношения польза/вред.
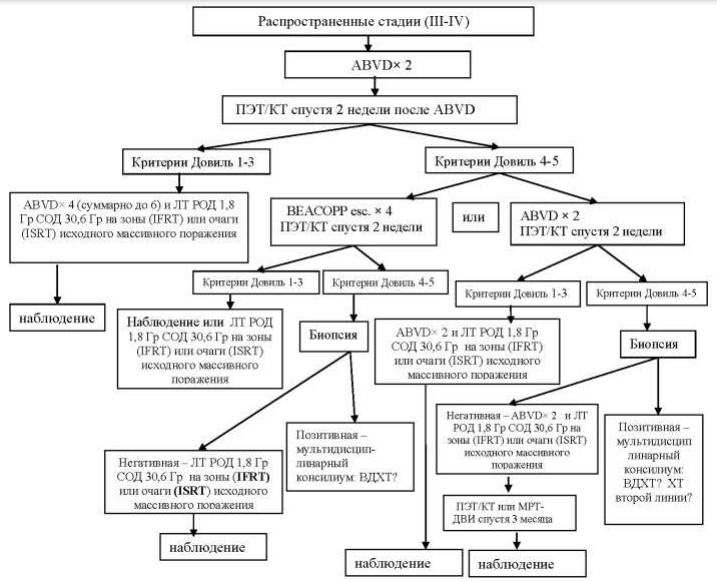
Рисунок 39.5 – Алгоритм лечения пациентов с распространенными стадиями (III–IV)
39.6.5. Лечение пациентов старше 65 лет
Выбор тактики лечения пожилых пациентов должен проводиться с учетом переносимости самой терапии и сохранения качества жизни пациента.
В целом, терапевтический подход у пациентов без выраженных функциональных нарушений должен строиться соответственно распространенности опухолевого процесса и наличию факторов риска, как и у молодых пациентов. Для химиотерапии у этих пациентов предпочтителен режим ABVD, обладающий высокой эффективностью и приемлемой токсичностью. После 2 курсов, при необходимости продолжения химиотерапии до 6 курсов из режима ABVD исключают блеомицин (режим AVD). С целью снижения риска кардиологических осложнений в режиме ABVD возможна замена доксорубицина митоксантроном (доксорубицин 50 мг/м2 = митоксантрон 12мг/м2).
Лучевая терапия у пожилых пациентов может быть также методом выбора, если имеются противопоказания к химиотерапии.
У пациентов с выраженными функциональными нарушениями в качестве альтернативных режимов химиотерапии могут использоваться режимы CVPP, ChVPP, COРP/АBV.
39.6.5.1. Схема CVPP:
Циклофосфамид 600 мг/м2 внутривенно в течение 60 мин, день 1-й и 8-й.
Винбластин 6 мг/м2 внутривенно, день 1-й и 8-й.
Прокарбазин 100 мг/м2 внутрь, день 1–14-й.
Преднизолон 40 мг/м2 внутрь, день 1–14-й.
Лечение возобновляется на 29-й день.
39.6.5.2. Схема ChVPP:
Хлорамбуцил (лейкеран) 6 мг/м2 внутрь, день 1–14-й.
Винбластин 6 мг/м2 внутривенно, день 1-й и 8-й.
Прокарбазин 100 мг/м2 внутрь, день 1–14-й.
Преднизолон 40 мг/м2 внутрь, день 1–14-й.
Лечение возобновляется на 29-й день.
39.6.5.3. Схема COРP/АBV:
Циклофосфамид 600 мг/м2 внутривенно в течение 60 мин, день 1-й.
Винкристин 1,4 мг/м2 (не более 2 мг) внутривенно, день 1-й.
Прокарбазин 100 мг/м2 внутрь, день 1–7-й.
Преднизолон 40 мг/м2 внутрь, день 1–14-й.
Доксорубицин 25 мг/м2 внутривенно в течение 20–30 мин, день 8-й.
Блеомицин 10 мг/м2 внутривенно в течение 10 мин, день 8-й.
Винбластин 6 мг/м2 внутривенно струйно, день 8-й.
Лечение возобновляется на 29-й день.
Варианты лечения соматически отягощенных пациентов должны обсуждаться индивидуально.
39.7. Лимфома Ходжкина и беременность
При выявлении лимфомы Ходжкина во время беременности для стадирования предпочтительно использовать УЗИ (периферические лимфатические зоны, органы брюшной полости) и МРТ всего тела.
При бессимптомном течении болезни в первом триместре беременности пациентки наблюдаются. Начало лечения может быть отложено до начала второго триместра.
Режимом выбора для лечения лимфомы Ходжкина на фоне беременности в течение второго и третьего триместра является режим ABVD. Возможно так же использование винбластина и дакарбазина в режиме монотерапии. Применения более интенсивных режимов химиотерапии, таких как BEACOPP, нежелательно. За месяц до родоразрешения химиотерапия прекращается.
При диагностировании лимфомы Ходжкина в III или IV стадии болезни в первом триместре беременности, когда требуется срочное начало лечения, решается вопрос о прерывании беременности консилиумом врачей онкологов и акушеров-гинекологов. При категорическом отказе от прерывания беременности пациенткой и наличии явных признаков прогрессирования болезни начинают химиотерапию винбластином в монорежиме до второго триместра.
Считается, что исход заболевания у беременных при своевременном начале лечения, такой же как и у небеременных.
39.8. Общие принципы лечения лимфомы Ходжкина с гистологическим вариантом нодулярный тип лимфоидного преобладания
Нодулярная лимфома Ходжкина с лимфоидным преобладанием является самостоятельным, редко встречающимся вариантом лимфомы Ходжкина. Характеризуется индолентным течением. В отличие от классической лимфомы Ходжкина В-лимфоциты при данном типе лимфомы Ходжкина интенсивно экспрессируют CD 20 рецепторы.
Стандартом лечения пациентов с IA стадией (без массивного поражения) с гистологическим вариантом нодулярный тип лимфоидного преобладания является лучевая терапия на вовлеченные зоны (IFRT) в РОД 1,8 Гр СОД 30,6 Гр.
Более распространенные стадии требуют проведения химиотерапии. Стандартная тактика в настоящее время не определена. Подход к терапии с соблюдением принципов лечения классической лимфомы Ходжкина уступает место использованию ритуксимаб- содержащей химиотерапии с применением режимов R-CHOP либо R-CVP, однако доказательной базы в виде проспективных исследований еще нет.
При IБ – IIА стадиях предпочтительно проведение 3 курсов химиотерапии по схеме R-CVP с последующим ПЭТ/КТ и определением дальнейшей тактики мультидисциплинарным консилиумом (продолжение химиотерапии, лучевая терапия либо наблюдение).
В остальных случаях показано проведение 6 курсов химиотерапии по схеме R-CHOP либо R-CVP.
При рецидиве заболевания обязательно должна выполняться биопсия в связи с высоким риском трансформации в неходжкинскую лимфому.
39.9. Лечение рецидивов лимфомы Ходжкина
Установление рецидива требует проведения обследования как при первичной диагностике для определения распространенности рецидива. Необходимо также получить морфологическую верификацию.
В случае рецидива (либо неэффективности терапии первой линии) лимфомы Ходжкина у соматически компенсированных пациентов в возрасте до 60 лет в случае сохранения чувствительности к химиотерапии необходимо определить возможность проведения высокодозной химиотерапии с аутологичной трансплантацией стволовых гемопоэтических клеток. Для этого пациент направляется в Республиканский центр трансплантации костного мозга.
В тех случаях, когда применение высокодозной химиотерапии с трансплантацией стволовых клеток невозможно (включая случаи отсутствия ответа на индукционную терапию), проводится химиотерапия по схемам лечения второй линии (терапия «спасения»).
Возможны и исключения – так, например, пациентам из Группы низкого риска с рецидивом болезни через несколько лет после первичного лечения, включавшего 2 цикла химиотерапии по схеме ABVD в комбинации с лучевой терапией, в качестве терапии «спасения» может быть успешно применена терапия по схеме BEACOPP escalated.
Вопрос о применении лучевой терапии при лечении рецидивов решается индивидуально.
Пациенты старше 60 лет получают лечение по индивидуальным программам с учетом физического состояния и сопутствующих заболеваний.
При рецидиве болезни после аутологичной трансплантации стволовых гемопоэтических клеток у молодых пациентов с сохранной химиочувствительностью следует обсуждать вопрос о возможности проведения аллогенной трансплантацией стволовых гемопоэтических клеток.
У пациентов с прогрессированием классической лимфомы Ходжкина на фоне двух линий химиотерапии по поводу рецидивного/рефрактерного течения в тех случаях, когда невозможно проведение высокодозной химиотерапии с трансплантацией стволовых гемопоэтических клеток, мультидисциплинарным консилиумом онкологического учреждения может быть рассмотрена возможность проведения анти-CD30 терапии брентуксимаб ведотином.
Режимы химиотерапии второй линии:
39.9.1. Схема DHAP:
Дексаметазон 40 мг внутривенно или внутрь 1, 2, 3, 4-й дни.
Цисплатин 100 мг/м2 внутривенно в 1-й день 24-часовая инфузия с пред- и постгидратацией.
Цитарабин по 2000 мг/м2 внутривенно во 2-й день 3-часовая инфузия с интервалом 12 часов (2 введения, суммарная доза 4000 мг/м2) с постгидратацией.
Интервал между курсами 3–4 недели.
39.9.2. Схема IGEV
Ифосфамид 2000 мг/м2 внутривенная 2-х часовая инфузия в 1, 2, 3, 4-й дни с пред- и постгидратацией;
Месна 2000 мг/м2 внутривенная 24-часовая инфузия в 1, 2, 3, 4-й дни, 200 мг/м2 вводится перед началом инфузии ифосфамида;
Гемцитабин 1000 мг/м2 внутривенная 30-минутная инфузия в 1-й и 4-й дни;
Винорельбин 20 мг/м2 внутривенная 6–10 минутная инфузия в 1-й день;
Преднизолон 100 мг/м2 внутривенно в 1, 2, 3, 4-й дни;
Гранулоцитарный колониестимулирующий фактор (G-CSF) дни 7–12.
Интервал между курсами 3 недели.
39.9.3. Схема ICE:
Ифосфамид 5000 мг/м2 внутривенная инфузия во 2-й день с пред- и постгидратацией;
Месна 2000 мг/м2 внутривенная 24-часовая инфузия во 2,3-й дни, 200 мг/м2 вводится перед началом инфузии ифосфамида;
Карбоплатин AUC 5 (но не более 800 мг) инфузия во 2-й день
Этопозид 100 мг/м2 внутривенная инфузия в 1, 2, 3-й дни
Интервал между курсами 3–4 недели.
39.10. Наблюдение, сроки и объем обследования
После завершения лечения контрольное обследование пациентов проводится в следующие сроки:
анамнез, физикальное обследование и общий анализ крови – каждые три месяца на первом году, каждые шесть месяцев в течение последующих трех лет, затем один раз в год;
ПЭТ-КТ по завершении программы лечения выполняется через 3 месяца по окончании лучевой терапии и спустя 6 недель после завершения курсов ПХТ в тех случаях, когда при предыдущем исследовании не был достигнут полный метаболический ответ.
МСКТ исследование может быть назначено через 6, 12 и 24 месяца после завершения лечения или по показаниям;
исследование функции щитовидной железы у пациентов, которым проводилось облучение шеи – через 12 и 24 месяца, и в дальнейшем раз в пять лет;
при облучении лимфоколлекторов, расположенных выше диафрагмы, женщинам, в пременопаузальном периоде, особенно в возрасте до 25 лет – должен проводиться скрининг на индуцированный рак молочной железы клинически, а после 40–50 лет – выполняться маммография.
Необходимо учитывать то, что риск поздних осложнений химиолучевого лечения, наиболее серьезными из которых являются индуцированные злокачественные опухоли и сердечно-сосудистая патология, увеличивается с каждым годом наблюдения. Через 15 лет смертность от таких осложнений уже превышает смертность от собственно прогрессирования лимфомы Ходжкина. Поэтому в наблюдении за пациентами, завершившими программное лечение, обязательным является участие онколога, в зависимости от характера проведенной химиотерапии (количество и доза алкилирующих препаратов, суммарная доза доксорубицина и блеоцина) и зон облучения в индивидуальном порядке определяющего целесообразность скрининга определенных форм рака и функциональных нарушений со стороны легких и сердечно-сосудистой системы.
Информация
Источники и литература
-
Постановления и приказы Министерства здравоохранения Республики Беларусь об утверждении клинических протоколов 2006-2019
- Постановления и приказы Министерства здравоохранения Республики Беларусь об утверждении клинических протоколов 2006-2019 -
-
www.minzdrav.gov.by
- www.minzdrav.gov.by -
Информация
ГЛАВА 2
ОЦЕНКА ОБЩЕГО СОСТОЯНИЯ ОНКОЛОГИЧЕСКОГО ПАЦИЕНТА
Общее состояние онкологического пациента (Performance status) рекомендовано оценивать по индексу Карновского (0–100 баллов) или шкале ECOG (0–4 балла) (таблицы 2.1, 2.2).
Таблица 2.1. Индекс Карновского
Таблица 2.1. Индекс Карновского
|
Нормальная физическая активность, пациент не нуждается в специальном уходе
|
100 баллов | Состояние нормальное, нет жалоб и симптомов заболевания |
| 90 баллов | Нормальная активность сохранена, но имеются незначительные симптомы заболевания | |
| 80 баллов | Нормальная активность возможна при дополнительных усилиях, при умеренно выраженных симптомах заболевания | |
|
Ограничение нормальной активности при сохранении полной независимости пациента
|
70 баллов | Пациент обслуживает себя самостоятельно, но не способен к нормальной деятельности или работе |
| 60 баллов | Пациент иногда нуждается в помощи, но в основном обслуживает себя сам | |
| 50 баллов | Пациенту часто требуется помощь и медицинское обслуживание | |
|
Пациент не может обслуживать себя самостоятельно, необходим уход или госпитализация
|
40 баллов | Большую часть времени пациент проводит в постели, необходим специальный уход и посторонняя помощь |
| 30 баллов | Пациент прикован к постели, показана госпитализация, хотя терминальное состояние не обязательно | |
| 20 баллов | Сильные проявления болезни, необходима госпитализация и поддерживающая терапия | |
| 10 баллов | Умирающий пациент, быстрое прогрессирование заболевания | |
| 0 баллов | Смерть |
Таблица 2.2. Оценка статуса пациента по шкале ECOG
| Оценка | |
| 0 | Пациент полностью активен, способен выполнять все, как и до заболевания (90–100 баллов по шкале Карновского) |
| 1 | Пациент неспособен выполнять тяжелую, но может выполнять легкую или сидячую работу (например, легкую домашнюю или канцелярскую работу, 70–80 баллов по шкале Карновского) |
| 2 | Пациент лечится амбулаторно, способен к самообслуживанию, но не может выполнять работу. Более 50 % времени бодрствования проводит активно – в вертикальном положении (50–60 баллов по шкале Карновского) |
| 3 | Пациент способен лишь к ограниченному самообслуживанию, проводит в кресле или постели более 50 % времени бодрствования (30–40 баллов по шкале Карновского) |
| 4 | Пациент, совершенно не способен к самообслуживанию, прикован к креслу или постели (10–20 баллов по шкале Карновского) |
Приложение
ТАБЛИЦЫ СООТВЕТСТВИЯ «СТАДИЯ-TNM» ДЛЯ РЯДА ЛОКАЛИЗАЦИЙ: ТОНКИЙ КИШЕЧНИК, АМПУЛА ФАТЕРОВА СОСКА, ТИМОМА, МЕЗОТЕЛИОМА ПЛЕВРЫ, КАРЦИНОМА МЕРКЕЛЯ КОЖИ, КОРА НАДПОЧЕЧНИКА
ТОНКИЙ КИШЕЧНИК C17
Таблица 1. Группировка по стадиям
| Стадия 0 | Tis | N0 | M0 |
| Стадия I | Т1, Т2 | N0 | M0 |
| Стадия IIА | Т3 | N0 | M0 |
| Стадия IIB | T4 | N0 | M0 |
| Стадия IIIA | Любая Т | N1 | M0 |
| Стадия IIIB | Любая Т | N2 | M0 |
| Стадия IV | Любая Т | Любая N | M1 |
АМПУЛА ФАТЕРОВА СОСКА C24.1
Таблица 2. Группировка по стадиям
| Стадия 0 | Tis | N0 | M0 |
| Стадия IA | Т1a | N0 | M0 |
| Стадия IB | Т1b, Т2 | N0 | M0 |
| Стадия IIА | Т3a | N0 | M0 |
| Стадия IIB | Т3b | N0 | M0 |
| Стадия IIIA | Т1a, Т1b, Т2, T3 | N1 | M0 |
| Стадия IIIB | Т4 | Любая N | M0 |
| Стадия IV | Любая Т | Любая N | M1 |
ТИМОМА C37, C38.1-3
Таблица 3. Группировка по стадиям
| Стадия I | T1 | N0 | M0 |
| Стадия II | T2 | N0 | M0 |
| Стадия IIIА | T3 | N0 | M0 |
| Стадия IIIB | T4 | N0 | M0 |
| Стадия IVA | Любая Т |
N1
N0, N1
|
M0
M1A
|
| Стадия IVB | Любая Т | Любая N | M1B |
МЕЗОТЕЛИОМА ПЛЕВРЫ C45.0
Таблица 4. Группировка по стадиям
| Стадия IA | T1 | N0 | M0 |
| Стадия IB | T2, T3 | N0 | M0 |
| Стадия II | T1, T2 | N1 | M0 |
| Стадия IIIА | T3 | N1 | M0 |
| Стадия IIIB | T1, T2, T3, T4 |
N1 Любая N |
M0 |
| Стадия IV | Любая Т | Любая N | M1 |
КАРЦИНОМА МЕРКЕЛЯ C44, C63.2
Таблица 5а. Группировка по стадиям клиническая
| Стадия 0 | Tis | N0 | M0 |
| Стадия I | Т1 | N0 | M0 |
| Стадия IIА | T2, Т3 | N0 | M0 |
| Стадия IIB | Т4 | N0 | M0 |
| Стадия III | Любая Т | N1, N2, N3 | M0 |
| Стадия IV | Любая Т | Любая N | M1 |
Таблица 5б. Группировка по стадиям патоморфологическая
| Стадия 0 | Tis | N0 | M0 |
| Стадия I | Т1 | N0 | M0 |
| Стадия IIА | Т2, T3 | N0 | M0 |
| Стадия IIB | Т4 | N0 | M0 |
| Стадия IIIA |
Т0
Т1, Т2, T3, Т4
|
N1b
N1a
|
M0 |
| Стадия IIIB | Любая Т | N1, N2, N3 | M0 |
| Стадия IV | Любая Т | Любая N | M1 |
КОРА НАДПОЧЕЧНИКА C74.0
Таблица 6. Группировка по стадиям
| Стадия I | Т1 | N0 | M0 |
| Стадия II | Т2 | N0 | M0 |
| Стадия III |
Т1, T2
Т3, T4
|
N1
N0, N1
|
M0 |
| Стадия IV | Любая Т | Любая N | M1 |
Под редакцией
д-р мед. наук, проф. О.Г.Суконко,
д-р мед. наук, проф., член-корр. НАН Беларуси С.А.Красный
Авторский коллектив:
Антоненкова Нина Н., д.м.н., доц.;
Ануфреенок И.В., к.м.н.;
Артемова Н.А., д.м.н., доц.;
Баранов А.Ю., к.м.н.;
Баранов Е.В., к.м.н.;
Бармотько М.А.;
Грачев Ю.Н., к.м.н.;
Демешко П.Д., д.м.н.;
Демидчик Ю.Е., д.м.н., проф.;
Дзюбан В.П.;
Доломанова Е.В.;
Дубровский А.Ч., к.м.н.;
Евмененко А.А.;
Ермаков Н.Б., к.м.н.;
Жаврид Э.А., д.м.н., проф.;
Жарков В.В, д.м.н., проф.;
Жиляева Е.П.;
Жуковец А.Г., к.м.н.;
Зеленкевич И.А., к.м.н.;
Ильин И.А., к.м.н.;
Караник В.С., к.м.н.;
Карман А.В., к.м.н., доц.;
Киселев П.Г., к.м.н.;
Клименко Д.П.;
Колядич Г.И., к.м.н.;
Кондратович В.А.;
Котов А.А., к.м.н.;
Кохнюк В.Т., д.м.н., проф.;
Красный С.А., д.м.н., проф.;
Крутилина Н.И., д.м.н., проф.;
Курченков А.Н., к.м.н.;
Курчин В.П., д.м.н.;
Левин Л.Ф.;
Леонова Т.А.;
Мавричев А.С., д.м.н., проф.;
Мавричев С.А., к.м.н.;
Малькевич В.Т., д.м.н., доц.;
Маньковская С.В.;
Матылевич О.П., к.м.н.;
Минайло И.И., к.м.н.;
Минич А.А., к.м.н.;
Моисеев П.И., к.м.н.;
Набебина Т.И., к.м.н.;
Науменко Л.В., к.м.н.;
Океанов А.Е., д.м.н., проф.;
Пархоменко Л.Б., к.м.н., доц.;
Петрушенко Ю.И.;
Писаренко А.М.;
Поляков С.Л., к.м.н.;
Портянко А.С., д.м.н., доц.;
Прохорова В.И., д.м.н., проф.;
Ребеко И.В., к.м.н.;
Ревтович М.Ю., к.м.н.;
Ролевич А.И., д.м.н.;
Рындин А.А.;
Рябчевский А.Н.;
Синайко В.В., к.м.н.;
Субоч Е.И., к.м.н.;
Суколинская Е.В., к.м.н.;
Суконко О.Г., д.м.н., проф.;
Суслова В.А., к.м.н.;
Тризна Н.М., к.м.н.;
Фридман М.В., д.м.н.;
Шаповал Е.В., д.м.н.;
Шмак А.И., д.м.н.
Список сокращений:
CTV – клинический объем облучения
GTV – определяемый объем опухоли
ICD – Международная классификация болезней
ITC – отдельные опухолевые клетки
PTV – планируемый объем облучения
UICC – Международный противораковый союз
АЛТ – аланинаминотрансфераза
АСТ – аспартатаминотрансфераза
АЧТВ – активированное частичное тромбопластиновое время
ВАТС – видео-ассистированной тораскопии
ВОЗ – Всемирная организация здравоохранения
ВПЧ – вирус папилломы человека
ВЯВ – внутренняя яремная вена;
ГИСО – гастроинтенстинальные стромальные опухоли
ГПДР – гастропанкреатодуоденальная резекция
ГЦР – гепатоцеллюлярный рак
ЖКТ – желудочно-кишечный тракт
ИГХ – иммуногистохимическое исследование
ИОУЗИ – интраоперационное УЗИ
КТ – компьютерная томография
ЛДГ – лактатдегидрогеназа
МНО – международное нормализованное отношение
МРТ – магнитно-резонансная томография
МСКТ – многослойная компьютерная томография
ОГК – органы Грудной клетки
ПВ – протромбиновое время
ПЖ – поджелудочная железа
ПЭТ – позитронно-эмиссионная томография
РЖП – рак желчного пузыря
РОД – разовая облучающая доза
РПК – рак прямой кишки
РПХГ – ретроградная панкреатохолангиография
СОД – суммарная облучающая доза
ТВ – тромбиновое время
ТДПЭ – тотальная дуоденопанкреатэктомия
УЗИ – ультразвуковое исследование
ФВД – функция внешнего дыхания
ФДГ – фтордезоксиглюкоза
ФЭГДС – фиброгастродуоденоскопия
ХЦР – холангиоцеллюлярного рака
ЦНС – центральная нервная система
ЧЧХГ – чрескожная чреспеченочная холангиография
ЧЭИ – чрескожная этаноловая инъекция
ЩФ – щелочная фосфатаза
ЭВВ – эмболизация воротной вены
ЭКГ – электрокардиограмма
ЭУЗИ – эндоскопическое ультразвуковое исследование
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.