Диагностика и лечение злокачественных новообразований: Гастроинтестинальные стромальные опухоли
 Версия: Клинические протоколы 2006-2019 (Беларусь)
Версия: Клинические протоколы 2006-2019 (Беларусь)
Злокачественное новообразование желудка (C16), Злокачественное новообразование забрюшинного пространства и брюшины (C48), Злокачественное новообразование ободочной кишки (C18), Злокачественное новообразование пищевода (C15), Злокачественное новообразование прямой кишки (C20), Злокачественное новообразование ректосигмоидного соединения (C19), Злокачественное новообразование тонкого кишечника (C17)
Онкология
Общая информация
Краткое описание
ПОСТАНОВЛЕНИЕ
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ
РЕСПУБЛИКИ БЕЛАРУСЬ
6 июля 2018 г. № 60
Об утверждении клинического протокола «Алгоритмы диагностики и лечения злокачественных новообразований»
На основании подпункта 8.3 пункта 8 Положения о Министерстве здравоохранения Республики Беларусь, утвержденного постановлением Совета Министров Республики Беларусь от 28 октября 2011 г. № 1446 «О некоторых вопросах Министерства здравоохранения и мерах по реализации Указа Президента Республики Беларусь от 11 августа 2011 г. № 360», Министерство здравоохранения Республики Беларусь
ПОСТАНОВЛЯЕТ:
1. Утвердить прилагаемый клинический протокол «Алгоритмы диагностики и лечения злокачественных новообразований».
2. Начальникам главных управлений по здравоохранению областных исполнительных комитетов, председателю комитета по здравоохранению Минского городского исполнительного комитета, руководителям государственных организаций, подчиненных Министерству здравоохранения Республики Беларусь, обеспечить проведение диагностики, лечение и профилактику заболеваний в соответствии с клиническим протоколом.
3. Настоящее постановление вступает в силу после его официального опубликования.
Министр В.А.Малашко
УТВЕРЖДЕНО
Постановление
Министерства здравоохранения
Республики Беларусь
06.07.2018 № 60
КЛИНИЧЕСКИЙ ПРОТОКОЛ «Алгоритмы диагностики и лечения злокачественных новообразований»
ГЛАВА 16
ГАСТРОИНТЕСТИНАЛЬНЫЕ СТРОМАЛЬНЫЕ ОПУХОЛИ (С15-С20; С48)
Классификация
ГЛАВА 1
ОБЩИЕ СВЕДЕНИЯ О TNM КЛАССИФИКАЦИИ
Система TNM для классификации злокачественных опухолей была разработана французом Р. Denoix в 1943–1952 гг. В 1953 г. Комитет по номенклатуре опухолей и статистике, организованный UICC, и Международная комиссия по стадированию рака достигли соглашения по классификации анатомической распространенности опухолей на основе системы TNM. В 1954 г. Международный противораковый союз (UICC) создает Комитет по клинической классификации и прикладной статистике, который в 1958 г. публикует первые рекомендации по клинической классификации рака молочной железы и гортани.
В результате многолетней деятельности Комитета в 1968 г. издается первая редакция TNM классификация злокачественных опухолей. По мере разработки классификации для новых локализаций опухолей и уточнения более ранних рекомендаций в 1974, 1978, 1987, 1997, 2002 и 2009 гг. публикуются 2-я, 3-я, 4-я, 5-я, 6-я и 7-я редакции.
Настоящая (8-я) редакция правил классификации и стадирования полностью соответствуют 8-й редакции руководства по стадированию рака и одобрена всеми национальными TNM комитетами.
В данном руководстве используются морфологические формы злокачественных новообразований в соответствии с классификацией МКБ-О-3, адаптированной под МКБ-10 (проставление кодов врачом-патологом в морфологическом заключении обязательно).
UICC признает необходимость постоянства TNM классификации в течение определенного периода времени, необходимого для накопления данных. Поэтому классификация не должна изменяться до тех пор, пока не будут сделаны крупные достижения в диагностике и лечении злокачественных опухолей, требующие пересмотра настоящей классификации.
Общие правила системы TNM.
TNM система для описания анатомической распространенности болезни основывается на оценке 3 компонентов:
Т – распространение первичной опухоли;
N – отсутствие или наличие метастазов в регионарных лимфатических узлах и степень их поражения;
М – отсутствие или наличие отдаленных метастазов.
К этим трем компонентам добавляются цифры, указывающие на распространенность злокачественного процесса:
Т0, Т1, Т2, Т3, Т4; N0, N1, N2, N3; M0, M1.
В действительности система является «стенографическим» описанием распространенности злокачественной опухоли.
Общие правила классификации, применяемые для опухолей всех локализаций, следующие:
Для каждой локализации имеются две классификации:
Клиническая классификация, обозначаемая TNM (или cTNM). Она основывается на результатах обследования до лечения. Эти данные получают при врачебном осмотре, лучевой диагностике, эндоскопии, биопсии, хирургическом диагностическом вмешательстве и других методах обследования.
Патологическая классификация, обозначаемая pTNM. Она основана на данных обследования до лечения, дополненных или измененных в результате хирургического вмешательства и морфологического исследования. Гистологическая оценка первичной опухоли включает резецированную опухоль или биопсию, позволяющую оценить наивысшую Т категорию. Гистологическая оценка регионарных лимфатических узлов включает исследование удаленных узлов в количестве, адекватном для установления отсутствия метастазов в регионарных лимфатических узлах (pN0) и достаточном для оценки наиболее высокой pN категории. Отдаленные метастазы должны быть подтверждены при микроскопическом исследовании (рМ).
После обозначения Т, N, М и/или рТ, pN и рМ категорий они могут группироваться по стадиям. TNM классификация и стадии, установленные однажды, должны оставаться неизменными в медицинских документах. Клиническая стадия служит основой для выбора лечения, тогда как патологическая стадия обеспечивает наиболее точные данные для оценки прогноза и расчета конечных результатов.
При сомнении в правильности оценки Т, N или М категории должно быть выбрано меньшее значение категории, (т.е. меньшее распространение опухоли).
В случае множественных опухолевых очагов в органе должна классифицироваться опухоль с более высокой Т категорией, а в скобках указываться множественность (т) или количество опухолей, например: Т2(т) или Т1(5). При одновременном поражении парных органов каждая опухоль должна классифицироваться отдельно. При опухолях печени, яичников и фаллопиевой трубы множественные очаги поражения являются критерием Т классификации.
Выявление второй опухоли в одном органе в течение 2 месяцев с момента выявления первой нужно расценивать как синхронное поражение.
TNM категории и стадия могут подразделяться или объединяться для клинических и научных целей (например, любые Т, N или М могут быть разбиты на подгруппы). Однако рекомендованные основные обозначения не должны изменяться.
Анатомические области и локализации.
Локализации в этой классификации обозначаются кодовым номером Международной классификации онкологических болезней.
TNM/pTNM классификация.
Используются следующие общие определения:
Т/рТ – первичная опухоль:
TX/рTX – первичная опухоль не может быть оценена;
Т0/рТ0 – нет доказательств первичной опухоли;
Tis/pTis – рак «in situ»;
Т1/рТ1, Т2/рТ2, ТЗ/рТЗ, Т4/рТ4 – размер или местное распространение опухоли в порядке увеличения.
N/pN – регионарные лимфатические узлы:
Nx/pNx – регионарные лимфатические узлы не могут быть оценены;
N0/pN0 – отсутствуют метастазы в регионарных лимфоузлах;
Nl/pNl, N2/pN2, N3/pN3 – возрастающее поражение регионарных лимфатических узлов.
Непосредственное распространение первичной опухоли на лимфатические узлы классифицируется как метастазы в лимфатических узлах. Метастаз в любом лимфоузле, не относящемся к регионарному, расценивается как отдаленный метастаз.
Опухолевый узел в области регионарных лимфатических узлов, не имеющий гистологических признаков лимфоузла, классифицируется как метастаз в регионарном лимфатическом узле, если имеет форму и ровный контур лимфатического узла. Опухолевый узел с неровным контуром классифицируется в рТ категории.
Когда размер является критерием pN классификации, производится измерение метастатического очага, а не всего лимфатического узла.
Случаи с микрометастазами, когда размеры метастазов не превышают 0,2 см, могут обозначаться добавлением «(mi)», например: pNl(mi) или pN2(mi).
М/рМ – отдаленные метастазы:
МХ/рМХ – отдаленные метастазы не могут быть оценены;
М0/рМ0 – нет отдаленных метастазов;
М1/рМ1 – имеются отдаленные метастазы;
Категория М может быть в дальнейшем специфицирована в соответствии со следующими обозначениями (таблица 1.1):
Таблица 1.1
| Легкие | PUL | Костный мозг | MAR |
| Кости | OSS | Плевра | PLE |
| Печень | HEP | Брюшина | PER |
| Головной мозг | BRA | Надпочечники | ADR |
| Лимфоузлы | LYM | Кожа | SKI |
| Другие | ОТН |
Подразделения TNM
Главные категории в классификации могут иметь подразделения, придающие критерию большую специфичность (например; Tla, lb или N2a, 2b).
Сигнальный лимфоузел
Это первый лимфоузел, получающий лимфу из первичной опухоли. Если в нем имеется метастаз, то и другие лимфоузлы могут быть поражены. Если этот лимфоузел не поражен, то и наличие метастазов в других узлах маловероятно. Иногда встречаются более одного сигнальных лимфоузлов.
При оценке сигнального лимфоузла применяются следующие определения:
Главные категории в классификации могут иметь подразделения, придающие критерию большую специфичность (например; Tla, lb или N2a, 2b).
Сигнальный лимфоузел
Это первый лимфоузел, получающий лимфу из первичной опухоли. Если в нем имеется метастаз, то и другие лимфоузлы могут быть поражены. Если этот лимфоузел не поражен, то и наличие метастазов в других узлах маловероятно. Иногда встречаются более одного сигнальных лимфоузлов.
При оценке сигнального лимфоузла применяются следующие определения:
- pNX(sn) – сигнальный узел не может быть оценен; pN0(sn) – нет поражения сигнального узла;
- pN1(sn) – есть поражение сигнального узла.
Отдельные опухолевые клетки
Отдельные опухолевые клетки (ITC) представляют собой единичные опухолевые клетки или маленькие кластеры клеток не более 0,2 мм в наибольшем измерении. ITC обычно не демонстрируют метастатической активности (пролиферацию или реакцию стромы) или инвазии стенок сосудистого или лимфатического синуса. Случаи с ITC в лимфатических узлах или отдаленных органах и тканях должны классифицироваться как N0 или М0 соответственно.
Это же применимо и к случаям, когда наличие опухолевых клеток или их компонентов подтверждается неморфологическими исследованиями, такими как проточная морфометрия или анализ ДНК.
Случаи с ITC должны анализироваться отдельно.
Классификация ITC:
- pN0 – гистологически не выявляются метастазы в регионарных лимфатических узлах, не проводились исследования по выявлению ITC;
- pN0(i-) – гистологически нет метастазов в регионарных лимфатических узлах, негативные морфологические данные по выявлению ITC;
- pN0(i+) – гистологически нет метастазов в регионарных лимфатических узлах, позитивные морфологические данные по выявлению ITC;
- pN0(mol-) – гистологически нет метастазов в регионарных лимфатических узлах, негативные неморфологические данные по выявлению ITC;
- pN0 (mol+) – гистологически нет метастазов в регионарных лимфатических узлах, неморфологическими методами выявляются ITC.
При исследовании ITC в сигнальном лимфоузле к обозначениям выше приведенной классификации в скобках указывается «(sn)», например: pN0(i+) (sn).
Отдельные опухолевые клетки, выявленные в костном мозгу морфологическими методами, классифицируются аналогично схеме для N, например: pM0(i+), а неморфологическими – pM0(mol+).
Гистопатологическая дифференцировка.
Это стадирование позволяет оценить степень агрессивности опухолей некоторых гистологических типов и может влиять на прогноз и выбор лечения.
Для большинства локализаций выделяется 4 степени дифференцировки опухолей:
- G1 – хорошо дифференцированные;
- G2 – умеренно дифференцированные;
- G3 – низко дифференцированные;
- G4 – недифференцированные.
При наличии различных степеней дифференцировки в опухоли указывается наименее благоприятная степень.
Саркомы костей и мягких тканей классифицируется также с использованием градаций «высокая степень» и «низкая степень» дифференцировки.
Для некоторых форм рака (молочной железы, тела матки, печени) рекомендуются специальные системы стадирования по степеням.
Дополнительные дескрипторы
Для идентификации особых случаев в TNM/pTNM используются символы m, у, r, а.
Хотя они не влияют на группировку по стадиям, но указывают опухоли, которые должны анализироваться отдельно:
- m – используется для обозначения множественных опухолей одной локализации;
- у – в тех случаях, когда классификация приводится в течение или после проведения комбинированного (многокомпонентного) лечения, cTNM или pTNM категория обозначается префиксом «у», например: ycTNM или ypTNM. При оценке распространения опухоли до начала комбинированного лечения символ «у» не исключается;
- r – рецидив опухоли после радикального лечения при классификации обозначается префиксом «r» (rcTNM или rpTNM);
- а – применяется для обозначения классификации опухолей, впервые выявленных при аутопсии.
Необязательные дескрипторы
L – инвазия лимфатических сосудов
Классифицируется как LX, L0 и L1.
V – инвазия вен
Классифицируется как VX, VO, VI (микроскопическая инвазия) и V2 (макроскопическая инвазия). Макроскопическое вовлечение стенки вены при отсутствии опухоли в просвете сосуда классифицируется как V2.
С-фактор
С-фактор или «фактор надежности» отражает достоверность классификации с учетом использованных методов диагностики. Его использование не является обязательным.
Определения С-фактора:
- С1 – данные стандартных диагностических методов (осмотр, пальпация, рентгенологическое исследование, эндоскопическое исследование),
- С2 – данные, полученные при использовании специальных диагностических методов (рентгенологическое исследование в специальных проекциях, томография, компьютерная томография, ультразвуковое исследование, лимфография, ангиография, сцинтиграфия, магнитно-резонансная томография, ПЭТ/КТ, эндоскопия, биопсия, цитологическое исследование);
- С3 – данные хирургического диагностического вмешательства, включая биопсию и цитологическое исследование;
- С4 – данные, полученные после радикальной операции и гистологического исследования удаленного препарата;
- С5 – данные патологоанатомического вскрытия.
Степени С-фактора могут использоваться при описании категорий Т, N и М (например: Т3С2, N2C1, М0С2).
Клиническая классификация TNM соответствует CI, С2 и С3 степеням, тогда как pTNM эквивалентна С4.
Классификация остаточных опухолей (R)
TNM/pTNM классификация описывает анатомическую распространенность опухоли без рассмотрения вопросов лечения. R-классификация описывает статус опухоли после лечения. Она отражает эффект лечения и является прогностическим фактором. При R- классификации оценивается не только первичная опухоль, но и остающиеся отдаленные метастазы.
Эта классификация может применяться после хирургического лечения, лучевой или химиотерапии, а также после комбинированного лечения. После консервативного лечения остаточная опухоль оценивается клиническими методами. После хирургического лечения R-классификация требует тесного сотрудничества хирурга и морфолога.
Случаи с макроскопически определяемой остаточной опухолью (R2) могут подразделяться на R2a (без микроскопического подтверждения) и R2b (микроскопически подтвержденные).
R0 группа может включать пациентов как с М0, так и с Ml. В последнем случае отдаленные метастазы, как и первичная опухоль, должны быть полностью удалены. Трудности с R-классификацией могут возникнуть при удалении опухоли по частям, а не «en blok». В таких случаях уместна категория RX.
Наличие микроскопически определяемой инвазивной опухоли по линии резекции классифицируется как R1, а в случае неинвазивной карциномы – R1 (is).
Группировка по стадиям.
Комбинация всех значений дескрипторов TNM позволяет получить 24 категории TNM, описывающие распространенность опухоли. Для табличного представления данных и анализа эти категории объединяются в ограниченное количество групп – стадий. Каждая стадия более или менее однородна по прогнозу и критерию выживаемости относящихся к ней пациентов.
Карцинома «in situ» относится к стадии 0, а опухоли с отдаленными метастазами – к стадии IV (за исключением некоторых локализаций, например, папиллярного и фолликулярного рака щитовидной железы).
Для патологической стадии необходимо морфологическое исследование достаточного количества тканей, позволяющее оценить наибольшее значение Т и N. Если же имеется морфологическое подтверждение отдаленных метастазов, то и классификация (рМ1) и стадия являются патологическими.
Термин «стадия» употребляется только для комбинаций Т, N, М или рТ, pN или рМ категорий. Необходимо избегать выражений типа «Т стадия» или «N стадия»
ГАСТРОИНТЕСТИНАЛЬНЫЕ СТРОМАЛЬНЫЕ ОПУХОЛИ (С15-С20; С48)
16.2.1. Определение степени дифференцировки GIST
Таблица 16.2. Определение степени дифференцировки GIST
| Низкий митотический индекс | Частота митозов 5 и менее в 50 полях зрения |
| Высокий митотический индекс | Частота митозов более 5 в 50 полях зрения |
Для стадирования ГИСО используется TNM классификация (8-ое издание, 2017 г.) (табл. 16.3)
16.3. Классификация TNM (8-я редакция, 2017 г.)
16.3.1. T – первичная опухоль
T1 Опухоль <2 см в наибольшем измерении
T2 Опухоль >2 см, но <5 см в наибольшем измерении
T3 Опухоль >5 см, но <10 см в наибольшем измерении
T4 Опухоль >10 см в наибольшем измерении
16.3.2. N – Регионарные лимфатические узлы
NX Недостаточно данных для оценки состояния регионарных лимфатических узлов
N0 Отсутствуют метастазы в регионарных лимфоузлах
N1 Метастазы в регионарных лимфатических узлах
Примечание: Регионарные лимфатические лимфоузлы редко поражаются при GIST, поэтому в случаях, когда состояние лимфоузлов не было оценено (клинически или морфологически), должна выставляться категория N0 вместо NX или pNX.
16.3.3. M – отдаленные метастазы
M0 Нет отдаленных метастазов
M1 Имеются отдаленные метастазы
16.3.4. Группировка по стадиям
Таблица 16.3. Группировка по стадиям
| Стадия | T | N | M | Митотический индекс |
| GIST желудка | ||||
| IA | T1, T2 | 0 | 0 | Низкий митотический индекс |
| IB | T3 | 0 | 0 | Низкий митотический индекс |
| II | T1, T2 | 0 | 0 | Высокий митотический индекс |
| T4 | 0 | 0 | Низкий митотический индекс | |
| IIIA | T3 | 0 | 0 | Высокий митотический индекс |
| IIIB | T4 | 0 | 0 | Высокий митотический индекс |
| IV | любое значение | 1 | 0 | Любое значение |
| любое значение | любое значение | 1 | Любое значение | |
| GIST тонкого кишечника | ||||
| I | T1, T2 | 0 | 0 | Низкий митотический индекс |
| II | T3 | 0 | 0 | Низкий митотический индекс |
| IIIA | T1 | 0 | 0 | Высокий митотический индекс |
| T4 | 0 | 0 | Низкий митотический индекс | |
| IIIB | T2, T3, T4 | 0 | 0 | Высокий митотический индекс |
| IV | любое значение | 1 | 0 | Любое значение |
| любое значение | любое значение | 1 | Любое значение | |
Примечание: критерии стадирования для опухолей желудка могут применяться у первичных солитарных ГИСО сальника, критерии стадирования для опухолей тонкого кишечника могут применяться при ГИСО пищевода, ободочной, прямой кишки и брыжейки.
Эпидемиология
16.1. Основные статистические показатели С15–С20; С48.
Таблица 16.1
Основные статистические показатели
| Показатель | Число | |
| 2011 | 2016 | |
| Число вновь выявленных случаев заболевания | 33 | 105 |
| Заболеваемость на 100 000 населения (грубый интенсивный показатель) | 0,3 | 1,1 |
|
Диагноз установлен в I стадии заболевания (% к вновь выявленным
случаям)
|
42,8 | 40 |
|
Диагноз установлен в II стадии заболевания (% к вновь выявленным
случаям)
|
28,6 | 23 |
|
Диагноз установлен в III стадии заболевания (% к вновь выявленным
случаям)
|
14,3 | 26 |
|
Диагноз установлен в IV стадии заболевания (% к вновь выявленным
случаям)
|
14,3 | 11 |
|
Прожили менее года с момента установления диагноза из числа
заболевших в предыдущем году (одногодичная летальность в %)
|
8,8 | 2,8 |
| Умерло от злокачественных новообразований | 4 | 21 |
| Смертность на 100 000 населения Грубый интенсивный показатель | 0 | 0,2 |
| Отношение смертности к заболеваемости в % (интенсивные показатели) | 13,3 | 22,3 |
| Число пациентов, состоящих на учете на конец года | 97 | 318 |
| Из них состоящих на учете 5 и более лет, % | 15,5 | 22,3 |
Гастроинтенстинальные стромальные опухоли (ГИСО, gastrointestinal stromal tumors, GIST, М8936/0-1-3) – редкие мезенхимальные новообразования желудочно-кишечного тракта с частотой встречаемости 10–20 случаев на 1 млн. населения в год. На долю ГИСО приходится 80 % мезенхимальных опухолей желудочно-кишечного тракта, которые имеют особые клинико-морфологические, иммуногистологические и молекулярные характеристики, что предполагает специальную стратегию их лечения. Одинаково часто заболевают мужчины и женщины. Медиана возраста пациентов с ГИСО приходится на 55–65 лет, редко на лиц моложе 40 лет. Могут развиваться в любом отделе желудочно-кишечного тракта, но наиболее часто встречаются в желудке (60–70 %) и тонкой кишке (25–35 %), реже – в толстой кишке (5 %), двенадцатиперстной кишке (5 %), пищеводе (<1 %) и аппендиксе (<2 %), а также определяют в сальнике, брыжейке кишечника и забрюшинном пространстве. ГИСО составляют до 94 % и 83 % сарком желудка и тонкой кишки соответственно. ГИСО могут иметь веретеноклеточный, эпителиоидный и смешанный гистологический тип клеток.
Ключевым механизмом развития опухоли является мутация в гене c-Kit (80 %) или PDGFRA (10 %). Прогрессирование проявляется метастазами в печени и/или по брюшине.
Факторы и группы риска
16.2. Стадирование, оценка степени дифференцировки и риска прогрессирования заболевания.
Основными прогностическими факторами являются: митотический индекс, размер и локализация опухоли. Основа стадирования – размер опухоли и митотический индекс. Митотический индекс определяется путем подсчета числа митозов в 50 полях зрения при большом увеличении микроскопа, объектив 40х, общая площадь исследуемого материала в 50 полях составляет 5 мм2 (таблица 1).
Дополнительные прогностические факторы – разрыв капсулы, наличие опухолевых клеток по линии резекции.
Диагностика
16.4. Диагностические мероприятия
План обследования включает изучение жалоб и анамнеза заболевания, общее физикальное обследование, пальцевое исследование прямой кишки, осмотр гинеколога у женщин, стандартные лабораторные тесты (группа крови, резус-фактор, анализ крови на сифилис (реакция микропреципитации), общий анализ крови, общий анализ мочи, биохимическое исследование крови (белок, креатинин, мочевина, билирубин, АсАТ, АлАТ, щелочная фосфатаза, амилаза, глюкоза, электролиты – K, Na, Ca, Cl), коагулограмма – по показаниям), функциональные тесты, состав которых определяется выраженностью сопутствующей патологии (ЭКГ, исследование функции внешнего дыхания, эхокардиография, холтеровское мониторирование, исследование ФВД, УЗИ сосудов (вен нижних конечностей, ультразвуковая допплерография сосудов и т.д.), а также консультация узких специалистов (по показанием с учетом сопутствующей патологии).
Эндоскопическое исследование желудочно-кишечного тракта с биопсией опухоли и морфологическим исследованием материала. При локализации опухоли в желудке эндоскопическая предоперационная биопсия предпочтительнее чрескожной.
Эндоскопическое ультразвуковое исследование (ЭУЗИ) с целью определения размеров опухоли, ее структуры, глубины инвазии, состояния регионарных лимфатических узлов является более предпочтительным методом, чем ЭГДС.
УЗИ органов брюшной полости, забрюшинного пространства, малого таза.
Чрескожная пункционная биопсия опухоли под контролем УЗИ противопоказана, вследствие повышенного риска развития диссеминации опухоли по брюшине (разрыв капсулы опухоли) и по ходу пункционного канала. Исключение – предоперационное назначение таргетной терапии.
Рентгенологическое исследование желудочно-кишечного тракта с контрастированием (по показанием).
Рентгенография органов Грудной клетки.
КТ Грудной клетки, брюшной полости и забрюшинного пространства с пероральным и внутривенным контрастированием является оптимальным методом диагностики.
Магнито-резонансная томография с/без болюсным контрастированием (МРТ/МРТА) по показанием. Обязательно выполняется при локализации опухоли в малом тазу (опухоли прямой кишки).
ФДГ ПЭТ-КТ выполняется для оценки метаболического эффекта лечения, а также может применяться при сомнительных результатах компьютерной томографии (по показаниям).
Лапароскопия (по показаниям).
Морфологического исследования биопсийного материала, удаленной опухоли.
Диагноз ГИСО основывается на данных световой микроскопии и иммуногистохимического исследования (95 % опухолей CD117 – позитивны, 80 % – CD34-позитивны, 85–95 % для c-Kit положительных и 30–36 % для c-Kit негативных – DOG1-позитивных). Наличие мутации в генах KIT и PDGFRA может подтвердить диагноз ГИСО в сложных диагностических случаях (в частности, при подозрении на CD117- негативные ГИСО).
16.4.1. Алгоритм диагностики ГИСО
Таблица 16.4. Алгоритм диагностики ГИСО
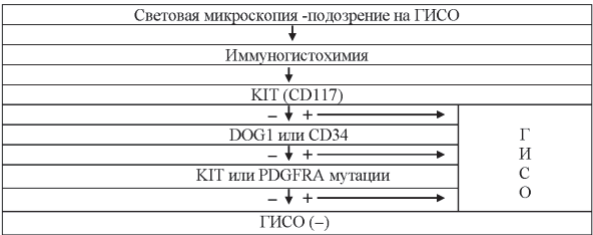
Анализ мутационного статуса генов KIT (9, 11, 13 и17 экзоны) и PDGFRA (12 и 18 экзоны) имеет чрезвычайно важное значение в оценке эффективности таргентной терапии и прогноза.
Пациенты с точечными мутациями, дупликациями в 11-м экзоне гена KIT и гене PDGFRA (кроме D842V) лучше отвечают на лечение и обладают благоприятным прогнозом.
Патогенез развития стромальных опухолей желудка в составе триады Карнея и синдрома Карнея-Стратакиса связан с дефицитом фермента сукцинатдегидрогеназы (SDH). Терапия ингибиторами тирозинкиназ в таких случаях неэффективна. У пациентов с диким типом могут выявляться мутации в генах SDH, KRAS, BRAF, NRAS.
В сложных случаях (трудности в установке морфологического или молекулярно-генетического диагноза, пациенты с триадой Карнея или с диким типом) уточняющую диагностику и лечение целесообразно проводить в специализированных онкологических учреждениях.
16.7. Наблюдение, сроки и объем обследования
КТ каждые 3–4 месяца в течение 3 лет, затем каждые 6 месяцев на протяжении 5 лет, и затем ежегодно. При опухолях с низким риском контрольное обследование осуществляется с помощью КТ каждые 6 месяцев на протяжении 5 лет.
Лечение
16.5. Лечение локализованных ГИСО
Объем диагностических исследований зависит от локализации опухоли и должен соответствовать стандартам обследования пациентов, страдающих раком данной локализации. Хирургическое вмешательство, проведенное как можно раньше, является наилучшим вариантом лечения локализованных стромальных опухолей ЖКТ.
В случае, когда подслизистая опухоль в пищеводе, желудке или двенадцатиперстной кишке имеет размер 2 см в диаметре и нет клинических проявлений заболевания, проводится динамическое наблюдение: эндоскопическая ультрасонография каждые 6–12 мес. При увеличении опухоли в размерах, пациентам выполняется лапароскопическая/лапаротомическая эксцизия. Альтернативой может стать, принятое совместно с пациентом, решение о выполнении диагностической операции с целью получения гистологического материала и последующей верификацией диагноза. При наличии опухолевых образований >2 см в диаметре стандартным подходом является выполнение биопсии или эксцизии.
При локализации любого размера опухоли в тонкой, толстой или прямой кишке стандартным подходом является выполнение биопсии, лапароскопического или открытого удаления опухоли.
При наличии патологического образования в брюшной полости, не поддающегося эндоскопической оценке, методом выбора является выполнение лапароскопической/лапаротомической эксцизии.
16.6. Общие принципы лечения
Ведущим методом лечения ГИСО является хирургический. Целью операции является выполнение R0 резекции. Пациентам с ГИСО оправданы выполнение экономных резекций, отступя от макроскопически видимого края опухоли не менее чем на 2 см. Энуклеация опухоли не является адекватным объемом хирургического вмешательства и не должна применяться при ГИСО. При клинически негативных лимфатических узлах лимфодиссекция не производится. Лапароскопическое удаление опухоли возможно при небольших размерах до 5.0 см Случай разрыва опухоли, возникший спонтанно или в процессе хирургической резекции, должен быть зафиксирован, потому что он имеет крайне неблагоприятное прогностическое значение вследствие контаминации брюшной полости. В случаях разрыва опухоли должны быть взяты смывы из брюшной полости.
При выявлении опухолевых клеток по краю резекции (R1) возможно выполнение повторной операции с учетом всех клинических факторов прогноза.
16.6.1. Лечение первично-резектабельных форм GIST.
Хирургическая R0 резекция является адекватной.
Пациентам высокой Группы риска (III–IV стадии заболевания) показано проведение адъювантной химиотерапии иматинибом (400мг внутрь ежедневно) в течение 1 года.
Если выполнена R1 резекция, то необходимо рассмотреть возможность повторного хирургического вмешательства.
16.6.2. Лечение первично-нерезектабельных форм GIST
При нерезектабельной опухоли и наличии метастазов лечение начинается с химиотерапии иматинибом в дозе 400 мг/сутки. Лечебный эффект по данным КТ/МРТ оценивается каждые 3 месяца. Если опухоль становится резектабельной, рассматривается вопрос о выполнении радикального хирургического вмешательства (R0).
16.6.3. Лечение нерезектабельных форм GIST
Стандартом первой линии химиотерапии является иматиниб в дозе 400 мг/сутки. При прогрессировании процесса дозу лекарственного средства повышают поэтапно до 800 мг/сутки. У пациентов с мутацией в 9 экзоне KIT-гена должна сразу использоваться высокая доза иматиниба (800мг/сутки, по 400мг два раза в день). Обнаружение мутации D842V в 18 экзоне гена PDGFRA, является маркером первичной резистентности опухоли к лекарственному средству. Лечение должно быть непрерывным. Непосредственно за прекращением лечения, практически во всех случаях ГИСО, следует относительно быстрая опухолевая прогрессия.
Эффективность лечения у большинства пациентов проявляется в уменьшении размера опухоли, но в некоторых случаях могут происходить только изменения в плотности опухоли по данным КТ-исследования или эти изменения могут предшествовать более позднему сокращению размеров опухоли. Некоторое увеличение размера опухоли может указывать на эффективность терапии, если одновременно с этим плотность опухоли по данным КТ уменьшилась. Внезапное выявление новых образований на КТ может быть связано с тем, что они становятся более визуализируемыми, когда теряют плотность. Следовательно, размер и плотность опухоли (должны рассматриваться как критерии эффективности проводимой терапии.
С другой стороны, опухолевая прогрессия может не сопровождаться изменениями размера опухоли. Некоторое увеличение плотности в пределах опухолевого образования может указывать на прогрессирование заболевания. Типичная картина прогрессирования – «узел в узле», при котором часть образования, ранее «ответившего» на лечение, приобретает повышенную плотность.
При прогрессировании заболевания или у пациентов нечувствительных к иматинибу, стандартом терапии второй линии является сунитиниб (по 50мг внутрь ежедневно в течение 4 недель, интервал между курсами – 2 недели).
При прогрессировании заболевания после 2-х стандартных линий лечения вариантом является применение лекарственного средства регорафениба. Рекомендуемая суточная доза составляет 160 мг (4 таблетки по 40 мг). Лекарственное средство назначается один раз в сутки в течение 3 недель. В последующую неделю (4-я неделя от начала лечения) следует перерыв в приеме лекарственного средства. Период продолжительностью 4 недели от начала приема является одним курсом лечения.
Оперативное лечение может рассматриваться в качестве паллиативной меры у отдельных пациентов при ограниченном характере прогрессирования. Так же могут быть рассмотрены такие методы локального лечения, как, например, абляция и эмболизация.
Информация
Источники и литература
-
Постановления и приказы Министерства здравоохранения Республики Беларусь об утверждении клинических протоколов 2006-2019
- Постановления и приказы Министерства здравоохранения Республики Беларусь об утверждении клинических протоколов 2006-2019 -
-
www.minzdrav.gov.by
- www.minzdrav.gov.by -
Информация
ГЛАВА 2
ОЦЕНКА ОБЩЕГО СОСТОЯНИЯ ОНКОЛОГИЧЕСКОГО ПАЦИЕНТА
Общее состояние онкологического пациента (Performance status) рекомендовано оценивать по индексу Карновского (0–100 баллов) или шкале ECOG (0–4 балла) (таблицы 2.1, 2.2).
Таблица 2.1. Индекс Карновского
Таблица 2.1. Индекс Карновского
|
Нормальная физическая активность, пациент не нуждается в специальном уходе
|
100 баллов | Состояние нормальное, нет жалоб и симптомов заболевания |
| 90 баллов | Нормальная активность сохранена, но имеются незначительные симптомы заболевания | |
| 80 баллов | Нормальная активность возможна при дополнительных усилиях, при умеренно выраженных симптомах заболевания | |
|
Ограничение нормальной активности при сохранении полной независимости пациента
|
70 баллов | Пациент обслуживает себя самостоятельно, но не способен к нормальной деятельности или работе |
| 60 баллов | Пациент иногда нуждается в помощи, но в основном обслуживает себя сам | |
| 50 баллов | Пациенту часто требуется помощь и медицинское обслуживание | |
|
Пациент не может обслуживать себя самостоятельно, необходим уход или госпитализация
|
40 баллов | Большую часть времени пациент проводит в постели, необходим специальный уход и посторонняя помощь |
| 30 баллов | Пациент прикован к постели, показана госпитализация, хотя терминальное состояние не обязательно | |
| 20 баллов | Сильные проявления болезни, необходима госпитализация и поддерживающая терапия | |
| 10 баллов | Умирающий пациент, быстрое прогрессирование заболевания | |
| 0 баллов | Смерть |
Таблица 2.2. Оценка статуса пациента по шкале ECOG
| Оценка | |
| 0 | Пациент полностью активен, способен выполнять все, как и до заболевания (90–100 баллов по шкале Карновского) |
| 1 | Пациент неспособен выполнять тяжелую, но может выполнять легкую или сидячую работу (например, легкую домашнюю или канцелярскую работу, 70–80 баллов по шкале Карновского) |
| 2 | Пациент лечится амбулаторно, способен к самообслуживанию, но не может выполнять работу. Более 50 % времени бодрствования проводит активно – в вертикальном положении (50–60 баллов по шкале Карновского) |
| 3 | Пациент способен лишь к ограниченному самообслуживанию, проводит в кресле или постели более 50 % времени бодрствования (30–40 баллов по шкале Карновского) |
| 4 | Пациент, совершенно не способен к самообслуживанию, прикован к креслу или постели (10–20 баллов по шкале Карновского) |
Приложение
ТАБЛИЦЫ СООТВЕТСТВИЯ «СТАДИЯ-TNM» ДЛЯ РЯДА ЛОКАЛИЗАЦИЙ: ТОНКИЙ КИШЕЧНИК, АМПУЛА ФАТЕРОВА СОСКА, ТИМОМА, МЕЗОТЕЛИОМА ПЛЕВРЫ, КАРЦИНОМА МЕРКЕЛЯ КОЖИ, КОРА НАДПОЧЕЧНИКА
ТОНКИЙ КИШЕЧНИК C17
Таблица 1. Группировка по стадиям
| Стадия 0 | Tis | N0 | M0 |
| Стадия I | Т1, Т2 | N0 | M0 |
| Стадия IIА | Т3 | N0 | M0 |
| Стадия IIB | T4 | N0 | M0 |
| Стадия IIIA | Любая Т | N1 | M0 |
| Стадия IIIB | Любая Т | N2 | M0 |
| Стадия IV | Любая Т | Любая N | M1 |
АМПУЛА ФАТЕРОВА СОСКА C24.1
Таблица 2. Группировка по стадиям
| Стадия 0 | Tis | N0 | M0 |
| Стадия IA | Т1a | N0 | M0 |
| Стадия IB | Т1b, Т2 | N0 | M0 |
| Стадия IIА | Т3a | N0 | M0 |
| Стадия IIB | Т3b | N0 | M0 |
| Стадия IIIA | Т1a, Т1b, Т2, T3 | N1 | M0 |
| Стадия IIIB | Т4 | Любая N | M0 |
| Стадия IV | Любая Т | Любая N | M1 |
ТИМОМА C37, C38.1-3
Таблица 3. Группировка по стадиям
| Стадия I | T1 | N0 | M0 |
| Стадия II | T2 | N0 | M0 |
| Стадия IIIА | T3 | N0 | M0 |
| Стадия IIIB | T4 | N0 | M0 |
| Стадия IVA | Любая Т |
N1
N0, N1
|
M0
M1A
|
| Стадия IVB | Любая Т | Любая N | M1B |
МЕЗОТЕЛИОМА ПЛЕВРЫ C45.0
Таблица 4. Группировка по стадиям
| Стадия IA | T1 | N0 | M0 |
| Стадия IB | T2, T3 | N0 | M0 |
| Стадия II | T1, T2 | N1 | M0 |
| Стадия IIIА | T3 | N1 | M0 |
| Стадия IIIB | T1, T2, T3, T4 |
N1 Любая N |
M0 |
| Стадия IV | Любая Т | Любая N | M1 |
КАРЦИНОМА МЕРКЕЛЯ C44, C63.2
Таблица 5а. Группировка по стадиям клиническая
| Стадия 0 | Tis | N0 | M0 |
| Стадия I | Т1 | N0 | M0 |
| Стадия IIА | T2, Т3 | N0 | M0 |
| Стадия IIB | Т4 | N0 | M0 |
| Стадия III | Любая Т | N1, N2, N3 | M0 |
| Стадия IV | Любая Т | Любая N | M1 |
Таблица 5б. Группировка по стадиям патоморфологическая
| Стадия 0 | Tis | N0 | M0 |
| Стадия I | Т1 | N0 | M0 |
| Стадия IIА | Т2, T3 | N0 | M0 |
| Стадия IIB | Т4 | N0 | M0 |
| Стадия IIIA |
Т0
Т1, Т2, T3, Т4
|
N1b
N1a
|
M0 |
| Стадия IIIB | Любая Т | N1, N2, N3 | M0 |
| Стадия IV | Любая Т | Любая N | M1 |
КОРА НАДПОЧЕЧНИКА C74.0
Таблица 6. Группировка по стадиям
| Стадия I | Т1 | N0 | M0 |
| Стадия II | Т2 | N0 | M0 |
| Стадия III |
Т1, T2
Т3, T4
|
N1
N0, N1
|
M0 |
| Стадия IV | Любая Т | Любая N | M1 |
Под редакцией
д-р мед. наук, проф. О.Г.Суконко,
д-р мед. наук, проф., член-корр. НАН Беларуси С.А.Красный
Авторский коллектив:
Антоненкова Нина Н., д.м.н., доц.;
Ануфреенок И.В., к.м.н.;
Артемова Н.А., д.м.н., доц.;
Баранов А.Ю., к.м.н.;
Баранов Е.В., к.м.н.;
Бармотько М.А.;
Грачев Ю.Н., к.м.н.;
Демешко П.Д., д.м.н.;
Демидчик Ю.Е., д.м.н., проф.;
Дзюбан В.П.;
Доломанова Е.В.;
Дубровский А.Ч., к.м.н.;
Евмененко А.А.;
Ермаков Н.Б., к.м.н.;
Жаврид Э.А., д.м.н., проф.;
Жарков В.В, д.м.н., проф.;
Жиляева Е.П.;
Жуковец А.Г., к.м.н.;
Зеленкевич И.А., к.м.н.;
Ильин И.А., к.м.н.;
Караник В.С., к.м.н.;
Карман А.В., к.м.н., доц.;
Киселев П.Г., к.м.н.;
Клименко Д.П.;
Колядич Г.И., к.м.н.;
Кондратович В.А.;
Котов А.А., к.м.н.;
Кохнюк В.Т., д.м.н., проф.;
Красный С.А., д.м.н., проф.;
Крутилина Н.И., д.м.н., проф.;
Курченков А.Н., к.м.н.;
Курчин В.П., д.м.н.;
Левин Л.Ф.;
Леонова Т.А.;
Мавричев А.С., д.м.н., проф.;
Мавричев С.А., к.м.н.;
Малькевич В.Т., д.м.н., доц.;
Маньковская С.В.;
Матылевич О.П., к.м.н.;
Минайло И.И., к.м.н.;
Минич А.А., к.м.н.;
Моисеев П.И., к.м.н.;
Набебина Т.И., к.м.н.;
Науменко Л.В., к.м.н.;
Океанов А.Е., д.м.н., проф.;
Пархоменко Л.Б., к.м.н., доц.;
Петрушенко Ю.И.;
Писаренко А.М.;
Поляков С.Л., к.м.н.;
Портянко А.С., д.м.н., доц.;
Прохорова В.И., д.м.н., проф.;
Ребеко И.В., к.м.н.;
Ревтович М.Ю., к.м.н.;
Ролевич А.И., д.м.н.;
Рындин А.А.;
Рябчевский А.Н.;
Синайко В.В., к.м.н.;
Субоч Е.И., к.м.н.;
Суколинская Е.В., к.м.н.;
Суконко О.Г., д.м.н., проф.;
Суслова В.А., к.м.н.;
Тризна Н.М., к.м.н.;
Фридман М.В., д.м.н.;
Шаповал Е.В., д.м.н.;
Шмак А.И., д.м.н.
Список сокращений:
CTV – клинический объем облучения
GTV – определяемый объем опухоли
ICD – Международная классификация болезней
ITC – отдельные опухолевые клетки
PTV – планируемый объем облучения
UICC – Международный противораковый союз
АЛТ – аланинаминотрансфераза
АСТ – аспартатаминотрансфераза
АЧТВ – активированное частичное тромбопластиновое время
ВАТС – видео-ассистированной тораскопии
ВОЗ – Всемирная организация здравоохранения
ВПЧ – вирус папилломы человека
ВЯВ – внутренняя яремная вена;
ГИСО – гастроинтенстинальные стромальные опухоли
ГПДР – гастропанкреатодуоденальная резекция
ГЦР – гепатоцеллюлярный рак
ЖКТ – желудочно-кишечный тракт
ИГХ – иммуногистохимическое исследование
ИОУЗИ – интраоперационное УЗИ
КТ – компьютерная томография
ЛДГ – лактатдегидрогеназа
МНО – международное нормализованное отношение
МРТ – магнитно-резонансная томография
МСКТ – многослойная компьютерная томография
ОГК – органы Грудной клетки
ПВ – протромбиновое время
ПЖ – поджелудочная железа
ПЭТ – позитронно-эмиссионная томография
РЖП – рак желчного пузыря
РОД – разовая облучающая доза
РПК – рак прямой кишки
РПХГ – ретроградная панкреатохолангиография
СОД – суммарная облучающая доза
ТВ – тромбиновое время
ТДПЭ – тотальная дуоденопанкреатэктомия
УЗИ – ультразвуковое исследование
ФВД – функция внешнего дыхания
ФДГ – фтордезоксиглюкоза
ФЭГДС – фиброгастродуоденоскопия
ХЦР – холангиоцеллюлярного рака
ЦНС – центральная нервная система
ЧЧХГ – чрескожная чреспеченочная холангиография
ЧЭИ – чрескожная этаноловая инъекция
ЩФ – щелочная фосфатаза
ЭВВ – эмболизация воротной вены
ЭКГ – электрокардиограмма
ЭУЗИ – эндоскопическое ультразвуковое исследование
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.