Диагностика и лечение гемолитико-уремического синдрома (детское население)
Гемолитико-уремический синдром у детей
 Версия: Клинические протоколы 2024 (Беларусь)
Версия: Клинические протоколы 2024 (Беларусь)
Гемолитико-уремический синдром (D59.3)
Гематология, Гематология детская, Педиатрия
Общая информация
Краткое описание
ПОСТАНОВЛЕНИЕ
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ
РЕСПУБЛИКИ БЕЛАРУСЬ
26 декабря 2024 г. № 180
Об утверждении клинического протокола
На основании абзаца девятого части первой статьи 1 Закона Республики Беларусь от 18 июня 1993 г. № 2435-XII «О здравоохранении», подпункта 8.3 пункта 8 и подпункта 9.1 пункта 9 Положения о Министерстве здравоохранения Республики Беларусь, утвержденного постановлением Совета Министров Республики Беларусь от 28 октября 2011 г. № 1446, Министерство здравоохранения Республики Беларусь
ПОСТАНОВЛЯЕТ:
-
Утвердить клинический протокол «Диагностика и лечение гемолитико- уремического синдрома (детское население)» (прилагается).
-
Признать утратившим силу постановление Министерства здравоохранения Республики Беларусь от 30 января 2017 г. № 11 «Об утверждении клинического протокола «Диагностика и лечение гемолитико-уремического синдрома у детей».
-
Настоящее постановление вступает в силу после его официального опубликования.
СОГЛАСОВАНО
Брестский областной исполнительный комитет
Витебский областной исполнительный комитет
Гомельский областной исполнительный комитет
Гродненский областной исполнительный комитет
Могилевский областной исполнительный комитет
Минский областной исполнительный комитет
Минский городской исполнительный комитет
УТВЕРЖДЕНО
Постановление
Министерства здравоохранения
Республики Беларусь
26.12.2024 № 180
Брестский областной исполнительный комитет
Витебский областной исполнительный комитет
Гомельский областной исполнительный комитет
Гродненский областной исполнительный комитет
Могилевский областной исполнительный комитет
Минский областной исполнительный комитет
Минский городской исполнительный комитет
УТВЕРЖДЕНО
Постановление
Министерства здравоохранения
Республики Беларусь
26.12.2024 № 180
КЛИНИЧЕСКИЙ ПРОТОКОЛ
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
ГЛАВА 1
ОБЩИЕ ПОЛОЖЕНИЯ
1. Настоящий клинический протокол устанавливает общие требования к объему оказания медицинской помощи пациентам (детское население) с гемолитико-уремическим синдромом (далее, если не установлено другое – ГУС) (шифр по Международной статистической классификации болезней и проблем, связанных со здоровьем, десятого пересмотра – D59.3 Гемолитико-уремический синдром).
2. Требования настоящего клинического протокола являются обязательными для юридических лиц и индивидуальных предпринимателей, осуществляющих медицинскую деятельность в порядке, установленном законодательством о здравоохранении.
3. Для целей настоящего клинического протокола используются основные термины и их определения в значениях, установленных Законом Республики Беларусь «О здравоохранении», Законом Республики Беларусь от 19 ноября 1993 г. № 2570-XII «О правах ребенка», а также следующие термины и их определения:
- артериальная гипертензия (далее – АГ) – стойкое повышение систолического и (или) диастолического артериального давления (далее – АД) выше 95 перцентиля для данного пола, возраста и длины тела пациента;
- атипичный ГУС (далее – аГУС) – хроническое системное заболевание генетической природы, в основе которого лежит неконтролируемая активация альтернативного пути комплемента, ведущая к генерализованному тромбообразованию в сосудах микроциркуляторного русла;
- ГУС – клинико-лабораторный симптомокомплекс, включающий микроангиопатическую гемолитическую анемию (далее – МАГА), тромбоцитопению и острое повреждение почек (далее – ОПП);
- МАГА – анемия, развивающаяся вследствие сужения или обструкции мелких кровеносных сосудов, с развитием механического повреждения эритроцитов при их взаимодействии с эндотелием сосудов;
- ОПП – синдром внезапного снижения скорости гломерулярной фильтрации, сопровождающийся нарастанием уровня креатинина крови более чем в 1,5 раза по сравнению с исходным (если он неизвестен, то в 1,5 раза выше верхней границы возрастной нормы), с или без развития олигурии (снижение диуреза менее 0,5 мл/кг/ч) в течение 6 часов (у пациентов в возрасте до 1 года жизни – менее 1 мл/кг/ч);
- типичный ГУС (далее – тГУС) – ГУС, ассоциированный с диареей и вызываемый шига-токсином энтерогеморрагических штаммов E. coli (далее – STEC), реже – S. dysenteriae I типа;
- тромботическая микроангиопатия (далее – ТМА) – это гетерогенная группа заболеваний, объединенных общностью гистологической картины и клинических проявлений при различии патогенетических механизмов, характеризующаяся тромбозом сосудов микроциркуляторного русла.
- атипичный ГУС (далее – аГУС) – хроническое системное заболевание генетической природы, в основе которого лежит неконтролируемая активация альтернативного пути комплемента, ведущая к генерализованному тромбообразованию в сосудах микроциркуляторного русла;
- ГУС – клинико-лабораторный симптомокомплекс, включающий микроангиопатическую гемолитическую анемию (далее – МАГА), тромбоцитопению и острое повреждение почек (далее – ОПП);
- МАГА – анемия, развивающаяся вследствие сужения или обструкции мелких кровеносных сосудов, с развитием механического повреждения эритроцитов при их взаимодействии с эндотелием сосудов;
- ОПП – синдром внезапного снижения скорости гломерулярной фильтрации, сопровождающийся нарастанием уровня креатинина крови более чем в 1,5 раза по сравнению с исходным (если он неизвестен, то в 1,5 раза выше верхней границы возрастной нормы), с или без развития олигурии (снижение диуреза менее 0,5 мл/кг/ч) в течение 6 часов (у пациентов в возрасте до 1 года жизни – менее 1 мл/кг/ч);
- типичный ГУС (далее – тГУС) – ГУС, ассоциированный с диареей и вызываемый шига-токсином энтерогеморрагических штаммов E. coli (далее – STEC), реже – S. dysenteriae I типа;
- тромботическая микроангиопатия (далее – ТМА) – это гетерогенная группа заболеваний, объединенных общностью гистологической картины и клинических проявлений при различии патогенетических механизмов, характеризующаяся тромбозом сосудов микроциркуляторного русла.
4. ГУС относится к ТМА с преимущественным поражением почек.
ТМА подразделяются на первичные (тромботическую тромбоцитопеническую пурпуру (далее – ТТП); тГУС; аГУС; ГУС, вызванный Streptococcus pneumoniae (далее – рГУС)) и вторичные (ТМА, возникающая в результате повреждения эндотелия сосудов после трансплантации паренхиматозных органов или гемопоэтических стволовых клеток (далее – ТА-ТМА), и иные).
7. МАГА при ГУС характеризуется:
- снижением уровней гемоглобина и гаптоглобина;
- повышением уровней лактатдегидрогеназы (далее – ЛДГ), свободного гемоглобина плазмы и билирубина (преимущественно непрямого), ретикулоцитов;
- повышением уровней лактатдегидрогеназы (далее – ЛДГ), свободного гемоглобина плазмы и билирубина (преимущественно непрямого), ретикулоцитов;
- появлением шизоцитоза в периферической крови (более 1 %);
- отрицательной прямой и непрямой реакцией Кумбса.
- отрицательной прямой и непрямой реакцией Кумбса.
8. Тромбоцитопения диагностируется при количестве тромбоцитов периферической крови менее 150х109/л. При ГУС снижение уровня тромбоцитов более чем на 25 % от исходного (даже в пределах возрастной нормы) свидетельствует о повышенном их потреблении и отражает развитие заболевания.
9. Стадии ОПП у пациентов с ГУС установлены согласно приложению 2.
10. Лечение пациентов с острым ГУС осуществляется в стационарных условиях.
Лечение пациентов с ГУС легкой степени тяжести проводится в организациях здравоохранения районного (межрайонного) уровня. При ухудшении состояния до ГУС средней степени тяжести пациент переводится в организацию здравоохранения областного уровня.
Пациенты с ГУС тяжелой степени тяжести, с подозрением на аГУС переводятся из организаций здравоохранения районного (межрайонного) уровня в организации здравоохранения областного уровня (при наличии оборудования для проведения заместительной почечной терапии (далее – ЗПТ)) или в Республиканский центр детской нефрологии и заместительной почечной терапии (далее – РЦДНиЗПТ) на базе учреждения здравоохранения «2-я городская детская клиническая больница» г. Минска для проведения ЗПТ. Пациенты в крайне тяжелом состоянии, а также дети в возрасте до 6 месяцев жизни, переводятся в РЦДНиЗПТ только после консультации руководителя РЦДНиЗПТ или его заместителя.
Медицинская транспортировка осуществляется в условиях реанимобиля.
Пациенты с ГУС тяжелой степени тяжести, с подозрением на аГУС переводятся из организаций здравоохранения районного (межрайонного) уровня в организации здравоохранения областного уровня (при наличии оборудования для проведения заместительной почечной терапии (далее – ЗПТ)) или в Республиканский центр детской нефрологии и заместительной почечной терапии (далее – РЦДНиЗПТ) на базе учреждения здравоохранения «2-я городская детская клиническая больница» г. Минска для проведения ЗПТ. Пациенты в крайне тяжелом состоянии, а также дети в возрасте до 6 месяцев жизни, переводятся в РЦДНиЗПТ только после консультации руководителя РЦДНиЗПТ или его заместителя.
Медицинская транспортировка осуществляется в условиях реанимобиля.
11. Фармакотерапия назначается в соответствии с настоящим клиническим протоколом с учетом всех индивидуальных особенностей пациента, его индивидуальных медицинских противопоказаний, аллергологического и фармакологического анамнеза, тяжести заболевания, наличия сопутствующей патологии и клинико-фармакологической характеристики лекарственного препарата (далее – ЛП).
Применение ЛП осуществляется по медицинским показаниям и в режиме дозирования в соответствии с общей характеристикой ЛП и инструкцией по медицинскому применению (листком-вкладышем). По решению врачебного консилиума допускается включение в схему лечения ЛП по медицинским показаниям, не предусмотренным в инструкции по медицинскому применению (листке-вкладыше), и дополнительно указываются особые условия назначения, способ применения, доза, длительность и кратность приема.
По решению врачебного консилиума объем лечения может быть расширен с использованием других методов, не включенных в настоящий клинический протокол, если это осуществляется в интересах пациента по жизненным показаниям.
По решению врачебного консилиума объем лечения может быть расширен с использованием других методов, не включенных в настоящий клинический протокол, если это осуществляется в интересах пациента по жизненным показаниям.
Классификация
5. Классификация ГУС в зависимости от этиологического фактора установлена согласно приложению 1.
6. Клиническая классификация ГУС основана на тяжести заболевания:
легкая степень тяжести: наличие симптомов (МАГА, тромбоцитопения, ОПП) без нарушений скорости мочеотделения;
средняя степень тяжести: наличие симптомов легкой степени тяжести ГУС, осложненных расстройствами со стороны центральной нервной системы (далее – ЦНС) (судорожный синдром, галлюцинации, кома, иные) и (или) АГ, без нарушений скорости мочеотделения;
тяжелая степень тяжести: МАГА, тромбоцитопения, ОПП (как правило, 3 стадия) в сочетании с или без олигоанурии и с необходимостью проведения диализной терапии.
средняя степень тяжести: наличие симптомов легкой степени тяжести ГУС, осложненных расстройствами со стороны центральной нервной системы (далее – ЦНС) (судорожный синдром, галлюцинации, кома, иные) и (или) АГ, без нарушений скорости мочеотделения;
тяжелая степень тяжести: МАГА, тромбоцитопения, ОПП (как правило, 3 стадия) в сочетании с или без олигоанурии и с необходимостью проведения диализной терапии.
Диагностика
ГЛАВА 2
ДИАГНОСТИКА ГУС В ОРГАНИЗАЦИЯХ ЗДРАВООХРАНЕНИЯ РАЙОННОГО (МЕЖРАЙОННОГО) И ОБЛАСТНОГО УРОВНЕЙ
12. Дифференциальная диагностика ГУС проводится согласно приложению 3.
13. Обязательными диагностическими исследованиями в организациях здравоохранения районного (межрайонного) и областного уровней являются:
- общий анализ крови с подсчетом лейкоцитарной формулы, количества тромбоцитов, ретикулоцитов, скорости оседания эритроцитов (далее – ОАК) – 1–3 раза в неделю;
- исследование параметров кислотно-основного состояния крови (далее – КОС) – 1– 3 раза в неделю;
- биохимическое исследование крови (далее – БАК) с определением уровней общего белка, альбумина, креатинина, мочевины, аланинаминотрансферазы (далее – АлАТ), аспартатаминотрансферазы (далее – АсАТ), билирубина общего и прямого, амилазы, липазы, глюкозы, калия, натрия, хлора, кальция, С-реактивного белка (далее – СРБ) – 1– 3 раза в неделю;
- общий анализ мочи (далее – ОАМ) (при ее наличии) с определением относительной плотности, кислотности, белка, глюкозы, микроскопия осадка – 1–3 раза в неделю;
- определение группы крови по системе АВ0 и резус фактора, антиэритроцитарных антител (непрямая проба Кумбса) – 1 раз;
- бактериологическое исследование крови и мочи, отделяемого из носа и зева на аэробные и факультативно-анаэробные микроорганизмы с оценкой чувствительности выделенных микроорганизмов к антибактериальным ЛП – 1 раз в неделю;
- анализ кала на патогенную кишечную флору – 3 дня подряд;
- ультразвуковое исследование (далее – УЗИ) почек и мочевого пузыря – 1–2 раза в неделю;
- электрокардиограмма (далее – ЭКГ) – 1 раз в неделю;
- неинвазивное измерение АД в отделении анестезиологии и реанимации – суточное мониторирование – каждые 1–3 часа;
- неинвазивное измерение АД в соматическом отделении – 4 раза в сутки – 3 суток, далее – 3 раза в сутки;
- термометрия общая – 2–3 раза в сутки.
14. Дополнительными диагностическими исследованиями в организациях здравоохранения районного (межрайонного) и областного уровней являются:
- исследование показателей гемостаза с определением активированного частичного тромбопластинового времени, протромбинового времени, международного нормализованного отношения, уровня фибриногена (далее – коагулограмма);
- УЗИ органов брюшной полости; рентгенография органов грудной клетки;
- определение антигена вируса гепатита В, антител к вирусу гепатита С.
15. Обязательными диагностическими исследованиями в организациях здравоохранения областного уровня являются диагностические исследования, указанные в пункте 13 настоящего клинического протокола, а также:
УЗИ почек с оценкой кровотока и мочевого пузыря – 1–2 раза в неделю.
16. Дополнительными диагностическими исследованиями в организациях здравоохранения областного уровня являются:
- коагулограмма;
- БАК с определением уровней ЛДГ, прокальцитонина; прямая проба Кумбса (антиэритроцитарные антитела);
- исследование кала экспресс методами для выявления антигенов шига-токсина и E. coli O157;
- консультация врача – детского невролога, врача-офтальмолога; рентгенография органов грудной клетки.
17. Дифференцированный подход к терапии ГУС установлен согласно приложению 4.
ГЛАВА 3
ДИАГНОСТИКА ГУС В РЦДНИЗПТ
30. Дифференциальная диагностика ГУС проводится согласно приложению 3.
Обязательными диагностическими исследованиями в РЦДНиЗПТ являются:
- ОАК с подсчетом количества ретикулоцитов и шизоцитов – 1–3 раза в неделю; исследование параметров КОС – 1–3 раза в неделю;
- БАК с определением уровней общего белка, альбумина, креатинина, мочевины, цистатина С, ЛДГ, АлАТ, АсАТ, билирубина общего и прямого, амилазы, липазы, глюкозы, калия, натрия, хлора, кальция, СРБ – 1–3 раза в неделю;
- определение гаптоглобина крови – 1–2 раза в неделю; ОАМ (при ее наличии) – 1–2 раза в неделю;
- определение группы крови по системе АВ0 и резус – 1 раз;
- коагулограмма с определением растворимых фибрин-мономерных комплексов – 1– 2 раза в неделю;
- прямая и непрямая (антиэритроцитарные антитела) пробы Кумбса – 1 раз; белки системы комплемента (фракции С3 и С4) – 1 раз в неделю; определение активности ADAMTS-13 – 1 раз;
- выявление аутоантител к фактору H системы комплемента – 1 раз;
- обнаружение антител к вирусу иммунодефицита человека (далее – ВИЧ) – 1 раз; бактериологическое исследование крови и мочи, отделяемого из носа и зева на аэробные и факультативно-анаэробные микроорганизмы с оценкой чувствительности выделенных микроорганизмов к АБ – 1 раз в неделю;
- анализ кала на патогенную кишечную флору, если не проводилось ранее, – 3 дня подряд;
- исследование кала экспресс методами для выявления антигенов шига-токсина и E. coli O157 (в случае отсутствия таковых методик: выделение E. coli O157:Н7 на средах с сорбитолом или обнаружение дезоксирибонуклеиновой кислоты (далее – ДНК) энтерогеморрагических E. coli в образцах стула) – 1 раз;
- УЗИ почек с оценкой кровотока и мочевого пузыря – 1–2 раза в неделю; УЗИ органов брюшной полости – 1–2 раза;
- ЭКГ – 1 раз в неделю; УЗИ сердца – 1–2 раза;
- неинвазивное измерение АД в отделении анестезиологии и реанимации – каждые 1– 3 часа;
- неинвазивное измерение АД в соматическом отделении – 4 раза в сутки – 3 суток, далее – 3 раза в сутки;
- термометрия общая – 2–3 раза в сутки.
31. Дополнительными диагностическими исследованиями в РЦДНиЗПТ являются:
- БАК с определением уровней прокальцитонина, пресепсина;
- определение D-димеров в крови;
- определение антигена вируса гепатита В, антител к вирусу гепатита С; определение NGAL в крови и при наличии диуреза – в моче;
- определение антител к шига-токсину и (или) липополисахаридам энтерогеморрагических E. coli через 10–14 дней от начала диареи;
- исследование крови с определением иммуноглобулинов классов A, M, G; определение антител к ADAMTS-13 в случае снижения ее активности менее 10 %; исследование уровней факторов H, I, MCP (CD46) в крови – у пациентов
- с подозрением на аГУС;
- определение уровней гомоцистеина крови, витамина В12 крови (при повышении среднего объема эритроцитов более 100 фемтолитров по данным ОАК), метионина, метилмалонил- и пропионилкарнитина крови (тандемная масс-спектрометрия), метилмалоновой кислоты в моче (газовая хроматография) + молекулярно-генетическое исследование с целью выявления мутаций в гене MMACHC и MMR – для подтверждения ГУС, обусловленного дефектным метаболизмом кобаламина С (далее – cblC-ГУС), и ГУС, обусловленного дефектным метаболизмом кобаламина G (далее – cblG-ГУС), соответственно;
- исследование крови на антитела к двухспиральной ДНК, антинуклеарные антитела, антитела к кардиолипину, антитела к b2-гликопротеину I, волчаночный антикоагулянт – при подозрении на вторичный ГУС;
- исследование концентрации растворимого терминального комплекса комплемента (далее – sC5b-9) крови;
- определение общей гемолитической активности комплемента крови (далее – CH50);
- определение антигена вируса гепатита B, антител к вирусному гепатиту C;
- тест на беременность (у пациентов женского пола в возрасте 14 лет и старше с клиникой ГУС или ТТП);
- молекулярно-генетическое исследование панели генов, ассоциированных с развитием аГУС: CD46, CFB, CFH, CFHR1, CFHR2, CFHR3, CFHR4, CFHR5, CFI, DGKE, PIGA, THBD, C3, ADAMTS13, SERPINE1, MTHFR, ITGA2, FGB, F13A1, F7, F5, F2, ITGB3,
- MMACHC, INF2, VTN – у пациентов с аГУС;
- проведение молекулярно-генетического исследования с целью исключения аГУС и определения дальнейшей тактики подготовки к трансплантации почки – у пациентов, перенесших ГУС и достигших терминальной стадии хронической болезни почек;
- обследование на сифилитическую инфекцию;
- консультация врача – детского невролога, врача-офтальмолога, врача-уролога, врача- акушера-гинеколога;
- УЗИ плевральных и брюшной полостей на наличие жидкости; рентгенография органов грудной клетки;
- суточное мониторирование АД;
- определение суточной потери белка с мочой (далее – СПУ) и суточной потери альбумина с мочой (при невозможности – соотношение белка и альбумина к креатинину в разовой моче);
- бактериологическое исследование диализата, ликвора на аэробные и факультативно- анаэробные микроорганизмы с оценкой чувствительности выделенных микроорганизмов к АБ;
- экспресс диагностика антигенов Streptococcus pneumoniae в моче при подозрении на рГУС;
- анализ диализата на цитоз и потерю белка;
- лейкоцитограмма диализата.
Лечение
ГЛАВА 2
ЛЕЧЕНИЕ ГУС В ОРГАНИЗАЦИЯХ ЗДРАВООХРАНЕНИЯ РАЙОННОГО (МЕЖРАЙОННОГО) И ОБЛАСТНОГО УРОВНЕЙ
18. Лечение пациентов с ГУС включает:
- коррекцию волемических расстройств, анемии, электролитного дисбаланса и параметров КОС, АГ, гипоксии и энцефалопатии, судорожного синдрома;
- нутритивную поддержку;
- установку назогастрального зонда при отказе пациента от приема жидкости и пищи через рот;
- катетеризацию мочевого пузыря при снижении диуреза или его отсутствии (при анурии более 1 суток мочевой катетер удаляется).
19. Антиперистальтические ЛП и бактерицидные антибиотики (далее – АБ) для лечения диареи, вызванной энтерогеморрагическими штаммами E. Coli, не применяются, так как это увеличивает риск развития тГУС. Назначение АБ показано при инвазивных диареях с примесью крови в стуле.
20. Лечебно-диагностическая проба для дифференциальной диагностики преренального, ренального и постренального ОПП проводится у пациентов с различными степенями дегидратации.
Лечение ОПП включает возмещение объема циркулирующей крови и стабилизацию гемодинамики:
- назначается внутривенная (далее – в/в) инфузия раствора натрия хлорида (далее – NaCl) (раствор для инфузий 9 мг/мл) 10–20 мл/кг в течение двух часов с в/в введением 1– 2 мг/кг фуросемида (раствор для инъекций (раствор для в/в и внутримышечного введения) 10 мг/мл 2 мл) после ее окончания. Если на этом фоне отмечается увеличение диуреза более 1 мл/кг в час, то диагностируется преренальное ОПП;
- при отсутствии эффекта продолжается регидратация в объеме 5–15 мл/кг в час с почасовой оценкой гидратации тканей пациента и диуреза. Если при этом сохраняется олигурия, повторно в/в вводится фуросемид (в дозе 1–2 мг/кг) через 2 и 4 часа. При появлении периферических отеков и (или) превышении центрального венозного давления (при наличии центрального венозного катетера) более 8 сантиметров водного столба инфузионная терапия прекращается и вводится в/в фуросемид 1–2 мг/кг. При отсутствии восстановления адекватного диуреза после шестичасовой инфузии (суммарно) и трех введений фуросемида (суточная доза не должна превышать 10 мг/кг в сутки) или ранее при достижении нормогидратации, диагностируется ренальное ОПП и требуется перевод пациента в больничные организации здравоохранения областного или республиканского уровней, где возможно проведение ЗПТ.
21. За время инфузионной терапии проводится УЗИ почек и мочевого пузыря с целью исключения постренальной ОПП (расширение чашечно-лоханочной системы обеих почек). Титрование дофамина в «почечных» дозах (2–4 мкг/кг в минуту) не рекомендуется.
22. При достижении эуволемии и сохранении олигурии суточный объем инфузионной терапии рассчитывается следующим образом: 400 мл/м2 поверхности тела (перспирационные потери) плюс диурез за предыдущие сутки плюс текущие патологические потери.
23. Медицинским показанием к переливанию эритроцитарной массы, обедненной лейкоцитами, или отмытых эритроцитов (10–15 мл/кг) является снижение гемоглобина менее 70 г/л или более высокие значения, но с клиническими проявлениями анемии (тахикардии, ортостатической гипотензии, застойной сердечной недостаточности и другого) или с быстрым снижением гематокрита.
24. У пациентов с ГУС без выраженной тромбоцитопении (число тромбоцитов более 20х109/л) и не имеющих тяжелых осложнений (кровотечения и иных) отсутствует необходимость в трансфузии тромбоконцентрата.
Медицинские показания для назначения тромбоконцентрата у пациентов с ГУС установлены согласно приложению 5.
25. Установлены следующие потребности пациента с ОПП в энергии и белке в зависимости от возраста:
0–6 месяцев – 95–115 ккал/кг / 1,5–2,0 г/кг;
6–12 месяцев – 95 ккал/кг / 1,5–1,6 г/кг;
1–3 года – 95 ккал/кг / 1,1 г/кг;
4–6 лет – 90 ккал/кг / 1,1 г/кг;
7–10 лет – 1740 ккал (для пациентов женского пола) и 1970 ккал (для пациентов мужского пола) / 28 г в сутки;
11–14 лет – 1845 ккал (для пациентов женского пола) и 2220 ккал (для пациентов мужского пола) / 42 г в сутки;
15–18 лет – 2110 ккал (для пациентов женского пола) и 2755 ккал (для пациентов мужского пола) / 45 г (для пациентов женского пола) и 55 г (для пациентов мужского пола) в сутки.
6–12 месяцев – 95 ккал/кг / 1,5–1,6 г/кг;
1–3 года – 95 ккал/кг / 1,1 г/кг;
4–6 лет – 90 ккал/кг / 1,1 г/кг;
7–10 лет – 1740 ккал (для пациентов женского пола) и 1970 ккал (для пациентов мужского пола) / 28 г в сутки;
11–14 лет – 1845 ккал (для пациентов женского пола) и 2220 ккал (для пациентов мужского пола) / 42 г в сутки;
15–18 лет – 2110 ккал (для пациентов женского пола) и 2755 ккал (для пациентов мужского пола) / 45 г (для пациентов женского пола) и 55 г (для пациентов мужского пола) в сутки.
26. В первый день поступления в больничную организацию необходимо отказаться от назначения жидкостей, содержащих белки (энтерально и парантерально), обеспечение суточного каллоража питания может быть недостижимо из-за ограничения потребления жидкости.
В последующие дни количество потребляемого белка определяется уровнем мочевины крови:
- более 40 ммоль/л – безбелковое высококалорийное питание;
- 30–40 ммоль/л – 0,5 г/кг «сухого» веса в сутки;
- 20–30 ммоль/л – 1 г/кг «сухого» веса в сутки;
- менее 20 ммоль/л – в соответствии с пунктом 25 настоящего клинического протокола.
27. Для коррекции тяжелого метаболического ацидоза (далее – МА) при уровне актуального бикарбоната <15 ммоль/л используется раствор гидрокарбоната натрия (далее – NaHCO3) (раствор для инфузий 40 мг/мл 100 мл и 300 мл а так же 84 мг/мл 100 мл), доза которого рассчитывается по формуле:
Доза NaHCO3 (ммоль) = (АВжелаемый – АВпациента) х МТ х к,
где АВ – актуальный бикарбонат (ммоль/л), МТ – масса тела (кг), к – коэффициент равен 0,3 до 1 года и 0,2 – после 1 года.
Инфузия рассчитанной дозы NaHCO3 проводится за 1–2 часа.
Гипонатриемия при олигоанурии чаще не требует коррекции натрием, так как обусловлена избыточным количеством гипотонических жидкостей (гипонатриемия разведения). Коррекция может быть достигнута за счет ограничения жидкости.
В случае развития тяжелой гипонатриемии (натрий менее 120 ммоль/л крови), необходимо восстанавливать его уровень за счет инфузии растворов NaCl (раствор для инфузий 9 мг/мл, 30 мг/мл, 100 мг/мл) (1 ммоль натрия = 6 мл 9 мг/мл NaCl или 2 мл 30 мг/мл NaCl, или 0,5 мл 100 мг/мл NaCl), объем которого рассчитывается по формуле:
Дефицит NaCl (ммоль) = (Na желаемый – Na пациента) х МТ х к,
где Na – натрий крови (ммоль/л), МТ – масса тела (кг), к – коэффициент равен 0,3 до 1 года и 0,2 – после 1 года.
28. Потенциально опасным для жизни пациента является развитие гиперкалиемии (более 6,0 ммоль/л), особенно при появлении признаков на ЭКГ (высокие, заостренные зубцы Т, удлинение интервала PR, снижение амплитуды зубца Р, удлинение интервала QRS и иные).
Неотложные мероприятия включают:
- ингаляцию сальбутамола* (аэрозоль для ингаляций дозированный 100 мкг/доза 200 доз, 400 доз; раствор для ингаляций 1 мг/мл, 2,5 мл) с использованием небулайзера, 1 месяц – 4 года: 2,5 мг, 5–11 лет: 2,5–5,0 мг, 12–17 лет: 5,0 мг трижды с интервалом 20 минут или с использованием аэрозоля для ингаляций у детей 5–17 лет – 100–200 мкг трижды с интервалом 20 минут;
- инфузию NaHCO3 1 ммоль/кг в/в за 30 минут при наличии МА;
- в/в введение раствора кальция глюконата (раствор для инъекций 100 мг/мл 5 мл, 10 мл) 0,5 мл/кг за 10–20 минут (максимально 20 мл на введение);
- инфузия глюкозы (раствор для инфузий 100 мг/мл, 200 мг/мл, 400 мг/мл) (0,5–1 г/кг) с аналоговым инсулином (1 ЕД инсулина на 3–4 г глюкозы) за 30–60 минут.
Консервативная терапия гиперкалиемии носит временный характер, особенно у пациентов с олигоанурией, поэтому с момента начала ее проведения, необходимо осуществлять подготовку к проведению гемодиализа (метод выбора) или других методов ЗПТ.
* Назначается по решению врачебного консилиума.
29. Неотложная терапия гипертензивного криза осуществляется ЛП, указанными в перечне согласно приложению 6.
Перечень ЛП, назначаемых при плановой антигипертензивной терапии у пациентов с ГУС, указан в приложении 7. Первыми назначаются блокаторы кальциевых каналов, при недостаточности эффекта добавляются бета-адреноблокаторы и (или) периферические антиадренергические ЛП. Если диурез не нарушен, то назначаются диуретики (при скорости клубочковой фильтрации (далее – СКФ) менее 30 мл/мин/1,73 м2 эффективен только фуросемид). В острый период ОПП на фоне азотемии и олигоанурии ингибиторы ангиотензин-превращающего фермента (далее – иАПФ) или блокаторы рецепторов ангиотензина II (далее – БРА) противопоказаны.
ГЛАВА 3
ЛЕЧЕНИЕ ГУС В РЦДНИЗПТ
32. У пациентов с ТА-ТМА также перед введением первой дозы экулизумаба проводится определение активности ADAMTS-13 и CH50, концентрации sC5b-9 крови, цистатина С крови с расчетом скорости клубочковой фильтрации, соотношения белок/креатинин разовой мочи.
На фоне терапии ТА-ТМА экулизумабом перед каждым введением осуществляются: контроль СН50;
2 раза в неделю – определение ЛДГ и sC5b-9 крови;
1 раз в неделю – ОАМ с соотношением белок/креатинин, определением гаптоглобина, свободного гемоглобина плазмы, цистатина С с расчетом СКФ.
33. Начальное лечение ГУС в стационарных условиях в РЦДНиЗПТ осуществляется в соответствии с пунктами 18–29 настоящего клинического протокола.
34. Эмпирическое лечение рГУС включает назначение комбинации следующих ЛП:
- ванкомицин в/в (порошок для приготовления раствора для инфузий 500 и 1000 мг;
- лиофилизированный порошок (лиофилизат) для приготовления раствора для инфузий 500 и 1000 мг), пациенты в возрасте 1 месяц – 11 лет: 10–15 мг/кг 4 раза в сутки
- (максимально 60 мг/кг в сутки), 12–17 лет: 15–20 мг/кг 2–3 раза в сутки (максимально 2 г на инфузию);
- цефтриаксон в/в (порошок для приготовления раствора для в/в и внутримышечного введения 250, 500, 1000 и 2000 мг), пациенты в возрасте 1 месяц – 11 лет: 50–80 мг/кг 1 раз в сутки (максимально 4 г в сутки), 12–17 лет: 1–2 г 1 раз в сутки (максимально 4 г в сутки) или меропенем в/в (порошок для приготовления раствора для в/в введения (для инъекций) 500 мг и 1000 мг), пациенты в возрасте 3 месяца – 11 лет (масса тела <50 кг): 20 мг/кг 3 раза в сутки, при массе тела >50 кг по 0,5–1,0 г 3 раза в сутки с последующим выбором ЛП в зависимости от результатов посевов и чувствительности к АБ.
Свежезамороженная плазма (далее – СЗП) противопоказана.
При возникновении необходимости переливания взвеси тромбоцитов или эритроцитов, они предварительно должны быть отмыты, чтобы исключить дополнительное попадание антител IgM к антигену Thomsen-Friedenreich пациента.
35. При развитии ГУС на фоне применения циклоспорина А или такролимуса требуется их отмена. Терапия вторичного ГУС основана на лечении основного заболевания, приведшего к его развитию.
36. Лечение аГУС, ассоциированного с мутацией гена DGKE (далее – DGKE-аГУС), в большинстве случаев ограничивается следующими нефропротективными мероприятиями:
- строгий контроль АД;
- блокада ренин-ангиотензин-альдостероновой системы с назначением иАПФ или БРА.
37. Лечение cblC-ГУС и cblG-ГУС включает:
- специальное лечебное высококалорийное питание, не содержащее метионин, треонин, валин, изолейцин;
- ограничение в рационе питания высокобелковых продуктов (мясо, творог, рыба);
- назначение цианокобаламина (раствор для инъекций 0,5 мг/мл) по 10 мг в сутки внутримышечно, фолиевой кислоты (таблетки 0,4 мг, 1 мг) по 5 мг в сутки, левокарнитина (раствор для приема внутрь 100 мг/мл) 100–200 мг/кг в сутки.
38. Лечение аГУС назначается в течение 24–48 часов с момента установления диагноза и включает комплементблокирующую терапию: гуманизированное моноклональное антитело против C5 компонента комплемента – экулизумаб (концентрат для приготовления раствора для инфузий 10 мг/мл 30 мл). Режим дозирования экулизумаба при аГУС зависит от массы тела пациента и установлен согласно приложению 8. Длительность терапии определяется видом дефектного компонента комплемента и характером течения заболевания.
При выявлении мутаций в гене CFH, CFB, С3 или наличии в анамнезе у пациента или близких родственников рецидивов аГУС, потребность в лечении экулизумабом будет пожизненной (с возможностью контролируемой отмены через 2 года). Длительность патогенетической терапии составит до двух лет (с возможностью контролируемой отмены через 1 год) в случаях выявления мутаций в гене CFI или мутаций с неизвестным эффектом или при отсутствии идентифицированных мутаций, а также у пациентов с наличием невысокого титра антител к фактору Н. До 1 года (с возможностью контролируемой отмены через 6 месяцев) терапия может понадобиться пациентам с изолированными мутациями гена CD46 (MCP), при длительном периоде отсутствия антител к фактору Н.
Под контролируемой отменой экулизумаба подразумевается тщательный мониторинг клинических и лабораторных параметров, направленных на своевременную диагностику рецидива ТМА, после его отмены, который включает контроль уровней гемоглобина, шизоцитов, тромбоцитов, ЛДГ, креатинина, протеинурии и гематурии еженедельно – 1 месяц, затем 1 раз в 2 недели – 2–4 месяца и далее 1 раз в месяц.
У пациентов с вторичным ГУС, DGKE-аГУС, рГУС, тГУС (чаще при наличии тяжелой неврологической симптоматики) и при выраженных признаках активации альтернативного пути комплемента (снижение более чем на 25 % ниже нижней границы нормы C3 фракции комплемента крови) с учетом возможной пользы и рисков по решению врачебного консилиума может быть назначен экулизумаб.
Комплементблокирующая терапия не эффективна у пациентов с cblC-ГУС и cblG- ГУС, а также с ГУС, ассоциированным с мутацией гена INF-2 или WT1.
В случае назначения экулизумаба необходимо проведение вакцинации против N. meningitidis с четырнадцатидневной медицинской профилактикой АБ, которые эффективны против менингококка и хорошо проникают через гематоэнцефалический барьер. В случае экстренного назначения экулизумаба, антибактериальная медицинская профилактика осуществляется на протяжении всего периода комплементблокирующей терапии до проведения вакцинации и затем продолжается еще 14 дней.
Комплементблокирующая терапия во время интеркуррентного заболевания, не вызванного инкапсулированными бактериями (пневмококк, гемофильная палочка), не прерывается из-за высокого риска рецидива аГУС.
39. При отсутствии возможности проведения комплементблокирующей терапии, при наличии осложнений или медицинских противопоказаний к ней у пациентов с аГУС может использоваться плазмотерапия или плазмообмены (далее – ПО). Рекомендуемая доза СЗП составляет 30–40 мл/кг в первые сутки и 10–20 мл/кг в сутки в последующем. При олигоанурии с признаками гипергидратации методом выбора является ПО. В ходе одного сеанса проводится обмен 1,5 объема плазмы (60 мл/кг). Рекомендуется проведение ПО в дозе 1,5 объема плазмы ежедневно первые 5 дней, далее 5 дней в неделю – 2 недели, далее 3 дня в неделю – 2 недели с оценкой эффективности терапии на всех этапах.
Критериями эффективности плазмотерапии является нормализация числа тромбоцитов и ЛДГ (прекращение гемолиза). При сохранении этих результатов более трех дней терапия отменяется.
Абсолютными медицинскими противопоказаниями к ПО являются:
- аллергия на введение СЗП, белковых ЛП и плазмозаменителей;
- нестабильная гемодинамика;
- тяжелая сердечная недостаточность;
- инфузия вазопрессоров (дофамина, норэпинефрина и других) в высоких дозах для поддержания гемодинамики;
- профузное кровотечение любой локализации;
- церебральный инсульт в острой фазе;
- отек легких.
Относительными медицинскими противопоказаниями к ПО являются:
- период новорожденности;
- анемия (число эритроцитов <3х1012/мл и гемоглобина <80–90 г/л);
- гипофибриногенемия (уровень фибриногена А <2,0 г/л);
- гипопротеинемия (общий белок в крови <55 г/л);
- сохраняющаяся гиповолемия.
У пациентов с плазморезистентностью (отсутствие эффекта от инфузий плазмы или ПО) или плазмозависимостью (рецидив ГУС при снижении частоты ПО или его отмене) с целью достижения стойкой ремиссии ГУС и предотвращения необратимых повреждений почек предпочтение отдается комплементблокирующей терапии при отсутствии медицинских противопоказаний к ее назначению.
40. На фоне лечения аГУС экулизумабом при получении результата уровня антител к фактору H комплемента с превышением референсных значений выставляется диагноз антительного аГУС (далее – АТ-аГУС), что потребует включения в лечение ПО и иммуносупрессивной терапии. Продолжение введения экулизумаба или его назначение (если не использовался ранее) осуществляется по решению врачебного консилиума с учетом течения заболевания и первоначального ответа на эту терапию. В случае продолжения введения экулизумаба на фоне ПО потребуется дополнительное введение ЛП в соответствии с алгоритмом введения дополнительной дозы экулизумаба при плазмотерапии, установленным согласно приложению 9.
41. Протокол ПО при АТ-аГУС включает: ежедневные ПО с заменой 1,5 объема плазмы (60 мл/кг) не менее 5 дней, далее 6 ПО через день с заменой 1,0 объема плазмы (40 мл/кг), а затем 6 ПО два раза в неделю до тех пор, пока на протяжении 2 дней уровень тромбоцитов не превысит 100х109/л и снизится число шизоцитов <2 %.
42. Протокол иммуносупрессии при АТ-аГУС включает:
- индукционную терапию глюкокортикоидами с в/в циклофосфамидом (далее – ЦФ) или ритуксимабом: преднизолон (таблетки 5 мг) / метилпреднизолон (таблетки 4 мг, 8 мг, 16 мг, 32 мг) 1/0,8 мг/кг в сутки внутрь – 4 недели, далее 1/0,8 мг/кг через сутки – 4 недели с последующим уменьшением на 0,25/0,2 мг/кг в сутки каждые 2 недели до 0,1–0,2/0,08– 0,16 мг/кг в сутки. После достижения гематологической ремиссии назначается ЦФ (порошок для приготовления раствора для в/в введения (для инъекций) 200 мг, 500 мг, 1000 мг) – в/в инфузия 500 мг/м2, каждые 3–4 недели, 2–5 доз или ритуксимаб* (концентрат для приготовления раствора для инфузий 10 мг/мл 10 мл, 30 мл, 50 мл) – две в/в инфузии по 375 мг/м2 с интервалом в 1 неделю (не назначается ПО в течение 48–72 часов после ЛП);
- поддерживающую терапию: преднизолон/метилпреднизолон 0,1–0,2/0,08–0,16 мг/кг до 12 месяцев с микофеноловой кислотой (капсулы, 250 мг; таблетки, покрытые оболочкой, 500 мг) или кишечнорастворимой формой микофеноловой кислоты (таблетки, покрытые кишечнорастворимой оболочкой, 180 мг, 360 мг) по 500–750 мг/м2 в сутки по микофеноловой кислоте внутрь или азатиоприном (таблетки 50 мг) по 1–2 мг/кг в сутки внутрь в течение 18–24 месяцев.
Если используется преднизолон + индукционная терапия (ЦФ или ритуксимаб) + поддерживающая, длительность терапии 1 год, если индукционная терапия не назначается – 2 года.
Требуется регулярный мониторинг уровня антител к фактору Н: на 7–14 день от дебюта АТ-аГУС, 28 день и далее каждые 3–6 месяцев.
Требуется регулярный мониторинг уровня антител к фактору Н: на 7–14 день от дебюта АТ-аГУС, 28 день и далее каждые 3–6 месяцев.
* Назначается по решению врачебного консилиума.
43. При подтверждении (гистологическом) или высокой вероятности диагноза ТА- ТМА, в качестве первой линии терапии рекомендуется комплементблокирующая терапия экулизумабом в соответствии с режимом дозирования экулизумаба при ТА-ТМА, установленным согласно приложению 10.
Первая доза экулизумаба у пациентов с массой тела <10 кг составляет 300 мг, 10– 39 кг – 600 мг, >40 кг – 900 мг.
У пациентов с повышенным уровнем sC5b-9 до терапии (>244 нг/мл) используется нагрузочный режим с введением экулизумаба с трехдневными интервалами до нормализации уровня sC5b-9 (не менее 5 введений). При определении нормальных значений sC5b-9 в 2 последовательных анализах осуществляется переход на еженедельный (индукционный режим, не менее 4 введений), с сохранением терапевтической минимальной концентрации экулизумаба в сыворотке >100 мкг/мл и полного подавления CH50 (<10 % от нижней границы референсного интервала).
Пациентам с нормальным значением sC5b-9 до терапии назначается индукционный режим экулизумаба с семидневными интервалами, не менее 4 доз или более до достижения контроля над активностью ТА-ТМА.
Частоту дозирования экулизумаба можно сократить, если это необходимо для достижения и поддержания его минимального терапевтического уровня, при полном подавлении CH50. Если терапевтический уровень экулизумаба не был достигнут при сокращении интервала дозирования до 48 часов, доза экулизумаба увеличивается на 300 мг. Переход на поддерживающий режим и режим снижения дозы осуществляется при сохранении терапевтического уровня экулизумаба в крови и CH50 <10 % в течение как минимум 2 последовательных введений после нормализации sC5b-9.
Экулизумаб может быть отменен после разрешения гематологических проявлений ТА-ТМА, стабилизации или улучшения синдрома полиорганной недостаточности, при сохранении нормального уровня sC5b-9 в 2 последовательных образцах крови после перехода на режим постепенного снижения.
Прекращение приема экулизумаба считается успешным, если не было признаков активности ТА-ТМА после выведения экулизумаба из крови (<25 мкг/мл) и восстановления активности CH50 до нормального уровня без повышения уровня sC5b-9.
44. Абсолютными медицинскими показаниями для начала ЗПТ при ОПП 3 стадии являются:
- сохранение анурии более 12 часов или олигурии более 24 часов;
- развитие жизнеугрожающих состояний, не поддающихся консервативной терапии: гипергидратация с отеком легких, головного мозга и резистентная к введению фуросемида; гиперкалиемия (>6,0 ммоль/л с ЭКГ признаками); уремическая энцефалопатия; злокачественная АГ.
Относительными медицинскими показаниями для начала ЗПТ у пациентов с ОПП 3 стадии и метаболическими расстройствами, не поддающимися консервативной терапии, являются:
- тяжелый МА (рН <7,2, ВЕ <–10);
-
гипо- и гипернатриемия (<120 ммоль/л и >160 ммоль/л).
45. Методами ЗПТ являются:
- перитонеальный диализ;
- интермиттирующий гемодиализ;
- постоянная вено-венозная гемофильтрация;
- постоянный вено-венозный гемодиализ;
- постоянная вено-венозная гемодиафильтрация.
При выборе метода ЗПТ учитываются тяжесть клинического состояния пациента, степень метаболических нарушений, наличие медицинских противопоказаний к определенному виду диализа, а также возраст, длина и масса тела пациента, доступность методов ЗПТ в организации здравоохранения.
46. Перитонеальный диализ является методом выбора при:
- преимущественно изолированном повреждении почек у пациентов в возрасте до 2 лет жизни;
- выраженных неврологических нарушениях;
- наличии или высоком риске геморрагических осложнений;
- тяжелой недостаточности кровообращения;
- невозможности или затруднении катетеризации центральных вен с обеспечением адекватного сосудистого доступа;
- наличии медицинских противопоказаний или отсутствии возможности проведения других методов ЗПТ.
Постоянная вено-венозная гемофильтрация (гемодиализ) является методом выбора:
- в случаях выраженной гипергидратации с отеком легких, мозга;
- при нестабильной гемодинамике, обусловленной присоединением сепсиса, развитием полиорганной недостаточности. Если при этом развивается анурия с выраженной азотемией, то пациент может быть переведен на режим постоянной вено-венозной гемодиафильтрации;
- при наличии медицинских противопоказаний к проведению перитонеального диализа.
Интермиттирующий гемодиализ является методом выбора при лечении пациентов со стабильной гемодинамикой, выраженной азотемией и гипергидратацией, с медицинскими противопоказаниями к другим методам ЗПТ.
При отсутствии возможности проведения ЗПТ с помощью методов выбора, диализ может проводиться иным доступным методом ЗПТ (при отсутствии медицинских противопоказаний).
47. У пациентов с ГУС и ОПП выявляется существенное изменение фармакокинетики всех ЛП, элиминируемых с мочой, что требует изменения дозы и кратности введения ЛП в зависимости от степени снижения СКФ и метода ЗПТ.
Лечение (амбулатория)
ГЛАВА 4
МЕДИЦИНСКОЕ НАБЛЮДЕНИЕ ПАЦИЕНТОВ С ГУС В АМБУЛАТОРНЫХ УСЛОВИЯХ
48. Медицинское наблюдение пациентов с ГУС в амбулаторных условиях в организациях здравоохранения, оказывающих медицинскую помощь по месту жительства (месту пребывания), осуществляется:
48. Медицинское наблюдение пациентов с ГУС в амбулаторных условиях в организациях здравоохранения, оказывающих медицинскую помощь по месту жительства (месту пребывания), осуществляется:
- врачами-педиатрами участковыми (врачами-педиатрами, врачами общей практики) не реже 1 раза в 3–6 месяцев;
- врачами-нефрологами РЦДНиЗПТ в соответствии с алгоритмом медицинского наблюдения пациентов с ГУС в РЦДНиЗПТ, установленным согласно приложению 11.
49. В организациях здравоохранения районного (межрайонного) и областного уровней при медицинском наблюдении пациентов с ГУС в амбулаторных условиях выполняются:
- ОАК, исследование параметров КОС, ОАМ, БАК с определением уровней креатинина, мочевины, АлАТ, глюкозы, калия, натрия, хлора, кальция общего, фосфора, железа, СРБ, других показателей по медицинским показаниям, клиренс по эндогенному креатинину (за сутки) с целью оценки СКФ, при невозможности сбора суточной мочи – использование расчетной СКФ по формуле CKiD U25–1 раз при контрольном посещении;
- УЗИ почек и мочевого пузыря – 1 раз в 6–12 месяцев.
50. В РЦДНиЗПТ при медицинском наблюдении пациентов с ГУС в амбулаторных условиях выполняются при контрольном посещении:
- БАК с определением цистатина С – 1 раз;
- исследование параметров КОС с целью выявления МА – 1 раз;
- определение СПУ, при невозможности сбора суточной мочи (пациенты раннего возраста), определение белка и креатинина в утренней порции мочи с расчетом соотношения белок (г) / креатинин (г) – 1 раз;
- определение суточной микроальбуминурии (далее – МАУ), при невозможности – определение альбумина и креатинина в утренней порции мочи с расчетом соотношения альбумин (мг) / креатинин (г) – 1 раз;
- клиренс по эндогенному креатинину (за сутки), при невозможности сбора суточной мочи – использование расчетной СКФ по формуле CKiD U25 – 1 раз.
51. При наличии АГ в амбулаторных условиях при плановой антигипертензивной терапии у пациентов с ГУС назначаются ЛП из перечня, установленного согласно приложению 7.
При выявлении МА (снижение рН крови, актуального бикарбоната менее 18 ммоль/л) назначается раствор NaHCO3 (раствор для инфузий 40 мг/мл) перорально, в дозе 0,5– 2 ммоль/кг в сутки в 3–4 приема.
52. Дальнейший объем лечения определяется стадией хронической болезни почек.
Информация
Источники и литература
-
Постановления и приказы Министерства здравоохранения Республики Беларусь об утверждении клинических протоколов 2024
- Постановления и приказы Министерства здравоохранения Республики Беларусь об утверждении клинических протоколов 2024 -
-
www.minzdrav.gov.by
- www.minzdrav.gov.by -
Информация
Приложение 1
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
Классификация ГУС в зависимости от этиологического фактора
|
№ п/п
|
Вид ГУС
|
Описание
|
|
1
|
тГУС
|
Для тГУС, вызываемого STEC (далее – STEC-ГУС), характерно наличие продромального периода в виде диареи. Заболевание начинается схваткообразными болями в животе, диарея приобретает кровянистый характер, могут присоединиться рвота, лихорадка, пациент становится бледным, вялым, отказывается от еды и питья.
У некоторых пациентов может появиться геморрагическая сыпь на коже, неврологические расстройства (судороги, кома и иные). В дальнейшем выявляется снижение диуреза вплоть до его полного исчезновения. тГУС, вызываемый S. dysenteriae I типа, как правило, осложняется бактериемией и септическим шоком, системным внутрисосудистым свертыванием крови и острым некрозом кортикального слоя почек |
|
2
|
ГУС, не ассоциированный с диареей и шига-токсином
|
Включает гетерогенную группу пациентов, у которых этиологическое значение инфекции, вызванной бактериями,
образующими шига-токсин и шига-подобные токсины, исключено |
|
2.1
|
рГУС, вызываемый Streptococcus pneumoniae, продуцирующим нейроминидазу
|
Развивается на фоне пневмонии, эмпиемы плевры, отита, менингита. Экстраренальными проявлениями являются: респираторный дистресс-синдром; неврологические нарушения; молниеносная пурпура; панкреатит; холецистит; тромбозы; кардиопатия; глухота
|
|
2.2
|
аГУС, вызываемый генетическими дефектами (мутации генов, кодирующих синтез белков-регуляторов: факторов H (CFH), I (CFI),
B (CFB), мембранного кофакторного протеина (MCP, CD46), тромбомодулина (THBD), белков 1–5, родственных фактору Н (CFHR 1–5), пропердина (CFP) и белков-активаторов системы комплемента: фактора В (CFB), C3 комплемента и компонентов С3-конвертазы) или аутоиммунной патологией (выработка аутоантител к фактору Н и I) |
Триггерами развития могут выступать острые кишечные
и респираторные инфекции, вакцинация, травмы, хирургические вмешательства и иное. Отличительными чертами аГУС являются: дебют в возрасте младше 6 месяцев и старше 5 лет жизни; волнообразное и рецидивирующее течение; наличие семейного анамнеза заболевания. Подозревается в следующих случаях: отсутствие диареи в продроме и (или) отрицательный тест на шига-токсин; стойкая тромбоцитопения более 1 недели при отсутствии сопутствующего инфекционного заболевания или сепсиса; ОПП, которое сохраняется более 4–6 недель при отсутствии наложившегося септического или гиповолемического шока; постоянно низкий уровень С3 фракции комплемента; тяжелое течение ГУС с вовлечением многих органов и систем, включая центральную нервную систему (судороги, кома и иное), не связанное с гипергидратацией, сепсисом, шоком |
|
2.3
|
Вторичный ГУС, который относится к вторичным ТМА
|
Может развиваться на фоне злокачественных новообразований, химиотерапии (митомицином, блеомицином, цисплатином), аутоиммунных заболеваний (системной красной волчанки, склеродермии, дерматомиозите, при антифосфолипидном синдроме), ВИЧ, злокачественной АГ, при приеме ЛП (ингибиторов сосудистого эндотелиального фактора роста, ингибиторов кальцинейрина (циклоспорина А, такролимуса), сиролимуса,
тиклопидина, клопидогреля, интерферона, хинина и иных) |
|
2.3.1
|
ТА-ТМА
|
Возникает в результате повреждения эндотелия после трансплантации паренхиматозных органов или гемопоэтических стволовых клеток. У реципиентов солидных органов основными триггерами ТА-ТМА могут выступать ишемически-реперфузионное повреждение, токсичность ингибиторов кальциневрина, антитело- опосредованное отторжение, инфекции, рецидив аГУС и STEC-ГУС, а у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток – инфекции, ингибиторы кальциневрина, реакция
«трансплантат против хозяина» и ЛП. ТА-ТМА, как правило, проявляется гемолизом и потреблением тромбоцитов, которым предшествует развитие АГ, а поражение почек чаще легкое и отмечается позже. Диагноз ТА-ТМА может быть подтвержден при гистологическом исследовании тканей (например, почек или слизистой желудочно- кишечного тракта). ТА-ТМА диагностируется, когда 4 из 7 следующих признаков возникают дважды в течение 14 дней: повышение уровней ЛДГ выше верхней границы нормы для данного возраста; повышение шизоцитов в периферической крови более 1 %; тромбоцитопения, определяемая как неспособность достичь восстановления тромбоцитов; более высокие, чем ожидалось, потребности в переливаниях тромбоцитов; рефрактерность к переливаниям тромбоцитов или 50 % снижение их исходного количества после полного восстановления нормального уровня тромбоцитов; анемия, определяемая как невозможность достичь независимости от трансфузий эритроцитов, несмотря на восстановление лейкоцитов; снижение гемоглобина на 10 г/л или впервые возникшая зависимость от переливаний крови; АГ при повышении систолического и (или) диастолического АД >99 перцентиля для данного пола, возраста и длины тела; протеинурия, соотношение белок/креатинин разовой порции мочи >1,0 г/г; повышение концентрации растворимого терминального комплекса комплемента (sC5b-9) выше нормы |
|
2.4
|
Редкие генетически-обусловленные варианты ГУС
|
|
|
2.4.1
|
DGKE-аГУС
|
Манифестирует чаще у пациентов в возрасте <2 лет. Триггером заболевания выступают инфекционные агенты. Может проявляться нефротическим синдромом с симптомами или без симптомов аГУС. Характерны экстраренальные проявления в виде поражения ЦНС: задержка развития; трудности обучения; расстройства
аутистического спектра |
|
2.4.2
|
cblC-ГУС и cblG-ГУС
|
Причиной является орфанное моногенное аутосомно-рецессивное заболевание – метилмалоновая ацидемия.
Выделяются 2 формы заболевания – с ранним (<1 года жизни) и поздним (с 1 года) началом. У пациентов с ранним началом часто имеются трудности с вскармливанием (рвота, срыгивания, отказ от еды), развивается гипотрофия, нарушения со стороны ЦНС (мышечная гипотония, летаргия, задержка развития, судороги, микроцефалия (гидроцефалия)), нарушения зрения (пигментная ретинопатия (нистагм)), тяжелая АГ. Для позднего начала характерны наличие легочной гипертензии, поражения ЦНС (когнитивные нарушения, атаксия, судороги, миелопатия), тяжелая АГ |
|
2.4.3
|
ГУС, ассоциированный с мутацией гена INF-2
(инвертированного формина-2) |
Манифестация чаще с протеинурии (морфологически: фокально- сегментарный гломерулосклероз). Возможен старт с развития периферической моторно-сенсорной нейропатии – болезни Шарко- Мари-Тута
|
|
2.4.4
|
ГУС, ассоциированный с мутацией гена WT1
|
Встречается у пациентов с синдром Дениса-Драша, для которого характерны следующие проявления: прогрессирующая гломерулопатия (врожденный (инфантильный) стероидрезистентный нефротический синдром, морфологически: мезангиальный склероз (фокально-сегментарный гломерулосклероз)), дисгенезия гонад и высокий риск
возникновения опухоли Вильмса в раннем возрасте |
Приложение 2
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
Стадии ОПП у пациентов с ГУС
|
Стадии ОПП
|
Уровень сывороточного креатинина (далее – SCr)
|
Скорость почасового диуреза
|
|
1
|
SCr в 1,5–1,9 раза выше исходного уровня*
|
<0,5 мл/кг в час** за 6–12 часов
|
|
2
|
SCr в 2,0–2,9 раза выше исходного уровня*
|
<0,5 мл/кг в час** за >12 часов
|
|
3
|
SCr в 3 раза выше исходного уровня*
или повышение SCr выше 353,6 мкмоль/л, или начало ЗПТ |
<0,3 мл/кг в час за >24 часов или
анурия >12 часов |
* При отсутствии исходных уровней креатинина, для оценки его повышения может использоваться верхняя граница референсного диапазона для соответствующего возраста жизни пациента.
** У пациентов до 1 года олигурия определяется при снижении скорости мочеотделения менее 1 мл/кг
в час.
Приложение 3
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
** У пациентов до 1 года олигурия определяется при снижении скорости мочеотделения менее 1 мл/кг
в час.
Приложение 3
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
Дифференциальная диагностика ГУС
|
№ п/п
|
Заболевание
|
Дифференциально-диагностические признаки
|
|
1
|
тГУС
|
положительный результат на STEC при бактериологическом исследовании кала или ректального мазка: посев на среды для выявления STEC (с сорбитолом для E. coli O157:H7); выделение ДНК STEC в образцах фекалий;
выявление в сыворотке антител к липополисахаридам наиболее распространенных серотипов STEC |
|
2
|
Сепсис
|
высокие уровни СРБ, прокальцитонина, пресепсина
|
|
3
|
Уремическая коагулопатия (при впервые выявленной терминальной стадии хронической болезни почек)
|
гипорегенераторная анемия (количество ретикулоцитов в норме или снижено);
отсутствие признаков гемолиза (нормальный уровень ЛДГ); уровни билирубина (в норме или несколько повышены); признаки хронической почечной недостаточности (задержка роста, костные деформации, уменьшение размеров почек по данным УЗИ); хорошая переносимость азотемии |
|
4
|
ТТП (наследственная или приобретенная)
|
дефицит ADAMTS-13, антитела к ADAMTS-13
|
|
5
|
Нарушение метаболизма кобаламина С и G (метилмалоновая ацидурия)
|
высокие уровни гомоцистеина и низкие уровни метионина в плазме крови;
повышение уровней метилмалоновой кислоты в крови и моче; тяжелый МА; выявления мутаций в гене MMACHC и MMR |
|
6
|
рГУС
|
ложноположительная прямая проба Кумбса (выявление антиэритроцитарных антител);
положительный экспресс тест на антигены Streptococcus pneumoniae в моче;положительный рост культуры Streptococcus pneumoniae или выделение ДНК методом полимеразной цепной реакции (кровь, ликвор); выявление антигена Томсона-Фредерикса (для подтверждения нейроминидазной активности) |
|
7
|
аГУС
|
снижение С3 фракции комплемента крови при нормальном уровне С4; дефицит факторов H, I, MCP (CD46) крови;
повышение уровня антител к фактору Н; выявления мутаций генов, кодирующих белки системы комплемента (CFH, CFI, CFB, MCP, THBD, C3 и другое) |
|
8
|
Аутоиммунные заболевания (системная красная волчанка, антифосфолипидный синдром и другое)
|
повышение уровня:
антител к двухспиральной ДНК; антинуклеарных антител; антител к кардиолипину; антител к b2-гликопротеину I; волчаночного антикоагулянта |
|
9
|
ВИЧ
|
положительные результаты лабораторных исследований на всех этапах диагностического тестирования на ВИЧ-инфекцию
|
|
10
|
Вторичный ГУС на фоне злокачественных новообразований, химиотерапии (митомицином, блеомицином, цисплатином), злокачественной АГ, после трансплантации костного мозга и солидных органов, при приеме ЛП (ингибиторов сосудистого эндотелиального фактора роста, ингибиторов
кальцинейрина (циклоспорина А, такролимуса), сиролимуса, тиклопидина, клопидогреля, интерферона, хинина и другое) |
|
Приложение 4
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
Дифференцированный подход к терапии ГУС
|
№ п/п
|
Заболевание
|
Причины
|
Лечение
|
|
1
|
тГУС
|
STEC
|
Симптоматическое
|
|
S. dysenteriae, тип 1
|
АБ, симптоматическое
|
||
|
2
|
рГУС
|
Streptococcus pneumoniae
|
АБ, СЗП противопоказана
|
|
3
|
Вторичный ГУС
|
Вирусы (ВИЧ)
|
СЗП
|
|
ЛП (противоопухолевые, антитромбоцитарные, иммунодепрессанты)
|
Отмена ЛП, назначение СЗП
|
||
|
Системные заболевания: системная красная волчанка; склеродермия; антифосфолипидный
синдром |
Глюкокортикоиды, СЗП. Пероральные антикоагулянты/ Экулизумаб
|
||
|
Идиопатический
|
СЗП.
Экулизумаб |
||
|
4
|
аГУС
|
Мутации генов, регулирующих синтез белков и компонентов комплемента: факторов H, I, В; мембранного кофакторного протеина,
тромбомодулина, C3, и иные |
ЛП, блокирующие образование мембраноатакующего комплекса (С5–
С9) комплемента: экулизумаб и иные, ПО, СЗП |
|
Антитела к фактору H
|
Экулизумаб, ПО, иммуносупрессивная терапия
|
Приложение 5
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
Медицинские показания для назначения тромбоконцентрата у пациентов с ГУС
| № п/п | Количество тромбоцитов | Медицинские показания |
|
1
|
<10х109/л
|
Все пациенты
|
|
2
|
11–19х109/л
|
Лихорадка >38 °С и (или) небольшое кровотечение, и (или) предполагаемый сепсис
|
|
3
|
20–50х109/л
|
Биопсия костного мозга и (или) спинномозговая пункция, небольшие хирургические вмешательства (внеполостные операции длительностью до 1 часа,
без кровопотери) и (или) массивное кровотечение |
|
4
|
50–100х109/л
|
«Стандартные» и «большие» хирургические вмешательства (длительность операции более 1 часа, с или без кровопотери более 10 % объема циркулирующей крови)
|
Приложение 6
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
Перечень ЛП неотложной терапии гипертензивного криза
|
№ п/п
|
ЛП
|
Форма выпуска
|
Режим дозирования
|
|
1
|
Нифедипин*
|
Таблетки 10 мг
|
перорально (сублингвально или внутрь): по 0,1–0,25 мг/кг (максимальная разовая доза – 10 мг) 2–4 раза в сутки
(максимально от 3 мг/кг в сутки до 90 мг в сутки) |
|
2
|
Эналаприл*
|
Раствор для инъекций 1,25 мг/мл 1 мл
|
в/в: разовая доза 0,005–0,01 мг/кг на введение, максимальная доза 1,25 мг/доза. Примечание:
с осторожностью при почечной недостаточности |
|
3
|
Клонидин*
|
Таблетки 0,15 мг
|
внутрь: 0,5–1 мкг/кг до максимальной суммарной дозы 25 мкг/кг в сутки (1,2 мг в сутки)
|
|
Раствор для инъекций 0,1 мг/мл 1 мл
|
в/в, не менее чем за 15 минут: у пациентов <12 лет разовая доза 2–5 мкг/кг на введение (максимально 300 мкг/доза) 3– 4 раза в сутки, у пациентов >12 лет 0,1 мг 2 раза в сутки, при необходимости повышение на 0,1 мг в сутки до 0,4 мг
2 раза в сутки |
||
|
4
|
Нитропруссид натрия*
|
Лиофилизированный порошок
для приготовления раствора для инфузий 30 мг 10 мл |
в/в титрование: 0,5–0,8 мкг/кг в минуту (доза может быть доведена до 8 мкг/кг в минуту). Примечание: при инфузии более 72 часов или снижении функции почек требуется контроль уровней тиоцианата в крови
|
|
5
|
Урапидил*
|
Раствор для в/в введения 5 мг/мл 5, 10 и 20 мл
|
в/в: начальная доза 0,5–4 мг/кг в час, поддерживающая –
0,2–2 мг/кг в час |
* Назначается по решению врачебного консилиума.
Приложение 7
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
Перечень ЛП, назначаемых при плановой антигипертензивной терапии у пациентов с ГУС
|
№ п/п
|
Класс |
Международное непатентованное название
|
Форма выпуска, начальная доза |
Кратность приема (раз в сутки)
|
Максимальная доза* |
|
1
|
Антагонисты ангиотензина II**
|
Кандесартан***
|
Таблетки 8, 16 и 32 мг.
1–5 лет: 0,2 мг/кг в сутки; 6–17 лет (масса тела <50 кг) 4–8 мг в сутки; 6–17 лет (масса тела >50 кг) 8–16 мг в сутки |
1
|
1–5 лет: максимально 0,4 мг/кг в сутки;
6–17 лет: максимально 32 мг в сутки |
|
Лозартан***
|
Таблетки, покрытые оболочкой, 12,5, 25, 50 и 100 мг.
6–17 лет (масса тела 20–49 кг) 0,7 мг/кг в сутки; 6–17 лет (масса тела >50 кг) 50 мг в сутки |
1–2
|
6–17 лет (масса тела 20–49 кг): максимально 50 мг в сутки;
6–17 лет (масса тела >50 кг): 1,4 мг/кг в сутки (максимально 100 мг в сутки) |
||
|
Валсартан***
|
Таблетки, покрытые оболочкой, 80 и 160 мг. 1,3 мг/кг в сутки (до 40 мг в сутки)
|
1
|
2,5 мг/кг в сутки (максимально 320 мг в сутки)
|
||
|
2
|
иАПФ**
|
Каптоприл***
|
Таблетки 12,5, 25 и 50 мг. 0,3–0,5 мг/кг/доза
|
2–3
|
6 мг/кг в сутки (максимально 450 мг в сутки)
|
|
Эналаприл***
|
Таблетки 2,5, 5, 10 и 20 мг. 0,1 мг/кг в сутки
|
1–2
|
0,6 мг/кг в сутки (максимально 40 мг в сутки)
|
||
|
Лизиноприл***
|
Таблетки 5, 10 и 20 мг.
0,07 мг/кг в сутки (максимально 5 мг/доза) |
1
|
0,6 мг/кг в сутки (максимально: 6–11 лет – 40 мг в сутки, 12–17 лет – 80 мг в сутки)
|
||
|
Фозиноприл***
|
Таблетки 5, 10 и 20 мг. 0,1 мг/кг в сутки
|
1
|
0,6 мг/кг в сутки (максимально 40 мг в сутки)
|
||
|
Рамиприл***
|
Таблетки 1,25 мг; таблетки (капсулы) 2,5, 5 и 10 мг. 1,25–2,5 мг в сутки
|
1
|
6 мг/м2 в сутки (максимально 20 мг в сутки)
|
||
|
3
|
Бета-адреноблокаторы
|
Карведилол***
|
Таблетки 3,125, 6,25, 12,5 и 25 мг; капсулы 6,25, 12,5 и 25 мг. 0,05 мг/кг/доза (до 6,25 мг в сутки)
|
2
|
0,7 мг/кг в сутки (максимально 25 мг в сутки)
|
|
Атенолол***
|
Таблетки 25, 50, 100 мг. 0,5–1 мг/кг в сутки
|
1–2
|
2 мг/кг в сутки (максимально 100 мг в сутки)
|
||
|
Бисопролол***
|
Таблетки, покрытые оболочкой, и капсулы 2,5, 5 и 10 мг. 2,5 мг в сутки
|
1
|
10 мг в сутки
|
||
|
Метопролол***
|
Таблетки 25, 50 и 100 мг; таблетки пролонгированного
действия 12,5, 25, 50 и 100 мг; таблетки с замедленным высвобождением 50 и 100 мг; капсулы с пролонгированным высвобождением 50 и 100 мг. 0,5–1 мг/кг в сутки |
1–2
|
2 мг/кг в сутки (максимально 200 мг в сутки)
|
||
|
Пропранолол***
|
Таблетки 10 и 40 мг. 1 мг/кг в сутки
|
2–3
|
4 мг/кг в сутки (максимально 320 мг в сутки)
|
||
|
4
|
Периферические антиадренергические ЛП
|
Доксазозин***
|
Таблетки 2 и 4 мг. 0,5–1 мг в сутки
|
1
|
4 мг в сутки
|
|
|
Амлодипин***
|
Таблетки 2,5, 5 и 10 мг. 0,1 мг/кг в сутки
|
1
|
0,6 мг/кг в сутки (максимально 10 мг в сутки)
|
|
| Селективные блокаторы кальциевых каналов с преимущественным влиянием на сосуды | Нифедипин*** | Таблетки, покрытые оболочкой с замедленным (контролируемым) высвобождением 20, 30, 40 и 60 мг. 0,25–0,5 мг/кг в сутки | 1–2 | 3 мг/кг в сутки (максимально 120 мг в сутки) |
|
5
|
ЛП центрального действия, уменьшающие стимулирующее влияние адренергической иннервации
|
Клонидин
|
Таблетки 0,15 мг. 1,5–3 мкг/кг в сутки
|
2
|
25 мкг/кг в сутки (макс. 1,2 мг в сутки)
|
|
6
|
Мочегонные ЛП
|
Фуросемид
|
Таблетки 40 мг. 0,5–2 мг/кг/доза
|
1–2
|
6 мг/кг в сутки
|
|
Гидрохлотиазид
|
Таблетки 25 и 100 мг. 0,5–1 мг/кг в сутки
|
1
|
3 мг/кг в сутки (максимально 50 мг в сутки)
|
||
|
Спиронолактон
|
Таблетки 25 и 50 мг, таблетки, покрытые оболочкой, 25
и 100 мг, капсулы 25, 50 и 100 мг. 1 мг/кг в сутки |
1–2
|
3,3 мг/кг в сутки (максимально 100 мг в сутки)
|
* Максимально разрешенные дозы для взрослых пациентов не превышаются.
** С осторожностью применяется у пациентов с СКФ менее 30 мл/мин/1,73 м2.
*** Назначается по решению врачебного консилиума.
** С осторожностью применяется у пациентов с СКФ менее 30 мл/мин/1,73 м2.
*** Назначается по решению врачебного консилиума.
Приложение 8
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
Режим дозирования экулизумаба при аГУС
|
№ п/п
|
Масса тела
|
Индукция
|
Поддерживающая терапия
|
|
1
|
>40 кг
|
900 мг 1 раз в неделю – 4 недели
|
1200 мг на 5 неделе, затем 1200 мг каждые 2 недели
|
|
2
|
30–<40 кг
|
600 мг 1 раз в неделю – 2 недели
|
900 мг на 3 неделе, затем 900 мг каждые 2 недели
|
|
3
|
20–<30 кг
|
600 мг 1 раз в неделю – 2 недели
|
600 мг на 3 неделе, затем 600 мг каждые 2 недели
|
|
4
|
10–<20 кг
|
600 мг 1 раз в неделю – 1 недели
|
300 мг на 2 неделе, затем 300 мг каждые 2 недели
|
|
5
|
5–<10 кг
|
300 мг 1 раз в неделю – 1 недели
|
300 мг на 2 неделе, затем 300 мг каждые 3 недели
|
Приложение 9
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
Алгоритм введения дополнительной дозы экулизумаба при плазмотерапии
|
№ п/п
|
Вид плазмотерапии
|
Предыдущая доза
экулизумаба |
Дополнительная доза экулизумаба после каждой
плазменной процедуры |
Время введения дополнительной дозы
экулизумаба |
|
|
1
|
Плазмаферез (далее –
ПФ) или ПО |
300 мг
|
300 мг на каждый ПФ/ПО
|
В течение 60 минуты после каждого ПФ/ПО
|
|
|
>600 мг
|
600 мг на каждый ПФ/ПО
|
||||
|
2
|
Трансфузии СЗП
|
>300 мг
|
300 мг на каждую единицу СЗП
|
За 60 минут до вливания каждой единицы СЗП
|
|
Приложение 10
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
Режим дозирования экулизумаба при ТА-ТМА
|
Масса тела
|
Первая доза экулизумаба
|
|
<10 кг
|
300 мг в/в в течение 1 часа
|
|
10–39 кг
|
600 мг в/в в течение 1 часа
|
|
>40 кг
|
900 мг в/в в течение 1 часа
|
|
Концентрация sC5b-9 в крови
|
|
|
>244 нг/мл
|
<244 нг/мл
|
|
Нагрузочный режим
|
Индукционный режим
|
|
инфузии каждые 3 дня при концентрации экулизумаба крови
>100 мкг/мл и СН50<10 % до нормализации уровня sC5b-9 или |
введение каждые 7 дней
до достижения устойчивых |
|
>5 введений
|
концентраций экулизумаба крови
>100 мкг/мл, sC5b-9<244 нг/мл |
|
Индукционный режим
|
|
|
инфузии каждые 7 дней до достижения устойчивых концентраций экулизумаба крови >100 мкг/мл, sC5b-9<244 нг/мл и СН50<10 %
в течение >4 введений или более, до достижения контроля над активностью ТА-ТМА |
и СН50<10 % в течение >4 введений
или более, до достижения контроля над активностью ТА-ТМА |
|
Поддерживающий режим
|
|
|
при массе тела <10 кг сохраняется доза 300 мг на введение, 1 раз в 2 недели, требуется 2 введения; при массе >10 кг – доза снижается на 300 мг на введение, 1 раз в неделю, требуется 4 введения
|
|
|
Режим снижения и отмены терапии
|
|
|
при массе тела 10–20 кг наименьшая доза 300 мг; >20 кг – 600 мг, 1 раз в неделю, 2 требуется 2 введения
|
|
Приложение 11
к клиническому протоколу
«Диагностика и лечение гемолитико-уремического синдрома (детское население)»
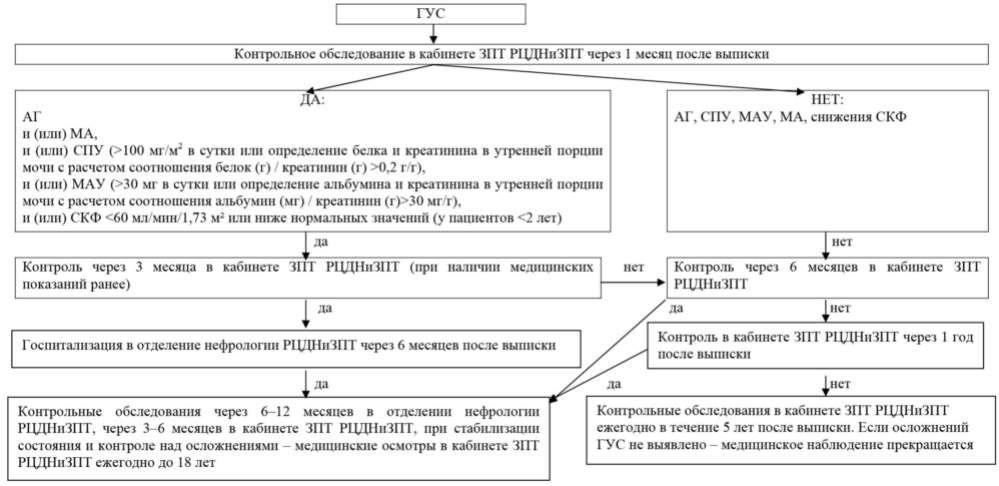
Алгоритм медицинского наблюдения пациентов с ГУС в РЦДНиЗПТ
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.