Гипертензивные состояния при беременности
 Версия: Клинические протоколы КР 2023 (Кыргызстан)
Версия: Клинические протоколы КР 2023 (Кыргызстан)
Общая информация
Краткое описание
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ КЫРГЫЗСКОЙ РЕСПУБЛИКИ
Национальный центр кардиологии и терапии при МЗ КР имени академика Мирсаида Миррахимова
Клиническая проблема:
Название документа:
Этапы оказания помощи:
Цель создания Клинического руководства:
Целевые группы:
Дата создания:
Планируемая дата обновления:
Определение и критерии диагноза
Классификация
Классификация гипертензивных состояний при беременности
Главным отличием в классификации беременных женщин с АГ по сравнению с небеременными взрослыми заключается в том, что категория гипертензивных расстройств зависит от того, на каком сроке беременности женщина находится на момент постановки первого диагноза. Двадцать недель беременности – это используемая точка отсечения, отражающая возвращение АД к исходному уровню после его снижения в первом триместре.
В настоящее время выделяют следующие основные формы АГ беременных: хроническую АГ (ХАГ), гестационную АГ (ГАГ), преэклампсию (ПЭ) и ПЭ, развившуюся на фоне ХАГ [5] (таблица 1, Приложение Б-4.).
Среди беременных с АГ хроническая АГ выявляется примерно у 30%, гестационная АГ и преэклампсия/эклампсия – у 70% пациенток [17].
Распространенность хронической АГ среди молодых женщин не велика, однако значительно возрастает по мере увеличения возраста пациенток.
Таблица 1. Классификация гипертензивных состояний у беременных
| 1. Гипертония диагностированная до беременности или до 20 недели гестации | |
| Хроническая артериальная гипертензия (эссенциальная и вторичная) |
Критерием ХАГ служит повышение АД ≥140/90 мм рт. ст. до беременности или в течение первых 20 нед., которое не исчезает после родов и обычно сохраняется в течение более 42 дней после родов.
ХАГ включает в себя следующие формы АГ:
Эссенциальная гипертензия (вторичная причина не установлена) – гипертоническая болезнь.
Вторичная (симптоматическая) гипертензия, причины которой могут включать:
• Заболевания почечной паренхимы (например, гломерулонефрит, хронический пиелонефрит со сморщиванием почки, интерстициальный нефрит, поликистоз почек, поражение почек при системных заболеваниях соединительной ткани и системных васкулитах, диабетическая нефропатия, гидронефроз)
• Реноваскулярные артериальные гипертензии (атеросклероз почечных артерий, фибромускулярная гиперплазия почечных артерий, неспецифический аорто-артериит, нефроптоз, тромбозы почечных артерий и вен, аневризмы почечных артерий)
• Опухоли почек, продуцирующие ренин
• Эндокринные (например, феохромоцитома, синдром Кушинга, первичный гиперальдостеронизм, гипер- или гипотиреоз и акромегалия).
• Коарктация аорты
• Обструктивное апноэ сна
• Прием лекарств или добавок (например, оральные контрацептивы, нестероидные противовоспалительные препараты, кортикостероиды, кокаин, стимуляторы, нейролептики).
|
| Гипертония «белого халата» |
Повышение АД при офисных измерениях (АД ≥140/90 мм рт. ст.), и АД <140/90 мм рт. ст. при самостоятельном (домашнем) измерении или при СМАД (среднесуточное АД <135/85 мм рт. ст.).
Встречается часто (30% хронической гипертензии) и связана с повышенным риском преэклампсии [18–19].
Необходимо внеофисное измерение АД (домашнее мониторирование АД (ДМАД) или СМАД) для ведения пациенток с гипертензий белого халата, так как целесообразно воздержаться от антигипертензивной терапии, если домашние значения АД в пределах нормы. При отсутствии тяжелой артериальной гипертензии (160/110 мм рт. ст.) мы предлагаем полагаться на среднее АД за несколько дней, а не на единичные показания [20].
|
| Маскированная артериальная гипертония |
Уровни АД <140/90 мм рт.ст. при офисном измерении и АД ≥140/90 мм рт.ст. при самостоятельном (домашнем) измерении или при СМАД (среднесуточное АД ≥135/85 мм рт.ст.).
Маскированная гипертензия, вероятно, менее распространена во время беременности, но об этом известно гораздо меньше, чем о гипертензии белого халата. Ее обычно диагностируют с помощью ДМАД или СМАД, которые назначаются при наличии признаков гипертензивного поражения органов-мишеней у матери (например, необъяснимой хронической болезни почек (ХБП) или гипертрофии левого желудочка сердца) или маточно-плацентарной дисфункции, но повышения уровня АД при его офисном измерении не наблюдается [5].
|
| 2. Гестационная артериальная гипертензия, диагностированная после 20 недели гестации | |
| Гестационная артериальная гипертензия |
Определяется как изолированное повышение САД ≥140 мм рт.ст. и/или ДАД >90 мм рт.ст. при измерении не менее 2 раз с интервалом в 4 ч, развивается после 20-й недели у женщин с нормальным уровнем АД до беременности, не сопровождается протеинурией и исчезает в течение 42 дней после родов.
Около 25% женщин с гестационной гипертензией на сроке менее 34 недель прогрессируют до преэклампсии и имеют более неблагоприятные исходы [21].
|
| Транзиторная гестационная гипертензия |
Выявляется в офисных условиях, но проходит после повторных измерений (например, полученных при наблюдении за АД в течение нескольких часов).
Транзиторная гестационная гипертензия связана с 40% риском последующей истинной гестационной гипертензии или преэклампсии [22], что требует дополнительного мониторинга на протяжении оставшейся части беременности, в идеале включая ДМАД/СМАД.
|
|
Преэклампсия
(de novo)
|
Преэклампсия (de novo) представляет собой гестационную АГ, сопровождающуюся одним или несколькими из следующих состояний, впервые возникших на сроке 20 и более недель:
1. Протеинурия (белок/креатинин ≥30мг/ммоль; альбумин/креатинин ≥8мг/ммоль, суточная протеинурия ≥300мг/сут; показатель индикаторной полоски ≥ «2+»)
2. Признаки дисфункции материнских органов-мишеней, в том числе:
• Неврологические осложнения (например, эклампсия, измененное психическое состояние, слепота, инсульт, клонус, сильные головные боли или стойкие зрительные скотомы)
• Отек легких
• Гематологические осложнения (например, количество тромбоцитов <150 000/мкл, ДВС-синдром, гемолиз)
• Острое поражение почек (ОПП) (например, креатинин ≥90 мкмоль/л)
• Поражение печени (например, повышение уровня трансаминаз, таких как АЛТ или АСТ) >40 МЕ/л) с болью в правом подреберье или эпигастральной области живота или без нее)
3. Маточно-плацентарная дисфункция (например, отслойка плаценты, ангиогенный дисбаланс, задержка роста плода, нарушение кровотока в артерии пуповины по данным допплеровского исследования или внутриутробная гибель плода) [5].
Обрати внимание! Для диагностики ПЭ протеинурия не должна считаться обязательной для клинического диагноза ПЭ, но часто присутствует (до 75% случаев) [23].
Обрати внимание! Другие проявления преэклампсии (например, сильная головная боль) также распространены во время беременности, но в контексте впервые развившейся гипертензии безопаснее рассматривать такую женщину как страдающую преэклампсией и проводить соответствующее лечение.
Обрати внимание! Наличие отеков не является диагностическим критерием ПЭ. При физиологически протекающей беременности частота отеков достигает 50-80%. Вместе с тем в случае резкого нарастания генерализованных отеков следует проявлять настороженность в отношении развития ПЭ, так как это может быть доклиническим или манифестным проявлением тяжелой ПЭ [24]. В зависимости от срока гестации выделяют:
Классификация ПЭ по степени тяжести
|
| Преэклампсия на фоне хронической артериальной гипертензии |
Диагностируется у беременных с хронической АГ при присоединении признаков преэклампсии.
ПЭ на фоне хронической АГ развивается в 20-50% случаев больных с ХАГ. К рискам ее развития относятся: курение, ДАД выше 100 мм рт. ст., длительность АГ более 4 лет, преэклампсия в анамнезе или наличие симптоматической АГ (в этом случае частота развития ПЭ приближается к 75%).
ПЭ на фоне ХАГ трудно дифференцировать от прогрессирования хронической гипертензии у женщин с ХАГ и исходной протеинурией. Наличие вновь возникшей тромбоцитопении или внезапное повышение уровня печеночных ферментов часто является первым признаком ПЭ на фоне ХАГ в этой группе.
Обрати внимание! У женщин с ХАГ одного повышения АД недостаточно для диагностики ПЭ на фоне ХАГ, так как такое повышение трудно отличить от обычного повышения АД после 20 недель беременности.
Обрати внимание! У женщин с протеинурической болезнью почек увеличение протеинурии во время беременности недостаточно для диагностики ПЭ на фоне ХАГ [5].
|
Классификация степеней повышения уровня АД у беременных
Таблица 2. Определение и классификация офисных показателей артериального давления (мм рт.ст.)
| Категория | Систолическое | Диастолическое | |
| Нормальное АД | <140 | и/или | <90 |
| Умеренная АГ | 140-159 | и/или | 90-109 |
| Тяжелая АГ | ≥160 | и/или | ≥110 |
Категория артериального давления (АД) определяется по наивысшему значению, не важно – систолическому или диастолическому.
Данная классификация может использоваться для характеристики степени повышения уровня АД при любой форме АГ в период беременности – ХАГ, ГАГ, ПЭ. Выделение двух степеней АГ, умеренной и тяжелой, при беременности имеет принципиальное значение для оценки прогноза, выбора тактики ведения, лечения и родовспоможения. Кроме того, известно, что тяжелая АГ при беременности ассоциируется с высоким риском развития инсульта и гипертензивной энцефалопатии даже при более низких уровнях АД в сравнении с общей популяцией [31, 32].
Ключевые рекомендации
- Рекомендуется выделять следующие основные формы АГ беременных: хроническую АГ, гестационную АГ, преэклампсию и преэклампсию, развившуюся на фоне ХАГ
- В зависимости от уровня АД рекомендуется выделять умеренную и тяжелую артериальную гипертензию независимо от сроков её возникновения
Примеры формулировки диагноза:
Беременность 12 недель. Хроническая умеренная АГ (гипертоническая болезнь) (у пациентки с установленным до беременности диагнозом при САД 140 – 159 мм рт. ст. и/или ДАД 90 – 109 мм рт. ст.).
Беременность 15 недель. Хроническая тяжелая АГ (реноваскулярная) (у пациентки с диагностированной до беременности или на ранних ее сроках реноваскулярной вторичной АГ при уровне АД > 160/110 мм рт. ст.).
Беременность 35 недель. Преэклампсия на фоне хронической АГ, умеренно выраженной степени тяжести (у беременной с ХАГ при уровне 140-159/90-109 мм рт. ст. и впервые выявленной суточной протеинурией > 0,3 г/сут при отсутствии признаков органной дисфункции).
Этиология и патогенез
Этиология и патогенез
Нормальная физиологическая реакция на беременность
Беременность представляет собой динамический процесс, во время которого наблюдается заметное увеличение метаболических потребностей и 8 гемодинамических механизмов адаптации, которые варьируются в зависимости от триместра и регрессируют к норме в послеродовом периоде.
Беременность вызывает изменения в сердечно-сосудистой системе, которые должны обеспечить увеличившиеся метаболические потребности матери и плода. С первых недель беременности и до конца I триместра снижается артериальное давление – САД на 10-15 мм рт. ст., ДАД на 5-15 мм рт. ст. Во II триместре АД остается стабильным, в III триместре повышается, достигая к моменту родов уровня АД до беременности, а в ряде случаев, превышая его на 10-15 мм рт. ст. Такая же динамика уровня АД характерна для беременных с АГ.
Объем плазмы и сердечный выброс увеличиваются максимально на 40- 50% от исходного уровня к 32-й неделе беременности, а 75% этого увеличения происходит уже к концу первого триместра. Увеличение сердечного выброса достигается за счет увеличения ударного объема в первой половине беременности и постепенного увеличения частоты сердечных сокращений после этого. Размеры камер сердца увеличиваются, при этом функции правого и левого желудочков сохранены. У женщин с сердечно-сосудистыми заболеваниями адаптация левого и правого желудочков к беременности может быть недостаточной. Дисфункция сердца у матери может приводить к нарушениям маточно-плацентарного кровотока и неблагоприятным последствиям для плода. Системное и легочное сосудистое сопротивление во время беременности снижаются [6-9].
Этиология и патогенез гестационных форм артериальной гипертензии
Патогенез ПЭ не вполне ясен, существующая в настоящее время теория развития ПЭ во время беременности предполагает две стадии процесса: на 1-й стадии происходит поверхностная инвазия трофобласта, что приводит к неадекватному ремоделированию спиральных артерий. Предполагается, что это является причиной 2-й стадии, которая включает реакцию на дисфункцию эндотелия у матери и дисбаланс между ангиогенными и антиангиогенными факторами, которые приводят к появлению клинических признаков заболевания [10,11].
В настоящее время активно обсуждается значение кальция в механизмах формирования преэклампсии. Доказано, что повышение внутриклеточного содержания кальция в эндотелиальных клетках – необходимый триггер для выработки эндотелием NO, который диффундирует из эндотелия в гладкую мышцу сосудов, способствуя синтезу циклического гуанозинмонофосфата, что в итоге приводит к расслаблению гладкой мускулатуры. При преэклампсии зарегистрировано значимое снижение продукции эндотелиальными клетками NO или его биодоступности, что непосредственно связано с дефицитом кальций-сигнализации [12, 13]. Указанные изменения распространяются не только на маточные сосуды, но и на материнскую системную артериальную и венозную сосудистую систему.
При позднем начале заболевания (с дебютом после 34 недель беременности) плацентация обычно происходит нормально, однако потребности фетоплацентарной системы превышают возможности кровоснабжения. Несмотря на то, что плацента, безусловно, играет важную роль в развитии ПЭ, появляется все больше доказательств того, что данное осложнение после 34 недель беременности развивается при участии сердечнососудистой системы и гемодинамических особенностей матери, влияющих на функцию плаценты [14].
Ключевые положения
- Ранние, чаще тяжелые формы гипертензивных нарушений (гестационная гипертензия, ранняя ПЭ), связаны с аномальной плацентацией, дисбалансом про- и антиангиогенных факторов и недостаточной перфузией плаценты, ассоциированы с высокой перинатальной и материнской заболеваемостью и смертностью.
- Поздняя ПЭ, чаще умеренная, как правило сопряжена с гемодинамическими и метаболическими особенностями организма матери и не сопровождается планцетарными нарушениями.
Эпидемиология
Эпидемиология
Осложнения АГ при беременности являются наиболее распространенными медицинскими осложнениями, затрагивающими 5-10% беременных по всему миру. Они остаются основной причиной материнской, фетальной и неонатальной заболеваемостей и смертностей [15]. Особое место при этом занимает ПЭ, частота которой во время беременности составляет 2-8%. По данным Министерства здравоохранения Кыргызской Республики в структуре материнской смертности гипертензивные расстройства при беременности в 2021 г вышли на первое место и составили 21,1% (против 7,5% в 2020г). По данным Центра электронного здравоохранения в 2022 году частота АГ в Кыргызской Республике составляла 44,3 случая на 1000 родов.
Преэклампсия является наиболее опасным из гипертензивных состояний. К материнским рискам относят отслойку плаценты, инсульт, полиорганную недостаточность и ДВС-синдром. Плод находится под высоким риском задержки внутриутробного развития (25% случаев преэклампсии), преждевременных родов (27% случаев преэклампсии) и антенатальной гибели плода (4% случаев преэклампсии). Около 2,5 млн преждевременных родов в мире обусловлены преэклампсией. Ежегодно во всем мире преэклампсия является причиной более 500 000 смертей плода и новорожденного и более 70 000 материнских смертей [16].
Поскольку последствия тяжелых гипертензивных расстройств снижают качество последующей жизни женщины, а частота нарушения физического, психосоматического развития рожденных детей достаточно высока, также, как и риск развития в будущем у них соматических заболеваний, эта проблема является значимой в социальном и медицинском плане.
Факторы и группы риска
ПРОГНОЗИРОВАНИЕ И ПРОФИЛАКТИКА ПРЕЭКЛАМПСИИ
Прогнозирование преэклампсии/эклампсии
Ни один тест не может надежно предсказать риск преэклампсии; однако сочетание параметров матери и плода может выявить более высокий риск преэклампсии. Хотя скрининг на риск преэклампсии может проводиться в любом сроке беременности, обычно его рассматривают в первом триместре (для проведения вмешательств для снижения риска в будущем) и во втором/третьем триместре (для краткосрочного прогнозирования вероятности и сроков начала преэклампсии) [5].
Клинические факторы риска развития преэклампсии
Таблица 6. Клинические факторы риска преэклампсии, выявляемые на ранних сроках беременности (с изменениями по данным Bartsch Е. et al [74]).
| Параметры | Факторы «высокого риска» (любой) | Факторы «умеренного риска» (два или более) |
| Акушерский анамнез (данные о течении предыдущей беременности) | ||
| Преэклампсия в анамнезе |
• Предшествующая отслойка плаценты
• Предшествующее мертворождение
• Предшествующая ЗРП
|
|
| Демографические данные | ||
| Индекс массы тела (ИМТ) до беременности >30 кг/м2 | Возраст матери >40 лет | |
| Ранее существовавшие заболевания | ||
|
• Хроническая гипертензия
• Предгестационный сахарный диабет
• Хроническая болезнь почек (включая женщин с трансплантацией почки)*
• Системная красная волчанка/ антифосфолипидный синдром*
|
||
| Данная беременность | ||
| Вспомогательные репродуктивные технологии** |
• Первая беременность
• Многоплодная беременность
|
|
Примечания: * – данные патологии отнесены к факторам «высокого риска» из-за более широкого спектра хронических заболеваний почек и связанных с ними неблагоприятных исходов; ** – риск зависит от используемых методов и является самым высоким среди женщин, получающих донорскую сперму или ооциты, а также после переноса замороженных эмбрионов.
Возраст матери
Количество родов в анамнезе
ПЭ в анамнезе
Исследование ПЭ в зависимости от тяжести заболевания показало, что ПЭ в анамнезе удваивает риск ранней ПЭ (в сроке <32 нед) при последующей беременности, но не поздней ПЭ [87]. В других исследованиях сообщалось, что существует риск рецидива ранней ПЭ (в сроке <34 нед беременности) у 5–17% беременных, имевших раннюю ПЭ в прошлом [87, 88]. Систематический обзор 11 исследований, в котором участвовали 2377 женщин, показал, что суммарно риск рецидива ранней ПЭ составляет примерно 8% у женщин, которым показано родоразрешение в сроках <34 нед беременности [89].
Интервалы между беременностями
Вспомогательная репродукция
Преэклампсия в семейном анамнезе
Ожирение
Расовая и этническая принадлежность
Сопутствующие заболевания
Недостатки метода скрининга на преэклампсию с использованием клинических факторов риска
По данным Национального института здоровья и клинического совершенствования (NICE) Великобритании, женщины считаются подверженными высокому риску развития ПЭ, если у них есть 1 фактор высокого риска (артериальная гипертензия при предыдущей беременности, хроническая артериальная гипертензия, хроническая болезнь почек, сахарный диабет или аутоиммунное заболевание) или 2 фактора умеренного риска (отсутствие родов в анамнезе, возраст ≥40 лет, ИМТ ≥35 кг/м2, ПЭ в семейном анамнезе или интервал между беременностями >10 лет) [153].
Важно! Скрининг с использованием только клинических факторов риска может быть полезным в клинической практике, но не является достаточным для эффективного прогнозирования ПЭ ввиду низкой чувствительности (до 40%).
Ключевые рекомендации
| Как минимум, женщины должны пройти скрининг на клинические маркеры риска преэклампсии при дородовом наблюдении | B/сильная |
Многопараметрический метод скрининга на риск развития преэклампсии
Уровень среднего АД
| СрАД следует измерять в качестве составного компонента оценки риска ПЭ с помощью сертифицированных автоматических и полуавтоматических тонометров | A/сильная |
Измерение биохимических маркеров
| В скрининге I триместра лучшим биохимическим маркером является ПФР. Маркер PAPP-A используется в тех случаях, когда измерение ПФР невозможно (недоступно) | А/сильная |
Измерение пульсационного индекса маточной артерии
С методологической точки зрения, измерение ПИ на уровне внутреннего зева в I триместре позволяет получить более воспроизводимые результаты, чем измерение на уровне пересечения наружных подвздошных артерий [177]. Кроме того, измерить ПИ на уровне внутреннего зева можно у большего числа женщин, чем на уровне пересечения наружных подвздошных артерий [177].
| Измерять пульсационный индекс маточной артерии следует во всех случаях, когда это доступно. Трансабдоминальное УЗИ следует проводить в сроке от 11 до 13 нед 6 дней [соответственно копчикотеменному размеру плода (КТР) 42–84 мм]. | А/сильная |
| Измерение ПИ должно проводиться специалистами по ультразвуковой диагностике, получившим соответствующий сертификат компетенции | А/сильная |
Для калькуляции указанных факторов риска возможно использовать калькулятор риска ПЭ, созданный фондом фетальной медицины – The Fetal Medicine Foundation (https://www.fetalmedicine.org/research/assess/ preeclampsia /first-trimester) [187].
Ключевые рекомендации
| Если тестирование доступно, после соответствующего консультирования женщин следует обследовать в 11–14 недель на риск преждевременной преэклампсии с использованием комбинации клинических факторов риска, среднего АД, индекса пульсации маточных артерий и ПФР (или РАРР-А). | А/сильная |
| В случаях, когда невозможно сделать анализ на ПФР (или РАРР-А), в базовый скрининговый тест возможно включение только клинических факторов риска, среднего АД и индекса пульсации маточных артерий. | В/слабая |
Профилактика преэклампсии
Физическая нагрузка
Физические упражнения противопоказаны всем женщинам с установленной преэклампсией и относительно противопоказаны женщинам с гестационной гипертензией [189].
Кальций
В РКИ с участием 1355 женщин с высоким риском преэклампсии на основании заболевания во время предшествующей беременности прием кальция (по сравнению с плацебо) в дозе 500 мг/сут до беременности и до 20 недель последующей беременности (с повышением уровня кальция до 1,5 г/сут после этого для всех женщин), снижал частоту преэклампсии только тогда, когда соблюдение режима приема таблеток до 20 недель (45,0%) составляло не менее 80%, и, возможно, уменьшало частоту невынашивания беременности или преэклампсии [192]. Эти данные служат для того, чтобы подчеркнуть, что низкое потребление кальция следует восполнять до беременности, если это возможно, особенно среди женщин с высоким риском, для которых соблюдение режима лечения имеет решающее значение.
Ацетилсалициловая кислота
Метод определения риска
Безопасность
Дозировка
Другие профилактические стратегии
| Всем женщинам | |
| Если нет противопоказаний, все женщины должны заниматься спортом во время беременности, чтобы снизить вероятность гестационной гипертензии и преэклампсии | В/сильная |
| Для женщин с потреблением кальция с пищей (<900 мг/день) рекомендуется пероральный прием кальция в дозе не менее 1 г/день | С/слабая |
| Женщины НЕ должны получать низкомолекулярный гепарин*, витамины С или Е или фолиевую кислоту для профилактики преэклампсии. Эта рекомендация касается использования гепарина для профилактики преэклампсии, а не по другим показаниям, таким как тромбопрофилактика при синдроме антифосфолипидных антител | D/сильная |
| Женщины с повышенным риском преэклампсии | |
| Рекомендуются низкие дозы аспирина (А/сильная) перед сном (В/сильная) желательно до 16 недель и его отмена к 36 неделе (В/сильная) | В/сильная |
| После многопараметрического скрининга следует назначить аспирин в дозе 150 мг/сут | А/сильная |
| После скрининга только клинических факторов риска и АД аспирин следует назначать в дозе 100 - 150 мг/сут | В/сильная |
Диагностика
ДИАГНОСТИЧЕСКОЕ ОБСЛЕДОВАНИЕ И МОНИТОРИНГ ЗА БЕРЕМЕННЫМИ С АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИЕЙ
Артериальную гипертензию следует определять как систолическое АД (САД) ≥140 мм рт. ст. и/или ДАД ≥90 мм рт. ст. на основании среднего значения не менее двух измерений. Если значения АД отличаются более чем на 10 мм рт. ст., следует провести третье измерение, а затем использовать среднее значение между вторым и третьим измерением.
Для подтверждения истинной артериальной гипертензии необходимо повторное измерение АД; при выраженной артериальной гипертензии (САД≥160 и/или ДАД≥110 мм рт. ст.) повторить в течение 15 мин; в случае более низких значений АД измерение следует повторить не менее чем через 4 часа или при двух последовательных амбулаторных посещениях.
Жалобы и сбор анамнеза
Рекомендуется собирать полный медицинский и семейный анамнез для оценки семейной предрасположенности к АГ и сердечно-сосудистым заболеваниям. Сбор анамнеза включает выяснение уровня АД до беременности, до 20 недель и после этого срока, сбор сведений о наличии факторов риска, субклинических симптомов поражения органов-мишеней, наличии в анамнезе сердечно-сосудистых заболеваний, церебро-васкулярных заболеваний, ХБП и вторичных форм АГ, образе жизни, предшествующем опыте лечения АГ [33].
Физикальное обследование
Следующие компоненты физикального осмотра должны рутинно документироваться при начальном обследовании [33-35]:
- определение антропометрических данных для выявления избыточной массы тела/ожирения (до беременности или на ранних сроках беременности),
- оценка неврологического статуса и когнитивной функции,
- исследование глазного дна для выявления гипертонической ретинопатии,
- пальпация и аускультация сердца и сонных артерий,
- пальпация и аускультация периферических артерий для выявления патологических шумов,
- сравнение АД между руками хотя бы однократно.
- всем пациенткам с АГ рекомендуется пальпировать пульс в покое для измерения его частоты и ритмичности с целью выявления аритмий.
Измерение артериального давления
Если в клинических условиях (на амбулаторном приеме или в стационаре) обнаруживается повышенное АД и нет признаков преэклампсии, рекомендован домашний мониторинг АД на протяжении всей беременности [5].
Домашнее мониторирование АД (ДМАД)
Если в клинических условиях (на амбулаторном приеме или в стационаре) обнаруживается повышенное АД и нет признаков преэклампсии, рекомендован домашний мониторинг АД на протяжении всей беременности. Целесообразно проверять домашний прибор для измерения АД у женщины (сравнивая с калиброванным прибором в офисе) до того, как она начнет ДМАД, а также время от времени после этого.
Данные СМАД являются лучшим предиктором поражения органов, обусловленного АГ, чем результаты офисных измерений [48]. Более того, убедительно доказано, что среднесуточное АД, зарегистрированное амбулаторно, более тесно взаимосвязано с заболеваемостью и смертностью [49-51], а также является более чувствительным предиктором риска СС исходов, в частности, фатальных коронарных событий и инсультов, чем офисное АД [51-55].
Критерии артериальной гипертонии по офисным и внеофисным значениям артериального давления, а также преимущества и недостатки методов ДМАД и СМАД представлены в Приложениях Б-2 и Б-3.
Оценка протеинурии
Протеинурия до 20 недели беременности является признаком ранее существовавшего заболевания почек. Важно выявить лежащую в основе ХБП, связанную с неблагоприятным течением беременности и отдаленными исходами во время беременности и в отдаленном периоде. Для выявления ХБП важным вторым компонентом является микроскопический анализ осадка мочи, позволяющий обнаружить эритроциты и лейкоциты, а также цилиндры.
Скрининг на протеинурию с помощью тест-полосок (ручной или автоматизированный) должен проводиться у всех женщин с АГ или у женщин с нормальным АД, но высоким риском преэклампсии при всех дородовых посещениях.
Количественное определение протеинурии (определение соотношения белок/креатинин мочи (PrCr) 30 мг/ммоль в выборочной (случайной) пробе мочи, альбумин/креатининовое соотношение ≥ 8 мг/ммоль, 2-х кратное определение белка в разовой моче или сбор мочи за 24 часа) следует проводить при подозрении на преэклампсию, в том числе:
- «1+» и выше протеинурия с помощью тест-полоски у женщин с артериальной гипертензией;
- у женщин с нормальным АД, но с симптомами или признаками, указывающими на преэклампсию.
Если подтверждающие количественные тесты на протеинурию недоступны, то протеинурия с полосками «2+» (>1 г/л) дает разумную оценку истинной протеинурии [56–57].
Инструментальные методы исследования:
- Ультразвуковое исследование (УЗИ) почек и надпочечников и исследование крови или мочи на наличие метанефринов при наличии признаков, позволяющих заподозрить феохромоцитому.
- Определение ренина, альдостерона и ренин-альдостеронового соотношения при подозрении на гиперальдостеронизм.
- Кортизол в слюне и крови, адренокортикотропный гормон при подозрении на болезнь Иценко-Кушинга и другие формы гиперкортицизма.
- Гормоны щитовидной железы (ТТГ, Т3, Т4), УЗИ щитовидной железы при подозрении на дисфункцию щитовидной железы.
- Полисомнография при подозрении синдром обструктивного апноэ сна.
Если нет симптомов и признаков, позволяющих заподозрить вторичную причину гипертензии, нет необходимости в рутинном проведении дополнительных обследований для ее исключения [5].
Ключевые рекомендации
| Артериальное давление во время беременности или после родов, следует измерять по стандартной методике с помощью устройства, утвержденного для использования при беременности и преэклампсии | А/сильная |
| Артериальную гипертензию следует определять как САД 140 мм рт. ст. и/или ДАД 90 мм рт. ст. на основании среднего значения не менее двух измерений | А/сильная |
| Для подтверждения истинной артериальной гипертензии необходимо повторное измерение АД; при выраженной артериальной гипертензии (САД 160 и/или ДАД 110 мм рт. ст.) повторить в течение 15 мин; в противном случае повторите не менее чем через 4 часа или при двух последовательных амбулаторных посещениях | В/сильная |
| Беременной пациентке с АГ рекомендовано назначить ежедневный самостоятельный мониторинг АД на протяжении всей беременности | В/сильная |
| Скрининг на протеинурию с помощью тест-полосок (ручной или автоматизированный) должен проводиться у всех женщин с АГ или у женщин с нормальным АД, но высоким риском преэклампсии (ПЭ) при всех дородовых посещениях | А/сильная |
| Количественное определение протеинурии следует проводить как часть обследования женщин с подозрением на преэклампсию или при наличии АГ с результатами скринингового теста «1+» и выше | А/сильная |
| Протеинурия должна быть определена как: - белок/креатинин мочи (PrCr) 30 мг/ммоль в выборочной (случайной) пробе мочи - альбумин/креатининовое соотношение ≥ 8 мг/ммоль - 0,3 г/л в 2-х пробах мочи с интервалом в 6 часов - или 0,3 г в суточной моче (полный сбор мочи за 24 часа) - или показатель индикаторной полоски ≥ «2+» (если другое тестирование недоступно) | А/сильная |
| Рутинное тестирование на вторичные причины гипертензии во время беременности при отсутствии клинических признаков этих состояний не рекомендуется | С/сильная |
Диагностическое обследование и наблюдение за беременными с хронической артериальной гипертензией.
Таблица 3. Хроническая артериальная гипертензия – диагностическое обследование и мониторинг [5].
| Диагностическое обследование | Мониторинг |
|
Все женщины с хронической гипертензией во время посещений должны пройти следующие тесты (РЛП):
• Микроскопия мочи и экскреция белка с мочой.
• Общий анализ крови на количество тромбоцитов (и гемоглобина);
• Креатинин сыворотки;
• Ферменты печени (АСТ, АЛТ)
При обнаружении отклонений могут быть проведены дополнительные исследования:
• электролиты,
• УЗИ почек, если креатинин сыворотки или анализ мочи с помощью тест-полоски не соответствуют норме,
• Лактатдегидрогеназа, мазок крови, если подозревается гемолиз (для анализа аномалий морфологии эритроцитов: наличие фрагментов эритроцитов (шизоцитоз, сфероцитоз) свидетельствует о развитии гемолиза при тяжелой преэклампсии).
• суточная протеинурия и сывороточный альбумин при подозрении на нефротический синдром.
Если ресурсы ограничены, нужно отдать приоритет оценке экскреции белка с мочой, определению креатинина сыворотки и подсчету числа тромбоцитов. |
Частота наблюдения должна определяться уровнем АД и другими индивидуальными рисками неблагоприятного исхода (РЛП). |
Примечание: РЛП – рекомендация лучшей практики.
Диагностическое обследование и наблюдение за беременными с гестационной артериальной гипертензией.
| Диагностическое обследование | Мониторинг |
|
Женщины должны пройти обследование на преэклампсию, чтобы исключить ее (А).
Ангиогенные маркеры* (если доступны) могут быть выполнены; если они в пределах нормы, диагноз гестационной гипертензии будет более вероятен (В).
Ультразвуковое исследование плода (при доступности) должно быть выполнено для оценки роста плода, объема амниотической жидкости и состояния маточно-плацентарного кровообращения (В).
При обнаружении ЗРП следует следовать рекомендациям ISUOG по наблюдению за плодом (РЛП).
|
Антенатальные контакты должны происходить не реже одного раза в неделю (РЛП).
Тестирование на протеинурию следует проводить при каждом последующем дородовом посещении (В).
Риск неблагоприятных материнских исходов увеличивается с более ранним гестационным сроком и/или появлением/ухудшением следующих признаков, о которых женщины должны сообщать между посещениями (А):
• головная боль/нарушения зрения
• боль в груди/одышка
• вагинальное кровотечение с болью в животе
• повышение САД (при самоконтроле)
• протеинурия с помощью тест- полоски (при самоконтроле)
• данные пульсоксиметрии (при самоконтроле).
По возможности риск неблагоприятных материнских исходов рассчитать в соответствии с моделью miniPIERS (https://pre-empt. obgyn.ubc.ca /home-page/past-projects/minipiers) (А)
УЗИ плода следует повторять не реже одного раза в месяц для оценки роста плода, объема амниотической жидкости и допплерографии пупочной артерии (В).
Если на основании клинических данных есть подозрение на преэклампсию, женщина должна быть повторно обследована на преэклампсию (А). |
Примечание: РЛП – рекомендация лучшей практики; ISUOG - Международное общество ультразвуковой диагностики в акушерстве и гинекологии; * - ангиогенный дисбаланс оценивается по сниженному плацентарному фактору роста (ПФР) (<5-го центиля для гестационного возраста) или по повышенному соотношению sFlt/ПФР; ЗРП – задержка развития плода; miniPIERS - прогностическая модель прогнозирования неблагоприятных материнских осложнений в течение первых 48ч.
Диагностическое обследование и наблюдение за беременными с преэклампсией
Таблица 5. Преэклампсия – диагностическое обследование и мониторинг [5].
| Диагностическое обследование | Мониторинг |
|
Женщины должны пройти комплексное обследование на преэклампсию (A).
Женщинам с подозрением на преэклампсию на фоне хронической гипертензии следует пройти такое же обследование, как и женщинам с преэклампсией «de novo» (A).
Для прогнозирования неблагоприятных исходов беременности в течение 48 часов у женщин, госпитализированных с преэклампсией в любом гестационном сроке возможно использовать онлайн-калькулятор fullPIERS (Preeclampsia Integrated Estimate of Risk) (https://pre-empt.obgyn .ubc.ca/home-page/past-projects/ fullpiers), который оценивает следующие параметры (A):
• срок беременности
• боль в груди или одышка
• данные пульсоксиметрии
• количество тромбоцитов
• креатинин сыворотки
• АСТ или АЛТ.
Ангиогенные маркеры* (если доступны) могут быть выполнены; если есть ангиогенный дисбаланс (см. ниже), то диагноз преэклампсии будет уточнен (B).
УЗИ плода следует проводить для оценки роста плода, объема амниотической жидкости и допплерографии пупочной и маточной артерий (B).
При обнаружении ЗРП следует следовать рекомендациям ISUOG по наблюдению за плодом [5] (РЛП).
|
Женщины с преэклампсией должны быть госпитализированы в акушерский стационар (A).
Женщины с преэклампсией на фоне хронической гипертензии должны проходить такое же наблюдение, как и женщины с преэклампсией «de novo» (A).
После подтверждения преэклампсии повторное тестирование на протеинурию не требуется (В).
Материнское тестирование, по крайней мере два раза в неделю, по возможности должно включать повторную оценку показателей fullPIERS (https://pre-empt.obgyn.ubc.ca/home-page/past-projects /fullpiers) (В):
• срок беременности
• боль в груди или одышка
• данные пульсоксиметрии
• количество тромбоцитов
• креатинин сыворотки
• АСТ или АЛТ.
При поступлении в родильное отделение женщинам с преэклампсией следует провести подсчет тромбоцитов, независимо от того, когда это было выполнена в последний раз (РЛП).
Там, где это возможно, следует проводить УЗИ плода один раз в две недели для оценки роста плода и не реже одного раза в две недели для оценки объема амниотической жидкости и допплерографию пупочной артерии (В).
Рекомендуется проводить допплерографию венозного протока на сроке менее 34 недель, когда имеются признаки ЗРП (где это возможно), для оценки риска неблагоприятного перинатального исхода (В/сильная).
Не рекомендуется использовать биофизический профиль для наблюдения за плодом, относящимся к группе риска при гипертензивной беременности (В/сильная).
|
Примечание: РЛП – рекомендация лучшей практики; ISUOG - Международное общество ультразвуковой диагностики в акушерстве и гинекологии; * - ангиогенный дисбаланс оценивается по сниженному плацентарному фактору роста (ПФР) (<5-го центиля для гестационного возраста) или по повышенному соотношению sFlt/ПФР; ЗРП – задержка развития плода; fullPIERS - прогностическая модель прогнозирования неблагоприятных материнских осложнений в течение первых 48ч.
Использование ангиогенных маркеров как руководство для лечения может снизить неблагоприятные материнские исходы (от 5% до 4%) [66], время до диагностики преэклампсии (в среднем на 2 дня) [66,67], выявить женщин с повышенным риском перинатальной тяжелой материнской заболеваемости (включая постнатальную гипертензию) [68]. Таким образом, в настоящее время имеется много доказательств к включению ангиогенных маркеров в качестве еще одного маркера маточно-плацентарной дисфункции, подобно дисрегуляции ангиогенных маркеров при ЗРП, но не в качестве единственного критерия диагностики преэклампсии. Ангиогенные маркеры могут быть особенно полезны при уже существующей протеинурии, хронической гипертензии или ХБП [69, 70].
Прогнозирование неблагоприятных исходов может быть улучшено за счет объединения ангиогенных маркеров с другими клиническими, рутинными лабораторными и ультразвуковыми данными [71–73].
Лечение
ЛЕЧЕНИЕ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ У БЕРЕМЕННЫХ
Цель лечения
Этот подход используется и у женщин с сопутствующими заболеваниями, ассоциированными с гипертонией, такими как хроническая почечная недостаточность.
Единственным исключением является гипертензия белого халата (за исключением случаев, когда уровень АД 160/110 мм рт. ст. в условиях офиса/больницы): у женщин с артериальной гипертензией внеофисное АД обычно ниже, чем офисное, но существуют большие различия и нет единого мнения в том, должно ли целевое внеофисное АД составлять 130/80 мм рт. (85 мм рт.ст.) или 135/85 мм рт.ст. (соответствует офисному АД 140/90 мм рт.ст.) [216]. В настоящее время ISSHP рекомендует использовать одинаковые целевые значения АД для внеофисного и офисного АД, чтобы свести к минимуму риск низкого АД дома [5].
Ключевые рекомендации
| Целевой уровень АД при беременности независимо от формы АГ определяется по диастолическому АД и составляет 85 мм рт.ст. Аналогичный целевой уровень АД рассматривается для женщин с ПЭ | А/сильная |
| Рекомендуется использовать одинаковые целевые значения АД для внеофисного и офисного АД, чтобы свести к минимуму риск низкого АД в домашних условиях | В/слабая |
Антигипертензивная терапия
Общие принципы медикаментозного лечения АГ у беременных:
Ключевые рекомендации
| АГТ рекомендована при АД ≥140/90 мм рт. ст. в любом сроке беременности или в послеродовом периоде под тщательным наблюдением | А/сильная |
| Беременным женщинам с АГ в качестве АГТ с целью контроля уровня АД препаратом первой линии рекомендуется назначение метилдопы и ретардной формы нифедипина | А/сильная |
| Резервными препаратами для плановой АГТ у беременных женщин с АГ являются амлодипин, бета-адреноблокаторы (бисопролол и метопролол, но не атенолол), клонидин и доксазозин | В/слабая |
| Не рекомендованы ингибиторы АПФ, блокаторы рецепторов ангиотензина II (АТ 1-подтип), прямые ингибиторы ренина, АРНИ, спиронолактон, блокаторы «медленных» кальциевых каналов: дилтиазем и фелодипин | А/сильная |
| Антигипертензивные средства, включая нифедипин, можно применять одновременно с сульфатом магния (для профилактики или лечения эклампсии) | В/сильная |
| При проведении АГТ пациентке рекомендован самостоятельный подсчет шевелений плода ежедневно | В/сильная |
Лечение умеренной (нетяжелой) артериальной гипертензии
Блокаторы кальциевых каналов, в частности нифедипин пролонгированного действия, являются лекарственными средствами первой линии в большинстве руководств [244-247, 250, 251]. Проспективное когортное исследование показало минимальный профиль тератогенности при приеме блокаторов кальциевых каналов в первом триместре [258]. Кроме того, было выявлено, что они превосходят метилдопу в отношении контроля АД и, возможно, безопаснее, чем лабеталол, в отношении достижения целевых уровней АД [255]. В одном рандомизированном контролируемом клиническом исследовании сравнивался пероральный прием нифедипина и лабеталола у беременных с ХАГ. В группе нифедипина отмечено более выраженное снижение центрального аортального давления (на 7,4 мм рт. ст.) при сопоставимом снижении периферического АД на обеих руках, а также незначительное увеличение количества госпитализаций в отделение интенсивной терапии и побочных эффектов со стороны новорождённых [259].
Пероральный лабеталол (альфа-бета-адреноблокатор) считается препаратом первого ряда при умеренной (нетяжёлой) АГ во время беременности в соответствии с международными рекомендациями [244-247, 250, 251] и фактически является единственным лекарственным средством первого ряда, рекомендованным британскими руководствами [251]. В проспективном обсервационном исследовании примерно 75% женщин имели положительный ответ на монотерапию пероральным лабеталолом [262]. В более ранних рандомизированных исследованиях, непосредственно сравнивавших его с метилдопой, не было обнаружено его преимуществ в отношении безопасности и эффективности [263, 264], а в другом исследовании показано пограничное превосходство лабеталола в профилактике протеинурии, тяжелой АГ и госпитализаций во время беременности; лабеталол также был независимо связан с меньшим количеством совокупных неблагоприятных материнских и перинатальных событий [265]. Кроме того, исследование, в котором сравнивались амбулаторные показатели АД у беременных, принимающих перорально лабеталол или нифедипин замедленного высвобождения, продемонстрировало, что в группе лабеталола отмечалось более частое снижение ДАД ниже 80 мм рт. ст., что может ассоциироваться с ухудшением маточно-плацентарной перфузии [266].
Основные и резервные препараты, используемые для лечения умеренной АГ при беременности, представлены в таблице 7.
| Препарат | Форма выпуска; дозы, способ применения | Примечание |
| Метилдопа |
Таблетки 250 мг.
Начальная доза 250 мг внутрь до или после еды 2-3 раза в сутки, далее титрация доз по уровню АД, средняя суточная доза – 1000 мг, максимальная суточная доза – 3000 мг.
|
Антигипертензивный препарат центрального действия. Препарат 1-й линии.
Наиболее изученный антигипертензивный препарат для лечения АГ в период беременности.
Осторожно применять при психической депрессии.
|
| Нифедипин-ретард |
Таблетки пролонгированного действия:
Нифедипин-ретард: прием по 20 мг 2 раза/день внутрь, не разжевывая, максимальная суточная доза – 80 мг.
Нифедипин XL: 30-60 мг 1 раз в сут, максимальная суточная доза – 60 мг.
|
Блокатор «медленных» кальциевых каналов.
Препарат 1-й линии для лечения.
АГ в период беременности и в послеродовом периоде.
Для плановой терапии не следует применять короткодействующие формы препарата (10 мг).
Показан пациенткам старше 18 лет.
Противопоказан при выраженном аортальном стенозе |
| Амлодипин |
Таблетки 5/10 мг.
Прием по 5-10 мг 1 раз/день внутрь, максимальная суточная доза – 10 мг.
|
Блокатор «медленных» кальциевых каналов.
Показан пациенткам старше 18 лет
Противопоказан при выраженном аортальном стенозе
|
| Клонидин |
Таблетки 0,15мг.
Прием по 0,075-0,15 мг 2-3 раза/день во время или после приема пищи.
|
Антигипертензивный препарат центрального действия.
Показан пациенткам старше 18 лет, с соотношением «пользы и риска».
|
| Лабеталол* |
Таблетки 100 мг
Прием 3-4 раза в день;
максимальная суточная доза 1200 мг
|
Альфа-бета-адреноблокатор
Противопоказан при неконтролируемой астме или сердечной недостаточности
|
|
Метопролола
сукцинат
|
Таблетки 25/50/100 мг.
Прием по 50-100мг 1-2 раза/день внутрь, вне зависимости от приема пищи, максимальная суточная доза– 200мг.
|
β-адреноблокатор селективный
Показан пациенткам старше 18 лет, с соотношением «пользы и риска».
Противопоказан при неконтролируемой астме
|
| Бисопролол |
Таблетки 2,5/5/10 мг.
Прием по 2,5-10 мг 1 раз/день внутрь, вне зависимости от приема пищи, максимальная суточная доза – 10 мг.
|
β-адреноблокатор селективный
Показан пациенткам старше 18 лет, с соотношением «пользы и риска».
Противопоказан при неконтролируемой астме
|
| Доксазозин |
Таблетки 1/2/4 мг.
Прием по 1 мг 1 раз в день; для достижения целевого АД суточную дозу увеличивать постепенно, соблюдая равномерные интервалы до 4 мг, 8 мг и до максимальной - 16 мг/сут.
|
Альфа-адреноблокатор
Показан пациенткам старше 18 лет, с соотношением «пользы и риска».
Противопоказан при кормлении грудью
|
При необходимости проведения комбинированной АГТ рациональными комбинациями являются:
- дигидропиридиновый антагонист кальция + β-АБ,
- дигидропиридиновый антагонист кальция + метилдопа,
- альфа-адреноблокатор + β-АБ.
Тройная комбинация:
Лечение тяжелой артериальной гипертензии
Необходимо снизить АД до уровня <160/110 мм рт. ст. в течение 60 минут. Подобная тактика может снизить частоту тяжелых материнских заболеваний [271]. Более интенсивное снижение АД может подвергнуть плод риску вследствие недостаточной перфузии. Рекомендации о постепенном снижении АД основаны на обострении церебральной ишемии при инсульте и преобладании неблагоприятных перинатальных исходов среди женщин, получавших препараты, быстро снижающие АД [272]. Тем не менее, успех был достигнут без побочных эффектов, когда АД было снижено в течение одного часа [273].
Более медленное снижение АД при тяжелой АГ возможно в случае ХАГ, отсутствия симптомов преэклампсии и у пациенток с более поздним гестационным сроком [274]. В этом случае АД необходимо снижать до уровня <160/110 мм рт.ст. с первоначальным снижением АД на 25% в первые 60 минут лечения и более постепенным снижением в последующие часы.
Тяжелая АГ, связанная с органной дисфункцией в виде отёка лёгких или острого повреждения почек, может расцениваться как гипертонический криз («emergency»), и АД в таком случае следует снижать намного быстрее. Однако при этом особое внимание следует уделять предотвращению резкого падения АД, которое может вызвать осложнения у матери или плода в результате падения ниже критических порогов перфузии. Повышенное АД следует снижать до уровня САД 130-140 мм рт.ст. / ДАД 85-90 мм рт.ст. со скоростью 10-20 мм рт.ст. каждые 10-20 мин.
В последующем (при снижении АД менее 160/110 мм рт.ст.) рекомендован перевод на двух-трехкомпонентную АГТ с использованием препаратов длительного действия.
Урапидил разрешен для лечения тяжелой АГ с осторожностью при беременности, но запрещен в послеродовом периоде на фоне грудного вскармливания [233].
При тяжелой АГ, осложненной отёком лёгких, рекомендуется использовать нитроглицерин в виде внутривенной инфузии. При любом исходном уровне АД его снижение должно быть плавным и составлять 10-20 мм рт.ст. каждые 20 минут до достижения целевого АД <140/85 мм рт.ст. Длительность его применения не должна составлять >4 ч из-за отрицательного воздействия на плод и риска развития отёка мозга у матери [276].
Применение диуретиков не показано, т.к. при преэклампсии уменьшается объем циркулирующей крови [31, 277].
Для предотвращения эклампсии и лечения судорог рекомендовано в/в введение сульфата магния [5, 278].
Препараты, используемые для лечения тяжелой АГ при беременности, представлены в таблице 8.
Таблица 8. Основные препараты для ургентной терапии тяжелой артериальной гипертонии у пациенток во время беременности
| 1. Нифедипин немедленного действия (перорально, 10 мг) | |
| Характеристика |
Блокатор кальциевых каналов (дигидропидиновый);
Применяется в качестве первоочередного лечения для быстрого снижения уровня АД;
Относится к препаратам оказания неотложной акушерской помощи
|
| ВАЖНО! |
Нифедипин применять только per os!
Не рекомендовать сублингвальное (под язык) применение из-за риска гипотонии и дистресс-плода!
|
| Начало действия |
Через 20 минут
Поэтому следует выдержать время наступления эффекта от приема препарата
|
| Режим дозирования |
Если АД через 20 минут не снижается, следует повторить прием препарата (10-20 мг в зависимости от уровня АД); если через 20 минут после приема препарата, АД не снижается, нужно повторить еще раз прием препарата (10 мг).
Схема приема общей дозы препарата: 10мг + 10мг + 10мг каждые 20 минут;
Общая продолжительность первичного лечения нифедипином немедленного действия составляет 60 минут (1час);
Внимание!!! Общая доза не должна превышать 30 мг/час.
Если после приема 30 мг нифедипина уровень АД за 1 час не снизится до уровня менее 160/110 мм рт.ст., то в данном случае для лечения гипертензии должны быть рассмотрены другие препараты (урапидил, инфузия нитроглицерина).
|
| Побочные эффекты | Возможны тахикардия и сильная головная боль у матери |
| Противопоказан | При выраженном аортальном стенозе, тахиаритмии, сердечной недостаточности (с низкой ФВ, ФК III–IV) |
| 2. Урапидил (в/в струйно или путем длительной в/в инфузии) | |
| Характеристика |
Альфа1-адреноблокатор;
Резервный препарат для лечения резистентной АГ;
Относится к препаратам оказания неотложной акушерской помощи;
Разрешён с осторожностью при беременности, но запрещен в послеродовом периоде на фоне грудного вскармливания
|
| ВАЖНО! | Урапидил вводят в/в струйно или путем длительной инфузии (пациентка должна находиться в положении лежа). |
| Начало действия | Через 2 минуты |
| Режим дозирования |
Для управляемого (контролируемого) снижения АД препарат урапидил вводят в/в в дозе 25 мг (0,5% - 5 мл). Рекомендуемая максимальная начальная скорость – 2 мг/мин. Снижение АД ожидается в течение 2 минут после введения. Если АД снизилось, то далее вводится поддерживающая доза 9 мг/ч, затем дозу уменьшают.
• Если АД не снизилось после первой дозы урапидила, то через 2 минуты вводят повторную в/в инъекцию урапидила в дозе 25 мг. Рекомендуемая максимальная начальная скорость – 2 мг/мин. Снижение АД также ожидается в течение 2 минут после введения. Если АД снизилось, то далее вводится поддерживающая доза 9 мг/ч, которую затем уменьшают.
• Если АД не снизилось после второй дозы урапидила, то через 2 минуты осуществляют медленное в/в введение урапидила в дозе 50 мг. Рекомендуемая максимальная начальная скорость - 2 мг/мин. Далее назначается поддерживающая доза 9 мг/ч, которую затем уменьшают.
• Поддерживающая в/в капельная или непрерывная инфузия урапидила проводится с помощью инфузомата. Поддерживающая доза – в среднем 9 мг/ч, т.е. 250 мг препарата урапидила (10 ампул по 5 мл или 5 ампул по 10 мл) разводят в 500 мл раствора для инфузий (1 мг = 44 капли = 2,2 мл). Максимальное допустимое соотношение – 4 мг препарата урапидила на 1 мл раствора для инфузий. Скорость капельного введения зависит от показателей АД пациентки.
• Особое внимание следует уделять предотвращению резкого падения АД, которое может вызвать осложнения у матери или плода в результате падения ниже критических порогов перфузии. Повышенное АД следует снижать до уровня САД 130-140 мм рт. ст., ДАД 85-90 мм рт. ст. со скоростью 10-20 мм рт. ст. каждые 10-20 минут.
|
| Побочные эффекты: | Тошнота, рвота, головная боль, тахикардия, боль в груди, аритмия. |
| Применять осторожно: | При коарктации аорты и открытом аортальном протоке. |
| 3. Нитроглицерин (в/в инфузия) | |
| Характеристика |
Вазодилатирующее средство – нитрат;
Показан при тяжелой АГ, осложненной отёком лёгких
|
| ВАЖНО! |
Нитроглицерин вводят в/в путем длительной инфузии (пациентка должна находиться в положении лежа).
Длительность его применения не должна составлять >4ч из-за отрицательного воздействия на плод и риска развития отёка мозга у матери.
|
| Начало действия |
1-2 мин
АД следует снижать со скоростью примерно 10-20 мм рт.ст. в течение 20 мин, после чего следует снижать скорость до достижения целевого АД <140/85 мм рт.ст.
|
| Режим дозирования |
Инфузионный раствор, содержащий 100 мкг/мл нитроглицерина (готовят путем разведения 1 ампулы Нитроглицерина 10 мг/мл (=20 мг нитроглицерина) в 200 мл 0,9% раствора натрия хлорида). Внутривенную инфузию можно начинать со скоростью 10-20 мкг/мин (2-4 кап/мин). В дальнейшем скорость можно увеличивать на 10-20 мкг/мин каждые 5-10 минут, в зависимости от реакции АД. Хороший терапевтический эффект наблюдается при скорости введения 50-100 мкг/мин. Максимальная доза составляет 8 мг нитроглицерина в час (133 мкг/мин) |
| Побочные эффекты: | Тахикардия, головная боль, покраснение лица, флебиты |
| Применять осторожно: | При гиповолемии, гипертрофической обструктивной кардиомиопатии, констриктивном перикардите, токсическом отеке легких; анемии; острой сосудистой недостаточности; артериальной гипоксемии. |
| 4. Метилдопа (перорально) | |
| Характеристика |
Агонист центральных альфа2-адренергических рецепторов.
В связи с относительно медленным развитием гипотензивного эффекта метилдопа не относится к препаратам выбора для купирования тяжелой гипертензии у беременных.
|
| Начало действия | Через 10-15 мин, максимальное снижение АД через 4-6 часов |
| Режим дозирования | При тяжёлой АГ показан прием per os 500 мг одномоментно (2 таб), допустимая суточная доза – 2000 мг |
| Побочные эффекты |
Может вызвать ортостатическую гипотензию, задержку жидкости, брадикардию.
Может маскировать повышение температуры при инфекционных заболеваниях.
|
| Применять осторожно | При психической депрессии, av-блокаде II-III степени, активных заболеваниях печени. |
| 5. Лабеталол* (в/в) | |
| Характеристика |
Альфа-бета-адреноблокатор
Применяется в качестве первоочередного лечения для быстрого снижения уровня АД;
Относится к препаратам оказания неотложной акушерской помощи
|
| Начало действия | Через 5 минут, пик действия – 30 мин |
| Режим дозирования |
В/в струйно: 20 мг в течение 2 минут;
при необходимости каждые 10 минут вводят 40–80 мг; максимальная доза 300 мг.
|
| Побочные эффекты | Информировать неонатологов о том, что женщина принимает лабеталол, т.к. препарат вызывает брадикардию у плода |
| Применять осторожно | Противопоказан при неконтролируемой астме и сердечной недостаточности |
Примечание: * - отсутствует в КР
| При тяжелой АГ у беременных | |
| При показателях САД ≥160 мм рт. ст. и/или ДАД ≥110 мм рт. ст. рекомендовано немедленное начало антигипертензивной терапии и госпитализация | С/сильная |
| Желательно снизить уровень АД <160/110 мм рт.ст. в течение 60 минут | С/сильная |
| При любом исходном уровне АД его снижение должно быть плавным и составлять 10-20 мм рт.ст. каждые 20 минут | В/сильная |
| Более медленное снижение АД при тяжелой АГ возможно в случае ХАГ, отсутствия симптомов преэклампсии и у пациенток с более поздним гестационным сроком | С/слабая |
| Препаратами выбора для лечения тяжелой АГ являются короткодействующий нифедипин, лабеталол* и урапидил | В/сильная |
| При тяжелой АГ, осложненной отёком лёгких, рекомендуется использовать нитроглицерин в виде внутривенной инфузии | А/сильная |
| При проведении экстренной антигипертензивной терапии следует опасаться чрезмерного снижения уровня АД, способного вызвать нарушение перфузии головного мозга матери, плаценты и вызвать ухудшение состояния плода | В/сильная |
| В последующем (при снижении АД менее 160/110 мм рт.ст.) рекомендован перевод на двух-трехкомпонентную антигипертензивную терапию с использованием препаратов длительного действия | В/сильная |
Примечание: * - отсутствует в КР
Подробно протокол магнезиальной терапии и тактика лечения преэклампсии приведены в соответствующих национальных клинических рекомендациях («Преэклампсия тяжелой степени. Эклампсия» [212]).
Ключевые рекомендации
| Женщины с эклампсией должны получать сульфат магния для предотвращения повторных припадков | А/сильная |
| Женщины с преэклампсией, у которых есть протеинурия и тяжелая гипертензия или гипертензия с неврологическими признаками или симптомами, должны получать сульфат магния для профилактики эклампсии | А/сильная |
| Показания к родам с любым видом гипертензивного нарушения (ХАГ, ГАГ, ПЭ) в любом гестационном сроке (А/сильная) включают: |
|
• Патологические неврологические признаки (такие как эклампсия, сильная головная боль или повторяющиеся зрительные скотомы);
• Повторяющиеся эпизоды тяжелой артериальной гипертензии, несмотря на поддерживающую терапию тремя классами антигипертензивных средств;
• Отек легких;
• Прогрессирующая тромбоцитопения или число тромбоцитов <50 ×109/л;
• Переливание любого препарата крови;
• Увеличение уровня креатинина в сыворотке;
• Увеличение ферментов печени;
• Печеночная дисфункция (МНО > 2 при отсутствии ДВС-синдрома или применения варфарина), гематома или разрыв печени;
• Отслойка плаценты с признаками патологии матери или плода;
• Тяжелое состояние плода (включая смерть).
|
| Решение о тактике не должно основываться исключительно на степени протеинурии (С/сильная), или гиперурикемии (С/сильная) |
Выжидательная тактика при преэклампсии связана с очень высокой перинатальной смертностью (>80%), а также с частыми материнскими осложнениями (в 27–71% случаев), которые могут включать смертельные исходы [5, 282]. Следует обсудить прерывание беременности и принять во внимание предпочтения пациентки, а также направить её в специализированный стационар.
При сроке (37+0 недель) женщинам с преэклампсией следует предлагать роды на основании результатов исследования HYPITAT [181]. У 2/3 женщин в исследовании HYPITAT, у которых была гестационная гипертензия в доношенном сроке, не наблюдалось повышения неблагоприятных исходов для матери (ОШ 0,81, 95% ДИ 0,63, 1,03) [285]. Женщины с гестационной гипертензией или с хронической гипертензией могут получить пользу от своевременного родоразрешения в сроке 38+0 – 39+6 недель, основываясь на данных наблюдений [5, 286].
Таблица 9. Рекомендации по родоразрешению в зависимости от гестационного срока при различных видах гипертензивных состояний.
| Гестационный срок | Преэклампсия | Гестационная гипертензия | Хроническая гипертония |
| Плод нежизнеспособен | Следует обсудить прерывание беременности (С/слабая) | Выжидательная тактика, если нет показаний к родам и стабильной гемодинамике и наличия положительного эффекта от проводимой терапии (С/сильная) | Выжидательная тактика, если нет показаний к родам и стабильной гемодинамике и наличия положительного эффекта от проводимой терапии (D/сильная) |
| Плод жизнеспособный, срок до 33+6 недель | Следует рассмотреть выжидательную тактику, но только в тех стационарах, где можно обеспечить уход за глубоко недоношенными детьми и больными матерями (В/слабая) | ||
| 34 +0 до 36 +6 недель | В 340 - 36+6 недель следует обсудить родоразрешение, так как это снижает материнский риск, но увеличивает неонатальный риск, особенно если антенатальные кортикостероиды не назначаются (В/сильная) | ||
| ≥37 +0 недель | Рекомендуется родоразрешение (А/сильная) |
Женщинам, достигшим 40+0 недель, следует предложить родоразрешение (С/сильная)
Женщинам
в сроке 37+0 39+6 недель можно предложить родоразрешение (С/слабая)
|
Женщинам, достигшим 40+0 недель, следует предложить родоразрешение (С/сильная)
Начало родов
можно предложить в сроке от 38+0 до 39+6 недель (С/слабая)
|
Ключевые рекомендации
| Женщинам с хронической артериальной гипертензией |
|
Женщинам с хронической артериальной гипертензией следует предпочесть выжидательную тактику в период от жизнеспособности плода до гестационного срока <37+0 недель, если нет показаний к родоразрешению (С/сильная).
Начало родоразрешения может быть предложено в сроке гестации от 38+0 до 39+6 недель (С/слабая), но рекомендуется от 40+0 недель гестации (С/сильная).
|
| Женщинам с гестационной гипертензией |
|
Женщинам с гестационной гипертензией следует проводить выжидательную тактику в период от жизнеспособности плода до <37+0 недель, если нет показаний к родоразрешению (D/сильная).
Если гестационная гипертензия возникает до 37+0 недель, родоразрешение может быть предложено в сроке от 38+0 до 39+6 недель беременности (С/слабая), но рекомендуется от 40+0 недель беременности (С/сильная).
Для женщин со сроком гестации 37+0 недель или позже следует обсудить начало родов и возможное родоразрешение (В/сильная).
|
| Для женщин с преэклампсией |
|
Для женщин с преэклампсией выжидательную тактику можно рассматривать с момента жизнеспособности плода до гестационного срока <34+0 недель, но только в перинатальных центрах, способных выхаживать глубоко недоношенных детей (В/слабая).
В сроке гестации 34+0–35+6 недель следует обсудить начало родов, так как это снижает материнский риск, но увеличивает неонатальный риск, особенно если антенатальные кортикостероиды не назначаются (В/сильная).
В сроке гестации 36+0–36+6 недель следует рассмотреть начало родов (В/сильная).
На 37+0 неделе беременности или позже рекомендуется начало родов (А/сильная).
|
Методы родоразрешения.
Ключевые рекомендации:
| Рекомендуется использование простагландинов при "незрелой" шейке матки с целью повышения шансов успешного родоразрешения при стабильной гемодинамике и удовлетворительном ответе на проводимую антигипертензивную терапию [287] (А) |
| Кесарево сечение возможно при повышении индекса резистентности в сосудах пуповины, что почти вдвое снижает процент успешных вагинальных родов (> 50%), а также при нулевом или реверсном кровотоке (по данным ультразвукового допплерографического исследования) (С) |
| Рекомендуется противосудорожная и антигипертензивная терапия на протяжении всего периода родоразрешения с достижением целевых уровней САД 130-135 мм рт. ст. и ДАД 80-85 мм рт. ст. (В) |
| Метилэргометрин НЕ рекомендуется с целью профилактики кровотечения в 3-м и раннем послеродовом периоде (противопоказан при АГ) (С) |
В 3-м периоде введение утеротонических препаратов должно выполняться для профилактики кровотечения: окситоцин 10 ЕД внутримышечно и/или 5 ЕД внутривенно капельно (под строгим контролем гемодинамики) (активное ведение III периода родов) [288].
Прогноз
ПОСЛЕРОДОВАЯ АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ И ВОПРОСЫ РЕАБИЛИТАЦИИ
Краткосрочные риски
Антигипертензивная терапия должна быть продолжена и направлена на то же целевое АД, что и до родов (ДАД <85 мм рт.ст.). Хороший контроль АД в течение нескольких месяцев после гипертензивной беременности может привести к уменьшению жесткости аорты, снижению АД и уменьшению сердечно-сосудистого риска в долгосрочной перспективе. Недавнее рандомизированное контролируемое исследование показало, что самоконтроль послеродовой гипертензии для достижения хорошего контроля АД в первые шесть недель после родов был связан с более низким ДАД через шесть месяцев после родов [5].
Пациенткам следует рекомендовать грудное вскармливание, поскольку, как показали обсервационные исследования, грудное вскармливание связано с более низким послеродовым артериальным давлением у женщин с гестационной гипертензией [292].
| 1. Рекомендуется наблюдение в палате интенсивной терапии до стабилизации состояния родильницы (минимум 24 часа) (В/сильная) |
| 2. Пациенток с тяжелой АГ и тяжелой ПЭ во время беременности рекомендуется выписывать не ранее 7 суток после родов (В/сильная) |
| 3. Антигипертензивную терапию, проводимую до родов, следует продолжать после родов. Также следует рассмотреть возможность назначения антигипертензивной терапии при любой артериальной гипертензии, диагностированной до шести дней после родов (С/слабая) |
| 4. При лактации не рекомендуется назначение диуретиков (фуросемид, гидрохлоритиазид и спиронолоктон), так как они могут снижать выработку молока (А/сильная) |
| 5. Целевое значение ДАД для послеродового антигипертензивного лечения должно составлять 85 мм рт. ст., как и в антенатальном периоде (С/слабая) |
| 6. Нестероидные противовоспалительные препараты для послеродовой анальгезии могут применяться у женщин с преэклампсией, если другие анальгетики неэффективны, и нет острого повреждения почек (ОПП) или других факторов риска (С/слабая) |
| 7. Рекомендуется грудное вскармливание (В/сильная) |
| 8. Следует информировать женщину о рисках гестационной гипертензии (не менее 4%) или преэклампсии (не менее 15%) при следующей беременности (В/сильная) |
| 9. Через 3 месяца после родов все женщины должны пройти обследование, чтобы убедиться, что АД, анализ мочи и любые лабораторные отклонения нормализовались. Если протеинурия или артериальная гипертензия сохраняются, то следует провести углубленное обследование (В/сильная) |
| 10. Через 6 месяцев после родов, по возможности, все женщины должны пройти повторное обследование, при АД ≥120/80 мм рт.ст. обсудить изменения образа жизни (В/сильная) |
| 11. После беременности, осложненной артериальной гипертензией, особенно преэклампсией, следует проинформировать женщину о высоких рисках для ее здоровья (особенно сердечно-сосудистых) и ее детей (В/сильная) |
| 12. Рекомендуется рассчитывать показатели сердечно-сосудистого риска в течение жизни (не 10 лет) для оценки сердечно-сосудистого риска у этих женщин (В/сильная) |
| 13. Рекомендуется ежегодное медицинское обследование после беременности с артериальной гипертензией в течение первых 5-10 лет после родов (С/слабая) |
| 14. После гипертензивной беременности все женщины и их дети должны вести здоровый образ жизни, который включает в себя правильное питание, физические упражнения, стремление к идеальной массе тела, отказ от курения и стремление к снижению АД <120/80 мм рт.ст. (А/сильная) |
Госпитализация
ОРГАНИЗАЦИЯ МЕДИЦИНСКОЙ ПОМОЩИ
Амбулаторное наблюдение беременных с АГ (при условии регулярного посещения учреждений первичного звена здравоохранения и мониторинга состояния беременной и плода) возможно при: медикаментозно контролируемом стабильном АД, нормальных показателях уровней тромбоцитов, креатинина и печеночных трансаминаз, а также отсутствии признаков ЗРП и нарушения кровотока по данным ультразвукового допплерографического исследования возможно.
Рекомендуется госпитализация беременных в стационар:
Тактика при хронической артериальной гипертензии (до 20 недели гестации):
Модели помощи могут включать серийные визиты в дневные отделения или уход на дому, но любая модель должна включать регулярные контакты для наблюдения за прогрессированием заболевания. Частота наблюдения должна определяться уровнем АД и другими индивидуальными рисками неблагоприятного исхода (наличие поражения органов-мишеней, сопутствующих сердечно-сосудистых заболеваний).
При тяжелой ХАГ (уровень АД ≥160/110 мм рт.ст.) показана госпитализация в стационар терапевтического (кардиологического) профиля, после 32 недели – в стационар акушерского профиля для решения вопроса о целесообразности пролонгирования беременности [211].
Тактика при гестационной артериальной гипертензии (после 20 недели гестации):
Модели помощи могут включать серийные визиты в акушерские дневные отделения или уход на дому, но любая модель должна включать регулярные контакты для наблюдения за прогрессированием заболевания.
При амбулаторном наблюдении антенатальные контакты должны происходить не реже одного раза в неделю с тестированием на протеинурию и оценкой риска неблагоприятных материнских исходов. По возможности риск материнских исходов должен оцениваться в соответствии с моделью miniPIERS (https://pre-empt.obgyn.ubc.ca/home-page/past-projects/ minipiers). УЗИ плода следует повторять не реже одного раза в месяц для оценки роста плода, объема амниотической жидкости и допплерографии пупочной артерии.
При тяжелой ГАГ (уровень АД ≥ 160/110 мм рт.ст.) показана госпитализация в стационар акушерского профиля [211].
Женщины, независимо от формы АГ, находящиеся на амбулаторном лечении [5]:
Уровень АД сам по себе не является надежным способом стратификации непосредственного риска при преэклампсии, поскольку у некоторых женщин может развиться серьезная дисфункция органов-мишеней или маточно-плацентарная дисфункция при минимально повышенном АД. Однако при повышении АД до 160/110 мм рт. ст. и выше женщинам требуется срочное стационарное наблюдение и лечение, учитывая дальнейшее повышение риска неблагоприятных исходов для матери и плода [211].
Информация
Источники и литература
-
Клинические протоколы Министерства здравоохранения Кыргызской Республики
- Клинические протоколы Министерства здравоохранения Кыргызской Республики - 1. Williams B., Mancia G., Spiering W., Agabiti Rosei E., Azizi M., Burnier M., et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension. Eur Heart J. 2018; 39(33): 3021– 104. 2. Magee L.A., Pels A., Helewa M., Rey E., von Dadelszen P., Canadian Hypertensive Disorders of Pregnancy Working Group. Diagnosis, evaluation, and management of the hypertensive disorders of pregnancy: executive summary. J Obstet Gynaecol Can. 2014; 36(5): 416-441. 3. American College of Obstetricians and Gynecologists. ACOG Practice Bulletin No. 125: Chronic hypertension in pregnancy. Obstet Gynecol. 2012; 119(2 Pt 1): 396-407. 4. Brown M.A., Magee L.A., Kenny L.C., Karumanchi S.A., McCarthy F.P., Saito S., et al. The hypertensive disorders of pregnancy: ISSHP classification, diagnosis & management recommendations for international practice. Pregnancy Hypertens. 2018; 13: 291-310. 5. The 2021 International Society for the Study of Hypertension in Pregnancy classification, diagnosis & management recommendations for international practice. Practice Guideline Pregnancy Hypertens. 2022 Mar;27:148-169. 6. Kampman M.A., Valente M.A., van Melle J.P., Balci A., Roos-Hesselink J.W., Mulder B.J., van Dijk A.P. et al. Cardiac adaption during pregnancy in women with congenital heart disease and healthy women. Heart 2016;102:1302–1308. 7. Cornette J, Ruys TP, Rossi A, Rizopoulos D, Takkenberg JJ, Karamermer Y, Opic P, Van den Bosch AE, Geleijnse ML, Duvekot JJ, Steegers EA, Roos-Hesselink JW. Hemodynamic adaptation to pregnancy in women with structural heart disease. Int J Cardiol 2013;168:825–831. 8. Wald RM, Silversides CK, Kingdom J, Toi A, Lau CS, Mason J, Colman JM, Sermer M, Siu SC. Maternal cardiac output and fetal doppler predict adverse neonatal outcomes in pregnant women with heart disease. J Am Heart Assoc 2015;4:e002414. 9. Pieper PG. Use of medication for cardiovascular disease during pregnancy. Nat Rev Cardiol 2015;12:718–729. 10. Jim B., Karumanchi S.A. Preeclampsia: Pathogenesis, Prevention, and Long-Term Complications. Semin Nephrol. 2017; 37(4): 386-397. 11. Chaiworapongsa T., Chaemsaithong P., Yeo L., Romero R. Pre-eclampsia part 1: current understanding of its pathophysiology. Nat Rev Nephrol. 2014; 10(8): 466-480. 12. Boeldt D.S., Bird I.M. Vascular adaptation in pregnancy and endothelial dysfunction in preeclampsia. J. Endocrinol. 2017; 232(1): 27–44. DOI: 10.1530/JOE-16-0340. 13. Alnaes-Katjavivi P., Roald B., Staff A.C. Uteroplacental acute atherosis in preeclamptic pregnancies: rates and clinical outcomes differ by tissue collection methods. Pregnancy Hypertens. 2020; 19: 11–17. DOI: 10.1016/j. preghy.2019.11.007. 68 14. Thilaganathan B. Pre-eclampsia and the cardiovascular-placental axis. Ultrasound Obstet Gynecol. 2018; 51(6): 714 -717. 15. Villar J, Carroli G, Wojdyla D, Abalos E, Giordano D, Ba'aqeel H, Farnot U, Bergsjo P, Bakketeig L, Lumbiganon P, Campodonico L, Al-Mazrou Y, Lindheimer M, Kramer M. Preeclampsia, gestational hypertension and intrauterine growth restriction, related or independent conditions? Am J Obstet Gynecol 2006;194:921–931. 16. Инициатива по преэклампсии Международной федерации гинекологии и акушерства (FIGO): практическое руководство по скринингу в I триместре и профилактике заболевания (адаптированная версия на русском языке под редакцией З.С. Ходжаевой, Е.Л. Яроцкой, И.И. Баранова) // Акушерство и гинекология: новости мнения, обучение. 2019. Т. 7, № 4.С. 32–60. doi: 10.24411/2303-9698-2019-14003. 17. ВНОК, Российское медицинское общество по артериальной гипертонии. Национальные рекомендации по диагностике и лечению артериальной гипертензии у беременных. М., 2010. 18. Brown M.A., Mangos G., Davis G., Homer C. The natural history of white coat hypertension during pregnancy BJOG, 112 (2005), pp. 601-606. 19. Rodrigues A., Barata C., Marques I., Almeida M.C. Diagnosis of White Coat Hypertension and pregnancy outcomes. Pregnancy Hypertens, 14 (2018), pp. 121-124. 20. Stergiou G.S., Kario K., Kollias A. et al. Home blood pressure monitoring in the 21st century J. Clin. Hypertens. (Greenwich), 20 (2018), pp. 1116-1121. 21. Saudan P., Brown M.A., Buddle M.L., Jones M. Does gestational hypertension become pre-eclampsia? Br. J. Obstet. Gynaecol., 105 (1998), pp. 1177-1184. 22. Lee-Ann Hawkins T., Brown M.A., Mangos G.J., Davis G.K. Transient gestational hypertension: Not always a benign event. Pregnancy Hypertens., 2 (2012), pp. 22-27. 23. Homer C.S., Brown M.A., Mangos G., Davis G.K.. Non-proteinuric pre-eclampsia: a novel risk indicator in women with gestational hypertension J. Hypertens., 26 (2008), pp. 295-302. 24. Milne F., RedmanC., Walker J., Baker P., BradleyJ., Cooper C., et al. The pre-eclampsia community guideline (PRECOG): how to screen for and detect onset of pre-eclampsia in the community. BMJ. 2005; 330(7491): 576 – 80. 25. LisonkovaS.,JosephK.S.Incidenceofpreeclampsia:riskfactorsandoutcomesassociated with early-versus late-onset disease. Am J Obstet Gynecol. 2013; 209(6): 544.e1 – 544.e12. 26. Lisonkova S., Sabr Y., Mayer C., Young C., Skoll A., Joseph K.S. Maternal morbidity associated with early-onset and late-onset preeclampsia. Obstet Gynecol. 2014; 124(4): 771 – 81. 27. Ходжаева З.С., Холин А.М., Вихляева Е.М. Ранняя и поздняя преэклампсия: парадигмы патобиологии и клиническая практика. Акушерство и Гинекология. 2013; 10. 28. Khodzhaeva Z.S., Kogan Y.A., Shmakov R.G., Klimenchenko N.I., Akatyeva 69 A.S., Vavina O.V. et al. Clinical and pathogenetic features of early- and late-onset pre-eclampsia. J Matern Fetal Neonatal Med. 2016; 29(18): 2980 – 2986. 29. Duffy J., Cairns A.E., Richards-Doran D., et al. A core outcome set for preeclampsia research: an international consensus development study. BJOG 2020; 127:1516-26. doi: 10.111/471-0528.16319. 30. 2018 ESC Guidelines for the management of cardiovascular diseases during pregnancy European Heart Journal. 2018; 39, 3165–3241. doi:10.1093/eurheartj/ehy340. 31. Диагностика и лечение сердечно-сосудистых заболеваний при беременности: Национальные рекомендации. Российский кардиологический журнал. 2018;(3):91-134. doi:10.15829/1560-4071-2018-3-91-134. 32. Гипертензивные расстройства во время беременности, в родах и послеродовом периоде. Преэклампсия. Эклампсия. Клинические рекомендации (протокол). М. 2016. с.72. 33. Nissaisorakarn P., Sharif S., Jim B. Hypertension in Pregnancy: Defining Blood Pressure Goals and the Value of Biomarkers for Preeclampsia. Curr Cardiol Rep. 2016; 18(12): 131. 34. Metoki H., Iwama N., Ishikuro M., Satoh M., Murakami T., Nishigori H. Monitoring and evaluation of out-of-office blood pressure during pregnancy. Hypertens Res. 2017; 40(2): 107 – 9. 35. American Academy of Pediatrics and the American College of Obstetricians and Gynecologists. Guidelines for perinatalcare. 8thed. Elk Grove Village, IL;Washington, DC;2017. 36. Bello N.A., Miller E., Cleary K., Wapner R., Shimbo D., Tita A.T.. Out of office blood pressure measurement in pregnancy and the postpartum period. Curr. Hypertens. Rep., 20 (2018), p. 101. 37. Waugh J.J., Gupta M., Rushbrook J., Halligan A., Shennan A.H. Hidden errors of aneroid sphygmomanometers. Blood Press Monit, 7 (2002), pp. 309-312. 38. Davis G.K., Roberts L.M., Mangos G.J., Brown M.A.. Comparisons of auscultatory hybrid and automated sphygmomanometers with mercury sphygmomanometry in hypertensive and normotensive pregnant women: parallel validation studies. J Hypertens, 33 (2015), pp. 499-505. 39. STRIDEBP. STRIDE-BP: Validated BP monitors in pregnancy. https://stridebp.org/bp=monitors Accessed 02 Jan 2021. 40. Parati G, Stergiou G, O'Brien E, et al. European Society of Hypertension practice guidelines for ambulatory blood pressure monitoring. J Hypertens 2014;32:1359–1366. 41. Stergiou GS, Parati G, Vlachopoulos C, et al. Methodology and technology for peripheral and central blood pressure and blood pressure variability measurement: current status and future directions - Position statement of the European Society of Hypertension Working Group on blood pressure monitoring and cardiovascular variability. J Hypertens 2016;34:1665–1677. 42. Parati G, Stergiou GS, Asmar R, et al. European Society of Hypertension guidelines for blood pressure monitoring at home: a summary report of the Second 70 International Consensus Conference on Home Blood Pressure Monitoring. J Hypertens 2008;26:1505–1526. 43. Bliziotis IA, Destounis A, Stergiou GS. Home versus ambulatory and office blood pressure in predicting target organ damage in hypertension: a systematic review and meta-analysis. J Hypertens 2012;30:1289–1299. 44. Ward AM, Takahashi O, Stevens R, Heneghan C. Home measurement of blood pressure and cardiovascular disease: systematic review and meta-analysis of prospective studies. J Hypertens 2012;30:449–456. 45. McManus RJ, Mant J, Bray EP, Holder R, Jones MI, Greenfield S, Kaambwa B, Banting M, Bryan S, Little P, Williams B, Hobbs FD. Telemonitoring and self-management in the control of hypertension (TASMINH2): a randomised controlled trial. Lancet 2010;376:163–172. 46. McManus RJ, Mant J, Haque MSet al. Effect of self-monitoring and medication self-titration on systolic blood pressure in hypertensive patients at high risk of cardiovascular disease: the TASMIN-SR randomized clinical trial. JAMA 2014;312:799–808. 47. Tucker KL, Sheppard JP, Stevens R, et al. Self-monitoring of blood pressure in hypertension: a systematic review and individual patient data meta-analysis. PLoS Med 2017;14:e1002389. 48. Gaborieau V, Delarche N, Gosse P. Ambulatory blood pressure monitoring versus self-measurement of blood pressure at home: correlation with target organ damage. J Hypertens 2008;26:1919–1927. 49. Clement DL, De Buyzere ML, De Bacquer DA, de Leeuw PW, Duprez DA, Fagard RH, Gheeraert PJ, Missault LH, Braun JJ, Six RO, Van Der Niepen P, O'Brien E, Office versus Ambulatory Pressure Study Investigators. Prognostic value of ambulatory blood-pressure recordings in patients with treated hypertension. N Engl J Med 2003;348:2407–2415. 50. Sega R, Facchetti R, Bombelli M, Cesana G, Corrao G, Grassi G, Mancia G. Prognostic value of ambulatory and home blood pressures compared with office blood pressure in the general population: follow-up results from the Pressioni Arteriose Monitorate e Loro Associazioni (PAMELA) study. Circulation 2005;111:1777–1783. 51. Banegas JR, Ruilope LM, de la Sierra A, Vinyoles E, Gorostidi M, de la Cruz JJ, Ruiz-Hurtado G, Segura J, Rodriguez-Artalejo F, Williams B. Relationship between clinic and ambulatory blood-pressure measurements and mortality. N Engl J Med 2018;378:1509–1520. 52. Investigators ABC-H, Roush GC, Fagard RH, Salles GF, Pierdomenico SD, Reboldi G, Verdecchia P, Eguchi K, Kario K, Hoshide S, Polonia J, de la Sierra A, Hermida RC, Dolan E, Zamalloa H. Prognostic impact from clinic, daytime, and night-time systolic blood pressure in nine cohorts of 13,844 patients with hypertension. J Hypertens 2014;32:2332–2340; discussion 2340. 53. Fagard RH, Celis H, Thijs L, Staessen JA, Clement DL, De Buyzere ML, De Bacquer DA. Daytime and nighttime blood pressure as predictors of death and cause-specific cardiovascular events in hypertension. Hypertension 2008;51:55– 71 61. 54. Parati G, Ochoa JE, Bilo G, Agarwal R, Covic A, et al. European Renal and Cardiovascular Medicine Working Group of the European Renal Association-European Dialysis and Transplant Association. Hypertension in chronic kidney disease part 2: role of ambulatory and home blood pressure monitoring for assessing alterations in blood pressure variability and blood pressure profiles. Hypertension 2016;67:1102–1110. 55. Piper MA, Evans CV, Burda BU, Margolis KL, O'Connor E, Whitlock EP. Diagnostic and predictive accuracy of blood pressure screening methods with consideration of rescreening intervals: a systematic review for the U.S. Preventive Services Task Force. Ann Intern Med 2015;162:192–204. 56. Cade T.J., Gilbert S.A., Polyakov A., Hotchin A. The accuracy of spot urinary protein-to-creatinine ratio in confirming proteinuria in pre-eclampsia. Aust. N. Z. J. Obstet. Gynaecol., 52 (2012), pp. 179-182. 57. Phelan L.K., Brown M.A., Davis G.K., Mangos G. A prospective study of the impact of automated dipstick urinalysis on the diagnosis of preeclampsia. Hypertens. Pregnancy, 23 (2004), pp. 135-142. 58. Schmella MJ, Clifton RG, Althouse AD, Roberts JM. Uric acid determination in gestational hypertension: Is it as effective a delineator of risk as proteinuria in high-risk women? Reprod Sci 2015;22:1212–1219. 59. Cade TJ, de Crespigny PC, Nguyen T, Cade JR, Umstad MP. Should the spot albumin-to-creatinine ratio replace the spot protein-to-creatinine ratio as the primary screening tool for proteinuria in pregnancy? Pregnancy Hypertens 2015;5:298–302. 60. Chappell LC, Shennan AH. Assessment of proteinuria in pregnancy. BMJ 2008;336:968–969. 61. Cote AM, Firoz T, Mattman A, Lam EM, von Dadelszen P, Magee LA. The 24-hour urine collection: Gold standard or historical practice? Am J Obstet Gynecol 2008;199:625 e621–626. 62. Brown M.A., Magee L.A., Kenny L.C. et al. Hypertensive disorders of pregnancy: ISSHP classification, diagnosis, and management recommendations for international practice. Hypertension, 72 (2018), pp. 24-43. 63. Яковлева Н.Ю., Хазова Е.Л., Васильева Е.Ю., Зазерская И.Е. Соотношение ангиогенных и антиангиогенного факторов при преэклампсии. Артериальная гипертензия. 2016;22(5):488–494. 64. Rana S., Powe C.E., Salahuddin S. et al. Angiogenic factors and the risk of adverse outcomes in women with suspected preeclampsia. Circulation, 125 (2012), pp. 911-919. 65. Zeisler H., Llurba E., Chantraine F. et al. Predictive value of the sFlt-1:PlGF ratio in women with suspected preeclampsia. N. Engl. J. Med., 374 (2016), pp. 13-22. 66. Duhig K.E., Myers J., Seed P.T. et al. Placental growth factor testing to assess women with suspected pre-eclampsia: a multicentre, pragmatic, stepped-wedge cluster-randomised controlled trial. Lancet, 393 (2019), pp. 1807-1818.
Информация
Адрес для переписки с рабочей группой:
СПИСОК СОКРАЩЕНИЙ
АГ - артериальная гипертензия
Протеинурия – потеря белка ≥ 0,3 г/сутки или > 0,3 г/л в 2-х порциях мочи, взятых с интервалом в 6 час.
Эклампсия – серия судорог, сначала тонических, а затем клонических, которые, как правило, возникают на фоне тяжелой ПЭ при отсутствии других причин [4].
Индикатор 2: % индивидуальных карт беременных, в которых оценен риск преэклампсии в сроки 11-14 недель
Индикатор 3: % индивидуальных карт беременных с высоким риском преэклампсии, которым назначен препарат аспирина в сроки 12-16 недель
Индикатор 4: % индивидуальных карт беременных с АГ, которым назначена антигипертензивная терапия
Индикатор 5: % индивидуальных карт беременных с АГ, которые достигли целевого уровня АД
Индикатор 6: % индивидуальных карт беременных с АГ, родивших в сроки 37+ недель
В состав междисциплинарной группы, кроме руководителей проекта, вошли врачи различных специальностей, эксперты по созданию клинических практических рекомендаций, беременные, страдающие гипертензивными состояниями, а также группа технической поддержки.
Руководитель группы
Руководитель обеспечивал эффективную деятельность группы и координацию взаимодействия между членами рабочего коллектива.
Ответственные исполнители
Для создания клинического руководства по гипертензивным состояниям при беременности были привлечены медицинские консультанты. В группу медицинских консультантов вошли представители специальностей, наиболее часто встречающиеся с гипертензивными состояниями при беременности, имеющие опыт клинической работы и написание научных статей, знающие английский язык и владеющие навыками работы на компьютере, практикующие семейные врачи из ЦСМ, врачи-кардиологи и акушеры-гинекологи, а также профессорско-преподавательский состав ведущих медицинских ВУЗов КР (КГМА, КГМИПиПК, КРСУ).
Приглашение медицинских консультантов в состав разработчиков позволило обсудить достоверность отдельных рекомендаций, для которых не было найдено доказательств, а также вопросов применимости руководства в учреждениях первичного звена здравоохранения КР.
Медицинские консультанты:
| Джумагулова А.С. | д.м.н., профессор, профессор кафедры кардиохирургии и рентгенхирургии КГМА им. И.А.Ахунбаева | кардиология |
| Джишамбаев Э.Д. | д.м.н., профессор, зав. отделением нарушений ритма НЦКиТ им. академика Мирсаида Миррахимова | кардиология |
| Сарыбаев А.Ш. | д.м.н., профессор, главный научный сотрудник отделения легочных гипертензий и горной медицины НЦКиТ им. академика Мирсаида Миррахимова, президент АВВМ | кардиология |
| Романова Т.А. | д.м.н., врач медицинского центра «Авиценна» | кардиология |
| Сабиров И.С. | д.м.н., профессор, зав. кафедрой терапии №2 специальность «лечебное дело» КРСУ | терапия |
| Максутова Э.М. | к.м.н., национальный координатор по ПС, зав ЦПС «брак и семья» НЦОМИД | акушерство, гинекология |
| Аскеров А.А. | д.м.н. профессор кафедры акушерства и гинекологии КРСУ, президент КААН | акушерство, гинекология |
| Абдувалиева С.Т. | к.м.н., зав. отделением патологии новорожденных и недоношенных детей НЦОМиД, главный внештатный неонатолог МЗ КР | неонатология |
| Зурдинова А.А. | д.м.н., профессор КРСУ | клиническая фармакология |
| Адамалиева А.Б. | заместитель директора ЧОЦСМ | акушерство, гинекология |
| Айылчиева В.М. | врач УЗИ диагностики КБ УДППКР | ультразвуковая диагностика |
| Самойленко Л.М. | пациентка |
Мнение разработчиков не зависело от производителей лекарственных средств и медицинской техники. Разработчики и медицинские консультанты подписали документ об отсутствии конфликта интересов.
| Макенжан уллу Алмаз | д.м.н., зав.кафедрой акушерства и гинекологии им.М.С.Мусуралиева КГМА | Внутренний рецензент |
| Мамасаидов Абдимуталиб Ташалиевич | д.м.н., профессор, зав.кафедрой внутренних болезней №3 медицинского факультета ОшГу |
Внешний
рецензент
|
Методологическая экспертная поддержка
| Матоморова А.А. | Зав. отделом доказательной медицины и медицинских технологий Центра развития здравоохранения при МЗ КР |
ПРИЛОЖЕНИЕ А2. Методология разработки клинических рекомендаций
Задача: создание новой единой системы по диагностике, лечению и профилактике гипертензивных состояний у беременных на разных этапах оказания им медицинской помощи, которая бы базировалась на принципах доказательной медицины и отражала последние достижения мировой медицинской науки и практики.
Шкала уровней доказательности
| Уровень доказательств | Пояснение | |
| А |
Высокий
(++++)
|
Есть большая уверенность в том, что истинный эффект близок к предполагаемому. Дальнейшие исследования вряд ли изменят уверенность в эффекте (несколько качественных исследований с последовательными результатами или в отдельных случаях одно крупное высококачественное многоцентровое исследование) |
| В |
Средний
(+++0)
|
Существует умеренная уверенность в оценке эффекта: истинный эффект, вероятно, будет близок к предполагаемому, но есть вероятность, что он существенно отличается (одно крупное высококачественное исследование или несколько с методологическими ограничениями) |
| С |
Низкий
(++00)
|
В оценочном эффекте имеется ограниченный эффект: истинный эффект может существенно отличаться от оцененного (несколько исследований с существенными методологическими ограничениями) |
| D | Очень низкий (+000) | Уверенность в оценке эффекта очень мала: истинный эффект, вероятно, будет существенно отличаться от предполагаемого (экспертные мнения, нет прямых доказательств, исследования с существенными методологическими ограничениями) |
Силу рекомендаций определяли в соответствии с уровнем доказательности, с учетом соотношения прогнозируемых положительных результатов и рисков, степени сложности предполагаемого вмешательства, настроя пациента и предполагаемых финансовых затрат на диагностику и лечение:
Сильная рекомендация: Преимущества доказано перевешивают риски и степень сложности вмешательства или наоборот. Обычно формулируются как «мы рекомендуем...».
Слабая рекомендация: Преимущества не могут быть определены или уравниваются с рисками и степенью сложности вмешательства. Обычно формулируются как «мы предлагаем...».
Стратегия поиска
Проанализированная специальная литература включала национальные и международные руководства и ссылки на гипертензию беременных, обновленный поиск литературы, охватывающий статьи с 2018 г до декабря 2022 г. Поиск руководств проводился в национальных и международных реестрах клинических руководств с использованием электронных баз данных в сети Интернет:
- World Health Organization https://www.who.int/
- International Society for the Study of Hypertension in Pregnancy https://isshp.org/
- American College of Obstetricians and Gynecologists https://www.acog.org/
- American College of Cardiology https://www.acc.org/
- American Heart Association https://www.heart.org/
- US Preventive Services Task Force https://www.uspreventiveservicestaskforce. org/
- The International Federation of Gynecology and Obstetrics https://www.figo.org/
- The Society of Obstetricians and Gynaecologists of Canada https://www.cshp.ca/
- Hypertension Canada https://hypertension.ca/
- Society of Obstetric Medicine of Australia and New Zealand https://www.somanz.org/
- Queensland Clinical Guideline https://www.health.qld.gov.au/qcg
- Brazilian Guideline of Arterial Hypertension https://www.sbh.org.br/
- German Society of Gynecology and Obstetrics https://www.omicsonline.org/
- Royal College of Physicians of Ireland National Institute for Health and Care Excellence https://www.rcpi.ie/
- European Society of Cardiology https://www.escardio.org/
- European Society of Hypertension https://www.eshonline.org/
- Российское кардиологическое общество https://scardio.ru/
- Российское общество акушеров-гинекологов https://roag-portal.ru/
Мы отдали приоритет международным руководствам, рандомизированным контролируемым испытаниям (РКИ) и систематическим обзорам и оценили значимые клинические исходы. Дальнейший поиск клинических рекомендаций и доказательств по данной проблеме проводился в электронной базе данных Кохрановской библиотеки и PubMed по выбранным критериям и охватывал период с 2018 по ноябрь 2022. В работе не использовались неопубликованные отчеты и обзоры.
Ключевые поисковые слова:
Значимые клинические исходы для детей: перинатальная смертность (perinatal death), мертворождение и неонатальная смерть (stillbirth and neonatal death); низкий вес при рождении (stillbirth and neonatal death); необходимость наблюдения и ухода в отделении интенсивной терапии (NICU (neonatal intensive care unit) care); значимые неонатальные заболевания (serious neonatal morbidity); долгосрочные риски для здоровья детей и развития нервной системы (long-term paediatric health and neurodevelopment).
Конфликт интересов
| Положение пациентки |
|
| Обстоятельства |
|
| Оснащение |
|
| Кратность измерения |
|
| Собственно измерение |
|
| Показания к проведению СМАД у беременных: | При СМАД необходимо выполнять следующие условия: |
|
|
Измерение АД в домашних условиях (ДМАД) является приемлемой альтернативой при недоступности СМАД.
Требования к прибору для измерения ДМАД:
1. Определение артериальной гипертензии по офисным и внеофисным значениям суточного и домашнего мониторирования артериального давления
| Категория |
САД
(мм рт.ст.)
|
ДАД
(мм рт.ст.)
|
|
| Офисное АД | ≥140 | и/или | ≥90 |
| Суточное амбулаторное АД | |||
| Дневное (бодрствование) | ≥135 | и/или | ≥85 |
| Ночное (сон) | ≥120 | и/или | ≥70 |
| Суточное | ≥130 | и/или | ≥80 |
| Домашнее мониторирование АД | ≥135 | и/или | ≥85 |
2. Сравнение методов суточного и домашнего мониторирования АД
| СМАД | ДМАД |
|
Преимущества:
– Позволяет идентифицировать гипертензию “белого халата” и маскированную гипертензию
– Более существенная прогностическая значимость
– Ночные измерения
– Измерения проводятся в условиях реальной жизни
– Дополнительное прогностическое значение характеристик АД
– Большой объем информации на основании одного исследования, включая краткосрочную вариабельность АД
|
Преимущества:
– Позволяет идентифицировать гипертензию “белого халата” и маскированную гипертензию
– Дешевизна и широкая доступность
– Измерения в домашних условиях, которые предоставляют больший комфорт, чем кабинет врача
– Вовлечение пациентки в процесс измерения АД
– Легко выполнимо, может быть использовано в течение длительного периода времени для оценки межсуточной вариабельности АД
|
|
Недостатки:
– Дороговизна и иногда ограниченная доступность
– Может доставлять дискомфорт
|
Недостатки:
– Возможно только статичное измерение АД
– Возможны ошибки измерений
– Отсутствие ночных измеренийa
|
Примечание: а — разработаны технологии, позволяющее оценивать ночное АД с помощью домашних устройств.
Приложение Б-4.

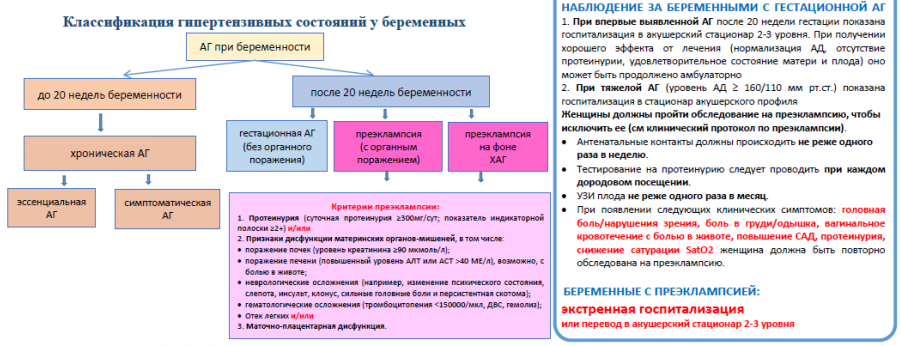
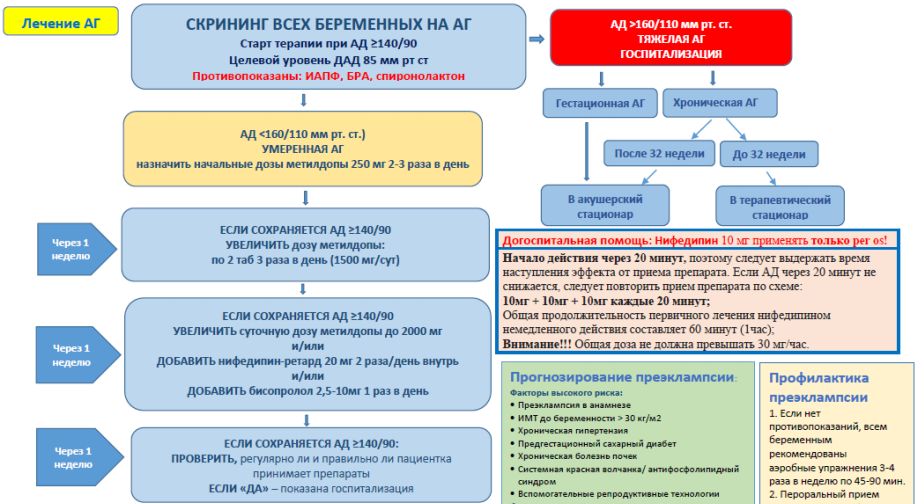
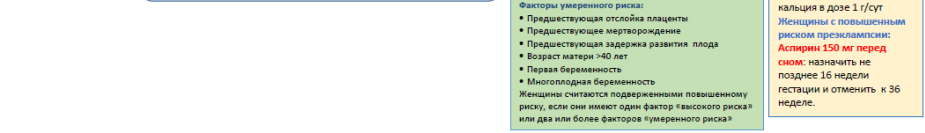
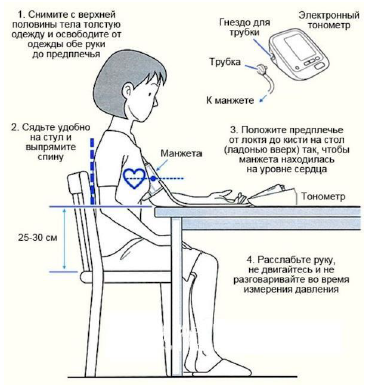
Если Вы относитесь к группе высокого риска преэклампсии (наличие преэклампсии в анамнезе) или определен высокий ее риск по данным скрининга 1-го триместра, Вам показан прием препаратов для профилактики преэклампсии с 12 до 36 недель беременности.
Тревожные признаки, при появлении которых Вы должны немедленно обратиться к врачу:
Дневник самоконтроля
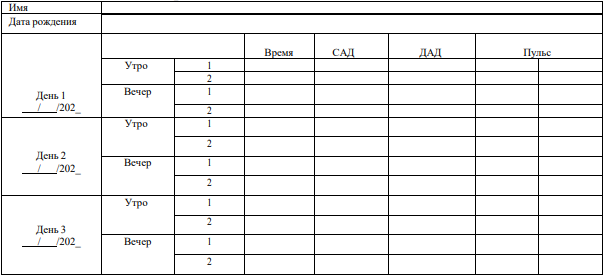
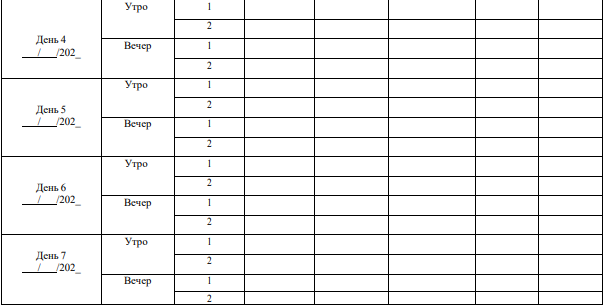
Действия при самоизмерении артериального давления
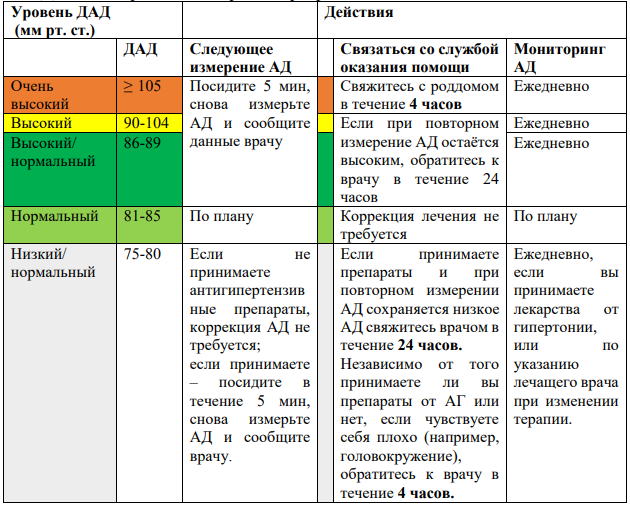
Индикатор 2: % индивидуальных карт беременных, в которых оценен риск преэклампсии в сроки 11-14 недель
Индикатор 3: % индивидуальных карт беременных с высоким риском преэклампсии, которым назначен препарат аспирина в сроки 12-16 недель
Индикатор 4: % индивидуальных карт беременных с АГ, которым назначена антигипертензивная терапия
Индикатор 5: % индивидуальных карт беременных с АГ, которые достигли целевого уровня АД
Индикатор 6: % индивидуальных карт беременных с АГ, родивших в сроки 37+ недель
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.