Гемофилия А и В: протокол диагностики и лечения
 Версия: Клинические протоколы 2024 (Узбекистан)
Версия: Клинические протоколы 2024 (Узбекистан)
Наследственный дефицит фактора IX (D67), Наследственный дефицит фактора VIII (D66)
Гематология, Гематология детская
Общая информация
Краткое описание
Приложение
к приказу № 107
от 29 марта 2024 года
Министерства здравоохранения Республики Узбекистан
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ УЗБЕКИСТАН
ЦЕНТР ДЕТСКОЙ ГЕМАТОЛОГИИ, ОНКОЛОГИИ И КЛИНИЧЕСКОЙ ИММУНОЛОГИИ
НАЦИОНАЛЬНЫЕ КЛИНИЧЕСКИЕ ПРОТОКОЛЫ ПО НОЗОЛОГИИ «ГЕМОФИЛИИ А и Б»
НАЦИОНАЛЬНЫЙ КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ ПО НОЗОЛОГИИ «ГЕМОФИЛИИ А и Б»
Вводная часть
Вводная часть
Коды МКБ-10/11:
|
МКБ-10:
|
|
|
D66.0
|
Наследственный дефицит фактора VIII
|
|
D67.0
|
Наследственный дефицит фактора IX
|
|
Скачать (ссылка с МКБ): https://mkb-10.com/index.php?pid=1456
|
|
Дата разработки/пересмотра протокола:
2023/2026 год.
Пользователи протокола: гематологи, терапевты, педиатры, врачи общей практики, врачи скорой помощи, хирурги, стоматологи, урологи, нейрохирурги, травматологи- ортопеды, физиотерапревты, сосудистые хирурги, трансфузиологи, медицинские сестры и специалисты по профилю жалоб и симптомов.
При наличии клинических признаков у пациента врач любой смежной специальности обязан направить больного к гематологу. При любом длительном кровотечении, независимо от его локализации (из пуповины и при кефалогематомах у новорожденных, при удалении зубов и оперативных вмешательствах у взрослых и пр.) должно возникать подозрение на гемофилию и необходимо проводить ее диагностику путем проверки показателей коагулограммы: АЧТВ, % факторов свертывания крови и др. показатели при необходимости установления диагноза.
Категория пациентов: пациенты с гемофилией А и В, взрослые, дети.
ОСНОВНАЯ ЧАСТЬ
Введение:
Гемофилия – относительно редкое нарушение, которое, однако, представляет собой сложность для диагностики и лечения. Оптимальное лечение таких пациентов, особенно тех, кто страдает заболеванием в тяжёлой форме, требует более серьёзных мер, чем терапия и предотвращение сильного кровотечения. Ключевыми аспектами улучшения состояния здоровья и повышения качества жизни являются:
Гемофилия – относительно редкое нарушение, которое, однако, представляет собой сложность для диагностики и лечения. Оптимальное лечение таких пациентов, особенно тех, кто страдает заболеванием в тяжёлой форме, требует более серьёзных мер, чем терапия и предотвращение сильного кровотечения. Ключевыми аспектами улучшения состояния здоровья и повышения качества жизни являются:
- Предотвращение кровотечений;
- Долгосрочное лечение повреждений суставов и мышц, а также других последствий кровотечения;
- Лечение осложнений после терапии, включая:
- Развитие ингибиторов;
- Вирусную(ые) инфекцию(и), передаваемую(ые) через производные крови и требующую(ие) длительного лечения.
Эти цели терапии лучше всего достигаются бригадой специалистов здравоохранения, которые обеспечивают комплексное медицинское обслуживание.
Определение: Гемофилия – наследственное, сцепленное с Х хромосомой, заболевание системы гемостаза, характеризующееся снижением или нарушением синтеза факторов свертывания крови VIII (FVIII) (при гемофилии А) или фактор IX(FIX) (при гемофилии В). Заболевание наследуется по аутосомно-рецессивному типу, сцеплено с Х-хромосомой. Это определяет преимущественное возникновение болезни у лиц мужского пола, а носительство – у лиц женского пола [1,5].
Классификация
Клиническая классификация:
-снижение активности фактора VIII –гемофилии А;
-снижение активности фактора IX – гемофилии В.
Таблица 1.
-снижение активности фактора IX – гемофилии В.
Таблица 1.
Классификация гемофилии по степени тяжести:
|
Степень тяжести
|
Уровень фактора свертывания крови
|
|
Тяжелая
|
Менее1% от нормы
|
|
Средняя
|
1-5% от нормы
|
|
Легкая
|
5-40% от нормы
|
При выявлении ингибирующих антител к факторам VIII или IX устанавливается ингибиторная форма:
Низкореагирующие пациенты – титр ингибирующих антител менее 5ВЕ.
Высокореагирующие пациенты – титр ингибирующих антител более 5ВЕ.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии:
Основными диагностическими критериями постановки диагноза являются совокупность клинических проявлений в виде кровоизлияний по гематомному типу (типы и характеристика кровоизлияний и кровотечений изложены в таблице 2), лабораторных тестов (удлинение активированного частичного тромбопластинового времени при нормальных показателях протромбинового времени, тромбинового времени, снижение активности фактора свертывания крови VIII/IX ниже 50%, при нормальной активности и свойствах фактора Виллебранда), у 2/3 пациентов – наличие семейного анамнеза.
Таблица 2
Таблица 2
Виды кровоизлияний и кровотечений и их характеристика
| Клинические признаки | Характеристика |
|
Гематомы
|
-кровоизлияния в подкожную область (по типу синяков, экхимозов), мышечные ткани, наиболее часто локализуются в области мышц, несущих на себе наибольшую статическую нагрузку (подвздошно-поясничная, четырехглавая мышца бедра, трехглавая мышца голени); гематомы в местах инъекций (поствакцинальные,
манипуляционные) |
|
Гемартроз
|
- кровоизлияние в суставы. Острый гемартроз сопровождается болевым синдромом, обусловленным повышением внутрисуставного давления. Сустав увеличен в объеме, кожа над ним гиперемирована и горячая на ощупь. При больших кровоизлияниях может определяться флюктуация. Если гемартроз возник после травмы, нужно исключить дополнительные повреждения (внутрисуставной перелом, отрыв мыщелка, ущемление тканей).
|
|
Гематурия
|
- наличие крови в моче. Может возникать спонтанно или в связи с травмами поясничной области. Гематурия может сопровождаться дизурическими явлениями, приступами почечной колики, обусловленными образованием сгустков крови в мочевыводящих путях. На основании исследования почек у больных гемофилией могут быть обнаружены такие нефрологические нарушения, как почечный капиллярный некроз, гидронефроз, пиелонефрит. Макрогематурия у больных гемофилией обусловлена наличием конкрементов в мочевом пузыре, пиелоэктазией, гидронефрозом. Гематурия может быть единственным симптомом начальной стадии гидронефроза, возникая вследствие внезапного и быстрого снижения внутрилоханочного давления. Особенно тяжело гематурия протекает у больных с ингибиторной формой гемофилии. Диагностика причин гематурии у больных гемофилией позволяет определить тактику дальнейшей терапии, как консервативной, так и оперативной.
|
|
Желудочно-кишечные кровотечения
|
- кровоизлияния из сосудов желудочно – кишечного тракта. Характеризуются появлением гематомезиса - рвоты в виде «кофейной гущей», меленой. Профузные желудочно-кишечные кровотечения при гемофилии могут быть спонтанными. Они могут быть вызваны приемом ацетилсалициловой кислоты, других нестероидных противовоспалительных средств. Кроме того, источником кровотечения являются латентные язвы желудка и двенадцатиперстной кишки, также эрозивные гастриты, геморроидальные узлы.
|
|
Кровоизлияния в брыжейку и сальник
|
- могут имитировать острое хирургическое заболевание органов брюшной полости (острый аппендицит, кишечную непроходимость и др.) и сопровождаются соответствующими симптомами.
|
|
Кровоизлияния в головной и спинной мозг
|
- возникают в связи с травмой. В отдельных случаях причиной таких кровоизлияний может быть гипертонический криз или прием препаратов, значительно нарушающих
оболочки гемостатическую функцию тромбоцитов (ацетилсалициловая кислота, бутадион и др.). Проявляются симптоматикой, характерной для нарушения мозгового кровообращения. |
|
Кровотечения при экстракции зубов
|
«Отсроченные» кровотечения
|
Таблица 3
Локализация кровоизлияний при гемофилии [1]
|
Серьезные
|
Суставы
|
|
Мышцы
|
|
|
Слизистые носа, рта, десен, мочевого тракта
|
|
|
Жизнеугрожающие
|
Внутричерепные
|
|
Шея/горло
|
|
|
Желудочно-кишечный тракт
|
Жалобы и анамнез:
Обычно больные чувствуют ранние симптомы кровоизлияния даже до проявления физических признаков. Такое ощущение они часто описывают как покалывающее ощущение предчувствия приступа или «ауру».[1]
- спонтанные кровоизлияния в крупные суставы; мышцы, мягкие ткани, это сопровождается жалобами на боли в соответствующих анатомических зонах;
- при наличии синовита, артроза отмечаются жалобы на «припухлость, отечность сустава», болезненные ощущения при движении в суставах;
- при наличии стойких контрактур – жалобы на ограничение движений вплоть до полной обездвиженности конечности, укорочение и утончение конечности в результате атрофии мышечной ткани;
- кровоизлияния на кожных покровах в виде гематом, синяков;
- спонтанные кровотечения из слизистых оболочек полости рта и носа;
- макрогематурия;
- головная боль и рвота (как признаки кровоизлияния в головной мозг);
- гематомезис - рвота «кофейной гущей», мелена;
- при псевдоопухоли – потемнение кожи, иногда прорывание содержимого наружу через свищевой канал.
Анамнез: следует обратить внимание на:
- наличие кровоточивости у родственников, особенно по линии матери (у 2/3 пациентов имеется семейный анамнез);
- наличие послеродовых осложнений в виде геморрагического синдрома (кровотечение у матери, кровотечение из пуповины или кефалогематома у новорожденного);
- условия возникновения кровоизлияния (кровотечения) (впервые, повторно, спонтанные либо посттравматические);
- наличие кровотечений при ранее проводимых оперативных вмешательствах (в том числе удаление зубов);
- наличие наследственной отягощенности в отношении гемофилии;
- указание на проведение ранее терапии антигемофильными препаратами; если да, то необходимо уточнить какими, в каком режиме, была ли она эффективна, отмечались ли аллергические реакции;
- указание на проведение обследования на выявление ингибирующих антител к факторам свертывания, если да – каковы его результаты;
- давность кровоизлияния при гемартрозах, уточнить его интенсивность, при каких обстоятельствах возникло кровоизлияние, наличие и интенсивность болевого синдрома в настоящее время.
Принято использовать специализированный опросник для больных гемофилией, который утверждается в организации на основе международных рекомендаций.
Клиническое течение болезни, объективные и физикальные обследования пациентов по данной нозологии:
Проводится осмотр кожных покровов, видимых слизистых и опорно –двигательной системы. В зависимости от степени тяжести гемофилии выявляются клинические признаки геморрагического синдрома (таблица 1).
Для тяжелой формы гемофилии характерно появление геморрагического синдрома на первом году жизни с начала активного периода у ребенка (гематомы мягких тканей, посттравматические кровотечения из слизистых, гемартрозы). Поражаются в основном крупные суставы: коленные, голеностопные, локтевые и тазобедренные. Гемофилия средней тяжести имеет сходные проявления. Первые признаки, как правило, развиваются после года. У пациентов с активностью факторов более 2% реже возникают кровоизлияния в суставы, забрюшинные гематомы, гематурии. Наиболее типичны посттравматические гематомы и длительные кровотечения, особенно при травмах слизистых оболочек. Легкая гемофилия может никак не проявляться на протяжении всей жизни. Геморрагический синдром обычно возникает вследствие значительных травм или при хирургическом лечении. Поражение опорно-двигательного аппарата встречается чрезвычайно редко.
Для тяжелой формы гемофилии характерно появление геморрагического синдрома на первом году жизни с начала активного периода у ребенка (гематомы мягких тканей, посттравматические кровотечения из слизистых, гемартрозы). Поражаются в основном крупные суставы: коленные, голеностопные, локтевые и тазобедренные. Гемофилия средней тяжести имеет сходные проявления. Первые признаки, как правило, развиваются после года. У пациентов с активностью факторов более 2% реже возникают кровоизлияния в суставы, забрюшинные гематомы, гематурии. Наиболее типичны посттравматические гематомы и длительные кровотечения, особенно при травмах слизистых оболочек. Легкая гемофилия может никак не проявляться на протяжении всей жизни. Геморрагический синдром обычно возникает вследствие значительных травм или при хирургическом лечении. Поражение опорно-двигательного аппарата встречается чрезвычайно редко.
Основные и дополнительные лабораторные исследования:
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5
Лабораторные исследования должны проводиться в каждом регионе Республики Узбекистан. Лабораторные исследования должны проводиться в лабораториях, где внедрен внутренний и внешний стандарт качества. Врачи лаборанты должны иметь сертификат или иное подтверждение прохождения обучения по диагностике болезни гемофилию.
Лабораторные исследования должны проводиться в каждом регионе Республики Узбекистан. Лабораторные исследования должны проводиться в лабораториях, где внедрен внутренний и внешний стандарт качества. Врачи лаборанты должны иметь сертификат или иное подтверждение прохождения обучения по диагностике болезни гемофилию.
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне:
- ОАК;
- Коагулограмма развернутая включая Активированное частичное тромбопластиновое время, тромбиновое время, Фибриноген;
- Определение активности факторов VIII/ IX;
- Определение активности ингибиторов к факторам VIII/ IX;
- Определение активности фактора Виллебранда в крови
Дополнительные диагностические обследования, проводимые на амбулаторном уровне:
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
- ОАМ
- Ристоцетин-кофакторная активность
- Группа крови и резус фактор
- Тест генерации тромбина
- Биохимический анализ крови (общий белок, билирубин, альбумин, креатинин, мочевина, АлАТ, АСаТ, глюкоза)
- ИФА на маркёры гепатитов В и С при положительных тестах ИФА на маркеры вирусных гепатитов;
- ИФА на маркеры ВИЧ
- ЭКГ
- УЗИ органов брюшной полости (печень, селезенка, поджелудочная железа, желчный пузырь, почек)
- Компьютерная томография;
- Магнитно-резонансная томография;
- Генетические исследования крови.
Основные (обязательные) и дополнительные диагностические обследования, проводимые на стационарном уровне.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
- общий анализ мочи (выявляются признаки гематурии: содержание эритроцитов, белка);
- группа крови и резус фактор (определяется каждый раз при госпитализации и острых кровотечениях при намерении применить
- трансфузионную терапию компонентами крови (свежезамороженной плазмы и криопреципитата), при хирургических вмешательствах.
- тест генерации тромбина [7] определяет индивидуальный режим подбора вида препарата, дозы, режима введения.
- биохимический анализ крови (общий белок, альбумин, общий
- билирубин, прямой билирубин, креатинин, мочевина, АЛаТ, АСаТ, глюкоза);
- ИФА на маркеры вирусных гепатитов (при постановке диагноза и, при гемотрансфузиях согласно соответствующим и нормативно – правовых актов в области трансфузиологии) [22].
- ПЦР на маркёры гепатитов В и С при положительных тестах ИФА на маркеры вирусных гепатитов (согласно соответствующим и нормативно – правовых актов в области трансфузиологии);[22]
- ИФА на маркеры ВИЧ (раз в год и после гемотрансфузий и хирургических вмешательств согласно соответствующим и нормативно – правовых актов в области трансфузиологии); [22]
- генетические исследования крови. Анализ мутаций на основе ДНК для определения специфических мутаций.
- бактериологическое исследование биологического материала;
- данный вид исследования следует проводить для идентификации возбудителя инфекции.
- сывороточное железо, ферритин; выполняется с целью ыявления постгеморрагической и/или иной сидеропении и назначения адекватной заместительной ферротерапии.
- определение активности фактора Виллебранда для проведения дифференциальной диагностики.
Основные и дополнительные инструментальные исследования
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Инструментальные исследования:
- ФГДС: обнаружение источника кровотечения, признаки эзофагита, гастрита, бульбита, дуоденита (поверхностный, катаральный, эрозивный, язвенный);
- ЭКГ: для определения степени поражения миокарда;
- УЗИ органов брюшной полости (печень, селезенка, поджелудочной железа, желчный пузырь, почек) – выявление возможных гематом, псевдоопухолей;
- Рентгенография органов грудной клетки выявление возможных гематом, псевдоопухолей;
- УЗИ суставов, мягких тканей (в зависимости от жалоб пациента выбирается конкретная анатомическая зона) определение органических изменений костных структур сустава и околосуставных тканей, в том числе синовиальной дистрофии, при артропатии обнаружение сужение хрящевого пространства, наличия поверхностных эрозий, субхондральных кист, ангулярных деформаций;
- Компьютерная томография (в зависимости от жалоб пациента выбирается конкретная анатомическая зона) выявление возможных гематом, гемартрозов, псевдоопухолей, синовиальной дистрофии, при артропатии обнаружение сужение хрящевого пространства, наличия поверхностных эрозий, субхондральных кист, ангулярных деформаций;
- Магнитно-резонансная томография (в зависимости от жалоб пациента выбирается конкретная анатомическая зона) выявление возможных гематом, гемартрозов, псевдоопухолей, синовиальной дистрофии, при артропатии обнаружение сужение хрящевого пространства, наличия поверхностных эрозий, субхондральных кист, ангулярных деформаций;
- МСКТ
- Эхокардиография: определение возможных очагов кровоизлияния; Бронхоскопия: обнаружение источника кровотечения; Колоноскопия: обнаружение источника кровотечения;
- Обзорный снимок органов брюшной полости и малого таза: обнаружение источника кровотечения.
- Рентгенография суставов: определение органических изменений костных структур сустава, в том числе синовиальной дистрофии; при артропатии обнаружение сужение хрящевого пространства, наличия поверхностных эрозий, субхондральных кист, ангулярных деформаций; стадии артропатии описаны в таблице 4.
Таблица 4.
Рентгенологические стадии артропатии
|
Стадии
|
Характеристика
|
|
I.
|
Ранняя стадия характеризуется увеличением объема сустава, расширением суставной щели за счет кровоизлияния.
Рентгенологически могут обнаруживаться утолщение и уплотнение суставной капсулы, умеренный остеопороз. Функция сустава при отсутствии кровоизлияния в «холодный» период не нарушена |
|
II.
|
Стадия характеризуется умеренным сужением суставной щели без нарушения конгруэнтности суставных поверхностей. Нарастание признаков остеопороза. Появление субхондрального склероза. Дальнейшее уплотнение периартикулярной ткани.
|
|
III.
|
Стадия характеризуется появлением краевых узур, деструкцией хрящевой ткани с образованием кист. Остеопороз более выражен.
Суставная щель сужена, местами нарушена конгруэнтность суставных поверхностей. В коленном суставе отмечается характерное изменение надколенника - квадратная форма его нижнего полюса и увеличение переднезаднего размера. Функция сустава умеренно снижена, незначительно ограничены движения, имеется атрофия мышц. |
|
IV.
|
Стадия, при которой суставы резко деформированы, суставные поверхности уплощены, эпифизы расширены за счет гиперостозов, диафизы уменьшены, суставная щель резко сужена. Внутрисуставные хрящи разрушены. Выраженная атрофия мышц. Объем движений значительно ограничен. Отмечается внутрисуставная крепитация при движении. Функция сустава значительно нарушена.
|
|
V.
|
Стадия характеризуется полной потерей функции сустава. Суставная щель плохо контурируется на рентгенограмме, часто заращена соединительной тканью. Выражен склероз субхондральных отделов кости, сочетающийся со значительной узурацией и кистозом эпифизов. Происходит формирование костного анкилоза.
|
Рисунок 1
Алгоритм применения лучевых методов исследования для контроля за состоянием суставов у пациентов с ГА
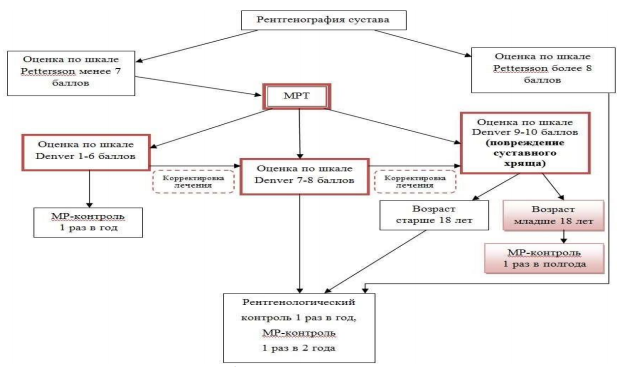
УЗИ суставов: определение объема излившейся крови, состояния синовиальной оболочки, признаков сдавления окружающих тканей.
Показания для консультации специалистов (профильного специалиста с указанием цели консультации)
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
- Хирург: определение показаний для хирургических вмешательств;
- Гепатолог: диагностика и лечение вирусного гепатита;
- Отоларинголог: осмотр слизистых оболочек носа, диагностика источника кровотечения, лечении воспалительных заболеваний придаточных пазух носа и среднего уха;
- Кардиолог: коррекция стойкой АГ, хронической сердечной недостаточности, нарушения ритма сердечной деятельности;
- Стоматолог: определение локализации кровоточащего участка слизистой, наличие подвижных зубов, инфильтрата в окружающих зуб тканях, лечение воспалительных заболеваний;
- Уролог: определение патологии мочевыделительной и половой системы;
- Офтальмолог: определение нарушения зрения, воспалительные заболевания и геморрагические состояния глаз и придатков;
- Невропатолог: диагностика и лечение острого нарушения мозгового кровообращения, нейропатий;
- Нейрохирург: определение показаний для нейрохирургических вмешательств;
- Инфекционист: подозрение на вирусные, бактериальные инфекции, лечение инфекций;
- Ревматолог: подозрение на наличие системного заболевания соединительной ткани;
- Дерматовенеролог: диагностика кожновенерологических заболеваний;
- Онколог: диагностика солидных опухолей, дифференциальная диагностика при постановке диагноза псевдоопухолей;
- Фтизиатр: диагностика туберкулеза, дифференциальная диагностика при постановке диагноза псевдоопухолей;
- Нефролог: определение показаний к терапии почечной недостаточности, диагностика и лечение патологии почечного тракта;
- Психолог: лечение и предупреждение психологических расстройств;
- Трансфузиолог: для подбора трансфузионных сред при положительном непрямом антиглобулиновом тесте, неэффективности трансфузий, острой массивной кровопотере;
- Реаниматолог: установка центральных венозных катетеров, лечение тяжелого сепсиса, шока, других жизнеугрожающих состояний (см. понятие жизнеугрожающих кровотечений в таблице 3);
- Врач ЛФК, реабилитолог: разработка индивидуальной программы реабилитации;
- Ортопед: определение объема ортохирургической коррекции, участие в разработке индивидуальной программы реабилитации, объема физических нагрузок;
- Сосудистые хирурги, интервенционные хирурги: определение сосудистого доступа для заместительной терапии, определение показаний для эмболизации сосудов при удалении псевдоопухолей, участие в мультидисциплинарных операционных бригадах, в том числе при ОНМК;
- Акушер-гинекологи: определение тактики ведения женщины при беременности и в родах, носительницы гена гемофилии, при беременности и планировании родов ребенка с предполагаемой или установленной формой гемофилии, решение вопроса о пролонгации беременности;
- Челюстно – лицевые хирурги: экстракция зубов, оперативные пособия при геморрагических и инфекционных осложнениях патологии челюстно – лицевой области;
- Рентгенологи, специалисты лучевой диагностики: расшифровка и вторая читка рентгенограмм при остеопатологии, наличии гематом и прочих геморрагических осложнений.
| - кровоизлияния в подкожную область (по типу синяков, |
Дифференциальный диагноз
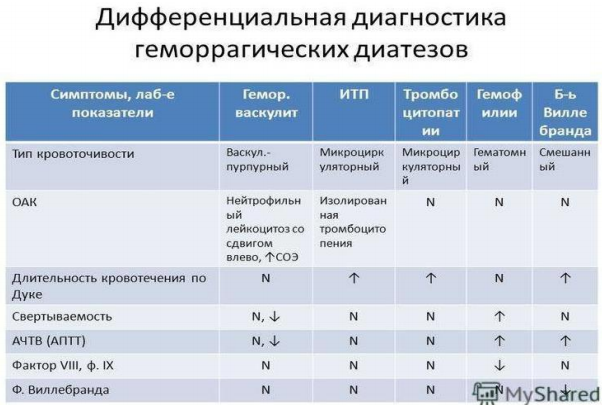
Таблица 6
Признаки и симптомы острого кровоизлияния в сустав
|
Раннее начало кровотечения
|
Прогрессирующее кровотечение
|
У новорожденных и маленьких детей
|
|
Боль
Необычные ощущения (покалывания), «аура» Ограничение движений в суставе Острое кровоизлияние в сустав с суставной болью |
Значительная боль
Отек Местное ощущение повышения температуры Значительное ограничение движений в суставе Неподвижность |
Уменьшение ограничения движений в суставе
Сопротивление при движении руки или ноги Предпочтение движений одной конечности перед другой Хромота Замедленная походка при беге Патологический отек или ригидность в суставе |
|
Острое кровоизлияние в сустав
|
Боль быстро исчезает после последующей инфузии концентрата фактора
|
|
|
Хронический артрит
|
Боль, связанная с активностью, быстро исчезает после отдыха
|
|
Дифференциальный диагноз и обоснование дополнительных исследований
Дифференциальный диагноз:
Дифференциальный диагноз:
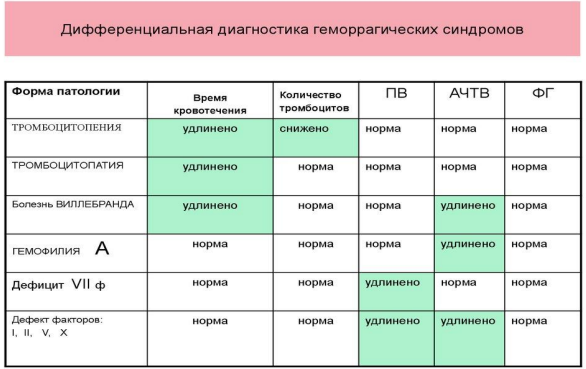
Дифференциальный диагноз проводится с болезнью Виллебранда, тромбоцитопатиями/тромбоцитопениями, болезнью Стюарта-Прауэра, наследственной гипоконвертинемией и другими геморрагическими состояниями.
Болезнь Виллебранда вызывается количественными или качественными изменениями содержания фактора Виллебранда. Заболевание наследуется по аутосомно- доминантному типу. Болезнь проявляется у обоих полов.
Кровоточивость преимущественно на уровне кожи и слизистых оболочек, а у женщин в виде гиперменорреи. В отличие от гемофилии гематомы и гемартрозы возникают крайне редко. При лабораторном исследовании: протромбиновое время в норме, активированное частичное тромбопластиновое время может быть как нормальным, так и удлиненным; длительность кровотечения - норма или удлинено, число тромбоцитов-нормальное или сниженное; активность фактора VIII - снижена или нормальная, активность фактора Виллебранда - снижена или нормальная; ристоцетин- кофакторная активность - снижена.
Тромбоцитопатии/тромбоцитопении характеризуются петехиально-синячковым типом кровоточивости. В анализах крови- регистрируется в разной степени выраженности снижение числа тромбоцитов, изменение морфологии тромбоцитов. В коагулограмме протромбиновое время, активированное частичное тромбопластиновое время не изменены. Длительность кровотечения нормальная или увеличенная.
Болезнью Стюарта-Прауэра наследуется по неполному аутосомно- рецессивному типу. При тяжелых формах дебют заболевания в период новорожденности (кефалогематомы). Имеют место профузные желудочно-кишечные кровотечения, подкожные гематомы, длительные носовые кровотечения, метроррагии. Гемартрозы крайне редки. В коагулограмме- удлинение протромбинового времени при одновременном, хотя и менее выраженном удлинении свертывания в активированном частичном тромбопластиновом времени. Снижена активность фактора X в плазме.
Наследственная гипоконвертинемия наследуется по неполному аутосомно- рецессивному типу. Тип кровоточивости- смешанный микроциркуляторно-гематомный (кефалогематомы, желудочно-кишечные кровотечения, упорные носовые кровотечения, метроррагии). В коагулограмме имеет место изолированное удлинение свертывания плазмы в протромбиновом тесте при нормальных показателях общего времени свертывания крови, активированном частичном тромбопластиновом времени.
Таблица 7
Болезнь Виллебранда вызывается количественными или качественными изменениями содержания фактора Виллебранда. Заболевание наследуется по аутосомно- доминантному типу. Болезнь проявляется у обоих полов.
Кровоточивость преимущественно на уровне кожи и слизистых оболочек, а у женщин в виде гиперменорреи. В отличие от гемофилии гематомы и гемартрозы возникают крайне редко. При лабораторном исследовании: протромбиновое время в норме, активированное частичное тромбопластиновое время может быть как нормальным, так и удлиненным; длительность кровотечения - норма или удлинено, число тромбоцитов-нормальное или сниженное; активность фактора VIII - снижена или нормальная, активность фактора Виллебранда - снижена или нормальная; ристоцетин- кофакторная активность - снижена.
Тромбоцитопатии/тромбоцитопении характеризуются петехиально-синячковым типом кровоточивости. В анализах крови- регистрируется в разной степени выраженности снижение числа тромбоцитов, изменение морфологии тромбоцитов. В коагулограмме протромбиновое время, активированное частичное тромбопластиновое время не изменены. Длительность кровотечения нормальная или увеличенная.
Болезнью Стюарта-Прауэра наследуется по неполному аутосомно- рецессивному типу. При тяжелых формах дебют заболевания в период новорожденности (кефалогематомы). Имеют место профузные желудочно-кишечные кровотечения, подкожные гематомы, длительные носовые кровотечения, метроррагии. Гемартрозы крайне редки. В коагулограмме- удлинение протромбинового времени при одновременном, хотя и менее выраженном удлинении свертывания в активированном частичном тромбопластиновом времени. Снижена активность фактора X в плазме.
Наследственная гипоконвертинемия наследуется по неполному аутосомно- рецессивному типу. Тип кровоточивости- смешанный микроциркуляторно-гематомный (кефалогематомы, желудочно-кишечные кровотечения, упорные носовые кровотечения, метроррагии). В коагулограмме имеет место изолированное удлинение свертывания плазмы в протромбиновом тесте при нормальных показателях общего времени свертывания крови, активированном частичном тромбопластиновом времени.
Таблица 7
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ:
Основная цель лечения гемофилии: предупреждение кровотечений. Именно в этом заключается понятие «профилактического лечения или заместительной терапии.[6]
Цель лечения проявлений гемофилии: остановить развившееся кровотечение или кровоизлияние, уменьшить частоту кровотечений и предотвратить прогрессию артропатии, улучшить качество жизни [2-6].
Основные аспекты (цели) лечения гемофилии и ее проявлений в виде кровотечений:
Цель лечения проявлений гемофилии: остановить развившееся кровотечение или кровоизлияние, уменьшить частоту кровотечений и предотвратить прогрессию артропатии, улучшить качество жизни [2-6].
Основные аспекты (цели) лечения гемофилии и ее проявлений в виде кровотечений:
-
предотвращение кровотечений и повреждений суставов;
-
безотлагательное лечение кровотечений;
-
контроль над возникающими осложнениями включает в себя: контроль; повреждений суставов, мышц и других осложнений кровотечений;
-
контроль развития ингибиторов;
-
контроль вирусных инфекций, передаваемых через производные крови;
-
внимание к психологическому здоровью;
-
внимание к здоровью ротовой полости.
Немедикаментозное лечение [10] [1]:
Режим: общеохранительный, избегать травм.
Режим: общеохранительный, избегать травм.
Среди больных со значительно дисфункцией костно-мышечной системы нужно поощрять виды активности с ношением тяжестей, которые способствуют развитию и поддержанию хорошей плотности костей, до степени, которую позволяет состояние их суставов. Определяет это при диспансеризации и разработке годовой программы реабилитации врач ортопед.
Следует поощрять неконтактные виды спорта, такие как плавание, ходьба, гольф, бадминтон, стрельба из лука, езда на велосипеде, гребля, парусный спорт и настольный теннис.
Следует поощрять неконтактные виды спорта, такие как плавание, ходьба, гольф, бадминтон, стрельба из лука, езда на велосипеде, гребля, парусный спорт и настольный теннис.
Высоко контактные виды спорта и виды спорта со столкновениями такие как футбол, хоккей, регби, бокс и борьба, а также высокоскоростные виды спорта такие как мотокросс и катание на лыжах следует избегать, поскольку они потенциально могут нанести травмы, угрожающие жизни, если больной не находится на профилактическом лечении для такого вида активности.
Программные виды спорта следует разрешать больному, который имеет высокую приверженность к лечению, соблюдает все принципы профилактического введения препаратов факторов свертывания крови.
Пораженные суставы во время активности можно защищать бандажами или шинами, особенно когда предварительно не введен фактор свертывания
Для того чтобы снизить вероятность повторного кровотечения, активность после кровотечения нужно возобновлять постепенно.
При наличии артропатии используют вспомогательные средства передвижения (костыли, ходунки, кресла, и пр).
Диета: назначается лечебный стол No15 (корректируется при наличии осложнений и/или сопутствующей патологии). Следует особенно внимательно относится к поддержанию нормального веса, избегать ожирения, корректировать диету при наличии сопутствующей патологии, особенно при вирусном поражении печени.
Программные виды спорта следует разрешать больному, который имеет высокую приверженность к лечению, соблюдает все принципы профилактического введения препаратов факторов свертывания крови.
Пораженные суставы во время активности можно защищать бандажами или шинами, особенно когда предварительно не введен фактор свертывания
Для того чтобы снизить вероятность повторного кровотечения, активность после кровотечения нужно возобновлять постепенно.
При наличии артропатии используют вспомогательные средства передвижения (костыли, ходунки, кресла, и пр).
Диета: назначается лечебный стол No15 (корректируется при наличии осложнений и/или сопутствующей патологии). Следует особенно внимательно относится к поддержанию нормального веса, избегать ожирения, корректировать диету при наличии сопутствующей патологии, особенно при вирусном поражении печени.
Медикаментозное лечение
Основным принципом лечения гемофилии является заместительная терапия, для чего используются: препарат фактора свертывания крови VIII (при гемофилии А) или фактора свертывания крови IX (при гемофилии В) (уровень доказательности А). Препараты факторов свертывания применяются плазматические и рекомбинантные [2,3].
Всемирная федерация гемофилии не отдает предпочтения в пользу одного из препаратов рекомбинантного или плазматического происхождения. UKHCDO рекомендует применение у пациентов с гемофилией А рекомбинантных препаратов свертывания, особенно тем, кто ранее не получал препараты плазмы (уровень доказательности С) [11].
Многочисленные исследования, в том числе CANAL отмечает отсутствие связи смены препаратов факторов свертывания крови с развитием ингибитора, это справедливо как для смены плазменных факторов свертывания крови на рекомбинантные (и наоборот), так и для смены разных плазменных или разных рекомбинантных факторов свертывания крови внутри группы [13,15,21].
Детям, ранее не получавшим профилактическое лечение, а также больным, которым только что поставили диагноз гемофилии В, особенно больным с семейной историей заболевания и / или с генетическими дефектами, предрасположенными к развитию ингибитора, первые введения препаратов следует проводить в стационаре, имеющем возможности лечить сильные аллергические реакции во время первых 10-20 сеансов лечения концентратами факторов.
Следует помнить, что препараты факторов свертывания крови являются биологическими лекарственными средствами. Как и на другие лекарственные средства на данные препараты могут возникнуть аллергические реакции. В данном случае необходимо прекратить введение лекарственного средства, ввести противоотечные препараты (стероидные гормоны, дефигидрамин и пр, согласно протоколам ведения анафилактических реакций и шоков. Взять подтверждающие тесты (Ig E, проверить уровень эозинофилов в крови, выполнить тест лейколизиса). Терапию в данном случае нужно подбирать в стационаре, используя весь арсенал препаратов заместительной терапии.
При индивидуальном подборе программы заместительной терапии следует по возможности пользоваться тестом генерации тромбина.
Существует два основных терапевтических режима, которые назначаются пациентам с гемофилией:
Всемирная федерация гемофилии не отдает предпочтения в пользу одного из препаратов рекомбинантного или плазматического происхождения. UKHCDO рекомендует применение у пациентов с гемофилией А рекомбинантных препаратов свертывания, особенно тем, кто ранее не получал препараты плазмы (уровень доказательности С) [11].
Многочисленные исследования, в том числе CANAL отмечает отсутствие связи смены препаратов факторов свертывания крови с развитием ингибитора, это справедливо как для смены плазменных факторов свертывания крови на рекомбинантные (и наоборот), так и для смены разных плазменных или разных рекомбинантных факторов свертывания крови внутри группы [13,15,21].
Детям, ранее не получавшим профилактическое лечение, а также больным, которым только что поставили диагноз гемофилии В, особенно больным с семейной историей заболевания и / или с генетическими дефектами, предрасположенными к развитию ингибитора, первые введения препаратов следует проводить в стационаре, имеющем возможности лечить сильные аллергические реакции во время первых 10-20 сеансов лечения концентратами факторов.
Следует помнить, что препараты факторов свертывания крови являются биологическими лекарственными средствами. Как и на другие лекарственные средства на данные препараты могут возникнуть аллергические реакции. В данном случае необходимо прекратить введение лекарственного средства, ввести противоотечные препараты (стероидные гормоны, дефигидрамин и пр, согласно протоколам ведения анафилактических реакций и шоков. Взять подтверждающие тесты (Ig E, проверить уровень эозинофилов в крови, выполнить тест лейколизиса). Терапию в данном случае нужно подбирать в стационаре, используя весь арсенал препаратов заместительной терапии.
При индивидуальном подборе программы заместительной терапии следует по возможности пользоваться тестом генерации тромбина.
Существует два основных терапевтических режима, которые назначаются пациентам с гемофилией:
-
Лечение по требованию
-
Профилактическое лечение.
Целью лечения «по требованию» является остановка возникших кровоизлияний или кровотечений. Иными словами, данное лечение проводится при остро возникших геморрагических состояниях.
Включение в клинический протокол незарегистрированных в Республике Узбекистан лекарственных средств не является основанием для возмещения в рамках гарантированного объема бесплатной медицинской помощи и в системе обязательного социального медицинского страхования.
Таблица 8
Перечень основных лекарственных средств (имеющих 100 % вероятность применения)
|
Таблица 9
Перечень дополнительных лекарственных средств (менее 100 % вероятности применения)
Перечень дополнительных лекарственных средств (менее 100 % вероятности применения)
|
Фармакотерапевтическая группа
|
МНН лекарственного средства
|
Способ применения
|
Уровень доказательности
|
|
Гемостатитики
|
Транексамовая кислота
Этамзилат |
в/в, таб
|
|
|
Антифибринолитики
|
Е-аминокапроновая
Кислота 5%,100мл |
в/в
|
|
|
Антибактериальные средства
|
Пеницилины
Макролиды Сульфаниламиды Фторхинолоны |
в/в, таб
|
|
|
Глюкокортикостероиды
|
Гидрокортизон
Преднизолон Дексаметазон |
наружное внутрисуставное
|
|
|
Нестероидные противовоспалительные препараты
|
парацетамол
целекоксиб мелоксикам нимесулид |
Растворы для в/в Таб
Капс Порошок |
|
|
Противотуберкулезные лекарственные средства
|
рифампицин лиофилизат для приготовления раствора для инъекций.
|
внутрисуставное
|
|
|
Спазмолитические лекарственные средства
|
Дротаверин
Спазмолгон |
в/в, таб
|
|
|
Растворы, применяемые для коррекции нарушений водного, электролитного и кислотно-основного баланса
|
натрия хлорид 0,9%;
калия хлорид; декстроза 5% калия хлорид 7,5% декстроза 10% |
раствор для инфузии –раствор для инъекции в ампулах;
|
|
|
Антисептики
|
хлоргексидин 0,05;
этанол раствор 70, 90 %; повидон – йод; перекись водорода раствор 3 %; йод раствор спиртовой 5 %. |
раствор для наружного применения
|
*Возможно применение только одного представителя группы или их комбинация
В данном протоколе представлены не все исчерпывающие лекарственные средства, так как при наличии патологии сопутствующей, например, инфекционных осложнений назначаются те препараты, которые указаны в соответствующих рекомендациях. По усмотрению лечащего врача и по консультации узких специалистов могут быть назначены синдромальная или симптоматическая терапия.
Таблица 10.
Медикаментозное лечение, оказываемое на амбулаторном уровне с целью обезболивания.
Стратегии обезболивания у больных с гемофилией (уровень доказательности В)
|
1
|
Парацетамол / ацетаменофен
Если не эффективны |
|
2
|
Ингибитор ЦОГ-2 (например: Целекоксиб, мелоксикам и нимесулид и другие;
ИЛИ парацетамол / ацетаменофен плюс кодеин (3-4 раза в день) ИЛИ Парацетамол / ацетаменофен плюс трамадол (3-4 раза в день) |
|
3
|
Морфин: использовать препарат пролонгированного действия с дополнительным препаратом быстрого действия. Увеличить препарат пролонгированного действия, если препарат быстрого действия используется более 4 раза в день
|
Хирургическое вмешательство, оказываемое в амбулаторных условиях:
Малоинвазивные хирургические вмешательства, включая стоматологические (удаление 1-2 зубов) могут осуществляться амбулаторно после консультации врача- гематолога, указывающего регламент заместительной терапии. (уровень доказательности С) в соответствии с настоящим протоколом (раздел «лечение по требованию».
До проведения любого хирургического вмешательства и через 2-3 месяца после него необходимо проведение лабораторного исследования на ингибитор к фактору свертывания.
До проведения любого хирургического вмешательства и через 2-3 месяца после него необходимо проведение лабораторного исследования на ингибитор к фактору свертывания.
Особенности сосудистого доступа.
С венами больного нужно обращаться с особой осторожностью. Поэтому рекомендуется использовать иглы-бабочки размером 23G или 25G. [1] После прокола вены нужно удерживать ее под давлением в течение 3-5 минут [2]
По возможности следует избегать устройств катетеризации вены, но они могут потребоваться для некоторых детей. [2]
По возможности следует избегать устройств катетеризации вены, но они могут потребоваться для некоторых детей. [2]
Избегать внутримышечных и подкожных инъекций, за исключением тех случаев, когда данный вид введения рекомендован гематологом (например, при вакцинации пациента, или лечении вирусного гепатита при параллельном профилактическом введении заместительной терапии препаратами факторов свертывания крови).
Если кровотечение не останавливается, несмотря на адекватное лечение, нужно измерить уровень фактора свертывания крови. Если уровень оказывается неожиданно низким, проводится тест на присутствие ингибитора.
Предотвращение кровотечения можно достичь путем профилактического введения заместительной терапии препаратом фактора свертывания крови.
Для лечения средних / умеренных кровотечений можно использовать терапию в домашних условиях.
Предотвращение кровотечения можно достичь путем профилактического введения заместительной терапии препаратом фактора свертывания крови.
Для лечения средних / умеренных кровотечений можно использовать терапию в домашних условиях.
Больным и лечащим врачам необходимо избегать лекарств, которые влияют на функцию тромбоцитов, особенно ацетилсалициловая кислота (ASA - аспирин) и нестероидные противовоспалительные препараты (НПВП), за исключением определенных ингибиторов ЦОГ-2. Парацетамол /ацетаменофен являются безопасной альтернативой для обезболивания.
До проведения любой инвазивной процедуры необходимо повышать уровни фактора до соответствующего уровня (см. соответствующую таблицу 11).
Дальнейшее ведение сопровождение пациента на амбулаторном уровне проводится врачом гематологом или врачом, проводившим терапию с консультацией гематолога.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения:
Терапия должна контролироваться клинически и лабораторно. При клиническом контроле, решение о недостаточной эффективности профилактической заместительной терапии принимается в случаях:
Терапия должна контролироваться клинически и лабораторно. При клиническом контроле, решение о недостаточной эффективности профилактической заместительной терапии принимается в случаях:
-
более 2 эпизодов спонтанных гемартрозов в год;
-
появления признаков хронического синовита или артропатии;
-
выраженных спонтанных геморрагических проявлениях другой локализации;
Лабораторный контроль заключается в анализе остаточной активности фактора перед следующим введением (не ниже 1%), анализа наличия ингибитора, и по- возможности построения фармакокинетической кривой в течение 3 – 5 дней.
Критерии ответа на терапию:
достижение индикаторов эффективности терапии.
Лечение (стационар)
Тактика лечения на стационарном уровне:
Карта наблюдения пациента, маршрутизация пациента (алгоритм)
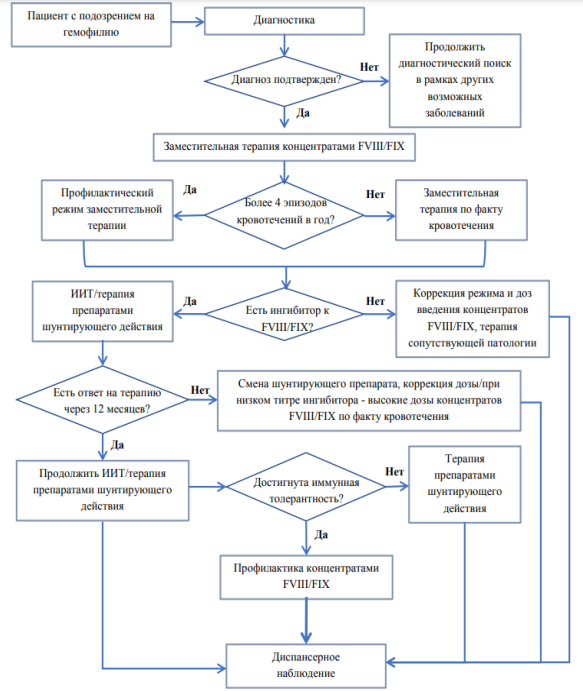
Принципы оказания экстренной помощи при возникновении кровотечения
-
Первичный осмотр пациента проводится врачом скорой медицинской помощи, амбулаторной организации, врачом приемного отделения стационарной организации, гематологом или врачом любой другой организации, в которую обратился пациент при возникновении кровотечения.
-
Осмотр пациента с гемофилией должен проводиться в ближайшей организации здравоохранения незамедлительно с целью раннего назначения заместительной терапии факторами свертывания крови и решения вопроса о госпитализации пациента.
-
При установлении факта кровотечения, незамедлительно (не позднее 2х часов с момента возникновения кровотечения) назначается заместительная терапия факторами свертывания крови. Внутривенное введение препаратов факторов свертывания крови VIII или IX осуществляется медицинскими работниками, специалистами скорой помощи, а в домашних условиях самим пациентом или иными лицами после обучения больного и его родителей (законных представителей). Для экстренной остановки кровотечения допускается применение препаратов факторов свертывания крови, находящихся у пациента в рамках профилактического лечения. Если есть сомнение лечить или не лечить, то нужно лечить. (уровень доказательности D).
-
Незамедлительно необходимо в экстренном порядке решить вопрос о госпитализации пациента в профильное отделение (гематология или отделение с учетом специфики геморрагического синдрома (нейрохирургия, челюстно- лицевая хирургия, хирургия, травматология, урология и пр.) в случае кровоизлияния в центральную нервную систему, желудочно-кишечное кровотечение, обширной гематомы, кровоизлияния в области головы, шеи, подвздошно-поясничную область, стойкой гематурии. Если госпитализация в профильное отделение затруднена, нужно госпитализировать пациента в ближайшую медицинскую организацию и вызывать профильных специалистов и гематологов по принципу «вызов на себя».
-
Все инвазивные методы исследования, включая эндоскопические инструментальные методы диагностики проводятся только под контролем введения факторов свертывания крови больному.
-
Не допускается внутримышечное введение любых лекарственных средств у больного с гемофилией.
-
Не допускается прием дезагрегантов и препаратов, влияющих на гемостаз без согласования с гематологом.
Формула расчета разовой дозы препарата для гемофилии А:
при тяжелой форме: Y = М х L х 0,5
при средней тяжести и легкой форме Y = M х (L-P) х 0,5
при средней тяжести и легкой форме Y = M х (L-P) х 0,5
Формула расчета разовой дозы препарата для гемофилии В
при тяжелой форме Y = М х L х 1,2
при средней тяжести и легкой форме Y = M х (L-P) х 1,2 где
Y - доза фактора свертывания крови для однократного введения (МЕ);
M - масса тела больного, кг;
L - процент желаемого уровня фактора в плазме пациента (см таблицу 5 «Процент желаемого уровня фактора и длительность терапии геморрагического эпизода»);
P - исходный уровень фактора у больного до введения препарата.
При этом надо учитывать, что 1 МЕ фактора VIII, введенного на 1 кг массы тела больного, повышает содержание фактора VIII в плазме больного на 1,5—2 %, а 1 МЕ фактора IX - повышает содержание фактора IX на 0,8%. (уровень доказательности C)
У детей первого года жизни повышение содержания фактора VIII в плазме больного может быть меньше 1%.
Расчет дозы концентрата фактора VIII у детей первого года жизни: Доза (МЕ) = Масса тела х (требуемая активность – базальная активность).
Таблица 11.
при средней тяжести и легкой форме Y = M х (L-P) х 1,2 где
Y - доза фактора свертывания крови для однократного введения (МЕ);
M - масса тела больного, кг;
L - процент желаемого уровня фактора в плазме пациента (см таблицу 5 «Процент желаемого уровня фактора и длительность терапии геморрагического эпизода»);
P - исходный уровень фактора у больного до введения препарата.
При этом надо учитывать, что 1 МЕ фактора VIII, введенного на 1 кг массы тела больного, повышает содержание фактора VIII в плазме больного на 1,5—2 %, а 1 МЕ фактора IX - повышает содержание фактора IX на 0,8%. (уровень доказательности C)
У детей первого года жизни повышение содержания фактора VIII в плазме больного может быть меньше 1%.
Расчет дозы концентрата фактора VIII у детей первого года жизни: Доза (МЕ) = Масса тела х (требуемая активность – базальная активность).
Таблица 11.
Процент желаемого уровня фактора и длительность терапии геморрагического эпизода.
(уровень доказательности В)
|
|
Гемофилия А
|
Гемофилия В
|
||
|
Тип кровотечения
|
Желаемый уровень(%)
|
Продолжительность (дней)
|
Желаемый уровень (%)
|
Продолжительность (дней)
|
|
Сустав
|
40–60
|
1–2, может быть дольше при неполном ответе
|
40–60
|
1–2, может быть дольше при неполном ответе
|
|
Неглубокие мышцы / без повреждения сосудисто- нервного пучка (за исключением подвздошно-поясничных мышц)
|
40–60
|
2–3, иногда дольше при неполном ответе
|
40–60
|
2–3, иногда дольше при неполном ответе
|
|
Подвздошно-поясничные и глубокие мышцы с повреждением сосудисто-нервного пучка или значительными кровопотерями
|
||||
|
начальная
|
80–100
|
1–2
|
60–80
|
1–2
|
|
поддержание
|
30–60
|
3–5, иногда дольше из-за вторичной профилактики
во время физиотерапии |
30–60
|
3–5, иногда дольше из-за вторичной профилактики
во время физиотерапии |
|
ЦНС/голова
|
||||
|
начальная
|
80–100
|
1–7
|
60–80
|
1–7
|
|
поддержание
|
50
|
8–21
|
30
|
8–21
|
|
Горло и шея
|
||||
|
начальная
|
80–100
|
1–7
|
60–80
|
1–7
|
|
поддержание
|
50
|
8–14
|
30
|
8–14
|
|
Желудочно-кишечные
|
||||
|
начальная
|
80–100
|
7–14
|
60–80
|
7–14
|
|
поддержание
|
50
|
8–14
|
30
|
8–14
|
|
Почечные
|
50
|
3–5
|
40
|
3–5
|
|
Глубокие ссадины
|
50
|
5–7
|
40
|
5–7
|
|
Хирургическая операция (крупная)
|
||||
|
До операции
|
80–100
|
1-7
|
60–80
|
1-7
|
|
После операции
|
60–80
40–60 30–50 |
1–3
4–6 7–14 |
40–60
30–50 20–40 |
1–3
4–6 7–14 |
|
Хирургическая операция (мелкая)
|
||||
|
До операции
|
50–80
|
1-7
|
50–80
|
1-7
|
|
После операции
|
30–80
|
1-5, в зависимости от типа процедуры
|
30–80
|
1-5, в зависимости от типа процедуры
|
При наличии обширных гематом с признаками сдавления окружающих тканей, в том числе забрюшинных, желудочно-кишечных кровотечениях поддержание гемостаза при гемофилии А проводится посредством введения фактора свертывания крови VIII каждые 8 ч, при гемофилии В – фактора свертывания крови IX каждые 18 ч (уровень фактора перед следующей инъекцией не должен быть менее 60 %) до полной остановки кровотечения, далее - поддерживающая терапия в течение 14 дней с интервалом 24 ч фактором свертывания крови VIII или IX.
При кровоизлиянии в головной или спинной мозг поддержание гемостаза при гемофилии А проводится посредством введения фактора свертывания крови VIII каждые 8 ч (уровень фактора перед повторной инъекцией не должен быть ниже 100 %), при гемофилии В - фактора свертывания крови IX каждые 12 ч (уровень фактора перед следующей инъекцией не должен быть менее 100 %) до полной остановки кровотечения, далее - поддерживающая терапия в течение 14 дней с интервалом 24 ч фактором свертывания крови VIII или IX.
При стоматологических вмешательствах, кровотечениях из слизистых оболочек, желудочно-кишечного тракта к заместительной терапии факторами свертывания может быть добавлена транексамовая кислота (уровень доказательности С).
У пациентов с легкой формой гемофилии для купирования геморрагического события может быть применен десмопрессин внутривенно или подкожно из расчета 0,3 мкг/кг веса, однократно. Либо в виде специального назального спрея, разовая доза 300 мкг. (уровень доказательности С)
В качестве дополнительного лечения можно использовать защитные приспособления (шины), покой, лед, компрессию и возвышенное положение конечности (PRICE) при кровотечениях в мышцах и суставах.
При воспалении суставов после острого кровотечения и при хроническом артрите могут использоваться определенные ингибиторы ЦОГ-2. (уровень доказательности С)
При стоматологических вмешательствах, кровотечениях из слизистых оболочек, желудочно-кишечного тракта к заместительной терапии факторами свертывания может быть добавлена транексамовая кислота (уровень доказательности С).
У пациентов с легкой формой гемофилии для купирования геморрагического события может быть применен десмопрессин внутривенно или подкожно из расчета 0,3 мкг/кг веса, однократно. Либо в виде специального назального спрея, разовая доза 300 мкг. (уровень доказательности С)
В качестве дополнительного лечения можно использовать защитные приспособления (шины), покой, лед, компрессию и возвышенное положение конечности (PRICE) при кровотечениях в мышцах и суставах.
При воспалении суставов после острого кровотечения и при хроническом артрите могут использоваться определенные ингибиторы ЦОГ-2. (уровень доказательности С)
Немедикаментозное лечение см. аналогичный раздел на амбулаторном уровне.
Медикаментозное лечение, оказываемое на стационарном уровне [14]:
В стационаре больному, госпитализированному по поводу острого кровотечения основная тактика основана на купировании геморрагического
синдрома, при наличии показаний к хирургическому вмешательству при остро возникших состояниях проводится коррекция гемостаза согласно таблице 11. Тактика лечения состояний, по поводу которых требуется хирургическое лечение или лечение иных патологий и состояний, развившихся у пациентов с диагнозом гемофилии, требуется использование дополнительных протоколов диагностики и лечения данных диагнозов с поправкой на принципы ведения больных с гемофилией.
При плановой госпитализации целью терапии является проведение оперативного вмешательства или коррекции иных патологий и состояний, развившихся у пациентов с диагнозом гемофилии, требуется использование дополнительных протоколов диагностики и лечения данных диагнозов с поправкой на принципы ведения больных с гемофилией.
синдрома, при наличии показаний к хирургическому вмешательству при остро возникших состояниях проводится коррекция гемостаза согласно таблице 11. Тактика лечения состояний, по поводу которых требуется хирургическое лечение или лечение иных патологий и состояний, развившихся у пациентов с диагнозом гемофилии, требуется использование дополнительных протоколов диагностики и лечения данных диагнозов с поправкой на принципы ведения больных с гемофилией.
При плановой госпитализации целью терапии является проведение оперативного вмешательства или коррекции иных патологий и состояний, развившихся у пациентов с диагнозом гемофилии, требуется использование дополнительных протоколов диагностики и лечения данных диагнозов с поправкой на принципы ведения больных с гемофилией.
Острые кровотечения следует лечить в кратчайшие сроки, предпочтительно в течение двух часов.
Оценить степень и категорию тяжести кровотечения (см таблицу).
Выяснить, имеется ли у пациента ингибитор к фактору свертывания (со слов пациента) факторам Немедленная госпитализация в ближайшую клинику, вызов гематолога, перейти к исполнению алгоритма оказания экстренной помощи.
При возможности ввести фактор свертывания крови 25 МЕ на кг веса по инструкции к препарату (См. инструкцию к препарату)
Для того чтобы облегчить лечение гемофилии в чрезвычайных случаях, больные должны носить с собой в легкодоступном месте карточку с информацией о диагнозе, тяжести заболевания, состоянии ингибитора, типе лекарства, используемого для лечения, начальной дозе для лечения тяжелого, среднего или легкого кровотечения и контактную информацию лечащего врача/ клиники. [2]
Выяснить, имеется ли у пациента ингибитор к фактору свертывания (со слов пациента) факторам Немедленная госпитализация в ближайшую клинику, вызов гематолога, перейти к исполнению алгоритма оказания экстренной помощи.
При возможности ввести фактор свертывания крови 25 МЕ на кг веса по инструкции к препарату (См. инструкцию к препарату)
Для того чтобы облегчить лечение гемофилии в чрезвычайных случаях, больные должны носить с собой в легкодоступном месте карточку с информацией о диагнозе, тяжести заболевания, состоянии ингибитора, типе лекарства, используемого для лечения, начальной дозе для лечения тяжелого, среднего или легкого кровотечения и контактную информацию лечащего врача/ клиники. [2]
Лечение ингибиторной гемофилии
Появление ингибитора FVIII/FIX считается самым тяжелым осложнением, связанным с лечением гемофилии. Ингибиторы – алло-антитела (IgG), которые нейтрализуют экзогенные FVIII/FIX
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5.
Появление ингибитора в основном проявляется отсутствием клинического ответа на стандартную терапию факторами свертывания крови (B02BD по АТХ классификации) или появлением кровотечений на профилактической терапии. Наиболее часто ингибиторы появляются у пациентов с тяжелой формой гемофилии (до 30% пациентов с тяжелой формой ГA и до 3-5% пациентов с тяжелой формой ГB).
Наиболее часто ингибитор развивается в первые 20-50 (до 100) ДВ фактора и после интенсивной терапии при хирургическом вмешательстве.
Поскольку при появлении ингибиторов стандартная заместительная терапия факторами свертывания крови VIII**/октокогом альфа**, мороктокогом альфа**, симоктокогом альфа (фактор свертывания крови VIII человеческий рекомбинантный)**, туроктокогом альфа, лоноктокогом альфа, руриоктокогом альфа пэгол или концентратом фактора свертывания крови IX**/нонакогом альфа**, албутрепенонакогом альфа становится неэффективной, риск тяжелых осложнений и даже смерти от кровотечения у этих больных выше. При умеренной или легкой гемофилии ингибитор может нейтрализовать эндогенный FVIII/FIX, преобразуя, тем самым, клинический фенотип заболевания в тяжелую форму.
Особенности течения ингибиторной ГB. До 50% пациентов с ингибиторной ГB могут иметь тяжелые аллергические реакции, в том числе анафилаксию, при применении FIX**. Такие реакции часто бывают первым симптомом развития ингибитора.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5.
Появление ингибитора в основном проявляется отсутствием клинического ответа на стандартную терапию факторами свертывания крови (B02BD по АТХ классификации) или появлением кровотечений на профилактической терапии. Наиболее часто ингибиторы появляются у пациентов с тяжелой формой гемофилии (до 30% пациентов с тяжелой формой ГA и до 3-5% пациентов с тяжелой формой ГB).
Наиболее часто ингибитор развивается в первые 20-50 (до 100) ДВ фактора и после интенсивной терапии при хирургическом вмешательстве.
Поскольку при появлении ингибиторов стандартная заместительная терапия факторами свертывания крови VIII**/октокогом альфа**, мороктокогом альфа**, симоктокогом альфа (фактор свертывания крови VIII человеческий рекомбинантный)**, туроктокогом альфа, лоноктокогом альфа, руриоктокогом альфа пэгол или концентратом фактора свертывания крови IX**/нонакогом альфа**, албутрепенонакогом альфа становится неэффективной, риск тяжелых осложнений и даже смерти от кровотечения у этих больных выше. При умеренной или легкой гемофилии ингибитор может нейтрализовать эндогенный FVIII/FIX, преобразуя, тем самым, клинический фенотип заболевания в тяжелую форму.
Особенности течения ингибиторной ГB. До 50% пациентов с ингибиторной ГB могут иметь тяжелые аллергические реакции, в том числе анафилаксию, при применении FIX**. Такие реакции часто бывают первым симптомом развития ингибитора.
-
У пациентов с гемофилией с низким титром ингибитора рекомендовано купировать кровотечение введением факторов свертывания крови (B02BD по АТХ классификации) в дозах, превосходящих стандартные в 3 раза, или введением препаратов шунтирующего действия [35].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5.
Комментарии: выбор препарата для лечения должен основываться на титре ингибитора, клиническом ответе на терапию и характере кровотечения.
Комментарии: выбор препарата для лечения должен основываться на титре ингибитора, клиническом ответе на терапию и характере кровотечения.
-
Рекомендовано проводить лечение кровотечений у пациентов с высоким титром ингибитора только препаратами шунтирующего действия [3, 9, 20, 36, 37]. Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2) Комментарии: в настоящее время к препаратам шунтирующего действия относятся 2 препарата: антиингибиторный коагулянтный комплекс** и эптаког альфа (активированный)**.
Достоверной разницы эффективности, безопасности и стоимости лечения этими препаратами не получено. Однако имеются данные об индивидуальных особенностях ответа пациента на каждый из препаратов, что необходимо учитывать при выборе лечения в каждом конкретном случае.
Дозы препаратов с шунтирующим действием для купирования кровотечения:
-
антиингибиторный коагулянтный комплекс** назначается в дозе 30-100 Ед/кг каждые 12-24 часа. Максимальная суточная доза 200 Ед/кг (для пациентов, получающих эмицизумаб** – не более 100 ЕД/кг/сут);
-
эптаког альфа (активированный)** назначается в дозе 90-120 мкг/кг каждые 2-4 часа до остановки кровотечения. Возможно однократное эптакога альфа (активированного)** введение в сутки в дозе 270 мкг/кг.
-
Рекомендовано при гемофилии, осложненной ингибитором, проведение длительной профилактической терапии антиингибиторным коагулянтным комплексом** в режиме 85 +/- 15 (60-100) Ед/кг каждые 12 часов при проведении индукции иммунологической толерантности (ИИТ), до снижения титра ингибитора менее 2 БЕ; вне ИИТ – проведение профилактической терапии #антиингибиторным коагулянтным комплексом** в дозе 50- 100 Ед/кг 2-3 раза в неделю или через день [38-40].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
-
Рекомендовано пациентам с гемофилией, осложненной ингибитором, проводить краткосрочную (в течение 3-х месяцев) профилактическую терапию эптаког альфа (активированным)** в режиме 90 мкг/кг 1 раз в день [9, 20].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
-
Эмицизумаб одобрен для профилактики кровотечений у больных гемофилией А (ГА) с ингибиторами фактора VIII (FVIII) и тяжелой формой ГА без ингибиторов FVIII [1, 2]. Эмицизумаб является моноклональным антителом и имеет отличный от препаратов шунтирующего действия (ПШД) и препаратов FVIII механизм действия и фармакокинетический профиль. Рекомендовано пациентам с ингибиторной формой гемофилии A проводить профилактическое лечение препаратом эмицизумаб** в дозах 3 мг/кг один раз в неделю в течение первых 4-х недель, затем 1,5 мг/кг один раз в неделю или 3.0 мг/кг 1 раз в 2 недели, или 6.0 мг/кг 1 раз в четыре недели. Эмицизумаб** вводится подкожно, выбор места для инъекции следует ограничить рекомендованными участками: область живота, верхняя часть наружной поверхности плеча и бедро [5, 34].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 2)
Комментарии: на действие эмицизумаба** не влияет концентрация FVIII и наличие ингибитора к нему.
Комментарии: на действие эмицизумаба** не влияет концентрация FVIII и наличие ингибитора к нему.
-
Первой линией терапии у пациентов с ингибиторной формой ГA рекомендовано проведение индукции иммунологической толерантности (ИИТ) с целью элиминации ингибитора [9, 10, 41, 42].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии: оптимальные сроки начала ИИТ – сразу после выявления ингибитора.
Эффективность ИИТ значительно повышается, если в начале терапии титр ингибитора не превышает 10 БЕ. Тем не менее, высокий титр ингибитора не является противопоказанием к ИИТ. ИИТ может проводиться с использованием любого препарата FVIII (фактор свертывания крови VIII**, фактор свертывания крови VIII + фактор Виллебранда**, октоког альфа**, мороктоког альфа**, симоктоког альфа (фактор свертывания крови VII человеческий рекомбинантный)**, лоноктоког альфа, туроктоког альфа, эфмороктоког альфа**, руриоктоког альфа пэгол)
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Предпочтительно проводить ИИТ фактором свертывания крови VIII**. При проведении ИИТ недопустимо менять фактор свертывания крови VIII**, поскольку это значительно ухудшает прогноз терапии. Перед проведением ИИТ необходимо убедиться в наличии достаточного количества препарата.
Оптимального режима проведения ИИТ нет. Для пациентов с высокореагирующим ингибитором, независимо от титра ингибитора на момент начала ИИТ, рекомендована начальная схема 100-150 МЕ/кг препарата FVIII каждые 12 часов. Для пациентов с низкореагирующим ингибитором рекомендовано начинать ИИТ по схеме 50-100 МЕ/кг препарата ежедневно или каждый второй день. Снижение дозы и кратности введения препарата начинается после достижения следующих показателей: титр ингибитора – менее 0,6 БЕ, нормализация теста восстановления (более 66%) и нормализация периода полувыведения (более 7 часов). Снижение дозы препарата проводится постепенно по схеме с постоянным лабораторным контролем. После достижения дозы в 30-50 МЕ/кг 1 раз в 2 дня необходимо продолжить терапию в режиме вторичной/третичной профилактики в данной дозе длительно.
Комментарии: оптимальные сроки начала ИИТ – сразу после выявления ингибитора.
Эффективность ИИТ значительно повышается, если в начале терапии титр ингибитора не превышает 10 БЕ. Тем не менее, высокий титр ингибитора не является противопоказанием к ИИТ. ИИТ может проводиться с использованием любого препарата FVIII (фактор свертывания крови VIII**, фактор свертывания крови VIII + фактор Виллебранда**, октоког альфа**, мороктоког альфа**, симоктоког альфа (фактор свертывания крови VII человеческий рекомбинантный)**, лоноктоког альфа, туроктоког альфа, эфмороктоког альфа**, руриоктоког альфа пэгол)
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Предпочтительно проводить ИИТ фактором свертывания крови VIII**. При проведении ИИТ недопустимо менять фактор свертывания крови VIII**, поскольку это значительно ухудшает прогноз терапии. Перед проведением ИИТ необходимо убедиться в наличии достаточного количества препарата.
Оптимального режима проведения ИИТ нет. Для пациентов с высокореагирующим ингибитором, независимо от титра ингибитора на момент начала ИИТ, рекомендована начальная схема 100-150 МЕ/кг препарата FVIII каждые 12 часов. Для пациентов с низкореагирующим ингибитором рекомендовано начинать ИИТ по схеме 50-100 МЕ/кг препарата ежедневно или каждый второй день. Снижение дозы и кратности введения препарата начинается после достижения следующих показателей: титр ингибитора – менее 0,6 БЕ, нормализация теста восстановления (более 66%) и нормализация периода полувыведения (более 7 часов). Снижение дозы препарата проводится постепенно по схеме с постоянным лабораторным контролем. После достижения дозы в 30-50 МЕ/кг 1 раз в 2 дня необходимо продолжить терапию в режиме вторичной/третичной профилактики в данной дозе длительно.
Альтернативным вариантом профилактики после достижения толерантности является применение эмицизумаба** в стандартных режимах. Отмена профилактического лечения может привести к рецидиву ингибитора. Максимальная длительность ИИТ 3 года. Критерии эффективности ИИТ представлены в таблице 12.
Таблица 12.
Критерии эффективности ИИТ
|
Эффективность
|
Критерии
|
|
Полный успех
|
Титр ингибитора < 0,6 БЕ (не менее чем при двух последовательных определениях)
Нормализация показателя восстановления (66% и более) на протяжении более чем двух месяцев Нормализация периода полувыведения (более 7 часов) |
|
Частичный успех
|
Присутствие двух из трех критериев
|
|
Частичный ответ
|
Присутствие одного из трех критериев
|
|
Отсутствие ответа
|
Не выполняется ни один из критериев на протяжении 12 месяцев и более
|
Выбор препарата для проведения ИИТ должен быть индивидуальным.
При проведении ИИТ необходимо избегать любых воздействий и препаратов, стимулирующих иммунные реакции, в том числе вакцинации, применения препаратов интерферона и других видов иммунотерапии.
-
Пациентам с ингибиторной формой ГA во время ИИТ для купирования геморрагического синдрома во время ИИТ рекомендовано применение препаратов шунтирующего действия: антиингибиторного коагулянтного комплекса** или эптакога альфа (активированного)** [3, 9]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5),
-
Пациентам с ингибиторной формой ГA во время ИИТ для профилактики геморрагического синдрома во время ИИТ рекомендовано применение эмицизумаба** в стандартных режимах [43] Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии: в случае использования эмицизумаба** при проведении ИИТ дозы и режимы введения концентратов #фактора свертывания крови VIII** должны быть изменены: 50-100 МЕ/кг с введением 3 раза в неделю, или через день, или ежедневно в зависимости от титра ингибитора [44].
В сериях клинических наблюдений пациентов, получающих ИИТ на фоне продолжающейся профилактики эмицизумабом** повышения риска побочных и/или тромботических явлений не зарегистрировано.
В сериях клинических наблюдений пациентов, получающих ИИТ на фоне продолжающейся профилактики эмицизумабом** повышения риска побочных и/или тромботических явлений не зарегистрировано.
-
Рекомендовано пациентам с ингибиторной формой ГA прекратить ИИТ и перевести пациента на терапию препаратами шунтирующего действия или эмицизумабом**, при отсутствии тенденции к снижению ингибитора в течение 12 месяцев от начала высокодозной терапии [45].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: возможно повторное проведение ИИТ с использованием другого препарата или изменением режима терапии.
Опыт проведения ИИТ у пациентов с ингибиторной Гемофилией B ограничен. Это обусловлено очень низкой эффективностью и аллергическими реакциями
Комментарии: возможно повторное проведение ИИТ с использованием другого препарата или изменением режима терапии.
Опыт проведения ИИТ у пациентов с ингибиторной Гемофилией B ограничен. Это обусловлено очень низкой эффективностью и аллергическими реакциями
Физиотерапевтическое лечение
Физиотерапия, включающая гидрокинезотерапию, короткоимпульсную электроанальгезию, ультразвуковая терапия, индуктотермия, электрофонофорез. (Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Данный вид лечения применяется в качестве реабилитации после гемартрозов, хирургических вмешательств на опорно – двигательной системе.
Данный вид лечения применяется в качестве реабилитации после гемартрозов, хирургических вмешательств на опорно – двигательной системе.
Противовирусная терапия гепатита В и С
Противовирусная терапия гепатита В и С (пегилированный интерферон, рибавирин). Все пациенты с гемофилией должны быть вакцинированы против гепатитов в детском возрасте и при отрицательных результатах лабораторных тестов во взрослом (ИФА, ПЦР) на гепатиты. Вакцины предпочтительно вводить подкожно. Больные с гемофилией и ВИЧ должны получать пневмококковую вакцину и ежегодно противогриппозную вакцинацию.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Вакцинация
Пациенты с гемофилией могут быть вакцинированы. Особенно важно проведение вакцинации от гепатита B. При вакцинации предпочтение отдается оральному или подкожному введению препарата, по сравнению с внутримышечным или внутрикожным. Если для данной вакцины доступен только внутримышечный путь введения, необходима заместительная терапия для предотвращения развития гематомы. В этом случае заместительную терапию проводят накануне вакцинации. В день вакцинации введение препарата не рекомендуется. Нельзя проводить вакцинацию во время кровотечения.
Включение в клинический протокол незарегистрированных в Республике Узбекистан лекарственных средств не является основанием для возмещения в рамках гарантированного объема бесплатной медицинской помощи и в системе обязательного социального медицинского страхования.
Таблица 12
Перечень основных лекарственных средств (имеющих 100 % вероятность применения)
Включение в клинический протокол незарегистрированных в Республике Узбекистан лекарственных средств не является основанием для возмещения в рамках гарантированного объема бесплатной медицинской помощи и в системе обязательного социального медицинского страхования.
Таблица 12
Перечень основных лекарственных средств (имеющих 100 % вероятность применения)
|
Фармакотерапевтическая группа
|
МНН лекарственного средства
|
Способ применения
|
Уровень доказательности
|
|
Препараты, получаемые из крови
|
фактор свертывания крови VIII, лиофилизат для приготовления раствора для внутривенного введения во флаконе (при гемофилии А)
|
внутривенно
|
Уровень
убедительности рекомендаций C (уровень достоверности доказательств – 5 |
|
|
фактор свертывания крови IX, порошок лиофилизированный для приготовления раствора для внутривенного введения во флаконе (при гемофилии В)
|
внутривенно
|
|
|
|
Антиингибиторный коагулянтный комплекс, лиофилизат для приготовления раствора для внутривенного введения во флаконе (при ингибиторной форме гемофилии А или В)
|
внутривенно
|
|
|
|
октоког альфа, лиофилизат для приготовления раствора для внутривенного введения во флаконе (при ингибиторной форме гемофилии А или В);
|
внутривенно
|
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2 |
|
|
мороктоког альфа, лиофилизат для приготовления раствора для внутривенного введения во флаконе (при гемофилии А);
|
внутривенно
|
|
|
|
нонаког альфа, лиофилизат для приготовления раствора для внутривенного введения во флаконе (при гемофилии В);
|
внутривенно
|
|
|
|
эптаког альфа, лиофилизат для приготовления раствора для внутривенного введения во флаконе (при ингибиторной форме гемофилии А или В);
|
внутривенно
|
|
|
Рекомбинантные факторы свёртывания крови
|
фактор свертывания крови VIII, лиофилизат для приготовления раствора для внутривенного введения во флаконе (при гемофилии А)
|
внутривенно
|
Уровень
убедительности рекомендаций А (уровень достоверности доказательств – 1 |
|
|
фактор свертывания крови IX, порошок лиофилизированный для приготовления раствора для внутривенного введения во флаконе (при гемофилии В)
|
внутривенно
|
|
|
Рекомбинантные факторы свёртывания крови
|
фактор свертывания крови VII, лиофилизат для приготовления раствора для внутривенного введения во флаконе (при массивном кровотечении)
|
внутривенно
|
|
|
Моноклональные антитела
|
Эмицизумаб
|
п/к
|
Уровень
убедительности рекомендаций C (уровень достоверности доказательств – 5 |
Препараты факторов свертывания крови выбираются по принципу индивидуальной переносимости. В международных рекомендациях нет четких указаний на преимущество выбора. Естественно, при конкретном случае назначается только один вид факторов свертывания крови. При ингибиторной форме возможно их сочетание.
Таблица 13
Перечень дополнительных лекарственных средств (менее 100 % вероятности применения)
Перечень дополнительных лекарственных средств (менее 100 % вероятности применения)
|
Фармакотерапевтическая группа
|
МНН лекарственного средства
|
Способ применения
|
Уровень доказательности
|
|
Свежезамороженная плазма
|
|
в/в
|
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5
|
|
Криопреципитат
|
|
в/в
|
|
|
Гемостатитики
|
Транексамовая кислота
Этамзилат |
в/в, таб
|
|
|
Антифибринолитики
|
Е-аминокапроновая Кислота 5%,100мл
|
в/в
|
|
|
Антибактериальные средства
|
Пеницилины Макролиды Сульфаниламиды Фторхинолоны
|
в/в, таб
|
|
|
Гормоны Глюкокортикостероиды
|
Десмопрессин, раствор 4мкг/мл Гидрокортизон Преднизолон Дексаметазон
|
Спрей Наружное, внутрисуставное
|
|
|
Нестероидные противовоспалительные препараты
|
парацетамол целекоксиб мелоксикам нимесулид
|
Растворы для в/в
Таб Капс Порошок |
|
|
Противотуберкулезные лекарственные средства
|
рифампицин лиофилизат для приготовления раствора для инъекций.
|
внутрисуставное
|
|
|
Опиоидные анальгетики
|
Трамадол
Морфин Промедол |
в/в
|
|
|
Спазмолитические лекарственные средства
|
Дротаверин Спазмолгон
|
в/в, таб
|
|
|
Растворы, применяемые для коррекции нарушений водного, электролитного и кислотноосновного баланса
|
натрия хлорид 0,9%;
калия хлорид; декстроза 5% калия хлорид 7,5% декстроза 10% |
раствор для инфузии –раствор для инъекции в ампулах;
|
|
|
Антисептики
|
хлоргексидин 0,05; этанол раствор 70, 90 %;
повидон йод; перекись водорода раствор 3 %; йод раствор спиртовой 5 %. |
раствор для наружного применения
|
|
|
Антиретровирусные лекарственные средства Нуклеозидные ингибиторы обратной транскриптазы
|
рибавирин
|
капсула
|
|
|
Иммуномодуляторы
|
пегинтерферон альфа 2в.
|
в/в
|
*Возможно применение только одного представителя группы или их комбинация.
В данном протоколе представлены не все исчерпывающие лекарственные средства, так как при наличии патологии сопутствующей, например, инфекционных осложнений назначаются те препараты, которые указаны в соответствующих рекомендациях. По усмотрению лечащего врача и по консультации узких специалистов могут быть назначены синдромальная или симптоматическая терапия.
В данном протоколе представлены не все исчерпывающие лекарственные средства, так как при наличии патологии сопутствующей, например, инфекционных осложнений назначаются те препараты, которые указаны в соответствующих рекомендациях. По усмотрению лечащего врача и по консультации узких специалистов могут быть назначены синдромальная или симптоматическая терапия.
Хирургическое вмешательство, оказываемое в стационарных условиях:
Плановое хирургическое вмешательство возможно в многопрофильных лечебных учреждениях, имеющих лабораторную службу, которая обладает техническим и кадровым потенциалом исследования системы гемостаза с определением активности факторов свертывания, ингибирующих антител;
анестезиолога, имеющего опыт лечения больных с нарушениями свѐртывания крови; гематолога [2] (уровень доказательности С).
Хирурги-ортопеды должны получить специальное обучение для проведения хирургического лечения больных с гемофилией [9].
анестезиолога, имеющего опыт лечения больных с нарушениями свѐртывания крови; гематолога [2] (уровень доказательности С).
Хирурги-ортопеды должны получить специальное обучение для проведения хирургического лечения больных с гемофилией [9].
Синовэктомия:
Синовэктомию следует предусматривать, если хронический синовит продолжает проявляться с частыми повторяющимися кровоизлияниями,
неконтролируемыми другими средствами. Варианты синовэктомии включают химический и радиоизотопный синовиортез и артроскопическую или открытую хирургическую синовэктомию. Нехирургическая синовэктомия – это предпочтительный метод лечения.
Химический синовиортез с рифампицином является адекватной альтернативой. Химический синовиортез включает еженедельные инъекции до тех пор, пока синовит не будет взят под контроль.
Эти болезненные инъекции требуют введения внутрисуставного ксилокаина за несколько минут до инъекции склерозирующего агента, болеутоляющих средств для приёма внутрь (комбинированный препарат с ацетаминофеном / парацетамолом и опиоидом) и дозы концентрата фактора до каждой инъекции.
Хирургическая синовэктомия, открытая или артроскопическая, требует большого запаса фактора свёртывания как для хирургической операции, так и для продолжительного периода реабилитации. Эту процедуру должна выполнять опытная бригада в специализированном центре по лечению гемофилии. Она рассматривается только тогда, когда менее инвазивные и равно эффективные процедуры безуспешны.
Хирургические вмешательства включают в себя также артроскопию, артродез, остеотомию, протезирование суставов.
неконтролируемыми другими средствами. Варианты синовэктомии включают химический и радиоизотопный синовиортез и артроскопическую или открытую хирургическую синовэктомию. Нехирургическая синовэктомия – это предпочтительный метод лечения.
Химический синовиортез с рифампицином является адекватной альтернативой. Химический синовиортез включает еженедельные инъекции до тех пор, пока синовит не будет взят под контроль.
Эти болезненные инъекции требуют введения внутрисуставного ксилокаина за несколько минут до инъекции склерозирующего агента, болеутоляющих средств для приёма внутрь (комбинированный препарат с ацетаминофеном / парацетамолом и опиоидом) и дозы концентрата фактора до каждой инъекции.
Хирургическая синовэктомия, открытая или артроскопическая, требует большого запаса фактора свёртывания как для хирургической операции, так и для продолжительного периода реабилитации. Эту процедуру должна выполнять опытная бригада в специализированном центре по лечению гемофилии. Она рассматривается только тогда, когда менее инвазивные и равно эффективные процедуры безуспешны.
Хирургические вмешательства включают в себя также артроскопию, артродез, остеотомию, протезирование суставов.
Лечение псевдоопухоли [1]
Лечение зависит от места, размера, темпов роста и влияния на прилегающие структуры. Варианты лечения включают замещение фактора и наблюдение, аспирацию и хирургическую абляцию. Необходима мультидисциплинарная бригада гематологов, хирургов, ортопедов, травматологов, сосудистых и интервенционных хирургов, невропатологов, нейрохирургов, урологов, реаниматологов. Вся бригада должна иметь знания и желательно опыт работы с подобными больными. Предпочтительней республиканский уровень оказания подобной помощи.
Рекомендуется шестинедельный курс лечения фактором с последующими повторением магнитно-резонансного исследования. Если опухоль уменьшается, продолжать лечение фактором и периодически повторять магнитно- резонансное исследование.
Если необходимо, провести хирургическую операцию; она пройдѐт намного легче, если опухоль сократилась в размерах.
Очень важно исключить возможную ингибиторную форму при подобных состояниях и обеспечивать гемостаз при хирургическом вмешательстве с использованием шунтирующих гемостатических средств (эптаког альфа, антиингибиторный коагулянтный комплекс).
Если необходимо, провести хирургическую операцию; она пройдѐт намного легче, если опухоль сократилась в размерах.
Очень важно исключить возможную ингибиторную форму при подобных состояниях и обеспечивать гемостаз при хирургическом вмешательстве с использованием шунтирующих гемостатических средств (эптаког альфа, антиингибиторный коагулянтный комплекс).
Дальнейшее ведение:
Наблюдение гематолога с целью диспансеризации:
-
пациенты с тяжелой формой и пациенты, получающие постоянное профилактическое лечение – не менее 4 раз в год;
-
остальные 1 – 2 раза в год.
Наблюдение ортопеда:
пациенты без нарушений опорно-двигательного аппарата – 1 раз в год;
остальные – не менее 2 раз в год.
остальные – не менее 2 раз в год.
Наблюдение стоматолога:
2 раза в год, при необходимости чаще;
остальные специалисты (врач ЛФК, психолог) должны осматривать пациента не реже 1 раза в год. При необходимости чаще.
Контроль уровня фактора и определение ингибитора:
остальные специалисты (врач ЛФК, психолог) должны осматривать пациента не реже 1 раза в год. При необходимости чаще.
Контроль уровня фактора и определение ингибитора:
-
первые 20 дней введения концентрата фактора свертывания – каждые 5 – дней введения;
-
после 20, до 50 дней введения 1 раз в 10 дней введения;
-
далее – не реже 1 раза в год.
Объем лабораторной диагностики на амбулаторном уровне описан в соответствующем разделе настоящего протокола.
Терапевты и/или врачи ВОП осматривают пациента по поводу обращений, направляют согласно рекомендациям гематолога на госпитализацию или
диспансеризацию. Самостоятельно не определяют индивидуальную программу лечения пациента, а только следуют указаниям гематологов и контролируют эффективность своих действий.
Индикаторы эффективности лечения [3]:
Терапия должна контролироваться клинически и лабораторно. При клиническом контроле, решение о недостаточной эффективности профилактической заместительной терапии принимается в случаях:
-
более 2 эпизодов спонтанных гемартрозов в год;
-
появления признаков хронического синовита или артропатии;
-
выраженных спонтанных геморрагических проявлениях другой локализации;
Лабораторный контроль заключается в анализе остаточной активности фактора перед следующим введением (не ниже 1%), анализа наличия ингибитора, и по- возможности построения фармакокинетической кривой в течение 3 – 5 дней.
Критерии ответа на терапию:
достижение индикаторов эффективности терапии.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УЧЕТОМ ВИДОВ ОКАЗАНИЯ МЕДИЦИНСКОЙ ПОМОЩИ:
Показания для плановой госпитализации:
Плановая госпитализация осуществляется преимущественно в отделения гематологии.
Допускается госпитализация пациента для получения плановой помощи в профильное отделение по превалирующей симптоматике, согласовывается с гематологом.
При ортопедической и хирургической реабилитации госпитализация осуществляется в отделение гематологии или травматологии и/или ортопедии. Реконструктивно-восстановительные операции, ортопедическая и хирургическая реабилитация больных с рецидивирующими гемартрозами и тяжелой артропатией, лечение ингибиторных форм гемофилии, плановое лечение при наличии сопутствующей патологии.
Преимущество для госпитализации должно оставляться за многопрофильным стационаром с наличием мультидисциплинарной бригадой хирургов, наличием штатного гематолога с опытом оказания пособия при хирургических вмешательствах больным с гемофилией, возможности провести лабораторную диагностику (определение факторов свертывания крови и ингибиторов к ним). Обеспечение факторами свертывания крови плановых операций производится в соответствии с нормативным регулированием в области лекарственного обеспечения в Республике Узбекистан. Допускается использование препаратов факторов свертывания крови, которыми обеспечиваются пациенты за счет целевых текущих трансфертов (по аналогии с больными сахарным диабетом), так как в данном случае расчет заместительной терапии производится на год.
Допускается госпитализация пациента для получения плановой помощи в профильное отделение по превалирующей симптоматике, согласовывается с гематологом.
При ортопедической и хирургической реабилитации госпитализация осуществляется в отделение гематологии или травматологии и/или ортопедии. Реконструктивно-восстановительные операции, ортопедическая и хирургическая реабилитация больных с рецидивирующими гемартрозами и тяжелой артропатией, лечение ингибиторных форм гемофилии, плановое лечение при наличии сопутствующей патологии.
Преимущество для госпитализации должно оставляться за многопрофильным стационаром с наличием мультидисциплинарной бригадой хирургов, наличием штатного гематолога с опытом оказания пособия при хирургических вмешательствах больным с гемофилией, возможности провести лабораторную диагностику (определение факторов свертывания крови и ингибиторов к ним). Обеспечение факторами свертывания крови плановых операций производится в соответствии с нормативным регулированием в области лекарственного обеспечения в Республике Узбекистан. Допускается использование препаратов факторов свертывания крови, которыми обеспечиваются пациенты за счет целевых текущих трансфертов (по аналогии с больными сахарным диабетом), так как в данном случае расчет заместительной терапии производится на год.
Показания для экстренной госпитализации: [2]
Кровоизлияния в жизненно важные органы (травмы головы, кровоизлияния в головной и спинной мозг, травмы в области спины, шеи, желудочно-кишечные кровотечения, забрюшинные гематомы, массивная гематурия, острая хирургическая патология: острый аппендицит, прободная язва, перитонит, разрыв селезенки и др.).
Госпитализация осуществляется преимущественно в гематологические отделения и/или в профильные отделения организаций здравоохранения в зависимости от наличия превалирующей симптоматики (хирургия, урология, неврология, нейрохирургия, травматология, ОРИТ и пр.), имеющих возможность консультации гематолога, проведения заместительной терапии и необходимых исследований.
При отсутствии необходимости в проведении хирургического вмешательства всегда показана госпитализация в гематологическое отделение. Наличие нарушений витальных функций, признаков шока является показанием для госпитализации в отделение интенсивной терапии.
Следует помнить, что при наличии у пациента жизнеугрожающих кровотечений (гематомезис - рвота «кофейной гущей», мелена, признаки ОНМК, легочное кровотечение и пр.) (см понятие жизнеугрожающих кровотечений в таблице 3) и информации о том, что он болен гемофилией (со слов родственников, пациента, при наличии паспорта больного гемофилией) необходимо как можно скорее ввести внутривенно препарат фактор свертывания крови. Дозировку и правила введения определить в соответствии с инструкцией к лекарственному средству. Если препарат фактора свертывания крови имеется у пациента на руках, можно воспользоваться для введения во избежание наступления угрозы жизни пациента.
Госпитализировать при этом нужно в ближайший стационар, вызвав гематолога на экстренную консультацию. Не допускается длительная транспортировка пациента с гемофилией или подозрением на нее при наличии жизнеугрожающих кровотечений. После стабилизации состояния допускается перевод в специализированный стационар.
При отсутствии в стационаре и на руках у пациента препаратов фактора свертывания крови и наличии жизнеугрожающих кровотечений необходимо незамедлительно начать переливание криопреципитата (с согласования регионального гематолога).
При наличии острых кровотечений помощь нужно оказать в течение 2 часов от момента развития кровотечения. [1]
Информация
Источники и литература
-
Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2024
- Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2024 - 1. World Federation of Hemophilia /Guidelines for the management of hemophilia, 2 edition. Montréal, Québec, Canada : Blackwell Publishing Ltd., 2012. DOI: 10.1111/j.1365- 2516.2022.02909.x.. 2. Алгоритм ведения больных гемофилией. Утвержден Экспертным Советом Министерства здравоохранения Республики Казахстан No 22 от 11.10. 2021. 3. Scottish Intercollegiate Guidelines Network (SIGN). SIGN 50: a guideline developer’s handbook. Edinburgh: SIGN (SIGN publication no. 50). [October 2019]. Available from URL: http://www.sign.ac.uk. Edinburgh : б.н., 2019. 4. Jul 29, 2022 — № 1446, Министерство здравоохранения Республики Беларусь. ПОСТАНОВЛЯЕТ: 1. Утвердить: клинический протокол «Оказание медицинской. 5. Srivastava A, Santagostino E, Dougall A, Kitchen S et al. World Federation of Hemophilia. WFH Guidelines for the Management of Hemophilia, 3rd edition. Haemophilia. 2020;26(Suppl 6):1–158. Santagostino E, Dougall A, Jackson M, Khair K et al. Comprehensive Care of Hemophilia. Haemophilia. 2020;26(Suppl 6):19-34 6. Acquired haemophilia A . Dr. Helen CHAN Man Hong. October 2021 г., Specialist in Haematology & Haematological Oncology. 7. Thrombin generation and whole blood viscoelastic assays in the management of hemophilia: current state of art and future perspectives. Guy Young, Benny Sørensen, Yesim Dargaud, Claude Negrier, Kathleen Brummel-Ziedins and Nigel S. Key. 2019 г., Blood. 8. Зозуля Н. и соавт. Протокол ведения больных «Гемофилия». Москва : Проблемы стандартизации в здравоохранении., 2023 г., Т. 1. 9. Aspects of current management: orthopaedic surgery in haemophilia. 2012, Rodriguez-Merchan EC. 18, 2018 : б.н., Haemophilia, Т. 1, стр. 8 -16. 10. Toward optimal therapy for inhibitors in hemophilia. Christine L. Kempton and Shannon L.Meeks. 364-371., 2019 : The American Society of Hematology Education program. 11. Inhibitor eradication with rituximab in haemophilia: where do we stand. Franchini M, Mannucci PM. 165, Jun 2018 г., Br J Haematol, Т. 6, стр. 600. 12. Optimal treatment strategies for hemophilia: achievements and limitations of current prophylactic regimens. J, Oldenburg. 125, 2021 г., Blood, Т. 13. 13. Risk stratification for inhibitor development at first treatment for severe haemophilia A: a tool for clinical practice. P. C. Ter Avest,* K. Fischer,* M. E. Mancuso, E. Santagostino, V. J. Yuste,§ H. M. Van Den Berg * And J. G. Van Der Bom*. Hemostasys and Trombosys. 2022 14. Guideline on the selection and use of therapeutic products to treat haemophilia and other hereditary bleeding disorders. D. KEELING,* C. TAIT_ and M. MAKRIS . 14, 2018 г., Haemophilia, стр. 671-684. 15. Treatment-related risk factors of inhibitor development in previously untreated patients with hemophilia A: the CANAL cohort study for the CANAL Study group From the Van Cre. Samantha C. Gouw, Johanna G. van der Bom, and H. Marijke van den Berg. 2017 г., Blood. 16. Scientific Working Group Quality of life and Symptoms guidelines. б.м. : European hematology Association 2023. 17. Inhibitors Prevalence, Causes and Diagnosis Owaidah King Faisal Specialist Hospital and RC Saudi Arabia . M., Tarek. March 2022 г., Hemophilia. 18. A randomized comparison of bypassing agents in hemophilia complicated by an inhibitor the FEIBA NоvoSeven Comparative Study. Astermark J. Donfield SM, DiMichele D.M. et.al. . 2, 2017 г., Blood, Т. 109, стр. 546 - 545. 19. How I treat imhibitors in haemophilia. Makris M., Hay C.R.M., Gringeri A., Doirons R. . 18, 2022 г., Haemophilia, стр. 48-53. 20. Pregnancy in carriers of hemophilia. Chi C, Lee CA, Shiltagh N, Khan A, Pollard D, Kadir RA. . 14, 2018 г., Haemophilia, Т. 1, стр. 56 - 54. 21. Switching treatments in haemophilia: is there a risk of inhibitor development Angelo Bianchi . 94, European Journal of Haematology , стр. (284–289), 2023.
Информация
Список основных авторов, дополнительного коллектива авторов:
Полатова Ж.Ш. - д.м.н., профессор, директор Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Махмудова А.Д. - д.м.н., заместитель директора по научной работе Республиканский научно-практический медицинский центр гематологии (РНПМЦГ) МЗ РУз; Узбекистан, г. Ташкент
Махамадалиева Г.З. к.м.н., главный гематолог Республики Узбекистан заведующий отделение трансплантации, Республиканский научно-практический медицинский центр гематологии (РНПМЦГ) МЗ РУз; Узбекистан, г. Ташкент
Бергер И.В. - к.м.н., заместитель главного врача, Республиканский научно-практический медицинский центр гематологии (РНПМЦГ) МЗ РУз; Узбекистан, г. Ташкент
Ибрагимова С. З. - д.м.н., заведующая 1-й онкогематологией Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Еримбетова И. О. - заведующая 3-й онкогематологией Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Арипова Н.В. - заведующая 2-й онкогематологией Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Бабаханова Н.Н. – к.м.н., врач-гематолог 1-й онкогематологии Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Ризаева Ф.А. – к.м.н., врач-гематолог 1-й онкогематологии Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Нигматов Х.К. – врач-гематолог 3-й онкогематологии Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Хадиев Р.К. - врач-гематолог 1-й онкогематологии Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Абдуллаев М.М. - врач-гематолог 2-й онкогематологии Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Якубова А.К. – заведующая дневным отделением Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Абдурахманова Н.Н. – врач-трансфузиолог Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Маматкулова Д.Ф. – к.м.н., врач-гематолог консултативной поликлиники Центра детской гематологии, онкологии и клинической иммунологии (ЦДГОКИ)
Киличева Г.Х. – к.м.н., врач физиотерапевт при РСНПМЦ Гематологии
Иноятов Х.П. – к.м.н., доцент кафедры гематологии и трансфузиологии «Центр развития профессиональной квалификации медицинских работников при” МЗ РУз
Садиев З.Р. – детский гематолог, главный специалист Самаркандской области, заведующий отделенеием онкогематологии Детского Многопрофильного Медицинского Центра МЗ РУз
Рахматова Н.Н. - детский гематолог, главный специалист Бухарской области, заведующий отделенеием онкогематологии Детского Многопрофильного Медицинского Центра МЗ РУз
Игамбердиева М. З. - детский гематолог, главный специалист Андижанской области, заведующий отделением онкогематологии Детского Многопрофильного Медицинского Центра МЗ РУз; Узбекистан;
Рецензенты:
1. Сулейманова Д.Н. – профессор, д.м.н., заведующая центром анемии при РСНПМЦ Гематологии
2. Hegine Khachatryan – PhD, MD Hemophilia and Thrombophilia center, MOH Armenia
Когда были проведены обсуждения: Ученый Совет был проведен 23 февраля 2024 года, заседание рабочей группы № 2.
Киличева Г.Х. – к.м.н., врач физиотерапевт при РСНПМЦ Гематологии
Иноятов Х.П. – к.м.н., доцент кафедры гематологии и трансфузиологии «Центр развития профессиональной квалификации медицинских работников при” МЗ РУз
Садиев З.Р. – детский гематолог, главный специалист Самаркандской области, заведующий отделенеием онкогематологии Детского Многопрофильного Медицинского Центра МЗ РУз
Рахматова Н.Н. - детский гематолог, главный специалист Бухарской области, заведующий отделенеием онкогематологии Детского Многопрофильного Медицинского Центра МЗ РУз
Игамбердиева М. З. - детский гематолог, главный специалист Андижанской области, заведующий отделением онкогематологии Детского Многопрофильного Медицинского Центра МЗ РУз; Узбекистан;
Рецензенты:
1. Сулейманова Д.Н. – профессор, д.м.н., заведующая центром анемии при РСНПМЦ Гематологии
2. Hegine Khachatryan – PhD, MD Hemophilia and Thrombophilia center, MOH Armenia
Когда были проведены обсуждения: Ученый Совет был проведен 23 февраля 2024 года, заседание рабочей группы № 2.
Сокращения, используемые в протоколе:
АГ – артериальная гипертензия
АД – артериальное давление
АЛат – аланинаминотрансфераза
АСат – аспартатаминотрансфераза
ВЕ – Бетезда единица
ИИТ – индукция иммунной толерантности
ИФА – иммуноферментный анализ
КТ – компьютерная томография
ОАК – общий анализ крови
ОАМ – общий анализ мочи
ПЦР – полемеразная цепная реакция
СОЭ – скорость оседания эритроцитов
УЗИ – ультрзвуковое исследование
ФГДС – фиброгастродуоденоскопия
ЧД – частота дыхания
ЧСС – частота сердечных сокращений
ЭКГ – электрокардиография
ЭхоКГ – эхокардиография
ЯМРТ – ядерно-магнитная резонансная томография
Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
АД – артериальное давление
АЛат – аланинаминотрансфераза
АСат – аспартатаминотрансфераза
ВЕ – Бетезда единица
ИИТ – индукция иммунной толерантности
ИФА – иммуноферментный анализ
КТ – компьютерная томография
ОАК – общий анализ крови
ОАМ – общий анализ мочи
ПЦР – полемеразная цепная реакция
СОЭ – скорость оседания эритроцитов
УЗИ – ультрзвуковое исследование
ФГДС – фиброгастродуоденоскопия
ЧД – частота дыхания
ЧСС – частота сердечных сокращений
ЭКГ – электрокардиография
ЭхоКГ – эхокардиография
ЯМРТ – ядерно-магнитная резонансная томография
Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД
|
Расшифровка
|
|
1 |
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа
|
|
2 |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинич. исследований, с применением мета-анализа
|
|
3 |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая
|
|
5
|
Имеется лишь обоснование механизма действия или мнение экспертов
|
Шкала оценки уровней достоверности доказательств (УДД) для профилактических, лечебных, реабилитационных вмешательств
|
УДД
|
Расшифровка
|
|
1
|
Систематический обзор РКИ с применением мета-анализа
|
|
2
|
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа
|
|
3
|
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль»
|
|
5
|
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
|
Шкала оценки уровней убедительности рекомендаций (УУР) для профилактических, диагностических, лечебных, реабилитационных вмешательств
|
УУР
|
Расшифровка
|
|
A |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
|
|
B |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
|
|
C |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
|
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА:
У авторов протоколов отсутствует конфликт интересов;
Данные экспертов (специалистов республики и зарубежных стран) Обзоры мета-анализов, рандомизированных проспективных контролируемых перекрестных клинических исследований.
• Обзоры опубликованных исследований случай-контроль или когортных исследований.
• Систематические обзоры с таблицами доказательств.;
Пересмотр протокола рекомендован через 5 лет после его разработки или при наличии новых методов с уровнем доказательности);
Данные экспертов (специалистов республики и зарубежных стран) Обзоры мета-анализов, рандомизированных проспективных контролируемых перекрестных клинических исследований.
• Обзоры опубликованных исследований случай-контроль или когортных исследований.
• Систематические обзоры с таблицами доказательств.;
Пересмотр протокола рекомендован через 5 лет после его разработки или при наличии новых методов с уровнем доказательности);
Приложение 1
Основные осложнения гемофилии [1, 6, 8, 9].
1.Осложнения со стороны костно – суставной системы:
Наиболее вероятными участками кровоизлияний являются кровоизлияния в суставы и мышцы конечностей. У ребёнка с тяжёлой гемофилией, первый гемартроз, как правило, происходит, когда ребёнок начинает ползать и ходить; обычно в возрасте до двух лет, но иногда позже. При неадекватном лечении, повторяющиеся кровоизлияния приводят к прогрессирующему ухудшению состояния суставов и мышц, к резкой потере функциональности из-за потери подвижности, мышечной атрофии, боли и деформации суставов, и контрактур в течение первых-вторых десяти лет жизни.
Синовит обусловлен постоянным воспалительным процессом после гемартрозов в области синовиальной оболочки, которая в последствии гипертрофируется.
Хроническая гемофилическая артропатия:
Хроническая гемофилическая артропатия может развиться в любое время, начиная со второго десятилетия жизни (и иногда раньше), в зависимости от тяжести кровоизлияния и его лечения. Обусловлен попаданием крови на хрящевую ткань сустава во время гемартроза и усиливается при не проходящем хроническом синовите и повторяющемся гемартрозе, приводя к необратимому поражению сустава. При продолжающейся потери хрящевой ткани развивается прогрессивный артрит, который, включает: вторичные контрактуры мягких тканей атрофию мышц ангулярные деформации.
Деформация может также усугубляться контрактурой, следующей за мышечными кровоизлияниями или невропатией. Стадии артропатии определяются рентгенологически (см. таблицу рентгенологические стадии гемофилической артропатии).
У больных гемофилией переломы встречаются не часто, возможно из-за более низкой способности к передвижению и более низкой интенсивности физической активности. Однако больной с гемофилической артропатией может рисковать получить переломы вокруг суставов со значительной потерей амплитуды подвижности и в костях с остеопорозом.
Деформация может также усугубляться контрактурой, следующей за мышечными кровоизлияниями или невропатией. Стадии артропатии определяются рентгенологически (см. таблицу рентгенологические стадии гемофилической артропатии).
У больных гемофилией переломы встречаются не часто, возможно из-за более низкой способности к передвижению и более низкой интенсивности физической активности. Однако больной с гемофилической артропатией может рисковать получить переломы вокруг суставов со значительной потерей амплитуды подвижности и в костях с остеопорозом.
1. Псевдоопухоли:
Псевдоопухоль – это потенциально угрожающее жизни состояние, уникальное для гемофилии, которое происходит в результате неадекватного лечения кровоизлияний в мягкие ткани, обычно в мышцы, прилегающие к кости, которые могут быть непосредственно поражены. Они чаще всего наблюдаются в длинной трубчатой кости или тазу. При отсутствии лечения Псевдоопухоль может достичь огромных размеров, оказывая давление на нервно-сосудистые структуры и приводя к патологическим переломам. В коже может образоваться свищ, развивается из гематом, патогномонична только для тяжелой формы гемофилии.
процессе развития Псевдоопухоли выделяют три фазы:
1- начальная или обратимая, характеризующаяся формированием вокруг гематомы грануляционного вала, продолжается в среднем около 6 месяцев. На этом этапе возможно спонтанное самоизлечение (детский тип Псевдоопухоли) и регресс на фоне шестинедельного курса заместительной терапии препаратами факторов свертывания.
2- фаза необратимых изменений, характеризуется полным замещением грануляционной фазы зрелой фиброзной, представляет собой ложную геморрагическую кисту, заполненную кровяным детритом и некротическими массами.
3- фаза осложнений зависит от локализации патологического процесса (например, дислокация магистральных сосудов, почек, органов брюшной полости, разрушение крыла подвздошной кости, прорыв наружу через некротизированную капсулу и мягкие ткани и т.д.)
процессе развития Псевдоопухоли выделяют три фазы:
1- начальная или обратимая, характеризующаяся формированием вокруг гематомы грануляционного вала, продолжается в среднем около 6 месяцев. На этом этапе возможно спонтанное самоизлечение (детский тип Псевдоопухоли) и регресс на фоне шестинедельного курса заместительной терапии препаратами факторов свертывания.
2- фаза необратимых изменений, характеризуется полным замещением грануляционной фазы зрелой фиброзной, представляет собой ложную геморрагическую кисту, заполненную кровяным детритом и некротическими массами.
3- фаза осложнений зависит от локализации патологического процесса (например, дислокация магистральных сосудов, почек, органов брюшной полости, разрушение крыла подвздошной кости, прорыв наружу через некротизированную капсулу и мягкие ткани и т.д.)
3. Ингибиторная форма:
«Ингибиторы» при гемофилии относятся к антителам иммуноглобулина (IgG), которые нейтрализуют факторы свёртывания. В настоящее время, когда концентраты факторов свёртывания подвергаются соответствующей вирусной инактивации, ингибиторы факторов FVIII и FIX считаются самыми сильными осложнениями при лечении гемофилии. Развитие ингибитора зависит от наличия генетических и негенетических факторов (возраст начала заместительной терапии, интенсивность лечения, тяжелые кровотечения, оперативные вмешательства) [10].
Присутствие нового ингибитора следует подозревать у любого больного, который клинически не отвечает на лечение факторами свёртывания, особенно, если он прежде отвечал на такое лечение. В этой ситуации, шансы на возврат к норме и период полувыведения перелитого фактора свёртывания сильно снижаются. Ингибиторы чаще встречаются у больных с тяжелыми формами гемофилии по сравнению с больными с умеренной или легкой формами гемофилии. Кумулятивная частота (т.е. риск в течение жизни) развития ингибитора при тяжелой гемофилии типа А находится в диапазоне 20- 30% и приблизительно 5-10% при умеренной и легкой форме заболевания [11].
В развитых странах при тяжелой форме гемофилии типа А ингибитор в среднем развивается к 3 годам жизни и раньше. При умеренной и легкой гемофилии типа А, ингибитор развивается ближе к 30 годам, и часто наблюдается при интенсивном лечении фактором FVIII во время хирургической операции [1,10,11,12,13]. При тяжелой гемофилии ингибиторы не меняют локализацию, частоту или тяжесть кровоизлияния. При умеренной или легкой гемофилии ингибиторы могут нейтрализовать эндогенно синтезируемый фактор FVIII, при этом фактически преобразуя фенотип больного в тяжелый.
Проявления кровоизлияний при умеренной / легкой гемофилии, осложнённых ингибиторами, чаще напоминают проявления наблюдаемые у больных с приобретенной гемофилией типа А (из-за аутоантител фактора FVIII с большим преобладанием кровоизлияний подкожных, в слизистую оболочку, урогенитальных и желудочно-кишечных. Следовательно, риск сильных осложнений или даже смертельного исхода от кровоизлияния у этих больных может быть значительным.
Присутствие нового ингибитора следует подозревать у любого больного, который клинически не отвечает на лечение факторами свёртывания, особенно, если он прежде отвечал на такое лечение. В этой ситуации, шансы на возврат к норме и период полувыведения перелитого фактора свёртывания сильно снижаются. Ингибиторы чаще встречаются у больных с тяжелыми формами гемофилии по сравнению с больными с умеренной или легкой формами гемофилии. Кумулятивная частота (т.е. риск в течение жизни) развития ингибитора при тяжелой гемофилии типа А находится в диапазоне 20- 30% и приблизительно 5-10% при умеренной и легкой форме заболевания [11].
В развитых странах при тяжелой форме гемофилии типа А ингибитор в среднем развивается к 3 годам жизни и раньше. При умеренной и легкой гемофилии типа А, ингибитор развивается ближе к 30 годам, и часто наблюдается при интенсивном лечении фактором FVIII во время хирургической операции [1,10,11,12,13]. При тяжелой гемофилии ингибиторы не меняют локализацию, частоту или тяжесть кровоизлияния. При умеренной или легкой гемофилии ингибиторы могут нейтрализовать эндогенно синтезируемый фактор FVIII, при этом фактически преобразуя фенотип больного в тяжелый.
Проявления кровоизлияний при умеренной / легкой гемофилии, осложнённых ингибиторами, чаще напоминают проявления наблюдаемые у больных с приобретенной гемофилией типа А (из-за аутоантител фактора FVIII с большим преобладанием кровоизлияний подкожных, в слизистую оболочку, урогенитальных и желудочно-кишечных. Следовательно, риск сильных осложнений или даже смертельного исхода от кровоизлияния у этих больных может быть значительным.
Ингибиторы намного реже встречаются при гемофилии B и имеют место у менее 5% пораженных больных.
Во всех случаях, ингибиторы затрудняют лечение гемофилии заместительными концентратами факторов. Поэтому больные, находящиеся на терапии фактором свёртывания, должны проходить скрининговые тесты на развитие ингибитора [19].
Детям скрининг на ингибиторы следует проводить один раз каждые 5 дней лечения фактором до 20 дней лечения, каждые 10 дней лечения фактором между 21 и 50 днём лечения, и, по крайней мере, два раза в год в течение 150 дней лечения. Для взрослых с более чем 150 днями лечения фактором, помимо 6-12 месячной оценки, любое отсутствие реакции на заместительную терапию концентратов адекватного фактора у ранее реагирующих больных является показанием для оценки на наличие ингибитора [15].
Измерение ингибитора следует также проводить у всех больных, которые интенсивно лечились в течение более пяти дней, в течение четырёх недель с момента последнего вливания. Ингибиторы следует также оценивать перед хирургической операцией или если тесты на возвращение к норме не такие как ожидаются, и когда в послеоперационный период клиническая реакция на лечение кровоизлияния ниже оптимальной. [16]
Низкореагирующий ингибитор определяется как уровень ингибитора, который постоянно удерживается < 5 ЕБ/мл, в то время как высокореагирующий ингибитора определяется по уровню ≥ 5 ЕБ/мл.
Высокореагирующие (см понятие в разделе лабораторной диагностики) ингибиторы имеет тенденцию не исчезать. Если их не лечить в течение долгого времени, то уровни титров могут упасть и даже стать не обнаруживаемыми, но при этом повторное лечение отдельными продуктами фактора через три-пять дней может дать повторную анамнестическую реакцию. [17]
Некоторые ингибиторы с низким титром имеют транзиторную форму, исчезая в течение шести месяцев первоначального документирования, несмотря на недавние антигенное лечение концентратами фактора.
Ингибиторы с очень низкими титрами могут не обнаруживаться тестом на ингибиторы Бетезда, но могут быть обнаружены ввиду низкого уровня возврата к норме и / или укороченного периода полувыведения (T-1/2) после введения фактора свёртывания.
У почти 50% больных с гемофилией В с ингибиторами могут развиваться сильные аллергические реакции, включая анафилаксию, на введение фактора FIX. Такие реакции могут быть первым симптомом развития ингибитора.
Во всех случаях, ингибиторы затрудняют лечение гемофилии заместительными концентратами факторов. Поэтому больные, находящиеся на терапии фактором свёртывания, должны проходить скрининговые тесты на развитие ингибитора [19].
Детям скрининг на ингибиторы следует проводить один раз каждые 5 дней лечения фактором до 20 дней лечения, каждые 10 дней лечения фактором между 21 и 50 днём лечения, и, по крайней мере, два раза в год в течение 150 дней лечения. Для взрослых с более чем 150 днями лечения фактором, помимо 6-12 месячной оценки, любое отсутствие реакции на заместительную терапию концентратов адекватного фактора у ранее реагирующих больных является показанием для оценки на наличие ингибитора [15].
Измерение ингибитора следует также проводить у всех больных, которые интенсивно лечились в течение более пяти дней, в течение четырёх недель с момента последнего вливания. Ингибиторы следует также оценивать перед хирургической операцией или если тесты на возвращение к норме не такие как ожидаются, и когда в послеоперационный период клиническая реакция на лечение кровоизлияния ниже оптимальной. [16]
Низкореагирующий ингибитор определяется как уровень ингибитора, который постоянно удерживается < 5 ЕБ/мл, в то время как высокореагирующий ингибитора определяется по уровню ≥ 5 ЕБ/мл.
Высокореагирующие (см понятие в разделе лабораторной диагностики) ингибиторы имеет тенденцию не исчезать. Если их не лечить в течение долгого времени, то уровни титров могут упасть и даже стать не обнаруживаемыми, но при этом повторное лечение отдельными продуктами фактора через три-пять дней может дать повторную анамнестическую реакцию. [17]
Некоторые ингибиторы с низким титром имеют транзиторную форму, исчезая в течение шести месяцев первоначального документирования, несмотря на недавние антигенное лечение концентратами фактора.
Ингибиторы с очень низкими титрами могут не обнаруживаться тестом на ингибиторы Бетезда, но могут быть обнаружены ввиду низкого уровня возврата к норме и / или укороченного периода полувыведения (T-1/2) после введения фактора свёртывания.
У почти 50% больных с гемофилией В с ингибиторами могут развиваться сильные аллергические реакции, включая анафилаксию, на введение фактора FIX. Такие реакции могут быть первым симптомом развития ингибитора.
4. Осложнения, возникающие из-за инфекций, передающихся при переливаниях крови, и других инфекций:
Появление и передача инфекций ВИЧ, вируса гепатита B и вируса гепатита C через продукты факторов свёртывания привело к высокой смертности больных гемофилией в 1980-ые годы и в начале 1990-х годов [1]. Многие исследования, проведённые во всём мире, указывают на то, что передача инфекций ВИЧ, вируса гепатита B и вируса гепатита C через концентраты фактора почти полностью устранена.
В настоящее время, при проведении адекватной заместительной терапии препаратами факторами свертывания крови имеется возможность терапии данных инфекций, которые рассмотрены в соответствующих разделах настоящего протокола.[21]
В настоящее время, при проведении адекватной заместительной терапии препаратами факторами свертывания крови имеется возможность терапии данных инфекций, которые рассмотрены в соответствующих разделах настоящего протокола.[21]
Приложение 2
Другие виды лечения, оказываемые при возникновении некоторых распространенных видов кровотечений [2,3]:
Острый гемартроз.
Целью лечения острого гемартроза является остановка кровоизлияния в кратчайшие сроки. Желательно это сделать, сразу же после того, как больной ощутит «ауру», чем после наступления явного отека и боли
В случае развития острого гемартроза необходимо предпринять следующие действия:
- Ввести препарат фактора свертывания крови VIII\IX (в зависимости от типа гемофилии) в дозе 20-30 МЕ/кг веса больного. В случае отсутствия полного регресса патологической симптоматики через 12 часов повторить введение препарата
- Защитить пораженный сустав от статической нагрузки массы тела не менее чем на 24–48 ч, в том числе поддержка костылями и фиксаторами.
- Пораженная конечность должна быть полностью расслаблена в наиболее комфортном для нее положении, что способствует ускорению рассасывания отека.
- Холод способствует уменьшению отека, предупреждает дальнейшее
кровотечение и облегчает боль. Необходимо использовать криопакеты сразу же после появления первых симптомов кровотечения. Криотерапию следует применять по 10–15 мин каждые 2 часа и не допускать контакта хладагента с кожей во избежание термической травмы.
- Компрессия снижает отечность, следовательно, и боль. Целесообразно применять эластичные бинты или фиксаторы, однако следует помнить, что
слишком тугая давящая повязка может вызвать дополнительные повреждения ткани. Желательно не допускать складок при наложении повязок и не оставлять их на ночь.
- Возвышенное положение конечности снижает приток крови и способствует оттоку крови из поврежденной области. Приподнимать конечность следует выше уровня сердца, освободив ее от сдавливающей повязки, на 20 минут, возвращая в исходное положение на 20.
- Защитить пораженный сустав от статической нагрузки массы тела не менее чем на 24–48 ч, в том числе поддержка костылями и фиксаторами.
- Пораженная конечность должна быть полностью расслаблена в наиболее комфортном для нее положении, что способствует ускорению рассасывания отека.
- Холод способствует уменьшению отека, предупреждает дальнейшее
кровотечение и облегчает боль. Необходимо использовать криопакеты сразу же после появления первых симптомов кровотечения. Криотерапию следует применять по 10–15 мин каждые 2 часа и не допускать контакта хладагента с кожей во избежание термической травмы.
- Компрессия снижает отечность, следовательно, и боль. Целесообразно применять эластичные бинты или фиксаторы, однако следует помнить, что
слишком тугая давящая повязка может вызвать дополнительные повреждения ткани. Желательно не допускать складок при наложении повязок и не оставлять их на ночь.
- Возвышенное положение конечности снижает приток крови и способствует оттоку крови из поврежденной области. Приподнимать конечность следует выше уровня сердца, освободив ее от сдавливающей повязки, на 20 минут, возвращая в исходное положение на 20.
Мышечные кровоизлияния: могут произойти в любой мышце тела, обычно из- за прямого удара или внезапного растяжения.
Мышечное кровоизлияние определяется как эпизод кровоизлияния в мышцу, определённое клинически и / или с помощью визуализирующих исследований, обычно связанный с болью и / или опуханием и ухудшением функциональности, например, хромотой из-за кровоизлияния в заднюю часть голени [1].
Раннее распознание и соответствующее лечение мышечных кровоизлияний важно для предупреждения стойкой контрактуры мышц, повторного кровоизлияния и образования псевдоопухолей.
Места мышечных кровоизлияний, которые связаны с повреждением нервно- сосудистого пучка, таких как глубокие группы мышц-сгибателей в конечностях, потребуют немедленного лечения, чтобы предупредить стойкое повреждение и потерю функциональности.
Эти группы включают:
-
подвздошно-поясничную мышцу (риск феморально-кожного, бедренного и феморального паралича)
-
верхне-задние и глубокие задние отделы низа ноги (риск повреждения заднего большеберцового и глубокого малоберцового нерва)
-
группу мышц-сгибателей предплечья (риск ишемической контрактуры Фолькмана)
-
Кровоизлияние может также иметь место в поверхностных мышцах, таких как двуглавая мышца, задние мышцы бедра (трицепс голени), икроножная мышца, четырёхглавая мышца и ягодичные мышцы.
-
Симптомы мышечного кровоизлияния:
-
Ноющая боль в мышце
-
Удерживание конечности в положении комфорта Сильная боль при растягивании мышцы
-
Боль при активном сокращении мышцы
-
Напряжение и болезненность при пальпации, и возможное опухание
Поднять фактор больного как можно скорее, желательно, когда больной почувствует первые признаки дискомфорта или после травмы. Если есть повреждение нервно-сосудистого пучка, поддерживать уровень от пяти до семи дней или дольше, как показывают симптомы. Дать покой повреждённой части и приподнять конечность. На мышцу в положении комфорта наложить шину и довести конечность до положения функциональности, насколько позволит боль.
Если это помогает, вокруг мышцы на 15-20 минут каждый час можно прикладывать холодные пакеты / пакеты со льдом. Лёд не должен быть в прямом контакте с кожей. В случае кровоизлияний в критические места, вызывающие синдром сдавливания, и если требуется длительная реабилитация, часто необходимы неоднократные вливания в течение двух-трёх дней или намного дольше. Больного следует непрерывно наблюдать на случай повреждения нервно-сосудистого пучка; в таких случаях может потребоваться фасциотомия.
Поскольку мышечные кровоизлияния могут привести к значительной потере крови, если необходимо, следует проверять и корректировать уровень гемоглобина.
Физиотерапию следует начинать как можно скорее при уменьшении боли и проводить её постепенно для восстановления полной длины, силы и функциональности мышцы.
Во время этого процесса разумно лечение фактором, кроме тех случаев, когда физиотерапевт имеет опыт в лечении гемофилии. Для этого может потребоваться периодическое наложение гипса или шин. Если был повреждён нерв, то потребуется поддерживающая повязка. Усиливающая боль во время физиотерапии может означать повторное кровоизлияние и должна регулярно подвергаться оценке.
Кровоизлияние в подвздошную-поясничную область.
У этого типа мышечного кровоизлияния уникальное проявление. Признаки могут включать боль внизу живота, в паху, и / или в пояснице и боль при растягивании, но не при вращении, тазобедренного сустава. При этом в средней части бедра может наблюдаться парестезия и другие признаки сдавливания феморального нерва, такие как потеря коленного рефлекса и слабость в четырёхглавой мышце.
Симптомы могут быть похожими на острый аппендицит, включая положительные симптомы Щеткина-Блюмберга.
Срочно поднять уровень фактора больного. Поддерживать уровень от пяти до семи дней или дольше в зависимости от симптомов
Госпитализировать больного для наблюдения и контроля боли. Придерживаться строго постельного режима. Ходьба с костылями не разрешается, поскольку для ходьбы требуется сокращение мышц
Ограничить активность больного до исчезновения боли и улучшения разгибания бедра. Программа физиотерапии с тщательным наблюдением – ключ к восстановлению полной активности и функциональности и предупреждению повторного кровоизлияния. До возврата к полной активности рекомендуется восстановление полного разгибания бедра. При сохранении остаточного нервномышечного дефицита может потребоваться дополнительная ортопедическая поддержка.
Симптомы могут быть похожими на острый аппендицит, включая положительные симптомы Щеткина-Блюмберга.
Срочно поднять уровень фактора больного. Поддерживать уровень от пяти до семи дней или дольше в зависимости от симптомов
Госпитализировать больного для наблюдения и контроля боли. Придерживаться строго постельного режима. Ходьба с костылями не разрешается, поскольку для ходьбы требуется сокращение мышц
Ограничить активность больного до исчезновения боли и улучшения разгибания бедра. Программа физиотерапии с тщательным наблюдением – ключ к восстановлению полной активности и функциональности и предупреждению повторного кровоизлияния. До возврата к полной активности рекомендуется восстановление полного разгибания бедра. При сохранении остаточного нервномышечного дефицита может потребоваться дополнительная ортопедическая поддержка.
Почечное кровотечение.
Следует назначить полный постельный режим, интенсивную гидратацию (3000 мл воды на 1 кв. метр площади тела) в течение 48 часов, ввести препараты факторов свертывания крови в дозе 20-25 МЕ/кг веса больного. Не использовать антифибринолитики.
При отсутствии клинического улучшения в течение 2х суток, либо рецидивирующего характера кровотечения необходима консультация уролога для исключения патологии мочевыводящих путей.
минут. [2] [3] [4] [5] [6] [7]
При отсутствии клинического улучшения в течение 2х суток, либо рецидивирующего характера кровотечения необходима консультация уролога для исключения патологии мочевыводящих путей.
минут. [2] [3] [4] [5] [6] [7]
Кровоизлияние в брюшную полость:
Острое кровоизлияние в брюшную полость, включая кровоизлияния в забрюшинное пространство, может проявляться болью в животе и вздутием живота и может ошибочно принято за инфекционные и другие заболевания, требующие хирургического вмешательства. Оно может также проявляться в виде паралитической непроходимости кишечника. Могут потребоваться соответствующие рентгенологические исследования. Немедленно поднять уровень фактора пациента. Поддерживать уровни фактора, до тех пор, пока не будет выяснена этиологии, затем лечить при консультации со специалистом.
Кровоизлияние в головной мозг и центральную нервную систему.
Это состояние, представляющее опасность для жизни и требующее срочной медицинской помощи. Сначала провести лечение, затем оценку.
Все посттравматические черепно-мозговые травмы, подтверждённые или подозреваемые, как и серьёзные головные боли должны рассматриваться как внутричерепные кровоизлияния. Не ждать появления последующих симптомов, лабораторной или рентгенологической оценки.
Когда происходит значительная травма или имеют место подобные симптомы, немедленно поднять уровень фактора больного. Дальнейшие дозы будут зависеть от результатов визуализирующих исследований. Уровень фактора поддерживать до тех пор, пока не будет определена этиология. Если кровоизлияние подтверждено, поддерживать адекватный уровень фактора в течение 10-14 дней.
Все посттравматические черепно-мозговые травмы, подтверждённые или подозреваемые, как и серьёзные головные боли должны рассматриваться как внутричерепные кровоизлияния. Не ждать появления последующих симптомов, лабораторной или рентгенологической оценки.
Когда происходит значительная травма или имеют место подобные симптомы, немедленно поднять уровень фактора больного. Дальнейшие дозы будут зависеть от результатов визуализирующих исследований. Уровень фактора поддерживать до тех пор, пока не будет определена этиология. Если кровоизлияние подтверждено, поддерживать адекватный уровень фактора в течение 10-14 дней.
Внутричерепные кровоизлияния могут быть показанием для долгосрочной вторичной профилактики (от трёх до шести месяцев), особенно, если наблюдается относительно высокий риск повторного эпизода (например, в присутствие ВИЧ инфекции). Требуется немедленная медицинская оценка и госпитализация.
Следует выполнить компьютерную томографию или магнитно-резонансное исследование мозга. На ранних стадиях следует пройти консультацию невролога. Сильные головные боли могут также быть признаком менингита у больных с ослабленным иммунитетом.
Следует выполнить компьютерную томографию или магнитно-резонансное исследование мозга. На ранних стадиях следует пройти консультацию невролога. Сильные головные боли могут также быть признаком менингита у больных с ослабленным иммунитетом.
Кровоизлияния в горло и шею.
Состояние, угрожающее жизни и требующее срочной медицинской помощи, поскольку может привести к нарушению проходимости дыхательных путей.
Сначала провести лечение, затем оценку. В случае значительной травмы или появления симптомов немедленно поднять уровень фактора больного. Поддерживайте уровни фактора до исчезновения симптомов. Ранняя госпитализация в хирургическое или гематологическое отделения. Для предупреждения кровоизлияния у больных с сильным тонзиллитом, показано лечение фактором в дополнение к лечению бактериальными культурами и соответствующими антибиотиками.
Сначала провести лечение, затем оценку. В случае значительной травмы или появления симптомов немедленно поднять уровень фактора больного. Поддерживайте уровни фактора до исчезновения симптомов. Ранняя госпитализация в хирургическое или гематологическое отделения. Для предупреждения кровоизлияния у больных с сильным тонзиллитом, показано лечение фактором в дополнение к лечению бактериальными культурами и соответствующими антибиотиками.
Острые кровоизлияния в ЖКТ.
Немедленно поднять уровень фактора больного, Поддерживать уровень фактора до остановки кровоизлияния и определения этиологии. Острые желудочно-кишечные кровоизлияния могут проявляться в виде гематомезиса (кровавой рвоты), кровавого или дёгтеобразного стула.
При признаках кровоизлияния в ЖКТ и /или острого кровоизлияния в брюшную полость потребуется медицинская оценка и возможно госпитализация.
Следует регулярно наблюдать уровень гемоглобина. По мере необходимости лечить шок или анемию, лечить источник кровоизлияния: В качестве вспомогательной терапии можно использовать ЭАК или транексамовую кислоту для больных с дефицитом фактора FVIII и больных с дефицитом фактора FIX, которые не получают лечения концентратами протромбинового комплекса.
При признаках кровоизлияния в ЖКТ и /или острого кровоизлияния в брюшную полость потребуется медицинская оценка и возможно госпитализация.
Следует регулярно наблюдать уровень гемоглобина. По мере необходимости лечить шок или анемию, лечить источник кровоизлияния: В качестве вспомогательной терапии можно использовать ЭАК или транексамовую кислоту для больных с дефицитом фактора FVIII и больных с дефицитом фактора FIX, которые не получают лечения концентратами протромбинового комплекса.
Носовые кровотечения:
Наклонить голову больного вперёд, чтобы он не глотал кровь и попросить его мягко выдыхать мелкие сгустки. В течение 10-20 минут следует придавливать марлю, смоченную в ледяной воде, к передней мягкой части носа. Антигистаминные препараты и лекарства от заложенности носа полезны для кровотечений, характерных для аллергий, инфекций верхних дыхательных путей и сезонных изменений. Если кровотечения продолжительные или происходят часто, провести оценку на наличие анемии и применить соответствующее лечение. Полезно местное прикладывание марли, смоченной ЭАК или транексамовой кислотой. Если кровотечение не проходит или повторяется, проконсультируйтесь с отоларингологом. Для контроля кровотечение может потребоваться передняя и задняя тампонада носа. Носовые кровотечение часто можно предупредить, повышая влажность в окружающей среде, нанося гели (например, вазелин или капли солевого раствора /гель) на слизистую оболочку носа для сохранения влажности, или применяя солевой спрей.
Особенности лечебной тактики у беременных [9]
В своем большинстве средний уровень фактора свёртывания крови у носителей гемофилии составляет 50% уровня здорового человека.
Во втором и третьем триместрах уровень фактора свёртывания FVIII обычно повышается до нормального диапазона. В связи с чем у носителей активность фактора следует измерять во время третьего триместра для того, чтобы принять решения о необходимости введении фактора свертывания крови во время родов (уровень доказательности С). В случае активности дефицитного фактора ниже 50%, необходимо в родах проводить заместительную терапию препаратом фактора свёртывания (уровень доказательности С)
Путь родоразрешения у носителей с нормальным плодом следует выбирать согласно акушерским показаниям. Во избежание риска кровотечений, роды младенцев с известной или подозреваемой гемофилией должны проходить атравматично независимо от того, происходят ли роды через естественные пути или кесаревым сечением (уровень доказательности С).
Во втором и третьем триместрах уровень фактора свёртывания FVIII обычно повышается до нормального диапазона. В связи с чем у носителей активность фактора следует измерять во время третьего триместра для того, чтобы принять решения о необходимости введении фактора свертывания крови во время родов (уровень доказательности С). В случае активности дефицитного фактора ниже 50%, необходимо в родах проводить заместительную терапию препаратом фактора свёртывания (уровень доказательности С)
Путь родоразрешения у носителей с нормальным плодом следует выбирать согласно акушерским показаниям. Во избежание риска кровотечений, роды младенцев с известной или подозреваемой гемофилией должны проходить атравматично независимо от того, происходят ли роды через естественные пути или кесаревым сечением (уровень доказательности С).
При влагалищных родах следует избегать использования акушерских щипцов и вакуумной экстракции, а также других инвазивных процедур по отношению к плоду (взятие проб крови с черепа и установка скальповых электродов на кожу черепа плода внутриутробно).
Лечение ингибиторной формы:
Остановка кровотечения при ингибиторной форме:
При гемофилии, осложненной развитием ингибирующих антител, низкореагирующим, расчет разовой дозы препарата фактора свертывания крови производится по формуле:
При гемофилии, осложненной развитием ингибирующих антител, низкореагирующим, расчет разовой дозы препарата фактора свертывания крови производится по формуле:
Y = (М х L х 0,5) + (40 х М х Т)
где
Y - доза фактора свертывания крови для однократного введения (МЕ); M - масса тела больного, кг;
L - процент желаемого уровня фактора в плазме пациента (см таблицу 5) «Процент желаемого уровня фактора и длительность терапии геморрагического эпизода»);
P - исходный уровень фактора у больного до введения препарата. Т- титр антигена
Купирование кровотечения или кровоизлияния у пациентов с ингибиторной формой гемофилии А высокореагирующим производится посредством введения одного из препаратов шунтирующего действия:
-антиингибиторный коагулянтный комплекс (активированный комплекс II, VII, IX, X) 50- 100 МЕ/кг веса каждые 8-12 часов (не более 200 МЕ/ сутки).
Клиническая эффективность обоих препаратов практически одинакова, составляет около 80% [2]. Однако имеет место индивидуальная эффективность одного из препаратов у 1/3 пациентов[3,4].
Купирование кровотечения у пациентов с ингибиторной формой гемофилии В производится посредством введения
Y - доза фактора свертывания крови для однократного введения (МЕ); M - масса тела больного, кг;
L - процент желаемого уровня фактора в плазме пациента (см таблицу 5) «Процент желаемого уровня фактора и длительность терапии геморрагического эпизода»);
P - исходный уровень фактора у больного до введения препарата. Т- титр антигена
Купирование кровотечения или кровоизлияния у пациентов с ингибиторной формой гемофилии А высокореагирующим производится посредством введения одного из препаратов шунтирующего действия:
-антиингибиторный коагулянтный комплекс (активированный комплекс II, VII, IX, X) 50- 100 МЕ/кг веса каждые 8-12 часов (не более 200 МЕ/ сутки).
Клиническая эффективность обоих препаратов практически одинакова, составляет около 80% [2]. Однако имеет место индивидуальная эффективность одного из препаратов у 1/3 пациентов[3,4].
Купирование кровотечения у пациентов с ингибиторной формой гемофилии В производится посредством введения
Лечение ингибиторной формы
У пациентов с ингибиторной формой гемофилии А элиминация ингибитора возможна при проведении терапии индукции иммунной толерантности (ИИТ) (уровень доказательности доказательств В). Оптимальные сроки начала ИИТ – сразу после выявления ингибитора, в случае титра ингибитора между 5 и 10 ВЕ.
Однако сроки лимитируются следующими факторами: комплаентностью пациента, состоянием венозного доступа, титром ингибитора, лабораторным контролем терапии (доступностью диагностики вышеперечисленных лабораторных тестов).
Эффективность ИИТ у пациентов с гемофилией А составляет 70%, с гемофилией В-30% [3]. Предикторами эффективности ИИТ являются: молодой возраст, титр ингибитора на начало ИИТ менее 10 ВЕ, максимальный пик ингибитора менее 200 ВЕ, менее 5 лет между диагностированием ингибитора и началом ИИТ, генетические мутации. В случае если титр выше указанного значения, рекомендуется прекратить инфузии фактора VIII и контролировать титр ингибитора до момента его снижения. (Уровень доказательности В). Сохранение высокого титра ингибитора, не смотря на элиминацию фактора VIII, не является противопоказанием к ИИТ. При проведении ИИТ предпочтение отдается плазменным концентратам фактора VIII, содержащим фактор Виллебранда.
Однако сроки лимитируются следующими факторами: комплаентностью пациента, состоянием венозного доступа, титром ингибитора, лабораторным контролем терапии (доступностью диагностики вышеперечисленных лабораторных тестов).
Эффективность ИИТ у пациентов с гемофилией А составляет 70%, с гемофилией В-30% [3]. Предикторами эффективности ИИТ являются: молодой возраст, титр ингибитора на начало ИИТ менее 10 ВЕ, максимальный пик ингибитора менее 200 ВЕ, менее 5 лет между диагностированием ингибитора и началом ИИТ, генетические мутации. В случае если титр выше указанного значения, рекомендуется прекратить инфузии фактора VIII и контролировать титр ингибитора до момента его снижения. (Уровень доказательности В). Сохранение высокого титра ингибитора, не смотря на элиминацию фактора VIII, не является противопоказанием к ИИТ. При проведении ИИТ предпочтение отдается плазменным концентратам фактора VIII, содержащим фактор Виллебранда.
(Уровень доказательности С).
Для пациентов с высокореагирующим ингибитором, не зависимо от титра ингибитора на момент начала ИИТ рекомендована начальная схема 100 – 150 МЕ/кг каждые 12 часов. [5]
Для пациентов с низкореагирующим ингибитором рекомендовано начинать ИИТ по схеме 50 – 100 МЕ/кг каждый второй день. Если после начала ИИТ титр ингибитора поднимется выше 5 – 7 БЕ необходимо перевести пациента на лечение по схеме, рекомендованной для ИИТ у пациентов с высокореагирующим ингибитором. Снижение дозы и кратности введения препарата начинается после получения лабораторных данных об элиминации ингибитора (титр ингибитора - менее 0,6 БЕ, нормализация теста восстановления и периода полувыведения).
Снижение проводится постепенно с постоянным лабораторным контролем. При этом каждое снижение дозы или кратности возможно только после получения лабораторных данных об отсутствии ингибитора. После достижения дозы в 30 – 50 МЕ/кг 1 раз в 2 дня необходимо продолжить терапию по этой схеме постоянно.
Отмена профилактического лечения часто приводит к рецидиву ингибитора. При проведении ИИТ не допустимо менять препарат концентрата ф. VIII, поскольку, это значительно ухудшает прогноз терапии.
При проведении процедуры ИИТ необходимо избегать любых воздействий и препаратов, стимулирующих иммунные реакции, в том числе вакцинации, применения препаратов интерферона и других видов иммунотерапии. Рецидивы кровоизлияний ухудшают прогноз ИИТ, поэтому у пациентов с частыми гемартрозами и массивными гематомами мягких тканей в курсе ИИТ показано проведение профилактического лечения шунтирующими препаратами до снижения титра ингибитора менее 1 БЕ. Если в течение 8 – 12 месяцев не происходит снижения титра ингибитора, рекомендовано прекратить ИИТ, перевести пациента на терапию шунтирующими препаратами. В дальнейшем, после снижения титра ингибитора возможно повторить ИИТ с использованием другого препарата [3-6] в сочетании с иммунносупрессивной терапией.
Для пациентов с высокореагирующим ингибитором, не зависимо от титра ингибитора на момент начала ИИТ рекомендована начальная схема 100 – 150 МЕ/кг каждые 12 часов. [5]
Для пациентов с низкореагирующим ингибитором рекомендовано начинать ИИТ по схеме 50 – 100 МЕ/кг каждый второй день. Если после начала ИИТ титр ингибитора поднимется выше 5 – 7 БЕ необходимо перевести пациента на лечение по схеме, рекомендованной для ИИТ у пациентов с высокореагирующим ингибитором. Снижение дозы и кратности введения препарата начинается после получения лабораторных данных об элиминации ингибитора (титр ингибитора - менее 0,6 БЕ, нормализация теста восстановления и периода полувыведения).
Снижение проводится постепенно с постоянным лабораторным контролем. При этом каждое снижение дозы или кратности возможно только после получения лабораторных данных об отсутствии ингибитора. После достижения дозы в 30 – 50 МЕ/кг 1 раз в 2 дня необходимо продолжить терапию по этой схеме постоянно.
Отмена профилактического лечения часто приводит к рецидиву ингибитора. При проведении ИИТ не допустимо менять препарат концентрата ф. VIII, поскольку, это значительно ухудшает прогноз терапии.
При проведении процедуры ИИТ необходимо избегать любых воздействий и препаратов, стимулирующих иммунные реакции, в том числе вакцинации, применения препаратов интерферона и других видов иммунотерапии. Рецидивы кровоизлияний ухудшают прогноз ИИТ, поэтому у пациентов с частыми гемартрозами и массивными гематомами мягких тканей в курсе ИИТ показано проведение профилактического лечения шунтирующими препаратами до снижения титра ингибитора менее 1 БЕ. Если в течение 8 – 12 месяцев не происходит снижения титра ингибитора, рекомендовано прекратить ИИТ, перевести пациента на терапию шунтирующими препаратами. В дальнейшем, после снижения титра ингибитора возможно повторить ИИТ с использованием другого препарата [3-6] в сочетании с иммунносупрессивной терапией.
Таблица 14.
Принципы лечения острого гемартроза у пациентов с гемофилией А
Принципы лечения острого гемартроза у пациентов с гемофилией А
|
Заместительная терапия
|
25–40 МЕ/кг фактора свёртывания крови VIII
50 МЕ/кг при тяжелом или посттравматическом гемартрозе |
|
Иммобилизация
|
Обычно требуется 2-3 инъекции каждые 12 часов (гемофилия А) или 18 часов (гемофилия В)
Без кольцевого пластыря |
|
Освобождение от весовой нагрузки
|
Необходима в острой фазе
|
|
Лед/ криотерапия
|
Лед прикладывается только на 5-15 минут в течение первых 6 часов. Избегать любого прямого контакта с кожей
|
|
Рентгено- логические
исследования |
Редко, за исключением случаев травм
|
|
Обезболивание
|
Парацетамол (с осторожностью при гепатите С), опиоиды, селективные НПВП ЦОГ-2
|
|
Аспирация сустава
|
Тяжелый и напряженный гемартроз после коррекции дефицита коагуляции, в условиях строгой дезинфекции и только в первые 24 часа. При легком гемартрозе не проводится
|
|
Реабилитация
|
Ранний срок начала в целях предотвращения утраты функциональности
|
Сокращения: FVIII – фактор свертывания крови VIII; ЦОГ – циклооксигеназа; НПВС – нестероидные противовоспалительные препараты.
Приложение 3
ПРИОБРЕТЕННАЯ ГЕМОФИЛИЯ
Приложение 3
ПРИОБРЕТЕННАЯ ГЕМОФИЛИЯ
Дифференциальная лабораторная диагностика приобретенной гемофилии
|
Патологическое состояние, терапия Pathological condition, therapy
|
Изменение лабораторных показателей Changes of laboratory parameters
|
Дополнительные лабораторные исследования и диагностические критерии Additional laboratory tests and diagnostic criteria
|
|
Приобретенная гемофилия Acquired hemophilia
|
Удлинение АЧТВ Снижение активности FVIII Тест смешивания по АЧТВ — нет коррекции (ИЦА > 15 %) Ингибитор FVIII > 0,6 БЕ/мл Снижение активности FIX, FXI и FXIIin vitro (при высоком титре ингибитора FVIII) Prolongation of Aptt Reduced FVIII activity APTT mixing test — no correction (ICA > 15 %) FVIII inhibitor > 0.6 BU/mL Reduced FIX, FXI, FXII activity in vitro (with a high duration of action of the FVIII inhibitor)
|
Семейный анамнез не отягощен Болеют мужчины и женщины Недлительный анамнез по кровоточивости Хромогенный метод определения активности FVIII и титра ингибитора к нему (снижает эффект ВА на результаты тестов) Лабораторная методика с предварительным разведением плазмы больного буферным раствором (снижение действия высокого титра ингибитора FVIII на активность FIX, FXI и FXII) Non-burdened familial history Affects both men and women Not a long history of bleeding Chromogenic method for determining the activity of FVIII and the titer of an inhibitor to it (reduces the effect of LA on test scores) Laboratory technique with preliminary dilution of the patient’s plasma with a buffer solution (reducing the effect of a high titer of a FVIII inhibitor on the activity of FIX, FXI and FXII)
|
|
Наследственная гемофилия А Hereditary hemophilia A
|
Удлинение АЧТВ Снижение активности FVIII Тест смешивания по АЧТВ — есть коррекция (ИЦА ≤ 15 %) Отсутствует ингибитор FIII < 0,6 БЕ/мл Prolongation of aPTT Reduced FVIII activity APTT mixing test — correction (ICA ≤ 15 %) FVIII inhibitor > 0.6 BU/mL
|
Семейный анамнез отягощен Чаще болеют мужчины Длительный анамнез по кровоточивости Burdened familial history Men get sick more often Long history of bleeding
|
|
Наследственная гемофилия А, ингибиторная форма Hereditary hemophilia A, inhibitory form
|
Удлинение АЧТВ Снижение активности FVIII Тест смешивания по АЧТВ — нет коррекции (ИЦА > 15 %) Ингибитор FVIII > 0,6 БЕ/мл Prolongation of aPTT Reduced FVIII activity APTT mixing test — no correction (ICA > 15 %) FVIII inhibitor > 0.6 BU/mL
|
Семейный анамнез отягощен Чаще болеют мужчины Длительный анамнез по кровоточивости Клиническое ухудшение и неэффективность заместительной терапии Burdened familial history Men get sick more often Long history of bleeding Clinical deterioration and failure of replacement therapy
|
|
Болезнь фон Виллебранда или приобретенный синдром фон Виллебранда von Willebrand disease or acquired von Willebrand syndrome
|
Удлинение АЧТВ Снижение активности FVIII, Снижение активности vWF:Ag и vWF:Rco (зависит от типа болезни фон Виллебранда) Prolongation of aPTT Reduced FVIII activity Reduced vWF:Ag and vWF:Rco activity (depending on the type of von Willebrand disease)
|
RIPA — ристоцетининдуцированная агрегация тромбоцитов vWF:FVIIIB — FVIII связывающая активность vWF vWF:CB — коллагенсвязывающая активность vWF Мультимерный анализ vWF RIPA — ristocetin-induced platelet aggregation vWF:FVIIIB — vWF: FVIII binding activity vWF:CB — vWF: collagenbinding activity vWF multimeric analysis
|
|
АФС APS
|
Удлинение АЧТВ Тест смешивания по АЧТВ — нет коррекции (ИЦА > 15 %) ВА «положительный»: может искажать результат определения активности FVIII в клоттинговых тестах Prolongation of aPTT APTT mixing test — no correction (ICA > 15 %) LA “positive”: distorts the result of determining the activity of FVIII in clotting tests
|
АЧТВ-реагент, чувствительный к эффекту ВА Тесты с разбавленным ядом гадюки Рассела (dRVVT Screen / dRVVT Confirm) и кварцевым активатором (SCT Screen / SCT Confirm) Антифосфолипидные антитела к кардиолипину IgM / IgG и бета-2- гликопротеину I IgM / IgG aPPT-reagent sensitive to the effect of LA The dilute Russell viper venom tests (dRVVT Screen / dRVVT Confirm) and quartz activator tests (SCT Screen / SCT Confirm) Antiphospholipid antibodies to anti-cardiolipin antibodies IgM / IgG and anti-β2 - glycoprotein I IgM / IgG
|
|
Дефицит факторов внутреннего пути: Дефицит FIX Дефицит FXI Дефицит FXII Deficiency of intrinsic pathway factors: FIX deficiency FXI deficiency FXII deficiency
|
Изолированное удлинение АЧТВ Снижение активности FIX Снижение активности FXI Снижение активности FXII Isolated aPTT prolongation Reduced FIX activity Reduced FXI activity Reduced FXII activity
|
Отмечается снижение активности FIX, FXI и FXII in vitro (при высоком титре ингибитора FVIII) Reduced FIX, FXI, FXII activity in vitro (with a high duration of action of the FVIII inhibitor)
|
|
Непрямые антикоагулянты (антагонисты витамина К) Indirect anticoagulant (vitamin K antagonists)
|
Влияние на ПВ (МНО) выражено сильнее, чем на АЧТВ (отмечается при передозировке препарата) Effect on PT (INR) often stronger than on aPTT (in case of drug overdose)
|
Определение ПВ (МНО) Определение активности витамин К-зависимых факторов (FII, FVII, FIX и FX) Determination of PT (INR) Determination of the activity of Vitamin K dependent factors (FII, FVII, FIX и FX)
|
|
Нефракционированный гепарин Unfractionated heparin
|
Удлинение АЧТВ Действует как «быстродействующий» ингибитор в тестах смешивания по АЧТВ — нет коррекции (ИЦА > 15 %) Prolongation of aPTT Acts as «fast acting» inhibitor in APTT mixing test — no correction (ICA > 15 %)
|
Определение тромбинового времени Определение анти-FХа активности для подтверждения или исключения действия антикоагулянтов Determination of thrombin time Anti-FXa assay to confirm or exclude anticoagulant drug action
|
|
Низкомолекулярный гепарин Low molecular weight heparin
|
Удлинение АЧТВ (отмечается при передозировке препарата) Prolongation of aPTT
|
Определение анти-FХа активности для подтверждения или исключения действия антикоагулянтов Отменить препарат и повторить исследование Anti-FXa assay to confirm or exclude anticoagulant drug action Withdraw drug and repeat testing
|
|
Прямые ингибиторы FХа Direct FXa inhibitors
|
Удлинение АЧТВ Prolongation of aPTT
|
Определение анти-FХа активности для подтверждения или исключения действия антикоагулянтов Влияние на ПВ выражено сильнее, чем на АЧТВ Отменить препарат и повторить исследование Anti-FXa assay to confirm or exclude anticoagulant drug action Effect on PT often stronger than on aPTT Withdraw drug and repeat testing
|
|
Прямые ингибиторы тромбина Direct thrombin inhibitors
|
Удлинение АЧТВ Prolongation of aPTT (in case of drug overdose)
|
Влияние на АЧТВ выражено сильнее, чем на ПВ Определение тромбинового времени Отменить препарат и повторить исследование Effect on aPTT often stronger than on prothrombin time Determination of thrombin time Withdraw drug and repeat testing
|
Примечание: МНО — международное нормализованное отношение, vWF:Ag — антиген фактора фон Виллебранда, vWF:Rco — ристоцетин-кофакторная активность фактора фон Виллебранда, RIPA — ристоцетин-индуцированная агрегация тромбоцитов, vWF:FVIIIB — фактор VIII-связывающая активность фактора фон Виллебранда, vWF:CB — коллагенсвязывающая активность фактора фон Виллебранда, dRVVT Screen/dRVVT Confirm — время свертывания с разбавленным ядом гадюки Рассела Скрининг/Подтверждение, SCT Screen/SCT Confirm — время свертывания с кварцевым активатором Скрининг/Подтверждение, ВА — волчаночный антикоагулянт.
Приложение 4
Образец протокола проведения заместительной /гемостатической терапии факторами свертывания крови в домашних условиях
Приложение 4
Образец протокола проведения заместительной /гемостатической терапии факторами свертывания крови в домашних условиях
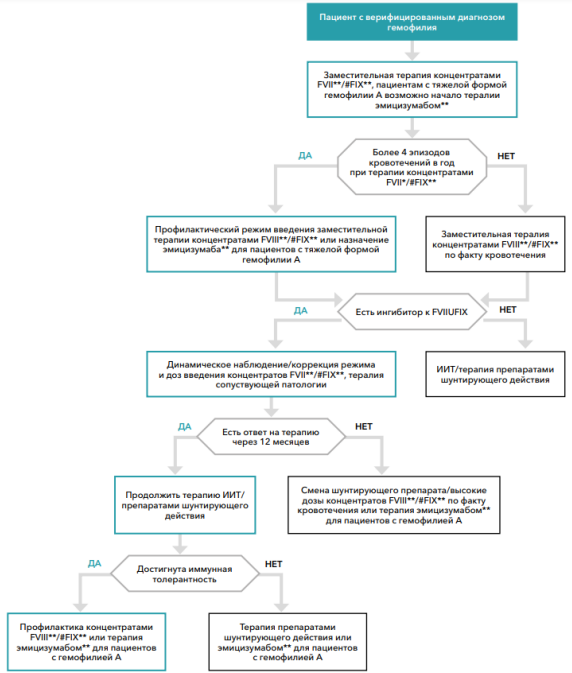
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.