Врожденная глаукома
 Версия: Клинические рекомендации РФ 2024 (Россия)
Версия: Клинические рекомендации РФ 2024 (Россия)
Врожденная глаукома (Q15.0)
Врожденные заболевания, Офтальмология детская, Педиатрия
Общая информация
Краткое описание
Разработчик клинической рекомендации
- Общероссийская общественная организация "Ассоциация врачей-офтальмологов"
- Общероссийская общественная организация «Общество офтальмологов России»
Одобрено Научно-практическим Советом Минздрава РФ
В соответствии с Правилами поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 –9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», утвержденных постановлением Правительства Российской Федерации от 19.11.2021 № 1968 с изменения, клинические рекомендации применяются следующим образом:
– размещенные в Рубрикаторе после 1 января 2024 года – с 1 января 2025 года.
Клинические рекомендации
Врожденная глаукома
Год утверждения (частота пересмотра): 2024
Возрастная категория: Дети
Пересмотр не позднее: 2026
ID: 112
Определение заболевания или состояния (группы заболеваний или состояний)
Врожденная глаукома (ВГ) – это группа гетерогенных заболеваний, характеризующихся повышением ВГД выше толерантного в первые месяцы/годы жизни, обусловленным нарушением эмбриогенеза (аномалии УПК и дренажной системы), с помутнением роговицы, деформацией и увеличением глаза в первые годы жизни, оптической нейропатией, с последующей атрофией зрительного нерва и снижением электрогенеза сетчатки (при прогрессирующем течении) [1-5].
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
Q 15.0. - Врожденная глаукома
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Классификации ВГ достаточно многочисленны, основаны на этиопатогенетических особенностях, тяжести клинических проявлениях, сроках манифестации глаукомного процесса. Для современной унификации номенклатуры и систематизации подхода, целесообразно использовать международную классификацию детских глауком, согласованную в 2013г Всемирной ассоциацией глаукоматологов [16,19], по которой первичную детскую глаукому подразделяют на первичную ВГ (с врожденными аномалиями структур угла передней камеры) и ювенильную открытоугольную (манифестирующую в возрасте от 3 до 35 лет). Первичную ВГ по срокам манифестации заболевания чаще делят на неонатальную (глаукома новорожденных) – с рождения до 1 месяца жизни, инфантильную – от 1 месяца до 2 лет и отсрочено манифестирующую глаукому – старше 2 лет. Вторичную детскую глаукому делят на 4 группы глауком: ассоциированную с врожденными аномалиями развития глазного яблока (такими как аномалия Аксенфельда-Ригера, Петерса, аниридия, эктопия хрусталика, ППГСТ и др.); вторичную глаукому с врожденными системными заболеваниями или синдромами (синдромами Реклингаузена, Марфана, Вейля-Марчезани, Стиклера, Лоу, гомоцистинурией, мукополисахаридозом, ювенильной ксантогранулемой и др.) и вторичную глаукому, ассоциированную с врожденными инфекциями, интоксикациями (врожденная краснуха, герпетическое поражение) и приобретенными состояниями (последствиями травм, увеитов, ретинопатии недоношенных, удаления катаракт-отдельно, опухолью).
Известны и отечественные классификации рассматриваемого заболевания, в т.ч. по Т.И. Ерошевского и Б.А. Токаревой (1971), Е.И. Ковалевского (1969; 1986), Э.С. Аветисова с соавторами (1987), Э.Г. Сидорова и М.Г. Мирзоянц (1991), Сидоренко Е.И. (2000),Е.Е.Сомова (1992, 2016) и других. Наибольшее распространение в нашей стране получила клиническая классификация, предложенная Э.С. Аветисовым, Е.И. Ковалевским, А.В. Хватовой в 1987 году [1], по которой основным критерием прогрессирования глаукомного процесса служит стадия заболевания, которая, в отличие от глауком у взрослых пациентов, определяется не по данным периметрии, а по увеличению диаметра роговицы и длины ПЗО глаз детей, учитывая, что у большинства детей ВГ протекает с увеличением этих параметров – «растяжением» роговицы и глазного яблока, особенно в первые 3 года жизни (Табл.2)
Таблица 2.
Классификация врожденной глаукомы (Аветисов Э.С., Ковалевский Е.И., Хватова А.В., 1987)
| Происхождение | Форма | Характер изменений УПК | Стадия | Компенсация | Динамика |
|---|---|---|---|---|---|
|
Наследственная
Внутриутробная
|
Простая (собственно гидрофтальм) - с изменениями в УПК
С аномалиями глазного яблока (аниридия, эктопия хрусталика, микрофтальм и другие)
С факоматозами (нейрофиброматоз, ангиоматоз и другие)
|
Наличие мезодермальной ткани
Переднее прикрепление радужки
Отсутствие дифференцировки зон УПК
|
1. Начальная– диаметр роговицы и длина сагиттальной оси глаза превышает возрастную норму не более, чем на 2 мм. Зрение почти не изменено
2. Развитая - диаметр роговицы превышает возрастную норму на 3 мм, длина сагиттальной оси глаза - на 3-4 мм, зрение значительно снижено
Далеко зашедшая-диаметр роговицы превышает возрастную норму на 4 мм и более, длина сагиттальной оси глаза - на 5 мм и более, зрение резко снижено
3. Почти абсолютная- зрение равно неправильной светопроекции
Абсолютная – резкий буфтальм, слепота
|
Компенсированная-ВГД* не превышает 26ммртст в начальной стадии и 24мм.рт.ст. в более поздних стадиях; суточные колебания ВГД в пределах 5 мм рт ст Некомпенсированная- ВГД выше 26мм рт ст в начальной стадии и выше 24 мм рт ст в более поздних стадиях; суточные колебания ВГД более 5мм рт ст
Декомпенсированная глаукома-острый приступ
|
Стабильная- глазное яблоко не увеличивается, зрение не снижается
Прогрессирующая – глазное яблоко увеличивается, зрение снижается
|
*- имеется в виду тонометрическое ВГД (Pt)
Сомов Е.Е. (1992) [17-18] предложил для оценки тяжести процесса, помимо учета диаметра роговицы добавить величину экскавации диска зрительного нерва (ДЗН) и состояние зрительных функций, поэтому остается весьма востребованной Объединенная клинико-патогенетическая классификация врожденной глаукомы по стадиям (Табл. 3) [20], хотя на практике нередко затруднительно отнесение ВГ к той или иной стадии в связи с несоответствием различных показателей и трудностями оценки зрительных функций.
Таблица 3.
Объединенная клинико-патогенетическая классификация врожденной глаукомы по стадиям (Катаргина Л.А. и др., 2016)
Объединенная клинико-патогенетическая классификация врожденной глаукомы по стадиям (Катаргина Л.А. и др., 2016)
| Стадия врожденной глаукомы | Оценочные критерии | ||
|---|---|---|---|
| Диаметр роговицы, мм | Экскавация диска зрительного нерва (ДЗН) | Состояние зрительных функций* | |
| I- начальная | До 12 | До 0,3 | Не нарушены |
| II- развитая | До 14 | До 0,5 | Существенно снижены |
| III- далекозашедшая | Более 14 | Более 0,5 | Снижены до светоощущения |
| IV- почти абсолютная | Буфтальм | - | Остаточные или слепота |
| V- абсолютная | Буфтальм | - | Слепота |
* При неосуществимости периметрии.
В настоящее время, в связи с развитием современных высокоинформативных методов визуализации и появлением новых данных, происходит усовершенствование подходов и критериев диагностики.
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Большинство авторов склоняются к мнению о многофакторной природе ВГ. ВГ может возникнуть, как следствие наследственных аномалий органа зрения, так и в результате воздействия в период с 7 по 36 неделю гестации на зародыш или плод различных внутриутробных патологических агентов.
Первичная ВГ в 15-40% случаев является наследственной, с аутосомно-рецессивным наследованием [Cyp1B1 (2p21), GLC3B (1p36) и GLC3C (14q24.3)] или аутосомно-доминантным типом наследования [GLC1ATIGR, MIOC)], с вариабельной пенетрантностью от 40 до 100%. Обнаружены многочисленные мутации гена Cyp1B1, включая миссенс-мутации, нонсенс-мутации, мутации сдвига рамки считывания, делецию и вставку со значительной гетерогенностью. Генетическая оценка детской глаукомы особенно важна в тех видах глаукомы, когда имеются генотипические и фенотипические корреляции (Табл.1) [4,7,10,11].
В большинстве случаев в этиологии ВГ играет роль многофакторное наследование с участием негенетических факторов – перенесенные во время беременности инфекционные болезни матери (грипп, паротит, полиомиелит, токсоплазмоз), вирусные заболевания (краснуха, цитомегаловирус), эндокринные и метаболические нарушения, интоксикации, прием лекарственных препаратов, алиментарные факторы (гипо и авитаминозы), факторы окружающей среды (физические, химические).
Таблица 1.
Синдромы, сочетанные с глаукомой и ассоциированные гены
| Синдром | Клинические проявления | Ген |
|---|---|---|
| Nail-patella syndrome | Дисплазия ногтей, отсутствие или гипоплазия коленной чашечки, аномалия почек, глаукома (9,6%). Зона темной пигментации в виде клевера вокруг центра радужки | LMX1B. 60 |
| Oculodentodigital dysplasia (AD) | Типичный внешний вид, поражения зубов, кистей рук, глаз (микрофтальм, микрокорнеа, глаукома) | Connexin-43 gene (GJAI) |
| Freak-ter Haar Syndrome (AR) | Брахицефалия, гипертелоризм, макрокорнеа, глаукома, проминирующий лоб, широкий родничок | TKS4 gene (SH3PXD2B) |
| Rubinstein-Taybi Syndrome | Умственная отсталость, постнатальная задержка развития, микроцефалия, дисморфия лицевого черепа, широкие пальцы, глаукома, катаракта, аномалии рефракции, косоглазие | CREBBP |
| Ehlers-Danlos type VI | Врожденная тяжелая мышечная гипотония, хрупкость и разрывы склеры, глаукома, сколиоз | PLODI |
| Neurofibromatosis type I (AD) | Развитие опухолей нервных оболочек, узелки Лиша, плексиформные нейрофибромы век, глаукома, глиома зрительного нерва, дисплазия клиновидной кости | Neurofibromin gene (NFI) |
| Peters Plus syndrome (AR) | Задержка психического развития, невысокий рост, брахиморфизм, аномалия ушей, аномалия Петерса | B3GALTL |
| Zellweger( Peroxisome biogenesis disorder (AR) | Тяжелые неврологические нарушения, краниофасциальные аномалии, нарушения функций печени, отсутствие пероксисомных ферментов (биохимические исследования), глаукома, катаракта, помутнение роговицы, нистагм, пигментный ретинит | PEXI |
| Marfan syndrome (AD) | Высокий рост, длинные конечности, деформация грудной клетки, дилатация аорты, эктопия хрусталика, глаукома | Fibrillin -1 gene (FBNI) |
| Klippel-Trenaunay-Weber Syndrome | Большие гемангиомы кожных покровов с гипертрофией прилежащих мягких тканей и костей. Клинически напоминает синдром Стерджа –Вебера | Ген в поиске |
| Charcot -Marie-Tooth disease type 4B2( CMT4B2) (AR) | Наследственная демиелинизирующая нейропатия (двигательная и чувствительная) | SBF2 |
| MIDAS (microphthalmia, dermal aplasia and sclerocornea) syndrome (XL-Dominant) | Односторонний или двусторонний микрофтальм, линейные дефекты кожи на лице и шее | HCCS |
| Renal Tubular Acidosis, Proximal, with Ocular Abnormalities and Mental Retardation (AR) | Ацидоз проксимальных почечных, задержка психического и физического развития, нистагм, катаракта, помутнение роговицы, глаукома | SLC4A4 |
Этиологическая диагностика ВГ базируется на тщательном сборе анамнеза (состояние и заболевания беременной женщины), на результатах иммунологических, вирусологических и генетических исследований.
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Врожденные заболевания глаз в настоящее время являются главной причиной слепоты и слабовидения у детей [3-6,12-18]. ВГ встречается относительно редко – 1 случай на 10-70 тысяч новорожденных, но удельный вес ВГ среди причин слепоты – до 11%. У 60 % детей ВГ проявляется в первые 6 месяцев, у 80 % – на первом году жизни. У 75% детей заболевание двустороннее. Чаще болеют мальчики. Успех лечения детей с ВГ в значительной степени зависит от ранней диагностики заболевания. При несвоевременно начатом лечении болезнь быстро прогрессирует и приводит к необратимым изменениям всех структур глазного яблока. Сложность диагностики таких заболеваний определяется клиническим разнообразием и возрастными особенностями поведения ребенка.
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Клинические формы врожденной глаукомы
ВГ рассматривают как группу заболеваний, каждое из которых характеризуется своеобразием клинического и патогистологического проявления [1-6,17-20].
Различают 3 формы врожденной глаукомы:
I форма - простая ВГ (собственно гидрофтальм),
II форма - глаукома, сочетанная с аномалиями развития переднего отрезка глаза (микрофтальм, микрокорнеа, аномалия/синдром Ригера, Аксенфельда, аномалии Петерса, склерокорнеа, аниридия, эссенциальная мезодермальная дистрофия радужки, колобома радужки, синдром Франка-Каменецкого, синдром Марфана, синдром Марчезани);
III форма - глаукома, сочетанная с факоматозами, ангиоматозами (синдром Стерджа-Вебера-Краббе и болезнь Реклингаузена).
Основными клиническими признаками ВГ (классическое течение гидрофтальма) являются:
- повышение уровня ВГД выше толерантного;
- увеличение сагиттальной оси глазного яблока по сравнению с возрастными нормами;
- увеличение диаметра роговицы и лимба;
- образование отека и помутнения роговицы различной степени, разрывов и трещин десцеметовой мембраны, дефектов эндотелия;
- углубление передней камеры (>3-3.5 мм);
- развитие субатрофии и атрофии радужной оболочки, иридодонез;
- развитие глаукомной атрофии зрительного нерва (с экскавацией),
- образование истончений склеры, выпячивающихся в виде стафилом;
Важным диагностическим признаком также является асимметрия выраженности перечисленных признаков (длины сагиттального размера, диаметра роговицы, усиления рефракции, экскавации ДЗН).
Жалобы связаны с особенностями клинической картины (у маленьких детей – со слов родителей):
- светобоязнь, слезотечение, блефароспазм (роговичный синдром);
- увеличение глаза и роговицы в размере;
- периодические затуманивания роговицы (явления отека), а затем –стойкое помутнение роговицы;
- снижение зрения (возможно обнаружить у детей старшего возраста)
- при болях в глазу меняется поведение ребенка (плохо спит, капризен, беспокоен, теряет аппетит).
Существуют различия в сроках появления клинических признаков при различных формах глаукомы. При I форме манифестация заболевания происходит в раннем возрасте до 1 года (80% случаев), при II и III формах - в более поздние сроки. Определение стадии заболевания осуществляется по «худшему» клиническому признаку на момент обследования ребенка (Таб. 3), хотя не всегда все клинико-морфологические признаки заболевания точно коррелируют со стадией его. Оптическая когерентная томография (ОКТ) сетчатки и зрительного нерва (истончение перипапиллярного слоя нервных волокон сетчатки, уменьшение ширины нейроретинального пояска, толщины слоя ганглиозных клеток в макуле) достоверно оценивают наличие и степень тяжести прогрессирования глаукомы.
Сопутствующая врожденной глаукоме патология глаз
ВГ может быть одним из проявлений целого ряда синдромов и системных заболеваний (II и III формы) [1-6,11,17,20,21-23,24]. При II и III формах врожденной глаукомы, как правило, офтальмотонус повышается в более старшем возрасте (на втором десятилетии жизни). В связи с повышением к этому возрасту прочностных характеристик оболочек глаза, клиническая картина при этих формах глаукомы отличается от классического гидрофтальма (растяжение глазного яблока, роговичный синдром), что зачастую является причиной поздней диагностики заболевания.
При этом также характерно развитие глаукоматозных изменений зрительного нерва с характерным снижением зрительных функций. В то же время отсутствие жалоб у ребенка на снижение зрения не всегда способствует своевременной диагностике и лечению.
Далее представлены наиболее часто встречаемые клиницистами аномалии развития и синдромы.
Врожденная аниридия – это редкая генетически опосредованная панокулярная патология. Наиболее ярким симптомом заболевания является врожденное отсутствие радужки или ее гипоплазия. К другим часто встречающимся проявлениям относятся кератопатия, обусловленная врожденным дефицитом стволовых клеток лимба, катаракта, глаукома, гипоплазия центральной ямки сетчатки, зрительного нерва, нистагм. В 75% случаев наблюдают доминантный тип наследования с высокой пенетрантностью.
Мутации Гена PAX6 в коротком плече 11-й хромосомы (локус В 11p13) ответственны за «классическую» врожденную аниридию (несиндромальную изолированную с доминантным наследованием) и семейную аниридию. PAX6-ассоциированную аниридию называют «аниридийный синдром» или PAX6-синдром. Повышение ВГД отмечается у 50-70% детей. Кроме того, аниридия может сопровождаться патологией других органов и систем, таких как нервная система, мочеполовая, эндокринная системы, пищеварительная) и проявляться как часть синдромов. Врожденная аниридия может быть несиндромальной (75 % случаев) и синдромальной (20 %), включая WAGR синдром (<10 %), в который, помимо аниридии, входит опухоль Вильмса, которая развивается в возрасте от 1 года до 5 лет, пороки развития мочеполовой системы, задержку психического развития и умственную отсталость. Синдром Гиллеспи (Gillespie) – генетическое заболевание, характеризующееся анаридией, мозжечковой атаксией, умственной недостаточностью, можно заподозрить у ребенка первого года жизни по сочетанию аниридии с выраженной мышечной гипотонией. Учитывая риск развития жизнеугрожающих состояний (опухоль почек), всем пациентам с аниридией рекомендовано генетическое обследование для исключения WAGR синдрома.
Врожденная глаукома может развиваться при сочетании гониодисгенеза с микрофтальмом, микрокорнеа, микросферофакии.
Аномалии Аксенфельда-Ригера, синдром Аксенфельда-Ригера (Синдром Ригера) относятся к наследственной двусторонней патологии органа зрения с аутосомно-доминантным типом передачи. Патология нервной и костной систем, двустороннее поражение глаз при этом встречаются в 50% случаев. Нередки семейные случаи.
Различают 3 степени периферического гониодисгенеза:
1 степень – «задний эмбриотоксон» – хорошо заметное проминирование и смещение кпереди переднего пограничного кольца Швальбе (на периферии роговицы видна четкая белесая линия по всей окружности или части роговицы).
2 степень – «аномалия Аксенфельда» – задний эмбриотоксон сращен с отростками или тяжами мезодермального листка радужки, которые тянутся от цилиарной, а иногда и от зрачковой зоны к кольцу Швальбе.
3 степень – аномалия Аксенфельда- Ригера, при которой симптомокомплекс аномалии Аксенфельда сочетается с гипоплазией стромы и даже пигмента радужки, вплоть до сквозных отверстий в радужке. Имеются деформации, эктопии зрачка, выворот пигментного листка, возможны изменения со стороны роговицы (мегало- или микрокорнеа) и хориоидеи, катаракта, косоглазие.
При сочетании глазных проявлений аномалии Аксенфельда - Ригера с различными системными изменениями (гипоплазия срединной линии лица, телекантус с широким, плоским корнем носа, уменьшение количества и размеров зубов, пупочная грыжа, врожденные пороки сердца, кондуктивная тугоухость, задержка умственного развития, гипоплазия мозжечка), симптомокомплекс верифицируют как «синдром Ригера». Примерно у 60% пациентов с данным синдромом возникает глаукома.
Аномалия Петерса – редкое генетическое заболевание с аутосомно-доминантным или рецессивным типом передачи, но чаще встречаются спорадические случаи. Мутации обнаружены в генах PAX6, REIG1, PITX2, FOXE3. Аномалия представляет собой центральный дисгенез роговицы – центральное помутнение роговицы с дефектом десцеметовой оболочки, сращенным с радужкой (часто – с ее зрачковым краем, с вовлечением стромы десцеметовой оболочки и эндотелия (1 тип) и нередким сращением с хрусталиком и помутнением его (2 тип). В 80% случаев поражение глаз двустороннее. Аномалия Петерса часто сочетается с микрофтальмом, уплощением роговицы, склерокорнеа, коректопией, гипоплазией радужки и полярной катарактой. В 30-70% случаев развивается ВГ на почве аномального строения УПК. Чаще сопровождается подъемом ВГД после 6-7 лет (есть случаи ранней манифестации глаукомы). Синдром «Петерс-плюс» (3 тип) – сочетание глазных проявлений синдрома Петерса с пороком сердца, патологией ЦНС, мочеполовой системы, укорочением туловища, конечностей, задержкой психомоторного развития и др.
Врожденный увеальный эктропион является редкой непрогрессирующей аномалией, характеризующейся наличием листка пигментного эпителия радужки на передней ее поверхности, передним прикреплением радужки, дисгенезом дренажной зоны УПК. Процесс характеризуется односторонностью и редко передается по наследству.
Синдром Франка – Каменецкого – наследственная аутосомно-рецессивная патология (по сцепленному с Х-хромосомой типу), характеризуется двусторонней гипоплазией или аплазией радужки и возникновением глаукомы. Отличительной чертой является двухцветность радужки: ее зрачковая зона – светлая, а цилиарная зона – темная, на почве более выраженной атрофии стромы, вследствие обнажения пигментного листка чаще всего имеет шоколадно-коричневый цвет. Одновременно могут наблюдаться аномалии зрачка (смещение, неправильная форма, отсутствие или гипертрофия зрачковой каймы), сквозные дефекты радужки, иридодиастаз, иридодиализ. У всех пациентов имеется гониодисгенез.
Несмотря на врожденную аномалию УПК, тенденция к увеличению ВГД чаще отмечается на 2-3-м десятилетии жизни. В ранние сроки ВГД повышается обычно у мальчиков при сочетании выраженного гониодисгенеза с мегалокорнеа. При этом процесс разрушения радужки продолжается и в послеоперационном периоде, при стабилизации ВГД и зрительных функций.
Синдром Марфана – эктопия хрусталика (кверху кнаружи), высокий рост, гиперлабильность суставов, брахидактилия, сколиоз, грубые врожденные пороки, коарктация аорты. Дислокация хрусталика, а также наличие гониодисгенеза могут быть у таких причиной нарушений гидродинамики глаза и манифестации глаукоматозного процесса.
Синдром Марчезани – микросферофакия, люксация хрусталика кпереди, сфинктер радужки проминирует в переднюю камеру, низкий рост, тугоподвижность суставов, не тяжелые пороки сердца. Глаукома развивается не часто. В ряде случаев повышение ВГД бывает связано с дисгенезом УПК, у некоторых пациентов – с блоком зрачка сферическим хрусталиком.
Гомоцистинурия. Внешние общие проявления болезни такие же, как при синдроме Марфана. В отличие от последнего гомоцистинурия передается по аутосомно-рецессивному типу и часто сопровождается задержкой умственного развития. Нарушение гомоцистеинового метаболизма является следствием энзимного дефекта. Дислокация хрусталика и глаукома наблюдаются чаше, чем при синдроме Марфана. Заболевание может осложняться отслойкой сетчатки.
Среди факоматозов и ангиоматозов, при которых наблюдается глаукома, чаще встречаются синдром Стерджа-Вебера-Краббе и болезнь Реклингаузена.
Синдром Стерджа - Вебера - Краббе (энцефалотригеминальный ангиоматоз, энцефалофациальный ангиоматоз) – врожденный ангиоматоз нервной системы, проявляющийся наличием сосудистого пятна на лице, судорог и внутричерепных кальцификатов. Частота болезни – 1 случай на 100 000 населения. Встречается в основном спорадически. На коже лица наблюдаются множественные ангиомы (ангиоматоз), обычно по ходу тройничного или лицевого нерва. Иногда расширенные сосуды принимают вид сосудисто-кавернозной опухоли красно-синего цвета. В головном мозге ангиоматоз затрагивает мягкую мозговую оболочку на той же стороне, преимущественно в затылочной и затылочно-теменной области, обычно, с одной стороны. С рождения у больных имеется одно большое или несколько сливающихся пятен сине-красного цвета на лице ("пламенеющие невусы"). Они могут быть также на туловище и конечностях. Ангиоматозные изменения иногда распространяются на ротовую полость, нос, глотку. У некоторых больных в связи с этим возникают кишечные кровотечения. В первые месяцы жизни у больных обнаруживаются судорожные припадки. Они чаще всего фокальные, как правило, на стороне, противоположной поражению сосудов. У больных нередко развиваются параличи, парезы, обычно по гемитипу. Примерно у половины больных наблюдается умственная отсталость (обычно глубокая). Изменения органа зрения характеризуются ангиомой сосудистой оболочки, колобомами, гетерохромией радужки. Иногда выявляются врожденные пороки сердца, дисплазия черепа и лица. На МРТ у детей обнаруживают атрофию гемисферы с расширением субарахноидальных пространств и боковых желудочков, при компьютерной томографии – кальцификаты по типу «железнодорожных путей». Все изменения часто выявляются после 4 – 5 лет. Частота случаев глаукомы при этом синдроме достигает 60%. Поскольку описаны случаи двустороннего глаукомного процесса у больных с синдромом Стерджа-Вебера с односторонней капиллярной гемангиомой лица, рекомендовано динамическое наблюдение обоих глаз таких детей.
Болезнь Реклингаузена - нейрофиброматоз относят к факоматозам. Он представляет собой нейроэктодермальную дисплазию, характеризующуюся пролиферацией периферических нервных элементов с образованием опухолеподобных структур. Заболевание передается по аутосомно-доминантному типу. Основные поражения локализуются в коже, периферической и центральной нервной системах. В глазной практике приходится иметь дело с поражением век, конъюнктивы, орбиты, роговицы, сосудистой оболочки, сетчатки, зрительного нерва. Особенно часто поражается верхнее веко, где образуется плексиформная фиброма, нередко распространяющаяся и на височную область. В процесс обычно вовлекается одна сторона, реже бывают двусторонние изменения. Нейрофиброматозные узелки или диффузная инфильтрация может возникать на конъюнктиве, эписклере, роговице и радужке. Иногда отмечается значительное утолщение хориоидеи и цилиарного тела за счет пролиферации ткани, В зрительном нерве описаны менингиомы, глиомы, в орбите – нейрофибромы. Глаукома развивается редко, часто сочетается с поражением верхнего века и обычно (но не всегда) бывает односторонней. Причиной повышения давления служат гониодисгенез, аномалии развития склерального синуса или претрабекулярная блокада нейрофиброматозной тканью. В некоторых случаях развивается закрытоугольная глаукома, вызванная смещением кпереди иридохрусталиковой диафрагмы из-за утолщения хориоидеи и цилиарного тела.
Врожденная глаукома выявляется также при более редких синдромах:
- Ротмунда-Томпсона, характеризующегося инфантильной пойкилодермией, гипогонадизмом, поражением скелета; при синдроме Ларсена в сочетании с множественным поражением суставов и низким ростом;
- Стиклера, проявившимся прогрессирующей артропатией, дефектами развития лицевого черепа и неба, нейросенсорной тугоухостью, прогрессирующей миопией, витреоретинальной дегенерацией, отслойкой сетчатки;
- Рубинштейн-Тауби, проявлениями которого являются эпикантус, патология слезоотводящих путей, птоз, страбизм, макрокорнеа, микрофтальм, колобомы радужки и ДЗН, катаракта;
- Пьера-Робена, характеризующегося микрогнатией (недоразвитие и смещение нижней челюсти кзади), расщелиной верхнего неба и глоссоптозом. Отмечается полиморфная патология органа зрения в виде ВГ, буфтальма, мегалокорнеа, микрофтальма, врожденной катаракты, высокой миопии, отслойки сетчатки.
При позднем установлении диагноза ВГ у детей с перечисленными синдромами отмечается высокий риск утраты зрительных функций.
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Диагноз ВГ выставляют на основании анамнестических данных и результатов клинического обследования, которое включает набор стандартных и высокоинформативных дополнительных методов исследования (таблица 4).
Таблица 4.
Методы обследования
| Стандартные диагностические методики | Расширенный спектр диагностических методик (дополнительно к стандартному набору) |
|---|---|
| Наружный осмотр | Кератопахиметрия |
| Визометрия, рефрактометрия, | Тонография |
| Офтальмотонометрия | Оптическое лазерное когерентное послойное исследование переднего и заднего отдела глаза с помощью компьютерного анализатора (оптическая когерентная томография переднего и заднего отделов-ОКТ) |
| Биомикроскопия глаза | Ультразвуковая биомикроскопия |
| Гониоскопия | Периметрия |
| Офтальмоскопия | Электрофизиологические методы исследования (регистрация зрительных вызванных потенциалов коры головного мозга, электроретинография) |
| Измерение диаметра роговицы, лимба (кератометрия, лимбометрия) | Фоторегистрация УПК гониоскопии с использованием ретинальной камеры |
| Ультразвуковое исследование глазного яблока (ультразвуковая биометрия и В-сканирование) | Фоторегистрация глазного дна с использованием фундус –камеры |
У детей с манифестацией глаукомы в раннем возрасте с развитием клинической картины классического гидрофтальма, диагностика глаукомы не представляет особых сложностей. При более поздней манифестации она может представлять трудности из-за отсутствия или слабой выраженности характерной симптоматики, а также растянутого во времени развития патологического процесса.
Ранняя диагностика направлена на выявление признаков растяжения глаза, вызванного подъемом ВГД, начальных проявлений атрофических процессов в диске зрительного нерва, слое нервных волокон сетчатки. Постановка раннего диагноза ВГ должна базироваться на комплексном анализе данных с учетом асимметричного характера клинических и морфофункциональных характеристик парных глаз.
1. Жалобы и анамнез
- Сбор анамнеза и жалоб рекомендуется у всех пациентов с врожденной глаукомой и подозрением на данное заболевание [1-6,17-18,20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Все дети должны быть обследованы педиатром, при необходимости невропатологом, кардиологом, генетиком и другими специалистами на предмет наличия соматической патологии. Выяснение сведений о раннем постнатальном периоде - частоте и тяжести перенесенных инфекционных заболеваний, хронической патологии, аллергических реакций. Выявление наличия возможных причин и предрасполагающих факторов возникновения заболевания (внутриутробные инфекции, алиментарные факторы и другие) путем ознакомления с состоянием здоровья матерей, сведений акушерско-гинекологического анамнеза.
Важным аспектом расспроса родителей является целенаправленный анализ времени появления признаков глаукомы, их взаимозависимости, а также выраженности на парных глазах.
2. Физикальное обследование
- Физикальное обследование неинформативно. Необходимо соблюдать общие пропедевтические принципы обследования пациентов. Рекомендуется направлять детей с ВГ с сопутствующими системными заболеваниями и факторами риска системных осложнений на профилактический прием (осмотр, консультация) врача-педиатра перед выполнением оперативного лечения с целью выявления возможных противопоказаний к данному виду лечения или минимизирования риска осложнений [1-6,17-18,20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
3. Лабораторные диагностические исследования
Лабораторная диагностика глаукомы в клинической практике пока малоприменима – продолжаются научные исследования.
4. Инструментальные диагностические исследования
- Визометрия A02.26.004 и рефрактометрия A03.26.008 рекомендуются всем пациентам с врожденной глаукомой и подозрением на данное заболевание при диагностике, динамическом наблюдении и контроле за лечением с целью определения тяжести зрительных расстройств [1-6,17-18,20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Визометрия проводится детям до 3 лет методом ориентировочной реакции на новизну, исследованием рефлекторных двигательных реакций (зрачковых, реакции слежения, др.), ориентировочными методами путем предъявления предметов разного размера (тест с шарами и др.; детям 3 – 6 лет – по картинкам, буквам, цифрам или другим знакам (таблицы Орловой, Сивцева и Головина, кольцам Ландольта, картинки проектора знаков и др.),. При отсутствии предметного зрения определяется наличие светоощущения и проекции света. Определение остроты зрения проводится сначала без коррекции, затем, если есть нарушения, с коррекцией (с использованием специальной оправы и линз).
Как известно, у детей с ВГ, по мере растяжения глаза, формируется миопическая рефракция, у трети – миопия высокой степени. При дальнейшем прогрессировании глаукомы и значительном и, зачастую, неравномерном растяжении оболочек глаза, увеличивается степень астигматизма, в значительной степени снижающего остроту зрения, и так достаточно низкую, у таких детей.
Соответственно, исследование клинической рефракции у детей с ВГ или подозрением на это заболевание преследует две цели: диагностики глаукомного процесса и оценки темпов его прогрессирования – с одной стороны и своевременной оптической коррекции аметропии – с другой.
Для определения рефракции возможно проведение скиаскопии или авторефрактометрии на стационарном или портативном рефрактометре. Неоспоримыми преимуществами портативных служат возможность проведения исследования в любых условиях, в том числе в наркозе, а также возможность точного определения меридиана астигматизма.
- Офтальмотонометрия A02.26.015 рекомендуется всем пациентам с врожденной глаукомой и подозрением на данное заболевание для исследования уровня ВГД и гидродинамики глаза [1-6,17-18,20,25-27].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: Для контроля ВГД рекомендовано использовать аппланационный тонометр Маклакова (стандарт тонометрии в РФ), аппланационный тонометр Гольдмана (стандарт тонометрии в мире) или различные типы бесконтактных тонометров, позволяющий измерять истинное ВГД без местной анестезии, в том числе у детей раннего возраста в различных положениях тела ребенка. Бесконтактную тонометрию (пневмотонометрию) следует рассматривать как скрининговый метод определения уровня ВГД. В РФ зарегистрированы тонометры ICare, PASCAL и анализатор биомеханических свойств глаза Ocular Response Analyzer - ORA. [25-27]. При динамическом наблюдении рекомендуется использовать один базовый метод тонометрии для корректного сравнения полученных результатов.
Многим современным методикам «приборной» тонометрии свойственны ошибки результатов измерения, обычно в сторону завышения показателей офтальмотонуса. Они во многом связаны с возрастной спецификой механических свойств роговицы, еще более изменяющихся на фоне развития гидрофтальма. Поэтому при получении противоречивых показателей ВГД или сомнении в их достоверности целесообразно прибегнуть к офтальмотонометрии с помощью тонометра Маклакова.
Цифры ВГД у детей могут не отражать истинной картины заболевания, так как растяжение фиброзной капсулы глаза компенсирует его повышением. Оптимальные характеристики офтальмотонуса должны рассматриваться в совокупности с морфометрией глаза.
Главной отличительной особенностью детского глаза является возможность обратного развития патологических изменений зрительного нерва (экскавации) при своевременно компенсированном ВГД [5].
При анализе данных тонометрии учитывают абсолютные цифры уровня ВГД, суточные колебания и разницу офтальмотонуса между глазами. Суточные колебания уровня ВГД, а также его асимметрия между парными глазами у здоровых лиц, как правило, находятся в пределах 2-3 мм рт ст и лишь в редких случаях достигают 4-6 мм рт ст.
Рt– показатели тонометрии при измерении ВГД контактным тонометром Маклакова, чаще грузом массой 10 г.Р0 – истинное ВГД – показатели тонометрии при измерении ВГД большинством современных методов (тонометрия по Гольдману, пневмотонометрия, тонометрия Icare и так далее).
Статистическая норма истинного уровня ВГД (P0) составляет от 10 до 21 мм рт ст, тонометрического уровня ВГД (Pt) — от 12 до 25 мм рт ст.
Таблица 5.
Оптимальные характеристики верхней границы «целевого» офтальмотонуса у больных глаукомой [20].
| Стадия глаукомы | Pt, мм рт ст | P0, мм рт ст |
| Начальная | 22–24 | 18–20 |
| Развитая | 19–21 | 15–17 |
| Стадия глаукомы | Pt, мм рт ст | P0, мм рт ст |
| Далекозашедшая | 16–18 | 10–14 |
На оценку данных тонометрии в значительной степени оказывает влияние толщина и диаметр роговицы, претерпевающие существенные изменения у детей на фоне развития глаукомы.
- Тонография A03.26.015 рекомендуется некоторым пациентам с врожденной глаукомой для уточнения особенностей гидродинамики глаза [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Дополнительная информация о гидродинамике глаза может быть получена при проведении тонографических исследований, при этом наибольшее значение имеют: данные уровня ВГД (норма P0 – от 10 до 21 мм рт.ст.)коэффициент легкости оттока (норма С=0,15 — 0,6 мм3/мин•мм рт.ст.; для пациентов старше 50 лет – более 0,13);минутный объем водянистой влаги (норма F=2,0 — 4,5 мм3/мин);коэффициент Беккера (норма КБ≤100).
- Исследование толщины роговицы (кератопахиметрия A03.26.011.001) рекомендуется всем пациентам с врожденной глаукомой и подозрением на данное заболевание с целью правильной интерпретации результатов тонометрии, а также для выявления одного из факторов риска [2,4,28-35].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Средняя толщина роговицы в оптической зоне (центральная толщина роговицы) у детей составляет 496-620 мкм, с возрастом толщина роговицы увеличивается, в возрасте 5 – 15 лет составляет 529 ± 0,034 мкм.
У детей с ВГ при некомпенсированном ВГД и развитии отека роговицы толщина роговицы увеличивается. При растяжении оболочек и компенсированном ВГД толщина роговицы у детей с ВГ меньше, чем у здоровых детей. (среднее - 540±30 мкм). Целесообразно проводить деление роговиц на тонкие (481-520 мкм), средние (521-560 мкм) и толстые (>561 мкм), и учитывать это при интерпретации значения ВГД. Данные тонометрии в глазах с роговицей, имеющей толщину в центре более 580 мкм, нуждаются в коррекции в сторону понижения (реальное ВГД ниже полученных данных).
- Биомикроскопия глаза A03.26.001 рекомендуется всем пациентам с врожденной глаукомой и подозрением на данное заболевание для оценки состояния структур переднего отрезка глаза и выявлении признаков глаукомы [1-6,17-18,20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии:
Конъюнктива
При подозрении на ВГ, в начальной и развитой ее стадиях с компенсированным и субкомпенсированным ВГД состояние конъюнктивы чаще всего не изменено. При далекозашедшей стадии или при стойком повышении офтальмотонуса возможно наличие застойной или смешанной инъекции глазного яблока.
При глаукоме, сочетанной с факоматозами (синдром Стерджа-Вебера) характерно наличие новообразованных сосудов в виде сосудистой сети, различной степени выраженности.
При наличии фильтрационных подушек (после хирургических вмешательств) необходимо обращать внимание на их ширину, высоту, толщину стенки, степень васкуляризации и кистозные изменения.
Роговица
При начальной стадии при минимальном растяжении роговицы наблюдается легкий ее отек в виде опалесценции. Примечательно, что он легко может быть купирован инстилляциями в конъюнктивальную полость гиперосмолярных жидкостей: р-р глюкозы 40%, р-р натрия хлорида 10%, глицерина и другие, что позволяет его дифференцировать с физиологической опалесценцией роговицы, часто наблюдаемой у новорожденных, при которой опалесценция не исчезает.
При дальнейшем прогрессировании глаукомы увеличивается диаметр роговицы, что вызывает образование на эндотелии и десцеметовой мембране разрывов и трещин в виде единичных, а затем и множественных полосчатых помутнений. За счет нарушения барьерной функции в строму роговицы проникает ВГЖ, нарушаются метаболические процессы, что вызывает отек, а затем и помутнение роговицы. Также происходит увеличение (растяжение) лимба, преимущественно верхнего, а в дальнейшем, при далекозашедшей стадии – во всех отделах (до 5-6 мм).
При развитии глаукомы у детей с аномалиями развития переднего отрезка глаза (II форма-аномалия Петерса) помутнения роговицы различной степени выраженности (чаще стромальные) выявляются уже с рождения. При развитии глаукомы у таких детей, подъем ВГД может вызывать ухудшение состояния роговицы: присоединение явлений отека или повышение интенсивности помутнения.
Передняя камера
В норме в области зрачка глубина передней камеры составляет 2,75–3,5 мм. У детей с начальной стадией ВГ передняя камера нормальной глубины или слегка глубже, чем в норме. По мере растяжения глазного яблока у таких детей передняя камера продолжает углубляться и может достигать 5-6 мм. Необходимо также проводить сравнительную оценку глубины камеры на обоих глазах. Асимметрия этого показателя является важным диагностическим признаком заболевания.
Радужка
В начальной стадии глаукомы зрачковые реакции чаще сохранены. По мере растяжения глаза при гидрофтальме нарастают атрофические изменения радужки: сглаживается рисунок, развивается атрофия зрачковой каймы, крипты становятся менее выражены, визуализируются сосуды глубокой сети (необходимо дифференцировать с неоваскуляризацией), появляется мидриаз, снижается реакция на свет. При аномалии Аксенфельда-Ригера, синдроме Франка-Каменецкого имеются характерные изменения радужки (рассмотрены выше), которые, как правило, предшествуют манифестации глаукомы и могут прогрессировать во времени: появляются трансиллюминационные дефекты, секторальная атрофия, возможны изменения формы зрачка и другие. Следует обращать внимание на присутствие послеоперационных изменений радужки: наличие базальной колобомы, следов лазерной иридэктомии и другие.
Хрусталик
Наряду с прозрачностью, размерами и формой отмечают скопления пигмента, факодонез, сублюксацию или иную дислокацию хрусталика.
- Гониоскопия A03.26.002 рекомендуется всем пациентам с врожденной глаукомой и подозрением на данное заболевание при наличии прозрачности роговицы. Методика позволяет исследовать УПК, включая дренажную зону, выявить уровень ретенции ВГЖ, степень дисгенеза и определить патогенетически ориентированную тактику лечения [1-6,17-18,20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Для ВГ характерно аномальное развитие или недоразвитие всех структур дренажной зоны УПК. Характерными являются:
- Наличие эмбриональной нерассосавшейся мезодермальной ткани (встречается наиболее часто: по данным отечественных авторов -в 50-60% случаев), которая представляет собой вуалевидную ткань, располагающуюся в виде непрерывной полосы или островками (чаще серо-белого или желтоватого цвета), закрывающую и тем самым блокирующую трабекулярную зону радужно-роговичного угла.
- Высокое прикрепление радужки, когда корень ее выдвинут вперед и закрывает трабекулу (10-15%), чаще бывает неравномерно высокое прикрепление радужки.
- Группа аномалий, приводящих к трабекулярной или интрасклеральной ретенции: отсутствие дифференцировки трабекулы (ее недоразвитие), недостаточное развитие или отсутствие шлеммова канала, которые затрудняют или блокируют отток ВГЖ через УПК (15-25%).
- Обнаруженные аномалии встречаются в различных сочетаниях.
Гониодисгенез – задержка в развитии и дифференцировки УПК – подразделяют на 3 степени (Э.Г. Сидоров и М.Г. Мирзаянц, 1991) [5]. I степень –широкое прикрепление пучков ресничной мышцы к гипопластичному трабекулярному переплету, относительная сохранность склерального синуса. II степень – выраженный трабекулодисгенез, с передним прикреплением радужной оболочки, нарушении топографии синуса и частым его сужением. III степень – тяжелая врожденная патология всех элементов дренажной зоны: переднее прикрепление радужной оболочки к измененной трабекуле, резкое сужение склерального синуса.
С помощью цифровой педиатрической ретинальной камеры возможно проведение исследования структур УПК с фоторегистрацией их и наблюдения в динамике.
- Офтальмоскопия A02.26.003 /биомикроскопия глазного дна A03.26.018 рекомендуется всем пациентам с врожденной глаукомой и подозрением на данное заболевание при сохранной прозрачности оптических сред с целью выявления глаукомной оптической нейропатии и возможных изменений сетчатки [1-6,17-18,20].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Одними из основных причин снижения зрительных функций у детей с ВГ является развитие глаукомной оптической нейропатии, что требует детальной характеристики изменений ДЗН. Сложность заключается в частой невозможности визуализации структур глазного дна у детей с ВГ из-за помутнений роговицы.
Для глаукомы характерны атрофические изменения в ДЗН, проявляющиеся в деколорации (побледнении) атрофических участков диска, в расширении и деформации его экскавации.
Оптимальным методом выявления изменений структуры ДЗН является офтальмоскопия:
- обратная офтальмоскопия на щелевой лампе с линзами 60, 78 или 90 Д;
- прямая офтальмоскопия на щелевой лампе через центральную часть линзы Гольдмана или Ван Бойнингена.
При осмотре ДЗН при подозрении на глаукому и при ВГ необходимо проводить количественную и качественную оценку следующих параметров.
1) Количественная оценка ДЗН:
- размер ДЗН;
- соотношение экскавации к диску (Э/Д);
- соотношение нейроретинального пояска (НРП) к диску.
2) Качественная оценка ДЗН:
- форма, высота и цвет НРП, его отсутствие (краевая экскавация) или тенденция к истончению;
- деколорация атрофических участков ДЗН;
- сдвиг сосудистого пучка.
Размер ДЗН. Среднестатистические размеры ДЗН находятся в пределах от 1,9 до 2,8 мм2. К малым размерам ДЗН относят диски площадью меньше 1,5 мм2, к средним – от 1,51 до 2,5 мм2, к большим >2,51 мм2. При ВГ вследствие растяжения глаза чаще встречаются большие ДЗН.
При миопии он может слегка (на 1,2±0,15%) возрастать на каждую диоптрию аметропии. Чем больше ДЗН, тем больше Э/Д и НРП. Соответственно, большая экскавация в большом ДЗН может быть физиологической, в то время как маленькая экскавация при очень маленьком ДЗН может свидетельствовать о глаукомном повреждении зрительного нерва, что существенно затрудняет офтальмоскопическую диагностику рассматриваемой патологии.
Соотношение Э/Д. Физиологическая экскавация ДЗН, как правило, имеет горизонтально-овальную форму: горизонтальный диаметр длиннее вертикального примерно на 8%. Увеличенная физиологическая экскавация при большом размере диска чаще имеет округлую форму. В норме экскавация на обоих глазах симметричная. При этом в 96% случаев соотношение Э/Д находится в пределах 0,3 ДД. В начальной стадии глаукомы чаще четких различий между физиологической и глаукомной экскавацией не существует. Можно визуализировать сдвиг и перегиб сосудистого пучка. При прогрессировании ВГ с высокими цифрами ВГД, уже при развитой стадии формируется довольно объемная экскавация.
Расширение экскавации при глаукоме обычно происходит во всех направлениях, однако чаще всего – в вертикальном направлении за счет истончения НРП в верхнем и нижнем секторах ДЗН, что связано с особенностями строения решетчатой пластинки.
В норме глубина экскавации зависит от площади экскавации и, косвенно, от размеров диска, а при врожденной глаукоме – от уровня ВГД. Самые глубокие экскавации наблюдаются в глазах с высоким уровнем ВГД. На глаукоматозный характер экскавации указывает обнажение решетчатой пластинки в верхней и нижней зоне экскавации. При обследовании пациента с повышенным уровнем ВГД следует придерживаться принципа: чем больше экскавация, тем больше вероятность, что она глаукоматозная.
Нейроретинальный поясок (НРП)
При развитии глаукоматозного процесса постепенно происходит уменьшение ширины НРП, которое может быть равномерным по всей окружности, локальным краевым или сочетанным. Для глаукомы характерны атрофические изменения в ДЗН. Клинически они проявляются в деколорации (побледнении) участков НРП, чаще в темпоральной зоне (необходимо дифференцировать с атрофией зрительного нерва неглаукомного генеза).
Перипапиллярная атрофия – истончение/разрушение хориоретинальной ткани вокруг ДЗН. При глаукоме распространенность перипапиллярной атрофии выше, особенно с носовой стороны перипапиллярного пространства.
Следует помнить, что отдельно каждого из приведенных симптомов в отдельности недостаточно для постановки правильного диагноза. Правильное решение может дать только комплексная оценка состояния ДЗН и перипапиллярной сетчатки. Для документирования состояния ДЗН желательно использовать фото глазного дна.
- Исследование поля зрения (периметрия: (статическая А02.26.005, компьютерная А03.26.020 ) рекомендуется всем пациентам с врожденной глаукомой и подозрением на данное заболевание для оценки степени нарушения светочувствительности зрительной системы с целью комплексной диагностики, оценки стадии и динамики течения глаукомного процесса [36-38].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: Исследование периферического зрения чрезвычайно важно для диагностики и оценки стадии и динамики течения глаукомного процесса, однако она осуществима лишь детям старшего возраста, с достаточным уровнем психомоторного и интеллектуального развития ребенка и наличия предметного зрения. При этом значение имеет исследование поля зрения как с помощью движущихся (кинетическая периметрия), так и неподвижных стимулов (статическая периметрия).
Кинетическая периметрия – оценка положения периферических границ поля зрения, наличие абсолютных и относительных скотом, границ слепого пятна.
Статическая периметрия (компьютерная или автоматическая), заключается в определении степени световой чувствительности в различных участках поля зрения с помощью неподвижных объектов переменной яркости. Может позволяет обнаружить даже минимальные дефекты как центрального, так и периферического поля зрения, существенно повышая эффективность мониторинга начальной и развитой ВГ у детей подросткового возраста, а также ранней диагностики глаукомы, при ее развитии у старших детей.
Оценке подлежат положение периферических границ поля зрения, наличие абсолютных и относительных скотом, границы слепого пятна. При оценке результатов статической автоматической периметрии, кроме того, используют такие индексы как средний дефект или среднее отклонение (MD) и очаговые дефекты (PSD).
Повторные исследования целесообразно проводить 2 раза в год, а при впервые выявленной глаукоме (или подборе терапии или после хирургического лечения) рекомендуется проведение исследований в течение первых двух лет наблюдений через 2-3 месяца.
Ультразвуковые методы исследования
- Ультразвуковая биометрия глаза А04.26.004 (А-сканирование или эхобиометрия) рекомендуется всем пациентам с врожденной глаукомой и подозрением на данное заболевание с целью определения размеров и структурных изменений глазного яблока, глубины передней камеры для выявления тенденции к прогрессированию глаукомы и оценки стадии процесса [1-6,17-18,20].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
- Ультразвуковое исследование глазного яблока А04.26.002 рекомендуется всем пациентам с врожденной глаукомой и подозрением на данное заболевание, позволяет оценить состояние внутренних структур глаза (положение и плотность оболочек, хрусталика, стекловидного тела и др.), что особенно актуально при непрозрачных преломляющих средах [1-6,17-18,20].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
- Ультразвуковое сканирование переднего отдела глаза A04.26.007 рекомендуется детям с врожденной глаукомой и подозрением на данное заболевание при необходимости получить четкое изображение структур переднего отрезка глаза (особенно важным это представляется при помутнении роговицы), структур УПК, дренажной зоны, в частности трабекулы (особенно при врожденных аномалиях). При этом возможно также измерить толщину роговицы (мм), радужки (мм), глубину передней камеры (мм), величину иридокорнеального угла (град.), определить наличие, структуру и размеры патологических образований переднего отрезка глаза и др. и другие [4,17,20].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: При ВГ акустическая картина переднего сегмента глаза характеризуется уплощением и уменьшением рельефа радужки на всем протяжении, гипоплазией склеральной шпоры, аномальным ее положением или ее отсутствием, уменьшением дистанции “трабекула-радужка” и другие. Патологические изменения можно обнаружить и в отношении структуры, размеров и положения цилиарного тела, его отростков и других структур глазного яблока. Причем особенности этих изменений в определенной мере характеризуют форму и стадию глаукомы, что позволяет выработать оптимальную тактику хирургического лечения таких больных, особенно при нарушении прозрачности оптических сред глаза.
- Оптическое исследование сетчатки с помощью компьютерного анализатора A03.26.019, оптическое исследование головки зрительного нерва и слоя нервных волокон с помощью компьютерного анализатора A03.26.019.003 (оптическая когерентная томография (ОКТ) сетчатки и ДЗН) рекомендуется всем пациентам с врожденной глаукомой и подозрением на данное заболевание при прозрачных средах для детальной объективной количественной и качественной оценки состояния зрительного нерва, изменений сетчатки и хориоидеи при диагностике и мониторинге заболевания [4,39-40].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: С помощью ОКТ получают комплекс объективных морфометрических данных, подтверждающих наличие значительных структурных и гемодинамических нарушений в заднем отделе глаза при ВГ, нарастающих по мере ее прогрессирования:
-значительное увеличение основных параметров экскавации ДЗН: объема экскавации, максимальной глубины и площади экскавации;
-уменьшение значений нейроретинального пояска (НРП): объема, площади, минимальной ширины сначала в нижне-носовом отделе;
- уменьшение толщины слоя нервных волокон сетчатки (СНВС) в перипапиллярной зоне с преимущественными изменениями в темпоральной зоне;
-уменьшение толщины слоя ганглиозных клеток и ганглиозного комплекса в макулярной зоне;
-уменьшение толщины хориоидеи.
При сравнительном анализе морфометрических параметров в начальной и далекозашедшей стадиях ВГ с учетом размера глаз, в ряде случаев выявляется менее выраженное увеличение глубины и площади экскавации при далекозашедших стадиях на значительно растянутых глазах, чем на ранних стадиях в глазах с менее растянутыми оболочками. Это можно объяснить характером структурных изменений глаз на поздних стадиях ВГ, когда растяжение оболочек приводит к увеличению размеров глаза, но снижает патологическое воздействие на нервные волокна в зоне ДЗН.
При нормализации ВГД у детей с ВГ может наблюдаться регресс ряда изменений ДЗН: уменьшение размеров экскавации и увеличение размеров НРП, что объясняется возрастными биомеханическими особенностями детского глаза.
- Оптическое исследование переднего отрезка глаза с помощью компьютерного анализатора А03.26.019.001 рекомендуется пациентам с врожденной глаукомой с целью количественной и качественной оценки изменений со стороны переднего отрезка глаза [4].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии. Бесконтактный, превосходящий по разрешающей способности ультразвуковые метод исследования позволяет оценить структуру, измерить и зарегистрировать состояние слоев роговицы, радужки и параметры УПК детей с ВГ. Приборы ОКТ оснащены компьютерными программами, которые способствуют получению изображения, а также формированию и хранению базы данных, обеспечивающей количественный анализ изображения.
Вместе с тем, следует подчеркнуть, что данные, полученные с помощью рассмотренных приборных методов, не являются “эталонными” в диагностике глаукомного процесса, а лишь дополняют результаты комплексного обследования ребенка, которые следует оценивать во всей совокупности. Однако подтвержденное при этом ухудшение состояния ДЗН является важным прогностическим признаком прогрессирования глаукомы.
- Электрофизиологические методы исследования (ЭФИ), включающие электроретинографию общую (A05.26.001), регистрацию комплекса ритмической электроретинограммы (развернутое исследование A05.26.001.003), регистрацию зрительных вызванных потенциалов коры головного мозга A05.26.002 рекомендуются пациентам для определения функционального состояния глаза [1,4,6,20]. Все исследования проводят в соответствии с международными стандартами ISSF.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Электроретинограмма (ЭРГ) и ее компоненты служат объективным показателем функционального состояния сетчатки у детей с ВГ. Прогрессирующее растяжение оболочек глаза обуславливает нарушение кровоснабжения, обменных и биохимических процессов в сетчатке, а также нарушение синаптических связей клеточных элементов сетчатки, образующих нейрональную сеть. Это ведет сначала к компенсаторной активизации процесса фототрансдукции и гиперполяризации, а затем– к снижению биоэлектрической активности, регистрируемой при ЭРГ.
Зрительные вызванные потенциалы (ЗВП) при ВГ уже в начальной стадии заболевания меняют свои амплитудно-временные характеристики во всем диапазоне пространственных частот, которые отражают состояние аксонов ганглиозных клеток сетчатки. Для регистрации ЗВП применяют современные компьютерные системы, позволяющие выделять потенциалы малой величины из шума, используют усреднение и фильтры, нивелирующие различные артефакты. Исследование проводят как во время бодрствования ребенка, так и в состоянии медикаментозного сна или наркоза. Основное внимание уделяют показателям латентности. При анализе полученных данных принимают во внимание, что на формирование пика Р1 ЗВП главным образом оказывает влияние сохранность ретинокортикального пути, зрелость фовеальной области сетчатки и сохранность стриарной коры. Кроме того, следует учитывать, что этот метод не дает возможности оценить сохранность ассоциативных и когнитивных функций головного мозга, которые обеспечивают «зрительное распознавание».
При ВГ серия последовательных ЭФИ до нормализации ВГД и после позволяет оценить состояние сетчатки и зрительного нерва, динамику изменений и спрогнозировать конечные функциональные результаты. Регистрация супернормальной ЭРГ одновременно с высокими цифрами ВГД свидетельствует о непродолжительном периоде гипертензии и благоприятном функциональном исходе. Высокие цифры ВГД с низкой амплитудой ЭРГ характерны для более выраженных патологических изменений в структуре сетчатки и более тяжелом функциональном прогнозе. После нормализации ВГД амплитуда ЭРГ в течении 3-6 месяцев снижается до величин соответствующих стадии заболевания и сохранности нейроэпителия сетчатки. При стойкой нормализации ВГД ЭРГ имеет тенденцию к умеренному повышению амплитуды.
Зрительные вызванные потенциалы при прогрессировании болезни имеют прямую корреляцию изменения амплитудно-частотных характеристик от стадии ВГ. Латентность по мере прогрессирования заболевания и перехода в более позднюю стадию увеличивается, а амплитуда снижается, и к абсолютной стадии ВГ ЗВП не регистрируются. При стойкой компенсации ВГД происходит стабилизация, а затем частичное восстановление амплитудно-временных характеристик ЗВП.
Особенно важными представляются данные ЭФИ при отсутствии возможности оценки остроты зрения из-за возраста ребенка и при помутнении роговицы, когда нельзя визуализировать структуры заднего полюса.
5. Иные диагностические исследования
При врожденной глаукоме у детей не применяются.
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
1. Медикаментозное гипотензивное лечение
– медикаментозная офтальмогипотензивная терапия (назначение противоглаукомных препаратов и миотических средств) рекомендуется в период подготовки ребенка к операции, а также, в ряде случаев, и после нее – при недостаточном гипотензивном эффекте вмешательства. Хотя основное лечение ВГ – хирургическое, в ряде случаев возможна также и длительная компенсация глаукомного процесса гипотензивными глазными каплями [1-6,17-18,20, 41-44].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии:
При выборе медикаментозного препарата необходимо учитывать возраст ребенка, а в процессе лечения тщательно контролировать общий и локальный статус пациента для исключения возможных осложнений гипотензивной терапии. Препараты с одинаковым фармакологическим действием не должны использоваться в комбинации. Выбор препаратов для лечения ВГ достаточно сложен, поскольку основная масса гипотензивных средств, разработанных в последнее время, не проходили клинические испытания на детях, и соответственно не могут быть рекомендованы для применения в детской практике. Тем не менее, при наличии соответствующих показаний, в ряде случаев при соответствующем информированном согласии родителей возможно применение офтальмогипотензивных средств, имеющихся в арсенале “взрослых” офтальмологов.
Основные положения гипотензивной терапии:
- лечение начинать с монотерапии;
- если препарат первой линии недостаточно эффективен, необходимо заменить неэффективный препарат или добавить новый или комбинированный;
- более 3 препаратов применять не целесообразно.
- препараты с одинаковым фармакологическим действием использовать в комбинации не рационально.
- При II и III формах ВГ в большинстве случаев глаукомы показано назначение комбинированных препаратов.
- При высоком ВГД начинать сразу с комбинированных препаратов, а при недостаточной эффективности – добавлять препарат из другой фарм-группы (Простагландин или Альфа-2 адреностимулятор, М-холиномиметик).
Показатели эффективности:
- удержание ВГД в пределах оптимального (толерантного) уровня с минимальным числом препаратов в течение суток;
- отсутствие ускользания эффекта в течение длительного периода;
- минимальное системное воздействие;
- минимум побочных эффектов;
- хорошая переносимость.
Показания к назначению современных гипотензивных препаратов при врожденной глаукоме (в том числе предоперационная подготовка)
Использование этих препаратов показано детям с различными формами ВГ. Их назначают:
- сразу после выявления повышенного ВГД у ребенка;
- включают в схему предоперационной подготовки с целью максимального снижения ВГД перед операцией или поддержания ВГД в нормальных пределах и стабилизации глаукомного процесса;
- применяют для коррекции уровня ВГД в послеоперационный период, а также для попытки нормализации ВГД у оперированных детей в ожидании повторного оперативного вмешательства.
- Рекомендуется назначение ингибиторов карбоангидразы и/или β-адреноблокаторов детям с ВГ для нормализации/снижения ВГД как препаратов первой линии выбора при ВГ. При недостаточной эффективности - комбинация этих препаратов с парасимпатомиметиками или с симпатомиметиками для лечения глаукомы или с аналогами простагландинов [1-6,17-18,20, 41-44].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии:
В настоящее время в России имеется широкий спектр современных гипотензивных средств. Механизм действия препаратов и их эффективность при ВГ представлены в таблице 6.
Таблица 6.
Медикаментозные средства для лечения глаукомы.
Медикаментозные средства для лечения глаукомы.
| Группа препаратов | Механизм действия | Ожидаемый гипотензивный эффект | Побочные эффекты |
|---|---|---|---|
|
β адрено-блокаторы
(S01ED)
|
Снижение продукции водянистой влаги:
-угнетение функции ресничного эпителия;
-сужение передних цилиарных артерий
|
20 – 25% от исходного уровня ВГД | Апноэ, бронхопазм, брадикардия |
| Ингибиторы карбоангидразы (S01EC) |
Снижение продукции водянистой влаги:
Торможение образования ионов бикарбоната с последующим снижением транспорта Na и жидкости
|
>25% от исходного уровня ВГД
(эффективность системного применения выше).
|
При системном применении – метаболический ацидоз, парестезии, диарея, анорексия, подавление роста, уролитиаз
При местном применении раздражение и воспалительные реакции переднего отрезка глазного яблока, головная боль, кожные реакции
|
| Аналоги простаглан-динов (S01EE) | Улучшение оттока водянистой влаги по увеосклеральному пути. | 25–35% от исходного уровня ВГД | Гиперемия, раздражение глаз, утолщение и удлинение ресниц, потемнение радужки, увеит, макулярный отек |
| Парасимпатомиметики (S01EB) |
Улучшение оттока водянистой влаги через трабекулярную сеть:
сокращение сфинктера зрачка и
цилиарной мышцы способствует открытию шлеммова канала и трабекулярной сети
|
17–20% от исходного уровня ВГД | Спазм аккомодации, гиперемия конъюнктивы, головные боли |
| Симпатомиметики для лечения глаукомы (S01EA) |
Снижение продукции водянистой влаги.
Улучшение оттока водянистой влаги по увеосклеральному пути
|
20% от исходного уровня ВГД | Раздражение глаза, катаракта, сонливость (у детей до 2 лет), тахиаритмия, апноэ повышение АД |
- Рекомендуется назначение ингибиторов карбоангидразы и/или β-адреноблокаторов детям до 1 года при ВГ для нормализации/снижения ВГД. Комбинированные противоглаукомные средства не разрешены в детском возрасте и применяются только по строгим показаниям [41,42].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии: Основные зарегистрированные лекарственные средства и их возрастные ограничения представлены в таблице 7.
Таблица 7.
Возрастные ограничения к назначению наиболее распространенных в Российской Федерации гипотензивных препаратов
| Действующее вещество | Минимальный возраст |
|---|---|
| Тимолол** | С рождения |
| Дорзоламид** | С 1 недели |
| Латанопрост | С 1 года |
| Бримонидин | С 2 лет |
| Пилокарпин** | Не указан |
При неосуществимости лечения разрешенными препаратами, с информированного согласия родителей пациента и с разрешения врачебной комиссии назначаются и те, что официально у детей не применяются.
- Рекомендуются бесконсервантные гипотензивные антиглаукомные капли пациентам с синдромом сухого глаза, дисфункцией мейбомиевых желез и хроническими аллергическими реакциями, в качестве препаратов стартовой терапии с целью снижения ВГД [ 44].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: У детей для снижения ВГД доступны бесконсервантные глазные капли дорзоламид** или тимолол**.
- Медикаментозное нейротрофическое лечение рекомендуется с целью сохранения и стимуляции зрительных функций у детей с врожденной глаукомой. Терапию следует проводить регулярно (1-2 раза в год) [1,2,4-6,14-17,20,48,63].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Ишемия зрительного нерва, возникающая вследствие растяжения оболочек и компрессионного давления на сетчатку и хориоидею при ВГ, приводит к потере клетками питательных веществ, накоплению свободных радикалов и продуктов метаболизма, что приводит к апоптозу нейрональных элементов зрительной системы.
В комплекс нейротрофического лечения включают препараты, влияющие на периферическое кровообращение и улучшающие микроциркуляцию: другие психостимуляторы и ноотропные препараты (N06BX), ангиопротекторы (C05), витамины, поливитамины в комбинации с другими средствами (A11A), другие препараты, применяемые в офтальмологии S01X. Терапию следует проводить регулярно 2 раза в год после приема врача-невролога (Прием (осмотр, консультация) врача-невролога).
При стойкой компенсации ВГД в течение 6 мес в комплекс лечения ВГ можно включить физиотерапевтические методы: электростимуляцию зрительного нерва A17.26.003, низкочастотную магнитотерапию на орган зрения A17.26.002.
Показания к назначению современного нейротрофического лечения при ВГ:
Любые формы ВГ с компенсированным ВГД.
Противопоказания к назначению современного нейротрофического лечения при ВГ:
- Нестабильная компенсация глаукоматозного процесса.
- Тяжелая сопутствующая общесоматическая патология.
- Непереносимость назначаемых медикаментозных средств.
- Отсутствие возможности регулярно контролировать ВГД.
2. Хирургическое лечение
- Рекомендуется хирургическое лечение врожденной глаукомы (основной метод лечения врожденной глаукомы) для снижения ВГД. Только хирургическим методом возможно устранить препятствия оттоку ВГЖ, создаваемые различными структурными аномалиями дренажной зоны. При ВГ – это срочное или наиболее раннее хирургическое лечение при первых признаках декомпенсации глаукомы [1-6,17-18,20,45-58].
Уровень убедительности рекомендаций В (уровень достоверности доказательств –2)
Комментарии:
Показания к неотложному хирургическому лечению (в том числе повторному):
- наличие гидрофтальма (I форма) или других форм глаукомы, при которых имеется высокий уровень ВГД, который не может быть нормализован каким-либо другим методом лечения, в том числе медикаментозным путем, кроме хирургического;
- неэффективность других методов лечения при изначально невысоком ВГД у детей с II и III клиническими формами ВГ;
- невозможность осуществления других методов лечения (в том числе несоблюдение врачебных рекомендаций, выраженные побочные эффекты) или недоступность соответствующей медикаментозной терапии.
Повторные операции необходимо проводить даже при остаточных зрительных функциях.
Методы хирургического гипотензивного лечения
- Рекомендуются хирургические методы формирования путей оттока водянистой влаги детям с некомпенсированной врожденной глаукомой [1-6,17-18,20,45-52].
Уровень убедительности рекомендаций В (уровень достоверности доказательств –2)
Комментарий: Данные методики делятся на две группы:
1. Операции, направленные на устранение органических препятствий (в основном, мезодермальной ткани) на пути водянистой влаги к трабекуле:
- Гониотомия (в том числе с гониопунктурой) A16.26.067;
- Трабекулотомия ab interno A16.26.069;
- Лазергониотрабекулопунктура A22.26.006;
2. Вмешательства фистулизирующего типа, предусматривающие формирование нового канала из передней камеры глаза наружу, в интрасклеральное пространство:
- Трабекулотомия ab externo и ее модификации A16.26.069;
- Синустрабекулоэктомия (трабекулоэктомия)и ее модификации A16.26.070;
- Прочие проникающие антиглаукоматозные операции А16.26.118 (диатермогониопунктура; микродиатермогониопунктура и др.);
В XXI веке расширилась сфера «ангулярных» операций: эндоскопические гониотомии, трабекулотомии с микрокатетером с подсветкой. Такие операции за рубежом считают предпочтительными для первых вмешательств при первичной ВГ. Трабекулоэктомию эффективно применяют и как первичную, и как повторную операцию при всех формах детских глауком. Теоретические и практические преимущества имеет комбинация трабекулотомии с трабекулоэктомией, чаще применяемая при далекозашедних стадиях ВГ, особенно при помутнении роговицы, когда ангулярные операции технически невозможны.
Как показывает практика, наиболее стабильный гипотензивный эффект имеет пока синустрабекулоэктомия и ее модификации, целью которых является формирование фистулы из передней камеры глаза в интрасклеральное пространство (объем которого расширен глубокой склерэктомией).
Наиболее применяемые у детей методики операций:
Гониотомия. A16.26.067. Этапы хирургического лечения включают парацентез роговицы, введение в камеру вискоэластика. Далее с помощью введенного в переднюю камеру гониотомического ножа производится разрушение ткани, закрывающей трабекулу и самой трабекулы с противоположной стороны камеры на 1000 – 1100 (в пределах визуализации гониолинзой). После успешной манипуляции ВГЖ дренируется в Шлеммов канал. В случаях неудачи манипуляции можно повторять. Возможные осложнения операции включают включают гифему, циклодиализ, иридодиализ, периферические передние синехии, а также катаракту.
Трабекулотомия. A16.26.069 Возможно выполнение трабекулотомии с использованием металлических зондов (151950) трабекулотомов ( многоразового использования 151940 или одноразового 341200) и с помощью нити или микрокатетера с освещенным атравматическим наконечником по окружности 360 градусов.
Стандартная трабекулотомия. После разреза конъюнктивы выкраивают склеральный лоскут на половину толщины склеры. Локализуют Шлеммов канал, вскрывают его радиально, а во входное отверстие вводят рабочий зонд трабекулотома насколько позволяет кривизна зонда, и, проворачивая его вращательным движением в сторону передней камеры, извлекают по принципу «разрушая-уходи».
Трабекулотомия с использованием нити по окружности 360 градусов. В ходе операции используется нить хирургическая полипропиленовая 256860***6/0 с оплавленным с помощью термокаутера закругленным концом. Нить в просвете Шлеммового канала медленно продвигают анатомическим пинцетом, а для контроля ее положения используют гониолинзу. После ее проведения проксимальный и дистальный концы выводят через разрез склеры и натягивают в противоположных направлениях иглодержателями, производя таким образом трабекулотомию на 360 градусов. Вместо полипропиленовой шовной нити в Шлеммов канал также можно ввести микрокатетер с подсвеченным концом, для лучшей визуализации катетера по мере его продвижения в канале.
Возможные осложнения трабекулотомии включают гифему, серозную или геморрагическую ЦХО, иридодиализ, циклодиализ, отслойку десцеметовой оболочки, отрыв цинновых связок.
Синустрабекулоэктомия (трабекулоэктомия) A16.26.070 – фистулизирующая операция, наиболее часто проводимая в качестве первичной операции при глаукоме различной этиологии у детей. Цель операции – создание обходного пути для оттока ВГЖ путем формирования роговично-склеральной фистулы.
Методика выполнения оперативного вмешательства. Разрез конъюнктивы выполняют в 6 мм от лимба, далее конъюнктиву отсепаровывают тупым путем максимально кпереди. При первичной операции разрез локализуется в верхнем отделе с 11 до 1 часа. Формируют склеральный лоскут, чаще П-образной формы, размерами 4 мм по лимбу и 3 мм от лимба толщиной от 1/2 до 2/3 склеры. Далее лезвием делают боковые радиальный разрезы в области трабекулярной зоны до входа в переднюю камеру и ножницами Vannas соединяют эти разрезы, выкраивая прямоугольный участок трабекулярной ткани. После формирования фистулы радужка может вставиться в нее, что облегчает выполнение иридэктомии. Ее захватывают пинцетом и иссекают в зоне над фистулой. Возможно выполнение ириденклейзиса, при этом радужку у корня не иссекают, а формируют из нее клапан основанием к лимбу, который выводят под склеральный лоскут. Затем склеральный лоскут фиксируют на своем ложе узловыми швами и накладывают шов на конъюнктиву.
Причиной неудач, особенно в отдаленный период, является послеоперационный эписклеральный фиброз зоны фильтрации, особенно выраженный в детском возрасте.
Интраоперационное применение антиметаболитов (фторурацил**, митомицин) значительно улучшает отдаленное результаты трабекулоэктомии, однако чревато серьезными осложнениями – истончением фильтрационной подушки, стойкой чрезмерной гипотонией, блебитом и эндофтальмитом [3,4,20,45-48]. В России применение антиметаболитов при антиглаукоматозных операциях у детей пока не разрешено.
Возможные осложнения гипотензивных операций включают гипотонию, синдром мелкой передней камеры, гифему, ЦХО, макулярный отек, формирование передних и / или задних синехий, инкапсуляцию фильтрационной подушки, чрезвычайно редко – отслойку сетчатки и эндофтальмит.
Преимуществом комбинации трабекулотомии с трабекулоэктомией являются два отдельных механизма увеличения оттока ВГЖ - через трабекулярную сеть и через трабекулэктомическую фистулу. Однако избыточной фильтрации и гипотонии не наблюдается, а ВГД может оставаться нормальным, даже если один из путей перестал функционировать.
- Рекомендуется склерэктомия, трепанация склеры (A16.26.073) детям с ВГ при выполнении синусотрабекулэктомии для профилактики цилиохориоидальной отслойки (ЦХО) в послеоперационном периоде [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
- Имплантация дренажных устройств, клапанов рекомендуется пациентам с рефрактерной врожденной глаукомой, чаще при отсутствии эффекта от вышеперечисленных операций для нормализации офтальмотонуса [51,52].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии:
Имплантация антиглаукоматозного дренажа рекомендована в наиболее сложных случаях с риском развития или наличием избыточного рубцевания в зоне операции, и выраженной патологией конъюнктивы вследствие ранее проведенных операций, активной неоваскуляризацией, афакией и др.
Выбор дренажного устройства зависит от технических возможностей и предпочтений хирурга. Как правило, дренажи с трубками являются резервными вмешательствами при наличии факторов риска недостаточной эффективности трабекулэктомии с применением антиметаболитов, хотя в недавних исследованиях было продемонстрировано, что их имплантация эффективна и безопасна в качестве первичного хирургического вмешательства. Антиглаукомные дренажи в зависимости от материала делятся на ауто-, алло- и эксплантодренажи. Аутодренажи – лоскуты аутосклеры (или другой аутоткани). Их недостатками являются быстрое рубцевание и постепенная блокада путей оттока, сформированных операцией. Аллодренажи ‒ биоматериалы из тканей донора. Наиболее распространенными отечественными дренажами являются дренажи из коллагена, а также губчатый аллогенный биоматериал, созданный по технологии «Аллоплант».
Наиболее распространенными отечественными дренажами являются дренажи из коллагена, а также из губчатого аллогенного биоматериала. Эксплантодренажи ‒ синтетические, из полимерных и других материалов.
У детей наиболее распространенными и часто используемыми являются гидрогелевые, коллагеновые и силиконовые дренажи: дренаж антиглаукоматозный резорбируемый, антиглаукомное фильтрационное устройство (шунт для лечения глаукомы***). Основной причиной повышения уровня ВГД при использовании дренажей является формирование соединительнотканной капсулы вокруг наружного конца дренажа.
- При врожденной глаукоме на фоне закрытия УПК подвывихнутым хрусталиком (синдром Марфана, сферофакия) рекомендуется первым этапом провести удаление подвывихнутого хрусталика (A16.26.092.002, A16.26.092.004, A16.26.092.005) [24,49,50].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 3)
Комментарии. В ряде случаев ленсэктомия позволяет добиться компенсации ВГД. При некомпенсации глаукомы следует выполнить одну из антиглаукоматозных операций в зависимости от клинической ситуации – фистулизизирующую, имплантацию антиглаукоматозного дренажа, циклодеструктивную операцию.
- Хирургические методы сокращения секреции водянистой влаги – циклодеструктивные операции (воздействие на цилиарные отростки, чаще лазерное, реже - крио) рекомендуются при неэффективности операций восстановления нормального оттока ВГЖ (ангулярных или фистулизирующих) и у детей с терминальной глаукомой [53-57].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии. Циклодеструктивные операции направлены на разрушение и атрофию цилиарного тела. В настоящее время наиболее часто применяется лазерная циклокоагуляция, для проведения которой предложено несколько доступов (транссклеральный, транспупиллярный, внутриглазной) и несколько типов лазеров – Nd:YAG лазер, диодный полупроводниковый лазер. Диодный лазер (длина волны 809 нм) обладает потенциальным преимуществом, по сравнению с YAG лазером из-за большего поглощения меланином пигментного эпителия цилиарного тела при хорошей сохранности других структур, через которые проходит лазерный луч. Соответственно, для достижения гистологических изменений в цилиарном теле требуется меньше энергии. Наиболее часто проводится контактная диодная лазерная транссклеральная циклокоагуляция A22.26.018.
Операцию, как правило, выполняют при тяжелых рефрактерных глаукомах, когда ангулярная, фистулизирующая и дренажная хирургия не дали эффекта или хирургия невыполнима из-за рубцовых изменений конъюнктивы, а также на глазах с низким функциональным прогнозом.
Энергия воздействия и число наносимых коагулятов варьируют в зависимости от исходного уровня ВГД и степени пигментации радужки (как косвенного показателя пигментации цилиарных отростков). Всего производится 15–20 аппликаций в 1,5 мм от лимба при перпендикулярном расположении зонда с легким поддавливанием по кругу, избегая верхних отделов. Мощность и экспозиция для диодного лазера соответственно составляют 0,5–1,0 вт и 0,5–2 с, начиная с минимальных значений и постепенно повышая дозу излучения. При появлении акустического хлопка в момент коагуляции (pop-corn – эффект) необходимо уменьшить мощность для минимизации риска чрезмерной травматизации цилиарного тела.
Возможные осложнения операции включают иридоциклит, гифему, гемофтальм, эрозию роговицы, деформацию зрачка, гипотонию, вплоть до субатрофии глазного яблока. Вместе с тем аккуратное дозирование параметров лазерного излучения позволяет свести число таких осложнений к минимуму.
Микроимпульсная диодная лазерная транссклеральная циклокоагуляция - современный более безопасный малотравматичный метод, который в отличие от непрерывно-волновой циклокоагуляции, имеет два цикла: «включения» и «выключения». Во время цикла «выключения» участки цилиарного тела, которые были подвержены тепловому воздействию, охлаждаются, что позволяет защитить их от чрезмерного термического повреждения. Гипотензивный эффект достигается за счет щадящего термического повреждения цилиарного тела и снижения секреции ВГЖ, усиления увеосклерального оттока. Метод позволяет избежать чрезмерного необратимого повреждения цилиарного тела и, помимо показаний к стандартной диод-лазерной циклокоагуляции, может быть использован не только как органосохранный метод при терминальных стадиях ВГ и противопоказаниях к фильтрующим операциям (как и стандартная диод-лазерная циклокоагуляция), но и как менее травматичное первичное вмешательство при отсутствии грубых изменений УПК и декомпенсации ВГД у детей более старшего возраста, а также на глазах с высокими зрительными функциями с ранней декомпенсаций ВГД после ТЭ.
- При развитии интра- и послеоперационных осложнений рекомендуется проведение консервативного медикаментозного и при необходимости хирургического лечения [1-6, 17, 20,45-52].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
- Рекомендуется всем детям при хирургическом лечении ВГ применять меры, препятствующие заращению оперативно созданных путей оттока внутриглазной жидкости [1-6, 17, 20,45-52,63].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии:
Рубцеванию в зоне хирургического воздействия способствуют: недостаточный объем иссекаемой части трабекулы, закрытие зоны операции гониосинехиями, которые являются последствиями послеоперационных иритов и кровоизлияний в переднюю камеру.
Современные способы, препятствующие избыточной пролиферации, а следовательно заращению оперативно созданных путей оттока внутриглазной жидкости, включают: уменьшение травматичности операций, применение кортикостероидов S01BA, протеолитических ферментов и использование цитостатиков из группы антиметаболитов (антиметаболиты, широко применяемые в зарубежной клинической практике, в настоящее время официально не зарегистрированы в качестве офтальмологических препаратов в Российской Федерации), процедура нидлинга (от анг. needle - игла – трансконъюнктивальная ревизия зоны фильтрации), лазерное устранение заращения внутренней фистулы после операции
- Рекомендуется неодим-ИАГ (Nd-YAG - кристалл иттрий-алюминиевого граната, активированный неодимием) - лазерное вмешательство (лазерный синехиолизис A22.26.020) для устранения заращения внутренней фистулы и иридокорнеальных сращений в ранние сроки (до 1-3мес) после трабекулоэктомии. или имплантации дренажных устройств [48,63].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии: В раннем послеоперационном периоде при врожденной глаукоме может развиться рецидив офтальмогипертензии вследствие блокады зоны трабекулоэктомии корнем радужки, образования иридокорнеальных сращений. Необходим гониоскопический контроль состояния внутренней фистулы и угла передней камеры после антиглаукоматозных операций для раннего выявления заращения внутренней фистулы, сращений и своевременного лазерного устранения их. Такая неинвазивная лазерная «рефистулизация» особенно эффективна в ранние сроки после трабекуолэктомии (не позднее 1-3 мес после операции)
Кроме избыточного рубцевания, эффект антиглаукоматозных операций зависит от ряда других осложнений: синдром мелкой передней камеры, цилиохориоидальная отслойка, гифема, макулярный отек.
Синдром мелкой передней камеры в послеоперационном периоде может быть связан: с усиленной фильтрацией ВГЖ через послеоперационную фистулу, плохой адаптацией коньюнктивального разреза и наличием наружной фильтрации, а также с цилиохориоидальной отслойкой (ЦХО).
- Рекомендуется детям после хирургического лечения ВГ в случае гифемы, гемофтальма и ЦХО консервативное лечение: гемостатические средства B02, мидриатические и циклоплегические средства S01F, противовоспалительные препараты S01B, противовоспалительные и противомикробные средства в комбинации S01C, ферментные препараты B01AD, рутозид в комбинации с другими средствами C05CA51 [2].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Причины ЦХО:
1 резкая декомпрессия во время вскрытия фиброзной капсулы глаза, приводящая к нарушению анатомических взаимоотношений глаза;
2. тракционное смещение цилиарного тела и иридохрусталиковой диафрагмы кпереди с формированием отрицательного давления в супрахориоидальном пространстве и транссудацией в него жидкой части крови;
3. гипотония, наступающая во время операции вследствии избыточной наружной фильтрации ВГЖ при неадекватности антиглаукоматозной фистулы или недостаточной герметизации операционной раны;
4. патологические изменения в гемодинамике жидкости супрахориоидального пространства.
В качестве редко встречающегося осложнения трабекулоэктомии у детей описана геморрагическая ретинопатия, напоминающая картину окклюзии центральной вены сетчатки.
ЦХО – самое частое послеоперационное осложнение при синдроме Стерджа-Вебера. Перепад ВГД, возникающий во время операции, является пусковым механизмом к клиническому проявлению сосудистой патологии: операционных и послеоперационных геморрагий, высокой частоте и более тяжелому, чем у взрослых, течению отслоек сосудистой оболочки.
При кровотечении немедленно после иссечения радужной оболочки надо надавить на глазное яблоко ватным тампоном, стараясь одновременно вымывать кровь из раны. Применяют введение стерильного воздуха в переднюю камеру. Если кровь вывести не удалось и образовались сгустки, не следует делать попытки к их извлечению. В течение ближайших нескольких суток становится ясной дальнейшая тактика: консервативное лечение или дополнительное выведение крови.
- Для профилактики и лечения инфекции и воспаления у детей с врожденной глаукомой в послеоперационном периоде рекомендуется применять противовоспалительные и антибактериальные препараты [1-6,14-17,20,48,63].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: В послеоперационном периоде назначают местную терапию -
- противомикробные препараты S01A
- противовоспалительные препараты S01B
- другие препараты, применяемые в офтальмологии
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- Детям с компенсированной врожденной глаукомой рекомендуется медицинская реабилитация, которая включает медикаментозное нейротрофическое лечение и физиотерапевтические методы с целью сохранения и стимуляции зрительных функций. Терапию следует проводить регулярно (1-2 раза в год) [1,2,4-6,14-17,20,48,58,59,63].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Комментарии: Препараты для медикаментозной нейротрофической терапии перечислены выше (раздел 3.1.). Чрескожная электростимуляция зрительного нерва (А17.26.002) через 6 мес после операции, эффективно повышает остаточные зрительные функции при глаукоматозной нейропатии. Терапию следует проводить регулярно 2 раза в год после приема врача-невролога (Прием (осмотр, консультация) врача-невролога).
Возможно также включение в схемы лечения:
- БРТ- биорезонансная терапия- лечение эндогенными и экзогенными электромагнитными полями.
- Цветоимпульсная терапия по методике Тетериной Т.П
- Рефлексотерапия- Акупунктура.
- Мануальная терапия.
-
Рекомендуется терапия, направленная на стимуляцию регенерации эпителия роговицы (декспантенол S01XA12, вязкоупругие вещества
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
- Рекомендуются инстилляции в конъюнктивальную полость гиперосмолярных жидкостей (#декстрозы** B05BA03 ) при легком отеке роговицы (в виде опалесценции) у детей с ВГ [61].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии:
- Инстилляции дорзоламида** S01EC03 часто устраняют отек роговицы при глаукоме, в отличие от физиологического помутнения (опалесценции) роговицы, часто наблюдаемого у новорожденных.
- При отеке роговицы, начальных дистрофических изменениях роговицы применяют также трофические гели ( другие препараты, применяемые в офтальмологии S01XA ) и витамино - насыщенные растворы (другие витаминные препараты A11HA).
- Рекомендуется хирургическое лечение (кератопластика сквозная A16.26.049.008 или кератопластика послойная A16.26.049.004) при стромальных тотальных помутнениях роговицы у детей при ВГ при условии компенсации глаукоматозного процесса. Консервативное лечение неэффективно [62].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
- Рекомендуется коррекция аметропий, включающая очковую коррекцию и коррекцию контактными линзами всем пациентам с ВГ [1-6,17-18,20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Важным является функциональное лечение, направленное на борьбу с амблиопией путем коррекции аметропии и плеоптики. У детей с ВГ чаще выявляется миопия, у большинства – миопия средней и высокой степеней, обязательно требующая коррекции.
- Рекомендуется санаторно-курортное лечение всем детям с компенсированной формой врожденной глаукомы с целью стабилизации и улучшения зрительных функций. [64].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Госпитализация
Организация оказания медицинской помощи
Оказание медицинской помощи пациентам с врожденной глаукомой и подозрением на это заболевание осуществляется в соответствии с Порядком оказания медицинской помощи детям при заболеваниях глаза, его придаточного аппарата и орбиты», утвержденного приказом МЗ РФ № 442н от 25.10.2012 г.
При наличии у ребенка подозрения на ВГ или подтвержденного диагноза глаукомы врачи-педиатры участковые, врачи общей практики (семейные врачи) направляют детей на консультацию к врачу-офтальмологу. Врач-офтальмолог оценивает состояние глаза, проводит обследование, включающее методы инструментальных исследований для уточнения диагноза. При необходимости проведения диагностических процедур с применением анестезии дети направляются в детское офтальмологическое отделение.
При наличии показаний к хирургическому лечению у ребёнка с установленным диагнозом глаукомы, данное лечение осуществляется в условиях стационара – детском офтальмологическом отделении. После оказания медицинской помощи детям в стационаре и при отсутствии показаний к направлению для оказания медицинской помощи в стационарных условиях дети направляются в детский офтальмологический кабинет. В дальнейшем ребёнок находится под диспансерным наблюдением врача-офтальмолога детского офтальмологического кабинета.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- Рекомендуется диспансерное наблюдение врачом офтальмологом (диспансерный прием (осмотр, консультация) врача-офтальмолога B04.029.001) всех детей с врожденной глаукомой и подозрением на данное заболевание, что является необходимым для мониторинга глаукомного процесса и коррекции лечения. Дети с подозрением на ВГ или установленным диагнозом ставятся на диспансерный учет в поликлинике с обязательным соблюдением установленной частоты осмотров (Таблица 9) [1-6, 20,48,63].
Таблица 9.
Частота осмотров детей с врожденной глаукомой
| Течение | Частота осмотров |
|---|---|
| Подозрение на глаукому | Ежемесячно |
| После хирургического лечения | Первый осмотр не позднее, чем через неделю после выписки из стационара |
| Нестабильное течение | Не реже 1 раза в месяц |
| Стабильное течение | 1 раз в 3-6 месяцев |
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии. Очень важен регулярный контроль за ВГД, размерами глаза, остротой зрения. Всем детям в рамках диспансерного наблюдения проводят комплекс обследований, включающий оценку состояния переднего и заднего отделов глаза, измерение ВГД, определение рефракции и зрительных функций: визометрия (A02.26.004), рефрактометрия(A03.26.008), офтальмотонометрия (A02.26.015), биомикроскопия глаза (A03.26.001), офтальмоскопия (A02.26.003) /биомикроскопия глазного дна (A03.26.018), гониоскопия (A03.26.002), ультразвуковая биометрия глаза (A04.26.004), ультразвуковое исследование глазного яблока (А04.26.002), компьютерная периметрия (статическая А02.26.005, компьютерная А03.26.020), при необходимости оптическое исследование сетчатки с помощью компьютерного анализатора (A03.26.019), оптическое исследование головки зрительного нерва и слоя нервных волокон с помощью компьютерного анализатора (A03.26.019.003), оптическая когерентная томография , ОКТ регистрация зрительных вызванных потенциалов коры головного мозга (A05.26.002) и электроретинография (A05.26.001), регистрацию комплекса ритмической электроретинограммы (развернутое исследование) (A05.26.001.003). Следует учесть, что контактные методы исследования осуществимы не всем детям, учитывая их возраст.
Информация
Источники и литература
-
Клинические рекомендации общероссийской общественной организации Ассоциация врачей-офтальмологов
- Клинические рекомендации общероссийской общественной организации Ассоциация врачей-офтальмологов - 1. Аветисов Э.С., Ковалевский Е.И., Хватова А.В. Руководство по детской офтальмологии. М.: Медицина, 1987, 496с. 2. Национальное руководство по глаукоме для практикующих врачей. Под ред. Е.А. Егорова, В.П. Еричева. 4е издание, исправленное и дополненное. М., «ГЕЭТАР-Медиа», 2021. 381 с. 3. Лазарева А.К., Кулешова О.Н., Айдагулова С.В., Черных В.В. Особенности детской глаукомы: обзор литературы. Национальный журнал глаукома 2019; 18(2):102-112. https://doi.org /10.25700/NJG.2019.02.11 4. Садовникова Н.Н., Зерцалова М.А. Врожденная глаукома //Неонатальная офтальмология: руководство для врачей/ под ред.В.В.Бржеского, Д.О.Иванова.-Москва: ГЭОТАР-Медиа,2021.C.205-253. DOI:10.33029|9704-6152-5-NOF-2021-1-288 5. Сидоров Э.Г., Мирзаянц М.Г. Врождённая глаукома и её лечение. М.: Медицина; 1991. 208с 6. Хватова А.В., Яковлев А.А., Теплинская Л.Е. Врожденная глаукома: современный взгляд на патогенез и лечение - Зрительные функции и их коррекция у детей. «Врожденная глаукома: современный взгляд на патогенез и лечение». Медицина. 2005; c.319-344. 7. Катаргина, Л. А., Кадышев, В. В., Сорокин, А. А., Плескова, А. В., Зинченко, Р. А. (2022). Генетические варианты врожденной глаукомы. Анализ литературы и описание клинического случая. Российский офтальмологический журнал, 2022;15(1):105-108. https://doi.org/10.21516/2072-0076-2022-15-1-105-108 8. Lewis CJ, Hedberg-Buenz A, DeLuca AP, Stone EM, Alward WLM, Fingert JH. Primary congenital and developmental glaucomas. Hum Mol Genet. 2017; 26(R1):R28-R36.doi: 10.1093/hmg/ddx205 9. Мотущук, А. Е., Рахманов, В. В.,Мандельштам, М. Ю. (2008). Молекулярно-генетические основы первичной врожденной глаукомы. Офтальмологические ведомости, 1(4), 44-51 10. Shah M, Bouhenni R, Benmerzouga I. Geographical Variability in CYP1B1 Mutations in Primary Congenital Glaucoma. J Clin Med. 2022 Apr 6;11(7):2048. doi: 10.3390/jcm11072048. PMID: 35407656; PMCID: PMC8999900. 11. Васильева, Т. А., Поздеева, Н. А., Воскресенская, А. А., Хлебникова, О. В., Зинченко, З. А., Гинтер, Е. К.Генетические аспекты врожденной аниридии. Практическая медицина, 2015; 2 (87); 26-33. 12. Fung D.S., Roensch M.A., Kooner K.S., Cavanagh H.D. et al. Epidemiology and characteristics of childhood glaucoma: results from the Dallas Glaucoma Registry. Clin Ophthalmol. 2013; 7:1739-1746. doi: 10.2147/opth.s45480 13. Abdolrahimzadeh S, Fameli V, Mollo R, et al.: Rare diseases leading to childhood glaucoma: epidemiology, pathophysiogenesis, and management. Biomed Res Int 2015; 2015:781294. http://doi.org/10.1155/2015/781294 14. Mandal A.K., Netland P.N. The Pediatric Glaucomas. Edinburgh: Elsevier, 2006,Р 113 15. Sampaolesi R, Zarate J, Sampaolesi JR. The Glaucomas (Volume I). Pediatric Glaucomas Springer Berlin Heidelberg, 2009, Р.486. 16. Weinreb RN, Grajewski A, Papadopoulos M,Grig J, Freeman S. Childhood Glaucoma. World glaucoma Association (Consensus Series-9), Kugler Publication, Amsterdam,Netherlands, 2013, Р.272. 17. Сомов Е.Е. Врожденная глаукома //Избранные разделы детской клинической офтальмологии/под ред.Е.Е.Сомова. Санкт-Петербург:Человек,2016.С 190-197. 18. Сомов Е.Е. Первичная глаукома. Медиздат; 1992, 8 с. 19. Thau A., Lloyda M., Freedman C ., Beck A. et al. New classification system for pediatric glaucoma implications for clinical care and a research registry. Curr Opin Ophthalmol 2018; 29:385-394. http://doi.org/10.1097/ICU.0000000000000516 20. Катаргина Л.А., Мазанова Е.В., Тарасенков А.О., Сайдашева Э.И., Бржеский В.В., Володин П.Л. и др. Федеральные клинические рекомендации «Диагностика, медикаментозное и хирургическое лечение детей с врожденной глаукомой» Российская педиатрическая офтальмология. 2016; 11 (1):33-51. 21. Суханова, Н. В., Кадышев, В. В., Васильева, Т. А., Марахонов, А. В., Катаргина, Л. А., Куцев, С. И., Зинченко, Р. А. Клинико-генетические особенности при полной и частичной врожденной аниридии. РМЖ. Клиническая офтальмология, 2023; 23(1), 2-8.doi: 10.32364/2311 -7729-2023-23-1-2- 8. 22. Суханова Н.В., Катаргина Л.А., Панова А.Ю., Зинченко Р.А. Клинико-генетические аспекты глаукомы, ассоциированной с врождённой аниридией. Российская педиатрическая офтальмология. 2023;18(2):67-74. doi:10.17816/rpoj321768 23. Клинические рекомендации «Аниридия врожденная» (Q13.1.Дети).Утверждены МЗ РФ в 2020г.-61с 24. Senthil, Sirisha MS, FRCS; Rao, Harsha L. MD, DNB; Hoang, Nguyen T.Q. MD; Jonnadula, Ganesh B. B Opt; Addepalli, Uday K. B Opt; Mandal, Anil K. MD; Garudadari, Chandra S. MD, FRCS. Glaucoma in Microspherophakia: Presenting Features and Treatment Outcomes. Journal of Glaucoma 23(4):p 262-267, doi: 10.1097/IJG.0b013e3182707437 25. Grigorian F, Grigorian AP, Olitsky SE. The use of the iCare tonometer reduced the need for anesthesia to measure intraocular pressure in children. J Aapos. 2012;16(6):508-10. 26. Flemmons MS, Hsiao YC, Dzau J, Asrani S, Jones S, Freedman SF. Icare rebound tonometry in children with known and suspected glaucoma. J Aapos. 2011;15(2):153-7. 27. Тугеева, Э. Э., Бржеский, В. В. Особенности измерения внутриглазного давления у детей. Офтальмологические ведомости. 2016; 9(3), 23-31. 28. Баранов, А. Ю., Бржеский, В. В. Исследование толщины роговицы у детей с глаукомой. Forcipe, 2019. 2(S3), 10-10.ISSN 2658-4174 29. Henriques MJ, Vessani RM, Reis FA, de Almeida GV, Betinjane AJ, Susanna R, Jr. Corneal thickness in congenital glaucoma. J Glaucoma. 2004;13(3):185-8.DOI: 10.1097/00061198-200406000-00002 30. Pediatric Eye Disease Investigator Group; Bradfield YS, Melia BM, Repka MX, Kaminski BM, Davitt BV, Johnson DA, Kraker RT, Manny RE, Matta NS, Weise KK, Schloff S. Central corneal thickness in children. Arch Ophthalmol. 2011 Sep;129(9):1132-8. doi: 10.1001/archophthalmol.2011.225. PMID: 21911662; PMCID: PMC3253021. 31. Dai E, Gunderson CA. Pediatric central corneal thickness variation among major ethnic populations. J AAPOS. 2006 Feb;10(1):22-5. doi: 10.1016/j.jaapos.2005.12.007. PMID: 16527675. 32. Doozandeh A, Yazdani S, Ansari S, Pakravan M, Motevasseli T, Hosseini B, Yasseri M. Corneal profile in primary congenital glaucoma. Acta Ophthalmol. 2017;95(7):e575-e581. 33. Zareei A, Razeghinejad MR, Salouti R. Corneal Biomechanical Properties and Thickness in Primary Congenital Glaucoma and Normal Eyes: A Comparative Study. Med Hypothesis Discov Innov Ophthalmol. 2018;7(2):68-72. PMID: 30250855.PMCID: PMC6146241 34. Баранов, А. Ю., Епифанова, Э. Э., Бржеский, В. В., Садовникова, Н. Н. Результаты ультразвуковой и ОКТ-пахиметрии у пациентов с врожденной глаукомой и здоровых детей. Офтальмология Восточная Европа. 2023; 13 (4): 324, 333. 35. Doughty M.J., Laiquzzaman M., Müller A. et al. Central corneal thickness in European (white) individuals, especially children and the elderly, and assessment of its possible importance in clinical measures of intra-ocular pressure. Ophthalmic Physiol Opt. 2002;22(6):491-504. doi: 10.1046/j.1475-1313.2002.00053.x. 36. Тарасенков, А. О.,Мазанова, Е. В. Роль статической компьютерной периметрии в комплексном обследовании детей с врожденной глаукомой. Российский общенациональный офтальмологический форум.2017; 1, 265-269. 37. Donahue SP, Porter A. SITA visual field testing in children. J AAPOS. 2001;5:114. doi: 10.1067/mpa.2001.113840 38. Sinha, G., Patil, B., Sihota, R., Gupta, V., Nayak, B., Sharma, R., Gupta, N.Visual field loss in primary congenital glaucoma. JAAPOS.2015; 19(2), 124-129. doi: 10.1016/j.jaapos.2014.12.008 39. Катаргина, Л. А., Мазанова, Е. В., Тарасенков, А. О., Рябцев, Д. И. Современные методы диагностики глаукомной оптической нейропатии при врожденной глаукоме у детей. Российская педиатрическая офтальмология,2012.1: 18-21. 40. Катаргина Л.А., Арестова Н.Н., Демченко Е.Н., Панова А.Ю., Сорокин А.А. Оптическая когерентная томография в диагностике глаукомной оптической нейропатии у детей с первичной врожденной глаукомой. Российский офтальмологический журнал. 2023;16(3):33-38. DOI: 10.21516/2072-0076-2023-16-3-33-38 41. Coppens G., Stalmans I., Zeyen T., Casteels I. The safety and efficacy of glaucoma medication in the pediatric population. J Pediatr Ophthalmol Strabismus. 2009; 46(1):12-8.DOI:10.3928/01913913-20090101-05 42. Катаргина, Л. А., Тарасенков, А. О., Мазанова, Е. В. Ретроспективный анализ применения гипотензивных медикаментозных средств при врожденной глаукоме на базе детского хирургического отделения. Российская педиатрическая офтальмология. 2013; (1), 8-12. 43. Катаргина, Л. А., Мазанова, Е. В.Применение препарата Альфаган® р в лечении глаукомы у детей. Российская педиатрическая офтальмология. 2014; (3), 10-13. DOI: https://doi.org/10.17816/rpoj37588 44. Еричев В.П., Волжанин А.В. Бесконсервантная терапия глаукомы. Национальный журнал глаукома. 2020; 19(1):69-78. DOI: 10.25700/NJG.2020.01.10 45. Mocan M.C., Mehta A.A., Aref A.A. Update in Genetics and Surgical Management of Primary Congenital Glaucoma. Turk. J Ophthalmol. 2019; 49:347-355 DOI: 10.4274/tjo.galenos.2019.28828 46. Gagrani M, Garg I, Ghate D. Surgical interventions for primary congenital glaucoma. Cochrane Database Syst Rev. 2020 Aug 25;8(8):CD008213. doi: 10.1002/14651858.CD008213.pub3. PMID: 32816311; PMCID: PMC8094178. 47. Ling L, Ji K, Li P, Hu Z, Xing Y, Yu Y, Zhou W. Microcatheter-Assisted Circumferential Trabeculotomy versus Conventional Trabeculotomy for the Treatment of Childhood Glaucoma: A Meta-analysis. Biomed Res Int. 2020 Nov 4;2020:3716859. doi: 10.1155/2020/3716859. PMID: 33204692; PMCID: PMC7657706. 48. Арестова Н.Н., Арестов Д.О., Панова А.Ю. Влияние различных факторов на эффективность трабекулэктомии у детей с врождённой глаукомой. Российская педиатрическая офтальмология. 2024; 19 (2):59-71 https://doi.org/10.17816/rpoj629264 49. Burugupally K, Senthil S, Parameshwarappa DC, Ali H, Balakrishnan D, Garudadri C. Outcomes of lensectomy with glued intraocular lens and factors associated with failure in eyes with spherophakia and glaucoma. Indian J Ophthalmol. 2023 Jun;71(6):2487-2492. doi: 10.4103/ijo.IJO_1866_22. 50. Venkataraman P, Haripriya A, Mohan N, Rajendran A. A systematic approach to the management of microspherophakia. Indian J Ophthalmol. 2022; 70(7):2262-2271. doi: 10.4103/ijo.IJO_2888_21. 51. Razeghinejad MR, Kaffashan S, Nowroozzadeh MH. Results of Ahmed glaucoma valve implantation in primary congenital glaucoma. J AAPOS. 2014 Dec;18(6):590-5. doi: 10.1016/j.jaapos.2014.08.008. Epub 2014 Nov 12. PMID: 25459201. 52. Wang S, Gao X, Qian N. The Ahmed shunt versus the Baerveldt shunt for refractory glaucoma: a meta-analysis. BMC Ophthalmol. 2016 Jun 8;16:83. doi: 10.1186/s12886-016-0265-6. PMID: 27277579; PMCID: PMC4898360. 53. Autrata R., Rehurek J. Long-term results of transscleral cyclophotocoagulation in refractory pediatric glaucoma patients. Ophthalmologica. 2003; 217:393–400. doi.org/10.1159/000073068 54. Elhefney E.M., Mokbel T.H., Hagras S.M., et al. Micropulsed diode laser cyclophotocoagulation in recurrent pediatric glaucoma. Eur J Ophthalmol. 2020; 30(5):1149-1155. doi: 10.1177/1120672119858226. 55. Abdelrahman A.M., El Sayed Y.M. Micropulse Versus Continuous Wave Transscleral Cyclophotocoagulation in Refractory Pediatric Glaucoma. J Glaucoma. 2018; 27(10):900-905. doi: 10.1097/IJG.0000000000001053. 56. Prager A.J.., Anchala A.R. Suprachoroidal hemorrhage after micropulse cyclophotocoagulation diode therapy. Am J Ophthalmol Case Rep. 2020; 18:100659. doi: 10.1016/j.ajoc.2020.100659. 57. Панова, А. Ю., Катаргина, Л. А., Денисова, Е. В., Сорокин, А. А. Ближайшие результаты микроимпульсной циклофотокоагуляции при глаукоме у детей. Российская педиатрическая офтальмология 2022; 17(3), 21-29.Doi: https://doi.org/10.17816/rpoj107300 58. Патеюк Л.С., Дракон А.К., Шелудченко В.М., Корчажкина Н.Б. Роль электростимуляции в лечении дегенеративно дистрофических заболеваний сетчатки и зрительного нерва. Обзор литературы. Офтальмология. 2021;18(3S):673-680. https://doi.org/10.18008/1816-5095-2021-3S-673-680 59. Мезенцева, В. С. Современные подходы к лечению частичной атрофии зрительного нерва физическими факторами (обзор литературы). Точка зрения. Восток-Запад. 2016;2; 101-103. 60. Бржеский В.В., Романова Е.А., Киреева В.А. Современные направления слезозаместительной терапии больных с синдромом «сухого глаза». Медицинский совет. 2022;16(23):255–261. doi.org/10.21518/2079-701X-2022-16-23-255-261. 61. Орлова А.С., Башкатов А.Н., Генина Э.А., Колбенев И.О., Каменских И.Д., Каменских Т.Г., Тучин В.В. Влияние 40%-го раствора глюкозы на структуру роговицы человека. Известия Саратовского университета. Новая серия. Серия Физика, 2014; 14(1): 11-19. 62. Плескова А. В., Мазанова Е. В., Катаргина Л. А. Клинические особенности и результаты кератопластики при врожденных помутнениях роговицы, сочетающихся с врожденной глаукомой у детей. Российская педиатрическая офтальмология. 2013; 1:27-30. 63. Арестова Н.Н. Вопросы диспансеризации и реабилитации детей с врожденной глаукомой после трабекулэктомии. XV Российский общенациональный офтальмологический форум: сб науч. тр. науч.-практ. конф. с международ. участием в 2-х т. / под ред В. В. Нероева: 2022. Т. 2: 466-470. 64. Каёткина Е. В., Кондратюк Г. И., Ляшенко Н.И. Реабилитация слабовидящих детей в специализированном центр. Российская детская офтальмология 2015; 1:13-18.
Информация
Список сокращений
ВГ – врожденная глаукома
ВГД – внутриглазное давление
ВГЖ – внутриглазная жидкость
ДЗН – диск зрительного нерва
ЗВП – зрительно вызванные потенциалы
МКБ 10 – международная классификация болезней 10-го пересмотра
НРП – нейроретинальный поясок
ОКТ – оптическая когерентная томография
ПЗ – поле зрения
ПЗР – передне-задний размер глазного яблока
СНВС – слой нервных волокон сетчатки
УПК – угол передней камеры
ЦХО – цилиохориоидальная отслойка
ЧЭС– чрескожная электростимуляция
ЭРГ – электроретинография
ЭФИ – электрофизиологические исследования
Э/Д – соотношение диаметра экскавации к диску
AD – аутосомно-доминантный тип наследования
AR – аутосомно-рецессивный тип наследования
Знак ** после наименования препарата – лекарственный препарат внесен в перечень ЖНВЛП
Знак *** – рекомендация относится к медицинскому изделию, имплантируемому в организм человека при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи (Перечень медицинских изделий, имплантируемых в организм человека при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи, утвержденный распоряжением Правительства Российской Федерации от 31 декабря 2018 г. N 3053-р).
Знак # перед наименованием препарата – препарат используется в несоответствии с показаниями к применению и противопоказаниями, способами применения и дозами, содержащимися в инструкции по применению лекарственного препарата
Термины и определения
Биомикроскопия глаза – это метод прижизненного визуального исследования оптических сред и тканей глаза, основанный на создании контраста между освещенными и неосвещенными участками, проводимый при помощи щелевой лампы и дополнительных диагностических линз (в частности, для биомикроскопии глазного дна).
Внутриглазное давление (ВГД) – давление жидкости внутри глаза, являющееся результатом баланса между продукцией камерной влаги, трабекулярным и увеосклеральным оттоком и давлением в эписклеральных венах, поддерживающее его форму и обеспечивающее постоянство циркулирующих питательных веществ, и нормальную трофику внутриглазных тканей.
Врожденная глаукома (ВГ) – группа гетерогенных заболеваний, характеризующихся повышением ВГД выше толерантного в первые месяцы/годы жизни, обусловленным нарушением эмбриогенеза (аномалии УПК и дренажной системы), с помутнением роговицы, деформацией и увеличением глаза в первые годы жизни,оптической нейропатией, с последующей атрофией зрительного нерва и снижением электрогенеза сетчатки (при прогрессирующем течении).
Аниридийная кератопатия – своеобразное нарушение прозрачности роговицы, возникающее на фоне первичной недостаточности лимбальных стволовых клеток и постепенно прогрессирующее от периферии к центру роговицы в виде васкуляризированного паннуса (нарушение развития и регенерации нормальной роговицы).
Гидрофтальм («водянка глаза») или буфтальм («бычий глаз») – форма врожденной глаукомы с классическим течением, с изменениями в углу передней камеры (УПК).
Глаукомная оптическая нейропатия (ГОН) –патология зрительного нерва, обусловленная повышенным ВГД, характеризующаяся прогрессирующей потерей ганглиозных клеток сетчатки и их аксонов и ведущая к структурному и функциональному повреждению зрительного нерва, нарушению зрительных функций и слепоте.
Гониодисгенез – врожденные аномалии УПК и дренажной системы глаза, возникающие в результате задержки в развитии и дифференциации этих структур.
Гониоскопия – это метод визуального исследования (осмотра) угла передней камеры глаза (УПК), проводимый при помощи щелевой лампы и гониолинзы (гониоскопа).
Гониотомия – хирургическое вмешательство, при котором под визуальным контролем (с помощью гониолинзы) в области УПК производят удаление тканей, препятствующих оттоку ВГЖ и восстановление переднего пути оттока.
Гониосинехия - спайка в радужно-роговичном углу глаза между корнем радужки и роговицей.
Диск зрительного нерва (ДЗН) – место выхода аксонов ганглиозных клеток сетчатки из глазного яблока.
Нейроретинальный поясок (НРП) ‒ это область между краем диска зрительного нерва и краем экскавации, где проецируется основная масса аксонов ганглиозных клеток сетчатки.
Нидлинг – хирургическая методика механической ревизии фильтрационной подушки с помощью инъекционной иглы на шприце.
Оптическая когерентная томография (ОКТ) ‒ это диагностический неинвазивный бесконтактный метод прижизненной визуализации, качественного и количественного анализа морфологических особенностей структур глазного дна, основанный на принципе световой интерферометрии.
Офтальмогипертензия – повышение уровня ВГД при отсутствии характерных для глаукомы изменений ДЗН, СНВС и дефектов ПЗ.
Офтальмоскопия – инструментальный метод осмотра глазного дна и его структур.
Офтальмотонометрия – метод инструментального измерения уровня ВГД, величина которого определяется анализом данных деформации глаза тонометром и оценивается в миллиметрах ртутного столба (мм рт.ст.).
Периметрия – метод исследования поля зрения (ПЗ).
Поле зрения – совокупность точек пространства, одновременно видимых глазом при неподвижном взоре.
Рефрактерная глаукома – форма заболевания с тяжелым, упорным течени
Синустрабекулоэктомия (трабекулоэктомия) – хирургическое вмешательство, целью которого является создание дополнительного пути оттока водянистой влаги из глазного яблока, который направлен под склеральную оболочку и конъюнктиву.
Скотома – дефект ПЗ, не связанный с периферическими границами.
Слой нервных волокон сетчатки (СНВС) – слой сетчатки, представляющий собой аксоны ганглиозных клеток сетчатки.
Стабилизированная и нестабилизированная глаукома - термины, обозначающие отсутствие или наличие отрицательной динамики в состоянии ДЗН и ПЗ, передне-заднего размера глаза (ПЗР), рефракции пациента при повторных исследованиях. При оценке динамики глаукомного процесса принимают во внимание также уровень ВГД и его соответствие «целевому» значению.
Стандартная автоматизированная периметрия – компьютерная пороговая статическая периметрия, при которой исследуют ПЗ с помощью белого стимула на белом фоне.
Угол передней камеры (УПК, радужно-роговичный угол) – пространство между роговично-склеральной областью и передней поверхностью радужки.
«Целевое» внутриглазное давление – это максимальное допустимое давление, при котором глаукома не прогрессирует: зрительные функции не снижаются, ГОН не прогрессирует, глазное яблоко не растягивается.
Экскавация диска зрительного нерва – углубление в ДЗН различной формы и размеров, в норме составляет не более 0,3 диаметра диска (физиологическая экскавация).
Электрофизиологические исследования – методы исследования функции зрительного нерва, сетчатой оболочки, зрительных областей в коре головного мозга.
Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Прогноз врожденной глаукомы у детей определяется возрастом ребенка, сроком выявления заболевания, стадией и тяжестью глаукоматозного поражения глаза ребенка на момент выявления глаукомы, своевременностью диагностики и хирургического лечения.
Критерии оценки качества медицинской помощи
Таблица 10.
Критерии оценки качества медицинской помощи
Критерии оценки качества медицинской помощи
|
Критерий
|
Оценка выполнения (да\нет)
|
|---|---|
|
Выполнена визометрия
|
да\нет
|
|
Выполнена тонометрия
|
да\нет
|
|
Выполнена эхобиометрия
|
да\нет
|
|
Выполнена биомикроскопия глаза
|
да\нет
|
|
Выполнена офтальмоскопия
|
да\нет
|
|
Выполнена компьютерная периметрия,
|
да\нет
|
|
Выполнено оптическое исследование сетчатки, головки зрительного нерва и слоя нервных волокон с помощью компьютерного анализатора (оптическая когерентная томография, ОКТ)
|
да\нет
|
|
Проведено хирургическое и/или лазерное лечение (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний)
|
да\нет
|
|
Выполнено назначение противоглаукомных препаратов и миотических средств (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний)
|
да\нет
|
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
-
Катаргина Людмила Анатольевна – руководитель группы, главный внештатный специалист детский офтальмолог Министерства здравоохранения РФ, Заместитель директора по научной работе ФГБУ «Национальный медицинский исследовательский центр глазных болезней им Гельмгольца» Минздрава России, начальник отдела патологии глаз у детей, профессор, д.м.н., Москва;
-
Арестова Наталия Николаевна – ведущий научный сотрудник отдела патологии глаз у детей ФГБУ «Национальный медицинский исследовательский центр глазных болезней им Гельмгольца» Минздрава России, доцент, д.м.н., Москва;
-
Панова Анна Юрьевна – научный сотрудник отдела патологии глаз у детей ФГБУ «Национальный медицинский исследовательский центр глазных болезней им Гельмгольца» Минздрава России, к.м.н., Москва;
-
Денисова Екатерина Валерьевна – старший научный сотрудник отдела патологии глаз у детей ФГБУ «Национальный медицинский исследовательский центр глазных болезней им Гельмгольца» Минздрава России, к.м.н., Москва;
-
Бржеский Владимир Всеволодович – заведующий кафедрой офтальмологии, ГБОУ ВПО «Санкт-Петербургский Государственный Педиатрический медицинский университет» Минздрава РФ, профессор, д.м.н., Санкт-Петербург;
-
Садовникова Наталия Николаевна – заведующая офтальмологическим отделением клиники ФГБОУ ВО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава РФ», к.м.н., доцент. Санкт-Петербург;
Конфликт интересов отсутствует.
Приложение А2. Методология разработки клинических рекомендаций
Методы, использованные для сбора/селекции доказательств: поиск в электронных базах данных; анализ современных научных разработок по проблеме глаукомы в России и за рубежом, обобщение практического опыта российских и иностранных коллег.
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которые прокомментировали доступность интерпретации доказательств, лежащих в основе рекомендаций, для практических врачей и пациентов.
Комментарии, полученные от экспертов, тщательно систематизированы и обсуждены председателем и членами рабочей группы. Каждый пункт обсужден и внесены соответствующие изменениям рекомендации.
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме.
Целевая аудитория данных клинических рекомендаций:
-
Врачи-офтальмологи;
-
Врачи педиатры (семейные врачи)
Таблица 1.
Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД
|
Расшифровка
|
|---|---|
|
1
|
Систематические обзоры исследований с контролем референтным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа
|
|
2
|
Отдельные исследования с контролем референтным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа
|
|
3
|
Исследования без последовательного контроля референтным методом или исследования с референтным методом, не являющимся независимым от исследуемого метода, или нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая
|
|
5
|
Имеется лишь обоснование механизма действия или мнение экспертов
|
Таблица 2.
Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
УДД
|
Расшифровка
|
|---|---|
|
1
|
Систематический обзор рандомизированных клинических исследований с применением метаанализа
|
|
2
|
Отдельные рандомизированные клинические исследований и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований с применением метаанализа
|
|
3
|
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль»
|
|
5
|
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
|
Таблица 3.
Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР
|
Расшифровка
|
|---|---|
|
А
|
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
|
|
В
|
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
|
|
С
|
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
|
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым клиническим рекомендациям, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учетом следующих документов:
-
«Порядка оказания медицинской помощи детям при заболеваниях глаза, его придаточного аппарата и орбиты», утвержденного приказом МЗ РФ № 442н от 25.10.2012 г.
-
Международная классификация болезней, травм и состояний, влияющих на здоровье, 10-го пересмотра (МКБ-10) (Всемирная организация здравоохранения) 1994.
-
Номенклатура медицинских услуг (Министерство здравоохранения и социального развития Российской Федерации) Приказ Минздрава России от 13.10.2017 N 804н (ред. от 24.09.2020, с изм. от 26.10.2022) "Об утверждении номенклатуры медицинских услуг" (Зарегистрировано в Минюсте России 07.11.2017 N 48808)
-
Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» от 21.11.2011 г. № 323 Ф3.
-
Перечень жизненно необходимых и важнейших лекарственных препаратов для медицинского применения на 2020 год. Распоряжение Правительства РФ от 12.10.2019 N 2406-р (ред. от 26.04.2020) «Об утверждении перечня жизненно необходимых и важнейших лекарственных препаратов на 2020 год, а также перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи».
-
Приказ МЗ РФ от 27 марта 2024 г. n 143н об утверждении классификации природных лечебных ресурсов, указанных в пункте 2 статьи 2.1 федерального закона от 23 февраля 1995 г. n 26-фз "о природных лечебных ресурсах, лечебно-оздоровительных местностях и курортах", их характеристик и перечня медицинских показаний и противопоказаний для санаторно-курортного лечения и медицинской реабилитации с применением таких природных лечебных ресурсов
Приложение Б. Алгоритмы действий врача
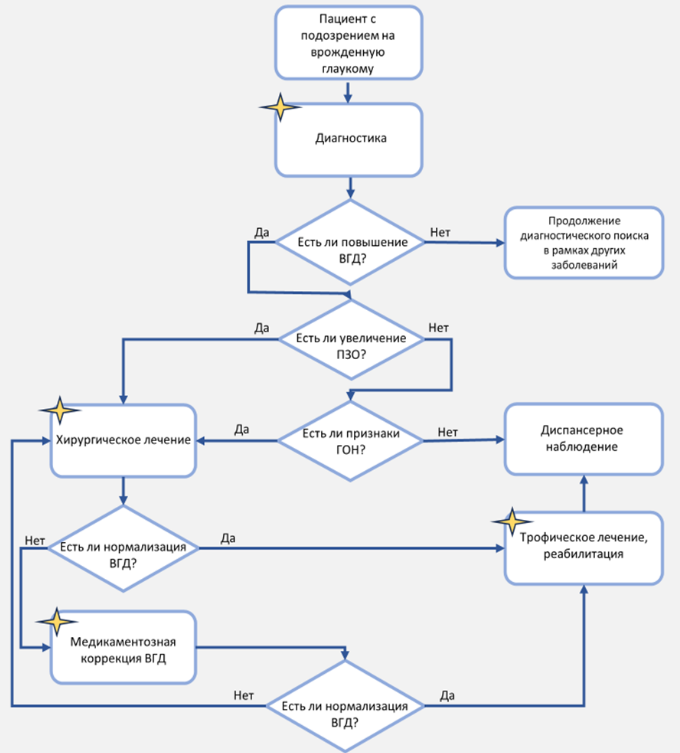
Приложение В. Информация для пациента
Врожденная глаукома – тяжелое врожденное заболевание, являющееся одной из основных причин слепоты, слабовидения и нарушений зрения у детей с раннего возраста. Успех лечения детей с врожденной глаукомой во многом зависит от раннего выявления заболевания и своевременного проводимого лечения. В поздних стадиях заболевания даже после хирургического лечения шансы на успешный исход значительно снижаются. При несвоевременно начатом лечении болезнь быстро прогрессирует и приводит к необратимым изменениям всех структур глазного яблока. Дети с подозрением на врожденную глаукому или установленным диагнозом ставятся на диспансерный учет в поликлинике. При подозрении на врожденную глаукому ребенок должен быть в обязательном порядке обследован и если диагноз не снимается, обследования повторяются ежемесячно. Ребенок с установленным диагнозом и нормализованным давлением должен показываться окулисту не реже одного раза в три месяца. После хирургического лечения первое обследование следует проводить не позднее, чем через неделю после выписки из стационара; при нестабильном течении – не реже 1 раза в месяц, при стабильном – 1 раз в 3-6месяцев.
Необходимо срочное обращение к врачу-офтальмологу при появлении любого из нижеперечисленных симптомов: покраснение глаза, светобоязнь, боль, снижение и/или затуманивание зрения, выпадение поля зрения, нарушение восприятия цветов, изменение цвета радужки, размеров и формы зрачка.
Необходимо строго соблюдать все назначения и рекомендуемую кратность обследования у врача-офтальмолога.
Пациент (родители пациента) должны владеть информацией о возможных побочных эффектах терапии, а также срочно обращаться к врачу-офтальмологу при их развитии.
В случае необратимой слепоты или слабовидения пациент (родители пациента) должны владеть полной информацией о возможностях социальной, психологической и профессиональной реабилитации.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Нет.
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.