Болезнь Крона у детей
гранулематозный или регионарный энтерит и/или колит, трансмуральный илеит, терминальный илеит, CD, Crohn Disease
 Версия: Клинические протоколы 2020-2023 (Узбекистан)
Версия: Клинические протоколы 2020-2023 (Узбекистан)
Болезнь Крона [регионарный энтерит] (K50), Болезнь Крона неуточненная (K50.9), Болезнь Крона толстой кишки (K50.1), Болезнь Крона тонкой кишки (K50.0), Другие разновидности болезни Крона (K50.8)
Гастроэнтерология детская, Педиатрия, Хирургия детская
Общая информация
Краткое описание
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ УЗБЕКИСТАН
НАЦИОНАЛЬНАЯ ПАЛАТА ИННОВАЦИОННОГО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ УЗБЕКИСТАН
НАЦИОНАЛЬНЫЙ КЛИНИЧЕСКИЙ ПРОТОКОЛ ПО ВЕДЕНИЮ ДЕТЕЙ СБОЛЕЗЬНЮ КРОНА
Вводная часть
Клиническая проблема: Педиатрия (Детская гастроэнтерология)
Название документа: Национальный клинический протокол по ведению детей с болезнью Крона
Этапы оказания помощи: Стационарный и амбулаторный
Дата создания: 13.12.2021 г
Планируемая дата обновления: 1 квартал 2025 года
Введение
Воспалительные заболевания кишечника (ВЗК) являются многофакторными заболеваниями неясной этиологии с доказанным влиянием окружающей среды на генетическую предрасположенность.
Болезнь Крона (БК) до настоящего времени остается одной из серьезных проблем гастроэнтерологии и колопроктологии. Несмотря на значительные достижения в области изучения патогенеза воспалительных заболеваний кишечника (ВЗК), принципиальных сдвигов в понимании их этиологии не произошло, а следовательно, не существует методов этиотропной терапии. Заболеваемость как язвенным колитом, так и болезнью Крона во всем мире возрастает с каждым годом, причем преимущественно среди трудоспособного контингента населения, что делает ВЗК социально значимыми заболеваниями. Клиническая картина ВЗК отличается многообразием, что часто затрудняет своевременную диагностику и назначение адекватной терапии и неизбежно негативно сказывается на прогнозе заболеваний. Определяется БК как хроническое рецидивирующее заболевание желудочно-кишечного тракта неясной этиологии, характеризующееся трансмуральным, сегментарным, гранулематозным воспалением с развитием местных и системных осложнений.
Болезнь Крона
Цели и задачи создания протокола по ведению детей с болезнью Крона
Цель:
Обеспечить качественную, своевременную диагностику больным детям с подозрением на болезнь Крона и лечение в соответствии с последними научными данными, основанных на доказательной медицине и принятых в качестве европейских и отечественных согласительных документов.
Задачи:
1. Обеспечение нормативной и методологической базы для своевременной качественной диагностики болезни Крона и ее лечения у детей;
Коды МКБ 10
К 50. Болезнь Крона
Категория пациентов
Больные с подозрением на болезнь Крона и с установленным диагнозом болезнь Крона.
Целевая аудитория данных клинических рекомендаций:
56. Врачи общей практики;
57. Врачи-педиатры;
58. Врачи-гастроэнтерологи
59. Врачи-диетологи
60. Врачи реаниматологи
61. Врачи хирурги
62. Преподаватели, студенты медицинских ВУЗов, клинические ординаторы и магистранты, докторанты
ГЛАВА 1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ
Определение
Болезнь Крона (БК) - хроническое, рецидивирующее заболевание желудочно-кишечного тракта неясной этиологии, характеризующееся трансмуральным, сегментарным, воспалением стенки тонкой и/или толстой кишки или всего желудочнокишечного тракта с развитием местных и системных осложнений. Синонимы: гранулематозный колит, терминальный илеит.
Особенности кодирования заболевания Болезнь Кронa тонкой кишки.
K50.1 Болезнь Кронa толстой кишки.
K50.8 Другие рaзновидности болезни Кронa.
K50.9 Болезнь Кронa неуточненнaя.
Классификация
Классификация
Для классификации БК по локализации поражения и фенотипическим вариантам течения рекомендуется использовать, применительно к детям, международную классификацию болезни Крона (табл.1) [8].
Таблица 1. Классификация Болезни Крона
|
Критерий
|
Градации
|
Сочетания
|
|
Возраст, начала болезни
|
А1а – 0 - < 10 лет
А1b – 10 - < 17 лет А2 – 17 – 40 лет А3 - > 40 лет |
|
|
Локализация
|
L1 - Терминальный илеит
L2 - Изолированный колит L3 - Илеит и колит L4a - Верхние отделы с поражением до связки Трейца L4b – Верхние отделы с поражением ниже связки Трейца, но выше дистальной 1/3 подвздошной кишки |
L1+L4
L2+L4
L3+L4
L4ab
|
|
Форма
|
В1 - нестриктурирующая и непенетрирующая (воспалительная)
В2 - стриктурирующая В3 – пенетрирующая В2В3 - стриктурирующая и пенетрирующая р – перианальные проявления |
B2B3 – сочетание стеноза и пенетрации
Сочетание с перианальным поражением В1р, В2р, В3р |
|
Рост
|
Go – нет задержки роста,
G1 – задержка роста |
|
Сейчас выделяют также ВЗК с очень ранним началом (ОРН ВЗК) – до 6 лет, а также младенческие ВЗК – с началом в первые 2 года жизни [5].
По характеру течения выделяют:
1. Острое течение (менее 6 месяцев от дебюта заболевания);
2. Хроническое непрерывное течение (отсутствие более чем 6-месячных периодов ремиссии на фоне адекватной терапии);
3. Хроническое рецидивирующее течение (наличие более чем 6-месячных периодов ремиссии).
По характеру течения выделяют:
1. Острое течение (менее 6 месяцев от дебюта заболевания);
2. Хроническое непрерывное течение (отсутствие более чем 6-месячных периодов ремиссии на фоне адекватной терапии);
3. Хроническое рецидивирующее течение (наличие более чем 6-месячных периодов ремиссии).
В зависимости от ответа на гормональную терапию и облегчения выбора рациональной лечебной тактики, поскольку целью консервативного лечения является достижение стойкой ремиссии с прекращением терапии ГКС выделяются: стероидорезистентность(сохранение активности заболевания несмотря напероральный приема декватной дозы ГКС в течение 7-14 дней).Стероидозависимость(определяется при достижении клинической ремиссии на фоне терапии глюкокортикостероидами и возобновлении симптомов при снижении дозы или в течение 3 месяцев после полной отмены, а также в случаях, если терапию стероидами не удается прекратить в течение 14-16 недель).Также определяется педиатрический индекс активности болезни Крона (приложениеГ1) [7].
Этиология и патогенез
Этиология и патогенез заболевания
Этиология воспалительных заболеваний кишечника (ВЗК), в том числе БК, точно не установлена: заболевание развивается в результате сочетания нескольких факторов, включающих генетическую предрасположенность, дефекты врожденного и приобретенного иммунитета, дисбиоз и различные факторы окружающей среды. Обнаружено более 100 генов, предрасполагающих к ВЗК, большинство из которых контролирует взаимодействие иммунной системы с внешними антигенами, среди них при БК с большей частотой встречаются мутации NOD2, IL23R, ATG16L1, IRGM, NKX2-3, 1q24, 5p13, HERC2, CCNY, 10q21. Более 50% генов, определяющих чувствительность к ВЗК, ассоциированы и с другими воспалительными и аутоиммунными заболеваниями, что может объяснить развитие внекишечных проявлений ВЗК [1]. При этом каких-либо специфических генетических особенностей, свойственных детям, обнаружено не было, за исключением группы детей раннего возраста.
Изменения кишечной микробиоты выявлены у всех больных БК, они характеризуются уменьшением видового разнообразия, уменьшением числа толерогенных видов (например, Faecalibacterium prausnitzii, Bacteroides thetaiotaomicron), увеличением жгутиковых бактерий, изменением вирома, усилением проницаемости слоя слизи и количества микробов, пенетрирующих слизистый слой [2]. Хроническое воспаление при ВЗК является следствием аномальной и пролонгированной активации иммунной системы кишечника. Многочисленные исследования продемонстрировали, что нарушения имеют место практически во всех звеньях иммунного ответа [3]. начиная от барьерных функций эпителия и распознавания антигена паттерн-распознающими рецепторами, передачи сигнала дендритными клетками и сигнальными молекулами, презентации антигена HLA, и заканчивая функциями моноцитов-макрофагов, Т- и В-лимфоцитов.
Образование инфламмасом, активация каспазы-1 и секреции провоспалительных цитокинов: IL-1, IL-17, IL-23, IL-6, TNF-a обусловливают кишечное воспаление с развитием массивной глубокой воспалительной инфильтрации кишечника. Младенческие формы ВЗК могутбыть обусловлены нарушением формирования иммунологической толерантности к собственной микробиоте кишечника вследствие мутации отдельных генов, например, IL-10, FOXP3, XIAP и др. [4].
Каскад гуморальных и клеточных реакций при БК приводит к трансмуральномувоспалению кишечной стенки с образованием характерных для БК саркоидныхгранулем, состоящих из эпителиоидных гистиоцитов без очагов некроза и гигантских клеток. При БК могут поражаться любые отделы желудочно-кишечного тракта - от полости рта до ануса. Тем не менее, в подавляющем большинстве случаев у детей доминирует поражение илеоцекального отдела (70%), изолированное поражение толстой кишки встречается в 30%, аноректальной области – у 20%, поражение верхних отделов ЖКТ – у 5-15% [5].
Эпидемиология
Эпидемиология
Во всем мире наблюдается рост частоты воспалительных заболеваний кишечника (ВЗК) у детей, в частности - болезни Крона (БК), заболеваемость которой варьирует от 1,5 до 11,4 на 100000[6,7], при этом расчетное значение распространенности БК составляет 58/100000. Точных данных о распространенности БК у детей в России нет, но отдельные региональные наблюдения указывают на аналогичную тенденцию. Так, в Санкт-Петербурге заболеваемость БК возросла за последние 10 лет более чем в 10 раз исоставила 5,5 на 100000, а распространенность – 20 на 100000 детей и подростков [5]. Примерно у 10% больных БК впервые манифестирует в возрасте до 17 лет, за последние 10 лет ВЗК с началом в детском возрасте возросли в 3 раза [8].
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания
В детском возрасте ВЗК характеризуются более агрессивным течением, чем у взрослых, процесс имеет более распространенный характер, склонен к прогрессирующему нарастанию тяжести, заболевание сопряжено с более вероятным развитием осложнений и требует более интенсивной терапии, в частности, назначения глюкокортикостероидов,(аналогов пурина) (тиопуринов), метотрексата и ингибиторов фактора некроза опухоли альфа (антицитокиновых препаратов) [9,10].Вероятность осложнений, требующих хирургического вмешательства, также более высока у пациентов с дебютом БК в детском возрасте. Клиническая картина на ранних этапах развития БК может быть стертой, симптоматика неспецифичной, что затрудняет своевременную диагностику. Иногда БК протекает латентно, проявляясь лишь задержкой физического развития ребенка, иногда первыми симптомами могут быть осложнения или внекишечные проявления (ВКП)[11].
К осложнениям БК относят: наружные свищи (кишечно-кожные), внутренние свищи (межкишечные, кишечно-пузырные, ректо-вагинальные), инфильтрат брюшной полости, межкишечные или интраабдоминальные абсцессы, стриктуры ЖКТ (с нарушением кишечной проходимости и без таковой), анальные трещины, парапроктит (при аноректальном поражении), кишечное кровотечение (редко). Более 40% детей имеют внекишечные проявления болезни (табл.2) [7]. Вероятность развития ВКП повышается с нарастанием длительности БК, они чаще встречаются притолстокишечной форме БК, ассоциированные с активностью заболевания ВКП нередко сочетаются друг с другом. Принципиально при ВЗК возможны поражения любых органов, но наиболее часто встречаются поражения суставов, печени, глаз и кожи [7].
Таблица 2 – Внекишечные проявления болезни Крона [7]
|
Аутоиммунные, связанные с активностью заболевания
|
Аутоиммунные, не связанные с активностью заболевания
|
Обусловленные длительным воспалением и метаболическими нарушениями
|
|
Периферическая артропатия 1-го типа (олигомоноартрит) Поражение кожи (узловатая эритема, гангренозная пиодермия, синдром Свита) Поражение слизистых (афтозный стоматит) Поражение глаз (увеит, ирит, иридоциклит, эписклерит)
|
Периферическая артропатия 2-го типа (полиартрит) Анкилозирующий спондилит (сакроилеит) Первичный склерозирующий холангит (редко) Остеопороз, остеомаляция Псориаз
|
Холелитиаз Стеатоз печени, стеатогепатит Тромбоз периферических вен, тромбоэмболия легочной артерии Амилоидоз
|
Аутоиммунные проявления, связанные с активностью воспалительного процесса, появляются вместе с основными кишечными симптомами обострения и исчезают вместе с ними на фоне лечения. Аутоиммунные проявления, не связанные с активностью процесса (сопутствующими аутоиммунными заболеваниями), имеют тенденцию к прогрессированию независимо от фазы основного заболевания (обострение или ремиссия) и часто определяют неблагоприятный прогноз болезни. Своевременная и точная диагностика, адекватная терапия способны изменить естественное течение БК, при этом выбор терапии должен соответствовать локализации процесса, его активности, учитывать индивидуальные особенности пациента, в частности, возраст и имеющиеся факторы риска.
Диагностика
ГЛАВА 2. ДИАГНОСТИКА БОЛЕЗНИ КРОНА
Однозначных диагностических критериев БК не существует, диагноз устанавливается на основании сочетания данных анамнеза, клинической картины и типичных эндоскопических ипатолого-анатомических (гистологических) изменений [12,13].
В практике возможно ориентироваться на критерии диагностики болезни Крона поLennrd-Johns:
1. Поражение любого отдела ЖКТ от полости рта до анального канала: хроническое гранулематозное поражение слизистой оболочки губ или щек; пилородуоденальное поражение, поражение тонкой кишки, хроническое перианальное поражение;
2. Прерывистый характер поражения ЖКТ;
3. Трансмуральный характер поражения: афтозные язвы, язвы-трещины, абсцессы, свищи;
4. Фиброз: стриктуры;
5. Лимфоидное: трансмуральное воспаление, лимфоидные скопления;
6. Муцин: нормальное содержание муцина в зоне активного воспаления слизистой оболочки толстой кишки;
7. Обнаружение неказеозной гранулемы.
Диагноз БК достоверен: 3 признака или 1 признак+гранулема. Также выделяют фенотипы ВЗК в зависимости от частоты и вероятный диагноз в зависимости от первоначального фенотипа (у не леченного ребенка) (табл.3)
Таблица 3. Фенотипы ВЗК в зависимости от частоты и вероятный диагноз в зависимости от первоначального фенотипа (у не леченного ребенка) [5,14].
|
Класс
|
Номер
|
Признак
|
|
1
|
1
|
Хотя бы одна гранулема в любом отделе ЖКТ, не связанная с криптом
|
|
2
|
Хотя бы одна глубокая язва или участок «булыжной мостовой» в любом отделе тонкой кишки или ЖКТ (исключая желудок)
|
|
|
3
|
Свищ, внутренний или перианальный
|
|
|
4
|
Значительные воспалительные изменения кожи и перианальной области
|
|
|
5
|
Утолщение стенки подвздошной или тонкой кишки, подтвержденное методами визуализации, или признаки воспаления тонкой кишке, обнаруженные видео капсулой
|
|
|
6
|
Признаки воспаления в подвздошной кишке при отсутствии поражения слепой кишки
|
|
|
2
|
7
|
Участки эндоскопически и гистологически нормальной слизистой толстой кишки, чередующиеся с пораженной (без лечения)
|
|
8
|
эндоскопически и гистологически нормальная слизистая оболочка прямой кишки
|
|
|
9
|
Эндоскопически нормальные участки толстой кишки среди воспаленных, но гистологически с признаками воспаления (очаговость)
|
|
|
10
|
Значительная задержка роста (>2 стандартных отклонений) не объяснимая другими причинами
|
|
|
11
|
Трансмуральное воспаление в толстой кишке при отсутствии тяжелого колита
|
|
|
12
|
Маленькие неглубокие (включая афтозные) язвы в 12 п/к, тонкой кишке или пищеводе, не объяснимыми другими причинами (ГЭРБ, НПВС, целиакия, H. Pylori и др.)
|
|
|
13
|
Множественные (более 5) маленькие неглубокие язвы (включая афтозные) в толстой кишке не объяснимыми другими причинами (ГЭРБ, НПВС, H. Pylori, и др.)
|
|
|
14
|
Илеит, похожий на ретроградный, но при небольшом воспалении в слепой кишке
|
|
|
15
|
ASCA (+), ANKA (-)
|
|
|
16
|
Обратное нарастание активности воспаления ( проксимальное > дистального)
|
|
|
17
|
Выраженный грубый рельеф слизистой оболочки в желудке или в 12п/к не объяснимыми другими причинами (целиакия, H. Pylori)
|
|
|
18
|
Глубокая язва или «булыжная мостовая» не объяснимыми другими причинами (целиакия, H. Pylori, НПВС)
|
|
|
3
|
19
|
Очаговый хронический дуоденит гистологически
|
|
20
|
Очаговый активный колит гистологически более чем в одном биоптате
|
|
|
21
|
Менее 5 афтозных язв в желудке или толстой кишке
|
|
|
22
|
Диарея без крови
|
|
|
23
|
Очаговый активный гастрит
|
Для верификации периода заболевания (обострение или ремиссия), оценки тяжести обострения, а также для динамической оценки эффективности лечения больного следует использовать расчет Педиатрического индекса активности болезни Крона (PCDAI)[7].
Оригинальное название: PCDAI (Pediatric Crohn’s Disease Activity Index)
Источник (официальный сайт разработчиков, публикация с валидацией): [15,16]/
Тип: индекс
Назначение: определение активности болезни Крона у детей
|
Критерии
|
|
Балл
|
|
Боли в животе
|
Нет
|
0
|
|
Малой интенсивности
|
5
|
|
|
Сильной интенсивности
|
10
|
|
|
Стул, частота, консистенция
|
0-1 раза в день, жидкий без примесей крови
|
0
|
|
2-5 раза в день, с небольшой примесью крови
|
5
|
|
|
Более 6 раза в день
|
10
|
|
|
Самочувствие, активность
|
Нет ограничения активности
|
0
|
|
Умеренное ограничение активности
|
5
|
|
|
Значительное ограничение активности
|
10
|
|
|
Масса тела
|
Нет снижения массы тела 0
|
0
|
|
Снижение массы тела на 1-9%
|
5
|
|
|
Снижение массы тела более 10%
|
10
|
|
|
Рост
|
Ниже одного центеля
|
0
|
|
От 1-2 центелей
|
5
|
|
|
Ниже двух центелей
|
10
|
|
|
Болезненность в животе Н
|
Нет болезненности
|
0
|
|
Болезненность, отмечается уплотнение
|
5
|
|
|
Выраженная болезненность
|
10
|
|
|
Параректальные проявления
|
Нет
|
0
|
|
Активная фистула, болезненность, абсцесс
|
10 | |
|
Внекишечные проявления
|
Нет
|
0 |
|
Одно
|
5
|
|
|
Более двух
|
10
|
|
|
Гематокрит у детей до 10 лет
|
>33
|
0
|
|
28-32
|
2,5
|
|
|
<28
|
5
|
|
|
Гематокрит (девочки 11-18 лет)
|
>35
|
0
|
|
30-34
|
2,5
|
|
|
<30
|
5
|
|
|
Гематокрит (мальчики 11-14 лет)
|
>35
|
0
|
|
30-34
|
2,5
|
|
|
<30
|
5
|
|
|
Гематокрит (мальчики 15-18 лет)
|
>37
|
0
|
|
32-36
|
2,5
|
|
|
<32
|
5
|
|
|
СОЭ (мм/час)
|
<20
|
0
|
|
20-50
|
2,5
|
|
|
>50
|
5
|
|
|
Альбумин (г/дл)
|
>3.50
|
0
|
|
3.1-3.4
|
5
|
|
|
<3.0
|
10
|
Ключ (интерпретация) PCDAI:
<10: отсутствие активности (ремиссия)
11-30: легкая или среднетяжелая форма
30-100: тяжелая форма
Клинический ответ на лечение:
Снижение индекса PCDAI ≥ 15 баллов по сравнению с исходным; суммарный
индекс PCDAI ≤ 30 баллов
Клиническая ремиссия:
PCDAI ≤ 10 баллов
Утрата ответа на лечение:
Увеличение PCDAI ≥ 15 баллов или PCDAI> 30 баллов
Жалобы и анамнез
К наиболее частым клиническим симптомам БК у детей относятся [7].
- длительная хроническая диарея (более 6 нед), чаще без примеси крови;
- боль в животе упорного характера с четкой локализацией;
- потеря массы, значительный дефицит массы тела, отставание в росте;
- длительная лихорадка неясного генеза;
- анемия, чаще железодефицитная;
- перианальные осложнения (хронические анальные трещины, парапроктит, свищи прямой кишки).
<10: отсутствие активности (ремиссия)
11-30: легкая или среднетяжелая форма
30-100: тяжелая форма
Клинический ответ на лечение:
Снижение индекса PCDAI ≥ 15 баллов по сравнению с исходным; суммарный
индекс PCDAI ≤ 30 баллов
Клиническая ремиссия:
PCDAI ≤ 10 баллов
Утрата ответа на лечение:
Увеличение PCDAI ≥ 15 баллов или PCDAI> 30 баллов
Жалобы и анамнез
К наиболее частым клиническим симптомам БК у детей относятся [7].
- длительная хроническая диарея (более 6 нед), чаще без примеси крови;
- боль в животе упорного характера с четкой локализацией;
- потеря массы, значительный дефицит массы тела, отставание в росте;
- длительная лихорадка неясного генеза;
- анемия, чаще железодефицитная;
- перианальные осложнения (хронические анальные трещины, парапроктит, свищи прямой кишки).
У пациентов с БК с поражением верхних отделов ЖКТ могут наблюдаться и другие гастроэнтерологические жалобы. Так, при поражении пищевода отмечаются жалобы на боли в грудной клетке, изжогу и срыгивание (напоминающие таковые при гастро-эзофагеальной рефлюксной болезни), в более тяжелых случаях – на дисфагию и одинофагию, рвоту и потерю массы тела. При БК с поражением желудка и двенадцатиперстной кишки больные могут предъявлять жалобы на боли, тяжесть и переполнение в эпигастральной области, тошноту, снижение аппетита [17,18]. При сборе анамнеза стоит обратить внимание на информацию о поездках в южные страны, непереносимости пищевых продуктов, приеме лекарственных препаратов (включая антибиотики и нестероидные противовоспалительные препараты (НПВП)), курении и семейном анамнезе в отношении ВЗК и других аутоиммунных заболеваний.
Физикальное обследование
В объективное обследование ребенка следует включать оценку физического и полового развития, полный осмотр, включая осмотр перианальной области. При осмотре могут быть обнаружены различные проявления болезни, включая дефицит питания, отставание в росте и половом развитии, афты слизистой рта, наличие инфильтрата брюшной полости, наружных кишечных свищей, перианальных проявлений (трещин, свищей), а также внекишечных проявлений.
Лабораторные диагностические исследования
Рекомендовано при подозрении на БК (см. раздел 2.1 «Жалобы и анамнез») провести исследование уровня кальпротектина в кале (определение кальпротектина в кале) как показателя активности воспаления в кишечнике с целью диагностики БК[19-21].
(УУР – А УДД - 1)
Комментарии: Уровень фекального кальпротектина значительно выше при толстокишечном воспалении. При повышении уровня фекального кальпротектина более чем в 5 раз (250 мг/г либо выше, в зависимости от возраста) ребенок должен быть направлен в гастроэнтерологическое отделение для углубленного исследования.
Физикальное обследование
В объективное обследование ребенка следует включать оценку физического и полового развития, полный осмотр, включая осмотр перианальной области. При осмотре могут быть обнаружены различные проявления болезни, включая дефицит питания, отставание в росте и половом развитии, афты слизистой рта, наличие инфильтрата брюшной полости, наружных кишечных свищей, перианальных проявлений (трещин, свищей), а также внекишечных проявлений.
Лабораторные диагностические исследования
Рекомендовано при подозрении на БК (см. раздел 2.1 «Жалобы и анамнез») провести исследование уровня кальпротектина в кале (определение кальпротектина в кале) как показателя активности воспаления в кишечнике с целью диагностики БК[19-21].
(УУР – А УДД - 1)
Комментарии: Уровень фекального кальпротектина значительно выше при толстокишечном воспалении. При повышении уровня фекального кальпротектина более чем в 5 раз (250 мг/г либо выше, в зависимости от возраста) ребенок должен быть направлен в гастроэнтерологическое отделение для углубленного исследования.
Детям с установленным диагнозом БК – контроль уровня фекального кальпротектина не реже, чем 1 раз в год с целью контроля воспалительной реакции кишечника и своевременной коррекции терапии либо при обострении.
Фекальный кальпротектин является чувствительным маркером воспаления, применяется также в качестве способа мониторинга активности заболевания.
Для повышения чувствительности фекального кальпротектина в мониторинге активности заболевания, рекомендовано также дополнительно определение СРБ и клинического индекса активности БК [7].
Рекомендовано всем пациентам при подозрении на БК и далее – при динамическом наблюдении исследовать Общий (клинический) анализ крови развернутый (оценка гематокрита, Исследование уровня эритроцитов в крови, Исследование уровня тромбоцитов в крови, Исследование уровня лейкоцитов в крови, Дифференцированный подсчет лейкоцитов (лейкоцитарная формула), Просмотр мазка крови для анализа аномалий морфологии эритроцитов, тромбоцитов и лейкоцитов, Определение размеров эритроцитов, скорость оседания эритроцитов(СОЭ) с целью выявления анемии и признаков воспалительной реакции, С-реактивный белок – для оценки воспалительной реакции [20-22].
(УУР – С УДД -3)
Комментарии: Доказательных данных по необходимой частоте проведения данных лабораторных исследований нет. Следует контролировать показатели общего(клинического) анализа крови развернутого и С-реактивного белка, в среднем не реже 1-2раза в год, при необходимости – чаще (при госпитализации – обязательно).
(УУР – С УДД -3)
Комментарии: Доказательных данных по необходимой частоте проведения данных лабораторных исследований нет. Следует контролировать показатели общего(клинического) анализа крови развернутого и С-реактивного белка, в среднем не реже 1-2раза в год, при необходимости – чаще (при госпитализации – обязательно).
Общий (клинический) анализ крови развернутый контролируется у пациентов, получающих иммунодепрессанты (аналоги пурина или метотрексат), не реже одного раза в 1-3 месяца.
Изменения в лабораторных данных при БК имеют неспецифический характер. В общем анализе крови могут быть обнаружены анемия (чаще железодефицитная или анемии хронического заболевания, реже В-12- или фолиево дефицитная), лейкоцитоз (на фоне хронического воспаления, при наличии абсцесса или на фоне стероидной терапии),увеличение СОЭ.
Всем детям с подозрением на БК рекомендовано проведение анализа крови биохимического общетерапевтического (общий белок, протеинограмма, печеночные ферменты (определение активности аланинаминторансферазы (АЛТ),аспартатаминотрансферазы (АСТ), гамма-глютамилтрансферазы(ГГТ), щелочной фосфатазы в крови) , электролиты (натрий, калий, магний, хлор), уровень железа сыворотки крови, трансферрин, ферритин, уровень общего билирубина в крови, уровня глюкозы в крови, Исследование уровня креатинина в крови, Исследование уровня мочевины в крови с целью оценки воспаления, функции печени, почек, обмена железа, электролитного баланса[20,21].
(УУР-С; УДД-3)
Комментарий: Биохимическое исследование позволяет выявить повышение С-реактивного белка (СРБ), диспротеинемию (в частности, гипоальбуминемию и повышение a - и γ-глобулинов). При поражении печени может быть повышен уровень АЛТ, АСТ, ГГТ, общего билирубина.
(УУР-С; УДД-3)
Комментарий: Биохимическое исследование позволяет выявить повышение С-реактивного белка (СРБ), диспротеинемию (в частности, гипоальбуминемию и повышение a - и γ-глобулинов). При поражении печени может быть повышен уровень АЛТ, АСТ, ГГТ, общего билирубина.
В дальнейшем при динамическом наблюдении следует контролировать параметры анализа крови биохимического общетерапевтического. Частота и выбор параметров устанавливается индивидуально, в зависимости от тяжести течения и клинических проявлений, в среднем – не реже 1-2 раз в год.
Пациентам, получающим аналоги пурина (тиопурины) или метотрексат), исследуются «печеночные» ферменты в среднем не реже 1 раза в 1-3 месяца.
Рекомендовано детям с подозрением на БК при первичной диагностике с целью исключения/подтверждения паразитарных инвазий провести микроскопическое исследование кала на гельминты с применением методов обогащения[5].
(УУР-С; УДД-5)
Комментарии: исследования могут проводиться и в процессе динамического наблюдения при подозрении на глистные инвазии.
(УУР-С; УДД-5)
Комментарии: исследования могут проводиться и в процессе динамического наблюдения при подозрении на глистные инвазии.
Рекомендовано при остром начале диареи выполнить исследование кала для исключения острой кишечной инфекции, исследование токсинов А и В Clostridioidesdifficile (устаревшее наименование - Clostridium difficile)(Определение токсинов возбудителя диффициального клостридиоза (Clostridium difficile) в образ цахфекалий, Исследование кала на наличие токсина клостридии диффициле(Clostridium difficile), Иммуно-хроматографическое экспресс-исследование кала натоксины А и В клостридии (Clostridium difficile)) или Определение ДНК возбудителя диффициального клостридиоза (Clostridium difficile) в образцах фекалий методом ПЦР (при недавно проведенном курсе антибиотикотерапии или пребывании в стационаре для исключения псевдомембранозного колита) . [5,21].
(УУР-С; УДД-3)
Комментарий: При подозрении на кишечные инфекции проводятся соответствующие тесты на выявление Salmonella, Shigella, Yersinia, Campylobacter (например: Микробиологическое (культуральное) исследование фекалий/ректального мазка на микроорганизмы рода сальмонелла (Salmonella spp.), Микробиологическое (культуральное) исследование фекалий/ректального мазка на иерсинии (Yersinia spp.), Микробиологическое (культуральное) исследование фекалий/ректального мазка на возбудитель иерсиниоза (Yersinia enterocolitica), Микробиологическое (культуральное) исследование фекалий/ректального мазка на возбудитель псевдотуберкулеза (Yersinia pseudotuberculosis), Микробиологическое (культуральное) исследование фекалий/ ректального мазка на патогенные кампилобактерии (Campylobacter jejuni/coli)). Определение антител к возбудителям стронгиллоидоза (Strongyloides stercoralis), Молекулярно-биологическое исследование фекалий на возбудителя стронгиллоидоза (Strongyloides stercoralis), Определение ДНК возбудителя стронгиллоидоза (Strongyloidesstercoralis) в фекалиях методом ПЦР Проводится 3-кратное бактериологическое исследование кала на кишечную группу, в том числе на кампилобактер, а также серологическое исследование крови для определения уровня антител к кишечным инфекциям. При наличии антител в невысоком титре исследование проводят повторно, при кишечной инфекции титр антител нарастает. В настоящее время расширяются возможности ПЦР-диагностики кишечных инфекций, что также следует использовать [5].
Детям с подозрением на БК при необходимости проведения дифференциальной диагностики с язвенным колитом рекомендовано исследование в крови иммунологических маркеров ВЗК: ASCA (Определение антител класса G (IgG) в крови к Sacchаromyces cerevisiae (ASCA)) и ANCA (Определение маркеров ANCA-ассоциированных васкулитов: PR3 (c-ANCA), МПО (p-ANCA)[20,21].
Детям с подозрением на БК при необходимости проведения дифференциальной диагностики с язвенным колитом рекомендовано исследование в крови иммунологических маркеров ВЗК: ASCA (Определение антител класса G (IgG) в крови к Sacchаromyces cerevisiae (ASCA)) и ANCA (Определение маркеров ANCA-ассоциированных васкулитов: PR3 (c-ANCA), МПО (p-ANCA)[20,21].
(УУР - С УДД - 3)
Комментарии: Наличие ASCA (антитела к Saccharomyces cerevisiae) - в пользу диагноза болезнь Крона и является маркером неблагоприятного фенотипа.
Комментарии: Наличие ASCA (антитела к Saccharomyces cerevisiae) - в пользу диагноза болезнь Крона и является маркером неблагоприятного фенотипа.
Отсутствие ASCA не исключает диагноз, т.к. положительны они лишь у 20% пациентов. В Номенклатуре медицинских услуг (Приказ Министерства здравоохранения РФ от 13 октября 2017 г. N 804н) услуга Определение антител класса G (IgG) в крови к Sacchаromyces cerevisiae (ASCA) отсутствует.
Рекомендовано проведение исследования биоптатов кишки на цитомегаловирус при остром стероидрезистентном колите с целью подтверждения/исключения колита цитомегаловирусной этиологии [21].
(УУР-С; УДД- 3)
Комментарии: предпочтительно в биоптате кишки, полученной при ректосигмоидоскопии (Определение ДНК цитомегаловируса (Cytomegalovirus) в биоптатах и пунктатах из очагов поражения органов и тканей методом ПЦР, качественное исследование, Определение ДНК цитомегаловируса (Cytomegalovirus) в биоптатах и пунктатах из очагов поражения органов и тканей методом ПЦР, количественное исследование).
При положительном результате теста требуется соответствующая терапия.
Всем детям при диагностике БК рекомендовано проведение диагностики гепатита В (Определение антигена (HbsAg) вируса гепатита В (Hepatitis В virus) в крови) с целью отбора пациентов для иммунизации против данной инфекции или назначения соответствующей терапии при выявлениии заболевания [21].
(УУР-С; УДД-3)
Рекомендовано перед началом анти-ФНО терапии и ежегодно на фоне лечения данными препаратами проведение исследования на туберкулез с целью выявления латентной туберкулезной инфекции и своевременного ее лечения (см. Приложение А3.1) [20].
(УУР-С; УДД-3)
Рекомендовано перед началом анти-ФНО терапии и ежегодно на фоне лечения данными препаратами проведение исследования на туберкулез с целью выявления латентной туберкулезной инфекции и своевременного ее лечения (см. Приложение А3.1) [20].
(УУР-С; УДД-3)
Комментарий: могут проводиться Внутрикожная проба с туберкулезным аллергеном и/или IGRA-тесты (Interferon-γ release assays) – иммунологические методы, основанные на стимуляции Т-лимфоцитов пептидными антигенами и выработке интерферона –γ, секретируемого клетками крови инфицированного M. tuberculosis человека (Исследование уровня интерферона-гамма на антигены Mycobacterium tuberculosis complex в крови).
Комментарий: могут проводиться Внутрикожная проба с туберкулезным аллергеном и/или IGRA-тесты (Interferon-γ release assays) – иммунологические методы, основанные на стимуляции Т-лимфоцитов пептидными антигенами и выработке интерферона –γ, секретируемого клетками крови инфицированного M. tuberculosis человека (Исследование уровня интерферона-гамма на антигены Mycobacterium tuberculosis complex в крови).
Следует относиться с осторожностью к результатам внутрикожных тестов, так как при воспалительных заболеваниях кишечника может быть анергия.
Кроме лабораторных исследований следует оценить данные анамнеза и клинической картины, а также рентгенографии органов грудной клетки.
Рекомендовано рассмотреть назначение исследования коагуляции Коагулограмма (ориентировочное исследование системы гемостаза) детям с подозрением на БК или с установленным диагнозом БК при подозрении на наличие изменений параметров гемостаза, в том числе, в комплексной оценке активности болезни с целью своевременной коррекции Matowicka-Karna J.
Markers of inflammation, activation of blood platelets and coagulationdisordersininflammatoryboweldiseases. PostepyHigMedDosw (Online). 2016 Apr 13;70:305-12.
(УУР - С УДД - 5)
Комментарии: возможно Определение тромбинового времени в крови, фибриногена, Определение международного нормализованного отношения (MHO), Определение концентрации Д-димера в крови и др.
(УУР - С УДД - 5)
Комментарии: возможно Определение тромбинового времени в крови, фибриногена, Определение международного нормализованного отношения (MHO), Определение концентрации Д-димера в крови и др.
Рекомендовано рассмотреть проведение Определения содержания антител к тканевой трансглютаминазе в крови (класса IgA) и Исследование уровня иммуноглобулина А в крови при необходимости проведения дифференциальной диагностики с целиакией [20,21,23].
(УУР - С УДД - 5)
(УУР - С УДД - 5)
Рекомендовано пациентам с БК регулярно проводить иссследование уровня витамина D (Исследование уровня 25-ОН витамина Д в крови) с целью определения возможного дефицита и проведении [21,24].
(УУР - С УДД - 3)
Комментарии: Исследование уровня 25-ОН витамина Д в крови следует проводить всем пациентам Исследование необходимо регулярно, в среднем, 1 раз в год.
(УУР - С УДД - 3)
Комментарии: Исследование уровня 25-ОН витамина Д в крови следует проводить всем пациентам Исследование необходимо регулярно, в среднем, 1 раз в год.
Рекомендовано пациентам с БК рассмотреть проведение иссследований уровней В12 (Определение уровня витамина В12 (цианокобаламин) в крови), Исследование уровня фолиевой кислоты в сыворотке крови, Исследование уровня цинка в крови А, Е при подозрении на витаминодефицитные состояния и/или дефицит цинка с целью своевременного выявления отклонений и назначения соответствующих препаратов для коррекции [20,21,23].
(УУР - С УДД - 5)
(УУР - С УДД - 5)
Комментарии: показания и частота исследований устанавливаются индивидуально, например: Исследование уровня 25-ОН витамина Д в крови следует проводить всем пациентам регулярно, цианокобаламин обязателен для контроля пациентам после терминальной резекции подвздошной кишки, цианокобаламина и фолиевой кислоты – при наличии макроцитарной анемии, цинка – пациентам с профузными диареями или высокими свищами.
Рекомендовано пациентам с БК с внутрибрюшными абсцессами проведение Микробиологического (культурального) исследования абсцессов на аэробные и факультативно-анаэробные микроорганизмы и Микробиологического исследования крови на аэробные и анаэробные/факультативно анаэробные микроорганизмы, а также на дрожжевые грибы (Микробиологическое (культуральное) исследование крови на стерильность, Микробиологическое (культуральное) исследование крови на дрожжевые грибы, микробиологическое (культуральное) исследование крови на облигатные анаэробные микроорганизмы), Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам с целью идентификации патогена, и коррекции стартовой антимикробной терапии[25].
(УУР - С УДД - 5)
Комментарий: В Номенклатуре услуг в настоящее время отсутствует услуга по Микробиологическому (культуральному) исследованию крови на аэробные и факультативно анаэробные микроорганизмы.
При необходимости может рассматриваться проведение экспресс-тестов для идентификации патогенов и их чувствительности к антимикробным препаратам.В случае развития септического состояния или подозрении на него ведение пациента осуществляется согласно ссответствующим рекомендациям
Инструментальные диагностические исследования
Эндоскопические методы исследования
Всем детям с подозрением на БК рекомендовано проводить: колоноскопию с илеоскопией (Колоноскопия, Видеоколоноскопия, Интестиноскопия) эзофагогастродуоденоскопию ступенчатую биопсию слизистой оболочки всех осмотренных отделов [20,21].
(УУР – C; УДД -5)
Комментарии: детям колоноскопия проводится под наркозом.
Инструментальные диагностические исследования
Эндоскопические методы исследования
Всем детям с подозрением на БК рекомендовано проводить: колоноскопию с илеоскопией (Колоноскопия, Видеоколоноскопия, Интестиноскопия) эзофагогастродуоденоскопию ступенчатую биопсию слизистой оболочки всех осмотренных отделов [20,21].
(УУР – C; УДД -5)
Комментарии: детям колоноскопия проводится под наркозом.
Данные исследования также проводятся в динамическом наблюдении – частота устанавливается индивидуально (в т.ч., при рецидивах, при подозрении на прогрессирование, при контроле после хирургического лечения)При подозрении на поражение тонкой кишки и невозможности достоверного подтверждения диагноза по данным колоноскопии (с исследованием терминального отдела тонкой кишки), КТ и МРТ, невозможности проведения видеока-псульного исследования рекомендовано рассмотреть проведение баллонной энтероскопии (Интестиноскопия двух баллонная) с биопсией (Биопсия тонкой кишки-эндоскопическая) с целью уточнения диагноза [26,27].
(УУР – В; УДД – 3)
(УУР – В; УДД – 3)
Методы визуализации
При подозрении на поражение тонкой кишки при БК рекомендовано проведение:МР-энтерографии (гидро-МРТ, (Магнитно-резонансная томография тонкой кишки; Магнитно-резонансной томографии тонкой кишки с контрастированием)) или КТ-энтерографии (гидро-КТ, (Компьютерная томография тонкой кишки с контрастированием)) с целью уточнения диагноза[21,28].
(УУР – С; УДД - 3)
Комментарии: МРТ может быть предпочтительна у детей в связи с отсутствием лучевой нагрузки, однако КТ больше подходит при неотложных состояниях.
При выборе исследования следует ориентироваться на состояние, возраст и возможности пациента, медицинской организации.
Наркоз проводится по показаниям.
Наркоз проводится по показаниям.
При невозможности проведения МРТ или КТ возможно рекомендовать рентгено-контрастное исследование тонкой кишки с бариевой взвесью (Рентгенография тонкой кишки с контрастированием) (после исключения признаков непроходимости) [20,21,29].
(УУР – С; УДД - 5)
(УУР – С; УДД - 5)
Детям с подозрением на ВЗК в качестве альтернативы МР-энтерографии (гидро-МРТ, (Магнитно-резонансная томография тонкой кишки, Магнитно-резонансная-томография тонкой кишки с контрастированием)), а также при отрицательном результате данного исследования, но при серьезном подозрении на БК рекомендуется рассмотреть проведение видео-капсульной эндоскопии(Тонкокишечная эндоскопия видео-капсульная, Толстокишечная эндоскопия видео-капсульная) c уточнения диагноза и оценки местного воспаления [20,21,30].
(УУР – С; УДД – 5)
(УУР – С; УДД – 5)
Комментарии:
Видео-капсульная эндоскопия (Тонкокишечная эндоскопия видео-капсульная, Толстокишечная эндоскопия видео-капсульная) более чувствительна по отношению квыявлению местных изменений слизистой оболочки по сравнению с МР-энтерографией (гидро-МРТ, (Магнитно-резонансная томография тонкой кишки, Магнитно-резонансная томография тонкой кишки с контрастированием) [30].
Ограничением к использованию Тонкокишечной эндоскопии видео-капсульной и Толсто кишечной эндоскопии видео-капсульной является невозможность взятия биоптата, однако малая инвазивность, отсутствие необходимости проведения наркоза позволяет применять данное исследование, в том числе, в процессе динамического наблюдения за пациентом.
При БК перед проведением видео-капсульной эндоскопии следует выполнить рентгенологические исследованиия (пассаж бария по кишечнику)[31-33]. (Рентгенография тонкой кишки с контрастированием, Рентгено контроль прохождения контрастного вещества по желудку, тонкой и ободочной кишке) или КТ-энтерография (Компьютерная томография тонкой кишки с контрастированием)) или МР-энтерографию (Магнитно-резонансная томография тонкой кишки, Магнитно-резонансная томография тонкой кишки с контрастированием) [34]. для исключения/подтверждения стриктур тонкой кишки при подозрении на данные состояни.
Тонкокишечная эндоскопия видео-капсульная проводится при подозрении на поражение тонкой кишки и при отсутствии стриктур [35]. Рекомендовано проведение ультразвукового исследования органов брюшной полости (Ультразвуковое исследование органов брюшной полости (комплексное)),забрюшинного пространства, малого таза (Ультразвуковое исследование органов малого таза (комплексное)), в том числе, с допплеровским анализом всем пациентам с целью выявления некоторых признаков и осложнений БК – утолщение стенки кишки, инфильтрат, абсцесс брюшной полости, наличие фистул, воспаление брюшины и др.[20,21].
(УУР – С, УДД - 3)
Комментарий: данный метод имеет ограниченные возможности в диагностике поражений кишечника. При этом процедура не инвазивна, что обусловливает ее широкое использование, особенно в детском возрасте.
(УУР – С, УДД - 3)
Комментарий: данный метод имеет ограниченные возможности в диагностике поражений кишечника. При этом процедура не инвазивна, что обусловливает ее широкое использование, особенно в детском возрасте.
При перианальных поражениях пациентам с БК рекомендовано проведение трансректального и/или трансперинеального ультразвукового или магнитно-резонансного исследования прямой кишки (Ультразвуковое исследование прямой кишки трансректальное, Магнитно-резонансная томография толстой кишки, Магнитно-резонансная томография толстой кишки с контрастированием) и Магнитно-резонансная томография органов малого таза с целью визуализации свищевых ходов и уточнения степени воспаления и протяженности поражения прямой кишки и анального канала[28,36].
(УУР – C, УДД - 4)
(УУР – C, УДД - 4)
Рекомендовано проведение Магнитно-резонансной томографии органов малоготаза (возможно с пероральным или внутривенным контрастированием)) детям сперианальными проявлениями БК в виде свищей прямой кишки при подозрении на них для диагностики фистул для подтверждения диагноза (в т.ч., определения локализации, протяженности свищевого хода и наличия отсутствия осложнений)[21,37].
(УУР – С; УДД - 5)
Комментарии: в случае невозможности проведения Магнитно-резонансной томографии органов малого таза с внутривенным контрастированием проводится КТ органов малого таза с контрастированием (Компьютерная томография органов малого таза у женщин с контрастированием, Компьютерная томография органов таза у мужчин с контрастированием) или фистулография (Фистулография свищей прямой кишки иперианальной области) или ультразвукового исследования ректальным датчиком.
(УУР – С; УДД - 5)
Комментарии: в случае невозможности проведения Магнитно-резонансной томографии органов малого таза с внутривенным контрастированием проводится КТ органов малого таза с контрастированием (Компьютерная томография органов малого таза у женщин с контрастированием, Компьютерная томография органов таза у мужчин с контрастированием) или фистулография (Фистулография свищей прямой кишки иперианальной области) или ультразвукового исследования ректальным датчиком.
Наркоз по показаниям.
Магнитно-резонансная холангиопанкреатография рекомендована детям с БК при наличии данных (предположений) о вовлечении в процесс печени и/или желчных протоков[20].
(УУР – С; УДД - 5)
(УУР – С; УДД - 5)
Пациентам при подозрении на осложнение БК - кишечную непроходимость или перфорацию кишечника - рекомендуется обзорная рентгенография брюшной полости для подтверждения данного состояния. [20,38].
(УУР – С, УДД - 3)
(УУР – С, УДД - 3)
Рекомендовано проведение рентгено-денситометрии детям с БК с целью оценки состояния костной ткани, своевременной диагностики остеопороза, оценки необходимости и терапии [39].
(УДД 5, УУР С)
Комментарии: снижение плотности костей отмечено у 30% детей с ВЗК.
(УДД 5, УУР С)
Комментарии: снижение плотности костей отмечено у 30% детей с ВЗК.
Частота проведения исследования определяется индивидуально согласно клиническим рекомендациям по остеопорозу и снижении минеральной плотности костной ткани[40-42].
Другие диагностические исследования
Патолого-анатомическое исследование (гистологическое исследование)
Патолого-анатомическое исследование взятых в ходе эндоскопического исследования биоптатов и резецированных участков кишечника рекомендуется для диагностики болезни Крона и оценки эффективности лечения [43,44].
Рекомендуется взять не менее 2 биоптатов из подвздошной кишки и, по меньшей мере, из 5 участков толстой кишки, включая прямую кишку. При верификации диагноза БК у пациентов с симптомами фульминантного колита рекомендуется взять не менее 2 биоптатов из одного отдела толстой кишки с целью постановки диагноза [43,44].
(УУР – С, УДД - 5)
Комментарии:
(УУР – С, УДД - 5)
Комментарии:
1.К признакам хронического воспаления относятся: базальный плазмоцитоз, нарушение архитектоники желез (крипт), пилорическая метаплазия в подвздошной кишке, не казеозные не криптолитические гранулемы. Отсутствие последних не исключает болезнь Крона. К признакам активного воспаления относятся: криптиты, крипт- абсцессы, эрозии и язвы.
2. Для болезни Крона характерны сегментарность поражения, фокальный и трансмуралный характер воспаления, хроническое активное воспаление в тонкой кишке и верхних отделах пищеварительного тракта.
3. Патолого-анатомический (гистологический) протокол должен содержать вывод о наличии воспалительного заболевания кишечника и заключение о том, что наиболее вероятным диагнозом является болезнь Крона.
Консультации специалистов
Рекомендовано при диагностике и ведении детей с БК применять мульти-дисциплинарный подход с привлечением необходимых специалистов на всех этапах диагностики и лечения с целью обеспечения адекватной диагностики, мониторинга и терапии [21].
(УУР – С; УДД - 5)
Комментарии: диагностику и ведение пациентов осуществляет врач-гастроэнтеролог (или врач-педиатр с соответствующей подготовкой), проводятся консультации, при необходимости, врача-диетолога, врача-детского хирурга, врача-клинического фармаколога, врача-детского гематолога, врача-детского онколога, врача- дермато-венеролога, врача-аллерголога-иммунолога, врача-детского эндокринолога, врача по лечебной физкультуре, медицинского психолога и др.
Дифференциальный диагноз
Дифференциальная диагностика
Дифференциальную диагностику проводят с рядом заболеваний. К ним относят: язвенный колит (табл. 4), острые кишечные инфекции (дизентерия, сальмонеллез, кампило-бактериоз, иерсиниоз, амебиаз, паразитозы), C.difficile-ассоциированную диарею, цитомегало-вирусный колит, туберкулез кишечника, системные васкулиты, неоплазии толстой и тонкой кишки, болезнь Бехчета, аппендицит, синдром раздраженного кишечника, целиакию, первичные иммуно-дефицитные состояния и др (табл. 5). [20,21]. Для исключения/подтверждения данных заболеваний/состояний проводится обследование согласно соответствующим клиническим рекомендациям Болезнь Крона часто приходится дифференцировать с язвенным колитом. Признаки данных заболеваний представлены в таблицах 4 и 5.
Таблица 4. Признаки болезни Крона и язвенного колита у детей [43,45].
|
Признаки
|
Болезнь Крона
|
Язвенный колит
|
|
Пол
|
мальчики = девочки
|
мальчики = девочки
|
|
Симптомы и признаки
|
Боль в животе, диарея, потеря массы тела, анорексия, задержка роста
|
Диарея с кровью в стуле, боль в животе
|
|
Диарея
|
Стул редко наблюдается, чаще чем 4-6 раз, кашицеобразный преимущественно в дневное время
|
Стул частый, жидкий, нередко с ночными дефекациями
|
|
Боли в животе
|
Типичны, чаще неинтенсивные
|
Только в период обострения, интенсивные перед дефекацией, после опорожнения стихают
|
|
Возраст начала болезни
|
до 7-10 лет - очень редко
|
Любой
|
|
Характер начала болезни
|
Острое - крайне редко, постепенное в течении нескольких лет О
|
Острое у 5-7% больных, у остальных постепенное (3-6 мес.)
|
|
Кровотечения
|
Редко, чаще - при вовлечении в процесс дистальных отделов толстой кишки
|
В период обострения – постоянные
|
|
Запор
|
Более типичен
|
Редко
|
|
Пальпация области живота
|
Инфильтраты и конгломераты кишечных петель, чаще в правой подвздошной зоне
|
Спазмированная, болезненна толстая кишка
|
|
Локализация процесса
|
Весь желудочно-кишечный тракт (от ротовой полости до ануса) вовлечение всех слоев кишечной стенки, наиболее часто поражается илеоцекальный отдел
|
Толстая кишка, поражается только слизистая оболочка, наиболее часто поражение на всем протяжении толстой кишки
|
|
Признаки
|
Болезнь Крона
|
Язвенный колит
|
|
Эндоскопическая картина
|
Сегментарность поражения, афтозные язвы, глубокие щелевидные язвы, «булыжная мостовая», перианальные осложнения (хронические анальные трещины (язвы), парапроктит, свищи прямой кишки, стриктуры)
|
Диффузная и непрерывная эритема, рыхлость, зернистость, потеря сосудистого рисунка прямой кишки в различной степени
|
|
Патологоанатомическая картина (гистология)
|
Хотя бы одна неказеозная гранулема в любом отделе ЖКТ (отсутствие гранулем не исключает БК); фокальное нарушение архитектоники; фокальное воспаление; фокальные криптиты; трансмуральное воспаление во отсутствие тяжелого колита; пилорическая метаплазия; активное воспаление в подвздошной кишке (при слабо выраженном воспалении в слепой кишке; в проксимальных отделах толстой кишки воспаление более выражено, чем в идстальных; наличие невоспаленных участков между очагами воспаления (у не леченных больных и, исключая скачкообразное поражение слепой кишки при левостороннем язвенном колите)
|
Отсутствие гранулем; диффузное нарушение архитектоники; диффузное воспаление; в дистальных отделах воспаление более выражено, чем в проксимальных; диффузные криптиты; отсутствие скачкообразного поражения (м.б. скачкообразное поражение слепой кишки при левостороннем колите); крипт-абсцессы; уменьшение слизи и бокаловидных клеток; метаплазия клеток Панета в левых отделах;
|
|
Рентенологические признаки
|
Ригидные стенозированные сегменты, сегментарные поражения, свищи
|
Дилатация толстой кишки, токсический мегаколон
|
|
Перфорации
|
Более типичны прикрытые
|
При токсической дилатации в свободную брюшную полость, протекают мало симптомно
|
|
Ремиссия
|
Отмечаются улучшения, абсолютной ремиссии нет, структура кишечника не восстанавливается
|
Характерна, возможно длительное отсутствие обострений с обратным развитием структурных изменения в кишечнике
|
Таблица 5. Воспалительные заболевания кишечника: дифференциальная диагностика у детей [20].
|
Симптомы
|
Внекишечные проявления
|
Дифференциальный диагноз
|
|
-Лихорадка
- Слабость - Бледность кожи и слизистых оболочек - Жидкий стул - Скрытая/видимая кровь в стуле - Диарея с кровью в стуле - Боль в животе - Болезненность при пальпации живота - Напряжением мышц живота при - пальнации (особенно в правой подвздошной области) - Тенезмы - Задержка развития |
- Нарушение/задержка роста
- Афтозный стоматит - Колцевидная эритема - Склерит, эписклерит - Артрит, артропатия - склерозирующий холангит - Камни в желчном пузыре - Аутоиммунный гепатит -Тромбоэмболия вен - Нефролитиаз - Панкреатит |
- Мальабсорбция углеводов
- Инфекционный колит, энтероколит - Аллергия к белкам коровьего молока - Целиакия - Геморрагический васкулит Аппендицит - Анальные трещины - Полипы кишечника - Геморрой - Инвагинация - Дивертикул Меккеля |
|
Перианальные фистулы, трещины, абсцессы
|
|
- Иммунодефициты
- Функциональные нарушения органов желудочно-кишечного тракта - Туберкулез кишечника - Неблагоприятные реакции на лекарственные средства |
Первичные иммуно-дефицитные состояния чаще всего дебютируют у детей младше 2 лет, следует обратить внимание на следующие признаки:
- Семейный анамнез первичного иммунодефицита;
- Родители или >2 кровных родственников в семье с ранним началом ВЗК;
- «Младенческий» (<2 лет) ВЗК;
- Тяжелое, рефрактерное к лечению ВЗК, в особенности с перианальным/ректовагинальным вовлечением/абсцессами;
- Рецидивирующие инфекции (легочные инфекции, кожные абсцессы) при отсутствии иммуно-супрессивной терапии;
- Нейтропения, тромбоцитопения, абнормальный иммунный статус (уровень Ig) при отсутствии иммуно-супрессивной терапии;
- Дистрофия ногтей и заболевания волос (trichorrhexis nodosa);
- Заболевания кожи (врожденная экзема, альбинизм) [46].
- Семейный анамнез первичного иммунодефицита;
- Родители или >2 кровных родственников в семье с ранним началом ВЗК;
- «Младенческий» (<2 лет) ВЗК;
- Тяжелое, рефрактерное к лечению ВЗК, в особенности с перианальным/ректовагинальным вовлечением/абсцессами;
- Рецидивирующие инфекции (легочные инфекции, кожные абсцессы) при отсутствии иммуно-супрессивной терапии;
- Нейтропения, тромбоцитопения, абнормальный иммунный статус (уровень Ig) при отсутствии иммуно-супрессивной терапии;
- Дистрофия ногтей и заболевания волос (trichorrhexis nodosa);
- Заболевания кожи (врожденная экзема, альбинизм) [46].
Лечение
ГЛАВА 3. ЛЕЧЕНИЕ
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Выбор терапии должен проводиться с учетом факторов риска неблагоприятного течения БК. По мнению экспертов ESPGHAN [10], это: глубокое язвенное поражение толстой кишки при эндоскопическом исследовании сохраняющееся тяжелое течение заболевания, несмотря на адекватную индукционную терапию распространенное поражение (тотальное поражение тонкой кишки) значительное замедление линейного роста (показатель отклонения роста Z> -2,5) тяжелый остеопороз стенозирующее и (или) пенетрирующее течение на момент дебюта заболевания (течение заболевания B2 и/или B3) тяжелое поражение перианальной области.
Наличие даже одного из этих факторов позволяет предположить неблагоприятный исход заболевания, что должно послужить основанием для оптимизации проводимой терапии и применения препаратов, которые, как было установлено, изменяют естественное течение заболевания, таких как (аналоги пурина) (тиопурины), #метотрексат** и ингибиторы фактора некроза опухоли альфа (биологические препараты), а при осложнениях -соответствующей операции.
Выбор терапии БК должен проводиться в соответствии с ее локализацией, распространенностью и тяжестью (табл.7). Недостаточная эффективность индукционной терапии требует интенсификации лечении. По достижении ремиссии проводится дальнейшая поддерживающая терапия.
Консервативная терапия
Индукция ремиссии
Потенциальное влияние БК на рост, половое и эмоциональное развитие пациентов подчеркивает необходимость специфического подхода к лечению в детском возрасте.
Целью терапии является не только ослабление симптомов, но также обеспечение физического развития в соответствии с возрастом и удовлетворительного качества жизни [47].
Полное энтеральное питание (ПЭП) в течение 6-8 недель рекомендуется в качестве терапии первой линии для индукции ремиссии у детей с вновь установленным диагнозом БК (за исключением тяжелого панколита, оральной или изолированной перианальной БК) или обострением воспалительной формы БК [20,48].
(УУР – С; УДД - 3)
(УУР – С; УДД - 3)
Энтеральное питание осуществляется с помощью жидких полимерных смесей, которые лучше переносятся, имеют лучшие органолептические свойства и низкую стоимость. В ряде исследований показано преимущество специализированных смесей, обогащенных противовоспалительным компонентом – трансформирующим фактором роста бета-2 (TGF β2). ПЭП рекомендуется на срок не менее 8 недель. Если клинический ответ при использовании ПЭП в течение первых 2 недель отсутствует, следует решить вопрос о применении альтернативных методов лечения. Решение о применении ПЭП или альтернативных методов лечения следует принимать индивидуально с учетом качества жизни пациента
Доказательная база в отношении перехода к обычному питанию после завершения применения ПЭП отсутствует. Эксперты ESPGHAN предлагают постепенное введение обычной пищи одновременно с уменьшением объема питательной смеси каждые 2-3 дня в течение 2-3 недель[49,50,51]
Доказательная база в отношении перехода к обычному питанию после завершения применения ПЭП отсутствует. Эксперты ESPGHAN предлагают постепенное введение обычной пищи одновременно с уменьшением объема питательной смеси каждые 2-3 дня в течение 2-3 недель[49,50,51]
Частичное энтеральное питание не рекомендовано при обострении БК или для индукции ремиссии, но оно способствует пролонгированию достигнутой ремиссии на фоне специализированной диеты [56].
(УУР – С; УДД - 5)
(УУР – С; УДД - 5)
Рекомендовано при болезни Крона назначать специализированную диету с исключением продуктов и блюд, предположительно способных нарушать кишечную микробиоту, повышать проницаемость кишечного барьера и вызывать хроническое воспаление (глютен, животные жиры, мясные продукты промышленного производства, эмульгаторы, консерванты и др.) с целью предотвращения негативного воздействия питания на состояние кишечника [52].
(УУР –А; УДД - 2)
(УУР –А; УДД - 2)
Эффективность глюкокортикоидов для местного применения и кортикостероидов системного действия
В исследованиях использовалась схема снижения дозы глюкокортико-стероидов продолжительностью от восьми до 12 недель. В клинической практике начало применения и снижение дозы глюкокортико-стероидов не стандартизировано и осуществляется на основании опыта врача. Однократный прием суточной дозы в утреннее время уменьшает потенциальное негативное влияние препаратов, связанное с замедлением роста[57]. Внутривенное введение глюкокортико-идов применяется только для лечения тяжелого обострения заболевания.
В исследованиях использовалась схема снижения дозы глюкокортико-стероидов продолжительностью от восьми до 12 недель. В клинической практике начало применения и снижение дозы глюкокортико-стероидов не стандартизировано и осуществляется на основании опыта врача. Однократный прием суточной дозы в утреннее время уменьшает потенциальное негативное влияние препаратов, связанное с замедлением роста[57]. Внутривенное введение глюкокортико-идов применяется только для лечения тяжелого обострения заболевания.
У пациентов с легкой или среднетяжелой формой БК с локализацией патологического процесса в подвздошной кишке или восходящей ободочной кишке применение будесонида предпочтительно [54,55,58].
Поддержание ремиссии с использованием глюкокортико-идов не рекомендуется, а в случае развития стероидо зависимости обязателен переход на другую терапию (аналоги пурина (тиопурины) или метотрексат, биологическая терапия).
Кортикостероиды системного действия рекомендуются для индукции ремиссии у детей со среднетяжелым и тяжелым обострением воспалительной формы БК при повторном обострении, а также при первой атаке, если применение ПЭП невозможно [20,21,48].
(УУР – С, УДД - 3)
(УУР – С, УДД - 3)
Рекомендуемая доза преднизолона (или аналогичного препарата) для приема внутрь при обострении БК для большинства пациентов детского возраста составляет 1 мг/кг (максимальная доза 40 мг/сутки) однократно в сутки утром. При недостаточном эффекте может потребоваться увеличение дозы до 1,5 мг/кг (максимальная доза 60 мг/сутки). При отсутствии эффекта от перорального применения кортикостероидов системного действия у некоторых пациентов может быть эффективным внутривенное введение кортикостероидов системного действия применения. Рекомендуется назначение первоначальной дозы в течение 2 недель с последующим постепенным снижением и отменой не позднее 12 недель.
Схема снижения дозы преднизолона приведена в таблице 5.
Таблица 5. Схема снижения дозы преднизолона при проведении индукционной терапии БК у детей (в соответствии с рекомендациями [7,10].
|
|
Масса тела
|
|
|
|
Неделя
|
10-20 кг
|
20–30 кг
|
> 30 кг
|
|
1-3
|
20 мг
|
30 мг
|
40 мг
|
|
4
|
15 мг
|
25 мг
|
35 мг
|
|
5
|
15 мг
|
20 мг
|
30 мг
|
|
6
|
12.5 мг
|
15 мг
|
25 мг
|
|
7
|
10 мг
|
15 мг
|
20 мг
|
|
8
|
7.5 мг
|
10 мг
|
15 мг
|
|
9
|
5 мг
|
10 мг
|
10 мг
|
|
10
|
2,5 мг
|
5 мг
|
5 мг
|
У детей с легким и среднетяжелым поражением илеоцекальной области при болезни Крона в качестве альтернативы кортикостероидам системного действия для индукции ремиссии рекомендовано использование будесонида (капсулы кишечнорастворимые) [20,21,59].
(УУР – С, УДД - 3)
(УУР – С, УДД - 3)
Начальная доза будесонида – 9 мг, препарат в дозе до 12 мг используется у детей в течение первых 4-х недель для индукции ремиссии.
Постепенное уменьшение дозы будесонида можно проводить в течение 10-12 недель.
Не рекомендовано использовать детям глюкокортико-стероиды (Кортикостероиды системного действия и глюкокортико-стероиды для местного применения ) в качестве поддерживающей терапии [20,48].
На фоне лечение глюкокортико-идами (кортикостероидами системного действия и глюкокортико-стероидами для местного применения), а также при дефицитных состояниях рекомендуется назначение препаратов кальция ( для детей с 2-х летнего возраста),а так же препараты кальция карбоната в комбинации с кальция лактоглюко-натом (для детей с 3-х летнего возраста) и с Колекальци-феролом** (для детей начиная с раннего возраста препарат применяют в виде порошка для приготовления суспензии для приема внутрь) и витамина D [60].
(УУР – С; УДД – 5)
(УУР – С; УДД – 5)
Комментарии: в практике удобнее применять комбинированные препараты (например, Кальция карбонат+Колекальциферол)
Рекомендуется использовать антибактериальные препараты системного действия, такие как метрони-дазолципрофлоксацин, для лечения пациентам с БК с формированием свищей в перианальной области только в комплексе с анти-ФНО терапией при необходимости регуляции микробной колонизации [48].
Рекомендуется использовать антибактериальные препараты системного действия, такие как метрони-дазолципрофлоксацин, для лечения пациентам с БК с формированием свищей в перианальной области только в комплексе с анти-ФНО терапией при необходимости регуляции микробной колонизации [48].
(УУР – С, УДД - 5)
Комментарии:
1. Стандартная суточная доза метронидазола составляет 30 мг/кг, а ципрофлоксацина – 20 мг/кг, возможно использование рифаксимина [61].
Длительность терапии не менее 8 недель.
2. При отсутствии эффекта при комбинированной терапии следует пересмотреть дозуингибиторов фактора некроза опухоли альфа (повысить дозу инфликсимаба ( поинструкции - с 6 лет)).
3. Применение #ципрофлоксацина ограничено у детей, согласно инструкции (с 18 летза исключением терапии синегнойной инфекции у детей с муковисцидозом и лечения сибирской язвы).В показаниях к препарату метронидазол, отсутствуют ВЗК. В связи с этим применение препарата в педиатрической популяции при болезни Крона возможно только по решению врачебной комиссии медицинской организации, с одобрения Локального этического комитета медицинской организации (при его наличии), при получении информированного согласия родителей/законных представителей и ребенка в возрасте старше 15 лет.
2. При отсутствии эффекта при комбинированной терапии следует пересмотреть дозуингибиторов фактора некроза опухоли альфа (повысить дозу инфликсимаба ( поинструкции - с 6 лет)).
3. Применение #ципрофлоксацина ограничено у детей, согласно инструкции (с 18 летза исключением терапии синегнойной инфекции у детей с муковисцидозом и лечения сибирской язвы).В показаниях к препарату метронидазол, отсутствуют ВЗК. В связи с этим применение препарата в педиатрической популяции при болезни Крона возможно только по решению врачебной комиссии медицинской организации, с одобрения Локального этического комитета медицинской организации (при его наличии), при получении информированного согласия родителей/законных представителей и ребенка в возрасте старше 15 лет.
Другие препараты могут быть рассмотрены в индивидуальном порядке по клинической ситуации. При более тяжелом течении заболевания, протекающего с формированием свищей, антибактериальные средства системного действия рекомендуется использовать в качестве дополнительной терапии, например, перед назначением иммуно-супрессивной терапии при невозможности ее начала в связи с необходимостью хирургического вмешательства [21].
(УУР – С, УДД - 3)
Комментарий: могут применяться метронидазол 30 мг/кг илиципрофлоксацин20 мг/кг
(УУР – С, УДД - 3)
Комментарий: могут применяться метронидазол 30 мг/кг илиципрофлоксацин20 мг/кг
Поддерживающая терапия
Эффективность азатиоприна и меркаптопурина.
В ретроспективных исследованиях серий случаев при использовании азатиоприна** наблюдался более длительный период поддержания ремиссии, более низкая частота госпитализаций, повторного назначения глюкокортико-идов системного действия и выполнения хирургических вмешательств[62,63].
Применение азатиопринав более высокой дозе 2,5 мг/кг/сутки было более эффективным по сравнению с более низкими дозами 1,0 или 2,0 мг/кг/сутки. [64,65].
Безопасность и побочные эффекты аналогов пурина (тиопуринов).
Побочные реакции при применении аналогов пурина (тиопуринов) были зарегистрированыу 15-46% пациентов [67,68,69]. В 8%–28% случаев они стали причиной снижения дозы препарата. Применение азатиоприна** более высокой дозе 3 мг/кг/сутки у детей, страдающих ВЗК, приводит к отмене препарата у 30% пациентов [66].
Токсичность, не зависящая от дозы препарата, обычно проявляется в течение первых недель после начала лечения. Панкреатит относится к наиболее частым проявлениям реакции гиперчувствительности и наблюдается у 3-4% пациентов. Другие нежелательные лекарственные реакции, не зависящие от дозы препарата, включают диспепсические расстройства (5-8%), лихорадку, гриппоподобные симптомы, миалгию, артралгию и сыпь (наблюдается ~ 9% пациентов). Замена препарата на меркаптопурин** может быть успешной примерно у 50% пациентов с непереносимостью азатиоприна**, в особенности при миалгии или артралгии, но также может быть эффективной в случае гепа-тотоксичности, симптомов со стороны желудочно-кишечного тракта, гриппоподобных проявлений и сыпи [68]. Результаты недавнего небольшого исследования серии случаев позволяют предположить, что попыткаприменения Меркаптопурина** может быть успешной и безопасной у некоторых пациентов с панкреатитом, индуцированным применением азатиоприна [70].
На основании долгосрочных наблюдений было установлено, что риск развития лимфомы у пациентов с ВЗК, получающих аналоги пурина (тиопурины), особенно у мужчин, увеличивается примерно в четыре раза, однако абсолютный риск у детей и подростков был меньшим [71,72]. Было рассчитано, что у детей риск составляет 4,5 случаев/10000пациенто-лет [73], он был задокументирован в детском регистре DEVELOP [74].
Следует избегать назначения аналогов пурина (тиопуринов) во время инфекции, вызванной вирусом Эпштейн-Барр [93].(ВЭБ), в связи с риском развития лимфом, ассоциированных с ВЭБ.
Следует избегать назначения аналогов пурина (тиопуринов) во время инфекции, вызванной вирусом Эпштейн-Барр [93].(ВЭБ), в связи с риском развития лимфом, ассоциированных с ВЭБ.
Аналоги пурина (тиопурины) (азатиопринили меркаптопурин) рекомендованыв качестве лечения для поддержания ремиссии у детей, получающих кортикостероиды системного действия и/или глюкокортикоиды для местного применения (будесонид капсулы кишечнорастворимые), а также детей из группы риска неблагоприятного исхода заболевания [20,21].843
(УУР – С; УДД - 3)
Комментарии:
Комментарии:
1. Аналоги пурина (тиопурины) эффективны в поддержании ремиссии БК, достигнутойна фоне кортикостероидов системного действия и/или глюкокортико-идов для местного применения. Для получения максимального эффекта от аналогов пурина (тиопуринов) может потребоваться от 8 до 14 недель, поэтому начинать терапию ими следует на фоне снижения дозы преднизолона.
2. У пациентов без нарушений метаболизма аналогов пурина (тиопуринов) рекомендуется применение азатиоприна в дозе 2,0-2,5 мг/кг или меркаптопуринав дозе 1,0-1,5 мг/кг в сутки.
3. Исследование активности тиопуринметил-трансферазы (ТПМТ) перед началом терапии аналогами пурина (тиопуринами) (норма 230-450 ед/мл) позволяет выявить пациентов с высоким риском миелосупрессии. Если проведение этого исследования невозможно, в начале лечения может быть назначена половинная доза аналоговпурина (тиопурина) с контролем общего анализа крови еженедельно в течение 2недель [53], если миелосупрессии не отмечается, рекомендуется постепенное увеличения дозы аналогов пурина (тиопурина) до полной. Снижение дозы аналогов пурина (тиопурина) в 2 раза рекомендуется при снижении лейкоцитов в крови ниже3000/мм, аналоги пурина (тиопурины) противопоказаны в редких случаях, когда абсолютное количество лейкоцитов снижается ниже 1500/мм.
4. В течение первого месяца после начала лечения обязателен контроль общего анализа крови и активности печеночных ферментов, первоначально – каждые 1-2недели с последующим уменьшением частоты; а в дальнейшем на протяжении всего лечения аналогами пурина (тиопуринами) необходим контроль этих показателей каждые 3 месяца у всех пациентов (независимо от активности ТПМТ).
6. Панкреатит может развиваться независимо от дозы в ранние сроки после начала применения аналогов пурина (тиопуринов), при его развитии обычно требуется отмена препарата. Необходимо уделить особое внимание дифференциальной диагностике истинной токсичности, связанной с применением аналогов пурина (тиопуринов), и внекишечными проявлениями ВЗК в форме панкреатита.
7. Решение о переводе с азатиоприна (AZA) на меркаптопурин (MP) и наоборот может быть принято у пациентов с гриппоподобным синдромом или острыми симптомами со стороны желудочно-кишечного тракта.
8. Увеличение активности трансаминаз более двух норм может носить транзиторный характер или потребовать снижения дозы препарата или его отмены. При повышении активности ТПМТ и уровня трансаминаз рекомендуется снижение дозы аналогов пурина (тиопурина) и назначение аллопуринола.844
2. У пациентов без нарушений метаболизма аналогов пурина (тиопуринов) рекомендуется применение азатиоприна в дозе 2,0-2,5 мг/кг или меркаптопуринав дозе 1,0-1,5 мг/кг в сутки.
3. Исследование активности тиопуринметил-трансферазы (ТПМТ) перед началом терапии аналогами пурина (тиопуринами) (норма 230-450 ед/мл) позволяет выявить пациентов с высоким риском миелосупрессии. Если проведение этого исследования невозможно, в начале лечения может быть назначена половинная доза аналоговпурина (тиопурина) с контролем общего анализа крови еженедельно в течение 2недель [53], если миелосупрессии не отмечается, рекомендуется постепенное увеличения дозы аналогов пурина (тиопурина) до полной. Снижение дозы аналогов пурина (тиопурина) в 2 раза рекомендуется при снижении лейкоцитов в крови ниже3000/мм, аналоги пурина (тиопурины) противопоказаны в редких случаях, когда абсолютное количество лейкоцитов снижается ниже 1500/мм.
4. В течение первого месяца после начала лечения обязателен контроль общего анализа крови и активности печеночных ферментов, первоначально – каждые 1-2недели с последующим уменьшением частоты; а в дальнейшем на протяжении всего лечения аналогами пурина (тиопуринами) необходим контроль этих показателей каждые 3 месяца у всех пациентов (независимо от активности ТПМТ).
6. Панкреатит может развиваться независимо от дозы в ранние сроки после начала применения аналогов пурина (тиопуринов), при его развитии обычно требуется отмена препарата. Необходимо уделить особое внимание дифференциальной диагностике истинной токсичности, связанной с применением аналогов пурина (тиопуринов), и внекишечными проявлениями ВЗК в форме панкреатита.
7. Решение о переводе с азатиоприна (AZA) на меркаптопурин (MP) и наоборот может быть принято у пациентов с гриппоподобным синдромом или острыми симптомами со стороны желудочно-кишечного тракта.
8. Увеличение активности трансаминаз более двух норм может носить транзиторный характер или потребовать снижения дозы препарата или его отмены. При повышении активности ТПМТ и уровня трансаминаз рекомендуется снижение дозы аналогов пурина (тиопурина) и назначение аллопуринола.844
9. При добавлении к лечению аллопуринола доза аналогов пурина (тиопурина) должна быть снижена до 25-33% от первоначальной дозы.
Стандартная доза аллопуринола для взрослых составляет 100 мг/сутки, доза аллопуринола для детей должна быть уменьшена (50-75 мг в зависимости от массы тела)[47].
10. Всем пациентам, которые применяют или ранее применяли аналоги пурина(тиопурины), рекомендуется избегать воздействия солнечных лучей в течение всей жизни, а также проходить регулярное дерматологическое обследование в связи с повышенным риском опухолей кожи.
10. Всем пациентам, которые применяют или ранее применяли аналоги пурина(тиопурины), рекомендуется избегать воздействия солнечных лучей в течение всей жизни, а также проходить регулярное дерматологическое обследование в связи с повышенным риском опухолей кожи.
Не рекомендуется применение у детей с БК аналогов пурина (тиопуринов) для индукции ремиссии БК [20,21,48,].
(УУР - С УДД - 5)
Рекомендовано рассмотреть возможность проведения Исследования активно ститиопуринметилтрансферазы (ТПМТ, TPMT) перед началом терапии аналогамипурина (тиопуринами) с целью выявления пациентов с высоким риском миелосупрессии (при доступности данного исследования) [20,21].
(УУР - С УДД -3)
Комментарий: исследование позволяет выявить пациентов с высоким риском миелосупрессии (норма 230-450 ед/мл). При отсуствии возможности определения поэтапное повышение дозы азатиоприна[5,14].
Рекомендовано рассмотреть пациентам с БК, получающим аналоги пурина(тиопурины) с субоптимальным ответом на терапию для выявления причин цитопении или повышенных «печеночных» ферментов, мониторинга жалоб и для оптимизации дозирования, определение уровней метаболитов (6-тиогуаниновыенуклеотиды [6-TGN] и 6-метилмеркаптопурин [6-MMP]) (при доступности данного исследования) [48].
Комментарий: исследование позволяет выявить пациентов с высоким риском миелосупрессии (норма 230-450 ед/мл). При отсуствии возможности определения поэтапное повышение дозы азатиоприна[5,14].
Рекомендовано рассмотреть пациентам с БК, получающим аналоги пурина(тиопурины) с субоптимальным ответом на терапию для выявления причин цитопении или повышенных «печеночных» ферментов, мониторинга жалоб и для оптимизации дозирования, определение уровней метаболитов (6-тиогуаниновыенуклеотиды [6-TGN] и 6-метилмеркаптопурин [6-MMP]) (при доступности данного исследования) [48].
(УУР - С УДД - 3)
Комментарии: Метотрексат рекомендуется в качестве одного из вариантов поддержания ремиссии у детей с высоким риском неблагоприятного исхода заболевания в качестве препарата первой линии для поддержания ремиссии или при неэффективности или непереносимости аналогов пурина (тиопуринов) [21].
Комментарии: Метотрексат рекомендуется в качестве одного из вариантов поддержания ремиссии у детей с высоким риском неблагоприятного исхода заболевания в качестве препарата первой линии для поддержания ремиссии или при неэффективности или непереносимости аналогов пурина (тиопуринов) [21].
Метотрексат следует назначать в дозе 15 мг/м 1 раз в неделю; максимальная доза –25 мг.
1. Если у пациента в течение нескольких месяцев наблюдается стойкая полная ремиссия с нормальными значениями маркеров воспаления, может быть предпринята попытка снижения дозы до 10 мг/м один раз в неделю (максимальная доза – 15 мг).
2. Метотрексат обычно назначается в виде подкожных инъекций, эффективность которых аналогична эффективности внутримышечных инъекций.
3. На фоне терапии метотрексатом рекомендуется прием внутрь фолиевой Кислоты(5 мг через 25-72 часа после введения метотрексата или 1 мг однократно в сутки 5 дней в неделю).
4. У пациентов со стойкой ремиссией необходим периодический контроль общего анализа крови и активности АЛТ.
1. Если у пациента в течение нескольких месяцев наблюдается стойкая полная ремиссия с нормальными значениями маркеров воспаления, может быть предпринята попытка снижения дозы до 10 мг/м один раз в неделю (максимальная доза – 15 мг).
2. Метотрексат обычно назначается в виде подкожных инъекций, эффективность которых аналогична эффективности внутримышечных инъекций.
3. На фоне терапии метотрексатом рекомендуется прием внутрь фолиевой Кислоты(5 мг через 25-72 часа после введения метотрексата или 1 мг однократно в сутки 5 дней в неделю).
4. У пациентов со стойкой ремиссией необходим периодический контроль общего анализа крови и активности АЛТ.
При плохой переносимости метотрексата (тошнота) следует ввести ондансетрон за час до инъекции в начале курса лечения.
Эффективность анти-ФНО терапии
Воспалительная форма заболевания. Эффективность инфликсимаба (по инструкции детям с 6 лет) для индукции и поддержания ремиссии у детей с БК доказана в нескольких РКИ. В рандомизированном исследовании REACH [75] дети в возрасте от 6 до 17 лет сактивной БК после предшествующего недостаточно эффективного лечения глюкокортико-стероидами и иммунодепрессантами получали инфликсимаб по схеме 0,2и 6 недель. В недавнем мета-анализе было установлено, что применение комбинированной терапии с использованием азатиопринадает лучшие клинические результаты, чем монотерапия инфликсимабом, даже в случае отсутствия эффекта от азатиоприна в анамнезе [88,89]. Прекращение комбинированной терапии является обоснованным только у пациентов, у которых была достигнута глубокая ремиссия (заживление слизистой оболочки). Тяжелые инфузионные реакции в виде гипоксии, гипотензии или затруднения дыхания являются противопоказанием для дальнейшего применения инфликсимаба [75,87,90].
Воспалительная форма заболевания. Эффективность инфликсимаба (по инструкции детям с 6 лет) для индукции и поддержания ремиссии у детей с БК доказана в нескольких РКИ. В рандомизированном исследовании REACH [75] дети в возрасте от 6 до 17 лет сактивной БК после предшествующего недостаточно эффективного лечения глюкокортико-стероидами и иммунодепрессантами получали инфликсимаб по схеме 0,2и 6 недель. В недавнем мета-анализе было установлено, что применение комбинированной терапии с использованием азатиопринадает лучшие клинические результаты, чем монотерапия инфликсимабом, даже в случае отсутствия эффекта от азатиоприна в анамнезе [88,89]. Прекращение комбинированной терапии является обоснованным только у пациентов, у которых была достигнута глубокая ремиссия (заживление слизистой оболочки). Тяжелые инфузионные реакции в виде гипоксии, гипотензии или затруднения дыхания являются противопоказанием для дальнейшего применения инфликсимаба [75,87,90].
Ингибиторы фактора некроза опухоли альфа (Анти-ФНО-инфликсимаб** или адалимумаб**) рекомендуются для индукции и поддержания ремиссии у детей с воспалительной формой БК в случае сохраняющейся активности, несмотря на предшествующую оптимизированную терапию иммуно-супрессорами [48].
УУР – С, УДД - 5)
Ингибиторы фактора некроза опухоли альфа (Анти-ФНО – инфликсимабили адалимумаб) рекомендуются для индукции ремиссии у детей с активной БК при гормоно-резистентности [48].
(УУР – С, УДД - 5)
(УУР – С, УДД - 5)
Ингибиторы фактора некроза опухоли (Анти-ФНО - (инфликсимаб или адалимумаб) рекомендуются в качестве препаратов первой линии для индукции и поддержания ремиссии активной болезни Крона у детей при наличии свищей в перианальной области (вместе с соответствующим хирургическим лечением)[20,21,48].Для индукции ремиссии инфликсимаб назначают в дозе 5 мг/кг, 3 дозы в течение 6 недель (недели 0-2-6) с последующей поддерживающей терапией с введением препарата в дозе 5 мг/кг каждые 8 недель. У пациентов, у которых наблюдается уменьшение эффективности препарата или при низкой концентрации препарата может потребоваться применение более высоких доз препарата до 10 мг/кг и/или сокращение продолжительности интервалов между введениями до 4-х недель. Уменьшение дозы инфликсимаба показано, если его остаточная концентрация превышает 8-10 мкг/мл.
Для индукции ремиссии адалимумаб детям с массой тела ˃40 кг назначают в дозе 2,4 мг/кг (максимальная доза 160 мг) на первую инъекцию, 1,2 мг/кг (максимальная доза 80 мг) через 2 недели, с последующим введением препарата в дозе 0,6 мг/кг (максимальная доза 40 мг) каждые 2 недели. У пациентов с массой тела до 40 кг: 80 мг на первую инъекцию, -40мг – через 2 недели, -20 мг – один раз в неделю. (40 мг для детей с массой тела ˃40 кг, 20 мг – для детей с массой тела ˂40 кг) Детям с массой тела ˃40 кг возможно назначения в такой ситуации дозы 80 мг один раз в 2 недели. Еженедельное введение показано при снижении эффективности и низкой остаточной концентрацией препарата 76. В случае отсутствия эффективности оптимизированной анти-ФНО терапии рекомендовано рассмотреть назначение устекинумаба или ведолизумаба [56].
(УУР – С; УДД – 5)
Применение препаратов Амино-салициловой кислоты и аналогичных препаратов в виде монотерапии рекомендуется только у отдельных пациентов с легким течением заболевания в связи с недостаточной эффективностью [21].
Доказательства того, что применение Амино-салициловой кислоты и на логичных препаратов (месалазин, сульфасалазин) индуцирует заживление слизистой оболочки, отсутствуют, и в связи с этим данные препараты должны рассматриваться в качестве вспомогательной терапии. Если Амино-салициловая кислота и аналогичные препараты используется в качестве единственного препарата для лечения легких форм при отсутствии глубоких язвенных дефектов, для подтверждения полной ремиссии необходим тщательный контроль таких показателей, как концентрация CРБ, СОЭ и концентрация фекального кальпротектина, а также должен быть установлен низкий порог для необходимости усиления терапии[48].
Показания к хирургическому лечению БК у детей
Показания к хирургическому лечению БК у детей
Рекомендовано показаниями к хирургическому лечению считать острые и хронические кишечные осложнения БК, а также неэффективность консервативной терапии с задержкой физического развития [56,77-80].
(УУР – С, УДД - 4)
(УУР – С, УДД - 4)
Хирургическое лечение рекомендовано рассмотреть у детей с БК в препубертатном и пубертатном возрасте, если есть задержка физического развития (с задержкой костного возраста за 6-12-месячный период) после оптимизации медикаментозной терапии и нутритивной поддержки [81].
Острые осложнения БК.
К ним относят кишечное кровотечение, перфорацию кишки и токсическую дилатацию ободочной кишки Хирургическое вмешательство по экстренным показаниям рекомендовано пациентам с БК, осложненной свободной перфорацией кишечника с перитонитом, а также при профузном кишечном кровотечении [81].
Хронические кишечные осложнения.
Хронические осложнения БК включают стриктуры кишки, внутрибрюшные инфильтраты и абсцессы, внутренние или наружные кишечные свищи, наличие дисплазии эпителия высокой степени - неоплазии [1,81,82].
Медицинская реабилитация
ГЛАВА 4. РЕАБИЛИТАЦИЯ
Реабилитация
Дети с болезнью Крона, как правило, нуждаются в социальной и психологической реабилитации [83]. В настоящее время нет доказательств достаточного уровня для выбора методики реабилитации при слабости и утомляемости, характерных для пациентов с БК [84].
Дети с болезнью Крона, как правило, нуждаются в социальной и психологической реабилитации [83]. В настоящее время нет доказательств достаточного уровня для выбора методики реабилитации при слабости и утомляемости, характерных для пациентов с БК [84].
Болезнь Крона в детском возрасте противопоказана для санаторно-курортного лечения.
Профилактика
ГЛАВА 5. ПРОФИЛАКТИКА И ДИСПАНСЕРНОЕ НАБЛЮДЕНИЕ
Профилактика
Профилактика заболевания не существует. Рекомендовано всем пациентам с БК перед началом терапии оценить статус иммунизации и, при наличии возможности, провести вакцинацию до старта иммуносупрессивной терапии с целью формирования защитного титра антител к вакцино управляемым инфекциям [85]. Пациентам с ВЗК рекомендовано проведение вакцинации согласно национальному календарю профилактических прививок [86]. Пациентам на фоне иммуно-супрессивной терапии противопоказаны живые аттенуированные вакцины[85]. Временным противопоказанием к проведению вакцинации является применение высоких доз ртикостероидной терапии.
Диспансерное наблюдение
В среднем, каждые 3 месяца - осмотр врачом-гастроэнтерологом (или врачом-педиатром с соответствующей специализацией) с полным объективным исследованием, включая перианальную область, оценка физического и полового развития, общий (клинический) анализ крови развернутый, исследование уровня СРБ, определение уровня фекального кальпротектина.
Диспансерное наблюдение
В среднем, каждые 3 месяца - осмотр врачом-гастроэнтерологом (или врачом-педиатром с соответствующей специализацией) с полным объективным исследованием, включая перианальную область, оценка физического и полового развития, общий (клинический) анализ крови развернутый, исследование уровня СРБ, определение уровня фекального кальпротектина.
Рутинное (ежегодное) эндоскопическое исследование при отсутствии клинических показаний (сомнений в диагнозе, необходимости исключения сопутствующих состояний, нарастания клинических проявлений, подозрений на осложнения, необходимости контроля после оперативного лечения) в большинстве случаев не проводится. При ухудшении состояния, нарастании уровня маркеров воспаления (С-реактивного белка, фекального кальпротектина) следует выполнять (илео) колоноскопию для оценки активности заболевания. Необходимо полное обследование, включая эндоскопическое, патологоанатомическое (гистологическое), лабораторное, при переходе подростка с БК во взрослую сеть для дальнейшего наблюдения
Примеры формулировки диагноза
Болезнь Крона: илеоколит с поражением терминального отдела подвздошной кишки, слепой и восходящей ободочной кишки (L3), пенетрирующая форма осложненная инфильтратом брюшной полости, наружным кишечным свищом иперианальными поражениями (передняя и задняя анальные трещины) (В3р), среднетяжелая атака, хроническое рецидивирующее течение, без нарушения роста(G0).
Примеры формулировки диагноза
Болезнь Крона: илеоколит с поражением терминального отдела подвздошной кишки, слепой и восходящей ободочной кишки (L3), пенетрирующая форма осложненная инфильтратом брюшной полости, наружным кишечным свищом иперианальными поражениями (передняя и задняя анальные трещины) (В3р), среднетяжелая атака, хроническое рецидивирующее течение, без нарушения роста(G0).
Болезнь Крона: терминальный илеит (L1), стенозирующая форма (стриктура терминального отдела подвздошной кишки без нарушения кишечной проходимости) (В2), хроническое рецидивирующее течение, ремиссия, без нарушения роста (G0).
Болезнь Крона: колит с поражением восходящей ободочной, сигмовидной и прямой кишки (L2), воспалительная форма (В1р), хроническое непрерывное течение, тяжелая атака. Перианальные проявления в виде анальной трещины. Гормональная зависимость, без нарушения роста (G0).
Болезнь Крона: колит с поражением прямой, сигмовидной и нисходящей ободочной кишки (L2), хроническое рецидивирующее течение, минимальной активности, осложненный стриктурой сигмовидной кишки с супрастеностическим расширением(В2), без нарушения роста (G0).
Информация
Источники и литература
-
Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2020
- Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2020 - 1. Franke A. Genome-wide meta-analysis increases to 71 the number of confermed Crohn’s disease susceptibility loci – Nature genet., 2010, v.42, p.1118-1125. 2. Maloy K.J., Powrie F. Intestinal homeostasis and its breakdown in inflammatory bowel disease – Nature insight, 2011, v.474, No7351, p.298-306. 3. Strober W., Fuss I., Mannon P. The fundamental basis of inflammatory bowel disease – J. Clin. Investigation, 2007, v.117 (3), p.514-521. 4. Langholz E., Munkholm P., Krasilnikoff P.A. Inflammatory bowel disease with onset in childhood. Clinical features, morbidity and mortality in a regional cohort. – Scand.J. Gastroenterol., 1997, v.32, p.139-147. 5. Корниенко, Е.А. Воспалительные заболевания кишечника у детей / Е.А. Корниенко // М.: Прима Принт. - 2019. - 228 с.: ил. - ISBN 978-5-60442241-1-3. 6. Benchimol EI, Fortinsky KJ, Gozdyra P, Van den Heuvel M, Van Limbergen J, Griffiths AM. Epidemiology of pediatric inflammatory bowel disease: a systematic review of international trends. Inflamm Bowel Dis. 2011;17(1):423-39.850 7. Patrick F van Rheenen, Marina Aloi, Amit Assa et al. The Medical Management of Paediatric Crohn’s Disease: an ECCO-ESPGHAN Guideline Update, Journal of Crohn"s and Colitis, 2020;, jjaa161, https://doi.org/10.1093/ecco-jcc/jjaa161. 8. Bernstein C., et al. WHO global guidelines on Inflammatory Bowel Disease – Guidelines for the Diagnosis and Management of IBD in 2010. Inflamm Bowel Dis. 2010 Jan; 16:112– 124. doi:10.1002/ibd.21048. 9. Van Limbergen J, Russell RK, Drummond HE, Aldhous MC, Round NK, Nimmo ER, et al. Definition of phenotypic characteristics of childhood-onset inflammatory bowel disease. Gastroenterology 2008; 135(4):1114-22. 10. Vernier-Massouille G, Balde M, Salleron J, Turck D, Dupas JL, Mouterde O, et al. Natural history of pediatric Crohn"s disease: a population-based cohort study. Gastroenterology 2008; 135(4): 1106-13. 11. Pigneur B, Seksik P, Viola S, Viala J, Beaugerie L, Girardet JP, et al. Natural history of Crohn"s disease: comparison between childhood- and adult-onset disease. Inflamm BowelDis 2010; 16(6):953-61. 12. Horsthuis K., Bipat S., Bennink R.J., Stoker J. Inflammatory bowel disease diagnosed with US, MR, scintigraphy, and CT: metaanalysis of prospective studies. Radiology. - 2008;247(1):64-79. 13. Чашкова Е.Ю., Владимирова А.А., Неустроев В.Г. и соавт. Воспалительные заболевания толстой кишки - аспекты диагностики. Бюллетень Восточно-Сибирского научного центра СО РАМН. - 2011. - № 4-2. - с.209-221. 14. Levine A., Koletzko S., Turner D., et al. ESPGHAN revised Porto criteria for the diagnosisof inflammatory bowel disease in children and adolescents – J.Pediatric Gasroenterol Nutr., 2014, v.58 (6), p.795-806.8,17] 15. Kammermeier J, Morris MA, Garrick V, et al. Management of Crohn’s disease. Arch Dis Child. 2016; 101:475–480. doi:10.1136/archdischild-2014-307217. 16. Turner D, Griffiths AM, Walters TD, Seah T, Markowitz J, Pfefferkorn M, Keljo D, Waxman J, Otley A, LeLeiko NS, Mack D, Hyams J, Levine A. Mathematical weighting of the pediatric Crohn"s disease activity index (PCDAI) and comparison with its other short versions. Inflamm Bowel Dis. 2012 Jan;18(1):55-62 17. Ивашкин В.Т., Шелыгин Ю.А., Абдулганиева Д.И. и соавт. Клинические рекомендации по диагностике и лечению болезни Крона у взрослых (проект). Колопроктология. 2020;19(2):8-38. https://doi.org/10.33878/2073-7556-2020-19-2-8-38.Horsthuis K., Bipat S., 18. Bennink R.J., Stoker J. Inflammatory bowel disease diagnosed withUS, MR, scintigraphy, and CT: metaanalysis of prospective studies. Radiology. -2008;247(1):64-79. 19. Waugh N, Cummins E, Royle P, Kandala NB, Shyangdan D, Arasaradnam R, et al. Faecal calprotectin testing for differentiating amongst inflammatory and non-inflammatory bowel diseases: systematic review and economic evaluation. Health Technol Assess 2013;17:xv–xix, 1–211. 20. D?britz J, Gerner P, Enninger A, Cla?en M, Radke M. Inflammatory Bowel Disease in Childhood and Adolescence. Dtsch Arztebl Int. 2017 May 12;114(19):331-338, 21. Oliveira SB, Monteiro IM. Diagnosis and management of inflammatory bowel disease in children. BMJ. 2017 May 31;357:j 22. Mack DR, Langton C, Markowitz J, LeLeiko N, Griffiths A, Bousvaros A, Evans J, Kugathasan S, Otley A, Pfefferkorn M, Rosh J, Mezoff A, Moyer S, Oliva-Hemker M, Rothbaum R, Wyllie R, delRosario JF, Keljo D, Lerer T, Hyams J, Pediatric Inflammatory Bowel Disease Collaborative Research Group Pediatrics. 2007;119(6):1113.). 23. Dai Y, Zhang Q, Olofson AM, Jhala N, Liu X. Celiac Disease: Updates on Pathology and Differential Diagnosis. AdvAnatPathol. 2019 Sep;26(5):292-312. doi: 10.1097/PAP.0000000000000242. 24. Ghishan FK, Kiela PR. Vitamins and Minerals in Inflammatory Bowel Disease. Gastroenterol Clin North Am. 2017 Dec;46(4):797-808. 25. Pfeferkorn MD, Marshalleck FE, Saeed SA, et al. NASPGHAN Clinical Report on the Evaluation and Treatment of Pediatric Patients With Internal Penetrating Crohn Disease: Intraabdominal Abscess With and Without Fistula. JPGN 2013; 57:394–400. doi: 10.1097/MPG.0b013e31829ef8. 26. Chen H, Liu Y, Fu L, Lin X, Fan D, Li C. Clinical utility of double-balloon enteroscopy in children: A single-centre experience in South China. J Paediatr Child Health. 2019 Feb;55(2):188-193. 27. UchidaK, Yoshiyama S, Inoue M, Koike Y, Yasuda H, Fujikawa H, Okita Y, Araki T, Tanaka K, Kusunoki M. Double balloon enteroscopy for pediatric inflammatory bowel disease. Pediatr Int. 2012 Dec;54(6):806-9. 28. MaltzR, Podberesky DJ, Saeed SA Imaging modalities in pediatric inflammatory bowel disease. CurrOpinPediatr. 2014;26(5):590-6. 29. Sturm , Maaser C, Calabrese E, eta al. ECCO-ESGAR Guideline for Diagnostic Assessment in IBD Part 2: IBD scores and general principles and technical aspects. J Crohns Colitis. 2019 Mar 26;13(3):273-284. doi: 10.1093/ecco-jcc/jjy114. PMID: 30137278. 30. Oliva S, Thomson M, de Ridder L, Mart?n-de-Carpi J, Van Biervliet S, Braegger C, Dias JA, Kolacek S, Miele E, Buderus S, Bronsky J, Winter H, Navas-L?pez VM, Assa A, Chong SKF, Afzal NA, Smets F, Shaoul R, Hussey S, Turner D, Cucchiara S. Endoscopy in Pediatric Inflammatory Bowel Disease: A Position Paper on Behalf of the Porto IBD Group of the European Society for Pediatric Gastroenterology, Hepatology and Nutrition. J Pediatr Gastroenterol Nutr. 2018 Sep;67(3):414-430. 31. Magline D. D., Sandrasegaran K., Chiorean M., Dewitt J. et al. Radiologic investigationscomplement and add diagnostic information to capsule endoscopy of small-bowel diseases Am. J. Roentgenol. 2007. Vol. 189. N 2. P. 306–312.852 32. Spada C., Riccioni M. E., Costamagna G. Patients with known small bowel stricture or with symptoms of small bowel obstructionsecondary to Crohn’s disease should not perform video capsule endoscopy without being previously tested for small bowel patency // Am. J. Gastroenterol. 2007. Vol. 102. N 7. P. 1542–1543. 33. Kopylov U, et al. Diagnostic yield of capsule endoscopy versus magnetic resonance enterography and small bowel contrast ultrasound in the evaluation of smallbowelCrohn’s disease: Systematic review and meta-analysis. Dig Liver Dis 2017;49:854–63. 34. Podg?rka J., Pacho R., Albrecht P. MR enterography imaging of Crohn’s disease in pediatric patients. PolJRadiol, 2014; 79: 79-87 doi:10.12659/PJR.889760. 35. Hijaz NM, Attard TM, Colombo JM, Mardis NJ, Friesen CA. Comparison of the use of wireless capsule endoscopy with magnetic resonance enterography in children with inflammatory bowel disease. World J Gastroenterol 2019; 25(28): 3808-3822. DOI:10.3748/wjg.v25.i28.3808. 36. J-Y Hang, H-K Yoon, W K Kim, Y A Cho, J S Lee, C H Yoon, Y J Lee, K M Kim. Transperineal ultrasonography for evaluation of the perianal fistula and abscess in pediatric Crohn disease: preliminary study. Ultrasonography 2014;33:184-190 doi:10.14366/usg.14009. 37. de Zoten EF, Pasternak BA, Mattei P, et al. Diagnosis and Treatment of Perianal Crohn Disease: NASPGHAN Clinical Report and Consensus Statement. JPGN. 2013 Sep; 57:401–412. doi: 10.1097/MPG.0b013e3182a025ee. 38. Kolara M., Pilkingtona M., Winthropa A., MacDonalda H., Justinichb C., Soboleskic D., Slyc L., Hurlbut D. Free intestinal perforation in children with Crohn"s disease. Journal of Pediatric Surgery Case Reports 32 (2018) 5–10. doi:10.1016/j.epsc.2018.01.002. 39. Sakka D, Cheung MS. Management of primary and secondary osteoporosis in children. Ther Adv Musculoskelet Dis. 2020 Nov 2;12:1759720X20969262 40. Herzog D, Bishop N, Glorieux F, Seidman EG Interpretation of bone mineral density values in pediatric Crohn"s disease Inflamm Bowel Dis. 1998;4(4):261-7. 41. Gokhale R, Favus MJ, Karrison T, Sutton MM, Rich B, Kirschner BS,. Bone mineral density assessment in children with inflammatory bowel disease. Gastroenterology. 1998;114(5):902-11. 42. Maratva K, Hradsky O, Matyskova J, Copova I, Soucek O, Sumnik Z, Bronsky J. Musculoskeletal system in children and adolescents with inflammatory bowel disease: normal muscle force, decreased trabecular bone mineral density and low prevalence of vertebral fractures. EurJPediatr. 2017 Oct;176(10):1355-1363. 43. Magro F, Langner C, Driessen A, Ensari A, Geboes K, Mantzaris GJ, Villanacci V, BecheanuG, Borralho Nunes P, Cathomas G, Fries W, Jouret-Mourin A, Mescoli C, de Petris G, Rubio CA, Shepherd NA, Vieth M, Eliakim R; European Society of Pathology (ESP); European Crohn"s and Colitis Organisation (ECCO). European consensus on the histopathology of inflammatory bowel disease. J Crohns Colitis. 2013 Nov;7(10):827-51. doi:10.1016/j.crohns.2013.06.001. Epub 2013 Jul 17. PMID: 23870728 44. Feakins RM; British Society of Gastroenterology. Inflammatory bowel disease biopsies: updated British Society of Gastroenterology reporting guidelines. J Clin Pathol. 2013 Dec;66(12):1005-26. doi: 10.1136/jclinpath-2013-201885. Epub 2013 Sep 2. PMID: 23999270. 45. Birimberg-Schwartz L, Zucker DM, Akriv A, Cucchiara S, Cameron FL, Wilson DC, Lazowska I, Yianni L, Paul SP, Romano C, Kolacek S, Buderus S, P?rregaard A, Russell RK, Escher JC, Turner D; Pediatric IBD Porto group of ESPGHAN. Development and Validation of Diagnostic Criteria for IBD Subtypes Including IBD-unclassified in Children: a Multicentre Study From the Pediatric IBD Porto Group of ESPGHAN. J Crohns Colitis. 2017 Sep 1;11(9):1078-1084. doi: 10.1093/ecco-jcc/jjx053. PMID: 2843089. 46. HH. Uhlig, F Charbit-Henrion, D. Kotlarz. Clinical Genomics for the diagnosis of monogenic forms of inflammatory bowel disease: A Position Paper from The Paediatric IBD Porto Group of ESPGHAN. Journal of Pediatric Gastroenterology and Nutrition, Publish Ahead of Print.2021.DOI: 10.1097/MPG.0000000000003017. 47. Ruemmele FM, Veres G, Kolho KL, Griffiths A, Levine A, Escher JC, et al; EuropeanCrohn"s and Colitis Organisation; European Society of PediatricGastroenterology,Hepatology and Nutrition. Consensus guidelines of ECCO/ESPGHAN on the medical management of pediatric Crohn"s disease. J Crohns Colitis. 2014 Oct;8(10):1179207. DOI: 10.1016/j.crohns.2014.04.005. 48. Benchimol EI, Fortinsky KJ, Gozdyra P, Van den Heuvel M, Van Limbergen J, Griffiths AM.Epidemiology of pediatric inflammatory bowel disease: a systematic review of international trends. Inflamm Bowel Dis. 2011;17(1):423-39. 49. Miele E, Shamir R, Aloi M, Assa A, Braegger C, Bronsky J, et al. Nutrition in PediatricInflammatory Bowel Disease: A Position Paper on Behalf of the Porto Inflammatory BowelDisease Group of the European Society of Pediatric Gastroenterology, Hepatology and Nutrition. J Pediatr Gastroenterol Nutr. 2018 Apr;66(4):687-708. DOI: 10.1097/MPG.0000000000001896. 50. Хавкин АИ, Сорвачёва ТН, Рославцева ЕА. Патогенетическое обоснование диетотерапии болезни Крона у детей. Экспериментальная и клиническая гастроэнтерология. 2021;186(2):94-105. DOI: 10.31146/1682-8658-ecg-186-2-94-105. 51. Hartman C, Berkowitz D, Weiss B, Shaoul R, Levine A, Adiv OE, Shapira R, Fradkin A, Wilschanski M, Tamir A, Shamir R. (2008) Isr Med Assoc J. 10(7):503-7. Nutritional supplementation with polymeric diet enriched with transforming growth fac tor-beta 2 for children with Crohn’s disease 52. Levine A, Wine E, Assa A, Sigall Boneh R, Shaoul R, Kori M, Cohen S, Peleg S, Shamaly H,On A, Millman P, Abramas L, Ziv-Baran T, Grant S, Abitbol G, Dunn KA, Bielawski JP, Van Limbergen J. Crohn"s Disease Exclusion Diet Plus Partial Enteral Nutrition Induces Sustained Remission in a Randomized Controlled Trial. Gastroenterology. 2019 Aug;157(2):440-450.e8. doi: 10.1053/j.gastro.2019.04.021. Epub 2019 Jun 4. 53. Bernstein C., et al. WHO global guidelines on Inflammatory Bowel Disease - Guidelinesfor the Diagnosis and Management of IBD in 2010. Inflamm Bowel Dis. 2010 Jan; 16:112– 124. doi:10.1002/ibd.21048. 54. Escher JC. Budesonide versus prednisolone for the treatment of active Crohn"s disease inchildren: a randomized, double-blind, controlled, multicentre trial. Eur J Gastroenterol Hepatol 2004;16(1):47-54. 55. Levine A, Weizman Z, Broide E, Shamir R, Shaoul R, Pacht A, et al. A comparison ofbudesonide and prednisone for the treatment of active pediatric Crohn disease. J Pediatr Gastroenterol Nutr 2003;36(2):248-52. 56. van Rhenen PF, Aloi M, Assa A, Bronsky J, Escher JC, Fagerberg UL, Gasparetto M,Gerasimidis K, Griffiths A, Henderson P, Koletzko S, Kolho KL, Levine A, van Limbergen J, Martin de Carpi FJ, Navas-L?pez VM, Oliva S, de Ridder L, Russell RK, Shouval D, Spinelli A, Turner D, Wilson D, Wine E, Ruemmele FM. The Medical Management of Paediatric Crohn"s Disease: an ECCO-ESPGHAN Guideline Update. J Crohns Colitis. 2020 Oct 7:jjaa161. doi: 10.1093/ecco-jcc/jjaa161. Epub ahead of print. PMID: 33026087. 57. Byron MA, Jackson J, Ansell BM. Effect of different corticosteroid regimens on hypothalamic-pituitary-adrenal axis and growth in juvenile chronic arthritis. J R Soc Med 1983;76(6): 452-7. 58. Jakobsen C, Munkholm P, Paerregaard A, Wewer V. Steroid dependency and pediatricinflammatory bowel disease in the era of immunomodulators—a population-based study. Inflamm Bowel Dis 2011; 17(8):1731 -40. 59. Cohen SA, Aloi M, Arumugam R, Baker R, Bax K, Kierku? J, Koletzko S, Lionetti P, PerssonT, Eklund S. Enteric-coated budesonide for the induction and maintenance of remission of Crohn"s disease in children. Curr Med Res Opin. 2017 Jul;33(7):1261-1268. doi: 10.1080/03007995.2017.1313213. Epub 2017 Apr 19. PMID: 28420280
- Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2020 - 60. Greenley RN, Stephens KA, Nguyen EU, Kunz JH, Janas L, Goday P, Schurman JV. Vitaminand mineral supplement adherence in pediatric inflammatory bowel disease. J Pediatr Psychol. 2013 Sep;38(8):883-92. doi: 10.1093/jpepsy/jst037. Epub 2013 Jul 1. PMID:23818680/ 61. Gawronska A, Banasiuk M, Lachowicz D, Pituch H, Albrecht P, Banaszkiewicz A. Metronidazole or Rifaximin for Treatment of Clostridium difficile in Pediatric Patients with Inflammatory Bowel Disease: A Randomized Clinical Trial. Inflamm Bowel Dis. 2017 Dec;23(12):2209-2214. 62. Barabino A, Torrente F, Ventura A, Cucchiara S, Castro M, Barbera C. Azathioprine inpaediatric inflammatory bowel disease: an Italian multicentre survey. Aliment Pharmacol Ther 2002;16(6):1125-30. 63. Jaspers GJ, Verkade HJ, Escher JC, de Ridder L, Taminiau JA, Rings EH. Azathioprinemaintains first remission in newly diagnosed pediatric Crohn"s disease. Inflamm Bowel Dis 2006;12(9):831-6. 64. CosnesJ, BourrierA, Laharie D, Nahon S, BouhnikY, Carbonnel F, et al. Early administration of azathioprine vs conventional management of Crohn"s Disease: a randomized controlled trial. Gastroenterology 2013;145(4):758-65 [e2; quize14-5]. 65. Panes J, Lopez-Sanroman A, Bermejo F, Garcia-Sanchez V, Esteve M, Torres Y, et al. Earlyazathioprine therapy is no more effective than placebo for newly diagnosed Crohn"s disease. Gastroenterology 2013;145(4):766-74 [e1]. 66. Fuentes D, Torrente F, Keady S, Thirrupathy K, Thomson MA, Walker-Smith JA, et al.High-dose azathioprine in children with inflammatory bowel disease. Aliment Pharmacol Ther 2003;17(7):913-21. 67. Gearry RB, Barclay ML, Burt MJ, Collett JA, Chapman BA. Thiopurine drug adverse effectsin a population of New Zealand patients with inflammatory bowel disease. Pharmacoepidemiol Drug Saf 2004; 13(8):563-7. 68. Hindorf U, Lindqvist M, Hildebrand H, Fagerberg U, Almer S. Adverse events leading tomodification of therapy in a large cohort of patients with inflammatory bowel disease.Aliment Pharmacol Ther 2006;24(2):331-42. 69. Kirschner BS. Safety of azathioprine and 6-mercaptopurine in pediatric patients withinflammatory bowel disease. Gastro¬enterology 1998; 115(4):813-21. 70. Ledder OD, Lemberg DA, Ooi CY, Day AS. Are thiopurines always contraindicated afterthiopurine-induced pancreatitis in inflammatory bowel disease? J Pediatr Gastroenterol Nutr 2013;57(5):583-6. 71. Kandiel A, Fraser AG, Korelitz BI, Brensinger C, Lewis JD. Increased risk of lymphomaamong inflammatory bowel disease patients treated with azathioprine and 6mercaptopurine. Gut 2005; 54(8):1121 -5. 72. Camus M, Seksik P, Bourrier A, Nion-Larmurier I, Sokol H, Baumer P, et al. Long-termoutcome of patients with Crohn"s disease who respond to azathioprine. Clin Gastroenterol Hepatol 2013; 11 (4):389-94. 73. Ashworth LA, Billett A, Mitchell P, Nuti F, Siegel C, Bousvaros A. Lymphoma risk inchildren and young adults with inflam¬matory bowel disease: analysis of a large singlecenter cohort. Inflamm Bowel Dis 2012;18(5):838-43. 74. Colletti RB, Cucchiara S, Dubinsky M, Escher JC, Faubion WA, Fell J, et al. 833 malignancies in children receiving infliximab and other inflammatory bowel disease therapies: an inflam¬matory bowel disease multicenter, prospective, long-term registry of pediatric patients (develop) registry data. Gastro¬enterology 2013;144(5, Supplement 1):S147. 75. Hyams J, Crandall W, Kugathasan S, Griffiths A, Olson A, Johanns J, et al. Induction andmaintenance infliximab therapy for the treatment of moderate-to-severe Crohn"s disease in children. Gastroenterology 2007;132(3):863-73 [quiz 1165-6]. 76. Ardura MI, Toussi SS, Siegel JD, Lu Y, Bousvaros A, Crandall WNASPGHAN ClinicalReport: Surveillance, Diagnosis, and Prevention of Infectious Diseases in Pediatric Patients With Inflammatory Bowel Disease Receiving Tumor Necrosis Factor-?Inhibitors.J Pediatr Gastroenterol Nutr. 2016 Jul;63(1):130-55. 77. Kim S. Surgery in Pediatric Crohn’s Disease: Indications, Timing and Post-OperativeManagement. Pediatr Gastroenterol Hepatol Nutr 2017 March 20(1):14-21. doi.org/10.5223/pghn.2017.20.1.14. 78. Мазанкова Л.Н., Водилова О.В., Халиф И.Л. Осложнения болезни Крона у детей.Колопроктология. - 2004. - № 3 (9). - С. 30-35. 79. Щербакова О.В. Практические рекомендации по хирургическому лечению осложненной болезни Крона у детей. Экспериментальная и клиническая гастроэнтерология. - 2015. - Т.1. - №113. - С.78-83. 80. Aloi M, Viola F, D’Arcangelo G, et al. Disease course and efficacy of medical therapy instricturing paediatric Crohn’s disease. Digestive and Liver Disease. 2013;45:464–468. doi:10.1016/j.dld.2013.01.020. 81. Baillie CT, Smith JA. Surgical strategies in paediatric inflammatory bowel disease. WorldJ Gastroenterol. 2015 May; 21(20):6101–6116. doi:10.3748/wjg.v21.i20.6101. 82. Papi C., Festa V., Fagnani C., et al. Evolution of clinical behaviour in Crohn’s disease: predictive factors of penetrating complications. Dig. Liver Dis. -2005;37:247-53. 83. Vanhelst J, Vidal F, Turck D, Drumez E, Djeddi D, Devouge E, Spyckerelle C, Zandzou SG,Legrand C, Michaud L, B?ghin L, Gottrand F, Coopman S, Ley D. Physical activity is associated with improved bone health in children with inflammatory bowel disease. Clin Nutr. 2020 Jun;39(6):1793-1798] 84. Lowe W, Kenwright D, Wyeth J, Blair N. Crohn disease: effect on children"s lifestyles. JPediatr Gastroenterol Nutr. 2012 Mar;54(3):397-400. doi: 10.1097/MPG.0b013e318231cf17. PMID: 21857249. 85. Farrell D, Artom M, Czuber-Dochan W, Jelsness-J?rgensen LP, Norton C, Savage E.Interventions for fatigue in inflammatory bowel disease. Cochrane Database Syst Rev. 2020 Apr 16;4(4):CD012005. doi: 10.1002/14651858.CD012005.pub2. PMID: 32297974; PMCID: PMC7161727. 86. Martinelli M, Giugliano FP, Strisciuglio C, Urbonas V, Serban DE, Banaszkiewicz A, AssaA, Hojsak I, Lerchova T, Navas-L?pez VM, Romano C, Sladek M, Veres G, Aloi M, Kucinskiene R, Miele E. Vaccinations and Immunization Status in Pediatric Inflammatory Bowel Disease:A Multicenter Study From the Pediatric IBD Porto Group of the ESPGHAN. Inflamm Bowel Dis. 2020 Aug 20;26(9):1407-1414 87. Hanauer SB, Feagan BG, Lichtenstein GR, Mayer LF, Schreiber S, Colombel JF, et al.Maintenance infliximab for Crohn"s disease: the ACCENT I randomised trial. Lancet 2002;359(9317):1541-9. 88. Armuzzi A, Pugliese D, Danese S, Rizzo G, Felice C, Marzo M, et al. Infliximab in steroiddependent ulcerative colitis: effectiveness and predictors of clinical and endoscopicremission. Inflamm Bowel Dis 2013;19(5):1065-72. 89. Sprakes MB, Ford AC, Warren L, Greer D, Hamlin J. Efficacy, tolerability, and predictorsof response to infliximab therapy for Crohn"s disease: a large single centre experience. J.Crohns Colitis 2012;6(2):143-53. 90. Fidder H, Schnitzler F, Ferrante M, Noman M, Katsanos K, Segaert S, et al. Long-termsafety of infliximab for the treatment of inflammatory bowel disease: a single-centre cohortstudy. Gut 2009;58(4):501-8. 91. Sturm , Maaser C, Calabrese E, eta al. ECCO-ESGAR Guideline for Diagnostic Assessmentin IBD Part 2: IBD scores and general principles and technical aspects.J Crohns Colitis. 2019Mar 26;13(3):273-284. doi: 10.1093/ecco-jcc/jjy114. PMID: 30137278. 92. Hyams JS, Grand RJ, Colodny AH, Schuster SR, Eraklis A. Course and prognosis aftercolectomy and ileostomy for inflammatory bowel disease in childhood and adolescence. JPediatr Surg. 1982 Aug;17(4):400-5. doi: 10.1016/s00223468(82)80498-3. PMID: 7120008 93. Bakouny Z, Yared F, El Rassy E, et al. Comparative efficacy of anti-TNF therapies for theprevention of postoperative recurrence of Crohn’s dis- ease: a systematic review and networkmeta-analysis of prospective trials. J Clin Gastroenterol 2019;53:409–17 94. Turner D, Levine A, Walters TD, Focht G, Otley A, L?pez VN, Koletzko S, Baldassano R,Mack D, Hyams J, Griffiths AM. Which PCDAI Version Best Reflects Intestinal Inflammationin Pediatric Crohn Disease? J Pediatr Gastroenterol Nutr. 2017 Feb;64(2):254-260
Информация
Адрес для переписки:
Узбекистан, г. Ташкент, ул. Чимбой-2, Проезд Талант
100176
Тел: (+71) 229-38-74
Факс: (+71) 229-38-73:
E-mail: u.rizamukhamedova@minzdrav.uz
Состав рабочей группы по созданию клинического протокола
1. Камилова Алтиной Турсуновна - д.м.н., профессор, руководитель отдела гастроэнтерологии РСНПМЦ Педиатрии МЗРУз, председатель Ассоциации детских гастроэнтерологв Узбекистана
2. Умарназарова Зульхумор Ерназаровна - д.м.н., г.н.с. отдела гастроэнтерологии РСНПМЦ Педиатрии МЗРУз, главный детский гастроэнтеролог МЗРУз
3. Азимова Ноиба Джамалитдиновна - м.н.с. отдела гастроэнтерологии РСНПМЦ Педиатрии МЗРУз.
Руководитель рабочей группы:
Ахмедова Д.И.- д.м.н., профессор, директор РСНПМЦ Педиатрии МЗРУз, председатель Ассоциации педиатров Узбекистана.
СПИСОК СОКРАЩЕНИЙ
МП –меркаптопурин
АЗА – азатиоприн
БК – болезнь Крона
ГКС - глюкокортикоиды
ЖКТ – желудочно-кишечный тракт
ИФМ – инфликсимаб
КТ – компьютерная томография
МР-энтерография – магнитно-резонансная энтерография
МРТ – магнитно-резонансная томография
МТ – метотрексат
НПВП – нестероидные противовоспалительные препараты
ПСХ – первичный склерозирующий холангит
ПЭП – полное энтеральное питание
РКИ – рандомизированное контролируемое исследование
СОЭ – скорость оседания эритроцитов
СРБ – С-реактивный белок
УЗИ – ультразвуковое исследование
ЯК – язвенный колит
PCDAI – педиатрический индекс активности болезни Крона
Приложение А. Алгоритмы действий врача
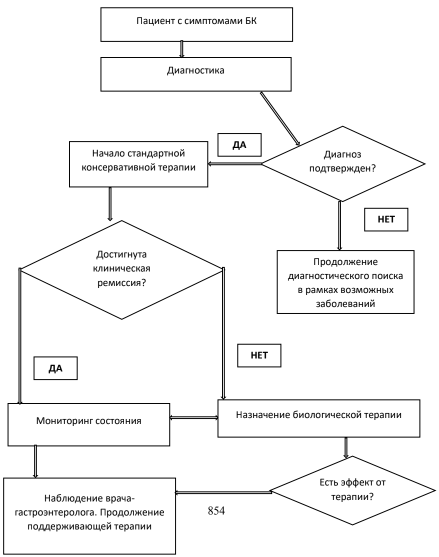
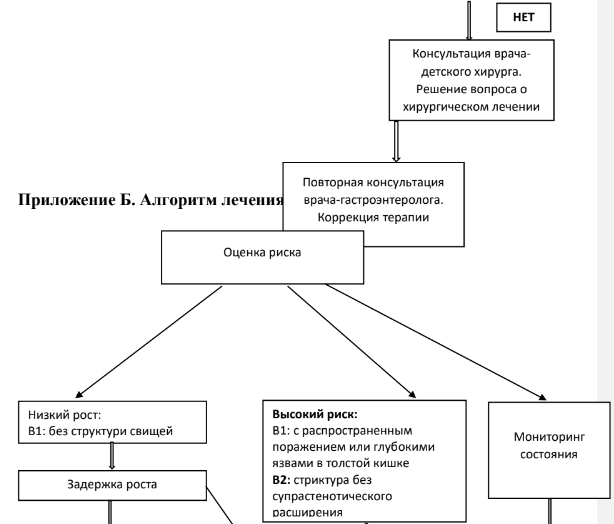
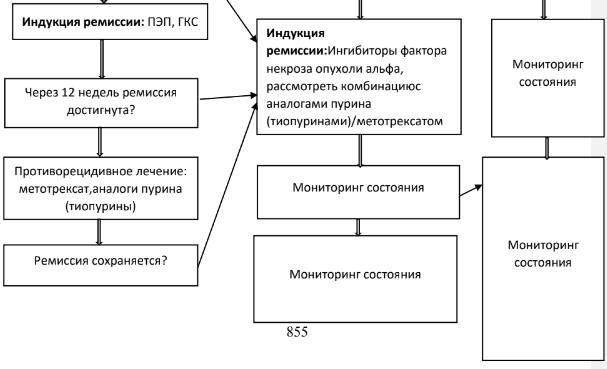
Приложение В.
Макро- и микроскопические признаки БК в биоптате тонкой кишки в соответствии с обновленными Порто критериями
Оригинальноеназвание (еслиесть): ESPGHAN revised Porto criteria for the diagnosis of inflammatory bowel disease in children and adolescents
Источник (официальный сайт разработчиков, публикация с валидацией): Levine A., Koletzko S., Turner D., et al. ESPGHAN revised Porto criteria for the diagnosis of inflammatory bowel disease in children and adolescents – J.Pediatric Gasroenterol Nutr., 2014, v.58 (6), p.795-806
Тип: другое (уточнить): критерии
Назначение: постановка диагноза болезни Крона
Содержание (шаблон) и Ключ (интерпретация):
Макро- и микроскопические признаки болезни Крона у детей
|
Макроскопические
|
Микроскопические
|
|
Специфические:
- Афтозные язвы - Щелевидные линейные или извитые язвы - Булыжная мостовая в терминальном илеуме - Стеноз с престенотической дилатацией - Утолщение стенки кишки с сужением просвета - Перианальные поражения (свищи, абсцессы, язвы или стеноз анального канала) - Язвы в тощей или подвздошной кишках |
Специфические:
- Неказеозные гранулемы на расстоянии от крипт - Очаговость и неравномерность воспаления - Трансмуральный характер инфильтрата - Подслизистый фиброз |
|
Неспецифические:
- Отек - Гиперемия - Ранимость - Гранулярность - Локальная потеря сосудистого рисунка |
Неспецифические:
- Гранулема, прилежащая к разрыву крипты - Слабый воспалительный инфильтрат в собственной пластинке СОК
- Эрозии и поверхностные язвы СОК
- Нарушение архитектоники крипт, уменьшение бокаловидных клеток, метаплазия клеток - Панета |
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.