Атопический дерматит
 Версия: Клинические протоколы 2024 (Узбекистан)
Версия: Клинические протоколы 2024 (Узбекистан)
Атопический дерматит (L20)
Аллергология, Аллергология детская, Дерматовенерология, Дерматология детская, Иммунология
Общая информация
Краткое описание
Приложение к приказу № 401
от «25» декабря 2024 года
Министра Здравоохранения Республики Узбекистан
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ УЗБЕКИСТАН
РЕСПУБЛИКАНСКИЙ СПЕЦИАЛИЗИРОВАННЫЙ НАУЧНО-ПРАКТИЧЕСКИЙ МЕДИЦИНСКИЙ ЦЕНТР АЛЛЕРГОЛОГИИ И КЛИНИЧЕСКОЙ ИММУНОЛОГИИ
НАЦИОНАЛЬНЫЕ КЛИНИЧЕСКИЕ ПРОТОКОЛЫ ПО НОЗОЛОГИИ «АТОПИЧЕСКИЙ ДЕРМАТИТ»
Вводная часть
Код(ы) МКБ-10:
|
Код
|
Название
|
|
L 20.0
|
Атопический дерматит
|
|
L 20.8
|
Другические атопические дерматиты
|
|
L 20.9
|
Атопический дерматит неуточненный
|
|
Скачать (ссылка с МКБ)
|
Дата разработки и пересмотра протокола: 2024 год, дата пересмотра 2026 г. или по мере появления новых ключевых доказательств. Все поправки к представленным рекомендациям будут опубликованы в соответствующих документах.
Категория пациентов
Больные, дети и взрослые, с подозрением на атопический дерматит и с установленным диагнозом атопический дерматит.
Целевая группа протокола
- врач-аллерголог-иммунолог;
- врач-анестезиолог-реаниматолог;
- врач-гастроэнтеролог;
- врач-генетик;
- врач-дерматовенеролог;
- врач-неонатолог;
- врач общей практики (семейный врач);
- врач-оториноларинголог;
- врач-педиатр;
- врач-педиатр городской (районный);
- врач-педиатр участковый;
- врач по гигиене детей и подростков;
- врач по гигиене труда;
- врач по общей гигиене;
- врач приемного отделения;
- врач скорой медицинской помощи;
- врач-терапевт;
- врач-терапевт подростковый;
- врач-терапевт участковый;
- врач-терапевт участковый цехового врачебного участка;
- врач функциональной диагностики;
- врач пульмонолог
ВВЕДЕНИЕ
Атопический дерматит (АтД)
В настоящем протоколе, предназначенном для специалистов, оказывающих помощь больным с АтД, приведены доступные к настоящему дню клинические доказательства, моменты надлежащей практики, а также мнения экспертов. Была проведена адаптация к местным условиям, были учтены особенности доступности лекарственных препаратов к применению у больных с АтД.
Основным требованием при разработке протокола, включившего данные, основанные на лучшем мировом опыте, было использование материалов лучших руководств по данной теме , а также методологии строго отбора научных данных при формировании рекомендаций как Российская ассоциация аллергологов и клинических иммунологов (РААКИ) , Белорусская ассоциация аллергологов и клинических иммунологов (БААКА), Европейская академия аллергологов и клинических иммунологов (ЕAACI), Всемирная аллергологическая организация (WAO).
Определение
Атопический дерматит (АтД) — аллергическое заболевание (АЗ) кожи, возникающее, как правило, в раннем детском возрасте у лиц с наследственной предрасположенностью к атопическим заболеваниям, имеющее хроническое рецидивирующее течение, возрастные особенности локализации и морфологии очагов воспаления, характеризующееся кожным зудом и обусловленное гиперчувствительностью, как к аллергенам, так и к неспецифическим раздражителям [1].
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
А Классификация АтД
Классификация
В настоящее время не существует единой общепринятой классификации АтД.
Условно выделяют:
-
экзогенный (аллергический) АтД, ассоциированный с респираторной аллергией и сенсибилизацией к аэроаллергенам;
-
эндогенный (неаллергический) АтД, не ассоциированный с респираторной аллергией и сенсибилизацией к каким-либо аллергенам.
Комментарии: Риск развития респираторной аллергии у больных, страдающих АтД, по разным данным, составляет 30–80%; 60% больных АтД имеют латентную склонность к развитию бронхиальной астмы (БА), а 30–40% заболевают БА [1].
В соответствии с документом «Пересмотренная номенклатура в аллергологии», предложено выделять синдром атопической экземы/дерматита аллергической и неаллергической природы. Неаллергическую природу АтД предполагают у 10–20% всех больных АтД, хотя, согласно последним данным, эту форму заболевания встречают лишь в 5,4% случаев[9,10].
В рабочей классификации АтД, предложенной отечественными авторами, выделяют возрастные периоды, стадии болезни, степень тяжести и распространенности кожного процесса[1].
Рабочая классификация АтД
Возрастные периоды болезни.
-
I возрастной период — младенческий (до 2 лет).
-
II возрастной период — детский (от 2 до 13 лет).
-
III возрастной период — подростковый и взрослый (старше 13 лет).
Стадии болезни.
-
Стадия обострения:
-
фаза выраженных клинических проявлений;
-
фаза умеренных клинических проявлений.
-
-
Стадия ремиссии:
-
неполная ремиссия;
-
полная ремиссия.
-
-
Распространенность процесса:
-
ограниченно-локализованный;
-
распространенный;
-
диффузный.
-
Степень тяжести процесса:
-
легкое течение;
-
средней тяжести;
-
тяжелое течение.
Таблица 1. Клинические формы Атопического дерматита (в зависимости от соотношения морфологических элементов выделяют 5 клинических форм заболевания)
|
Клинические формы
|
Возрастной период
|
Морфологическая характеристика
|
|
Экссудативная
|
I
|
Преобладают эритема, отек, микровезикуляция с развитием мокнутия, образование корок
|
|
Эритемато-сквамозная
|
I и II
|
Эритема и шелушение в виде сливающихся очагов поражения с нечеткими границами, мелкие папулы, расчесы
|
|
Эритемато-сквамозная с лихенизацией
|
II, реже III
|
Картина эритемато-сквамозной формы с присоединением множественных папул, формированием лихенизации
|
|
Лихеноидная
|
II и III
|
Слияние папул в сплошные очаги поражения с четкими границами тусклого сероватого цвета с отрубевидным шелушением, расчесами, серозно-геморрагическими корками на местах экскориаций
|
|
Пруригоподобная
|
II и III (в целом данную форму встречают редко)
|
Образование пруригинозных папул, преимущественно на разгибательных поверхностях конечностей; эта форма, как правило, сочетается с другими формами (чаще с лихеноидной) АтД
|
Комментарии: Поскольку у одного и того же больного клиническая картина АтД может быть представлена различными формами, указывать клиническую форму заболевания при формулировке диагноза необязательно.
Наличие возрастных особенностей локализации и морфологии кожных элементов отличает АтД от других экзематозных и лихеноидных заболеваний кожи (табл. 2).
Таблица 2. Возрастная характеристика и локализация очагов поражения кожи
|
Возрастные периоды
|
Морфологическая характеристика
|
Локализация
|
|
Младенческий
|
Преобладание экссудативной формы АтД. Воспаление носит острый или подострый характер. Присутствуют гиперемия, отечность, мокнутие, корки
|
Лицо, наружная поверхность голеней, сгибательные и разгибательные поверхности конечностей.
К концу периода очаги локализуются преимущественно в области локтевых сгибов и подколенных ямок, в области запястий и шеи |
|
Детский
|
Процесс носит характер хронического воспаления: эритема, папулы, шелушение, утолщение кожи (инфильтрация), усиление кожного рисунка (лихенизация), множественные экскориации (расчесы), трещины.
На местах разрешения высыпаний участки гипо- или гиперпигментации. У некоторых детей в этом периоде формируется дополнительная складка нижнего века (симптом Денни–Моргана) |
Локтевые и подколенные складки, задняя поверхность шеи, сгибательные поверхности голеностопных и лучезапястных суставов, заушные области
|
|
Подростковы й и взрослый
|
Преобладают явления инфильтрации с лихенизацией; эритема имеет синюшный оттенок.
Папулы сливаются в очаги сплошной папулезной инфильтрации |
Верхняя половина туловища, лицо, шея, верхние конечности
|
Распространенность процесса оценивают по площади поражения кожи в процентах от общей площади кожных покровов (табл. 3).
Таблица 3. Распространенность поражения кожи при АтД
Таблица 3. Распространенность поражения кожи при АтД
|
Распространенность процесса
|
Площадь поражения кожи
|
Локализация
|
|
Ограниченно- локализованный
|
<10%
|
Локтевые и/или подколенные складки, кожа кистей рук, кожа шеи и/или лица
|
|
Распространенный
|
10–50%
|
Частично поражена кожа груди, спины; помимо локтевых и подколенных складок, в процесс вовлекаются другие участки кожи конечностей (плечи, предплечья, голени, бедра)
|
|
Диффузный
|
>50%
|
Кожа всего тела, волосистая часть головы
|
При оценке степени тяжести заболевания следует учитывать (табл. 4):
-
длительность и частоту обострений;
-
длительность ремиссий;
-
распространенность кожного процесса;
-
морфологические особенности кожного процесса;
-
интенсивность кожного зуда;
-
нарушение сна;
-
эффективность проводимой терапии.
Таблица 4. Степени тяжести АтД
|
Степень тяжести
|
Характеристика
|
|
Легкая
|
Ограниченно локализованное поражение кожи. Редкие обострения (1–2 раза в год), преимущественно в холодное время года продолжительностью до месяца.
Продолжительность ремиссии 6–8 мес. Хороший эффект проводимой терапии |
|
Среднетяжелая
|
Распространенное поражение кожи. Обострения более частые (3–4 раза в год), до нескольких месяцев.
Продолжительность ремиссии менее 4 мес. Упорное течение с невыраженным эффектом проводимой терапии |
|
Тяжелая
|
Распространенное или диффузное поражение кожи.
Частые (более шести раз в год) и длительные (несколько месяцев или постоянные) обострения. Редкие и непродолжительные (менее 2 мес) ремиссии. Лечение приносит кратковременное и незначительное улучшение |
Комментарии:
Cтепень тяжести АтД принято оценивать также с помощью полуколичественных шкал; наиболее широкое применение получила шкала SCORAD (ScoringofAtopicDermatitis) (Приложение Г),а также EASI (ExzemaAreaandSeverityIndex), IGA (Investigators’ GlobalAssessment).
Этиология и патогенез
Этиология атопического дерматита
https://raaci.ru/dat/pdf/atopik dermatit.pdf
https://elib.vsmu.by/handle/123/17826
Факторы, которые могут влиять на развитие и проявления АтД, приведены в табл. 1
https://elib.vsmu.by/handle/123/17826
Факторы, которые могут влиять на развитие и проявления АтД, приведены в табл. 1
Таблица 1. Факторы, влияющие на развитие и проявления БА [21]
|
Факторы
|
Описание
|
|
Внутренние факторы
|
|
|
Факторы окружающей среды
|
|
Мультифакториальность патогенеза АтД обусловлена вкладом целого ряда факторов – как генетических – наследственности, так и эпигенетических – реализуемых при множественном экспосомальном воздействии.
Патогенез атопического дерматита
Патогенез АтД – иммуноопосредованное заболевание, имеющее генетическую предрасположенность и сложные иммунные механизмы развития. На сегодняшний день известны основные генетические и этиологические факторы АтД, доказана роль иммунной системы, аллергии к клещам домашней пыли, энтеротоксинам золотистого стафилококка, плесневым грибам, IgE-аутореактивности в механизмах развития заболевания. Последнее десятилетие ознаменовалось открытием гена филаггрина, показана роль мутаций этого гена в нарушении реализации функции эпидермального барьера при АтД [2].
Первоначально АтД рассматривался только как Тh2-зависимый процесс, однако со временем было накоплено достаточно свидетельств о роли Thl-клеток в развитии этого заболевания. При АтД общепризнанна концепция дихотомии Th1/Th2 лимфоцитов, которая лежит в основе, так называемой двухфазной иммунологической модели, согласно которой в различные периоды течения заболевания преобладает активность как Th2-, так и Thl -клеток.Основными эффекторными клетками острой фазы АтД являются Th2 – лимфоциты, а при хроническом течении заболевания происходит переключение сТh2 на Th1 – иммунный ответ. В острую фазу, принепосредственном воздействии на кожу больного причинно-значимого аллергена происходит активация антиген-представляющих клеток (АПК), а именно – клеток Лангерганса (КЛ) и дендритных клеток (ДК), инфильтрирующих эпидермис и несущих на своей поверхности Fc?R1 рецепторы (высокоаффинные рецепторы к IgE). Активированные КЛ инициируют высвобождение хемокинов и миграцию их и клеток-предшественниц ДК в лимфатические узлы, где, в свою очередь, происходит активация Th2-лимфоцитов, секретирующих провоспалительные цитокины аллергического воспаления в коже: ИЛ 4, ИЛ5, ИЛ13. Последние необходимы для переключения синтеза иммуноглобулинов на IgE ответ, вызывают экспрессию молекул межклеточной адгезии (ICAM-1), определяющих миграцию эозинофилов и мононуклеаров непосредственно в очаг воспаления. Мононуклеары у больных АтД отличаются повышенной активностью сАМР- фосфодиэстеразы, способствующей продукции ИЛ4, ИЛ10, простагландина Е2 и IgE. Кроме того, при АтД кератиноциты способны продуцировать ИЛ7-подобный тимусно-стромальный лимфопоэтин (TSLP), который дает сигнал ДК активировать T клетки в Тh 2 направлении. Все эти факторы обеспечивают сигналы, необходимые для развития Th2 – иммунного ответа и выработки специфических IgE В-клетками. Активация синтеза IgE антител – это ведущее патогенетическое звено возникновения клинических проявлений АтД. При хроническом течении АтД вследствие постоянного воздействия экзогенных факторов, хронического повреждения кожных покровов (зуд, расчесывание), высвобождения внутриклеточных белков, которые действуют как аутоантигены, воспалительный процесс приобретает хроническое течение, для которого характерно преобладание активности Th1-ответа, тогда как количество цитокинов Th2-профиля резко сокращается. Для этого этапа характерно повышение синтеза ИЛ12 макрофагами и эозинофилами, повышение уровня ИЛ5, ИЛ8 и ИФН?, которые являются маркерами хронического воспаления в коже, а при длительном аллергическом процессе – также ИЛ3 и GM - CSF. При хронической стадии доминирует активация макрофагов и эозинофилов, которые продуцируют ИЛ12. Повышенная продукция IFN? отмечается у 80% больных, что коррелирует с тяжестью заболевания, но снижается при успешном лечении [3].
Первоначально АтД рассматривался только как Тh2-зависимый процесс, однако со временем было накоплено достаточно свидетельств о роли Thl-клеток в развитии этого заболевания. При АтД общепризнанна концепция дихотомии Th1/Th2 лимфоцитов, которая лежит в основе, так называемой двухфазной иммунологической модели, согласно которой в различные периоды течения заболевания преобладает активность как Th2-, так и Thl -клеток.Основными эффекторными клетками острой фазы АтД являются Th2 – лимфоциты, а при хроническом течении заболевания происходит переключение сТh2 на Th1 – иммунный ответ. В острую фазу, принепосредственном воздействии на кожу больного причинно-значимого аллергена происходит активация антиген-представляющих клеток (АПК), а именно – клеток Лангерганса (КЛ) и дендритных клеток (ДК), инфильтрирующих эпидермис и несущих на своей поверхности Fc?R1 рецепторы (высокоаффинные рецепторы к IgE). Активированные КЛ инициируют высвобождение хемокинов и миграцию их и клеток-предшественниц ДК в лимфатические узлы, где, в свою очередь, происходит активация Th2-лимфоцитов, секретирующих провоспалительные цитокины аллергического воспаления в коже: ИЛ 4, ИЛ5, ИЛ13. Последние необходимы для переключения синтеза иммуноглобулинов на IgE ответ, вызывают экспрессию молекул межклеточной адгезии (ICAM-1), определяющих миграцию эозинофилов и мононуклеаров непосредственно в очаг воспаления. Мононуклеары у больных АтД отличаются повышенной активностью сАМР- фосфодиэстеразы, способствующей продукции ИЛ4, ИЛ10, простагландина Е2 и IgE. Кроме того, при АтД кератиноциты способны продуцировать ИЛ7-подобный тимусно-стромальный лимфопоэтин (TSLP), который дает сигнал ДК активировать T клетки в Тh 2 направлении. Все эти факторы обеспечивают сигналы, необходимые для развития Th2 – иммунного ответа и выработки специфических IgE В-клетками. Активация синтеза IgE антител – это ведущее патогенетическое звено возникновения клинических проявлений АтД. При хроническом течении АтД вследствие постоянного воздействия экзогенных факторов, хронического повреждения кожных покровов (зуд, расчесывание), высвобождения внутриклеточных белков, которые действуют как аутоантигены, воспалительный процесс приобретает хроническое течение, для которого характерно преобладание активности Th1-ответа, тогда как количество цитокинов Th2-профиля резко сокращается. Для этого этапа характерно повышение синтеза ИЛ12 макрофагами и эозинофилами, повышение уровня ИЛ5, ИЛ8 и ИФН?, которые являются маркерами хронического воспаления в коже, а при длительном аллергическом процессе – также ИЛ3 и GM - CSF. При хронической стадии доминирует активация макрофагов и эозинофилов, которые продуцируют ИЛ12. Повышенная продукция IFN? отмечается у 80% больных, что коррелирует с тяжестью заболевания, но снижается при успешном лечении [3].
Большое внимание уделяется изучению антимикробных пептидов (АМП) – ? – дефензинов 2 и 3(HBD-2 и HBD-3), кателицидина hCAP18/LL-37 (С-концевой фрагментчеловеческого катионного антимикробного белка - 37 аминокислот)и их роли в противомикробной защите. Все АМП обладают широким спектром активности: HBD-2 активны против Грам-отрицательных бактерий, таких как Escherichia coli, Pseudomonas aeruginosa, а HBD-3 и HBD-3 демонстрируют более мощную антибактериальную активность против широкого спектра Грам-положительных и Грам-отрицательных бактерий, а также против Candidaalbicans. При АтД существенно снижена экспрессия АМП в коже, что является причиной п одверженности больных АтД развитию микробных осложнений [4,5].
Получены доказательства участия аутоиммунных механизмов в развитии АтД. В особенности это касается тяжелых форм заболевания, при которых развивается IgE ответ к аутоаллергенам. Последние представлены группой белков – гомологов экзоаллергенов, против которых вырабатываются IgE антитела. К таким аутоаллергенам относятся транкрипционный фактор LEDGF/DSF7013, аутоантигены, связанные с атопией - atopy- relatedauto-antigens (ARA) HomS1-S5, продуцируемые кератиноцитами, и марганец супероксид дисмутаза – manganese superoxide dismutase (MnSOD). Дрожжевой гриб Malasseziasympodialis, колонизирующий кожу больных АтД, вызывает сенсибилизацию к человеческой MnSOD благодаря своей высокой гомологичности к последней. Такая кросс-сенсибилизация наблюдается в основном у больных АтД с локализацией поражений в области головы и шеи, обусловленной преимущественной колонизацией Malasseziasympodialis. Показано, что IgE-аутореактивность развивается уже в течение первых лет жизни [6]. и смешанные, которые могут иметь общие генетические, эпигенетические, метаболические, нейрогенные и ремоделирующие характеристики [1].
Диагностика
Диагностика
Основные жалобы на интенсивный и постоянный кожный зуд, сухость и стянутость кожных покровов, высыпания, покраснение, шелушение, мокнутие, нарушение сна и дневной активности, при распространенном кожном процессе могут присутствовать признаки общей интоксикации – повышение температуры тела, озноб, увеличение периферических лимфатических узлов.
Комментарии: АтД нередко осложняет вторичная инфекция: бактериальная, грибковая или вирусная. В первом случае возникают пиодермии: фолликулиты, реже импетиго, фурункулы. Грибковая инфекция, обусловленная Malassezia spp., Candida spp., чаще поражает кожу волосистой части головы, лица, шеи и воротниковой зоны. У больных АтД нередко возникает распространенная герпетическая инфекция; в особо тяжелых случаях — герпетиформная экзема Капоши, которая может привести к летальному исходу при отсутствии надлежащего лечения, особенно у детей раннего возраста.
Комментарии: АтД нередко осложняет вторичная инфекция: бактериальная, грибковая или вирусная. В первом случае возникают пиодермии: фолликулиты, реже импетиго, фурункулы. Грибковая инфекция, обусловленная Malassezia spp., Candida spp., чаще поражает кожу волосистой части головы, лица, шеи и воротниковой зоны. У больных АтД нередко возникает распространенная герпетическая инфекция; в особо тяжелых случаях — герпетиформная экзема Капоши, которая может привести к летальному исходу при отсутствии надлежащего лечения, особенно у детей раннего возраста.
При сборе анамнеза рекомендуется обращать внимание на:
- начало в раннем возрасте;
- наличие атопических заболеваний у самого больного (наряду с АтД он может страдать АР, БА);
- наличие атопических заболеваний у близких родственников; сезонность обострений;
- выявление провоцирующих факторов;
- связь обострений с воздействием аллергенов;
- выявление сопутствующей бактериальной или другой инфекции, осложняющей течение заболевания (частота осложнений, их влияние на тяжесть течения АтД).
В соответствии с общепринятыми международными рекомендациями, на основе ранее предложенных критериев HanifinJ.M. и RajkaG. [12], в настоящее время разработаны диагностические критерии АтД с учетом данных анамнеза, жалоб, результатов клинического и лабораторного обследования, дифференциального диагноза (Табл.5) [13].
Таблица 5. Диагностические критерии Атопического дерматита
| Критерии | Характеристика |
|
Обязательные (должны присутствовать) |
Зуд кожи; Характерные морфологические особенности поражения кожив зависимости от возраста; Характер воспаления (острое, подострое, хроническое) Хроническое, рецидивирующее течение |
|
Важные (определяются в большинстве случаев) |
Дебют заболевания в раннем детском возрасте; Наличие атопии: наличие сопутствующих аллергических заболеваний, семейный анамнез атопии, наличие IgE – опосредованной сенсибилизации; Сухость кожи |
|
Дополнительные (важны для подтверждения диагноза, но не являются обязательными и специфичными для постановки диагноза) |
Атипичные сосудистые реакции (белый дермографизм, бледность лица и т.п.); Фолликулярный кератоз, простой белый лишай, исчерченность ладоней, сухость кожи - ксероз; Поражение периорбитальной области и век; Поражение периоральной области, околоушной области, наружных слуховых проходов, хейлит; Лихенизация, перифолликулярные изменения, экскориации вследствие кожного зуда |
| Критерии исключения |
Чесотка; Себорейный дерматит; Пеленочный дерматит; Контактный дерматит (аллергический или простой ирритантный); Ихтиоз обыкновенный; Т – клеточная лимфома кожи; Псориаз обыкновенный; Фоточувствительные дерматозы; Иммунодефицитные заболевания; Эритродермии другого генеза |
Комментарии: АтД может проявиться в любом возрасте, но чаще в течение первых пяти лет жизни, хотя у большинства больных первые признаки АтД появляются уже на 1 – м году жизни. Очень важным диагностическим критерием является семейный анамнез аллергических заболеваний: если мать болеет атопическим заболеванием (аллергический ринит, бронхиальная астма, атопический дерматит), то вероятность передачи предрасположенности к атопии детям составит 75%, если отец – то 60%, если даже в семье никто не болеет аллергией, то % вероятности составит 15% .
При физикальном обследовании рекомендуется обратить внимание на:
- характер и локализацию высыпаний, наличие или отсутствие расчесов, свидетельствующих об интенсивности кожного зуда, признаки инфицирования кожи, на симптомы АР, конъюнктивита и БА.
- сухость кожи;
- возрастные изменения характерных поражений кожи;
- белый дермографизм;
- склонность к кожным инфекциям;
- хейлит;
- симптом Денни–Моргана (дополнительная складка нижнего века);
- гиперпигментация кожи периорбитальной области;
Уровень убедительности рекомендаций B (уровень достоверности доказательств 3a).
- При наличии показаний для выявления сопутствующих заболеваний и очагов хронической инфекции рекомендовано проведение общеклинического обследования [1].
Уровень убедительности рекомендаций D (уровень достоверности доказательств 4).
- Поскольку течение БА крайне вариабельно, степень тяжести заболевания может меняться на протяжении месяцев и лет.
Лабораторная диагностика.
https://raaci.ru/dat/pdf/atopik dermatit.pdf
https://onlinelibrary.wiley.com/doi/10.1111/all.15032
https://elib.vsmu.by/handle/123/17826
https://onlinelibrary.wiley.com/doi/10.1111/all.15032
https://elib.vsmu.by/handle/123/17826
- Рекомендовано выполнение клинического анализа крови (эозинофилия периферической крови)
Уровень убедительности рекомендаций В (уровень достоверности доказательств 3a).
Инструментальная диагностика
https://raaci.ru/dat/pdf/atopik dermatit.pdf
https://onlinelibrary.wiley.com/doi/10.1111/all.15032
https://elib.vsmu.by/handle/123/17826
- При наличии показаний, после консультаций специалистов гастроэнтеролога, пульмонолога, эндокринолога и др., рекомендовано проведение дообследования, которое может включать в себя эзофагогастродуоденоскопию; УЗИ органов брюшной полости (при наличии показаний - других органов); рентгенологическое исследование органов грудной клетки, придаточных пазух носа; оценку функции внешнего дыхания (ФВД) и др.
Уровень убедительности рекомендаций D (уровень достоверности доказательств).
- Рекомендованы консультации аллерголога, дерматолога, других узких специалистов при наличии показаний, определяемых лечащим врачом.
Уровень убедительности рекомендаций С.
Аллергологическое обследование
Аллергологическое обследование
- При отсутствии обострения больным рекомендовано проведение кожного тестирования: prick – тесты, или скарификационные тесты со стандартным набором ингаляционных аллергенов.
Уровень убедительности рекомендаций D (уровень достоверности доказательств 2b).
- Иммунологическое обследование необязательно. Рекомендовано определение содержания IgА, IgМ и IgG в сыворотке для исключения селективного дефицита IgA, сопровождающегося признаками АтД.
Уровень убедительности рекомендаций D (уровень достоверности доказательств 4).
- При наличии диффузного кожного процесса или других противопоказаний к аллергологическому обследованию in vivo рекомендовано проведение лабораторной аллергодиагностики — определение уровня общего сывороточного IgE (в большинстве случаев существенно превышает нормальные значения, но не является специфическим признаком) и антител изотипа IgE к неинфекционным аллергенам или их компонентам с помощью различных методов [9,12]: иммуноферментного анализа (ИФА);радиоаллергосорбентного теста (РАСТ), множественного аллергосорбентного теста (МАСТ), молекулярной аллергодиагностики (ISAC), (Madex, Alex, Phadia-200).
Уровень убедительности рекомендаций B (уровень достоверности доказательств 2b).
Комментарии: Аллергологическое обследование включает сбор аллергологического анамнеза, обследование invivo (кожные тесты, провокационные тесты), а также лабораторную диагностику invitro (см. соответствующий раздел).
Аллергологический анамнез – обязательный этап, помогающий выявить причинно-значимый аллерген и другие провоцирующие факторы [1].
Комментарии: Аллергологическое обследование включает сбор аллергологического анамнеза, обследование invivo (кожные тесты, провокационные тесты), а также лабораторную диагностику invitro (см. соответствующий раздел).
Аллергологический анамнез – обязательный этап, помогающий выявить причинно-значимый аллерген и другие провоцирующие факторы [1].
-
Семейный анамнез – история развития аллергических заболеваний у близких родственников больного;
-
История развития кожного процесса у больного АтД (включая наличие или отсутствие бактериальной, вирусной и грибковой инфекции), установление сезонности обострений, связи с воздействием аллергенов;
-
Наличие респираторных симптомов;
-
Анамнестические сведения о факторах риска АтД: течение беременности и родов у матери, питание во время беременности, профессиональные вредности родителей, жилищно – бытовые условия, характер вскармливания ребенка, перенесенные инфекции, сопутствующие заболевания, пищевой и фармакологический анамнез, выявление возможных провоцирующих факторов и другое;
Современные лабораторные методы определения аллерген-специфических антител основаны на использовании экстрактов аллергенов (РАСТ, МАСТ, ИФА), или их компонентов (молекулярные методы аллергодиагностики - микрочипирование на твердой фазе - ISAC). Последние имеют преимущества перед методами с использованием экстрактов аллергенов, заключающиеся в возможности выявления аллергенных молекул, а также перекрестных аллергенов, что позволяет более точно определить показания к аллерген–специфической иммунотерапии (АСИТ) и прогнозировать ее эффективность, а также назначить индивидуальные элиминационные диеты у больных с перекрестной пищевой аллергией. анализах крови при БА характерных изменений нет. Часто выявляется эозинофилия, однако ее нельзя считать патогномоничным симптомом. В мокроте у детей с БА могут выявляться эозинофилы, спирали Куршмана, кристаллы Шарко-Лейдена.
Показания для консультации специалистов:
- консультация аллерголога-иммунолога;
- консультация дерматолога;
- консультация пульмонолога ;
- консультация оториноларинголога (с целью выявления сопутствующей патологии ЛОР- органов);
- консультация гастроэнтеролога (с целью выявления сопутствующей патологии органов пищеварения.
Формулировка диагноза у больного атопическим дерматитом
В диагнозе должны быть указаны:
- этиология (если установлена);
- степень тяжести;
- уровень контроля;
- сопутствующие заболевания, которые могут оказать влияние на течение АтД
- при наличии – обострение с указанием его степени тяжести.
Атопический дерматит – хроническое аллергическое воспалительное заболевание кожи, сопровождающееся зудом, возрастной морфологией высыпаний и стадийностью.
МКБ-10
L20 Атопический дерматит
L20.8 Другие атопические дерматиты
L20.9 Атопический дерматит неуточнённый
Рабочая классификация атопического дерматита у детей (Российская ассоциация аллергологов и клинических иммунологов, 2002)
Возрастные периоды
Младенческая (с 1 мес. до 2 лет)
Детская (с 2 до 13 лет)
Подростковая (старше 13 лет)
Стадии: Острая, Подострая, Хроническая
Клинико-морфологические формы: Экссудативная; Эритемато-сквамозная; Эритемато-сквамозная с лихенизацией; Лихеноидная
Тяжесть течения: Легкое течение; Средне-тяжелое; Тяжелое
Распространенность процесса: Ограниченный; Распространенный; Диффузный
Клинико-этиологические варианты: С пищевой сенсибилизацией; С грибковой сенсибилизацией; С клещевой/бытовой сенсибилизацией; С пыльцевой сенсибилизацией
Диагностические критерии атопического дерматита:
Основные критерии:
- Зуд кожи
- Типичная морфология высыпаний и локализация: 1. дети первых лет жизни – эритема, папулы, микровезикулы с локализацией на лице и разгибательных поверхностях конечностей; 2. дети старшего возраста – папулы, лихенификация симметричных участков сгибательных поверхностей конечностей
- Ранняя манифестация первых симптомов
- Хроническое рецидивирующее течение
- Наследственная отягощенность по атопии
Дополнительные критерии (помогают заподозрить атопический дерматит, но являются неспецифическими)
-
Ксероз (сухость кожи)
-
Реакции немедленного типа при тестировании с аллергенами
-
Ладонная гиперлинейность и усиление рисунка («атопические» ладони)
-
Стойкий белый дермографизм
-
Экзема сосков
- Рецидивирующий конъюктивит
- Продольная суборбитальная складка (линия Денни-Моргана)
- Периорбитальная гиперпигментация
- Кератоконус (коническое выпячивание роговицы в ее центре)
По распространённости воспалительного процесса на коже различают:
- ограниченный атопический дерматит (локализация преимущественно на лице, площадь поражения кожи не более 5-10%)
- распространённый атопический дерматит (площадь поражения 10-50%)
- диффузный атопический дерматит (обширное поражение кожи — более 50%).
По стадиям течения атопического дерматита выделяют:
-
острую стадию (зуд кожи, папулы, микровезикулы на фоне эритемы, множественные расчёсы и эрозии, выделение серозного экссудата)
-
подострую стадию (эритема, шелушение, расчёсы, в том числе на фоне уплотнения кожи)
-
хроническую стадию (утолщённые бляшки, фиброзные папулы, подчёркнутый рисунок кожи – лихенизация).
Оценка тяжести атопического дерматита по выраженности клинических проявлений
Лёгкое течение
Среднетяжелое течение
Тяжёлое течение
Ограниченные участки поражения кожи, слабая эритема или лихенизация, слабый зуд кожи, редкие обострения —1-2 раза в год
Распространенный характер поражения кожи с умеренной экссудацией, гиперемией и/или лихенизацией, умеренный зуд, более частые обострения — 3- 4 раза в год с короткими ремиссиями
Диффузный характер поражения кожи с выраженной экссудацией, гиперемией и/или лихенизацией, постоянный сильный зуд и практически непрерывное рецидивирующее течение.
Примеры формулировки диагноза: Атопический дерматит, младенческий период, острая стадия, экссудативная форма, среднетяжелое течение, распространенный, с пищевой сенсибилизацией. Атопический дерматит, детский период, подострая стадия, эритемато-сквамозная форма, среднетяжелое течение, распространенный, с пищевой/бытовой сенсибилизацией. Атопический дерматит, подростковый период, хроническая стадия, лихеноидная форма, тяжелое течение, диффузный, с бытовой/пыльцевой сенсибилизацией
Дифференциальный диагноз
Дифференциальная диагностика
https://raaci.ru/dat/pdf/atopikdermatit.pdf
https://onlinelibrary.wiley.com/doi/10.1111/all.15032
https://elib.vsmu.by/handle/123/17826
Дифференциальную диагностику АтД рекомендовано проводить со следующими заболеваниями:
https://onlinelibrary.wiley.com/doi/10.1111/all.15032
https://elib.vsmu.by/handle/123/17826
Дифференциальную диагностику АтД рекомендовано проводить со следующими заболеваниями:
-
Себорейный дерматит;
-
Пеленочный дерматит;
-
АКД;
-
Чесотка;
-
Строфулюс;
-
Ихтиоз обыкновенный;
-
Псориаз обыкновенный;
-
Ограниченный нейродермит (лишай Видаля);
-
Микробная экзема;
-
Розовый лишай Жибера;
-
Дерматофитии;
-
Лимфома кожи в ранней стадии;
-
Герпетиформный дерматит Дюринга;
-
Фенилкетонурия;
-
Синдром гипериммуноглобулинемии E;
-
Синдром Вискотта–Олдрича;
-
Десквамативная эритродермия Лейнера–Муссу.
Уровень убедительности рекомендаций С.
В соответствии с общепринятыми международными рекомендациями, на основе ранее предложенных критериев HanifinJ.M. и RajkaG. [12], в настоящее время разработаны диагностические критерии АтД с учетом данных анамнеза, жалоб, результатов клинического и лабораторного обследования, дифференциального диагноза (Табл.5) [13].
Таблица 5. Диагностические критерии Атопического дерматита
|
Критерии
|
Характеристика
|
|
Обязательные
(должны присутствовать) |
Зуд кожи;
Характерные морфологические особенности поражения кожив зависимости от возраста; Характер воспаления (острое, подострое, хроническое) Хроническое, рецидивирующее течение |
|
Важные
(определяются в большинстве случаев) |
Дебют заболевания в раннем детском возрасте;
Наличие атопии: наличие сопутствующих аллергических заболеваний, семейный анамнез атопии, наличие IgE – опосредованной сенсибилизации; Сухость кожи |
|
Дополнительные
(важны для подтверждения диагноза, но не являются обязательными и специфичными для постановки диагноза) |
Атипичные сосудистые реакции (белый дермографизм, бледность лица и т.п.);
Фолликулярный кератоз, простой белый лишай, исчерченность ладоней, сухость кожи - ксероз; Поражение периорбитальной области и век; Поражение периоральной области, околоушной области, наружных слуховых проходов, хейлит; Лихенизация, перифолликулярные изменения, экскориации вследствие кожного зуда |
|
Критерии исключения
|
Чесотка;
Себорейный дерматит; Пеленочный дерматит; Контактный дерматит (аллергический или простой ирритантный); Ихтиоз обыкновенный; Т – клеточная лимфома кожи; Псориаз обыкновенный; Фоточувствительные дерматозы; Иммунодефицитные заболевания; Эритродермии другого генеза |
Лечение (амбулатория)
Тактика лечения на амбулаторном уровне:
https://raaci.ru/dat/pdf/atopik dermatit.pdf
https://onlinelibrary.wiley.com/doi/10.1111/all.15032
https://elib.vsmu.by/handle/123/17826
Цели лечения
-
Достижение клинической ремиссии заболевания;
-
Воздействие на состояние кожи: устранение или уменьшение воспаления и кожного зуда, предупреждение и устранение вторичного инфицирования, увлажнение и смягчение кожи, восстановление ее защитных свойств;
-
Профилактика развития тяжелых форм АтД;
-
Профилактика развития и лечение респираторных проявлений у больных АтД;
-
Восстановление утраченной трудоспособности;
-
Улучшение качества жизни.
Основные принципы комплексного подхода к лечению больных АтД:
-
элиминация причинно-значимых аллергенов;
-
наружная терапия и рациональный уход за кожей;
-
системная фармакотерапия;
-
АСИТ;
-
физиотерапевтические методы лечения;
-
обучение;
-
реабилитация и профилактика.
В настоящее время принят ступенчатый подход к лечению АтД, который предусматривает поочередное включение различных терапевтических методов воздействия в зависимости от степени тяжести заболевания (Табл.6). В случаях присоединения вторичной инфекции необходимо включение в схему лечения антисептических и противомикробных средств на любой стадии заболевания.

Комментарии: Ступенчатый подход к лечению АтД был предложен в 2006 году международной группой PRACTALL, в состав которой входили Европейская Академия Аллергологии и Клинической Иммунологии и Американская Академия Аллергии, Астмы и Международным консенсусом Европейских научных ассоциаций в 2012 году, в состав которых входили: Европейский Дерматологический Форум (European Dermatology Forum (EDF); Европейская Академия Дерматологии и Венерологии (European Academy of Dermatology and Venereology (EADV); Европейская Федерация Аллергии (European Federation of Allergy (EFA); Европейская Комиссия по Атопическому Дерматиту European Task Forceon Atopic Dermatitis (ETFAD); Европейской Общество Педиатрической Дерматологии (European Society of Pediatric Dermatology (ESPD); Global Allergy and Asthma European Network (GA2LEN).
-
В случаях подтвержденной сенсибилизации к конкретным аллергенам рекомендовано проведение АСИТ.
Уровень убедительности рекомендаций С (уровень достоверности доказательств 3a)
-
В случаях неэффективного лечения рекомендовано учитывать приверженность больного к лечению, рекомендовано тщательное проведение дифференциальной диагностики.
Уровень убедительности рекомендаций D (уровень достоверности доказательств 4)
Элиминационные мероприятия
-
Рекомендовано уменьшение влияния провоцирующих факторов, таких как потливость, стресс, резкие колебания температуры окружающей среды, грубая одежда, использование мыла и детергентов и т.д.
Убедительных данных КИ по данным мероприятиям нет, в связи с этим [9,14].
Уровень убедительности рекомендации D (уровень достоверности доказательств 4)
-
Рекомендовано соблюдение неспецифической гипоаллергенной диеты.
Уровень убедительности рекомендаций D(уровень достоверности доказательств 4 ).
-
Рекомендовано соблюдение индивидуальной гипоаллергенной диеты с исключением определенных продуктов при доказанной пищевой аллергии (с помощью провокационных тестов) [9, 14].
Уровень убедительности рекомендаций В, (уровень достоверности доказательств 2a)
Элиминация причинно-значимых аллергенов (индивидуальные охранительные режимы):
-
Рекомендовано соблюдение элиминационных мероприятий против клеща домашней пыли, что может улучшать течение АтД [9].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2b)
-
Рекомендовано обустроить гипоаллергенный быт и проводить элиминацию клещей домашней пыли, что в сочетании с высокогорным климатом также приводит к улучшению течения АтД [9].
Уровень убедительности рекомендаций В (уровень достоверности доказательств –3b)
-
Рекомендовано уменьшить или исключить контакт с пыльцой растений у больных с пыльцевой сенсибилизацией, с шерстью животных – у больных с эпидермальной сенсибилизацией, с контактными аллергенами – у больных с контактной гиперчувствительностью (например, к никелю) [9].
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 4)
Комментарии:
Элиминация причинно-значимых аллергенов и триггеров
Среди провоцирующих факторов принято выделять специфические (причинно-значимые аллергены) и неспецифические провоцирующие факторы. Их воздействие на кожу больного с АтД может провоцировать обострение заболевания, поэтому соблюдение элиминационных мероприятий является одним из важнейших методов лечения АтД [1, 7].
К неспецифическим провоцирующим факторам относят:
К неспецифическим провоцирующим факторам относят:
-
физические (механические раздражители – одежда из грубых тканей, шерсть и т.п.)
-
химические (кислоты, детергенты, мыла, отбеливатели и т.п.),
-
биологические (инфекционные агенты),
-
факторы окружающей среды (летучие органические вещества, табачный дым и пр.).
К специфическим факторам относят причинно – значимые аллергены, такие как бытовые, эпидермальные, пыльцевые, пищевые и микробные аллергены.
Наружная противовоспалительная терапия
Средства для наружной противовоспалительной терапии АтД:
-
топические глюкокортикостероиды (ТГКС);
-
топические ингибиторы кальциневрина (ТИК).
-
ТГКС
1. ТГКС обладают выраженным противовоспалительным эффектом и приводят к улучшению состояния кожных покровов по сравнению с плацебо.
Уровень убедительности рекомендаций A, (уровень достоверности доказательств – 1a).
-
ТГКС рекомендованы, как препараты первой линии для лечения АтД [9,10,15].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1a)
-
Применение низко – и умеренно – активных ТГКС рекомендовано уже при легком течении АтД (SCORAD> 15), а при среднем и тяжелом течении АтД целесообразно применение активных и высокоактивных ТГКС в минимальных эффективных дозах [9,10,14,15]. (Приложение Г2)
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1а)
Комментарии: ТГКС различают по силе противовоспалительной активности. В таблице 1 (Приложение Д) приведена Европейская классификация ТГКС по биологической активности (Miller JA, Munro DD., 1980).
Также существует классификация ТГКС по 7- балльной шкале, принятая в ряде стран, в том числе США, которая учитывает не только силу действующего вещества, но и лекарственную форму препарата (таблица 2 Приложение Г2).
Также существует классификация ТГКС по 7- балльной шкале, принятая в ряде стран, в том числе США, которая учитывает не только силу действующего вещества, но и лекарственную форму препарата (таблица 2 Приложение Г2).
-
Для наибольшей эффективности и во избежание побочных эффектов при терапии ТГКС рекомендовано соблюдать следующие правила:
-
использовать непродолжительно - не более 4 недель, затем 1 – 2 раза в неделю на ранее пораженные участки кожи длительно – метод проактивной терапии с целью профилактики обострений (показано для мометазона фуроата и флутиказона пропионата),
-
чередовать участки воздействия;
-
не использовать под повязки, кроме тяжелых случаев АтД, при которых возможно применение влажных окклюзионных повязок с ТГКС в малых дозах в течение 3 дней;
-
уменьшать частоту аппликаций после достижения лечебного действия;
-
использовать ТГКС, обладающих высокой эффективностью, низкой системной абсорбцией и низким атрофогенным потенциалом [15].
Уровень убедительности рекомендаций B, (уровень достоверности доказательств 2b)
-
Проактивная терапия (использование 2 раза в неделю в течение длительного времени) может предотвращать рецидивы заболевания [15].
Уровень убедительности рекомендаций B, (уровень достоверности доказательств - 1b)
-
При осложненном микробной инфекцией АтД рекомендовано применять комбинированные наружные ЛС, содержащие помимо ГКС антибиотик, эффективный в отношении стафилококка (фузидовую кислоту, гентамицин, неомицин и др.), и противогрибковый компонент (клотримазол, натамицин и др.) (Приложение Г4).
Уровень убедительности рекомендаций D, (уровень достоверности доказательств 3a).
-
Применение комбинированных препаратов, содержащих противомикробные и противогрибковые ЛС, рекомендовано в течение непродолжительного периода времени (не более 2 недель) в связи с высоким риском увеличения роста антибиотико-устойчивых штаммов бактерий и грибов.
Уровень убедительности рекомендаций D (уровень достоверности доказательств 4).
-
Рекомендовано применение белья с антисептическим свойствами (содержащих серебро, системаAEGIS)
Уровень убедительности рекомендаций В, (уровень достоверности доказательств - 2b).
2. ТИК
-
ТИК рекомендованы для купирования обострения АтД и для профилактики рецидивов.
Уровень убедительности рекомендаций A, (уровень достоверности доказательств - 1b).
-
Применение ТИК безопасно также при поражении кожи лица, складок
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1b).
-
Поддерживающая терапия с применением мази такролимуса** 0,1% 2 раза в неделю в течение длительного времени предотвращает развитие обострений заболевания.
Уровень убедительности рекомендаций A, (уровень достоверности доказательств - 1b) .
Комментарии: К данной группе препаратов относятся такролимус и пимекролимус, которые являются нестероидными клеточно-селективными ингибиторами кальциневрина, принадлежащими к классу аскомициновых макролактамов. ТИК обладают локальной иммунотропной активностью и не приводят к нежелательным эффектам, характерным для ТГКС и системных иммуносупрессоров. В европейских инструкциях по медицинскому применению данных препаратов показанием для назначения такролимуса является АтД среднетяжелого и тяжелого течения, тогда как пимекролимус позиционируется для лечения легкого и среднетяжелого АтД.
Пимекролимус крем 1% разрешен с 3-х месячного возраста. Препарат назначают 2 раза в сутки на пораженные участки кожи любых частей тела, включая голову, лицо, шею, области опрелостей. Лечение продолжают до полного исчезновения симптомов. При первых признаках рецидива АтД терапию следует возобновить. Если симптомы заболевания сохраняются в течение 6 недель, следует провести повторную оценку состояния больного.
Пимекролимус крем 1% разрешен с 3-х месячного возраста. Препарат назначают 2 раза в сутки на пораженные участки кожи любых частей тела, включая голову, лицо, шею, области опрелостей. Лечение продолжают до полного исчезновения симптомов. При первых признаках рецидива АтД терапию следует возобновить. Если симптомы заболевания сохраняются в течение 6 недель, следует провести повторную оценку состояния больного.
Такролимус представлен двумя лекарственными формами - 0,03% мазь для детей старше 2 лет и 0,1% мазь для взрослых старше 16 лет. Такролимус назначают при обострении 2 раза в день до достижения эффекта, затем в режиме поддерживающей терапии 2 раза в неделю длительно для профилактики обострений.
Эмолиенты
-
Применение эмолиентов (увлажняющих средств) рекомендовано для лечения АтД и показано на всех стадиях заболевания
Уровень убедительности рекомендаций A (уровень достоверности доказательств -1a)
Комментарии: Их использование приводит к уменьшению сухости кожи, увлажнению эпидермиса, улучшению микроциркуляции и восстановлению функции эпидермального барьера. К увлажняющим средствам, предотвращающим трансэпидермальную потерю воды за счет создания эффекта компресса, относят вазелин, парафин, воск, ланолин и другие животные жиры. Они блокируют прохождение жидкости через роговой слой.
Кроме того, эти увлажняющие средства оказывают смягчающее действие. В состав увлажняющих средств могут быть включены и вещества, способные притягивать и удерживать воду: мочевина, глицерин, сорбит, гиалуроновая кислота, гель алоэ, гидроксилированные органические кислоты. Увлажняющие средства нового поколения включают липиды, идентичные натуральным липидам кожи: церамиды, холестерин, жирные кислоты. Эмолиенты нужно назначать в достаточном количестве, необходимо их обильное и многократное использование в течение дня, например, для эмолиентов в форме крема или мази минимальное количество в неделю составляет 250 г. Также возможно применение эмолиентов в виде масел для душа и ванн.
Кроме того, эти увлажняющие средства оказывают смягчающее действие. В состав увлажняющих средств могут быть включены и вещества, способные притягивать и удерживать воду: мочевина, глицерин, сорбит, гиалуроновая кислота, гель алоэ, гидроксилированные органические кислоты. Увлажняющие средства нового поколения включают липиды, идентичные натуральным липидам кожи: церамиды, холестерин, жирные кислоты. Эмолиенты нужно назначать в достаточном количестве, необходимо их обильное и многократное использование в течение дня, например, для эмолиентов в форме крема или мази минимальное количество в неделю составляет 250 г. Также возможно применение эмолиентов в виде масел для душа и ванн.
-
В зимнее время рекомендовано применять эмолиенты с повышенным содержанием липидов [10,15].
Уровень убедительности рекомендаций C, (уровень достоверности доказательств - 3b)
-
Регулярное применение эмолиентов в сочетании с ТГКС как при их кратковременном применении, так и при длительной поддерживающей терапии приводит к снижению потребности в ТГКС у больных АтД[15].
Уровень убедительности рекомендаций B, (уровень достоверности доказательств – 2a)
Комментарии:
Требования к наружной терапии:
-
устранение или уменьшение кожного зуда;
-
купирование воспалительных реакций и стимулирование репаративных процессов в коже;
-
предупреждение и устранение вторичного инфицирования;
-
увлажнение и смягчение кожи;
-
восстановление защитных свойств кожи.
Основные принципы применения средств для наружной терапии:
-
достаточная сила действия ЛС;
-
достаточная доза ЛС;
-
правильное применение ЛС.
В зависимости от клинической картины АтД и локализации очагов поражения средства для наружной терапии применяют в различных лекарственных формах.
Наружные ЛС всегда необходимо наносить на увлажненную кожу. Эмолиенты в форме крема наносят на кожу за 15 минут до нанесения ЛС, а в форме мази – через 15 минут после нанесения противовоспалительных ЛС. У пациентов тяжелыми формами АтД в стадии обострения с явлениями мокнутия, особенно у детей, возможно применение влажных окклюзионных повязок (wetwraps) с топическими глюкокортикостероидами (ТГКС) в малых дозах в течение нескольких дней до устранения мокнутия. Их применение в течение 3 - 14 дней является эффективным способом лечения тяжелых, устойчивых форм заболевания по сравнению с применением системных ГКС, которые могут вызывать серьезные нежелательные побочные эффекты.
Системная фармакотерапия
Системную фармакотерапию АтД проводят в комплексе с элиминационными мероприятиями и наружной терапией. В нее включено применение блокаторов Н1 - рецепторов, ГКС, антибактериальных, седативных и других психотропных средств, иммунотропных препаратов и препаратов, воздействующих на другие органы при нарушении их функции.
Блокаторы Н1 -рецепторов
-
В настоящее время нет убедительных данных об эффективности АГ препаратов для лечения кожного зуда при АтД[10].
Уровень убедительности рекомендаций A, (уровень достоверности доказательств - 1b)
Системные ГКС
-
Системные ГКС рекомендовано назначать в случае длительного выраженного обострения распространенных форм АтД при неэффективности наружной терапии, а также больным с тяжелым диффузным АтД, протекающим без клинических ремиссий.
Уровень убедительности рекомендаций С, (уровень достоверности доказательств 3a)
-
Рекомендовано использовать ГКС у детей, страдающих АтД [9].
Уровень убедительности рекомендаций D
Комментарии: Применение системных ГКС при АтД необходимо тщательно обосновывать, сопоставляя ожидаемую пользу и возможные нежелательные эффекты, значительно ограничивающие использование этих препаратов.
Побочные эффекты могут возникать при длительном постоянном применении системных ГКС, особенно у детей. (Приложение Г3.)
Побочные эффекты могут возникать при длительном постоянном применении системных ГКС, особенно у детей. (Приложение Г3.)
-
Непродолжительное применение (до 1 недели) может применяться при тяжелом течении АтД [9].
Уровень убедительности доказательств D
Иммуносупрессивная терапия
Назначение иммуносупрессивной терапии рекомендовано при тяжелом персистирующем течении АтД и неэффективности других видов терапии, главным образом:
Назначение иммуносупрессивной терапии рекомендовано при тяжелом персистирующем течении АтД и неэффективности других видов терапии, главным образом:
-
циклоспорина А (в дозе 3-5 мг/кг в день) [10]
Уровень убедительности рекомендаций A, (уровень достоверности доказательств - 1а, 1b)
-
азатиоприна (в дозе 2,5 мг/кг в день), метотрексата, мофетила микофенолата* [10]
Уровень убедительности рекомендаций В, (уровень достоверности доказательств – 2b)
-
Метотрексат может назначаться при тяжелом АтД при неэффективности циклоспорина в дозе от 10 мг в неделю с постепенным снижением до 2,5 мг в неделю в течение 12 недель [10].
Уровень убедительности рекомендаций С, (уровень достоверности доказательств – 1+)
Комментарии: Мофетила микофенолат не зарегистрирован в РФ.
Следует помнить, что длительный прием этих препаратов может привести к тяжелым осложнениям со стороны органов кроветворения, печени и почек. Также описаны случаи обострения заболевания после их отмены.
Следует помнить, что длительный прием этих препаратов может привести к тяжелым осложнениям со стороны органов кроветворения, печени и почек. Также описаны случаи обострения заболевания после их отмены.
Аллерген – специфическая иммунотерапия
-
Проведение АСИТ рекомендовано больным с АтД с доказанной сенсибилизацией к определенным группам аллергенов, и назначается только после проведения предварительного этапа лечения, предусматривающего купирование обострения, подбора адекватной наружной терапии, санацию очагов хронической инфекции и лечение сопутствующих заболеваний.
Уровень убедительности рекомендаций С, (уровень достоверности доказательств 3b)
-
Наиболее обоснована АСИТ аллергенами клещей домашней пыли у больных с подтвержденной сенсибилизацией и сопутствующими респираторными проявлениями аллергии [9,10].
Уровень убедительности рекомендаций B, (уровень достоверности доказательств - 2b)
Лечение вторичной бактериальной инфекции:
АтД часто осложняется развитием пиодермий, для лечения которых используют комбинированные препараты, содержащие противобактериальные компоненты (см. выше).
-
При неэффективности наружной терапии и распространении бактериальной инфекции на обширную поверхность тела рекомендовано назначение антибиотиков системного действия) [10].
Уровень убедительности рекомендаций B, (уровень достоверности доказательств - 2b
-
Также рекомендовано применение антисептических средств [10].
Уровень убедительности рекомендаций C, (уровень достоверности доказательств - 4)
Лечение вторичной грибковой инфекции
Преимущественная локализация поражения в области воротниковой зоны, шеи, лица и волосистой части кожи головы указывает на присоединение грибковой инфекции, обусловленной грибом Malassezia spp. В таких случаях назначают наружные комбинированные препараты с противогрибковым компонентом (см. выше).
-
При неэффективности наружной терапии рекомендовано применение противогрибковых препаратов системного действия: кетоконазола, итраконазола, тербинафина, флуконазола и др [10].
Уровень убедительности рекомендаций B, (уровень достоверности доказательств - 2b)
Физиотерапевтические методы лечения
Физиотерапевтические методы лечения
Физиотерапевтические методы лечения, а также искусственные и природные курортные факторы применяют в комплексе с наружной терапией и фармакотерапией. Основное место занимает ультрафиолетовое облучение, оказывающее хороший терапевтический эффект при различных стадиях АтД.
У больных АтД применяют:
У больных АтД применяют:
-
широкополосную фототерапию (UVA+UVB = 290-400 нм)
-
узкополосную фототерапию UVB (311-313 нм)
-
UVA1 (340-400 нм)
Комментарии: За исключением UVA1, фототерапию не назначают при обострении АтД, целесообразно ее применение при тяжелом хроническом течении с преобладанием зуда и лихеноидных форм заболевания. Фототерапию не назначают детям младше 12 лет.
При тяжелом и упорном течении АтД применяют метод фотохимиотерапии или ПУВА- терапии, основа которого — сочетанное использование фотосенсибилизаторов фурокумаринового ряда и длинноволнового ультрафиолетового излучения в диапазоне волн 320–400 нм.
-
Наиболее эффективным методом для лечения АтД является узкополосная фототерапия.
Уровень убедительности рекомендаций A, (уровень достоверности доказательств – 1a).
-
Средние дозы UVA 1 также эффективны как узкополосная фототерапия.
Уровень убедительности рекомендаций A, (уровень достоверности доказательств – 1b).
-
Высокие дозы UVA 1 эффективны при тяжелом течении АтД [10].
Уровень убедительности рекомендаций A, (уровень достоверности доказательств - 1b)
-
Имеется положительный международный опыт применения интерферона гамма, который оказался умеренно эффективным у больных с тяжелым АтД [10].
Уровень убедительности доказательств A, (уровень достоверности доказательств - 1b)
-
Имеется положительный опыт применения ретиноевой кислоты на примере алитретиноина
(Уровень убедительности доказательств D, (уровень достоверности доказательств -) [10].
-
В настоящее время проводятся клинические исследования по изучению эффективности моноклональных антител к IgE (омализумаб), к ИЛ 4 и ИЛ 13 – (дупилумаб), анти CD20 антител (ритуксимаб), и других биологических препаратов [10].
Уровень убедительности доказательств C, (уровень достоверности доказательств –3b)
-
Имеются опубликованные зарубежные данные по применению витаминов, в особенности, высоких доз витамина Е и D при тяжелом АтД, однако число исследований недостаточно для определения уровня доказательности рекомендаций [10].
Медицинская реабилитация
Реабилитация.
-
У всех пациентов с АтД рекомендуется включать в программу реабилитации обучение пациентов и методы физической реабилитации [151].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: Использование лазерного излучения оказываетвыраженное положительное влияние на трофику тканей и иммуностимулирующее действие. Установлено положительное влияние низкоинтенсивного лазерного излучения инфракрасного и красного диапазонов при воздействии на область проекции сосудов (в локтевом сгибе, подколенных ямках), печени, надпочечников и на точки акупунктуры. Важно, что у больных с дермато-респираторным синдромом одновременно улучшается состояние кожи и уменьшаются клинические симптомы бронхиальной астмы [11, 12].
С учетом положительного влияния ультразвука на функциональное состояние различных регулирующих систем организма и ферментативную активность, его рассасывающего и противовоспалительного действий показано включение этого метода в комплексную терапию АД, особенно при пролиферативной и смешанной формах заболевания [13].
Одним из немедикаментозных методов лечения различных дерматозов, в том числе АД, является светотерапия: общее или локальное ультрафиолетовое облучение кожи с помощью ртутно-кварцевых ламп, селективная фототерапия (СФТ), фотохимиотерапия. В лечебных целях используют ультрафиолетовые лучи А (УФА- лучи) с длиной волны 320—400 нм,в том числе УФА-лучи 1 (350—400 нм) и УФА-лучи 2 (320—340 нм); ультрафиолетовые лучи В (УФВ-лучи) с длиной волны 280—350 нм, в том числе с узким спектром диапазона волн: 300—311 нм. В детской практике наиболее широко применяют СФТ, терапевтический эффект которой связан с УФА- и УФВлучами (280—320 нм). Метод СФТ применяется у детей с 5-летнего возраста, повышает эффективность лечения и увеличивает продолжительность ремиссии больных АД, что существенно отражается на качествеих жизни [14, 15]. Использование светотерапии может уменьшить потребность в топических стероидах и местном применении иммуномодуляторов. В последнее время широко применяется более щадящий, мягкий вид светотерапии — поляризованный свет. Установлена высокая эффективность применения поляризованного света при АД у детей, он способствует регрессу кожного воспалительного процесса, уменьшению отека, зуда, экскориаций, снижает уровень общего IgE и степень выраженности аллергического воспаления кожи, оказывает мембраностабилизирующее действие на клетки организма, повышает адаптационно-компенсаторные возможности за счет сбалансированности процессов перекисного окисления липидов в мембранах эритроцитов [16].
С учетом положительного влияния ультразвука на функциональное состояние различных регулирующих систем организма и ферментативную активность, его рассасывающего и противовоспалительного действий показано включение этого метода в комплексную терапию АД, особенно при пролиферативной и смешанной формах заболевания [13].
Одним из немедикаментозных методов лечения различных дерматозов, в том числе АД, является светотерапия: общее или локальное ультрафиолетовое облучение кожи с помощью ртутно-кварцевых ламп, селективная фототерапия (СФТ), фотохимиотерапия. В лечебных целях используют ультрафиолетовые лучи А (УФА- лучи) с длиной волны 320—400 нм,в том числе УФА-лучи 1 (350—400 нм) и УФА-лучи 2 (320—340 нм); ультрафиолетовые лучи В (УФВ-лучи) с длиной волны 280—350 нм, в том числе с узким спектром диапазона волн: 300—311 нм. В детской практике наиболее широко применяют СФТ, терапевтический эффект которой связан с УФА- и УФВлучами (280—320 нм). Метод СФТ применяется у детей с 5-летнего возраста, повышает эффективность лечения и увеличивает продолжительность ремиссии больных АД, что существенно отражается на качествеих жизни [14, 15]. Использование светотерапии может уменьшить потребность в топических стероидах и местном применении иммуномодуляторов. В последнее время широко применяется более щадящий, мягкий вид светотерапии — поляризованный свет. Установлена высокая эффективность применения поляризованного света при АД у детей, он способствует регрессу кожного воспалительного процесса, уменьшению отека, зуда, экскориаций, снижает уровень общего IgE и степень выраженности аллергического воспаления кожи, оказывает мембраностабилизирующее действие на клетки организма, повышает адаптационно-компенсаторные возможности за счет сбалансированности процессов перекисного окисления липидов в мембранах эритроцитов [16].
Поляризованный свет при АД более эффективен при воздействии на очаги поражения и на сегментарно-рефлекторные зоны шейно-грудного или пояснично- крестцового отделов позвоночника в зависимости от локализации процесса. Значимостьполяризованного света при АД определяется тем,что его можно использовать во все периоды заболевания с первых месяцев жизни ребенка.
На основе проведенных исследований доказана возможность применения селективной хромотерапии синего и зеленого спектров у детей с АД. Установлена целесообразность воздействия селективной хромотерапии синего спектра на проекцию очагов поражения кожи и зеленого — на рефлекторно-сегментарные зоны у детей с АД среднетяжелого и легкого течения в период хронической или подострой фазы, что подтверждается снижением выраженности объективных симптомов (отек, гиперемия, наличие папулезных высыпаний, корок), значительным уменьшением площади поражения кожи, а также интенсивности зуда и нарушения сна [17].
В лечении АД широко используется лекарственный электрофорез. При этом методе лечебный эффект формируется за счет сочетанного влияния электрического тока и лекарственного препарата, который вводится либо через слизистую носовых ходов, либо по общей методике. Использование для электрофореза антигистаминных препаратов или сернокислой магнезии оказывает гипосенсибилизирующее и противоотечное действия.
Имеются сообщения об успешном применении галотерапии в медицинской реабилитации детей с заболеваниями кожи (аллергический дерматит, экзема, псориаз и др.). Сухой солевой аэрозоль оказывает положительное влияние на динамику клинических симптомов АД, что проявляется уменьшением зуда и сухости кожных покровов. Клинические наблюдения выявили выраженный терапевтический эффект галотерапии, характеризующийся противовоспалительным, гипосенсибилизирующим и иммунокорригирующим действиями [18—20]. Быстрому регрессу клинических проявлений АД у детей, особенно со среднетяжелым течением заболевания, и у пациентов с младенческой формой способствует применение динамической электронейростимуляции. Возникающая в ответ на ритмическую стимуляцию импульсными токами фибрилляция мышц кожи и гладких мышц артериол активизирует процессы разрушения в болевом очаге брадикинина, ацетилхолина, гистамина. В месте воздействия активируется клеточное дыхание, повышаются защитные свойства тканей. Усиление локального кровотока обеспечивает приток крови к ишемизированным тканям. Уменьшение периневрального отека улучшает возбудимость и проводимость кожных афферентов [21].
На основании проведенных исследований доказана высокая эффективность массажа эластичным псевдокипящим слоем, при АД он оказывает благо программа обучения пациентов с БА должна включать предоставление информации о заболевании, составление индивидуального плана лечения для пациента, и обучение технике управляемого самоведения. Физическая реабилитация улучшает сердечно- легочную функцию. В результате проведения тренировки при физической нагрузке увеличивается максимальное потребление кислорода и увеличивается максимальная вентиляция легких. По имеющимся наблюдениям применение тренировки с аэробной нагрузкой, плавание, тренировка инспираторной мускулатуры с пороговой дозированной нагрузкой улучшают течение БА.
Реабилитация пациентов с АтД включает санаторно-курортное лечение в санаториях дерматологического профиля.
Профилактика
Профилактика и диспансерное наблюдение
Профилактика направлена на сохранение длительной ремиссии и предупреждение обострений и включает элиминационные мероприятия, выполнение пациентом рекомендаций по уходу за кожей даже при отсутствии признаков воспаления, своевременное лечение сопутствующей патологии. Неотъемлемой частью реабилитационных и профилактических мер является обучение.
Цель обучения — сообщить пациенту с АтД и членам его семьи информацию, необходимую для максимально эффективного лечения. Обучение предусматривает проведение просветительской работы среди всех участников лечебного процесса: самого больного АтД, членов его семьи, медицинских работников.
Наиболее распространенная форма обучения — аллергошколы. Примерный план занятий в аллергошколе для больных АтД — включает следующие темы:
Цель обучения — сообщить пациенту с АтД и членам его семьи информацию, необходимую для максимально эффективного лечения. Обучение предусматривает проведение просветительской работы среди всех участников лечебного процесса: самого больного АтД, членов его семьи, медицинских работников.
Наиболее распространенная форма обучения — аллергошколы. Примерный план занятий в аллергошколе для больных АтД — включает следующие темы:
- знакомство с проблемой аллергии в целом;
- анатомия и физиология кожи;
- что такое АтД и как его распознавать;
- причины возникновения и факторы риска АтД;
- взаимосвязь АтД с респираторной аллергией;
- основные принципы лечения АтД;
- барьерная функция кожи и вторичные инфекции;
- основные правила личной гигиены и ухода за кожей при АтД;
- элиминационные мероприятия при АтД;
- основы рационального питания при АтД;
- лекарственная терапия АтД;
- правильное использование наружных средств при АтД;
- профилактика и лечение обострений АтД.
Образовательные программы (такие как аллергошколы, различные тренинги) для детей с АтД, их родителей и взрослых доказали свою целесообразность во многих странах[9].
Уровень убедительности доказательств А, (уровень достоверности доказательств - 1a)
Основные положения профилактических мер:
- Убедительных данных об эффективности гипоаллергенных или элиминационных диет во время беременности не получено.
- Назначение гипоаллергенных диет женщинам из групп риска во время лактации значительно уменьшает частоту возникновения АтД у детей.
- На протяжении первых 4 месяцев жизни ребенку из группы риска рекомендуют исключительно грудное вскармливание, при необходимости для докармливания разрешают профилактические или лечебно-профилактические гипоаллергенные смеси (на основе гидролизатов молочного белка).
- Введение прикормов оправдано только после 4-го месяца жизни продуктами с низкой сенсибилизирующей активностью;
- Имеются данные о назначении с профилактическими целями пробиотиков, содержащих лактобактерии, беременным и новорожденным из групп риска (возможен положительный эффект за счет индукции синтеза ИФН ?);
- Обучение больных профилактическим мероприятиям и правильному уходу за кожей.
- Контроль за факторами внешней среды должен предусматривать:
- Исключение воздействия табачного дыма (курение недопустимо во время беременности и лактации; пассивное курение исключают с первых дней жизни ребенка);
- Уменьшение экспозиции аллергенов в первые годы жизни (домашняя пыль и клещи домашней пыли, животные, тараканы);
- Поддержание низкой влажности и адекватной вентиляции в помещениях, где находится ребенок (исключение сырости);
- Уменьшение воздействия поллютантов.
Любые профилактические элиминационные мероприятия, назначаемые на длительное время, могут оказывать негативное влияние на членов семьи, ухудшая качество их жизни, поэтому в профилактические программы включают только мероприятия с доказанной эффективностью.
Профилактика АтД предполагает образовательные программы для больных атопическим дерматитом.
Обучение необходимо для достижения эффекта лечебных и профилактических мероприятий. В настоящее время требуется изменение сложившейся ранее практики лечения, нередко ограничивавшейся лишь местной терапией АтД. Эта тактика повсеместно должна быть заменена эффективной системой оказания помощи больным с АтД на различных этапах (поликлиника, общесоматический стационар, специализированное отделение, санаторий), направленной на проведение длительного противовоспалительного лечения с регулярным контролем его эффективности и коррекцией при необходимости.
Внедрить такую систему в практику невозможно без активного участия больного и членов его семьи. Больной с АтД, особенно в сочетании с БА и (или) АР, требует соблюдения режима, соответствующего тяжести и особенностям болезни, разработки индивидуального плана лечения, учитывающего гипоаллергенный быт, а также адекватность физической нагрузки и оптимальный психологический микроклимат в семье. Образование больных с АтД – это неотъемлемая составная часть программ их лечения.
Цель обучения, являющегося непрерывным процессом обеспечить страдающего АтД, и его семью необходимой информацией для успешного контроля течения болезни и действий в соответствии с планом медикаментозного лечения, разработанным врачом. Акцент в обучении должен делаться на развитие постоянного партнерства между врачом, больным и членами его семьи.
Обучение необходимо для достижения эффекта лечебных и профилактических мероприятий. В настоящее время требуется изменение сложившейся ранее практики лечения, нередко ограничивавшейся лишь местной терапией АтД. Эта тактика повсеместно должна быть заменена эффективной системой оказания помощи больным с АтД на различных этапах (поликлиника, общесоматический стационар, специализированное отделение, санаторий), направленной на проведение длительного противовоспалительного лечения с регулярным контролем его эффективности и коррекцией при необходимости.
Внедрить такую систему в практику невозможно без активного участия больного и членов его семьи. Больной с АтД, особенно в сочетании с БА и (или) АР, требует соблюдения режима, соответствующего тяжести и особенностям болезни, разработки индивидуального плана лечения, учитывающего гипоаллергенный быт, а также адекватность физической нагрузки и оптимальный психологический микроклимат в семье. Образование больных с АтД – это неотъемлемая составная часть программ их лечения.
Цель обучения, являющегося непрерывным процессом обеспечить страдающего АтД, и его семью необходимой информацией для успешного контроля течения болезни и действий в соответствии с планом медикаментозного лечения, разработанным врачом. Акцент в обучении должен делаться на развитие постоянного партнерства между врачом, больным и членами его семьи.
Информация
Источники и литература
-
Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2024
- Клинические протоколы, руководства, рекомендации Министерства здравоохранения Республики Узбекистан 2024 - 1. Атопический дерматит: рекомендации для практических врачей. Российский национальный согласительный документ под общей ред. Хаитова Р.М., Кубановой А.А., коллектив авторов, 2002, Москва, кн. № 1, 192 с. 2. PalmerC.N., IrvineA.D., Terron-KwiatkowskiA., ZhaoY., LiaoH., LeeS.P. etal. Common loss- of-function variants of the epidermal barrier protein filaggrin are a major predisposing factor for atopic dermatitis. Nat. Genet. 2006;38:441–446. 3. Bieber Th. Atopic dermatitis: from the clinical phenotype to the molecular taxonomy and stratified medicine. Allergy. 2012; 67, p. 1475–1482 4. McGirt LY, Beck LA. Innate immune defects in atopic dermatitis. J Allergy Clin Immunol. 2006;118:202–208. 5. Schauber J., Gallo R.L. Antimicrobial peptides and the skin immune defense system. J. Allergy Clin. Immunol., 2008; 122(2): 261–266. 6. Mothes N, Niggemann B, Jenneck C, Hagemann T, Weidinger S, Bieber T, et al. The cradle of IgE autoreactivity in atopic eczema lies in early infancy. JAllergyClinImmunol. 2005;116:706– 709. 7. BieberT. Atopic Dermatitis. Ann Dermatol. 2010; №n22 (2): 125–137. 8. Аллергология и иммунология. Национальное руководство под общ. ред. Хаитова Р.М. и Ильиной Н.И. М., Геотар-Медиа, 2009, 650с. 9. Ring J, Alomar A, Bieber Tet al.,Guidelines for treatment of atopic eczema (atopic dermatitis) Part I.J Eur Acad Dermatol Venereol. 2012 Aug;26(8):1045-60. 10. Ring J, Alomar A, Bieber Tet al.,Guidelines for treatment of atopic eczema (atopic dermatitis) Part II. J Eur Acad Dermatol Venereol. 2012 Sep;26(9):1176-93. 11. Сoгласительный документ WAO-ARIA-GA2LEN по молекулярной диагностике. Российский алл журнал, 2013, приложение, 20 с. 12. Hanifin JM, Rajka G. Diagnostic features of atopic dermatitis. Acta Derm Venerol. 1980, v. 92 (suppl), p. 44-47. 13. Eichenfield LF, Tom WL, Chamlin SL et al. Guidelines of care for the management of atopic dermatitis: section 1. Diagnosis and assessment of atopic dermatitis. J Am Acad Dermatol. 2014, v.70, p.338-351. 14. Akdis C.A. Review article Diagnosis and treatment of atopic dermatitis in children and adults: Europian Academy of Allergology and Clinical Immunology/ American Academy of Allergy, Asthma and Immunology. PRACTALL Consensus report. Allergy. 2006, v. 61, p.969-987 15. Eichenfield LF., Tom WL., Berger TG et al. Guidelines of care for the management of atopic dermatitis: section 2. Management and treatment of atopic dermatitis with topical therapies.J Am Acad Dermatol. 2014 Jul, v.71(1), p.116-32. 16. Ray, A., Camiolo, M., Fitzpatrick, A., Gauthier, M., & Wenzel, S. E. (2020). Are We Meeting the Promise of Endotypes and Precision Medicine in Asthma? Physiological Reviews, 100(3), 983–1017. https://doi.org/10.1152/PHYSREV.00023.2019 17. Moore, W. C., Meyers, D. A., Wenzel, S. E., Teague, W. G., Li, H., Li, X., D’Agostino, R., Castro, M., Curran-Everett, D., Fitzpatrick, A. M., Gaston, B., Jarjour, N. N., Sorkness, R., Calhoun, W. J., Chung, K. F., Comhair, S. A. A., Dweik, R. A., Israel, E., Peters, S. P., … 18. Bleecker, E. R. (2010). Identification of asthma phenotypes using cluster analysis in the Severe Asthma Research Program. American Journal of Respiratory and Critical Care Medicine, 181(4), 315–323. https://doi.org/10.1164/RCCM.200906-0896OC 19. Abbafati, C., Abbas, K. M., Abbasi, M., Abbasifard, M., Abbasi-Kangevari, M., Abbastabar, H., Abd-Allah, F., Abdelalim, A., Abdollahi, M., Abdollahpour, I., Abedi, A., Abedi, P., Abegaz, K. H., Abolhassani, H., Abosetugn, A. E., Aboyans, V., Abrams, E. M., Abreu, L. G., Abrigo, M. R. M., … Murray, C. J. L. (2020). Global burden of 369 diseases and injuries in 204 countries and territories, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet (London, England), 396(10258), 1204– 1222. https://doi.org/10.1016/S0140-6736(20)30925-9 20. GLOBAL STRATEGY FOR ASTHMA MANAGEMENT AND PREVENTION Updated 21. 2020. (2020). www.ginasthma.org 22. Chuchalin, A. G., Khaltaev, N., Antonov, N. S., Galkin, D. V., Manakov, L. G., Antonini, P., Murphy, M., Solodovnikov, A. G., Bousquet, J., Pereira, M. H. S., & Demko, I. V. (2014). Chronic respiratory diseases and risk factors in 12 regions of the Russian Federation. International Journal of Chronic Obstructive Pulmonary Disease, 9, 963–974. https://doi.org/10.2147/COPD.S67283 23. Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика», IV издание. – М., 2012. – 182 с. 24. Most Recent Asthma Data | CDC. (n.d.). Retrieved February 9, 2024, from https://www.cdc.gov/asthma/most_recent_data.htm 25. mednet.ru — Яндекс: нашлось 4 тыс. результатов. (n.d.). Retrieved February 8, 2024, from https://yandex.ru/search/?text=mednet.ru&lr=213&clid=2270455&win=587 26. ФГБУ «ЦНИИОИЗ» Минздрава России - Главная страница. (n.d.). Retrieved February 9, 2024, from https://mednet.ru/ 27. Krahn, M., Berka, C., Langlois, P., & Detsky, A. S. (1996). Direct and indirect costs of asthma in Canada, 1990. CMAJ : Canadian Medical Association Journal = Journal de l’Association Medicale Canadienne. 28. Braman, S. S., & Kaemmerlen, J. T. (1990). Intensive Care of Status Asthmaticus: A 10- Year Experience. JAMA, 264(3), 366–368. https://doi.org/10.1001/JAMA.1990.03450030090038 29. Weber, E. J., Silverman, R. A., Callaham, M. L., Pollack, C. V., Woodruff, P. G., Clark, S., & Camargo, C. A. (2002). A prospective multicenter study of factors associated with hospital admission among adults with acute asthma. American Journal of Medicine, 113(5), 371–378. https://doi.org/10.1016/S0002-9343(02)01242-1 30. Salmeron, S., Liard, R., Elkharrat, D., Muir, J. F., Neukirch, F., & Ellrodt, A. (2001). Asthma severity and adequacy of management in accident and emergency departments in France: A prospective study. Lancet, 358(9282), 629–635. https://doi.org/10.1016/S0140- 31. 6736(01)05779-8 32. Krishnan, V., Diette, G. B., Rand, C. S., Bilderback, A. L., Merriman, B., Hansel, N. N., & Krishnan, J. A. (2006). Mortality in patients hospitalized for asthma exacerbations in the United States. American Journal of Respiratory and Critical Care Medicine, 174(6), 633– 638. https://doi.org/10.1164/RCCM.200601-007OC 33. Ненашева Н.М. Клинические фенотипы атопической бронхиальной астмы: диагностика и лечение. Palmarium Academic Publishing, 2012, 319с. (n.d.). Retrieved February 9, 2024, from https://bookmix.ru/book.phtml?id=2271191 34. Moore, W. C., Meyers, D. A., Wenzel, S. E., Teague, W. G., Li, H., Li, X., D’Agostino, R., Castro, M., Curran-Everett, D., Fitzpatrick, A. M., Gaston, B., Jarjour, N. N., Sorkness, R., Calhoun, W. J., Chung, K. F., Comhair, S. A. A., Dweik, R. A., Israel, E., Peters, S. P., 35. … Bleecker, E. R. (2010). Identification of asthma phenotypes using cluster analysis in the Severe Asthma Research Program. American Journal of Respiratory and Critical Care Medicine, 181(4), 315–323. https://doi.org/10.1164/RCCM.200906-0896OC 36. Pearce, N., Pekkanen, J., & Beasley, R. (1999). How much asthma is really attributable to atopy? Thorax, 54(3), 268–272. https://doi.org/10.1136/THX.54.3.268 37. Reddel, H. K., Taylor, D. R., Bateman, E. D., Boulet, L. P., Boushey, H. A., Busse, W. W., Casale, T. B., Chanez, P., Enright, P. L., Gibson, P. G., De Jongste, J. C., Kerstjens, H. A. M., Lazarus, S. C., Levy, M. L., O’Byrne, P. M., Partridge, M. R., Pavord, I. D., Sears, M. R., Sterk, P. J., … Wenzel, S. E. (2009). An official American Thoracic Society/European Respiratory Society statement: asthma control and exacerbations: standardizing endpoints 38. for clinical asthma trials and clinical practice. American Journal of Respiratory and Critical Care Medicine, 180(1), 59–99. https://doi.org/10.1164/RCCM.200801-060ST 39. Taylor, D. R., Bateman, E. D., Boulet, L. P., Boushey, H. A., Busse, W. W., Casale, T. B., Chanez, P., Enright, P. L., Gibson, P. G., De Jongste, J. C., Kerstjens, H. A. M., Lazarus, 40. S. C., Levy, M. L., O’Byrne, P. M., Partridge, M. R., Pavord, I. D., Sears, M. R., Sterk, P. J., Stoloff, S. W., … Reddel, H. K. (2008). A new perspective on concepts of asthma severity and control. The European Respiratory Journal, 32(3), 545–554. https://doi.org/10.1183/09031936.00155307 41. Chung, K. F., Wenzel, S. E., Brozek, J. L., Bush, A., Castro, M., Sterk, P. J., Adcock, I. M., Bateman, E. D., Bel, E. H., Bleecker, E. R., Boulet, L. P., Brightling, C., Chanez, P., Dahlen, 42. S. E., Djukanovic, R., Frey, U., Gaga, M., Gibson, P., Hamid, Q., … Teague, W. 43. G. (2014). International ERS/ATS guidelines on definition, evaluation and treatment of severe asthma. The European Respiratory Journal, 43(2), 343–373. https://doi.org/10.1183/09031936.00202013 44. GINA Main Report 2023 Front Cove. Global Strategy for Asthma Management and Prevention, Global Initiative for Asthma (GINA) 2023. [Электронный ресурс], 10.06.2023. URL: http://www.ginasthma.org/. 45. Barnes, P. J., Szefler, S. J., Reddel, H. K., & Chipps, B. E. (2019). Symptoms and perception of airway obstruction in asthmatic patients: Clinical implications for use of reliever medications. The Journal of Allergy and Clinical Immunology, 144(5), 1180– 1186. https://doi.org/10.1016/J.JACI.2019.06.040 46. Killian, K. J., Watson, R., Otis, J., St. Amand, T. A., & O’Byrne, P. M. (2000). Symptom perception during acute bronchoconstriction. American Journal of Respiratory and Critical Care Medicine, 162(2 Pt 1), 490–496. https://doi.org/10.1164/AJRCCM.162.2.9905079 47. Авдеев С.Н. Дыхательная недостаточность. Практическая пульмонология. 2004., 48. №1, с.21-26. 49. Горячкина Л.А., Ненашева Н.М., Тотикова М.Ч. Шмелева Н.В. Особенности бронхиальной астмы у подростков мужского пола. Пульмонология, 2008, №2, с.15- 50. 19. https://doi.org/10.18093/0869-0189-2008-0-2-15-19 51. Шальнова О.А., Кириллов М.М., Орлова М.М. Изучение патологии легких у юношей призывного возраста как возможность исследования ранних форм бронхиальной астмы и хронического бронхита. Пульмонология, 2005, №2, с.57-62. https://doi.org/10.18093/0869-0189-2005-0-2-57-62 52. Жолондзь Н.Н., Воронина Н.В., Мамровская Т.П., Щукина М.П., Долгаева Н.С. Особенности течения бронхиальной астмы у подростков и юношей призывного возраста. Дальневосточный медицинский журнал. 2011, №3. https://cyberleninka.ru/article/n/osobennosti-techeniya-bronhialnoy-astmy-u-podrostkov-i- yunoshey-prizyvnogo-vozrasta 53. Астафьева Н.Г. (2005). Бронхиальная астма у подростков. Аллергология, №2, с.12– 16. 54. Емельянов А.В. Особенности бронхиальной астмы в пожилом и старческом возрасте. РМЖ, 2016, №16, с. 1102-1107. https://doi.org/10.18565/PHARMATECA.2020.5.85-94 55. Mellis, C. (2009). Respiratory noises: how useful are they clinically? Pediatric Clinics of North America, 56(1), 1–17. https://doi.org/10.1016/J.PCL.2008.10.003 56. Louis, R., Satia, I., Ojanguren, I., Schleich, F., Bonini, M., Tonia, T., Rigau, D., Brinke, A. ten, Buhl, R., Loukides, S., Kocks, J. W. H., Boulet, L. P., Bourdin, A., Coleman, C., Needham, K., Thomas, M., Idzko, M., Papi, A., Porsbjerg, C., … Usmani, O. S. (2022). 57. European Respiratory Society Guidelines for the Diagnosis of Asthma in Adults. The European Respiratory Journal, 60(3). https://doi.org/10.1183/13993003.01585-2021 58. Вишнева Е. А., Намазова-Баранова Л. С., Селимзянова Л. Р., Алексеева А. А., Новик Г. А., Эфендиева К. Е., Левина Ю. Г., Добрынина Е. А. Актуальная тактика ведения детей с бронхиальной астмой // Педиатрическая фармакология. 2017. № 14 (6). С. 443– 59. 458. https://doi.org/10.15690/pf.v14i6.1828 60. Reddel, H. K., Taylor, D. R., Bateman, E. D., Boulet, L. P., Boushey, H. A., Busse, W. W., Casale, T. B., Chanez, P., Enright, P. L., Gibson, P. G., De Jongste, J. C., Kerstjens, H. A. M., Lazarus, S. C., Levy, M. L., O’Byrne, P. M., Partridge, M. R., Pavord, I. D., Sears, M. R., Sterk, P. J., … Wenzel, S. E. (2009). An official American Thoracic Society/European Respiratory Society statement: asthma control and exacerbations: standardizing endpoints for clinical asthma trials and clinical practice. American Journal of Respiratory and Critical Care Medicine, 180(1), 59–99. https://doi.org/10.1164/RCCM.200801-060ST 61. Thomas, M., Kay, S., Pike, J., Williams, A., Carranza Rosenzweig, J. R., Hillyer, E. V., & Price, D. (2009). The Asthma Control Test (ACT) as a predictor of GINA guideline- defined asthma control: analysis of a multinational cross-sectional survey. Primary Care Respiratory Journal : Journal of the General Practice Airways Group, 18(1), 41–49. https://doi.org/10.4104/PCRJ.2009.00010 62. Liu, A. H., Zeiger, R., Sorkness, C., Mahr, T., Ostrom, N., Burgess, S., Rosenzweig, J. C., & Manjunath, R. (2007). Development and cross-sectional validation of the Childhood 63. Asthma Control Test. The Journal of Allergy and Clinical Immunology, 119(4), 817–825. https://doi.org/10.1016/J.JACI.2006.12.662 64. Juniper, E. F., Gruffydd-Jones, K., Ward, S., & Svensson, K. (2010). Asthma Control Questionnaire in children: validation, measurement properties, interpretation. The European 65. Respiratory Journal, 36(6), 1410–1416. https://doi.org/10.1183/09031936.00117509 66. Nguyen, J. M., Holbrook, J. T., Wei, C. Y., Gerald, L. B., Teague, W. G., & Wise, R. A. (2014). Validation and psychometric properties of the Asthma Control Questionnaire among children. The Journal of Allergy and Clinical Immunology, 133(1). https://doi.org/10.1016/J.JACI.2013.06.029 67. Авдеев С. Н. Опросник ACQ – новый инструмент оценки контроля над бронхиальной астмой. Пульмонология. 2011. № 2. с.93–99. https://doi.org/10.18093/0869-0189-2011- 0-2-276-287 68. Murphy, K. R., Zeiger, R. S., Kosinski, M., Chipps, B., Mellon, M., Schatz, M., Lampl, K., Hanlon, J. T., & Ramachandran, S. (2009). Test for respiratory and asthma control in kids 69. (TRACK): a caregiver-completed questionnaire for preschool-aged children. The Journal of Allergy and Clinical Immunology, 123(4). https://doi.org/10.1016/J.JACI.2009.01.058 70. Papadopoulos, N. G., Arakawa, H., Carlsen, K. H., Custovic, A., Gern, J., Lemanske, R., Le Souef, P., Mäkelä, M., Roberts, G., Wong, G., Zar, H., Akdis, C. A., Bacharier, L. B., Baraldi, E., Van Bever, H. P., De Blic, J., Boner, A., Burks, W., Casale, T. B., … Zeiger, 71. R. S. (2012). International consensus on (ICON) pediatric asthma. Allergy, 67(8), 976– 997. https://doi.org/10.1111/J.1398-9995.2012.02865.X 72. Bousquet, J., Boulet, L. P., Peters, M. J., Magnussen, H., Quiralte, J., Martinez-Aguilar, N. E., & Carlsheimer, Å. (2007). Budesonide/formoterol for maintenance and relief in uncontrolled asthma vs. high-dose salmeterol/fluticasone. Respiratory Medicine, 101(12), 2437–2446. https://doi.org/10.1016/J.RMED.2007.07.014 73. Buhl, R., Kuna, P., Peters, M. J., Andersson, T. L. G., Naya, I. P., Peterson, S., & Rabe, K. 74. F. (2012). The effect of budesonide/formoterol maintenance and reliever therapy on the risk of severe asthma exacerbations following episodes of high reliever use: an exploratory analysis of two randomised, controlled studies with comparisons to standard therapy. Respiratory Research, 13(1). https://doi.org/10.1186/1465-9921-13-59 75. Albers, F. C., Licskai, C., Chanez, P., Bratton, D. J., Bradford, E. S., Yancey, S. W., Kwon, N., & Quirce, S. (2019). Baseline blood eosinophil count as a predictor of treatment 76. response to the licensed dose of mepolizumab in severe eosinophilic asthma. Respiratory Medicine, 159. https://doi.org/10.1016/J.RMED.2019.105806 77. Bush, A. (2018). Management of asthma in children. Minerva Pediatrica, 70(5), 444–457. https://doi.org/10.23736/S0026-4946.18.05351-3 78. Price, D. B., Rigazio, A., Campbell, J. D., Bleecker, E. R., Corrigan, C. J., Thomas, M., Wenzel, S. E., Wilson, A. M., Small, M. B., Gopalan, G., Ashton, V. L., Burden, A., Hillyer, 79. E. V., Kerkhof, M., & Pavord, I. D. (2015). Blood eosinophil count and prospective annual asthma disease burden: a UK cohort study. The Lancet. Respiratory Medicine, 3(11), 849– 858. https://doi.org/10.1016/S2213-2600(15)00367-7 80. Kerkhof, M., Tran, T. N., Berge, M. van den, Brusselle, G. G., Gopalan, G., Jones, R. C. M., Kocks, J. W. H., Menzies-Gow, A., Nuevo, J., Pavord, I. D., Rastogi, S., & Price, D. 81. B. (2018). Association between blood eosinophil count and risk of readmission for patients with asthma: Historical cohort study. PloS One, 13(7). https://doi.org/10.1371/JOURNAL.PONE.0201143
Информация
Список основных авторов, дополнительного коллектива авторов:
-
Разикова И.С. - д.м.н., профессор, директор РСНПМЦАКИ
-
Дустбабаева Н. Д. - доцент, Центра развития профессиональной квалификации медицинских работников , к.м.н.
-
Айдарова Н.П - заместитель директора по научной работе РСНПМЦАКИ,PhD
-
Кузиев Г. Э -заместитель директора по лечебной работе РСНПМЦАКИ,
-
Ишмухаммедова Ш. Б - заведующая отделом аллергологии РСНПМЦАКИ
-
Қудратуллаева Б. Т - заведующая отделом аллергологии РСНПМЦАКИ
-
Бойбекова В.Ф – ученый секретарь РСНПМЦАКИ
-
Акромов А. Т - врач аллерголог РСНПМЦАКИ
-
Хасанова.Ф.Р - врач аллерголог РСНПМЦАКИ
-
Тураев Н. Т - врач аллерголог РСНПМЦАКИ
Рецензенты:
-
Ирсалиева Ф.Х Профессор, кафедры аллергологии , клинической иммунологии и сестринского дела, д.м.н
-
Мавлянова Ш. З. Профессор, Республиканский Центр Дермато-венерологии и косметологии, д.м.н
Внешняя экспертная оценка:
Фомина Дарья Сергеевна Руководитель Московского городского научно-практического центра аллергологии и иммунологии, врач аллерголог-иммунолог высшей квалификационной категории, к.м.н, главный внештатный аллерголог-иммунолог доцент кафедры клинической иммунологии и аллергологии ФГАОУ ВО Первого МГМУ им. И.М. Сеченова.
Клинический протокол обсужден и рекомендован к утверждению путем достижения неформального консенсуса на заключительном Совещании рабочей группы с участием профессорско-преподавательского состава высших учебных заведений, организаторов здравоохранения (директор РСНПМЦАИКИ и их заместителей), врачей региональных учреждений системы аллергологии в онлайн-формате 06 ноябрь 2023 г., протокол №7.
Клинический протокол рассмотрен и утвержден Ученым Советом Республиканского специализированного научно-практического медицинского центра аллергологии и клинической иммунологии 28 ноября 2023 г., протокол №8
Список сокращений
|
АГ
|
антигистаминные препараты
|
|
АЗ
|
аллергические заболевания
|
|
АПК
|
антиген – презентирующие клетки
|
|
АР
|
аллергический ринит
|
|
АСИТ
|
аллерген – специфическая иммунотерапия
|
|
АтД
|
атопический дерматит
|
|
БА
|
бронхиальная астма
|
|
ДК
|
дендритные клетки
|
|
ГКС
|
глюко-кортикостероиды
|
|
ИФА
|
иммуноферментный анализ
|
|
КИ
|
клинические исследования
|
|
КЛ
|
клетки Лангерганса
|
|
ЛС
|
лекарственные средства
|
|
МКБ 10
|
международная классификация болезней 10 пересмотра
|
|
нм
|
нанометр
|
|
РКИ
|
рандомизированное контролируемое исследование
|
|
ТГКС
|
топические глюко-кортикостероиды
|
|
ТИК
|
топические ингибиторы кальциневрина
|
|
ФВД
|
функция внешнего дыхания
|
|
ARA
|
atopy-relatedauto – antibody – аутоантитело, связанное с атопией
|
|
CD
|
clusterofdifferentiation – кластер дифференцировки
|
|
Fc?R
|
высоко аффинный рецептор к Fc- фрагменту IgE
|
|
GM-CSF
|
гранулоцитарно-макрофагальный колониестимулирующий фактор
|
|
HBD
|
humanB defesine – человеческий дефензин
|
|
HNP
|
humanneutrophilspeptide – человеческий нейтро фильный пептид
|
|
hCAP18
|
человеческий катионный антимикробный белок
|
|
ICAM-1 1
|
Inter-Cellular Adhesion Molecule - молекула межклеточной адгезии 1
|
|
IgE
|
иммуноглобулин класса Е
|
|
IgM
|
иммуноглобулин класса M
|
|
IFN
|
интерферон
|
|
IL
|
интерлейкин
|
|
ISAC – ImmunoSolidPhaseAllergyChip
|
Иммунохемилюминесценция на иммунном твердофазном аллергочипе
|
|
LEDGF -lensepithelium- derivedgrowthfactor
|
lensepithelium-derivedgrowthfactor – эпителиальный фактор роста
|
|
DSF7013
|
белокDSF7013
|
|
Th
|
Т-хелперы (Th1, Th2)
|
|
TSLP– Thymic stromal lymphopoietin
|
тимусно-стромальный лимфопоэтин
|
|
MnSOD – manganesesuperoxidedismutasae
|
manganesesuperoxidedismutasae – марганец супероксиддисмутаза
|
|
SCORAD – ScoringofAtopicDermatitis
|
ScoringofAtopicDermatitis – шкала для оценки степени тяжести АтД
|
Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД |
Расшифровка
|
|
1 |
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа
|
|
2 |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа
|
|
3 |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Не сравнительные исследования, описание клинического случая
|
|
5
|
Имеется лишь обоснование механизма действия или мнение экспертов
|
Шкала оценки уровней достоверности доказательств (УДД) для профилактических, лечебных, реабилитационных вмешательств
|
УДД
|
Расшифровка
|
|
1
|
Систематический обзор РКИ с применением мета-анализа
|
|
2 |
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета- анализа
|
|
3
|
Не рандомизированные сравнительные исследования, в т.ч. когортные исследования
|
|
4
|
Не сравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль»
|
|
5
|
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
|
Шкала оценки уровней убедительности рекомендаций (УУР) для профилактических, диагностических, лечебных, реабилитационных вмешательств
|
УУР
|
Расшифровка
|
|
A |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
|
|
B |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
|
|
C |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
|
Критерии оценки качества медицинской помощи
|
№
|
Критерии качества
|
Уровень достоверности доказательств
|
Уровень убедительности рекомендации
|
|
1.
|
Выполнена консультация больного дерматологом
|
А
|
1а
|
|
2.
|
Выполнена консультация больного аллергологом
|
А
|
1a
|
|
3.
|
Выполнена постановка диагноза в соответствии с диагностическими критериями
|
А
|
1a
|
|
4.
|
Выполнено определение стадии и степени тяжести АтД
|
А
|
1a
|
|
5.
|
Выполнено назначение наружной терапии топическими глюкортикостероидами в зависимости от стадии, тяжести и локализации АтД
|
А
|
1a
|
|
6.
|
Выполнено назначение наружной терапия топическими ингибиторами кальциневрина в зависимости от стадии, тяжести и локализации АтД
|
А
|
1a
|
|
7.
|
Выполнено назначение увлажняющих средств
|
А
|
1a
|
|
8.
|
Выполнено назначение системной фармакотерапии при тяжелом течении АтД
|
В
|
2a
|
|
9.
|
Выполнено стационарное лечение при тяжелом течении АтД
|
С
|
2b
|
|
10.
|
Выполнены элиминационные мероприятии в соответствии с выявленным спектром причинно – значимых аллергенов
|
А
|
1a
|
|
11.
|
Выполнено определение показаний к физиотерапевтическим методам лечения, включая фототерапию
|
С
|
2a
|
|
12.
|
Достигнуто клиническое улучшение: уменьшение клинических проявлений АтД - воспаления и зуда кожи, индекса SCORAD
|
В
|
2a
|
Приложение
Методология разработки клинических рекомендаций
Методология разработки клинических рекомендаций
Методы, использованные для сбора/селекции доказательств:
Поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств:
Доказательной базой для рекомендаций являются публикации, вошедшие в базы данных EMBASE и PubMed/MEDLINE, данные международных согласительных документов по атопическому дерматиту Европейского Дерматологического Форума European Dermatology Forum (EDF); Европейской Академии Дерматологии и Венерологии (European Academy of Dermatology and Venereology (EADV); Европейской Федерации Аллергии (European Federation of Allergy (EFA); Европейской Комиссии по Атопическому Дерматиту European Task Force on Atopic Dermatitis (ETFAD); Европейского Общества Педиатрической Дерматологии (European Society of Pediatric Dermatology (ESPD); Global Allergy and Asthma European Network (GA2LEN), 2009, 2022 .
Методы, использованные для оценки качества и силы доказательств:
Исследования оценивали с использованием методологического перечня для рандомизированных контролируемых исследований (РКИ) в соответствии с принятыми критериями для исследований в области дерматологии. На основании этих критериев и типа исследования определяли уровень доказательств (от 1а до 4), что приводило к классу рекомендаций (A-D). (таб. 1)
Таблица П1. Уровень достоверности доказательств [RingG., etal, 2012 ].
|
Уровни достоверности доказательств |
Описание |
|
1а
|
Мета-анализ РКИ
|
|
1b
|
Единичные РКИ
|
|
2a |
Cистематический обзор когортных исследований |
|
2b |
Единичные когортные исследования и/или РКИ с высоким риском систематической ошибки |
|
3a |
Систематический обзор исследований, имеющих структуру случай-контроль |
|
3b |
Единичные исследования, имеющие структуру случай- контроль |
|
4 |
Неаналитические исследования, например, сообщение о случае, ряде случаев, или когортные исследования ограниченного качества |
При подготовке рекомендаций необходимо отличать силу рекомендаций от качества соответствующих доказательств. Данная система позволяет обосновать сильные рекомендации доказательствами низкого, или, значительно реже, очень низкого качества, полученными в РКИ более низкого уровня, или в наблюдательных исследованиях.
Одновременно слабые рекомендации могут основываться на высококачественных доказательствах. Первая ситуация складывается в редких случаях, когда не доказательства из включенных исследований, а другие факторы определяют силу рекомендаций, в то время как вторая ситуация отмечается не так редко.
Таблица П2. Уровни убедительности рекомендаций
|
A
|
Высокая достоверность
|
Основана на заключениях систематических обзоров рандомизированных контролируемых испытаний. Систематический обзор получают путём системного поиска данных из всех опубликованных клинических испытаний, критической оценки их качества и обобщения результатов методом метаанализа (1a, 1b)
|
|
B
|
Умеренная достоверность
|
Основана на результатах, по меньшей мере, одного независимого рандомизированного контролируемого клинического испытания (2a, 2b, 3a, 3b)
|
|
C
|
Ограниченная достоверность
|
Основана на результатах, по меньшей мере, одного клинического испытания, не удовлетворяющего критериям качества, например, без рандомизации (4)
|
|
D
|
Неопределённая достоверность
|
Утверждение основано на мнении экспертов; клинические исследования отсутствуют (мнение экспертов)
|
Сила рекомендаций может быть оценена как «сильная» и «слабая».
«Сильная» рекомендация может быть интерпретирована как:
-
Большинство людей могут получить это вмешательство;
-
Большинство хорошо информированных людей согласились бы с таким воздействием, меньшинство – отказались бы;
-
Может использоваться как тактическое руководство, или как показатель качества.
«Слабая» рекомендация может быть интерпретирована как:
-
Большинство хорошо информированных людей согласились бы следовать предложенному варианту действия, значительная часть – нет;
-
Широкий диапазон ценности и преимуществ;
-
Разработка тактического руководства или показателя качества требует широкого обсуждения заинтересованных лиц.
Слова «мы рекомендуем» используются для сильных рекомендаций, слова «мы предлагаем» - для слабых рекомендаций.
Экономический анализ
Анализ стоимости не проводился, и публикации по фармакоэкономике не анализировались.
Метод валидации рекомендаций:
Метод валидации рекомендаций:
-
Внешняя экспертная оценка
-
Внутренняя экспертная оценка
Описание метода валидизации рекомендаций:
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать, прежде всего, то, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания.
Получены комментарии со стороны врачей первичного звена и терапевтов в отношении доходчивости изложения рекомендаций и их оценки важности рекомендаций, как рабочего инструмента повседневной практики.
Получены комментарии со стороны врачей первичного звена и терапевтов в отношении доходчивости изложения рекомендаций и их оценки важности рекомендаций, как рабочего инструмента повседневной практики.
Предварительная версия была также направлена рецензенту, не имеющему медицинского образования, для получения комментариев с точки зрения перспектив пациентов.
Комментарии, полученные от экспертов, тщательно систематизировались и обсуждались председателем и членами рабочей группы. Каждый пункт обсуждался, и вносимые в рекомендации изменения регистрировались. Если же изменения не вносились, то регистрировались причины отказа от внесения изменений.
Приложение Б. Алгоритмы ведения пациента
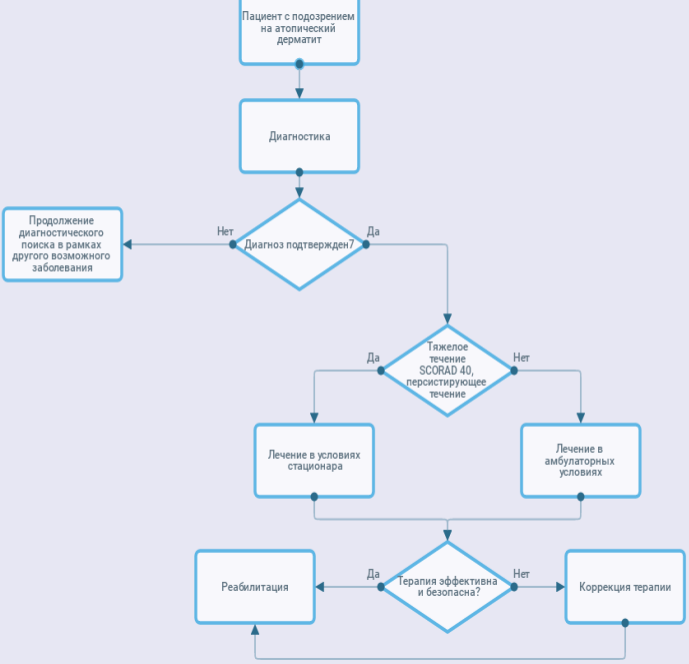
Приложение В. Информация для пациентов
Комментарии, полученные от экспертов, тщательно систематизировались и обсуждались председателем и членами рабочей группы. Каждый пункт обсуждался, и вносимые в рекомендации изменения регистрировались. Если же изменения не вносились, то регистрировались причины отказа от внесения изменений.
Приложение Б. Алгоритмы ведения пациента

Приложение В. Информация для пациентов
Рекомендации больному атопическим дерматитом
1. Не держите в комнате ковры.
2. Желательно не иметь мягкой мебели – гладкие поверхности накапливают меньше пыли.
3. Избегайте открытых книжных полок и книг как накопителей пыли.
4. Не разбрасывайте одежду по комнате. Храните одежду в закрытом стенном шкафу. Шерстяную одежду складывайте в чемоданы с застежкой «молния» или в коробки с плотными крышками. Не используйте нафталиновые шарики и другие резко пахнущие вещества.
5. Не держите домашних животных, птиц, аквариумных рыбок.
6. Не держите мягкие игрушки, пользуйтесь моющимися (пластиковыми, деревянными, металлическими).
7. Не следует разводить домашние цветы.
8. Не используйте духи и другие резко пахнущие вещества, особенно в спреях.
9. Покрытие стен: следует предпочесть моющиеся обои или крашенные стены.
10. Занавески должны быть хлопчатобумажными или синтетическими и стираться не реже 1 раза в 3 месяца. Не используйте драпирующиеся занавески.
11. Если у вас установлен кондиционер, мойте фильтры не реже 1 раза в 2 недели.
12. Не используйте электрические вентиляторы.
13. НЕ КУРИТЕ!
14. Не используйте перьевые и пуховые подушки и одеяла. Подушки должны быть из синтепона или других синтетических волокон, из ваты.
15. Не используйте плотные ткани для наперников и наматрасников.
16. Покрывала для кроватей должны быть из легких стирающихся тканей без ворса.
17. Не храните вещи под кроватью.
18. Ежедневно проводите влажную уборку комнаты. При уборке используйте респиратор «лепесток».
19. Тщательную уборку с пылесосом проводите не реже 1 раза в неделю.
Приложение Г.
А площадь поражения (оценивается врачом)
2. Желательно не иметь мягкой мебели – гладкие поверхности накапливают меньше пыли.
3. Избегайте открытых книжных полок и книг как накопителей пыли.
4. Не разбрасывайте одежду по комнате. Храните одежду в закрытом стенном шкафу. Шерстяную одежду складывайте в чемоданы с застежкой «молния» или в коробки с плотными крышками. Не используйте нафталиновые шарики и другие резко пахнущие вещества.
5. Не держите домашних животных, птиц, аквариумных рыбок.
6. Не держите мягкие игрушки, пользуйтесь моющимися (пластиковыми, деревянными, металлическими).
7. Не следует разводить домашние цветы.
8. Не используйте духи и другие резко пахнущие вещества, особенно в спреях.
9. Покрытие стен: следует предпочесть моющиеся обои или крашенные стены.
10. Занавески должны быть хлопчатобумажными или синтетическими и стираться не реже 1 раза в 3 месяца. Не используйте драпирующиеся занавески.
11. Если у вас установлен кондиционер, мойте фильтры не реже 1 раза в 2 недели.
12. Не используйте электрические вентиляторы.
13. НЕ КУРИТЕ!
14. Не используйте перьевые и пуховые подушки и одеяла. Подушки должны быть из синтепона или других синтетических волокон, из ваты.
15. Не используйте плотные ткани для наперников и наматрасников.
16. Покрывала для кроватей должны быть из легких стирающихся тканей без ворса.
17. Не храните вещи под кроватью.
18. Ежедневно проводите влажную уборку комнаты. При уборке используйте респиратор «лепесток».
19. Тщательную уборку с пылесосом проводите не реже 1 раза в неделю.
Приложение Г.
А площадь поражения (оценивается врачом)
|
Площадь поверхности отдельных участков тела у детей старше 2 лет и взрослых
|
Площадь проявлений атопического дерматита на отдельных участках тела
|
|
Площадь поражения
|
Участки тела
|
|
|
Передняя поверхность головы (4,5%)
|
|
|
Задняя поверхность голов ы (4,5%)
|
|
|
Передняя поверхность тулов ища (18%)
|
|
|
Задняя поверхность тулов ища (18%)
|
|
|
Гениталии (1%)
|
|
|
Передняя поверхность левой руки (4,5%)
|
|
|
Задняя поверхность левой руки (4,5%)
|
|
|
Передняя поверхность право й руки (4,5%)
|
|
|
Задняя поверхность право й руки (4,5%)
|
|
|
Передняя поверхность левой ноги (9%)
|
|
|
Задняя поверхность левой ноги (9%)
|
|
|
Передняя поверхность право й ноги (9%)
|
|
|
Задняя поверхность левой ноги (9%)
|
|
|
Итого
|
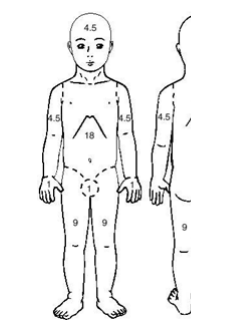
Показатель А =
В интенсивность клинических проявлений (оценивается врачом)
Оценка клинических проявлений АтД:
Оценка клинических проявлений АтД:
|
Клинические проявления |
Оценка в баллах |
|
Эритема
|
|
|
Отек или папулезность
|
|
|
Мокнутие/корки
|
|
|
Расчесы
|
|
|
Лихенификация
|
|
|
Сухость
|
|
|
Итого
|
|
Способ оценки:
0 = отсутствие проявлений
1 = легкие проявления
2 = умеренные проявления
3 = тяжелые проявления
1 = легкие проявления
2 = умеренные проявления
3 = тяжелые проявления
Показатель В =
С выраженность субъективных симптомов (оценивается пациентом)
|
отсутствие зуда
|
очень сильный зуд
|
|
Отсутств ие нарушен ий сна
|
очень сильное нарушен ие сна
|
Показатель С =
SCORAD=A/5+7*B/2+C=
Приложение Г2. Классификация ТГКС по биологической активности и силе активности
Таблица 1. Международная классификация ТГКС по биологической активности.
SCORAD=A/5+7*B/2+C=
Приложение Г2. Классификация ТГКС по биологической активности и силе активности
Таблица 1. Международная классификация ТГКС по биологической активности.
|
Группа активности
|
Препараты
|
|
Низко активные (Класс 1)
|
Флуоцинолон ацетонид 0,0025%,
гидрокортизон 1%, преднизолон 0,5% |
|
Умеренно активные (Класс 2)
|
Алклометазон дипропионат 0,05%,
бетаметазона валерат 0,025%, клобетазона бутират 0,05%, дезоксиметазон 0,05%, триамцинолона ацетонид 0,1%, флуметазона пивалат 0,02%; 2% |
|
Активные (Класс 3)
|
Бетаметазона дипропионат 0,025%,
0,05%, бетаметазона валерат 0,1%, будесонид 0,025%, фторлоролона ацетонид 0,025%, фторциноид 0,05%, фторцинолона ацетонид 0,025%, гидрокортизона бутират 0,1%, метилпреднизолона ацепонат 0,1%, мометазона фуроат 0,1%, триамцинолона ацетонид 0,1% |
|
Высоко активные (Класс 4)
|
Клобетазола пропионат 0,05%,
дифлукортолона валерат 0,3%, галцинонид 0,1% |
Таблица 2. Международная классификация ТГКС по силе активности
|
Группа активности
|
Препараты
|
|
Класс 1 (очень сильные)
|
Клобетазола пропионат 0,05%, мазь, крем
Бетаметазона дипропионат 0,05%, мазь, крем |
|
Класс 2 (сильные)
|
Мометазона фуроат 0,1%, мазь
Дезоксиметазон 0,25%, крем, мазь, гель Триамцинолона ацетонид 0,5%, мазь |
|
Класс 3 (сильные)
|
Бетаметазона валерат 0,1%, мазь
Флутиказона пропионат 0,005%, мазь Триамцинолона ацетонид 0,1%, мазь Триамцинолона ацетонид 0,5%, крем |
|
Класс 4 (средней силы)
|
Флуоцинолон ацетонид 0,025%, мазь
Мометазона фуроат 0,1%, крем, Триамцинолона ацетонид 0,1%, крем Метилпреднизолона ацепонат 0,1%, крем, мазь, мазь жирная, лосьон |
|
Класс 5 (средней силы)
|
Бетаметазона валерат 0,01%, крем
Гидрокортизона бутират 0,1%, крем, мазь Флуоцинолон ацетонид 0,025%, крем, линимент Флутиказона пропионат 0,005%, крем |
|
Класс 6 (средней силы)
|
Алклометазон дипропионат 0,05%, мазь, крем
|
|
Класс 7 (слабые)
|
Гидрокортизон 0,5%, 1%, 2,5% мазь
Преднизолон 0,5% мазь Флуметазон 0,02% крем, мазь Метилпреднизолон 1% |
Рассчитано еженедельное безопасное количество ТГКС, в зависимости от длительности применения и силы его противовоспалительной активности (табл. 3).
Таблица 3. Еженедельное безопасное количество ТГКС (г)
|
Продолжительность применения
|
Степень противовоспалительной активности
|
||
|
Умеренная
|
Сильная
|
Очень сильная
|
|
|
<2 мес
|
100
|
50
|
30
|
|
2–6 мес
|
50
|
30
|
15
|
|
6–12 мес
|
25
|
15
|
7,5
|
Приложение Г3. Побочные эффекты системных ГКС
Системные побочные эффекты:
-
стероидная зависимость;
-
артериальная гипертензия;
-
гастродуоденальные язвы;
-
панкреатит;
-
остеопороз;
-
асептический некроз костей;
-
катаракта;
-
сахарный диабет;
-
нарушение липидного обмена;
-
миопатия;
-
синдром Иценко–Кушинга;
-
острый психоз;
-
задержка физического развития.
Местные проявления побочных эффектов
-
атрофия кожи;
-
стрии;
-
телеангиэктазии;
-
стероидные акне;
-
розацеа;
-
периоральный дерматит;
-
гипертрихоз;
-
вторичные бактериальная, грибковая и вирусная инфекции.
Приложение Г4. Комбинированные препараты, содержащие ГКС
|
Группа лекарственных средств
|
Препараты
|
|
Препараты, содержащие ТГКС и
антибиотики |
Бетаметазон + гентамицин, флуоцинолона ацетонид + неомицин, гидрокортизон + окситетрациклин, гидрокортизон + хлорамфеникол, преднизолон + окситетрациклин, преднизолон + триамцинолон, гидрокортизона ацетат + фузидовая кислота, бетаметазон + фузидовая кислота
|
|
Препараты, содержащие ТГКС и антисептики
|
Гидрокортизон + хлоргексидин, галометазон + триклозан, флуметазон + клиохинол, флуоцинолон + клиохинол, преднизолон + клиохинол
|
|
Препараты, содержащие ТГКС и противогрибковые ЛС
|
Бетаметазон + клотримазол, беклометазон + клотримазол, мазипредон + миконазол, дифлукортолон + изоконазол
|
|
Препараты, содержащие ТГКС,
противомикробные и противогрибковые ЛС |
Бетаметазон + гентамицин + клотримазол, гидрокортизон + неомицин + натамицин, гидрокортизон + клиохинол + нистатин
|
|
Препараты, содержащие ГКС и салициловую кислоту
|
Бетаметазон + салициловая кислота Мометазона фуроат+салициловая кислота
|
Приложение 1. Информация для пациентов
ЧТО ТАКОЕ АТОПИЧЕСКИЙ ДЕРМАТИТ?
Атопический дерматит (АтД) — это хроническое аллергическое заболевание кожи, развивающееся у детей с наследственной предрасположенностью к атопии (повышенной выработке иммуноглобулинов Е – особых белков, участвующих в аллергических реакциях), характеризующееся рецидивирующим течением.
КАК ЧАСТО ВСТРЕЧАЕТСЯ АТОПИЧЕСКИЙ ДЕРМАТИТ?
В последние два десятилетия как в России, так и во многих странах мира отмечают неуклонный рост числа больных АтД. Распространённость атопического дерматита в Узбекистане среди детей составляет от 5 до 15%, чаще болеют дети в возрасте до 3 лет.
ПОЧЕМУ ВОЗНИКАЕТ АТОПИЧЕСКИЙ ДЕРМАТИТ?
В настоящее время основной причиной считают передающийся по наследству сбой в работе иммунной системы.
В грудном и раннем возрасте к развитию заболевания чаще приводит повышенная чувствительность организма к пищевым аллергенам, например к белку коровьего молока, яичному белку и др. В старшем возрасте ведущую роль в развитии АтД играют аллергены, попадающие в организм с дыханием: домашняя пыль и содержащиеся в ней микроскопические клещи, эпидермис (клетки поверхностного слоя кожи) животных, споры грибов, пыльца растений. Однако эти аллергены могут вызывать аллергию не только при вдыхании, но и при контакте с кожей. Причиной АтД могут быть некоторые лекарства (антибиотики, сульфаниламидные препараты и др.), местные анестетики (препараты для местного обезболивания), витамины группы B, паразитарные инфекции (гельминтозы, лямблиоз), а также многие химические раздражители (синтетические материалы, парфюмерия, косметика, бытовые моющие средства), факторы окружающей природы (жёсткая вода, резкие колебания температуры и влажности воздуха), эмоциональная и физическая нагрузка.
В грудном и раннем возрасте к развитию заболевания чаще приводит повышенная чувствительность организма к пищевым аллергенам, например к белку коровьего молока, яичному белку и др. В старшем возрасте ведущую роль в развитии АтД играют аллергены, попадающие в организм с дыханием: домашняя пыль и содержащиеся в ней микроскопические клещи, эпидермис (клетки поверхностного слоя кожи) животных, споры грибов, пыльца растений. Однако эти аллергены могут вызывать аллергию не только при вдыхании, но и при контакте с кожей. Причиной АтД могут быть некоторые лекарства (антибиотики, сульфаниламидные препараты и др.), местные анестетики (препараты для местного обезболивания), витамины группы B, паразитарные инфекции (гельминтозы, лямблиоз), а также многие химические раздражители (синтетические материалы, парфюмерия, косметика, бытовые моющие средства), факторы окружающей природы (жёсткая вода, резкие колебания температуры и влажности воздуха), эмоциональная и физическая нагрузка.
ОПАСЕН ЛИ АТОПИЧЕСКИЙ ДЕРМАТИТ?
Непосредственной опасности для жизни АтД не представляет, однако он существенно снижает качество жизни ребёнка и членов его семьи.
КАК ПРОЯВЛЯЕТСЯ АТОПИЧЕСКИЙ ДЕРМАТИТ?
Основные проявления АтД — зуд кожи, а также её покраснение, сухость, шелушение и утолщение (результат воспаления), чаще всего на лице, шее, волосистой части головы, локтевых сгибах, в подколенных ямках. Дети всегда расчёсывают эти участки.
При распространённом длительно протекающем атопическом дерматите возможно попадание микробов в расчёсы и гнойники, увеличение лимфатических узлов. АтД часто сочетается с заболеваниями желудочно-кишечного тракта. Отличительная черта АтД — ремиссия (относительное благополучие, уменьшение проявлений болезни) летом. Следует помнить, что кожный зуд может быть признаком многих других заболеваний.
При распространённом длительно протекающем атопическом дерматите возможно попадание микробов в расчёсы и гнойники, увеличение лимфатических узлов. АтД часто сочетается с заболеваниями желудочно-кишечного тракта. Отличительная черта АтД — ремиссия (относительное благополучие, уменьшение проявлений болезни) летом. Следует помнить, что кожный зуд может быть признаком многих других заболеваний.
КАК ДИАГНОСТИРУЮТ АТОПИЧЕСКИЙ ДЕРМАТИТ?
АД диагностируют на основании жалоб ребёнка, данных врачебного осмотра, а также специальных тестов: кожных тестов, тестов с пищевыми аллергенами и других.
КАКИЕ СУЩЕСТВУЮТ МЕТОДЫ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ АТОПИЧЕСКОГО ДЕРМАТИТА?
Лечение АтД комплексное. Лекарственная терапия включает приём следующих препаратов.
Местное (наружное) лечение:
Местное (наружное) лечение:
-
увлажняющие и смягчающие средства;
-
местные глюкокортикоиды (препараты первой линии);
-
препараты дёгтя;
-
местные антибиотики (эффективны у пациентов с подтверждённой бактериальной инфекцией кожи).
Лекарственные препараты, назначаемые для приёма внутрь:
-
антигистаминные препараты;
-
стабилизаторы мембран тучных клеток;
-
аллергенспецифическая иммунотерапия.
Кроме приёма лекарств большое значение имеют соблюдение режима, диеты, фототерапия (применяемая у пациентов с распространёнными кожными поражениями, устойчивыми к стандартному лечению), биорезонансная терапия, психотерапия.
Элиминационную диету (то есть диету, основанную на сокращении до минимума или полном исключении из питания выявленных пищевых аллергенов) подбирают каждому ребёнку индивидуально с учётом данных о развитии болезни и результатов аллергологического обследования. Общие рекомендации для больных АтД:
-
исключение из пищевого рациона экстрактивных мясных и рыбных бульонов, шоколада, кофе, какао, цитрусовых, земляники, дыни, мёда, орехов, грибов, икры, крабов, креветок, специй, пива и алкоголя, сыров, кондитерских изделий, а также консервов, копчёностей, пряностей и других продуктов, содержащих пищевые добавки и консерванты;
-
можно давать отварное мясо, крупяные и овощные супы, масло, отварной картофель, каши, молочно-кислые продукты (простокваша, творог), яблоки и компоты из них, ржаной и пшеничный хлеб.
Необходимо соблюдать особый режим и знать некоторые правила. Максимально ограничивать контакт ребёнка с факторами внешней среды,
вызывающими обострение заболевания.
В период обострения ребёнок должен спать в хлопчатобумажных носках и перчатках, ему нужно коротко стричь ногти.
Для мытья детей применять мыло и моющие средства с увлажняющим эффектом.
Ограничивать по времени водные процедуры (в течение 5–10 мин), проводить их в тёплой (не горячей) воде.
Стирать новую одежду ребёнка перед её использованием. Одежда должна быть просторной, из чистого хлопка.
Для стирки одежды и постельных принадлежностей родители должны использовать жидкие, а не порошковые моющие средства.
Применять минимальное количество кондиционера для белья, после чего дополнительно полоскать его.
В жаркую погоду пользоваться кондиционером.
В солнечную погоду смазывать кожу ребёнка солнцезащитным кремом, не вызывающим раздражения кожи.
После посещения бассейна ребёнку нужно принимать душ и наносить на кожу крем или мазь на жировой основе.
Пациент с атопическим дерматитом должен: Выполнять все назначения лечащего врача.
Не использовать спиртсодержащие средства гигиены.
Не пользоваться средствами с антимикробными компонентами без рекомендации лечащего врача.
Не носить грубую и тяжёлую одежду. Не загорать.
Не участвовать в спортивных состязаниях, так как это вызывает интенсивное потоотделение и сопровождается тесным контактом кожи с одеждой.
Не принимать слишком часто водные процедуры.
Во время мытья не тереть интенсивно кожу и пользоваться для мытья губкой или мочалкой, не более жёсткой, чем мочалка из махровой ткани.
Профилактика АтД: будущим мамам, входящим в группу риска рождения ребёнка с аллергическим заболеванием, обязательно соблюдать низкоаллергенную диету; стараться кормить ребёнка только грудным молоком и соблюдать эту диету весь период кормления грудью; при невозможности грудного вскармливания давать малышу низкоаллергенные смеси, правильно ухаживать за его кожей, соблюдать режим профилактических прививок после консультации с врачом- аллергологом и, если необходимо, обследования.
Профилактика обострений и осложнений атопического дерматита заключается в соблюдении ребёнком специального режима, диеты, выполнении назначений врача. Большую роль в профилактике АтД может сыграть обучение пациента и членов его семьи в аллергошколах.
Приложение
Дополнительный опросник по оценке уровня контроля симптомов бронхиальной астмы у детей от 6 до 11 лет
Дополнительный опросник по оценке уровня контроля симптомов бронхиальной астмы у детей от 6 до 11 лет
|
Контроль над симптомами БА
|
|
|
Дневные симптомы
|
Спросите, как часто у ребенка бывает кашель, свистящее дыхание, одышка или тяжелое дыхание (с частотой в неделю или в день)? Что провоцирует симптомы? Как удается справиться с симптомами?
|
|
Ночные симптомы
|
Кашель, пробуждение, усталость в течение дня? (Если единственным симптомом является кашель, рассмотрите другие диагнозы, такие как ринит или гастроэзофагеальная рефлюксная болезнь).
|
|
Использование
препаратов, облегчающих симптомы |
Как часто используются препараты, облегчающие исмптомы БА? Необходимо дифференцировать использование препаратов перед физической нагрузкой (спортивной тренировкой) и их использованием для облегчения симптомов.
|
|
Уровень активности
|
Какие виды спорта/хобби/интересы есть у ребенка, в школе и в свободное время? Каков уровень активности ребенка по сравнению с его сверстниками или братьями и сестрами? Сколько дней ребенок отсутствует в школе? Постарайтесь получить точную картину дня ребенка от самого ребенка, не перебивая его и/или сопровождающее лицо.
|
|
Факторы риска неблагоприятного исхода.
|
|
|
Обострение
|
Спросите, как вирусные инфекции влияют на астму ребенка? Мешают ли симптомы занятиям в школе или спортом? Как долго длятся симптомы? Сколько эпизодов было с момента последнего визита к врачу? Были ли неотложные обращения за амбулаторной или стационарной медицинской помощью? Имеется ли письменный план действий? Факторы риска обострений включают в себя наличие обострений в анамнезе, плохой контроль симптомов, низкую приверженность к лечению, низкий достаток и стойкий положительный БДТ даже если у ребенка симптомы малочисленны.
|
|
Легочная функция
|
Проверка легочной функции. Основное внимание уделяется ОФВ1 и соотношению ОФВ1/ФЖЕЛ.
Изобразите эти значения в виде в процентах от предполагаемых значений, чтобы оценить временную тенденцию. |
|
Побочный эффект
|
Проверяйте рост ребенка не реже одного раза в год, т.к. плохо контролируемая астма может влиять на рост, а скорость роста может быть ниже в первые 1- 2 года лечения ИГКС. Спросите о кратности приема и дозе ИГКС и оральных кортикостероидов.
|
|
Факторы, относящиеся к лечению
|
|
|
Техника ингаляции
|
Попросите ребенка показать, как он использует свой ингалятор. Проверьте технику с инструкцией к конкретному устройству.
|
|
Приверженность лечению
|
Спросите, имеются ли в доме назначенные ребенку лекарственные препараты (ингаляторы и/или таблетки)? Сколько дней в неделю ребенок пользуется ими (например, 0, 2, 4, 7 дней)? Легче ли ребенку помнить о необходимости приема лекарства утром или вечером? Где хранится лекарство - на виду ли оно, чтобы не забыть? Проверьте дату на ингаляторе
|
|
Цели/опасения
|
Есть ли у ребенка, его родителей/опекунов какие- либо опасения по поводу астмы (например, страх перед лекарствами, побочными эффектами, помехами в деятельности)? лекарств, побочные эффекты, влияние на повседневную деятельность)? Каковы их цели в отношении лечения?
|
|
Сопутствующие заболевания
|
|
|
Аллергический ринит
|
Зуд, чихание, обструкция носа? Может ли ребенок дышать через нос? Какие лекарства принимаются для лечения назальных симптомов?
|
|
Экзема
|
Нарушение сна, топические кортикостероиды?
|
|
Пищевая аллергия
|
Есть ли у ребенка аллергия на какие-либо продукты? (Подтвержденная пищевая аллергия является фактором риска смерти, связанной с астмой).
|
|
Ожирение
|
Проверьте индекс массы тела с поправкой на возраст. Спросите о диете и физической активности.
|
|
Другие исследования (при необходимости)
|
|
|
Ведение дневника (в течение 2 недель)
|
Если на основании вышеприведенных вопросов невозможно четко оценить степень контроля заболевания, попросите ребенка или его родителей/опекунов вести ежедневный дневник, включающий внесение симптомов БА, лекарственных препаратов для облегчения симптомов, а также пиковой скорости выдоха (лучшее значение из 3-х показателей) в течение 2 недель
|
|
Тест с физической нагрузкой
|
Предоставляет информацию о гиперреактивности дыхательных путей и физической форме.
Проводится в том случае, если при использовании других инструментов все равно трудно оценить контроль астмы. |
|
Факторы риска стойкого ограничения воздушного потока
|
|
Факторы риска развития побочных эффектов лекарственных средств
|
Ключ (интерпретация): согласно «Глобальной стратегии лечения и профилактики бронхиальной астмы» (GINA 2023) для определения уровня контроля над симптомами заболевания у детей 5 лет и младше используют опросник, состоящий из 4 вопросов, позволяющий оценить состояние пациента за последние 4 недели. В зависимости от количества положительных ответов уровень контроля оценивают, как хороший, частичный или не контроль.
Пояснения: неконтролируемая бронхиальная астма – 3-4 клинических признака за последние 4 недели, частично контролируемая – 1-2 клинических признака за последние 4 недели, хорошо контролируемая – отсутствие перечисленных клинических признаков у пациента.
Приложение
Дополнительный опросник по оценке уровня контроля симптомов бронхиальной астмы у детей младше 5 лет
Дополнительный опросник по оценке уровня контроля симптомов бронхиальной астмы у детей младше 5 лет
|
А. Контроль симптомов БА
|
Уровень контроля симптомов БА
|
||
|
Були ли за последние 4 недели у ребенка:
|
Хорошо контролируемый
|
Частично контролируемый
|
Неконтролируемый
|
|
Дневные симптомы астмы, длящиеся несколько минут и более 1 раза в неделю?
|
Ничего из перечисленного
|
1-2 пункта из перечисленного
|
3- 4 пункта из перечисленного
|
|
Ограничивает ли ребенок свою активность в связи с БА (играет/бегает меньше, чем другие дети, быстро устает во время прогулки/игры)
|
|
|
|
|
Потребность в КДБА более 1 раза в неделю
|
|
|
|
|
Ночные пробужден ия или ночной кашель, связанные с БА
|
|
|
|
|
Б. Прогнозируемый риск неблагоприятных исходов при БА
|
|||
|
Факторы риска обострений астмы в ближайшие несколько месяцев
- Неконтролируемые симптомы астмы - Одно или несколько тяжелыхобострений (вызов бригады скорой помощи, госпитализация или курс оральных кортикостероидов) в течение предыдущего года - Начало обычного для ребенка сезона обострений (особенно осенью) - Экспозиция табачного дыма; воздействие поллютантов в помещении или на улице; экспозиция аллергенов в помещении (например, клещи домашней пыли, тараканы, домашние животные, плесень), особенно в сочетании с вирусной инфекцией [373] - Серьезные психологические или социально-экономические проблемы у ребенка или семьи - Низкая приверженность к приему ИГКС или неправильная техника ингаляции - Загрязнение окружающей среды (NO2 и др поллютанты) [374] |
|||
Приложение
Вопросы, котрые могут помочь диагностировать БА у ребенка младше 5 лет [21]
Вопросы, котрые могут помочь диагностировать БА у ребенка младше 5 лет [21]
|
Бывают ли у Вашего ребенка свистящие хрипы? Свист – это высокочастотный шум, который может исходить из грудной клетки или из горла.
Если это возможно, попросите родителей зафиксировать на видео эпизод свистящего дыхания для того, чтобы отдифференциировать синдром бронхиальной обструкции от патологии верхних дыхательных путей. |
|
Просыпается ли Ваш ребенок ночью по причине кашля, свистящего дыхания, одышки, затруднения дыхания, тяжелого дыхания?
|
|
Останавливается ли Ваш ребенок во время бега или игры по причине кашля, свистящего дыхания, затруднения дыхания, тяжелого дыхания, одышки?
|
|
Появляется ли у Вашего ребенка кашель, свистящее дыхание, затруднение дыхания, тяжелое дыхание, одышка при смехе, плаче, контакте с животными или при нахождении в помещении, где курят?
|
|
Была ли диагностирована ранее у Вашего ребенка пищевая аллергия или атопический дерматит?
|
|
В Вашей семье кто-нибудь страдает бронхиальной астмой, поллинозом, пищевой аллергией, атопическим дерматитом, либо имеет другие заболевания, связанные с респираторными проблемами?
|
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта", не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения "MedElement (МедЭлемент)", "Lekar Pro", "Dariger Pro", "Заболевания: справочник терапевта" являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.